Диета при ахалазии кардии пищевода: Рекомендации по питанию при ахалазии кардии
Рекомендации по питанию при ахалазии кардии
Дата публикации: .
Климович А.Е., Жартун С.А.
Ахалазия кардии – хроническое нервно-мышечное заболевание, при котором нарушается прохождение пищевых масс по пищеводу и из пищевода в желудок вследствие патологических изменений пищеводной перистальтики и отсутствия рефлекторного расслабления нижнего пищеводного сфинктера во время глотания.
Больным с ахалазией кардии необходимо соблюдать определённый режим питания и особые рекомендации относительно приёма пищи.
Рекомендации по питанию:
- Большое значение имеет регулярное питание (5–6 раз в день).
- Исключить переедание и закуски перед сном. Последний прием пищи не позднее, чем за 2 часа до сна.
- Во время сна строго горизонтальное положение тела также не показано, так как пища может задерживаться в пищеводе до нескольких часов, а верхний пищеводный сфинктер во время сна расслабляется, что создаёт предпосылки для аспирации.

- Не лежать после еды в течение 2 часов.
- Прекратить употребление алкоголя.
- Принимать пищу необходимо медленно, тщательно её пережёвывая.
- Умеренно щадящая диета: избегать острой, жирной, горячей, очень холодной пищи, которая оказывает повреждающее действие на слизистую пищевода.
- Исключить газированные напитки, повышающие внутрижелудочное давление.
- Ограничить употребление кислых продуктов, продуктов, содержащих грубые виды клетчатки (капуста, яблоки др.), свежей выпечки и хлеба.
- Исключить или уменьшить потребление жиров, которые угнетают двигательную активность желудка.
- При формировании белково-энергетической недостаточности показано искусственное питание.
ДИЕТА ПРИ АХАЛАЗИИ КАРДИИ – Диетические рекомендации для пациентов, страдающих ахалазией кардии
грыжа-пищевода.рф // Ахалазия кардии // Диетические рекомендации для пациентов, страдающих ахалазией кардии
Лицам, страдающим ахалазией кардии, обязательно следует соблюдать определённые диетические ограничения и придерживаться рекомендуемого им режима питания. Это даст возможность предупредить прогрессирование заболевания и предотвратить развитие осложнений.
Это даст возможность предупредить прогрессирование заболевания и предотвратить развитие осложнений.Во-первых, есть нужно медленно, не отвлекаясь, очень тщательно пережёвывая пищу. Как правило, процесс проглатывания облегчается при употреблении жидкости, так как за счёт создания дополнительного давления на нижний пищеводный сфинктер, облегчается прохождение проглоченных масс в желудок. Сам же объём пищи ни в коем случае не должен быть чрезмерным, в виду того, что переедание чревато ухудшением состояния пациента. В идеале рекомендуют придерживаться четырёх- или пятиразового режима питания. К тому же пища не должна быть как излишне горячей, так и очень холодной (это же касается и напитков).
Во-вторых, сразу после приёма пищи больным необходимо избегать наклона туловища вперёд и горизонтального положения тела. Свою кровать им лучше установить таким образом, чтобы её головной конец был приподнят на угол где-то градусов в десять, так как во время сна строго горизонтальное положение тела не показано в виду того, что пища у пациентов способна задерживаться в просвете пищеводе до нескольких часов, а верхний эзофагеальный сфинктер во сне расслабляется, что ведёт к созданию предпосылок для аспирации.
В-третьих, что касается непосредственно самого рациона, он не должен включать в себя те продукты, которые могут усилить проявления дисфагии. По сути, речь идёт об умеренно механически и химически щадящей диете. Больным рекомендуют избегать употребления зажаренных блюд, солёных и копчёных продуктов, острых приправ, соусов и т.п. Желательно ограничивать употребление консервов, в особенности овощных и рыбных, поскольку в них содержится большое количество томатного соуса и растительного масла, подвергшегося термической обработке.
Кроме того, есть также ряд продуктов, которые сами по себе усиливают проявления дисфагии у пациентов с ахалазией кардии. Это свежий мягкий хлеб, кефир, хурма, яблоки, персики, вареный картофель, жирное мясо. От их употребления следует отказаться.
В ряде случаев рацион у больных данной категории определяется и их привычками и индивидуальными особенностями. К примеру, вкусные и любимые человеком блюда вызывают у него дисфагию в меньшей степени, чем те, что рекомендует врач. Причём последние могут не просто восприниматься им равнодушно, но даже с некоторым отвращением (то есть срабатывает психологический фактор).
Причём последние могут не просто восприниматься им равнодушно, но даже с некоторым отвращением (то есть срабатывает психологический фактор).
В этом плане иногда допускается отступление от строгой диеты и рекомендуются продукты, вызывающие у пациента положительные эмоции. При этом рацион должен быть полноценным и обеспечивать человека всеми необходимыми витаминами (в частности группой В) и микроэлементами. На период пребывания больных с ахалазией кардии в стационаре им назначается стандартная диета по Певзнеру (№1 или 5а) или типа пищеводного стола.
Необходимо отметить, что сама по себе диета не является методом лечения ахалазии кардии, это лишь часть (но очень важная!) общей схемы.
(495) 51-722-51 – хирургия грыжи пищевода и ахалазии кардии в Москве и за рубежом
ОФОРМИТЬ ЗАЯВКУ на ЛЕЧЕНИЕ
Непосредственные результаты оперативного лечения ахалазии пищевода
Среди 170 наблюдавшихся нами больных оперативное лечение выполнено у 75 чел. (44,1+3,8%). Преобладали пациенты с III и IV стадией АП (по 32 чел. 42,7+5,7%), со II стадией было 11 больных (14,6+0,2%). Пациентам с I стадией АП оперативное лечение не применялось.
(44,1+3,8%). Преобладали пациенты с III и IV стадией АП (по 32 чел. 42,7+5,7%), со II стадией было 11 больных (14,6+0,2%). Пациентам с I стадией АП оперативное лечение не применялось.Использованы различные оперативные доступы (Табл. 15). Большинство больных оперировано видеолапароскопически -50 чел (66,7+5,4%). До внедрения в практику нашей клиники видеоэндоскопических технологий операции выполнялись из традиционных доступов – у 4 пациентов (5,3+0,3%) использована торакотомия, у 21 (28,0+5,2%) – лапаротомия. С 1997 г. все больные с АП нами оперированы видеолапароскопически. Независимо от доступа выполнялась эзофагокардиомиотомия по Геллер с эзофагофундопликацией по Дор для закрытия мышечного дефекта в стенке пищевода и создания антирефлюксного механизма.
Таблица 15. Применяемые оперативные доступы при АПМодифицированная нами видеолапароскопическая эзофагокардиомиотомия по Геллер с эзофагофундопликацией по Дор выполнялась следующим образом.

Положение больного на операционном столе при введении в наркоз и установки лапаропортов – горизонтальное, на спине. После визуализации брюшной полости больного переводили в положение с поднятым головным концом операционного стола на 20-25 градусов инаклономнаправыйбок на 25-30 градусов. Это положение позволяет сместить внутренние органы и увеличить объем пространства в области оперативного вмешательства. Операционная бригада состоит из 4 человек. Справа от больного находится оперирующий хирург и операционная сестра, слева -2 ассистента.
Справа и слева от головной части операционного столанаходятся двавидеомонитора – один в поле зрения оперирующего хирурга, другой для ассистентов. (Рис. 8).
Рисунок 8. Схема расположения операционной бригады (объяснение в тексте)
Для постановки лапаропортов использовали 5 точек (Рис. 9). Точка 1 непосредственно над пупком по срединной линии, где устанавливался 10 мм порт для эндовидеокамеры.
 Точка 2- вмезогастрии, по среднеключичной линии справа для 10 мм троакара, через который выполнялись основные манипуляции на кардиальном отделе и дне желудка, абдоминальном отделе пищевода. Расположение данной точки было индивидуальным и зависело от анатомических особенностей – расположение круглой связки печени и левой доли печени.
Точка 2- вмезогастрии, по среднеключичной линии справа для 10 мм троакара, через который выполнялись основные манипуляции на кардиальном отделе и дне желудка, абдоминальном отделе пищевода. Расположение данной точки было индивидуальным и зависело от анатомических особенностей – расположение круглой связки печени и левой доли печени. Рисунок 9. Точки установки лапаропортов при выполнении видеолапароскопической эзофагокардиомиотомии по Геллер с передней гемиэзофагофундопликацией по Дор (объяснение в тексте)
Точка 3- под мечевидным отростком, где устанавливался 5 мм лапаропорт для ретрактора печени. Точка 4- на 2-3 см ниже левой реберной дуги по среднеключичной линии вводился 5 мм троакар для работы диссектором, аспиратором-ирригатором, иглодержателем, а также для установки контрольного дренажа после операции. Точка 5- влевой боковойобласти живота по передней подмышечной линии для 5 мм лапаропорта через который выполнялась тракция желудка зажимом Бебкокка.

Указанные места введения лапаропортов – по окружности, обеспечивали равноудаленное расположение инструментов по отношению к области оперативного вмешательства и отсутствие механического взаимодействия инструментов в брюшной полости. Оператор использовал в своей работе инструменты установленные в точках 2 и 3, первый ассистент в точках 3 и 4, второй ассистент -1 и 5.
После установки первого лапаропорта создавали пневмокарбоксиперитонеум с поддержанием давления на уровне 12-14 мм рт ст. Операцию начинали с осмотра брюшной полости для исключения сопутствующей патологии брюшной полости, оценки индивидуальных анатомических особенностей и постановки других лапаропортов. Затем выделяли переднюю поверхность абдоминального отдела пищевода и область пищеводно-желудочного перехода. Для этого проводилась послойная пристеночная мобилизация малой кривизны желудка, начиная выше верхних ветвей a. gastric sinistra, идущих перпендикулярно к ней.
Затем рассекалась пищеводно-диафрагмальная связка в области пищеводно-желудочного перехода по направлению к углу Гиса (левому ребру пищевода). Далее пищеводно-диафрагмальная связка по левому ребру пищевода рассекалась до диафрагмы, а затем вдоль диафрагмы до правого ребра пищевода (Рис. 10, 13). Таким образом, выполнялась мобилизация только передней поверхности пищевода и желудочно-пищеводного перехода, без нарушения анатомических соотношений пищевода и желудка в области угла Гиса и связочных структур между дном желудка и селезенкой, удерживающих его в исходном положении, которое в последующем способствует созданию тракции при подшивании рассеченной мышечной оболочки пищевода. Эти манипуляции выполнялись с помощью ультразвукового гармонического скальпеля «Ultrasision» или эндохирургического крючка.
Далее пищеводно-диафрагмальная связка по левому ребру пищевода рассекалась до диафрагмы, а затем вдоль диафрагмы до правого ребра пищевода (Рис. 10, 13). Таким образом, выполнялась мобилизация только передней поверхности пищевода и желудочно-пищеводного перехода, без нарушения анатомических соотношений пищевода и желудка в области угла Гиса и связочных структур между дном желудка и селезенкой, удерживающих его в исходном положении, которое в последующем способствует созданию тракции при подшивании рассеченной мышечной оболочки пищевода. Эти манипуляции выполнялись с помощью ультразвукового гармонического скальпеля «Ultrasision» или эндохирургического крючка.
Рисунок 10. Схема эзофагокардиомиотомии:
1- зона мобилизации пищевода, пищеводно-желудочного перехода и желудка,
2- слизистая оболочка пищевода, пролабирующая через миотомный разрез,
3- желудочно-селезеночная связка,
4 – диафрагмально-селезеночная связка,
5- селезеночно-почечная и селезеночно-поджелудочная связка
Рисунок 11.
 Схема эзофагокардиомиотомии: 1- слизистая оболочка пищевода, пролабирующая через миотомный разрез, 2- дно желудка подшито к левому краю миотомного разреза
Схема эзофагокардиомиотомии: 1- слизистая оболочка пищевода, пролабирующая через миотомный разрез, 2- дно желудка подшито к левому краю миотомного разреза
Рисунок 12. Стоп-кадр видеофрагмента операции – мобилизована область пищеводно-желудочного перехода. Обозначения:1 – абдоминальный отдел пищевода, 2 – дно желудка, 3 – пищеводное отверстие диафрагмы
Передняя поверхность пищевода и область пищеводно-желудочного перехода выделялись таким образом, чтобы на их поверхности не было жировой клетчатки (Рис. 12). Протяженность суженого сегмента пищевода определялась визуально. Если престенотическое расширение пищевода располагалось выше уровня диафрагмы, производилось её сагиттальное рассечение, чтобы выделить пищевод не менее чем на 1,5-2 см выше сужения.
На толстом желудочном зонде, эндохирургическим крючком, в режиме резания, по срединной линии передней полуокружности пищевода выполнялась передняя продольная миотомия на протяжении суженого сегмента пищевода.
На 1,5-2 см выше него и дистально до зоны интимного сращения подслизистой и мышечной оболочки кардиального отдела желудка, что соответствует пищеводно-желудочному переходу, мышцы которого составляют единый замыкательный механизм кардии, вместе с мышцами нижней трети пищевода (Рис. 13). При выполнении миотомии важным техническим моментом является полное пересечение всех циркулярных мышечных волокон.
Рисунок 13. Стоп-кадр видеофрагмента операции – выполняется эзофагокардиомиотомия. Обозначения:1 – левый край рассеченной мышечной оболочки пищевода, 2 – слизистая оболочка пищевода
Слизисто-подслизистый слой по левому ребру пищевода отсепаровывался от мышечной оболочки на V окружности пищевода (Рис.14), после чего слизистая оболочка начинала про лавировать между разошедшимися краями мышечного слоя (Рис. 15).
Рисунок 14. Отделение левого края рассеченной мышечной оболочки пищевода от слизистой оболочки на V окружности.
 Обозначения:1 – левый край рассеченной мышечной оболочки пищевода, 2 – правый край рассеченной мышечной оболочки пищевода, 3 – слизистая оболочка пищевода, пролабирующая в миотомный разрез, 4 – отделение мышечной оболочки от слизистой с помощью эндохирургического крючка
Обозначения:1 – левый край рассеченной мышечной оболочки пищевода, 2 – правый край рассеченной мышечной оболочки пищевода, 3 – слизистая оболочка пищевода, пролабирующая в миотомный разрез, 4 – отделение мышечной оболочки от слизистой с помощью эндохирургического крючка
Рисунок 15. Стоп-кадр видеофрагмента операции – окончательный вид выполненной эзофагокардиомиотомии. Обозначения:1 – левый край рассеченной мышечной оболочки пищевода, 2 – слизистая оболочка пищевода, пролабирующая в миотомный разрез, 3 – правый край рассеченной мышечной оболочки пищевода
Указанный прием существенно увеличивает диаметр пищевода и предотвращает последующее смыкание рассеченных краев его мышечной оболочки. Этот эффект усиливается за счет оттягивания левого края рассеченной мышечной оболочки пищевода путем подшивания к дну желудка, которое, в некоторой степени, остается фиксированным за счет сохранения анатомических взаимоотношений в области угла Гиса и с селезенкой, которая мало смещена из-за наличия связочного аппарата с окружающими органами.

Далее передняя стенка желудка без натяжения фиксировалась швами к правому краю рассеченной мышечной оболочки. Для этого непрерывным швом снизу вверх дно желудка подшивали к левому краю рассеченной стенки пищевода, а затем сверху вниз по правому краю разреза. Шов накладывается с помощью иглодержателя неабсорбирующимся шовным материалом на атравматичной игле (Рис. 16).
Рисунок 16. Стоп-кадр видеофрагмента операции – подшивание дна желудка к правому краю миотомного разреза. Обозначения:1 – правый край рассеченной мышечной оболочки пищевода, 2- дно желудка
На 2 сутки всем пациентам выполнялось контрольное рентгенологическое исследование для исключения нарушения целостности стенки пищевода, очем судили по отсутствию затеков контрастного вещества за контур пищевода. Подобных осложнений не выявлено ни у одного больного. После этого пациенты начинали питаться с соблюдением строгой диеты – на протяжении 25 суток после операции принимали только жидкую пищу, сисключением острой, холодной, горячей пищи.
 Начиная с 6 суток, в рацион включали кашицеобразную пищу. Больные выписывались на 7-9 сутки после оперативного лечения.
Начиная с 6 суток, в рацион включали кашицеобразную пищу. Больные выписывались на 7-9 сутки после оперативного лечения.После видеолапароскопической кардиомиотомии с фундопликацией по Дор интраоперационные осложнения возникли у 4 больных (8,0+0,4%). При выполнении эзофагокардиомиотомии с помощью эндокрючка у них произошла перфорация слизистой оболочки пищевода. Диаметр перфоративного отверстия составил не более 2-3 мм. Осложнение возникало у пациентов с резким истончением стенки пищевода при АП III – IV стадии. Дефект слизистой оболочки зашивали наложением интракорпорального шва абсорбирующимся шовным материалом (Викрил 3-0 на круглой игле). На начальном этапе освоения эндохирургических технологий в 1 наблюдении (2,0+0,2%) потребовалась конверсия доступа (лапаротомия) из-за технических трудностей при наложении интракорпорального шва. При выполнении миотомии из открытых доступов аналогичное осложнение было у 4,0+0,4% больных.
При сопоставлении частоты и характера послеоперационных осложнений (Табл. 16), установлено, что после торакального доступа у всех больных развилась пневмония. Местных осложнений в зоне оперативного вмешательства не отмечено, что объясняется хорошей визуализацией зоны оперативного вмешательства. После операций из лапаротомного доступа осложнения возникали реже, чем после торакального. Однако у одного из больных вследствие перфорации пищевода развилась эмпиема плевры с летальным исходом. После видеолапароскопических и торакальных операций летальных исходов не было. После видеолапароскопической кардиомиотомии осложнений в раннем послеоперационном периоде не было.
16), установлено, что после торакального доступа у всех больных развилась пневмония. Местных осложнений в зоне оперативного вмешательства не отмечено, что объясняется хорошей визуализацией зоны оперативного вмешательства. После операций из лапаротомного доступа осложнения возникали реже, чем после торакального. Однако у одного из больных вследствие перфорации пищевода развилась эмпиема плевры с летальным исходом. После видеолапароскопических и торакальных операций летальных исходов не было. После видеолапароскопической кардиомиотомии осложнений в раннем послеоперационном периоде не было.
У 1 больного после выписки его из стационара на 10 сутки после видеолапароскопической эзофагокардиомиотомии по Геллер с эзофагофундопликацией по Дор наступила перфорация пищевода. Приводим это наблюдение. Больной среднего возраста поступил с жалобами на затруднение прохождения по пищеводу твердой, кашицеобразной и жидкой пищи, боль за грудиной во время еды, периодически возникающее срыгивание пищей.
 При рентгеноскопии – пищевод содержит слизь в большом количестве, просвет его расширен до 7,0 см. В дистальном отделе пищевод конически сужен до 0,1 см, контуры четкие. Газовый пузырь желудка отсутствует. ЭФГДС – слизистая пищевода бледно-розовая. В просвете мутная жидкость, следы пищи. В дистальном отделе пищевод слегка расширен. Кардия плотно сомкнута, проходима. Поставлен диагноз: Ахалазия пищевода III стадии.
При рентгеноскопии – пищевод содержит слизь в большом количестве, просвет его расширен до 7,0 см. В дистальном отделе пищевод конически сужен до 0,1 см, контуры четкие. Газовый пузырь желудка отсутствует. ЭФГДС – слизистая пищевода бледно-розовая. В просвете мутная жидкость, следы пищи. В дистальном отделе пищевод слегка расширен. Кардия плотно сомкнута, проходима. Поставлен диагноз: Ахалазия пищевода III стадии.Выполнена видеолапароскопическая эзофагокардиомиотомия по Геллер с эзофагофундопликацией по Дор. Во время операции произошла перфорация слизистой оболочки пищевода, которая была зашита одиночным швом. На 3 сутки после операции пациенту выполнено контрольное рентгенологическое исследование – пищевод расширен до 5 см в диаметре, кардия проходима для густой бариевой взвеси, опорожнение пищевода замедленно. Затеков контраста за контур пищевода нет. На 8 сутки больной выписан в удовлетворительном состоянии. На 10 сутки после употребления грубой, твердой пищи у больного появилась острая боль в верхних отделах живота.
Госпитализирован, при обследовании диагностирована перфорация пищевода. Выполнена лапаротомия, зашивание перфоративного отверстия пищевода, санация и дренирование брюшной полости. Гастростомия. Проводилась комбинированная антибактериальная терапия. Состояние больного стабилизировалось, но в эпигастральной области сформировался трубчатый пищеводный свищ, который самостоятельно закрылся. Через 4 месяца выполнено внебрюшинное закрытие гастростомы. Пациент стал питаться пищей любой консистенции, явлений дисфагии нет.
Время операции из открытого доступа составило 93,9+1,9 минут, при применении видеолапароскопического доступа несколько больше – 108,2+3,5 минут, р<0,05. Последние три года отмечена тенденция к уменьшению продолжительности видеолапароскопической кардиомиотомии по Геллер с передней фундопликацией по Дор до 100,8+3,2 минут.
У ослабленных пациентов с АП IV стадии в предоперационном периоде для коррекции нутритивной недостаточности энтеральное питание проводилось через назогастральный зонд.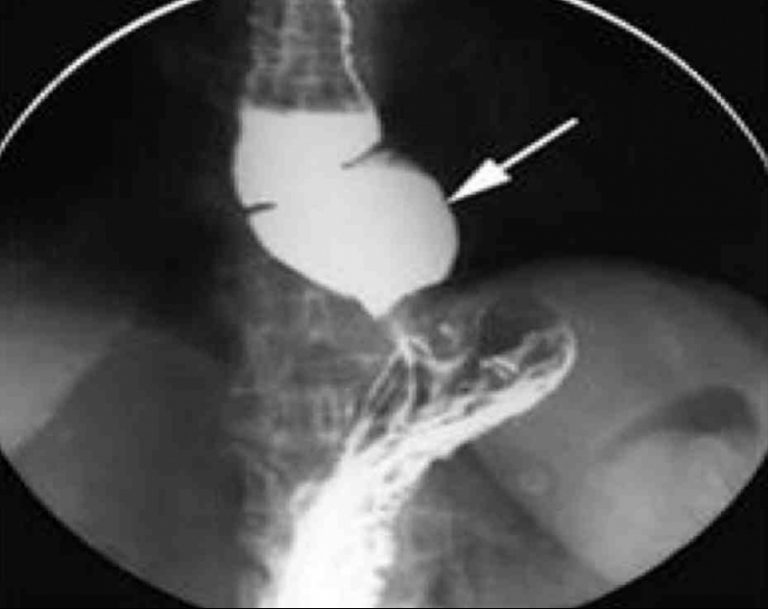 Приводим эти наблюдения.
Приводим эти наблюдения.
Пациент пожилого возраста поступил в тяжелом состоянии с жалобами на афагию, срыгивание съеденной пищей в неизмененном виде, чувство давления за грудиной после еды.
Рисунок 17. Рентгенограмма пищевода больного АП IV стадии. А – до оперативного лечения, Б – через 12 месяцев после оперативного лечения (объяснение в тексте)
Снижение массы тела на 8 кг за последние 6 месяцев. Затрудненное прохождение пищи отмечает около 5 лет. За 2 недели до поступления в стационар наступила афагия. Для обеспечения энтерального питания был установлен назогастральный зонд. Для этого была выполнена ЭФГДС, в ходе которой в желудок через биопсийный канал проведен жесткий проводник, по которому был установлен назогастральный зонд. Проводилось смешанное энтеральное и парентеральное питание, инфузионная терапия. При рентгенологическом исследовании пищевод значительно расширен на всем протяжении до 9 см. Содержит большое количество жидкости и слизи.
 Рельеф слизистой оболочки на этом фоне не определяется. Перистальтические волны не прослеживаются.
Рельеф слизистой оболочки на этом фоне не определяется. Перистальтические волны не прослеживаются.Барий через кардию проходит порциями, при даче нитроглицерина кардия не расслабляется. Гастроэзофагеальных рефлюксов и грыжи пищеводного отверстия диафрагмы не выявлено (Рис. 17а). ФЭГДС -просвет пищевода до 3-4 см, в просвете пищевые массы. Кардиальный жом выражен, сомкнут, при приложении усилия фиброскоп проводится через него с трудом. Биопсия – слизь, гнойно-некротические массы, фрагменты многослойного плоского эпителия с явлениями острого воспаления и эрозированием. Манометрия пищевода (Рис. 18) – Базальный тонус пищевода 0-2 mmHg, за период исследования отсутствовали сокращения пищевода даже на глоток. Установлен диагноз: Ахалазия пищевода IV стадии.
В ходе проводившегося обследования диагностирована двухсторонняя нижнедолевая аспирационная пневмония, что потребовало дополнительного лечения – дезинтоксикационной терапии, комбинированного антибактериального лечения.
На фоне проводимого лечения состояние больного значительно улучшилось – отмечено увеличение массы тела, признаки пневмонии разрешились.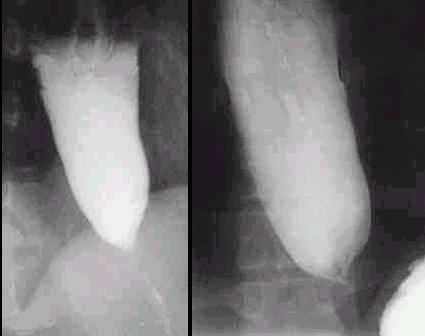 После стабилизации состояния выполнена видеолапароскопическая передняя продольная эзофагокардиомиотомия по Геллер, передняя гемиэзофагофундопликация по Дор.
После стабилизации состояния выполнена видеолапароскопическая передняя продольная эзофагокардиомиотомия по Геллер, передняя гемиэзофагофундопликация по Дор.
В послеоперационном периоде больной в течение 5 дней находился в отделении реанимации по причине сопутствующей миокардиодистрофии, сердечной недостаточности, выраженной гипотонии. Проводилась коррекция сопутствующей патологии.
Рисунок 18. Манометрия больного АП IV стадии до оперативного лечения (объяснение в тексте)
Питание осуществляли через назогастральный зонд. После стабилизации состояния больной переведен в общую палату. В послеоперационном периоде на 6 сутки назогастральный зонд удален. После чего пациент стал питаться кашицеобразной пищей, явлений дисфагии не было. Выписан в удовлетворительном состоянии. При контрольном обследовании через 1 год жалоб не предъявлял, дисфагии не было. По данным рентгенологического исследования (Рис. 176)- пищевод содержит немного слизи, гипотоничен, контуры четкие, в нижней трети деформация контура вследствие выполненной фундопликационной манжетки.
 Проходимость в области кардии свободная, просвет пищевода до 5,0 см. Эвакуация контрастного вещества в желудок не затруднена.
Проходимость в области кардии свободная, просвет пищевода до 5,0 см. Эвакуация контрастного вещества в желудок не затруднена.По результатам ФЭГДС слизистая оболочка пищевода розовая, просвет пищевода расширен, пищи натощак нет. Кардия свободно проходима для фиброгастроскопа 9,8 мм в диаметре.
Приведем пример тактики ведения больной АП IV стадии с пищевым завалом. Больная среднего возраста, поступила с жалобами полную непроходимость пищевода для пищи любой консистенции которая развилась постепенно, втечение 3 суток. Из анамнеза выяснено, что первые признаки затрудненного прохождения пищи по пищеводу появились 5 лет назад. Тогда больная была обследована, установлен диагноз АП, от направления на специализированное лечение отказалась из-за слабовыраженных симптомов.
Больная госпитализирована в дежурное отделение оториноларингологии с диагнозом инородное тело пищевода: пищевой завал. Выполнена рентгенография пищевода – пищевод резко расширен до 9,0 см. Впросвете пищевода неравномерное затемнение зернистой структуры.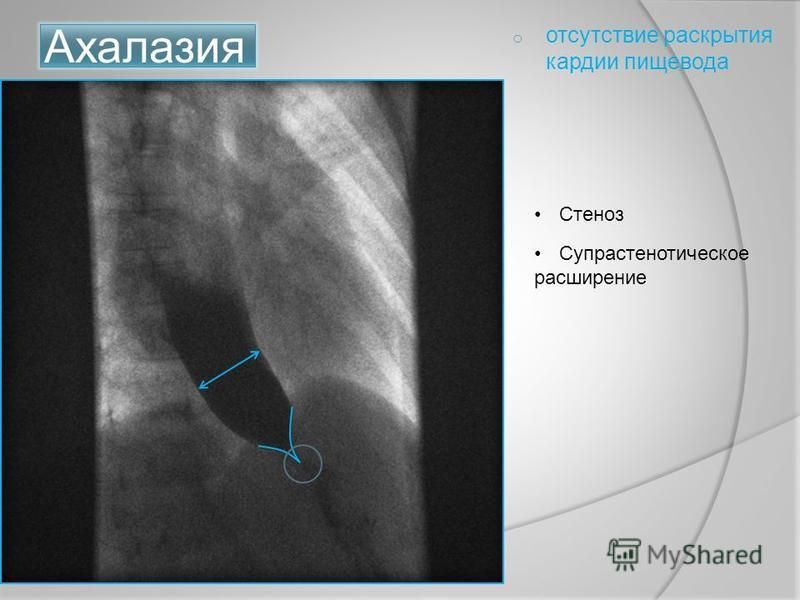 Заключение: рентгенологическая картина пищевого завала (Рис. 19). Попытка промывания пищевода оказалась не эффективной. На следующие сутки больная была переведена в нашу клинику. При поступлении больная нормостенического телосложения, нормального питания, ИМТ 21,4 кг/м2. При осмотре в передней области шеи контурировалось выпячивание расположенное ниже уровня щитовидного хряща до яремной вырезки грудины, шириной около 7 см (расширенный пищевод).
Заключение: рентгенологическая картина пищевого завала (Рис. 19). Попытка промывания пищевода оказалась не эффективной. На следующие сутки больная была переведена в нашу клинику. При поступлении больная нормостенического телосложения, нормального питания, ИМТ 21,4 кг/м2. При осмотре в передней области шеи контурировалось выпячивание расположенное ниже уровня щитовидного хряща до яремной вырезки грудины, шириной около 7 см (расширенный пищевод).
По лабораторным данным гипопротеинемия – общий белок плазмы 59,4 г/л. При ЭФГДС аппарат удалось ввести только до области глоточно-пищеводного перехода – пищевод был забит пищевыми массами. Во время исследования у больной развился приступ ларингобронхоспазма, острая дыхательная недостаточность, что потребовало проведения интенсивной терапии. После улучшения состояния проведено промывание пищевода с помощью толстого желудочного зонда, при котором было удалено около 3 литров пищи. Выполнена ФЭГДС, во время которой пройти в желудок не удалось – просвет пищевода значительно расширен на всем протяжении, слизистая серовато-розовая с налетом фибрина, в области кардии пищевой комок.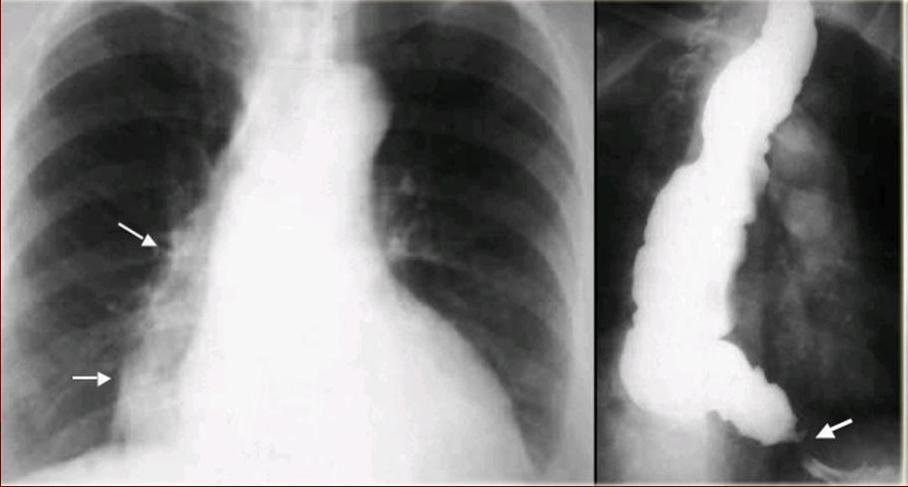
Попытка удалить инородное тело струйным промыванием через биопсийный канал фиброгастроскопа, а также биопсийными щипцами не удалась. Выполнена эзофагоскопия жестким эзофагогастроскопом, при которой удалось удалить из кардии фрагменты пищи с помощью эндоскопического аспиратора-ирригатора, после чего был установлен назогастральный зонд. Учитывая данные анамнеза, поставлен диагноз: Ахалазия пищевода IV стадии. Пищевой завал. Алиментарная недостаточность легкой степени.
После стабилизации состояния, на 7 сутки после поступления выполнена Видеолапароскопическая эзофагокардиомиотомия по Геллер, эзофагофундопликация по Дор.
Послеоперационный протекал период без осложнений. На 3 сутки выполнена рентгеноскопия пищевода – пищевод содержит слизь в большом количестве, просвет его 6,0 см, эвакуация своевременна, происходит струйно, небольшими количествами. К моменту выписки через 9 дней пациентка питалась кашицеобразной пищей. Явления дисфагии отсутствовали.
Рисунок 19.
 Рентгенограмма пищевода больной до оперативного лечения больной с диагнозом АП IV стадии, пищевой завал (объяснение в тексте)
Рентгенограмма пищевода больной до оперативного лечения больной с диагнозом АП IV стадии, пищевой завал (объяснение в тексте)
Пациентка обследована через 1 год – питается без ограничений, редко отмечает чувство тяжести за грудиной после употребления твердой пищи. Рентгенологическое исследование – пищевод расширен до 4,0 см. В просвете пищевода пристеночные скопления слизи. Кардия функционирует, проходима.
Эвакуация из пищевода не затруднена. Суточная внутрипищеводная рН-метрия – без патологических изменений.
Эндоскопическое исследование и манометрия пищевода не выполнены из-за выраженного рвотного рефлекса.
В.И. Оскретков, Д.В. Балацкий, А.А. Гурьянов
Опубликовал Константин Моканов
Ахалазия кардии
- Врачи
- Лечение
- Диагностика
- Статья обновлена: 18 июня 2020
Ахалазия кардии – это хроническое нервно-мышечное заболевание, при котором не происходит рефлекторного раскрытия отверстия на границе желудка и пищевода при глотании. В результате нарушается перистальтика и тонус пищевода и прохождение пищи по нему.
В результате нарушается перистальтика и тонус пищевода и прохождение пищи по нему.
Ахалазия кардии (от латинского а – отсутствие, chalasia) – это хроническое нервно-мышечное заболевание, при котором не происходит рефлекторного раскрытия кардии (отверстия на границе желудка и пищевода) при глотании. В результате нарушается перистальтика и тонус пищевода и прохождение пищи по нему. Впервые заболевание описано T. Willis в 1672 г., но до сих пор причина его возникновения неизвестна.
Симптомы ахалазии кардии
Основными симптомами заболевания являются нарушение проглатывания пищи (дисфагия), срыгивание и пищеводная рвота и боль за грудиной. Дисфагия вначале возникает эпизодически на фоне стресса или при поспешной еде, затем становится постоянной и препятствует прохождению по пищеводу не только твердой пищи, но и жидкой (бульон, сок, вода). Невозможность проглотить пищу приводит к пищеводной рвоте – обратному поступлению пищи в глотку и рот при наклоне туловища и в положении лежа, особенно ночью во время сна. Это опасно, так как существует риск попадания содержимого пищевода в дыхательные пути, что может вызвать кашель, приступы удушья, аспирационную пневмонию. Боль за грудиной возникает при переполнении пищевода или вследствие гипермоторики (усиления перистальтики) грудного отдела пищевода. Нередко на фоне заболевания отмечается снижение массы тела, причем значительное.
Это опасно, так как существует риск попадания содержимого пищевода в дыхательные пути, что может вызвать кашель, приступы удушья, аспирационную пневмонию. Боль за грудиной возникает при переполнении пищевода или вследствие гипермоторики (усиления перистальтики) грудного отдела пищевода. Нередко на фоне заболевания отмечается снижение массы тела, причем значительное.
Осложнения ахалазии
Наиболее частым осложнением ахалазии является застойный эзофагит (воспаление пищевода), который может привести к развитию рака пищевода. Также расширенный пищевод может сдавливать возвратный и блуждающий нервы, правый бронх, верхнюю полую вену. Ахалазия может провоцировать хронические неспецифические заболевания легких вследствие аспирации пищи в дыхательные пути, приводить к образованию дивертикулов пищевода игрыжи пищеводного отверстия диафрагмы.
Диагностические обследования
Диагностировать заболевание можно на основании данных рентгеноскопического (обзорный снимок органов грудной клетки и более информативная рентгеноскопия с контрастированием пищевода взвесью сульфата бария) или эндоскопического исследования.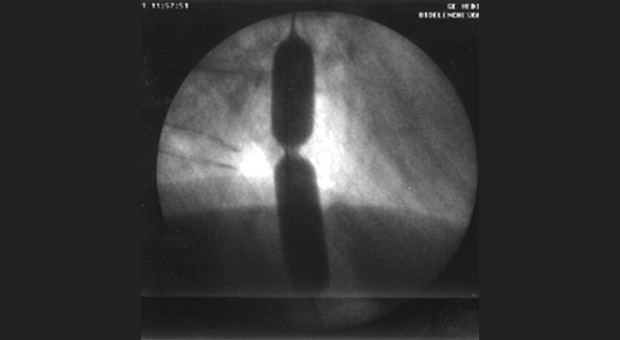 Большую ценность для постановки диагноза ахалазии имеет эзофагоманометрия. Как дополнительный метод используют фармакологические пробы с внутримышечным введением растворов карбахолина или ацетилхолина.
Большую ценность для постановки диагноза ахалазии имеет эзофагоманометрия. Как дополнительный метод используют фармакологические пробы с внутримышечным введением растворов карбахолина или ацетилхолина.
Лечение и профилактика болезни
Лечение заболевания проводят препаратами, нормализующими моторику пищевода. Для профилактики и лечения воспаления пищевода (эзофагита) рекомендуется частое (4-5 раз в день) питание, умеренно-щадящая диета (избегать острой, жареной, слишком горячей или холодной пищи, исключить алкоголь), прием обволакивающих, вяжущих средств. Больные должны избегать чрезмерных физических и психологических нагрузок. Также выполняется интенсивное растяжение кардии (дилатация) с помощью специального баллона. Эффект дилатации обычно сохраняется на протяжении 8-12 лет и более, при повторном появлении симптомов процедуру выполняют повторно. Пациенты с ахалазией кардии, в том числе и после дилатации, должны состоять на диспансерном учете у гастроэнтеролога.
Источники
- Zhang B.
 , Wang Y., Liao Y., Zhang J., Wu Y., Xiao T., Zhang Y., Bao Y., Qiu H., Sun S., Guo J. Advances in The Diagnosis and Treatment of Achalasia of The Cardia: a Review. // J Transl Int Med – 2021 – Vol9 – N1 – p.24-31; PMID:33850798
, Wang Y., Liao Y., Zhang J., Wu Y., Xiao T., Zhang Y., Bao Y., Qiu H., Sun S., Guo J. Advances in The Diagnosis and Treatment of Achalasia of The Cardia: a Review. // J Transl Int Med – 2021 – Vol9 – N1 – p.24-31; PMID:33850798 - Liu D., Liu YY., Chen JX., Song L., Zhou YY., Ullah S., Zhao LX., Hai B., Zheng QF., Li DY., He DZ., Liu BR. Influence of esophageal morphology on the clinical efficacy of peroral endoscopic myotomy in treating advanced achalasia cardia. // Exp Ther Med – 2021 – Vol21 – N3 – p.196; PMID:33488805
- C S N., B L D. Laparoscopic esophago-gastrostomy in the management of achalasia cardia – A case report. // Int J Surg Case Rep – 2020 – Vol76 – NNULL – p.335-337; PMID:33207406
- Nabi Z., Karyampudi A., Nageshwar Reddy D. Esophageal hyposensitivity in achalasia cardia: Do we finally have an answer? // United European Gastroenterol J – 2020 – Vol8 – N9 – p.1128-1129; PMID:33151834
- Jain M., Baijal N., Srinivas M., Baijal R., Pratap N., Bachkaniwala V.
 , Ganesh P., Venkataraman J. Retrospective study on symptoms and treatment modalities used and short-term follow up of achalasia cardia in Indian setting. // JGH Open – 2020 – Vol4 – N5 – p.856-859; PMID:33102755
, Ganesh P., Venkataraman J. Retrospective study on symptoms and treatment modalities used and short-term follow up of achalasia cardia in Indian setting. // JGH Open – 2020 – Vol4 – N5 – p.856-859; PMID:33102755 - Bale M., Modi A., Parshad R., Suhani S., Makharia G., Sharma R. Long-term Outcomes of Laparoscopic Heller’s Cardiomyotomy in Achalasia Cardia With Megaesophagus. // Surg Laparosc Endosc Percutan Tech – 2020 – Vol31 – N2 – p.175-180; PMID:32890251
- Patil G., Dalal A., Maydeo A. Early outcomes of peroral endoscopic myotomy with fundoplication for achalasia cardia – Is it here to stay? // Dig Endosc – 2020 – Vol – NNULL – p.; PMID:32691889
- Mandavdhare HS., Samanta J., Varma P., Kumar-M P., Gupta P., Singh H., Dutta U., Kochhar R. Per oral endoscopic myotomy with fundoplication is a technically feasible NOTES for achalasia cardia. // Minim Invasive Ther Allied Technol – 2020 – Vol – NNULL – p.1-6; PMID:32608297
- Siow SL., Mahendran HA., Najmi WD., Lim SY.
 , Hashimah AR., Voon K., Teoh KH., Boo HS., Chuah JS., Nurazim S., Faqihuddin MH. Laparoscopic Heller myotomy and anterior Dor fundoplication for achalasia cardia in Malaysia: Clinical outcomes and satisfaction from four tertiary centers. // Asian J Surg – 2021 – Vol44 – N1 – p.158-163; PMID:32423838
, Hashimah AR., Voon K., Teoh KH., Boo HS., Chuah JS., Nurazim S., Faqihuddin MH. Laparoscopic Heller myotomy and anterior Dor fundoplication for achalasia cardia in Malaysia: Clinical outcomes and satisfaction from four tertiary centers. // Asian J Surg – 2021 – Vol44 – N1 – p.158-163; PMID:32423838 - Danielyan SN., Abakumov MM., Tatarinova EV., Gasanov AM. [Difficulties of differential diagnosis and treatment of achalasia cardia after previous hiatal hernia repair]. // Khirurgiia (Mosk) – 2020 – Vol – N2 – p.79-83; PMID:32105260
Ахалазия кардии и кардиоспазм > Клинические рекомендации РФ 2013-2017 (Россия) > MedElement
Лабораторные исследования
Всем пациентам с ахалазией кардии необходимо выполнить общий анализ крови (определение уровня эритроцитов, гемоглобина, лейкоцитов, тромбоцитов), оценить коагулограмму (для определения риска развития кровотечения перед выполнением пневмокардиодилатации или оперативным вмешательством), установить уровень сывороточного креатинина и альбумина, провести общий анализ мочи (определение кетоновых тел, которые обнаруживают в моче при длительном голодании).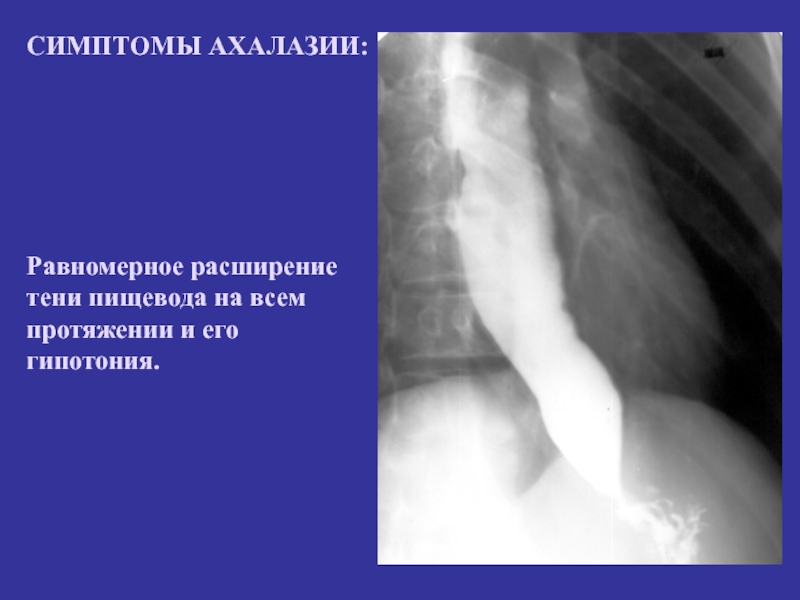
Инструментальные исследования
Для подтверждения диагноза идиопатической ахалазии необходимо использовать инструментальные методы обследования, такие как рентгенография пищевода с контрастированием, ЭГДС и манометрия, которая признана «золотым стандартом» диагностики. Некоторые авторы рекомендуют перед проведением рентгеноконтрастного исследования выполнить обзорную рентгенографию грудной клетки, по результатам которой можно определить наличие уровня жидкости в средостении, обусловленного застоем пищевых масс в пищеводе, а также выявить расширение средостения и отсутствие газового пузыря желудка. Рентгеноконтрастное исследование выполняют с бариевой взвесью, при этом оценивают степень расширения пищевода, его деформацию (S-образный пищевод), длительность задержки контрастной массы в пищеводе, рельеф абдоминального отдела пищевода и области пищеводно-желудочного перехода в момент открытия кардиоэзофагеального сфинктера, наличие или отсутствие газового пузыря желудка и некоторые другие параметры (рис. 1).
1). Рис. 1. Рентгенограммы пищевода.
Умеренное расширение пищевода, длительная задержка в нем бариевой взвеси. Раскрытия кардии при проглатывании контрастного вещества не происходит, оно начинает поступать в желудок тонкой струей лишь при значительном наполнении пищевода, заметны слабые неперистальтические сокращения, не смыкающие стенки пищевода (данные Клиники пропедевтики внутренних болезней, гастроэнтерологии, гепатологии УКБ № 2 ФГБОУ ВО «Первый МГМУ им. И.М. Сеченова»)
У больных с кардиоспазмом при рентгенологическом исследовании выявляют усиление моторики пищевода с выраженными сегментарными сокращениями, при ахалазии кардии — снижение моторной активности пищевода (отсутствие первичной перистальтики в дистальных 2/3 пищевода). При обеих формах заболевания просвет пищевода расширен, иногда может иметь С- или S-образную форму, типичной находкой является конусовидное сужение в области НПС, похожее на мышиный хвостик или птичий клюв, отмечается замедление эвакуации контрастного вещества из пищевода в желудок.
Для определения стадии заболевания предложены многочисленные классификации, например четырехстадийная классификация кардиоспазма Б.В. Петровского (1962), классификация Т.А. Суворовой (1966), впоследствии дополненная А.Л. Гребеневым (1987), в которой выделены два типа ахалазии пищевода; трехстадийная классификация кардиоспазма, предложенная Г.Д. Вилявиным (1978). Однако наибольшее распространение получила классификация Б.В. Петровского:
I стадия — функциональный непостоянный спазм кардии без расширения пищевода;
II стадия — стабильный спазм кардии с нерезко выраженным расширением пищевода и усиленной моторикой стенок;
III стадия — рубцовые изменения (стеноз) мышечных слоев НПС с выраженным расширением пищевода и нарушениями тонуса и перистальтики;
IV стадия — резко выраженный стеноз кардии со значительной дилатацией, удлинением, S-образной деформацией пищевода, эзофагитом и периэзофагитом.
Для ахалазии кардии характерна положительная проба Хурста, когда начало опорожнения пищевода происходит вне акта глотания и зависит от высоты столба бариевой взвеси, при повышении гидростатического давления НПС раскрывается и контрастное вещество «проваливается» в желудок.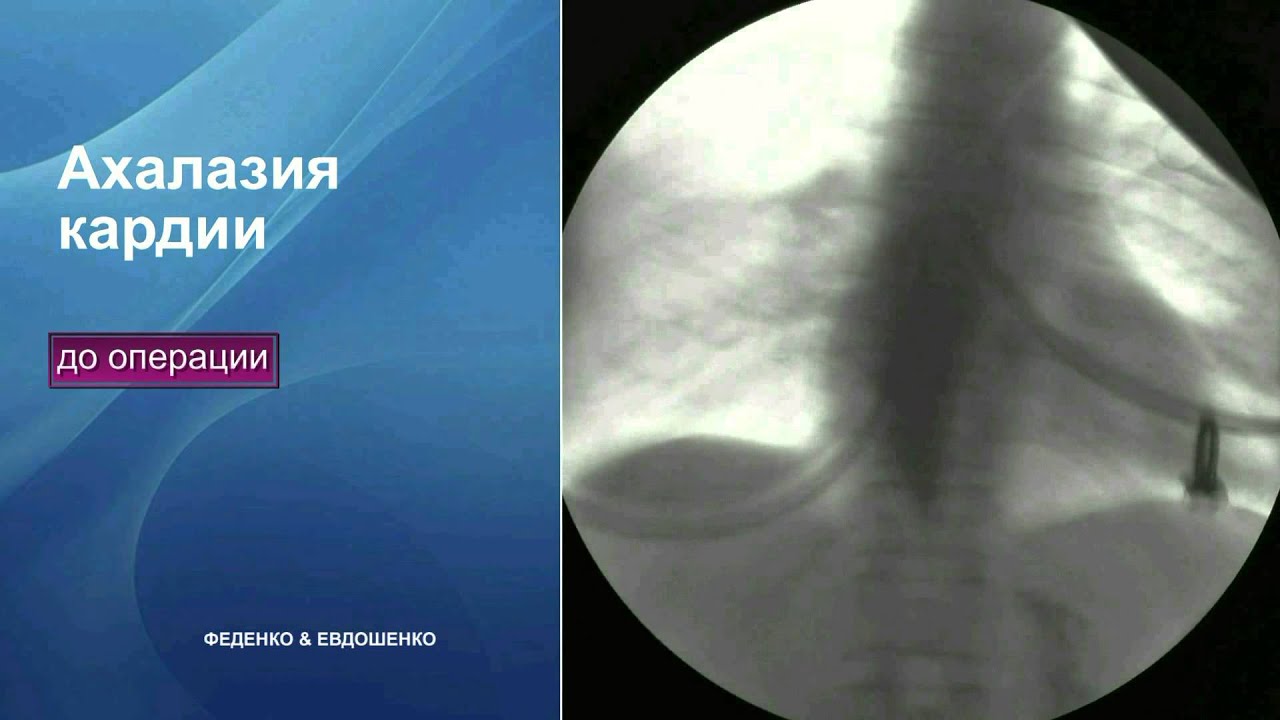
При проведении контрастного исследования важное значение имеют фармакологические пробы. Широкое распространение получила проба с нитроглицерином: через некоторое время после введения бариевой взвеси пациент помещает под язык 1–2 таблетки нитроглицерина, что при ахалазии приводит к снижению тонуса НПС и быстрому продвижению контрастного вещества из пищевода в желудок. Проводят также пробы с карбахолином и ацетилхолином, при введении которых возникают непропульсивные беспорядочные сокращения мускулатуры в грудном отделе пищевода и повышается тонус НПС, что приводит к длительной задержке бариевой взвеси в пищеводе. Похожий эффект дает введение синтетического аналога холецистокинина синкалида, который в норме расслабляет НПС, однако из-за утраты тормозящих нейронов развивается парадоксальный эффект в виде его стойкого сокращения, что вызывает задержку контрастного вещества в пищеводе.
При возникновении подозрения на наличие ахалазии кардии необходимо провести ЭГДС с целью исключения псевдоахалазии, которую выявляют у 2–4% пациентов с диагнозом ахалазии. При эндоскопическом исследовании в первую очередь обращают внимание на степень дилатации и девиации просвета пищевода, наличие в нем остатков пищи, принятой накануне, жидкости и слизи. Одновременно оценивают состояние слизистой оболочки пищевода, ее толщину, цвет, блеск, определяют наличие перистальтики.
При эндоскопическом исследовании в первую очередь обращают внимание на степень дилатации и девиации просвета пищевода, наличие в нем остатков пищи, принятой накануне, жидкости и слизи. Одновременно оценивают состояние слизистой оболочки пищевода, ее толщину, цвет, блеск, определяют наличие перистальтики.
После визуализации кардии, которую не всегда легко осуществить при значительно деформированном пищеводе, оценивают ее положение относительно оси пищевода, наличие воспалительных и рубцовых изменений слизистой оболочки в этой зоне, эластичность стенок, равномерность раскрытия кардии при инсуффляции воздуха и возможность проведения эндоскопа в желудок. Необходимым условием обеспечения безопасности исследования является выполнение его только под визуальным контролем, исключая проведение аппарата «вслепую» через остатки пищи и слизь, так как в этом случае высока опасность перфорации стенки пищевода, измененной в результате хронического воспалительного процесса.
Заключительный этап эндоскопического исследования включает тщательный осмотр желудка и двенадцатиперстной кишки и обязательный ретроградный осмотр кардии для исключения кардиоэзофагеального рака.
Стадию заболевания целесообразно определять, основываясь на следующих критериях [8].
При I стадии заболевания эндоскопических изменений просвета пищевода, перистальтики, состояния слизистой оболочки, положения кардии и ее открытия выявить не удается.
При II стадии определяется умеренное (до 3–4 см) расширение просвета пищевода; остатков пищи в пищеводе, как правило, нет, может быть небольшое количество прозрачной жидкости или слизи; слизистая оболочка гладкая, ровная, блестящая, ее складки расположены продольно; перистальтика усилена; кардия расположена по центру, обычно плотно сомкнута, но достаточно легко раскрывается при избыточной (по сравнению с обычным эндоскопическим исследованием) инсуффляции воздуха (рис.
 2). При ретроградном осмотре складки в области пищеводно-желудочного перехода плотно обхватывают эндоскоп, слизистая оболочка мягкая, эластичная.
2). При ретроградном осмотре складки в области пищеводно-желудочного перехода плотно обхватывают эндоскоп, слизистая оболочка мягкая, эластичная. Рис. 2. Эндофото.
Наличие пенистой слизи и остатков пищи в расширенном пищеводе (данные Клиники пропедевтики внутренних болезней, гастроэнтерологии, гепатологии УКБ № 2 ФГБОУ ВО «Первый МГМУ им. И.М. Сеченова»)
В III стадии кардиоспазма и ахалазии кардии пищевод расширен до 4–8 см, в его просвете остатки жидкой и твердой пищи, много слизи. Перистальтика очень вялая или «рваная» из-за снижения мышечного тонуса пищевода, вследствие чего формируются четкообразные участки — неравномерное расширение просвета на разных уровнях. В дистальном отделе пищевода отмечается начинающаяся S-образная деформация, из-за чего кардия расположена эксцентрично, отклоняясь вначале вправо от продольной оси пищевода, а затем немного влево. Вторая часть изгиба становится более выраженной при прогрессировании болезни. Выраженный изгиб свидетельствует о начинающемся удлинении пищевода, что проявляется в увеличении расстояния от резцов до кардии: вместо 38– 40 см в норме 41–45 см или более. Кардия, как правило, плотно сомкнута, раскрывается при избыточной инсуффляции воздуха. Слизистая оболочка пищевода несколько утолщена, может быть гиперемирована в дистальном отделе.
Вторая часть изгиба становится более выраженной при прогрессировании болезни. Выраженный изгиб свидетельствует о начинающемся удлинении пищевода, что проявляется в увеличении расстояния от резцов до кардии: вместо 38– 40 см в норме 41–45 см или более. Кардия, как правило, плотно сомкнута, раскрывается при избыточной инсуффляции воздуха. Слизистая оболочка пищевода несколько утолщена, может быть гиперемирована в дистальном отделе.
При IV стадии заболевания просвет пищевода значительно расширен (часто более 8–10 см), пищевод удлинен и извит, имеет вид неперистальтирующего мешка вследствие отсутствия мышечного тонуса. В просвете содержится большое количество жидкости и остатков пищи. Слизистая оболочка утолщена, рыхлая, местами имеет крупноячеистый вид, иногда с эрозиями, обусловленными длительным стазом пищи или развитием кандидозного эзофагита, отмечается поперечная складчатость слизистой оболочки из-за удлинения и растяжения пищевода. Очень часто пищевод заканчивается «слепым мешком», заполненным остатками пищи, а кардия резко смещена в сторону и, как правило, находится выше дна этого «мешка». Расстояние от резцов до кардии в ряде случаев значительно увеличено — от 45 до 70 см. Часто она сомкнута неплотно, возможны рубцовые изменения слизистой оболочки.
Очень часто пищевод заканчивается «слепым мешком», заполненным остатками пищи, а кардия резко смещена в сторону и, как правило, находится выше дна этого «мешка». Расстояние от резцов до кардии в ряде случаев значительно увеличено — от 45 до 70 см. Часто она сомкнута неплотно, возможны рубцовые изменения слизистой оболочки.
Визуализация кардии при III и особенно IV стадиях кардиоспазма может быть затруднена из-за большого количества содержимого в пищеводе и резкой деформации просвета, так как могут наблюдаться несколько изгибов пищевода. Однако необходимо отметить, что при любой стадии ахалазии кардии, в отличие от органического стеноза на уровне пищеводно-желудочного перехода (злокачественная опухоль или рубцовая стриктура), удается провести эндоскоп в желудок без сопротивления. Затруднения связаны не с преодолением спазма как такового, а с удлинением пищевода и формированием одного или нескольких «колен», в том числе в верхней трети, и эксцентричным положением кардии. Если же для проведения эндоскопа через кардию требуется заметное усилие или осуществить его не удается, отмечается выраженное «побеление» стенок пищевода и пищеводно-желудочного перехода из-за ригидности, необходимо заподозрить опухолевый характер стеноза.
Рис. 3. Кардиоспазм II стадии.
а — рентгенограмма; б — эндофото (данные ФГБНУ «РНЦХ им. акад. Б.В. Петровского»). Рис. 4. Кардиоспазм III стадии.
а — рентгенограмма; б — эндофото (данные ФГБНУ «РНЦХ им. акад. Б.В. Петровского»)
Рис. 5. Кардиоспазм IV стадии.
а — рентгенограмма; б — эндофото (данные ФГБНУ «РНЦХ им. акад. Б.В. Петровского»).
Рис. 6. Подтягивание НПС и укорочение грудного отдела пищевода у пациента с ахалазией кардии.
Сплошная стрелка — истинное расположение НПС, пунктирная — подтягивание НПС (данные Клиники пропедевтики внутренних болезней, гастроэнтерологии, гепатологии УКБ № 2 ФГБОУ ВО «Первый МГМУ им. И.М. Сеченова»)
Рис. 7. Три типа ахалазии кардии.
а — I тип; б — II тип; в — III тип (данные Клиники пропедевтики внутренних болезней, гастроэнтерологии, гепатологии УКБ № 2 ФГБОУ ВО «Первый МГМУ им. И.М. Сеченова»)
Чикагская классификация нарушений моторики пищевода
| Ахалазия | Тип I Тип II Тип III Нарушение проходимости кардии |
Заболевания, связанные с нарушением моторики | Диффузный эзофагоспазм Чрезмерная интенсивность сокращений (DCI >8000 — «отбойный молоток») Гипокинезия/отсутствие сокращений |
Изменения перистальтики | Нарушение перистальтики с большими разрывами Нарушение перистальтики с малыми разрывами Незавершенная перистальтика Ускоренные сокращения Гиперкинезия грудного отдела пищевода («пищевод щелкунчика») |
Для всех типов заболевания характерны повышение суммарного давления расслабления (выше 15 мм рт. ст.) и отсутствие перистальтической волны сокращения грудного отдела пищевода, при этом давление покоя (Resting Pressure) может быть повышено или в пределах нормальных значений (норма 10–35 мм рт. ст.). При I типе (классическая ахалазия кардии) при 100% влажных глотков отсутствует любая перистальтика грудного отдела пищевода. При ахалазии кардии II типа отсутствует нормальная перистальтическая волна сокращения, однако наблюдается равномерное спастическое сокращение умеренной интенсивности по всей длине пищевода от верхнего до нижнего пищеводного сфинктера более чем при 20% влажных глотков. Ахалазия кардии III типа характеризуется отсутствием нормальной перистальтической волны, наличием отдельных эпизодов перистальтики в грудном отделе пищевода или преждевременными спастическими сокращениями (дистальный эзофагоспазм), зарегистрированными более чем при 20% влажных глотков.
Истинную ахалазию кардии следует отличать от феномена нарушения проходимости кардии, при котором повышается суммарное давление расслабления НПС, однако сохраняется нормальная перистальтика грудного отдела пищевода или отмечается снижение интенсивности сокращения в этом отделе с малыми разрывами.
Наилучших результатов лечения достигают у пациентов с ахалазией II типа. В то же время отсутствие перистальтики (I тип) и выраженную гипермоторную дискинезию грудного отдела пищевода (III тип) можно рассматривать в качестве прогностических критериев высокого риска рецидива ахалазии кардии после кардиодилатации.
MedWeb – Диетический стол № 1
Диетический стол № 1
Диетический стол № 1 Диета при заболеваниях ЖКТ характеризуется менее строгим соблюдением принципов щадящего воздействия на слизистую оболочку желудка по сравнению с диетами № 1а, 1б.Показания к диетическому столу № 1
Диета № 1 предписана при язвенной болезни желудка (язве желудка) и двенадцатиперстной кишки (в период затухающего обострения, при нерезком обострении, в период выздоровления и ремиссии), при остром гастрите в период выздоровления, при хроническом гастрите с нормальной и повышенной секрецией, при хроническом гастрите с секреторной недостаточностью в стадии обострения, а так же при заболеваниях пищевода (ГЭРБ, пептический эзофагит, эзофагоспазм, ахалазия кардии и т.д.).
При язве и гастрите с нормальной и повышенной секрецией диета применяется в течение 3–5 месяцев.
Цель диетического стола № 1
Целью диеты № 1 является, в первую очередь, ускорение заживления эрозий, язв, уменьшение воспалений слизистых оболочек желудка и кишечника. Диета направлена на нормализацию секреции желудка и улучшение моторики желудка и кишечника.
Общая характеристика диетического стола № 1
Диета № 1 полностью удовлетворяет физиологические потребности человека в энергии и питательных веществах как в условиях стационара, так и в случае амбулаторного лечения (при условии работы, не связанной с физической нагрузкой).
Диетический стол № 1 обеспечивает умеренное щажение желудка от механического, химического и температурного раздражения. Щадящий режим достигается путем ограничения блюд, имеющих сильное воздействие на стенки и слизистую желудочно-кишечного тракта. Из рациона исключаются блюда, возбуждающие секрецию, трудноперевариваемые продукты, а также блюда, химически раздражающие слизистые оболочки, очень горячие и очень холодные блюда. Пищу следует тщательно пережевывать.
Диета № 1 предусматривает дробный режим приема пищи 5–6 раз в сутки, небольшими порциями. Перерыв между приемами пищи не должен превышать 4 часов. Прием пищи прекращается за 1–1,5 часа до сна, перед сном допускается стакан молока или нежирных сливок.
Большинство блюд диетического стола № 1 жидкие, протертые, пюрированные, кашицеобразные. Разрешено употребление рыбы и мягкого мяса целым куском. Способ приготовления – отваривание или на пару. Допускается запекание без корочки.
Сокращается употребление продуктов, богатых клетчаткой: бобовых, белокочанной капусты, некоторых корнеплодов (репа, редька, редис), незрелых ягод, твердых фруктов и фруктов с грубой кожицей, хлеба из муки грубого помола. Исключены мясные хрящи, кожа птицы и рыбы, мясная шкурка.
Химический состав и энергоценность диетического стола № 1
Белки: 85–90 г (не менее 50% белков животного происхождения).
Жиры: 70–80 г (не менее 30% жиров растительного происхождения).
Углеводы: 300–330 г (не более 40 г простых углеводов).
Суточная калорийность: 2 200–2 400 ккал.
Свободная жидкость: 1,5–2 л.
Поваренная соль: 6–8 г.
Витамины: ретинол (А) 2 мг, рибофлавин (В2) 4 мг, тиамин (В1) 4 мг, никотиновая кислота (В3) 30 мг.
Макроэлементы: кальций 0,8 г, магний 0,5 г, фосфор 1,6 г.
Микроэлементы: железо 15 мг.
Оптимальная температура блюд: от 15 до 62 градусов Цельсия.
Рекомендуемые продукты и блюда диетического стола № 1
Хлеб: из пшеничной муки высшего сорта, подсушенный или вчерашний, сухие бисквиты и печенье, несдобные булочки, печеные пирожки с творогом, джемом, яблоками, отварным мясом.
Супы: молочные супы, протертые крупяные супы на овощном бульоне, вермишелевый суп на слабом курином бульоне, овощные супы-пюре, суп-крем. Заправляют супы сливочным маслом или яично-молочной смесью.
Мясные блюда: отварные или приготовленные на пару из говядины, телятины, постной баранины, свинины, курицы, индейки, кролика. Предпочтительны паровые котлеты, пюре, тефтели, кнели, биточки, суфле. Допускаются бефстроганов из отварного мяса, отварной язык, отварное мягкое мясо куском.
Рыбные блюда: отварная рыба нежирных сортов куском или в виде котлет, суфле и т. д.
Гарниры: отварные овощи (картофель, морковь, цветная капуста, свекла, тыква, кабачок, изредка зеленый горошек), отварные макаронные изделия, полувязкие или протертые рис, греча.
Каши: манная, гречневая, рисовая, овсяная на воде или молоке, полувязкие или протертые; крупяные пудинги, суфле на молоке.
Молочные продукты: молоко, сливки, простокваша, некислые ацидофилин, кефир, сметана и творог; молочные суфле, вареники, пудинги, паровые или запеченные сырники, периодически неострый сыр ломтиками.
Яйца: всмятку или паровой омлет (не более 2 яиц в день).
Закуски: салаты из отварных овощей, язык, докторская колбаса, заливная рыба, паштет из печени, вымоченная нежирная сельдь.
Соусы: бешамель без пассировки муки, сметана, кисели, фруктовые соусы.
Сладкие блюда: желе, пюре, кисели из фруктов и ягод, протертый компот, мед, зефир, пастила, безе, сливочный крем, варенье, некислые джемы.
Напитки: слабый чай (можно с молоком), некрепкое какао, некрепкий кофе с молоком, сладкие компоты, отвар шиповника, сладкие соки.
Жиры: несоленое сливочное масло, топленое масло, рафинированное растительное масло.
Исключаемые продукты и блюда диетического стола № 1
Из рациона следует исключить продукты, вызывающие болевые ощущения, возбуждающие секрецию, раздражающие стенки ЖКТ.
А именно: соленья, копченья, консервы, маринады, приправы, соусы, газированные напитки (в том числе квас). Исключают также крепкие чай и кофе, крепкие мясные и рыбные бульоны, жареные и тушеные блюда, грибы, свежий хлеб, ржаной хлеб, сдобное тесто, кислые молочные продукты, острые сыры, грубые крупы (пшено, кукуруза, ячневая и перловая крупы), щавель, лук, огурцы, помидоры, бобовые, белокочанную капусту, шпинат, репу, редьку, редис, кислые фрукты и ягоды.
Примерное меню диетического стола № 1
Первый завтрак: овсяная молочная каша, вареники со сметаной, компот.
Второй завтрак: печеные яблоки с сахаром.
Обед: молочная вермишель, тефтели из индейки с цветной капустой, чай.
Полдник: сухой бисквит, кисель.
Ужин: отварная рыба с картофельным пюре, чай с молоком.
На ночь: сливки.
Варианты диетического стола № 1
Диетический стол № 1А, диетический стол № 1Б, диетический стол № 1Р (расширенный).
Источники:
- Приказ Министерства здравоохранения Российской Федерации № 330 «О мерах по совершенствованию лечебного питания в лечебно-профилактических учреждениях РФ» от 05.08.2003
Рецепты диетического стола № 1:
- яйцо куриное вареное всмятку
- каша рисовая молочная
- отвар шиповника
- суп овсяный молочный
- фрикадельки мясные паровые
- морковное пюре
- мусс фруктовый
- рыба отварная, запеченная под молочным соусом
- картофельное пюре
- паровой омлет
- каша гречневая рассыпчатая
- яблоко печеное с сахаром
- суп рисовый молочный
- суфле мясное паровое с картофельным пюре
- желе яблочное
- суфле творожное паровое
- кисель фруктовый
- каша манная молочная
- творожный пудинг
- суп картофельный вегетарианский
- мясо отварное, запеченное под соусом бешамель
- морковь отварная
- компот из разваренных сухофруктов
- несдобная булочка
- рулет морковно-яблочный
- ленивые вареники со сметаной
- овсяная молочная каша
- молочный суп с вермишелью
- кнели из мяса индейки с гарниром из отварной цветной капусты
- ягодный мусс
- груша печеная с сахаром
- суп-пюре из овощей
- судак отварной
- вермишель
- мясное суфле
- творожная запеканка
- отварной кролик
- карп отварной под соусом бешамель
- салат овощной
Ахалазия пищевода лечение
Ахалазия пищевода – редкое заболевание, встречающееся у одного человека на 100 тысяч. Первые упоминания о болезни приходятся на 1672 год. Характерной особенностью ахалазии пищевода является отсутствие рефлекса, вызывающего раскрытие кардии при глотании. Заболеванию сопутствует понижение тонуса пищевода в грудинном отделе и проблемы с перистальтикой кишечника. Чаще всего ахалазию пищевода диагностируют у 40-50-летних пациентов, преимущественно у женщин, более склонных к заболеванию. У детей она встречается крайне редко и составляет 3,9% от общего числа пациентов. Эндоскопия пищевода один из способов обследования и выявления заболевания.
Что способствует заболеванию ахалазией
Конкретную причину, вызывающую развитие заболевания, специалисты не называют. Связывают его с инфекциями, сдавливанием пищевода, воспалениями, опухолями злокачественного происхождения, инфильтративными поражениями и т.д. В детском возрасте ахалазию пищевода обнаруживают обычно после пяти лет.
Первые проявления заболевания остаются незамеченными, поэтому диагностируется оно с опозданием. Если у ребенка дисфагия и после приема пищи у него начинается рвота, необходимо бить тревогу. Это распространенные симптомы, характерные для ахалазии.
Часто встречающиеся симптомы
В симптоматике ахалазии главной считается дисфагия, встречающаяся почти у всех заболевших. Время между появлением первых симптомов и визитом к доктору может составлять от одного до десяти лет. Второй по распространенности признак – застойные явления в пищеводе. Проявляется кашлем и приступами удушья ночью.
Изжога и болезненные ощущения в грудной клетке также могут быть признаками ахалазии. Локализуясь в основном за грудиной, сжимающие или сдавливающие боли ощущаются в нижней челюсти, шее и спине. Нередко ахалазию ошибочно принимают за желудочно-пищеводный рефлюкс или другое заболевание, сопровождающееся изжогой. Если она возникает не от еды и не проходит после употребления антацидных препаратов, есть вероятность, что проблема имеет отношение к ахалазии пищевода.
Какие бывают осложнения
При ахалазии во всем организме происходят необратимые изменения. Среди наиболее распространенных осложнений, связанных с заболеванием пищевода, называют:
- рак плоскоклеточный;
- безоары;
- объемные образования на шее;
- отслаивающийся подслизистый слой;
- дивертикул дистального отдела;
- варикозное расширение вен;
- заболевание легких;
- перикардит гнойный;
- пневмоперикард и др.
При продолжительном протекании заболевания пищевод расширяется, истончаются его стенки, что и становится причиной осложнений. У страдающих ахалазией в большинстве случаев (85%) отмечают заметное снижение веса.
Как диагностировать ахалазию пищевода
Обструкция кардии и несущественная дилятация проксимального отдела наблюдается на всех стадиях заболевания. Характерные признаки прогрессирующей болезни можно увидеть на рентгеновских снимках. Заметным становится расширение пищевода, в нижнем отделе которого наблюдается сужение и клювовидное расширение в месте сужения.
Клинические признаки заболевания характерные, но нередко при обследовании пациентов после 50 лет их принимают за раннюю стадию рака пищевода. Наиболее эффективной для диагностики ахалазии является эзофагоскопия. Заболевание подтверждается изучением функциональных особенностей пищевода.
В нем выявляется дилятация просвета, сопровождаемая пониженным давлением. Также отсутствует перистальтика после глотания, а по всей протяженности пищевода поднимается давление. Точность диагноза подтверждает не раскрытый эзофагеальный сфинктер. У некоторых пациентов нарушения, связанные с отсутствием перистальтики, приводят к диффузному спазму. После глотания спазмы повторяются и усиливаются.
Как лечат ахалазию
Медикаментозному лечению заболевание поддается с трудом, оно лишь облегчает симптомы. Назначают щадящую диету, витаминные и седативные препараты, антиспастики. Терапию медикаментами проводят лишь с целью временного облегчения, но не излечения заболевания.
Форсировать расширение кардии можно при помощи дилятатора. Используются приборы механического, пневматического или гидростатического действия. Самыми распространенными и безопасными считаются пневматические.
Зонд с прикрепленным на его конец баллоном вводится в желудок. Процесс отслеживается при помощи рентгенологического исследования. Попадая в желудок, воздух надувает баллон и вытягивает его наружу. Так происходит расширение просвета пищевода.
При использовании дилятации симптомы исчезают у 80% больных, что говорит об эффективности метода. Применение механического устройства в 6% случаев может вызывать разрыв слизистой или стенок пищевода. При использовании эластичного дилятатора риск снижается до 1%.
Если лечение не эффективно, понадобится хирургическое вмешательство. Наиболее актуальной на сегодняшний день считают двустороннюю кардиомиотомию – продольное рассечение мышц дистального отдела пищевода. В некоторых случаях делается только передняя кардиомиотомия.
Операция дает шанс излечиться 90% больных. Отрицательные последствия имеют отношение в основном к рубцеванию. Этот метод предпочтителен при лечении запущенной детской ахалазии.
Это изжога, ГЭРБ или еще хуже?
Что такое Ахаласия?
Ахалазия возникает, когда процессы, перемещающие пищу в желудок, не работают должным образом. Чтобы пища и жидкости перешли изо рта в желудок, после глотания должны произойти две вещи. Во-первых, пищевод, трубка, по которой пища попадает в желудок, должна перемещать пищу, сжимая и расслабляя ее. Как только пища достигает желудка, небольшой мышечный лоскут или клапан в нижней части пищевода должен открыться, чтобы позволить пище вытечь в желудок.
Если у вас ахалазия, ни один из этих процессов не работает должным образом. Пищевод не может выталкивать пищу вниз. Кроме того, клапан не открывается полностью. Это приводит к тому, что пища попадает в основание пищевода, как забитая раковина, и вымывается обратно в рот.
Ахалазия встречается редко. Его получит примерно 1 из 100 000 человек. На развитие могут уйти годы, и некоторые люди годами игнорируют симптомы, прежде чем обратиться к врачу. Хотя это состояние нельзя вылечить, лечение поможет вам с ним жить.
Причины ахалазии
Эксперты не уверены, почему возникает ахалазия. Но возможные причины:
- Передается от ваших родителей (генетика)
- Аутоиммунные проблемы
- Вирусная инфекция
- Потеря нервной функции (нейродегенеративная)
Факторы риска ахалазии
Люди всех рас могут получить ахалазию. Он одинаково встречается у мужчин и женщин. В основном это происходит у людей от 30 до 60 лет, хотя иногда бывает и у детей.Ахалазия иногда наблюдается у людей с синдромом Дауна.
Симптомы ахалазии
Самым большим симптомом ахалазии является затруднение глотания жидкостей и твердой пищи.
У людей с этим заболеванием также могут быть:
- Боль в груди, особенно после еды
- Пища возвращается в горло
- Изжога и отрыжка
- Потеря веса
- Ночной кашель
- Рвота
- Пневмония от дыхательной пищи в легкие
Прием пищи в течение 4 часов перед сном может усугубить симптомы.Такие продукты, как мясо и хлеб, также могут вызывать проблемы.
Диагноз ахалазии
Поскольку симптомы ахалазии очень похожи на изжогу, ваш врач может сначала вылечить вас от изжоги. Если это не сработает, они, вероятно, проверит вас на ахалазию.
Они могут заглянуть в ваше горло с помощью специального инструмента, называемого эндоскопом. К нему прикреплена крошечная камера, прикрепленная к длинной трубке, чтобы врач мог видеть ваш пищевод.
Проба с проглатыванием бария является обычным скрининговым тестом на ахалазию.Так называется манометрия. Когда вы делаете глотки воды, врач вводит вам в горло тонкую трубку, чтобы проверить силу мышц пищевода. Он также измеряет, насколько хорошо работает ваш желудочный клапан.
Лечение ахалазии
Хирургия
Хирургия – наиболее успешное лечение ахалазии. С хирургическим вмешательством большинство людей получают долгосрочное облегчение симптомов.
Самая распространенная процедура называется миотомией Хеллера. В большинстве случаев это делается с помощью телескопа с камерой и фонарем, а также других инструментов.Врач делает несколько крошечных надрезов на животе и хирургическими инструментами достигает той области, над которой ему нужно работать. Цель операции – открыть часть нижнего отдела пищевода, чтобы облегчить глотание. Обычно это очень успешно.
Другой вариант хирургического вмешательства называется пероральной эндоскопической миотомией или ПОЭМ. С помощью этой процедуры врачам не нужно вырезать за пределами тела. Вместо этого врач вставляет эндоскоп (небольшой инструмент с камерой на конце) в рот и в глотку.Как только они заглянут внутрь, они сделают небольшой надрез на внутренней поверхности пищевода. Они проходят через него, чтобы достичь внутренней мышцы нижней части пищевода, где они делают еще один разрез. Это помогает облегчить глотание.
Обе операции обычно проходят успешно. Но у некоторых людей они могут вызвать кислотный рефлюкс.
Ваш врач обсудит, какая процедура подойдет вам лучше всего.
Другие виды лечения
Вам может не потребоваться операция по поводу ахалазии.Есть вещи, которые могут помочь, но обычно они не работают. И вам, возможно, придется пройти несколько процедур.
Некоторые варианты:
Инъекции расслабляющего мышцы лекарства. Ваш врач вводит ботокс (ботулинический токсин) в напряженные мышцы пищевода. Это помогает временно расслабить мышцы, чтобы вы могли нормально глотать.
Растяжение пищевода (пневматическое расширение). Врач вставляет баллон в клапан между пищеводом и желудком и надувает его, чтобы растянуть напряженные мышцы.Эта процедура может понадобиться вам несколько раз, прежде чем она поможет.
Лекарства. Два класса препаратов, нитраты и блокаторы кальциевых каналов, обладают расслабляющим действием на мышцы LES. Эти препараты могут уменьшить симптомы у людей с ахалазией.
Ваш врач может также ввести в пищевод лекарство, которое поможет лучше усваивать пищу. Но это длится от 6 месяцев до года.
Лучшее лечение для вас зависит от многих вещей. Ваш врач может помочь вам решить, что вам нужно.
Жизнь с ахалазией
Специальной диеты при этом заболевании не существует, но вы можете самостоятельно выяснить, какие продукты легче проходят через пищевод.
Может помочь пить больше воды во время еды. Иногда также помогают газированные напитки, например кола. Карбонизация, кажется, помогает продвигать пищу по пищеводу.
Если у вас тяжелая ахалазия, на какое-то время лучшим выбором будет жидкая диета. Всегда говорите со своим врачом о правильных питательных веществах, если вы не едите твердую пищу.Если вы сильно похудеете, обязательно сообщите об этом своему врачу, потому что это может означать, что вы недоедаете.
Некоторые люди с ахалазией подвержены риску рака пищевода. По этой причине очень важно регулярно посещать врача.
Повторное питание после операции по ахалазии
Жизнь после операции на ахалазии
Тако.
Пицца.
Стейк среднего размера с начинкой из печеного картофеля.
«И хрустящее яблоко», – добавил Дориан Брантли.«Я ела яблочное пюре, но тут нет сравнения».
Это были главные пункты в списке Брантли, что нужно есть в первую очередь после операции по поводу ахалазии – редкого заболевания пищеварительной системы, из-за которого трудно есть или пить.
После успешной эндоскопической процедуры 35-летняя Брантли с радостью заполнила свой список блюд.
История пациента Дориана Брантли с ахалазией
Около года назад Брантли, медсестра из Калифорнийского университета в Чикаго, заметила, что, похоже, пища проходит по ее пищеводу очень долго.Сначала она подумала, что, может быть, ее порции слишком велики или она ела слишком быстро.
Но состояние становилось все более и более неудобным. И вскоре и употребление твердой пищи, и питье жидкости вызвали боль.
«Если бы мои пациенты сказали мне это, я бы очень обеспокоилась», – подумала она.
Диета ахалазии
Брантли попробовал мягкую диету, но это не помогло. Тест с глотанием бария в Калифорнийском университете в Чикаго показал, что ее пищевод не функционирует должным образом.
Гастроэнтерологи выполнили эндоскопию верхних отделов желудка, чтобы исключить рак желудка или пищевода.Роберт Кавитт, доктор медицины, магистр здравоохранения, затем провел манометрию пищевода – тест, который измеряет мышечные сокращения – и подтвердил диагноз ахалазии. Вместо того чтобы расслабиться, чтобы пропустить пищу, гладкий мышечный клапан на нижнем конце пищевода Брантли (нижний пищеводный сфинктер) все время оставался закрытым.
Эндоскопический подход предлагает пациентам быстрое выздоровление, отсутствие рубцов и короткое пребывание в больнице.
Причина ахалазии неизвестна, это прогрессирующее и необратимое заболевание.Это может привести к серьезным проблемам с легкими и недоеданию. Брантли похудел на 30 фунтов с июня по октябрь.
Даже будучи медсестрой, Брантли никогда не слышала об ахалазии. «Мои врачи ответили на все мои вопросы и успокоили меня», – сказала она.
ПОЭМ хирургия ахалазии
В конце октября 2017 года Брантли перенесла эндоскопическую процедуру под названием пероральная эндоскопическая миотомия (ПОЭМ). В пищевод Брантли через ее рот был помещен гибкий зонд, и между слоями пищевода был создан туннель, ведущий к нижнему сфинктеру, где мышцы были разрезаны, и клапан навсегда открылся.
Эндоскопический подход предлагает пациентам быстрое выздоровление, отсутствие рубцов и короткое пребывание в больнице.
Восстановление после операции на ахалазии
После процедуры Брантли сначала беспокоился о том, чтобы вернуться к твердой пище.
«Но мои коллеги, друзья и семья побуждали меня« пойти и поесть еще раз », – сказал Брантли. «Вы знаете, что я сделал. Все было восхитительно ».
Лечение ахалазии
Clin Exp Gastroenterol.2011; 4: 33–41.
Лука Дугера
1 Отделение внутренних болезней, перистальтики и эндоскопии,
Микеле Чиаверина
1 Отделение внутренних болезней, перистальтики и эндоскопии,
Лука Каччиотелла, Отделение подвижности и эндоскопии 1
,
Fabio Cisarò
2 Отделение гастроэнтерологии и гепатологии, Медицинское отделение, Госпиталь Сан-Джованни Баттиста, Турин, Италия
1 Отделение внутренних болезней, моторики и эндоскопии,
2 Отделение гастроэнтерологии и гастроэнтерологии Отделение медицины, больница Сан-Джованни Баттиста, Турин, Италия
Для корреспонденции: Лука Дугера, Отделение моторики и эндоскопии, Больница Сан-Джованни Баттиста, Виа Генова, 3 10121 Турин, Италия, тел. +3911 633 6762, факс +3911 661 4652, электронная почта ти[email protected] Авторские права © 2011 Dughera et al, издатель и лицензиат Dove Medical Press Ltd.Это статья в открытом доступе, разрешающая неограниченное некоммерческое использование при условии правильного цитирования оригинальной работы.
Эта статья цитируется в других статьях в PMC.Abstract
Сообщалось о нескольких теориях этиологии и патофизиологии ахалазии, но на сегодняшний день широко признано, что потеря перистальтики и отсутствие вызванной глотанием релаксации нижнего сфинктера пищевода являются основными функциональными аномалиями.Лечение ахалазии часто направлено на облегчение симптомов ахалазии, а не на коррекцию основного заболевания. Медикаментозная терапия неэффективна, поэтому пациентам, которые являются хорошими кандидатами на хирургическое вмешательство, следует предложить либо лапароскопическую миотомию, либо дилатацию с помощью пневматического баллона. Их собственные предпочтения должны быть включены в процесс принятия решений, а лечение должно соответствовать местным специалистам в этих процедурах. Лапароскопическая хирургическая эзофагомиотомия – безопасный и эффективный метод. Его можно рассматривать как начальное лечение или как вторичное лечение, если пациент не отвечает на менее инвазивные методы лечения.Пневматическая дилатация зарекомендовала себя как безопасный, эффективный и долговечный метод лечения, выполняемый опытными людьми, и, по-видимому, является наиболее рентабельной альтернативой. Для пациентов с множественными сопутствующими заболеваниями и пожилых пациентов, которые не подходят для хирургического вмешательства, эндоскопическая инъекция ботулинического токсина должна считаться безопасной и эффективной процедурой. Однако его положительный эффект со временем ослабевает, и необходимо учитывать необходимость многократных повторных сеансов.В ведении пациентов с ахалазией важную роль играют аспекты питания. Когда изменения образа жизни недостаточны, необходимо перейти к чрескожной гастростомии под рентгенологическим контролем. В будущем, возможно, станут возможными варианты внутрипросветной миотомии или эндоскопической мукозэктомии. Необходимы дальнейшие исследования для изучения роли иммуносупрессивной терапии в тех случаях, когда подозревается аутоиммунная этиология.
Ключевые слова: ахалазия, пищеводный сфинктер, ботулинический токсин А, дилатация
Введение
Ахалазия – редкое моторное заболевание пищевода и нижнего пищеводного сфинктера.Более конкретно, это нервно-мышечное заболевание, характеризующееся дегенеративными изменениями миэнтериального сплетения, ведущими к избирательной потере тормозных нервных окончаний. Последствиями этого повреждения являются необратимое нарушение перистальтических сокращений и нарушение расслабления нижнего сфинктера пищевода в ответ на глотание. 10 / 100,000. Первичная ахалазия у детей является частью синдромов Аллгроува и Альпорта и чаще встречается при синдроме Дауна.2
Вторичная ахалазия имеет общие клинические признаки с первичной ахалазией, но всегда есть идентифицируемая причина. Во всем мире наиболее частой причиной вторичной ахалазии является протозойная инфекция, вызываемая Trypanosoma cruzi , обнаруженная в Центральной и Южной Америке. Описана связь с человеческими лейкоцитарными антигенами класса II3,4 и некоторыми вирусными инфекциями5. Аутоиммунный патогенез при ахалазии поддерживается благодаря описанию антител к антимиэнтерическим нейронам у подгруппы пациентов.6
Когда ахалазия вызвана инфильтрацией нижнего сфинктера пищевода, злокачественными новообразованиями или такими заболеваниями, как амилоидоз, или в результате паранеопластического синдрома, используется термин псевдоахалазия. Злокачественные новообразования приводят к псевдоахалазии, чаще всего в результате прямой инвазии в пищевод и нижний сфинктер пищевода (чаще всего аденокарцинома желудочно-кишечного тракта, а также овсяноклеточная карцинома, бронхогенная карцинома, плоскоклеточная карцинома пищевода или поражение лимфоидных клеток) или феномен паранеопластической опухоли нижних отделов пищевода. пищеводный сфинктер.
Ахалазная картина может быть имитирована осложнениями хирургического вмешательства на желудочно-пищеводном переходе, которые могут привести к нарушению прохождения содержимого пищевода в желудок и его дилатации, например, фундопликации, бандажированию желудка, а также в результате повреждения блуждающего нерва. .7
С клинической точки зрения ахалазия – это прогрессирующее заболевание, которое проявляется симптомами дисфагии как в отношении жидкой, так и твердой пищи, болью в груди и срыгиванием непереваренной пищи, которое возникает во время еды, вскоре после этого или через несколько часов, когда пациент меняется. в положение лежа.Более незаметные симптомы включают замедление скорости еды и растяжку или движение из стороны в сторону, а также ходьбу после еды для выполнения болюсного прохождения через неперистальтический пищевод и через гипертонический нижний сфинктер пищевода. Аспирация пищи из пищевода может привести к пневмонии. Снижение веса и недоедание – явление редкое, но они могут возникать при запущенной стадии заболевания и у пожилых пациентов.
Всем пациентам с дисфагией следует пройти эндоскопию верхних отделов желудочно-кишечного тракта и рентгенологию, чтобы исключить анатомические поражения в качестве первого диагностического шага.8 Диагностическая точность обеспечивается только манометрическими исследованиями пищевода в более чем 96% случаев, демонстрирующих типичную картину как первичной ахалазии, так и псевдоахалазии.9
Лечение ахалазии традиционно основывалось на хирургическом подходе. Появление малоинвазивной хирургии с более коротким пребыванием в больнице, снижением заболеваемости и более быстрым возвращением к повседневной деятельности делает этот вариант еще более привлекательным. Напротив, есть доказательства того, что некоторые медицинские и нехирургические стратегии могут быть полезными для многих пациентов с этим расстройством.В этом обзоре обобщены текущие знания и перспективы лечения ахалазии.
Патофизиология
Хотя полное описание сложных и все еще плохо изученных механизмов, лежащих в основе ахалазии, не является целью этого обзора, их краткое изложение полезно для понимания обоснования различных вариантов лечения.
Отличительным признаком ахалазии является невозможность полного расслабления нижнего пищеводного сфинктера. Механизм релаксации нижнего сфинктера пищевода сложен и требует скоординированного взаимодействия нервов, гладких мышц, интерстициальных клеток Кахаля (ICC) и гормонов.Скоординированные перистальтические волны, которые перемещают пищевой комок через дистальный отдел пищевода, зависят от возбуждающего и тормозящего воздействия местных кишечных рефлексов, которые возникают в кишечном нервном сплетении и от внешних парасимпатических нервов. Перистальтический рефлекс включает холинергическую и пептидную возбуждающую нейротрансмиссию, что приводит к сокращению как круговой, так и продольной мышцы проксимальнее болюса, которому предшествует аборальное расслабление перед болюсом. В то время как ацетилхолин опосредует большую часть нейротрансмиссии между блуждающим нервом и внутренними нейронами, похоже, что более одного нейромедиатора играет роль между тормозящим нейроном тонкой кишки, ICC и гладкими мышцами.Было предложено множество медиаторов, но основным ингибирующим фактором является оксид азота.10,11 Таким образом, нейроны, высвобождающие оксид азота, являются мишенью при идиопатической ахалазии. Триггерное событие, которое приводит к дегенерации ганглиозных клеток при ахалазии, до сих пор неясно, но потеря нейронов, секретирующих оксид азота, приводит к дисбалансу между возбуждающими и тормозными нейронами мышечно-кишечного сплетения, вызывая необратимые манометрические изменения у таких пациентов.12,13
Внутримышечные ICC были четко идентифицированы в нижнем сфинктере пищевода.14 ICC в желудочно-кишечном тракте выполняют несколько различных функций, выступая в качестве кардиостимуляторов, генераторов фактора гиперполяризации гладких мышц, 15 в качестве механических датчиков, 16 и в качестве медиаторов нейротрансмиссии.17 Вместе с потерей нейронов кишечника сокращается их количество. ICC в области нижнего пищеводного сфинктера также сообщалось при идиопатической ахалазии.18,19 В то время как ICC играют установленную роль в передаче азота и холинергической нейротрансмиссии в других областях желудочно-кишечного тракта, определяя роль ICC в нормальной функции нижнего пищеводного сфинктера. потребуется дальнейшая работа.
Варианты лечения
Лечение ахалазии направлено на расслабление или механическое разрушение нижнего сфинктера пищевода. Ахалазия – довольно редкое заболевание, поэтому существует несколько рандомизированных и контролируемых клинических испытаний, чтобы определить оптимальную стратегию лечения. Безопасность, эффективность и долговечность существующих вариантов лечения сильно различаются.
Развитие ахалазии происходит в первую очередь из-за сопротивления прохождению болюса через плохо расслабляющий и открывающийся нижний сфинктер пищевода.Если не лечить ахалазию, разовьется расширенный пищевод с тяжелым нарушением транзита болюса, и это состояние сигнализирует о высоком риске аспирационной пневмонии или перфорации. Таким образом, целью лечения ахалазии является ранняя диагностика и лечение до достижения этой конечной стадии, когда операция становится обязательной, но обычно с плохим результатом. Обзор текущих терапевтических возможностей при ахалазии представлен в.
Таблица 1
Текущие терапевтические возможности при ахалазии
| Терапевтические методы | Способ действия | Побочные эффекты | ||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Ингибирование мышечного сокращения, индукция расслабления, способствует опорожнению пищевода | Гипотония, головная боль, сонливость | ➢ Блокаторы кальциевых каналов (нифедипин, верапамил) | -ингибиторы фосфоразы силденафил) | Индукция высвобождения NO, снижение давления LES | Гипертония, стенокардия | Эндоскопическая терапия | ➢ Ботулотоксин (инъекция LES в мышечный слой) | Мощное ингибирование высвобождения ацетилхол ине улучшает пассивное опорожнение пищевода | Возможно и безопасно в амбулаторных условиях; Миотомия геллера могла быть более сложной у пациентов, перенесших повторные инъекции | ➢ Пневматическое расширение гипертонической зоны LES | Направлено на перелом собственных мышечных волокон | Перфорация или разрыв пищевода, кровотечение, местная боль | Хирургия | ➢ Лапароскопическая миотомия Хеллера плюс антирефлюксная фундопликация | Глубокое разрушение мышечных гипертонических волокон в LES | Хотя наиболее «патофизиологическое» решение является дорогостоящим; возможные послеоперационные осложнения | Хронический гастроэзофагеальный рефлюкс и синдром Барретта ➢ Эзофагогастрэктомия с интервалом желудка или толстой кишки | Полная модификация анатомии LES; оставить для терминальной стадии | Очень инвазивный, возможные тяжелые осложнения | | ||||||||
Фармакологическая терапия
Фармакологическая терапия для лечения ахалазии будет предпочтительнее более инвазивных вариантов лечения.К сожалению, такое лечение не устраняет основной процесс заболевания, а лишь временно приводит к расслаблению нижнего сфинктера пищевода и может улучшить симптомы. В настоящее время медикаментозная терапия включает нитраты, блокаторы кальциевых каналов и доноры оксида азота в попытке облегчить расслабление нижнего сфинктера пищевода и / или усилить перистальтику пищевода.
Блокаторы кальциевых каналов и нитраты, обычно принимаемые за 30–60 минут до еды, традиционно были в центре внимания фармакологической терапии.Блокаторы кальциевых каналов подавляют клеточный захват кальция, и, поскольку внутриклеточный кальций необходим для сокращения нижнего сфинктера пищевода, происходит расслабление. Блокаторы кальциевых каналов оценивались при долгосрочном лечении ахалазии, но использование этих препаратов часто вызывает толерантность, что со временем сильно снижает эффекты. Было показано, что нифедипин вызывает длительную ремиссию и даже нормализацию физиологии у меньшинства пациентов. Было показано, что верапамил снижает давление нижнего сфинктера пищевода, но не продемонстрировал значимого симптоматического улучшения.20–23
Нитратная терапия действует, противодействуя снижению тормозящего нейромедиатора, оксида азота. Это приводит к снижению тонуса нижнего сфинктера пищевода с последующим снижением давления нижнего сфинктера пищевода. Было показано, что сублингвальный прием изосорбида динитрата снижает давление базального нижнего сфинктера пищевода и улучшает опорожнение пищевода.24 Недавний метаанализ использования нитратов в лечении ахалазии показал слишком мало контролируемых исследований с разнородными данными. и о значительных побочных эффектах, о которых сообщалось, поэтому было невозможно рекомендовать клиническое использование этих препаратов для лечения этого заболевания.25 Поскольку у нитратов побочные эффекты более выражены, блокаторы кальциевых каналов по-прежнему используются более широко. обобщены данные и результаты хронических проспективных и контролируемых исследований с участием блокаторов кальциевых каналов и нитратов при ахалазии.
Таблица 2
Клинические исследования блокаторов кальциевых каналов и нитратов при ахалазии
| Автор | Лекарство | Пациенты (кол-во пациентов) | Эффективность (%) 9006 | вверх (месяцев)|||||
|---|---|---|---|---|---|---|---|---|
| Gelfonc 1981 | Изосорбид | 24 | 79 | 2–19 | ||||
| Silverstein 1982 | Diltiazem | 902902 1982 | Нифедипин | 15 | 53 | 8–18 | ||
| Бортолотти и др. 19 | Нифедипин | 20 | 90 | 65–80 | 6 | |||
| Кочча 1992 | Нифедипин | 14 | 77 | 21 | ||||
| Триадафилопулос и др. 20 | Нифедипин | 14 | NA | 10 | ||||
| Триадафилопулос и др. Ингибитор 5-фосфодиэстеразы, который снижает распад циклического GMP, второго посредника, опосредующего индуцированную оксидом азота релаксацию, был предложен в качестве альтернативного фармакологического агента для лечения ахалазии.Экспериментальные данные демонстрируют его способность снижать тонус нижнего сфинктера пищевода и остаточное давление26. Необходимы дальнейшие исследования, чтобы определить, может ли это иметь клиническую ценность при ахалазии. Хотя клинические рекомендации по лечению ахалазии до сих пор отсутствуют, мы можем предположить, что фармакологические методы лечения в настоящее время имеют очень ограниченную ценность в лечении. Однако использование нифедипина сублингвально перед едой, по-видимому, остается исключительно показанным для пациентов, не желающих или неспособных пройти какие-либо другие процедуры и / или ожидающих более окончательной терапии, или в качестве поддерживающего лечения при рефрактерной боли в груди. Эндоскопическая терапияНа сегодняшний день основным методом эндоскопической терапии ахалазии является инъекция ботулинического токсина А в нижний сфинктер пищевода. Ботулинический токсин А является мощным ингибитором высвобождения ацетилхолина, который оказывает возбуждающее влияние на тонус нижнего сфинктера пищевода. Инъекция ботулинического токсина А в нижний сфинктер пищевода улучшает «пассивное» опорожнение пищевода, уравновешивая избирательную потерю тормозящих нейронов в кишечном сплетении, снижая давление нижнего сфинктера пищевода и увеличивая раскрытие нижнего сфинктера пищевода по сравнению с инъекцией плацебо.27,28 Средняя продолжительность эффекта от однократной инъекции ботулинического токсина А составляет 10–12 месяцев с широкой вариабельностью от трех месяцев до трех лет. Причина такой вариабельности неизвестна, но, вероятно, связана с другим недостатком токсина, а именно с развитием аутоиммунного ответа с выработкой антител, которые, в свою очередь, могут снизить его эффективность у некоторых пациентов. Ботулинический токсин А 80–100 Ед вводят через иглу 5 мм в нижний сфинктер пищевода, а аликвоты 20–25 Ед токсина вводят в четыре квадранта нижнего сфинктера пищевода.Процедура не более сложна, чем обычная эндоскопия, и, за исключением периодических жалоб на преходящую боль в груди, пациенты ее переносят очень хорошо. Они могут пойти домой после того, как оправятся от седативных препаратов, и им разрешат есть мягкую пищу в течение дня. Симптоматическое улучшение наступает постепенно и обычно достигает пика через 1–3 дня, хотя у случайных пациентов это может быть отложено еще больше. После однократного лечения ботулиническим токсином А облегчение симптомов было зарегистрировано почти у 80% пациентов.Через шесть месяцев у 50% пациентов может сохраниться ремиссия, в то время как другим потребуются повторные инъекции или другие варианты лечения, такие как пневматическая дилатация или хирургическая миотомия. Annese28 сообщил об успехе в 68% через 24 месяца после повторного введения инъекции ботулинического токсина A, в то время как Pasricha29 обнаружил 30% эффективность после среднего периода наблюдения в течение двух лет. Инъекция ботулинического токсина А кажется простой и безопасной, без какого-либо риска перфорации.30 Оценка после лечения показала, что ни давление нижнего сфинктера пищевода перед лечением, ни амплитуда сокращений пищевода, ни продолжительность заболевания не могут быть использованы для прогнозирования результата. инъекции ботулинического токсина А.Вместо этого было обнаружено, что молодой возраст и мужской пол отрицательно влияют на результат. Хирурги сообщают, что миотомия Геллера может быть более сложной у пациентов, которые подвергаются повторной инъекции ботулинического токсина А из-за повышенной адгезии мышечного слоя, но до сих пор этот терапевтический вариант должен быть выбран в качестве первого шага для всех пациентов. кто имеет право на это.31 Напротив, ботулинический токсин А широко продемонстрирован как наиболее эффективный вариант лечения у пожилых пациентов или пациентов с сопутствующими заболеваниями, у которых дилатация или хирургическое вмешательство представляют собой высокий риск.32 Было обнаружено, что при однократной инъекции пожилым людям облегчение симптомов длится до 1-2 лет. Исторически пневматическая дилатация была первой попыткой лечения ахалазии пищевода и была описана в 1674 году сэром Томасом Уиллисом.32 Пневматическая дилатация нижнего сфинктера пищевода у пациентов с ахалазией направлена на разрушение волокон собственной мышечной ткани. Бужирование или «стандартный» баллон для расширения обычно неэффективны, но было показано, что пневматическое расширение с помощью жесткого баллона большого размера через нижний сфинктер пищевода является эффективным и довольно недорогим.На сегодняшний день сильное расширение нижнего сфинктера пищевода считается наиболее эффективным нехирургическим методом лечения ахалазии, хотя детали процедуры различаются в разных учреждениях. Хотя нет четкого консенсуса по техническим деталям баллонной дилатации, большинство ведущих операторов использовали свою собственную технику пневматической дилатации, переданную от опытных врачей младшим врачам. Стационарное и амбулаторное лечение, седативное или неседатированное расширение, используемое седативное средство, расширительная система, начальный размер баллона, скорость, давление, продолжительность, количество расширений за эндоскопический сеанс и время повторных расширений различаются от центра к центру.34–37 Обычно пневматическое расширение выполняется по проволочному проводнику под рентгеноскопическим контролем. Это позволяет оценить прогресс дилатации по мере исчезновения суженной «талии» нижнего сфинктера пищевода. Однако, помимо радиационного облучения, это требует громоздкого и дорогого рентгеноскопического оборудования, которое может быть востребовано или недоступно для общего использования. Выполнение пневматической дилатации под прямой эндоскопической визуализацией является хорошей альтернативой рентгеноскопическому контролю.После размещения расширителя над проволочным проводником эндоскоп снова вводят в пищевод. Эффекты размещения и расширения баллона наблюдаются проксимальнее баллона. Этот метод применялся более 20 лет 38, и Американское общество гастроинтестинальной эндоскопии предположило, что любой метод визуализации приемлем для безопасной дилатации при ахалазии. 39 Серьезные осложнения после пневматической дилатации редки. Наиболее серьезным осложнением является перфорация пищевода, частота которой в среднем составляет около 2.5% .40 Гастроэзофагеальный рефлюкс – наиболее частое хроническое осложнение после расширения нижнего сфинктера пищевода при ахалазии. С помощью 24-часового мониторинга pH и манометрии пищевода можно определить патофизиологическую подгруппу рефлюкса, поскольку он почти всегда связан с гипотензивным нижним пищеводным сфинктером и неэффективной моторикой тела пищевода.41 Некоторые исследователи спорят о роли ботулина. инъекция токсина А по сравнению с пневматическим расширением. В недавнем Кокрановском обзоре шести рандомизированных контролируемых исследований, включающих 178 пациентов, оценивали рецидив симптомов после дилатации пищевода по сравнению с эндоскопической инъекцией ботулинического токсина А через один, шесть и 12 месяцев после лечения.Тридцать процентов пациентов, перенесших дилатацию, испытали рецидив симптомов и неэффективность лечения через 12 месяцев по сравнению с 74% пациентов, получавших ботулинический токсин A.42 Кроме того, систематический обзор и метаанализ 105 статей, в которых сообщалось о 761 пациенте с ахалазией, перенесших эндоскопическое лечение с дилатацией пищевода или ботулиническим токсином А показало, что облегчение симптомов было лучше при дилатации, и необходимость в дальнейшем лечении значительно снижалась.43 ХирургияМинимально инвазивные хирургические методы резко изменили алгоритм лечения ахалазии.Преимущество менее инвазивного, безопасного и эффективного хирургического метода побуждает гастроэнтерологов выбирать пациентов для операции раньше, поскольку это устраняет необходимость в расширении.44,45 В настоящее время стандартным хирургическим лечением ахалазии является сначала лапароскопическая миотомия Геллера. сообщалось в 1991 году.46 Этот метод связан с большим уменьшением дисфагии, более коротким пребыванием в больнице, меньшим риском послеоперационного гастроэзофагеального рефлюкса и низкой частотой осложнений.47 Антирефлюксная процедура может дополнительно снизить частоту послеоперационной изжоги на 80%, а также риск эзофагита и язвенной болезни.Фундопликация Дор или Тупе снижает рефлюкс так же, как и процедура Ниссена, но частичные обертывания имеют тенденцию к уменьшению дисфагии. Частота дисфагии, связанная с фундопликацией, колеблется от 0% до 8%. Отсутствие улучшения при дилатации предполагает неполную миотомию и необходимость повторной манометрии. Оптимальная длина кардиомиотомии не менее 2 см. Хотя о фундопликации Дор чаще сообщается, выбор Тупе или Дор зависит от предпочтений хирурга. 48 Существует очень мало рандомизированных проспективных исследований, изучающих эзофагомиотомию в сравнении с пневматической дилатацией.49 Одно исследование показало эквивалентную эффективность в облегчении симптомов на начальном этапе, но при последующем наблюдении оно показало, что у пациентов, перенесших эзофагомиотомию, рецидивирующих симптомов было меньше, чем у пациентов с пневматической дилатацией. Последние предварительные данные большого и мощного многоцентрового рандомизированного клинического исследования, сравнивающего эффективность лечения этими двумя разными методами лечения, показывают, что после двух лет наблюдения пневматическая дилатация и лапароскопическая миотомия имеют сопоставимый процент успеха 87–92%. 50 Некоторые исследования показывают, что пневматическая дилатация может обеспечить долгосрочное облегчение симптомов у пациентов старше 50 лет.51 Несмотря на улучшение симптомов с помощью пневматической дилатации или хирургической миотомии у пациентов с ахалазией, у 10–15% пациентов, прошедших такое лечение, будет наблюдаться прогрессирующее ухудшение функции пищевода, а до 5% в конечном итоге может потребоваться эзофагэктомия. Оптимальной реконструкцией резецированного пищевода должна быть интерпозиция желудка, интерпозиции толстой кишки и интерпозиции тощей кишки, каждая из которых имеет свои преимущества и недостатки. клеточная карцинома) – это неудачное хирургическое вмешательство или невозможность последующего наблюдения.Развитие аденокарциномы после миотомии с последствиями пищевода Барретта может быть связано с слишком длинной миотомией, и имеется лишь несколько отчетов о случаях этой связи.54 Подход к питаниюВедение пациента с ахалазией и проблемами питания очень тщательное. аналогична таковой у пациентов с дисфагией из-за неврологического заболевания или рака пищевода и желудка.55,56 Пероральное кормление имеет соответствующее психосоциальное значение для пациентов и их семей, и его следует продолжать, когда это возможно.У некоторых пациентов пероральный прием часто бывает недостаточным даже при отсутствии значительных затруднений с глотанием. При легкой и умеренной ахалазии питание, как правило, слегка нарушается, и, если семья поощряет пациента к изменению диеты, потеря веса и недоедание происходит редко. Диеты при дисфагии должны быть строго индивидуализированы, включая изменение текстуры пищи или вязкости жидкости. Пища может быть нарезана, измельчена или пюрирована, а жидкости могут быть загущены.57 Если пациент не может есть или пить, или потреблять достаточное количество пищи, либо высок риск легочной аспирации, следует обеспечить питание через зонд. .Если есть возможность хирургической миотомии, энтеральное питание через назальный зонд для питания будет адекватным в качестве временной меры, учитывая, что у истощенного пациента всегда есть большой риск послеоперационных осложнений. В очень редких и отобранных случаях терминальной ахалазии, когда существует дополнительная возможность хирургического вмешательства или пневматической дилатации, предпочтительным лечением будет введение питательной трубки через чрескожную радиологическую гастростомию, а не хирургическую гастростомию.Чрескожное кормление через желудочный зонд является эффективным и обычно приемлемым для пациентов и лиц, осуществляющих за ними уход. Долгосрочные осложнения включают непроходимость трубки и раневую инфекцию. У некоторых пациентов, получающих питание через желудочный зонд, может произойти легочная аспирация, и в этих случаях предлагается обычное интраджунальное кормление.58 Возможные методы лечения в будущемПерспективно целесообразно использовать саморасширяющиеся эндоскопические металлические стенты диаметром 30 мм при ахалазии. оценивалась у 75 пациентов в одном центре за 13-летний период.Уровень клинического успеха после 10 лет наблюдения после удаления стента был высоким (83%). Не было перфорации или смертности, связанных с лечением, но миграция стента произошла у 5% пациентов, рефлюкс у 20% и боль в груди у 38,7% .59 Pasricha сообщил о методе эндоскопической миотомии подслизистой оболочки без разреза кожи в экспериментальная модель.59 Совсем недавно Иноуэ описал клиническое применение модифицированной техники Пасрича, как пероральной эндоскопической миотомии (ПОЭМ), для обеспечения менее инвазивного постоянного лечения ахалазии пищевода.60 Тридцать пять пациентов с ахалазией, у которых были стойкие симптомы дисфагии, получали ПОЭМ.61 Проглатывание бария до и после процедуры продемонстрировало полное высвобождение утолщенного нижнего сфинктера пищевода. Среднее время операции составило около 120 минут, а среднее время пребывания в больнице после процедуры – 4,9 дня. Сообщений о серьезных осложнениях не было, и после процедуры симптомы дисфагии исчезли. Среднее давление сфинктера в покое упало. Оценка субъективных симптомов была значительно улучшена во всех случаях.Этот метод достигается с помощью уже имеющихся методик и устройств для рутинной эндоскопической миотомии. Эта процедура позволяет осуществлять прямой доступ к утолщенному внутреннему мышечному слою без разреза кожи и эффективно снимает давление на нижний сфинктер пищевода. Длину миотомии можно гибко определять в зависимости от симптомов пациента, таких как дисфагия и боль в груди. Это кажется очень многообещающим методом, который, возможно, открывает новые горизонты для эндотерапии ахалазии, но ожидаются дальнейшие исследования долгосрочной эффективности и сравнение ПОЭМ с другими интервенционными методами лечения.62 Ввиду того факта, что кишечные нейроны, иннервирующие пищевод и нижний сфинктер пищевода, могут исчезнуть из-за аутоиммунного механизма, иммуносупрессивная терапия может предотвратить прогрессирование заболевания.63 Однако на момент постановки диагноза количество нейронов уже уменьшилось. уменьшилась, что привело к значительной дисфункции и появлению симптомов. Хотя этот подход теоретически может предотвратить дальнейшее исчезновение нейронов, возможно, что это произойдет слишком поздно и не удастся восстановить функцию. Недавние экспериментальные исследования на мышах предполагают, что трансплантация нейрональных стволовых клеток может стать терапевтическим вариантом в будущем. В самом деле, нейрональные стволовые клетки, введенные в привратник, выживают и даже экспрессируют синтазу оксида азота. 64 Преимущество такого метода состоит в том, что восстанавливается не только функция сфинктера, но, возможно, даже перистальтика. Это очень многообещающая гипотеза, и очевидно, что для дальнейшего изучения этого подхода еще предстоит провести много исследований. Принятие решений и рентабельностьПодходящее лечение для любого пациента с ахалазией зависит от его готовности пройти инвазивные процедуры и от их физической способности переносить их.Для лечения ахалазии была разработана модель анализа решений. Были оценены четыре терапевтических варианта: лапароскопическая миотомия Хеллера и частичная фундопликация, пневматическая дилатация, инъекция ботулинического токсина и торакоскопическая миотомия Хеллера. Основываясь на осложнениях, необходимости повторных процедур и общей стоимости лечения, было обнаружено, что лапароскопическая миотомия Геллера с фундопликацией была предпочтительной стратегией лечения.65 Авторы рекомендовали тем пациентам, которые соответствуют диагностическим критериям ахалазии (манометрическим, эндоскопическим, рентгенологическим) в специализированном центре и тем, кто является хорошими кандидатами на операцию, следует направить к опытному хирургу для минимально инвазивной модифицированной миотомии Хеллера.Пациентов, которые не подходят для хирургического вмешательства и не могут принять риск пневматической дилатации, можно лечить однократной или повторной инъекцией ботулинического токсина А или лечить фармакологическими средствами. Было проведено несколько анализов затрат, чтобы проверить, какой метод лечения является наиболее рентабельным. Многочисленные исследования, оценивающие стоимость начальных 5–10 лет терапии, показали, что пневматическая дилатация является наиболее экономически эффективным методом у здоровых в остальном людей населения.66 У пациентов с другими сопутствующими заболеваниями, снижающими продолжительность жизни, ботулинический токсин А является более экономичным. 67 Хотя хирургическое вмешательство кажется наиболее окончательным и эффективным методом лечения ахалазии, оно оказывается дорогостоящим в первые годы терапии. РезюмеХотя конечной целью лечения ахалазии пищевода должно быть восстановление перистальтики пищевода и расслабление нижнего пищеводного сфинктера, в настоящее время не существует известного терапевтического варианта для решения этой задачи, и как гастроэнтерологи, так и хирурги продолжают разрушать нижний сфинктер пищевода.В то время как медикаментозная терапия дает плохие результаты, если таковые имеются, миотомия Геллера и пневматическая дилатация успешны у 70–90% пациентов в первый год, но процент успеха со временем медленно снижается. Инъекция ботулинического токсина в нижний сфинктер пищевода безопасна и эффективна, но ее следует применять только пожилым пациентам с сопутствующими заболеваниями. Пневматическая дилатация или миотомия Геллера кажется лучшим решением, поскольку каждый метод имеет технические проблемы и возможные осложнения. Какой из этих методов лечения может быть терапией выбора при ахалазии в определенных подгруппах пациентов, еще предстоит исследовать.Очевидно, что необходимы дополнительные исследования для разработки методов восстановления функциональной анатомии нижнего сфинктера пищевода. СноскиРаскрытие информации Авторы сообщают об отсутствии конфликта интересов в этой работе. Ссылки1. Park W, Vaezi MF. Этиология и патогенез ахалазии: современное понимание. Am J Gastroenterol. 2005; 100: 1404–1404. [PubMed] [Google Scholar] 2. Зарате Н., Мерин Ф., Жиль-Верне Дж. М. и др. Ахалазия и синдром Дауна: случайное совпадение или что-то еще? Am J Gastroenterol.1999; 94: 1674–1677. [PubMed] [Google Scholar] 3. Wong RK, Maydonovitch CL, Metz SJ, Baker JR., Jr. Значительная связь DQw1 при ахалазии. Dig Dis Sci. 1989; 34: 349–352. [PubMed] [Google Scholar] 4. Руис-де-Леон А., Мендоса Дж., Севилья-Мантилья С. и др. Миэнтерические антиплексусные антитела и HLA класса II при ахалазии. Dig Dis Sci. 2002; 47: 15–19. [PubMed] [Google Scholar] 5. Робертсон С.С., Мартин Б.А., Аткинсон М. ДНК вируса ветряной оспы в кишечном сплетении пищевода при ахалазии. Кишечник. 1993; 34: 299–302.[Бесплатная статья PMC] [PubMed] [Google Scholar] 6. Верн Г. Н., Саллюсто Дж. Э., Икер Е. Ю.. Антитела к миэнтериальным нейронам у пациентов с ахалазией. Перспективное исследование. Dig Dis Sci. 1997. 42: 307–313. [PubMed] [Google Scholar] 7. Гокель I, Эккардт В.Ф., Шмитт Т., Юнгингер Т. Псевдоахалазия: серия случаев и анализ литературы. Сканд Дж Гастроэнтерол. 2005. 40: 378–385. [PubMed] [Google Scholar] 8. Пох Д.Л., Тутуян Р. 2007. Ахалазия: обзор диагностики и лечения. J Gastrointestin Liver Dis.2007; 4: 297–303. [PubMed] [Google Scholar] 10. Аггеструп С., Уддман Р., Сандлер Ф. и др. Отсутствие вазоактивных кишечных полипептидных нервов при ахалазии пищевода. Гастроэнтерология. 1983; 84: 924–927. [PubMed] [Google Scholar] 11. Хирано И. Патофизиология ахалазии и диффузного спазма пищевода. GI Motility Online. 2006 doi: 10.1038 / gimo22 .. [CrossRef] [Google Scholar] 12. Крайчелин Р.Э., Фарруджа Г. Ахалазия: физиология и этиопатогенез. Dis Esophagus. 2006; 19: 213–223. [PubMed] [Google Scholar] 13.Faussone-Pellegrini MS, Cortesini C. Ультраструктурные особенности и локализация интерстициальных клеток Кахаля в гладкомышечном слое пищевода человека. J Submicrosc Cytol. 1985; 17: 187–197. [PubMed] [Google Scholar] 14. Szurszewski JH, Farrugia G. Окись углерода является эндогенным гиперполяризующим фактором в желудочно-кишечном тракте. Нейрогастроэнтерол Мотил. 2004. 16: 81–85. [PubMed] [Google Scholar] 15. Фокс Е.А., Филлипс Р.Дж., Мартинсон Ф.А., Бароновски Е.А., Паули Т.Л. Мутантные мыши C-Kit имеют избирательную потерю блуждающих внутримышечных механорецепторов в преддверии желудка.Анат Эмбриол. 2001; 204: 11–26. [PubMed] [Google Scholar] 16. Уорд С.М., Моррис Г., Риз Л., Ван XY, Сандерс К.М. Интерстициальные клетки Кахаля опосредуют кишечную тормозную нейротрансмиссию в нижнем пищеводном и пилорическом сфинктерах. Гастроэнтерология. 1998. 115: 314–329. [PubMed] [Google Scholar] 17. Зарате Н., Ван XY, Тугас Г. и др. Внутримышечные интерстициальные клетки Кахаля, связанные с тучными клетками, выживают при нитрергических нервах при ахалазии. Нейрогастроэнтерол Мотил. 2006. 18: 556–568. [PubMed] [Google Scholar] 18.Huizinga JD, Zarate N, Farrugia G. Физиология, травма и восстановление интерстициальных клеток Кахала: фундаментальные и клинические науки. Гастроэнтерология. 2009; 137: 1548–1556. [Бесплатная статья PMC] [PubMed] [Google Scholar] 19. Бортолотти М., Лабо Г. Клинические и манометрические эффекты нифедипина у пациентов с ахалазией пищевода. Гастроэнтерология. 1981; 80: 39–44. [PubMed] [Google Scholar] 20. Триадафилопулос Г., Ааронсон М., Сакель С., Буракофф Р. Медикаментозное лечение ахалазии пищевода. Двойное слепое перекрестное исследование с пероральным приемом нифедипина, верапамила и плацебо.Dig Dis Sci. 1991; 36: 260–267. [PubMed] [Google Scholar] 21. Траубе М., Дубовик С., Ланге Р.С., МакКаллум Р.В. Роль терапии нифедипином при ахалазии: результаты рандомизированного двойного слепого плацебо-контролируемого исследования. Am J Gastroenterol. 1989; 84: 1259–1262. [PubMed] [Google Scholar] 22. Бортолотти М. Медикаментозная терапия ахалазии: преимущество для немногих. Пищеварение. 1999; 60: 11–16. [PubMed] [Google Scholar] 23. Бортолотти М., Кочча Г., Брунелли Ф. и др. Изосорбид динитрат или нифедипин: что предпочтительнее в медикаментозной терапии ахалазии? Ital J Gastroenterol.1994; 26: 379–382. [PubMed] [Google Scholar] 25. Бортолотти М., Мари С., Лопилато С., Порраццо Дж., Мильоли М. Влияние силденафила на моторику пищевода у пациентов с идиопатической ахалазией. Гастроэнтерология. 2000. 118: 253–257. [PubMed] [Google Scholar] 26. Пасрича П.Дж., Равич В.Дж., Хендрикс Т.Р., Состре С., Джонс Б., Каллоо А.Н. Внутрисфинктерный ботулинический токсин для лечения ахалазии. N Engl J Med. 1995; 332: 774–778. [PubMed] [Google Scholar] 28. Аннезе В., Бассотти Дж., Кочча Дж. И др. Многоцентровое рандомизированное исследование интрасфинктерного ботулинического токсина у пациентов с ахалазией пищевода.GISMAD Группа изучения Ахалазии. Кишечник. 2000. 46: 597–600. [Бесплатная статья PMC] [PubMed] [Google Scholar] 29. Пасрича П.Дж., Рай Р., Равич В.Дж., Хендрикс Т.Р., Каллоо А.Н. Ботулинический токсин при ахалазии: долгосрочные результаты и предикторы ответа. Гастроэнтерология. 1996; 110: 1410–1415. [PubMed] [Google Scholar] 30. Пехливанов Н., Пасрича П.Ж. Ахалазия: Ботокс, дилатационная или лапароскопическая операция в 2006 году. Нейрогастроэнтерол Мотил. 2006; 18: 799–804. [PubMed] [Google Scholar] 31. Дугера Л., Батталья Э, Маджио Д. и др. Лечение ботулиническим токсином ахалазии пищевода у пожилых и пожилых людей: последующее исследование через год.Наркотики старения. 2005. 22: 779–783. [PubMed] [Google Scholar] 32. Уиллис Т. Фармацевтика Рационис Сив Диатриба до Медикаментоз Операбус в Humano Corpore. Лондон: Hagea Comitis; 1674. [Google Scholar] 33. Mikaeli J, Bishehsari F, Montazeri G, Yaghoobi M, Malekzadeh R. Расширение пневматического баллона при ахалазии: перспективное сравнение безопасности и эффективности баллонов разного диаметра. Алимент Pharmacol Ther. 2004. 20: 431–436. [PubMed] [Google Scholar] 34. Кадакия СК, Вонг РК. Постепенная пневматическая дилатация с использованием расширителей ахалазии Rigiflex у пациентов с первичной ахалазией пищевода.Am J Gastroenterol. 1993; 88: 34–38. [PubMed] [Google Scholar] 35. Вонг РК. Пневматическое расширение при ахалазии. Am J Gastroenterol. 2004. 99: 578–580. [PubMed] [Google Scholar] 36. Zerbib F, Thetiot V, Richy F, Benajah DA, Message L, Lamouliatte H. Повторные пневматические дилатации в качестве долгосрочной поддерживающей терапии ахалазии пищевода a . Am J Gastroenterol. 2006; 101: 692–697. [PubMed] [Google Scholar] 37. Левин М.Л., Дорф Б.С., Московиц Г., Банк С. Пневматическая дилатация при ахалазии под эндоскопическим контролем: корреляция пре- и постдилатации радионуклидным сцинтисканом.Am J Gastroenterol. 1987. 82: 311–314. [PubMed] [Google Scholar] 38. Американское общество гастроинтестинальной эндоскопии. Расширение пищевода. Gastrointest Endosc. 1998. 48: 702–704. [PubMed] [Google Scholar] 39. Моавад Ф.Дж., Вонг РК. Современное лечение ахалазии. Курр Опин Гастроэнтерол. 2010; 26: 384–388. [PubMed] [Google Scholar] 40. Novais PA, Lemme EM. 24-часовой мониторинг pH и клинический ответ после лечения ахалазии с помощью пневматической дилатации или лапароскопической миотомии Хеллера. Алимент Pharmacol Ther.2010. 32: 1257–1265. [PubMed] [Google Scholar] 41. Leyden JE, Moss AC, MacMathuna P. Эндоскопическая пневматическая дилатация по сравнению с инъекцией ботулотоксина при лечении первичной ахалазии. Кокрановская база данных Syst Rev.2006: CD005046. [PubMed] [Google Scholar] 42. Ван Л., Ли Ю. М., Ли Л. Мета-анализ рандомизированных и контролируемых исследований лечения ахалазии. Dig Dis Sci. 2009; 54: 2303–2301. [PubMed] [Google Scholar] 43. Патти М.Г., Физикелла П.М., Перретта С. и др. Влияние малоинвазивной хирургии на лечение ахалазии пищевода: десятилетие перемен.J Am Coll Surg. 2003; 196: 698–703. [PubMed] [Google Scholar] 44. Исхак С. Лечение ахалазии: следует подчеркнуть роль лапароскопической кардиомиотомии. Am J Gastroenterol. 2004. 99: 2278–2279. [PubMed] [Google Scholar] 45. Минео Т.К., Амброджи В. Долгосрочные результаты и качество жизни после операции по поводу ахалазии пищевода: опыт одного хирурга. Eur J Cardiothorac Surg. 2004. 25: 1089–1096. [PubMed] [Google Scholar] 46. Финли Р. Дж., Клифтон Дж. К., Стюарт К. К., Грэм А. Дж., Уорсли Д. Ф.. Лапароскопическая миотомия Хеллера улучшает опорожнение пищевода и улучшает симптомы ахалазии.Arch Surg. 2001; 136: 892–896. [PubMed] [Google Scholar] 47. Litle VR. Лапароскопическая миотомия Хеллера при ахалазии: обзор противоречий. Ann Thorac Surg. 2008; 85 (Дополнение 7): 43–46. [Google Scholar] 48. Чендес А., Брагетто И., Энрикес А. и др. Поздние результаты проспективного рандомизированного исследования, сравнивающего принудительную дилатацию и эзофагомиотомию у пациентов с ахалазией. Кишечник. 1989; 30: 299–304. [Бесплатная статья PMC] [PubMed] [Google Scholar] 49. Boeckxstaens GE, Annese V, Bruley des Varannes S и др.Европейское исследование ахалазии: рандомизированное многоцентровое исследование, сравнивающее эндоскопическую пневмодилатацию и лапароскопическую миотомию Хеллера в качестве основного лечения идиопатической ахалазии. Кишечник. 2010; 59 (Дополнение III): A25. [Google Scholar] 50. Вела М.Ф., Рихтер Дж. Э., Кхандвала Ф. и др. Долгосрочная эффективность пневматической дилатации и миотомии Геллера для лечения ахалазии. Clin Gastroenterol Hepatol. 2006; 4: 580–587. [PubMed] [Google Scholar] 51. Дюрансау А., Либерман М., Мартин Дж., Ферраро П. Ахалазия в конечной стадии.Dis Esophagus. Декабрь 2010 г .; [Epub перед печатью]. [Google Scholar] 52. Hsu HS, Wang CY, Hsieh CC, Huang MH. Интерпозиция короткого сегмента толстой кишки при конечной стадии ахалазии. Ann Thorac Surg. 2003. 76: 1706–1710. [PubMed] [Google Scholar] 53. Гокель И., Тимм С., Сгуракис Г.Г., Мушолт Т.Дж., Ринк А.Д., Ланг Х. Ахалазия – если хирургическое лечение не помогает: анализ восстановительной хирургии. J Gastrointest Surg. 2010; 14 (Приложение 1): S46 – S57. [PubMed] [Google Scholar] 54. Фоли Н., Тизелл Р., Салтер К., Крюгер Е., Мартино Р. Лечение дисфагии после инсульта: систематический обзор рандомизированных контролируемых испытаний.Возраст Старение. 2008. 37: 258–264. [PubMed] [Google Scholar] 55. Бауэр М.Р., Мартин Р.К., 2-е Управление питанием во время неоадъювантной терапии рака пищевода. J Surg Oncol. 2009. 100: 82–87. [PubMed] [Google Scholar] 56. Пардое Э.М. Разработка многоступенчатой диеты при дисфагии. J Am Diet Assoc. 1993; 93: 568–571. [PubMed] [Google Scholar] 57. Учитывая MF, Hanson JJ, Lee MJ. Методы интервенционной радиологии для обеспечения энтерального питания. Cardiovasc Intervent Radiol. 2005; 28: 692–703. [PubMed] [Google Scholar] 58.Чжао Дж. Г., Ли Ю. Д., Ченг Ю. С. и др. Долгосрочная безопасность и исход временного саморасширяющегося металлического стента при ахалазии: проспективное исследование с 13-летним опытом работы в одном центре. Eur Radiol. 2009; 19: 1973–1980. [Бесплатная статья PMC] [PubMed] [Google Scholar] 59. Пасрича П.Дж., Хавари Р., Ахмед И. и др. Подслизистая эндоскопическая миотомия пищевода: новый экспериментальный подход к лечению ахалазии. Эндоскопия. 2007. 39: 761–764. [PubMed] [Google Scholar] 60. Иноуэ Х., Минами Х., Кобаяси Й. и др.Пероральная эндоскопическая миотомия (ПОЭМ) при ахалазии пищевода. Эндоскопия. 2009. 42: 265–271. [PubMed] [Google Scholar] 61. Минами Х., Иноуэ Х., Хосоя Т. и др. Пероральная эндоскопическая миотомия: ПОЭМ – 35 клинических случаев – эффективное эндоскопическое лечение ахалазии пищевода. Кишечник. 2010; 59 (Дополнение III): A2. [Google Scholar] 62. Де Джорджио Р., Геррини С., Барбара Дж. И др. Воспалительные невропатии кишечной нервной системы. Гастроэнтерология. 2004; 126: 1872–1873. [PubMed] [Google Scholar] 63. Миччи М.А., Лириш Р.Д., Ли Х. и др.Нервные стволовые клетки экспрессируют RET, продуцируют оксид азота и выживают после трансплантации в желудочно-кишечном тракте. Гастроэнтерология. 2001; 121: 757–766. [PubMed] [Google Scholar] 64. Урбах Д.Р., Хансен П.Д., Хаджанчи Ю.С. и др. Анализ решения оптимального начального подхода к ахалазии: лапароскопическая миотомия Хеллера с частичной фундопликацией, торакоскопическая миотомия Хеллера, пневматическая дилатация или инъекция ботулинического токсина. J Gastrointest Surg. 2001; 5: 192–205. [PubMed] [Google Scholar] 65. О’Коннор Дж. Б., Певец М. Е., Империале Т. Ф., Ваези М. Ф., Рихтер Дж. Э.Экономическая эффективность стратегий лечения ахалазии. Dig Dis Sci. 2002; 47: 1516–1525. [PubMed] [Google Scholar] 66. Паначчоне Р., Грегор Дж. К., Рейнольдс Р. П., Прейксаитис Х. Г.. Внутрисфинктерный ботулотоксин против пневматической дилатации при ахалазии: анализ минимизации затрат. Gastrointest Endosc. 1999; 50: 492–498. [PubMed] [Google Scholar] 67. Заят Э.Н., Шустер ММ. Оксид азота – важный фактор в моторике пищевода. Am J Gastroenterol. 2000; 95: 1584–1585. [PubMed] [Google Scholar]Жизнь с ахалазией пищевода: Rockland Thoracic & Vascular Associates: торакальная хирургияВ идеале, каждый раз, когда вы глотаете, пища и жидкость спускаются по пищеводу, длинной трубке, ведущей в желудок. Мышцы пищевода перемещают пищу вниз, и когда она достигает дна трубки, она встречается со сфинктером, который обычно находится в закрытом положении, чтобы не дать желудочной кислоте снова подняться вверх. Затем сфинктер открывается и позволяет пище попасть в желудок. Но при редком состоянии, называемом ахалазия пищевода, мышцы пищевода не сокращаются и не расслабляются, поэтому пища не может попасть в желудок, по крайней мере, с трудом. Gravity может протянуть руку помощи и заставить часть того, что вы проглатываете, соскользнуть вниз, но когда она попадает в нижний сфинктер пищевода, доступ недоступен.Сфинктер остается закрытым и не позволяет пище попасть в желудок. Пища просто застревает в пищеводе, и вы чувствуете, как кусок еды застрял в горле. Когда некуда идти, еда может вылететь изо рта. Если это звучит знакомо и вы думаете, что страдаете ахалазией пищевода, есть только один способ узнать. Вам необходимы специализированные диагностические тесты, которые могут провести опытные медицинские специалисты, такие как наша команда Rockland Thoracic and Vascular Associates. Ежегодно в Америке диагностируется только около 3000 случаев ахалазии пищевода, что объясняет, почему вы, возможно, не слышали о ней. Но если вы один из них, вы, вероятно, искали ответы и облегчение своих симптомов. Здесь наши специалисты объяснят вам варианты лечения и стратегии, которые могут помочь вам жить более комфортно с ахалазией пищевода. Как определить, есть ли у вас ахалазия пищеводаКлассическими симптомами ахалазии пищевода являются неспособность глотать пищу и питье, изжога, срыгивание и боль в груди после еды.Вы также можете заметить нежелательную потерю веса. Единственный способ узнать наверняка, есть ли у вас это заболевание (или что-то еще не так с пищеводом), – это пройти диагностическое обследование. ЭндоскопияВ этом тесте мы вставляем тонкую гибкую трубку с крошечной камерой на конце в ваше горло, чтобы мы могли видеть внутреннюю часть пищевода, чтобы определить, есть ли какие-либо видимые проблемы, такие как опухоли или повреждения. Манометрия пищеводаПодобно эндоскопии, манометрия пищевода включает в себя длинную узкую трубку в горле, но на этот раз мы просим вас что-нибудь проглотить во время теста.Этот инструмент позволяет нам оценить, как двигаются ваши мышцы и работают ли они со сбоями. Бариевая ласточкаБарий – это мелово-белое вещество, поглощающее рентгеновские лучи. Мы смешиваем его с водой, чтобы вы могли пить и покрывать пищевод. Затем мы используем рентген, чтобы выделить ваш пищевод и определить, есть ли у вас структурные или функциональные проблемы. Жизнь с ахалазией пищеводаПричина ахалазии пищевода неизвестна, но возможные причины включают аутоиммунное заболевание, перенесенную вирусную инфекцию и генетику.Если она у вас есть, ваша приоритетная задача – найти способ с ней справиться. Изменения образа жизниХотя ахалазия пищевода неизлечима, есть способы облегчить жизнь с ней.
Эти методы могут принести вам небольшое облегчение, но в основном это навыки совладания с трудностями, которые эффективны для тех, у кого легкие случаи заболевания.Если ваши симптомы мешают вам есть и поддерживать вес, вам может потребоваться медицинское вмешательство. РасширениеПервый курс лечения – расширение нижнего сфинктера пищевода настолько, чтобы позволить пище попасть в желудок. Мы вставляем в пищевод небольшой инструмент, похожий на баллон, и осторожно растягиваем сфинктер. Для многих пациентов эта простая процедура – все, что требуется для восстановления достаточной функциональности и уменьшения симптомов. Для других нам может потребоваться повторить процесс, но шансы на успех этого лечения снижаются с каждой попыткой. ХирургияЕсли дилатация не помогает, мы можем порекомендовать лапароскопическую эзофагомиотомию. Эта хирургическая процедура включает в себя несколько разрезов в четверть дюйма, чтобы мы могли получить доступ к вашему нижнему отделу пищевода. Мы разрезаем неисправный сфинктер, а затем создаем новый сфинктер из верхней части желудка, оборачивая его вокруг нижней части пищевода. Это помогает предотвратить кислотный рефлюкс. Около 95% людей, перенесших эту операцию, получают хоть какое-то облегчение от ахалазии пищевода. Получение помощиЕсли вы страдаете ахалазией пищевода, лечение возможно. Чтобы назначить консультацию с нашей командой торакальных специалистов, позвоните в один из наших пяти офисов или воспользуйтесь нашим удобным онлайн-инструментом для записи на прием. Наши офисы расположены в Помоне, Гошене, Фишкилле и районе Форт Вашингтон на Манхэттене в Нью-Йорке и в Энглвуде, Нью-Джерси. Мы с нетерпением ждем встречи с вами в ближайшее время. Ахалазия – NHSАхалазия – это редкое заболевание пищевода (пищевода), которое может затруднять глотание пищи и питья. Обычно мышцы пищевода сокращаются, проталкивая пищу по направлению к желудку. Мышечное кольцо на конце пищевой трубки расслабляется, позволяя пище попасть в желудок. При ахалазии мышцы пищевода не контактируют должным образом, и мышечное кольцо может не открываться должным образом или вообще не открывается. Еда и напитки не могут попасть в желудок и застревают. Его часто возвращают. Причины ахалазииСчитается, что ахалазия возникает, когда нервы пищевода повреждаются и перестают работать должным образом, поэтому мышцы и мышечное кольцо не работают.Точная причина этого неизвестна. У некоторых людей это может быть связано с вирусной инфекцией. Это также может быть связано с аутоиммунным заболеванием, когда иммунная система организма атакует здоровые клетки, ткани и органы. В редких случаях ахалазия может передаваться по наследству. Лечение ахалазииЛекарства от ахалазии нет, но лечение может помочь облегчить симптомы и облегчить глотание. Ваши врачи расскажут вам о рисках и преимуществах различных вариантов лечения. МедицинаЛекарства, такие как нитраты или нифедипин, могут помочь расслабить мышцы пищевода. Это облегчает глотание и делает его менее болезненным для некоторых людей, хотя они работают не для всех. Эффект длится непродолжительное время, поэтому можно использовать лекарство для облегчения симптомов, пока вы ждете более длительного лечения. Они могут вызывать головные боли, но обычно со временем они проходят. Растяжение мышцы (баллонная дилатация)Под седативным или общим наркозом баллон вводится в пищевод с помощью длинной тонкой гибкой трубки (эндоскопа).Затем воздушный шар надувается, чтобы помочь растянуть мышечное кольцо, которое пропускает пищу в желудок. Это улучшает глотание у большинства людей, но вам может потребоваться лечение несколько раз, прежде чем ваши симптомы улучшатся. Баллонная дилатация сопряжена с небольшим риском разрыва пищевода (разрыв пищевода), что может потребовать неотложной операции. Инъекция ботоксаС помощью эндоскопа ботокс вводится в мышечное кольцо, которое пропускает пищу в желудок, вызывая его расслабление. Обычно он эффективен в течение нескольких месяцев, а иногда и в течение нескольких лет, но его необходимо повторять. Обычно это безболезненно и может использоваться для временного облегчения у людей, которые не могут получить другие методы лечения. ХирургияПод общим наркозом разрезаются мышечные волокна в мышечном кольце, через которое пища попадает в желудок. Это делается с помощью хирургии замочной скважины (лапароскопия) и называется миотомией Хеллера. Может навсегда облегчить глотание. Часто вторая процедура проводится одновременно, чтобы предотвратить кислотный рефлюкс и изжогу, которые могут быть побочным эффектом операции миотомии Хеллера. Ваш хирург расскажет вам об этом. В редких случаях некоторым людям может потребоваться операция по удалению части пищевода. Последующее лечениеРасширение баллона и хирургическое вмешательство могут вызывать такие побочные эффекты, как кислотный рефлюкс, изжога и боль в груди. Врач общей практики может выписать лекарство, чтобы помочь с этим, и ваш хирург может посоветовать вам регулярно принимать это лекарство. Если боль в груди не проходит какое-то время после лечения, это нормально. Питьевая холодная вода может помочь облегчить это. Вам следует обратиться к терапевту, если у вас все еще есть проблемы с глотанием или вы продолжаете худеть после лечения. Необычная, но важная причина затруднения глотания Симптомы, диагностика и лечение. ИндияЧто такое Ахаласия Кардия?Ахалазия – это редкое нарушение глотания, при котором пища и жидкость затрудняются попадать в желудок.Большинству людей диагноз ставится в возрасте от 25 до 60 лет. Но это редко можно увидеть и у детей. При ахалазии нервные клетки пищевода (или того, что мы называем пищевой трубкой) дегенерируют по неизвестным причинам. Это приводит к нарушению глотательной функции пищевой трубки. Пищевая трубка – это трубка, по которой пища переносится изо рта в желудок. Нормальное глотаниеЧтобы понять, что происходит в Achalasia Cardia, давайте сначала разберемся с нормальным процессом глотания.Обычно, когда мы глотаем пищу, пища проталкивается по пищевой трубке за счет ритмических сокращений мышц пищевой трубки. Эти сокращения называются перистальтикой. Кроме того, когда мы глотаем пищу, клапан LES расслабляется и открывается, позволяя пище пройти в желудок. Клапан LES или нижний сфинктер пищевода, расположенный в нижнем конце пищевой трубки, расслабляется. И как только еда достигает желудка, клапан плотно закрывается. Таким образом, он также предотвращает возврат пищи и кислоты из желудка обратно в пищевод.Кислотный рефлюкс вызывает язвы в пищеводе и приводит к изжоге. Таким образом, правильное функционирование этого клапана важно Что происходит с пищевой трубкой в Кардии АхалазииУ людей с ахалазией потеря нервных клеток в пищеводе, который является пищеводом, вызывает две основные проблемы, мешающие глотанию: Во-первых, мышцы, выстилающие пищевую трубку, не сокращаются должным образом. Таким образом, проглоченная пища не попадает из пищевода в желудок обычным образом. Во-вторых, нижний сфинктер пищевода, который является клапаном LES, не может нормально расслабиться при глотании. Это создает барьер, предотвращающий попадание пищи и жидкостей в желудок. С течением времени трубка для питания над клапаном LES расширяется, и в расширенной трубке для питания могут накапливаться большие объемы пищи и слюны. Симптомы ахалазии кардии: Что происходит с пациентом при ахалазии кардииСамый частый симптом ахалазии – затруднение глотания.Пациенты часто испытывают ощущение, что проглоченный материал, как твердые, так и жидкие вещества, застревает в груди. Это может вызвать боль в груди во время еды. Пища и жидкость, которые часто застревают в груди, возвращаются в рот, когда пациенты ложатся. Иногда это может вызвать кашель или выделение воды из носа во время сна. Остатки пищи, оставшиеся в пищевом тракте, могут вызвать язвы и изжогу. Похудание также наблюдается у большинства пациентов с диагнозом ахалазия. Пациенты с ахалазией также имеют более высокий шанс развития рака пищевода в будущем, поэтому своевременное лечение и хорошее последующее наблюдение важны Эта проблема часто начинается медленно и постепенно прогрессирует.Многие люди не обращаются за помощью, пока не проявятся симптомы. Некоторые люди компенсируют это тем, что едят медленнее и используют маневры, такие как поднятие шеи или запрокидывание плеч, чтобы улучшить опорожнение пищевода. Диагностика ахалазии кардииАхалазию можно не заметить или поставить неверный диагноз, потому что у нее есть симптомы, схожие с другими расстройствами пищеварения. Первым тестом для любого пациента, жалующегося на проблемы с глотанием, является эндоскопия и тест на краситель. Верхняя эндоскопия ЭндоскопияВаш врач вводит вам в горло тонкую гибкую трубку, оснащенную светом и камерой, называемую эндоскопом, чтобы исследовать внутреннюю часть пищевода и желудка.У пациентов с ахалазией остатки пищи обычно видны в пищевом тракте. Кроме того, клапан не открывается легко при прохождении эндоскопа, как это бывает у нормального человека. Основная роль эндоскопии – исключить другие причины затруднения глотания, такие как опухоли, сужения (стриктуры), серьезные язвы и инородные тела. Тест на проглатывание бария / красителя Бариевая ласточка в Achalasia Cardia. Отображение внешнего вида хвоста крысыРентген делается после того, как вы выпьете меловую жидкость, называемую барием, или жидкий водянистый краситель, который покрывает и заполняет внутреннюю поверхность вашей пищевой трубки.Радиолог может увидеть прохождение этого красителя через пищевую трубку в желудок на рентгеновском аппарате. У людей с ахалазией рентгеновские снимки покажут скопление красителя в пищевом трубке, расширение пищевода и его сужение на нижнем конце, что указывает на то, что клапан не открывается. Хотя эти данные довольно точны, они иногда отсутствуют на начальной стадии болезни, когда ваш пищевой канал не сильно расширен. Манометрия пищевода Манометрия пищеводаМанометрия является последним подтверждающим тестом и обязательным условием для подтверждения диагноза ахалазии.Этот тест измеряет ритмические сокращения мышц пищевода при глотании, координацию и силу мышц пищевода, а также то, насколько хорошо ваш нижний сфинктер пищевода расслабляется или открывается во время глотания. На ранней стадии ахалазии, когда барий и эндоскопия могут быть нормальными, манометрия может быть единственным тестом, который диагностирует ахалазию. Это также помогает в определении типа ахалазии кардии. Результат лечения зависит от типа ахалазии, поэтому манометрия также помогает предсказать результат и выбрать лечение. Лечение ахалазии кардииЧто касается лечения, мы должны понимать, что ни одно из методов лечения не может остановить или обратить вспять основную потерю нервных клеток в пищеводе. Кроме того, ожидается, что ни одно из доступных методов лечения не восстановит нормальные перистальтические сокращения в пищевом тракте пациентов с ахалазией. Все виды лечения направлены на ослабление нижнего сфинктера пищевода, который является клапаном LES, до такой степени, что он больше не является препятствием для прохождения пищи. Таким образом, пища будет проходить по пищевой трубе под действием силы тяжести. А без сопротивления клапана LES он легко пройдет в желудок. В целом, хирургическое лечение обычно эффективно для улучшения симптомов. Давайте сначала поговорим о нехирургических вариантахБезоперационный вариант включает прием лекарств, эндоскопическую инъекцию ботокса и эндоскопическую баллонную дилатацию. Но мы не обсуждаем подробно лекарства и инъекцию ботокса , поскольку они не дают хороших результатов и обычно не рекомендуются пациентам. Таким образом, нехирургический вариант, доступный для всех практических целей, – это пневматическая дилатация.
Операция по поводу ахалазии кардииХирургия – более эффективное лечение с очень хорошими долгосрочными результатами.Здесь мышца клапана LES систематически разделяется на вид, чтобы клапан оставался открытым. Хирургические варианты включают лапароскопическую и эндоскопическую хирургию. Давайте обсудим один за другим Лапароскопическая операция при ахалазии кардии: называется кардиомиотомией Хеллера с фундопликацией Дор / Тупе
Пред- и послеоперационный курс лапароскопической хирургииОбычно пациент поступает в день операции или накануне вечером.В тот же день после операции начинается прием жидкости. После переноса жидкости следует мягкая диета. Приблизительно через неделю можно вернуться к нормальной диете. Пациенты встают с постели и могут нормально передвигаться через несколько часов после операции. Большинство пациентов выписываются на следующий день после операции. Если отверстие в пищевом тракте было заделано во время операции, диета и выписка могут быть отложены на один или два дня. Результаты лапароскопической операции по поводу ахалазии кардииЭта операция дает отличные долгосрочные результаты.70-90% пациентов имеют хорошее облегчение симптомов в долгосрочной перспективе. Результат зависит от типа ахалазии, определяемого манометрией, и от степени расширения пищевода, как видно в тесте с проглатыванием красителя. Пациенты, идущие на операцию на ранней стадии, имеют лучшие результаты по сравнению с игнорируемыми и запущенными случаями, когда пищевой канал слишком расширен. Кроме того, с добавлением фундопликации вероятность кислотного рефлюкса значительно снижается. Эндоскопическая хирургия: Пероральная эндоскопическая миотомия (POEM)Эта операция выполняется путем введения эндоскопа и инструмента через рот.Хирург с помощью эндоскопа вводит вам через рот в горло, чтобы сделать разрез или разрез на внутренней стороне пищевода. Затем, как при миотомии Хеллера, хирург разрезает мышцу на нижнем конце сфинктера пищевода на глазах. Разрез на внутренней подкладке окончательно закрывается эндоскопическими зажимами. Разрешение симптомов сравнимо с лапароскопической хирургией, но это более новая процедура, и, следовательно, необходимо увидеть долгосрочные результаты. Эндоскопическая хирургия ахалазии кардии: POEMПредоперационный и послеоперационный курс после POEMОбычно пациент поступает в день операции или накануне вечером.В рамках подготовки к операции пациентам рекомендуется соблюдать диету с прозрачными жидкостями за 2 дня до операции. Это необходимо, поскольку хирургия требует разрезания внутреннего слоя пищевой трубки. По его причине ваш хирург хотел бы, чтобы ваша трубка для питания была чистой во время операции и не была заполнена частицами пищи. Пациент встал с постели и может двигаться через несколько часов после операции. Жидкая диета начинается примерно через 2 дня после операции, а через несколько дней следует мягкая диета. Рекомендуется начальное ограничение в диете, чтобы дать отдых заживлению пореза во внутреннем слое пищевода. Итоги стихотворенияУлучшение глотания после ПОЭМЫ очень хорошее. Почти как при лапароскопической операции. Основным недостатком этой процедуры является то, что она не включает антирефлюксную процедуру, то есть фундопликацию. Следовательно, вероятность кислотного рефлюкса очень высока, в пределах 40-60%. Пациентам, у которых после операции развивается кислотный рефлюкс, необходимо длительное время принимать антацидные препараты. Achalasia Cardia, продолжение Поскольку ни один из методов лечения ахалазии не излечивает основное заболевание, и поскольку существует более высокая вероятность развития рака пищевода, необходимо регулярное наблюдение. Задача l – распознавать и лечить повторяющиеся симптомы или осложнения, особенно ГЭРБ. Надеюсь, эта информация помогла вам разобраться в вашей проблеме. Для дальнейших запросов или разъяснений вы звоните нам, в WhatsApp или отправляете нам отчеты по электронной почте 8146078064 / 079-29703438 или [email protected]. Почему лечение ахалазии кардии в Adroit CenterПроблемы с моторикой пищевода , включая Achalasia cardia и GERD , находятся в центре нашего внимания.Мы являемся центром, имеющим все возможности для полной оценки и лечения этих состояний. Мы входим в число очень немногих центров, имеющих оборудование для манометрии пищевода и 24-часового pH с исследованием Impednace . Мы, как центр, и доктор Чираг Таккар, как специалист в этих условиях, имеем большой опыт в решении этих проблем. Мы досконально понимаем, с какими проблемами сталкиваются пациенты. И помимо лечения и хирургии, мы прилагаем дополнительные усилия, чтобы обеспечить нашим пациентам отличный результат.Это причина того, что в нашем центре очень высоки результаты и удовлетворенность пациентов. И причина, по которой пациенты считают нас лучшими в лечении ахалазии кардии. Посмотрите эти видео, чтобы узнать об опыте пациентов с ахалазией Cardia
Также читаютГЭРБ / Кислотный рефлюкс / Изжога: диета и образ жизниГЭРБ / кислотный рефлюкс / изжога: действительно ли операция решает проблему?Дилемма пациента с изжогой: как долго страдать? Когда искать постоянное решение?Хронический панкреатит: обзор, исследование и лечениеРуководство для пациентов по бариатрической хирургииКамень желчного пузыря и диетаБорьба с ожирением: соответствующие роли бариатрической хирургии (потеря веса) и модификации образа жизниАктивность и упражнения после операции по удалению грыжиХирургия камня желчного пузыря: что происходит до, во время и после операцииСообщение навигацииАхалазия кардия: симптомы, диагностика и лечениеАхалазия кардия – редкое заболевание, затрудняющее прохождение пищи и жидкости из глотательной трубки, соединяющей рот и желудок (пищевод), в желудок. Ахалазия Кардия возникает при повреждении нервов пищевода. В результате пищевод со временем парализуется и расширяется и в конечном итоге теряет способность проталкивать пищу в желудок. Затем пища скапливается в пищеводе, иногда ферментируется и смывается обратно в рот, который может иметь горький вкус. Некоторые люди ошибочно принимают это за гастроэзофагеальная рефлюксная болезнь (ГЭРБ). Однако при ахалазии пища поступает из пищевода, а при ГЭРБ – из желудка. Нет лекарства от Ахалазии Кардии. Как только пищевод парализован, мышца снова не может нормально работать. Но симптомы обычно можно лечить с помощью эндоскопии, малоинвазивной терапии или хирургического вмешательства. Каковы симптомы ахалазии кардии?Симптомы ахалазии обычно появляются постепенно и со временем ухудшаются. Признаки и симптомы могут включать:
Каковы причины ахалазии кардии? Точная причина ахалазии кардии точно не известна.Суперспециалисты подозревают, что это может быть вызвано потерей нервных клеток в пищеводе. Есть научные статьи о том, что вызывает это, но есть подозрения на вирусную инфекцию или аутоиммунные реакции. Очень редко ахалазия кардии может быть вызвана наследственным генетическим заболеванием или инфекцией. Как диагностировать ахалазию кардии?Achalasia Cardia можно не заметить или поставить неверный диагноз, потому что у нее есть симптомы, схожие с другими расстройствами пищеварения. Для проверки на ахалазию кардии мы рекомендуем:
Какие варианты лечения доступны при ахалазии кардии?Процедура Achalasia Cardia направлена на расслабление или растяжение нижнего сфинктера пищевода, чтобы пища и жидкость могли легче перемещаться по пищеварительному тракту. Конкретное лечение зависит от вашего возраста, состояния здоровья и степени тяжести ахалазии. Лекарства: Гастроэнтролог может порекомендовать миорелаксант перед едой. Эти лекарства имеют ограниченный лечебный эффект и серьезные побочные эффекты. Лекарства обычно рассматриваются только в том случае, если вы не являетесь кандидатом на пневматическое расширение или операцию, а другие лекарства не помогли. Этот вид терапии показан редко. Хирургические варианты лечения ахалазии кардии включают: Миотомия Хеллера: Хирург разрезает мышцу на нижнем конце сфинктера пищевода, чтобы пища легче проходила в желудок.Процедура может быть выполнена неинвазивно (лапароскопическая миотомия Хеллера). У некоторых людей, перенесших миотомию Геллера, позже может развиться гастроэзофагеальная рефлюксная болезнь (ГЭРБ). Чтобы избежать проблем с ГЭРБ в будущем, процедура, известная как фундопликация, может выполняться одновременно с миотомией Хеллера. При фундопликации хирург оборачивает верхнюю часть желудка вокруг нижней части пищевода, чтобы создать антирефлюксный клапан, предотвращающий возврат кислоты (ГЭРБ) в пищевод. Фундопликация обычно выполняется с помощью малоинвазивной (лапароскопической) процедуры. Пероральная эндоскопическая миотомия (ПОЭМ): В процедуре ПОЭМ Гастроэнтерологи вводят эндоскоп через рот в горло, чтобы сделать разрез на внутренней стороне пищевода. Затем, как при миотомии Хеллера, хирург разрезает мышцу на нижнем конце сфинктера пищевода. POEM может также сочетаться или сопровождаться последующей фундопликацией для предотвращения ГЭРБ. Некоторые пациенты, у которых есть ПОЭМА и у которых после процедуры развивается ГЭРБ, лечат ежедневными пероральными препаратами. . |


 , Wang Y., Liao Y., Zhang J., Wu Y., Xiao T., Zhang Y., Bao Y., Qiu H., Sun S., Guo J. Advances in The Diagnosis and Treatment of Achalasia of The Cardia: a Review. // J Transl Int Med – 2021 – Vol9 – N1 – p.24-31; PMID:33850798
, Wang Y., Liao Y., Zhang J., Wu Y., Xiao T., Zhang Y., Bao Y., Qiu H., Sun S., Guo J. Advances in The Diagnosis and Treatment of Achalasia of The Cardia: a Review. // J Transl Int Med – 2021 – Vol9 – N1 – p.24-31; PMID:33850798 , Ganesh P., Venkataraman J. Retrospective study on symptoms and treatment modalities used and short-term follow up of achalasia cardia in Indian setting. // JGH Open – 2020 – Vol4 – N5 – p.856-859; PMID:33102755
, Ganesh P., Venkataraman J. Retrospective study on symptoms and treatment modalities used and short-term follow up of achalasia cardia in Indian setting. // JGH Open – 2020 – Vol4 – N5 – p.856-859; PMID:33102755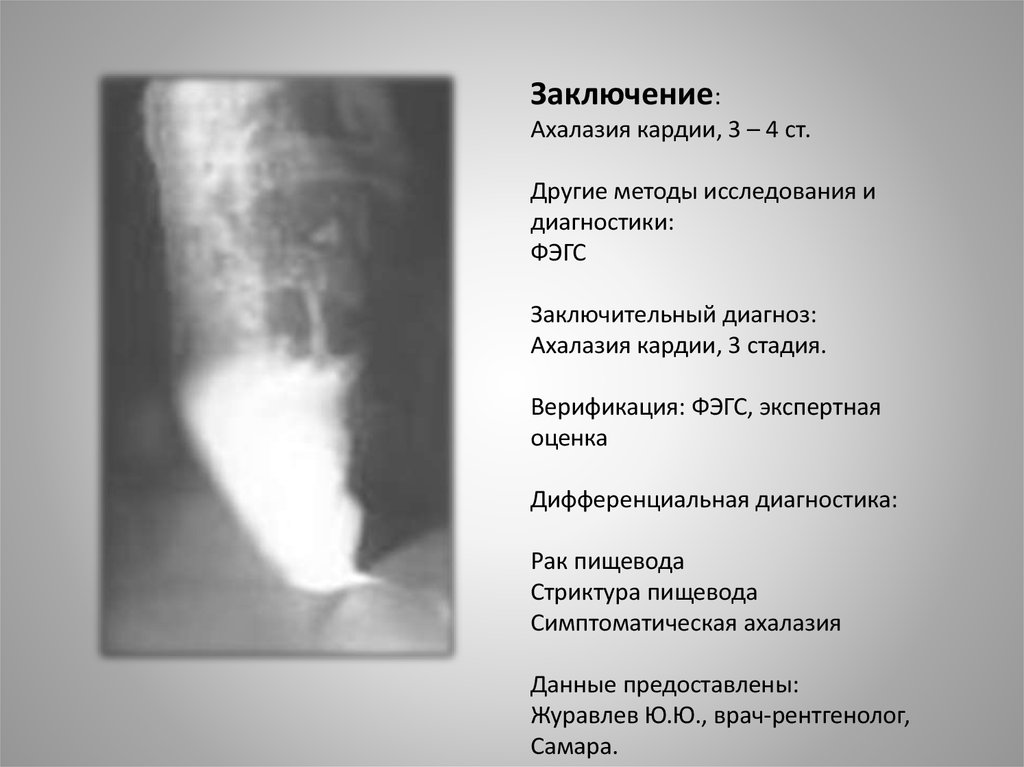 , Hashimah AR., Voon K., Teoh KH., Boo HS., Chuah JS., Nurazim S., Faqihuddin MH. Laparoscopic Heller myotomy and anterior Dor fundoplication for achalasia cardia in Malaysia: Clinical outcomes and satisfaction from four tertiary centers. // Asian J Surg – 2021 – Vol44 – N1 – p.158-163; PMID:32423838
, Hashimah AR., Voon K., Teoh KH., Boo HS., Chuah JS., Nurazim S., Faqihuddin MH. Laparoscopic Heller myotomy and anterior Dor fundoplication for achalasia cardia in Malaysia: Clinical outcomes and satisfaction from four tertiary centers. // Asian J Surg – 2021 – Vol44 – N1 – p.158-163; PMID:32423838