Диета при атрофическом гастрите с пониженной кислотностью: Диета при атрофическом гастрите желудка: меню и продукты
Диета при атрофическом гастрите : меню и рецепты
Разновидности диет при различных видах заболевания
В данной статье мы поговорим о том, какая диета при атрофическом гастрите наиболее эффективна, и в каких ситуациях она может быть назначена, а также разберем возможные варианты меню и ежедневного рациона в период лечения заболевания.
Диета 2 при атрофическом гастрите
Диета №2 (или лечебный стол №2) – это рациональный принцип питания, цель которого – обеспечить организм всем необходимым комплексом микроэлементов, витаминных веществ, протеинов, жиров и углеводов, при этом, не нагружая, а нормализуя деятельность всей пищеварительной системы.
Для приготовления блюд используют в основном пароварку, отваривание в воде и (реже) запекание. Пища должна быть максимально измельченная, для того чтобы пищеварительная система не испытывала дополнительной механической нагрузки. К тому же, мелко смолотая еда стимулирует ферментативную деятельность желудка. Перетиранию подвергают все продукты, которые применяются для приготовления.
Специалисты диетологи советуют питаться очень небольшими порциями, но достаточно часто, примерно каждые 2-3 часа.
Далее мы рассмотрим основные акценты диетического питания при различных видах заболевания.
[5], [6], [7]
Диета при хроническом атрофическом гастрите
Хроническая форма заболевания – это продолжительное заболевание, которое требует длительного и терпеливого лечения. Провоцирующим фактором развития болезни становится неправильный пищевой рацион, употребление спиртных напитков, частый и неграмотный прием медикаментов. Роль правильного питания при хроническом течении заболевания неоспорима: атрофические изменения в стенках желудка, разрастание соединительнотканных элементов там, где должны располагаться железы – всё это нарушает естественную выработку соляной кислоты и пищеварительных ферментов.
При атрофии слизистой любой гастроэнтеролог будет настаивать на соблюдении диеты. Как правило, назначается строгое и щадящее питание. Дегенеративные изменения в стенках желудка чаще всего снижается продукция соляной кислоты, поэтому употребляемая пища должна способствовать её выработке, усиливать ферментативную функцию пищеварительной системы. Обязательно контролируется поступление всех необходимых витаминов других питательных веществ с продуктами питания.
[8], [9]
Диета при очаговом атрофическом гастрите
Очаговый гастрит отличается формированием зон атрофии стенок желудка. Говоря иначе, в желудке появляются зоны, которые перестают выполнять свою секреторную функцию, так как железистая ткань частично замещается эпителием.
Чаще при очаговой форме заболевания назначают диету №1а, через некоторое время переводят пациента на диету №2. Помимо этого, рекомендуется питье лечебной минеральной воды, типа «Нарзан», «Ессентуки-4» или «Ессентуки-17», за 15-20 минут до приема пищи.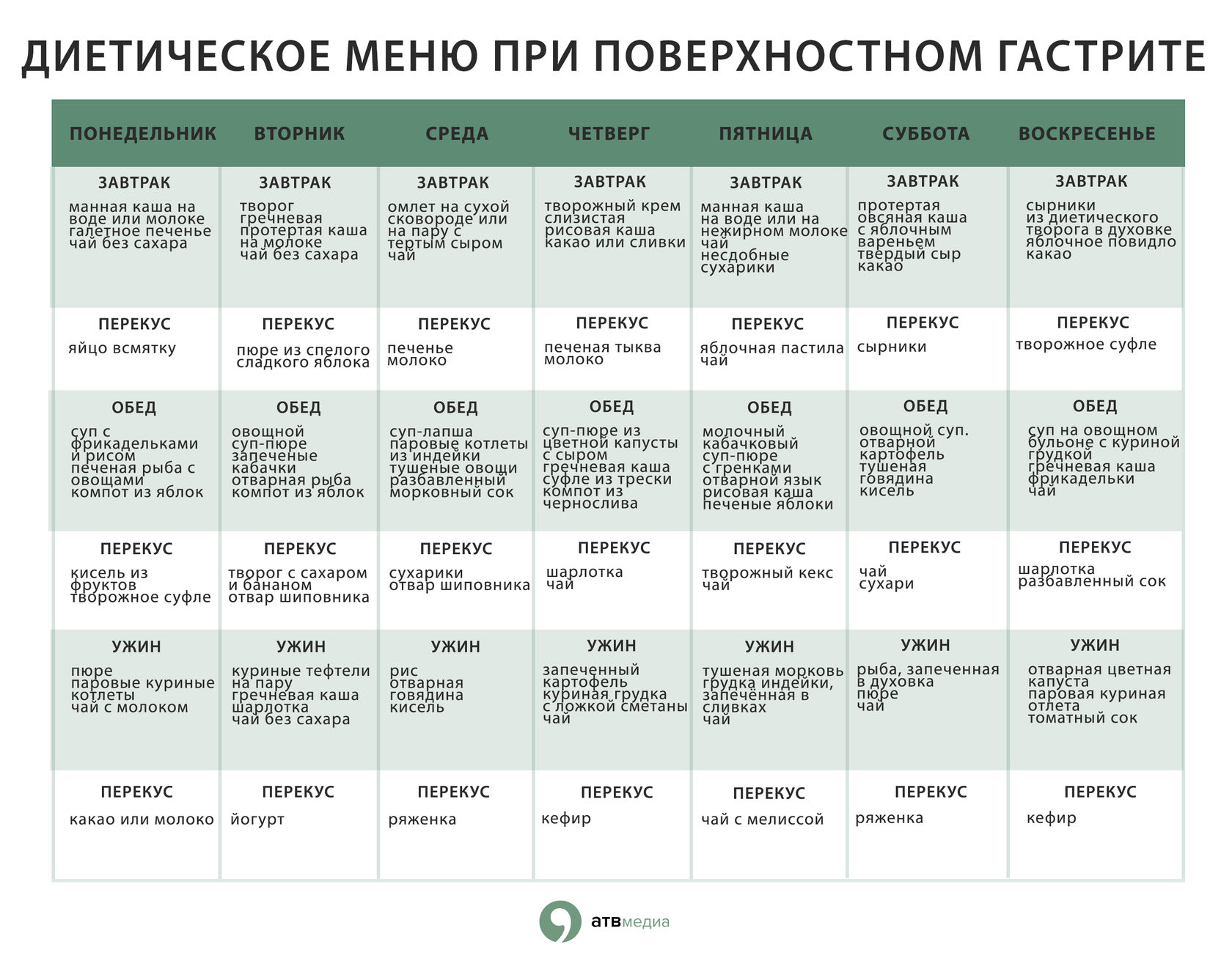 Такая методика помогает стимулировать работу неповрежденных желез.
Такая методика помогает стимулировать работу неповрежденных желез.
Рекомендуется употребление травяных чаев на основе плодов шиповника, листьев подорожника, травы зверобоя, полыни и др., на полчаса до приема пищи.
Запрещается употребление спиртных напитков, а также пищевых продуктов и блюд, которые могут повредить и без того страдающую желудочную слизистую. Если такие меры не предпринять, то лечение может растянуться на очень длительный период, либо не принести эффекта вообще.
[10], [11], [12]
Диета при диффузном атрофическом гастрите
Диагноз диффузной формы заболевания в большинстве случаев означает, что серьезные дистрофические проблемы в желудке пока отсутствуют. Это некая переходная форма, когда повреждения слизистой носят ещё поверхностный характер, однако уже наблюдаются локальные участки перерождения железистых тканей. Симптомы расстройства секреторной функции железистых клеток в такой стадии уже налицо.
Диетическое питание при диффузном поражении может быть как никогда эффективным, однако, если данное состояние запустить, то негативные последствия неизбежны.
Рекомендуемой диетой считается лечебный стол №2. Он предусматривает полноценный пищевой рацион пациента, активирующий функцию желез. Блюда готовятся обязательно в отварном виде, либо тушенном или запеченном, но не должны обжариваться. Нельзя употреблять слишком холодные продукты, а также пищу с грубой текстурой (грубоволокнистые).
Питание диеты №2 может быть достаточно разнообразным, с использованием мясной и рыбной продукции. Допустимы молочные продукты, изделия из муки. Яйца готовят в виде паровых омлетов или же отваривают вкрутую.
Обязательно вводят в рацион достаточное количество овощей и фруктов.
[13], [14], [15]
Диета при атрофическом гастрите с пониженной кислотностью
Пониженная кислотность появляется в результате атрофических процессов в слизистых тканях желудка. При этом степень повреждения может зависеть от того, насколько большим по площади является поврежденный участок. Отмершие железистые клетки теряют способность к выработке кислоты, которая помогает пище перерабатываться и перевариваться. К тому же, в недостатке оказывается и слизь, а также ферменты, благодаря которым происходит процесс усвоения питательных веществ.
К тому же, в недостатке оказывается и слизь, а также ферменты, благодаря которым происходит процесс усвоения питательных веществ.
Изменение питания считается, пожалуй, самым важным этапом терапии гастрита с пониженной кислотностью. Рацион должен включать в себя продукты, стимулирующие продукцию компонентов желудочного сока. Среди таких продуктов – нежирное мясо, рыба, подкисленные свежевыжатые соки, фруктовые и овощные блюда. Запрещаются блюда, которые могут спровоцировать процессы брожения в пищеварительном тракте: свежая выпечка, цельное молоко и пр. Еда должна быть разнообразной и сытной. Тем не менее, переедание следует категорически исключить: пациенты с гипоацидным атрофическим гастритом питаются дробным методом, то есть часто и маленькими порциями. Это позволяет пище усваиваться полностью, не отягощая желудок.
[16], [17], [18], [19]
Диета при атрофическом гастрите с повышенной кислотностью
Развитие атрофического гастрита с повышенной кислотностью напрямую связано с питанием, то есть, данная патология появляется на фоне неправильного питания. Это означает, что первым делом пациент должен внести коррективы в свое меню.
Это означает, что первым делом пациент должен внести коррективы в свое меню.
Собственно, любой гастрит предполагает исключение из употребления пикантной, обжаренной и жирной пищи. Не следует забывать и о вредных привычках, которые также необходимо исключить – это курение и прием спиртных напитков.
Повышенную кислотность сока желудка требуется понизить, а при наличии воспаления с атрофией, а также при периодических приступах рвоты, важно стимулировать работу оставшихся функционирующих желез.
Принимают пищу не менее пяти раз на протяжении дня. При обострении процесса диеты придерживаются не менее 3-х месяцев.
Исключаются из рациона различные повреждающие и кислотообразующие продукты: грибы, редька, жирные сорта мяса, обжаренные блюда, цитрусовые, виноград, газировка, кофе, темный хлеб, острые приправы, лук и чеснок, горчица. Нельзя позволять пище долго задерживаться в полости желудка: по этой причине исключают горячую и холодную еду, а также тяжелую и обильную пищу.
Рекомендовано употребление обезжиренного свежего молока. Сырые фрукты лучше заменить отварными или пропаренными, а также пюре или компотами. Приветствуется употребление каш из риса, манки, овсяной крупы. Все продукты предпочтительно измельчать, например, в блендере.
[20], [21], [22], [23], [24]
Диета при атрофическом гастрите с нормальной кислотностью
Пациенты с нормальной кислотностью желудочного сока питаются по принципу течения заболевания: при обострениях диета ужесточается, а в периоды ремиссии – ослабляется.
При обострении заболевания рекомендуется питаться в основном так называемыми «слизистыми» первыми блюдами, приготовленными с добавлением рисовой, ячменной крупы. Можно употреблять овсяную кашу на молоке или воде. Кушать следует малыми дозами, но достаточно часто, хорошо прожевывая кусочки пищи – это благоприятствует нормальной функции пищеварительных органов.
Важным моментом является нормализация дефекации. Если преобладает жидкий стул, то рекомендуется пить свежевыжатые соки из граната, кизила, черники, черной смородины, груши.
Не следует употреблять сладости, сдобные изделия. Рекомендуется пить зеленый чай в промежутках между приемами пищи (но не во время еды).
[25], [26], [27], [28]
Диета при антральном атрофическом гастрите
Антральный атрофический гастрит сопровождается поражением нижних участков желудка, расположенных практически у выхода из органа, на границе с 12-перстной кишкой. При антральном гастрите часто появляется утренняя тошнота, быстрое насыщение с тяжестью в животе и неприятной отрыжкой.
Чаще всего в таких случаях назначают лечебный стол №1а, особенно при выраженном болевом синдроме. Такого питания следует придерживаться первые несколько дней заболевания. Цель – уменьшить раздражение и рефлекторную возбудимость слизистых тканей желудка. Из рациона вычеркиваются стимулирующие секрецию продукты.
После диеты №1а пациент переходит на диету №1, которая способствует восстановлению поврежденной слизистой. Это относительно расширенный вариант питания, назначение которого – нормализовать секрецию и моторику пищеварительной системы. Не рекомендуются блюда с большим содержанием клетчатки, поэтому все овощи и фрукты подают только в обработанном виде (отварные, запеченные, желированные и пр., но не сырые).
Диета при атрофическом гиперпластическом гастрите
Атрофический гипертрофический гастрит сопровождается появлением образований на поверхности слизистой желудка – это могут быть кистозные или полипозные образования. Причиной появления заболевания считаются такие факторы, как употребление алкоголя, ненатуральных синтетических продуктов, авитаминоз, аллергические реакции на продукты.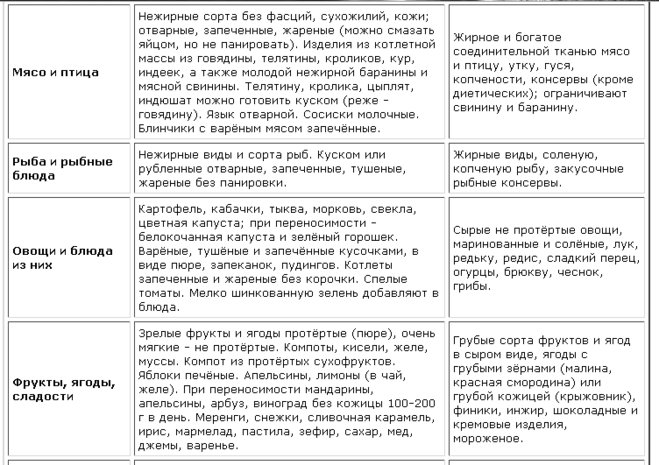
Диетологи в самом начале гиперпластического процесса назначают диетическое питание с исключением из пищевого рациона всех продуктов, раздражающих внутренние стенки желудка. Это все жирные блюда, соленья, сдоба и изделия и муки, кислые и острые продукты, сырые фрукты и овощи. Также необходимо отказаться от сигарет и спиртных напитков.
Цели изменений в питании:
- остановка гиперплазии слизистых желудка;
- восстановление моторики и секреции желудка;
- нормализация функции кишечника;
- стабилизация уровня гемоглобина в крови.
Если гастрит носит хронический характер, то диетического питания, скорее всего, придется придерживаться всю жизнь.
[31], [32], [33], [34]
Меню диеты при атрофическом гастрите
Первые сутки (понедельник):
- I завтрак – манная каша, отварное яйцо, чай из шиповника;
- II завтрак – яблочное суфле;
- обед – вермишелевый суп, отварная грудинка со сметаной, абрикосовый кисель;
- полдник – печенье, чай;
- ужин – творог с йогуртом;
- перед сном – чашка кефира.

Вторые сутки (вторник):
- I завтрак – овсянка с яблоком и корицей, чай;
- II завтрак – кусочек домашнего сыра;
- обед – суп с тефтелями, картофельно-мясное пюре, морковный сок;
- полдник – половинка яблока, запеченного с творогом;
- ужин – творожники со сметаной, чай с медом;
- перед сном – чашка простокваши.
Третьи сутки (среда):
- I завтрак – рисовая запеканка, чай зеленый;
- II завтрак – черника с медом;
- обед – куриный суп, лапша с мясом, компот из ягод;
- полдник – протертая груша;
- ужин – кусочек отварной рыбы, кисель;
- перед сном – йогурт.
Четвертые сутки (четверг):
- I завтрак – вермишель с сыром, какао;
- II завтрак – яблочный пудинг;
- обед – рисовый суп, гречневые котлеты с картофелем, компот;
- полдник – мармелад, зеленый чай;
- ужин – картофельно-рыбная запеканка, чай;
- перед сном – чашка кефира.
Пятые сутки (пятница):
- I завтрак – порция ленивых вареников со сметаной, чай;
- II завтрак – ягодный мусс;
- обед – щи из свежей капусты, паровая куриная котлета, чай со смородиной;
- полдник – морковно-яблочный салат со сметаной;
- ужин – молочная сосиска с рисом, чай;
- перед сном – чай с медом.

Шестые сутки (суббота):
- I завтрак – омлет, чай с печеньем;
- II завтрак – пюре из персика;
- обед – капустно-морковный суп, картофельные котлеты с мясной подливой, компот;
- полдник – зефир, какао;
- ужин – кусочек отварного языка с картофелем, компот;
- перед сном – чашка свежей простокваши.
Седьмые сутки (воскресенье):
- I завтрак – сырная запеканка, чай;
- II завтрак – банановый мусс;
- обед – рыбный бульон, запеченная куриная грудка с пюре из цветной капусты, чай;
- полдник – кисель с сухариком;
- ужин – мясная тефтеля с рисом, клубничный чай;
- перед сном – стаканчик йогурта.
Рецепты диеты при атрофическом гастрите
Что интересного и вкусного можно приготовить пациенту для того чтобы разнообразить скучное и однообразное меню? Вариантов много: главное, включить фантазию и стараться мыслить нестандартно. Представляем вашему вниманию небольшую подборку вкусных и полезных блюд.
- Воздушные паровые котлеты. Ингредиенты блюда: 1 кг картофеля, ½ кг отваренной цветной капусты, одна морковь, одна луковица, одно яйцо, панировочные сухари, соль.
Отваренную капусту нарезаем на кубики, припускаем на подсолнечном масле с измельченным луком и морковкой. Из картофеля делаем пюре, примешиваем его к капусте, прибавляем яйцо и панировочные сухари. Из полученного «фарша» лепим котлетки, присыпаем сухарями и готовим в пароварке. Приятного аппетита.
- Нежное желе. Ингредиенты: немного ванильного сахара, 2 ст. ложки какао, сахар, два яичных желтка, стакан варенья, 600 мл сметаны, 3 ст. ложки желатина, 3 стакана воды, немного лимонного сока. Желатин заливаем прохладной водой, оставляем до набухания, после чего немного нагреваем. Взбиваем желтки с ½ стакана сахара до пышности, прибавляем немного лимонного сока, ванилин или ванильный сахар, смешиваем. Прибавляем 200 мл сметаны и стакан желатина, вымешиваем. В подготовленную ёмкость наливаем смесь и убираем в холодильник.
 Оставляем, пока не застынет.
Оставляем, пока не застынет.
Готовим следующий слой: смешиваем 200 мл сметаны с сахаром (1-2 ст. ложки), прибавляем стакан измельченного варенья, стакан желатина, размешиваем. Выливаем смесь на уже застывшее в холодильнике желе, опять прячем в холодильник.
Последний слой: 200 мл сметаны, ½ ст. сахара и какао перемешиваем, доливаем оставшийся желатин. Смесь добавляем к нашему желе в виде третьего слоя и помещаем в холодильник до полного застывания. Перед подачей режем на порции и подаем.
- Паштет баклажанный. Ингредиенты: баклажан, 2 луковицы, 2 яйца (отварных), соль и перец, растительное масло (примерно 40 г).
Баклажан запекаем целиком. После того, как баклажан приготовиться, мякоть выскребаем ложкой, кожура нам не понадобится. Лук припускаем на сковородке. В блендере смешиваем мякоть баклажана, отварные яйца, лук и измельчаем. Солим и перчим по вкусу. Паштет готов – его можно намазывать на гренки или тосты.
- Монастырская каша. Ингредиенты: гречка 100 г, перловка 100 г, рис 100 г, кус-кус 100 г, три луковицы, 2-3 небольшие моркови, баклажан, вода, растительное масло (примерно 60 г), зелень, соль.

Нарезанные лук, баклажан и морковь припускаем на сковородке на растительном масле. В кастрюлю кладем мытую гречневую крупу, поверх неё третью часть припущенных овощей. Следующий слой – мытая перловка и снова третья часть овощей. Далее – кус-кус и оставшиеся овощи. Последний слой – промытый рис. Один литр теплой подсоленной воды осторожно выливаем в емкость, стараясь не повредить слои. Сверху посыпаем зеленью и закрываем крышкой. Ставим на малый огонь или в духовку до полного впитывания жидкости. Приятного аппетита.
[35], [36]
Диета при атрофическом гастрите – диета
3.1k –
Полезная информация
Существуют разные формы данного заболевания, и одной из самых распространенных является антральный гастрит (слизистая воспаляется в пилорическом отделе желудка). Диета при атрофическом гастрите антрального отдела желудка не имеет серьезных отличий от лечебного плана питания, рекомендованного при других формах заболевания (важно лишь учитывать, как именно изменилась кислотность желудочного сока).
Продукты рекомендуется отваривать, запекать без корочки, тушить. При пониженной кислотности допустимо обжаривать их (без панировки и без образования корочки). Пищу, содержащую грубую клетчатку, нужно протирать. При пониженной кислотности норма соли составляет 15 г в сутки, а при повышенной она должна быть несколько ниже. Температура подачи блюд комфортная, питание дробное.
Основа рациона
Из категории мучных изделий позволительно употреблять булочки из пресного теста, белый хлеб, пресное печенье, бисквит. Иногда можно кушать пирожки с мясом, сладким джемом, яблоками. Супы рекомендуется готовить на овощном отваре (при низкой и высокой кислотности), на слабом мясном бульоне (при высокой кислотности), на молоке. Мясо можно отваривать, протирать в пюре, подавать куском. Рыбу подают в отварном, жареном (без панировки) или паровом виде. Можно готовить котлеты и прочие изделия из фарша. Допустимо вводить в рацион нежирные колбасные изделия, вымоченную сельдь. Можно включать в меню молочные продукты средней и низкой жирности (при повышенной кислотности кисломолочные продукты исключаются). Из яиц допустимо готовить запеченные в духовке или паровые омлеты. Также яйца могут быть сварены всмятку. Ассортимент круп – рис, гречка, овсянка, манка. Полезно вводить в рацион блюда из овощей. При приготовлении салатов можно сочетать овощи с мясом, сыром, ветчиной. Диета при атрофическом гастрите не исключает сладостей, но их ассортимент ограничен медом, сахаром, киселями, желе, джемами. В некрепко заваренные чай, какао и кофе рекомендуется добавлять молоко или сливки. Можно пить соки. Жиры представлены рафинированным растительным и сливочным маслом.
Можно включать в меню молочные продукты средней и низкой жирности (при повышенной кислотности кисломолочные продукты исключаются). Из яиц допустимо готовить запеченные в духовке или паровые омлеты. Также яйца могут быть сварены всмятку. Ассортимент круп – рис, гречка, овсянка, манка. Полезно вводить в рацион блюда из овощей. При приготовлении салатов можно сочетать овощи с мясом, сыром, ветчиной. Диета при атрофическом гастрите не исключает сладостей, но их ассортимент ограничен медом, сахаром, киселями, желе, джемами. В некрепко заваренные чай, какао и кофе рекомендуется добавлять молоко или сливки. Можно пить соки. Жиры представлены рафинированным растительным и сливочным маслом.
Продукты под запретом
Диета, назначаемая при атрофическом гастрите, ограничивает потребление некоторых круп (это пшено, кукурузная и ячневая крупы, перловка). Исключаются бобы. Противопоказаны жирные продукты, грибы, копчености и консервы, овощи, стимулирующие выделение желудочного сока и ягоды с мелкими косточками.
Отзывы
Диета при атрофическом гастрите с пониженной кислотностью и с повышенным ее уровнем достаточно разнообразна. При условии постоянного соблюдения щадящего рациона, состояние больного улучшается.
Атрофический гастрит – причины, симптомы особенности диеты и лечения
Гастритом называют воспалительные процессы на слизистой желудка. Под атрофическим гастритом подразумевается воспалительно-дегенеративный процесс с потерей желудочных желез, отвечающий за выработку веществ расщепляющих пищу. Морфологической особенностью атрофического гастрита считается сокращение грандулоцитов (клетки секреторной железы слизистой оболочки желудка), с последующей заменой их простыми клетками вырабатывающими слизкую субстанцию. Широкая атрофия слизистой чаще всего обуславливается нарушением (уменьшением) секреции соляной кислоты и пепсина (фермент отвечающий за расщепление белков), приводя к пониженной кислотности. Иными словами атрофический гастрит с пониженной кислотностью способствует широкому распространению атрофических участков. При этом для атрофического гастрита с повышенной кислотностью (при гиперсекреции соляной кислоты и пепсиногена) характерно очаговое распространение. Очаговый атрофический гастрит представляет собой участки истощенной слизистой теля желудка с сокращением толщины и выраженной сосудистой сеткой. Помимо основной причины, чаще всего вызывающей атрофический гастрит – патогенной бактерии Helikobacter pylori, существуют ряд дополнительных причин: неправильное питание, бесконтрольное употребление алкоголя, предпочтение жирных и жаренных продуктов, отравление токсичными веществами, длительный прием лекарственных средств, раздражающих слизистую желудка и рефлюкс. Рефлюск – заброс содержимого кишечника в желудок, а в некоторый случаях в пищевод. При повторяющемся рефлюксе в пищевод, говорят от необходимости диагностики гастроэзофагеальной рефлюксной болезни, поскольку эта патология может провоцировать перерождение гастрита в предраковое состояние с последующим развитием онкологического заболевания.
Иными словами атрофический гастрит с пониженной кислотностью способствует широкому распространению атрофических участков. При этом для атрофического гастрита с повышенной кислотностью (при гиперсекреции соляной кислоты и пепсиногена) характерно очаговое распространение. Очаговый атрофический гастрит представляет собой участки истощенной слизистой теля желудка с сокращением толщины и выраженной сосудистой сеткой. Помимо основной причины, чаще всего вызывающей атрофический гастрит – патогенной бактерии Helikobacter pylori, существуют ряд дополнительных причин: неправильное питание, бесконтрольное употребление алкоголя, предпочтение жирных и жаренных продуктов, отравление токсичными веществами, длительный прием лекарственных средств, раздражающих слизистую желудка и рефлюкс. Рефлюск – заброс содержимого кишечника в желудок, а в некоторый случаях в пищевод. При повторяющемся рефлюксе в пищевод, говорят от необходимости диагностики гастроэзофагеальной рефлюксной болезни, поскольку эта патология может провоцировать перерождение гастрита в предраковое состояние с последующим развитием онкологического заболевания. Рефлюкс эзофагит (ГЭРБ) может быть следствием асцита, который в свою очередь чаще всего проявляется при серьезном нарушении функции печени. Асцит печени провоцируется острым токсическим гепатитов, алкогольным гепатитом, очаговым фиброзом печени и не только. Таким образом патологии гастроэнтерологического характера очень тесно связанны, имеют схожие симптомы и требуют комплексного подхода.
Рефлюкс эзофагит (ГЭРБ) может быть следствием асцита, который в свою очередь чаще всего проявляется при серьезном нарушении функции печени. Асцит печени провоцируется острым токсическим гепатитов, алкогольным гепатитом, очаговым фиброзом печени и не только. Таким образом патологии гастроэнтерологического характера очень тесно связанны, имеют схожие симптомы и требуют комплексного подхода.
Симптомы при атрофическом гастрите характерны клинической картине с нарушениями функций пищеварения, и проявляются тяжестью в желудке, преимущественно после принятия пищи, тошнотой, отрыжка после еды, часто в неприятным привкусом, общее недомогание и снижение веса, потеря аппетита и изжога. Особенными симптомами указывающими на атрофический гастрит, а не на иные отклонение кастроэнтерологической области – снижение зрения и необычная сухость кожи, как следствие нарушения усваивания витамина А из за ферментных отклонений в желудке.
Хронический атрофический гастрит, приводящий к существенному снижению кислотности в среде желудка, незамедлительно требуем заместительную терапию, в отсутствии которой наблюдаются все признаки нарушения пищеварительных процессов. При худшем сценарии, обострение атрофического гастрита может выразится в трансформации в онкологическую форму, иными словами в рак желудка.
При худшем сценарии, обострение атрофического гастрита может выразится в трансформации в онкологическую форму, иными словами в рак желудка.
Различают четыре основных разновидности заболевания: субатрофический гастрит – начальный этап атрофических процессов, очаговый атрофический гастрит – проявление очагов с атрофированной слизистой, замещенной клетками простого эпителия, антральный атрофический гастрит – достижение атрофическими процессами антрального отдела желудка, и мультифакторный – предраковое состояние с обширной площадью поражения. При этом заболевание классифицируют и по степени морфологических изменений: умеренный, выраженный и гиперпластический атрофический гастрит, при котором наблюдается явное изменение морфологической структуры желудка, в некоторых случаях с образованием кист и жировыми дегенеративными процессами.
Атрофический гастрит желудка требует незамедлительного вмешательства квалифицированных медиков, поскольку промедление может упустить момент перехода гастрита в рак и стоить жизни пациенту.
Над вопросом: можно ли вылечить атрофический гастрит, бились не один год величайшие светилы мира медицины и израильские врачи в том числе. Благодаря прогрессивным методам лечения гастрита в клиниках Израиля и использованию высоко технологичного, суперсовременного оборудования, лечение атрофического гастрита стало возможным и дает замечательные результаты при своевременном обращении.
Методы лечения атрофического гастрита зависят от симптомов, составляющих клиническую картину. После некоторых исследований состояния желудка, при помощи серологических методов исследования (иммунные тесты), гастродуоденоскопии (высокоинформативное исследование, применяемое израильскими медиками, дающее широкую картину о состоянии слизистой желудка) и биопсии слизистой (забор ткани при эндоскопии, для гистологического исследования (структура ткани)), врач назначит адекватные терапевтические меры.
Поскольку кислотность при атрофическом гастрите играет большую роль, медики делают попытки регулировать состояние желудочной среды при помощи диеты. Диета при атрофическом гастрите с пониженной кислотностью включает продукты, провоцирующие и раздражающие железы, ответственные за выработку пепсина и гастрина. Это одни из не многих случаев в гастроэнтерологии когда позволительно принимать некоторое количество жаренной пищи, при рекомендации врача, ягодные соки, позволительно употребления чая и кофе, а так же мясных и рыбных бульонов. При этом следует исключить ягоды содержащие крупные косточки, продукты с грубой клетчаткой, слишком жирную и копченную пищу.
Диета при атрофическом гастрите с пониженной кислотностью включает продукты, провоцирующие и раздражающие железы, ответственные за выработку пепсина и гастрина. Это одни из не многих случаев в гастроэнтерологии когда позволительно принимать некоторое количество жаренной пищи, при рекомендации врача, ягодные соки, позволительно употребления чая и кофе, а так же мясных и рыбных бульонов. При этом следует исключить ягоды содержащие крупные косточки, продукты с грубой клетчаткой, слишком жирную и копченную пищу.
Питание при атрофическом гастрите с повышенной кислотностью исключает все продукты провоцирующие секреторные железы желудка: жаренные продукты, пряности и посолы, копчения и маринады, кофе и газированные напитки. При этом варенная овсянка натощак, благотворно влияет на слизистую, так же рекомендуется варить «слизистые» супы и использованием риса, овсяных хлопьев, отварного картофеля.
Ответом израильских медиков на вопрос: как вылечить атрофический гастрит, стал целый комплекс мероприятий направленный на остановку дегенеративного процесса и восстановления нормальной функции пищеварения.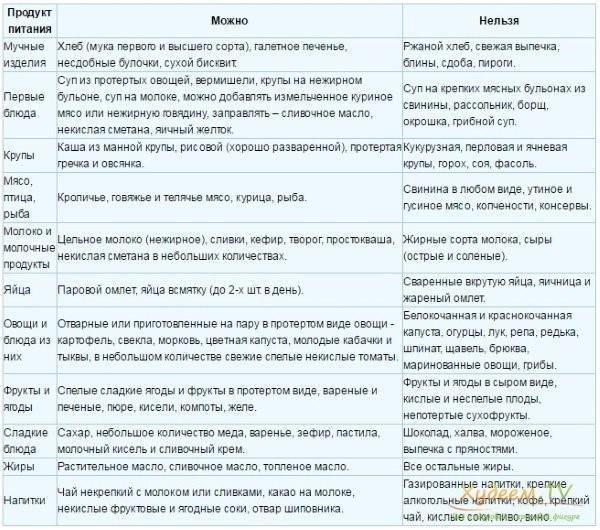 Лечение хронического атрофического гастрита предусматривает использование медикаментозной терапии, в том числе витаминной (для поддержания метаболических процессов), применения медикаментов заместительной терапии (препараты содержащие ферменты для окисления среды желудка и нормализации пищеварения). Для исключение аутоиммунного компонента, при необходимости назначают глюкортикоиды, а так же возможно применение антигистаминных, седативных средств и гастроцитопротекторов.
Лечение хронического атрофического гастрита предусматривает использование медикаментозной терапии, в том числе витаминной (для поддержания метаболических процессов), применения медикаментов заместительной терапии (препараты содержащие ферменты для окисления среды желудка и нормализации пищеварения). Для исключение аутоиммунного компонента, при необходимости назначают глюкортикоиды, а так же возможно применение антигистаминных, седативных средств и гастроцитопротекторов.
Лечение атрофического гастрита в Израиле, позволяет применение радикальных методов при выявлении опасной метаплазии (изменения клеток), предшествующей раковым образованиям, и хирургическое вмешательство с частичной резекцией атрофированной слизистой желудка с последующим наложением анастомоза – искусственное соединение, в данном случае меж двенадцатиперстной кишкой и телом желудка.
Loading…Хронический атрофический гастрит —
Хронический атрофический (автоиммунный, типа А, с пониженной кислотностью, фундальный) гастрит. Как видно из названия эта разновидность гастрита проявляется атрофией клеток слизистой оболочки желудка (чаще всего фундального отдела-то есть дна(купола) желудка), вследствие, как правило, автоиммунного процесса, что приводит к снижению кислотности желудочного сока и соответствующих симптомов.
Как видно из названия эта разновидность гастрита проявляется атрофией клеток слизистой оболочки желудка (чаще всего фундального отдела-то есть дна(купола) желудка), вследствие, как правило, автоиммунного процесса, что приводит к снижению кислотности желудочного сока и соответствующих симптомов.
Как уже отмечалось выше, атрофический гастрит может быть ассоциирован с НР-инфекцией. В этом случае он развивается вследствие нелеченого долгое время бактериального гастрита. Этот механизм составляет львиную долю всех атрофических гастритов. При автоиммунном гастрите (составляет до 10% всех случаев хронического гастрита) в организме вырабатываются антитела к определенным клеткам слизистой оболочки желудка. Чаще всего это париетальные клетки дна желудка, вырабатывающие соляную кислоту, а также внутренний фактор Касла-фермент, способствующий усвоению витамина В12.
Как бы там ни было атрофический гастрит характеризируется симптомами пониженной кислотности желудочного сока: ухудшение аппетита, отрыжка тухлым, неприятный привкус во рту, тошнота. Имеет место чувство тяжести, переполнения желудка, плохой запах изо рта.
Имеет место чувство тяжести, переполнения желудка, плохой запах изо рта.
Синдром избыточного бактериального роста (связан с ухудшением бактерицидной функции желудка): урчание, вздутие живота, неустойчивость стула, непереносимость молочных продуктов, иногда частые поносы сопровождаются потерей веса. Болевой синдром неярко выражен, боль возникает в случае растяжения желудка непереваренной пищей, носит тупой, ноющий характер, усиливается после приема пищи.
При автоиммунном характере атрофического гастрита может нарушатся всасывание витамина В12 и, соответственно, страдать кроветворение. Это проявляется слабостью, головокружением, тахикардией, одышкой. Кроме того, страдает и нервная ткань- характерно жжение, покалывание, онемение, чувство жара в кончиках пальцев, которое со временем распространяется от пальцев к туловищу. В крови-значительное уменьшение количества эритроцитов при относительно нормальном уровне гемоглобина (гиперхромная анемия).
Для диагностики атрофического гастрита кроме проведения гастроскопии и выявления НР очень важно также проведение суточной рН-метрии, что позволяет не только с постановкой диагноза, но и с выбором тактики лечения, а также оценкой ее эффективности. Лабораторные методы диагностики атрофического гастрита (гастропанель-измерение уровня пепсиногена-1, пепсиногена-2, гастрина-17 в сыворотке крови; а также уровня антипариетальных антител и антител к внутреннему фактору Касла) не обладают высокой специфичностью (то есть могут быть положительными и при других заболеваниях) и достоверностью, однако могут использоваться для скрининга (отсеивания) рака желудка.
Лабораторные методы диагностики атрофического гастрита (гастропанель-измерение уровня пепсиногена-1, пепсиногена-2, гастрина-17 в сыворотке крови; а также уровня антипариетальных антител и антител к внутреннему фактору Касла) не обладают высокой специфичностью (то есть могут быть положительными и при других заболеваниях) и достоверностью, однако могут использоваться для скрининга (отсеивания) рака желудка.
Очень важным фактором, который постоянно недооценивается и, на фоне которого должно проходить лечение, является диетотерапия. При атрофическом гастрите возможно применение 4 разных диет (по классификации М. И. Певзнера) -в зависимости от фазы процесса. Базовой является диета №2, однако при обострении начинают с диеты №1а.
Она предусматривает минимальную нагрузку на пищеварение. Сюда относится жидкая пища (супы) и пюре (протертые, приготовленные на пару). По мере стихания обострения (воспалительного процесса) больной переводится на диету №1.
Она предусматривает нормализацию секреторной деятельности желудка. Это обычный рацион питания за исключением горячих и сильно охлажденных блюд, а также блюд с высоким содержанием клетчатки. Диета №4 назначается в случае выраженного энтерального синдрома (нарушение стула) и предусматривает резкое ограничение молочных и других продуктов, употребление которых сопровождается непереносимостью. При этом предусматривается дробный режим питания.
Это обычный рацион питания за исключением горячих и сильно охлажденных блюд, а также блюд с высоким содержанием клетчатки. Диета №4 назначается в случае выраженного энтерального синдрома (нарушение стула) и предусматривает резкое ограничение молочных и других продуктов, употребление которых сопровождается непереносимостью. При этом предусматривается дробный режим питания.
После стихания острого процесса всегда нужно возвратится к базовой для атрофического гастрита диете-№2. Эта диета предусматривает полноценное питание больного с целью нормализации функций ЖКТ и стимуляции желез, вырабатывающих желудочный сок. Поэтому диета №2 наиболее разнообразная из всех вышеперечисленных. Она предусматривает употребление практически любых видов пищи, кроме охлажденной с грубой структурой. Всего в ее состав входит около 30 блюд.
Прежде чем начать лечение атрофического гастрита, необходимо ответить на 2 вопроса:
- Связь с НР-инфекцией;
- Уровень рН желудка.
В большинстве случаев у пациентов с атрофическим гастритом имеется НР-инфекция, следовательно, они нуждаются в эрадикации, которая имеет особенности в зависимости от уровня рН желудка. При атрофическом гастрите уровень рН колеблется от 3 до 6 (чем выше показатель, тем ниже кислотность!!!). Учитывая то, что в схему уничтожения Н.Рylori входят препараты, понижающие кислотность желудочного сока, логически следует, что назначать их вне зависимости от уровня рН неразумно. Таким образом при уровне рН от 3 до 6 ИПП входят в схему лечения, а при уровне больше 6 (анацидное («бескислотное») состояние) уничтожение H.pylori осуществляется только с помощью антибиотиков.
При атрофическом гастрите уровень рН колеблется от 3 до 6 (чем выше показатель, тем ниже кислотность!!!). Учитывая то, что в схему уничтожения Н.Рylori входят препараты, понижающие кислотность желудочного сока, логически следует, что назначать их вне зависимости от уровня рН неразумно. Таким образом при уровне рН от 3 до 6 ИПП входят в схему лечения, а при уровне больше 6 (анацидное («бескислотное») состояние) уничтожение H.pylori осуществляется только с помощью антибиотиков.
В случае НР-негативного атрофического гастрита наиболее вероятной является автоиммунная этиология. Однако в случае автоиммунного гастрита нет эффективного лечения, направленного на причину болезни, а патогенетическая терапия глюкокортикоидами (позволяющая изменить ход патологического процесса) показана только в случае развития В12-дефицытной анемии, обусловленной недостаточностью внутреннего фактора Касла, вследствие поражения париетальных клеток слизистой желудка. Таким образом при автоиммунной причине атрофического гастрита приходится использовать только симптоматическую и заместительную терапию.
Заместительная терапия осуществляется с целью восполнения недостающего желудочного сока. С этой целью используются натуральный желудочный сок, ацидин-пепсин (таблетки, которые в растворе образуют соляную кислоту), препараты желудочных ферментов (например, абомин). Используют также средства, усиливающие секрецию соляной кислоты. Естественно они уступают в эффективности препаратам заместительной терапии, однако могут быть полезны при легком течении или в фазе ремиссии заболевания. Это минеральные воды Миргородская, Нарзан, Ессентуки №4 и № 17; соки (лимонный, томатный, капустный, разбавленные кипяченой водой), отвар шиповника; препараты на основе лекарственных растений (подорожника, зверобоя, полыни, чабреца)- особенно часто используется Пантаглюцид на основе подорожника; препараты содержащие лимонную и (или) янтарную кислоты (Лимонтар, Пангаст).
Показаны к применению средства, направленные на защиту слизистой желудка (препараты висмута и алюминия), а также способствующие ее регенерации,- к примеру солкосерил (чаще используется при эрозивном гастрите).
При усиленной моторике желудка, которая часто имеет место при атрофическом гастрите, применяются прокинетики (домперидон, цизаприд).
В фазе ремиссии используются средства заместительной терапии или препараты, стимулирующие секреторную функции желудка-в зависимости от выраженности процесса и уровня кислотности желудочного сока.
Атрофический гастрит: признаки и лечение
Атрофический гастрит – это патологический процесс, при котором слизистая желудка истончается, а количество секреторных клеток уменьшается. В серьезных случаях процесс сопровождается формированием кист.
Признаки
Признаки атрофического гастрита проявляются при развитии заболевания. Самые распространенные признаки атрофического гастрита: переполненности желудка, тяжести, дискомфорта. Болевые ощущения наблюдаются редко. После еде возникает отрыжка с неприятным послевкусием, изжога. Сопровождается снижением веса. Потерей аппетита, нарушением стула.
После еде возникает отрыжка с неприятным послевкусием, изжога. Сопровождается снижением веса. Потерей аппетита, нарушением стула.
Очаговый атрофический гастрит
Очаговый атрофический гастрит – это чаще хронический гастрит, при котором истончение слизистой происходит на небольших участках. При этом симптомы могут быть смазанными, проявляться в меньшей степени.
Кислотность при атрофическом гастрите часто снижена из-за недостаточного количества клеток, выделяющих желудочный сок и пищеварительные ферменты. В этом случае производится коррекция лечебных процедур.
Лечение
Лечение атрофического гастрита проводится в комплексе, и при всей эффективности лекарственных средств требует диеты и пробиотической поддержки. При лечении важно понять, как изменена кислотность: это определяет диету и подбор препаратов.
При атрофическом гастрите с пониженной кислотностью необходимо отказаться от хлебобулочных изделий и молока.
При повышенной кислотности запрещен: творог, кисломолочные продукты, соленая, копченая, острая пища и томаты. Так же противопоказаны мясные супы, густые наваристые бульоны, жирная пища.
Эффективность комплекса
Атрофический гастрит с пониженной и повышенной кислотностью требует применения пробиотиков для восстановления функций слизистой. Комплекс Бифидум БАГ Трилакт Экофлор оптимально сбалансирован для лечения гастрита.
В первые 10-15 дней производится снятие воспаления, для чего рекомендуются повышенные дозы Бифидум БАГ(10 мл). в дальнейшем пробиотики корректируют флору ЖКТ и нормализуют кислотность. При пониженной кислотности рекомендуется применение Трилакта для стимулирования выработки ферментов.
После выздоровления рекомендуется в течении месяца принимать половинную дозу Бифидума натощак для закрепления результатов.
Наши пробиотики:
Посмотреть все
Какие фрукты можно есть при гастрите?
Гастрит характеризуется воспалением слизистой оболочки желудка, которое развивается вследствие агрессивного воздействия соляной кислоты на стенки органа. Чтобы предупредить дальнейшую прогрессию патологии, необходимо правильно скорректировать свой рацион. Большинство вопросов возникает по поводу фруктов. Важно понять, какие фрукты можно есть при гастрите.
Список разрешенных фруктов
Допускается употребление следующих фруктов при развитии гастрита.
- Груши. Мягкая структура этих фруктов помогает вывести из организма токсины, шлаковые массы и избыток холестерина. Активные растительные компоненты нормализуют пищеварение, улучшают регенерацию тканей. Злоупотреблять грушами при гастрите не следует, чтобы не спровоцировать развитие желудочно-кишечного расстройства. Для получения витаминов можно принимать их в пищу 2-3 раза в неделю.
- Яблоки. Сладкие сорта фруктов в сыром виде допускаются к употреблению при эрозивном гастрите с повышенной кислотностью. При этом необходимо употреблять их без кожуры. На фоне гиперацидного гастрита разрешается принимать в пищу кислые сорта яблок в свежем или приготовленном виде. Фрукты в виде пюре не рекомендуется принимать на ночь, чтобы снизить риск развития колик.
- Бананы. Их можно есть при гастрите как острой, так и хронической формы. Они особенно полезны при воспалении, возникающем по причине повышенной кислотности желудочного сока. Бананы отличаются мягкой волокнистой структурой, содержащей жиры и сложные углеводы (крахмал). Последние мягко обволакивают пораженные стенки органа, защищая его от воздействия соляной кислоты. Чтобы нормализовать пищеварение, достаточно съедать по 1 банану в день. В то же время при наличии метеоризма не стоит злоупотреблять фруктами.
- Арбуз. Водянистая ягода помогает вывести из организма ядовитые вещества, освобождает желудочно-кишечный тракт от шлаков. При гастрите не рекомендуется злоупотреблять арбузом, чтобы не спровоцировать развитие диареи. Можно принимать ягоду каждый день по 200-400 г для улучшения общего самочувствия. Для получения лекарственного эффекта допускается употребление отвара на основе арбузной корки. Высушенные части плода в размере 5 ст. л. следует залить 1 л горячей воды и кипятить средство в течение 30 минут. В отфильтрованном виде нужно принимать отвар по 200 мл 4-5 раз в день перед приемом пищи.
- Хурма. Данный фрукт оказывает сильный антибактериальный эффект, что полезно при гастрите. Хурма помогает подавить число патогенных бактерий и стабилизировать пищеварение. Кроме того, плод улучшает работу иммунной системы, оказывает щадящее воздействие на воспаленные слизистые оболочки желудка. Для получения лечебного эффекта достаточно употреблять 1-2 фрукта в сутки в свежем виде. Высокое содержание тиамина в составе продукта помогает стабилизировать уровень кислотности желудочного сока.
- Авокадо. Плоды оказывают мощное противомикробное действие, которое помогает улучшить динамику выздоровления и стабилизирует работу пищеварительной системы человека. Для получения максимального эффекта гастроэнтерологи рекомендуют употреблять 1 плод в сутки. Растительные масла создают гидрофобную пленку на пораженных стенках органа, защищая их от действия соляной кислоты.
При гастритах, спровоцированных ростом колонии helicobacter pylori, рекомендуется употреблять клюкву. Это природный антибиотик, подавляющий размножение патогенных микроорганизмов. Продукты с клюквой можно принимать как при низкой, так и при высокой кислотности желудочного сока. При гипоацидном гастрите рекомендуется употребление охлажденных клюквенных морсов.
Для улучшения регенерации тканей можно добавить в напиток мед.
Эрозивный гастрит и язва желудка
При тяжелом гастрите с высоким риском развития язвы желудка рекомендуется ужесточить рацион питания, исключив любые раздражающие слизистую оболочку продукты. Специальное меню разрабатывается при эрозивном гастрите. Фрукты исключаются в период обострения патологического процесса. Их рекомендуется принимать только в периоды ремиссии.
По окончанию острой фазы эрозивного гастрита следует постепенно вводить в рацион зрелые груши и яблоки, освобожденные от кожуры, в пюрированном виде. Можно употреблять сладкие сливы, очищенные от кожицы. Такие продукты не создают дополнительной нагрузки на органы пищеварения и не вызывают раздражение слизистых оболочек желудка.
Наиболее подходящим продуктом являются бананы. Высокое содержание калия и дубильных веществ стабилизирует обмен веществ, ускоряет регенерацию тканей. Активные растительные соединения обволакивают поврежденные стенки органа, создавая гидрофобную оболочку. Последняя не пропускает соляную кислоту к поврежденным эпителиальным клеткам. Банан нейтрализует повышенную кислотность желудка.
При высоком риске развития эрозивно-язвенной болезни рекомендуется отказаться от употребления кислых продуктов и фруктов, вызывающих сильное брожение в желудке. К данной категории относятся цитрусовые, персики, виноград, дыни.
Атрофический гастрит
Атрофический гастрит характеризуется хроническим течением, сопровождающимся истончением слизистых оболочек органа с последующей деградацией пищеварительных желез. Они прекращают вырабатывать сок в достаточном количестве, что приводит к снижению кислотности желудка. При данном виде гастрита разрешается употреблять как кислые, так и щелочные фрукты и ягоды.
Из цитрусовых следует заваривать чай, который можно пить вместе с десертом. При употреблении в сыром виде они могут повредить истонченные стенки органа. Помимо кислых фруктов можно употреблять следующие виды.
- Бананы. Благодаря мягкой структуре они легко перевариваются и быстро усваиваются в тонком кишечнике, не создавая дополнительную нагрузку на желудок.
- Яблоки. Рекомендуется увеличить употребление фруктов кислых сортов, чтобы повысить кислотность желудочного сока. При атрофическом гастрите необходимо пюрировать плоды, чтобы облегчить нагрузку на пищеварение.
- Арбузы. Чтобы не навредить ослабленному органу, рекомендуется употреблять водяные ягоды в конце лета. В этот период они практически не обрабатываются пестицидами, которые могли бы спровоцировать ухудшение общего состояния.
Продукты с грубой растительной клетчаткой необходимо исключить из рациона. Инжир, финики и некоторые ягоды требуют длительного переваривания, из-за чего могут навредить ослабленным стенкам органа пищеварения.
Что нельзя есть?
В группу запрещенных продуктов входят фрукты, которые могут спровоцировать обострение заболевания и привести к ухудшению общего состояния больного. Даже после полного выздоровления от гастрита следует ограничить или вовсе исключить их употребление, чтобы снизить риск рецидива заболевания.
Цитрусовые
Характерная черта всех цитрусовых фруктов — это высокое содержание различных органических кислот, особенно лимонной и яблочной. Последние вызывают резкое обострение симптомов гастрита, ухудшают динамику заболевания и приводят к сильному раздражению слизистых оболочек.
Небольшое количество цитрусовых фруктов разрешается употреблять после приема пищи при гастрите с низким уровнем кислотности в желудке. При этом необходимо сначала проконсультироваться с гастроэнтерологом.
Чтобы снизить кислотность фруктов, рекомендуется разбавлять их сок или употреблять их вместе со стаканом минеральной воды.
Виноград
Виноград отличается сложной структурой, содержащей много растительных волокон и питательных соединений. Эта ягода переваривается слишком долго, из-за чего выделяется много кислоты. Обилие желудочного сока негативно воздействует на поврежденные слизистые оболочки, вызывая их дальнейшее разрушение. При попадании в желудок винограда на фоне гастрита раздраженная слизистая от отека и острой боли практически не функционирует. За этот период ягода начинает гнить, развивается брожение. Состояние больного ухудшается, повышается риск развития эрозивно-язвенной патологии в желудке.
Киви
Киви разрешены только при гастритах, характеризующихся пониженной кислотностью пищеварительного сока. Но даже при развитии заболевания с гипоацидной средой в желудке зеленые плоды можно употреблять после приема пищи. Эти фрукты насыщены аскорбиновой кислотой, которая не только повышает уровень кислотности в органе. Витамин C повышает аппетит, тем самым способствуя увеличению секреции желудочного сока.
Дыня
Несмотря на высокое содержание витаминов и минералов, данный представитель бахчевых культур противопоказан при воспалении слизистой желудка. Для переваривания продукта потребуется много времени и энергетических запасов. Чем дольше длится пищеварение в желудке, тем больше соляной кислоты вырабатывается и сильнее повреждается стенка органа.
При тяжелом гастрите дыня практически не переваривается и начинает бродить, из-за чего может привести к развитию перфоративной язвы или кровотечению в желудке.
Персики
Персики не рекомендуется принимать при гастрите в свежем виде, потому как активные растительные соединения в их составе оказывают сильный слабительный эффект. При усилении перистальтики гладкой мускулатуры органов пищеварения обостряется боль и раздражение поврежденных стенок желудка. Кроме того, персик улучшает выработку желудочного сока, что может ухудшить состояние больного. Персики при заболеваниях ЖКТ рекомендуется принимать в приготовленном виде: в составе киселей, компотов или выпечки.
Фруктовый рацион при повышенной кислотности
При повышенной кислотности желудочного сока запрещено применение фруктов и ягод с высоким содержанием органических кислот, которые могут привести к ухудшению динамики патологии. В этот период рекомендуется есть щелочные продукты, нейтрализующие соляную кислоту. Допускается применение фруктов, не оказывающих влияния на уровень кислотности в желудке.
Фрукты рекомендуется есть без кожуры. Для нормализации пищеварения можно употреблять бананы. Крахмалистый овощ содержит слизистые соединения, создающие защитную пленку в области воспаления. При высокой кислотности пищеварительного сока разрешается применение следующих фруктов.
- Ананасы. Экзотические плоды обладают высоким содержанием щелочей, которые помогают частично нейтрализовать соляную кислоту.
- Сливы. Улучшают перистальтику гладкой мускулатуры, оказывают легкий слабительный эффект. При гастрите активизируют регенерацию поврежденных стенок желудка.
- Яблоки сладких сортов. Рыхлая структура фруктов не влияет на уровень кислотности, поэтому их можно употреблять по 2-3 штуки в день без опасения за желудок.
- Груши мягких сортов. Оказывают противовоспалительный эффект в области очага поражения. Дубильные вещества улучшают регенерацию слизистых оболочек, уменьшают кислотность.
- Тыква. В приготовленном виде легко усваивается, улучшает пищеварение и снижает кислотность в желудке. Свежевыжатый сок способствует очистке организма.
- Авокадо. Растительные масла и витамин E обволакивают стенки желудка, облегчая процесс пищеварения. Помогают при язве желудка, снижают кислотность пищеварительного сока.
Какие плоды полезны при обострении?
В период обострения заболевания гастроэнтерологи рекомендуют отказаться от употребления в пищу любых фруктов. В это время интенсивность проявления симптомов достигает своего пика, слизистая оболочка желудка становится более чувствительной. Растительная пища приводит к раздражению стенок органа, нарушает пищеварение и ухудшает динамику заболевания.
В первые 3-4 дня пациенту рекомендуется принимать постные и молочные супы, жидкие злаковые каши и кисели. После этого периода, когда состояние больного стабилизируется, можно вводить в рацион тушеную растительную пищу. Позднее можно попробовать печеные яблоки с ложкой меда. Остальные фрукты в свежем виде можно принимать только в периоды ремиссии.
О том, как питаться при гастрите, смотрите в следующем видео.
Диета при гастрите с пониженной кислотностью
Диета при гастрите с пониженной кислотностью во время лечения заболевания имеет большое значение, поскольку помогает улучшить состояние, предупреждает дальнейшее снижение секреции желудочного сока и нормализует работу пищеварительной системы.
Основы диеты при хроническом гастрите с пониженной кислотностью
Рацион при наличии такого заболевания должен включать в себя продукты, которые активируют выработку желудочного сока. Важно чтобы пища не переваривалась в желудке длительное время. Необходимо исключить из рациона продукты, которые вызывают процесс брожения, к примеру, свежую выпечку, молоко, продукты с большим количеством животных жиров. Готовить еду можно разными способами, за исключением жарки. Основа диеты при атрофическом гастрите с пониженной кислотностью – супы, приготовленные на нежирном бульоне. Мясо и рыбу варите или запекайте. Фрукты можно есть в любых количествах, а вот из овощей лучше всего делать пюре. Важно исключать продукты, которые содержат большое количество клетчатки. Необходимо отказаться от слишком кислых продуктов. Хлеб должен быть немного подсушенным и лучше ограничить количество ржаной выпечки. Что касается круп, то лучше всего отдавать предпочтение овсянке, гречке и рису. Исключить из меню стоит копченое, соленое и блюда с большим количеством специй. После жестких ограничений, можно добавить в рацион немного жареного и жирного.
Ежедневное меню диеты при гастрите с пониженной кислотностью может выглядеть так:
Завтрак: порция овсяной каши, хлебец с сыром, 1 ст. сока из морковки со сливками, кофе.
Перекус: йогурт.
Обед: суп-пюре из грибов, шницель с пюре из картофеля, салат из помидоров и зелени, который заправляется оливковым маслом, желе и морс.
Перекус: отвар из отрубей и хлебцы.
Ужин: рыба, запеченная в духовке, с тушеными овощами и чай.
Перед сном: 1 ст. кефира.
Распространенность, причины, симптомы, типы и лечение
По определению, атрофический гастрит возникает, когда слизистая оболочка желудка со временем воспаляется в результате бактериальной инфекции, вызванной воздействием вируса H. pylori. По сути, эти бактерии отвечают за разрушение защитного слоя слизи, окружающего слизистую оболочку желудка, и за нарушение его барьера от вредных кислых жидкостей, которые способствуют правильному пищеварению. Как только эти жидкости вступают в прямой контакт со слизистой оболочкой желудка, она может инфицироваться и сильно воспалиться.Если не лечить слишком долго, эта инфекция может полностью уничтожить здоровые клетки слизистой оболочки желудка. Этот тип бактериальной инфекции обычно начинается в детстве и может постепенно ухудшаться по мере взросления.
Какие бывают типы атрофического гастрита?
Существует два основных типа атрофического гастрита:
Атрофический гастрит типа А (аутоиммунный атрофический гастрит):
Люди, страдающие различными аутоиммунными заболеваниями, также могут быть предрасположены к атрофическому гастриту.Антитела, которые создаются иммунной системой с целью атаковать и уничтожать деструктивные чужеродные вирусы в организме, по ошибке атакуют здоровые клетки, которые вырабатываются организмом естественным образом для поддержания нормальных функций. Сюда входят клетки, которые включают в себя внутренний фактор желудка, который в первую очередь отвечает за поглощение и переработку витамина B-12.
Атрофический гастрит типа B:
Это мультифокальный тип атрофического гастрита, имеющий ряд причин, главная из которых – появление H.pylori в систему. Этот вирус атакует и ослабляет слизь, окружающую слизистую оболочку желудка, что подвергает ее вредному воздействию кислых соков, выделяемых некоторыми продуктами. Факторы окружающей среды, такие как неправильная диета, лишенная надлежащей питательной ценности и плохие гигиенические правила, также могут способствовать заражению вирусом H. pylori и развитию атрофического гастрита типа B.
Причины атрофического гастрита и связанные с ним осложнения
Как уже упоминалось, атрофический гастрит обычно начинается в детстве, когда человек изначально инфицирован H.pylori вирус. Если у них разовьется аутоиммунное заболевание, симптомы могут проявиться в течение многих лет, если вообще проявятся. Начало аутоиммунного атрофического гастрита происходит в результате того, что иммунная система активно инструктирует антитела атаковать все здоровые клетки организма. Эти антитела вырабатываются иммунной системой с основной целью выявления и уничтожения потенциально вредных чужеродных веществ, клеток и вирусов в организме.
В случае аутоиммунных заболеваний антитела начинают атаковать здоровые клетки желудка, что может вызвать сильное воспаление слизистой оболочки.Кроме того, эти антитела также атакуют внутренний фактор вашего желудка, который представляет собой естественный белок, который помогает усвоению и переработке витамина B-12.
В результате у вас может развиться дефицит витамина B12 и злокачественная анемия из-за сильно сниженного количества эритроцитов и неспособности вашего организма производить достаточное количество эритроцитов для поддержания нормальных функций. Хроническое воспаление желудка ослабляет способность организма перерабатывать различные витамины и питательные вещества.В худшем случае это также может негативно повлиять на способность вашего организма предотвращать и защищать себя от серьезных заболеваний, в первую очередь рака.
Распространенность атрофического гастрита
Точная распространенность атрофического гастрита неизвестна, потому что многие потенциальные случаи заболевания не диагностируются из-за того, что оно протекает бессимптомно или симптомы, как правило, трудно идентифицировать. Дело в том, что многие симптомы, приписываемые атрофическому гастриту, также соответствуют ряду других физических недугов.У человека может потребоваться много лет, чтобы даже развить атрофический гастрит, поскольку он обычно начинается в детстве и часто неправильно диагностируется или не диагностируется до взрослого возраста.
Вирус H. pylori, который, как известно, вызывает большинство случаев атрофического гастрита, поражает примерно 20 процентов людей в возрасте до 40 лет только в Соединенных Штатах и 50 процентов населения старше 60 лет. инфекции наиболее распространены среди определенных культурных групп, включая людей азиатского, афроамериканского и латиноамериканского происхождения.Он наиболее распространен в Азии, однако, по оценкам, около 50 процентов населения мира в настоящее время инфицировано вирусом H. pylori. Люди в развивающихся странах подвергаются наибольшему риску развития и смерти от этого заболевания из-за плохих условий жизни.
Каковы признаки и симптомы атрофического гастрита?
По большей части атрофический гастрит протекает бессимптомно, что означает, что человек может быть инфицирован вирусом H. pylori всю свою жизнь, не проявляя никаких симптомов вплоть до более позднего возраста.Или они могут быть несимптоматическими носителями вируса и легко передавать его другим через зараженную пищу, слюну и другие жидкости организма. Различные типы атрофического гастрита также имеют свой уникальный набор симптомов.
Ниже приводится список симптомов атрофического гастрита типа А:
- Сильные боли в груди
- Дурнота и головокружение
- Учащенное сердцебиение
- Звон в ушах, известный как тиннитус
- Физическая слабость
- Дефицит B12, имеющий собственный уникальный список симптомов и последствий
Атрофический гастрит типа B обычно проявляется следующими симптомами:
- Тошнота и рвота
- Язвенная болезнь желудка
- Снижение или полная потеря аппетита
- Значительная незапланированная потеря веса из-за отсутствия аппетита
- Сильные боли в животе
- Дефицит железа в результате злокачественной анемии (снижение количества эритроцитов и неспособность производить новые эритроциты)
Диагностика и лечение атрофического гастрита
Диагностика
Точная диагностика атрофического гастрита обычно включает серию клинических тестов, наблюдений, а иногда и обширный анализ крови.Планирование регулярных медицинских осмотров имеет важное значение для раннего выявления и предотвращения перехода атрофического гастрита в другие, более опасные для жизни заболевания.
Эти тесты предназначены для определения уровня пепсиногена и гастрина. Уровни пепсиногена обычно чрезвычайно низкие у людей, страдающих атрофическим гастритом, тогда как уровни гастрина обычно опасно и обманчиво высоки, поскольку этот гормон способствует выработке желудочного сока. Они также помогают определить, есть ли у вас дефицит витамина B-12.Во время регулярных посещений врач также может определить, есть ли у вас аутоиммунное заболевание, из-за которого иммунная система атакует здоровые клетки по всему телу, включая те, которые составляют слизистую оболочку желудка.
Каким бы неудобным это ни было, в некоторых случаях биопсия желудка также может оказаться необходимой и более полезной для точного определения симптомов атрофического гастрита. Во время этой процедуры ваш врач вставит эндоскоп (тонкий, длинный металлический инструмент с прикрепленным к нему маленьким фонариком) в ваше горло и опустит его до вашего желудка.С этого момента они будут извлекать небольшой образец ткани из слизистой оболочки желудка для дальнейшего и более детального исследования, чтобы определить, есть ли какие-либо признаки возможного атрофического гастрита. Этот образец ткани из вашего желудка также может показывать явные признаки вирусной инфекции H. pylori.
Во время этих различных обследований ваш врач будет прощупывать определенные части вашего живота, чтобы проверить необычную болезненность и обнаружить признаки возможного дефицита B-12, такие как неврологические проблемы, нехарактерная бледность и учащенный пульс.
Лечение
Антибиотики – наиболее эффективный метод лечения атрофического гастрита типа А, поскольку они помогают бороться с вирусом H. pylori, вызывающим его, и полностью уничтожают его. Некоторые противовоспалительные препараты также могут быть назначены для уменьшения внутреннего воспаления желудка и контроля выработки кислот в желудке, которые помогают переваривать пищу. Людям, у которых в результате этого вируса наблюдается легкий или серьезный дефицит витамина B-12, также могут потребоваться регулярные инъекции B-12, особенно если человек страдает аутоиммунным атрофическим гастритом.
Рекомендуемая диета для больных атрофическим гастритом
Как обычно бывает с любым хроническим заболеванием, есть определенные продукты, которые вполне приемлемы и даже полезны для употребления, а также другие, которых вам, вероятно, следует избегать, как чумы, если вы страдаете атрофическим гастритом типа A или типа B.
Вот список продуктов, которые следует исключить из своего рациона:
- Кофе
- Острая пища
- Алкоголь
- Любые кислые продукты (помидоры, цитрусовые и др.))
- Продукты с высоким содержанием жира
- Жареные продукты
- Соки фруктовые (натуральные и концентрированные)
- Газированные напитки, например газированная вода или газированные напитки
- Аллергенные или симптоматические продукты
С другой стороны, лучшая диета при атрофическом гастрите должна включать в умеренных количествах следующие продукты:
- Продукты, являющиеся хорошим источником клетчатки
- Нежирные продукты
- Газированные напитки, например обычная вода
- Продукты питания и напитки с низким уровнем кислотности
- Любые напитки, не содержащие кофеина
- Продукты, содержащие пробиотики, так как они могут помочь очистить пищеварительный тракт и улучшить пищеварение.
Однако, прежде чем вносить какие-либо радикальные изменения в свой общий рацион, вы всегда должны проконсультироваться со своим терапевтом и убедиться, что вы следуете подробному диетическому плану под его наблюдением и советами.
Прежде чем вносить какие-либо радикальные изменения в свой общий рацион, вы всегда должны проконсультироваться со своим терапевтом и обязательно следовать подробному плану питания и упражнений, который они составят для вас под его непосредственным наблюдением и советами. Периодически консультируйтесь с врачом, чтобы он мог изучить, как эти физические изменения влияют на ваше общее состояние здоровья и можете ли вы эффективно управлять атрофическим гастритом и лечить его.
В зависимости от типа имеющегося у вас атрофического гастрита и степени его прогрессирования лечение может быть эффективным немедленно или может потребоваться значительное время, чтобы оно подействовало.Суть в том, что если вы испытываете какой-либо один или комбинацию вышеупомянутых симптомов, вам следует немедленно обратиться к врачу.
Связано: ощущение жжения в желудке: причины, симптомы и домашние средства
Наследственный аутоиммунный атрофический гастрит | Палео диета®
Доктор Кордейн,
Спасибо, что нашли время в конце дня, чтобы перезвонить мне в пятницу. Жалко, что я пропустил твой звонок, потому что прямой разговор более обстоятельный.Я благодарен за получение вашего адреса электронной почты.
В прошлый понедельник я вышел из кабинета врача-терапевта, размышляя над его словами о том, что он хотел бы продолжать обследовать меня каждые шесть месяцев, чтобы уловить это пораньше. Первоначально меня обследовали в октябре 2011 года, и тогда я узнал, что мой живот серый и гладкий, как шар; В отчете о патологии и лабораторных исследованиях был поставлен диагноз: наследственный аутоиммунный атрофический гастрит, хроническое воспаление с кишечной метаплазией. Нарисованные лаборатории показали, что у меня 124 антитела к париетальным клеткам.6, что не соответствовало графику, так как оно не должно было быть больше 20. Моя спасительная милость за то, что у меня не развилась пагубная анемия, заключалась в том, что я принимал добавки (довольно много) в течение нескольких лет.
В то время моя слизистая оболочка исчезла, и мой тогдашний врач-терапевт и врач-терапевт сказали мне, что это необратимо из-за того, что это «унаследованное» аутоиммунное заболевание. 3 года назад мне поставили диагноз целиакия, и в то время я не употреблял глютен в течение 3 лет.Прошлой зимой я посетил презентацию аутоиммунных заболеваний в Медицинском центре Anschutz (sp?), И в общей сложности 6 врачей мне сказали, что то, что у меня есть, встречается редко, и что это необратимо, и что более чем вероятно, что я проиграю. мой желудок по крупицам, если бы не моя жизнь. Первый врач, изучивший меня, не поддержал работу, которую выполняет мой основной врач, поскольку, хотя она (Моник Мали, доктор медицины) является доктором медицины, она широко практикует альтернативное здравоохранение. Мой ответ на то, что этот солдатик мне не подходит, заключался в том, что я получил второе мнение с другим солдатом, доктором.Люк Эванс, который уже дважды изучал меня. Он чувствует жизнь других врачей-терапевтов и патологоанатома, что в моем состоянии чрезвычайно высок риск развития рака желудка.
В ноябре 2011 года доктор Мали провел у меня тщательный анализ стула, который показал, что я все еще питаюсь H-Pylori, и из-за хрупкости моего желудка мы лечили его ботаническими препаратами (Pyloricil), которые действительно искоренили H-Pylori. Я также отказался от кофеина в октябре, узнав о состоянии своего желудка.
В апреле 2012 года меня снова обследовали, и эндоскопический осмотр моего желудка показал, что у меня снова была нормальная, здоровая слизистая оболочка, но также обнаружилось, что у меня 3 полипа желудка, в отчете о патологии говорилось, что у меня все еще был аутоиммунный атрофический гастрит, но количество париетальных антител упало до 106,3; все еще слишком высоко.
Я продолжал есть «без глютена», но ел хлеб, крупы и злаки без глютена, а также продолжал пить зеленый напиток (который я употреблял в течение 8 лет), продукт Garden of Life, Perfect Food.Затем я прекратил употреблять все молочные продукты.
Мне снова сделали осмотр в октябре 2012 года, и, хотя 3 полипа исчезли, слизистая оболочка выглядит великолепно и визуально, мой врач-врач не заметил воспаления; однако отчет о патологии вернулся с атрофическим гастритом с умеренным воспалением; повторный подсчет париетальных антител составил 105,1. Несмотря на то, что он снизился, это все еще далеко от графика.
Я встретился со своим основным доктором медицины в пятницу, 30 ноября, и она считает, что мое тело продолжает перекрестно реагировать на «что-то», и она упомянула о проведении теста на пищевую аллергию, который я проводил ранее (много лет назад, до моего отказавшись от глютена).Затем я встретился с врачом-терапевтом в понедельник, 3 декабря, чтобы подробно изучить мои отчеты из области 10/24, и именно тогда он очень четко определил, что хочет продолжать обследовать меня (эндоскопия) каждые 6 месяцев и «он рано поймает» (рак). В ответ на мой вопрос, который я задавал с тех пор, как год назад узнал о моем аутоиммунном заболевании, он не знает, как регулировать мой иммунный ответ, и ответ, опять же, был отрицательным (он принимал стероиды в прошлом для людей с ревматоидными заболеваниями), и мы с ним знаем, что стероиды – это не ответ.
Я вышел из его офиса в тот день неделю назад и остановился в Vitamin Cottage, магазине, в котором я часто езжу по магазинам. В разговоре с диетологом (мой диетолог в декрете) я поделилась с ней своей историей, а также своим разочарованием. От нее я впервые с тех пор, как узнал что-либо о целиакии и глютене, узнал, что другие злаки и бобовые могут быть такой же проблемой для некоторых, как глютен. Она провела время со мной, предоставив мне информацию, она прислала мне видеопрезентацию: Глютен, нерассказанная история, пшеница – не единственная глава; и она познакомила меня с концепцией / теорией / верованием палеодиеты.Выйдя из этого магазина, я понял, что, хотя я предпринял большие шаги, чтобы сделать все возможное, чтобы стать здоровым, мне нечего терять, включив палеодиету / образ жизни в свою жизнь.
Я зашел на ваш веб-сайт, прочитал там большую часть материала и вчера вечером купил вашу книгу «Поваренная книга палеодиеты», которую я с радостью начал читать. Вчера вечером я ходил в тот магазин за вашей книгой «Палеодиета», из которой они вышли.
На прошлой неделе я связался с компанией Garden of Life и рассказал им о том, как я использую их продукт в течение 8 лет, что у меня целиакия и я не употребляю глютен, но у меня также есть аутоиммунный атрофический гастрит и что мой главный врач считает, что я продолжаю перекрестно реагировать на «что-то», и они поделились со мной, что людям с целиакией не следует использовать их продукты.Излишне говорить, что я его прекратил.
Мое личное мнение о моем состоянии состоит в том, что это была реакция окружающей среды из-за моей генетической предрасположенности, из-за того, что я укрывал (без моего ведома) H-Pylori, в сочетании с тем, что мое тело продолжает реагировать на то, что я продолжая принимать работают с людьми с такими условиями, как у меня.Я считаю, что мой иммунный ответ продолжается из-за продолжающегося приема пищи, которую я ел. У меня действительно есть семейный анамнез со стороны отца, у которого было какое-то слабоумие (вскрытия не проводились) у моего отца, его матери и двух моих теток по отцовской линии. Я подозреваю, что вполне возможно, что у них тоже была та же проблема, что и у меня, но их состояния никогда не были известны и не лечились. Мои обширные добавки до этого момента были моей спасительной милостью, так как все мои лаборатории по питанию превосходны.
Я действительно позвонил своему терапевту, оставив слово, сообщение, что я начал соблюдать палеодиету, и ее офис перезвонил мне, сообщив, что она очень поддерживает мое включение диеты в мою жизнь; говоря, что если я хочу встретиться с ней, чтобы обсудить это, она доступна. Насколько мне известно, хотя она поддерживает это, я вижу ее уже около 4 лет, и так было до тех пор, пока я не упомянул о палеодиете (после моей встречи с диетологом в Vitamin Cottage 12/3, который представил меня к концепции, о которой я никогда не слышал), что она сказала, что одобряет то, что я делаю.Я бы хотел встретиться с врачом, который активно работает с людьми с аутоиммунными заболеваниями, который также хорошо осведомлен о палео-образе жизни. Одним из многих аспектов работы с доктором Мали было то, что, несмотря на то, что она доктор медицины, которая также принимает мою страховку Blue Cross Insurance (PPO) (очень важный факт из-за стоимости), она полностью выглядит нестандартно, используя альтернативное здравоохранение, которое я ценил.
Я понимаю, что отправил вам электронное письмо уже давно, и я уважаю то, что ваше время и то, как вы его тратите, очень ценны для вас.Я работал в сфере здравоохранения помощником по административным вопросам (17,5 лет в Детской больнице Денвера; 5,5 лет в Шведском медицинском центре) и знаю, насколько ценны преподаватели на таких должностях, как ваша.
Я буду ждать от вас известий, если позволит ваше расписание.
С благодарностью,
Екатерина
Ответ доктора Кордейна:
Привет, Кэти,
Прежде всего, я очень хотел бы выразить вам признательность за то, что вы страдали этим аутоиммунным заболеванием.Во-вторых, нет никакой гарантии, что палеодиета приведет к ремиссии вашего заболевания. Тем не менее, многие люди во всем мире с различными аутоиммунными заболеваниями сообщали о терапевтических эффектах или даже о полной ремиссии своих симптомов после того, как следовали этому пожизненному способу питания. Вместе с моим аспирантом Тревором мы только что завершили крупное тематическое исследование с участием около 100 пациентов с аутоиммунными заболеваниями, которые приняли палеодиету. Мы опубликуем результаты этого исследования в научной литературе, и наши результаты обнадеживают, особенно для пациентов с аутоиммунными заболеваниями желудочно-кишечного тракта.У нас не было пациентов с аутоиммунным атрофическим гастритом. Принятие палеодиеты не несет никаких рисков для здоровья или питания, на самом деле верно противоположное, поскольку такой способ питания фактически снижает риск многих распространенных хронических заболеваний и увеличивает питательную ценность рациона, поскольку фрукты, овощи, морепродукты и мясо по питательности значительно превосходят зерновые, обработанные пищевые продукты и молочные продукты, которые составляют около 70% калорий в типичной диете США.
Как вы правильно поняли, практически все аутоиммунные заболевания являются результатом как наследственных (генетических) факторов, так и факторов окружающей среды.Основным наследственным фактором, связанным с аутоиммунными заболеваниями, является часть иммунной системы, называемая системой человеческого лейкоцитарного антигена (HLA). Существуют тысячи разновидностей молекул HLA, но лишь некоторые из них связаны с аутоиммунными заболеваниями. Если вы унаследовали один из этих так называемых гаплотипов чувствительности к HLA, то ваш риск аутоиммунного заболевания резко возрастает. Однако было подсчитано, что около 70% риска аутоиммунитета связано с факторами окружающей среды. Многие иммунологи и ученые (включая меня), изучающие аутоиммунные заболевания, теперь считают, что повышенная кишечная проницаемость или «дырявый кишечник» представляет собой фундаментальный триггер окружающей среды, который предшествует развитию большинства аутоиммунных заболеваний.
Безглютеновая диета оказалась терапевтической для многих аутоиммунных пациентов (не только пациентов с глютеновой болезнью), и известно, что пшеница содержит по крайней мере три соединения (глиадин, агглютинин зародышей пшеницы [WGA] и тауматиноподобные белки), которые увеличивают проницаемость кишечника. . Другие зерна, содержащие глиадин, включают рожь и ячмень. С помощью палеодиеты мы рекомендуем исключить все злаки и все псевдозерна (лебеда, амарант, гречка и семена чиа). В моей последней книге «Палео-ответ» я описываю проблемы с питанием всех злаков и то, как они увеличивают кишечную проницаемость.
Вы упомянули, что употребляли Garden of Life’s, Perfect Food, Green Drink в течение 8 лет до того, как вам поставили диагноз аутоиммунный атрофический гастрит. Я направил свой интернет-браузер на веб-сайт этой компании и нашел ингредиенты в этом продукте, который на самом деле помечен как «Смесь сырого органического зеленого сока». 5 перечисленных ингредиентов: 1) органический сок травы ячменя, 2) органический сок травы люцерны, 3) органический сок травы овса, 4) органический сок травы пшеницы и 5) органический сок травы камута.Все эти ингредиенты в этом продукте содержат множество соединений, которые отрицательно влияют на проницаемость кишечника и функцию эпителиальных клеток (эпителиальные клетки – это клетки, выстилающие желудочно-кишечный тракт, включая желудок). Четыре из пяти ингредиентов получены из листьев злаков (ячмень, овес, пшеница, камут). Камут – это сорт пшеницы, известный как Хорасанская пшеница. Листья или стебли трав (семена которых мы называем зернами) также содержат высокие концентрации антинутриентов, которые также содержатся в их семенах, в том числе глиадин, WGA и тауматиноподобные белки, которые увеличивают проницаемость кишечника и отрицательно влияют на нормальную функцию иммунной системы. .Ростки люцерны содержат одни из самых высоких концентраций соединений, известных как «сапонины», в любых продуктах питания, обычно потребляемых в западной диете. Сапонины увеличивают проницаемость кишечника, но, кроме того, обладают мощным стимулирующим действием на иммунную систему – настолько, что иммунологи регулярно используют эти соединения в вакцинах (так называемых адъювантах) для усиления (возбуждения) иммунного ответа. Следовательно, этот продукт будет одной из худших добавок, которые может потреблять любой человек с генетической предрасположенностью к аутоиммунным заболеваниям.
Помимо зерна, листьев злаков и ростков люцерны, другие элементы типичной западной диеты также могут увеличивать кишечную проницаемость, включая все бобовые (арахис – это бобовые, как и все бобы), картофель, помидоры и другие растения, а также пасленовые. В моей последней книге «Палео-ответ» я изложил научные доказательства с сотнями цитат, показывающих, как эти продукты повышают проницаемость кишечника и действуют как иммунологические адъюванты, нарушая нормальное функционирование иммунной системы.Зеленые помидоры, помидоры черри и желтые помидоры содержат высокие концентрации соединения альфа-томатина, который увеличивает кишечную проницаемость. Спелые красные помидоры почти не содержат этого соединения, поэтому, если у вас нет аутоиммунного заболевания, вам не придется отказываться от этой вкусной еды. Картофель содержит два токсичных гликоалкалоидных соединения, которые представляют собой сапонины, известные как альфа-соланин и альфа-чаконин, которые также увеличивают кишечную проницаемость и быстро попадают в кровоток и могут вызывать неблагоприятные последствия для здоровья.В моей последней книге «Палео-ответ» я показываю, как возникают эти эффекты, и даю научные ссылки.
Другие продукты, которые могут быть проблематичными для аутоиммунных пациентов, поскольку они увеличивают кишечную проницаемость: этанол (алкоголь), аспирин, ибупрофен и другие НПВП, антациды, содержащие гидроксид алюминия (квасцы), противозачаточные таблетки, острый острый перец, содержащий капсаицин (сальса, острый перец). соус, перец чили, кайенский перец и т. д.).
При аутоиммунных заболеваниях я рекомендую вам сначала исключить очевидные продукты (зерновые, молочные, бобовые), а затем поэкспериментировать с исключением других продуктов, которые увеличивают проницаемость кишечника.Еще один последний продукт, который следует учитывать – яичные белки, которые представляют собой обычную аллергию, также содержат соединение, называемое лизоцимом, которое может нарушать функцию кишечника и обеспечивать доступ больших белковых молекул (антигенов) к системной иммунной системе
Большинство врачей, в отличие от академиков, не имеют возможности глубоко читать научную литературу, чтобы установить связь между диетой и аутоиммунитетом, а большинство иммунологов не читают литературу по питанию.
Сердечно,
Лорен Кордейн, Ph.D., заслуженный профессор
Уровни прогепсидина в сыворотке ниже у пациентов с атрофическим гастритом
Предпосылки / цель . Уровень гепсидина, гормона, регулирующего железо, повышается в ответ на воспаление и некоторые инфекции. Мы исследовали взаимосвязь между прогепсидином в сыворотке крови, статусом железа, статусом инфекции Helicobacter pylori и наличием атрофии слизистой оболочки желудка. Методы . Семьдесят субъектов, подвергшихся эзофагогастродуоденоскопии, прошли многократную биопсию желудка, и вероятность H.pylori и степень эндоскопического и гистологического гастрита. У всех испытуемых оценивались параметры сывороточного прогепсидина и железа. Результаты . Никаких корреляций между уровнями прогепсидина в сыворотке и другими маркерами анемии, такими как гемоглобин, сывороточное железо, ферритин и общая железосвязывающая способность, не наблюдалось. Уровни прогепсидина в сыворотке существенно не различались между группой H. pylori и отрицательной группой H. pylori .Уровни прогепсидина в сыворотке крови у пациентов с атрофическим гастритом были значительно ниже, чем у пациентов без атрофического гастрита, независимо от инфекции H. pylori . Заключение . Уровни прогепсидина в сыворотке крови не были изменены инфекцией H. pylori . Уровни прогепсидина в сыворотке крови снижаются у пациентов с атрофическим гастритом, независимо от инфекции H. pylori . Это предполагает, что гепсидин может снижаться из-за атрофии желудка, состояния, которое вызывает потерю продуцирующих гепсидин париетальных клеток.Для подтверждения этого утверждения необходимы дальнейшие исследования с большим количеством пациентов.
1. Введение
Человеческий гепсидин, 25-аминокислотный пептид, впервые идентифицированный в моче и плазме человека, который секретируется в основном печенью, проявляет антибактериальную и противогрибковую активность in vitro [1, 2]. Прогепсидин, форма-предшественник гепсидина, состоящая из 84 аминокислот, обнаруживается в крови [3]. Гепсидин является реагентом острой фазы, и его экспрессия повышается с помощью интерлейкина (ИЛ) -6 во время бактериальной инфекции и воспаления [4].Кроме того, гепсидин играет важную роль в гомеостатической регуляции метаболизма железа. Этот пептид действует, связываясь с ферропортином, экспортирующим клеточное железо, и индуцирует его интернализацию и деградацию, таким образом задерживая железо в энтероцитах, макрофагах и гепатоцитах [5]. Синтез гепсидина увеличивается при перегрузке железом и снижается при дефиците железа [6, 7].
Инфекция Helicobacter pylori с сопутствующим аутоиммунным гастритом или без него была вовлечена в нескольких недавних исследованиях как важная причина железодефицитной анемии (ЖДА) у пациентов с необъяснимой ЖДА [8].Возможные патогенные механизмы включают скрытую кровопотерю на фоне хронического эрозивного гастрита, снижение абсорбции железа на фоне гипохлоргидрии желудка, ассоциированной с атрофией, и повышенное поглощение и утилизацию железа H. pylori [9]. Более того, железодефицитные пациенты с инфекцией H. pylori , по-видимому, плохо реагируют на пероральную терапию железом до тех пор, пока бактерия не будет уничтожена [10–12]. Эта гипотеза была подтверждена исследованием, показывающим нарушение всасывания железа после пероральной нагрузки у инфицированных субъектов и восстановление нормального состояния после эрадикации [13].Было высказано предположение, что причиной неспособности пациентов с инфекцией H. pylori реагировать на железо может быть продукция гепсидина или миметиков гепсидина микроорганизмами [14, 15]. Недавнее исследование показало, что экспрессия гепсидина желудка была значительно повышена у инфицированных H. pylori пациентов и нормализовалась после эрадикации H. pylori [16]. Исследование также показало, что гепсидин желудка локализован в париетальных клетках, которые регулируют выработку кислоты желудочного сока.
Концентрации прогепсидина в сыворотке значительно снижаются у пациентов с наследственным гемохроматозом [3], повышаются при снижении функции почек [17] и положительно коррелируют с гематокритом у пациентов, находящихся на хроническом гемодиализе [18]. В этом исследовании мы оценили взаимосвязь между прогепсидином в сыворотке, статусом железа, статусом инфекции H. pylori и наличием атрофии слизистой оболочки желудка.
2. Материалы и методы
2.1. Популяция исследования
Это было одноцентровое обсервационное исследование случай-контроль с участием 70 субъектов, которые прошли обычное эндоскопическое обследование желудочно-кишечных симптомов в клинике Ыйджонбу-стрит.Mary’s Hospital в период с сентября 2005 г. по август 2006 г. Критериями исключения были предыдущая эрадикационная терапия или использование соединений бистма, ингибиторов протонной помпы, антибиотиков или антисекреторных препаратов в течение предыдущих 2 месяцев. Дополнительными критериями исключения были беременность или период лактации, тяжелое системное заболевание, явные нарушения свертывания крови или использование антикоагулянтов, а также переливание крови или прием препаратов железа в анамнезе.
2.2. Диагностика
H. pylori ИнфекцияВо время эндоскопии были взяты четыре биопсии (две из антрального отдела, две из тела).Окрашивание гематоксилином и эозином (HE) и окрашивание по Гимзе проводили с использованием серийных срезов четырех образцов. Срезы независимо оценивали два слепых патологоанатома. Тест 13 C-Urea Breath Test (UBT) проводился после ночного голодания или, по крайней мере, 8-часового голодания. Базовый образец дыхания помещали в пробирку для сбора. Аликвоту 75 мг 13 C-мочевины, растворенной в 75 мл раствора лимонной кислоты, вводили перорально (Helikit; Isodiagnostika, Эдмонтон, Канада).Другой образец дыхания был взят через 30 мин. Затем образцы дыхания анализировали для определения отношения 13 C / 12 C с помощью масс-спектрометрии (HeliView; MediChems, Сеул, Республика Корея). Отношение 13 C / 12 C каждого образца выдыхаемого воздуха выражалось в миллипроцентах (). Изменение значения 13 C по сравнению с исходным уровнем было выражено как дельта 13 C. Положительный результат был определен как увеличение> 4. Пациенты считались отрицательными для H.pylori , если результаты гистологического исследования и 13 C-UBT были отрицательными. Пациенты считались положительными на H. pylori , если какой-либо из тестов был положительным.
2.3. Диагностика атрофического гастрита
Атрофические изменения слизистой оболочки желудка при эндоскопии классифицировались по классификации Kimura-Takemoto [19]. Атрофические паттерны были разделены на восемь типов по расположению атрофической границы. Картина C-0 показывает эндоскопически нормальный желудок без атрофических изменений в какой-либо области.C-1, -2 и -3 обозначают атрофические паттерны закрытого типа. При типе С-1 атрофические изменения ограничиваются антральным отделом. Атрофические границы, лежащие на малой кривизне нижней части тела, определяют шаблон C-2, а границы на верхней части тела определяют шаблон C-3. Между тем, O-1, -2 и -3 обозначают атрофические паттерны открытого типа. В типе О-1 атрофическая граница располагается в пределах малой кривизны тела; в типе О-2 граница располагается в передней и задней стенках; а у типа О-3 граница расположена по большей кривизне.Гистологический диагноз атрофического гастрита был поставлен по обновленной Сиднейской системе с использованием биоптата, взятого из малой кривизны нижней части тела [20]. Воспаление слизистой оболочки желудка (инфильтрация мононуклеарных клеток), воспалительная активность (инфильтрация нейтрофилов), атрофия и кишечная метаплазия оценивались полуколичественно и оценивались как 0, 1, 2 или 3.
2.4. Лабораторный анализ
Образцы крови были взяты у всех участников, голодавших в течение ночи.Лабораторные тесты, включая общий анализ крови, общий белок, альбумин, тесты функции печени и почек, уровень железа в сыворотке, общую связывающую способность железа (TIBC) и ферритин, были выполнены с использованием стандартных лабораторных методов. Пациенты с гемоглобином (Hb) <14,0 г / дл (мужчины) или <12,0 г / дл (женщины) считались анемичными, а концентрация ферритина составляла <30 мк г / л (мужчины) или <13 . μ г / л (женщины) считались показателем дефицита железа.
Уровень прогепсидина в сыворотке измеряли с помощью иммуноферментного анализа (ELISA) DRG Diagnostics Hepcidin Prohormone (ELISA) (DRG Instruments GmbH, Марбург, Германия) в соответствии с инструкциями производителя.Используемое антитело обнаруживает как прорегион, так и прогепсидин (а.о. 25–84). Чувствительность анализа составляла 3,95 нг / мл, коэффициент вариации внутри анализа (CV) составлял 4,69%, а CV между анализами составлял 4,82%.
2,5. Статистический анализ
Значения выражены как среднее ± стандартное отклонение (SD). Непрерывные данные сравнивались с использованием теста независимых выборок t , тогда как категориальные данные анализировались с использованием точных критериев Фишера. Для корреляционного анализа использовалась непараметрическая корреляция Спирмена.Данные обрабатывались и анализировались с помощью SPSS, версия 12.0 (Чикаго, Иллинойс, США). Считалось, что значение указывает на статистическую значимость для всех тестов.
2.6. Заявление об этике
Этот протокол исследования был одобрен Советом по этике институциональных исследований Больницы Святой Марии в Уиджонбу Католического университета Кореи (IRB № UCMC06BR006) и соответствовал Хельсинкской декларации. Все участники исследования заполнили форму информированного согласия перед участием в исследовании.Информированное согласие было подтверждено правлением.
3. Результаты
Всего в исследование были включены 70 пациентов с желудочно-кишечными симптомами (29 мужчин, 31 женщина; средний возраст 41,7 года; диапазон 21–77 лет). Когда пациенты были разделены на H. pylori -положительные () и H. pylori -отрицательные () группы, не наблюдалось значительных различий в гематологических или биохимических параметрах между двумя группами. Однако была выявлена разница в атрофическом гастрите, которая была значительно более частой () у H.pylori -положительная группа, чем в H. pylori -отрицательная группа (71,4% против 28,6%, соответственно). Анемия была диагностирована у девяти (12,9%) пациентов, трое из которых были H. pylori -положительными и шесть – H. pylori -отрицательными. Среди пациентов с анемией только трое в группе H. pylori -отрицательных имели дефицит железа. Средний уровень прогепсидина в сыворотке составлял 241,4 нг / мл (SD, 58,6; диапазон 137-401) среди всех субъектов, 238,8 нг / мл (SD, 60,9; диапазон 144-401) в H.pylori -положительная группа и 244,1 нг / мл (стандартное отклонение 57,0; диапазон 137–359) в группе H. pylori -отрицательных. Уровень прогепсидина в сыворотке коррелировал с уровнями гемоглобина (,) и ферритина (,) в группе H. pylori -положительных. Не наблюдалось корреляции между уровнем прогепсидина в сыворотке крови и другими маркерами анемии, такими как гемоглобин, сывороточное железо, ферритин и TIBC, в группе H. pylori -отрицательных.
Двадцать пять испытуемых с отрицательным результатом на H. pylori показали эндоскопически нормальный желудок с атрофической границей C-0 и гистологически нормальной слизистой оболочкой фундального отдела, а у 10 испытуемых наблюдались легкие атрофические изменения (C-1).У десяти H. pylori -положительных субъектов не было выявлено атрофических изменений и гистологически нормальная слизистая оболочка фундального отдела, а у 25 субъектов были выявлены различные эндоскопические атрофические изменения (C-1,; C-2, и C-3,). Описательная статистика представлена в таблице 1. Пациенты с атрофическим гастритом были старше, чем пациенты без атрофического гастрита. Однако корреляции между возрастом и уровнем прогепсидина в сыворотке у всех испытуемых не было. Уровни прогепсидина в сыворотке были значительно ниже у пациентов с атрофическим гастритом, чем у пациентов без атрофического гастрита (по сравнению с нг / мл), независимо от H.pylori (рисунок 1). Однако у пациентов с атрофическим гастритом степень атрофии не коррелировала с уровнем прогепсидина в сыворотке (). Не наблюдалось корреляции между уровнем прогепсидина в сыворотке крови и другими маркерами анемии, такими как гемоглобин, сывороточное железо, ферритин и TIBC, у пациентов с атрофическим гастритом и без него (Таблица 2).
4. ОбсуждениеС момента своего открытия гепсидин привлек внимание исследователей из-за его способности регулировать метаболизм железа и оказывать противомикробное действие против многочисленных бактерий и грибов [1, 2, 4-7]. В настоящем исследовании оценивали сывороточный уровень прогепсидина, предшественника гепсидина, и его связь с метаболизмом железа и инфекцией H. pylori . Не было никакой связи между прогепсидином, параметрами дефицита железа и H.pylori инфекция. Гепсидин играет важную роль в механизме регуляции железа через ингибирование экспорта железа из энтероцитов, макрофагов и гепатоцитов [5]. Уровни гепсидина повышаются в ответ на нагрузку железом, уменьшая всасывание железа в кишечнике и подавляя высвобождение железа из запасов [21]. Между тем, дефицит железа вызывает низкий уровень гепсидина, что приводит к усилению всасывания железа и его мобилизации из запасов. Кроме того, гепсидин индуцируется воспалением, вызывая его секвестрацию в магазинах [7].Возникающее в результате снижение содержания железа способствует развитию анемии при хронических заболеваниях. Связь гепсидина с нарушениями метаболизма железа была установлена путем измерения концентрации гепсидина в моче с помощью иммунодот [7], электрофореза в полиакриламидном геле с додецилсульфатом натрия (SDS-PAGE), вестерн-блоттинга [4] и поверхностно-усиленного лазера. времяпролетная масс-спектрометрия десорбции / ионизации (SELDI-TOF-MS) [22]. В недавних исследованиях сообщалось о двух типах тестов на гепсидин для полуколичественного или количественного определения в сыворотке крови человека.Во-первых, масс-спектрометрические анализы определяют характерную массу активных 25-аминокислотных форм гепсидина или его фрагментов [23–25]. Однако эти анализы требуют доступа к специализированному оборудованию и не являются широко доступными. Во-вторых, был разработан ELISA, специфичный для повторно свернутой зрелой 25-аминокислотной формы [26]. Уровень гепсидина в сыворотке по данным ELISA обратно коррелировал с абсорбцией железа из дополнительных источников железа и негемовых источников железа на основе пищи у здоровых женщин с высоким содержанием железа [27]. Однако для подтверждения полезности этого метода требуется последующая оценка. В настоящем исследовании мы измерили сывороточные уровни прогепсидина; это одно из ограничений данного исследования. Прогепсидин гораздо более иммуногенен, чем гепсидин, и ИФА с прогепсидином коммерчески доступен. Наше исследование не показало никакой связи между концентрацией прогепсидина в сыворотке крови и параметрами дефицита железа. Эти результаты согласуются с результатами предыдущих исследований, в которых концентрация прогепсидина в сыворотке плохо коррелировала с маркерами гомеостаза железа, такими как абсорбция железа в кишечнике [27–29].Кроме того, не было обнаружено взаимосвязи между сывороточными концентрациями прогепсидина и гепсидина 25 [27]. Однако в другом исследовании сообщалось о значительной положительной корреляции между уровнями прогепсидина и гепсидина в сыворотке [30]. Сообщалось о связи между инфекцией H. pylori и ЖДА [8–12]. Наше исследование показало, что анемия не увеличивалась у субъектов с инфекцией H. pylori и не показала никакой связи с гепсидином. Это может быть связано с небольшим размером выборки, тем фактом, что когорта исследования была довольно однородной, и тем фактом, что у большинства субъектов были нормальные запасы железа.Тем не менее, наши данные не подтверждают предположение, что гепсидин играет ключевую роль в первичном механизме анемии, индуцированной H. pylori . Предыдущие исследования показали, что уровни гепсидина и прогепсидина в сыворотке с помощью ELISA не были изменены инфекцией или эрадикацией H. pylori , даже если гепсидин был обнаружен в желудочном соке человека [16, 31, 32]. Эти данные свидетельствуют о том, что гепсидин может выполнять местные, а не системные функции. Schwarz et al. недавно сообщили о новой роли гепсидина в желудке [16].В этом исследовании количественная ОТ-ПЦР продемонстрировала обильную экспрессию гепсидина в части дна / тела железистого желудка у мышей, крыс и людей. Гепсидин был локализован в париетальных клетках желудка с помощью иммунофлуоресцентного окрашивания и гибридизации in situ . Экспрессия желудочного гепсидина у пациентов и в клетках AGS была значительно повышена во время инфекции H. pylori . Кроме того, эрадикация H. pylori привела к нормализации уровней экспрессии гепсидина.Более того, мыши с нокаутом гепсидина демонстрировали пониженную экспрессию гена H + / K + -АТФазы, значительный бактериальный рост и пониженную экспрессию желудочного гена. Эти данные свидетельствуют о том, что гепсидин регулирует выработку кислоты в желудке и может способствовать развитию язвы желудка. В настоящем исследовании было обнаружено, что атрофический гастрит присутствует в 50% случаев. В Корее распространенность вируса H. pylori была высокой (59,6%) среди бессимптомных взрослых корейцев в 2005 г. [33].Кроме того, распространенность атрофического гастрита в антральном отделе и теле составляла 42,5% и 20,1%, соответственно, в корейской популяции без значительных гастродуоденальных заболеваний [34]. Мы обнаружили, что уровни прогепсидина в сыворотке крови снижались у субъектов с атрофией желудка, независимо от инфекции H. pylori . Это открытие можно объяснить потерей клеток, продуцирующих гепсидин, вызванной атрофией желудка. Однако мы не обнаружили, что уровни прогепсидина в сыворотке связаны со степенью атрофии.Кроме того, у пациентов с атрофическим гастритом не было обнаружено корреляции между сывороточным прогепсидином и параметрами анемии. Это можно объяснить небольшим количеством пациентов, включенных в исследование, и отсутствием оценки экспрессии гепсидина в тканях желудка. Недавнее исследование продемонстрировало, что экспрессия желудочного гепсидина снижалась у гипергастринемических ING-мышей с хронической желудочной инфекцией H. pylori и приводила к усилению экспрессии различных последующих генов абсорбции и оттока железа, таких как ферропортин 1, транспортер двухвалентных металлов 1 и Рецептор трансферрина 1 [35].Эти данные свидетельствуют о том, что снижение экспрессии гепсидина желудка из-за потери париетальных клеток, продуцирующих гепсидин, может функционировать как регулятор железа. Однако необходимы дальнейшие исследования функциональной роли гепсидина и транспортера железа в слизистой оболочке желудка, поскольку железо в основном всасывается в тонком кишечнике. Пепсиноген, аспарагиновая протеиназа, секретируемая в основном клетками желудка, иммунологически классифицируется как пепсиноген I (PG I) и пепсиноген II (PG II).В то время как PG I секретируется только слизистой оболочкой дна желудка, PG II секретируется сердечными, фундальными и антральными слизистыми оболочками желудка [36]. Атрофия желудка влияет на концентрацию PG в сыворотке крови: более низкие уровни PG I и стабильные или повышенные уровни PG II, что приводит к более низкому соотношению PG I / II [37]. Гастрин является еще одним действенным инструментом для выявления атрофии слизистой оболочки тела желудка, а повышенный уровень гастрина в сыворотке крови является обычным признаком атрофического гастрита тела из-за потери отрицательной обратной связи по кислотности желудочного сока [38].Необходимы дальнейшие исследования для оценки взаимосвязи между гепсидином и атрофией слизистой оболочки желудка с использованием соотношения I / II гастрина и / или пепсиногена. В заключение, наши данные показывают, что уровни прогепсидина в сыворотке не были изменены инфекцией H. pylori . Уровни прогепсидина в сыворотке крови снижались у пациентов с атрофическим гастритом, независимо от инфекции H. pylori . Это предполагает, что гепсидин может снижаться из-за атрофии желудка, состояния, которое вызывает потерю продуцирующих гепсидин париетальных клеток.Необходимы дальнейшие исследования с большим количеством пациентов с атрофическим гастритом, чтобы лучше изучить взаимосвязь между гепсидином и атрофическим гастритом. Конфликт интересовВсе авторы не заявляют о конфликте интересов. Вклад авторовХ.-К. Ким и Э.-К. Янг внес равный вклад в это исследование. БлагодарностьЭта работа была частично поддержана грантом Национального исследовательского фонда Кореи (NRF), финансируемым Министерством образования, науки и технологий (2010-0023295). Перспективы вмешательства в канцерогенез желудка: обратимость атрофии желудка и кишечной метаплазииБолее четверти века было широко признано, что большинство рака желудка возникает в результате многоступенчатого процесса, начинающегося с хронического гастрита и прогрессирующего через атрофию кишечная метаплазия (IM) и дисплазия до инвазивной карциномы.1 Атрофия тела приводит к гипохлоргидрии, которая способствует образованию канцерогенов, тогда как атрофический гастрит и метаплазия являются гиперпролиферативными состояниями, способствующими мутагенезу.Таким образом, атрофия и метаплазия обычно считаются предраковыми состояниями, хотя сила связи оспаривается. Совсем недавно было установлено, что инфекция Helicobacter pylori является основным фактором риска желудочного канцерогенеза, и, соответственно, инфекция непосредственно участвует в развитии атрофии и IM.2-4 Это ставит вопрос: « Может ли эрадикация H pylori обратить эти предраковые состояния и прервать последовательность атрофии-карциномы? » Чтобы ответить на этот вопрос, нужно сначала понять биологию и естественную историю этих состояний, а затем изучить возможности их обращения. Природа атрофииАтрофия желудка условно (и просто) определяется как «потеря желез». Такая потеря может последовать за изъязвлением с разрушением железистого слоя или, что более часто, быть результатом длительного воспалительного процесса, при котором несколько железистых единиц по отдельности подвергаются разрушению. Однако атрофию также можно рассматривать как «потерю специализированных клеток ». В это более широкое определение можно включить потерю париетальных и главных (зимогенных) клеток без разрушения желез.Такая частичная или «пре-атрофия» была описана при аутоиммунном гастрите человека5 и часто встречается на животных моделях как аутоиммунного гастрита6, так и хронической инфекции Helicobacter на животных. клетки (MNC). Что еще более интересно, частичная потеря париетальных клеток и замена их MNC – частая, но в значительной степени нераспознанная находка в воспаленном теле при гастрите H pylori .8 MNC первоначально считались промежуточным звеном популяции транзитных клеток между стволовыми клетками и полностью дифференцированными париетальными и главными клетками. Однако репертуар трилистниковых пептидов и факторов роста, продуцируемых MNC, указывает на то, что они представляют собой отдельный клеточный клон, который разделяет свойства других клонов защитных слизистых оболочек клеток желудочно-кишечного тракта.9 Более того, очевидно, что пролиферация MNC объясняет появление новые железы образовались в результате атрофии, так называемой «пилорической метаплазии». Существует два основных пути к атрофии: один, при котором компартмент стволовых клеток и / или железы разрушается либо прямым повреждением, либо в результате реакции воспалительных клеток хозяина, и второй, когда происходит избирательное разрушение специализированных эпителиальных клеток с сохранение стволовых клеток. Оба пути могут применяться при хронической инфекции H pylori ; с одной стороны, бактериальные токсины или, что более вероятно, протеазы, высвобождаемые активированными полиморфами, могут разрушать железистый эпителий и стволовые клетки10, а с другой стороны продуцируются аутоантитела, которые реагируют с эпитопами на протонном насосе париетальных клеток.11 Природа кишечной метаплазииМетаплазия представляет собой неопухолевое изменение клеточного фенотипа, которое обычно возникает в ответ на устойчивую неблагоприятную среду. Измененный фенотип является либо следствием соматической мутации в стволовых клетках, либо эпигенетических событий, которые вызывают дивергентную дифференцировку в дочерних клетках. Последующее появление измененного фенотипа в качестве доминирующей популяции является результатом давления отбора, оказываемого измененным микросредой.12 , 13 Характер экспрессии генов, определяющий фенотип клетки, находится под контролем сложной иерархии факторов транскрипции, важными членами которой являются гомеодоменных белков . Эти белки сами регулируются генами гомеобокса , экспрессия которых имеет решающее значение для клеточной дифференцировки и органогенеза.14 Таким образом, гомеобоксовые гены Cdx-1 и Cdx-2 обычно экспрессируются только в кишечнике, но соответствующий фактор транскрипции (белок CDX-1) присутствует в желудке внутримышечно.15 Однако, является ли такая экспрессия результатом мутации в стволовых клетках или эпигенетических изменений, не установлено. Безусловно, широкий спектр генетических изменений, включая сокращение теломер, микросателлитную нестабильность и мутации в p53, APC и k- ras , был описан в IM, даже до появления дисплазии. IM можно разделить на три подтипа, которые, вероятно, будут различаться по своему гистогенезу и соотношению с канцерогенезом, а именно, тип I (полный), который очень похож на тонкий кишечник, тип II (неполный – метаплазия бокаловидных клеток) и тип III (неполный – «толстокишечный» тип).Интересно, что именно последний тип несет в себе большинство генетических изменений17. , 18 и единственный фенотип IM, который несет более высокий риск рака желудка.19 Возможна ли обратимость?При любом рассмотрении обратимости атрофии необходимо проводить различие между заменой утраченных желез и регенерацией специализированных клеток в интактных железах. В последнем случае компартмент стволовых клеток сохраняется, и удаление повреждающего фактора может привести к регенерации париетальных и главных клеток и полному восстановлению функции.Это было ясно продемонстрировано на животной модели, где отмена препарата, вызывающего избирательную потерю париетальных клеток, сопровождалась полным восстановлением оксинтной слизистой оболочки.20 Если железы и связанные с ними стволовые клетки были полностью разрушены, замены должны были возникнуть из соседние неповрежденные ямочные сальники. В развивающемся желудке млекопитающих умножение оксинтных желез происходит посредством процесса почкования, удвоения, деления и разделения 21. Происходит ли подобный процесс у взрослых, остается спорным.Кажется очевидным, что большая часть регенерации после потери железы происходит по линии MNC, но есть доказательства, хотя и от небольшого числа субъектов, чтобы указать, что полное восстановление оксинтических желез может следовать за атрофией. далее ограничено. При IM единицы ямочной железы заменяются неокриптами, в которых компартмент стволовых клеток расположен, как и в нормальном кишечнике, в основании крипты. Хотя почкование кишечных крипт вполне возможно, оно очень маловероятно, чтобы дать начало нормально расположенным оксинтическим железам, а просто привело бы к расширению метапластических очагов. IM с большей вероятностью будет обратимым, если оно будет развиваться как адаптация к неблагоприятному фактору, который может быть идентифицирован и устранен. Например, цитокины из хронических воспалительных клеток и, в частности, лимфоцитов-помощников Th3 могут быть ответственны за «адаптивный» IM при инфекции H pylori .23 Конечно, кишечные клетки не могут быть колонизированы организмом и, следовательно, будут иметь преимущество в выживании. Однако IM может иметь другие причины (например, рефлюкс желчи, диета с высоким содержанием соли и алкоголь), некоторые из которых могут действовать синергетически.Это означает, что даже у инфицированных H. pylori субъектов другие факторы, помимо инфекции, могут провоцировать или ускорять метапластические изменения. Если IM является следствием стабильных соматических мутаций в стволовых клетках, изменения в непосредственной слизистой оболочке могут не привести к обратимости. Хотя соматическая мутация может быть фактором всех типов IM, интересно, что генетические поражения, обнаруживаемые при IM типа III, аналогичны тем, которые обнаруживаются при дисплазии желудка (интраэпителиальная неоплазия) 16-18. , 24 Эти данные ставят под сомнение потенциальную обратимость этого конкретного подтипа IM.Даже когда IM является следствием эпигенетических изменений, например, возникающих в результате метилирования генов, участвующих в дифференцировке клеток, 25 возможности для реверсии могут быть строго ограничены. Происходит ли обращение атрофии и IM?Есть несколько препятствий для правильной оценки обратимости, которые включают ошибки в гистологической интерпретации, ошибки выборки и «спонтанную регрессию». Когда имеется глубокая инфильтрация железистого слоя хроническими воспалительными клетками, отделение желез может произвести ложное впечатление атрофии.Разрешение воспаления после эрадикации H pylori приведет в течение нескольких месяцев к возвращению нормальной плотности железы. Это не обращение атрофии, а неправильная гистологическая интерпретация. Точно так же предположение о том, что несколько небольших образцов слизистой являются репрезентативными для всего целого, весьма сомнительно при работе с мультифокальными процессами. Таким образом, при сравнении атрофии и IM между исходной и последующей эндоскопией возникают трудности. Наконец, даже в отсутствие лечения все последующие исследования хронического гастрита показывают очевидный регресс у меньшинства субъектов.В большом когортном исследовании, проведенном в Колумбии, 26 показатели «регресса» при переходе от атрофии к норме (или поверхностного гастрита) и от IM к атрофии составили 7,5 и 4,4 на 100 человеко-лет соответственно. Несмотря на то, что в целом было получено прогрессии , важность ошибок выборки для получения этих результатов была подчеркнута. Учитывая, что ошибки выборки всегда затрудняют гистологическую интерпретацию, можно подумать, что косвенные измерения атрофии дадут более точную оценку, но этот подход также ошибочен.В настоящее время четко установлено, что гипохлоргидрия и изменения в соотношении пепсиногена I и II в сыворотке могут быть результатом только воспаления тела.27 Таким образом, у некоторых пациентов с выраженной гипохлоргидрией наблюдается значительное увеличение выхода кислоты после эрадикации H pylori , что связано с разрешением воспаления и не к регенерации кислородных желез 28. Ошибки выборки еще более проблематичны при оценке IM. Однако прицельная биопсия на краях пептических язв и последующий «рубец» ясно демонстрируют, что ИМ (обычно I и II типов) часто развивается в регенерирующем эпителии и со временем регрессирует.29 Каковы перспективы вмешательства?С осознанием того, что H pylori играет центральную роль в канцерогенезе желудка, идея вмешательства путем искоренения инфекции становится все более привлекательной. Устранение воспаления будет иметь свои собственные положительные последствия, но можно ли ожидать регресса атрофии и ИМ? Опубликованные исследования, изучающие обратимость атрофии и IM после эрадикации H. pylori , дали противоречивые результаты.В целом, чем дольше период наблюдения, тем больше вероятность того, что исследование покажет регресс атрофии, но степень изменения невелика. Согласно консенсусу недавних исследований статуса IM, заметных изменений нет. Более существенное преимущество заявлено в первом рандомизированном интервенционном исследовании, посвященном эффективности эрадикации H pylori и пищевых добавок с витамином C или β-каротином.30 Оно было проведено в регионе с высокой заболеваемостью раком желудка (в Колумбии) на 852 человеке. инфицированные субъекты, у которых при поступлении был атрофический гастрит и / или внутримышечная инъекция, которым была сделана биопсия через 36 и 72 месяца после интервенционного лечения.Авторы пришли к выводу, что устранение H pylori вызывает «заметное и статистически значимое увеличение скорости регресса предшествующих поражений». Но аналогичные относительные риски были получены только для других методов лечения, и, как указал Блот, 31 вызывает беспокойство то, что лечение анти- H pylori было эффективным, когда его применяли отдельно, но не давало (дополнительных) преимуществ, когда давалось с витамином С или β. -каротин. Хотя результаты многообещающие, Блот пришел к выводу, что ввиду отсутствия согласованности результаты следует интерпретировать с осторожностью.Возможно, потребуется дополнительная осторожность, когда станет понятно, что изменение от IM на исходном уровне до мультифокального атрофического гастрита при последующем наблюдении квалифицируется как «регресс» в соответствии с их гистологическим протоколом. Хотя истинный регресс атрофии и ИМ зависит от способности слизистой оболочки регенерировать специализированную железистую ткань, по крайней мере, можно ожидать, что правильное определение и устранение причины предотвратит прогрессирование. Однако очевидно, что атрофия и ИМ имеют ряд причин – рефлюкс желчи, пищевые раздражители и аутоиммунитет, а также инфекция H pylori .Таким образом, удаления инфекции может быть недостаточно для того, чтобы вылечить ее. Кажется наиболее вероятным, что регенерация нормальных кислородных желез после истинной железистой атрофии с замещающим фиброзом будет по крайней мере ограничена. Точно так же восстановление нормальной дифференцировки в IM маловероятно при наличии стабильных мутаций в стволовых клетках. Фактически, определенные формы атрофии и ИМ прошли «точку невозврата», и их изменение становится невозможным. На мой взгляд, надежда на то, что вмешательство путем элиминации H. pylori само по себе приведет к значительному обращению атрофии и IM, является нереалистичным.Однако уже установлен более реалистичный результат. H pylori эрадикация приводит к разрешению воспаления, устранению повреждений ДНК реактивными формами кислорода, снижению клеточного обмена, увеличению выхода кислоты у субъектов с пониженным содержанием хлорида натрия и постепенному возврату секреции аскорбиновой кислоты в желудочный сок. Эти доказанные последствия могут быть гораздо более важными для предотвращения рака желудка, чем ожидаемые последствия атрофии и IM. Сокращения, использованные в этой статье
Почему я всегда так устал? Виноват аутоиммунный гастритАвтор: Dr.Мэтт Льюис , округ Колумбия, DACBN, CFMP® Постоянная усталость – загадка, которую сложно разгадать. Причины включают анемию, беспокойство, депрессию, инфекцию, рак, синдром хронической усталости (СХУ), плохое питание, слишком мало или слишком много упражнений, плохой сон, заболевания печени или почек и этот список можно продолжить. Одним из наиболее недооцененных состояний, которые могут вызвать усталость, является аутоиммунный гастрит – хроническое воспалительное заболевание, при котором иммунная система по ошибке разрушает париетальных клеток – клеток, вырабатывающих желудочную кислоту и внутренний фактор (IF), который необходим организму для уметь усваивать витамин B12. В результате люди с аутоиммунным гастритом часто страдают злокачественной анемией – состоянием, при котором организм не может усваивать витамин B12, необходимый для производства здоровых эритроцитов. Неудивительно, что без достаточного количества здоровых эритроцитов для переноса кислорода по всему телу люди с пагубной анемией страдают от стойкой усталости.
К сожалению, обычные врачи часто не обращают внимания на аутоиммунный гастрит у пациентов, сообщающих о хронической усталости. Они могут проверить анемию и лечить ее добавками железа или тестом на дефицит B12, убедиться, что ваш уровень B12 в порядке, и никогда не задумываться о том, действительно ли ваше тело способно усваивать и использовать этот B12.Хуже того, некоторым людям, которые сообщают об усталости, просто ставят диагноз тревожности или депрессии и прописывают седативные средства или антидепрессанты. Они могут испытать временное облегчение, но основное состояние остается невыявленным и не леченным. Признание важности париетальных клеток Париетальные клетки секретируют два важных вещества:
Хотя желудочную кислоту часто называют причиной расстройства желудка и кислотного рефлюкса, она необходима для правильного пищеварения.Он помогает расщеплять белок и стимулирует желчный пузырь вырабатывать желчь, обеспечивая адекватное переваривание жиров. Желудочная кислота также помогает убить любые инфекционные агенты, попадающие в желудок с пищей или водой; многие патогены не могут выжить в очень кислой среде. Когда париетальные клетки находятся в осаде иммунной системы, ваша способность вырабатывать желудочную кислоту снижается и становится недостаточной. Белок не переваривается должным образом, что увеличивает нагрузку на желчный пузырь и нижние части пищеварительного тракта.Кроме того, недостаток кислоты в желудке делает организм более восприимчивым к заражению от испорченной пищи или напитков.
Другое вещество, теряемое в результате аутоиммунного гастрита, – это внутренний фактор – гликопротеин, который связывает B12, позволяя ему всасываться в кишечнике и в кровоток.Без достаточного внутреннего фактора B12 теряется через кишечник и должен быть восполнен внутримышечно или с помощью липосомального препарата. Неспособность усваивать и использовать B12 приводит ко многим симптомам, описанным в этом посте. Подробнее о пагубной анемии «Пагубный» означает постепенное или незаметное вредное воздействие. Самый распространенный тип анемии не является пагубным; это происходит из-за дефицита железа, и его легко обнаружить при обычных анализах крови – уровень железа и количество эритроцитов низкие.При пернициозной анемии количество эритроцитов ниже, но клетки больше ( мегалобластов, ). На ранних стадиях циркулирующий уровень B12 может казаться нормальным, а дефицит B12 и возникающая в результате анемия легко не заметить с помощью обычных лабораторных тестов. Без надлежащего лечения ткань желудка продолжает ослабевать и атрофироваться, что приводит к ослаблению слизистой оболочки желудка (слизистой оболочки желудка). Со временем у людей с нелеченной злокачественной анемией часто начинают проявляться признаки гастрита (воспаление слизистой оболочки желудка, которое приводит к кислотному рефлюксу) или холестаза (проблемы с желчным пузырем). Аутоиммунный гастрит – не единственная причина злокачественной анемии. К другим причинам относятся следующие:
Дефицит витамина B12 скрыт и недостаточно диагностируется, часто потому, что его начало и прогрессирование происходит медленно, а люди привыкают к их симптомам. Тем не менее, клинические последствия недиагностированного дефицита витамина B12 могут быть серьезными, включая широкий спектр неврологических расстройств и расстройств настроения. Последствия для переработки и сбыта продукции Проблемы со здоровьем, вызванные неспособностью усваивать витамин B12, выходят далеко за пределы желудка и желчного пузыря и могут быть гораздо более серьезными, чем гастрит и холестаз. Эти условия я называю «последующими последствиями». Вот несколько примеров:
Распознавание симптомов аутоиммунного гастрита и пагубной анемии Симптомы аутоиммунного гастрита и вызванной им злокачественной анемии разнообразны и часто незаметны:
Тестирование на аутоиммунный гастрит и злокачественную анемию Когда лечащие врачи подозревают дефицит витамина B12, они делают логический шаг и проверяют уровень B12 в кровотоке.Однако исследования показывают, что этот подход не обеспечивает адекватной оценки статуса B12. Тот факт, что B12 присутствует в кровотоке, не означает, что организм его усваивает и использует должным образом. Следовательно, у вас может быть нормальный уровень B12 и все еще есть проблемы, связанные с дефицитом B12. Требуется более тщательное тестирование, например:
Если все это звучит технически, то это так. Простой прием качественной добавки B12 или добавки комплекса B, включающей фолиевую кислоту, не обязательно решает проблему.Обследование и лечение следует доверить врачу, который регулярно ищет эти проблемы и знает, как их исправить. Уход должен быть индивидуальным, и людей, которые остаются уставшими, следует дополнительно обследовать, даже если традиционная система здравоохранения записала это на свой счет: «С вами все в порядке, ваши лаборатории выглядят нормально». Тестирование может включать эндоскопию ( – нехирургическая процедура, используемая для исследования вашего пищеварительного тракта с помощью камеры ), дальнейшие анализы крови и генетическое тестирование, чтобы назвать несколько возможностей.При поиске проблем с B12 необходимо учитывать и другие витамины. Это потому, что B12 не активируется изолированно – ему нужны другие коферменты и минералы, чтобы обеспечить абсорбцию и ассимиляцию. Такой тщательный врач, как я, изучает множество факторов, влияющих на B12, и не перестает разгадывать тайну, пока ваша энергия не восстановится! Если вы чувствуете переутомление или испытываете какие-либо симптомы, описанные в этом посте, я настоятельно рекомендую вам обратиться к врачу, у которого есть знания, подготовка и опыт диагностики и лечения заболеваний на клеточном уровне, например, к врачу с обучение функциональной медицине.Ваша усталость и другие симптомы могут быть связаны или не быть связаны с аутоиммунным гастритом, поэтому вам нужен врач, который знает обо всех возможных состояниях, которые могут вызывать ваши симптомы. Не принимайте никого, кто говорит вам, что «с вами все в порядке» или что вы просто в стрессе или депрессии. Любой врач, с которым вы проконсультируетесь, должен глубоко копнуть, чтобы выявить и устранить основные причины того, что вас беспокоит, и этот врач не должен останавливаться, пока ваше здоровье и физическая форма не будут полностью восстановлены. ——— Заявление об отказе от ответственности: Информация в этом сообщении в блоге предназначена только для общих информационных целей и может не отражать текущее медицинское мышление или практику.Никакая информация, содержащаяся в этом сообщении, не должна толковаться как медицинский совет доктора Мэтта Льюиса, округ Колумбия, DACBN, CFMP ® , а также этот пост не предназначен для замены медицинского совета по любому вопросу. Ни один читатель этого поста не должен действовать или воздерживаться от действий на основании любой информации, содержащейся в этом посте или доступной через нее, без обращения за соответствующей медицинской консультацией по конкретным фактам и обстоятельствам, о которых идет речь, у лицензированного медицинского специалиста в государстве-получателе. страна или другая соответствующая лицензионная юрисдикция.——— Об авторе: Доктор Мэтт Льюис, округ Колумбия, DACBN, CFMP ® , специализируется на диагностике и лечении основных причин симптомов, связанных с хроническими и необъяснимыми заболеваниями, с помощью питания, образа жизни, хиропрактики и других естественных подходов. к общему исцелению в Тампе, Флорида. Он получил степень бакалавра наук. Имеет степень доктора биологии Университета Шенандоа, докторскую степень по хиропрактике в Университете Лайф, статус дипломированного специалиста по клиническому питанию Американского клинического совета по питанию, сертификат CFMP ® Университета функциональной медицины и сертификат специалиста по здоровью пищеварительной системы (DHS). Институт пищевых ферментов.Страсть доктора Льюиса к здоровью и благополучию проистекает из его личного опыта. Имея семейный анамнез аутоиммунных состояний и диабета, а также его собственные лабораторные тесты, показывающие его генетическую предрасположенность к тиреоидиту Хашимото (аутоиммунный тиреоид), он научился восстанавливать собственное здоровье и бодрость, чтобы предотвратить начало этих и других болезней и жить достойно. невероятно активная жизнь. Благодаря этому процессу он приобрел более глубокое понимание здоровья и благополучия, которое он теперь предлагает своим пациентам в Тампе. Теги: Антациды, Аутоиммунный гастрит, Блокаторы B12, h3, Париетальные клетки, Ингибиторы протонной помпы, Кислота желудка, Дефицит витамина B12Гипохлоргидрия: симптомы, причины и советыЭто сообщение в блоге посвящено кислоте желудка, а точнее, когда нам ее не хватает, состоянию, называемому гипохлоргидрия (гипохлоргидрия = низкий, хлоргидрия = гидрохлорид или желудочная кислота) . Этот блог отвечает на вопрос: «Что такое гипохлоргидрия?» а также расскажет, как его идентифицировать и управлять. Желудочная кислота 101Желудочная кислота, также называемая соляной кислотой (HCl), выделяется из клеток желудка, чтобы помочь расщепить нашу пищу. Кислота должна оставаться в желудке и не попадать вверх в пищевод и / или горло. Мышца, называемая сфинктером пищевода, действует как дверь, которая обычно защищает содержимое желудка от выхода. Желудочная кислота отвечает за поддержание в желудке низкого уровня pH (он же кислый), который необходим для правильного переваривания белков, поглощения определенных питательных веществ и защиты от вредных насекомых. Иногда желудок не может производить достаточное количество желудочной кислоты, и это нарушает начальные этапы пищеварения. Каковы признаки гипохлоргидрии?Признаки гипохлоргидрии могут звучать так же, как при диагностировании ГЭРБ или изжоги. Это потому, что низкий уровень кислоты в желудке может повысить давление в желудке. Это может привести к тому, что желудочная кислота, присутствующая в и , будет подниматься в пищевод, вызывая изжогу.Ой. Кроме того, это некоторые ключевые признаки низкого уровня кислоты в желудке:
Низкий уровень кислоты в желудке может быть вызван множеством факторов, включая:
Существуют определенные тесты для проверки на гипохлоргидрию, включая:
Хронически низкий уровень кислоты в желудке является проблемой по нескольким причинам. Желудочная кислота защищает от бактериальных инфекций и необходима для правильного пищеварения. Без достаточного количества этого могут возникнуть проблемы, такие как:
Ахлоргидрия (отсутствие желудочного сока) со временем может возникнуть в результате нелеченного атрофического гастрита.В конечном итоге это может привести к дефициту B12 (злокачественной анемии) и повышению риска рака желудка. Рак желудка очень агрессивен и имеет низкую выживаемость. Пять советов по уменьшению гипохлоргидрииГипохлоргидрия не обязательно является постоянным заболеванием. Выявление и лечение первопричины, а затем внесение изменений в свой образ жизни и использование некоторых добавок могут помочь улучшить ее. Вот мои 5 лучших советов по борьбе с гипохлоргидрией:
Симптомы гипохлоргидрии аналогичны симптомам ГЭРБ и включают вздутие живота, расстройство желудка, кислотный рефлюкс и изжогу. Поговорите со своим врачом о вариантах тестирования на пониженную кислотность желудка перед лечением. Важно выяснить, почему у вас может быть гипохлоргидрия, чтобы разработать правильный протокол лечения. Небольшие изменения в образе жизни для снижения уровня стресса и некоторые ключевые добавки могут изменить это состояние. Свяжитесь с Эрин сегодня и разработайте индивидуальный план лечения гипохлоргидрии. ГОСТЕВАЯ СТАТЬЯ, ПРЕДСТАВЛЕННАЯ: ELIZABETH HERBERT, MS CANDIDATE AT THE MARYLAND UNIVERSITY INTEGRATIVE HEALTHИсточники: Lipski, E.(2011). Здоровье пищеварительной системы: укрепление иммунной системы и профилактика заболеваний посредством здорового пищеварения . McGraw Hill Professional. Кинес, К., и Крупчак, Т. (2016). Пищевые вмешательства при гастроэзофагеальном рефлюксе, синдроме раздраженного кишечника и гипохлоргидрии: отчет о болезни. Интегративная медицина: журнал клинициста , 15 (4), 49. http://articles.mercola.com/sites/articles/archive/2009/04/25/news-flash-acid-reflux- вызвано-слишком-мало-кислоты-не слишком-много.aspx Смолка, А. Дж., и Шуберт, М. Л. (2017). Индуцированные Helicobacter pylori изменения секреции желудочной кислоты и заболевания верхних отделов желудочно-кишечного тракта. In Molecular Pathogenesis and Signal Transduction by Helicobacter pylori (стр. 227-252). Издательство Springer International. Урбас, Р., Хантингтон, В., Наполеон, Л. А., Вонг, П., и Маллин, Дж. М. (2016). Проблемы, связанные с мальабсорбцией, связанные с хроническим использованием ингибиторов протонной помпы. Остин Дж. Нутр Метаб , 3 (2), 1041. Джонсон, Д. А. (2016). Пищевые последствия длительного подавления кислотности; они клинически важны ?. Текущее мнение в гастроэнтерологии , 32 (2), 136-140. Салем А. и Рональд Б. С. (2014). Избыточный бактериальный рост в тонком кишечнике (СИБР). J Gastroint Dig Syst , 4 (225), 2. Park, J. Y., Lam-Himlin, D., & Vemulapalli, R. (2013). Обзор аутоиммунного метапластического атрофического гастрита. Эндоскопия желудочно-кишечного тракта , 77 (2), 284-292. Как лечить необъяснимую рефрактерную железодефицитную анемию | КровьДефицит железа – одна из наиболее распространенных проблем с питанием человечества. Это связано с серьезными рисками для здоровья, включая аномалии умственного и моторного развития в младенчестве, снижение трудоспособности, повышенный риск преждевременных родов, а при тяжелой анемии – повышение материнской и младенческой смертности. 1 Развитие дефицита железа является следствием взаимодействия трех различных факторов риска: повышенных потребностей хозяина, ограниченного предложения и повышенной кровопотери. Принципы диагностики и лечения железодефицитной анемии (ЖДА) хорошо известны и определены в ряде подробных руководств и рекомендаций. 2-5 Поскольку повышенные потребности являются результатом повышенных физиологических потребностей, связанных с нормальным развитием, эту категорию дефицита железа часто называют физиологической или пищевой.Напротив, патологический дефицит железа чаще всего является результатом желудочно-кишечных заболеваний, связанных с аномальной кровопотерей или мальабсорбцией. Интенсивность диагностических усилий по выявлению основной патологии зависит от вероятности столкновения с такой патологией (Рисунок 1). У субъектов с повышенными потребностями и у пациентов с низким риском, таких как большинство фертильных женщин, подробные анатомические исследования необходимы редко. Напротив, у взрослых мужчин и женщин в постменопаузе риск основного желудочно-кишечного заболевания высок, и требуется интенсивное обследование желудочно-кишечного тракта.После завершения диагностической процедуры следует лечить дефицит железа, предпочтительно пероральными препаратами. Рисунок 1 Диагностическое обследование, предшествующее распознаванию необъяснимой рефрактерной ЖДА. Диагностическое обследование, предшествующее выявлению субъектов с необъяснимой рефрактерной ЖДА: у мужчин и женщин в постменопаузе подробные желудочно-кишечные исследования являются обязательными. Напротив, у пациентов с повышенными физиологическими потребностями и у большинства пациентов с низким риском, таких как женщины детородного возраста, эндоскопические желудочно-кишечные исследования перед пероральным лечением железом редко необходимы.Ограничения этого диагностического подхода заключаются в том, что (1) полное обследование желудочно-кишечного тракта не позволяет определить причину ЖДА у значительной части субъектов и (2) такие пациенты и пациенты, у которых ЖДА предположительно является физиологическим, могут быть невосприимчивыми к пероральному лечению. железная терапия. CHr – содержание Hb в ретикулоцитах; sTfR, растворимый рецептор трансферрина; Tf, трансферрин; ЗПП, протопорфирин цинка. Рисунок 1 Диагностическое обследование, предшествующее распознаванию необъяснимой рефрактерной ЖДА. Диагностическое обследование, предшествующее выявлению субъектов с необъяснимой рефрактерной ЖДА: у мужчин и женщин в постменопаузе подробные желудочно-кишечные исследования являются обязательными. Напротив, у пациентов с повышенными физиологическими потребностями и у большинства пациентов с низким риском, таких как женщины детородного возраста, эндоскопические желудочно-кишечные исследования перед пероральным лечением железом редко необходимы. Ограничения этого диагностического подхода заключаются в том, что (1) полное обследование желудочно-кишечного тракта не позволяет определить причину ЖДА у значительной части субъектов и (2) такие пациенты и пациенты, у которых ЖДА предположительно является физиологическим, могут быть невосприимчивыми к пероральному лечению. железная терапия.CHr – содержание Hb в ретикулоцитах; sTfR, растворимый рецептор трансферрина; Tf, трансферрин; ЗПП, протопорфирин цинка. Однако этот общий дизайн может потерпеть неудачу в нескольких отношениях: во-первых, обычные эндоскопические и рентгенографические методы не могут определить источник желудочно-кишечной кровопотери у значительной части пациентов даже после использования капсульной эндоскопии. 6-9 Во-вторых, отсутствие реакции на пероральное введение железа происходит у значительной части пациентов независимо от категории риска.Распространенность рефрактерности к железу трудно определить, потому что на нее также влияет комплаентность пациента, а также опыт и склонность врача использовать парентеральное железо. В настоящей статье рефрактерность к пероральному железу определяется как отсутствие ответа на лечение в дозе не менее 100 мг элементарного железа в день после 4-6 недель терапии. Субъекты, у которых ЖДА не реагирует на стандартное пероральное лечение железом или у которых анемия сохраняется, несмотря на отрицательные результаты обследования желудочно-кишечного тракта, представляют собой важную подгруппу пациентов, направленных на гематологическое обследование. Исследования в конце 90-х установили целиакию как возможную причину ЖДА, резистентного к пероральному лечению железом, без других явных проявлений синдрома мальабсорбции. 10 Кроме того, Helicobacter pylori участвовал в нескольких более ранних исследованиях как причину ЖДА, резистентного к пероральному лечению железом, с благоприятным ответом на эрадикацию H. pylori . 11,12 Аналогичным образом, аутоиммунный атрофический гастрит, состояние, связанное с хроническим идиопатическим дефицитом железа, оказалось ответственным за рефрактерную ЖДА у более чем 20% пациентов без признаков желудочно-кишечной кровопотери. 13,14 Доступность удобных неинвазивных методов скрининга для выявления целиакии (антитела к тканевой трансглутаминазе [TTG]), аутоиммунного атрофического гастрита (сывороточный гастрин, париетальные клетки или антитела к внутреннему фактору) и инфекции H pylori (скрининг на антитела или фекальный антиген и дыхательный тест на уреазу), а недавнее признание редких наследственных форм дефицита железа значительно облегчило диагностику этих состояний, что привело к повышению осведомленности об этих состояниях и их возможной роли в возникновении ЖДА.Цель настоящего сообщения состоит в том, чтобы сосредоточить внимание на роли вышеупомянутых субъектов в патогенезе рефрактерной ЖДА, но оно не предназначено для представления подробной общей стратегии диагностики и лечения дефицита железа. Результаты проспективного исследования 300 последовательных пациентов с ЖДА, направленных в гематологическую амбулаторию с неясной или рефрактерной ЖДА 15 , показаны в Таблице 1.Рефрактерность к пероральному лечению железом определялась как прирост гемоглобина (Hb) <1 г / дл после 4–6 недель терапии при суточной дозе не менее 100 мг элементарного железа. Средний возраст всех испытуемых составил 39 ± 18 лет, из них 84% составляли женщины репродуктивного возраста. Поскольку исследуемая популяция была ограничена возрастом 14 лет и старше, описанные результаты могут не относиться к детской возрастной группе. Глютеновая болезнь взрослых выявляется в 5%. Аутоиммунный атрофический гастрит был обнаружен у 26%, и около половины из них (51%) имели сопутствующую инфекцию H. pylori .Инфекция H pylori была единственной находкой у 19%, но она также была частой находкой, сосуществующей у 55% всей группы. В таблице 1 не указаны 4 пациента, перенесших гастропластику. Использование аспирина или нестероидных противовоспалительных препаратов (НПВП) указано в качестве дополнительной информации, но не учитывается отдельно в общем числе пациентов. Рефрактерность к пероральному лечению железом была обнаружена у 100% пациентов с глютеновой болезнью, 69% с аутоиммунным атрофическим гастритом, 68% с инфекцией H. pylori и только у 10% пациентов без каких-либо патологий.В следующих разделах мы хотим обсудить последствия вышеуказанных открытий для патогенеза и лечения необъяснимой или рефрактерной ЖДА. Таблица 1Основные диагностические категории и сопутствующие результаты у 300 последовательных пациентов с ЖДА
Основные диагностические категории и сопутствующие данные у 300 последовательных пациентов с ЖДА, направленных на гематологическое обследование (Hershko et al., 15 ) . *Всего сто шестьдесят пять H pylori . Роль H pylori в возникновении ЖДА представляет значительный интерес в настоящее время. Основные опросы населения, проведенные в различных географических регионах 16-23 показывают, что положительный результат H. pylori связан с повышенной распространенностью дефицита железа, а метаанализ 19 наблюдательных эпидемиологических исследований и 6 интервенционных испытаний выявил повышенный риск ЖДА с объединенное отношение шансов (OR) 2.8 среди человек, инфицированных H. pylori . 24 Метаанализ 16 рандомизированных исследований с участием 956 пациентов с подтвержденной инфекцией H. pylori и ЖДА показал, что прирост от исходного уровня до конечной точки Hb, сывороточного железа и сывороточного ферритина был значительно выше при лечении анти- H. pylori плюс пероральное железо по сравнению с пероральным пероральным препаратом. 25 Положительный эффект эрадикации H pylori был более очевидным, а результаты более стабильными у пациентов с умеренной и тяжелой анемией, то есть с уровнями гемоглобина до лечения <9 г / дл.Подобные результаты были представлены в другом метаанализе рандомизированных контролируемых испытаний с участием 450 человек. 26 Лекарство от анемии с помощью эрадикации H. pylori является самым убедительным доказательством причинно-следственной связи. В группе из 25 пациентов мужского пола с активной инфекцией H pylori с (n = 10) или без (n = 15) сопутствующим аутоиммунным гастритом, 27 после эрадикации H. pylori все ранее резистентные пациенты достигли нормальных уровней Hb с последующим периоды повышения квалификации от 4 до 69 месяцев (38 ± 15 месяцев, среднее ± 1 стандартное отклонение).Это сопровождалось значительным снижением антител к иммуноглобулину G (IgG) H pylori и уровня гастрина в сыворотке крови. Шестнадцать пациентов прекратили лечение железом, поддерживая нормальный уровень гемоглобина и ферритина, и могут считаться вылеченными, то есть с показателем излечения 64%. Примечательно, что 4 из 16 достигли нормального уровня гемоглобина без приема перорального железа после эрадикации H. pylori . Аналогичные результаты были получены в недавнем исследовании 84 взрослых пациентов, у которых изучалось влияние эрадикации H pylori на железорезистентную или железозависимую анемию неизвестного происхождения. 28 Показатели излечения у мужчин и женщин в постменопаузе (75%) были намного выше, чем у женщин в пременопаузе (23%, P <0,0001), что подчеркивает усиливающийся эффект увеличения менструальной кровопотери. Ввиду накопленных данных, подтверждающих значительную роль инфекции H pylori в патогенезе ЖДА, в опубликованных руководящих принципах по ведению инфекции H. pylori для лечения необъяснимой ЖДА рекомендуется эрадикация H. pylori большое количество национальных и международных экспертных комитетов. 2,29-35 Что касается патогенеза ЖДА, ассоциированного с H pylori , был предложен ряд возможных механизмов для объяснения связи между гастритом H pylori и ЖДА, включая скрытое желудочно-кишечное кровотечение и конкуренцию бактерий за пищевое железо. Кроме того, всасывание железа у субъектов, инфицированных H. pylori , нарушено из-за влияния H pylori на состав желудочного сока.Исследования с участием H pylori –позитивных субъектов показали коррекцию нарушения всасывания перорального железа после эрадикации H. pylori . 36 Аналогичным образом, исследования Annibale et al и других 37 показали, что на кислотность желудочного сока и содержание аскорбата, которые имеют решающее значение для нормального всасывания железа, отрицательно влияет инфекция H pylori и эрадикация H. pylori приводит к нормализации внутрижелудочного рН и содержания аскорбата. Причина, по которой некоторые пациенты устойчивы к долговременной колонизации H. pylori и почему повреждение слизистой оболочки желудка сильно варьируется, в настоящее время неизвестна. Недавние наблюдения, указывающие на то, что генетическая изменчивость факторов хозяина, а также состав белков внешней мембраны, репрессируемых железом H pylori , могут определять клиническое проявление заболевания, могут представлять собой важную новую информацию о механизме и тяжести H pylori . инфекционное заболевание. 38,39 Achylia gastrica как причина ЖДА была впервые описана Фабером как клиническое явление в 1909 г. 40 ; ахлоргидная атрофия желудка, синоним того же самого явления, долгое время считалась основной причиной ЖДА 41 , но полностью игнорировалась в последующих крупных исследованиях желудочно-кишечных причин ЖДА. Совсем недавно ахлоргидная атрофия желудка была вновь открыта Dickey et al., 14 и затрагивала 20% пациентов с ЖДА без признаков желудочно-кишечной кровопотери.Это наблюдение было подтверждено и значительно расширено в серии важных исследований Аннибале и др. 13 , которые обнаружили, что 27% пациентов с рефрактерной ЖДА без желудочно-кишечных симптомов страдают атрофическим гастритом тела, процентная доля идентична доле субъектов с аутоиммунным атрофическим телом. гастрит, обнаруженный впоследствии в наших собственных исследованиях. 15,42 Абсорбция железа серьезно нарушена при ахилии желудка 43 , поскольку нормальная желудочная секреция и кислотность необходимы для растворения и снижения количества железа, поступающего с пищей. 44,45 С целью определить взаимосвязь между ЖДА, ассоциированной с аутоиммунным гастритом, и пернициозной анемией (ПА), мы изучили 160 пациентов с аутоиммунным гастритом, из которых 83 имели ЖДА, 48 – нормоцитарную анемию и 29 – макроцитарную анемию 46 ( Таблица 2).
Аутоиммунный гастрит: форма представления, связанные данные и результаты эндоскопии у 160 пациентов (Hershko et al 46 ). GI, желудочно-кишечный тракт; MALT, лимфома, связанная со слизистой оболочкой. Пациенты с ЖДА отличались от пациентов с классической ПА по ряду особенностей: они были примерно на 20 лет моложе, преимущественно женщины, и с большей вероятностью имели активную инфекцию H pylori , что подтверждается положительными серологическими исследованиями и дыхательным тестом на уреазу. . Гистологически, хотя пациенты с ЖДА имели высокую долю атрофического гастрита, активное хроническое воспаление было почти в 4 раза чаще у пациентов с ЖДА, чем у пациентов с макроцитозом, что, вероятно, отражает их более высокую частоту активной инфекции H pylori . С другой стороны, пациенты с аутоиммунным гастритом, поступившие с ЖДА, имели много признаков, совпадающих или идентичных с признаками классической ПА. Распространенность заболеваний щитовидной железы у них составляла 18%, а сахарного диабета – 8%, заболеваний, хорошо известных своей ассоциацией с ПА как частью аутоиммунных полиэндокринных синдромов. 47 Пациенты с ЖДА и аутоиммунным гастритом имели распространенность аномального кобаламина в сыворотке крови 46%.Наконец, серопозитивность для антител, блокирующих внутренний фактор, тест с низкой чувствительностью, но высокой специфичностью для ПА составила 38% у пациентов с ЖДА, как и в других двух подгруппах в настоящем исследовании. Принимая во внимание эти открытия, следует поднять вопрос о том, можем ли мы быть свидетелями более ранней фазы в эволюции того же заболевания. 48 Для окончательного ответа на этот вопрос потребуется 20-летнее наблюдение когорты пациентов с аутоиммунным гастритом из IDA.В качестве альтернативы мы могли бы стратифицировать всю популяцию из 160 пациентов по возрасту (таблица 3). Такая стратификация выявляет замечательную регулярную корреляцию между возрастом и гематологическими осложнениями аутоиммунного гастрита. С возрастом обращения наблюдалось прогрессивное увеличение среднего корпускулярного объема (MCV), а также увеличение тяжести гипергастринемии и степени дефицита кобаламина. Дефицит железа и активная инфекция H pylori , которые были очень распространены в младшей возрастной группе, постепенно заменялись дефицитом кобаламина и серонегативностью H pylori в самой старшей возрастной группе. Таблица 3Влияние возраста на проявление аутоиммунного гастрита
Среднее ± 1 стандартное отклонение (Hershko et al. ) 46 902 Если аутоиммунный атрофический гастрит нарушает абсорбцию как железа, так и кобаламина из пищи, каковы факторы, определяющие его клиническую картину в виде микроцитарной ЖДА или макроцитарной мегалобластной анемии? В этом отношении могут иметь значение возраст, пол, продолжительность и тяжесть заболевания.Хотя атрофический гастрит может ухудшать всасывание как кобаламина, так и железа одновременно, у фертильных женщин дефицит железа будет развиваться за много лет до истощения запасов кобаламина. Высокая распространенность положительности H pylori у молодых пациентов с аутоиммунным гастритом и его почти полное отсутствие у пожилых пациентов с ПА поднимают вопрос о том, может ли гастрит H pylori представлять собой раннюю фазу заболевания, при которой инфекционный процесс постепенно развивается. сменяется аутоиммунным заболеванием, заканчивающимся перегоревшей инфекцией и необратимым разрушением слизистой оболочки тела желудка.Хотя этот вопрос давно интересовал исследователей, связь между H pylori и патогенезом ПА до сих пор не решена. 49,50 Субъекты, инфицированные H. pylori , имеют циркулирующие антитела IgG, направленные против эпитопов на клетках слизистой оболочки желудка. Из них H + K + -ATPase, наиболее распространенный аутоантиген в PA, является возможной мишенью аутоиммунного механизма, запускаемого H pylori посредством антигенной мимикрии. 51-55 И наоборот, эрадикация H pylori у пациентов с аутоиммунным атрофическим гастритом сопровождается улучшением секреции желудочного сока и аскорбата у многих, а также частичной или полной ремиссией атрофического гастрита у некоторой части пациентов. 56-60 По нашему опыту, эрадикация H pylori сопровождается значительным снижением уровня гастрина в сыворотке почти у всех пациентов, но полная ремиссия, сопровождающаяся исчезновением циркулирующих антител к париетальным клеткам (APCA), наблюдается только в ограниченном количестве. пациентов. Неспособность достичь полной ремиссии путем эрадикации H pylori у большинства пациентов не обязательно является аргументом против роли H pylori в патогенезе аутоиммунного гастрита, но, скорее, указывает на то, что может быть достигнута точка невозврата, за пределами которой аутоиммунный процесс может больше не требовать постоянного присутствия возбудителя. ЖДА без явных клинических доказательств кишечной мальабсорбции является одним из наиболее частых внекишечных проявлений целиакии. 61,62 И наоборот, среди пациентов с необъяснимой ЖДА, целиакия является причиной анемии в 5–6% случаев. 63-65 Демонстрация гистологических изменений слизистой оболочки тонкой кишки по-прежнему считается золотым стандартом диагностики целиакии. 66,67 Однако открытие антиэндомизиальных антител у пациентов с глютеновой болезнью оказало большое влияние на алгоритмы скрининга и диагностики для распознавания целиакии. 68 Его специфичность и чувствительность оцениваются в 99% и более 90% соответственно. Совсем недавно иммуноферментный анализ был разработан для измерения активности антител IgA к TTG, и он более удобен, дешевле и дает сопоставимую чувствительность и специфичность с более старым антиэндомизиальным непрямым флуоресцентным тестом. 67 Дополнительные диагностические критерии включают идентификацию генотипов HLA-DQ2 или DQ8 и реакцию на безглютеновую диету. 69,70 14 пациентов с глютеновой болезнью в нашей серии были неотличимы от остальных пациентов с анемией по возрасту, тяжести ЖДА или сывороточного альбумина. Их наиболее устойчивой клинической особенностью была полная невосприимчивость к пероральному лечению железом. Наиболее очевидной причиной анемии при целиакии является нарушение всасывания железа и других питательных веществ, включая фолиевую кислоту и кобаламин.О скрытой желудочно-кишечной кровопотере сообщалось в одном исследовании, 71 , но, по-видимому, не играет значительной роли в возникновении анемии. Сам по себе недостаточность питания не объясняет анемию во всех случаях, и у некоторых пациентов, по-видимому, способствует воспаление, о чем свидетельствует наличие маркеров хронической анемии (ACD) примерно у 17% пациентов с глютеновой болезнью. 72,73 Сообщалось о высокой доле серонегативной клинически легкой целиакии среди пациентов с необъяснимой ЖДА, удовлетворяющих всем другим критериям целиакии, включая генотип HLA-DQ2 / DQ8, биопсию дистального отдела двенадцатиперстной кишки и ответ на специфическую терапию. 74 Будущие исследования серонегативной целиакии могут пролить свет на вклад генетических факторов, а не факторов окружающей среды в фенотипическое проявление этого заболевания. IRIDA представляет собой аутосомно-рецессивное заболевание, вызванное мутациями в гене трансмембранной сериновой протеазы 6 (TMPRSS6), кодирующем Матриптазу-2 (MT-2). 77 MT-2 представляет собой трансмембранную сериновую протеазу, необходимую для подавления активности гепсидина, главного регулятора гомеостаза железа.Исследования in vitro на трансфицированных линиях клеток печени предполагают, что MT-2 расщепляет гемоювелин, активатор экспрессии гепсидина. 78 Эта функция нарушается при мутациях с участием TMPRSS6, приводящих к IRIDA. Следовательно, уровень гепсидина в сыворотке неоправданно высок, и пациенты не могут реагировать на недостаток железа подавлением экспрессии гепсидина. 79-81 Пациенты с наследственной ИРИДА страдают гипохромной микроцитарной анемией с очень низким содержанием железа и трансферрина в сыворотке крови.Однако, в отличие от дефицита железа в питательных веществах, их сывороточный ферритин нормален или неадекватно высок для степени дефицита железа. Степень тяжести анемии варьирует, обычно умеренная; он отсутствует при рождении и развивается после неонатального периода. Хотя в детстве анемия обычно протекает тяжелее, чем в более позднем возрасте, корреляции между возрастом на момент постановки диагноза и тяжестью анемии нет. Хотя распространенность ИРИДА в настоящее время неизвестна, следует рассмотреть возможность применения ИРИДА, особенно у детей и молодых людей, когда исключены другие известные причины рефрактерной ЖДА. 76 Распознавание затронутых братьев и сестер может указывать на унаследованное состояние, но спорадические случаи могут возникать из-за рецессивного способа передачи или когда количество братьев и сестер ограничено. Уровни гепсидина в IRIDA нормальные или повышенные, в отличие от дефицита пищевого железа, при котором гепсидин низкий или неопределяемый. 82 ACD может напоминать IRIDA во многих отношениях, поскольку провоспалительные цитокины стимулируют синтез гепсидина и связаны с анемией, низким уровнем сывороточного железа и повышенным уровнем сывороточного ферритина.Дифференциальный диагноз с IRIDA основан на легкой нормоцитарной или умеренно микроцитарной природе анемии при ACD в сочетании с клиническими и лабораторными признаками воспаления. Диагностика IRIDA требует идентификации генетических поражений путем секвенирования экзонов и границ экзон-интрон гена TMPRSS6. 83,84 Причинные мутации – это нуклеотидные изменения, которые мешают синтезу белка или аминокислотные замены, которые распространяются по всем внеклеточным доменам белка.Хотя некоторые мутанты полностью подавляют протеолитическую активность, другие сохраняют остаточную активность в исследованиях in vitro с использованием промотора гепсидина. 85 К настоящему времени зарегистрировано более 50 пациентов из 34 семей с широким диапазоном этнического происхождения, представляющих> 40 различных мутаций TMPRSS6. 76,86,87 ПолиморфизмTMPRSS6 был связан с вариациями параметров железа 88 и с повышенным риском дефицита железа. 89 Интересно, что варианты TMPRSS6 были связаны с ЖДА в небольшой группе пациентов с аутоиммунным гастритом с полиэндокринным аутоиммунным синдромом 90 , что предполагает взаимодействие между генетическими и приобретенными факторами в рефрактерной ЖДА. Как подразумевает термин IRIDA, пациенты не могут удовлетворительно реагировать на пероральное лечение железом. Однако не все пациенты с IRIDA полностью невосприимчивы к пероральному лечению железом.Длительный прием перорального железа смог вызвать частичную коррекцию анемии у пациентов из 4 неродственных семей. 87,91-93 Однако даже при внутривенном введении железа ответ на лечение медленный, а коррекция анемии частичная. Напротив, сывороточный ферритин увеличивается при внутривенной терапии железом в зависимости от дозы. Все эти корреляции соответствуют известным взаимодействиям гепсидин-ферропортин и подавляющему эффекту неадекватно высокого производства гепсидина на абсорбцию и рециркуляцию железа.В целом потребность в лечении железом наиболее высока у детей и незначительна у взрослых с ограниченными потребностями в железе. В некоторых случаях при многолетнем наблюдении взрослые вылечивают анемию, хотя тяжелый микроцитоз и низкий уровень сывороточного железа сохраняются. 94 Поскольку методы диагностики ЖДА хорошо известны, 2-5 следующий текст ограничен особыми требованиями пациентов с рефрактерной анемией после того, как все стандартные диагностические требования уже выполнены.Как указывалось ранее, наше определение рефрактерной анемии – это отсутствие ответа на пероральное лечение железом 100 мг элементарного железа в день в течение 4–6 недель путем увеличения Hb по крайней мере на 1 г / дл. В первую очередь следует исключить другие причины неэффективности лечения. По общему признанию, это непростая задача, поскольку даже опытные врачи могут быть введены в заблуждение из-за низкой приверженности, неточного анамнеза, ложного диагноза и случайной искусственной анемии. Следует проявлять осторожность, чтобы исключить ACD с использованием C-реактивного белка и других белков, реагирующих в острой фазе, хронической почечной недостаточности, использования ингибиторов протонной помпы, снижающих кислотность желудочного сока, и желудочно-кишечного кровотечения, вызванного лекарствами или наследственными нарушениями свертываемости крови. Помимо истории хронической ЖДА, не реагирующей на пероральное введение железа, история болезни и физикальное обследование имеют ограниченную ценность для определения конкретной причины рефрактерности к железу. У некоторых пациентов с аутоиммунным гастритом может встречаться сопутствующий дефицит кобаламина. Рефрактерная ЖДА, начинающаяся в раннем детстве с положительным семейным анамнезом, обнаруживается у некоторых, но не у всех пациентов с ИРИДА.Вероятность возникновения ЖДА, связанного с H. pylori , особенно высока у мужчин и женщин в постменопаузе без анатомических изменений со стороны желудочно-кишечного тракта. Предлагается, чтобы все пациенты, обследованные на предмет необъяснимой рефрактерной анемии, прошли серологическое обследование на целиакию, H pylori IgG-антитела или фекальный антиген, сывороточный гастрин и антитела к париетальному и / или внутреннему фактору 67,95,96 ( Таблица 4). Таблица 4Предлагаемое диагностическое обследование при необъяснимой или рефрактерной ЖДА
Пациенты с положительной серологией H pylori или фекальным антигеном должны быть направлены на уреазный дыхательный тест для подтверждения инфекции H. pylori .Эндоскопическое подтверждение гастрита H. pylori не является обязательным. Пациенты с аутоиммунным гастритом, на что указывает сочетание повышенного содержания гастрина в сыворотке и антител к париетальным клеткам или внутренним факторам, должны быть обследованы на заболевание щитовидной железы и истощение запасов кобаламина. Эндоскопия верхних отделов желудочно-кишечного тракта с биопсией слизистой оболочки рекомендуется всем новым пациентам с аутоиммунным гастритом при постановке диагноза, а затем с интервалом от 5 до 10 лет. Пациенты с положительным результатом серологии целиакии должны быть направлены на биопсию двенадцатиперстной кишки и проверены на генотипы HLA-DQ2 и -DQ8. Пациентам с историей, предполагающей наследственный дефицит железа с уровнем ферритина в сыворотке крови выше ожидаемого, рекомендуется генетическое обследование. 75 При подозрении на IRIDA в Приложении перечислены доступные лаборатории Национального центра биотехнологической информации (NCBI) для секвенирования TMPRSS6. Стандартная тройная терапия для эрадикации H pylori состоит из ингибитора протонной помпы, кларитромицина и амоксициллина в течение 10–14 дней или по протоколу на основе висмута. 29-35 Для подтверждения эрадикации дыхательный тест с уреазой следует повторить через 1 месяц после завершения тройной терапии. Специфического лечения аутоиммунного гастрита не существует. Следует контролировать уровни кобаламина в сыворотке, чтобы определить необходимость приема добавок кобаламина. У пациентов с аутоиммунным гастритом с сопутствующей активной инфекцией H pylori эрадикация H. pylori может быть полезной для остановки прогрессирования заболевания и улучшения реакции на пероральное введение железа. 56-60 Пациентам с глютеновой болезнью следует начинать диету без глютена с регулярным наблюдением, чтобы гарантировать ответ и соблюдение. 67 Для перорального применения доступно большое количество соединений железа со значительными различиями в биодоступности железа. Соли двухвалентного железа обладают более высокой биодоступностью по сравнению с солями трехвалентного железа. Из-за относительно низкой стоимости и разумной биодоступности сульфат двухвалентного железа является соединением железа, наиболее часто используемым для пероральной терапии железом.Был разработан ряд препаратов с медленным высвобождением железа, но по большей части биодоступность не равна биологической доступности стандартных таблеток сульфата железа. 4 В целом эритропоэтический ответ на терапию железом должен наблюдаться в течение 4-6 недель после заместительной терапии железом. Ожидается, что уровень гемоглобина повысится на ~ 0,1 г / дл в день после начала терапии железом. Кроме того, содержание гемоглобина в ретикулоцитах (CHr) является ранним, чувствительным индикатором благоприятного ответа на введение железа. 97-99 Одновременный прием аскорбиновой кислоты усиливает всасывание железа. У некоторых наших пациентов серин-сульфат железа и глицина сульфат вызвали хорошие результаты, когда другие препараты железа оказались неэффективными, но относительное преимущество этих препаратов все еще требует объективной оценки в проспективных рандомизированных исследованиях. 100 Внутривенное введение железа показано пациентам, не отвечающим на лечение пероральным железом.В настоящее время доступны несколько препаратов железа для внутривенного введения. 101 Они состоят из ядра оксогидроксида железа с защитной углеводной оболочкой из сахарных полимеров. 102 После инъекции железо медленно высвобождается и захватывается трансферрином плазмы. Скорость диссоциации железа из комплекса непостоянна. Глюконат железа является наиболее лабильным с наиболее быстрым высвобождением железа, и, следовательно, дозы от 62,5 до 125 мг являются максимальными, которые можно переносить при однократной инфузии.Сахароза железа более стабильна, и можно безопасно назначать более высокие дозы, обычно 200 мг железа. Наиболее стабильными препаратами железа являются декстраны железа, прочно связанные со своими ядрами оксогидроксида железа. Есть высокомолекулярные и низкомолекулярные декстраны железа. Согласно недавним отчетам фармаконадзора из Северной Америки и Европы, ОШ сообщенных абсолютных абсолютных показателей неблагоприятных для жизни событий при парентеральном введении железа составляет 38 на миллион доз: риск анафилаксии при применении декстрана железа по сравнению с сахарозой железа составляет 17.От 7 до 16,9 раза. 103 Ввиду повышенного риска опасных для жизни побочных эффектов и доступности гораздо более безопасных соединений железа для внутривенного введения, использование высокомолекулярного декстрана железа больше не оправдано. Недавно стали доступны несколько дополнительных препаратов железа для внутривенного введения, включая карбоксимальтозу железа, изомальтозид железа 1000 и ферумокситол. Эти препараты позволяют вводить гораздо более высокие дозы железа внутривенно за более короткое время. 104 Их можно безопасно и эффективно использовать для восстановления железа в организме, возможно, даже за один сеанс лечения. В настоящее время существует потребность в хорошо спланированных сравнительных исследованиях, позволяющих судить об относительном преимуществе в отношении безопасности и эффективности всех вновь доступных соединений. Кроме того, все еще существует неопределенность в отношении долгосрочной безопасности внутривенного введения железа в отношении его способности повышать восприимчивость к инфекциям и способствовать окислительному стрессу. 3 Препараты железа для парентерального введения могут использоваться для коррекции дефицита железа или поддержания запасов железа.Приблизительно 170 мг железа требуется для повышения уровня гемоглобина на 10 г / л у человека с массой тела 70 кг, исходя из общего объема крови 4,9 л. Уровень железа у пациентов, принимающих препараты железа, перорально или внутривенно, должен быть периодически контролируется, чтобы установить, пополняются ли запасы железа в достаточной мере, и избежать перегрузки железом, которая может возникнуть при неконтролируемой долгосрочной замене железа. У пациентов с ЖДА высокого риска полное эндоскопическое обследование является обязательным.Напротив, пациенты с низким риском, представляющие подавляющее большинство субъектов с рефрактерной ЖДА, остаются в сфере ответственности гематолога. Гематолог, в свою очередь, теперь оснащен мощными неинвазивными инструментами для выявления пациентов с ЖДА, требующих особого внимания. Признание соответствующих ролей H pylori, аутоиммунного гастрита, целиакии и наследственных заболеваний в патогенезе дефицита железа должно оказать сильное влияние на текущие диагностические исследования и лечение рефрактерной ЖДА, а также на резкое снижение доли Пациенты с ЖДА по-прежнему называются «необъяснимыми».” Вклад: C.H. и C.C. написал газету. Раскрытие информации о конфликте интересов: авторы заявляют об отсутствии конкурирующих финансовых интересов. Для корреспонденции: Хаим Хершко, Отдел обеспечения качества, Министерство здравоохранения Израиля, Habirah Towers, Rm 317 Jeremia St 39, PO Box 1176, Иерусалим, Израиль; электронная почта: hershkoc @ netvision. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||


 Оставляем, пока не застынет.
Оставляем, пока не застынет.