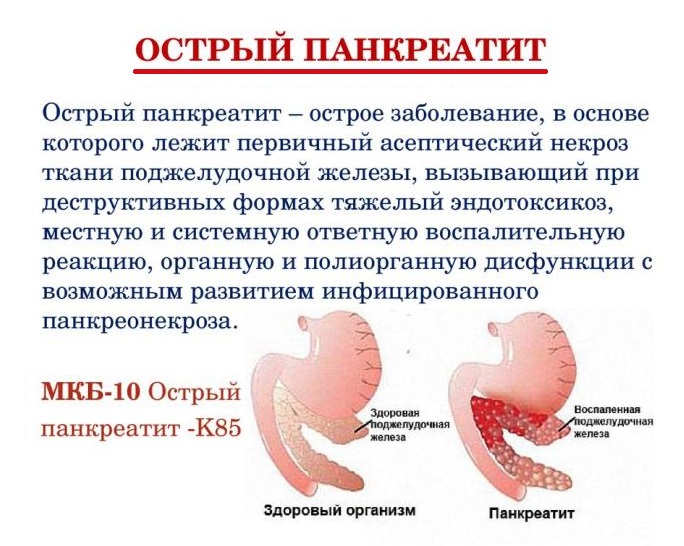
Лечение острого панкреатита медикаментами препараты: какие лекарства принимают при панкреатите и как они действуют?
таблетки, препараты и лекарственные средства
Помощь организму в борьбе с панкреатитом требует знания степени тяжести заболевания. Лечить панкреатит нужно непременно! Исходя из состояния и срока заболевания врач производит назначения лекарств. Задача состоит в облегчении состояния больного, устранении болевого синдрома, остановке воспаления и наладке пищеварительного процесса.
Как известно, при панкреатите воспаляется поджелудочная железа. Это орган, выполняющий важнейшие функции – секрецию пищеварительных ферментов и вырабатывающий инсулин. При недостаточном количестве инсулина появляется заболевание сахарный диабет. Панкреатит известен в двух формах – острой и хронической. Если первый случай поддается лечению и препараты при остром панкреатите в силах восстановить функции поджелудочной железы, при втором случае функция снижается. Лечение заболевания определяется видом и тяжестью.
Болевые ощущения хочется устранить побыстрее. Обязательным становится лечение панкреатита медикаментами. В начале заболевания рекомендуют соблюдать покой, ограничить употребления еды. На болевую область прикладывают холод. Препараты в первые дни – либо Омепразол, либо Ранитидин. Действуя в организме, вещества уменьшают выработку соляной кислоты. Таким образом, кислота перестает стимулировать работу поджелудочной железы. При легком течении заболевания не возникает осложнения, преимущественно назначается поддерживающая терапия. Лекарство-анальгетик останавливает боль. Периодически возникает рвота, организм теряет жидкость, на помощь приходит терапия. Антибактериальные препараты применяют, если появляется инфекция (развивается в дыхательной системе или в желчевыводящих путях).
В начале заболевания рекомендуют соблюдать покой, ограничить употребления еды. На болевую область прикладывают холод. Препараты в первые дни – либо Омепразол, либо Ранитидин. Действуя в организме, вещества уменьшают выработку соляной кислоты. Таким образом, кислота перестает стимулировать работу поджелудочной железы. При легком течении заболевания не возникает осложнения, преимущественно назначается поддерживающая терапия. Лекарство-анальгетик останавливает боль. Периодически возникает рвота, организм теряет жидкость, на помощь приходит терапия. Антибактериальные препараты применяют, если появляется инфекция (развивается в дыхательной системе или в желчевыводящих путях).
Лечение острого панкреатита медикаментами сопровождается строгим ограничением пищи – таково необходимое условие для облегчения состояния больного. Кушать позволяется через 3 дня, за указанное время стихают болевые ощущения, в норму приходит перистальтика.
Читайте также дополнительные материалы, это важно знать.
Тяжелая форма
Тяжелое течение заболевания диктует правила. Становится невозможно употреблять еду здоровых людей в течение месяца. Привычная еда заменяется парентеральной. Разновидность заболевания опасна возникновением некротизирующего вида. Перед назначением медикаментозного лечения хронического панкреатита выполняется диагностика.
Для определения формы болезни используется томография. Указанный вид компьютерного исследования предусматривает использование контрастного вещества. Выявленные осложнения станут показанием к беспрестанному наблюдению врачей. Запрещенными в период острого панкреатита тяжелой формы становятся лекарственные средства сосудосуживающего действия. В начальный период под строгим контролем удерживается объем жидкости, циркулирующей в организме. При потере жидкость восполняется переливанием. Средний уровень – 6 литров либо больше.
Уменьшение воды сказывается на работе почек, используется инфузионная терапия.
Применяемые препараты
Определив стадию, форму заболевания, врач назначает требуемые препараты при панкреатите:
- Препараты обезболивающего действия предписаны при острой форме.
 Действие понятно – устранить боль. Результативными считаются но-шпа или папаверин.
Действие понятно – устранить боль. Результативными считаются но-шпа или папаверин. - Ферментосодержащие медикаменты направлены на снижение нагрузки. Поджелудочной железе с помощью мезима либо креона обеспечивается спокойное состояние.
- Препараты-антациды для устранения различных расстройств (к примеру, изжоги).
- При лечении панкреатита в сложных случаях врач применяет антибиотик. Следует помнить о побочных эффектах препарата.
Соответствующее лечение с применением действенных лекарств назначает исключительно опытный врач, исходя из оценки состояния больного!
Лечение панкреатита таблетками проходит индивидуально. Любой пациент нуждается в индивидуальном подходе, исходя из симптомов и формы заболевания. В случае приобретения острой формы болезни пища под запретом, разрешается пить воду. Потом применяется диета.
При хроническом панкреатите рацион постепенно, после улучшения состояния, расширяется. Включается пища, богатая на белки. Как при любой болезни желудочно-кишечного тракта под запретом жирное, соленое, кислое и острое.
Ферменты
Лечение панкреатита невозможно без ферментов. Подобные препараты назначаются не единственно для лечения хронического панкреатита. Они – главный способ борьбы и с холециститом. Действие заключается в уменьшении секреции поджелудочной железы, человек ощущает меньшие боли.
Панкреатин – база ферментных препаратов, применяемых для лечения хронического панкреатита и преследующих заместительную цель. От степени недостаточности органа зависит доза лекарства. Ферментная терапия с помощью амилазы, находящейся в отдельных препаратах, подавляет панкреатическую секрецию. Для лечения и полного восстановления поджелудочной железы ферменты используют давно. Современная медицина не стоит на месте, регулярно появляются новые подходы и средства для лечения панкреатита. Новейшее, хорошо зарекомендовавшее себя средство – вобэнзим.
Немало людей отмечает положительные стороны препарата. Пациенты говорят, что исключительно вобэнзим способен держать поджелудочную железу в норме. Из-за положительного влияния лекарства больные не хотят замены на иные препараты для лечения панкреатита. Помните, принимают медикамент при хронических формах заболевания курсом от трех до шести месяцев. Детям до 5 лет препарат запрещен.
Из-за положительного влияния лекарства больные не хотят замены на иные препараты для лечения панкреатита. Помните, принимают медикамент при хронических формах заболевания курсом от трех до шести месяцев. Детям до 5 лет препарат запрещен.
Вобэнзим легко переносится больными. Продолжительное применение препарата не вызывало побочных эффектов либо привыкания. Вобэнзим состоит из ферментов, подобных человеческим. Решение о назначении препарата – исключительно в компетенции лечащего врача. Доза не превышает таблетки три раза в день. Вобэнзим требуется принимать, соблюдая диету. Прием препарата происходит месяц.
Проверенный временем препарат, применяемый совместно с другими – фестал. Лекарство расщепляет жиры, углеводы и белки благодаря липолитическому, амилолитическому и протеолитическому действиям. Препарат применяют длительно.
Помните, что только врач советует, какие лучше выбрать ферменты в каждом случае.
Чага
Не только медикаментозное лечение панкреатита показывает удовлетворительное действие на организм. Известно немало природных средств. Березовый гриб – прекрасное природное средство. Темного, почти черного цвета чага прирастает к коре березы. Запасаются чагой в весенний или осенний период, когда гриб набирает максимальное количество полезных веществ. Рубят топором на куски и сушат.
Известно немало природных средств. Березовый гриб – прекрасное природное средство. Темного, почти черного цвета чага прирастает к коре березы. Запасаются чагой в весенний или осенний период, когда гриб набирает максимальное количество полезных веществ. Рубят топором на куски и сушат.
Гриб чага присутствует в отдельных лекарственных препаратах, приготовляют с помощью чаги полезный настой. Гриб содержит высокополимерные соединения и применяется для лечения многих заболеваний. Панкреатит – не исключение. Настойка: чагу необходимо вымыть и погрузить в кипяток. Держат там несколько часов, измельчают, выстоянную воду нагревают и заливают гриб. Примерные пропорции – один к пяти, хранить допускается четыре дня. Нетоксичность гриба позволяет пить такой настой при панкреатите поджелудочной железы, в день до трех приемов по 200 граммов.
Инновация в отечественной фармацевтике
Так называют энтеросгель. Лекарство «съедает» токсины, представляющие опасность здоровью человека, поэтому часто применяется при панкреатите.
Этиология токсинов неважна, энтеросгель выводит любые виды. Информация касается ядовитых веществ, антигенов, бактерий, различных аллергенов. Препарат назначают в комплексе с прочими лекарствами при лечении заболеваний, связанных с интоксикацией. Гель не имеет запаха или вкуса, из организма выводится в первоначальном виде. Лечение панкреатита у взрослых отличается от лечения, назначаемого маленьким пациентам. Минимум противопоказаний позволяет применять энтеросгель многим людям, женщинам в положении, детям.
При интенсивной боли
Лекарства для поджелудочной железы незаменимы при сильной боли. В подобные периоды человеку особенно тяжело, хочется быстрее избавиться от болевых ощущений. Часто в это время идёт в ход платифиллин. Снимая спазм, укол производят подкожно. Выбор средства очевиден – у лекарства меньше ненужных последствий на организм.
Пчелы в помощь
Пчелы – полезные существа, приходят на помощь даже при панкреатите. Насекомые производят натуральный лечащий препарат, консервируя пыльцу в сотах. Сочетание с нектаром, ферментами самих пчел и медом делают пергу прекрасным помощником в борьбе с панкреатитом.
Сочетание с нектаром, ферментами самих пчел и медом делают пергу прекрасным помощником в борьбе с панкреатитом.
Это хорошее средство для борьбы со многими заболеваниями. Обилие витаминов, микроэлементов и прочих веществ действуют на поджелудочную железу восстанавливающее. Для органа и пищеварительного тракта перга – необходимый продукт. Поврежденные функции клеток и тканей улучшаются, усваивая превосходное легкоусвояемое терапевтическое средство. Принимать разрешено когда угодно – перга не влияет на уровень сахара в крови, повышает иммунитет, устраняет истощение.
Полезный отвар
Календула часто приходит на помощь при лечении панкреатита. Цветок снижает отечность, уменьшает болевые ощущения, выступает прекрасным бактерицидным средством. Календула положительно влияет на кишечный тракт, убирает застой в желчном пузыре.
Лекарство для защиты клеток
Таблетки от панкреатита назначает врач. Важно выбрать опытного доктора, который подберет индивидуальное лечение. Существует множество препаратов. Популярное средство для лечения болезни – Эссенциале. Используют лекарство курсами по назначению врача. Фосфолипиды в составе направлены на восстановление и защиту клеток. Хорошо влияя на метаболизм, медикамент обнаруживает мало побочных эффектов, передозировка не представляет опасности.
Существует множество препаратов. Популярное средство для лечения болезни – Эссенциале. Используют лекарство курсами по назначению врача. Фосфолипиды в составе направлены на восстановление и защиту клеток. Хорошо влияя на метаболизм, медикамент обнаруживает мало побочных эффектов, передозировка не представляет опасности.
Для регулирования работы кишечника
Перистальтика кишечника также требует помощи при заболевании. Тримедат – лекарство, регулирующее моторную функцию желудочно-кишечного тракта. Препарат по-разному действует на кишечник. При необходимости повышает активность либо, наоборот, подавляет работу мускулатуры кишечника.
Тримедат – лекарство, регулирующее моторную функцию желудочно-кишечного тракта. Препарат по-разному действует на кишечник. При необходимости повышает активность либо, наоборот, подавляет работу мускулатуры кишечника.
Долго находящаяся в желудке пища вызывает бродильный процесс. Препарат тримедат способствует выводу пищи вовремя. Врачи отмечают и иные положительные качества. Приняв лекарство, легко уменьшить спазмы.
Нольпаза
Подавляя выработку соляной кислоты, нольпаза способствует избавлению от боли при панкреатите. Симптомы заболевания отходят. Попутное положительное качество препарата – в замедлении процессов разрушения органа.
Когда в ход идут антибиотики
Антибиотики применяются при лечении панкреатита редко. Использование в ряде случаев продиктовано сложностью заболевания, когда без противомикробных лекарств не обойтись. Часто на помощь приходит метронидазол. Врач принимает решение о назначении лекарства при сложных формах течения болезни, когда присутствует угроза заражения инфекцией тканей поджелудочной железы.
Главное успеть вовремя. Принимать метронидазол начинают своевременно. При вовремя начатом лечении избавиться от болезни можно. После прохождения диагностирования врач назначит список лекарств, необходимый на развивающейся стадии.
препараты для медикаментозного лечения острого и хронического воспаления поджелудочной железы
Панкреатитом называют воспалительное заболевание поджелудочной железы. Оно возникает из-за того, что ферменты, необходимые для обеспечения пищеварительных процессов, вырабатываются в недостаточном количестве. При таком заболевании нередки обострения, протекающие на фоне острых болевых ощущений, а запущенный недуг переходит в хронический. Если болезнь протекает без осложнений, проводится лечение панкреатита медикаментами, в рамках которого назначаются фармпрепараты нескольких групп.
Содержание материала:
Причины и симптомы заболевания
Более чем в 50% случаев панкреатит развивается из-за несдержанности в приёме алкогольных напитков. Этаноловые соединения вызывают нарушения в органах ЖКТ и способны блокировать выработку ферментов, за счёт чего и происходит воспаление поджелудочной железы.
Этаноловые соединения вызывают нарушения в органах ЖКТ и способны блокировать выработку ферментов, за счёт чего и происходит воспаление поджелудочной железы.
Иными факторами, провоцирующим развитие патологии, считаются:
- неправильное питание с преобладанием острой и жирной пищи;
- воспаления и инфекции, затронувшие желудочно-кишечный тракт;
- паразитарные заболевания;
- травмы органов брюшной полости;
- хирургические операции;
- химические отравления;
- некорректное применение медикаментов.
На заметку. Точную причину развития недуга может установить только гастроэнтеролог после проведения диагностических мероприятий. На основании этих данных и назначаются препараты для лечения панкреатита.
К основным симптомам хронического панкреатита относятся следующие проявления:
- боли в области живота;
- обильное выделение слюны и отрыжка;
- потеря аппетита;
- тошнота и рвотные позывы;
- расстройства пищеварения;
- нарушения стула;
- метеоризм и чувство тяжести в нижней части живота.

Если игнорировать эти симптомы, запущенный панкреатит может привести к развитию ряда осложнений, представляющих угрозу для жизни.
Лечение панкреатита медикаментами
В терапии хронического и острого панкреатита применяется ряд средств. Основными целями медикаментозного лечения являются снятие болевого синдрома, борьба с воспалением и восстановление функции поджелудочной железы.
Если заболевание вторично и вызвано какими-либо хроническими процессами в организме, дополнительно назначаются лекарства и для терапии основного недуга.
Хроническое воспаление поджелудочной железы
При хроническом панкреатите назначаются лекарственные препараты следующих групп:
- Ферментативные средства. Эти медикаменты позволяют снизить нагрузку на поджелудочную железу и ускорить процесс регенерации в тканях. Поступающие в организм ферменты помогают нормализовать пищеварение и восстановить работу ЖКТ, что приводит к исчезновению тошноты, отрыжки и прочих неприятных проявлений.
 Наиболее популярными средствами, применяющимися в терапии заболевания, являются «Панкреатин», «Креон» и «Панцитрат».
Наиболее популярными средствами, применяющимися в терапии заболевания, являются «Панкреатин», «Креон» и «Панцитрат». - Антиферменты. Такие средства применяются в случаях, когда происходит выброс большого объема активных энзимов, которые способствуют разрушительным процессам в пищеварительных органах. Чаще всего назначаются «Контрикал» и «Гордокс» для внутривенного введения.
- Антибактериальные препараты. Нередко болезненный процесс, затронувший поджелудочную, распространяется и на соседние ткани. В таких ситуациях возникает потребность в антибиотиках. Хорошо зарекомендовали себя «Тетрациклин» и «Бисептол».
- Антацидные средства. Основной функцией этих медикаментов является восстановление нормального уровня кислотности и снижение активности ферментов. Помимо этого, они защищают слизистую оболочку желудка и кишечника, предотвращая язвенные поражения. Одними из лучших препаратов этой группы признаны «Фосфалюгель» и «Омепразол».
- Блокаторы Н2. Такие лекарственные средства регулируют кислотность и обладают анальгезирующим действием.
 Используют их не так часто, поскольку они способны провоцировать побочные реакции. При возникновении такой потребности назначают «Ранитидин» и «Фамотидин».
Используют их не так часто, поскольку они способны провоцировать побочные реакции. При возникновении такой потребности назначают «Ранитидин» и «Фамотидин». - Гормональные средства. Эти препараты используются лишь в случаях, когда причиной развития панкреатита стал аутоиммунный процесс. Выбор лекарства зависит от состояния пациента и его индивидуальных особенностей, но довольно часто назначают «Преднизолон».
- Комплексы витаминов. Поскольку при панкреатите нарушаются обменные процессы, организм особенно нуждается в полезных микроэлементах, чтобы нормально функционировать. Как правило, в рамках терапии назначаются комплексы, содержащие витамины группы A, B и E, а также никотиновую и аскорбиновую кислоту.
Если панкреатит вызвал какие-либо осложнения, назначаются дополнительные медикаменты в соответствии с состоянием больного.
Острый панкреатит
Процесс лечения острого панкреатита мало чем отличается от терапии хронического. Разница заключается лишь в том, что в моменты обострений возникают сильные болевые ощущения и спазмы, и для их устранения используются анальгезирующие препараты.
В случаях, когда болевой синдром выражен особенно остро, применяются седативные средства, которые также могут использоваться и при лечении хронического панкреатита.
Наиболее распространенными препаратами подобного действия являются «Доксепин» и «Амитриптилин». Принимать эти средства можно в течение непродолжительного периода и только под строгим медицинским контролем.
Чем снимать боль при заболевании
Когда приступы панкреатита сопровождаются острыми, нестерпимыми болями, назначаются мощные препараты следующих групп:
- Анальгетики. Такие средства позволяют блокировать болевой синдром и снижают выраженность воспаления. Чаще всего применяются «Анальгин», «Баралгин» и «Парацетамол».
- Спазмолитики. Такие препараты помогают расслаблению гладких мышц и используются при лечении панкреатитов, сопровождающихся холециститом и дискинезией желчевыводящих путей.
 Лучшими средствами в терапии таких состояний признаны «Но-шпа» и «Папаверин» в сочетании с «Платифиллином».
Лучшими средствами в терапии таких состояний признаны «Но-шпа» и «Папаверин» в сочетании с «Платифиллином».
В отдельных случаях могут назначаться и более сильные препараты для однократного применения, позволяющие снять тяжелый приступ.
В таких ситуациях рекомендованы дозы «Промедола» или «Трамадола», но применять эти медикаменты нужно с особенной осторожностью и только с разрешения врача.
Как правильно принимать препараты при панкреатите
Препараты, схему приема, дозировку и длительность лечения определяет врач, он же и разъясняет, как пить то или иное средство.
Но есть правила, которые нужно соблюдать при приеме лекарств от панкреатита любых групп:
- Принимать медикаменты в соответствии с инструкцией и назначениями специалиста.
- Запивать таблетки только водой в объеме не менее 100 – 150 мл.
- Стараться пить лекарства в одни и те же часы.
- На протяжении курса лечения исключить алкоголь, поскольку это приведет к дополнительной нагрузке на пищеварительный тракт.

- При любых ухудшениях состояния сообщать об этом лечащему врачу.
Чтобы повысить эффективность проводимого лечения, важно не только принимать лекарства, но и соблюдать диету.
Неправильное питание может привести к обострению заболевания и возникновению осложнений.
Несмотря на то, что на сегодняшний день существует большое количество лекарственных средств для поддержания поджелудочной железы, вылечить панкреатит довольно трудно. Поэтому каждый больной должен осознавать, что исход заболевания во многом зависит от того, насколько дисциплинированно он соблюдает предписания. Если игнорировать рекомендации специалистов, неправильно питаться и употреблять алкогольные напитки, медикаментозное лечение почти бесполезно.
Консервативное лечение острого панкреатита медикаментами
Википедия гласит, что острый панкреатит представляет собой остро протекающий воспалительный процесс в поджелудочной железе. По последним медицинским данным, летальность при остром приступе составляет от 7 до 70%, в зависимости от этиологии заболевания, степени запущенности и своевременности обращения к специалистам. Консервативное лечение медикаментами – обязательный этап терапии. В тяжелых случаях прибегают к операционному вмешательству.
Консервативное лечение медикаментами – обязательный этап терапии. В тяжелых случаях прибегают к операционному вмешательству.
Чем и как лечить острый панкреатит
Содержание статьи
Правильно подобранные медикаменты – основа лечения. Их задача – погасить воспалительный процесс как можно скорее и восстановить функциональность органа. Так как при остром воспалении поджелудочной железе был нанесен серьезный урон, обойтись единственной таблеткой, которая бы решила все проблемы разом не удастся. По крайней мере, до такого современная медицина еще не дошла.
Вести борьбу за здоровье приходится сразу по нескольким фронтам. Именно поэтому показан прием ряда лекарственных средств, отличающихся свой направленностью: Мезим, Креон, Гастрозол, Панкреатин, Пензистал, Эрмиталь, Маалокс, Алмагель,Мебеверин, Но-шпа, Папаверин и пр.
Острый панкреатит: лечение, препараты ферментные
Ферментные препараты необходимы для компенсации недостатка функциональности, обеспечения покоя и избавления от лишней нагрузки на орган.
Один из самых распространенных медикаментов данной группы – Мезим. Его пьют в виде таблеток по 1 шт. трижды в сути перед приемом пищи. Его конкурент – Креон, выпускается в форме устойчивых к разъедающему желудочному соку капсул.
Для лучшего усвоения ферментов прибегают также к лекарствам, которые способны подавлять секрецию – Гастрозол и Омепразол. В числе их полезных свойств значатся кроме того снижение агрессивности сока.
Не менее известны ферментные средства под названиями Пензистал и Панкреатит, которые наравне с Мезимом, мягко воздействуют на пострадавшую железу, попутно снимания болевой синдром. Они имеют отличную переносимость и удостоились множества положительных отзывов. О них хорошо отзываются не только пациенты, но и доктора.
На их фоне Креон – более сложный медикамент. По аналогии с ним частенько назначают другой капсульный препарат для заместительной терапии – Эрмиталь.
Антацидные
препараты для лечения: острый панкреатит
Нейтрализовать кислотность, являющуюся виновницей отрыжки, вздутия живота, изжоги, тошноты и других диспепсических отклонений, помогают такие антацидные средства как Алмагель, выпускающийся в виде раствора, и Маалокс, продающийся в таблетках.
Врачи призывают не употреблять данную группу препаратов без надобности и злоупотреблять ей даже несмотря на перенесенный острый приступ, так как существует вероятность развития побочных действий. Неправильный и излишний прием сведет общий результат лечения к минимуму, а то и усугубит положение дел.
Лекарства при остром панкреатите: антибиотики
Высокий риск появления осложнений заставляет обращаться к антибиотикам. Если возникает подозрение или того хуже диагностируется сепсис или перитонит, антибактериальная терапия – единственный шанс на спасение. Препараты-антибиотики могут быть введены посредством таблеток или инъекций. Наименование и дозировка лекарства подбирается строго индивидуально в соответствии с противопоказаниями.
Лечение острого панкреатита: препараты с обезболивающим эффектом
Для купирования болевых ощущений выписывают Мебеверин, Дицетел, Но-шпу, Одестон или Папаверин. Данные лекарства оказывают расслабляющее воздействие на мускулатуру и устраняют болевой синдром. На усмотрения врача могут быть назначены обезболивающие уколы.
Данные лекарства оказывают расслабляющее воздействие на мускулатуру и устраняют болевой синдром. На усмотрения врача могут быть назначены обезболивающие уколы.
Помимо вышеописанных медикаментозных средств обязательным является прием в комплексе витаминов, повышающих иммунную сопротивляемость организма и восполняющих дефицит полезных веществ.
Пожалуйста, оцените статью: Загрузка… Сохранить себе или поделиться с друзьями:Лечение панкреатита медикаментами: препараты выбора. Препараты для лечения поджелудочной железы: обзор лекарств
Простыми словами объяснить это можно так: происходит отравление тканей.
Чем занимается поджелудочная железа?
У нее две основные функции:
регулирует показатель сахара за счет выброса инсулина;
участвует в системе переработки еды в двенадцатиперстной кишке.
Панкреатит подразумевает сбой пищеварительной системы из-за нарушения работы поджелудочной железы, в результате чего происходит избыточное скопление ферментов в протоке. При таком раскладе железа выделяет сок, который разрушает ткани и нарушает ее функциональность. Соединяющая ткань начинает восполнять поврежденные клетки, но такой процесс только воссоздает объем, но не возрождает способность вырабатывать гормоны. Новые клетки не могут выполнять функции своих умерших предшественников. И в итоге пищеварение нагружает остальные клетки, вызывая острое железы.
При таком раскладе железа выделяет сок, который разрушает ткани и нарушает ее функциональность. Соединяющая ткань начинает восполнять поврежденные клетки, но такой процесс только воссоздает объем, но не возрождает способность вырабатывать гормоны. Новые клетки не могут выполнять функции своих умерших предшественников. И в итоге пищеварение нагружает остальные клетки, вызывая острое железы.
Панкреатит способен протекать в острой или хронической форме. Как и другие болезни, первые стадии характеризуются приступами. И лишь в случае отсутствия лечения они могут перетечь в хроническую форму.
Причины появления панкреатита
Как и большинство болезней, этот недуг могут вызвать несколько причин, одна из них или 2-3 в комплексе. Вот список самых распространенных:
чрезмерное употребление спиртных напитков или алкогольное отравление;
желчнокаменная болезнь;
сбой обмена веществ;
лекарственная интоксикация;
травмы в области живота или оперативное вмешательство;
заболевание сосудов;
инфекции.
Методы лечения
Способов избавиться от этого недуга несколько. Все зависит от признаков, резкости проявления и текущих заболеваний. К хирургической операции прибегают редко, только в том случае, если были обнаружены гнойные спайки в железах. Если оперативно не вмешаться в такую ситуацию, человек умрет от заражения крови. Существует множество способов предупредить или вылечить заболевание. В таком деле, как лечение панкреатита, препараты играют основную роль. Но не стоит забывать и о народной медицине. Врачи ведущих клиник считают, что быстрое и эффективное лечение панкреатита в любой форме – это воздержание от пищи. Голод многократно снижает выработку ферментов, тем самым отравляющее воздействие на поджелудочную железу тоже сводится к минимуму.
Обследования и незамедлительные меры при панкреатите
Развитие современной медицины позволило сделать лечение данной болезни быстрым и эффективным. Современные препараты разрешают отказаться от оперативного вмешательства и перейти к ступенчатой терапии. Перед тем как начать лечение, назначают обследование, общие анализы, ультразвуковое исследование.
Перед тем как начать лечение, назначают обследование, общие анализы, ультразвуковое исследование.
Больные поступают в диспансер в основном с острым проявлением болезни. Первым делом при назначении терапии начинают лечение антибактериальными и противовоспалительными препаратами. Если было выявлено гнойное образование, кроме основной терапии, проводят малоинвазивное вмешательство, противомикробную санацию гнойных образований.
Быстрый положительный эффект достигается путем подавления распада ферментов и выведения из крови токсинов, тормозящих выздоровление пациента.
Применение медикаментов
Препаратами состоит из применения следующих средств:
обезболивающие препараты – “Папаверин”, “Но-шпа”, “Кетарол”, “Анальгин”;
антацидные препараты – “Фосфалюгель”, “Алмагель”, “Ранитидин”;
ферментативные средства – “Креон”, “Панкреатин”, “Омез”.
Правильное для которого может выписать только врач, невозможно без антацидов и гистаминоблокаторов. Такие лекарства принимаются для охраны стенок желудочного тракта от разрушающего воздействия содержимого поджелудочной железы.
Такие лекарства принимаются для охраны стенок желудочного тракта от разрушающего воздействия содержимого поджелудочной железы.
Очень важно начать своевременное лечение панкреатита. Препараты для него чаще всего назначаются одни и те же: “Омепразол” и “Ранитидин”. Данные средства снижают кислотность и считаются более эффективными по сравнению с другими препаратами. Но при чрезмерном употреблении лекарств нарушается норма выделения сока и процесс расщепления еды в желудке.
В определенных ситуациях при лечении панкреатита принимаются препараты другой группы. Они служат заменителями натуральных ферментов – “Панкреатин”, “Креон 800”, “Креон 25000”. Лекарства снижают выработку поджелудочного сока, который разрушает ткани.
Неприятные эффекты от лечения
Для проведения правильной медикаментозной терапии нужна комплексная схема лечения, которая учитывает не только панкреатические изменения железы, но и побочные симптомы:
сбой работы выделения желчи в печени;
повышенную температуру;
чрезмерную утомляемость.

Хронический панкреатит: народное лечение
Если болезнь уже вышла из острой стадии, а лечение оказалось неэффективным, тогда вас ждет долгая терапия. Хронический панкреатит – это длительный воспалительный процесс в От данного недуга больше страдают женщины среднего возраста.
Хронический панкреатит может стать последствием таких заболеваний:
закупорка сосудов железы;
инфекции;
отравление тяжелыми металлами.
желчнокаменная болезнь;
При первых признаках болезни необходимо бить тревогу, но прежде чем начать лечение панкреатита у взрослых, препараты необходимо согласовать с врачом. При лечении травами рекомендуется внимательно выбирать рецепты.
В случае хронического панкреатита без природных трав невозможно было бы устранить болезнь одними таблетками. Существуют народные методы лечения панкреатита, которые помогают восстановить работу поджелудочной железы:
- применение настоя, локализующего воспалительный процесс в желчи;
- употребление здоровой пищи пять раз в день;
- строгое соблюдение диеты.

снимающие спазм;
нормализующие пищеварение;
обволакивающие и защищающие слизистую.
Для уменьшения количества желчи в одинаковых пропорциях смешивают бессмертник, ромашки, пижмы, спорыша и насыпают в литровую банку, заливают кипятком и оставляют на один-два часа в темном месте. Пьют отвар по одному стаканчику через полчаса после каждого приема пищи.
Для снятия воспалительного процесса используют подорожник. Он богат витаминами и природными гепатопротекторами. По одной ложке свежевыжатого сока принимают до еды в течение 30 дней. После перерыва в два-три месяца продолжают курс.
Для обезболивания необходимо взять измельченные листья одуванчика, пустырника, сушеницы, подорожника и тысячелетника. Две столовые ложки смеси добавляют в термос с кипятком и настаивают семь часов. Лекарство желательно выпивать ночью для снятия боли и снижения выработки желчи. В таком серьезном деле, как лечение панкреатита, препараты, выписанные врачом, – не единственное, на что можно положиться. Как видно, травы тоже могут сыграть существенную роль.
Как видно, травы тоже могут сыграть существенную роль.
Острый панкреатит: лечение
Препараты для этой стадии заболевания также назначаются исключительно специалистом. Спровоцировать болезнь в такой форме может хроническое течение недуга. Если вовремя не выявить заболевание и не вылечить, на железах могут образоваться псевдокисты. Вырастая и накапливая лишнюю жидкость, они начнут сдавливать другие органы, тем самым вызывая очень сильную боль.
Лечение в первую очередь начинают со строгой диеты, минимум неделю пьют лишь только минеральную воду и чай без сахара. Это делается для ликвидации провоцирующего фактора, вызывающего спазм поджелудочной железы.
От хронической стадии не сильно отличается и препараты и диета очень похожи. Основной упор делается на медикаменты:
замедляющие деятельность поджелудочной железы и снимающие спазм – “Фестал”, “Но-шпа”, “Мезим”, “Панкреатин”;
уменьшающие выработку панкреатического сока и снимающие воспаление тканей – “Дюспаталин”;
снижающие секрецию поджелудочного сока – “Пирензепин”;
замедляющие работу железы, за счет чего она успевает восстановиться – гормональный препарат “Октреотид”.
Но лучше любого лечения всегда была профилактика. Еще раз пересмотрите факторы, которые провоцируют появление этой болезни. Пусть некоторые из пунктов неподвластны нашей воле, но отказаться от алкоголя и питаться здоровой пищей может каждый. Это очень сильно сократит вероятность заболеть панкреатитом.
Панкреатит – это заболевание, для которого характерны воспалительные изменения в паренхиме поджелудочной железы. Оно может возникать в результате различных неблагоприятных факторов, но в любом случае патология требует обязательного лечения, так как может привести к тяжёлым осложнениям.
Как правило, заболевание начинают лечить медикаментозными средствами, какие лучше использовать – зависит от особенностей пациента и степени прогрессирования недуга. Сегодня существует масса препаратов, которые успешно борются с подобной проблемой. Но стоит отметить, что прежде чем лечить панкреатит, нужно полностью обследовать свой организм для постановки окончательного диагноза.
Лечение панкреатита медикаментами
Лечение данного заболевания направлено на устранение воспалительных изменений в органе, снятие болевого синдрома, нормализацию пищеварения, а также оно предполагает купирование сопутствующих симптомов. С этой целью используют лекарственные средства из группы холинолитиков, Н2-блокаторов, спазмолитиков, ферментов, в отдельных случаях необходимо применение антибактериальных препаратов. Как влияет каждое из вышеперечисленных средств – рассмотрим дальше более подробно.
С этой целью используют лекарственные средства из группы холинолитиков, Н2-блокаторов, спазмолитиков, ферментов, в отдельных случаях необходимо применение антибактериальных препаратов. Как влияет каждое из вышеперечисленных средств – рассмотрим дальше более подробно.
Н2-блокаторы
Медикаменты из этой группы способствуют снижению продукции соляной кислоты. Подобное влияние необходимо для того, чтобы разгрузить поджелудочную железу и предотвратить выделение её ферментов. Подобными свойствами обладают такие препараты: Фанитидин, Ранитидин, Омепразол, Низатидин.
- Ранитидин может вводиться внутримышечно, внутривенно, а также приниматься в виде таблеток. Последние пациент должен применять независимо от употребления продуктов питания дважды в сутки.
- Омепразол вводится раз в сутки путём внутривенного капельного введения, также может использоваться в виде капсул, таблеток.
Чтобы добиться выздоровления больного, препараты Н2-блокаторы необходимо использовать на протяжении 14 дней. Их прием может сопровождаться следующими побочными действиями:
Их прием может сопровождаться следующими побочными действиями:
- Аллергическими проявлениями.
- Выпадением волос.
- Тошнотой.
- Склонностью к запорам.
- Нарушением работы сердца.
- Снижением сексуального влечения, нарушением менструального цикла среди женщин.
Данные медикаменты нельзя использовать детям младше 12 лет, в период беременности, лактации, при нарушении функций печени.
Холинолитики
Медикаментозное лечение панкреатита предусматривает обязательное применение этих средств. Они способствуют нормализации функций пищеварительной системы, а также предотвращают воздействие ацетилхолина и холиномиметиков. К этому ряду относится:
- Платифиллин.
- Хлорозин.
- Метацин.
- Атропин.
- Спазмолитин.
Антацидные средства
Воспалительный процесс в поджелудочной железе нередко сопровождается патологией желудка, при которой происходит повышенное выделение соляной кислоты. С целью её нейтрализации, а также для образования защитного барьера на стенках органа показано применение антацидных препаратов. При панкреатите, как правило, используют невсасывающиеся медикаменты этой группы: Фосфалюгель, Маалокс, Алюмаг, Палмагель, Алтацид. В их составе присутствует гидроксид магния и алюминия, чем и обусловлено их положительное воздействие.
С целью её нейтрализации, а также для образования защитного барьера на стенках органа показано применение антацидных препаратов. При панкреатите, как правило, используют невсасывающиеся медикаменты этой группы: Фосфалюгель, Маалокс, Алюмаг, Палмагель, Алтацид. В их составе присутствует гидроксид магния и алюминия, чем и обусловлено их положительное воздействие.
Эти препараты нельзя применять при почечной недостаточности, дефиците фосфора, при кормлении грудью, в период беременности. Кроме того, эти таблетки нельзя применять людям, которые не переносят галактозу и фруктозу.
Что касается препарата Фосфалюгель, то он может назначаться детям с полугода, также разрешён кормящим мамочкам и беременным женщинам. Практически не сопровождается побочными эффектами. Иногда может вызвать развитие запора.
Спазмолитики
В большинстве случаев заболевание сопровождается болевым синдромом. Для его купирования назначаются спазмолитики. Они способствуют устранению спазма гладкой мускулатуры. Кроме того, эти лекарства используют для лечения панкреатита и холецистита, ведь эти патологии зачастую развиваются вместе. К этой группе относятся: Риабал, Но-шпа, Спазмолин, Спазмомен, Дротаверин, Папаверин и другие. Последний может вызвать побочные эффекты со стороны работы сердечнососудистой системы.
Кроме того, эти лекарства используют для лечения панкреатита и холецистита, ведь эти патологии зачастую развиваются вместе. К этой группе относятся: Риабал, Но-шпа, Спазмолин, Спазмомен, Дротаверин, Папаверин и другие. Последний может вызвать побочные эффекты со стороны работы сердечнососудистой системы.
Ферментные препараты
К ряду ферментов относятся такие препараты как Панзинорм, Фестал, Креон, Энзистал, Панкурмен, Панкреатин. В их составе присутствуют липаза, амилаза и протеаза. Подобный состав медикаментов обеспечивает следующее влияние на состояние здоровья пациента:
- Борется с диспепсическими расстройствами.
- Нормализует переваривание пищи.
- Способствует правильному всасыванию органических веществ.
- Облегчает работу поджелудочной железы.
Когда необходимы антибактериальные средства?
Начинают лечение заболевания с приёма вышеперечисленных препаратов. Если же при соблюдении всех назначений врача на протяжении нескольких дней облегчение не наступает, специалист может прописать антибиотики. Также эти лекарства при панкреатите применяют в случаях развития осложнений болезни. Они способствуют уничтожению бактериальной микрофлоры, которая может служить источником инфекции.
Также эти лекарства при панкреатите применяют в случаях развития осложнений болезни. Они способствуют уничтожению бактериальной микрофлоры, которая может служить источником инфекции.
Курс лечения данными медикаментами определяется в зависимости от тяжести патологии. В большинстве случаев он составляет 5 – 7 дней. Чтобы получить максимально быстрый эффект, антибактериальные средства вводят парентерально. Если заболевание протекает в тяжёлой форме, может применяться комбинированная терапия, которая предусматривает введение лекарства инъекционно, а также приём внутрь.
Вместе с антибактериальными средствами показано применение пробиотиков, так как под влиянием первых гибнет абсолютно вся микрофлора кишечника, что способно спровоцировать расстройство работы пищеварительного канала. С этой целью назначают Йогурт, Линекс. Курс зависит от длительности лечения антибиотиками. В виде таблеток часто применяют такие средства:
- Амоксиклав. Оказывает противомикробное действие в кротчайшие сроки.
 Применяется 1 раз в сутки.
Применяется 1 раз в сутки. - Азитромицин. Имеет широкий спектр действия. Курс применения может составлять до 10 дней. Таблетки необходимо пить дважды в сутки после приёма пищи.
- Сумамед. Данное лекарственное средство широко используется для лечения панкреатита, так как даёт хороший эффект. Препарат принимается 2 раза в день.
- Абактал. Также даёт отличный эффект от лечения. Употреблять его нужно 1 раз в день, курс составляет 3 – 5 суток.
Для внутримышечного введения в большинстве случаев назначают такие средства:
- Доксициклин.
- Ампиокс.
- Цефтриаксон.
- Цефатоксим.
Любые антибактериальные средства должны использоваться исключительно по назначению врача и под его обязательным контролем, так как неправильное применение данных медикаментов способно ещё больше усугубить ситуацию.
Чтобы медикаментозное лечение принесло необходимый результат, пациенту нужно соблюдать строгую диету, которая предполагает отказ от жирных, жареных, острых блюд.
Лечение панкреатита лекарственными препаратами предполагает использование различных групп медикаментов. Подобный подход способен полностью избавить пациента от проблем с поджелудочной железой.
Лечение панкреатита медикаментами необходимо при острой форме заболевания или обострении хронической.
Панкреатит – это патология поджелудочной железы, развивающаяся по причине нарушений оттока панкреатических ферментов из нее. Застой может быть вызван желчными камнями, блокирующими проток поджелудочной железы, злокачественной или доброкачественной опухолью, кистой, травмой брюшной полости. В результате панкреатические соки начинают переваривать ткани поджелудочной железы, что приводит к их некротизации, может стать причиной кровотечения или абсцесса.
Если вовремя не провести адекватное лечение панкреатита, наступает смерть пациента.
Если идет острый воспалительный процесс поджелудочной железы, пациент должен быть срочно госпитализирован. Это обязательное условие лечения, так как поражения железы могут привести к нарушению жизненно важных функций человека и летальному исходу.
Схема лечения при панкреатите поджелудочной железы основывается на трех принципах:
- голод;
- холод;
- покой.
Параллельно необходимо принимать медикаменты, которые помогут снять воспаление поджелудочной железы. Какие лекарства принимать при панкреатите в острой стадии, определяет врач-гастроэнтеролог, учитывая состояние пациента, его физиологические особенности и степень поражения внутренних органов.
Сразу же следует оговориться: лечить панкреатит нужно комплексно, какое-то одно средство от панкреатита не поможет снять воспаление и восстановить функции поджелудочной железы.
Используются лекарственные препараты таких групп в различных комбинациях:
- Средства спазмолитического и анальгезирующего действия в таблетках или инъекциях.
- Антациды в аналогичных фармацевтических формах.
- Ферментные препараты при панкреатите, а в некоторых случаях – антиферментные.
- Н2-блокаторы гистаминных рецепторов.
- Препараты седативного действия.

Если при воспалении поджелудочной железы были затронуты клетки, которые отвечают за выработку гормона инсулина, то комбинацию стандартных препаратов при панкреатите нужно дополнять инсулиновыми препаратами. Оптимальное лекарство подбирает в этом случае врач-эндокринолог.
Большая часть лекарств от панкреатита для взрослых отпускается в аптеках совершенно свободно, без рецепта врача. Но самостоятельно принимать (даже, на первый взгляд, безобидные) препараты категорически воспрещено. Это может привести к непредсказуемым последствиям. Если воспалилась поджелудочная железа, только лекарствами ее не вылечить. Необходимо соблюдать диету и вести правильный образ жизни.
И главное здесь – не вносить свои коррективы в медикаментозное лечение панкреатита.
Чем снимать боли при панкреатите
Если начинает воспаляться поджелудочная железа, пациент испытывает очень сильные боли в левом подреберье. Ощущение может быть просто непереносимым, вплоть до того, что человек не может спокойно стоять, сидеть, разговаривать и даже дышать. Иногда боли иррадиируют в область спины между лопатками или поясницу – зависит от того, какой участок поджелудочной железы страдает.
Чем лучше снимать болевой синдром при лечении панкреатита?
- Препараты из группы нестероидных противовоспалительных – Парацетамол, Ибупрофен и т. д.
- Сильнодействующие анальгетики – Баралгин, Анальгин и пр.
Любые препараты при панкреатите следует принимать с большой осторожностью, чтобы не вызвать еще большее раздражение желудка, поджелудочной железы и кишечника.
Следующие после болей типичные симптомы панкреатита – это тошнота, кишечные расстройства и рвота. Принятый препарат может попросту не успеть усвоиться. Поэтому если пациент доставлен в больницу в тяжелом состоянии, с неукротимой рвотой или диареей, все медикаменты, и обезболивающие в том числе, вводятся внутривенно.
При очень выраженных болях в условиях стационара пациенту могут ввести внутримышечно обезболивающие наркотические препараты для лечения обострившегося панкреатита, которые приобрести в аптеке без рецепта врача невозможно.
Это:
- Промедол;
- их аналоги.
Любые средства, снимающие боль при панкреатите, запрещено принимать на регулярной основе, даже если они не наркотические и не вызывают привыкания, как указывает инструкция по применению.
Пациент всегда должен понимать, что даже самый хороший и качественный препарат, эффективно снимающий боль, не решает проблему. Боли вызваны тем, что поджелудочная железа начинает сама себя переваривать. Ее ферменты, которые должны были попасть сначала в проток, а оттуда – в двенадцатиперстную кишку, вместо этого скапливаются в ней самой, разъедают ее ткани и вместе с кровотоком разносятся по всему организму. Это означают сильнейшую интоксикацию всех внутренних органов – почек, печени, легких. Поэтому при воспалении поджелудочной железы лечение заключается не в том, чтобы снять боль, а в том, чтобы устранить ее причину и предупредить возможные осложнения. Сделать это могут только квалифицированные врачи в условиях стационара.
Спазмолитики – это медикаменты, которые воздействуют на гладкую мускулатуру и тем самым способствуют оттоку панкреатических ферментов. При обострении заболевания их вводят внутривенно или внутримышечно. В дальнейшем, при лечении хронического панкреатита, эти препараты можно принимать в таблетках. Обычно используются Папаверин, Но-шпа, Атропин.
Какое действие оказывают эти препараты при панкреатите?
Они расслабляют запирательные мышцы поджелудочной железы, и панкреатический сок получает выход в проток. Таким образом, спазмолитики не просто снимают боль, а частично устраняют причину боли. Человек, принимающий эти лекарственные средства, быстро ощутит, как уходит боль, уменьшаются тошнота и изжога. Через время останавливается рвота, и самочувствие пациента значительно улучшается.
Если боли очень выраженные, то практикуется комбинированное введение анальгетиков и спазмолитиков. Обычно это Анальгин и Но-шпа, или Баралгин и Папаверин. Бригада «скорой помощи» может ввести Платифиллин. Это очень серьезный медикамент, который можно приобрести в аптеке, только предъявив рецепт врача. Платифиллин опасен целым рядом побочных эффектов, один из которых – расстройства психического характера. Поэтому лучше все-таки предпочесть внутримышечную инъекцию Но-шпы.
Медикаментозные средства спазмолитического действия, как и анальгетики, не лечат панкреатит как таковой, а лишь устраняют его неприятные проявления. Выпитый или введенный в мышцу препарат начинает действовать уже спустя 7-10 минут, но и эффективность его сохраняется недолго. А потом боли вернутся вновь и задуматься о серьезном, комплексном лечении все равно придется.
Антациды и ферментативные средства
Что такое антациды? Это лекарственные средства, основное действие которых – нормализация уровня кислотности желудочного сока. Их рекомендуют пить при панкреатите, чтобы нейтрализовать желудочные кислоты. Это позволит снизить нагрузку на поджелудочную железу и улучшить самочувствие пациента.
Самые популярные средства:
- Маалокс;
- Гастрацид;
- Алюмаг.
К сожалению, все эти препараты не обладают длительным действием. Они действительно изменяют уровень кислотности в желудке, но ненадолго. И практически никак не влияют на работу непосредственно поджелудочной железы.
Добиться стойкого эффекта можно только с помощью ферментных или антиферментных средств. И препарат, и их дозировку подбирает только врач. Очень важна очередность приема лекарственных средств различного действия при панкреатите. Антациды активно взаимодействуют почти со всеми лекарствами, уменьшая их действие. Поэтому промежуток между приемом антацидов и других препаратов должен составлять не менее 2-2,5 часов.
Прием ферментов оказывает такое действие:
- способствует расщеплению белков, жиров и углеводов;
- уменьшает рези в желудке, метеоризм и вздутие;
- стимулирует всасывание и усваивание полезных веществ из принимаемой пищи;
- разгружает поджелудочную железу и тем самым улучшают самочувствие пациента.
Ферменты эффективны при длительном курсе лечения. Врач наблюдает, насколько эффективен принимаемый препарат, или оставляет его в программе терапии, или заменяет аналогом. Очень важно: таблетка должна быть принята обязательно во время еды или сразу после. Если принять ферменты на голодный желудок, поджелудочная железа может воспалиться еще сильнее.
Качественные, хорошие ферментативные препараты содержат вытяжку из поджелудочной железы крупного рогатого скота, идентичную веществу, которое вырабатывает поджелудочная железа человека, – панкреатин. Панкреатин способствует расщеплению продуктов до тех составляющих, которые без труда всасываются кишечником и желудком и максимально усваиваются организмом человека.
В состав панкреатина входят:
- Липаза – этот элемент помогает расщеплять жиры.
- Амилаза – стимулирует усваивание углеводов любого вида.
- Протеаза – способствует усваиванию белков.
Получая панкреатин в достаточном количестве, организм может компенсировать недостаточность поджелудочной железы. Все вещества, поступающие с продуктами питания, хорошо перевариваются, и пациент не страдает от истощения или авитаминоза. В списке назначений при панкреатите можно встретить препараты Фестал, Мезим, Креон, Панкреатин, Панзинорм, Дигестал.
Все эти медикаменты относятся к ферментативным, но имеют различные составы и механизмы действия, поэтому только врач может сказать, чем лечить панкреатит будет лучше в каждом отдельном случае. Оцениваются, прежде всего, степень поражения поджелудочной железы и нарушения работы других органов – желчного пузыря, печени, кишечника.
Что касается антиферментных препаратов, то они вводятся в условиях стационара внутримышечно или внутривенно в первые сутки после острого приступа болезни. Эти средства нужны, чтобы не допустить еще большего воспаления тканей при выбросе панкреатитного секрета.
Прочие медикаменты при воспалении поджелудочной железы
Когда панкреатит обостряется, временно нужно притормозить выработку желудочного сока. Но только временно, потом, наоборот, нужно ее стимулировать, чтобы пищеварительная система смогла работать нормально.
Краткосрочно назначаются такие препараты:
- Циметидин;
- Низатидин.
При остром воспалительном процессе могут использоваться лекарственные средства из группы противовоспалительных нестероидных. Однако их прием нежелателен, так как можно упустить истинную динамику болезни. Кроме того, эти лекарства имеют ряд побочных эффектов и не назначаются курсом более 7-10 дней. Это Диклофенак, Найз, Нимесулид, Ибупрофен.
Антибиотики назначаются при панкреатите очень редко, только после получения результатов всех анализов и исследований.
Показаниями к приему антибактериальных препаратов являются:
- Застой желчи.
- Выявление инфекции бактериальной природы.
- Повреждение протока поджелудочной железы.
- Холангит, панкреонекроз или образование кисты.
В больнице антибиотики могут использоваться в форме инъекций, если врач посчитает, что состояние пациента критическое и нужна срочная помощь. При лечении хронических инфекций и патологий возможен пероральный прием. Назначаются, как правило, Амоксиклав, Цефотаксим, Ампициллин, Абактал, Ванкомицин.
Если ткани поджелудочной железы начинают некротизироваться, то бактериальная инфекция часто сопровождается грибковой. Лечение в этом случае сложное и длительное, так как нужно одновременно подавить патогенную микрофлору, но не затронуть полезную, чтобы организм мог бороться с грибком.
Как правильно принимать медикаменты
При панкреатите важно не только правильно подобрать лекарственные средства, но и принимать их по определенной схеме.
Существуют свои особенности приема препаратов при остром или хроническом воспалении поджелудочной железы.
Правила таковы:
- Так, средства, снимающие боль, можно выпить когда угодно, если того требует состояние пациента.
- Ферменты допустимо вводить только во время приема пищи.
- Антибиотики желательно принимать после него.
Таблетки запиваются только чистой водой без газа, ни молоком, ни чаем и соком. Тем более нельзя сочетать медикаменты со спиртным. Это вообще табу не только на время лечения, но и в период ремиссии.
Продолжительность курса устанавливает врач – прерывать при панкреатите медикаментозное лечение раньше срока нельзя. Только тогда лечение будет успешным и не возникнет рецидив. С особой ответственностью должны относиться к медикаментозной терапии беременные и те пациенты, у которых сочетается целый ряд хронических заболеваний.
Таблетки и инъекции подбираются так, чтобы одно средство не подавляло действие другого, в то же время не наносился большой вред другим органам.
Если, несмотря на прием медикаментов и соблюдение всех рекомендаций, состояние пациента ухудшилось, поднимается температура, отмечается вздутие живота, сильные рвота или диарея, посинение кожных покровов живота, следует немедленно вызывать «скорую помощь». Без госпитализации и срочной медицинской помощи пациент может погибнуть.
Панкреатит серьезное заболевание, приводящее к . Чтобы избежать формирования тяжелых осложнений, способных иногда приводить к смерти больного, нужно сразу обращаться за помощью к врачам и начинать терапию.
Сегодня используются для лечения панкреатита различные медикаменты, способные облегчить самочувствие больного и не допустить развитие неблагоприятных последствий.
Прежде чем начать лечение патологии, врачом будет составлена схема лечения, зависящая от тяжести панкреатита и самочувствия пациента. Необходимо понимать, что классических мероприятий, когда наблюдается воспаление поджелудочной железы, не существует. Лекарства при панкреатите подбираются в индивидуально.
Прежде всего, в острый период панкреатита необходим постельный режим. Потому если наблюдается тяжелая форма острого течения заболевания, то лечение панкреатита проходит только в условиях стационара. Это является обязательным условием, поскольку воспалительные изменения железы способны привести к нарушению важных функций необходимых для жизни.
В течение 3-х суток нужно лишь пить жидкость, чтобы не допустить обезвоживания организма, а также вывести токсичные вещества из организма.
Из препаратов при остром средства, препараты обезболивающие и снимающие спазмы, антибиотики. А ферментные лекарства, пилюли и инъекции, которые снимают спазмы, противовоспалительные препараты помогут для лечения хронического панкреатита. Помимо этого в обязательном порядке применяют средства, которые оказывают желчегонный, обволакивающий эффект, а также потребуется терапия витаминами.
Применяемые препараты
При появлении симптомов болезни, лечение у взрослых изначально проводится терапевтом с назначением ряда анализов. Перед использованием лекарства от панкреатита посетите гастроэнтеролога, который пропишет курс лечения, подходящее больному пациенту по всем показателям. Медикаментозное лечение препаратами поможет улучшить самочувствие, но избавиться средствами от болезни не получиться. Благодаря диетологу будет определен режим питания и назначена диета.
Применяются такие группы препаратов для лечения панкреатита:
- Лекарства в таблетках, инъекциях, которые избавляют от спазмов и оказывают анальгезирующее воздействие.
- Антациды.
- Ферментные и антиферментные средства.
- h3-блокаторы гистаминовых рецепторов.
- Группы препаратов седативного воздействия.
Конкретные препараты, количество и доза регулируются доктором. Это связано с тем, что при медикаментозном запрещено принимать многие лекарственные средства.
Если при поражении железы были вовлечены клетки, отвечающие за выработку гормона инсулина, к пакету стандартных средств, включают инсулиновые средства. Оптимальный медикамент подбирается эндокринологом.
Подобное лечение становится причиной развития непредсказуемых последствий. Когда воспаляется железа, одними препаратами ее вылечить не выйдет. Требуется , придерживаться правильного образа жизни.
Важно, при приеме медикаментов следовать тех предписаний, что прописаны в инструкции по применению.
Ферменты
Чтобы изменить показатель кислотности в желудке и наладить работу железы можно с помощью ферментных и антиферментных препаратов. Лекарственные препараты, их дозировка подбираются исключительно врачом.
В данном случае важен поочередный прием средств разного воздействия.
Влияет на организм следующим образом:
- помогает расщепиться белкам, жирам и углеводам;
- метеоризм, вздутие и рези в желудке уменьшаются;
- стимулирует абсорбцию и усвояемость полезных элементов из употребляемых продуктов;
- освобождает железу, улучшая состояние пациента.
Ферменты действенны, если терапия панкреатита будет длительной. Доктор ведет наблюдение, за эффективностью принимаемого средства, оставляя его для последующего приема либо заменяет аналогичным.
Важно принимать ферментные лекарства при панкреатите поджелудочной железы во время еды, либо сразу после. Если выбить таблетки натощак, возможно еще большее воспаление органа.
В качественных, хороших ферментативных препаратах содержится вытяжка из железы крупного рогатого скота, которая идентична веществу, вырабатываемому человеческой железой – панкреатин. Он помогает расщепиться продуктам до тех молекул, которые кишечник и желудок поглотят и усвоит организм.
Если получать панкреатин в достаточном количестве, то организм возместит нехватку поджелудочной железы. Все элементы, которые поступают с продуктами питания, имеют хорошую усвояемость, и больной не сталкивается с проблемой истощения и авитаминозом.
Назначают при лечении панкреатита такие таблетки:
- Фестал.
- Мезим.
- Креон.
- Панкреатин.
- Панзинорм.
- Дигестал.
Данные препараты являются ферментативными. У них различные механизмы влияния и составы, потому специалист укажет, какой лучше принимать для лечения панкреатита в конкретной ситуации:
- степень воспаления железы;
- изменения деятельности иных органов – желчный пузырь, кишечник, печень.
При использовании антиферментных средств, для лечения:
- снижается интоксикация организма;
- уменьшается болевой синдром;
- улучшается самочувствие пациента;
- снижается угроза летального исхода;
- блокируется развитие отека и некроз тканей.
Выделяют следующие препараты этой группы:
- Гордокс.
- Контрикал.
- Трасилол.
- Трасколан.
- Ингитрил.
Антиферментные препараты вводятся в стационаре внутрь мышцы или в вену на первых сутках после приступа болезни. Такие медикаменты необходимы, чтобы приостановить еще более воспаление тканей в результате выброса панкреатического секрета.
Чага
Для лечения заболеваний, поскольку они натуральные и не оказывают побочных эффектов и решить проблему. Однако прием также невозможен без одобрения врача.
Одним из народных средств является чага. Ее разрешено использовать при лечении заболеваний ЖКТ, поджелудочной железы только после постановки диагноза и следуя рекомендациям врача.
Лечить панкреатит чагой можно, когда окончится острый этап болезни, поскольку обострение способно увеличивать секрецию железы.
Чагу для железы зачастую назначают в качестве чая. Благодаря этому средству можно:
- устранить признаки болезни – тошноту, головокружение;
- восстановить слизистые ткани;
- вывести токсины из организма;
- увеличить гемоглобин;
- предотвратить рост болезнетворных бактерий.
В сетях аптек продают препараты на основе гриба в виде пилюль либо концентрированного экстракта. Чага встречается в составе отдельных средств, для лечения панкреатита гомеопатического спектра, Бадах. Однако большей эффективностью обладает натуральный сделанный настой.
Чтобы сделать настой вымывается чага и отправляется в кипяток. Так гриб находится несколько часов. Затем его измельчают, а выстоянной подогретой водой гриб заливают снова. Хранить такое средство не более 4 дней. Лечение напитком проводится в 3 приема по 200 граммов на день.
Если принимать лекарство во время обострения возникают осложнения. Чагу не допускают к приему при панкреатите, если присутствует язва в кишечнике, желудке.
Инновация в отечественной фармацевтике
При обострении панкреатита, необходимо проводить временное торможение выработки желудочного сока. Эта процедура временная, затем потребуется ее стимулировать, для нормальной работы системы пищеварения.
Лекарства при обострении панкреатита:
- Ранитидин.
- Циметидин.
- Низатидин.
Группа противовоспалительных препаратов потребуется в случае острого воспаления. Но принимать такие таблетки при панкреатите нежелательно, поскольку возможно упущение истинной динамики заболевания.
Помимо этого средства имеют побочные проявления и не назначаются больше чем на 10 суток:
- Диклофенак.
- Найз.
- Ибупрофен.
- Нимесулид.
Для абсорбции и вывода из организма вредоносных элементов, в борьбе с болезнетворной микрофлорой кишечника назначают препарат с широким спектром воздействия Полифепан. Лекарство на натуральной основе. Его аналогом выступает Энтеросгель. Его часто используют для лечения панкреатита. Лекарство пьют вместе с иными средствами при лечении болезни, которые связаны с отравлением.
При поражении кишечника, дисбактериозе, аллергическом проявлении поможет Аципол. Он приведет кишечник в норму.
Улучшит пищеварение прописывают Иберогаст. Препарат также тонизирует и оказывает желчегонное действие.
К одному из лекарств на растительной основе, который лечит желчевыводящие пути, относится Фламин. Это средство является холекинетическим, оно снимает спазмы и воспаление, помогает выработать необходимый объем желчи. Из аналогичных препаратов выделяют:
- Гепазин;
- Хепель Н.
Перед тем как приступать к лечению, необходимо понимать, какие пить таблетки при панкреатите, отчего они помогают, знать о возможных побочных явлениях, противопоказаниях. Потому важно по этому поводу проконсультироваться с доктором.
Полезный отвар
Чтобы поддерживать работу железы при хроническом развитии панкреатита, используются народные средства, включающие в данном случае травы и отвары из них. . Благотворно влияет на функцию секреции желудочного сока – петрушка, корневая ее часть.
Отвары бывают комплексные, включать несколько видов трав. Главное при лечении следовать дозе и рецептуре.
В восстановительный период приготавливается отвар из зеленого лука с петрушкой, зверобоем и мятой. При остром воспалении используется мята с тысячелистником, сушеницей.
Желчегонные препараты , оказывающими более мягкое действие. Подбираются травы индивидуально.
- Корень лопуха, цикория.
- Плоды шиповника.
- Куркума.
- Кукурузные рыльца.
- Алоэ.
Используя травы или сборы исключается присутствие аллергии на них.
При интенсивной боли
Когда воспаляется железа, у больного появляются сильные болевые ощущения с левого бока под ребрами, в верхней части живота. Дискомфорт бывает настолько невыносимым, что невозможно стоять, сидеть, говорить, дышать. Бывает, что болевой синдром затрагивает спину, между лопатками, поясницу. Эти зоны указывают на то, какой участок органа поражен.
Для устранения болевого синдрома используются такие препараты при панкреатите:
- нестероидная группа – Парацетамол, Ибупрофен;
- анальгетики сильного действия – Баралгин, Анальгин.
Чтобы снять боль при невыносимых ее проявлениях, прописывают наркотические анальгетики, которые вводятся внутримышечно:
- Бупренорфин.
- Трамадол.
Обезболивающие таблетки запрещено употреблять постоянно, даже при отсутствии в них наркотических веществ и они не вызывают привычку.
Обезболивающие препараты спазмолитики используются, когда необходимо снять спазмы и облегчить ферментные выведения:
- Дротаверин.
- Спазмалгон.
- Но-шпа.
- Спазмол.
- Риабал.
Эти медикаменты при болезни оказывают следующее влияние:
- облегчают состояние пациента благодаря устранению боли;
- снижают нагрузку на орган, способствуя улучшению выхода эффектов пищеварения.
Помогут победить болезнь средства, которые предупреждают либо ослабляют действие ацетилхолина, холиномиметических средств.
Медикаменты препятствуют патологическим импульсам в нервных узлах и мозгу.
Рабочий ход ЖКТ приходит в норму:
- Атропин.
- Хлорохин.
- Спазмолитин.
- Платифиллин.
Лекарство для защиты клеток
Для восстановления клеток печени используются таблетки от панкреатита как: Эссенциале Форте. Употребляется средство параллельно с назначением лекарств-антибиотиков.
Назначают лекарство по 1 капсуле 3 раза в сутки в период еды. Применяется средство курсами, по назначению врача Фосфолипиды, которые присутствуют в составе, направлены, чтобы восстановить и защитить клетки. Хорошо влияет на метаболизм, имеет мало побочных проявлений. Передозировка не несет угрозу здоровью.
Лекарства при панкреатите у взрослых имеют следующие аналоги:
- Резалют про;
- Эссливер Форте.
Когда в ход идут антибиотики
Назначаются крайне редко и только после наличия результатов полного обследования.
В больницах антибактериальная терапия используется в форме уколов, если доктор увидит, что ситуация критическая и пациенту нужно срочная помощь. Антибиотики при остром течении панкреатита назначаются, чтобы снять воспаление, максимально разгрузить орган:
- Доксициклин.
- Цефуроксим.
Лечение хронического течения болезни, возможно пероральным использованием антибиотиков:
- Амоксиклав.
- Цефотаксим.
- Ампициллин.
- Абактал.
- Ванкомицин.
Важно помнить, что медикаменты принимаются только после назначения врача.
Симптомы панкреатита чаще всего наблюдаются у взрослых людей, перешагнувших тридцатилетний порог. В группу риска входят мужчины, злоупотребляющие спиртным. Огромное значение при терапии этой болезни имеют правильно подобранные лекарства.
Симптомы воспаления поджелудочной железы
Главным симптомом панкреатита у взрослого человека является болевой синдром. Он опоясывает все тело, включая живот и спину. Тошнота, слабость, сонливость сочетаются с мучительной рвотой, которая не приносит облегчения.
У 50% пациентов снижается вес. У 15% наблюдается диарея. Во время пальпации обнаруживаются признаки пареза, вздутия кишечника. Когда патология прогрессирует, появляется симптоматика раздражения брюшной полости, а также близлежащих органов.
Кожные покровы бледнеют, наблюдаются признаки цианоза. Это характерно для острой формы болезни. В зоне пупка появляется синюшность, лицо больного краснеет.
Лечение панкреатита у взрослых
Обнаружив один или несколько признаков воспаления поджелудочной железы, необходимо незамедлительно обратиться к терапевту. Он направит на сдачу анализов. После этого больной должен посетить кабинет гастроэнтеролога. Врач прописывает пациенту необходимые лекарства. Затем нужно обратиться к диетологу. Специалист определит режим питания. Также больному назначается диета.
Как лечится панкреатит у взрослых? Терапия предполагает:
- Купирование боли.
- Устранение воспалений в пораженном органе.
- Ликвидацию симптомов недостаточности железы.
- Купирование воспалений в близлежащих органах.
- Предотвращение осложнений.
Для лечения этого заболевания назначаются антиферментные медикаменты, анальгетики, спазмолитики, h3–блокаторы, антациды. Наилучший эффект достигается в первое время применения лекарственных средств. Мощнейшим воздействием обладают медикаменты, имеющие в своем составе полипептид апротинин. Одновременно проводятся процедуры, очищающие организм от панкреатических ферментов.
Препараты для устранения боли
Когда пациент жалуется на мучительные болевые ощущения, врач прописывает ему Парацетамол, Анальгин, Баралгин. Эти лекарства назначаются как взрослым, так и детям. Если человек жалуется на невыносимую боль, ему назначается применение наркотических анальгетиков. Прописываются такие таблетки при панкреатите у взрослых, как Бупренорфин, Трамадол. Иногда врач рекомендует принимать Стелазин, Мелипрамин. Пить эти лекарства необходимо осторожно, поскольку существует риск привыкания.
Лечение ферментами и антиферментными средствами
При отеке поджелудочной у взрослых назначаются антиферментные лекарства от панкреатита. Практикуется внутривенное капельное введение. Пациентам рекомендован прием Апротинина, Контрикала. Применяются эти лекарства дважды в сутки. Продолжительность терапевтического курса для взрослых варьируется от 1 до 1,5 недели. Не назначаются эти медикаменты только при выявлении индивидуальной непереносимости.
Для лечения панкреатита у взрослых прописываются следующие лекарства:
- Ферестал;
- Энзим форте;
- Фестал;
- Креон 25000;
- Панкреатин;
- Мезим;
- Креон 8000.
Действующие вещества и состав этих таблеток совпадают. Ферменты при панкреатите необходимо пить сразу после приема пищи. Дозировка устанавливается врачом в зависимости от уровня дефицита липазы. Если присутствуют признаки стеатореи, пациенту рекомендован прием витаминов В, А, Е, Д, К.
Лечение панкреатита спазмолитическими препаратами
При остром панкреатите у взрослых назначаются холино и спазмолитические лекарства
- Бускопан.
- Анальгин.
- Парацетамол.
- Баралгин.
- Но-Шпа.
Эти медикаменты хорошо снимают спазмы. Если человек мучается очень сильными болями, то ему назначаются не таблетированные препараты, а инъекции.
Все препараты для лечения панкреатита у взрослых должны приниматься только в соответствии с рекомендациями врача.
Применение дополнительных медикаментов
Лечение этого заболевания предполагает назначение Н2-блокаторов. Больному рекомендован прием Ранитидина, Фамотидина. При внешнесекреторной недостаточности пациенту прописывается применение антацидов. Они способствуют нормализации функционирования 12-перстной кишки. Лечение при остром панкреатите у взрослых предполагает прием Фосфалюгеля, Алмагеля.
Большую пользу здоровью приносит употребление обволакивающих, желчегонных, седативных медикаментов. Также рекомендуется пить гормоны, кальций.
С целью профилактики панкреатита у взрослых назначается прием Асентры, Галстены, Гордокса, Дигестала, Дюспаталина, Йогулакта, Креона 10000, Пангрола 10000, Панкреофлата, Реополиглюкина, Хофитола.
Терапия хронического панкреатита
Главной терапевтической целью при панкреатите является купирование болевого синдрома, а также избегание дальнейшего обострения в железе. Нормализуется способность принимать и переваривать пищу.
Если у пациента не имеется серьезных осложнений, он выписывается из стационара. При сильном болевом синдроме назначаются анальгетики. При хроническом панкреатите человек обязуется следовать диете. Можно есть только те продукты, которые практически не содержат жиров. Нельзя пить алкоголь. Иногда при хроническом панкреатите у взрослых прописываются дополнительные лекарства. Пациенту рекомендован прием ферментов поджелудочной.
Если орган не вырабатывает нормальное количество инсулина, врач назначает ему соответствующие инъекции.
Комментарий о прогнозе
Если больной обратился за врачебной помощью вовремя, то вскоре наступает выздоровление, а железа возвращается к нормальному функционированию. Угрожающие жизни проявления наблюдаются примерно у 5-10% пациентов. Наиболее серьезным осложнением является диабет. У некоторых больных появляются признаки почечной недостаточности, повреждения головного мозга.
Хронический панкреатит не вылечивается полностью. Повреждение органа представляет собой непрерывный процесс. Это часто становится причиной возникновения кровотечений, псевдокист или рака.
Антиферментные лекарственные препараты, применяемые для лечения острого панкреатита – Справочник лекарств
Антиферментные препараты (ингибиторы протеолиза) – это группа лекарственных средств, которые блокируют действие пищеварительных ферментов поджелудочной железы и используются для лечения острого панкреатита.
Поджелудочная железа является органом смешанной секреции. Эндокринная ее часть, которая представлена островками Лангерганса, продуцирует прямо в кровь гормоны, влияющие на обмен углеводов – инсулин и глюкагон. Экзокринная же часть поджелудочной железы вырабатывает критично необходимый для нормального пищеварения панкреатический сок, который выделяется через проток в просвет двенадцатиперстной кишки.
Панкреатический сок представляет собой смесь ферментов, способных расщеплять все основные компоненты пищи – белки, жиры и углеводы – до простейших соединений, которые смогут далее всосаться в тонком кишечнике.
Ферменты поджелудочной железы (панкреатические ферменты) обладают чрезвычайно мощной «переваривающей» силой, поэтому поджелудочная железа синтезирует их в исходно неактивной (зимогенной) форме. В нормальных условиях переход панкреатических ферментов в активную форму происходит только в просвете двенадцатиперстной кишки, при взаимодействии с компонентами пищи.
В случае нарушения оттока панкреатического сока, например, при острых заболеваниях поджелудочной железы, ферменты активируются прямо в ткани самой железы. Это, в свою очередь приводит к так называемому аутолизу – «самоперевариванию» поджелудочной железы и ферментативному «расплавлению» окружающих тканей.
Аутолиз поджелудочной железы является острым состоянием, угрожающим жизни человека. При отсутствии адекватных мер помощи существует высокий риск смерти пациента.
К одной из базовых групп лекарственных препаратов, которые применяют для профилактики и лечения аутолиза поджелудочной железы, относят антиферментные препараты – ингибиторы протеолиза.
Показания к применению
Антиферментные препараты применяют при заболеваниях, которые сопровождаются нарушением оттока панкреатического сока из поджелудочной железы: острых панкреатитах, обострениях хронического панкреатита, тяжелых травмах поджелудочной железы, опухолях поджелудочной железы, отеках стенок двенадцатиперстной кишки при длительном активном приеме алкоголя.
Также антиферментные препараты используют для профилактики сильных кровотечений и тяжелой кровопотери в случае операций на сердце, сердечных (коронарных) сосудах, легких и т.д.
Фармакологическое действие
Антиферментные препараты блокируют самый мощный панкреатический фермент – трипсин. Трипсин расщепляет белки (протеины), осуществляя биохимический процесс, который называется протеолиз. Именно поэтому антиферментные препараты еще называют ингибиторами протеолиза. При этом останавливаются процессы самопереваривания в поджелудочной железе и прекращают выделяться в кровь токсины – продукты аутолиза.
Антиферментные препараты дополнительно оказывают кровоостанавливающее действие, блокируя действие других ферментов-протеаз в крови, отвечающих за расщепление белков. В частности, антиферментные препараты ингибируют активность фермента фибринолизина (плазмина), который отвечает за разрушение нитей фибрина, стабилизирующих тромбы, и препятствует тем самым остановке кровотечений.
Кроме того, антиферментные препараты оказывают неспецифическое противовоспалительное действие.
Классификация антиферментных препаратов
К антиферментным препаратам относят апротинин.
Также к ингибиторам протеолиза можно отнести аминокапроновую кислоту.
Основы лечения антиферментными препаратами
Учитывая особенности и сложности в подборе индивидуальной дозы антиферментных препаратов конкретному пациенту, а также широкий спектр побочных эффектов и особенностей взаимодействия с другими лекарствами, ингибиторы протеолиза назначает только опытный врач в условиях стационара.
Апротинин может вызвать сильную аллергическую реакцию вплоть до анафилактического шока. Категорически противопоказано назначать препарат пациентам, которым в течение последнего года вводили апротинин.
Особенности лечения антиферментными препаратами
Перед назначением апротинина рекомендуется провести тест-реакцию на специфические антитела.
Учитывая мощный аллергизирующий потенциал апротинина, до применения его в терапевтической дозе следует ввести пациенту небольшое количество препарата (около 1 мл) внутривенно под контролем артериального давления. При отсутствии симптомов острой аллергии через 10-15 минут можно ввести пациенту полноценную дозу апротинина.
препараты, схема лечения, как лечить народными методами
Острый панкреатит — острое воспаление поджелудочной железы, без правильного и своевременного лечения это состояние может привести к смерти пациента. Терапия в первую очередь проводится консервативными методами, лечение острого панкреатита медикаментами должно проходить строго под наблюдением врача. Сначала лечение ведется в стационаре; когда состояние пациента приходит в норму, лечение продолжают дома.
Средства для лечения острого панкреатита
Приступ панкреатита требует немедленной госпитализации пациента, схему лечения панкреатита лекарствами врач расписывает подробно для каждого пациента, выбор конкретных препаратов зависит от тяжести заболевания. Терапия основывается на принципе соблюдения покоя, голода и холода, дополнение — медикаменты строго по показаниям.
Купирование острых болей
Приступ острого панкреатита сопровождается невыносимой болью, если не предпринимать попытки для ее устранения, пациент может получить болевой шок. Поэтому в первую очередь врач назначает обезболивающие препараты. Для купирования болевого синдрома применяют:
- Промедол. Наркотический анальгетик, способный снимать самые сильные боли. Препарат вводится подкожно по 1 мл 2−3 раза в сутки;
- Растворы папаверина, атропина и платифиллина при инъекционном введении снижают секреторную активность поджелудочной железы, снимают спазм и болевые ощущения;
- Новокаин. Раствор новокаина относится к группе анестетиков, с его помощью проводят поясничную новокаиновую блокаду или же вводят раствор внутривенно;
- Но-шпа. Раствор спазмолитика вводится внутримышечно; при устранении спазма внутренних органов снижается интенсивность болей.
Сила болевых ощущений снижается при воздействии холода на область поджелудочной железы. Для этого пузырь, наполненный льдом, укладывают на эпигастральную область. Пациент соблюдает постельный режим.
Предупреждение обезвоживания
Острое состояние приводит к обезвоживанию организма; чтобы избежать усиленной потери жидкости, а также вывести токсины из крови и предупредить развитие шока, применяют внутривенные вливания растворов электролитов. Внутривенно капельно вводят:
- раствор натрия хлорида изотонический;
- раствор Рингера;
- Реополиглюкин;
- Гемодез;
- раствор глюкозы.
При возникновении рвоты капают гипертонический раствор натрия хлорида, при развитии гипергликемии вводят инсулин. Нередко возникает необходимость в использовании плазмозаменителей и переливании крови. Если ситуация осложняется резким снижением артериального давления, применяют инъекции глюкокортикоидов.
На протяжении первых 3−5 дней терапии внутривенные вливания заменяют пациенту питание — используют белковые, солевые и углеводные препараты, также назначают инъекции витаминов.
Антиферментная терапия
Важная задача терапии острой формы панкреатита — снижение ферментной активности поджелудочной железы. Для этого назначают препараты, которые тормозят протеолитическую активность ферментов. Наиболее часто применяют Контрикал, Гордокс, Пантрипин, эпсилон-аминокапроновую кислоту. Препараты вводят внутривенно каждые 3−4 часа в максимальных дозировках.
Для подавления секреции поджелудочной железы также используют Даларгин, рибонуклеазу, Липофундин-эмульсию.При развитии отечности назначают антикоагулянты, периодически проводят анализ крови на свертываемость (коагулограмму).
Антиферментные препараты назначают сразу же при поступлении пациента в стационар, их применение прекращают только после стабилизации состояния пациента.
Дополнительные средства
При развитии острого панкреатита нарушается деятельность всех органов и систем, поэтому для лечения используют множество дополнительных лекарственных средств. Пациенту могут быть назначены:
- Антибактериальные средства. Внутривенное введение антибиотиков применяют при сильном воспалительном процессе и угрозе его перехода на брюшную полость.
- Мочегонные препараты назначают для выведения из организма токсических веществ.
- Противоаллергические средства применяются для снижения отечности и с целью десенсибилизации организма.
- Иммуностимуляторы необходимы для повышения сопротивляемости организма факторам воспаления.
- Седативные (успокоительные) препараты назначаются с целью нормализации психологического состояния пациента.
- Препараты, снижающие секрецию желудочного сока, антациды. Их применение необходимо для защиты желудка от раздражающего действия соляной кислоты, которая содержится в желудочном соке.
- Панкреатические ферменты применяются после выхода пациента из острого состояния, когда разрешен прием пищи.
Режим питания
На протяжении 3−5 дней пациенту нельзя принимать никакую пищу. После того как устранены острые явления, нужно плавно переводить организм на обычное питание. Нередко пациента к этому времени выписывают домой, он должен продолжать лечение панкреатита в домашних условиях медикаментозно, соблюдая при этом строгую диету.
Диета при панкреатите носит название «Стол № 5П», прием пищи должен быть частым, 6−8 раз в день небольшими порциями. Первые 3−5 дней, пока не купированы острые симптомы, пациенту запрещен прием любой пищи. Разрешается пить щелочную минеральную воду, кипяченую воду (жидкость пьют маленькими глотками).
С пятого дня в рацион вводят крупяной и овощной отвар, кисель, слабо заваренный чай с сахаром. Ещё через два дня в меню можно включить творожную массу, овощные пюре без соли. Далее в рацион постепенно вводят протертые каши, овощные супы, нежирное мясо, рыбу, кисломолочные продукты.
Запрещены: жирное мясо, сдоба, яйца (кроме парового омлета), бобовые, грибы, кислая капуста. Правильно составить меню помогает врач-диетолог, пациенты должны неукоснительно следовать его рекомендациям, чтобы не спровоцировать рецидив заболевания.
Народные методы лечения
Нередко лечение панкреатита медикаментами сочетают с народными методами. Рецепты нетрадиционной медицины разрешается использовать в неострой фазе после предварительной консультации с лечащим врачом.
Можно использовать такие рецепты:
- Готовят сбор из сухих цветков ромашки и календулы, листьев мяты и рылец кукурузы. Столовую ложку смеси заливают двумя стаканами воды и настаивают на водяной бане 20 минут. Затем настой оставляют охлаждаться в течение 60 минут, после полного остывания его процеживают. Пьют в течение двух недель по 50 мл за полчаса до еды.
- Смешивают в равных количествах цветки бессмертника, плоды боярышника и семена тмина или укропа. Готовят настой по схеме, описанной в первом рецепте. Принимают состав по 100 мл ежедневно после каждого приема пищи.
- Перед едой два раза в день (утром и вечером) выпивают 100 мл смеси свежевыжатых соков моркови и картофеля. Курс лечения — неделя, через 10−14 дней курс можно повторить.
Терапия при неэффективности медикаментов
При остром панкреатите лечение препаратами может оказаться неэффективным, в этом случае прибегают к хирургическому вмешательству. Проводятся такие операции:
- дистальная резекция — удаляют хвост и часть тела поджелудочной железы;
- субтотальная резекция — удаляется хвост, тело, часть головки железы вместе с селезенкой, при этом остается маленький ободок железистой ткани;
- некрсеквестрэктомия заключается в удалении жидкостных образований в воспаленном органе через дренажные трубки.
Оперативное вмешательство может осложняться панкреатогенным или септическим шоком; в позднем периоде у пациентов, перенесших операцию на поджелудочной железе, могут развиться псевдокисты, частые диспепсические расстройства, сахарный диабет.
Даже зная названия препаратов, которые используются для лечения острого панкреатита, пациентам запрещено заниматься самолечением. При первых признаках заболевания (острой боли в левом подреберье, рвоте, повышенной температуре) нужно срочно обращаться в медучреждение.
Острый панкреатит: лечение
Острый панкреатит относится к числу заболеваний, требующих экстренной госпитализации в хирургический стационар. Факт времени здесь играет едва ли не решающую роль: чем быстрее пациент получит необходимую помощь, тем менее опасным будет для него острый панкреатит. Поэтому при первых признаках острого панкреатита необходимо не только обращается к врачу, но и настаивать на госпитализации.
Самое главное правило при лечении острого панкреатита
Неукоснительным правилом для каждого больного должно быть следующее: ни в коем случае не прибегать к самолечению, не предпринимать промываний желудка, не ставить горячих грелок на живот, не вызывать искусственно рвоту. Важно также помнить, что домашние средства, применяемые обычно в случаях острых заболеваний, при остром панкреатите категорически противопоказаны, поскольку они могут усугубить ситуацию.
При обнаружении у ребёнка или взрослого гнойного панкреатита, или воспаления брюшины необходимо оперативное вмешательство. При установлении острого панкреатита у детей в первые 2 суток следует применить комплексное консервативное лечение.
Развитие острого панкреатита требует прежде всего полного воздержание от пищи и жидкости. Вот почему в первые 3-5 дней пациента врачи «держат» на голодной диете.
Лечение острого панкреатита лекарствами
Лечебные меры на догоспитальном этапе: строгий постельный режим, использование пузыря с холодной водой или льдом с целью охлаждения области верхнего отдела живота и приём лекарственных препаратов, снимающих спазмы сосудов и кишечника (но-шпа, папаверин, аторпин, платифиллин, нитроглицерин и т.д.).
Примечание для врачей: несмотря на сильнейшие боли, пациенту нельзя вводить морфин, так как он усиливает спазм сфинктера Одди и способствует нарастанию панкреатита.
Список лекарственных препаратов приведённый ниже использовать для лечения острого панкреатита принимать только после консультации с врачами. Самолечение в острой стадии панкреатита очень опасно. Кроме того, список позволит вам контролировать врачей, которые могут не правильно назначать курс лечения. Будьте здоровы.
Список лекарственных средств для лечения острого панкреатита
Но-шпа (дротаверин) – оказывает выраженное спазмолитическое действие. Показана при спазмах желудка и кишечника, спазматических запорах, приступах желчно- и мочекаменной болезни и стенокардии.
Применяется внутрь по 0,04-0,08 г 2-3 раза в день; внутривенно (медленно) 2-4 мл 2% раствора. При облитерирующем эндартериите используется внутриартериально.
Из побочных действий возможны: головокружение, сердцебиение, потливость, чувство жара, аллергический дерматит, запор.
Папаверин (папаверина гидрохлорид) – миотропный спазмолитический препарат, в больших дозах понижающий возбудимость сердечной мышцы и замедляющий внутрисердечную проводимость. Показан при спазмах сосудов головного мозга, стенокардии, эндартериите, холецистите, пилорозспазме, спастическом колите, спазме мочевыводящих путей и бронхоспазме.
Применяется внутрь по 0,04-0,06 г 3-5 раз в день, подкожно по 1-2 мл 2% раствора 2-4 раза в день; при остром спазме коронарных сосудов и гладкой мускулатуры органов брюшной полости внутривенно (медленно0 1 мл 2% раствора. Внутрь назначают в чистом виде, а также в сочетании с фенобарбиталом. Входит в состав суппозиториев. Высшая доза для взрослых внутрь 0,4 г, суточная 0,6 г; парентерально разовая доза 0,1 г, суточная 0,3. Выпускается в виде порошка, таблеток, ампул, ректальных суппозиториев и сложных таблеток.
Побочные действия: атриовентрикулярная блокада, желудочковая экстрасистолия; при внутреннем введении снижение артериального давления, запор.
Атропин (атропина сульфат) – сульфат атропинового эфира d,1 –троповой кислоты. Обладает м-холинолитической активностью, блокирует м-холинореактивные системы организма. Показан при язвенной болезни желудка и двенадцатиперстной кишки, пилороспазме, желчнокаменной болезни, холецистите, спазмах кишечника и мочевых путей, почечной и печёночной колике, а также бронхиальной астме. В офтальмологии используется для расширения зрачка.
Применяется внутрь по 0,00025-0,001 г 1-2 раза в день, под кожу по 0,25-1 мл 0,1% раствора, в офтальмологии 1-2 капли для инсталляций 1% раствора.
Высшая разовая доза – 0,001 г суточная – 0,003 г.
Побочные действия: сухость во рту, сердцебиение, расширение зрачков, нарушение аккомодации, атония кишечника (снижение или отсутствие перистальтики), головокружение, тахикардия, затруднение мочеиспускания.
Противопоказания: глаукома.
Платифиллин (платифиллина гидротартрат) – винокаменная соль алкалоида, содержащегося в крестовнике широколистном. Оказывает м-холинолитическое, сосудорасширяющее и успокаивающее действие. Показан при спазмах гладкой мускулатуры органов брюшной полости, язвенной болезни желудка и двенадцатиперстной кишки, бронхиальной астме, гипертонии, а также кишечных, печёночных и почечных коликах. В офтальмологии используется для расширения зрачка.
Применяется внутрь по 0,0025-0,005 г 203 раза в день, подкожно 1-2 мл 0,2% раствора.
Побочные действия: сухость во рту, нарушение аккомодации, сердцебиение, затруднение мочеиспускания.
Противопоказания: глаукома, органические заболевания печени и почек.
Нитроглицерин (тринитрат глицерина) – расширяет кровеносные сосуды (преимущественно коронарные артерии и сосуды мозга), расслабляет гладкую мускулатуру желудочно-кишечного тракта, желчевыводящих путей и других органов. Показан для купирования приступов стенокардии, иногда при дискинезии желчевыводящих путей и эмболии центральной артерии сетчатки. Применятся по ?-1 таблетке (или 1-2 капли 0,5-1 % раствора) сублингвально. Побочные действия: шум в ушах, головная боль, головокружение, коллапс.
Список лекарственных средств для лечения острого панкреатита в стационаре
Лечебные меры в условиях стационара: для ферментной токсемии необходимо применение антиферментных препаратов (трасилол, пантрипин, пентоксил, контрикал) и цитостатиков (циклофосфан, фторафур, 5-фторурацил), для профилактики гнойных осложнений – антибиотики широкого спектра действия (ампиокс, гентамицин, канамицин), а при некоторых формах острого панкреатита – средства, стимулирующие восстановительные процессы в железе (метилурацил, пентоксил, анаболические гормоны).
Трасилол – препарат животного происхождения, получаемый из околоушных слюнных желез крупного рогатого скота. Инактивирует ферменты поджелудочной железы — калликреин и трипсин, применяется при патогенетической терапии панкреатита (при остром панкреатите, хроническом панкреатите и обострениях хронического панкреатита, для лечения панкренекроза, а также для предупреждения панкреатита при оперативных вмешательствах в верхней части брюшной полости).
Трасилол особенно эффективен в отёчной фазе острого панкреатита, когда ещё не развился геморрагический некроз.
Применение трасилола рекомендуется начинать возможно раньше и в комбинации с кортикостероидами и антибиотиками.
Трасилол назначается внутривенно одномоментно (медленно) и капельно в дозе 10 000–15 000 ЕД.
Введение в связи с быстрым исчезновением из крови «Трасилола» лучше производить капельным методом, для чего трасилол разводят в изотоническом растворе хлорида натрия или в 5% растворе глюкозы.
При хроническом панкреатите вводят 5 000 – 10 000 ЕД препарата ежедневно.
При остром панкреатите и в случаях панкреанекроза вводят сразу 25 000–50 000 ЕД Трасилола, затем 25 000–75 00 ЕД капельно. В последующие 4–5 дней вводят по 25 000 – 50 000 ЕД в сутки в два приёма, по мере улучшения клинической картины и данных лабораторных исследований дозу Трасилола постепенно снижают до 2 500 – 5 000 ЕД.
При обострении хронического панкреатита препарат вводят в тех же дозах во время приступа, затем дозу снижают.
Для профилактики панкреатита при оперативных вмешательствах в верхней части брюшной полости перед операцией вводят 10 000 ЕД, по ходу операции — 10 000 – 20 000 ЕД и после операции — ежедневно в течение 2–4 дней по 10 000 – 20 000 ЕД.
Побочные явления: при быстром введении трасилола могут наблюдаться тошнота и рвота.В отдельных случаях при повторении курса лечения трасилолом возможны аллергические реакции.
Особые указания: для выявления индивидуальной чувствительности к препарату перед началом лечения вводят 0,2 мл трасилола.
Пантрипин – ингибитор протеолиза. Оказывает тормозящее действие на активность протеолитических ферментов – трипсина и химотрипсина, калликреина, фибринолизина (плазмина) и других протеаз. Показан при остром и хроническом панкреатите, панкреатическом, дуоденальном, желчном или кишечном свище, для профилактики панкреатита при операции на желудке и желчных путях.
Противопоказан при гиперчувствительности к действующему веществу препарата.
Побочные действия: аллергические реакции.
Применяется в/в, разведённым 0,5-1 л 0,9% раствора NaCl для инъекций или в стерильном 5% растворе декстрозы с добавлением инсулина, в соотношении: на 3 г сухого остатка декстрозы – 1 ЕД инсулина. Полученный раствор вводят в/в капельно, по 40-60 кап/мин. Длительность введения – не менее 2 ч.
В зависимости от клинической картины и состояния больного при тяжёлых формах панкреатита концентрированный раствор вводят одномоментно, в/в (100-120 ЕД пантрипина на 10-20 мл 5% раствора декстрозы или 0.9% раствора NaCl). Затем, в течение первых суток, каждые 4 ч – в/в капельно, по 25-30 ЕД на 0,5-1 л 0,5% раствора декстрозы или 0,9% раствора NaCl, всего – до 300 ЕД в первые сутки в 2 приёма. В последующие сутки (на основании клинических и лабораторных данных) дозу уменьшают до 120-150 ЕД/сут. и продолжают вводить до выздоровления больного.
При лёгких формах панкреатита первичная доза составляет 12-25 ЕД. В дальнейшем дозу выбирают в зависимости от состояния больного.
При других заболеваниях (панкреатических, желчных, дуоденальных и высоких кишечных свищах) – в/в капельно, в дозе 6-12 ЕД. В зависимости от клинической картины введение повторяют, но не чаще 1 раза в сутки.
В случаях оперативного вмешательства при острых панкреатитах – местно, под капсулу поджелудочной железы, в дозе 50-62 ЕД, разведённой в 20 мл 0,9% раствора NaCl.
В послеоперационном периоде – в/в, по схеме, рекомендованной для тяжёлых форм панкреатита.
При оперативных вмешательствах на желудке и желчных путях с профилактической целью – в/в и местно, в дозе 50-80 ЕД, в зависимости от тяжести оперативного вмешательства и опасности развития послеоперационного панкреатита.
Пентоксил – 4-Метил-5-оксиметилурацил. Стимулирует лейкопоэз, повышает фагоцитарную активность лейкоцитов и рекулоэндотелиальной системы. Показан при лейкопении различной этиологии, алиментарной токсической алейкии, агранулоцитарной ангине, некоторых видах лекарственных агранулоцитозов, хронических отравлениях бензолом.
Способ применения: внутрь взрослым по 0,200,4 г 3-4 раза в день после еды, детям в соответствии с возрастом. В среднем на курс лечения (15-20 дней) требуется 6-10 г препарата.
Побочное действие: диспепсия.
Противопоказания: лимфогранулематоз, злокачественные новообразования костного мозга.
Контрикал – полипептид, получаемый из лёгких крупного рогатого скота. Ингибирует активность ряда ферментов (трипсин, химопсин, плазмин, калликереин) и образует с ними неактивные компоненты.
Показан при остром панкреатите, обострении хронического панкреатита, остром панкреонекрозе: для предупреждения панкреатита при операциях на поджелудочной железе и близко расположенных к ней органах.
Применяется в/в (медленно одномоментно или капельно) 10 000-20 000 ЕД, при необходимости по 50 000 ЕД/сут., внутрибрюшинно 10 000-20 000 ЕД.
Побочные действия: возможны аллергические реакции.
Циклофосфан – 0-триметиленовый эфир диамида фосфорной кислоты. Цитостатический препарат, оказывающий терапевтической действие при опухолевых процессах. Угнетает кроветворение. Показан при раке яичников, раке молочной железы, раке лёгких. Лимфогранулематозе, лимфосаркоме, ретикуласаркоме, множественной миеломе, хроническом и остром лимфолейкозе.
Применяется внутривенно, внутримышечно, внутриплеврально и внутрибрюшинно. Внутривенно или внутримышечно по 0,2 г ежедневно, 0,4 г через день или 0,6 г через 2 дня. Ослабленным больным при ухудшении показателей крови или плохой переносимости дневную дозу уменьшают до 0,2 г. На курс лечения 8-14 г, затем препарат назначают в поддерживающих дозах; внутривенно или внутримышечно по 0,1-0,2 2 раза в неделю.
В ходе лечения кровь исследуется два раза.
Среди побочных действий возможны: лейкопения, тошнота, тромбоцитопения, рвота, алопеция. Иногда возникают боли в мышцах и костях. В редких случаях наблюдаются цистит или токсический гепатит.
Противопоказания: кахексия (крайнее истощение организма) с резкой анемией, лейкопения, тромбоцитопения, сердечная недостаточность и тяжёлые заболевания печени и почек.
Фторафур – 2-Фуранидил -5-фторурацил. По фармакологическим свойствам близок к 5-фторурацилу, но менее токсичен и лучше переносится больными.
Показан при раке прямой или толстой кишки, раке желудка, а также раке молочной железы.
Применяется в/в через каждые 12 часов по 1.2-2 г (30 мг кг). На курс лечения требуется 30-40 г препарата, в отдельных случаях 50-60 г. Лечение проводят через 1 месяц после предшествующего лучевой терапии и химиотерапии.
Побочные действия: в момент введения возможно головокружение; при длительном применении, введении больших доз и повышенной чувствительности у больного развиваются тошнота, рвота, стоматит, диарея, лейкопения и тромбоцитопения.
Противопоказания: терминальные стадии болезни; болезни печени и почек; лейкопения (менее 3 х10/л9).
5-фторурацил – 2,4-Диоксо-5-фторпиримидин, или 5-фторурацил. Относится к группе антиметаболитов нуклеинового обмена. Эффективен при опухолях ЖКТ. Токсичен, особенно сильно угнетает функции костного мозга и ЖКТ.
Показан при инопербальных формах, рецидивах и метастазах рака желудка, опухолях различных отделов толстой кишки и поджелудочной железы.
Способ применения: внутривенно (медленно) ежедневно по 10-15 мг/кг в день до появления побочных реакций со стороны ЖКТ (понос, рвота и др.). Иногда препарат вводят в тех же дозах ежедневно в течение 4 дней и при отсутствии побочных реакций через день: на 6-й, 8-й, 10-й и 12-й день по 5-7,5 мг/кг.
Как правило, курс лечения составляет 12 дней (3-7 г) суточная доза равняется не более чем 1 г.
При хорошей переносимости препарата через 4-6 недель курс лечения повторяют.
Побочные действия: лейкопения, тромбоцитопения, тошнота, рвота, понос, язвенный стоматит, язвенные поражения слизистой оболочки ЖКТ, алопеция.
Противопоказания: терминальные стадии заболевания, кахексия, лейкопения, тромбоцитопения. Тяжёлые поражения печени и почек.
Не следует вводить препарат ранее чем через 3-4 недели после сложных хирургических вмешательств и ранее чем через 1 месяц после лучевой терапии и лечения другими противоопухолевыми препаратами, а также при обширных метастазах в костный мозг.
Ампиокс (ампиокс натрия) – представляет собой смесь ампициллина натриевой соли и оксациллина натриевой соли в соотношении 2:1. Обладает антибактериальным спектром входящих в состав препарата антибиотиков. Устойчив в отношении пенициллиназообразующих стафилококков.
Показан при тяжело протекающих инфекциях (сепсис, эндокардит, последродовая инфекция), для профилактики и лечения послеоперационных осложнений и инфекций недоношенных и новорождённых детей.
Способ применения: внутримышечно взрослым по 2 г/сут., детям соответственно возрасту от 10 до 50 мг/кг. Суточную дозу принято делить на 3-4 порции.
Побочные действия: аллергические реакции, болезненность в месте введения.
Противопоказания: необходима осторожность при наличии в анамнезе повышенной чувствительности к препаратам пенициллина.
Гентамицин (гентамицина сульфат) – антибиотик, обладающий широким спектром антимикробного действия. Подавляет рост большинства грамотрицательных и грамположительных микроорганизмов. Высокоактивен в отношении палочки сине-зелёного гноя. Быстро всасывается. Проникается через гематоэнцефалический барьер. Максимальная концентрация в сыворотке крови отмечается через 1 ч после инъекции. При повтором введении в дозе 0,4-0,8мг/кг с интервалом 8 ч наблюдается кумуляция препарата. Выводится из организма почками.
Показан при инфекциях мочевыводящих путей (цистит, пиелонефрит, уретрит), дыхательного тракта) пневмония, плеврит, эмпиема, абсцесс лёгкого), хирургические инфекции (хирургический сепсис, перитонит), инфекции кожи (фурункулёз. Дерматит, трофические язвы, ожоги), вызванные возбудителями, устойчивыми к другим антибиотикам широкого спектра действия.
Способ применения: вводится внутремышечно; при инфекциях мочевыводящих путей разовая доза для взрослых составляется 0,4 мг-кг, суточная 0,8-1,2 мг/кг (вводят в 2-3 приёма). При инфекциях других локализаций суточная доза равна 2,4-3,2 мг/кг.
Курс лечения подразумевает 6-8 дней. Место применяют в виде 0,1% растворов, присыпок, мазей. Кроме того, возможны ингаляции – 4 мг/мл 4 раза в день.
Побочные действия: в некоторых случаях даёт ототоксический или нефротоксический эффект.
Канамицин (канамицина моносульфат) – имеет широкий спектр антимикробного действия. Устойчивость к нему развивается медленно. При приёме внутрь почти е всасывается из пищеварительного тракта. Не обладает кумулятивным действием.
Показан при кишечных инфекциях (дизентерии, дизентерийном бактерионосительстве, бактериальном колите и энтероколите). Используется также для подготовки больных к операциям на ЖКТ.
Способ применения: внутрь 4-6 раз в сутки по 0,5-0,75 г. Высшая суточная доза составляет 4 г. Детям препарат даётся из расчёта 50 мг/(кг*сут.). Недоношенным детям и детям первого месяца жизни назначается только по жизненным показаниям.
Обыкновенно курс лечения подразумевает 7-10 дней.
В предоперационном периоде взрослым назначается в первые сутки 6 г, а в последующие двое суток – по 1 г 4 раза.
Побочные действия: в некоторых случаях возникают тошнота и жидкий стул.
Противопоказания: нарушения функции почек, поражения слухового нерва, непроходимость кишечника. Кроме этого, канамицин нельзя совмещать с некоторыми препаратами: мономицином, неомицином, гентамицином, стрептомицином, флормицином.
Метилурацил – 2,4 –Диокси-6-метил-1,2,3,4-тетрагидропиримидин, или 4-метилурацил. Ускоряет процессы клеточного размножения и рост в различных тканях и органах при резорбтивном и местном действии. Резорбтивное действие проявляется в основном в стимуляции лейкопоэза при угнетении кроветворения.
Показан при алиментарно-токсической алейкии, агранулоцитозе и лейкопении различной этиологии; лучевых поражениях кожи, вяло заживающих ожогах, ранах, переломах костей, язвенной болезни желудка и двенадцатиперстной кишки.
Способ применения: внутрь во время или после еды 1 г 3-4 раза в день; в отдельных случаях суточная доза увеличивается до 5-6 г. Детям дозы устанавливаются в соответствии с возрастом. Наружно препарат применяется в виде 5% или 10% мази с антибиотиками (фурацилин, синтомицин, окситетрациклин) и виде суппозиториев.
Противопоказания: лейкемические формы лейкоза (особенно миелоидные).
Лекарства от острого панкреатита: другие анальгетики, антибиотики
Telem DA, Bowman K, Hwang J, Chin EH, Nguyen SQ, Divino CM. Избирательное ведение пациентов с острым билиарным панкреатитом. Дж Гастроинтест Сург . 2009 13 декабря (12): 2183-8. [Медлайн].
Banks PA, Bollen TL, Dervenis C и др., Для Рабочей группы по классификации острого панкреатита. Классификация острого панкреатита – 2012: пересмотр классификации и определений Атланты на основе международного консенсуса. Кишечник . 2013 Январь 62 (1): 102-11. [Медлайн].
Haydock MD, Mittal A, van den Heever M и др., Для Сети поджелудочной железы Новой Зеландии. Национальное исследование инфузионной терапии при остром панкреатите: в текущей практике отсутствует надежная доказательная база. Мир J Surg . 2013 Октябрь 37 (10): 2428-35. [Медлайн].
Ai X, Qian X, Pan W. и др. Чрескожный дренаж под контролем УЗИ может снизить смертность от тяжелого острого панкреатита. Дж Гастроэнтерол . 2010. 45 (1): 77-85. [Медлайн].
Li H, Qian Z, Liu Z, Liu X, Han X, Kang H. Факторы риска и исход острой почечной недостаточности у пациентов с тяжелым острым панкреатитом. J Crit Care . 2010 июн.25 (2): 225-9. [Медлайн].
Whitcomb DC, Yadav D, Adam S, et al, для Североамериканской группы по изучению поджелудочной железы. Многоцентровый подход к рецидивирующему острому и хроническому панкреатиту в США: Североамериканское исследование панкреатита 2 (NAPS2). Панкреатология . 2008. 8 (4-5): 520-31. [Медлайн]. [Полный текст].
Эльмунцер Б.Дж., Шейман Дж.М., Леман Г.А. и др., Для Американского кооператива по исследованию исходов в эндоскопии (USCORE). Рандомизированное исследование ректального применения индометацина для профилактики панкреатита после ЭРХПГ. N Engl J Med . 2012 апр. 12, 366 (15): 1414-22. [Медлайн].
Камисава Т., Фуната Н., Хаяси Ю. и др. Новый клинико-патологический субъект аутоиммунного заболевания, связанного с IgG4. Дж Гастроэнтерол . 2003. 38 (10): 982-4. [Медлайн].
Yadav D, Lowenfels AB. Эпидемиология панкреатита и рака поджелудочной железы. Гастроэнтерология . 2013 июнь 144 (6): 1252-61. [Медлайн]. [Полный текст].
Пири А.Ф., Деллон Э.С., Лунд Дж. И др. Бремя желудочно-кишечных заболеваний в США: обновление 2012 г. Гастроэнтерология . 2012 ноябрь 143 (5): 1179-1187.e3. [Медлайн]. [Полный текст].
Singla A, Csikesz NG, Simons JP, et al.Объем общенациональной больницы при остром панкреатите: анализ общенациональной стационарной выборки за 1998-2006 гг. Е.П.Б. (Оксфорд) . 2009 11 августа (5): 391-7. [Медлайн]. [Полный текст].
Кришна С.Г., Камбодж А.К., Харт П.А., Хинтон А., Конвелл Д.Л. Изменяющаяся эпидемиология госпитализаций при остром панкреатите: десятилетие тенденций и влияние хронического панкреатита. Поджелудочная железа . 2017 Апрель 46 (4): 482-8. [Медлайн]. [Полный текст].
Пири А.Ф., Крокетт С.Д., Мерфи С.К. и др.Бремя и стоимость заболеваний желудочно-кишечного тракта, печени и поджелудочной железы в США: обновление 2018 г. Гастроэнтерология . 2019 января 156 (1): 254-72.e11. [Медлайн]. [Полный текст].
Банки П.А. Эпидемиология, естественное течение и предикторы исхода заболевания при остром и хроническом панкреатите. Гастроинтест Endosc . 2002 г., декабрь 56 (6 доп.): S226-30. [Медлайн].
Morinville VD, Barmada MM, Lowe ME. Рост заболеваемости острым панкреатитом в американском педиатрическом центре третичной медицинской помощи: есть ли большая осведомленность среди ответственных врачей ?. Поджелудочная железа . 2010 января 39 (1): 5-8. [Медлайн].
Ахтар А.Дж., Шахин М. Экстрапанкреатические проявления острого панкреатита у афроамериканцев и латиноамериканцев. Поджелудочная железа . 2004 29 ноября (4): 291-7. [Медлайн].
Huh JH, Jeon H, Park SM, et al. Сахарный диабет связан со смертностью при остром панкреатите. Дж Клин Гастроэнтерол . 2018 Февраль 52 (2): 178-83. [Медлайн].
Уиткомб округ Колумбия.Клиническая практика. Острый панкреатит. N Engl J Med . 2006 18 мая. 354 (20): 2142-50. [Медлайн].
Суппиа А., Малде Д., Араб Т. и др. Прогностическое значение отношения нейтрофилов-лимфоцитов (NLR) при остром панкреатите: определение оптимального NLR. Дж Гастроинтест Сург . 2013 Апрель 17 (4): 675-81. [Медлайн].
Хан А., Сарма Д., Гоуда С., Родригес Г. Роль модифицированной оценки раннего предупреждения (MEWS) в прогнозе острого панкреатита. Оман Мед. J . 2021 Май. 36 (3): e272. [Медлайн]. [Полный текст].
Mikolasevic I, Orlic L, Poropat G, et al. Безалкогольная жировая дистрофия печени и тяжесть острого панкреатита. Eur J Intern Med . 2017 Март 38: 73-8. [Медлайн].
Котари С., Калиновский М., Кобешко М., Альмуради Т. Компьютерная томография в диагностике острого неосложненного панкреатита: полезность против стоимости . Мир Дж. Гастроэнтерол .2019 7 марта. 25 (9): 1080-7. [Медлайн]. [Полный текст].
Имамура Ю., Хирота М., Ида С. и др. Значение степени почечного края при компьютерной томографии в оценке тяжести острого панкреатита. Поджелудочная железа . 2010 январь 39 (1): 41-6. [Медлайн].
Balthazar EJ, Ranson JH, Naidich DP, Megibow AJ, Caccavale R, Cooper MM. Острый панкреатит: прогностическое значение КТ. Радиология . 1985 Сентябрь 156 (3): 767-72. [Медлайн].
Бальтазар Э.Дж., Робинсон Д.Л., Мегибоу А.Дж., Рэнсон Дж. Х.Острый панкреатит: значение КТ для установления прогноза. Радиология . 1990 Февраль 174 (2): 331-6. [Медлайн].
Balthazar EJ. Стадия острого панкреатита. Радиол Клин Норт Ам . 2002 Декабрь 40 (6): 1199-209. [Медлайн].
Бадалов Н., Теннер С., Бэйли Дж. Профилактика, распознавание и лечение панкреатита после ЭРХПГ. СОП . 2009 9 марта. 10 (2): 88-97. [Медлайн].
Тестони П.А., Мариани А., Джуссани А. и др. Для группы компаний SEIFRED.Факторы риска пост-ЭРХПГ панкреатита в центрах с большим и малым объемом операций, а также среди опытных и неспециализированных операторов: проспективное многоцентровое исследование. Ам Дж. Гастроэнтерол . 2010 августа 105 (8): 1753-61. [Медлайн].
Parihar V, Ridgway PF, Conlon KC, Huggett M, Ryan BM. Роль эндоскопического вмешательства в лечении воспалительных скоплений жидкости поджелудочной железы. евро J Гастроэнтерол Hepatol . 2017 Апрель 29 (4): 371-9. [Медлайн].
Имри CW.Прогностические показатели при остром панкреатите. Банка J Гастроэнтерол . 2003 май. 17 (5): 325-8. [Медлайн].
Кришнан К. Нутритивное лечение острого панкреатита. Curr Opin Gastroenterol . 2017 марта 33 (2): 102-6. [Медлайн].
Jacobson BC, Vander Vliet MB, Hughes MD, Maurer R, McManus K, Banks PA. Проспективное рандомизированное исследование прозрачных жидкостей в сравнении с твердой диетой с низким содержанием жиров в качестве начального приема пищи при легком остром панкреатите. Клин Гастроэнтерол Гепатол . 2007 5 августа (8): 946-51; викторина 886. [Медлайн]. [Полный текст].
Баккер О.Дж., ван Бруншот С., ван Сантворт Х.С. и др. Для Голландской исследовательской группы по панкреатиту. Раннее кормление через назоэнтерический зонд в сравнении с кормлением по требованию при остром панкреатите. N Engl J Med . 2014 20 ноября. 371 (21): 1983-93. [Медлайн].
Марави-Пома Е., Дженер Дж., Альварес-Лерма Ф. и др., Испанская группа по изучению септических осложнений при тяжелом остром панкреатите.Раннее лечение антибиотиками (профилактика) септических осложнений при тяжелом остром некротическом панкреатите: проспективное рандомизированное многоцентровое исследование, в котором сравниваются две схемы лечения имипенем-циластатином. Intensive Care Med . 2003 29 ноября (11): 1974-80. [Медлайн].
Изенманн Р., Рунци М., Крон М. и др. Для Немецкой исследовательской группы по антибиотикам при тяжелом остром панкреатите. Профилактическое лечение антибиотиками у пациентов с прогнозируемым тяжелым острым панкреатитом: плацебо-контролируемое двойное слепое исследование. Гастроэнтерология . 2004 апр. 126 (4): 997-1004. [Медлайн].
Джонсон С.Д., Кингснорт А.Н., Имри К.В. и др. Двойное слепое рандомизированное плацебо-контролируемое исследование антагониста фактора активации тромбоцитов, лексипафанта, в лечении и профилактике органной недостаточности при прогнозируемом тяжелом остром панкреатите. Кишечник . 2001, январь, 48 (1): 62-9. [Медлайн]. [Полный текст].
Абулиан А., Чан Т., Ягубиан А. и др. Ранняя холецистэктомия безопасно сокращает время пребывания в стационаре у пациентов с желчнокаменным панкреатитом легкой степени: рандомизированное проспективное исследование. Энн Сург . 2010 Апрель 251 (4): 615-9. [Медлайн].
Guadagni S, Cengeli I, Palmeri M, et al. Ранняя холецистэктомия при нетяжелом остром желчнокаменном панкреатите: легче сказать, чем сделать. Минерва Чир . 2017 Апрель 72 (2): 91-7. [Медлайн].
van Santvoort HC, Besselink MG, Bakker OJ, et al, для Голландской исследовательской группы по панкреатиту. Пошаговый подход или открытая некрэктомия при некротическом панкреатите. N Engl J Med .2010, 22 апреля. 362 (16): 1491-502. [Медлайн].
[Рекомендации] Теннер С., Бэйли Дж., ДеВитт Дж., Ведж С.С. и Американский колледж гастроэнтерологии. Рекомендации Американского колледжа гастроэнтерологии: ведение острого панкреатита. Ам Дж. Гастроэнтерол . 2013 сентябрь 108 (9): 1400-15; 1416. [Медлайн].
[Рекомендации] Crockett SD, Wani S, Gardner TB, Falck-Ytter Y, Barkun AN, Комитет клинических рекомендаций Института Американской гастроэнтерологической ассоциации.Руководство Института Американской гастроэнтерологической ассоциации по начальному ведению острого панкреатита. Гастроэнтерология . 2018 Март 154 (4): 1096-101. [Медлайн].
[Рекомендации] Веге С.С., Зиринг Б., Джайн Р., Моайеди П. и Комитет по клиническим рекомендациям Американской гастроэнтерологической ассоциации. Руководство института Американской гастроэнтерологической ассоциации по диагностике и лечению бессимптомных неопластических кист поджелудочной железы. Гастроэнтерология .2015 апр. 148 (4): 819–22; викторина 12-3. [Медлайн].
[Рекомендации] Леппаниеми А., Толонен М., Тараскони А. и др. Рекомендации WSES 2019 по ведению тяжелого острого панкреатита. Мир J Emerg Surg . 2019. 14:27. [Медлайн]. [Полный текст].
Грейнджер Дж., Ремик Д. Острый панкреатит: модели, маркеры и медиаторы. Ударная . 2005 24 декабря, приложение 1: 45-51. [Медлайн].
Wu BU, Hwang JQ, Gardner TH, et al.Лактатный раствор Рингера уменьшает системное воспаление по сравнению с физиологическим раствором у пациентов с острым панкреатитом. Клин Гастроэнтерол Гепатол . 2011 августа, 9 (8): 710-7.e1. [Медлайн].
Ким С.Б., Ким Т.Н., Чунг Х.Х., Ким К.Х. Небольшой размер желчных камней и отсроченная холецистэктомия увеличивают риск рецидивов панкреатобилиарных осложнений после разрешения острого билиарного панкреатита. Dig Dis Sci . 2017 Март 62 (3): 777-83. [Медлайн].
Петров М.С., Ядав Д.Глобальная эпидемиология и комплексная профилактика панкреатита. Нат Рев Гастроэнтерол Гепатол . 2019 16 марта (3): 175-84. [Медлайн]. [Полный текст].
Мачикадо Дж. Д., Ядав Д. Эпидемиология рецидивирующего острого и хронического панкреатита: сходства и различия. Dig Dis Sci . 2017 Июль 62 (7): 1683-91. [Медлайн]. [Полный текст].
[Рекомендации] Веге С.С., ДиМаньо М.Дж., Форсмарк С.Е., Мартель М., Баркун А.Н. Первичное лечение острого панкреатита: Технический обзор Института Американской Гастроэнтерологической Ассоциации. Гастроэнтерология . 2018 Март 154 (4): 1103-39. [Медлайн].
Jeon CY, Papachristou GI, Pisegna JR, et al. Дизайн исследования Case-CrossovEr для информирования о специальных вмешательствах для предотвращения прогрессирования заболевания при остром панкреатите (ACCESS-AP) – дизайн исследования и популяция. Панкреатология . 2021, 24 июня. [Medline].
Дузенци Д., Ялныз М., Испироглу М. Сравнение прогностических показателей при органной недостаточности с острым панкреатитом. Ulus Travma Acil Cerrahi Derg . 2021 июля 27 (4): 410-20. [Медлайн].
Фармакологическая терапия острого панкреатита
Abstract
В то время как консервативные методы лечения, такие как прием жидкости, отдыха кишечника и антибиотики, являются основой текущего лечения острого панкреатита, есть много перспектив в фармакологической терапии, направленной на различные аспекты патогенеза панкреатита. . Обсуждается обширный обзор доклинических исследований, которые включают оценку методов лечения, таких как антисекреторные агенты, ингибиторы протеаз, противовоспалительные агенты и антиоксиданты.Многие из этих исследований показали терапевтическую пользу и улучшение выживаемости на экспериментальных моделях. На основе имеющихся доклинических исследований мы обсуждаем потенциальные новые целевые фармакологические подходы, которые могут быть многообещающими при лечении острого панкреатита. На сегодняшний день различные клинические исследования оценили трансляционный потенциал эффективных экспериментальных методов лечения на животных моделях и показали либо неудачные, либо смешанные результаты в исследованиях на людях. Несмотря на эти обескураживающие клинические исследования, существует большая клиническая потребность и существует несколько доклинических эффективных методов лечения, которые ждут исследования на пациентах.Лучшее понимание патофизиологии острого панкреатита и уроки, извлеченные из прошлых клинических исследований, вероятно, станут хорошей основой для расширения будущих методов лечения острого панкреатита.
Ключевые слова: Острый панкреатит, Антисекреторы, Ингибиторы протеазы, Противовоспалительные, Антиоксиданты, Синдром системной воспалительной реакции, Органная недостаточность, Смертность
Основной совет: В настоящее время нет утвержденных методов лечения острого панкреатита.В этом обзоре суммируются и обсуждаются доклинические и клинические исследования острого панкреатита, а также обсуждаются потенциальные многообещающие методы лечения.
ВВЕДЕНИЕ
В США в 2009 году у более 274000 пациентов был диагностирован острый панкреатит, что делает его наиболее распространенным желудочно-кишечным заболеванием, требующим острой госпитализации с затратами на лечение, превышающими 2,5 миллиарда долларов в год [1]. Прогноз для пациентов с острым панкреатитом в значительной степени определяется наличием органной недостаточности и инфицированного панкреонекроза с соответствующими показателями смертности 15-30% [2].Другие осложнения панкреатита включают синдром системного воспалительного ответа (SIRS), сепсис и острый респираторный дистресс-синдром (ARDS). Несмотря на рост заболеваемости [3], в настоящее время нет доступной фармакологической терапии для смягчения заболевания и его течения. Текущее лечение панкреатита в основном является поддерживающим. Лечение органной недостаточности состоит из поддерживающих мероприятий [4], в то время как лечение инфицированного панкреонекроза состоит из дренирования или санации раны и антибиотиков [5].
Самыми частыми причинами острого панкреатита у западного населения являются алкоголь и камни в желчном пузыре, но также описаны многие другие причины, и независимо от триггера существует основной общий патогенетический исход [6,7]. Считается, что острый панкреатит представляет собой местный воспалительный процесс, включающий преждевременную внутриклеточную активацию пищеварительных ферментов в ацинарных клетках, ведущую к самоперевариванию ткани, которое может прогрессировать и вовлекать отдаленные органы. Также считается, что секреторные ацинарные клетки выделяют хемокины и цитокины, которые привлекают лейкоциты, вызывая воспалительный ответ, ответственный за отек поджелудочной железы и накопление нейтрофилов [8].Этот интерстициальный отек иногда может прогрессировать до некроза части поджелудочной железы и возможной бактериальной инфекции. Острый панкреатит также может влиять на микрососудистое кровообращение и нарушать перфузию и оксигенацию тканей [9]. Хотя поддерживающая терапия в значительной степени является единственным доступным лечением этого заболевания, исследования панкреатита и лучшее понимание патофизиологии привели к разработке некоторых фармакологических методов лечения, нацеленных на различные этапы патогенеза панкреатита.В обзоре, опубликованном в 2008 г., описаны некоторые фармакологические методы лечения, исследованные на экспериментальных моделях животных [10]. С тех пор некоторые из этих методов лечения были дополнительно изучены, новые лекарства были обнаружены в каждом классе терапии, и было проведено больше клинических исследований на людях, оценивающих клиническую полезность этих методов лечения.
Этот обзор посвящен новейшим фармакологическим методам лечения острого панкреатита и не касается фармакологии стандартного лечения, используемого в настоящее время, такого как обезболивание и антибиотики.В статье резюмируются экспериментальные доклинические исследования, которые предоставляют доказательства терапевтического потенциала различных классов новых лекарств, описываются клинические испытания, в которых оценивался их трансляционный потенциал, а также комментарии относительно будущих методов лечения и потенциальных многообещающих агентов, ожидающих перевода в клиническую практику. Этот обзор посвящен фармакологической терапии острого панкреатита, который не является вторичным по отношению к эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ).
МОЛЕКУЛЯРНЫЙ ПАТОГЕНЕЗ ПАНКРЕАТИТА
В физиологических условиях секреция неактивных предшественников ферментов из ацинарных клеток происходит в ответ на цитозольный кальций.Однако устойчивое повышение уровня этого кальция может привести к преждевременной активации и секреции пищеварительных ферментов из ацинарных клеток, что является одним из самых ранних обнаруживаемых событий при панкреатите [11]. После первоначального поражения ацинарной клетки поджелудочной железы прогрессирование заболевания представляет собой многофазный процесс, который включает локальное воспаление поджелудочной железы, за которым следует генерализованный воспалительный ответ и заключительная стадия сепсиса, включающая полиорганную недостаточность у пациентов с тяжелым заболеванием. [8].После первоначального повреждения воспалительные клетки часто рекрутируются в поджелудочную железу через молекул адгезии, что может усугубить воспалительную реакцию, приводящую к тяжелому острому панкреатиту [8]. Одним из ключевых факторов воспалительной реакции при остром панкреатите, вероятно, являются циркулирующие цитокины и хемокины. Активные пищеварительные ферменты являются мощными стимуляторами макрофагов, которые впоследствии вызывают выработку провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNF-α) и интерлейкины [12].
Производство цитокинов регулируется большим количеством факторов транскрипции, наиболее заметным из которых является ядерный фактор, усиливающий легкую каппа-цепь активированных В-клеток (NF-κB) [12]. Различные типы высвобождаемых цитокинов могут вызывать свои эффекты через высокоспецифичных рецепторов клеточной поверхности и стимулировать ферменты, такие как циклооксигеназа-2 и индуцибельная синтаза оксида азота (iNOS), которые опосредуют воспалительный процесс. Следовательно, ингибирование этих ферментов, вероятно, ограничит местное и системное повреждение, вызванное провоспалительными лейкоцитами [12].Активные формы кислорода (ROS) и активные формы азота (RNS) также участвуют в патогенезе острого панкреатита. Механизм, с помощью которого эти агенты вызывают панкреатит, двоякий. АФК и РНС действуют непосредственно на биомолекулы (липиды, белки и нуклеиновые кислоты) и окисляют эти компоненты клеточной мембраны в поджелудочной железе, что приводит к разрушению мембраны и некрозу клеток поджелудочной железы. В дополнение к прямым пагубным окислительным эффектам, ROS и RNS могут также служить вторичными посредниками во внутриклеточной передаче сигналов и вызывать провоспалительные каскады [13].
ПРЕКЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Антисекреторные агенты
Острый панкреатит характеризуется повреждением панкреатической и перипанкреатической жировой ткани, частично опосредованным аутопищеварительными ферментами. Чрезмерная стимуляция экзокринной части поджелудочной железы усугубляет острый панкреатит [9] и, таким образом, является основанием для тестирования антисекреторных агентов в качестве потенциальных методов лечения острого панкреатита. Первоначальные исследования на животных в 1970-х годах тестировали глюкагон, а последующие исследования изучали использование соматостатина и аналога соматостатина длительного действия.
Глюкагон увеличивает кровоток в верхней брыжеечной артерии и снижает экзокринную секрецию поджелудочной железы [14]. Однако исследование с использованием модели панкреатита на собаках не показало, что лечение глюкагоном само по себе или в сочетании с объемной реанимацией лучше, чем только объемная реанимация [15]. Фактически, в их модели кровоизлияние в поджелудочную железу было связано с лечением глюкагоном, что предполагает возможное ухудшение заболевания. В более позднем исследовании на свиньях сообщалось о положительном влиянии глюкагона [16], но другие экспериментальные исследования в дополнение к вышеупомянутому исследованию не подтвердили использование терапии глюкагоном при экспериментальном остром панкреатите [17-19].
Соматостатин – это гормон-ингибитор с множественным действием на перистальтику желудочно-кишечного тракта и внешнесекреторную секрецию поджелудочной железы [20]. Одно доклиническое исследование с использованием таурохолат-индуцированной крысиной модели острого панкреатита показало, что соматостатин эффективен в подавлении базальной и гормональной стимуляции секреции панкреатических ферментов, но не влияет на степень панкреонекроза, отек поджелудочной железы, инфильтрацию лейкоцитов или содержание ферментов в поджелудочная железа после панкреатита индуцировалась и не приводила к общему снижению смертности [21].Другое исследование показало, что соматостатин стимулирует ретикулоэндотелиальную функцию печени и селезенки у крыс, что позволяет предположить пользу при лечении панкреатита [22]. Доклинические исследования показали преимущества использования соматостатина и его аналога длительного действия, что является основой для клинических испытаний, обсуждаемых ниже.
Использование антисекреторных агентов имеет ограничения, учитывая, что поджелудочная железа не только секретирует ферменты, но также секретирует бикарбонат и жидкости, а исследования на животных показали, что стимуляция протоковой секреции бикарбоната оказывает защитное действие на тяжесть панкреатита [23]. ].
Ингибиторы протеаз
Внутрипанкреатическая активация пищеварительных ферментов играет важную роль в патогенезе острого панкреатита. По этой очевидной причине ингибиторы протеазы были и остаются терапевтическим интересом при остром панкреатите. Ранние исследования на собаках с хирургически индуцированным панкреатитом, получавших ингибиторы трипсина из яичного белка или соевых бобов, а также тразилол (апротинин), ингибитор трипсин-калликреин из крупного рогатого скота, были эффективны в подавлении острого панкреатита [24].Несколько других исследований на животных, включая модель на морских свинках с индуцированным таурохолатом некротическим панкреатитом, также показали пользу от использования ингибиторов протеазы, таких как хлорофилл-а [25, 26]. Интересно, однако, что в модели тяжелого геморрагического панкреатита с добавлением холин-дефицитного DL-этионина (CDE) ни тразилол, ни хлорофилл-а не приводили к снижению заболеваемости или смертности [27]. Несмотря на использование ингибиторов протеаз во время индукции острого панкреатита CDE, разница в скорости, степени и высвобождении внутриклеточной протеазы, а также степени и / или проникновения лекарственного средства в ткань, связанная с различными экспериментальными моделями, может способствовать наблюдаемым противоположным результатам. [23].Тем не менее, более позднее исследование более соответствовало результатам клинических испытаний, обсуждаемых ниже.
Противовоспалительные и иммуномодуляторы
При экспериментальном остром панкреатите обнаружены измененные продукты метаболизма арахидоновой кислоты [28]. При остром панкреатите уровни тромбоксана B повышены, тогда как уровни простагландина E (PGE) снижены. Было показано, что терапия PGE оказывает защитное действие на течение экспериментального острого панкреатита на моделях грызунов с таурохолатами, диетой CDE или панкреатитом, индуцированным церулеином [29–31].Ингибиторы циклооксигеназы, такие как индометацин, использовались для лечения экспериментального острого панкреатита с противоречивыми результатами в более ранних исследованиях [32], но последующие исследования подтвердили положительный эффект индометацина, особенно при его использовании на ранней стадии или до индукции заболевания на моделях крыс с индуцированным таурохолатом. острый панкреатит [33,34]. Подобно циклооксигеназе, липоксигеназа находится ниже арахидоновой кислоты, и исследования показали, что ее ингибирование на моделях крыс с острым панкреатитом, индуцированным таурохолатами, приводит к снижению тяжести заболевания [35].Однако было показано, что антагонизм к лейкотриеновым рецепторам либо ухудшает, либо не влияет на острый панкреатит у крыс [33,36], что указывает на сложность этого пути и необходимость дальнейших углубленных исследований.
Стероидная терапия при остром панкреатите представляет интерес в течение нескольких десятилетий из-за связанной с ней активации лейкоцитов и высвобождения воспалительных цитокинов и хемокинов во время прогрессирования острого панкреатита. Одно экспериментальное исследование на крысах с острым панкреатитом, вызванным церулеином, показало, что эффективность стероидной терапии зависит от тяжести заболевания, причем дексаметазон более эффективен против панкреатита с тяжелым воспалением [37].Другое экспериментальное исследование показало, что дексаметазон уменьшал повреждение поджелудочной железы при профилактическом применении за счет снижения экспрессии молекулы-1 межклеточной адгезии, но был неэффективен в предотвращении рекрутирования лейкоцитов в поджелудочную железу при терапевтическом введении крысам с острым панкреатитом, индуцированным таурохолатами [38]. С другой стороны, стероиды также считаются причиной острого панкреатита, и некоторые исследования показывают, что высокие дозы гидрокортизона могут увеличивать смертность и частоту осложнений, таких как сепсис или инфекция [39–43].
Исследования на животных показали, что интерлейкин-10 (ИЛ-10), противовоспалительный цитокин, может уменьшить тяжесть церулеин-индуцированного острого панкреатита на моделях грызунов, если его вводить до или после индукции заболевания [44]. IL-10 играет защитную роль в местных и системных последствиях заболевания, поскольку было показано, что IL-10 блокирует воспаление, что приводит к улучшению результатов в экспериментальных моделях [45]. Лексипафант, антагонист фактора активации тромбоцитов [46], вызывает системные эффекты и участвует в качестве медиатора в прогрессировании острого панкреатита [47].Исследования показали, что лечение лексипафантом моделей панкреатита на грызунах, индуцированных тауродезоксихолатом и церулеином, снижает тяжесть связанных с панкреатитом осложнений, таких как кишечная дисфункция, системная активация ИЛ-1 и локальное рекрутирование лейкоцитов [48]. Лексипафант уменьшил воспаление, ассоциированное с острым панкреатитом [49], и уменьшил острый некротический панкреатит [50]. Несмотря на положительные результаты применения ИЛ-10 и лексипафанта в исследованиях на животных, их перевод в клиническое использование оказался сложной задачей.
Антиоксиданты
Окислительный стресс и травмы участвуют во многих воспалительных заболеваниях. Свободные радикалы, полученные из кислорода, образуются при экспериментальном остром панкреатите [51], и есть данные о снижении уровня антиоксидантов в крови у пациентов с тяжелым острым панкреатитом [52]. Эти наблюдения привели к экспериментальным исследованиям, которые показали защитный эффект экзогенно вводимых антиоксидантов, таких как селен, за счет уменьшения повреждения поджелудочной железы [53]. Доклинические исследования на грызунах с моделями острого панкреатита, вызванного различными методами, включая инъекцию каррагинана в плевральную полость или л -аргинина гидрохлорида, показали снижение уровня глутатиона и повышение уровня окисленного глутатиона, что свидетельствует о пользе этого вмешательства [ 54].Клинические исследования, которые будут подробно обсуждаться ниже, однако, не дали положительных результатов, и может оказаться, что антиоксиданты более полезны для профилактики и / или в качестве синергических агентов.
Возможные будущие многообещающие терапевтические цели
Одним из основных ограничений доклинических исследований является неопределенность и отсутствие идеальной модели, которая воспроизводит все аспекты болезни человека. Кроме того, доклиническая терапия часто назначается либо на ранней стадии, либо во время индукции острого панкреатита, тогда как на самом деле пациенты часто обращаются с текущим или поздним началом острого панкреатита.Доклинические исследования, демонстрирующие эффективность терапии при назначении препарата после прогрессирования заболевания, с большей вероятностью дадут многообещающие результаты в клинических испытаниях. За исключением острого панкреатита, вызванного ЭРХПГ, при котором можно назначить профилактическую терапию, маловероятно, что агенты, препятствующие возникновению острого панкреатита, будут эффективными, а скорее те, которые нацелены на последующее повреждение, восстановление или воспалительные пути. быть полезным при лечении острого панкреатита.По этой причине мы обсуждаем несколько многообещающих доклинических исследований, нацеленных на эти пути.
Считается, что индуцируемая активность синтазы оксида азота увеличивается при экспериментальном остром панкреатите [55]. Экспериментальные исследования на модели крыс показали, что такие агенты, как S -метилизотиомочевина, индуцибельный ингибитор синтазы оксида азота, могут уменьшать бактериальную транслокацию из кишечника в панкреонекроз, тем самым снижая септические осложнения и смертность при остром панкреатите [56].Лечение такими агентами, как AR-C102222AA или L – N 6 – (1-иминоэтил) -лизин, высокоселективные ингибиторы iNOS, в начале курса после индукции острого панкреатита также показали значительный положительный эффект. эффекты при остром панкреатите у австралийских опоссумов [57] и могут иметь терапевтический эффект за счет уменьшения повреждения поджелудочной железы в будущих клинических исследованиях.
Экспериментальные исследования пентоксифиллина и гепарина показали защитный эффект на моделях крыс с острым панкреатитом.Исследования показали, что пентоксифиллин ослабляет активацию нейтрофилов, провоспалительную передачу сигналов, системное воспаление и уровни цитокинов при экспериментальном остром панкреатите, особенно при раннем введении [58]. Гепарин также представляет собой фармакологическую терапию, вызывающую интерес в последнее время, и растет число сообщений, предполагающих его потенциал в лечении острого панкреатита. Первоначально гепарин изучался в первую очередь из-за его способности улучшать микроциркуляцию, учитывая, что нарушение микроциркуляции способствует воспалительному процессу острого панкреатита.Механизм антикоагуляции гепарина также связан с его противовоспалительным действием, частично вторичным по отношению к снижению стимуляции макрофагов и моноцитов [59]. Экспериментальные исследования показывают, что добавление гепарина приводит к снижению амилазы, эндотелина-1 и воспалительных цитокинов, таких как TNFα, активации NF-κB, а также к улучшению морфологических изменений и сосудистого кровотока в поджелудочной железе [60]. Такие агенты могут улучшить заживление, ослабляя провоспалительные пути, и могут принести пользу при клиническом остром панкреатите.
Повышающая регуляция гемооксигеназы-1 (НО-1) или лечение ее последующими эффекторами и продуктами разложения гема, биливердин и монооксид углерода оказывают защитное действие на различных моделях острого панкреатита на грызунах, индуцированного диетой с таурохолатом, церулеином или CDE [61 -66]. Макрофаги со сверхэкспрессией HO-1 защищают от острого панкреатита [61,67]. Панхематин, одобренный FDA препарат гемина для лечения острой перемежающейся порфирии, может стимулировать выработку HO-1 [68]. Исследования показали, что пангематин, если его назначить до развития экспериментального панкреатита, может активировать гемин-активированные макрофаги и привести к меньшему повреждению поджелудочной железы, а если его назначить после развития острого панкреатита, он также может уменьшить степень повреждения, связанного с панкреатитом [63].Примечательно, что мононуклеарные клетки периферической крови пациентов с острым панкреатитом легкой степени обладают обратимой повышающей регуляцией HO-1, которая связана с клиническим выздоровлением, поддерживая терапевтический потенциал HO-1 и продуктов распада гема у пациентов с острым панкреатитом. Биливердин через рецептор арилуглеводородов активирует IL-22 [66]. В последнее время возник большой интерес к роли IL-22, цитокина, продуцируемого гемопоэтическими клетками, нацеленного на неиммунные клетки [66].Интересно, что поджелудочная железа имеет самую высокую экспрессию рецептора IL-22 среди любых других тканей [69], и было показано, что лечение IL-22 улучшает экспериментальный острый панкреатит [70]. Таким образом, HO-1 и его нижестоящие эффекторы являются потенциальными мишенями для клинического острого панкреатита.
TNFα играет центральную роль в патогенезе местных и отдаленных осложнений острого панкреатита [71], а его блокада улучшает экспериментальный острый панкреатит, вызванный церулеином, таурохолатом или диетой CDE в исследованиях на мышах [72,73].Хотя теоретически существует повышенный риск инфекционных осложнений при терапии анти-TNF, есть сообщения о случаях с положительным исходом у пациентов с острым панкреатитом, которые получали анти-TNF из-за сопутствующего заболевания, для которого была показана терапия против TNF [74,75] . Таким образом, при тщательном отборе пациентов вполне вероятно, что терапия анти-TNF даст положительные результаты в клинических испытаниях.
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Основываясь на патофизиологии острого панкреатита и проведенных фундаментальных научных исследованиях, дающих доказательства перспективной фармакологической терапии, было проведено множество клинических исследований для оценки эффективности этих методов лечения, включая антисекреторные агенты, ингибиторы протеазы, иммуномодуляторы, антисекреторные препараты. -воспалительные агенты и антиоксиданты.
Антисекреторные агенты
Впервые об использовании глюкагона при остром панкреатите в 1971 году сообщили Knight et al [76], и с тех пор несколько последующих неконтролируемых клинических испытаний показали клиническое улучшение, уменьшение боли и снижение уровня ферментов. мероприятия при остром панкреатите [77-79]. Однако в последующем двойном слепом исследовании с участием 69 пациентов было обнаружено, что глюкагон не оказывает значительного влияния на смертность пациентов по сравнению с плацебо [80]. Дальнейшие клинические испытания не выявили различий в смертности и заболеваемости, таких как боль и продолжительность пребывания в стационаре [81,82].
Атропин также изучался в рандомизированном клиническом исследовании, но не оказал значительного влияния на клиническое течение пациентов по сравнению с отсутствием лечения [83]. Считалось также, что вливание кальцитонина лосося сильно подавляет секрецию желудочного сока, такую как желудочная кислота, пепсин и гастрин [84-86], а также секрецию ферментов поджелудочной железы, стимулируемую различными стимуляторами секреции, не влияя на секрецию жидкости и электролитов [87], таким образом смягчая патогенез. острого панкреатита [88].Многоцентровое рандомизированное двойное слепое исследование по оценке использования синтетического кальцитонина лосося при остром панкреатите показало, что, хотя смертность не изменилась, количество пациентов без боли и нормализованной сывороточной амилазы было выше в группе лечения по сравнению с группой плацебо. Другие параметры, такие как доза анальгетика, количество лейкоцитов и нормализация семи клинических и лабораторных критериев, показали положительную динамику в группе лечения, но не были клинически значимыми [88].
Клинические испытания хорошо изучили использование соматостатина для лечения острого панкреатита, учитывая, что он подавляет экзокринную секрецию поджелудочной железы, снижает внутренний кровоток, стимулирует ретикулоэндотелиальную систему печени и модулирует каскад воспалительных цитокинов [89].Однако несколько рандомизированных клинических исследований не показали клинически значимого преимущества соматостатина [90–94]. С другой стороны, метаанализ семи публикаций действительно показал улучшение общей смертности от соматостатина при тяжелом остром панкреатите (OR = 0,36, 95% CI: 0,2-0,64), но не было значительного снижения частоты осложнений у пациентов с острый панкреатит [95].
Октреотид, синтетический аналог соматостатина, также прошел клинические испытания. Хотя первоначальные небольшие исследования не показали какого-либо общего улучшения показателей смертности, они предположили снижение тяжести острого панкреатита, уменьшение местных осложнений и более ранний возврат к пероральному приему [96].Однако одно из крупнейших клинических испытаний с участием 302 пациентов с панкреатитом средней и тяжелой степени не показало какой-либо клинической пользы [97], но меньшее исследование с участием 50 пациентов с тяжелым острым панкреатитом показало клинически значимое снижение частоты сепсиса (76–24%). , ОРДС (56–28%), пребывание в больнице (33,1–20,6 дня) и смертность (8–2 смерти) [98]. В то время как более старый проведенный метаанализ действительно показал улучшение смертности от тяжелого острого панкреатита (OR = 0,57, 95% ДИ: 0,35–0,88) [95], другой более свежий метаанализ, ограничивавший их оценку четырьмя исследованиями более высокого качества, не дал показать какие-либо преимущества в отношении сепсиса, смертности или осложнений [99].
Таким образом, клинические исследования, оценивающие использование антисекреторных агентов, предоставили неубедительные доказательства их преимуществ. По всей видимости, пользы от этих агентов при легком остром панкреатите нет, а при тяжелом остром панкреатите польза не ясна. Следовательно, эти агенты в настоящее время не рекомендуются в клинической практике [4,100].
Ингибиторы протеазы
Одним из первых изученных ингибиторов протеаз является апротинин, и первоначальные исследования показали некоторое улучшение показателей смертности, хотя последующие исследования не смогли повторить такие результаты [101,102].Исследования доставки апротинина через перитонеальный лаваж показали меньший некроз в экспериментальной группе со снижением активации комплемента (в частности, меньше C3a и больше уровней ингибитора C1 в плазме), но нет общей разницы в смертности [103-105]. Апротинин все еще может играть роль в лечении острого панкреатита, учитывая, что он не вводился в достаточно высоких дозах, чтобы вызвать достаточное ингибирование активности протеазы, а исследования не имели достаточной мощности [106].
Габексат мезилат представляет собой меньший ингибитор протеазы, который изучался в клинических испытаниях на людях [107].В то время как ранние более мелкие клинические исследования предполагали снижение смертности от применения этой терапии [108, 109], более крупное рандомизированное контролируемое исследование пациентов с умеренным и тяжелым острым панкреатитом не обнаружило клинической пользы [110, 111]. Два других метаанализа также демонстрируют отсутствие преимущества в отношении смертности, хотя они показали снижение потребности в хирургическом вмешательстве и меньшее количество осложнений [95, 112]. Недавнее исследование показало некоторую пользу габексата при непрерывной регионарной артериальной инфузии (CRAI) [113].
Нафомостат – новый синтетический ингибитор протеазы, в сто раз более мощный, чем габексат [107]. Клинические исследования, оценивающие доставку нафомостата через CRAI вместе с антибиотиками, показали более высокую смертность и меньшую частоту некроза при более раннем введении препарата [114]. Исследования также показали, что доставка лекарства через CRAI по сравнению с не-CRAI снижает потребность в хирургическом вмешательстве и улучшает выживаемость [115,116].
Ни один из упомянутых выше ингибиторов протеазы в настоящее время не является частью стандартной клинической помощи при лечении острого панкреатита, поскольку необходимы более масштабные и адекватно обоснованные исследования, прежде чем их рекомендовать для клинического использования.Нафомостат, однако, является наиболее перспективным из трех, особенно при введении через CRAI в сочетании с антибиотиками.
Иммуномодуляторы
На основании положительных доклинических результатов Лексипафант прошел клинические испытания у пациентов с тяжелым острым панкреатитом. Первое клиническое испытание, оценивающее использование этой терапии, не показало разницы в смертности, но показало снижение органной недостаточности [117]. Другое исследование показало значительно меньшую органную недостаточность, снижение смертности и ССВО [118].Однако самое крупное рандомизированное клиническое исследование, включающее эту терапию, не показало значительного снижения органной недостаточности или местных осложнений, что привело к выводу, что лексипафант сам по себе не может лечить тяжелый острый панкреатит [119].
Дотрекогин альфа, аналог эндогенного протеина С, показал некоторые преимущества при лечении острого панкреатита [120]. Эндогенный протеин С вырабатывается в печени и ингибирует образование тромбина и облегчает тромболизис. Учитывая, что более низкие уровни активированного протеина C связаны с более высокой смертностью при остром панкреатите, активированный протеин C, как полагали, смягчает тяжелый острый панкреатит, модулируя иммунную систему через регулирование взаимодействия лейкоцитов с эндотелием и митоген-активированными киназами и улучшая кишечную микроциркуляцию [121].Первые сообщения о клинических случаях показали некоторую пользу от использования дотрекогина альфа при остром панкреатите [122], но последующее пилотное исследование не показало каких-либо клинически значимых различий с использованием дотрекогина альфа [123].
Противовоспалительные средства
Индометацин, который ингибирует активность фосфолипазы A2 и активность циклооксигеназы, уменьшая, таким образом, нейтрофильно-опосредованное воспаление, был клинически изучен на основе более ранних доклинических исследований [124]. Однако одно исследование, оценивающее эту терапию, сообщило только об уменьшении боли и употреблении опиатов при назначении пациентам с острым панкреатитом [125], предполагая обезболивающее, но не связанное с противовоспалительным действием.До сих пор преимущества индометацина в значительной степени ограничивались панкреатитом после ЭРХПГ [126].
Стероидная терапия широко используется для уменьшения воспаления в различных системах органов. Хотя было показано, что стероидная терапия эффективна при лечении аутоиммунного панкреатита [127], однако при остром панкреатите стероидная терапия участвует в индукции заболевания [128]. Посмертное исследование, проведенное Carone и Liebow, показало гистологические доказательства острого панкреатита или перипанкреатического некроза жира у 16 из 54 пациентов, получавших стероиды [129].Первые сообщения о случаях также связывают использование стероидов с острым панкреатитом [130]. Исследования также показали, что кортикостероиды не имеют положительного эффекта в профилактике панкреатита после ЭРХПГ [131]. Однако, учитывая, что некоторые доклинические исследования предполагают, что стероиды могут уменьшать воспалительный каскад, рекрутирование лейкоцитов и последующее повреждение поджелудочной железы при профилактическом применении [38], необходимы дальнейшие хорошо спланированные исследования.
Антиоксидантные агенты
В нескольких клинических испытаниях оценивалась польза антиоксидантных агентов при остром панкреатите с учетом роли активных форм кислорода и клеточного повреждения при остром панкреатите, а также доказательств, полученных в ходе доклинических исследований.Изученные антиоксиданты включают н-ацетилцистеин, метионин, бета-каротин, селен, аскорбиновую кислоту и альфа-токоферол.
Рандомизированное клиническое испытание, оценивающее лечение ацетилцистеином, селеном и витамином С, показало повышение уровня антиоксидантов в сыворотке и снижение маркеров окислительного стресса, но не улучшило дисфункцию органов [132]. Другое исследование с пациентами, получавшими витамин С, н-ацетилцистеин и другие антиоксиданты, не показало значительной разницы в частоте осложнений или продолжительности пребывания в больнице [133].Третье недавнее клиническое исследование витаминов A, C и E также не показало значительных различий в дисфункции органов [134].
Исследования по оценке использования глутамина, более мощного антиоксиданта, были более многообещающими. Одно исследование, в котором 80 пациентов были рандомизированы для приема глутамина, показало уменьшение количества осложнений, продолжительности госпитализации, необходимости в хирургическом вмешательстве и смертности при введении препарата на раннем этапе после госпитализации [135]. Метаанализ рандомизированных контрольных исследований глутамина показал улучшение показателей смертности (ОР = 0.3, 95% ДИ: 0,15–0,6) и снижение инфекционных осложнений (ОР = 0,58, 95% ДИ: 0,39–0,87), но без разницы в продолжительности пребывания в больнице. Польза от глутамина наблюдалась только у пациентов, получавших полное парентеральное питание [136]. Таким образом, роль антиоксидантной терапии при остром панкреатите еще предстоит определить.
Другие методы лечения
В клинических исследованиях также оценивались различные другие методы лечения острого панкреатита. Считается, что антифибринолитики, такие как эпсилон-аминокапроновая кислота (EPCA), улучшают патогенез острого панкреатита, подавляя активацию плазминогена, плазмина и трипсина, подавляя калликреин поджелудочной железы и повышая активность антитрипсина в сыворотке [137].Однако клиническое исследование, оценивающее использование EPCA и апротинина при остром панкреатите, не показало какого-либо клинически значимого улучшения исходов, таких как продолжительность госпитализации и нормализация лабораторных показателей, по сравнению с группой обычного лечения и группами лечения апротинином [138].
Свежезамороженная плазма (СЗП) также оценивалась при лечении острого панкреатита с учетом лабораторных исследований, которые показали ингибирующее действие СЗП на протеолитическую активность в сыворотке крови пациентов с острым панкреатитом [139].В то время как одно первоначальное проспективное пилотное клиническое исследование показало снижение смертности при приеме СЗП у пациентов с острым панкреатитом при введении в течение первых пяти дней от начала заболевания [139], более крупное многоцентровое контролируемое клиническое исследование не показало улучшения клинических результатов в группа, получавшая СЗП, в отличие от группы, получавшей коллоиды [140].
Молекулярные пути развития мишеней включают калликреин-кинин и систему комплемента, учитывая, что тяжелый острый панкреатит связан с повышенными уровнями C3a и sC5b-9 [141].Ингибитор C1-эстеразы блокирует множество протеолитических ферментов, включая активированный C1-комплекс и калликреин [142], и как экспериментальные исследования, так и небольшие исследования на людях показали, что ингибитор C1-эстеразы обладает некоторым защитным действием при тяжелом остром панкреатите [143]. В настоящее время фармакологические мишени системы комплемента используются при множестве других заболеваний, таких как наследственный ангионевротический отек, пароксизмальная ночная гемоглобинурия и гемолитико-уремический синдром [144], которые могут способствовать более быстрой трансляции.
ЗАКЛЮЧЕНИЕ
Доклинические и клинические исследования (Таблицы и) показали многообещающие возможности для новой фармакологической терапии острого панкреатита, которая может дополнять традиционное лечение, включающее поддерживающие меры, такие как жидкостная реанимация, нутритивная поддержка, контроль боли и антибиотики, такие как нужный. Доклинические и клинические исследования показали многообещающие возможности применения различных классов терапии, которые включают антисекреторные агенты, ингибиторы протеаз, иммуномодуляторы и противовоспалительные агенты, а также антиоксиданты.Хотя некоторые доказательства в пользу этих методов лечения все еще остаются неубедительными и не были переведены в текущие стандартные методы лечения, существует огромная потенциальная терапевтическая польза, как продемонстрировано в этих исследованиях. Иммуномодулирующие фармакологические методы лечения также еще предстоит превратить в стандартную клиническую помощь при остром панкреатите [67].
Таблица 1
Резюме фармакологических агентов, изученных при экспериментальном остром панкреатите
| Фармакологическое средство | Модель на животных | Оценка результатов | 4 Цитаты | Механизм индукции панкреатита | ||
| Антисекреторные агенты | ||||||
| Глюкагон | Собака | Обструкция двенадцатиперстной кишки, инфузия протока поджелудочной железы 48 инфузия раствора лактатного протока 4 или инфузия протока поджелудочной железы 4 полезен по сравнению с простой объемной реанимацией | [15] | |||
| Свинья | Геморрагический панкреатит, вызванный инъекцией желчи в проток поджелудочной железы | Сниженная смертность | [16] | атин|||
| Таурохолат | Отсутствие снижения смертности | [21, 22] | ||||
| Ингибиторы протеаз | ||||||
| Апротинин | Собака | Геморрагический панкреатит | 906– терапевтический потенциал 906 Геморрагический панкреатит, терапевтический потенциал 904–197 ]||||
| Хлорофилл-а | Морская свинка | Таурохолат-индуцированный некротический панкреатит | Выживаемость | [25-27] | ||
| Противовоспалительная терапия | 448470 P448470 мышиТаурохолат, диета CDE или церулеин | Защитный эффект | [29-31] | |||
| Индометацин | Крыса | Оливковое масло или таурохолат | , особенно в раннем возрасте] | |||
| Ингибитор липоксигеназы | Крыса | Таурохолевая кислота 9 0470 | Защитный эффект | [35] | ||
| Стероид | Крыса | Церулеин и таурохолат | Уменьшение воспаления и защитное действие | [37-43] | ||
| [37-43] | ||||||
| [37-43] | ||||||
| Caer 9048 IL-10 | Снижение степени тяжести заболевания | [44, 48-50] | ||||
| Лексипафант | Крыса, мыши | Внутрипротоковое введение 5% тауродезоксихолата или церулеина натрия | Снижение степени тяжести SIR | , бактериальная транслокация | [46, 47] | |
| Гемин / пангематин / биливердин / CO / IL-22 | Крыса, мыши | диета с церулеином, таурохолатом или CDE | Защитные и терапевтические эффекты | [61-67] | ||
| Анти-TNF альфа | Мыши | диета с церулеином, таурохолатом или CDE | Снижение воспалительной реакции и гибели клеток | [72-75] 904 70 | ||
| Антиоксиданты | ||||||
| Tempol | Мыши | каррагинан, введенный в плевральную полость | Снижение воспаления и шока | [54] | ||
| Селен | гидрохлорид 9048 Селен Хлор6 9048 Селен 9048 Уменьшение травмы поджелудочной железы[53, 145] | |||||
Таблица 2
Резюме фармакологических агентов, изученных при клиническом остром панкреатите
| Фармакологическое средство | 70 Дизайн выборки 903 | Оценка результатов | Цитаты | ||||||||
| Снижение SIRS | Снижение органной недостаточности | Снижение продолжительности пребывания | 9018 Снижение продолжительности пребывания 470 9018 9018 904 90 466Антисекреторные агенты | ||||||||
| Глюкагон | РКИ | 22-69 | Не сообщалось | Не сообщалось | Нет | Нет | [76-82] | 51 | Не сообщалось | Не сообщалось | Нет | Нет | [83] |
| Кальцитонин | RCT | 94 | Не сообщалось | Не сообщалось | Не сообщалось | Не сообщалось | ↓ боль, более ранняя нормализация лабораторных показателей | [84-86] | |||
| Соматостатин | РКИ / метаанализ | 50-703 | Не сообщалось | Неопределено (не влияет на полиорганную недостаточность, но ↓ местные осложнения) | Неопределенный | Неопределенный | ↓ абсцесс и некроз поджелудочной железы, ↓ местное воспаление | [90-95] | |||
| Октреотид | РКИ / метаанализ | 19–948 | Да | Да | Неопределенный | Неопределенный | [97-99] | ||||
| 48-105 | Не сообщалось | Нет | Да | Нет | ↓ панкреонекроз, ↓ активация комплемента | [101-105] | |||||
| Анализ мезилата Gabexate | 42-898 | Не сообщалось | Нет | Нет | Нет | CRAI ↓ пребывание в больнице и SIRS | [108-113] | ||||
| Нафомостат | RCT | инфекция некротической ткани поджелудочной железы) | Не сообщается | Не сообщается | Да | Только CRAI + abx имеет преимущество | [114-11 6] | ||||
| Иммуномодуляторы | |||||||||||
| Lexipafant | РКИ | 50-290 | Да | Да | Не сообщалось | Да | 117-1190 ] | ||||
| Dotrecogin alfa | RCT | 32 | Да | Нет | Не сообщается | Нет | [122, 123] | ||||
| Acety | 39-53 | Неопределенный (↓ CRP, но не sig) | Нет (тенденция к ↑ MOF) | Нет | Нет | [132-134] | |||||
| Глютамин | RCT / мета-анализ | 505 | Да | Да | Нет | Да | [135, 136] | ||||
Есть также новые цели для p хармакологическая терапия, которая может расширить возможности лечения острого панкреатита.Стратегии, которые изменяют активность ключевых иммунных клеток в воспалительном каскаде, вызванном острым панкреатитом, имеют большой потенциал [67]. Другие молекулярные мишени, такие как те, которые мешают калликреин-кининовой, протеолитической и системе комплемента, как обсуждается при дальнейших разработках, потенциально могут быть применены и к острому панкреатиту в будущем. В дополнение к расширению целей фармакологической терапии, существующие методы лечения должны быть лучше изучены в клинических испытаниях в будущем.Экспериментальные доклинические исследования выявили несколько методов лечения, которые не доказали свою эффективность в клинических испытаниях и, таким образом, не были переведены на клиническую арену. Одна из причин этого несоответствия может заключаться в том, что в моделях на животных фармакологическая терапия часто назначается до того, как наступает повреждение поджелудочной железы, что дает доказательства того, что терапия может обеспечивать защитный, но не обязательно терапевтический эффект.
В клинических исследованиях, однако, интересующее лекарство часто тестируется после того, как повреждение поджелудочной железы уже произошло и воспалительный каскад, вызванный острым панкреатитом, уже начался.В будущем улучшенный дизайн клинических испытаний, в рамках которых лечение будет проводиться раньше, с момента появления симптомов, может максимизировать способность препарата прерывать воспалительный каскад и давать лучшие результаты. Клинические испытания также необходимо стандартизировать в отношении критериев отбора, поддерживающих подходов к лечению и измеряемых результатов. Следует четко указать клинически значимые первичные и вторичные исходы, такие как смертность, органная недостаточность, ССВО, некроз поджелудочной железы и местные осложнения, продолжительность пребывания в больнице, потребность в обезболивающих, качество жизни и стоимость лечения.
Несмотря на неубедительные доказательства терапевтического эффекта многих изученных к настоящему времени фармакологических методов лечения острого панкреатита, существует большая потребность и перспективность в разработке эффективной фармакологической терапии острого панкреатита. Лучшее понимание патофизиологии заболевания и уроки, извлеченные из прошлых клинических исследований, предлагают отличную основу для расширения, так что текущее лечение панкреатита, в значительной степени характеризующееся поддерживающей терапией, может в конечном итоге быть переведено не только на профилактическую, но и на репаративную и эффективную терапию. .Лучшая характеристика и стандартизация популяции пациентов, наряду с хорошо контролируемыми и адекватно обоснованными клиническими исследованиями, привязанными к стандартизованным результатам, обеспечат надежную и достоверную оценку терапевтической роли доклинических испытанных агентов.
Фармакологическая терапия острого панкреатита
Abstract
В то время как консервативное лечение, такое как введение жидкости, покой кишечника и антибиотики, является основой текущего лечения острого панкреатита, есть много перспектив в фармакологической терапии, которая нацелена на различные аспекты патогенеза панкреатит.Обсуждается обширный обзор доклинических исследований, которые включают оценку методов лечения, таких как антисекреторные агенты, ингибиторы протеаз, противовоспалительные агенты и антиоксиданты. Многие из этих исследований показали терапевтическую пользу и улучшение выживаемости на экспериментальных моделях. На основе имеющихся доклинических исследований мы обсуждаем потенциальные новые целевые фармакологические подходы, которые могут быть многообещающими при лечении острого панкреатита. На сегодняшний день различные клинические исследования оценили трансляционный потенциал эффективных экспериментальных методов лечения на животных моделях и показали либо неудачные, либо смешанные результаты в исследованиях на людях.Несмотря на эти обескураживающие клинические исследования, существует большая клиническая потребность и существует несколько доклинических эффективных методов лечения, которые ждут исследования на пациентах. Лучшее понимание патофизиологии острого панкреатита и уроки, извлеченные из прошлых клинических исследований, вероятно, станут хорошей основой для расширения будущих методов лечения острого панкреатита.
Ключевые слова: Острый панкреатит, Антисекреторы, Ингибиторы протеазы, Противовоспалительные, Антиоксиданты, Синдром системной воспалительной реакции, Органная недостаточность, Смертность
Основной совет: В настоящее время нет утвержденных методов лечения острого панкреатита.В этом обзоре суммируются и обсуждаются доклинические и клинические исследования острого панкреатита, а также обсуждаются потенциальные многообещающие методы лечения.
ВВЕДЕНИЕ
В США в 2009 году у более 274000 пациентов был диагностирован острый панкреатит, что делает его наиболее распространенным желудочно-кишечным заболеванием, требующим острой госпитализации с затратами на лечение, превышающими 2,5 миллиарда долларов в год [1]. Прогноз для пациентов с острым панкреатитом в значительной степени определяется наличием органной недостаточности и инфицированного панкреонекроза с соответствующими показателями смертности 15-30% [2].Другие осложнения панкреатита включают синдром системного воспалительного ответа (SIRS), сепсис и острый респираторный дистресс-синдром (ARDS). Несмотря на рост заболеваемости [3], в настоящее время нет доступной фармакологической терапии для смягчения заболевания и его течения. Текущее лечение панкреатита в основном является поддерживающим. Лечение органной недостаточности состоит из поддерживающих мероприятий [4], в то время как лечение инфицированного панкреонекроза состоит из дренирования или санации раны и антибиотиков [5].
Самыми частыми причинами острого панкреатита у западного населения являются алкоголь и камни в желчном пузыре, но также описаны многие другие причины, и независимо от триггера существует основной общий патогенетический исход [6,7]. Считается, что острый панкреатит представляет собой местный воспалительный процесс, включающий преждевременную внутриклеточную активацию пищеварительных ферментов в ацинарных клетках, ведущую к самоперевариванию ткани, которое может прогрессировать и вовлекать отдаленные органы. Также считается, что секреторные ацинарные клетки выделяют хемокины и цитокины, которые привлекают лейкоциты, вызывая воспалительный ответ, ответственный за отек поджелудочной железы и накопление нейтрофилов [8].Этот интерстициальный отек иногда может прогрессировать до некроза части поджелудочной железы и возможной бактериальной инфекции. Острый панкреатит также может влиять на микрососудистое кровообращение и нарушать перфузию и оксигенацию тканей [9]. Хотя поддерживающая терапия в значительной степени является единственным доступным лечением этого заболевания, исследования панкреатита и лучшее понимание патофизиологии привели к разработке некоторых фармакологических методов лечения, нацеленных на различные этапы патогенеза панкреатита.В обзоре, опубликованном в 2008 г., описаны некоторые фармакологические методы лечения, исследованные на экспериментальных моделях животных [10]. С тех пор некоторые из этих методов лечения были дополнительно изучены, новые лекарства были обнаружены в каждом классе терапии, и было проведено больше клинических исследований на людях, оценивающих клиническую полезность этих методов лечения.
Этот обзор посвящен новейшим фармакологическим методам лечения острого панкреатита и не касается фармакологии стандартного лечения, используемого в настоящее время, такого как обезболивание и антибиотики.В статье резюмируются экспериментальные доклинические исследования, которые предоставляют доказательства терапевтического потенциала различных классов новых лекарств, описываются клинические испытания, в которых оценивался их трансляционный потенциал, а также комментарии относительно будущих методов лечения и потенциальных многообещающих агентов, ожидающих перевода в клиническую практику. Этот обзор посвящен фармакологической терапии острого панкреатита, который не является вторичным по отношению к эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ).
МОЛЕКУЛЯРНЫЙ ПАТОГЕНЕЗ ПАНКРЕАТИТА
В физиологических условиях секреция неактивных предшественников ферментов из ацинарных клеток происходит в ответ на цитозольный кальций.Однако устойчивое повышение уровня этого кальция может привести к преждевременной активации и секреции пищеварительных ферментов из ацинарных клеток, что является одним из самых ранних обнаруживаемых событий при панкреатите [11]. После первоначального поражения ацинарной клетки поджелудочной железы прогрессирование заболевания представляет собой многофазный процесс, который включает локальное воспаление поджелудочной железы, за которым следует генерализованный воспалительный ответ и заключительная стадия сепсиса, включающая полиорганную недостаточность у пациентов с тяжелым заболеванием. [8].После первоначального повреждения воспалительные клетки часто рекрутируются в поджелудочную железу через молекул адгезии, что может усугубить воспалительную реакцию, приводящую к тяжелому острому панкреатиту [8]. Одним из ключевых факторов воспалительной реакции при остром панкреатите, вероятно, являются циркулирующие цитокины и хемокины. Активные пищеварительные ферменты являются мощными стимуляторами макрофагов, которые впоследствии вызывают выработку провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNF-α) и интерлейкины [12].
Производство цитокинов регулируется большим количеством факторов транскрипции, наиболее заметным из которых является ядерный фактор, усиливающий легкую каппа-цепь активированных В-клеток (NF-κB) [12]. Различные типы высвобождаемых цитокинов могут вызывать свои эффекты через высокоспецифичных рецепторов клеточной поверхности и стимулировать ферменты, такие как циклооксигеназа-2 и индуцибельная синтаза оксида азота (iNOS), которые опосредуют воспалительный процесс. Следовательно, ингибирование этих ферментов, вероятно, ограничит местное и системное повреждение, вызванное провоспалительными лейкоцитами [12].Активные формы кислорода (ROS) и активные формы азота (RNS) также участвуют в патогенезе острого панкреатита. Механизм, с помощью которого эти агенты вызывают панкреатит, двоякий. АФК и РНС действуют непосредственно на биомолекулы (липиды, белки и нуклеиновые кислоты) и окисляют эти компоненты клеточной мембраны в поджелудочной железе, что приводит к разрушению мембраны и некрозу клеток поджелудочной железы. В дополнение к прямым пагубным окислительным эффектам, ROS и RNS могут также служить вторичными посредниками во внутриклеточной передаче сигналов и вызывать провоспалительные каскады [13].
ПРЕКЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Антисекреторные агенты
Острый панкреатит характеризуется повреждением панкреатической и перипанкреатической жировой ткани, частично опосредованным аутопищеварительными ферментами. Чрезмерная стимуляция экзокринной части поджелудочной железы усугубляет острый панкреатит [9] и, таким образом, является основанием для тестирования антисекреторных агентов в качестве потенциальных методов лечения острого панкреатита. Первоначальные исследования на животных в 1970-х годах тестировали глюкагон, а последующие исследования изучали использование соматостатина и аналога соматостатина длительного действия.
Глюкагон увеличивает кровоток в верхней брыжеечной артерии и снижает экзокринную секрецию поджелудочной железы [14]. Однако исследование с использованием модели панкреатита на собаках не показало, что лечение глюкагоном само по себе или в сочетании с объемной реанимацией лучше, чем только объемная реанимация [15]. Фактически, в их модели кровоизлияние в поджелудочную железу было связано с лечением глюкагоном, что предполагает возможное ухудшение заболевания. В более позднем исследовании на свиньях сообщалось о положительном влиянии глюкагона [16], но другие экспериментальные исследования в дополнение к вышеупомянутому исследованию не подтвердили использование терапии глюкагоном при экспериментальном остром панкреатите [17-19].
Соматостатин – это гормон-ингибитор с множественным действием на перистальтику желудочно-кишечного тракта и внешнесекреторную секрецию поджелудочной железы [20]. Одно доклиническое исследование с использованием таурохолат-индуцированной крысиной модели острого панкреатита показало, что соматостатин эффективен в подавлении базальной и гормональной стимуляции секреции панкреатических ферментов, но не влияет на степень панкреонекроза, отек поджелудочной железы, инфильтрацию лейкоцитов или содержание ферментов в поджелудочная железа после панкреатита индуцировалась и не приводила к общему снижению смертности [21].Другое исследование показало, что соматостатин стимулирует ретикулоэндотелиальную функцию печени и селезенки у крыс, что позволяет предположить пользу при лечении панкреатита [22]. Доклинические исследования показали преимущества использования соматостатина и его аналога длительного действия, что является основой для клинических испытаний, обсуждаемых ниже.
Использование антисекреторных агентов имеет ограничения, учитывая, что поджелудочная железа не только секретирует ферменты, но также секретирует бикарбонат и жидкости, а исследования на животных показали, что стимуляция протоковой секреции бикарбоната оказывает защитное действие на тяжесть панкреатита [23]. ].
Ингибиторы протеаз
Внутрипанкреатическая активация пищеварительных ферментов играет важную роль в патогенезе острого панкреатита. По этой очевидной причине ингибиторы протеазы были и остаются терапевтическим интересом при остром панкреатите. Ранние исследования на собаках с хирургически индуцированным панкреатитом, получавших ингибиторы трипсина из яичного белка или соевых бобов, а также тразилол (апротинин), ингибитор трипсин-калликреин из крупного рогатого скота, были эффективны в подавлении острого панкреатита [24].Несколько других исследований на животных, включая модель на морских свинках с индуцированным таурохолатом некротическим панкреатитом, также показали пользу от использования ингибиторов протеазы, таких как хлорофилл-а [25, 26]. Интересно, однако, что в модели тяжелого геморрагического панкреатита с добавлением холин-дефицитного DL-этионина (CDE) ни тразилол, ни хлорофилл-а не приводили к снижению заболеваемости или смертности [27]. Несмотря на использование ингибиторов протеаз во время индукции острого панкреатита CDE, разница в скорости, степени и высвобождении внутриклеточной протеазы, а также степени и / или проникновения лекарственного средства в ткань, связанная с различными экспериментальными моделями, может способствовать наблюдаемым противоположным результатам. [23].Тем не менее, более позднее исследование более соответствовало результатам клинических испытаний, обсуждаемых ниже.
Противовоспалительные и иммуномодуляторы
При экспериментальном остром панкреатите обнаружены измененные продукты метаболизма арахидоновой кислоты [28]. При остром панкреатите уровни тромбоксана B повышены, тогда как уровни простагландина E (PGE) снижены. Было показано, что терапия PGE оказывает защитное действие на течение экспериментального острого панкреатита на моделях грызунов с таурохолатами, диетой CDE или панкреатитом, индуцированным церулеином [29–31].Ингибиторы циклооксигеназы, такие как индометацин, использовались для лечения экспериментального острого панкреатита с противоречивыми результатами в более ранних исследованиях [32], но последующие исследования подтвердили положительный эффект индометацина, особенно при его использовании на ранней стадии или до индукции заболевания на моделях крыс с индуцированным таурохолатом. острый панкреатит [33,34]. Подобно циклооксигеназе, липоксигеназа находится ниже арахидоновой кислоты, и исследования показали, что ее ингибирование на моделях крыс с острым панкреатитом, индуцированным таурохолатами, приводит к снижению тяжести заболевания [35].Однако было показано, что антагонизм к лейкотриеновым рецепторам либо ухудшает, либо не влияет на острый панкреатит у крыс [33,36], что указывает на сложность этого пути и необходимость дальнейших углубленных исследований.
Стероидная терапия при остром панкреатите представляет интерес в течение нескольких десятилетий из-за связанной с ней активации лейкоцитов и высвобождения воспалительных цитокинов и хемокинов во время прогрессирования острого панкреатита. Одно экспериментальное исследование на крысах с острым панкреатитом, вызванным церулеином, показало, что эффективность стероидной терапии зависит от тяжести заболевания, причем дексаметазон более эффективен против панкреатита с тяжелым воспалением [37].Другое экспериментальное исследование показало, что дексаметазон уменьшал повреждение поджелудочной железы при профилактическом применении за счет снижения экспрессии молекулы-1 межклеточной адгезии, но был неэффективен в предотвращении рекрутирования лейкоцитов в поджелудочную железу при терапевтическом введении крысам с острым панкреатитом, индуцированным таурохолатами [38]. С другой стороны, стероиды также считаются причиной острого панкреатита, и некоторые исследования показывают, что высокие дозы гидрокортизона могут увеличивать смертность и частоту осложнений, таких как сепсис или инфекция [39–43].
Исследования на животных показали, что интерлейкин-10 (ИЛ-10), противовоспалительный цитокин, может уменьшить тяжесть церулеин-индуцированного острого панкреатита на моделях грызунов, если его вводить до или после индукции заболевания [44]. IL-10 играет защитную роль в местных и системных последствиях заболевания, поскольку было показано, что IL-10 блокирует воспаление, что приводит к улучшению результатов в экспериментальных моделях [45]. Лексипафант, антагонист фактора активации тромбоцитов [46], вызывает системные эффекты и участвует в качестве медиатора в прогрессировании острого панкреатита [47].Исследования показали, что лечение лексипафантом моделей панкреатита на грызунах, индуцированных тауродезоксихолатом и церулеином, снижает тяжесть связанных с панкреатитом осложнений, таких как кишечная дисфункция, системная активация ИЛ-1 и локальное рекрутирование лейкоцитов [48]. Лексипафант уменьшил воспаление, ассоциированное с острым панкреатитом [49], и уменьшил острый некротический панкреатит [50]. Несмотря на положительные результаты применения ИЛ-10 и лексипафанта в исследованиях на животных, их перевод в клиническое использование оказался сложной задачей.
Антиоксиданты
Окислительный стресс и травмы участвуют во многих воспалительных заболеваниях. Свободные радикалы, полученные из кислорода, образуются при экспериментальном остром панкреатите [51], и есть данные о снижении уровня антиоксидантов в крови у пациентов с тяжелым острым панкреатитом [52]. Эти наблюдения привели к экспериментальным исследованиям, которые показали защитный эффект экзогенно вводимых антиоксидантов, таких как селен, за счет уменьшения повреждения поджелудочной железы [53]. Доклинические исследования на грызунах с моделями острого панкреатита, вызванного различными методами, включая инъекцию каррагинана в плевральную полость или л -аргинина гидрохлорида, показали снижение уровня глутатиона и повышение уровня окисленного глутатиона, что свидетельствует о пользе этого вмешательства [ 54].Клинические исследования, которые будут подробно обсуждаться ниже, однако, не дали положительных результатов, и может оказаться, что антиоксиданты более полезны для профилактики и / или в качестве синергических агентов.
Возможные будущие многообещающие терапевтические цели
Одним из основных ограничений доклинических исследований является неопределенность и отсутствие идеальной модели, которая воспроизводит все аспекты болезни человека. Кроме того, доклиническая терапия часто назначается либо на ранней стадии, либо во время индукции острого панкреатита, тогда как на самом деле пациенты часто обращаются с текущим или поздним началом острого панкреатита.Доклинические исследования, демонстрирующие эффективность терапии при назначении препарата после прогрессирования заболевания, с большей вероятностью дадут многообещающие результаты в клинических испытаниях. За исключением острого панкреатита, вызванного ЭРХПГ, при котором можно назначить профилактическую терапию, маловероятно, что агенты, препятствующие возникновению острого панкреатита, будут эффективными, а скорее те, которые нацелены на последующее повреждение, восстановление или воспалительные пути. быть полезным при лечении острого панкреатита.По этой причине мы обсуждаем несколько многообещающих доклинических исследований, нацеленных на эти пути.
Считается, что индуцируемая активность синтазы оксида азота увеличивается при экспериментальном остром панкреатите [55]. Экспериментальные исследования на модели крыс показали, что такие агенты, как S -метилизотиомочевина, индуцибельный ингибитор синтазы оксида азота, могут уменьшать бактериальную транслокацию из кишечника в панкреонекроз, тем самым снижая септические осложнения и смертность при остром панкреатите [56].Лечение такими агентами, как AR-C102222AA или L – N 6 – (1-иминоэтил) -лизин, высокоселективные ингибиторы iNOS, в начале курса после индукции острого панкреатита также показали значительный положительный эффект. эффекты при остром панкреатите у австралийских опоссумов [57] и могут иметь терапевтический эффект за счет уменьшения повреждения поджелудочной железы в будущих клинических исследованиях.
Экспериментальные исследования пентоксифиллина и гепарина показали защитный эффект на моделях крыс с острым панкреатитом.Исследования показали, что пентоксифиллин ослабляет активацию нейтрофилов, провоспалительную передачу сигналов, системное воспаление и уровни цитокинов при экспериментальном остром панкреатите, особенно при раннем введении [58]. Гепарин также представляет собой фармакологическую терапию, вызывающую интерес в последнее время, и растет число сообщений, предполагающих его потенциал в лечении острого панкреатита. Первоначально гепарин изучался в первую очередь из-за его способности улучшать микроциркуляцию, учитывая, что нарушение микроциркуляции способствует воспалительному процессу острого панкреатита.Механизм антикоагуляции гепарина также связан с его противовоспалительным действием, частично вторичным по отношению к снижению стимуляции макрофагов и моноцитов [59]. Экспериментальные исследования показывают, что добавление гепарина приводит к снижению амилазы, эндотелина-1 и воспалительных цитокинов, таких как TNFα, активации NF-κB, а также к улучшению морфологических изменений и сосудистого кровотока в поджелудочной железе [60]. Такие агенты могут улучшить заживление, ослабляя провоспалительные пути, и могут принести пользу при клиническом остром панкреатите.
Повышающая регуляция гемооксигеназы-1 (НО-1) или лечение ее последующими эффекторами и продуктами разложения гема, биливердин и монооксид углерода оказывают защитное действие на различных моделях острого панкреатита на грызунах, индуцированного диетой с таурохолатом, церулеином или CDE [61 -66]. Макрофаги со сверхэкспрессией HO-1 защищают от острого панкреатита [61,67]. Панхематин, одобренный FDA препарат гемина для лечения острой перемежающейся порфирии, может стимулировать выработку HO-1 [68]. Исследования показали, что пангематин, если его назначить до развития экспериментального панкреатита, может активировать гемин-активированные макрофаги и привести к меньшему повреждению поджелудочной железы, а если его назначить после развития острого панкреатита, он также может уменьшить степень повреждения, связанного с панкреатитом [63].Примечательно, что мононуклеарные клетки периферической крови пациентов с острым панкреатитом легкой степени обладают обратимой повышающей регуляцией HO-1, которая связана с клиническим выздоровлением, поддерживая терапевтический потенциал HO-1 и продуктов распада гема у пациентов с острым панкреатитом. Биливердин через рецептор арилуглеводородов активирует IL-22 [66]. В последнее время возник большой интерес к роли IL-22, цитокина, продуцируемого гемопоэтическими клетками, нацеленного на неиммунные клетки [66].Интересно, что поджелудочная железа имеет самую высокую экспрессию рецептора IL-22 среди любых других тканей [69], и было показано, что лечение IL-22 улучшает экспериментальный острый панкреатит [70]. Таким образом, HO-1 и его нижестоящие эффекторы являются потенциальными мишенями для клинического острого панкреатита.
TNFα играет центральную роль в патогенезе местных и отдаленных осложнений острого панкреатита [71], а его блокада улучшает экспериментальный острый панкреатит, вызванный церулеином, таурохолатом или диетой CDE в исследованиях на мышах [72,73].Хотя теоретически существует повышенный риск инфекционных осложнений при терапии анти-TNF, есть сообщения о случаях с положительным исходом у пациентов с острым панкреатитом, которые получали анти-TNF из-за сопутствующего заболевания, для которого была показана терапия против TNF [74,75] . Таким образом, при тщательном отборе пациентов вполне вероятно, что терапия анти-TNF даст положительные результаты в клинических испытаниях.
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Основываясь на патофизиологии острого панкреатита и проведенных фундаментальных научных исследованиях, дающих доказательства перспективной фармакологической терапии, было проведено множество клинических исследований для оценки эффективности этих методов лечения, включая антисекреторные агенты, ингибиторы протеазы, иммуномодуляторы, антисекреторные препараты. -воспалительные агенты и антиоксиданты.
Антисекреторные агенты
Впервые об использовании глюкагона при остром панкреатите в 1971 году сообщили Knight et al [76], и с тех пор несколько последующих неконтролируемых клинических испытаний показали клиническое улучшение, уменьшение боли и снижение уровня ферментов. мероприятия при остром панкреатите [77-79]. Однако в последующем двойном слепом исследовании с участием 69 пациентов было обнаружено, что глюкагон не оказывает значительного влияния на смертность пациентов по сравнению с плацебо [80]. Дальнейшие клинические испытания не выявили различий в смертности и заболеваемости, таких как боль и продолжительность пребывания в стационаре [81,82].
Атропин также изучался в рандомизированном клиническом исследовании, но не оказал значительного влияния на клиническое течение пациентов по сравнению с отсутствием лечения [83]. Считалось также, что вливание кальцитонина лосося сильно подавляет секрецию желудочного сока, такую как желудочная кислота, пепсин и гастрин [84-86], а также секрецию ферментов поджелудочной железы, стимулируемую различными стимуляторами секреции, не влияя на секрецию жидкости и электролитов [87], таким образом смягчая патогенез. острого панкреатита [88].Многоцентровое рандомизированное двойное слепое исследование по оценке использования синтетического кальцитонина лосося при остром панкреатите показало, что, хотя смертность не изменилась, количество пациентов без боли и нормализованной сывороточной амилазы было выше в группе лечения по сравнению с группой плацебо. Другие параметры, такие как доза анальгетика, количество лейкоцитов и нормализация семи клинических и лабораторных критериев, показали положительную динамику в группе лечения, но не были клинически значимыми [88].
Клинические испытания хорошо изучили использование соматостатина для лечения острого панкреатита, учитывая, что он подавляет экзокринную секрецию поджелудочной железы, снижает внутренний кровоток, стимулирует ретикулоэндотелиальную систему печени и модулирует каскад воспалительных цитокинов [89].Однако несколько рандомизированных клинических исследований не показали клинически значимого преимущества соматостатина [90–94]. С другой стороны, метаанализ семи публикаций действительно показал улучшение общей смертности от соматостатина при тяжелом остром панкреатите (OR = 0,36, 95% CI: 0,2-0,64), но не было значительного снижения частоты осложнений у пациентов с острый панкреатит [95].
Октреотид, синтетический аналог соматостатина, также прошел клинические испытания. Хотя первоначальные небольшие исследования не показали какого-либо общего улучшения показателей смертности, они предположили снижение тяжести острого панкреатита, уменьшение местных осложнений и более ранний возврат к пероральному приему [96].Однако одно из крупнейших клинических испытаний с участием 302 пациентов с панкреатитом средней и тяжелой степени не показало какой-либо клинической пользы [97], но меньшее исследование с участием 50 пациентов с тяжелым острым панкреатитом показало клинически значимое снижение частоты сепсиса (76–24%). , ОРДС (56–28%), пребывание в больнице (33,1–20,6 дня) и смертность (8–2 смерти) [98]. В то время как более старый проведенный метаанализ действительно показал улучшение смертности от тяжелого острого панкреатита (OR = 0,57, 95% ДИ: 0,35–0,88) [95], другой более свежий метаанализ, ограничивавший их оценку четырьмя исследованиями более высокого качества, не дал показать какие-либо преимущества в отношении сепсиса, смертности или осложнений [99].
Таким образом, клинические исследования, оценивающие использование антисекреторных агентов, предоставили неубедительные доказательства их преимуществ. По всей видимости, пользы от этих агентов при легком остром панкреатите нет, а при тяжелом остром панкреатите польза не ясна. Следовательно, эти агенты в настоящее время не рекомендуются в клинической практике [4,100].
Ингибиторы протеазы
Одним из первых изученных ингибиторов протеаз является апротинин, и первоначальные исследования показали некоторое улучшение показателей смертности, хотя последующие исследования не смогли повторить такие результаты [101,102].Исследования доставки апротинина через перитонеальный лаваж показали меньший некроз в экспериментальной группе со снижением активации комплемента (в частности, меньше C3a и больше уровней ингибитора C1 в плазме), но нет общей разницы в смертности [103-105]. Апротинин все еще может играть роль в лечении острого панкреатита, учитывая, что он не вводился в достаточно высоких дозах, чтобы вызвать достаточное ингибирование активности протеазы, а исследования не имели достаточной мощности [106].
Габексат мезилат представляет собой меньший ингибитор протеазы, который изучался в клинических испытаниях на людях [107].В то время как ранние более мелкие клинические исследования предполагали снижение смертности от применения этой терапии [108, 109], более крупное рандомизированное контролируемое исследование пациентов с умеренным и тяжелым острым панкреатитом не обнаружило клинической пользы [110, 111]. Два других метаанализа также демонстрируют отсутствие преимущества в отношении смертности, хотя они показали снижение потребности в хирургическом вмешательстве и меньшее количество осложнений [95, 112]. Недавнее исследование показало некоторую пользу габексата при непрерывной регионарной артериальной инфузии (CRAI) [113].
Нафомостат – новый синтетический ингибитор протеазы, в сто раз более мощный, чем габексат [107]. Клинические исследования, оценивающие доставку нафомостата через CRAI вместе с антибиотиками, показали более высокую смертность и меньшую частоту некроза при более раннем введении препарата [114]. Исследования также показали, что доставка лекарства через CRAI по сравнению с не-CRAI снижает потребность в хирургическом вмешательстве и улучшает выживаемость [115,116].
Ни один из упомянутых выше ингибиторов протеазы в настоящее время не является частью стандартной клинической помощи при лечении острого панкреатита, поскольку необходимы более масштабные и адекватно обоснованные исследования, прежде чем их рекомендовать для клинического использования.Нафомостат, однако, является наиболее перспективным из трех, особенно при введении через CRAI в сочетании с антибиотиками.
Иммуномодуляторы
На основании положительных доклинических результатов Лексипафант прошел клинические испытания у пациентов с тяжелым острым панкреатитом. Первое клиническое испытание, оценивающее использование этой терапии, не показало разницы в смертности, но показало снижение органной недостаточности [117]. Другое исследование показало значительно меньшую органную недостаточность, снижение смертности и ССВО [118].Однако самое крупное рандомизированное клиническое исследование, включающее эту терапию, не показало значительного снижения органной недостаточности или местных осложнений, что привело к выводу, что лексипафант сам по себе не может лечить тяжелый острый панкреатит [119].
Дотрекогин альфа, аналог эндогенного протеина С, показал некоторые преимущества при лечении острого панкреатита [120]. Эндогенный протеин С вырабатывается в печени и ингибирует образование тромбина и облегчает тромболизис. Учитывая, что более низкие уровни активированного протеина C связаны с более высокой смертностью при остром панкреатите, активированный протеин C, как полагали, смягчает тяжелый острый панкреатит, модулируя иммунную систему через регулирование взаимодействия лейкоцитов с эндотелием и митоген-активированными киназами и улучшая кишечную микроциркуляцию [121].Первые сообщения о клинических случаях показали некоторую пользу от использования дотрекогина альфа при остром панкреатите [122], но последующее пилотное исследование не показало каких-либо клинически значимых различий с использованием дотрекогина альфа [123].
Противовоспалительные средства
Индометацин, который ингибирует активность фосфолипазы A2 и активность циклооксигеназы, уменьшая, таким образом, нейтрофильно-опосредованное воспаление, был клинически изучен на основе более ранних доклинических исследований [124]. Однако одно исследование, оценивающее эту терапию, сообщило только об уменьшении боли и употреблении опиатов при назначении пациентам с острым панкреатитом [125], предполагая обезболивающее, но не связанное с противовоспалительным действием.До сих пор преимущества индометацина в значительной степени ограничивались панкреатитом после ЭРХПГ [126].
Стероидная терапия широко используется для уменьшения воспаления в различных системах органов. Хотя было показано, что стероидная терапия эффективна при лечении аутоиммунного панкреатита [127], однако при остром панкреатите стероидная терапия участвует в индукции заболевания [128]. Посмертное исследование, проведенное Carone и Liebow, показало гистологические доказательства острого панкреатита или перипанкреатического некроза жира у 16 из 54 пациентов, получавших стероиды [129].Первые сообщения о случаях также связывают использование стероидов с острым панкреатитом [130]. Исследования также показали, что кортикостероиды не имеют положительного эффекта в профилактике панкреатита после ЭРХПГ [131]. Однако, учитывая, что некоторые доклинические исследования предполагают, что стероиды могут уменьшать воспалительный каскад, рекрутирование лейкоцитов и последующее повреждение поджелудочной железы при профилактическом применении [38], необходимы дальнейшие хорошо спланированные исследования.
Антиоксидантные агенты
В нескольких клинических испытаниях оценивалась польза антиоксидантных агентов при остром панкреатите с учетом роли активных форм кислорода и клеточного повреждения при остром панкреатите, а также доказательств, полученных в ходе доклинических исследований.Изученные антиоксиданты включают н-ацетилцистеин, метионин, бета-каротин, селен, аскорбиновую кислоту и альфа-токоферол.
Рандомизированное клиническое испытание, оценивающее лечение ацетилцистеином, селеном и витамином С, показало повышение уровня антиоксидантов в сыворотке и снижение маркеров окислительного стресса, но не улучшило дисфункцию органов [132]. Другое исследование с пациентами, получавшими витамин С, н-ацетилцистеин и другие антиоксиданты, не показало значительной разницы в частоте осложнений или продолжительности пребывания в больнице [133].Третье недавнее клиническое исследование витаминов A, C и E также не показало значительных различий в дисфункции органов [134].
Исследования по оценке использования глутамина, более мощного антиоксиданта, были более многообещающими. Одно исследование, в котором 80 пациентов были рандомизированы для приема глутамина, показало уменьшение количества осложнений, продолжительности госпитализации, необходимости в хирургическом вмешательстве и смертности при введении препарата на раннем этапе после госпитализации [135]. Метаанализ рандомизированных контрольных исследований глутамина показал улучшение показателей смертности (ОР = 0.3, 95% ДИ: 0,15–0,6) и снижение инфекционных осложнений (ОР = 0,58, 95% ДИ: 0,39–0,87), но без разницы в продолжительности пребывания в больнице. Польза от глутамина наблюдалась только у пациентов, получавших полное парентеральное питание [136]. Таким образом, роль антиоксидантной терапии при остром панкреатите еще предстоит определить.
Другие методы лечения
В клинических исследованиях также оценивались различные другие методы лечения острого панкреатита. Считается, что антифибринолитики, такие как эпсилон-аминокапроновая кислота (EPCA), улучшают патогенез острого панкреатита, подавляя активацию плазминогена, плазмина и трипсина, подавляя калликреин поджелудочной железы и повышая активность антитрипсина в сыворотке [137].Однако клиническое исследование, оценивающее использование EPCA и апротинина при остром панкреатите, не показало какого-либо клинически значимого улучшения исходов, таких как продолжительность госпитализации и нормализация лабораторных показателей, по сравнению с группой обычного лечения и группами лечения апротинином [138].
Свежезамороженная плазма (СЗП) также оценивалась при лечении острого панкреатита с учетом лабораторных исследований, которые показали ингибирующее действие СЗП на протеолитическую активность в сыворотке крови пациентов с острым панкреатитом [139].В то время как одно первоначальное проспективное пилотное клиническое исследование показало снижение смертности при приеме СЗП у пациентов с острым панкреатитом при введении в течение первых пяти дней от начала заболевания [139], более крупное многоцентровое контролируемое клиническое исследование не показало улучшения клинических результатов в группа, получавшая СЗП, в отличие от группы, получавшей коллоиды [140].
Молекулярные пути развития мишеней включают калликреин-кинин и систему комплемента, учитывая, что тяжелый острый панкреатит связан с повышенными уровнями C3a и sC5b-9 [141].Ингибитор C1-эстеразы блокирует множество протеолитических ферментов, включая активированный C1-комплекс и калликреин [142], и как экспериментальные исследования, так и небольшие исследования на людях показали, что ингибитор C1-эстеразы обладает некоторым защитным действием при тяжелом остром панкреатите [143]. В настоящее время фармакологические мишени системы комплемента используются при множестве других заболеваний, таких как наследственный ангионевротический отек, пароксизмальная ночная гемоглобинурия и гемолитико-уремический синдром [144], которые могут способствовать более быстрой трансляции.
ЗАКЛЮЧЕНИЕ
Доклинические и клинические исследования (Таблицы и) показали многообещающие возможности для новой фармакологической терапии острого панкреатита, которая может дополнять традиционное лечение, включающее поддерживающие меры, такие как жидкостная реанимация, нутритивная поддержка, контроль боли и антибиотики, такие как нужный. Доклинические и клинические исследования показали многообещающие возможности применения различных классов терапии, которые включают антисекреторные агенты, ингибиторы протеаз, иммуномодуляторы и противовоспалительные агенты, а также антиоксиданты.Хотя некоторые доказательства в пользу этих методов лечения все еще остаются неубедительными и не были переведены в текущие стандартные методы лечения, существует огромная потенциальная терапевтическая польза, как продемонстрировано в этих исследованиях. Иммуномодулирующие фармакологические методы лечения также еще предстоит превратить в стандартную клиническую помощь при остром панкреатите [67].
Таблица 1
Резюме фармакологических агентов, изученных при экспериментальном остром панкреатите
| Фармакологическое средство | Модель на животных | Оценка результатов | 4 Цитаты | Механизм индукции панкреатита | ||
| Антисекреторные агенты | ||||||
| Глюкагон | Собака | Обструкция двенадцатиперстной кишки, инфузия протока поджелудочной железы 48 инфузия раствора лактатного протока 4 или инфузия протока поджелудочной железы 4 полезен по сравнению с простой объемной реанимацией | [15] | |||
| Свинья | Геморрагический панкреатит, вызванный инъекцией желчи в проток поджелудочной железы | Сниженная смертность | [16] | атин|||
| Таурохолат | Отсутствие снижения смертности | [21, 22] | ||||
| Ингибиторы протеаз | ||||||
| Апротинин | Собака | Геморрагический панкреатит | 906– терапевтический потенциал 906 Геморрагический панкреатит, терапевтический потенциал 904–197 ]||||
| Хлорофилл-а | Морская свинка | Таурохолат-индуцированный некротический панкреатит | Выживаемость | [25-27] | ||
| Противовоспалительная терапия | 448470 P448470 мышиТаурохолат, диета CDE или церулеин | Защитный эффект | [29-31] | |||
| Индометацин | Крыса | Оливковое масло или таурохолат | , особенно в раннем возрасте] | |||
| Ингибитор липоксигеназы | Крыса | Таурохолевая кислота 9 0470 | Защитный эффект | [35] | ||
| Стероид | Крыса | Церулеин и таурохолат | Уменьшение воспаления и защитное действие | [37-43] | ||
| [37-43] | ||||||
| [37-43] | ||||||
| Caer 9048 IL-10 | Снижение степени тяжести заболевания | [44, 48-50] | ||||
| Лексипафант | Крыса, мыши | Внутрипротоковое введение 5% тауродезоксихолата или церулеина натрия | Снижение степени тяжести SIR | , бактериальная транслокация | [46, 47] | |
| Гемин / пангематин / биливердин / CO / IL-22 | Крыса, мыши | диета с церулеином, таурохолатом или CDE | Защитные и терапевтические эффекты | [61-67] | ||
| Анти-TNF альфа | Мыши | диета с церулеином, таурохолатом или CDE | Снижение воспалительной реакции и гибели клеток | [72-75] 904 70 | ||
| Антиоксиданты | ||||||
| Tempol | Мыши | каррагинан, введенный в плевральную полость | Снижение воспаления и шока | [54] | ||
| Селен | гидрохлорид 9048 Селен Хлор6 9048 Селен 9048 Уменьшение травмы поджелудочной железы[53, 145] | |||||
Таблица 2
Резюме фармакологических агентов, изученных при клиническом остром панкреатите
| Фармакологическое средство | 70 Дизайн выборки 903 | Оценка результатов | Цитаты | ||||||||
| Снижение SIRS | Снижение органной недостаточности | Снижение продолжительности пребывания | 9018 Снижение продолжительности пребывания 470 9018 9018 904 90 466Антисекреторные агенты | ||||||||
| Глюкагон | РКИ | 22-69 | Не сообщалось | Не сообщалось | Нет | Нет | [76-82] | 51 | Не сообщалось | Не сообщалось | Нет | Нет | [83] |
| Кальцитонин | RCT | 94 | Не сообщалось | Не сообщалось | Не сообщалось | Не сообщалось | ↓ боль, более ранняя нормализация лабораторных показателей | [84-86] | |||
| Соматостатин | РКИ / метаанализ | 50-703 | Не сообщалось | Неопределено (не влияет на полиорганную недостаточность, но ↓ местные осложнения) | Неопределенный | Неопределенный | ↓ абсцесс и некроз поджелудочной железы, ↓ местное воспаление | [90-95] | |||
| Октреотид | РКИ / метаанализ | 19–948 | Да | Да | Неопределенный | Неопределенный | [97-99] | ||||
| 48-105 | Не сообщалось | Нет | Да | Нет | ↓ панкреонекроз, ↓ активация комплемента | [101-105] | |||||
| Анализ мезилата Gabexate | 42-898 | Не сообщалось | Нет | Нет | Нет | CRAI ↓ пребывание в больнице и SIRS | [108-113] | ||||
| Нафомостат | RCT | инфекция некротической ткани поджелудочной железы) | Не сообщается | Не сообщается | Да | Только CRAI + abx имеет преимущество | [114-11 6] | ||||
| Иммуномодуляторы | |||||||||||
| Lexipafant | РКИ | 50-290 | Да | Да | Не сообщалось | Да | 117-1190 ] | ||||
| Dotrecogin alfa | RCT | 32 | Да | Нет | Не сообщается | Нет | [122, 123] | ||||
| Acety | 39-53 | Неопределенный (↓ CRP, но не sig) | Нет (тенденция к ↑ MOF) | Нет | Нет | [132-134] | |||||
| Глютамин | RCT / мета-анализ | 505 | Да | Да | Нет | Да | [135, 136] | ||||
Есть также новые цели для p хармакологическая терапия, которая может расширить возможности лечения острого панкреатита.Стратегии, которые изменяют активность ключевых иммунных клеток в воспалительном каскаде, вызванном острым панкреатитом, имеют большой потенциал [67]. Другие молекулярные мишени, такие как те, которые мешают калликреин-кининовой, протеолитической и системе комплемента, как обсуждается при дальнейших разработках, потенциально могут быть применены и к острому панкреатиту в будущем. В дополнение к расширению целей фармакологической терапии, существующие методы лечения должны быть лучше изучены в клинических испытаниях в будущем.Экспериментальные доклинические исследования выявили несколько методов лечения, которые не доказали свою эффективность в клинических испытаниях и, таким образом, не были переведены на клиническую арену. Одна из причин этого несоответствия может заключаться в том, что в моделях на животных фармакологическая терапия часто назначается до того, как наступает повреждение поджелудочной железы, что дает доказательства того, что терапия может обеспечивать защитный, но не обязательно терапевтический эффект.
В клинических исследованиях, однако, интересующее лекарство часто тестируется после того, как повреждение поджелудочной железы уже произошло и воспалительный каскад, вызванный острым панкреатитом, уже начался.В будущем улучшенный дизайн клинических испытаний, в рамках которых лечение будет проводиться раньше, с момента появления симптомов, может максимизировать способность препарата прерывать воспалительный каскад и давать лучшие результаты. Клинические испытания также необходимо стандартизировать в отношении критериев отбора, поддерживающих подходов к лечению и измеряемых результатов. Следует четко указать клинически значимые первичные и вторичные исходы, такие как смертность, органная недостаточность, ССВО, некроз поджелудочной железы и местные осложнения, продолжительность пребывания в больнице, потребность в обезболивающих, качество жизни и стоимость лечения.
Несмотря на неубедительные доказательства терапевтического эффекта многих изученных к настоящему времени фармакологических методов лечения острого панкреатита, существует большая потребность и перспективность в разработке эффективной фармакологической терапии острого панкреатита. Лучшее понимание патофизиологии заболевания и уроки, извлеченные из прошлых клинических исследований, предлагают отличную основу для расширения, так что текущее лечение панкреатита, в значительной степени характеризующееся поддерживающей терапией, может в конечном итоге быть переведено не только на профилактическую, но и на репаративную и эффективную терапию. .Лучшая характеристика и стандартизация популяции пациентов, наряду с хорошо контролируемыми и адекватно обоснованными клиническими исследованиями, привязанными к стандартизованным результатам, обеспечат надежную и достоверную оценку терапевтической роли доклинических испытанных агентов.
Фармакологическая терапия острого панкреатита
Abstract
В то время как консервативное лечение, такое как введение жидкости, покой кишечника и антибиотики, является основой текущего лечения острого панкреатита, есть много перспектив в фармакологической терапии, которая нацелена на различные аспекты патогенеза панкреатит.Обсуждается обширный обзор доклинических исследований, которые включают оценку методов лечения, таких как антисекреторные агенты, ингибиторы протеаз, противовоспалительные агенты и антиоксиданты. Многие из этих исследований показали терапевтическую пользу и улучшение выживаемости на экспериментальных моделях. На основе имеющихся доклинических исследований мы обсуждаем потенциальные новые целевые фармакологические подходы, которые могут быть многообещающими при лечении острого панкреатита. На сегодняшний день различные клинические исследования оценили трансляционный потенциал эффективных экспериментальных методов лечения на животных моделях и показали либо неудачные, либо смешанные результаты в исследованиях на людях.Несмотря на эти обескураживающие клинические исследования, существует большая клиническая потребность и существует несколько доклинических эффективных методов лечения, которые ждут исследования на пациентах. Лучшее понимание патофизиологии острого панкреатита и уроки, извлеченные из прошлых клинических исследований, вероятно, станут хорошей основой для расширения будущих методов лечения острого панкреатита.
Ключевые слова: Острый панкреатит, Антисекреторы, Ингибиторы протеазы, Противовоспалительные, Антиоксиданты, Синдром системной воспалительной реакции, Органная недостаточность, Смертность
Основной совет: В настоящее время нет утвержденных методов лечения острого панкреатита.В этом обзоре суммируются и обсуждаются доклинические и клинические исследования острого панкреатита, а также обсуждаются потенциальные многообещающие методы лечения.
ВВЕДЕНИЕ
В США в 2009 году у более 274000 пациентов был диагностирован острый панкреатит, что делает его наиболее распространенным желудочно-кишечным заболеванием, требующим острой госпитализации с затратами на лечение, превышающими 2,5 миллиарда долларов в год [1]. Прогноз для пациентов с острым панкреатитом в значительной степени определяется наличием органной недостаточности и инфицированного панкреонекроза с соответствующими показателями смертности 15-30% [2].Другие осложнения панкреатита включают синдром системного воспалительного ответа (SIRS), сепсис и острый респираторный дистресс-синдром (ARDS). Несмотря на рост заболеваемости [3], в настоящее время нет доступной фармакологической терапии для смягчения заболевания и его течения. Текущее лечение панкреатита в основном является поддерживающим. Лечение органной недостаточности состоит из поддерживающих мероприятий [4], в то время как лечение инфицированного панкреонекроза состоит из дренирования или санации раны и антибиотиков [5].
Самыми частыми причинами острого панкреатита у западного населения являются алкоголь и камни в желчном пузыре, но также описаны многие другие причины, и независимо от триггера существует основной общий патогенетический исход [6,7]. Считается, что острый панкреатит представляет собой местный воспалительный процесс, включающий преждевременную внутриклеточную активацию пищеварительных ферментов в ацинарных клетках, ведущую к самоперевариванию ткани, которое может прогрессировать и вовлекать отдаленные органы. Также считается, что секреторные ацинарные клетки выделяют хемокины и цитокины, которые привлекают лейкоциты, вызывая воспалительный ответ, ответственный за отек поджелудочной железы и накопление нейтрофилов [8].Этот интерстициальный отек иногда может прогрессировать до некроза части поджелудочной железы и возможной бактериальной инфекции. Острый панкреатит также может влиять на микрососудистое кровообращение и нарушать перфузию и оксигенацию тканей [9]. Хотя поддерживающая терапия в значительной степени является единственным доступным лечением этого заболевания, исследования панкреатита и лучшее понимание патофизиологии привели к разработке некоторых фармакологических методов лечения, нацеленных на различные этапы патогенеза панкреатита.В обзоре, опубликованном в 2008 г., описаны некоторые фармакологические методы лечения, исследованные на экспериментальных моделях животных [10]. С тех пор некоторые из этих методов лечения были дополнительно изучены, новые лекарства были обнаружены в каждом классе терапии, и было проведено больше клинических исследований на людях, оценивающих клиническую полезность этих методов лечения.
Этот обзор посвящен новейшим фармакологическим методам лечения острого панкреатита и не касается фармакологии стандартного лечения, используемого в настоящее время, такого как обезболивание и антибиотики.В статье резюмируются экспериментальные доклинические исследования, которые предоставляют доказательства терапевтического потенциала различных классов новых лекарств, описываются клинические испытания, в которых оценивался их трансляционный потенциал, а также комментарии относительно будущих методов лечения и потенциальных многообещающих агентов, ожидающих перевода в клиническую практику. Этот обзор посвящен фармакологической терапии острого панкреатита, который не является вторичным по отношению к эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ).
МОЛЕКУЛЯРНЫЙ ПАТОГЕНЕЗ ПАНКРЕАТИТА
В физиологических условиях секреция неактивных предшественников ферментов из ацинарных клеток происходит в ответ на цитозольный кальций.Однако устойчивое повышение уровня этого кальция может привести к преждевременной активации и секреции пищеварительных ферментов из ацинарных клеток, что является одним из самых ранних обнаруживаемых событий при панкреатите [11]. После первоначального поражения ацинарной клетки поджелудочной железы прогрессирование заболевания представляет собой многофазный процесс, который включает локальное воспаление поджелудочной железы, за которым следует генерализованный воспалительный ответ и заключительная стадия сепсиса, включающая полиорганную недостаточность у пациентов с тяжелым заболеванием. [8].После первоначального повреждения воспалительные клетки часто рекрутируются в поджелудочную железу через молекул адгезии, что может усугубить воспалительную реакцию, приводящую к тяжелому острому панкреатиту [8]. Одним из ключевых факторов воспалительной реакции при остром панкреатите, вероятно, являются циркулирующие цитокины и хемокины. Активные пищеварительные ферменты являются мощными стимуляторами макрофагов, которые впоследствии вызывают выработку провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNF-α) и интерлейкины [12].
Производство цитокинов регулируется большим количеством факторов транскрипции, наиболее заметным из которых является ядерный фактор, усиливающий легкую каппа-цепь активированных В-клеток (NF-κB) [12]. Различные типы высвобождаемых цитокинов могут вызывать свои эффекты через высокоспецифичных рецепторов клеточной поверхности и стимулировать ферменты, такие как циклооксигеназа-2 и индуцибельная синтаза оксида азота (iNOS), которые опосредуют воспалительный процесс. Следовательно, ингибирование этих ферментов, вероятно, ограничит местное и системное повреждение, вызванное провоспалительными лейкоцитами [12].Активные формы кислорода (ROS) и активные формы азота (RNS) также участвуют в патогенезе острого панкреатита. Механизм, с помощью которого эти агенты вызывают панкреатит, двоякий. АФК и РНС действуют непосредственно на биомолекулы (липиды, белки и нуклеиновые кислоты) и окисляют эти компоненты клеточной мембраны в поджелудочной железе, что приводит к разрушению мембраны и некрозу клеток поджелудочной железы. В дополнение к прямым пагубным окислительным эффектам, ROS и RNS могут также служить вторичными посредниками во внутриклеточной передаче сигналов и вызывать провоспалительные каскады [13].
ПРЕКЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Антисекреторные агенты
Острый панкреатит характеризуется повреждением панкреатической и перипанкреатической жировой ткани, частично опосредованным аутопищеварительными ферментами. Чрезмерная стимуляция экзокринной части поджелудочной железы усугубляет острый панкреатит [9] и, таким образом, является основанием для тестирования антисекреторных агентов в качестве потенциальных методов лечения острого панкреатита. Первоначальные исследования на животных в 1970-х годах тестировали глюкагон, а последующие исследования изучали использование соматостатина и аналога соматостатина длительного действия.
Глюкагон увеличивает кровоток в верхней брыжеечной артерии и снижает экзокринную секрецию поджелудочной железы [14]. Однако исследование с использованием модели панкреатита на собаках не показало, что лечение глюкагоном само по себе или в сочетании с объемной реанимацией лучше, чем только объемная реанимация [15]. Фактически, в их модели кровоизлияние в поджелудочную железу было связано с лечением глюкагоном, что предполагает возможное ухудшение заболевания. В более позднем исследовании на свиньях сообщалось о положительном влиянии глюкагона [16], но другие экспериментальные исследования в дополнение к вышеупомянутому исследованию не подтвердили использование терапии глюкагоном при экспериментальном остром панкреатите [17-19].
Соматостатин – это гормон-ингибитор с множественным действием на перистальтику желудочно-кишечного тракта и внешнесекреторную секрецию поджелудочной железы [20]. Одно доклиническое исследование с использованием таурохолат-индуцированной крысиной модели острого панкреатита показало, что соматостатин эффективен в подавлении базальной и гормональной стимуляции секреции панкреатических ферментов, но не влияет на степень панкреонекроза, отек поджелудочной железы, инфильтрацию лейкоцитов или содержание ферментов в поджелудочная железа после панкреатита индуцировалась и не приводила к общему снижению смертности [21].Другое исследование показало, что соматостатин стимулирует ретикулоэндотелиальную функцию печени и селезенки у крыс, что позволяет предположить пользу при лечении панкреатита [22]. Доклинические исследования показали преимущества использования соматостатина и его аналога длительного действия, что является основой для клинических испытаний, обсуждаемых ниже.
Использование антисекреторных агентов имеет ограничения, учитывая, что поджелудочная железа не только секретирует ферменты, но также секретирует бикарбонат и жидкости, а исследования на животных показали, что стимуляция протоковой секреции бикарбоната оказывает защитное действие на тяжесть панкреатита [23]. ].
Ингибиторы протеаз
Внутрипанкреатическая активация пищеварительных ферментов играет важную роль в патогенезе острого панкреатита. По этой очевидной причине ингибиторы протеазы были и остаются терапевтическим интересом при остром панкреатите. Ранние исследования на собаках с хирургически индуцированным панкреатитом, получавших ингибиторы трипсина из яичного белка или соевых бобов, а также тразилол (апротинин), ингибитор трипсин-калликреин из крупного рогатого скота, были эффективны в подавлении острого панкреатита [24].Несколько других исследований на животных, включая модель на морских свинках с индуцированным таурохолатом некротическим панкреатитом, также показали пользу от использования ингибиторов протеазы, таких как хлорофилл-а [25, 26]. Интересно, однако, что в модели тяжелого геморрагического панкреатита с добавлением холин-дефицитного DL-этионина (CDE) ни тразилол, ни хлорофилл-а не приводили к снижению заболеваемости или смертности [27]. Несмотря на использование ингибиторов протеаз во время индукции острого панкреатита CDE, разница в скорости, степени и высвобождении внутриклеточной протеазы, а также степени и / или проникновения лекарственного средства в ткань, связанная с различными экспериментальными моделями, может способствовать наблюдаемым противоположным результатам. [23].Тем не менее, более позднее исследование более соответствовало результатам клинических испытаний, обсуждаемых ниже.
Противовоспалительные и иммуномодуляторы
При экспериментальном остром панкреатите обнаружены измененные продукты метаболизма арахидоновой кислоты [28]. При остром панкреатите уровни тромбоксана B повышены, тогда как уровни простагландина E (PGE) снижены. Было показано, что терапия PGE оказывает защитное действие на течение экспериментального острого панкреатита на моделях грызунов с таурохолатами, диетой CDE или панкреатитом, индуцированным церулеином [29–31].Ингибиторы циклооксигеназы, такие как индометацин, использовались для лечения экспериментального острого панкреатита с противоречивыми результатами в более ранних исследованиях [32], но последующие исследования подтвердили положительный эффект индометацина, особенно при его использовании на ранней стадии или до индукции заболевания на моделях крыс с индуцированным таурохолатом. острый панкреатит [33,34]. Подобно циклооксигеназе, липоксигеназа находится ниже арахидоновой кислоты, и исследования показали, что ее ингибирование на моделях крыс с острым панкреатитом, индуцированным таурохолатами, приводит к снижению тяжести заболевания [35].Однако было показано, что антагонизм к лейкотриеновым рецепторам либо ухудшает, либо не влияет на острый панкреатит у крыс [33,36], что указывает на сложность этого пути и необходимость дальнейших углубленных исследований.
Стероидная терапия при остром панкреатите представляет интерес в течение нескольких десятилетий из-за связанной с ней активации лейкоцитов и высвобождения воспалительных цитокинов и хемокинов во время прогрессирования острого панкреатита. Одно экспериментальное исследование на крысах с острым панкреатитом, вызванным церулеином, показало, что эффективность стероидной терапии зависит от тяжести заболевания, причем дексаметазон более эффективен против панкреатита с тяжелым воспалением [37].Другое экспериментальное исследование показало, что дексаметазон уменьшал повреждение поджелудочной железы при профилактическом применении за счет снижения экспрессии молекулы-1 межклеточной адгезии, но был неэффективен в предотвращении рекрутирования лейкоцитов в поджелудочную железу при терапевтическом введении крысам с острым панкреатитом, индуцированным таурохолатами [38]. С другой стороны, стероиды также считаются причиной острого панкреатита, и некоторые исследования показывают, что высокие дозы гидрокортизона могут увеличивать смертность и частоту осложнений, таких как сепсис или инфекция [39–43].
Исследования на животных показали, что интерлейкин-10 (ИЛ-10), противовоспалительный цитокин, может уменьшить тяжесть церулеин-индуцированного острого панкреатита на моделях грызунов, если его вводить до или после индукции заболевания [44]. IL-10 играет защитную роль в местных и системных последствиях заболевания, поскольку было показано, что IL-10 блокирует воспаление, что приводит к улучшению результатов в экспериментальных моделях [45]. Лексипафант, антагонист фактора активации тромбоцитов [46], вызывает системные эффекты и участвует в качестве медиатора в прогрессировании острого панкреатита [47].Исследования показали, что лечение лексипафантом моделей панкреатита на грызунах, индуцированных тауродезоксихолатом и церулеином, снижает тяжесть связанных с панкреатитом осложнений, таких как кишечная дисфункция, системная активация ИЛ-1 и локальное рекрутирование лейкоцитов [48]. Лексипафант уменьшил воспаление, ассоциированное с острым панкреатитом [49], и уменьшил острый некротический панкреатит [50]. Несмотря на положительные результаты применения ИЛ-10 и лексипафанта в исследованиях на животных, их перевод в клиническое использование оказался сложной задачей.
Антиоксиданты
Окислительный стресс и травмы участвуют во многих воспалительных заболеваниях. Свободные радикалы, полученные из кислорода, образуются при экспериментальном остром панкреатите [51], и есть данные о снижении уровня антиоксидантов в крови у пациентов с тяжелым острым панкреатитом [52]. Эти наблюдения привели к экспериментальным исследованиям, которые показали защитный эффект экзогенно вводимых антиоксидантов, таких как селен, за счет уменьшения повреждения поджелудочной железы [53]. Доклинические исследования на грызунах с моделями острого панкреатита, вызванного различными методами, включая инъекцию каррагинана в плевральную полость или л -аргинина гидрохлорида, показали снижение уровня глутатиона и повышение уровня окисленного глутатиона, что свидетельствует о пользе этого вмешательства [ 54].Клинические исследования, которые будут подробно обсуждаться ниже, однако, не дали положительных результатов, и может оказаться, что антиоксиданты более полезны для профилактики и / или в качестве синергических агентов.
Возможные будущие многообещающие терапевтические цели
Одним из основных ограничений доклинических исследований является неопределенность и отсутствие идеальной модели, которая воспроизводит все аспекты болезни человека. Кроме того, доклиническая терапия часто назначается либо на ранней стадии, либо во время индукции острого панкреатита, тогда как на самом деле пациенты часто обращаются с текущим или поздним началом острого панкреатита.Доклинические исследования, демонстрирующие эффективность терапии при назначении препарата после прогрессирования заболевания, с большей вероятностью дадут многообещающие результаты в клинических испытаниях. За исключением острого панкреатита, вызванного ЭРХПГ, при котором можно назначить профилактическую терапию, маловероятно, что агенты, препятствующие возникновению острого панкреатита, будут эффективными, а скорее те, которые нацелены на последующее повреждение, восстановление или воспалительные пути. быть полезным при лечении острого панкреатита.По этой причине мы обсуждаем несколько многообещающих доклинических исследований, нацеленных на эти пути.
Считается, что индуцируемая активность синтазы оксида азота увеличивается при экспериментальном остром панкреатите [55]. Экспериментальные исследования на модели крыс показали, что такие агенты, как S -метилизотиомочевина, индуцибельный ингибитор синтазы оксида азота, могут уменьшать бактериальную транслокацию из кишечника в панкреонекроз, тем самым снижая септические осложнения и смертность при остром панкреатите [56].Лечение такими агентами, как AR-C102222AA или L – N 6 – (1-иминоэтил) -лизин, высокоселективные ингибиторы iNOS, в начале курса после индукции острого панкреатита также показали значительный положительный эффект. эффекты при остром панкреатите у австралийских опоссумов [57] и могут иметь терапевтический эффект за счет уменьшения повреждения поджелудочной железы в будущих клинических исследованиях.
Экспериментальные исследования пентоксифиллина и гепарина показали защитный эффект на моделях крыс с острым панкреатитом.Исследования показали, что пентоксифиллин ослабляет активацию нейтрофилов, провоспалительную передачу сигналов, системное воспаление и уровни цитокинов при экспериментальном остром панкреатите, особенно при раннем введении [58]. Гепарин также представляет собой фармакологическую терапию, вызывающую интерес в последнее время, и растет число сообщений, предполагающих его потенциал в лечении острого панкреатита. Первоначально гепарин изучался в первую очередь из-за его способности улучшать микроциркуляцию, учитывая, что нарушение микроциркуляции способствует воспалительному процессу острого панкреатита.Механизм антикоагуляции гепарина также связан с его противовоспалительным действием, частично вторичным по отношению к снижению стимуляции макрофагов и моноцитов [59]. Экспериментальные исследования показывают, что добавление гепарина приводит к снижению амилазы, эндотелина-1 и воспалительных цитокинов, таких как TNFα, активации NF-κB, а также к улучшению морфологических изменений и сосудистого кровотока в поджелудочной железе [60]. Такие агенты могут улучшить заживление, ослабляя провоспалительные пути, и могут принести пользу при клиническом остром панкреатите.
Повышающая регуляция гемооксигеназы-1 (НО-1) или лечение ее последующими эффекторами и продуктами разложения гема, биливердин и монооксид углерода оказывают защитное действие на различных моделях острого панкреатита на грызунах, индуцированного диетой с таурохолатом, церулеином или CDE [61 -66]. Макрофаги со сверхэкспрессией HO-1 защищают от острого панкреатита [61,67]. Панхематин, одобренный FDA препарат гемина для лечения острой перемежающейся порфирии, может стимулировать выработку HO-1 [68]. Исследования показали, что пангематин, если его назначить до развития экспериментального панкреатита, может активировать гемин-активированные макрофаги и привести к меньшему повреждению поджелудочной железы, а если его назначить после развития острого панкреатита, он также может уменьшить степень повреждения, связанного с панкреатитом [63].Примечательно, что мононуклеарные клетки периферической крови пациентов с острым панкреатитом легкой степени обладают обратимой повышающей регуляцией HO-1, которая связана с клиническим выздоровлением, поддерживая терапевтический потенциал HO-1 и продуктов распада гема у пациентов с острым панкреатитом. Биливердин через рецептор арилуглеводородов активирует IL-22 [66]. В последнее время возник большой интерес к роли IL-22, цитокина, продуцируемого гемопоэтическими клетками, нацеленного на неиммунные клетки [66].Интересно, что поджелудочная железа имеет самую высокую экспрессию рецептора IL-22 среди любых других тканей [69], и было показано, что лечение IL-22 улучшает экспериментальный острый панкреатит [70]. Таким образом, HO-1 и его нижестоящие эффекторы являются потенциальными мишенями для клинического острого панкреатита.
TNFα играет центральную роль в патогенезе местных и отдаленных осложнений острого панкреатита [71], а его блокада улучшает экспериментальный острый панкреатит, вызванный церулеином, таурохолатом или диетой CDE в исследованиях на мышах [72,73].Хотя теоретически существует повышенный риск инфекционных осложнений при терапии анти-TNF, есть сообщения о случаях с положительным исходом у пациентов с острым панкреатитом, которые получали анти-TNF из-за сопутствующего заболевания, для которого была показана терапия против TNF [74,75] . Таким образом, при тщательном отборе пациентов вполне вероятно, что терапия анти-TNF даст положительные результаты в клинических испытаниях.
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Основываясь на патофизиологии острого панкреатита и проведенных фундаментальных научных исследованиях, дающих доказательства перспективной фармакологической терапии, было проведено множество клинических исследований для оценки эффективности этих методов лечения, включая антисекреторные агенты, ингибиторы протеазы, иммуномодуляторы, антисекреторные препараты. -воспалительные агенты и антиоксиданты.
Антисекреторные агенты
Впервые об использовании глюкагона при остром панкреатите в 1971 году сообщили Knight et al [76], и с тех пор несколько последующих неконтролируемых клинических испытаний показали клиническое улучшение, уменьшение боли и снижение уровня ферментов. мероприятия при остром панкреатите [77-79]. Однако в последующем двойном слепом исследовании с участием 69 пациентов было обнаружено, что глюкагон не оказывает значительного влияния на смертность пациентов по сравнению с плацебо [80]. Дальнейшие клинические испытания не выявили различий в смертности и заболеваемости, таких как боль и продолжительность пребывания в стационаре [81,82].
Атропин также изучался в рандомизированном клиническом исследовании, но не оказал значительного влияния на клиническое течение пациентов по сравнению с отсутствием лечения [83]. Считалось также, что вливание кальцитонина лосося сильно подавляет секрецию желудочного сока, такую как желудочная кислота, пепсин и гастрин [84-86], а также секрецию ферментов поджелудочной железы, стимулируемую различными стимуляторами секреции, не влияя на секрецию жидкости и электролитов [87], таким образом смягчая патогенез. острого панкреатита [88].Многоцентровое рандомизированное двойное слепое исследование по оценке использования синтетического кальцитонина лосося при остром панкреатите показало, что, хотя смертность не изменилась, количество пациентов без боли и нормализованной сывороточной амилазы было выше в группе лечения по сравнению с группой плацебо. Другие параметры, такие как доза анальгетика, количество лейкоцитов и нормализация семи клинических и лабораторных критериев, показали положительную динамику в группе лечения, но не были клинически значимыми [88].
Клинические испытания хорошо изучили использование соматостатина для лечения острого панкреатита, учитывая, что он подавляет экзокринную секрецию поджелудочной железы, снижает внутренний кровоток, стимулирует ретикулоэндотелиальную систему печени и модулирует каскад воспалительных цитокинов [89].Однако несколько рандомизированных клинических исследований не показали клинически значимого преимущества соматостатина [90–94]. С другой стороны, метаанализ семи публикаций действительно показал улучшение общей смертности от соматостатина при тяжелом остром панкреатите (OR = 0,36, 95% CI: 0,2-0,64), но не было значительного снижения частоты осложнений у пациентов с острый панкреатит [95].
Октреотид, синтетический аналог соматостатина, также прошел клинические испытания. Хотя первоначальные небольшие исследования не показали какого-либо общего улучшения показателей смертности, они предположили снижение тяжести острого панкреатита, уменьшение местных осложнений и более ранний возврат к пероральному приему [96].Однако одно из крупнейших клинических испытаний с участием 302 пациентов с панкреатитом средней и тяжелой степени не показало какой-либо клинической пользы [97], но меньшее исследование с участием 50 пациентов с тяжелым острым панкреатитом показало клинически значимое снижение частоты сепсиса (76–24%). , ОРДС (56–28%), пребывание в больнице (33,1–20,6 дня) и смертность (8–2 смерти) [98]. В то время как более старый проведенный метаанализ действительно показал улучшение смертности от тяжелого острого панкреатита (OR = 0,57, 95% ДИ: 0,35–0,88) [95], другой более свежий метаанализ, ограничивавший их оценку четырьмя исследованиями более высокого качества, не дал показать какие-либо преимущества в отношении сепсиса, смертности или осложнений [99].
Таким образом, клинические исследования, оценивающие использование антисекреторных агентов, предоставили неубедительные доказательства их преимуществ. По всей видимости, пользы от этих агентов при легком остром панкреатите нет, а при тяжелом остром панкреатите польза не ясна. Следовательно, эти агенты в настоящее время не рекомендуются в клинической практике [4,100].
Ингибиторы протеазы
Одним из первых изученных ингибиторов протеаз является апротинин, и первоначальные исследования показали некоторое улучшение показателей смертности, хотя последующие исследования не смогли повторить такие результаты [101,102].Исследования доставки апротинина через перитонеальный лаваж показали меньший некроз в экспериментальной группе со снижением активации комплемента (в частности, меньше C3a и больше уровней ингибитора C1 в плазме), но нет общей разницы в смертности [103-105]. Апротинин все еще может играть роль в лечении острого панкреатита, учитывая, что он не вводился в достаточно высоких дозах, чтобы вызвать достаточное ингибирование активности протеазы, а исследования не имели достаточной мощности [106].
Габексат мезилат представляет собой меньший ингибитор протеазы, который изучался в клинических испытаниях на людях [107].В то время как ранние более мелкие клинические исследования предполагали снижение смертности от применения этой терапии [108, 109], более крупное рандомизированное контролируемое исследование пациентов с умеренным и тяжелым острым панкреатитом не обнаружило клинической пользы [110, 111]. Два других метаанализа также демонстрируют отсутствие преимущества в отношении смертности, хотя они показали снижение потребности в хирургическом вмешательстве и меньшее количество осложнений [95, 112]. Недавнее исследование показало некоторую пользу габексата при непрерывной регионарной артериальной инфузии (CRAI) [113].
Нафомостат – новый синтетический ингибитор протеазы, в сто раз более мощный, чем габексат [107]. Клинические исследования, оценивающие доставку нафомостата через CRAI вместе с антибиотиками, показали более высокую смертность и меньшую частоту некроза при более раннем введении препарата [114]. Исследования также показали, что доставка лекарства через CRAI по сравнению с не-CRAI снижает потребность в хирургическом вмешательстве и улучшает выживаемость [115,116].
Ни один из упомянутых выше ингибиторов протеазы в настоящее время не является частью стандартной клинической помощи при лечении острого панкреатита, поскольку необходимы более масштабные и адекватно обоснованные исследования, прежде чем их рекомендовать для клинического использования.Нафомостат, однако, является наиболее перспективным из трех, особенно при введении через CRAI в сочетании с антибиотиками.
Иммуномодуляторы
На основании положительных доклинических результатов Лексипафант прошел клинические испытания у пациентов с тяжелым острым панкреатитом. Первое клиническое испытание, оценивающее использование этой терапии, не показало разницы в смертности, но показало снижение органной недостаточности [117]. Другое исследование показало значительно меньшую органную недостаточность, снижение смертности и ССВО [118].Однако самое крупное рандомизированное клиническое исследование, включающее эту терапию, не показало значительного снижения органной недостаточности или местных осложнений, что привело к выводу, что лексипафант сам по себе не может лечить тяжелый острый панкреатит [119].
Дотрекогин альфа, аналог эндогенного протеина С, показал некоторые преимущества при лечении острого панкреатита [120]. Эндогенный протеин С вырабатывается в печени и ингибирует образование тромбина и облегчает тромболизис. Учитывая, что более низкие уровни активированного протеина C связаны с более высокой смертностью при остром панкреатите, активированный протеин C, как полагали, смягчает тяжелый острый панкреатит, модулируя иммунную систему через регулирование взаимодействия лейкоцитов с эндотелием и митоген-активированными киназами и улучшая кишечную микроциркуляцию [121].Первые сообщения о клинических случаях показали некоторую пользу от использования дотрекогина альфа при остром панкреатите [122], но последующее пилотное исследование не показало каких-либо клинически значимых различий с использованием дотрекогина альфа [123].
Противовоспалительные средства
Индометацин, который ингибирует активность фосфолипазы A2 и активность циклооксигеназы, уменьшая, таким образом, нейтрофильно-опосредованное воспаление, был клинически изучен на основе более ранних доклинических исследований [124]. Однако одно исследование, оценивающее эту терапию, сообщило только об уменьшении боли и употреблении опиатов при назначении пациентам с острым панкреатитом [125], предполагая обезболивающее, но не связанное с противовоспалительным действием.До сих пор преимущества индометацина в значительной степени ограничивались панкреатитом после ЭРХПГ [126].
Стероидная терапия широко используется для уменьшения воспаления в различных системах органов. Хотя было показано, что стероидная терапия эффективна при лечении аутоиммунного панкреатита [127], однако при остром панкреатите стероидная терапия участвует в индукции заболевания [128]. Посмертное исследование, проведенное Carone и Liebow, показало гистологические доказательства острого панкреатита или перипанкреатического некроза жира у 16 из 54 пациентов, получавших стероиды [129].Первые сообщения о случаях также связывают использование стероидов с острым панкреатитом [130]. Исследования также показали, что кортикостероиды не имеют положительного эффекта в профилактике панкреатита после ЭРХПГ [131]. Однако, учитывая, что некоторые доклинические исследования предполагают, что стероиды могут уменьшать воспалительный каскад, рекрутирование лейкоцитов и последующее повреждение поджелудочной железы при профилактическом применении [38], необходимы дальнейшие хорошо спланированные исследования.
Антиоксидантные агенты
В нескольких клинических испытаниях оценивалась польза антиоксидантных агентов при остром панкреатите с учетом роли активных форм кислорода и клеточного повреждения при остром панкреатите, а также доказательств, полученных в ходе доклинических исследований.Изученные антиоксиданты включают н-ацетилцистеин, метионин, бета-каротин, селен, аскорбиновую кислоту и альфа-токоферол.
Рандомизированное клиническое испытание, оценивающее лечение ацетилцистеином, селеном и витамином С, показало повышение уровня антиоксидантов в сыворотке и снижение маркеров окислительного стресса, но не улучшило дисфункцию органов [132]. Другое исследование с пациентами, получавшими витамин С, н-ацетилцистеин и другие антиоксиданты, не показало значительной разницы в частоте осложнений или продолжительности пребывания в больнице [133].Третье недавнее клиническое исследование витаминов A, C и E также не показало значительных различий в дисфункции органов [134].
Исследования по оценке использования глутамина, более мощного антиоксиданта, были более многообещающими. Одно исследование, в котором 80 пациентов были рандомизированы для приема глутамина, показало уменьшение количества осложнений, продолжительности госпитализации, необходимости в хирургическом вмешательстве и смертности при введении препарата на раннем этапе после госпитализации [135]. Метаанализ рандомизированных контрольных исследований глутамина показал улучшение показателей смертности (ОР = 0.3, 95% ДИ: 0,15–0,6) и снижение инфекционных осложнений (ОР = 0,58, 95% ДИ: 0,39–0,87), но без разницы в продолжительности пребывания в больнице. Польза от глутамина наблюдалась только у пациентов, получавших полное парентеральное питание [136]. Таким образом, роль антиоксидантной терапии при остром панкреатите еще предстоит определить.
Другие методы лечения
В клинических исследованиях также оценивались различные другие методы лечения острого панкреатита. Считается, что антифибринолитики, такие как эпсилон-аминокапроновая кислота (EPCA), улучшают патогенез острого панкреатита, подавляя активацию плазминогена, плазмина и трипсина, подавляя калликреин поджелудочной железы и повышая активность антитрипсина в сыворотке [137].Однако клиническое исследование, оценивающее использование EPCA и апротинина при остром панкреатите, не показало какого-либо клинически значимого улучшения исходов, таких как продолжительность госпитализации и нормализация лабораторных показателей, по сравнению с группой обычного лечения и группами лечения апротинином [138].
Свежезамороженная плазма (СЗП) также оценивалась при лечении острого панкреатита с учетом лабораторных исследований, которые показали ингибирующее действие СЗП на протеолитическую активность в сыворотке крови пациентов с острым панкреатитом [139].В то время как одно первоначальное проспективное пилотное клиническое исследование показало снижение смертности при приеме СЗП у пациентов с острым панкреатитом при введении в течение первых пяти дней от начала заболевания [139], более крупное многоцентровое контролируемое клиническое исследование не показало улучшения клинических результатов в группа, получавшая СЗП, в отличие от группы, получавшей коллоиды [140].
Молекулярные пути развития мишеней включают калликреин-кинин и систему комплемента, учитывая, что тяжелый острый панкреатит связан с повышенными уровнями C3a и sC5b-9 [141].Ингибитор C1-эстеразы блокирует множество протеолитических ферментов, включая активированный C1-комплекс и калликреин [142], и как экспериментальные исследования, так и небольшие исследования на людях показали, что ингибитор C1-эстеразы обладает некоторым защитным действием при тяжелом остром панкреатите [143]. В настоящее время фармакологические мишени системы комплемента используются при множестве других заболеваний, таких как наследственный ангионевротический отек, пароксизмальная ночная гемоглобинурия и гемолитико-уремический синдром [144], которые могут способствовать более быстрой трансляции.
ЗАКЛЮЧЕНИЕ
Доклинические и клинические исследования (Таблицы и) показали многообещающие возможности для новой фармакологической терапии острого панкреатита, которая может дополнять традиционное лечение, включающее поддерживающие меры, такие как жидкостная реанимация, нутритивная поддержка, контроль боли и антибиотики, такие как нужный. Доклинические и клинические исследования показали многообещающие возможности применения различных классов терапии, которые включают антисекреторные агенты, ингибиторы протеаз, иммуномодуляторы и противовоспалительные агенты, а также антиоксиданты.Хотя некоторые доказательства в пользу этих методов лечения все еще остаются неубедительными и не были переведены в текущие стандартные методы лечения, существует огромная потенциальная терапевтическая польза, как продемонстрировано в этих исследованиях. Иммуномодулирующие фармакологические методы лечения также еще предстоит превратить в стандартную клиническую помощь при остром панкреатите [67].
Таблица 1
Резюме фармакологических агентов, изученных при экспериментальном остром панкреатите
| Фармакологическое средство | Модель на животных | Оценка результатов | 4 Цитаты | Механизм индукции панкреатита | ||
| Антисекреторные агенты | ||||||
| Глюкагон | Собака | Обструкция двенадцатиперстной кишки, инфузия протока поджелудочной железы 48 инфузия раствора лактатного протока 4 или инфузия протока поджелудочной железы 4 полезен по сравнению с простой объемной реанимацией | [15] | |||
| Свинья | Геморрагический панкреатит, вызванный инъекцией желчи в проток поджелудочной железы | Сниженная смертность | [16] | атин|||
| Таурохолат | Отсутствие снижения смертности | [21, 22] | ||||
| Ингибиторы протеаз | ||||||
| Апротинин | Собака | Геморрагический панкреатит | 906– терапевтический потенциал 906 Геморрагический панкреатит, терапевтический потенциал 904–197 ]||||
| Хлорофилл-а | Морская свинка | Таурохолат-индуцированный некротический панкреатит | Выживаемость | [25-27] | ||
| Противовоспалительная терапия | 448470 P448470 мышиТаурохолат, диета CDE или церулеин | Защитный эффект | [29-31] | |||
| Индометацин | Крыса | Оливковое масло или таурохолат | , особенно в раннем возрасте] | |||
| Ингибитор липоксигеназы | Крыса | Таурохолевая кислота 9 0470 | Защитный эффект | [35] | ||
| Стероид | Крыса | Церулеин и таурохолат | Уменьшение воспаления и защитное действие | [37-43] | ||
| [37-43] | ||||||
| [37-43] | ||||||
| Caer 9048 IL-10 | Снижение степени тяжести заболевания | [44, 48-50] | ||||
| Лексипафант | Крыса, мыши | Внутрипротоковое введение 5% тауродезоксихолата или церулеина натрия | Снижение степени тяжести SIR | , бактериальная транслокация | [46, 47] | |
| Гемин / пангематин / биливердин / CO / IL-22 | Крыса, мыши | диета с церулеином, таурохолатом или CDE | Защитные и терапевтические эффекты | [61-67] | ||
| Анти-TNF альфа | Мыши | диета с церулеином, таурохолатом или CDE | Снижение воспалительной реакции и гибели клеток | [72-75] 904 70 | ||
| Антиоксиданты | ||||||
| Tempol | Мыши | каррагинан, введенный в плевральную полость | Снижение воспаления и шока | [54] | ||
| Селен | гидрохлорид 9048 Селен Хлор6 9048 Селен 9048 Уменьшение травмы поджелудочной железы[53, 145] | |||||
Таблица 2
Резюме фармакологических агентов, изученных при клиническом остром панкреатите
| Фармакологическое средство | 70 Дизайн выборки 903 | Оценка результатов | Цитаты | ||||||||
| Снижение SIRS | Снижение органной недостаточности | Снижение продолжительности пребывания | 9018 Снижение продолжительности пребывания 470 9018 9018 904 90 466Антисекреторные агенты | ||||||||
| Глюкагон | РКИ | 22-69 | Не сообщалось | Не сообщалось | Нет | Нет | [76-82] | 51 | Не сообщалось | Не сообщалось | Нет | Нет | [83] |
| Кальцитонин | RCT | 94 | Не сообщалось | Не сообщалось | Не сообщалось | Не сообщалось | ↓ боль, более ранняя нормализация лабораторных показателей | [84-86] | |||
| Соматостатин | РКИ / метаанализ | 50-703 | Не сообщалось | Неопределено (не влияет на полиорганную недостаточность, но ↓ местные осложнения) | Неопределенный | Неопределенный | ↓ абсцесс и некроз поджелудочной железы, ↓ местное воспаление | [90-95] | |||
| Октреотид | РКИ / метаанализ | 19–948 | Да | Да | Неопределенный | Неопределенный | [97-99] | ||||
| 48-105 | Не сообщалось | Нет | Да | Нет | ↓ панкреонекроз, ↓ активация комплемента | [101-105] | |||||
| Анализ мезилата Gabexate | 42-898 | Не сообщалось | Нет | Нет | Нет | CRAI ↓ пребывание в больнице и SIRS | [108-113] | ||||
| Нафомостат | RCT | инфекция некротической ткани поджелудочной железы) | Не сообщается | Не сообщается | Да | Только CRAI + abx имеет преимущество | [114-11 6] | ||||
| Иммуномодуляторы | |||||||||||
| Lexipafant | РКИ | 50-290 | Да | Да | Не сообщалось | Да | 117-1190 ] | ||||
| Dotrecogin alfa | RCT | 32 | Да | Нет | Не сообщается | Нет | [122, 123] | ||||
| Acety | 39-53 | Неопределенный (↓ CRP, но не sig) | Нет (тенденция к ↑ MOF) | Нет | Нет | [132-134] | |||||
| Глютамин | RCT / мета-анализ | 505 | Да | Да | Нет | Да | [135, 136] | ||||
Есть также новые цели для p хармакологическая терапия, которая может расширить возможности лечения острого панкреатита.Стратегии, которые изменяют активность ключевых иммунных клеток в воспалительном каскаде, вызванном острым панкреатитом, имеют большой потенциал [67]. Другие молекулярные мишени, такие как те, которые мешают калликреин-кининовой, протеолитической и системе комплемента, как обсуждается при дальнейших разработках, потенциально могут быть применены и к острому панкреатиту в будущем. В дополнение к расширению целей фармакологической терапии, существующие методы лечения должны быть лучше изучены в клинических испытаниях в будущем.Экспериментальные доклинические исследования выявили несколько методов лечения, которые не доказали свою эффективность в клинических испытаниях и, таким образом, не были переведены на клиническую арену. Одна из причин этого несоответствия может заключаться в том, что в моделях на животных фармакологическая терапия часто назначается до того, как наступает повреждение поджелудочной железы, что дает доказательства того, что терапия может обеспечивать защитный, но не обязательно терапевтический эффект.
В клинических исследованиях, однако, интересующее лекарство часто тестируется после того, как повреждение поджелудочной железы уже произошло и воспалительный каскад, вызванный острым панкреатитом, уже начался.В будущем улучшенный дизайн клинических испытаний, в рамках которых лечение будет проводиться раньше, с момента появления симптомов, может максимизировать способность препарата прерывать воспалительный каскад и давать лучшие результаты. Клинические испытания также необходимо стандартизировать в отношении критериев отбора, поддерживающих подходов к лечению и измеряемых результатов. Следует четко указать клинически значимые первичные и вторичные исходы, такие как смертность, органная недостаточность, ССВО, некроз поджелудочной железы и местные осложнения, продолжительность пребывания в больнице, потребность в обезболивающих, качество жизни и стоимость лечения.
Несмотря на неубедительные доказательства терапевтического эффекта многих изученных к настоящему времени фармакологических методов лечения острого панкреатита, существует большая потребность и перспективность в разработке эффективной фармакологической терапии острого панкреатита. Лучшее понимание патофизиологии заболевания и уроки, извлеченные из прошлых клинических исследований, предлагают отличную основу для расширения, так что текущее лечение панкреатита, в значительной степени характеризующееся поддерживающей терапией, может в конечном итоге быть переведено не только на профилактическую, но и на репаративную и эффективную терапию. .Лучшая характеристика и стандартизация популяции пациентов, наряду с хорошо контролируемыми и адекватно обоснованными клиническими исследованиями, привязанными к стандартизованным результатам, обеспечат надежную и достоверную оценку терапевтической роли доклинических испытанных агентов.
Фармакологическая терапия острого панкреатита
Abstract
В то время как консервативное лечение, такое как введение жидкости, покой кишечника и антибиотики, является основой текущего лечения острого панкреатита, есть много перспектив в фармакологической терапии, которая нацелена на различные аспекты патогенеза панкреатит.Обсуждается обширный обзор доклинических исследований, которые включают оценку методов лечения, таких как антисекреторные агенты, ингибиторы протеаз, противовоспалительные агенты и антиоксиданты. Многие из этих исследований показали терапевтическую пользу и улучшение выживаемости на экспериментальных моделях. На основе имеющихся доклинических исследований мы обсуждаем потенциальные новые целевые фармакологические подходы, которые могут быть многообещающими при лечении острого панкреатита. На сегодняшний день различные клинические исследования оценили трансляционный потенциал эффективных экспериментальных методов лечения на животных моделях и показали либо неудачные, либо смешанные результаты в исследованиях на людях.Несмотря на эти обескураживающие клинические исследования, существует большая клиническая потребность и существует несколько доклинических эффективных методов лечения, которые ждут исследования на пациентах. Лучшее понимание патофизиологии острого панкреатита и уроки, извлеченные из прошлых клинических исследований, вероятно, станут хорошей основой для расширения будущих методов лечения острого панкреатита.
Ключевые слова: Острый панкреатит, Антисекреторы, Ингибиторы протеазы, Противовоспалительные, Антиоксиданты, Синдром системной воспалительной реакции, Органная недостаточность, Смертность
Основной совет: В настоящее время нет утвержденных методов лечения острого панкреатита.В этом обзоре суммируются и обсуждаются доклинические и клинические исследования острого панкреатита, а также обсуждаются потенциальные многообещающие методы лечения.
ВВЕДЕНИЕ
В США в 2009 году у более 274000 пациентов был диагностирован острый панкреатит, что делает его наиболее распространенным желудочно-кишечным заболеванием, требующим острой госпитализации с затратами на лечение, превышающими 2,5 миллиарда долларов в год [1]. Прогноз для пациентов с острым панкреатитом в значительной степени определяется наличием органной недостаточности и инфицированного панкреонекроза с соответствующими показателями смертности 15-30% [2].Другие осложнения панкреатита включают синдром системного воспалительного ответа (SIRS), сепсис и острый респираторный дистресс-синдром (ARDS). Несмотря на рост заболеваемости [3], в настоящее время нет доступной фармакологической терапии для смягчения заболевания и его течения. Текущее лечение панкреатита в основном является поддерживающим. Лечение органной недостаточности состоит из поддерживающих мероприятий [4], в то время как лечение инфицированного панкреонекроза состоит из дренирования или санации раны и антибиотиков [5].
Самыми частыми причинами острого панкреатита у западного населения являются алкоголь и камни в желчном пузыре, но также описаны многие другие причины, и независимо от триггера существует основной общий патогенетический исход [6,7]. Считается, что острый панкреатит представляет собой местный воспалительный процесс, включающий преждевременную внутриклеточную активацию пищеварительных ферментов в ацинарных клетках, ведущую к самоперевариванию ткани, которое может прогрессировать и вовлекать отдаленные органы. Также считается, что секреторные ацинарные клетки выделяют хемокины и цитокины, которые привлекают лейкоциты, вызывая воспалительный ответ, ответственный за отек поджелудочной железы и накопление нейтрофилов [8].Этот интерстициальный отек иногда может прогрессировать до некроза части поджелудочной железы и возможной бактериальной инфекции. Острый панкреатит также может влиять на микрососудистое кровообращение и нарушать перфузию и оксигенацию тканей [9]. Хотя поддерживающая терапия в значительной степени является единственным доступным лечением этого заболевания, исследования панкреатита и лучшее понимание патофизиологии привели к разработке некоторых фармакологических методов лечения, нацеленных на различные этапы патогенеза панкреатита.В обзоре, опубликованном в 2008 г., описаны некоторые фармакологические методы лечения, исследованные на экспериментальных моделях животных [10]. С тех пор некоторые из этих методов лечения были дополнительно изучены, новые лекарства были обнаружены в каждом классе терапии, и было проведено больше клинических исследований на людях, оценивающих клиническую полезность этих методов лечения.
Этот обзор посвящен новейшим фармакологическим методам лечения острого панкреатита и не касается фармакологии стандартного лечения, используемого в настоящее время, такого как обезболивание и антибиотики.В статье резюмируются экспериментальные доклинические исследования, которые предоставляют доказательства терапевтического потенциала различных классов новых лекарств, описываются клинические испытания, в которых оценивался их трансляционный потенциал, а также комментарии относительно будущих методов лечения и потенциальных многообещающих агентов, ожидающих перевода в клиническую практику. Этот обзор посвящен фармакологической терапии острого панкреатита, который не является вторичным по отношению к эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ).
МОЛЕКУЛЯРНЫЙ ПАТОГЕНЕЗ ПАНКРЕАТИТА
В физиологических условиях секреция неактивных предшественников ферментов из ацинарных клеток происходит в ответ на цитозольный кальций.Однако устойчивое повышение уровня этого кальция может привести к преждевременной активации и секреции пищеварительных ферментов из ацинарных клеток, что является одним из самых ранних обнаруживаемых событий при панкреатите [11]. После первоначального поражения ацинарной клетки поджелудочной железы прогрессирование заболевания представляет собой многофазный процесс, который включает локальное воспаление поджелудочной железы, за которым следует генерализованный воспалительный ответ и заключительная стадия сепсиса, включающая полиорганную недостаточность у пациентов с тяжелым заболеванием. [8].После первоначального повреждения воспалительные клетки часто рекрутируются в поджелудочную железу через молекул адгезии, что может усугубить воспалительную реакцию, приводящую к тяжелому острому панкреатиту [8]. Одним из ключевых факторов воспалительной реакции при остром панкреатите, вероятно, являются циркулирующие цитокины и хемокины. Активные пищеварительные ферменты являются мощными стимуляторами макрофагов, которые впоследствии вызывают выработку провоспалительных цитокинов, таких как фактор некроза опухоли альфа (TNF-α) и интерлейкины [12].
Производство цитокинов регулируется большим количеством факторов транскрипции, наиболее заметным из которых является ядерный фактор, усиливающий легкую каппа-цепь активированных В-клеток (NF-κB) [12]. Различные типы высвобождаемых цитокинов могут вызывать свои эффекты через высокоспецифичных рецепторов клеточной поверхности и стимулировать ферменты, такие как циклооксигеназа-2 и индуцибельная синтаза оксида азота (iNOS), которые опосредуют воспалительный процесс. Следовательно, ингибирование этих ферментов, вероятно, ограничит местное и системное повреждение, вызванное провоспалительными лейкоцитами [12].Активные формы кислорода (ROS) и активные формы азота (RNS) также участвуют в патогенезе острого панкреатита. Механизм, с помощью которого эти агенты вызывают панкреатит, двоякий. АФК и РНС действуют непосредственно на биомолекулы (липиды, белки и нуклеиновые кислоты) и окисляют эти компоненты клеточной мембраны в поджелудочной железе, что приводит к разрушению мембраны и некрозу клеток поджелудочной железы. В дополнение к прямым пагубным окислительным эффектам, ROS и RNS могут также служить вторичными посредниками во внутриклеточной передаче сигналов и вызывать провоспалительные каскады [13].
ПРЕКЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Антисекреторные агенты
Острый панкреатит характеризуется повреждением панкреатической и перипанкреатической жировой ткани, частично опосредованным аутопищеварительными ферментами. Чрезмерная стимуляция экзокринной части поджелудочной железы усугубляет острый панкреатит [9] и, таким образом, является основанием для тестирования антисекреторных агентов в качестве потенциальных методов лечения острого панкреатита. Первоначальные исследования на животных в 1970-х годах тестировали глюкагон, а последующие исследования изучали использование соматостатина и аналога соматостатина длительного действия.
Глюкагон увеличивает кровоток в верхней брыжеечной артерии и снижает экзокринную секрецию поджелудочной железы [14]. Однако исследование с использованием модели панкреатита на собаках не показало, что лечение глюкагоном само по себе или в сочетании с объемной реанимацией лучше, чем только объемная реанимация [15]. Фактически, в их модели кровоизлияние в поджелудочную железу было связано с лечением глюкагоном, что предполагает возможное ухудшение заболевания. В более позднем исследовании на свиньях сообщалось о положительном влиянии глюкагона [16], но другие экспериментальные исследования в дополнение к вышеупомянутому исследованию не подтвердили использование терапии глюкагоном при экспериментальном остром панкреатите [17-19].
Соматостатин – это гормон-ингибитор с множественным действием на перистальтику желудочно-кишечного тракта и внешнесекреторную секрецию поджелудочной железы [20]. Одно доклиническое исследование с использованием таурохолат-индуцированной крысиной модели острого панкреатита показало, что соматостатин эффективен в подавлении базальной и гормональной стимуляции секреции панкреатических ферментов, но не влияет на степень панкреонекроза, отек поджелудочной железы, инфильтрацию лейкоцитов или содержание ферментов в поджелудочная железа после панкреатита индуцировалась и не приводила к общему снижению смертности [21].Другое исследование показало, что соматостатин стимулирует ретикулоэндотелиальную функцию печени и селезенки у крыс, что позволяет предположить пользу при лечении панкреатита [22]. Доклинические исследования показали преимущества использования соматостатина и его аналога длительного действия, что является основой для клинических испытаний, обсуждаемых ниже.
Использование антисекреторных агентов имеет ограничения, учитывая, что поджелудочная железа не только секретирует ферменты, но также секретирует бикарбонат и жидкости, а исследования на животных показали, что стимуляция протоковой секреции бикарбоната оказывает защитное действие на тяжесть панкреатита [23]. ].
Ингибиторы протеаз
Внутрипанкреатическая активация пищеварительных ферментов играет важную роль в патогенезе острого панкреатита. По этой очевидной причине ингибиторы протеазы были и остаются терапевтическим интересом при остром панкреатите. Ранние исследования на собаках с хирургически индуцированным панкреатитом, получавших ингибиторы трипсина из яичного белка или соевых бобов, а также тразилол (апротинин), ингибитор трипсин-калликреин из крупного рогатого скота, были эффективны в подавлении острого панкреатита [24].Несколько других исследований на животных, включая модель на морских свинках с индуцированным таурохолатом некротическим панкреатитом, также показали пользу от использования ингибиторов протеазы, таких как хлорофилл-а [25, 26]. Интересно, однако, что в модели тяжелого геморрагического панкреатита с добавлением холин-дефицитного DL-этионина (CDE) ни тразилол, ни хлорофилл-а не приводили к снижению заболеваемости или смертности [27]. Несмотря на использование ингибиторов протеаз во время индукции острого панкреатита CDE, разница в скорости, степени и высвобождении внутриклеточной протеазы, а также степени и / или проникновения лекарственного средства в ткань, связанная с различными экспериментальными моделями, может способствовать наблюдаемым противоположным результатам. [23].Тем не менее, более позднее исследование более соответствовало результатам клинических испытаний, обсуждаемых ниже.
Противовоспалительные и иммуномодуляторы
При экспериментальном остром панкреатите обнаружены измененные продукты метаболизма арахидоновой кислоты [28]. При остром панкреатите уровни тромбоксана B повышены, тогда как уровни простагландина E (PGE) снижены. Было показано, что терапия PGE оказывает защитное действие на течение экспериментального острого панкреатита на моделях грызунов с таурохолатами, диетой CDE или панкреатитом, индуцированным церулеином [29–31].Ингибиторы циклооксигеназы, такие как индометацин, использовались для лечения экспериментального острого панкреатита с противоречивыми результатами в более ранних исследованиях [32], но последующие исследования подтвердили положительный эффект индометацина, особенно при его использовании на ранней стадии или до индукции заболевания на моделях крыс с индуцированным таурохолатом. острый панкреатит [33,34]. Подобно циклооксигеназе, липоксигеназа находится ниже арахидоновой кислоты, и исследования показали, что ее ингибирование на моделях крыс с острым панкреатитом, индуцированным таурохолатами, приводит к снижению тяжести заболевания [35].Однако было показано, что антагонизм к лейкотриеновым рецепторам либо ухудшает, либо не влияет на острый панкреатит у крыс [33,36], что указывает на сложность этого пути и необходимость дальнейших углубленных исследований.
Стероидная терапия при остром панкреатите представляет интерес в течение нескольких десятилетий из-за связанной с ней активации лейкоцитов и высвобождения воспалительных цитокинов и хемокинов во время прогрессирования острого панкреатита. Одно экспериментальное исследование на крысах с острым панкреатитом, вызванным церулеином, показало, что эффективность стероидной терапии зависит от тяжести заболевания, причем дексаметазон более эффективен против панкреатита с тяжелым воспалением [37].Другое экспериментальное исследование показало, что дексаметазон уменьшал повреждение поджелудочной железы при профилактическом применении за счет снижения экспрессии молекулы-1 межклеточной адгезии, но был неэффективен в предотвращении рекрутирования лейкоцитов в поджелудочную железу при терапевтическом введении крысам с острым панкреатитом, индуцированным таурохолатами [38]. С другой стороны, стероиды также считаются причиной острого панкреатита, и некоторые исследования показывают, что высокие дозы гидрокортизона могут увеличивать смертность и частоту осложнений, таких как сепсис или инфекция [39–43].
Исследования на животных показали, что интерлейкин-10 (ИЛ-10), противовоспалительный цитокин, может уменьшить тяжесть церулеин-индуцированного острого панкреатита на моделях грызунов, если его вводить до или после индукции заболевания [44]. IL-10 играет защитную роль в местных и системных последствиях заболевания, поскольку было показано, что IL-10 блокирует воспаление, что приводит к улучшению результатов в экспериментальных моделях [45]. Лексипафант, антагонист фактора активации тромбоцитов [46], вызывает системные эффекты и участвует в качестве медиатора в прогрессировании острого панкреатита [47].Исследования показали, что лечение лексипафантом моделей панкреатита на грызунах, индуцированных тауродезоксихолатом и церулеином, снижает тяжесть связанных с панкреатитом осложнений, таких как кишечная дисфункция, системная активация ИЛ-1 и локальное рекрутирование лейкоцитов [48]. Лексипафант уменьшил воспаление, ассоциированное с острым панкреатитом [49], и уменьшил острый некротический панкреатит [50]. Несмотря на положительные результаты применения ИЛ-10 и лексипафанта в исследованиях на животных, их перевод в клиническое использование оказался сложной задачей.
Антиоксиданты
Окислительный стресс и травмы участвуют во многих воспалительных заболеваниях. Свободные радикалы, полученные из кислорода, образуются при экспериментальном остром панкреатите [51], и есть данные о снижении уровня антиоксидантов в крови у пациентов с тяжелым острым панкреатитом [52]. Эти наблюдения привели к экспериментальным исследованиям, которые показали защитный эффект экзогенно вводимых антиоксидантов, таких как селен, за счет уменьшения повреждения поджелудочной железы [53]. Доклинические исследования на грызунах с моделями острого панкреатита, вызванного различными методами, включая инъекцию каррагинана в плевральную полость или л -аргинина гидрохлорида, показали снижение уровня глутатиона и повышение уровня окисленного глутатиона, что свидетельствует о пользе этого вмешательства [ 54].Клинические исследования, которые будут подробно обсуждаться ниже, однако, не дали положительных результатов, и может оказаться, что антиоксиданты более полезны для профилактики и / или в качестве синергических агентов.
Возможные будущие многообещающие терапевтические цели
Одним из основных ограничений доклинических исследований является неопределенность и отсутствие идеальной модели, которая воспроизводит все аспекты болезни человека. Кроме того, доклиническая терапия часто назначается либо на ранней стадии, либо во время индукции острого панкреатита, тогда как на самом деле пациенты часто обращаются с текущим или поздним началом острого панкреатита.Доклинические исследования, демонстрирующие эффективность терапии при назначении препарата после прогрессирования заболевания, с большей вероятностью дадут многообещающие результаты в клинических испытаниях. За исключением острого панкреатита, вызванного ЭРХПГ, при котором можно назначить профилактическую терапию, маловероятно, что агенты, препятствующие возникновению острого панкреатита, будут эффективными, а скорее те, которые нацелены на последующее повреждение, восстановление или воспалительные пути. быть полезным при лечении острого панкреатита.По этой причине мы обсуждаем несколько многообещающих доклинических исследований, нацеленных на эти пути.
Считается, что индуцируемая активность синтазы оксида азота увеличивается при экспериментальном остром панкреатите [55]. Экспериментальные исследования на модели крыс показали, что такие агенты, как S -метилизотиомочевина, индуцибельный ингибитор синтазы оксида азота, могут уменьшать бактериальную транслокацию из кишечника в панкреонекроз, тем самым снижая септические осложнения и смертность при остром панкреатите [56].Лечение такими агентами, как AR-C102222AA или L – N 6 – (1-иминоэтил) -лизин, высокоселективные ингибиторы iNOS, в начале курса после индукции острого панкреатита также показали значительный положительный эффект. эффекты при остром панкреатите у австралийских опоссумов [57] и могут иметь терапевтический эффект за счет уменьшения повреждения поджелудочной железы в будущих клинических исследованиях.
Экспериментальные исследования пентоксифиллина и гепарина показали защитный эффект на моделях крыс с острым панкреатитом.Исследования показали, что пентоксифиллин ослабляет активацию нейтрофилов, провоспалительную передачу сигналов, системное воспаление и уровни цитокинов при экспериментальном остром панкреатите, особенно при раннем введении [58]. Гепарин также представляет собой фармакологическую терапию, вызывающую интерес в последнее время, и растет число сообщений, предполагающих его потенциал в лечении острого панкреатита. Первоначально гепарин изучался в первую очередь из-за его способности улучшать микроциркуляцию, учитывая, что нарушение микроциркуляции способствует воспалительному процессу острого панкреатита.Механизм антикоагуляции гепарина также связан с его противовоспалительным действием, частично вторичным по отношению к снижению стимуляции макрофагов и моноцитов [59]. Экспериментальные исследования показывают, что добавление гепарина приводит к снижению амилазы, эндотелина-1 и воспалительных цитокинов, таких как TNFα, активации NF-κB, а также к улучшению морфологических изменений и сосудистого кровотока в поджелудочной железе [60]. Такие агенты могут улучшить заживление, ослабляя провоспалительные пути, и могут принести пользу при клиническом остром панкреатите.
Повышающая регуляция гемооксигеназы-1 (НО-1) или лечение ее последующими эффекторами и продуктами разложения гема, биливердин и монооксид углерода оказывают защитное действие на различных моделях острого панкреатита на грызунах, индуцированного диетой с таурохолатом, церулеином или CDE [61 -66]. Макрофаги со сверхэкспрессией HO-1 защищают от острого панкреатита [61,67]. Панхематин, одобренный FDA препарат гемина для лечения острой перемежающейся порфирии, может стимулировать выработку HO-1 [68]. Исследования показали, что пангематин, если его назначить до развития экспериментального панкреатита, может активировать гемин-активированные макрофаги и привести к меньшему повреждению поджелудочной железы, а если его назначить после развития острого панкреатита, он также может уменьшить степень повреждения, связанного с панкреатитом [63].Примечательно, что мононуклеарные клетки периферической крови пациентов с острым панкреатитом легкой степени обладают обратимой повышающей регуляцией HO-1, которая связана с клиническим выздоровлением, поддерживая терапевтический потенциал HO-1 и продуктов распада гема у пациентов с острым панкреатитом. Биливердин через рецептор арилуглеводородов активирует IL-22 [66]. В последнее время возник большой интерес к роли IL-22, цитокина, продуцируемого гемопоэтическими клетками, нацеленного на неиммунные клетки [66].Интересно, что поджелудочная железа имеет самую высокую экспрессию рецептора IL-22 среди любых других тканей [69], и было показано, что лечение IL-22 улучшает экспериментальный острый панкреатит [70]. Таким образом, HO-1 и его нижестоящие эффекторы являются потенциальными мишенями для клинического острого панкреатита.
TNFα играет центральную роль в патогенезе местных и отдаленных осложнений острого панкреатита [71], а его блокада улучшает экспериментальный острый панкреатит, вызванный церулеином, таурохолатом или диетой CDE в исследованиях на мышах [72,73].Хотя теоретически существует повышенный риск инфекционных осложнений при терапии анти-TNF, есть сообщения о случаях с положительным исходом у пациентов с острым панкреатитом, которые получали анти-TNF из-за сопутствующего заболевания, для которого была показана терапия против TNF [74,75] . Таким образом, при тщательном отборе пациентов вполне вероятно, что терапия анти-TNF даст положительные результаты в клинических испытаниях.
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Основываясь на патофизиологии острого панкреатита и проведенных фундаментальных научных исследованиях, дающих доказательства перспективной фармакологической терапии, было проведено множество клинических исследований для оценки эффективности этих методов лечения, включая антисекреторные агенты, ингибиторы протеазы, иммуномодуляторы, антисекреторные препараты. -воспалительные агенты и антиоксиданты.
Антисекреторные агенты
Впервые об использовании глюкагона при остром панкреатите в 1971 году сообщили Knight et al [76], и с тех пор несколько последующих неконтролируемых клинических испытаний показали клиническое улучшение, уменьшение боли и снижение уровня ферментов. мероприятия при остром панкреатите [77-79]. Однако в последующем двойном слепом исследовании с участием 69 пациентов было обнаружено, что глюкагон не оказывает значительного влияния на смертность пациентов по сравнению с плацебо [80]. Дальнейшие клинические испытания не выявили различий в смертности и заболеваемости, таких как боль и продолжительность пребывания в стационаре [81,82].
Атропин также изучался в рандомизированном клиническом исследовании, но не оказал значительного влияния на клиническое течение пациентов по сравнению с отсутствием лечения [83]. Считалось также, что вливание кальцитонина лосося сильно подавляет секрецию желудочного сока, такую как желудочная кислота, пепсин и гастрин [84-86], а также секрецию ферментов поджелудочной железы, стимулируемую различными стимуляторами секреции, не влияя на секрецию жидкости и электролитов [87], таким образом смягчая патогенез. острого панкреатита [88].Многоцентровое рандомизированное двойное слепое исследование по оценке использования синтетического кальцитонина лосося при остром панкреатите показало, что, хотя смертность не изменилась, количество пациентов без боли и нормализованной сывороточной амилазы было выше в группе лечения по сравнению с группой плацебо. Другие параметры, такие как доза анальгетика, количество лейкоцитов и нормализация семи клинических и лабораторных критериев, показали положительную динамику в группе лечения, но не были клинически значимыми [88].
Клинические испытания хорошо изучили использование соматостатина для лечения острого панкреатита, учитывая, что он подавляет экзокринную секрецию поджелудочной железы, снижает внутренний кровоток, стимулирует ретикулоэндотелиальную систему печени и модулирует каскад воспалительных цитокинов [89].Однако несколько рандомизированных клинических исследований не показали клинически значимого преимущества соматостатина [90–94]. С другой стороны, метаанализ семи публикаций действительно показал улучшение общей смертности от соматостатина при тяжелом остром панкреатите (OR = 0,36, 95% CI: 0,2-0,64), но не было значительного снижения частоты осложнений у пациентов с острый панкреатит [95].
Октреотид, синтетический аналог соматостатина, также прошел клинические испытания. Хотя первоначальные небольшие исследования не показали какого-либо общего улучшения показателей смертности, они предположили снижение тяжести острого панкреатита, уменьшение местных осложнений и более ранний возврат к пероральному приему [96].Однако одно из крупнейших клинических испытаний с участием 302 пациентов с панкреатитом средней и тяжелой степени не показало какой-либо клинической пользы [97], но меньшее исследование с участием 50 пациентов с тяжелым острым панкреатитом показало клинически значимое снижение частоты сепсиса (76–24%). , ОРДС (56–28%), пребывание в больнице (33,1–20,6 дня) и смертность (8–2 смерти) [98]. В то время как более старый проведенный метаанализ действительно показал улучшение смертности от тяжелого острого панкреатита (OR = 0,57, 95% ДИ: 0,35–0,88) [95], другой более свежий метаанализ, ограничивавший их оценку четырьмя исследованиями более высокого качества, не дал показать какие-либо преимущества в отношении сепсиса, смертности или осложнений [99].
Таким образом, клинические исследования, оценивающие использование антисекреторных агентов, предоставили неубедительные доказательства их преимуществ. По всей видимости, пользы от этих агентов при легком остром панкреатите нет, а при тяжелом остром панкреатите польза не ясна. Следовательно, эти агенты в настоящее время не рекомендуются в клинической практике [4,100].
Ингибиторы протеазы
Одним из первых изученных ингибиторов протеаз является апротинин, и первоначальные исследования показали некоторое улучшение показателей смертности, хотя последующие исследования не смогли повторить такие результаты [101,102].Исследования доставки апротинина через перитонеальный лаваж показали меньший некроз в экспериментальной группе со снижением активации комплемента (в частности, меньше C3a и больше уровней ингибитора C1 в плазме), но нет общей разницы в смертности [103-105]. Апротинин все еще может играть роль в лечении острого панкреатита, учитывая, что он не вводился в достаточно высоких дозах, чтобы вызвать достаточное ингибирование активности протеазы, а исследования не имели достаточной мощности [106].
Габексат мезилат представляет собой меньший ингибитор протеазы, который изучался в клинических испытаниях на людях [107].В то время как ранние более мелкие клинические исследования предполагали снижение смертности от применения этой терапии [108, 109], более крупное рандомизированное контролируемое исследование пациентов с умеренным и тяжелым острым панкреатитом не обнаружило клинической пользы [110, 111]. Два других метаанализа также демонстрируют отсутствие преимущества в отношении смертности, хотя они показали снижение потребности в хирургическом вмешательстве и меньшее количество осложнений [95, 112]. Недавнее исследование показало некоторую пользу габексата при непрерывной регионарной артериальной инфузии (CRAI) [113].
Нафомостат – новый синтетический ингибитор протеазы, в сто раз более мощный, чем габексат [107]. Клинические исследования, оценивающие доставку нафомостата через CRAI вместе с антибиотиками, показали более высокую смертность и меньшую частоту некроза при более раннем введении препарата [114]. Исследования также показали, что доставка лекарства через CRAI по сравнению с не-CRAI снижает потребность в хирургическом вмешательстве и улучшает выживаемость [115,116].
Ни один из упомянутых выше ингибиторов протеазы в настоящее время не является частью стандартной клинической помощи при лечении острого панкреатита, поскольку необходимы более масштабные и адекватно обоснованные исследования, прежде чем их рекомендовать для клинического использования.Нафомостат, однако, является наиболее перспективным из трех, особенно при введении через CRAI в сочетании с антибиотиками.
Иммуномодуляторы
На основании положительных доклинических результатов Лексипафант прошел клинические испытания у пациентов с тяжелым острым панкреатитом. Первое клиническое испытание, оценивающее использование этой терапии, не показало разницы в смертности, но показало снижение органной недостаточности [117]. Другое исследование показало значительно меньшую органную недостаточность, снижение смертности и ССВО [118].Однако самое крупное рандомизированное клиническое исследование, включающее эту терапию, не показало значительного снижения органной недостаточности или местных осложнений, что привело к выводу, что лексипафант сам по себе не может лечить тяжелый острый панкреатит [119].
Дотрекогин альфа, аналог эндогенного протеина С, показал некоторые преимущества при лечении острого панкреатита [120]. Эндогенный протеин С вырабатывается в печени и ингибирует образование тромбина и облегчает тромболизис. Учитывая, что более низкие уровни активированного протеина C связаны с более высокой смертностью при остром панкреатите, активированный протеин C, как полагали, смягчает тяжелый острый панкреатит, модулируя иммунную систему через регулирование взаимодействия лейкоцитов с эндотелием и митоген-активированными киназами и улучшая кишечную микроциркуляцию [121].Первые сообщения о клинических случаях показали некоторую пользу от использования дотрекогина альфа при остром панкреатите [122], но последующее пилотное исследование не показало каких-либо клинически значимых различий с использованием дотрекогина альфа [123].
Противовоспалительные средства
Индометацин, который ингибирует активность фосфолипазы A2 и активность циклооксигеназы, уменьшая, таким образом, нейтрофильно-опосредованное воспаление, был клинически изучен на основе более ранних доклинических исследований [124]. Однако одно исследование, оценивающее эту терапию, сообщило только об уменьшении боли и употреблении опиатов при назначении пациентам с острым панкреатитом [125], предполагая обезболивающее, но не связанное с противовоспалительным действием.До сих пор преимущества индометацина в значительной степени ограничивались панкреатитом после ЭРХПГ [126].
Стероидная терапия широко используется для уменьшения воспаления в различных системах органов. Хотя было показано, что стероидная терапия эффективна при лечении аутоиммунного панкреатита [127], однако при остром панкреатите стероидная терапия участвует в индукции заболевания [128]. Посмертное исследование, проведенное Carone и Liebow, показало гистологические доказательства острого панкреатита или перипанкреатического некроза жира у 16 из 54 пациентов, получавших стероиды [129].Первые сообщения о случаях также связывают использование стероидов с острым панкреатитом [130]. Исследования также показали, что кортикостероиды не имеют положительного эффекта в профилактике панкреатита после ЭРХПГ [131]. Однако, учитывая, что некоторые доклинические исследования предполагают, что стероиды могут уменьшать воспалительный каскад, рекрутирование лейкоцитов и последующее повреждение поджелудочной железы при профилактическом применении [38], необходимы дальнейшие хорошо спланированные исследования.
Антиоксидантные агенты
В нескольких клинических испытаниях оценивалась польза антиоксидантных агентов при остром панкреатите с учетом роли активных форм кислорода и клеточного повреждения при остром панкреатите, а также доказательств, полученных в ходе доклинических исследований.Изученные антиоксиданты включают н-ацетилцистеин, метионин, бета-каротин, селен, аскорбиновую кислоту и альфа-токоферол.
Рандомизированное клиническое испытание, оценивающее лечение ацетилцистеином, селеном и витамином С, показало повышение уровня антиоксидантов в сыворотке и снижение маркеров окислительного стресса, но не улучшило дисфункцию органов [132]. Другое исследование с пациентами, получавшими витамин С, н-ацетилцистеин и другие антиоксиданты, не показало значительной разницы в частоте осложнений или продолжительности пребывания в больнице [133].Третье недавнее клиническое исследование витаминов A, C и E также не показало значительных различий в дисфункции органов [134].
Исследования по оценке использования глутамина, более мощного антиоксиданта, были более многообещающими. Одно исследование, в котором 80 пациентов были рандомизированы для приема глутамина, показало уменьшение количества осложнений, продолжительности госпитализации, необходимости в хирургическом вмешательстве и смертности при введении препарата на раннем этапе после госпитализации [135]. Метаанализ рандомизированных контрольных исследований глутамина показал улучшение показателей смертности (ОР = 0.3, 95% ДИ: 0,15–0,6) и снижение инфекционных осложнений (ОР = 0,58, 95% ДИ: 0,39–0,87), но без разницы в продолжительности пребывания в больнице. Польза от глутамина наблюдалась только у пациентов, получавших полное парентеральное питание [136]. Таким образом, роль антиоксидантной терапии при остром панкреатите еще предстоит определить.
Другие методы лечения
В клинических исследованиях также оценивались различные другие методы лечения острого панкреатита. Считается, что антифибринолитики, такие как эпсилон-аминокапроновая кислота (EPCA), улучшают патогенез острого панкреатита, подавляя активацию плазминогена, плазмина и трипсина, подавляя калликреин поджелудочной железы и повышая активность антитрипсина в сыворотке [137].Однако клиническое исследование, оценивающее использование EPCA и апротинина при остром панкреатите, не показало какого-либо клинически значимого улучшения исходов, таких как продолжительность госпитализации и нормализация лабораторных показателей, по сравнению с группой обычного лечения и группами лечения апротинином [138].
Свежезамороженная плазма (СЗП) также оценивалась при лечении острого панкреатита с учетом лабораторных исследований, которые показали ингибирующее действие СЗП на протеолитическую активность в сыворотке крови пациентов с острым панкреатитом [139].В то время как одно первоначальное проспективное пилотное клиническое исследование показало снижение смертности при приеме СЗП у пациентов с острым панкреатитом при введении в течение первых пяти дней от начала заболевания [139], более крупное многоцентровое контролируемое клиническое исследование не показало улучшения клинических результатов в группа, получавшая СЗП, в отличие от группы, получавшей коллоиды [140].
Молекулярные пути развития мишеней включают калликреин-кинин и систему комплемента, учитывая, что тяжелый острый панкреатит связан с повышенными уровнями C3a и sC5b-9 [141].Ингибитор C1-эстеразы блокирует множество протеолитических ферментов, включая активированный C1-комплекс и калликреин [142], и как экспериментальные исследования, так и небольшие исследования на людях показали, что ингибитор C1-эстеразы обладает некоторым защитным действием при тяжелом остром панкреатите [143]. В настоящее время фармакологические мишени системы комплемента используются при множестве других заболеваний, таких как наследственный ангионевротический отек, пароксизмальная ночная гемоглобинурия и гемолитико-уремический синдром [144], которые могут способствовать более быстрой трансляции.
ЗАКЛЮЧЕНИЕ
Доклинические и клинические исследования (Таблицы и) показали многообещающие возможности для новой фармакологической терапии острого панкреатита, которая может дополнять традиционное лечение, включающее поддерживающие меры, такие как жидкостная реанимация, нутритивная поддержка, контроль боли и антибиотики, такие как нужный. Доклинические и клинические исследования показали многообещающие возможности применения различных классов терапии, которые включают антисекреторные агенты, ингибиторы протеаз, иммуномодуляторы и противовоспалительные агенты, а также антиоксиданты.Хотя некоторые доказательства в пользу этих методов лечения все еще остаются неубедительными и не были переведены в текущие стандартные методы лечения, существует огромная потенциальная терапевтическая польза, как продемонстрировано в этих исследованиях. Иммуномодулирующие фармакологические методы лечения также еще предстоит превратить в стандартную клиническую помощь при остром панкреатите [67].
Таблица 1
Резюме фармакологических агентов, изученных при экспериментальном остром панкреатите
| Фармакологическое средство | Модель на животных | Оценка результатов | 4 Цитаты | Механизм индукции панкреатита | ||
| Антисекреторные агенты | ||||||
| Глюкагон | Собака | Обструкция двенадцатиперстной кишки, инфузия протока поджелудочной железы 48 инфузия раствора лактатного протока 4 или инфузия протока поджелудочной железы 4 полезен по сравнению с простой объемной реанимацией | [15] | |||
| Свинья | Геморрагический панкреатит, вызванный инъекцией желчи в проток поджелудочной железы | Сниженная смертность | [16] | атин|||
| Таурохолат | Отсутствие снижения смертности | [21, 22] | ||||
| Ингибиторы протеаз | ||||||
| Апротинин | Собака | Геморрагический панкреатит | 906– терапевтический потенциал 906 Геморрагический панкреатит, терапевтический потенциал 904–197 ]||||
| Хлорофилл-а | Морская свинка | Таурохолат-индуцированный некротический панкреатит | Выживаемость | [25-27] | ||
| Противовоспалительная терапия | 448470 P448470 мышиТаурохолат, диета CDE или церулеин | Защитный эффект | [29-31] | |||
| Индометацин | Крыса | Оливковое масло или таурохолат | , особенно в раннем возрасте] | |||
| Ингибитор липоксигеназы | Крыса | Таурохолевая кислота 9 0470 | Защитный эффект | [35] | ||
| Стероид | Крыса | Церулеин и таурохолат | Уменьшение воспаления и защитное действие | [37-43] | ||
| [37-43] | ||||||
| [37-43] | ||||||
| Caer 9048 IL-10 | Снижение степени тяжести заболевания | [44, 48-50] | ||||
| Лексипафант | Крыса, мыши | Внутрипротоковое введение 5% тауродезоксихолата или церулеина натрия | Снижение степени тяжести SIR | , бактериальная транслокация | [46, 47] | |
| Гемин / пангематин / биливердин / CO / IL-22 | Крыса, мыши | диета с церулеином, таурохолатом или CDE | Защитные и терапевтические эффекты | [61-67] | ||
| Анти-TNF альфа | Мыши | диета с церулеином, таурохолатом или CDE | Снижение воспалительной реакции и гибели клеток | [72-75] 904 70 | ||
| Антиоксиданты | ||||||
| Tempol | Мыши | каррагинан, введенный в плевральную полость | Снижение воспаления и шока | [54] | ||
| Селен | гидрохлорид 9048 Селен Хлор6 9048 Селен 9048 Уменьшение травмы поджелудочной железы[53, 145] | |||||
Таблица 2
Резюме фармакологических агентов, изученных при клиническом остром панкреатите
| Фармакологическое средство | 70 Дизайн выборки 903 | Оценка результатов | Цитаты | ||||||||
| Снижение SIRS | Снижение органной недостаточности | Снижение продолжительности пребывания | 9018 Снижение продолжительности пребывания 470 9018 9018 904 90 466Антисекреторные агенты | ||||||||
| Глюкагон | РКИ | 22-69 | Не сообщалось | Не сообщалось | Нет | Нет | [76-82] | 51 | Не сообщалось | Не сообщалось | Нет | Нет | [83] |
| Кальцитонин | RCT | 94 | Не сообщалось | Не сообщалось | Не сообщалось | Не сообщалось | ↓ боль, более ранняя нормализация лабораторных показателей | [84-86] | |||
| Соматостатин | РКИ / метаанализ | 50-703 | Не сообщалось | Неопределено (не влияет на полиорганную недостаточность, но ↓ местные осложнения) | Неопределенный | Неопределенный | ↓ абсцесс и некроз поджелудочной железы, ↓ местное воспаление | [90-95] | |||
| Октреотид | РКИ / метаанализ | 19–948 | Да | Да | Неопределенный | Неопределенный | [97-99] | ||||
| 48-105 | Не сообщалось | Нет | Да | Нет | ↓ панкреонекроз, ↓ активация комплемента | [101-105] | |||||
| Анализ мезилата Gabexate | 42-898 | Не сообщалось | Нет | Нет | Нет | CRAI ↓ пребывание в больнице и SIRS | [108-113] | ||||
| Нафомостат | RCT | инфекция некротической ткани поджелудочной железы) | Не сообщается | Не сообщается | Да | Только CRAI + abx имеет преимущество | [114-11 6] | ||||
| Иммуномодуляторы | |||||||||||
| Lexipafant | РКИ | 50-290 | Да | Да | Не сообщалось | Да | 117-1190 ] | ||||
| Dotrecogin alfa | RCT | 32 | Да | Нет | Не сообщается | Нет | [122, 123] | ||||
| Acety | 39-53 | Неопределенный (↓ CRP, но не sig) | Нет (тенденция к ↑ MOF) | Нет | Нет | [132-134] | |||||
| Глютамин | RCT / мета-анализ | 505 | Да | Да | Нет | Да | [135, 136] | ||||
Есть также новые цели для p хармакологическая терапия, которая может расширить возможности лечения острого панкреатита.Стратегии, которые изменяют активность ключевых иммунных клеток в воспалительном каскаде, вызванном острым панкреатитом, имеют большой потенциал [67]. Другие молекулярные мишени, такие как те, которые мешают калликреин-кининовой, протеолитической и системе комплемента, как обсуждается при дальнейших разработках, потенциально могут быть применены и к острому панкреатиту в будущем. В дополнение к расширению целей фармакологической терапии, существующие методы лечения должны быть лучше изучены в клинических испытаниях в будущем.Экспериментальные доклинические исследования выявили несколько методов лечения, которые не доказали свою эффективность в клинических испытаниях и, таким образом, не были переведены на клиническую арену. Одна из причин этого несоответствия может заключаться в том, что в моделях на животных фармакологическая терапия часто назначается до того, как наступает повреждение поджелудочной железы, что дает доказательства того, что терапия может обеспечивать защитный, но не обязательно терапевтический эффект.
В клинических исследованиях, однако, интересующее лекарство часто тестируется после того, как повреждение поджелудочной железы уже произошло и воспалительный каскад, вызванный острым панкреатитом, уже начался.В будущем улучшенный дизайн клинических испытаний, в рамках которых лечение будет проводиться раньше, с момента появления симптомов, может максимизировать способность препарата прерывать воспалительный каскад и давать лучшие результаты. Клинические испытания также необходимо стандартизировать в отношении критериев отбора, поддерживающих подходов к лечению и измеряемых результатов. Следует четко указать клинически значимые первичные и вторичные исходы, такие как смертность, органная недостаточность, ССВО, некроз поджелудочной железы и местные осложнения, продолжительность пребывания в больнице, потребность в обезболивающих, качество жизни и стоимость лечения.
Несмотря на неубедительные доказательства терапевтического эффекта многих изученных к настоящему времени фармакологических методов лечения острого панкреатита, существует большая потребность и перспективность в разработке эффективной фармакологической терапии острого панкреатита. Лучшее понимание патофизиологии заболевания и уроки, извлеченные из прошлых клинических исследований, предлагают отличную основу для расширения, так что текущее лечение панкреатита, в значительной степени характеризующееся поддерживающей терапией, может в конечном итоге быть переведено не только на профилактическую, но и на репаративную и эффективную терапию. .Лучшая характеристика и стандартизация популяции пациентов, наряду с хорошо контролируемыми и адекватно обоснованными клиническими исследованиями, привязанными к стандартизованным результатам, обеспечат надежную и достоверную оценку терапевтической роли доклинических испытанных агентов.
Точная медицина острого панкреатита: текущее состояние и перспективы на будущее | Точная клиническая медицина
Аннотация
Острый панкреатит – распространенное воспалительное заболевание поджелудочной железы, преимущественно вызванное желчными камнями, избытком алкоголя и гипертриглицеридемией, при тяжелом заболевании, приводящем к смерти до 50%.Несмотря на значительные исследования и доклинические перспективы, не существует целевых лекарственных препаратов для лечения этого заболевания, а подходы точной медицины значительно отсутствуют по сравнению с другими состояниями здоровья. Достижения в области применения omics будут способствовать усовершенствованию доклинических моделей и идентификации целей, а также обнаружению биомаркеров для уточнения дизайна испытаний с упором на стратификацию риска, выбор субъектов и определение результатов. Рандомизированное лечение острого панкреатита инфликсимабом: двойное слепое плацебо-контролируемое многоцентровое исследование (RAPID-I) – это новаторское исследование острого панкреатита, которое в настоящее время проводится, и может служить инновационной моделью для внедрения точной медицины. стратегии острого панкреатита в будущем.
Введение
Точная медицина – понятие не новое. Гиппократ, так называемый «отец западной медицины», писал более 2500 лет назад, что «разные (лекарства) для разных пациентов, потому что сладкие не приносят пользу всем, а также вяжущие, и не все пациенты могут их лечить». пейте то же самое ». 1 Действительно, практика адаптации и модификации стратегий лечения в зависимости от пациента, которого лечат, практиковалась на протяжении веков превосходными врачами и хирургами.Уильям Ослер, выдающийся канадский врач, писал в 1892 году: «Если бы не большое разнообразие людей, медицина с таким же успехом могла бы быть наукой, а не искусством». только на основании клинического опыта в значительной степени предрасположен к предвзятости и ограничен недостатками имеющихся научных знаний. Методы применения точной медицины появились недавно и уже прочно обосновались. Текущие технологические и научные достижения позволяют нам идентифицировать важные геномные и молекулярные паттерны, которые облегчают определение индивидуального риска, раннюю диагностику, оценку серьезности, прогноз заболевания и определение оптимальных стратегий лечения.Тем не менее, применение этих технологий в различных условиях здоровья человека не было равным: одни органы и заболевания приносили пользу быстрее, чем другие. Например, первое полногеномное ассоциативное сканирование (GWAS) для острых респираторных воспалительных состояний (астма) было опубликовано в 2010 году, 3 , и хотя первый GWAS по хроническому панкреатиту был опубликован вскоре после того, как в 2012 году, 4 первый GWAS острый панкреатит все еще ожидается.Сравнение количества проиндексированных публикаций Pubmed, связанных с точной медициной, по годам и типу органа, показывает, насколько далеко позади болезнь поджелудочной железы (рис. 1). Число публикаций по точной медицине, посвященных заболеваниям поджелудочной железы, росло медленнее всего, и среди всех оцениваемых систем органов было меньше всего. Хотя это несоответствие может быть объяснено различиями в заболеваемости, отсутствием целевого лечения, доступностью финансирования исследований и социально-экономическим бременем здравоохранения, 5 очевидно, что когда дело доходит до точной медицины, лечение заболеваний поджелудочной железы в настоящее время далеко не точное. .
Рис. 1.
Публикации по точной медицине, индексируемые по системам органов. Количество публикаций в различных областях заболеваний, оцененных с помощью поиска по конкретным органам MeSH и точной медицины в базе данных Pubmed (10.04.19).
Рисунок 1.
Индексированные публикации по точной медицине по системам органов. Количество публикаций в различных областях заболеваний, оцененных с помощью поиска по конкретным органам MeSH и точной медицины в базе данных Pubmed (10.04.19).
Острый панкреатит – это воспалительное заболевание поджелудочной железы, заболеваемость которым за последние 50 лет увеличилась во всем мире. 6,7 Согласно пересмотренной классификации Атланты, состояние классифицируется как легкое примерно у 60% пациентов, умеренное у 20-30% и тяжелое у 5-10%, с риском смерти до 50% у пациентов. тяжелое заболевание. 8–10 Желчные камни и алкоголь – две наиболее распространенные этиологии у взрослых в западных странах и Японии, 11,12 , в то время как в Китае наблюдается выраженная частота острого панкреатита, связанного с гипертриглицеридемией (рис.2) 13–18 , что составляет примерно 30% пациентов в больших когортных сериях. 19,20 Факторы риска тяжелого острого панкреатита включают старение, сопутствующие заболевания, повышенный индекс массы тела и ранее существовавший диабет. 21,22 Несмотря на большое количество текущих международных исследований со значительными доклиническими перспективами, в настоящее время нет доступных лицензированных целевых лекарственных препаратов. 23 Этот факт, вместе с резким падением общих инвестиций в исследования, наблюдался при падении с 25.От 7% до 10,7% воспалительных заболеваний желудочно-кишечного тракта в США за последние 50 лет 5 были значительными препятствиями на пути внедрения точной медицины при панкреатите. Доклинический успех не был преобразован в успех испытания по ряду причин, вероятно, из-за неправильного выбора мишеней и недостаточной доклинической характеристики, отбор подгрупп пациентов, вряд ли покажет максимальные положительные эффекты, скорость проведения лечения и отсутствие широко применимых результатов. меры. 24 Однако там, где есть дефицит, есть возможности. Из-за отсутствия эффективных лекарственных препаратов прецизионная медицина при остром панкреатите находится на более ранней стадии, чем большинство других состояний (рис. 1), при этом усилия точной медицины в первую очередь направлены на прогнозирование, уточнение испытаний и оптимизацию лечения осложнений. В настоящее время панкреатология набрала значительный импульс, и в настоящее время осуществляется множество совместных национальных и международных сетей и инициатив, 25 готовых использовать технологические достижения, способствующие персонализированным подходам.Обрисовываются и обсуждаются области текущего применения и будущие возможности для подходов точной медицины при остром панкреатите.
Рисунок 2.
Объединенная частота острого панкреатита, связанного с гипертриглицеридемией, по данным многочисленных исследований в Китае. Объединенная заболеваемость составила 0,13 (95% ДИ: 0,1–0,17).
Рисунок 2.
Объединенная частота острого панкреатита, связанного с гипертриглицеридемией, по данным многочисленных исследований в Китае.Объединенная заболеваемость составила 0,13 (95% ДИ: 0,1–0,17).
Доклинические модели и идентификация целей
Точные механизмы, приводящие к острому панкреатиту, еще предстоит полностью выяснить, хотя в последние десятилетия был достигнут большой прогресс в лучшем понимании механизмов поражения ацинаров поджелудочной железы. 26 Они выявили перегрузку кальцием ацинарных клеток поджелудочной железы, 27 митохондриальную дисфункцию, 27,28 преждевременную активацию пищеварительных ферментов, 29 активацию NF-κB, 30 нарушение аутофагии, 31 32 и вакуолизацию все имеют решающее значение в патогенезе острого панкреатита.Дальнейшие исследования подчеркивают ключевую роль врожденного иммунитета 33 и высвобождение ключевых молекулярных паттернов, связанных с клеточными повреждениями (DAMP), особенно HMGB1 34 и гистонов. 35,36 Три очень многообещающие стратегии фармакологического ингибирования: ингибирование канала высвобождения кальция (CRAC), 37 ингибирование митохондриальной проницаемости переходной поры (MPTP), 28 и ингибирование кинуренин-3-монооксигеназы (KMO), 38 все это стало результатом обширных исследований механики животных.В большинстве этих моделей используются ткани грызунов из-за сложности получения соответствующей ткани человека. Хотя исследования паренхиматозных клеток поджелудочной железы показали, что пути в клетках грызунов отражают таковые у людей, 28,39–41 , необходимо помнить, что существенные различия сохраняются, особенно потому, что люди, страдающие острым панкреатитом, остаются разнообразными, демонстрируя генетическую и эпигенетическую гетерогенность. а также различные воздействия окружающей среды. Все это способствует различию в восприимчивости, тяжести и прогрессировании острого панкреатита.
Применение омикс-технологий с подходом системной медицины будет способствовать пониманию неоднородности реакции в противоположных моделях и, что наиболее важно, в условиях человеческого существования, позволяя проводить соответствующие сравнения. Затем это определит оптимальную полезность различных доклинических моделей, а также разработает более новые клинически значимые модели, чтобы помочь текущему открытию трансляционных лекарств и идентификации дальнейших мишеней. По мере того, как многообещающие терапевтические стратегии продвигаются к клиническим испытаниям, биомаркеры будут иметь важное значение для стратификации риска, выбора субъектов и определения оптимального результата, и все это применимо для получения улучшенных результатов.
Обнаружение биомаркеров для улучшения дизайна исследования
Раннее прогнозирование тяжелого острого панкреатита с помощью новых биомаркеров крови и изображений имеет важное значение для стратификации риска будущих клинических испытаний. Это по-прежнему тесно связано с лучшими методами определения значимых биологических путей, влияющих на тяжесть, способствующих лучшему отбору пациентов и более четким определенным результатам. В целом, сосредоточение внимания на этих областях позволит применить более «индивидуальный» подход к терапии.
Стратификация риска
Хотя количество серьезных осложнений, связанных с острым панкреатитом, в целом остается небольшим, последствия стойкой органной недостаточности могут быть опасными для жизни. В результате были приложены значительные усилия для раннего выявления пациентов с повышенным риском осложнений. Были разработаны многочисленные подходы к стратификации риска, которые включают оценки клинического прогноза, биохимические параметры и алгоритмы машинного обучения. 42 Сравнение девяти систем оценки в двух проспективно собранных когортах пациентов, госпитализированных с острым панкреатитом, не продемонстрировало явных преимуществ какого-либо конкретного подхода к выявлению пациентов с повышенным риском стойкой органной недостаточности. 42 Недавние крупные когортные исследования страдали от неточных прогностических индексов для стратификации степени тяжести. 43 Этот провал прогноза является значительным ущербом для точной стратификации исследования и, вероятно, частично объясняется отсутствием исследований, использующих подходы системной медицины и применения точной медицины. 44 Применение омикс-стратегий для выявления новых биомаркеров принесло бы очевидную пользу, но такие исследования острого панкреатита отсутствуют.
Определение результата
В предыдущем систематическом обзоре литературы клинических испытаний острого панкреатита с участием людей было выявлено 61 исследование с 1996 по 2014 год. 45 Наиболее частым первичным результатом была смертность (16%). Другие общие параметры исхода включали органную недостаточность (15%), инфекции поджелудочной железы (13%) и синдром системного воспалительного ответа (SIRS, 10%). Выбор конечных точек исследования при остром панкреатите следует определять в зависимости от контекста предлагаемого вмешательства.Традиционные подходы к разработке новых терапевтических средств при остром панкреатите сосредоточены на профилактике или уменьшении тяжелых форм болезни. Эти исследования включали начальную стратификацию риска для выявления подгрупп пациентов с более высоким риском для улучшения таких исходов, как стойкая органная недостаточность или смертность. 45 Эти стратегии не были оптимальными, особенно в исследованиях, в которых набор участников проводился в течение 72–96 часов после поступления, несмотря на экстренный характер состояния.Альтернативным подходом было бы включение всех пациентов с острым панкреатитом сразу после начала заболевания. Параллельно с этим улучшение сообщаемых пациентами результатов, связанных с болью, дефицитом питания и качеством жизни, наряду с включением суррогатных результатов тяжести, таких как С-реактивный белок (СРБ), альбумин и нейтрофилы, предлагает потенциал для более легкого исследования. поведения и большей обобщаемости результатов, но требует подтверждения.
RAPID-I: пример для точной медицины будущего
Ожидаются результаты нескольких стратегий omics-платформы при остром панкреатите, сфокусированных на геномных, транскриптомных, протеомных и метаболомных стратегиях человека.Многообещающее и активно использующее вопросы, поднятые в этом обзоре, представляет исследование RAPID-I (рандомизированное лечение острого панкреатита инфликсимабом: двойное слепое, плацебо-контролируемое, многоцентровое испытание). Это испытание включает обнаружение транскриптомных биомаркеров и механистическую оценку терапии анти-TNF-α при остром панкреатите. Взрослые, поступившие с новым диагнозом острого панкреатита любой степени тяжести и болями менее чем за 24 часа до госпитализации, рандомизированы для получения двойной слепой инфузии 5 или 10 мг / кг инфликсимаба или физиологического раствора, начатой в течение 12 часов после допуск.Первичным критерием исхода является кумулятивный СРБ (измеряется через определенные промежутки времени в течение 28 дней), с вторичными критериями исхода – боль, дефицит питания, SIRS, баллы оценки последовательной органной недостаточности (SOFA), повреждение поджелудочной железы при компьютерной томографии, осложнения, продолжительность пребывания в больнице. пребывание и результаты, сообщаемые пациентом (например, используйте анкету EQ-5D-5L). Будет проведен анализ субпопуляции транскриптома, цитокинов и лейкоцитов, чтобы получить представление о механизме и проверить прогностические и прогностические маркеры тяжести и ответа на лечение.RAPID-I разработан, чтобы служить моделью для будущих испытаний острого панкреатита, чтобы ускорить достижение цели индивидуализированных подходов к медицине.
В будущих исследованиях персонализированной медицины может потребоваться адаптивный дизайн исследований для получения максимальной пользы; мы бы предложили как можно шире использовать подходы системной медицины, независимо от того, используют ли они более традиционные или новые разработки. Подходы могут включать объединение фаз (например, фазы I и II или фазы II и III с соответствующими статистическими соображениями, чтобы включить точки, которые не годятся) с первым приоритетом для получения лицензированного лекарства, которое оказывает большое влияние на легкие, умеренные и / или тяжелый острый панкреатит.Более умозрительные подходы могут включать зонтичные испытания (для изучения нескольких целевых терапий в контексте одного заболевания), корзины испытаний (для изучения одной целевой терапии в контексте нескольких заболеваний или подтипов заболеваний) и платформенные испытания (для изучения нескольких целевых терапий). в контексте одного заболевания на постоянной основе, с терапией, позволяющей входить или уходить с платформы на основе алгоритма принятия решений). 46
Заключение
Прецизионная медицина при остром панкреатите остается на ранней стадии эволюции, чему в значительной степени препятствует отсутствие целевой лекарственной терапии в результате ранее несовершенных стратегий доклинических исследований и дизайна клинических испытаний.Существует прекрасная возможность исправить это положение благодаря ожидаемым результатам крупных омиковых исследований острого панкреатита, которые потенциально могут облегчить идентификацию целей и открытие биомаркеров, открывая путь для улучшенных и потенциально более успешных будущих испытаний. Мы с нетерпением ждем результатов исследования RAPID-I и их применения в подходах точной медицины для лечения острого панкреатита в будущем.
Благодарности
Р.М. имеет стипендию факультета здравоохранения и наук о жизни Ливерпульского университета и пользуется поддержкой больниц Королевского Ливерпульского и Бродгринского университетов NHS Trust; Р.С. имеет награду старшего исследователя Национального института исследований в области здравоохранения (R.S.) и поддерживается Советом по медицинским исследованиям, Национальным институтом исследований в области здравоохранения и Европейским союзом.
Заявление о конфликте интересов
R.S. получил финансирование на исследования (выплаченное Ливерпульскому университету в течение последних трех лет) от AbbVie, CalciMedica, Cypralis, GlaxoSmithKline, Merck / MSD и Novartis.
Список литературы
1Sykiotis
GP
,Kalliolias
GD
,Papavassiliou
AG
.Фармакогенетические принципы в трудах Гиппократа
.J Clin Pharmacol
2005
;45
(11
):1218
–20
. .2W., O., Принципы и практика медицины [Книга].
1892
.3Moffatt
MF
,Gut
IG
,Demenais
F
и др.Крупномасштабное геномное ассоциативное исследование астмы на основе консорциума
.N Engl J Med
2010
;363
(13
):1211
–21
. .4Whitcomb
DC
,LaRusch
J
,Krasinskas
AM
и др.Общие генетические варианты в локусах CLDN2 и PRSS1-PRSS2 изменяют риск связанного с алкоголем и спорадического панкреатита
.Нат Генет
2012
;44
(12
):1349
–54
..5Szentesi
A
,Tóth
E
,Bálint
E
и др.Анализ научно-исследовательской деятельности в области гастроэнтерологии: панкреатит в реальной опасности
.PLoS One
2016
;11
(10
):e0165244
. .6Xiao
AY
,Tan
ML
,Wu
LM
и др.Глобальная заболеваемость и смертность от болезней поджелудочной железы: систематический обзор, метаанализ и мета-регрессия популяционных когортных исследований
.Ланцет Гастроэнтерол Гепатол
2016
;1
(1
):45
–55
. .7Peery
AF
,Crockett
SD
,Murphy
CC
и др.Бремя и стоимость заболеваний желудочно-кишечного тракта, печени и поджелудочной железы в США: обновление 2018 г.
.Гастроэнтерология
2019
;156
(1
):254
–272.e11
. .8Mofidi
R
,Duff
MD
,Wigmore
SJ
и др.Связь между ранней системной воспалительной реакцией, тяжестью полиорганной дисфункции и смертью при остром панкреатите
.Br J Surg
2006
;93
(6
):738
–44
. .9Бутер
A
,Имри
CW
,Картер
CR
и др.Динамический характер ранней органной дисфункции определяет исход острого панкреатита
.Br J Surg
2002
;89
(3
):298
–302
. .10Бэнкс
PA
,Bollen
TL
,Dervenis
C
и др.Классификация острого панкреатита — 2012: пересмотр классификации и определений Атланты на основе международного консенсуса
.Кишечник
2013
;62
(1
):102
–11
. .11Ядав
D
,Whitcomb
DC
.Роль алкоголя и курения при панкреатите
.Нат Рев Гастроэнтерол Гепатол
2010
;7
(3
):131
–45
. .12Wang
GJ
,Gao
CF
,Wei
D
и др.Острый панкреатит: этиология и общий патогенез
.World J Gastroenterol
2009
;15
(12
):1427
–30
. .13Zhu
Y
,Pan
X
,Zeng
H
и др. .Исследование этиологии, тяжести и смертности 3260 пациентов с острым панкреатитом в соответствии с пересмотренной классификацией Атланты в Цзянси, Китай, за 8-летний период
.Поджелудочная железа
2017
;46
:504
–9
. .14 Инь
G
,Cang
X
,Yu
G
и др. .Различные клинические проявления гиперлипидемического острого панкреатита: ретроспективное исследование
.Поджелудочная железа
2015
;44
:1105
–10
. .15Zheng
Y
,Zhou
Z
,Li
H
и др..Многоцентровое исследование этиологии острого панкреатита в Пекине в течение 5 лет
.Поджелудочная железа
2015
;44
:409
–14
. .16Huang
YX
,Jia
L
,Jiang
SM
и др. .Заболеваемость и клинические особенности гиперлипидемического острого панкреатита в Гуандуне, Китай: ретроспективное многоцентровое исследование
.Поджелудочная железа
2014
;43
:548
–52
..17Kong
H
,Ding
Z
,Zhu
XC
и др. .Изменение d-димера при остром панкреатите человека, определенное с помощью сывороточного триглицерида
.Поджелудочная железа
2011
;40
:1103
–6
. .18Chang
MC
,Su
CH
,Sun
MS
и др. .Этиология острого панкреатита – многоцентровое исследование, Тайвань
.Гепатогастроэнтерология
2003
;50
:1655
–7
.20Zhang
R
,Deng
L
,Jin
T
и др.Острый панкреатит, связанный с гипертриглицеридемией: диагностика и влияние на степень тяжести
.HPB (Оксфорд)
2019
. pii: S1365-182X (19) 30071-1. . [Epub перед печатью] .21Párniczky
A
,Kui
B
,Szentesi
A
, et al.Проспективные многоцентровые общенациональные клинические данные о 600 случаях острого панкреатита
.PLoS One
2016
;11
(10
):e0165309
. .22Ядав
D
,Lowenfels
AB
.Эпидемиология панкреатита и рака поджелудочной железы
.Гастроэнтерология
2013
;144
(6
):1252
–61
..23Moggia
E
,Koti
R
,Belgaumkar
AP
и др.Фармакологические вмешательства при остром панкреатите
.Кокрановская база данных Syst Rev
2017
;4
:CD011384
. .24Roberts
SE
,Akbari
A
,Thorne
K
и др.Заболеваемость острым панкреатитом: влияние социальной депривации, потребления алкоголя, сезонных и демографических факторов
.Алимент Фармакол Тер
2013
;38
(5
):539
–48
. .25Abu-El-Haija
M
,Gukovskaya
AS
,Andersen
DK
и др.Ускорение конвейера доставки лекарств для острого и хронического панкреатита: резюме Рабочей группы по разработке и испытанию лекарств при остром панкреатите в Национальном институте диабета, болезней органов пищеварения и почек, семинар
.Поджелудочная железа
2018
;47
(10
):1185
–92
. .26Гуковская
AS
,Pandol
SJ
,Гуковский
I
.Новые сведения о путях инициации и управления панкреатитом
.Curr Opin Gastroenterol
2016
;32
(5
):429
–35
. .27Huang
W
,Cane
MC
,Mukherjee
R
и др.Кофеин защищает от экспериментального острого панкреатита путем ингибирования высвобождения Ca 2+ , опосредованного инозитол-1,4,5-трифосфатным рецептором,
.Кишечник
2017
;66
(2
):301
–13
. .28Мукерджи
R
,Маренинова
OA
,Одинокова
IV
и др.Механизм индукции поры перехода митохондриальной проницаемости и повреждения в поджелудочной железе: ингибирование предотвращает острый панкреатит, защищая производство АТФ
.Кишечник
2016
;65
(8
):1333
–46
. .29Logsdon
CD
,Ji
B
.Роль синтеза белка и пищеварительных ферментов в повреждении ацинарных клеток
.Нат Рев Гастроэнтерол Гепатол
2013
;10
(6
):362
–70
. .30Huang
H
,Liu
Y
,Daniluk
J
и др.Активация ядерного фактора-κB в ацинарных клетках увеличивает тяжесть панкреатита у мышей
.Гастроэнтерология
2013
;144
(1
):202
–10
. .31Biczo
G
,Vegh
ET
,Shalbueva
N
и др.Дисфункция митохондрий из-за нарушения аутофагии приводит к стрессу эндоплазматического ретикулума, нарушению регуляции липидного обмена и панкреатиту в моделях на животных
.Гастроэнтерология
2018
;154
(3
):689
–703
. .32Воронина
S
,Кольер
D
,Чванов
M
и др.Роль притока Ca 2+ в образовании эндоцитарных вакуолей в ацинарных клетках поджелудочной железы
.Biochem J
2015
;465
(3
):405
–12
. .33Zhao
Q
,Wei
Y
,Pandol
SJ
и др.Передача сигналов STING способствует воспалению при экспериментальном остром панкреатите
.Гастроэнтерология
2018
;154
(6
):1822
–1835.e2
. .34Kang
R
,Zhang
Q
,Hou
W
и др.Внутриклеточный Hmgb1 подавляет высвобождение воспалительных нуклеосом и ограничивает острый панкреатит у мышей
.Гастроэнтерология
2014
;146
(4
):1097
–107
..35Liu
T
,Huang
W
,Szatmary
P
и др.Точность циркулирующих гистонов в прогнозировании стойкой органной недостаточности и смертности у пациентов с острым панкреатитом
.Br J Surg
2017
;104
(9
):1215
–25
. .36Merza
M
,Hartman
H
,Rahman
M
и др.Внеклеточные ловушки нейтрофилов вызывают активацию трипсина, воспаление и повреждение тканей у мышей с тяжелым острым панкреатитом
.Гастроэнтерология
2015
;149
(7
):1920
–1931.e8
. .37Wen
L
,Voronina
S
,Javed
MA
и др.Ингибиторы ORAI1 предотвращают связанное с цитозольным кальцием повреждение ацинарных клеток поджелудочной железы человека и острый панкреатит в 3 моделях мышей
.Гастроэнтерология
2015
;149
(2
):481
–492.e7
. .38Mole
DJ
,Webster
SP
,Uings
I
и др.Ингибирование кинуренин-3-монооксигеназы предотвращает полиорганную недостаточность на моделях острого панкреатита на грызунах
.Nat Med
2016
;22
(2
):202
–9
..39Wan
MH
,Huang
W
,Latawiec
D
и др.Обзор экспериментальных животных моделей острого билиарного панкреатита и последних достижений в фундаментальных исследованиях
.HPB (Оксфорд)
2012
;14
(2
):73
–81
. .40Murphy
JA
,Criddle
DN
,Sherwood
M
и др.Прямая активация цитозольной передачи сигналов Ca 2+ и секреции ферментов холецистокинином в ацинарных клетках поджелудочной железы человека
.Гастроэнтерология
2008
;135
(2
):632
–41
. .41Criddle
DN
,Booth
DM
,Mukherjee
R
и др.Холецистокинин-58 и холецистокинин-8 проявляют сходные действия на передачу сигналов кальция, секрецию зимогена и судьбу клеток в ацинарных клетках поджелудочной железы мышей
.Am J Physiol Gastrointest Liver Physiol
2009
;297
(6
):G1085
–92
. .42Mounzer
R
,Langmead
CJ
,Wu
BU
и др.Сравнение существующих клинических систем оценки для прогнозирования стойкой органной недостаточности у пациентов с острым панкреатитом
.Гастроэнтерология
2012
;142
(7
):1476
–82
.quiz e15-6 .43Продавцы
ZM
,MacIsaac
D
,Yu
H
и др.Общенациональные тенденции развития острого и хронического панкреатита среди детей, получающих частную страховку, и взрослых лиц пожилого возраста в США, 2007–2014 годы
.Гастроэнтерология
2018
;155
(2
):469
–478.e1
. .44Uc
A
,Andersen
DK
,Borowitz
D
и др.Ускорение поставок лекарств для лечения острого и хронического панкреатита – пробелы в знаниях и возможности для исследований: краткий обзор семинара
Национального института диабета, болезней органов пищеварения и почек.Поджелудочная железа
2018
;47
(10
):1180
–4
. .45Афганский
E
,Pandol
SJ
,Shimosegawa
T
и др.Острый панкреатит – прогресс и проблемы: отчет о международном симпозиуме
.Поджелудочная железа
2015
;44
(8
):1195
–210
. .46Вальдшнеп
J
,LaVange
LM
.Основные протоколы для изучения нескольких методов лечения, нескольких заболеваний или того и другого
.N Engl J Med
2017
;377
(1
):62
–70
. .© Автор (ы) 2019. Опубликовано Oxford University Press от имени Международной ассоциации коммуникаций.
Панкреатит – заболевания систем органов
Принципы и практика фармакотерапии, второе издание (Чизхолм-Бернс, Фармакотерапия), 2-е изд.
23 Панкреатит
Джозеф Дж. Кишель
ЦЕЛИ ОБУЧЕНИЯ
По завершении главы читатель сможет:
1. Опишите патофизиологию острого и хронического панкреатита.
2. Отличите признаки и симптомы острого панкреатита от хронического.
3. Обсудите клинические последствия скопления жидкости поджелудочной железы, абсцесса поджелудочной железы и некроза поджелудочной железы при остром панкреатите.
4. Составьте планы лечения острого панкреатита.
5. Определите фармакологические и нефармакологические средства предотвращения повторных эпизодов хронического панкреатита.
6. Выберите подходящие добавки ферментов поджелудочной железы для пациентов с хроническим панкреатитом.
КЛЮЧЕВЫЕ ПОНЯТИЯ
Наиболее частыми причинами острого и хронического панкреатита у взрослых являются злоупотребление этанолом и желчные камни.
Некроз поджелудочной железы возникает в течение первых 2 недель острого панкреатита и развивается у 10–30% пациентов с острым панкреатитом.
Терапия острого панкреатита в первую очередь является поддерживающей, если не установлена конкретная этиология. Поддерживающая терапия включает восполнение жидкости, нутритивную поддержку и обезболивание.
Лекарства, направленные на снижение высвобождения ферментов поджелудочной железы (например, соматостатин), назогастральное отсасывание и антихолинергические препараты, не помогли в лечении острого панкреатита.
Долгосрочные последствия хронического панкреатита включают нарушение всасывания в питании, нарушение толерантности к глюкозе, холангит и потенциальную зависимость от опиоидных анальгетиков.
Лечение хронического панкреатита направлено на устранение причины (злоупотребление этанолом или желчные камни), обезболивание, добавление препаратов ферментов поджелудочной железы и соблюдение диетических ограничений.
ВВЕДЕНИЕ
Поджелудочная железа – это железа в брюшной полости, лежащая в кривизне желудка, впадающая в двенадцатиперстную кишку.Поджелудочная железа функционирует в основном как экзокринная железа, хотя она также выполняет эндокринную функцию. Экзокринные клетки поджелудочной железы называются ацинарными клетками, которые производят щелочную жидкость, известную как панкреатический сок, которая содержит различные пищеварительные ферменты. Сок поджелудочной железы выделяется через ампулу Фатера в двенадцатиперстную кишку, чтобы помочь в процессе пищеварения, а также в качестве буферной кислой жидкости, выделяемой из желудка (рис. 23–1).
Эти ферменты производятся и хранятся в виде неактивных проферментов в гранулах зимогена для предотвращения автолиза и переваривания поджелудочной железы.Гранулы зимогена также отвечают за транспорт ферментов в проток поджелудочной железы. Амилаза и липаза высвобождаются из гранул зимогена в активной форме, тогда как протеолитические ферменты активируются в двенадцатиперстной кишке энтерокиназой. Энтерокиназа запускает преобразование трипсиногена в активную протеазу трипсин. Затем трипсин активирует другие проферменты до их активных ферментов. Поджелудочная железа содержит ингибитор трипсина для предотвращения автолиза.
РИСУНОК 23–1. Анатомическое строение поджелудочной железы и желчевыводящих путей. (Из Berardi RR, Montgomery PA. Pancreatitis. In: DiPiro JT, Talbert RL, Yee GC, et al., Eds. Фармакотерапия: патофизиологический подход, 7-е изд. Нью-Йорк: McGraw-Hill, 2005: 660, с разрешения. )
ОСТРЫЙ ПАНКРЕАТИТ
ЭПИДЕМИОЛОГИЯ И ЭТИОЛОГИЯ
В Западном полушарии острый панкреатит вызывается в основном употреблением / злоупотреблением этанолом и желчными камнями (желчнокаменная болезнь). Другие частые причины острого панкреатита включают гипертриглицеридемию, эндоскопическую ретроградную холангиопанкреатографию (ЭРХПГ), беременность и аутопереваривание из-за ранней активации ферментов поджелудочной железы. Множество лекарств также считаются причинами острого панкреатита (, таблица 23–1, ).
ПАТОФИЗИОЛОГИЯ
Злоупотребление этанолом может вызвать преципитацию ферментов поджелудочной железы в протоках поджелудочной железы, что приводит к хроническому воспалению и фиброзу, что приводит к потере экзокринной функции.Сам этанол может быть токсичным для клеток поджелудочной железы, усугубляя этот эффект. Камни в желчном пузыре могут блокировать ампулу Фатера, вызывая ретроградное движение ферментов поджелудочной железы или желчи в поджелудочную железу. Это ретроградное движение может быть ответственным за автолиз поджелудочной железы. 1
Таблица 23–1 Избранные лекарства, связанные с острым панкреатитом
Аутолиз поджелудочной железы может происходить, когда зимогены активируются в поджелудочной железе перед тем, как попасть в двенадцатиперстную кишку.Острый панкреатит может быть результатом начального повреждения клеток, продуцирующих зимоген, за которым следует инвазия нейтрофилов в поджелудочную железу и дальнейшая активация ферментов поджелудочной железы. Этот каскад событий разрушителен для поджелудочной железы и вреден для пациента.
Острый панкреатит может иметь несколько различных последствий. Забор жидкости поджелудочной железы (или псевдокиста поджелудочной железы) – это скопление ткани, ферментов поджелудочной железы и крови, которое образуется через несколько недель после острого панкреатита.Многие псевдокисты поджелудочной железы рассасываются спонтанно, но некоторые требуют хирургического дренирования. 2 Разрыв псевдокисты поджелудочной железы с сопутствующей эрозией и кровоизлиянием крупных кровеносных сосудов брюшной полости может привести к летальному исходу, приближающемуся к 60%; таким образом, целесообразно продолжать наблюдение за псевдокистой. 3
Некроз поджелудочной железы – диффузное воспаление поджелудочной железы инфекционной этиологии. Некроз поджелудочной железы возникает в течение первых 2 недель острого панкреатита и развивается у 10–30% пациентов с острым панкреатитом. Некротизированная поджелудочная железа может вторично инфицироваться кишечными грамотрицательными бактериями (такими как Escherichia coli), и диссеминированная инфекция может возникнуть в результате некроза поджелудочной железы. 4,5
Абсцесс поджелудочной железы – это скопление гноя, которое образуется в поджелудочной железе через 4–6 недель после острого панкреатита. Абсцесс поджелудочной железы обычно менее опасен для жизни, чем некроз поджелудочной железы или псевдокиста поджелудочной железы, и его можно лечить с помощью чрескожного дренирования. 2 Накопление жидкости поджелудочной железы и абсцессы поджелудочной железы могут образовываться во время острого панкреатита.Некроз поджелудочной железы может возникнуть, когда ферменты поджелудочной железы повреждают ткань поджелудочной железы или когда абсцессы поджелудочной железы становятся вторично инфицированными. Эта инфекция обычно вызывается бактериями, которые обычно встречаются в желудочно-кишечном тракте, включая E. coli, Enterobacteriaceae, Staphylococcus aureus, стрептококков группы viridans и анаэробы.
КЛИНИЧЕСКАЯ ПРЕЗЕНТАЦИЯ И ДИАГНОСТИКА
У пациента с острым панкреатитом может развиться множество тяжелых местных и системных осложнений.Боль и вздутие живота могут быть вызваны местными осложнениями, такими как скопление жидкости, некроз или абсцесс поджелудочной железы. Гипотония, тахикардия и лихорадка могут быть результатом системных осложнений, которые могут затронуть практически любую систему органов, но, как правило, поражают легочную и сердечно-сосудистую системы, а также почки. Полиорганная недостаточность – плохой прогностический показатель. Синдром острого респираторного дистресс-синдрома (ОРДС) – это опасный для жизни синдром острого повреждения легких с последующей гипоксией. ОРДС может быть следствием системного высвобождения ферментов поджелудочной железы, вызывающих разрушение легочного сурфактанта, который необходим для правильной функции легких. 7 Циркулирующие ферменты поджелудочной железы могут вызвать сердечно-сосудистый шок. Острая почечная недостаточность может быть следствием гиповолемии. 8
Пациенты с наибольшим риском смерти от острого панкреатита – это пациенты с полиорганной недостаточностью (например, гипотензия, дыхательная недостаточность или почечная недостаточность), некрозом поджелудочной железы, ожирением, истощением объема, старше 70 лет и с повышенной физиологией, возрастом и оценка хронического здоровья (APACHE) II. 9–10
Клиническая картина и диагностика острого панкреатита
Симптомы
• Боль в животе с иррадиацией в спину является наиболее частым симптомом.Боль может быть связана с неподвижностью кишечника или химическим перитонитом, вызванным ферментами поджелудочной железы.
• Другие общие симптомы включают тошноту, рвоту и боль в животе.
Знаки
• Могут присутствовать тахикардия, гипотензия, лихорадка и вздутие живота.
• Может быть положительный признак Каллена (голубоватое изменение цвета кожи вокруг пупка, указывающее на наличие крови в брюшине).
• Через 2–3 дня острого геморрагического панкреатита может появиться положительный симптом Тернера (локальное изменение цвета [синяк] и уплотнение кожи около пупка из-за экстравазации крови).
Лабораторные исследования
• Уровень амилазы сыворотки может быть повышен в три раза по сравнению с верхним пределом нормы в течение первых 12 часов от начала острого панкреатита. Степень возвышения не предсказывает тяжесть заболевания.
• По мере прогрессирования острого панкреатита уровень липазы и колипазы в сыворотке повышается. 6
• Другие возможные лабораторные отклонения включают повышенное количество лейкоцитов, гипергликемию, гипокальциемию, гипербилирубинемию, повышенную сывороточную лактатдегидрогеназу (ЛДГ) и гипертриглицеридемию.
ДИАГНОСТИКА
Диагноз острого панкреатита основывается на анамнезе пациента и его признаках и симптомах. Оценка лабораторных результатов, в частности липазы сыворотки, помогает в диагностике. Уровень амилазы в сыворотке повышен на ранней стадии заболевания, но может вернуться в норму в течение 12 часов. 8 Хотя повышенный уровень амилазы в сыворотке был стандартом диагностики, его полезность ограничена отсутствием специфичности. Липаза и колипаза сыворотки теперь являются золотыми стандартами для лабораторных исследований из-за специфичности более 90% для острого панкреатита.Липаза сыворотки будет оставаться повышенной в течение нескольких дней после острого события и может быть более полезной для диагностики в зависимости от того, когда пациент явится на обследование. 8,11 КТ сложнее, чем рентгенография брюшной полости или УЗИ, но это наиболее полезный инструмент для диагностики и определения стадии острого панкреатита. 12
Встреча с пациентом, часть 1
Женщина 32 лет во втором триместре беременности обратилась в отделение неотложной помощи с жалобами на резкую стойкую боль в области RUQ живота.Боль началась 3 дня назад и стала очень сильной. Дома ее тошнило, а в отделении неотложной помощи ее дважды рвало. На этом этапе беременности пациентка имеет нормальный вес. Все дородовые посещения были нормальными. Пациент не курит и не употребляет этанол, но в анамнезе болел желчнокаменной болезнью.
Какая информация о пациенте соответствует острому панкреатиту?
Какие факторы риска есть у пациента по поводу острого панкреатита?
Какие дополнительные лабораторные исследования вы бы порекомендовали?
В анамнезе пациента будут указаны факторы риска острого панкреатита, такие как возраст старше 70 лет или злоупотребление алкоголем в анамнезе.Наконец, компьютерная томография или УЗИ брюшной полости могут помочь выявить скопления жидкости поджелудочной железы. 12 Оценка APACHE II представляет собой шкалу оценки тяжести заболевания у пациентов в критическом состоянии. Индекс тяжести КТ имеет самую высокую чувствительность и специфичность в диагностике острого панкреатита.
ЛЕЧЕНИЕ
Желаемые результаты
Цели лечения острого панкреатита включают: (а) устранение тошноты, рвоты, боли в животе и лихорадки; (б) способность переносить пероральный прием; (c) нормализация сывороточной амилазы, липазы и количества лейкоцитов; и (d) разрешение абсцесса, псевдокисты или скопления жидкости, измеренное с помощью компьютерной томографии.
Нефармакологическая терапия
Многие лекарства могут спровоцировать приступ острого панкреатита. Если установлено, что лекарство является причиной острого панкреатита, его следует прекратить и рассмотреть альтернативную терапию. 13,14
Терапия острого панкреатита в первую очередь является поддерживающей, если не установлена конкретная этиология (рис. 23–2). Поддерживающая терапия включает восполнение жидкости, нутритивную поддержку и обезболивание. Пациентам с острым панкреатитом внутривенно вводят жидкости для поддержания гидратации и артериального давления.Жидкости можно давать в форме кристаллоидов (например, 0,9% хлорида натрия для инфузий) или коллоидов (например, декстрана или альбумина для инфузий). 15 0,9% натрия хлорид для инфузии (физиологический раствор) со скоростью от 50 до 100 мл / ч целесообразен для пациентов с умеренным или умеренным истощением жидкости. Однако для пациентов с тяжелой потерей жидкости может потребоваться до 200 мл / ч. 16 При необходимости к настоям могут быть добавлены электролиты, такие как калий и магний. С гипергликемией можно справиться с помощью внутривенных инфузий инсулина.
РИСУНОК 23–2. Алгоритм оценки и лечения острого панкреатита. (ЭРХПГ, эндоскопическая ретроградная холангиопанкреатография.) (От Berardi RR, Montgomery PA. Pancreatitis. In: DiPiro JT, Talbert RL, Yee GC, et al., Eds. Pharmacotherapy: A Pathophysiologic Approach, 7th ed. New York: McGraw-Hill, 2008: 664, с разрешения.)
Прекращение приема пищи внутрь во время приступа острого панкреатита является обычной практикой. Теоретически прекращение приема внутрь снизит секреторную функцию поджелудочной железы и сведет к минимуму дальнейшие осложнения заболевания.Некоторых пациентов можно кормить минимальным пероральным приемом даже при тяжелом остром панкреатите. Питание через зонд через назоеюнальный зонд будет кормить пациента за пределами ампулы Фатера, что сводит к минимуму стимуляцию поджелудочной железы. 15,16 Если пероральный прием прекращается на длительный период, необходимо использовать полное парентеральное питание для поддержания адекватного питания. 17,18
Если выявлен некроз поджелудочной железы, хирургическая обработка раны необходима, поскольку летальность приближается к 100% без дренирования или хирургического вмешательства.Чрескожный дренаж – это вариант лечения некроза поджелудочной железы, но его лучше всего использовать только у нестабильных пациентов в качестве моста к операции. Пациентам с затяжным или прогрессирующим заболеванием может потребоваться повторная операция. 2,19
Фармакологическая терапия
Анальгетики
Меперидин исторически был самым популярным анальгетиком при остром панкреатите, потому что он, как предполагается, вызывает меньше спазмов и боли в сфинктере Одди , чем другие опиоиды.Однако клиническое значение этого явления неясно. 15,20 В результате пациентам с острым панкреатитом следует назначать наиболее эффективные анальгетики. Гидроморфон и фентанил являются разумной альтернативой меперидину и могут быть более желательными из-за других побочных эффектов, связанных с меперидином. Обратитесь к главе 30, посвященной обезболиванию, для получения рекомендаций по выбору дозы обезболивающего.
Антибиотики
Эмпирические антибиотики не нужны, если у пациента легкое заболевание или острый панкреатит неинфекционной этиологии.Доказано, что антибиотики не предотвращают образование абсцесса или некроза поджелудочной железы при раннем применении в течение острого панкреатита.
Антибиотики могут быть подходящими при некрозе поджелудочной железы, который может быть инфицирован изначально или быть восприимчивым к вторичной инфекции; однако опубликованные данные дают противоречивые результаты относительно смертности и уровня инфицирования в этих условиях. 16,21,22 Таким образом, решение об использовании антибиотиков очень индивидуально. Избранные схемы внутривенного введения антибиотиков показаны в таблице 23–2 . Если некроз подтвержден, антибиотиков в качестве единственной терапии недостаточно; хирургическая обработка раны необходима для излечения.
Подходят антибиотики широкого спектра действия против кишечных грамотрицательных бактерий. Часто бывает трудно сузить спектр активности выбранного антибиотика, поскольку инфекции обычно являются полимикробными. Таким образом, пациенты могут получать длительные курсы антибиотиков широкого спектра действия, таких как меропенем, и могут развиваться суперинфекции из-за более устойчивых бактерий или бактерий, не чувствительных к меропенему.Противогрибковые средства, такие как флуконазол, могут быть рассмотрены, если перитонит или перфорация желудочно-кишечного тракта развиваются из-за присутствия грибов, таких как Candida alicans , в желудочно-кишечном тракте. 23
Встреча с пациентом, часть 2: история болезни, физический осмотр и диагностические тесты
PMH: Gravida 2, пункт 1; холелитиаз
Аллергии: Аллергии неизвестны
ФХ: Отец и мать живы и здоровы
SH: В настоящее время нет этанола, но есть один-два напитка за ночь до беременности; без табака
Meds: Лекарства, отпускаемые по рецепту, не отпускаются; поливитамины по одной таблетке перорально один раз в день; сульфат железа 324 мг перорально один раз в день; карбонат кальция 500 мг перорально два раза в день
PE:
VS: Вес 80 кг (176 фунтов), высота 5’5 дюймов (165 см), АД 110/60 мм рт. Ст., Стр. 120 ударов в минуту, RR 18 в минуту, T 37.9 ° С (100,2 ° F)
CV: Регулярная частота и ритм, шумов нет
Abd: Беременная, (+) болезненность при отскоке, (+) шумы кишечника, гепатоспленомегалии нет
Лаборатории: Амилаза 50 единиц / л (0,83 мкКат / л), липаза 1000 единиц / л (16,7 мкКат / л)
УЗИ брюшной полости: Ожидаемые результаты
Учитывая эту дополнительную информацию, как вы оцениваете состояние пациента?
Почему амилаза низкая, а липаза высокая?
Таблица 23–2 Избранные схемы внутривенных антимикробных препаратов при некрозе поджелудочной железы
Неэффективные методы лечения
Доказано, что несколько фармакологических методов лечения неэффективны в снижении заболеваемости или смертности от этого заболевания.Неэффективные методы лечения включают: снижение секреции поджелудочной железы путем введения соматостатина или атропина, снижение кислотности желудочного сока и уменьшение секреции поджелудочной железы с помощью антагонистов рецепторов гистамина 2 , ингибирование ферментов поджелудочной железы с использованием ингибиторов протеазы и иммуномодуляция. 11–24,27 Назогастральное отсасывание было эффективным только у пациентов с кишечной непроходимостью или постоянной рвотой. 28
Встреча с пациентом, часть 3: лечение и мониторинг
У пациента острая декомпенсация после выхода из КТ-сканера, поэтому его переводят в хирургическое отделение интенсивной терапии для искусственной вентиляции легких, поддержки артериального давления и хирургического обследования. Поставлен диагноз: острый панкреатит с некрозом поджелудочной железы.
Составьте план ухода за этим пациентом.
Каковы возможные причины дыхательной недостаточности и гипотонии у этого пациента? Являются ли эти данные плохими прогностическими показателями?
Какое лечение рекомендуется при некрозе поджелудочной железы?
Какая эмпирическая схема приема антибиотиков была бы разумным выбором для этого пациента? Укажите препарат, дозу, способ приема и частоту.
Предположим, хирург запросил у этого пациента 600 мг клиндамицина внутривенно каждые 8 часов. Будет ли это разумным выбором? Почему или почему нет?
ОЦЕНКА РЕЗУЛЬТАТОВ
Учитывая тяжесть острого панкреатита, пациенты находятся под тщательным наблюдением в отделениях интенсивной терапии. Пациентам с легкой формой заболевания можно вести более консервативное лечение при наблюдении и поддерживающей терапии. Пациентам в критическом состоянии может потребоваться операция и агрессивные меры жизнеобеспечения. 16,29
ХРОНИЧЕСКИЙ ПАНКРЕАТИТ
ЭПИДЕМИОЛОГИЯ И ЭТИОЛОГИЯ
Заболеваемость хроническим панкреатитом составляет примерно 1 из 10 000 человек. Наиболее частой причиной хронического панкреатита у взрослых в западных странах является злоупотребление этанолом. Наиболее частой причиной у детей является муковисцидоз из-за ранее существовавшей недостаточности поджелудочной железы, присущей этому заболеванию. Камни в желчном пузыре могут возникать одновременно с хроническим панкреатитом, но не часто являются причиной.В отличие от острого панкреатита, хронический панкреатит в значительном количестве случаев (30%) имеет неизвестную этиологию. 29,30
ПАТОФИЗИОЛОГИЯ
Хронический панкреатит – воспалительный процесс, протекающий в течение длительного периода времени. Воспаление повреждает производящие ферменты клетки поджелудочной железы, а также может нарушить или разрушить эндокринную функцию поджелудочной железы, вызывая диффузное рубцевание и фиброз. 30,31 Злоупотребление этанолом может вызвать преципитацию ферментов поджелудочной железы в протоках поджелудочной железы, что приводит к хроническому воспалению и повреждению.Этанол также может быть токсичным для клеток поджелудочной железы. 32 Как ни странно, количество потребляемого этанола не коррелирует с частотой или прогрессированием хронического панкреатита. 33 Пациент, который «выпивает» из-за употребления большого количества этанола в течение коротких периодов времени, имеет такую же вероятность развития хронического панкреатита, как и тот, кто хронически употребляет социально приемлемые количества алкоголя. Пациенты, которые умирают от первого диагностированного эпизода хронического панкреатита, в течение некоторого времени могут иметь недиагностированный хронический панкреатит. 34
Долгосрочные последствия хронического панкреатита включают нарушение всасывания в питании, нарушение толерантности к глюкозе, холангит и потенциальную зависимость от опиоидных анальгетиков. По мере того, как пациенты теряют внешнесекреторную функцию поджелудочной железы, у них снижается способность абсорбировать липиды и белок, поступающие при нормальном потреблении с пищей. Похудание из-за нарушения всасывания, связанного с питанием, является частым симптомом хронического панкреатита, который не часто наблюдается при остром панкреатите. Стул, содержащий жир или белок, также является обычным явлением; всасывание углеводов обычно не изменяется.Несмотря на то, что у пациентов с хроническим панкреатитом снижена способность абсорбировать липиды из желудочно-кишечного тракта, у этих пациентов не наблюдается повышенного риска дефицита жирорастворимых витаминов. 36
КЛИНИЧЕСКАЯ ПРЕЗЕНТАЦИЯ И ДИАГНОСТИКА
Отличить эпизод острого панкреатита от хронического может быть сложно, поскольку клинические проявления могут быть схожими. Диагноз хронического панкреатита ставится на основании изучения последствий хронического воспаления поджелудочной железы и рубцевания поджелудочной железы и пациента в целом.КТ или ЭРХПГ позволят визуализировать хронические кальцинированные поражения поджелудочной железы, если они есть. 39
ЛЕЧЕНИЕ
Желаемые результаты
Целями фармакотерапии хронического панкреатита являются: (а) профилактика и разрешение хронической боли в животе и (б) коррекция диетической мальабсорбции с помощью экзогенных ферментов поджелудочной железы.
Нефармакологическая терапия
Изменение образа жизни – важная часть терапии хронического панкреатита.Пациенты, которые полностью избегают этанола после приступа панкреатита, вызванного этанолом, имеют значительно меньшую вероятность рецидива, чем пациенты, принимающие даже незначительное количество этанола. Избегание этанола и жирной пищи может уменьшить боль при хроническом панкреатите.
Клиническая картина и диагностика хронического панкреатита
Общие
• Хронический панкреатит может быть похож на острый панкреатит.
Симптомы
• Боль – самая частая основная жалоба. Боль может быть тупой или острой, локализоваться в области живота или распространяться в спину. Боль не снимается антацидами и может быть спровоцирована приемом этанола или жирной пищи. 35
• Потеря веса может быть результатом хронической мальабсорбции жиров и белков.
Знаки
• Пациенты часто обращаются с хронической диареей, содержащей жир, из-за нарушения всасывания липидов с пищей.
• Желудочно-кишечное кровотечение может быть результатом эрозии кишечных кровеносных сосудов ферментами поджелудочной железы или в результате тромбоза.
• Хроническая обструкция общего желчного протока воспаленной поджелудочной железой может вызвать желтуху, холангит и билиарный цирроз. 37
Лабораторные исследования
• Непереносимость глюкозы может возникнуть из-за хронического нарушения эндокринной функции поджелудочной железы. 38
• При хроническом панкреатите уровни амилазы и липазы в сыворотке крови обычно не повышаются.
• Уровень сывороточного билирубина или щелочной фосфатазы может быть повышен из-за воспаления около общего желчного протока.
Многие хирургические процедуры использовались для уменьшения воспаления или удаления стриктур, вызывающих боль при хроническом панкреатите. Однако эффективность большинства процедур, включая блокаду нервов, не доказана в клинических испытаниях, и они сопряжены с высоким риском заболеваемости и смертности. 40
Фармакологическая терапия
Анальгетики
Обезболивание – важный компонент терапии, аналогичный лечению острого панкреатита. Неопиоидные анальгетики (например, трамадол) предпочтительны, но сильный и стойкий характер боли часто требует опиоидной терапии. Пациентам могут потребоваться постоянные дозы опиоидных анальгетиков, что влечет за собой риск привыкания. Боль также можно контролировать, удалив стимул обострения, если он выявлен. 32,41
Ферменты поджелудочной железы
Цель добавления ферментов поджелудочной железы – доставить экзогенный фермент в двенадцатиперстную кишку, не вызывая дальнейших побочных эффектов со стороны желудочно-кишечного тракта от лекарства, рискуя несоблюдением режима лечения из-за большого количества требуемых дозированных единиц или вызывая чрезмерные расходы на лекарства. 42
Добавление ферментов поджелудочной железы может уменьшить боль и жирную диарею, связанные с хроническим панкреатитом ( Таблица 23–3 ). Наилучшие результаты достигаются у пациентов с легкой формой неалкогольной болезни поджелудочной железы. Обычные добавки ферментов поджелудочной железы содержат липазу, амилазу и протеазу в различных пропорциях. Таким образом, доза может быть адаптирована к потребностям пациента в добавлении экзогенных ферментов и ответу на терапию.
Добавки ферментов поджелудочной железы без кишечного покрытия требуют высоких доз, чтобы компенсировать потерю фермента из-за разрушения из-за низкого pH желудка.Этот эффект можно свести к минимуму путем введения антагониста гистаминовых рецепторов 2 или ингибитора протонной помпы (ИПП). Добавки ферментов поджелудочной железы, не покрытые кишечным покрытием, могут иметь преимущество в уменьшении боли на ранних стадиях заболевания за счет регуляции протеаз в двенадцатиперстной кишке.
Таблица 23–3 Часто используемые препараты ферментов поджелудочной железы
Добавки ферментов поджелудочной железы без кишечного покрытия могут использоваться для начальной терапии.Относительная доза амилазы, липазы и протеазы может быть увеличена до тех пор, пока не будет достигнут контроль боли и жирной диареи или пока пациент не испытает непереносимые побочные эффекты. Если достигается контроль над болью и диареей, пациента можно перевести на добавку с энтеросолюбильным покрытием для максимального соблюдения режима лечения. Разумным примером начального режима является Viokase-8, шесть таблеток с каждым приемом пищи и перед сном, с фамотидином 20 мг перед сном.
Встреча с пациентом 2
Этой же пациентке, описанной при первом обращении, сейчас 34 года (она родила здорового мальчика без осложнений).Она обратилась в клинику с болью в области RUQ, которая иррадирует в спину. У нее также желтуха и тошнота.
PMH: Беременная 2 пара 2, холелитиаз
SH: Употребляет от одного до двух алкогольных напитков за вечер; без табака
Meds: Мультивитамины по одной таблетке в день; пантопразол 40 мг перорально один раз в сутки; маалокс 15 мл перорально четыре раза в день по мере необходимости при изжоге / расстройстве желудка; ацетаминофен 325 мг перорально каждые 6 часов по мере необходимости при боли / головной боли
ROS: Положительный результат при острой боли в животе RUQ с иррадиацией в спину, тошноте и недавней непреднамеренной потере веса; отрицательный на боль в груди или одышку, жирная диарея, присутствует в течение месяцев
PE:
VS: BP 130/86 мм рт. Ст., P 80 ударов в минуту, RR 16 в минуту, T 37.0 ° C (98,6 ° F), вес 80 кг (176 фунтов), высота 5’5 дюймов (165 см).
CV: Регулярная частота и ритм, шумов нет
Abd: Вздутие, (+) болезненность при отскоке, (+) звуки кишечника, выраженная гепатоспленомегалия
Лаборатории: Амилаза 100 единиц / л (1,67 мкКат / л), липаза 100 единиц / л (1,67 мкКат / л)
Компьютерная томография: Диффузное рубцевание и кальцификации поджелудочной железы
Составьте план ухода за этим пациентом.
Почему сывороточные амилаза и липаза в норме?
Какие изменения в образе жизни пациентка может сделать, чтобы свести к минимуму влияние ее болезненного состояния?
Принимает ли этот пациент какие-либо лекарства, которые могут обострить панкреатит? Если да, то какие альтернативы вы можете предложить?
Какие лекарства могут помочь облегчить жирную диарею, которую испытывает пациент?
Как бы вы контролировали эффективность своих рекомендаций?
Большинство добавок ферментов поджелудочной железы имеют энтеросолюбильное покрытие для высвобождения ферментов в щелочной среде кишечника; это сводит к минимуму разрушение ферментов в желудке.Добавки ферментов поджелудочной железы с энтеросолюбильным покрытием требуют меньшего количества суточных доз, но доставка лекарства к месту действия и эффективность могут быть отложены из-за времени опорожнения желудка. 43
Добавки ферментов поджелудочной железы следует принимать непосредственно перед едой, чтобы способствовать перевариванию и усвоению пищи. В качестве альтернативы пациенты могут дополнять свой рацион триглицеридами со средней длиной цепи (MCT) или употреблять в пищу продукты, богатые MCT, поскольку им не требуются ферменты поджелудочной железы для абсорбции.Подходящий режим включает успешные дозы каждого фермента (амилазы, липазы и протеазы) из начального режима лечения без кишечного покрытия. Как и в предыдущем примере, пациент, стабилизированный на Viokase-8, шесть таблеток с каждым приемом пищи, может быть переведен на три таблетки Pancrease MT-16 во время еды. После этого прием фамотидина можно прекратить.
ОЦЕНКА РЕЗУЛЬТАТОВ
• Следите за адекватным обезболиванием и необходимостью усиления или деэскалации анальгезии.
Уход за пациентами и наблюдение
1. Определите, является ли этанол способствующим причинным фактором. Если да, усилите консультирование о необходимости воздержания и предоставьте соответствующие ресурсы для поддержания воздержания (например, профессиональные консультации, анонимные алкоголики).
2. Получите подробную историю приема рецептурных, безрецептурных и диетических добавок, чтобы определить продукты, которые могут обострить хронический панкреатит.
3. Направьте пациента на консультацию по питанию, если наблюдается снижение потребления калорий и потеря веса.Сравните фактическую массу тела с идеальной массой тела.
4. Составьте план обезболивания вместе со службой обезболивания, если это возможно, чтобы контролировать и предотвращать боль. Рекомендовать анальгетик с простотой дозирования и минимальными побочными эффектами, учитывая, что пациентам с хроническим панкреатитом могут потребоваться большие дозы опиоидов.
5. Оптимизируйте добавление ферментов поджелудочной железы, начав сначала с добавок ферментов, не покрытых кишечной оболочкой, и антагониста гистаминовых рецепторов 2 .Когда боль и диарея стабилизируются, рассмотрите возможность перехода на ферментную добавку с энтеросолюбильным покрытием для облегчения дозирования.
6. Разработайте план переоценки добавок ферментов поджелудочной железы и обезболивания в амбулаторных условиях.
7. Оцените улучшение качества жизни по таким показателям, как физическое, психологическое и социальное функционирование и благополучие.
• Если облегчение боли достигается за счет отказа от этанола или жирной пищи, поощряйте продолжение этих практик.
• При нарушении всасывания с пищей следует контролировать пациентов на предмет увеличения или уменьшения веса, уровня активности и способности выполнять повседневную деятельность.
• Попросите пациентов контролировать частоту и постоянство стула как показатель мальабсорбции.
• Объясните пациентам, что соблюдение и правильное использование пищевых добавок с ферментами поджелудочной железы является ключом к улучшению результатов. 32,35,41 ~ 43
Сокращения, используемые в этой группе
Вопросы и ответы для самооценки доступны по адресу http://www.mhpharmacotherapy.com/pp.html.
ССЫЛКИ
1. Рос Э, Наварро С., Брю С. и др. Скрытый микролитиаз при «идиопатическом» остром панкреатите: профилактика рецидивов с помощью холецистэктомии или терапии урсодезоксихолевой кислотой. Гастроэнтерология 1991; 101: 1701-1709.
2. Брэдли Е.Л., III. Клинически обоснованная система классификации острого панкреатита. Резюме Международного симпозиума по острому панкреатиту, Атланта, Джорджия, 11-13 сентября 1992 г. Arch Surg 1993; 128: 586-590.
3. Balthazar EJ. Стадия острого панкреатита. Радиол Клин Норт Ам 2002; 40: 1199-1209.
4. Perez A., Whang EE, Brooks DC, et al. Увеличивается ли тяжесть некротического панкреатита при обширном некрозе и инфицированном некрозе? Поджелудочная железа 2002; 25: 229-233.
5. Ланкиш П.Г., Пфлихтофер Д., Лехник Д. Острый панкреатит: какой пациент наиболее подвержен риску? Поджелудочная железа 1999; 19: 321-324.
6. Казмерчак С. Биохимические показатели острого панкреатита. В: Lott J, ed.Клиническая патология заболеваний поджелудочной железы. Тотова, Нью-Джерси: Humana Press, 1997: 75.
7. Изенманн Р., Рау Б., Бегер Х.Г. Ранний тяжелый острый панкреатит: характеристики новой подгруппы. Поджелудочная железа 2001; 22: 274-278.
8. Cappell MS. Острый панкреатит: этиология, клиника, диагностика и терапия. Med Clin North Am 2008; 92: 889-923.
9. Теннер С., Сика Дж., Хьюз М. и др. Связь некроза с органной недостаточностью при тяжелом остром панкреатите. Гастроэнтерология 1997; 113: 899-903.
10. Дервенис С., Джонсон С.Д., Басси С. и др. Диагностика, объективная оценка степени тяжести и лечение острого панкреатита. Консенсусная конференция Санторини. Int J Pancreatol 1999; 25: 195-210.
11. Marshall JB. Острый панкреатит. Обзор с акцентом на новые разработки. Arch Intern Med 1993; 153: 1185-1198.
12. Гурлейк Г., Эмир С., Киликоглу Г. и др. Индекс тяжести компьютерной томографии, оценка APACHE II, концентрация СРБ в сыворотке для прогнозирования тяжести острого панкреатита.JOP 2005; 6: 562-567.
13. Бадалов Н., Барадарян Р., Исвара К. и др. Острый панкреатит, вызванный лекарственными средствами: обзор, основанный на фактах. Clin Gastroenterol Hepatol 2007; 5: 648-661.
14. Пеззилли Р., Билли П., Меландри Р. и др. Хронический панкреатит, вызванный противосудорожными препаратами. Отчет о болезни. Итал Дж. Гастроэнтерол 1992; 24: 245-246.
15. Mayerle J, Simon P, Lerch MM. Медикаментозное лечение острого панкреатита. Gastroenterol Clin North Am 2004; 33: 855-869.
16. Бэнкс PA, Freeman ML.Практическое руководство при остром панкреатите. Am J Gastroenterol 2006; 101: 2379-2400.
17. Петров М.С., Коррейя М.И., Виндзор Я. Питание через назогастральный зонд при прогнозе тяжелого острого панкреатита. Систематический обзор литературы для определения безопасности и переносимости. СП 2008; 9: 440-448.
18. Иоаннидис О., Лаврентьева А., Ботсиос Д. Нутриционная поддержка при остром панкреатите. JOP 2008; 9: 375-390.
19. Брэдли Е.Л., III, Аллен К. Проспективное продольное исследование наблюдения и хирургического вмешательства при лечении некротического панкреатита.Am J Surg 1991; 161: 19-24; обсуждение 24-25.
20. Томпсон ДР. Наркотические анальгетические эффекты на сфинктер Одди: обзор данных и терапевтического значения при лечении панкреатита. Am J Gastroenterol 2001; 96: 1266-1272.
21. Ю Б, Гао Дж, Цзоу Д. и др. Профилактические антибиотики не могут снизить инфицированный панкреонекроз и смертность при остром некротическом панкреатите: данные метаанализа рандомизированных контролируемых исследований. Am J Gastroenterol 2008; 103: 104-110.
22. Sainio V, Kemppainen E, Puolakkainen P, et al. Раннее лечение антибиотиками при остром некротизирующем панкреатите. Ланцет 1995; 346: 663-667.
23. Bassi C, Larvin M, Villatoro E. Антибактериальная терапия для профилактики инфекции панкреонекроза при остром панкреатите. Кокрановская база данных Syst Rev 2003 (4): CD002941.
24. Pezzilli R. Gabexate mesilate при остром панкреатите: Ни чудо, ни мираж, просто поиск оптимальной дозировки. Дайджест Liver Dis 2001; 33: 502.
25. Педерзоли П., Басси С., Фалькони М. и др. Габексат мезилат в лечении острого панкреатита. Annali Italiani di Chirurgia 1995; 66: 191-195.
26. Norman JG. Новые подходы к острому панкреатиту: роль медиаторов воспаления. Пищеварение 1999; 60 (Приложение 1): 57-60.
27. Бесселинк М.Г., ван Сантвоорт Х.С., Бускенс Э. и др. Голландская группа по изучению острого панкреатита. Пробиотическая профилактика при прогнозируемом тяжелом остром панкреатите: рандомизированное двойное слепое плацебо-контролируемое исследование.Ланцет 2008; 37: 651-659.
28. Levant JA, Secrist DM, Resin H, et al. Назогастральный отсос в лечении алкогольного панкреатита. Контролируемое исследование. JAMA 1974; 229: 51-52.
29. Натенс А.Б., Кертис Дж. Р., Бил Р. Дж. И др. Ведение тяжелобольного пациента с тяжелым острым панкреатитом. Crit Care Med 2004; 32: 2524-2536.
30. Сарлес Х., Бернард Дж. П., Джонсон С. Патогенез и эпидемиология хронического панкреатита. Анну Рев Мед 1989; 40: 453-468.
31.Сарлес Х., Адлер Г., Дани Р. и др. Классификация панкреатита Марсель-Рим 1988. Scand J Gastroenterol 1989; 24: 641-642.
32. Стир М.Л., Ваксман И., Фридман С. Хронический панкреатит. N Engl J Med 1995; 332: 1482-1490.
33. Пелли Х., Лаппалайнен-Лехто Р., Пийронен А. и др. Факторы риска рецидивирующего острого алкогольного панкреатита: проспективный анализ. Scand J Gastroenterol 2008; 43: 614-621.
34. Lowenfels AB, Maisonneuve P, Cavallini G, et al. Прогноз хронического панкреатита: международное многоцентровое исследование.Международная группа по изучению панкреатита. Am J Gastroenterol 1994; 89: 1467-1471.
35. Bornman PC, Marks IN, Girdwood AW, et al. Патогенез боли при хроническом панкреатите: загадка. World J Surg 2003; 27: 1175-1182.
36. Beglinger C. Актуальные аспекты физиологии хронического панкреатита. Дайджест Диск 1992; 10: 326-329.
37. Ammann RW, Akovbiantz A, Largiader F, Schueler G. Течение и исход хронического панкреатита. Продольное исследование смешанной медико-хирургической серии 245 пациентов.Гастроэнтерология 1984; 86 (5 баллов): 820-828.
38. Малка Д., Хаммель П., Сованет А. и др. Факторы риска сахарного диабета при хроническом панкреатите. Гастроэнтерология 2000; 119: 1324-1332.
39. Этемад Б., Уиткомб, округ Колумбия. Хронический панкреатит: диагностика, классификация и новые генетические разработки. Гастроэнтерология 2001; 120: 682-707.
40. Уоршоу А.Л., Бэнкс П.А., Фернандес-Дель Кастильо С. Технический обзор AGA: Лечение боли при хроническом панкреатите. Гастроэнтерология 1998; 115: 765-776.
41. Ammann RW, Muellhaupt B. Естественная история боли при алкогольном хроническом панкреатите. Гастроэнтерология 1999; 116: 1132-1140.
42. Браун А., Хьюз М., Теннер С., Бэнкс, Пенсильвания. Уменьшает ли прием ферментов поджелудочной железы боль у пациентов с хроническим панкреатитом: метаанализ. Am J Gastroenterol 1997; 92: 2032-2035.
43. Layer P, Keller J. Панкреатические ферменты: секреция и переваривание питательных веществ в просвете при здоровье и болезни. Дж. Клин Гастроэнтерол 1999; 28: 3-10.
.
 Действие понятно – устранить боль. Результативными считаются но-шпа или папаверин.
Действие понятно – устранить боль. Результативными считаются но-шпа или папаверин.
 Наиболее популярными средствами, применяющимися в терапии заболевания, являются «Панкреатин», «Креон» и «Панцитрат».
Наиболее популярными средствами, применяющимися в терапии заболевания, являются «Панкреатин», «Креон» и «Панцитрат». Используют их не так часто, поскольку они способны провоцировать побочные реакции. При возникновении такой потребности назначают «Ранитидин» и «Фамотидин».
Используют их не так часто, поскольку они способны провоцировать побочные реакции. При возникновении такой потребности назначают «Ранитидин» и «Фамотидин». Лучшими средствами в терапии таких состояний признаны «Но-шпа» и «Папаверин» в сочетании с «Платифиллином».
Лучшими средствами в терапии таких состояний признаны «Но-шпа» и «Папаверин» в сочетании с «Платифиллином».


 Применяется 1 раз в сутки.
Применяется 1 раз в сутки.