Что можно кушать при панкреатите обострение: меню на неделю, что можно и нельзя есть, отзывы диетологов
Что можно есть при обострении поджелудочной железы? (Часть 2) | Нетгастриту
Что можно есть при панкреатите?
При появлении дискомфорта в животе, в области желудка нужно сразу отказаться от тех продуктов, которые противопоказаны при панкреатите – это все жирные продукты, кислые, соленые, острые, газированные напитки и консервы. В диете таких продуктов просто нет.
Пища диеты при панкреатите должна быть разнообразной и содержать все полезные вещества:
- Белок – до 90 грамм ежедневно;
- Углеводы – до 75 грамм;
- Жиры – до 40 грамм, желательно растительного происхождения.
В рацион питания при панкреатите должны входить все полезные микроэлементы: калий, кальций, фосфор, магний, железо, весь впектр витаминов и пр. Диете должна помогать организму повышать иммунитет и бороться с патологиями внутри железы.
Рацион при панкреатите должен быть полноценным, но все продукты готовятся только путем варки, тушением, на пару, запеканием.Никакой жареной пищи в питании и диете быть не должно.
Поджелудочная железа у взрослых
Причин возникновения воспаления поджелудочной железы у взрослых – огромное множество.
Основными являются:
- Неправильное питание;
- Переедание;
- Употребление алкоголя;
- Наличие иных заболеваний желудочно-кишечного тракта;
- Инфекционные болезни;
- Малоподвижный образ жизни;
- Пониженный иммунитет;
- Сбои в работе гормональной и эндокринной систем и пр.
В соответствии с основной причиной возникновения панкреатита медики различают виды болезни:
- Алкогольный – основная причина алкоголь;
- Лекарственный – хаотичный или длительный прием лекарств;
- Билиарный – возникает как следствие желчекаменной болезни;
- Кальцинированный – избыток соли в организме и пр.
Все заболевания поджелудочной железы объединены в общую группу – панкреопатию.
При любом виде панкреопатии назначают диету при помощи тестов и другим методов дифференциальной диагностики – лабораторной (анализы) и инструментальной (УЗИ, рентген, лапароскопия, эндоскопия и пр.). Особенно диета становится строгой при обострении болезни.
Что кушать, когда обострение?
В период обострения заболевания врач назначает голод на 2-3 суток. эта диета называется стол № 0. В это время пациент может пить только щелочную негазированную воду – до 2 литров в день.
Если стадия панкреатита тяжелая, то проводится экстренная операция по удалению части или всей железы, камней из желчных путей и пр. До и после операции пациент также не должен ничего есть и придерживать диеты стола № 0. Все полезные микроэлементы, необходимые организму пациента, врач назначает путем внутривенных капельниц или инъекций.
Если даже оперативное вмешательство не показано, все равно голод – это тот период, когда доктор купирует боль и дает железе отдохнуть от пищеварительных процессов. Поэтому при хронической форме панкреатита, при обострениях, так или иначе, придется поглодать.
Меню
Затем после купирования боли и голода при панкреатите пациенту разрешают пить отвары шиповника, ромашки и других трав, имеющий противовоспалительное, антисептической, антимикробное действие. Спустя 2-3 дня рацион диеты расширяется вегетарианскими бульонами, чуть позже в диете появляются пюре, мясные или рыбные нежирные бульоны.
Спустя 2-3 дня рацион диеты расширяется вегетарианскими бульонами, чуть позже в диете появляются пюре, мясные или рыбные нежирные бульоны.
При положительной динамике выздоровления рацион расширяется и пациенту назначается диета – стол № 5, которая состоит из каш, овощных пюре, нежирных бульонов, приготовленной на пару рыбе или диетическом мясе, фруктов и овощей.
Условия приема пищи при диете должны соответствовать критериям:
- Пища должна быть размельченной;
- Подаваться при температуре 37 градусов;
- За один раз пациент может употребить не более 200 грамм продуктов;
- В течение дня можно есть 5-6 раз без перекусов и запиваний.
Даже размельченную пищу при панкреатите пациент должен тщательно прожевывать. Соблюдая все правила диетического питания при панкреатите, пациент максимально поможет своей поджелудочной железе восстановиться и начать нормально функционировать.
Конечно, при самой тяжелой некрозной стадии, когда единственным эффективным методом лечения является операция по удалению железы, пациент садится на строгую диету пожизненно.
Во время лечебного процесса диета – основное условие эффективного лечения. Без соблюдения диеты никакие медикаменты не помогут восстановиться этому важному органу.
Как питаться после прохождения основного курса лечения панкреатита, вам расскажет ваш лечащий врач. Но, как правило, схема и рацион питания при диете остаются неизменными, даже когда панкреатит отступает.
Ведь спровоцировать новый приступ и обострение панкреатита легко – достаточно один раз позволить себе, к примеру, жареную или жирную пищу. Тогда диета становится неэффективной, и панкреатит возвращается новым приступом и обострением.
Вся информация предоставлена сайтом http://NetGastritu.com
С уважением.
Основы диеты при панкреатите – МК
+ A –
Если панкреатит имеет хроническое течение, тогда периоды активации процесса сменяются периодами затухания, когда изменения внутри железы минимальны
Панкреатит – это воспалительный процесс в зоне тканей поджелудочной железы, одного из важнейших органов пищеварения.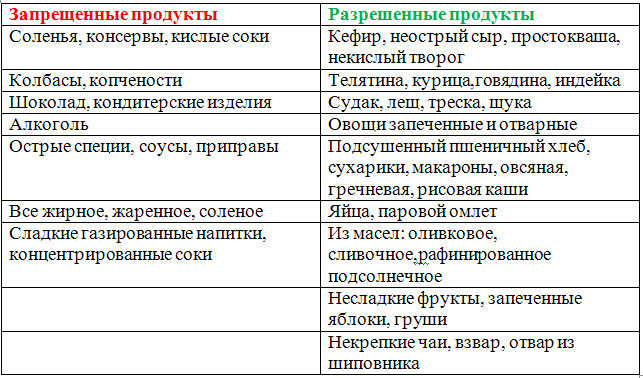 При остром процессе резко нарушается состояние, пациент чувствует себя крайне плохо и воспаление грозит серьезными осложнениями, вплоть до летальных исходов. Однако, стоит помнить, что малейшие патогенные влияния способны привести к обострению процесса, что требует госпитализации и активного лечения. С целью предотвращения обострений или снижения их частоты применяется особая диета при панкреатите.
При остром процессе резко нарушается состояние, пациент чувствует себя крайне плохо и воспаление грозит серьезными осложнениями, вплоть до летальных исходов. Однако, стоит помнить, что малейшие патогенные влияния способны привести к обострению процесса, что требует госпитализации и активного лечения. С целью предотвращения обострений или снижения их частоты применяется особая диета при панкреатите.
Хронический панкреатит
Обычно хронический процесс формируется после острых воспалений, если лечение было проведено не в полном объеме, и по мере улучшения состояния пациент перестал выполнять все предписания врача. Это не самая благоприятная ситуация, так как наличие постоянного очага вяло текущего воспаления грозит и нарушением функций органа, и его дистрофическими изменениями, а также при провоцирующих факторах – снова и снова будут обострения. Кроме того, хронический панкреатит может формироваться вторично, на фоне имеющихся различных пищеварительных проблем – патологий желудка и тонкой кишки, глистных инвазий, камнеобразования в желчном пузыре.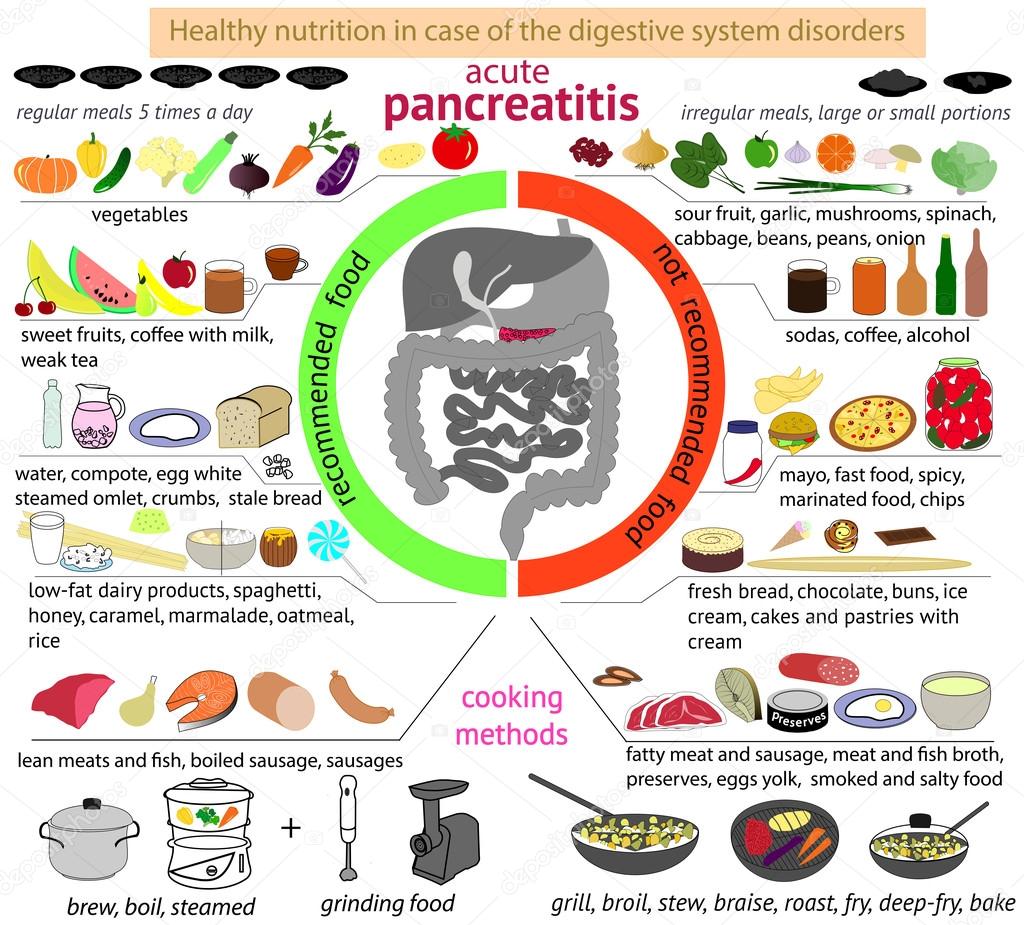 Наличие проблем с работой поджелудочной железы осложняет течение этих патологий и требует более основательного и длительного лечения. Немалую роль в терапии будут играть и диетические рекомендации, соблюдение которых может существенно помочь в снятии воспалительного процесса, нормализации обменных процессов и улучшении общего состояния.Диета при панкреатите
Наличие проблем с работой поджелудочной железы осложняет течение этих патологий и требует более основательного и длительного лечения. Немалую роль в терапии будут играть и диетические рекомендации, соблюдение которых может существенно помочь в снятии воспалительного процесса, нормализации обменных процессов и улучшении общего состояния.Диета при панкреатите
Естественно, что только одна диета при панкреатите не сможет полностью вылечить пациента, но она может существенно снизить риски обострения и разгрузит пищеварение, дав ему возможность работать с меньшим напряжением. Соблюдение принципов питания поможет существенно снизить частоту обострений, снижает риск осложнений и улучшает процессы переваривания пищи и усвоение питательных веществ.
Для лечения панкреатитов существует особая диета, стол №5. Ее стоит придерживаться на протяжении длительного времени, в идеале – всю жизнь при наличии хронического панкреатита, при котором функции железы полностью уже не восстанавливаются. В зависимости от того, обострение это процесса или стадия его ремиссии, имеются особенности питания. Если это острое воспаление (на фоне провоцирующих факторов), показано голодание на протяжении нескольких суток, что разгрузит железу и даст ей отдых. По мере того, как постепенно сходит отек железы, и она может хотя бы частично выполнять свои функции, расширяют диету до щелочных напитков, не раздражающих ткани железы и протертой парой и отварной пищи. Это могут быть овсяный отвар, кисель или желе, подсушенный в сухарики хлеб, пюре из картофеля на воде и без масла, протертые овощные супы и каши, галетное печенье.Что стоит исключать в обострение
В зависимости от того, обострение это процесса или стадия его ремиссии, имеются особенности питания. Если это острое воспаление (на фоне провоцирующих факторов), показано голодание на протяжении нескольких суток, что разгрузит железу и даст ей отдых. По мере того, как постепенно сходит отек железы, и она может хотя бы частично выполнять свои функции, расширяют диету до щелочных напитков, не раздражающих ткани железы и протертой парой и отварной пищи. Это могут быть овсяный отвар, кисель или желе, подсушенный в сухарики хлеб, пюре из картофеля на воде и без масла, протертые овощные супы и каши, галетное печенье.Что стоит исключать в обострение
При обострении панкреатита, особенно в первое время, в питании категорически запрещены острые и жирные блюда, специи, наваристые супы и бульоны, масла и избыток белка. В первые дни исключают мясо и рыбу, яйца, молочные блюда и бобовые, сыры и избыток свежих овощей и фруктов.
По мере улучшения диета при панкреатите немного расширяется за счет творога и паровых омлетов, нежирных кисломолочных продуктов, отварных и приготовленных на пару овощей, перетертых в пюре, легких супов, также протертых, фруктовых пюре и каш на воде.
По мере того, как пациент приходит в себя, из питания на последующее время исключают алкоголь и раздражающие блюда, острое и жирное, слишком кислые продукты и много специй. Основу рациона должны составлять сложные углеводы, белок и совсем немного жиров. Блюда готовят отварными, паровыми, запеченными без масла и жира.
Всё о панкреатите Вы можете прочитать на сайте MedAboutMe – https://medaboutme.ru/zdorove/spravochnik/slovar-medicinskih-terminov/pankreatit/
18+
На правах рекламы
Диета при панкреатите поджелудочной железы, примерное меню
Диета при болезни поджелудочной железы с условием верного выбора рациона поможет избежать перехода недуга в острую форму, а впоследствии и вовсе излечить его. При остром панкреатите, лучшим лекарством, несомненно, станет полный отказ от пищи хотя бы на пару деньков, дабы предоставить органу отдых и полный покой. Если обострение сопровождается болью, к месту ее локализации нужно дополнительно прикладывать лед.
Хронический панкреатит зачастую развивается как следствие острой формы, однако может наступать и сразу в тех случаях, когда у пациента наблюдается цирроз, гепатит или аллергические проявления. В подобных случаях гармоничное питание поможет предотвратить процесс обострения. Кушать при панкреатите нужно часто и понемножку, калорийность пищи должна соответствовать образу жизни больного. С целью дополнительного очищения желудочно-кишечного тракта имеет смысл употреблять послабляющие напитки.
Кроме этого, какая бы ни была выбрана диета при панкреатите поджелудочной железы, существует одно общепринятое правило: не переедать. Лучше разбить большую порцию на несколько маленьких, чем съедать все в один присест, переедая при этом.
Что можно кушать, а от чего лучше отказаться?
Решающее значение при панкреатите имеют характеристики продуктов и частота приемов пищи. Есть определенные нюансы, на которые следует обратить внимание больным.
| Рекомендованное питание | Категорически запрещаются |
| Пища, приготовленная паровым способом | Жареные, копченые, соленые продукты, а также сладости и алкоголь |
| Употребление перетертых и наполовину жидких продуктов | Некоторые соки, сладкие газированные напитки |
| Дробные и частые приемы пищи | Переедание |
| Употребление в пищу блюд исключительно теплыми (не стоит принимать как слишком холодную, так и очень горячую пищу) | Чересчур холодная и чересчур горячая пища |
| При приготовлении каш их следует варить исключительно на воде, а после этого перетирать | Продукты, сдобренные перцем или вообще любыми приправами |
Помимо этого, существует ряд продуктов, имеющих благоприятное влияние на поджелудочную, а также и тех, которые имеют свойство еще больше усугублять недуг. Прежде чем выбирать диету при панкреатите поджелудочной железы, составлять примерное меню, стоит ознакомиться с перечнем таких продуктов.
Прежде чем выбирать диету при панкреатите поджелудочной железы, составлять примерное меню, стоит ознакомиться с перечнем таких продуктов.
| Категория, к которой принадлежит продукт | Вредная пища |
| Мясные изделия | Утиное мясо, баранина и свинина, колбасные изделия и всевозможные консервы |
| Жиры | Маргарин и любой животный жир |
| Хлебобулочные изделия | Блины, пицца, сдоба и жареные пироги, свежеиспеченный хлеб |
| Каши и крупы | Бобовые культуры, пшенная и кукурузная крупы, ячмень, перловка |
| Первые блюда | Супы и борщи, сваренные на жирном мясном бульоне |
| Приправы, соусы | Поджарки, томатные соусы и подливки, абсолютно любые острые приправы |
| Напитки | Крепкий чай, кофе, газировка, спиртное, сок из апельсина, яблока, винограда и грейпфрута |
Общие рекомендации
В норме, поджелудочная железа обладает свойством производить нужные для переваривания пищи ферменты и гормоны, поддерживающие в организме нормальный обмен веществ. Если железа здорова, ее ферменты активизируются только при попадании в кишечник. Однако бывают случаи, когда синтезируемые элементы начинают работать преждевременно, что ведет к аутоперевариванию органа. Такое состояние называется острым панкреатитом.
Если железа здорова, ее ферменты активизируются только при попадании в кишечник. Однако бывают случаи, когда синтезируемые элементы начинают работать преждевременно, что ведет к аутоперевариванию органа. Такое состояние называется острым панкреатитом.
Принцип диеты при панкреатите поджелудочной железы, примерное меню, находится в прямой зависимости от стадии, на которой находится недуг: разгар острого процесса, обострение хронического, период реабилитации или же ремиссия. При остром приступе настоятельно рекомендуется воздерживаться от пищи в период от одного до трех дней. При этом нужно употреблять негазированную минералку комнатной температуры, отвары из сушеных яблок или шиповника (по 1-2 стакана ежедневно).
После затихания основного обострения допустимо пить в маленьком количестве некрепкий и несладкий чай. Где-то с четвертого-пятого дня от начала острого приступа можно потихоньку начинать пить овощной отвар, а еще через пару деньков – полностью переходить на общепринятый для больных панкреатитом режим.
Основные правила диетического питания при панкреатите вне обострения
Если рекомендованное меню диеты, по каким-либо причинам не подходит пациенту, он может сформировать его самостоятельно, следуя таким основным принципам организации питания при наличии воспаления:
- Пищу следует принимать в течение дня не менее 5 раз, что дозирует нагрузку на воспаленный орган. Объем пищи, потребляемой за один прием не должен превышать 250-300 г.
- Предпочтение отдается пище, приготовленной на пару, отваренной или запеченной. Перед приемом пища охлаждается до максимум 50 и перетирается, что облегчит работу железы. Также запрещается употребление излишне холодной пищи.
- Суточный объем килокалорий снижается до 1500, а соли – до 10 г.
- Ограничивается количество жирной и соленой пищи, исключаются специи и продукты с высоким содержанием грубых волокон и углеводов, а также кислые фрукты.
Щадящая диета при остром процессе
Нижеописанный способ хорош в случае острого приступа болезни и подразумевает два дня абсолютного голодания. Итак, в случае обострения, диета при панкреатите поджелудочной железы (примерное меню) будет выглядеть следующим образом:
Итак, в случае обострения, диета при панкреатите поджелудочной железы (примерное меню) будет выглядеть следующим образом:
| 1-2 день | Не употреблять пищу совершенно. Пить теплую и негазированную минералку, отвар из сухих яблок или шиповника |
| 3 день | По-прежнему минеральная вода и отвары. Разрешается осторожно добавлять к рациону несладкий и некрепко заваренный чай |
| 5 день | Можно дополнить рацион пюре из картофеля или моркови |
| 7 день | Разрешена речная рыба, приготовленная разными способами (кроме жарки) |
| 10 день | Можно понемножку пить молоко и добавить в рацион пудинг из творога |
Большую пользу организму при обострении принесут также супы на легком бульоне и парная говядина. Однако вводить их следует постепенно и очень осторожно, тщательно отслеживая реакцию организма – если появляется хоть какой дискомфорт от употребления того или иного продукта, его следует сразу же отменить.
Несколько правил диетического питания
Рационально подобранная диета при панкреатите поджелудочной железы – залог выздоровления. Составляя для себя меню, стоит внимательно отнестись к некоторым общим предписаниям:
- Принимать пищу лучше всего около шести раз за день, очень маленькими порциями.
- В восстановлении внутренних органов и тканей организма незаменимым помощником станет белок. Его суточное потребление должно доходить примерно до 120 граммов, из которых семьдесят процентов должны быть животными белками.
- Мясные продукты, которые разрешены пациенту с панкреатитом – кролик, курица, индейка и говядина. Жирное мясо категорически воспрещено. Рыба также не должна содержать в себе много жира. Готовить как рыбу, так и мясо нужно на пару.
- Очень хорошо помогает в восстановлении поджелудочной домашний творог, однако жирность его не должна быть выше пяти процентов.
- Недостаток растительных белков восполняется при помощи овсянки, круп и макарон.

- В рационе недопустимо содержание более чем семидесяти граммов растительного жира. Разрешается употребление сливочного масла, но только понемногу. При этом его следует добавить в тарелку перед едой, не допуская присутствия в пище при ее термической обработке.
- Все овощи лучше есть отваренными, разрешается употребление в сыром виде некислых фруктов. При употреблении в пищу яблок их нужно предварительно печь и перетирать.
- Диета при панкреатите поджелудочной железы (примерное меню) подразумевает полное исключение соленых и острых сортов сыра, сваренных вкрутую яиц, и бобовых культур. Нужно ограничить до минимума употребление соли.
Лучшим вариантом при составлении диеты будет опираться на индивидуальные особенности своего организма, определяя, какие из продуктов усваиваются наилучшим образом.
Примерная диета на неделю
Еще одна диета при панкреатите поджелудочной железы, примерное меню которой расписано на целую неделю. Завтрак
Завтрак
| День недели | Прием пищи | Примерное меню |
| Понедельник | Завтрак | Галеты с сыром |
| Второй завтрак | Омлет, приготовленный на пару, хлеб с чаем | |
| Обед | Гречка, творог, вареный кабачок | |
| Полдник | Тертое яблоко | |
| Ужин | Овсянка, салат из свеклы, печеное яблоко | |
| Перед сном | Стакан кефира | |
| Вторник | Завтрак | Творог |
| Второй завтрак | Салат из зеленого горошка и морковки | |
| Обед | Говядина с хлебом | |
| Ужин | Овощной суп, морковное или яблочное пюре, йогурт | |
| Перед сном | Стакан кефира | |
| Среда | Яблоко и йогурт | |
| Второй завтрак | Запеченное яблоко с изюмом | |
| Обед | Хлеб, рыба, гречневая каша | |
| Ужин | Суп-пюре из овощей, курага, хлеб | |
| Перед сном | Стакан кефира | |
| Четверг | Завтрак | Творог |
| Второй завтрак | Вареное мясо, кефир, овощное пюре | |
| Обед | Омлет, приготовленный на пару, хлеб, отвар из шиповника | |
| Ужин | Творожно-рисовый пудинг, йогурт | |
| Перед сном | Стакан кефира | |
| Пятница | Завтрак | Немного подсушенный хлеб и минералка без газа |
| Второй завтрак | Паровые котлеты, салат из свеклы | |
| Обед | Пюре из моркови и тыквы, тушеное мясо | |
| Ужин | Рисовая каша и йогурт | |
| Перед сном | Стакан кефира | |
| Суббота | Завтрак | Омлет, приготовленный паровым способом |
| Второй завтрак | Отварное мясо и слабозаваренный чай | |
| Обед | Рис, сваренный на пару, запеченное мясо, шиповниковый отвар | |
| Ужин | Йогурт с рисовым пудингом | |
| Перед сном | Стакан кефира | |
| Воскресенье | Завтрак | Творог (в чистом виде) |
| Второй завтрак | Чечевичный суп | |
| Обед | Курица, приготовленная на пару и пюре из яблок | |
| Ужин | Вареная свекла и картошка, парное мясо и не слишком крепкий чай | |
| Перед сном | Стакан кефира |
При этом обязательно учитывать, что объем каждого из вышеуказанных продуктов на одну порцию составляет двести грамм. Если имеет место большая любовь к сладостям, можно позволить себе немножко молочных конфет.
Если имеет место большая любовь к сладостям, можно позволить себе немножко молочных конфет.
Как питаться детям при панкреатите?
Диета у детей немного отличается от питания взрослых, поскольку должна учитывать, что для правильного роста и развития организм ребенка нуждается в богатом пищевом разнообразии. По аналогии со взрослыми, дети должны кушать почаще и крошечными порциями, воспрещается переедать. В обязательном порядке в рационе должно найтись место мясу, сливочному маслу и омлетам.
При остром протекании патологии омлет готовится исключительно из белков, при хроническом вполне допускается есть и желтки. Естественно, яйца нужно приготавливать паровым способом. Масло предполагается класть исключительно в тарелку перед едой. Запрещается термически обрабатывать его, а также кушать бутерброды с маслом. Очень полезно кушать творог, как в неприготовленном виде, так и в виде простых и фруктовых творожных запеканок.
Супы готовятся согласно тому же принципу, что и для взрослых, и варятся на постном бульоне. Блюда очень желательно употреблять как в тертом, так и попросту в вареном виде. Для десерта подойдет фруктовый кисель. В качестве сладостей можно изредка позволять ребенку зефир. Строго воспрещается кушать торты, шоколадные конфеты, черный хлеб. Нужно помнить, что, невзирая на перечень предполагаемых ограничений, еда обязана приносить максимальную пользу, быть достаточно калорийной и рационально сбалансированной.
Блюда очень желательно употреблять как в тертом, так и попросту в вареном виде. Для десерта подойдет фруктовый кисель. В качестве сладостей можно изредка позволять ребенку зефир. Строго воспрещается кушать торты, шоколадные конфеты, черный хлеб. Нужно помнить, что, невзирая на перечень предполагаемых ограничений, еда обязана приносить максимальную пользу, быть достаточно калорийной и рационально сбалансированной.
С целью восполнения в организме недостатка полезных микроэлементов и витаминов можно принимать соответствующие витаминные комплексы (однако обязательна предварительная консультация с лечащим врачом). Ни в каких случаях не стоит отступать от предписанных ограничений и позволять себе запрещенные продукты вплоть до полного выздоровления – ведь соблюдать разумные ограничения намного лучше, чем переходить на полное голодание вследствие очередного обострения болезни.
Соблюдение правильного диетического питания при панкреатите поджелудочной железы играет решающую роль в выздоровлении пациента, ничуть не меньшую, чем лечение медицинскими средствами. По сути, именно она-то и является главным методом лечения этого неприятного заболевания. Благодаря данной статье каждый человек, которого мучает проблема панкреатита, может подобрать для себя подходящее по всем параметрам меню из полезных продуктов, наиболее приемлемых для его организма.
По сути, именно она-то и является главным методом лечения этого неприятного заболевания. Благодаря данной статье каждый человек, которого мучает проблема панкреатита, может подобрать для себя подходящее по всем параметрам меню из полезных продуктов, наиболее приемлемых для его организма.
Ознакомившись со всеми перечнями как разрешенных, так и недозволенных продуктов, легко понять, какие из них будут способствовать скорейшему восстановлению организма, а какие, напротив, окажутся серьезным препятствием на пути к полноценному выздоровлению. Правильно сочетая разрешенные продукты, несложно будет добиться разнообразия в питании.
В любом случае, следует помнить, что полное восстановление поджелудочной железы (как и любого другого внутреннего органа) – процесс далеко не легкий и не быстрый. Поэтому нужно будет запастись терпением – впоследствии оно с лихвой окупится полученным результатом.
меню, рацион, диета и лечение
- Зачем соблюдать диету
- Питание в острой стадии панкреатита
- Правила диеты при хроническом панкреатите
- Как построить рацион при панкреатите
Правильность организации повседневного питания имеет большое значение для людей, страдающих панкреатитом. Ведь при этом заболевании поражается поджелудочная железа. Она относится к органам пищеварительной системы и ответственна за секрецию комплекса ферментов, которые действуют в просвете двенадцатиперстной кишки. Поэтому воспаление этого органа сопровождается нарушением переваривания основных питательных веществ (нутриентов) и развитием вторичных кишечных расстройств, а это требует соблюдения некоторых пищевых ограничений.
Ведь при этом заболевании поражается поджелудочная железа. Она относится к органам пищеварительной системы и ответственна за секрецию комплекса ферментов, которые действуют в просвете двенадцатиперстной кишки. Поэтому воспаление этого органа сопровождается нарушением переваривания основных питательных веществ (нутриентов) и развитием вторичных кишечных расстройств, а это требует соблюдения некоторых пищевых ограничений.
В медицине система лечебно-профилактического питания при панкреатите называется стол №5п по Певзнеру. Он может иметь разную степень пищевых ограничений. Ведь меню на диете при панкреатите подбирается с учетом ряда факторов. Рацион зависит от стадии и формы болезни, выраженности основных симптомов и степени ферментной недостаточности. При сочетании панкреатита с холециститом обычно назначается диета 5а.
Зачем соблюдать диету
Лечение и питание при панкреатите – взаимосвязанные понятия. Правильно составленный повседневный рацион позволяет решать ряд важных задач:
- Исключение избыточной нагрузки на воспаленную поджелудочную железу, что обеспечивается дробным питанием и исключением тяжелых для переваривания блюд.
 При панкреатите это является первостепенной задачей.
При панкреатите это является первостепенной задачей. - Обеспечение полноценного переваривания базовых нутриентов. Гармонично составленное меню при панкреатите обеспечивает поступление необходимого количества питательных веществ, а адекватное количество потребляемой пищи и сбалансированность блюд способствуют достаточному их перевариванию под действием ферментов поджелудочной железы.
- Предотвращение повторного обострения, ведь рецидив при этом заболевании в подавляющем большинстве случаев связан с погрешностями в питании. Поэтому при хроническом панкреатите диеты желательно придерживаться постоянно.
- Снижение риска развития сахарного диабета. Дело в том, что поджелудочная железа относится не только к пищеварительной системе, но и является эндокринным (гормонально активным) органом. Ее ткани содержат особые образования – островки Лангерганса. В них вырабатывается гормон инсулин, при его недостаточной продукции у человека формируется сахарный диабет. Хроническое или часто повторяющееся воспаление чревато постепенной гибелью функционально активных клеток, в том числе островков Лангерганса.
 Именно поэтому панкреатит рассматривают как один из основных факторов риска развития сахарного диабета, а погрешности в питании – как важный предрасполагающий фактор.
Именно поэтому панкреатит рассматривают как один из основных факторов риска развития сахарного диабета, а погрешности в питании – как важный предрасполагающий фактор.
Диета при панкреатите направлена на создание условий, при которых пищеварение будет максимально полноценным.
Питание в острой стадии панкреатита
В острейшей стадии болезни с выраженным болевым синдромом и признаками значительного нарушения пищеварения может быть использовано непродолжительное лечебное голодание. Эта рекомендация озвучена еще врачами прошлых веков, которые при остром панкреатите назначали своим пациентам холод (на область воспаленного органа), голод и физический покой. В этот период допустимо нераздражающее витаминизированное и щелочное питье, при необходимости назначается парентеральное (внутривенное) питание. А вот применение ферментов в этот период нецелесообразно, ведь в кишечник попросту не поступает никакая нуждающаяся в переваривании пища.
Голодание при остром панкреатите обычно длится 2–3 дня. За это время симптоматика утихает, что дает возможность переходить на диетическое питание – поэтапно:
За это время симптоматика утихает, что дает возможность переходить на диетическое питание – поэтапно:
- Первые дни после голодания питание малокалорийное и максимально щадящее. Блюда пюре образные, полужидкие, протертые. Их готовят на пару или отваривают, при подаче охлаждают до температуры тела. Такое меню преимущественно углеводное и не предполагает использования многокомпонентных рецептов и специй.
- После уменьшения выраженности симптомов панкреатита питание становится более разнообразным и калорийным. При этом меню расширяют постепенно, ориентируясь на самочувствие и степень усвоения пищи. На 4–5 день вводят легко усваивающиеся белки (творог, вываренное нежирное мясо, яйца), затем небольшое количество сливочного масла. Растительные масла пока не используются. Блюда по-прежнему отварные и паровые. Их уже не протирают, а измельчают или подают в виде супов, суфле и запеканок.
- В последующие 8–12 месяцев питание при панкреатите остается щадящим и дробным, хотя и не столь строгим.
 В целом в этот период рацион напоминает меню при хроническом панкреатите. Вводятся растительные масла, блюда становятся более разнообразными.
В целом в этот период рацион напоминает меню при хроническом панкреатите. Вводятся растительные масла, блюда становятся более разнообразными.
Диету с первых дней после завершения голодания дополняют использованием ферментных препаратов. Для этого назначается, например, Микразим®. Это позволяет частично компенсировать недостаток собственных ферментов поджелудочной железы, избежать ее перегрузки. Это особенно важно при потреблении жиросодержащих продуктов.
Соблюдение диеты при панкреатите – важнейший лечебный момент в период обострения. Именно она способствует постепенной нормализации работы воспаленной поджелудочной железы и всего пищеварительного тракта. А назначаемые препараты помогают справиться с симптомами, частично снять нагрузку с пораженного органа и компенсировать относительную ферментную недостаточность.
Правила диеты при хроническом панкреатите
Важно понимать, что при панкреатите диета нужна не только в период обострения. Большую роль она играет и после стихания основных симптомов, особенно при переходе болезни в хроническую форму. Ведь погрешности в питании при панкреатите даже в этот период чреваты быстрым и значительным ухудшением самочувствия. В таком случае говорят о рецидиве или обострении заболевания, а используемая при этом лечебная тактика, сходна с терапией первичного острого приступа болезни.
Ведь погрешности в питании при панкреатите даже в этот период чреваты быстрым и значительным ухудшением самочувствия. В таком случае говорят о рецидиве или обострении заболевания, а используемая при этом лечебная тактика, сходна с терапией первичного острого приступа болезни.
Поэтому, диета при хроническом панкреатите имеет скорее поддерживающее и профилактическое значение. При ее соблюдении человек не страдает от физического дискомфорта и ощутимого ухудшения качества жизни. Хотя некоторым людям требуется достаточно много времени, чтобы привыкнуть к строгим запретам на употребление некоторых продуктов и блюд.
По рекомендации врача, такую диету часто комбинируют с поддерживающей медикаментозной терапией – приемом ферментных препаратов.
«Запретные» продукты: от чего при панкреатите следует отказаться
Диета при панкреатите подразумевает как отказ от некоторых продуктов, так и исключение некоторых способов приготовления пищи. Причем рекомендации направлены в первую очередь на ограничение потребления блюд, которые способны раздражать пищеварительную систему или провоцируют усиление секреции.
Особое внимание уделяется продуктам с высоким содержанием жира. Их переваривание требует повышенной секреции липазы (одного из ферментов поджелудочной железы), что может спровоцировать обострение заболевания. Но и самовольно полностью отказываться от жиров в рационе нельзя. Ведь они необходимы для синтеза гормонов и ферментов, для построения клеточных стенок и оболочек нервных волокон, поддержания нормального состояния кожи.
| Продукт | Почему при панкреатите исключают |
|---|---|
Соки |
Соки при панкреатите относят к нежелательным продуктам. Ведь содержащаяся в них кислота нередко оказывает раздражающее действие и провоцирует усиленную выработку желудочного сока и всех пищеварительных ферментов. А это чревато обострением панкреатита. Лишь в период стойкого улучшения иногда разрешаются разведенные водой соки. |
Свежие (термически не обработанные) фрукты, ягоды |
Оказывают на пищеварительный тракт примерно такое же действие, как и соки. Фрукты при панкреатите могут употребляться изредка в запеченном виде или в составе не концентрированных компотов. Фрукты при панкреатите могут употребляться изредка в запеченном виде или в составе не концентрированных компотов. |
Кислые и богатые клетчаткой овощи. Соленья, маринады, консервы (в том числе домашнего приготовления) |
Оказывают раздражающее действие. Особенно нежелательны при панкреатите помидоры, репа, редька, редис, шпинат и щавель, свежая белокочанная капуста. Под запретом также квашеные овощи, маринованные и засоленные для долгого хранения продукты, консервы. |
Бобовые. Грибы. |
Содержащийся в них растительный белок может спровоцировать усиление активности поджелудочной железы. К тому же бобовые способствуют усилению газообразования в просвете кишечника, что обычно негативно сказывается на самочувствии человека с хроническим панкреатитом. |
Алкоголь, газированные напитки |
Стимулируют выработку всех пищеварительных ферментов, раздражающе действуют на слизистую оболочку всего желудочно-кишечного тракта. Примерно в 25% случаев обострение панкреатита связано с употреблением алкоголя. |
|
|
Являются источником большого количества быстроусвояемых углеводов, которые провоцируют быстрый выброс значительного количества инсулина. А это сопровождается значительной стимуляцией поджелудочной железы. Ее перегрузке способствует также сочетание большого количества углеводов и жиров в сдобе, кремах, выпечке. |
Жареные блюда |
Жарка продуктов с образованием характерной аппетитной корочки сопровождается образованием ряда потенциально вредоносных веществ. К ним относят нитрозамины, акролеин, акриламид и некоторые другие. Они обладают канцерогенным действием, раздражают слизистую оболочку пищеварительного тракта и провоцируют усиление выработки ферментов. Жарка также сопровождается повышением жирности продукта. |
Колбасные изделия |
Запрещены копченые и варено-копченые колбасы, сосиски и колбасы с большим количеством добавок. Раздражают и излишне стимулируют весь пищеварительный тракт. При этом иногда допустимы отварные сосиски из нежирных сортов мяса, ветчина из мяса птицы. |
Майонез, кетчуп, другие соусы фабричного производства |
Раздражающе действуют на слизистую оболочку желудочно-кишечного тракта, чрезмерно стимулируют поджелудочную железу. |
Снеки (чипсы, ароматизированные сухарики и др.), печенья и торты фабричного производства |
Входящие в их состав многочисленные химические соединения раздражают пищеварительный тракт. А повышенное количество жиров невысокого качества провоцирует перегрузку поджелудочной железы. |
Нежелательны также сало, жирные сорта мяса, сало, кисломолочные продукты высокой жирности, обжаренные на масле овощи (для заправки супов и соусов). Можно ли при панкреатите употреблять другие продукты с достаточно высоким процентом жира, необходимо уточнять у лечащего врача или диетолога.
Можно ли при панкреатите употреблять другие продукты с достаточно высоким процентом жира, необходимо уточнять у лечащего врача или диетолога.
А что можно есть?
Получив от врача немаленький список нежелательных продуктов, многие задумываются, что же кушать при панкреатите? Ведь для людей с этим заболеванием диета – отнюдь не кратковременная мера. А питаться хочется вкусно и не однообразно.
Крупы |
Используют гречневую и манную крупу, овсяные и пшеничные хлопья, рис. Пшенная и ячневая крупы допустимы нечасто, лишь при хорошей переносимости. Перловая используется редко, для большинства людей она тяжела для переваривания. |
Овощи |
Преимущественно отварные или паровые. Разрешены кабачки, морковь, цветная капуста, горошек, картофель, свекла, огурцы. Помидоры вводятся в период стойкого улучшения в небольшом количестве и лишь при хорошей переносимости. |
Мясо, птица |
Нежирные сорта (говядина, кролик, курица, индейка). Попадающиеся жировые прослойки обязательно тщательно срезают. Мясо отваривают, готовят на пару. В период стойкого улучшения его допустимо иногда запекать в рукаве без маринования. Попадающиеся жировые прослойки обязательно тщательно срезают. Мясо отваривают, готовят на пару. В период стойкого улучшения его допустимо иногда запекать в рукаве без маринования. |
Рыба |
Нежирные сорта, приготовленные на пару или отварные. Припускать (тушить в малом объеме воды) не рекомендуется, так как это способствует образованию раздражающих экстрактивных веществ. Подходят судак, треска, минтай, щука, сазан, окунь, хек, путассу. |
Яйца |
Жареные и вареные вкрутую яйца исключают. Предпочтительны паровые и запеченные омлеты, но могут использоваться и другие способы готовки. |
Молочные продукты |
Только нежирные. Можно использовать творог, ацидофилин, кефир, простокваша. Молоко в основном идет как добавка к кашам и напиткам, в составе суфле и омлетов. Сыр – разрешены нежирные сорта в небольшом количестве, причем лишь как добавка к блюдам. |
Хлеб, печенья |
Хлеб – рекомендуется пшеничный, несвежий, подсушенный. Печенье употребляется нечасто, при этом оно должно быть несдобным, галетным. Печенье употребляется нечасто, при этом оно должно быть несдобным, галетным. |
|
|
Преимущественно в запеченном виде или в составе компотов, киселей, желе, муссов, пастилы. Оптимально подходят яблоки, сухофрукты (в небольшом количестве). |
Напитки |
Некрепкий чай (можно с небольшим количеством лимона), не концентрированные компоты, минеральная вода, настой шиповника |
Как построить рацион при панкреатите
Примерное меню при панкреатите обычно включает 3 основных приема пищи (завтрак, обед, ужин), 2 перекуса между ними и кисломолочное питье незадолго до сна.
На завтрак предпочтительно готовить вязкие каши на воде, в период стабильного улучшения для варки использую разведенное молоко. Вначале их перетирают или подают в виде суфле, в последующем достаточно хорошо разварить. Завтрак дополняется бутербродом из суточного подсушенного хлеба с небольшим количеством масла (не более 10 гр. в сутки). Можно съесть кусочек сыра нежирных сортов или нежирной ветчины.
в сутки). Можно съесть кусочек сыра нежирных сортов или нежирной ветчины.
Второй завтрак (перекус) может состоять из творожного или мясного суфле, запеченного яблока с творогом или медом, подслащенного творога, парового или запеченного омлета. Также подается компот или настой шиповника.
Обед состоит из различных супов, второго блюда и напитка. Супы варят на втором бульоне и иногда заправляют небольшим количеством сметаны. Второе блюдо обязательно включает белковое блюдо, которое можно дополнять овощным или крупяным гарниром.
На полдник выбор блюд примерно такой же, как для первого перекуса. Он может состоять также из киселя и галетного печенья, иногда из банана.
Ужин должен быть достаточно легким для переваривания, но с достаточным количеством белка и углеводов. Это могут быть суфле, запеканки, мясо-творожные кнели, мясные рулеты в омлете, отварное мясо/рыба, к ним добавляется гарнир.
На ночь – кефир или другие разрешенные нежирные кисломолочные продукты.
Соблюдение диеты при панкреатите позволяет быстро улучшить и надолго стабилизировать состояние. Ведь лечебный рацион на столе 5п сбалансирован, обеспечивает организм всеми необходимыми питательными веществами, максимально щадит пораженную поджелудочную железу и способствует нормализации ее функции.
При отсутствии погрешностей в питании, панкреатит долго остается компенсированным и не сопровождается дискомфортными симптомами, а дополнительное использование ферментных препаратов позволяет избежать недостаточного переваривания пищи.
Важно: перед применением ознакомьтесь с инструкцией или проконсультируйтесь с лечащим врачом.
Можно ли при панкреатите? Диета при обострении воспаления желчного пузыря
Рассказываем, из-за чего может воспалиться желчный пузырь и что можно есть и пить при таком заболевании.
– Мне 30, поставили диагноз «панкреатит». Подскажите, чем питаться? Что можно, а что нельзя?
Причиной панкреатита (воспаления поджелудочной железы) в большинстве случаев является злоупотребление алкоголем. Кроме того, спровоцировать заболевание может длительный приём большого количества лекарств, неправильное питание и частые стрессы. Вторичный (реактивный) панкреатит возникает на фоне неблагополучия в желудочно-кишечном тракте (ЖКТ), часто заболевание провоцирует желчекаменная болезнь и состояние после удаления желчного пузыря.
Кроме того, спровоцировать заболевание может длительный приём большого количества лекарств, неправильное питание и частые стрессы. Вторичный (реактивный) панкреатит возникает на фоне неблагополучия в желудочно-кишечном тракте (ЖКТ), часто заболевание провоцирует желчекаменная болезнь и состояние после удаления желчного пузыря.
Как отмечают в клинике «Наедине» при хроническом течении заболевания человек чувствует постоянную тупую боль в животе, из-за нехватки ферментов для переваривания пищи может возникать понос, вздутие в животе, неустойчивый стул. Острая форма или обострение характеризуется очень сильной болью в животе. Терпеть её невозможно, поэтому пациенту сразу вызывают скорую и везут в больницу. Иногда в таких случаях требуется хирургическое вмешательство.
Можно ли полностью вылечить панкреатит?
По словам гастроэнтеролога клиники «Наедине» Татьяны Кузьминых, острая форма может закончиться только одним приступом, хроническую вылечить невозможно, но можно добиться ремиссии. Для этого необходимо вовремя принимать лекарства, сдавать анализы (кровь на ферменты, кал на копрограмму, узи брюшной полости, КТ и МРТ), заниматься профилактикой и следить за питанием.
Для этого необходимо вовремя принимать лекарства, сдавать анализы (кровь на ферменты, кал на копрограмму, узи брюшной полости, КТ и МРТ), заниматься профилактикой и следить за питанием.
Диета при панкреатите
Людям с хронической формой воспаления всю жизнь приходится соблюдать диету. В противном случае вы рискуете спровоцировать обострение. Диета заключается в отказе от продуктов, которые раздражают слизистую оболочку ЖКТ и обладают сокогонным действием. Также стоит исключить холодные напитки и блюда.
Еду можно запекать или готовить на пару, также разрешена протёртая пища. Питаться лучше часто: по пять или шесть раз в день. Пожилым людям с хроническим панкреатитом и сопутствующими сердечно-сосудистыми заболеваниями ко всему прочему необходимо исключить соль. В списке запрещённых продуктов и блюд – бобовые, пшено, соленья, виноград, клюква, вишня, кислые соки, холодные, газированные напитки, шоколад, наваристые супы на мясных и рыбных бульонах. Ниже мы более подробно расскажем о напитках и еде, которые вызывают больше всего вопросов.
Можно ли пить алкоголь?
Длительное и регулярное употребление алкоголя недопустимо. По праздникам можно позволить себе немного выпить, но стоит исключить холодные и газированные напитки: они особенно вредны. Острое воспаление может вызвать даже немного шампанского в Новый год, подчеркнула Татьяна Кузьминых.
Можно ли масло?
Запрещены тугоплавкие жиры – маргарин, бараний или говяжий жир. В ограниченных количествах можно несолёное сливочное масло (30 грамм в день), оливковое или рафинированное подсолнечное (10-15 грамм в день).
Можно ли яйца?
Гастроэнтеролог советует съедать не больше одного яйца в день. Например, можно сделать омлет. Жареные и сваренные вкрутую яйца стоит ограничить.
Какие овощи разрешены и как их готовить?
Все овощи нужно варить или запекать, сырые под строгим запретом. Нужно отказаться от белокочанной капусты, репы, редиса, бобовых, лука, чеснока, сладкого перца, особенно в сыром виде. Можно есть морковь, свёклу, кабачки, тыкву, стручковую фасоль, цветную капусту, картошку, зелёный горошек. Квашенная капуста, солёные помидоры и огурцы запрещены также.
Квашенная капуста, солёные помидоры и огурцы запрещены также.
Можно ли хлеб?
Нельзя употреблять ржаной хлеб, сдобную выпечку, слоёное тесто. Пшеничный хлеб можно, но только вчерашний и II сорта, разрешено несладкое сухое печенье.
Можно ли молоко и молочные продукты?
Нужно отказаться от мороженого, сладких сливок, сметаны. Разрешается нежирный и некислый творог, молоко и некислый кефир, ряженка, простокваша.
Можно ли мясо?
Необходимо отказаться от жирной свинины, баранины и колбасы. Также нельзя печёнку, почки, мозги, куриную шкурку. Врачи рекомендуют есть филе курицы, говядину, индейку и кролика.
Можно ли кофе?
Кофе, как и какао, нужно пить с осторожностью. Лучше ограничить количество выпитых в день чашек до одной, кофе можно только с молоком.
Можно ли заниматься спортом при панкреатите?
При тяжёлой стадии панкреатита спорт противопоказан. При хроническом истинном панкреатите запрещены тяжёлые физические нагрузки. В остальных случаях заниматься можно.
В остальных случаях заниматься можно.
Коротко о главном:
1. Чтобы избежать обострений при хроническом панкреатите, нужно тщательно следить за своим питанием. Нужно есть по пять или шесть раз в день, при этом порции не должны быть большими.
2. Полностью из рациона необходимо исключить продукты, которые механически раздражают слизистую оболочку желудочно-кишечного тракта и обладают сокогонным действием. Запрещены холодные блюда, а также холодные, газированные и алкогольные напитки.
3. Всю пищу нужно готовить на пару, также еду можно запекать в духовке.
4. Если вам поставили диагноз «хронический панкреатит», придерживаться диеты придётся всю жизнь.
Если у вас есть вопросы, на которые вы не можете найти ответ, задайте их нам, и мы постараемся на них ответить.
Фото: Сергей Зыков
0
Диета при остром панкреатите: после обострения поджелудочной железы у взрослых, что можно и нельзя есть, меню с рецептами, разрешенные и запрещенные продукты
Диета при остром панкреатите не прихоть, а жизненная необходимость, которая является частью терапии. Цели лечебного питания: уменьшение болевых ощущений, обеспечение отдыха пораженному органу, нормализация ферментации.
Цели лечебного питания: уменьшение болевых ощущений, обеспечение отдыха пораженному органу, нормализация ферментации.
Чем опасен панкреатит?
Под острым панкреатитом понимают воспаление поджелудочной железы с острым течением. Спровоцировать приступ могут:
- избыточное потребление спиртосодержащих напитков, жирной пищи;
- воспаление органов пищеварения;
- желчекаменная болезнь;
- прием медикаментов с выраженным патологическим воздействием на поджелудочную железу;
- травмы, хирургические манипуляции, вирусные заболевания.
Главным симптомом является боль, которая локализуется в эпигастральной области, под левым ребром, ирригировать под левую лопатку. Практически всегда болевой синдром усиливается после употребления жирных или острых блюд, спиртосодержащих напитков. Дополняют клиническую картину:
- вздутие;
- изжога;
- рвота;
- подташнивание;
- повышенная температура тела.
Важно! При наличии симптоматики острого панкреатита следует безотлагательно вызывать бригаду «Скорой помощи».
До приезда врача не рекомендован прием медикаментов, пищи и напитков, за исключением небольшого количества негазированной воды.
Самостоятельное лечение и игнорирование проблемы может привести к печальным последствиям для пациента. Заболевание опасно развитием осложнений:
- разрушение тканей участков поджелудочной железы;
- абсцесс;
- формирование псевдокист;
- сахарный диабет;
- асцит;
- нарушения работы дыхательной, сердечно-сосудистой систем.
Некоторые из этих состояний приводят к смертельному исходу.
Диета при остром панкреатите поджелудочной железы при обострении
Чаще всего больной нуждается в госпитализации. Терапевтическая стратегия определяется врачом сугубо индивидуально. Но диета при остром панкреатите – это всегда одна из составляющих лечебного процесса. Она предназначена не для коррекции веса, а преследует сугубо лечебные цели:
- сокращение выработки ферментов;
- уменьшение нагрузки на поджелудочную железу;
- устранение болевого синдрома;
- нормализация кислотно-щелочного баланса;
- стимулирование безопасного пищеварения.

В совокупности эти факторы запускают регенеративные процессы и сокращают воспалительные очаги.
В первые 3 суток диета при остром панкреатите у взрослых предполагает лечебное голодание, которое проводится под ригористичным контролем гастроэнтеролога, хирурга в стационарных условиях. При тяжелых формах недуга срок продляется до 5 дней.
На этапе голодания пациенту разрешены:
- отвар шиповника или боярышника;
- чистая питьевая вода;
- на 2-е сутки голода щелочные минерализованные воды «Славянская», «Поляна Квасова», «Смирновская», «Боржоми», «Ессентуки №4», перед употреблением бутылку следует оставить открытой, чтобы удалить газ.
Если у пациента есть сопутствующие патологии ЖКТ, список минеральных вод на усмотрение врача может быть сокращен или расширен. Дополнительно назначают внутривенное вливание глюкозы, которое помогает предотвратить обезвоживание, устраняют интоксикацию.
Так как питание в пищеварительный канал на этом этапе не поступает, желудочный сок и ферменты не синтезируются, начинается регенерация пищеварительного органа. На фоне приема медикаментов и соблюдения пищевого покоя пациент чувствует значительное улучшение. Однако для полноценной реабилитации поджелудочной железы диета при остром панкреатите соблюдается и далее. Особенно скрупулезно придерживаться диетических рекомендаций необходимо в первый месяц после обострения.
На фоне приема медикаментов и соблюдения пищевого покоя пациент чувствует значительное улучшение. Однако для полноценной реабилитации поджелудочной железы диета при остром панкреатите соблюдается и далее. Особенно скрупулезно придерживаться диетических рекомендаций необходимо в первый месяц после обострения.
Диета при остром панкреатите после голодания
По окончании терапии голодом пациенту показана диета Стол №5 П. У нее есть 2 варианта:
- Назначается при манифестации острого панкреатита или усилении симптомов хронического течения недуга сразу после этапа голодания. По сути, это переходная фаза между пищевым покоем и диетическим меню.
- Показан при стихании симптоматики, вялотекущем хроническом панкреатите.
Диета при панкреатите: что можно в первые дни после обострения?
Цель – снятие острой симптоматики, улучшение переваривающей функции ЖКТ. Первый вариант характеризуется низкой калорийностью. Ввиду того что такой рацион не отвечает физиологическим нормам и потребностям, длительность этапа составляет 3–7 дней.
Основные постулаты диеты после острого панкреатита:
- Частое употребление пищи миниатюрными порциями (100–300 г) 7–8 раз в сутки.
- Все блюда полужидкой консистенции, предварительно продукты отвариваются, затем перетираются. На 5–6 день больной может есть полувязкую еду.
- Температурный диапазон пищи 45–60°С.
- Суточная углеводная норма 200–250 г, белков 60–70 г, жиров 50 г, последние вводятся на 5–6 сутки.
- Полное отсутствие соли.
- Калорийность рациона увеличивается постепенно от 600 до 1000 ккал.
Прием пищи после голодания начинается с углеводной, чтобы избежать стимуляции желудочной и поджелудочной секреции:
- редкие супы-пюре, супы-муссы из перетертых отваров овощей, круп, за исключением пшена, перловки и кукурузной;
- водянистые каши, протертые;
- жидкий пюреобразный картофельный, тыквенный, морковный гарнир без включения масла или паровые муссы их указанных овощей;
- черствый пшеничный хлеб, лимит 50 г;
- настой из сушеных фруктов, ягод;
- некрепкий черный чай с сахаром;
- фруктовые кисели с натуральным заменителем сахара.

Через 1–2 дня порцион диеты при остром панкреатите расширяется белковыми блюдами:
- перетертый супец из вываренного мяса цыпленка;
- 1 яйцо всмятку, пашот или омлет, приготовленный без масла;
- диетические шницели из индейки, кролика, телятины, предварительно на мясе обрезают кожу, сухожилия, жирные фрагменты;
- биточки или суфле из трески, тунца, морского окуня, судака, хека, щуки;
- паровая запеканка из свежеприготовленного пресного творога;
- 100 г пастеризованного молока сугубо в блюдах.
На 3–4 сутки каши можно сварить на молоке, для улучшения вкусовых качеств добавить сливочное масло, но не более 5 г на одну порцию, запекать яблоки.
Важно! Категорически нельзя питаться в этот период свежими овощами, фруктами, блюдами из грибов, бобовых, цельных макарон, ржаным и свежим хлебом, сдобой, растительным маслом консервами, специями, пряностями, кофе, сырами, жирными молокопродуктами, цельным молоком, шоколадом, кондитерскими изделиями.
Диета при остром панкреатите: что можно есть, что нельзя для предотвращения приступов?
После уменьшения болевых синдромов пациенту показан второй вариант Стола №5 П. С учетом предписаний врача, соблюдать его придется до года или всю оставшуюся жизнь. Это позволит избежать рецидивов или увеличить интервалы между эпизодами обострения. Диета при остром панкреатите 2-я вариация показана и лицам, страдающим хроническим панкреатитом.
Основная концепция:
- Еда только паровая или отварная, другие способы термической обработки под запретом. Тушеные или приготовленные посредством запекания можно вводить в порцион не ранее, чем через декаду. О жареных продуктах необходимо забыть на весь период диеты.
- Протертый стол плавно заменяется измельченным провиантом. При благоприятном течении недуга это происходит через 2 месяца.
- По сравнению с предыдущим вариантом объем протеиновой пищи увеличен до 100 г, углеводной до 450 г. Постепенное увеличение жиров до 80 г.

- В случае ухудшения состояния, манифестации приступа острого панкреатита диета перестраивается, и пациент возвращается к 1 варианту с пониженным суточным калоражем.
- Допускается введение соли, но в ограниченном объеме – в сутки не более 6 г.
- Нельзя есть излишне холодную или слишком горячую пищу. Рекомендованный температурный диапазон 45–60°С.
- Грубая клетчатка исключается. Также противопоказаны экстрактивные вещества. С целью снижения их количества мясо или рыба варятся небольшими кусками в большом объеме воды. Первичный бульон сливается после закипания через 10–15 минут.
- Сохраняются принципы дробного питания. 5–6 трапез в день.
- Категорически исключается переедание.
- На алкоголь и курение табу.
Разрешенные продукты диеты после панкреатита:
- 200 г черствого хлеба или сухарей;
- овощные, крупяные супы с протертой вермишелью, допускается заправка из сливочного масла или сметаны;
- нежирные виды морской и речной рыбы;
- фарш мелкого помола из телятины, говядины, индейки, кролика;
- паровой белковый омлет, желток не более 1шт.
 в день;
в день; - свежие однодневные кисломолочные напитки, так как выдержанные 2 и 3 дня провоцируют запор, пресный творог – все молочные продукты с низким показателем жирности;
- из корнеплодов молодой картофель и морковь, цветная капуста, кабачки, тыква, в стадии ремиссии – молодой зеленый горошек, стручковая зеленая фасоль;
- каши, сваренные в равных соотношениях на воде и молоке из риса, гречневой, овсяной, перловой, манной крупы;
- яблоки некислых сортов без кожуры, их нужно перетирать или запекать, сладкие фрукты;
- кисели средней консистенции, желе без сахара;
- добавление в блюда до 30 г несоленого сливочного масла и 15 г растительного;
- некрепкий зеленый, черный чай, отвар боярышника, шиповника, листьев и ягод смородины, компоты.
В стадии стойкой ремиссии в лимитированном количестве разрешаются:
К абсолютно запрещенному провианту причислены:
Отзывы
Инна Валентиновна, Воронеж:
«Страдаю от панкреатита уже около 10 лет. Пока соблюдаю диетические предписания – все хорошо. Но стоит только побаловаться салом или сочным, зажаренным до румяной корочки стейком – сразу боли. Умудренная опытом, уже не допускаю критического состояния и сразу перехожу на протертый стол».
Пока соблюдаю диетические предписания – все хорошо. Но стоит только побаловаться салом или сочным, зажаренным до румяной корочки стейком – сразу боли. Умудренная опытом, уже не допускаю критического состояния и сразу перехожу на протертый стол».
Екатерина Петровна, Москва:
«После обострения пролежала 3 дня в стационаре. Врач разрешил только пить воду. Потом сын отправил меня для последующей реабилитации в санаторий. Первые 2 недели, кроме перетертых супов, вообще ничего не давали. Но зато каждый раз разные. В санаторном режиме в компании с такими же страждущими намного комфортнее выдерживать диетический порцион».
Диета при остром панкреатите взрослых – рецепты меню на каждый день
После устранения болей перечень разрешенных продуктов вполне обширный. В зависимости от своих предпочтений, каждый сможет составить меню. Чтобы диета при остром панкреатите не наскучила, рекомендуется разнообразить порцион новыми рецептами.
Морковно-кабачковый суп
В отдельной емкости отварить порезанные молодые кабачки (2 шт. ) до состояния мягкости. Отварить 2 средних картофелины и одну морковку. Все овощи перетереть посредством сита или блендера, добавить оставшийся отвар, в качестве альтернативы – горячее нежирное молоко, доводя до нужной консистенции.
) до состояния мягкости. Отварить 2 средних картофелины и одну морковку. Все овощи перетереть посредством сита или блендера, добавить оставшийся отвар, в качестве альтернативы – горячее нежирное молоко, доводя до нужной консистенции.
Картофельный суп-пюре
Очистить картофель, поместить его в воду на 3-4 часа, с целью уменьшения в нем содержания крахмала. Отварить, тщательно потолочь и разбавить отваром или молоком. При использовании картофельного отвара допускается добавление сметаны (1–2 ст. л.) или небольшой кусочек сливочного масла.
Мясной суп
Телятину нарезать порционными кусками, поместить в скороварку с водой. После закипания слить первичный отвар. Залить свежую воду и варить мясо до готовности. Измельчить в блендере или в мясорубке до паштетообразного состояния.
Отварить рис, протереть его. Смешать протертый рис, слизистый отвар и полученный мясной паштет, закипятить. Перед подачей на стол добавить в порционную чашу кусочек сливочного масла.
Паровые куриные колеты
Очистить мясо птицы от кожи, измельчить в мясорубке, если насадка с крупными отверстиями – несколько раз. Добавить в фарш яйцо, вымоченный в молоке кусок пшеничного хлеба. Сформировать котлеты и готовить в пароварке.
Добавить в фарш яйцо, вымоченный в молоке кусок пшеничного хлеба. Сформировать котлеты и готовить в пароварке.
Мясной паровой рулет
Приготовить постный телячий фарш (300 г). Добавить белок одного яйца, 150 г перетертой отварной моркови, тщательно перемешать. Сформировать пласт из массы, в качестве начинки и украшения положить яйцо, нарезанное кружочками. Придать форму рулета, приготовить на пару или сварить в пищевой пленке.
Оригинальные куриные кнели
Приготовить фарш мелкого помола из мяса птицы. Смешать с некислым свежим творогом, взбитым яйцом. Полужидкую массу набирать ложкой и опускать в кипящую воду.
Пудинг из манки с яблоками
Сварить манную кашу жидкой консистенции. Яблоки очистить от кожуры, натереть на мелкой терке. Соединить ингредиенты, ввести взбитое яйцо, немножко сахара, если позволяет диета. Выложить массу в форму и готовить на пару в течение 30 минут.
Творожное суфле
Стакан свежего творога размешать с 2 ст. л. манной крупы. Добавить мелко порезанный банан или персик, очищенный от кожуры, взбитое яйцо. Творожную массу выложить в формочки и готовить на пару.
л. манной крупы. Добавить мелко порезанный банан или персик, очищенный от кожуры, взбитое яйцо. Творожную массу выложить в формочки и готовить на пару.
Особенности диеты у детей
При диагностировании панкреатита у ребенка, ему, как и взрослому, назначается диетотерапия. Однако голодание не всегда показано детям, так как оно может спровоцировать дистрофию, что повлечет отставание в развитии росте. В первые дни после обострения возможно парентеральное питание.
Суточная калорийность рациона ребенка рассчитывается в соответствии с его возрастом, весом, ростом. Главные принципы детской диеты: частое питание небольшими порциями, сбалансированный рацион, щадящие способы приготовления. Список разрешенных и запрещенных продуктов не отличается о такового для взрослых.
ВАЖНО! Статья информационного характера! Перед применением необходимо проконсультироваться со специалистом.
Бананы при Панкреатите – можно или нет / польза или вред
Панкреатит — заболевание поджелудочной железы, характеризующееся воспалением и
расстройством ее функций. Эти нарушения приводят к дисфункции всей системы
Эти нарушения приводят к дисфункции всей системы
пищеварения, могут стать причиной ряда серьезных осложнений. Одним из ключевых
принципов лечения панкреатита является соблюдение правил диетического питания.
Полезные свойства
Несоблюдение рекомендаций, потребление нежелательных продуктов уменьшает шансы на нормализацию функций поджелудочной железы. Нарушение диеты может спровоцировать обострение заболевания. Из привычного рациона исключаются продукты, имеющие раздражающее действие, в первую очередь — овощи и фрукты. Со временем допускается их постепенное введение, после термической обработки. Банан — фрукт, который больным панкреатитом употреблять разрешено. Ряд гастроэнтерологов считают его полезным, при условии соблюдения некоторых условий. Соблюдение рекомендаций позволяет избежать появление негативных симптомов.
Введение бананов в состав диетического питания во время терапии панкреатита обосновано высокой концентрацией витаминов, микроэлементов. Экзотический фрукт содержит: сложные и простые углеводы, фитопротеины, калий, кальций, железо, магний, целый комплекс витаминов В, РР, А, С, Е.
Исследование состава фрукта позволило выделить триптофан — гормон счастья. Действие этого компонента весьма благоприятно для центральной нервной системы.
К ценным свойствам относятся:
- диуретическое — выведение избытка жидкости;
- снижение кислотности, предупреждение изжоги;
- нормализация гемоглобина при анемии;
- предупреждение нарушения состава кишечной флоры;
- активизация восстановления тканей пищеварительной системы;
- нормализация функций сердечно-сосудистой системы;
- антиаллергенное действие;
- активизация перистальтики тонкого и толстого кишечника;
- противоотечное действие;
- противотошнотное действие при заболеваниях органов пищеварения;
- положительное влияние на нервную систему;
- противовоспалительное действие при некоторых заболеваниях;
- предупреждение развития злокачественных опухолей;
- усиление образования желчи, более быстрое выведение ее в тонкий кишечник;
- мягкий слабительный эффект, профилактика запоров;
- восстановление флоры ЖКТ.

Содержание глюкозы в бананах
Расстройство секреторной деятельности поджелудочной железы заключается в снижении синтеза инсулина. Для нормального усваивания глюкозы гормон должен сохраняться на оптимальном уровне. При панкреатите пациенты должны контролировать уровень сахара в крови. Сахарный диабет может стать последствием воспаления поджелудочной железы. Большое количество натурального легкоусвояемого сахара делает бананы безопасными при воспалении поджелудочной железы.
Противопоказания к употреблению
Большое количество полезных качеств не делает фрукт абсолютно безопасным для некоторых категорий пациентов. Исключить эти фрукты из рациона необходимо лицам, страдающим сахарным диабетом, аллергией на растительную клетчатку. Нежелательны они для тех, кто имеет в анамнезе инсульт, инфаркт, ишемическую болезнь сердца. При тромбофлебите и патологии процессов свертываемости крови следует пересмотреть наличие бананов в привычном рационе.
Совместимость с другими продуктами
Лучше всего употреблять бананы самостоятельно, в перерывах между основными приемами питания. Они несовместимы с белковыми продуктами. Одновременное поедание белковых продуктов и бананов значительно замедляет процесс переваривания и всасывания пищи.
Они несовместимы с белковыми продуктами. Одновременное поедание белковых продуктов и бананов значительно замедляет процесс переваривания и всасывания пищи.
Фрукт провоцирует брожение. В результате этого образуется большее количество газов, развивается интоксикация желудочно-кишечного тракта. Под воздействием неблагоприятных факторов возможно обострение воспалительных заболеваний пищеварительных органов.
Возможные осложнения
К негативным симптомам приводит, неправильное употребление фрукта, неспособность организма усваивать их растительные компоненты. Вследствие этих индивидуальных особенностей возможно развитие осложнений:
- метеоризма;
- болезненные ощущения;
- чувство раздувания живота.
Любое из этих проявлений затрудняет терапию панкреатита, способствует развитию хронической формы заболевания. При длительном воспалении поджелудочной железы побочные эффекты могут вызывать обострение основной симптоматики.
Хроническое течение панкреатита
Экзотические плоды, которым посвящена статья, стали привычными и любимыми в наших широтах. Гастроэнтерологи практически каждый день слышат вопрос, можно ли кушать бананы при хроническом панкреатите. Патология требует выполнения всех предписаний врача, соблюдения правил строгой диеты. Физиологическое неприятие некоторых продуктов может вызвать ухудшение общего состояния здоровья.
Гастроэнтерологи практически каждый день слышат вопрос, можно ли кушать бананы при хроническом панкреатите. Патология требует выполнения всех предписаний врача, соблюдения правил строгой диеты. Физиологическое неприятие некоторых продуктов может вызвать ухудшение общего состояния здоровья.
Хроническое течение патологии поджелудочной железы предусматривает употребление бананов исключительно протертыми или запеченными. Их вводят в каши, суфле для разнообразия основного питания пациентов. При покупке фруктов необходимо выбирать спелые, натуральные плоды. Если перед вами в супермаркете лежат одинаковые по размеру фрукты, с равномерной окраской, без минимальных повреждений, это говорит об их генетически модифицированном происхождении.
Бананы при панкреатите прекрасно сочетаются с кисломолочными напитками — кефиром, простоквашей, ряженкой. Разрешено готовить из них коктейли. Белок свежего молока плохо усваивается при панкреатите, поэтому оно не рекомендуется для употребления в пищу. Высушенные фрукты подходят для приготовления компота.
Высушенные фрукты подходят для приготовления компота.
Ограничения
Введение бананов в диету требует строгого соблюдения некоторых правил:
- Перед едой, фрукты очень мелко нарезают ножом или перетирают через сито.
- Термическая обработка проводится методом запекания или на пару.
- В сутки можно кушать не более одного банана, не следует перегружать пищеварительную систему.
- Завтрак — наиболее подходящее время для употребления фруктов, так как для их переваривания требуется достаточно много времени. Прием в утренние часы обеспечивает усваивание полезных веществ и снабжает энергией.
- Фрукты, с которыми допускается комбинированное употребление бананов, определяет лечащий врач. Нельзя самостоятельно готовить фруктовые смеси.
- Обеспечить наличие специальных лекарственных средств, которые могут понадобиться при развитии болевого синдрома или других негативных последствий.
- При появлении побочных эффектов, чувства резкой боли в области желудка или шеи, фрукты сразу же исключаются из диеты.

При соблюдении рекомендаций есть бананы при панкреатите можно. Поэтапное введение плодов в рацион разрешается через неделю после купирования острых болезненных ощущений. Банан — кладезь витаминов, микроэлементов, пищевых волокон. Несмотря на хорошее усвоение, не рекомендовано кушать более одного фрукта в день в протертом виде или после обработки паром.
Для приготовления блюд можно использовать сушеные бананы. Из них получается очень полезный компот. Высушенные фрукты улучшают вкус каш, пудингов, суфле. Вкусные и полезные коктейли готовятся из банана и кисломолочных напитков. Для приготовления нужно измельчить половину плода в блендере и перемешать с 0,5 л кефира, простокваши или ряженки. Есть только одно требование — кисломолочные напитки должны быть свежими. Нельзя смешивать банановое пюре с молоком. При воспалении поджелудочной железы оно плохо усваивается и может вызвать неприятные симптомы.
Специфика употребления
Больным панкреатитом назначают диету № 5, которая подразумевает соблюдение некоторых пищевых ограничений. Смысл лечебного питания в том, чтобы снизить нагрузку на пищеварительную систему, особенно — на поджелудочную железу. Бананы относят к полезным фруктам, но затруднение их переваривания обусловливается наличием растительных волокон (клетчатки). Для легкого пищеварения рекомендуется мякоть плодов тщательно измельчать.
Смысл лечебного питания в том, чтобы снизить нагрузку на пищеварительную систему, особенно — на поджелудочную железу. Бананы относят к полезным фруктам, но затруднение их переваривания обусловливается наличием растительных волокон (клетчатки). Для легкого пищеварения рекомендуется мякоть плодов тщательно измельчать.
При покупке следует уделять внимание качеству и зрелости фруктов. Кожура должна быть чистой, без черных пятен, признаков гниения.
При патологиях поджелудочной железы не рекомендовано употребление сырых овощей и фруктов.
Особенности употребления:
- зеленые плоды могут вызвать приступ панкреатита;
- неспелые фрукты активизируют усиленное газообразование, метеоризм;
- один банан среднего размера — допустимая доза при панкреатите;
- для обеспечения энергии, устранения чувства голода лучше кушать фрукт утром.
Употребление бананов при панкреатите разрешено при соблюдении определенных рекомендаций. Плоды вводятся в лечебную диету маленькими порциями. Обработка бананов посредством пара или в духовке помогает снизить возможность развития негативных реакций со стороны пищеварительной системы. Бананы могут стать полезным компонентом в составе пюре, суфле, творожных запеканок. Мякоть фруктов подойдет для приготовления коктейлей, соков.
Обработка бананов посредством пара или в духовке помогает снизить возможность развития негативных реакций со стороны пищеварительной системы. Бананы могут стать полезным компонентом в составе пюре, суфле, творожных запеканок. Мякоть фруктов подойдет для приготовления коктейлей, соков.
Можно ли кушать свежие бананы?
Допускается употребление бананов при панкреатите при выполнении ряда рекомендаций. Плоды запрещено кушать в остром периоде панкреатита — в это время больной должен соблюдать лечебное голодание. Из-за большого содержания калорий бананы не желательно употреблять перед сном. Запрещено съедать более плода в сутки.
Среди прочих тонкостей употребления бананов выделяют:
- Добавлять фрукты при приготовлении кулинарных блюд — запеканок, каш, напитков, коктейлей. Это способствует предупреждению негативных симптомов.
- Употребление бананов, прошедших термическую обработку, уменьшает нагрузку на органы пищеварительной системы.
- Допускается добавление свежих плодов в диету только после наступления стойкой ремиссии заболевания.

- Пюре подходит для пробного употребления. Для этого очищенный банан можно размять вилкой или измельчить в блендере. Качественный состав блюда при таком способе приготовления не страдает, а усвоение проходит намного быстрее.
Блюда для завтрака
Завтрак является основным приемом еды, поэтому бананы подойдут для приготовления витаминных, энергетических блюд. Плоды выступают в качестве основного или дополнительного компонента. Главное соблюдать рекомендации диетологов и не вводить слишком большое количество бананов в рацион.
Запеканка творожная
Ингредиенты: банан — 2 шт, манная крупа — 1 стакан, творог — 500 г.
Способ приготовления: творог тщательно перемешать с манной крупой, мелко нарезанные бананы добавить в полученную массу. Можно кусочки бананов выложить поверх творожной массы. Выпекать в течение 15 минут.
Пудинг рисовый с банановым пюре
Ингредиенты: рис — ½ стакана, банан — 1-2 шт.
Способ приготовления: рис отварить до готовности, бананы растереть до состояния пюре (блендером, вилкой или посредством терки), все компоненты перемешать. Допускается взбивание смеси миксером.
Допускается взбивание смеси миксером.
Бананы, запеченные в духовке
Способ приготовления: нарезанные кружочками бананы укладывают на фольгу и запекают на протяжении 5 минут при температуре 150 градусов.
Домашний банановый торт
Ингредиенты: желатин, йогурт, печенье, банан, персик.
Способ приготовления: желатин разводят в 0,5 л натурального йогурта. В форму для выпечки одним слоем выкладывают печенье. Вторым слоем выкладывают кружочки бананов. Далее — еще один слой печенья, один слой бананов. Последний верхний слой — порезанный персик. Каждый из слоев обильно смазывается желатиново-йогуртовой смесью. После выкладывания всех слоев форма с тортом ставится в холодильник на 1 час.
Врачи-диетологи, гастроэнтерологи не рекомендуют употреблять более одного кусочка бананового торта. Нельзя злоупотреблять блюдом во избежание обострения симптомов, усугубления течения заболевания. Каждый новый рецепт следует обсуждать с лечащим врачом.
Коктейли
Цельное молоко не подойдет для приготовления диетических коктейлей при панкреатите. В состав напитка можно вводить только обезжиренное молоко или один из кисломолочных напитков — кефир, ряженку, простоквашу. Во избежание появления отрицательных симптомов молочные продукты можно разбавлять водой.
В состав напитка можно вводить только обезжиренное молоко или один из кисломолочных напитков — кефир, ряженку, простоквашу. Во избежание появления отрицательных симптомов молочные продукты можно разбавлять водой.
Способ приготовления: измельченный в блендере или на терке фрукт соединяют со стаканом одного из выбранных кисломолочных напитков. Полученный состав можно взбить блендером еще раз.
Сок
В состав соков, представленных в магазинах, входят вредные элементы — ароматизаторы, консерванты, подсластители, красители. Такие напитки запрещено употреблять при панкреатите. Соки следует готовить в домашних условиях. Самостоятельное приготовление обеспечивает натуральность и безвредность продукта. Особенности строения плотной мякоти плодов не позволяют выжать из банана достаточное количество сока. Для достижения нужной консистенции можно добавлять другие овощные или фруктовые соки: морковный, яблочный.
Лечебная диета при воспалении поджелудочной железы запрещает употреблять консервированные продукты, представленные в магазинах. Агрессивные компоненты — усилители вкуса, красители, консерванты могут вызвать усиление негативных признаков заболевания, ухудшение пищеварительных функций. Сок банана вводится в рацион не ранее десятого дня после устранения приступа острого панкреатита. Для снижения концентрации его можно разводить водой, другими соками.
Агрессивные компоненты — усилители вкуса, красители, консерванты могут вызвать усиление негативных признаков заболевания, ухудшение пищеварительных функций. Сок банана вводится в рацион не ранее десятого дня после устранения приступа острого панкреатита. Для снижения концентрации его можно разводить водой, другими соками.
Творог также входит в список продуктов, разрешенных для диетического питания при панкреатите и холецистите.
Как правильно запекать бананы?
Запекание может осуществляться двумя способами — очищенными или в кожуре. Запекание фруктов очень полезно для органов пищеварения. Блюда, приготовленные таким образом, не стимулируют усиленное газообразование. Высокая температура нейтрализует неблагоприятные свойства фитоклетчатки. Для разнообразия вкусового восприятия запеченные бананы можно кушать с медом, орехами, корицей.
Запекание без кожуры
Бананы разрезаются вдоль на две части. Их можно притрусить ванилином, корицей или орешками. Каждую фруктовую дольку заворачивают в пищевую фольгу и выкладывают в жаростойкую посуду. Запекать необходимо около 10 минут.
Запекать необходимо около 10 минут.
Запекание неочищенных бананов
Фрукты тщательно вымывают. В кожуре делают аккуратные надрезы, в которые можно поместить добавки. Бананы заворачивают в фольгу и также запекают в течение 10 минут.
Влияние на здоровье
Влияние на поджелудочную железу при панкреатите может быть двойственным. Они станут полезными в составе комплексной диеты при соблюдении рекомендаций врача. В таком случае фрукты восполняют витаминный дефицит, избавляют организм от избыточной жидкости, способствуют быстрому восстановлению травмированных тканей. Кроме воздействия на пищеварение, бананы оказывают положительное влияние на нервную систему.
Несоблюдение правил обработки, ранее введение бананов в рацион может вызвать отрицательные реакции:
- усиленное газообразование;
- частая отрыжка;
- расстройство пищеварения в виде диареи;
- спазмы в брюшной полости;
- метеоризм;
- обострение панкреатита.
Бананы при остром панкреатите
Обострение панкреатита выражается усилением воспалительных процессов. В этот период пациенты соблюдают лечебное голодание. После купирования приступа, нормализации анализов допускается постепенное введение продуктов питания. Бананы при остром панкреатите, как и остальные фрукты, допускаются к употреблению не ранее десятого дня после последнего приступа.
Общие рекомендации для больных панкреатитом заключаются в обязательной термической обработке бананов, употреблении ограниченного их количества.
Бананы при обострении хронического панкреатита
При хроническом течении панкреатита наблюдаются периоды ремиссии. Даже длительный бессимптомный период не говорит о том, что заболевание отступило. Во время обострения клиники употреблять свежие бананы категорически запрещается. Они вводятся в диетическое питание маленькими порциями не ранее десятого дня после купирования острого приступа. Разрешено употребление фруктов только после термической обработки. В запеченном виде бананы не вредят пищеварительной системы.
Влияние бананов на поджелудочную
При соблюдении рекомендаций диетологов бананы при панкреатите благоприятно влияют на поджелудочную железу. Мякоть, богатая клетчаткой, всасывает и выводит избыток пищеварительного сока. Пектин и крахмал обладают обволакивающими свойствами, облегчающими течение заболеваний с повышенной кислотностью. Бананы защищают поджелудочную железу от раздражения неблагоприятными веществами, облегчают пищеварение.
Можно ли есть бананы в фазу ремиссии?
Во время обострения хронического процесса употребление бананов запрещается. Свежие фрукты, имеющие в своем активные вещества, вредят органам пищеварения. При ремиссии важно соблюдение строгой диеты. Правильно обработанные бананы в этом случае будут способствовать нормализации процессов всасывания.
часто задаваемых вопросов о панкреатите | Колумбийский университет, хирургический факультет
Обзор | Причины | Генетика | Симптомы | Диагностика | Лечение | Автоматическая пересадка островков | Диета | Прогноз | FAQ
Диета
Можно ли употреблять алкоголь после того, как мне поставили диагноз панкреатит?
Если панкреатит вызван чрезмерным употреблением алкоголя, следует воздержаться от алкоголя. Если другие причины острого панкреатита были устранены и устранены (например, путем удаления желчного пузыря) и поджелудочная железа вернулась в норму, вы сможете вести нормальный образ жизни, но алкоголь все равно следует принимать только в умеренных количествах (максимум 1 порция / день).При хроническом панкреатите продолжается воспаление и мальабсорбция – пациенты постепенно теряют пищеварительную функцию и в конечном итоге теряют функцию инсулина, поэтому регулярное употребление алкоголя неразумно.
Какая диета рекомендуется, чтобы избежать обострения панкреатита?
При хроническом панкреатите поджелудочная железа постепенно теряет способность функционировать должным образом, и в конечном итоге эндокринная функция утрачивается. Это подвергает пациентов риску развития диабета 1 типа. Пациентам следует избегать рафинированного сахара и простых углеводов и вместо этого употреблять сложные углеводы и цельнозерновые продукты.В целом лучше всего подходят диеты с высоким содержанием белка и умеренным содержанием жиров.
Почему иногда я могу есть определенные продукты, а иногда эти же продукты вызывают проблемы?
Многие люди сталкиваются с этим явлением, хотя оно недостаточно изучено и на него нет однозначного ответа. Важно помнить, что нужно регулярно принимать добавки с ферментами поджелудочной железы, чтобы быть уверенным, что недостаток ферментов не является их причиной.
Нужно ли мне принимать ферменты поджелудочной железы, даже если я чувствую себя хорошо?
Да.Поскольку функция поджелудочной железы снижается, важно иметь ферменты для питания. Кроме того, ваши врачи часто назначают ферменты, чтобы избежать стимуляции поджелудочной железы и, следовательно, боли. Поджелудочная железа стимулируется высвобождением ферментов поджелудочной железы, когда в кишечнике остается непереваренная пища. Ферменты начинают перевариваться, когда пища находится в желудке, поэтому поджелудочная железа отдыхает.
Могу ли я принимать другие витамины или добавки?
Пациенты с хроническим панкреатитом подвержены риску хронической мальабсорбции, поэтому их необходимо регулярно проверять на дефицит питательных веществ.Витаминная терапия должна основываться на этих ежегодных анализах крови. Как правило, можно принимать поливитамины, кальций, железо, фолиевую кислоту, витамин E, витамин A, витамин D и витамин B12, в зависимости от результатов анализа крови.
Обезболивание
Какие виды обезболивания доступны?
Цель состоит в том, чтобы продолжать жить не в больнице, а бодрствовать и функционировать. Многие пациенты принимают несколько видов лекарств. Пероральные препараты включают наркотики, такие как Percocet и оксикодон, и их можно использовать в сочетании с ненаркотическими лекарствами, такими как миорелаксанты и антидепрессанты.После того, как назначен пероральный режим, можно справиться с острыми приступами, добавляя лекарства. Если пероральные лекарства не переносятся, вам может потребоваться госпитализация для внутривенного введения лекарств. Блокады нервов могут использоваться для снятия боли в течение нескольких месяцев: при блокаде нервов вводят иглу через кожу в спине, чтобы заблокировать основные нервы, идущие к поджелудочной железе. Эта процедура также может быть выполнена эндоскопически, при которой пучок нервов поджелудочной железы вводится (через эндоскоп в желудке) с обезболивающим препаратом длительного действия, действующим в течение нескольких месяцев.Блокады нервов разрушают нервы, но со временем они отрастают, поэтому пациентам требуется повторное лечение. Другой подход к борьбе с болью – использование имплантируемых болевых насосов в позвоночник. Большинство имплантируемых насосов доставляют постоянные низкие дозы для облегчения боли, и их можно использовать вместе с пероральными лекарствами. Оральный метадон – очень хорошее лекарство от хронической боли.
Если я буду принимать лекарства по рецепту в течение длительного времени, попаду ли я в зависимость?
Психологическое сложение и психологическая зависимость – это разные вещи.Понятие зависимости обычного человека относится к психологической зависимости. Однако для пациентов с панкреатитом необходимо устранить сильную продолжающуюся боль, и необходимость в обезболивающих не является психологической зависимостью. Некоторым пациентам необходимо всегда принимать лекарства, потому что хронический панкреатит не проходит, а боль необходимо контролировать, чтобы они могли нормально функционировать. Если организм привыкает к определенному обезболивающему, вы не можете просто прекратить его внезапно: его нужно будет отменить медленно и под тщательным наблюдением врача.Если проблема хронического панкреатита заключается в продолжающемся микроскопическом воспалении поджелудочной железы, боль будет присутствовать всегда, и устранение боли не является социальной зависимостью, а, скорее, является необходимой терапией, такой как прием лекарств от кровяного давления. Наша команда старается использовать комбинации различных лекарств, чтобы максимально снизить дозировку наркотиков.
Если боль, вызванная моей болезнью, станет больше, чем мои обезболивающие, какие еще варианты у меня будут?
Другие варианты включают болеутоляющие насосы, имплантируемые нервные стимуляторы и, в некоторых случаях, хирургические стратегии.Лучший подход определяется в зависимости от конкретного заболевания и анатомии каждого человека.
Один из вариантов хирургического вмешательства – стентирование, которое может быть выполнено эндоскопически. При хроническом воспалении части протока поджелудочной железы могут сужаться или сужаться. Когда поджелудочная железа стимулируется пищей в кишечнике, она усердно работает, чтобы перекачивать пищеварительные соки через это сужение, вызывая боль и обострение. Размещение стента в протоке может сделать суженную область более открытой, предотвращая или уменьшая боль.
В крайних случаях может быть выполнено удаление всей поджелудочной железы (панкреатэктомия) для уменьшения или устранения боли, связанной с панкреатитом. Панкреатэктомия снимает боль в 90% случаев, но приводит к диабету. Для решения этой проблемы программа по панкреатиту предлагает инновационный процесс извлечения собственных инсулино-продуцирующих клеток пациента и их повторной инъекции в печень после удаления поджелудочной железы. Эта процедура, называемая трансплантацией аутологичных островковых клеток, позволяет пациентам сохранить часть их инсулино-продуцирующей функции, предотвращая трудноизлечимую форму диабета, известную как хрупкий диабет.
Повседневная жизнь
Смогу ли я заниматься обычными делами?
Вам может понадобиться набор поддерживающих лекарств, но если правильно контролировать боль и другие симптомы, вы сможете жить нормальной жизнью.
Повлияет ли ежедневный стресс на мою болезнь?
У нас нет убедительных данных по этому поводу, но опыт показывает, что стресс действительно усугубляет симптомы хронического панкреатита.
Предлагает ли Центр поджелудочной железы систему поддержки пациентов, страдающих хроническим панкреатитом?
Наш центр свяжет пациентов, находящихся на разных стадиях заболевания, так как есть пациенты, которые хотят поговорить с другими о стратегиях выживания.
Повлияет ли курение на мою болезнь?
Да. В целом, как мы все знаем, курение вредно для нашего здоровья. Курение увеличивает риск рака поджелудочной железы, а панкреатит увеличивает риск рака поджелудочной железы, поэтому мы хотим минимизировать факторы риска.
Эпизоды панкреатита
Как долго длится серия?
Острые эпизоды могут длиться всего один день, в то время как пациенты с хроническим панкреатитом могут испытывать эпизоды боли, которые длятся недели или дольше.
Что можно сделать для предотвращения приступов?
Возможность предотвращения эпизодов будет зависеть от причины болезни каждого человека. Возможные подходы могут включать удаление желчного пузыря, воздержание от алкоголя, диету с низким содержанием жиров, прекращение приема лекарств, которые могут вызвать панкреатит, и многое другое.
Что можно сделать, чтобы ограничить продолжительность эпизода?
Лучший способ минимизировать эпизод – это гидратация и нутритивная поддержка. Временное прекращение перорального приема пищи позволит поджелудочной железе отдохнуть.
Когда у меня будет эпизод, меня госпитализируют?
Пациенты могут справиться с обострениями дома с помощью повышенных доз обезболивающих или придерживаясь чистой жидкой диеты в течение нескольких дней. Если вы не можете справиться с болью или что-либо съесть или выпить, вас необходимо госпитализировать.
Симптомы
У меня появились симптомы, но я боюсь звонить врачу, потому что мои анализы отрицательные, и я не хочу его беспокоить. Что мне делать?
Вам следует позвонить своему врачу.Вашему врачу может потребоваться изменить режим приема обезболивающих или ферментов.
Я могу справиться с болью – действительно ли мне нужно вызывать врача?
Вам следует позвонить врачу, если боль станет невыносимой, если вы не можете есть или пить, или если у вас поднимется температура или возникнет желтуха.
Если симптомы требуют госпитализации, как долго я буду в больнице?
В зависимости от ситуации вам может потребоваться находиться в больнице в течение нескольких дней или недель.
Как мне справиться с неловкими ситуациями, такими как газы и диарея?
В дополнение к назначению пищеварительных ферментов ваш врач может порекомендовать соответствующие лекарства, отпускаемые без рецепта, такие как симетикон или ломотил, чтобы помочь с такими симптомами.
Все мои диагностические тесты в норме, но симптомы есть. Значит ли это, что у меня больше нет панкреатита?
Нет. В какой-то момент поджелудочная железа может покрыться рубцами и перестать вырабатывать ферменты, поэтому анализы крови кажутся нормальными, несмотря на панкреатит.
Почему у меня возникают волны тошноты, когда у меня нет боли?
Нарушения пищеварения могут вызывать тошноту, вздутие живота и другие симптомы.
Другое
Придется ли мне делать операцию?
Какая операция? Наиболее распространенные процедуры при панкреатите включают дренаж и удаление части или всей поджелудочной железы.Потребуется ли вам процедура, зависит от многих факторов и требует индивидуального обсуждения с врачом.
Бывает ли панкреатит у детей?
Панкреатит у детей встречается очень редко. Иногда его диагностируют у молодых людей, у которых в анамнезе болит живот. Обычно боль в животе – это боль в животе, но в редких случаях может указывать на панкреатит, особенно когда боль связана с приемом пищи, возникает после употребления жирной пищи, если локализация боли распространяется вокруг спины вокруг лопаток и если ребенок испытывает повторяющиеся эпизоды.
Следующие шаги
Если вы или кто-то, о ком вы заботитесь, страдаете панкреатитом, Центр поджелудочной железы здесь для вас. Если вам нужен диагноз, лечение или другое мнение, у нас есть специальная программа по панкреатиту, готовая помочь.
Позвоните нам по телефону (212) 305-4795 или воспользуйтесь нашей онлайн-формой, чтобы связаться с нами сегодня.
Чтобы узнать больше о панкреатите:
Обзор | Причины | Генетика | Симптомы | Диагностика | Лечение | Автоматическая пересадка островков | Диета | Прогноз | FAQ
Сопутствующие услуги
Связанные темы
Острый панкреатит, вызванный пищевыми продуктами
Dig Dis Sci.Авторская рукопись; доступно в PMC 1 декабря 2018 г.
Опубликован в окончательной редакции как:
PMCID: PMC5718054
NIHMSID: NIHMS
4
, Ph.D, 1, $ , Ph.D, 1, $ , к.т.н., 1 , д.м.н., 2 и, к.т.н. 1, *Мурли Манохар
1 Департамент медицины, отделение легочных заболеваний, Центр эозинофильных заболеваний Тулейна, Школа медицины Тулейнского университета, Новый Орлеан, Лос-Анджелес, 70112, США
Алок К.Verma
1 Департамент медицины, Отделение легочных заболеваний, Центр эозинофильных заболеваний Тулейна, Медицинский факультет Тулейнского университета, Новый Орлеан, Лос-Анджелес, 70112, США
Сатиша Уппарахалли Венкатешайя
1 Департамент медицины, Отделение легочных заболеваний, Центр эозинофильных заболеваний Тулейна, Медицинский факультет Тулейнского университета, Новый Орлеан, Лос-Анджелес 70112, США
Хемант Гоял
2 Кафедра внутренней медицины, Медицинский факультет Университета Мерсер, 707 Pine St.Macon, GA 31201
Анил Мишра
1 Департамент медицины, Отделение легочных заболеваний, Центр эозинофильных заболеваний Тулейна, Школа медицины Тулейнского университета, Новый Орлеан, Лос-Анджелес 70112, США
1 Департамент медицины, Отделение легочных заболеваний, Тулейнский центр эозинофильных расстройств, Школа медицины Тулейнского университета, Новый Орлеан, Лос-Анджелес 70112, США
2 Кафедра внутренней медицины, Медицинский факультет Университета Мерсер, 707 Pine St.Macon, GA 31201
* Автор, ответственный за переписку: Анил Мишра, доктор философии, заведующий кафедрой Шлидера, профессор и директор Тулейнского центра эозинофильных расстройств, департамент медицины, отделение легочной медицины, Медицинская школа Тулейнского университета, Новый Орлеан, LA 70112 , США. Тел: 504-988-3840; Факс: 504-988-2144; ude.enalut@arhsima$ Авторы внесли одинаковый вклад: Мурли Манохар, Алок К. Верма
Окончательная отредактированная версия этой статьи издателем доступна на Dig Dis SciSee, другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
Пищевая аллергия – широко распространенная во всем мире проблема, определяемая как неблагоприятный иммунный ответ на пищу. Множество связанных с иммунитетом эффекторных клеток, таких как тучные клетки, эозинофилы, нейтрофилы и Т-клетки, участвуют в пищевых аллергических ответах, которые классифицируются как IgE-опосредованные, не-IgE-опосредованные и смешанные (IgE и не-IgE) в зависимости от основные иммунологические механизмы. Пищевые антигены в основном нацелены на желудочно-кишечный тракт, включая поджелудочную железу, которая воспаляется из-за пищевой аллергии и приводит к острому панкреатиту.Отчеты показывают, что некоторые пищевые белки вызывают панкреатит; однако подробный механизм, лежащий в основе панкреатита, вызванного пищевыми продуктами, не изучен. Цель обзора – понять и обновить текущий сценарий пищевого панкреатита. Через PubMed был проведен всесторонний поиск литературы по соответствующим исследовательским статьям, и статьи были выбраны на основе их актуальности для панкреатита, опосредованного пищевыми аллергенами. Несколько случаев в литературе, указывающих на то, что острый панкреатит был спровоцирован после употребления горчицы, молока, яиц, бананов, рыбы и киви.Панкреатит, вызванный пищевыми продуктами, – это игнорируемая и неизученная область исследований. В обзоре подчеркивается значение пищи в развитии панкреатита и обращается внимание врачей и ученых на то, чтобы рассматривать пищевую аллергию как возможную причину инициирования патогенеза панкреатита.
Ключевые слова: Пищевая аллергия, панкреатит, эозинофилы, тучные клетки, нейтрофилы
Введение
Растущая распространенность аллергических заболеваний является тревожной проблемой во всем мире, и пищевые аллергены вносят основной вклад в развитие аллергических проявлений, включая желудочно-кишечные расстройства [ 1–4] Распространенность пищевой аллергии оценивается примерно в 3–8%, и она значительно влияет на качество жизни восприимчивых людей [5].Пищевая аллергия может быть определена как провокация неблагоприятной аллергической реакции на безвредные пищевые антигены из-за чрезмерной реакции иммунной системы на эти пищевые антигены. Признаки и симптомы пищевой аллергии могут варьироваться от легкой до тяжелой и могут включать рвоту, диарею, крапивницу, зуд, отек языка, низкое кровяное давление и затрудненное дыхание [6]. Аллергические реакции, вызванные пищевыми продуктами, обычно возникают в течение от нескольких минут до нескольких часов после воздействия, а при тяжелых симптомах они могут вызвать тяжелую анафилаксию [7].Чрезмерная реакция иммунной системы организма на пищевые антигены может поражать несколько органов, включая дыхательные и желудочно-кишечные (ЖКТ) тракты, что приводит к развитию обострения астмы, дыхательной недостаточности, эзофагита и гастроэнтерита [2, 8, 9]. аллергия считается одной из причин, способствующих развитию острого панкреатита [10–14]. Панкреатит характеризуется острым или хроническим воспалением, которое может быть вызвано различными вредными раздражителями, такими как камни в желчном пузыре, алкоголь и мутация в гене трипсиногена [15–17].Ежегодная заболеваемость острым и хроническим панкреатитом колеблется от 13 до 45 и от 4,4 до 11,9 на 100 000 человек в США соответственно [15, 18]. Более того, различные сообщения указывают на повышенную заболеваемость панкреатитом среди населения Японии по сравнению с США [15, 19, 20]. К сожалению, в текущем сценарии распространенность острого или хронического панкреатита, вызванного пищевыми продуктами, все еще недостаточно хорошо известна. С 1933 г. известно, что пищевая аллергия является причиной острого панкреатита у собак [21]; кроме того, несколько случаев острого панкреатита у человека, вызванного аллергией на горчицу [22], молоко [13, 23], икру трески [14], яйца [24], бананы [10], рыбу [25] и киви [ 26] описаны в литературе.Несколько исследований показывают, что высокая гликемическая нагрузка [27], жир, мясо, яйца и т. Д. [28] связаны с риском острого панкреатита, не связанного с желчнокаменной болезнью. В то время как другие исследования сообщают, что овощи и рыба (включая жирную и нежирную рыбу) могут быть связаны со снижением риска нежечнокаменного острого панкреатита [29, 30]. Все эти исследования показывают, что определенные продукты связаны с повышенным риском острого панкреатита, в то время как другие продукты могут быть защитными.
Согласно клиническим данным и тестам на аллергию, известны три типа пищевых аллергий: опосредованные IgE (немедленный тип, гиперчувствительность I типа), не опосредованные IgE (замедленный тип, клеточная гиперчувствительность, гиперчувствительность IV типа) и смешанные (IgE / Non-IgE) [31], но в случае пищевого панкреатита механизм неизвестен, и эта область исследований игнорируется и остается неизученной.В этом обзоре мы стремимся предоставить текущую информацию, касающуюся пищевых аллергических реакций, с особым акцентом на панкреатит, вызванный пищевыми продуктами. Текущий обзор также предоставляет исследователям и врачам платформу для понимания участия различных типов эффекторных иммунных клеток, а также действующих молекулярных механизмов, которые могут проложить путь к новым методам лечения панкреатита, вызванного пищевыми продуктами.
Аллергические расстройства, вызванные пищевыми продуктами
Аллергические расстройства, вызванные пищевыми продуктами, растут во всем мире, и некоторые продукты питания были отмечены как фактор риска развития аллергических заболеваний [32].Пищевая аллергия в основном связана с увеличением цитокинов Th3, эозинофилов и тучных клеток в ответ на аллергены [33–36]. Пищевая аллергия сообщается при нескольких аллергических заболеваниях, включая астму [33–35], аллергический ринит [37, 38], желудочно-кишечные расстройства, такие как эозинофильный гастроэнтерит [2, 39] и панкреатит [23, 24]. Здесь мы суммировали текущее понимание и имеющиеся данные о развитии эозинофильного гастроэнтерита-зависимого и независимого панкреатита.
Эозинофильный гастроэнтерит и панкреатит, вызванный пищевыми аллергенами
Эозинофильный гастроэнтерит (ЭГ) – это воспалительное заболевание, опосредованное эозинофилами, которое характеризуется инфильтрацией эозинофилов в желудке, тонком и толстом кишечнике [2, 39]. Базовые эозинофилы обычно присутствуют в желудочно-кишечном тракте [40]; но увеличение их количества наблюдалось в ответ на несколько раздражителей, таких как повреждение тканей и инфекции, включая пищевые аллергены.Эти накопленные эозинофилы активируются, что приводит к дальнейшей дегрануляции и секреции различных цитокинов, которые приводят к развитию EG [41]. Примечательно, что данные указывают на то, что 50–75% пациентов с ЭГ имеют в личном или семейном анамнезе сопутствующие аллергии или атопические расстройства [42, 43]. Было высказано предположение, что пищевая аллергия способствует стимулированию ЭГ у этих пациентов, а увеличение общего IgE и пищевого специфического IgE свидетельствует о пищевой аллергии в стимулировании ЭГ у пациентов [44]. Сообщалось, что коровье молоко вызывает эрозивный гастрит, и его исключение из рациона показало исчезновение аллергических симптомов у младенцев [45].Некоторые данные свидетельствуют о том, что пищевые антигены играют решающую роль в патогенезе эозинофильного гастроэнтерита, а также колита [46].
Впервые о пищевой аллергии и ее связи с панкреатитом сообщили в 1933 году Couvelaire и Bargeton [21], продемонстрировав экспериментальный анафилактический шок, вызванный пищевыми аллергенами, у собак. Несколько сообщений о случаях острого панкреатита, спровоцированного пищевой аллергией на горчицу [22], молоко [13, 23], яйца [24], бананы [10], рыбу [25] и киви [26], у человека были опубликованы в литература.Также сообщалось о хроническом панкреатите, сохраняющемся от 8 до 10 лет из-за употребления различных видов пищи, таких как говядина, молоко, картофель, рыба и яйца [12]. Основные симптомы этих пациентов включают острую боль в животе и повышение уровня ферментов поджелудочной железы в сыворотке крови. Однако результаты ультразвукового исследования брюшной полости и компьютерной томографии выявили отечность поджелудочной железы только у одного пациента. Уровень IgE в сыворотке был повышен у одного пациента [12]. Этих пациентов лечили путем прекращения приема провоцирующей пищи (говядины, молока, картофеля, рыбы и яиц) и одновременно с приемом препарата кромогликат, стабилизатора тучных клеток [47], который предотвращает высвобождение гистамина из тучных клеток.Также сообщалось о случае острого панкреатита, связанного с молоком, у 23-летнего пациента с повторяющимися эпизодами боли в животе, повышенными уровнями амилазы, липазы, сывороточного IgE, бета-лактоглобулина и увеличенной поджелудочной железой в ультразвуковом отчете. У пациента были рецидивирующие эпизоды острого панкреатита, сопровождавшиеся эритемой лица с инъекцией конъюнктивы, генерализованным зудом, диареей и эозинофилией после употребления молока [13]. Inamura et al. [10] опубликовали случай рецидивирующего острого панкреатита (три эпизода), вызванного аллергией на бананы, у 47-летней женщины с аллергическим ринитом в анамнезе.Пациент лечился консервативно, с легкой диетой и внутривенным введением жидкости, с исчезновением клинических симптомов в течение нескольких дней. Кроме того, повышенные уровни амилазы вернулись к нормальным значениям параллельно с клиническими симптомами. Общий уровень IgE в сыворотке составлял 644 МЕ / мл, при этом уровень специфического IgE к бананам составлял 2,18 UA / мл, что свидетельствует о значительной аллергии на бананы. Gastaminza et al. [26] представили клинический случай острого панкреатита, развившегося после употребления киви у 48-летнего мужчины с язвой двенадцатиперстной кишки и кровотечением из верхних отделов желудочно-кишечного тракта в анамнезе.Этот пациент также имел в анамнезе ринит, бронхиальную астму и аллергию на пиразолоны. Сообщалось о повышении уровня амилазы и лейкоцитоза в сыворотке крови на 835 Ед / л (N = 60–190) и 13 000 / мм 2 соответственно. Примечательно, что после 48 часов лечения легкой диетой, внутривенными жидкостями, антацидами и анальгетиками; уровни амилазы и липазы в сыворотке вернулись к норме. Поскольку пациент умеренно пил, у него изначально был диагностирован алкогольный панкреатит, но примерно через две недели он перенес еще один эпизод панкреатита после употребления в пищу киви.Позже прокол показал аллергию на киви, и ему поставили диагноз панкреатит, вызванный фруктами киви. Согласно отчету, после отказа от употребления киви в течение последних пяти лет пациент больше не страдал панкреатитом. Сводка каждого из этих отчетов о случаях острого панкреатита, связанного с пищевыми продуктами, представлена в. Более того, несколько крупных многонациональных когортных исследований показали, что высокая гликемическая нагрузка, насыщенные жиры, холестерин, красное мясо и яйца повышают риск острого панкреатита, не связанного с желчнокаменной болезнью [27, 28]; Напротив, недавние отчеты показали, что потребление овощей и рыбы (жирной и нежирной рыбы вместе) может быть связано со снижением риска нежечнокаменного острого панкреатита [29, 30].Резюме проспективных когортных исследований, связанных с острым панкреатитом, вызванным пищевыми продуктами, у человека было представлено в.
Таблица 1
Обобщенные детали отчетов о случаях острого панкреатита, вызванного пищевыми аллергенами
| S. No. | Возраст (год) | Пол | Аллергическая пища | Симптомы | s) | IgE | Другие ассоциированные заболевания | Список литературы | |
|---|---|---|---|---|---|---|---|---|---|
| 1. | 26 | F | NA | Боль в животе, аллергические симптомы | Эозинофилы | Повышенный уровень IgE в сыворотке | EP | [11] | |
| 2. | M | Говядина (дважды) Молоко Картофель Рыба Яйцо | Боль в животе, Мигрень, Зуд, Повышенная амилаза в сыворотке крови, Боль в эпигастрии, связанная с диффузной головной болью | Нормальный уровень эозинофилов | Повышенный уровень IgE 9026 у одного пациента NA | [12] | |||
| 3. | 23 | NA | Молоко | Боль в животе, эритема лица с инъекцией конъюнктивы, генерализованный зуд, диарея, эозинофилия, повышенные уровни ферментов поджелудочной железы в сыворотке крови, увеличение поджелудочной железы и отек | на сонограмме | Уровень IgE | NA | [13] | |
| 4. | 48 | M | Киви | Боль в эпигастрии, рвота, диарея, эритема лица, зуд, повышение сывороточного уровня | Повышенный уровень сывороточного аминофосфата | общий IgE 257 мкл / мл | Язвенная болезнь двенадцатиперстной кишки в анамнезе, кровотечение из верхних отделов пищеварительного тракта, аллергия на пиразолоны, ринит и бронхиальная астма | [26] | |
| 5. | 47 | F | Банан | Эпигастралгия, Тошнота, Рвота, Диарея, Повышенный уровень амилазы в сыворотке и моче, Ампула Фатера опухшая и отечная | Повышение 64 Тучных клеток, Общее количество IUE в сыворотке | увеличено и специфический IgE к бананам (2,18 UA / мл) | NA | [10] | |
| 6. | – | M | Молоко | Симптомы ЭГ, такие как тошнота, рвота, боль в животе, диспепсия, Нарушение всасывания, асцит и потеря веса, повышение ферментов поджелудочной железы в сыворотке и общий билирубин | Повышение эозинофилов | – | EG | [23] | |
| 7. | 8 | M | треска | Анафилактическая реакция, Боль в животе, Повышенный уровень ферментов поджелудочной железы в сыворотке крови, Паренхиматозный отек при УЗИ | NA | Специфический IgE для трески = 1,30 kU / л | ребенка в первый год жизни атопический дерматит и хроническая диарея с мукореей и ректальным кровотечением, соблюдение диеты без коровьего молока[25] | ||
| 8. | 25 | F | Яйцо | Рвота, боль в животе, диарея 263 | Повышенный уровень эозинофилов 2300–2500 эозиофилов / мкл | Общий IgE = 89.7 кЕд / л Уровень специфического для яиц IgE = 6,25 кЕд / л | История перемежающихся желудочно-кишечных симптомов EG | [24] |
Таблица 2
Проспективные когортные исследования, связанные с пищевым острым панкреатитом
| S. No. | Возраст, лет | Пол | Тип питания | Показатели заболеваемости | Результаты | Заключение | Ссылка |
|---|---|---|---|---|---|---|---|
| 1. | 45–84 | M Высокие гликемические факторы питания | 49 случаев на 100000 человеко-лет в наивысшем квартиле гликемической нагрузки и 33 случая на 100000 человеко-лет в самом низком | 364 случаях инцидентов, не связанных с GS-AP (236 у мужчин и 128 у женщин) | диеты с высоким гликемическим индексом связаны с повышенным риском non-GS-AP | [27] | |
| 2. | 45–84 | M-39,267 F-32,191 | Жирная и нежирная рыба | Потребление рыбы ≤2,0–3,0 порций в неделю было связано со значительным снижением риска заболевания. | 320 случаев (209 случаев у мужчин и 111 случаев у женщин) инцидентов Non-GS-AP | Потребление всей рыбы (жирная рыба и нежирная рыба вместе) может быть связано со снижением риска non-GS-AP | [30] |
| 3. | 46–84 | 80 019 женщин и мужчин, | Овощи, фрукты | Снижение риска на 17% при потреблении овощей | 320 инцидентов (216 мужчин и 104 женщин) с non-GS-AP | Потребление овощей, но не потребление фруктов, может играть роль в предотвращении non-GS-AP | [29] |
| 4. | 45–75 | 145,886 Мужчины и женщины | Факторы питания: жир, яйца, красное мясо, молоко, кофе и т. Д. | Более высокая частота ассоциаций между факторами питания и панкреатитом наблюдалась в основном для GS-AP | GS – ОП (n = 1210), AP, не связанное с камнями в желчном пузыре (n = 1222), или рецидивирующий AP, или подозрение на хронический панкреатит (n = 378). | Насыщенные жиры, источники холестерина, такие как красный цвет и яйца, положительно связаны с GS-AP. Витамин D из молока, кофе, клетчатки, защищающей от GS-AP. | [28] |
Связь ЭГ с панкреатитом также хорошо известна в литературе, и основной причиной ЭГ является пищевая аллергия [23, 24, 48]. Многочисленные сообщения о случаях показывают, что ЭГ может возникать из-за коровьего молока [23] и аллергии на яйца [24], а тяжелые симптомы ЭГ могут усугублять острый панкреатит. Судзуки и др. [23] сообщили о случае панкреатита, связанного с аллергией на молоко, который быстро улучшился после прекращения приема молока из рациона и лечения кортикостероидами.У пациента отмечено снижение сывороточных титров ферментов поджелудочной железы и общего билирубина с нормализацией количества эозинофилов в крови. Пациент не проявлял никаких симптомов в течение более 20 месяцев после исключения коровьего молока из своего рациона. Таким образом, аллергия на коровье молоко у взрослых встречается редко; но они могут вызвать серьезные осложнения, такие как анафилаксия, гастроэнтерит и панкреатит.
Tse и соавторы [24] представили первое сообщение о панкреатите, связанном с аллергией на яйца, у 25-летней женщины, не страдающей атопией, у которой в течение 30 минут после еды яйца возникла боль в животе, иррадирующая в левый подреберь и грудь.Лабораторные исследования выявили уровень липазы в сыворотке 2400 Ед / л и периферическую эозинофилию 23,3% (2300 эозинофилов / мкл), который оставался повышенным, увеличившись до 26% (2500 эозинофилов / мкл) на следующей неделе. Дальнейшая диагностическая визуализация, такая как УЗИ, КТ брюшной полости и MRCP, не выявила расширения желчных протоков или обструкции, что могло бы указывать на наличие камней в желчном пузыре. Другие частые причины панкреатита, такие как алкоголь и лекарства, также были исключены. Верхняя эндоскопия в норме. Тесты на аллергию in vitro подтвердили положительный уровень яичных специфических IgE на уровне 6.25 кЕд / л, тогда как все другие протестированные продукты были отрицательными, а общий IgE составил 89,7 кЕд / л. Однако биопсия двенадцатиперстной кишки показала 80 эозинофилов / поле высокой мощности, а анализ образца кала на яйцеклетки и паразитов был отрицательным, за исключением присутствия кристаллов Шарко-Лейдена, что указывает на лежащий в основе эозинофильный желудочно-кишечный процесс. У этого пациента ЭГ была достаточно тяжелой, чтобы вызвать острый панкреатит. Возможный механизм, предсказанный для опосредованной пищевой гиперчувствительностью и острого панкреатита, связанного с ЭГ, связан с обструкцией протока поджелудочной железы из-за местного воспаления двенадцатиперстной кишки [49].
Несмотря на то, что в большинстве случаев пищевого панкреатита наблюдались отек кишечной стенки и воспаление двенадцатиперстной кишки, компьютерная томография показала нормальную поджелудочную железу [10, 23, 24, 26]. Это указывает на то, что визуализации поджелудочной железы недостаточно для диагностики панкреатита. В пересмотренной классификации панкреатита в Атланте говорится, что для диагностики панкреатита следует рассматривать два из трех следующих критериев, например, классическую боль в животе, уровень амилазы или липазы в крови, индуцированный примерно в 3 раза, а визуализация показывает воспалительные изменения в поджелудочной железе.Кроме того, следует учитывать индекс Бальтазара и систему оценки тяжести КТ для диагностики острого панкреатита как степени А и оценки 0 соответственно, потому что панкреатит может возникать даже без каких-либо видимых морфологических изменений после компьютерной томографии [50]. Однако есть некоторые сообщения о случаях, которые указывают на боль в животе и повышение липазы более чем в 3 раза, и отсутствие панкреатита. Несмотря на то, что они соответствуют клиническим критериям острого панкреатита, у них могут быть язвы кишечника или отек стенки кишечника.В клинических условиях, когда есть сомнения в достоверности повышения липазы, клиницисты обычно проводят КТ / МРТ для подтверждения интерстициального отека / воспаления поджелудочной железы. Когда он присутствует, то нет никаких сомнений в том, что панкреатит возник. Когда он отсутствует при соблюдении клинических критериев, остается сомнительным, действительно ли возник панкреатит. Следовательно, некоторые из этих случаев могут не быть панкреатитом, но как минимум соответствуют текущим общепринятым клиническим критериям.
Механизм, связанный с пищевым панкреатитом
Inamura et al. (2005) предположили, что заброс желчи в проток поджелудочной железы из-за обструкции ампулы Фатера и неправильной активации зимогенов может быть причиной панкреатита, индуцированного пищей [10]. Они обнаружили воспалительные изменения в ампуле Фатера при эндоскопическом исследовании, а патология показала накопление большого количества тучных клеток в слизистой и подслизистой оболочке при иммуногистохимическом окрашивании против триптазы тучных клеток человека.Кроме того, тучные клетки играют ключевую роль в панкреатите [51, 52]. Этот пациент ел бананы каждый раз перед приступами рецидивирующего острого панкреатита и имел специфический IgE к бананам 2,18 МЕ / л, что является низким положительным результатом. Другой пациент с панкреатитом, связанным с аллергией на молоко, имел специфический IgE к коровьему молоку 2,17 KU / 1 [13]. Следовательно, гиперчувствительность к пищевому веществу также может привести к закупорке ампулы Фатера, вызывая рефлюкс желчи в проток поджелудочной железы и несоответствующую активацию ферментов поджелудочной железы, приводящую к приступу панкреатита.
Индуцированный пищевым аллергеном IgE играет роль в индукции панкреатита
Пищевая аллергия, опосредованная IgE, вызывается, когда антитела IgE связываются с рецепторами FcεRI (фрагмент, кристаллизующаяся область эпсилон R1), присутствующими на тучных клетках и базофилах, вызывая высвобождение биологически активные медиаторы и последующее развитие реакции гиперчувствительности в отношении съеденных пищевых белков [1]. Как правило, пищевая аллергия, опосредованная IgE, проходит в два этапа: сенсибилизацию и дегрануляцию.Первичное воздействие аллергена вызывает сенсибилизацию, а вторичное воздействие того же аллергена вызывает дегрануляцию иммунных клеток. Когда происходит первичное воздействие пищевых аллергенов, эти аллергены улавливаются и превращаются в небольшие пептидные фрагменты антигенпрезентирующими клетками (APC) с помощью протеасомного комплекса. Позже эти процессированные пептидные фрагменты были представлены вместе с основным комплексом гистосовместимости класса II (MHC-II) с помощью APC наивным CD4 + Т-клеткам. Эти наивные CD4 + Т-клетки дифференцируются в клетки Th3 в присутствии IL-4 и продуцируют специфические цитокины Th3, такие как IL-5 и IL-13 [53].Эти высвободившиеся цитокины Th3, особенно IL-4 и IL-13, были ответственны за перекрестную связь между T- и B-клетками и индуцировали дифференцировку B-клеток в плазматические клетки, продуцирующие IgE. Эти пищевые аллерген-специфические антитела IgE связываются с поверхностными рецепторами FcεRI на тучных клетках и базофилах [54]. Эта стадия обычно известна как «фаза сенсибилизации», и теперь сенсибилизированные иммунные клетки готовы спровоцировать более сильный аллергический ответ при повторном воздействии того же пищевого аллергена. Вторичное воздействие того же пищевого аллергена вызывает перекрестное связывание аллерген-специфических антител IgE с рецепторами FcεRI на тучных клетках и / или базофилах.Это событие, в свою очередь, вызывает дегрануляцию тучных клеток или базофилов, высвобождая несколько медиаторов аллергии, таких как гистамин, простагландин D2 и т. Д., Что приводит к развитию характерных симптомов аллергии [55].
Кроме того, сообщалось об IgE при панкреатите, и несколько исследований показали, что пациенты с хроническим панкреатитом имеют высокие уровни IgE в сыворотке крови, особенно во время острых воспалительных эпизодов или если пациент принимал алкоголь [56, 57]. Более того, в более раннем отчете о клиническом случае также было показано повышение уровня IgE у пациента с рецидивирующим панкреатитом, длившимся несколько лет, что предполагает пищевую аллергию как причину рецидивирующего панкреатита [12].Кроме того, аллергия на молочный белок была связана с острым панкреатитом, а сывороточные уровни IgE, специфичных к молочным белкам и бета-лактоглобулину, были повышены у пациентов с острым панкреатитом [13]. Кроме того, даже при возникновении острого панкреатита сообщалось о аллергии на фрукты, в том числе бананы [10] и киви [26]. У этих пациентов не было рецидива панкреатита после отказа от ответственной пищи [26]. Кроме того, повышенная гликемическая нагрузка [27], потребление насыщенных жиров, холестерина, красного мяса и яиц [28] повышают риск острого панкреатита, не связанного с желчными камнями.На большой выборке из 80 019 шведов (в возрасте 46–84 лет) Оскарссон и его коллеги показали, что потребление овощей может играть роль в профилактике острого панкреатита, не связанного с желчными камнями [26]. Аналогичным образом сообщалось о случае 26-летней женщины с большим количеством эозинофилов в резецированной поджелудочной железе, у которой подозревали эозинофильный панкреатит. Интересно, что у нее неоднократно было нормальное количество эозинофилов, гистологически нормальные биопсии гастродуоденальных, селезеночных и чревных лимфатических узлов.Было высказано предположение, что это могло быть связано с редким проявлением аллергических проявлений в анамнезе пациента и повышением сывороточных уровней IgE [11]. Эти исследования показывают, что некоторые продукты могут вызвать приступ панкреатита, тогда как некоторые продукты минимизируют риск развития панкреатита.
Не-IgE-опосредованный панкреатит, вызванный пищевыми аллергенами
Не-IgE-опосредованные пищевые аллергии были вызваны компонентами иммунной системы, отличными от IgE-антител. При пищевой аллергии, не опосредованной IgE, задействован клеточный иммунный ответ с преимущественным воздействием на слизистую оболочку желудочно-кишечного тракта [58].Сообщалось об эозинофильной инфильтрации и вовлечении Т-клеток при желудочно-кишечных пищевых аллергических расстройствах, не опосредованных IgE (не-IgE-EGID), таких как синдром энтероколита, индуцированного пищевым белком (FPIES) и энтеропатия, индуцированная пищевым белком (FPE) [2, 59] . Кроме того, активация и рекрутирование эозинофилов рядом цитокинов, включая IL-3, IL-5 и GM-CSF, а также хемокины, приводит к дегрануляции эозинофилов. Дегрануляция эозинофилов вызывает высвобождение нескольких провоспалительных медиаторов, в том числе катионных белков, хранящихся в гранулах, и многих цитокинов, таких как TGF-β, IL-3, IL-4, IL-5, IL-8, IL-13, IL-18 и TNF-α, которые были ответственны за повреждение тканей в месте аллергии [2, 15].В литературе цитируется несколько сообщений о случаях накопления эозинофилов у пациентов с панкреатитом, и это состояние названо «эозинофильным панкреатитом (ЭП)» [11, 60]. В совокупности можно предположить, что пищевые специфические реакции, не опосредованные IgE, могут играть решающую роль в индукции воспаления поджелудочной железы, но необходимы дальнейшие усилия, чтобы установить этот феномен.
Роль воспалительных клеток в панкреатите, опосредованном пищевыми аллергенами
Известно, что некоторые иммунные эффекторные клетки, такие как тучные клетки, базофилы, эозинофилы, нейтрофилы и Т-клетки, играют решающую роль в стимулировании пищевых аллергических реакций при панкреатите [61, 62 ].Вкратце подробности каждой ячейки представлены ниже.
Тучные клетки
Сообщалось об участии тучных клеток в желудочно-кишечных расстройствах, вызванных пищевой аллергией [63, 64]. В IgE-опосредованных реакциях происходит выработка аллерген-специфического IgE, и последующее связывание с рецепторами FcεRI на тучных клетках инициирует аллергический ответ через высвобождение нескольких медиаторов, что приводит к расширению сосудов, отеку и бронхоспазму [65]. Тучные клетки играют решающую роль в остром летальном [66], хроническом панкреатите [52, 67] и полиорганной недостаточности [68].Также было выявлено участие тучных клеток в развитии панкреатита и возможность аллергической основы заболевания [66].
Базофилы
Базофилы составляют менее 1% лейкоцитов периферической крови и участвуют в развитии IgE-опосредованных аллергических заболеваний [1]. Недавнее наблюдение, основанное на первоначальных результатах, показало, что активированные базофилы играют важную роль в патофизиологии аутоиммунного панкреатита через активацию сигнального пути TLR [69].Однако роль базофилов в индуцированном пищевыми аллергенами патогенезе острого и хронического панкреатита все еще не ясна и требует дальнейшего изучения.
Эозинофилы
Эозинофилы также играют ключевую роль в пищевых аллергических реакциях [23, 24]. Сообщалось об эозинофилии крови и тканей с выраженной дегрануляцией при ряде аллергических заболеваний, связанных с пищевыми продуктами [2]. Эотаксины являются важными молекулами и действуют как хемоаттрактант эозинофилов, который способствует накоплению эозинофилов в ткани [70].Эозинофильный панкреатит – относительно редкое заболевание, характеризующееся местной или диффузной инфильтрацией эозинофилов в поджелудочную железу [60] во время острого панкреатита, а также зарегистрированное в связи с эозинофильным гастроэнтеритом [48, 71]. Эти наблюдения предполагают, что аллергические реакции, вызванные пищевыми аллергенами, могут быть вовлечены в развитие эозинофильного панкреатита, но еще недостаточно изучены, и их необходимо изучить, чтобы лучше понять механистические аспекты индуцированного пищевыми продуктами панкреатита.Совсем недавно мы сообщили о важной роли эозинофилов в хроническом панкреатите, вызванном церулеином. Наш отчет показывает, что у мышей с дефицитом эозинофилов GATA 1 наблюдается снижение ремоделирования поджелудочной железы по сравнению с мышами дикого типа или с дефицитом гена IL-5 после 4 недель лечения церулеином [72].
Нейтрофилы
Решающая роль нейтрофилов была показана у пациентов с пищевой аллергией [73] и хорошо документирована при остром панкреатите [15, 74, 75]. Медиаторы нейтрофилов вызывают активацию трипсина, воспаление и могут способствовать патогенезу панкреатита [74] через IgE-независимые анафилактические реакции [76].Внеклеточные ловушки нейтрофилов (NET) представляют собой деконденсированную ДНК и гистоны, которые улавливают микробные патогены и организуют инициирование и разрешение воспаления [17, 77]. NET образуются в поджелудочной железе мышей во время АП, вызывают индукцию трипсина и способствуют патогенезу панкреатита [74]. На основании этих сообщений, индукция нейтрофилов, связанная с пищевыми аллергенами, может быть связана с прогрессированием острого панкреатита.
Лимфоциты
Несколько исследований показывают, что пищевые аллерген-специфические Т-лимфоциты запускают выработку ИЛ-4 и ИЛ-13, необходимых для синтеза IgE, а Т-лимфоциты хорошо документированы в патогенезе острых состояний [78, 79] и хронический панкреатит [80].CD4 + Т-клетки играют решающую роль в прогрессировании заболевания при остром экспериментальном панкреатите [78]. Лиганд CD40 (CD40L), присутствующий на Th-клетках, связывается с рецептором CD40, присутствующим на APC, и регулирует события панкреатита [81]. Кроме того, Т-клетки участвуют как в опосредованных IgE, так и в не-IgE пищевых аллергических реакциях [82, 83] и могут играть важную роль в регуляции патогенеза панкреатита. Следовательно, необходимы дальнейшие исследования для понимания глубоких молекулярных механизмов, участвующих в патогенезе пищевой аллергии и панкреатита.
В соответствии с пониманием, кажется, что могут действовать IgE-опосредованные и не-IgE-опосредованные аллергические механизмы. Таким образом, тучные клетки, базофилы, эозинофилы, нейтрофилы и Т-клетки могут играть решающую роль в панкреатите, вызванном приемом пищи, и в будущем их необходимо будет протестировать для разработки вариантов лечения. Возможный рабочий механизм острого панкреатита, вызванного пищевыми аллергенами, и участие различных типов иммунных клеток были показаны на рис.
Возможный рабочий механизм при остром панкреатите, индуцированном пищевыми аллергенамиПищевые аллергены интернализуются и обрабатываются антигенпрезентирующими клетками (APC) с помощью протеосомного комплекса и представлены основным комплексом гистосовместимости класса II (MHC-II) наивным CD4 + Т-клетки, которые дифференцируются в клетки Th3 в присутствии IL-4 и продуцируют IL-5 и IL-13, которые активируют последующие аллергические пути и вызывают острый панкреатит, связанный с пищевым аллергеном.Аллергическая реакция поджелудочной железы, вызванная пищевыми аллергенами, может быть опосредованной IgE или не-IgE. При ответе, опосредованном IgE, клетки Th3 секретируют IL-4 и IL-13, которые вызывают активацию B-клеток и переключение класса IgE. Антитела IgE связываются с поверхностными рецепторами FcεRI, присутствующими на тучных клетках и базофилах, которые приводят к дегрануляции и высвобождению нескольких медиаторов аллергии. Эти аллергические медиаторы, вероятно, вызывают активацию трипсиногена и развитие панкреатита. Однако эта гипотеза требует дальнейшего изучения для разработки стратегии лечения.Напротив, может также возникать не-IgE-опосредованная реакция, которая включает в себя роль активных хемокинов IL-5 и эозинофилов, эотаксинов, которые привлекают, активируют и высвобождают несколько медиаторов воспаления и приводят к активации трипсиногена. Повышенный уровень трипсина последовательно запускает эпизод острого панкреатита. Кроме того, нейтрофилы образуют нейтрофильные внеклеточные ловушки (NET) деконденсированной ДНК и гистонов, которых достаточно, чтобы вызвать активацию трипсина и способствовать патогенезу панкреатита.
Существуют пробелы в знаниях между острым панкреатитом, вызванным пищевыми продуктами, и патогенезом панкреатита. . Панкреатит – смертельное заболевание со значительной заболеваемостью и смертностью. Хотя острый панкреатит, вызванный пищевыми продуктами, является редким заболеванием, четкое понимание острого панкреатита, связанного с пищевыми продуктами, с этим заболеванием должно насторожить врача, чтобы он мог надлежащим образом диагностировать и лечить этих пациентов с острым панкреатитом, пораженным пищевыми продуктами.Дальнейшие исследования должны быть выполнены для понимания молекулярных механизмов острого панкреатита, вызванного пищевыми продуктами, и его клинических последствий. Кроме того, оценка аллергологом и гастроэнтерологом пищевых продуктов, обычно связанных с состоянием панкреатита, поможет установить более ранний диагноз. Ранняя диагностика может облегчить и ускорить прекращение неприятной пищи, тем самым уменьшив количество осложнений и продолжительность пребывания в больнице.
Усилия, необходимые для установления панкреатита, вызванного пищевыми аллергенами
В настоящее время очень мало сообщений о случаях причастности пищевых аллергенов к индукции панкреатита; Следовательно, медицинскому сообществу необходимо приложить больше усилий для выявления пищи, вызывающей острый панкреатит, и лучшего понимания механистических аспектов панкреатита, опосредованного пищевыми продуктами.Кроме того, необходимо тесное сотрудничество между аллергологом и гастроэнтерологом для диагностики и понимания патогенеза пищевого панкреатита путем разработки новых и эффективных подходов, таких как идентификация определенного типа пищевого аллергена для конкретного пациента.
Лечение острого панкреатита, вызванного пищевыми продуктами
Панкреатит, вызванный пищевой аллергией, можно вылечить путем исключения определенных диетических аллергенов; избегая определенного типа пищи. «Nil per Os» – это первая линия лечения наряду с агрессивной гидратацией, которая помогает поджелудочной железе отдохнуть и восстановиться [24, 26].В зависимости от основной причины панкреатита варианты лечения могут различаться в зависимости от конкретной причины. При необходимости можно использовать анальгетики и противорвотные средства. Кромоглициевая кислота (стабилизатор тучных клеток) и кортикостероиды часто используются для лечения острого панкреатита, вызванного пищевыми продуктами [12, 24, 26]. Кроме того, использование терапии микронутриентами, включая несколько витаминов, метионин и β-каротин, дает очень многообещающие результаты при лечении хронического панкреатита. В одном исследовании микронутриентная терапия была приготовлена другим способом для обеспечения метиловых и тиоловых фрагментов, которые ограничивают образование активных форм кислорода, деактивируют провоспалительные реакции и предотвращают дегрануляцию тучных клеток [51].Следовательно, препараты, стабилизирующие тучные клетки, могут стать вариантом лечения пищевого панкреатита в будущем.
Заключение
В настоящем обзоре дается всестороннее понимание механизмов пищевой аллергии и связанных с ней расстройств, включая акцент на панкреатите, вызванном пищевыми продуктами. Острый или хронический панкреатит, вызванный пищевыми продуктами, представляет собой проблему для научного сообщества, поскольку его патогенез до сих пор не ясен и как происходит развитие / прогрессирование заболевания с помощью иммунных компонентов, активируемых пищевым антигеном.Однако литературы о влиянии пищи на индукцию панкреатита очень мало. В этом обзоре мы обобщили имеющиеся отчеты о случаях панкреатита, связанного с пищевой аллергией, и его возможные механизмы. Наш обзор литературы побуждает к дальнейшим размышлениям в этом направлении, и будет интересно узнать, как и почему определенные продукты вызывают панкреатит у некоторых восприимчивых людей. Улучшение клинических исходов для пациентов остается в центре внимания обширных фундаментальных научных и клинических исследований, и многие из текущих проблем, связанных с панкреатитом, вызванным пищевыми продуктами, особенно актуальны для клинических биохимиков и поставщиков медицинских услуг.Существует необходимость в дальнейших исследованиях в этой области пищевого панкреатита, и мы настоятельно рекомендуем не игнорировать пищевой панкреатит и обследовать пациентов у аллерголога. Поэтому мы призываем клиницистов проявлять особую бдительность в отношении панкреатита, вызванного пищевыми продуктами, особенно у пациентов, у которых диагностирован идиопатический панкреатит. Расширенный диетический анамнез, включая недавно употребленные продукты, вызывающие симптомы, может привести врачей к диагнозу пищевого панкреатита.
Благодарности
Д-р Мишра – председатель совета директоров Schlieder; поэтому авторы благодарят Образовательный фонд Эдварда Г. Шлидера за поддержку.
Сноски
Конфликт интересов
Все авторы заявляют об отсутствии конфликта интересов.
Ссылки
1. Стоун К.Д., Пруссин С., Меткалф Д.Д. IgE, тучные клетки, базофилы и эозинофилы. J Allergy Clin Immunol. 2010; 125 (2 приложение 2): S73–80. [Бесплатная статья PMC] [PubMed] [Google Scholar] 2.Шукла А., М.А., Венкатешайа С.У., Манхоар М., Махадеваппа С.П., Мишра А. Элементы, участвующие в развитии эозинофильных желудочно-кишечных расстройств. J Genet Syndr Gene Ther. 2015; 6: 265. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Verma AK, MMUVSU, Blecker U, Collins MH, Mishra A. Роль вазоактивного кишечного пептида в продвижении патогенеза эозинофильного эзофагита (EoE) Cell Mol Gastroenterol Hepatol. 2017 сен; Принято, статья в печати. [Бесплатная статья PMC] [PubMed] [Google Scholar] 4. Верма А.К., Манохар М., УВС, Мишра А.Эндокринные клетки, производные хемокинового вазоактивного кишечного полипептида (VIP) при аллергических заболеваниях. Cytokine Growth Factor Rev.2017 Сентябрь; В прессе. [Бесплатная статья PMC] [PubMed] 5. Каттан Дж. Распространенность и естественная история пищевой аллергии. Curr Allergy Asthma Rep.2016; 16 (7): 47. [PubMed] [Google Scholar] 8. Вулф Дж. Л., Асевес СС. Желудочно-кишечные проявления пищевой аллергии. Pediatr Clin North Am. 2011. 58 (2): 389–405. Икс. [PubMed] [Google Scholar] 9. Verma AK, et al. Комплексный обзор аллергии на бобовые.Clin Rev Allergy Immunol. 2013. 45 (1): 30–46. [PubMed] [Google Scholar] 10. Inamura H, et al. Острый панкреатит, возможно, вызванный аллергией на бананы. J Исследование Allergol Clin Immunol. 2005. 15 (3): 222–4. [PubMed] [Google Scholar] 11. Flejou JF, Potet F, Bernades P. Эозинофильный панкреатит: редкое проявление пищеварительной аллергии? Гастроэнтерол Clin Biol. 1989. 13 (8–9): 731–3. [PubMed] [Google Scholar] 12. Маттео А., Сарлес Х. Является ли пищевая аллергия причиной острого панкреатита? Поджелудочная железа. 1990; 5 (2): 234–7.[PubMed] [Google Scholar] 13. де Диего Лоренцо А. и др. Острый панкреатит, связанный с аллергией на молоко. Int J Pancreatol. 1992. 12 (3): 319–21. [PubMed] [Google Scholar] 14. Ивата Ф., Одадзима Ю. Острый панкреатит, связанный с пищевой аллергией. Eur J Pediatr. 1997; 156 (6): 506. [PubMed] [Google Scholar] 17. Манохар М., В.А., Венкатешайя С.У., Сандерс Н.Л., Мишра А. Острая респираторная недостаточность, связанная с хроническим панкреатитом. Минюст иммунологии. 2017; 5 (2): 1–7. [Google Scholar] 19. Ян А.Л. и др. Эпидемиология связанных с алкоголем заболеваний печени и поджелудочной железы в США.Arch Intern Med. 2008. 168 (6): 649–56. [PubMed] [Google Scholar] 20. Hirota M, et al. Шестое общенациональное эпидемиологическое исследование хронического панкреатита в Японии. Панкреатология. 2012. 12 (2): 79–84. [PubMed] [Google Scholar] 21. Couvelaire RBD. Quelques résultats expérimentaux sur la génèse des oedèmes aigus et des hémorragies pancréatiques. Les pancréatites anaphylactiques. CR Soc Biol. 1933; 11: 1435–1437. [Google Scholar] 22. Каррильо Т., А.М., Гусман Т.М., Виларделл В.Ю., Гойри И.М. Панкреатит более сложный, чем анафилаксия.Rev Esp Alergol Immunol Clin. 1987; 2: 388–390. [Google Scholar] 23. Suzuki S и др. Эозинофильный гастроэнтерит, вызванный аллергией на коровье молоко, проявляющийся острым панкреатитом. Int Arch Allergy Immunol. 2012; 158 (Дополнение 1): 75–82. [PubMed] [Google Scholar] 24. Це К.Ю., Кристиансен СК. Эозинофильный гастроэнтерит, вызванный аллергией на яйца, проявляющейся как острый панкреатит. Allergy Rhinol (Providence) 2015; 6 (1): 80–1. [Бесплатная статья PMC] [PubMed] [Google Scholar] 25. Пеллегрино К. и др. Тяжелая реакция у ребенка с бессимптомной аллергией на треску: проблема с едой, реактивирующая рецидивирующий панкреатит.Ital J Pediatr. 2012; 38: 16. [Бесплатная статья PMC] [PubMed] [Google Scholar] 26. Gastaminza G, Bernaola G, Camino ME. Острый панкреатит, вызванный аллергией на киви. Аллергия. 1998. 53 (11): 1104–5. [PubMed] [Google Scholar] 27. Оскарссон В. и др. Высокая гликемическая нагрузка в питании увеличивает риск острого панкреатита, не связанного с желчнокаменной болезнью: проспективное когортное исследование. Clin Gastroenterol Hepatol. 2014. 12 (4): 676–82. [PubMed] [Google Scholar] 28. Setiawan VW и др. Факторы питания снижают риск острого панкреатита в большой многонациональной когорте.Clin Gastroenterol Hepatol. 2017; 15 (2): 257–265 e3. [Бесплатная статья PMC] [PubMed] [Google Scholar] 29. Оскарссон В. и др. Овощи, фрукты и риск острого панкреатита, не связанного с желчнокаменной болезнью: популяционное проспективное когортное исследование. Кишечник. 2013; 62 (8): 1187–92. [PubMed] [Google Scholar] 30. Оскарссон В. и др. Потребление рыбы и риск острого панкреатита, не связанного с желчнокаменной болезнью: проспективное когортное исследование. Am J Clin Nutr. 2015; 101 (1): 72–8. [PubMed] [Google Scholar] 31. Ho MH, Wong WH, Chang C. Клинический спектр пищевых аллергий: всесторонний обзор.Clin Rev Allergy Immunol. 2014. 46 (3): 225–40. [PubMed] [Google Scholar] 32. Босолей Дж. Л., Фидлер Дж., Спергель Дж. М.. Пищевая непереносимость и детская астма: какая связь? Педиатрические препараты. 2007. 9 (3): 157–63. [PubMed] [Google Scholar] 34. Brandt EB, et al. Экспериментальная желудочно-кишечная аллергия усиливает реакцию легких на специфические и неродственные аллергены. J Allergy Clin Immunol. 2006. 118 (2): 420–7. [PubMed] [Google Scholar] 35. Чо К.А. и др. IL-33 вызывает Th27-опосредованное воспаление дыхательных путей через тучные клетки у мышей, зараженных овальбумином.Am J Physiol Lung Cell Mol Physiol. 2012; 302 (4): L429–40. [PubMed] [Google Scholar] 36. Bihouée T, BG, Chesné J, Lair D, Rolland-Debord C, Braza F, Cheminant MA, Aubert P, Mahay G, Sagan C, Neunlist M, Brouard S, Bodinier M, Magnan A. Пищевая аллергия усиливает аллергическую астму у мышей . Respir Res. 2014; 30 (15): 142. [Бесплатная статья PMC] [PubMed] [Google Scholar] 37. Тарик С.М. и др. Аллергия на яйца в младенчестве предсказывает респираторное аллергическое заболевание к 4 годам. Pediatr Allergy Immunol. 2000. 11 (3): 162–7. [PubMed] [Google Scholar] 38.Джеймс Дж. М., Бернхизел-Бродбент Дж., Сэмпсон ГА. Респираторные реакции, вызванные двойным слепым приемом пищи у детей. Am J Respir Crit Care Med. 1994. 149 (1): 59–64. [PubMed] [Google Scholar] 39. Torpier G, et al. Эозинофильный гастроэнтерит: ультраструктурные доказательства избирательного высвобождения основного основного белка эозинофилов. Clin Exp Immunol. 1988. 74 (3): 404–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 40. Мишра А. и др. Основные сигналы, регулирующие возвращение эозинофилов в желудочно-кишечный тракт.J Clin Invest. 1999. 103 (12): 1719–27. [Бесплатная статья PMC] [PubMed] [Google Scholar] 41. Uppal V, Kreiger P, Kutsch E. Эозинофильный гастроэнтерит и колит: всесторонний обзор. Clin Rev Allergy Immunol. 2016; 50 (2): 175–88. [PubMed] [Google Scholar] 42. Хан С, Оренштейн СР. Эозинофильный гастроэнтерит: эпидемиология, диагностика и лечение. Педиатрические препараты. 2002. 4 (9): 563–70. [PubMed] [Google Scholar] 43. Альфадда А.А., Сторр М.А., Шаффер Е.А. Эозинофильный колит: эпидемиология, клинические особенности и текущее лечение.Therap Adv Гастроэнтерол. 2011; 4 (5): 301–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 44. Jaffe JS и др. Доказательства аномального профиля интерлейкина-4 (IL-4), IL-5 и гамма-интерферона (гамма-IFN) в Т-клетках периферической крови пациентов с аллергическим эозинофильным гастроэнтеритом. J Clin Immunol. 1994. 14 (5): 299–309. [PubMed] [Google Scholar] 45. Эль-Музан М.И., Аль-Куорайн А.А., Anim JT. Эрозивный гастрит у грудного ребенка, вызванный коровьим молоком. J Pediatr Gastroenterol Nutr. 1990. 10 (1): 111–3. [PubMed] [Google Scholar] 46.Bischoff SC. Пищевая аллергия и эозинофильный гастроэнтерит и колит. Curr Opin Allergy Clin Immunol. 2010. 10 (3): 238–45. [PubMed] [Google Scholar] 47. Валле-Дорадо М.Г. и др. Стабилизатор тучных клеток кромогликат натрия снижает высвобождение гистамина и вызванное эпилептическим статусом повреждение нейронов в гиппокампе крыс. Нейрофармакология. 2015; 92: 49–55. [PubMed] [Google Scholar] 48. Васкес Родригес Дж. Дж. И др. Панкреатит и эозинофильный гастроэнтерит. Int Surg. 1973; 58 (6): 415–9. [PubMed] [Google Scholar] 49.Caglar E, Karismaz K, Dobrucali A. Случай эозинофильного гастроэнтерита, имитирующего лимфому желудка, связанный с панкреатитом из-за поражения двенадцатиперстной кишки. Turk J Gastroenterol. 2012; 23 (5): 585–9. [PubMed] [Google Scholar] 50. Goyal H, et al. Различия в степени тяжести и исходах между гипертриглицеридемией и алкогольным панкреатитом. N Am J Med Sci. 2016; 8 (2): 82–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Браганса JM, Дорманди TL. Микронутриентная терапия хронического панкреатита: обоснование и влияние.JOP. 2010. 11 (2): 99–112. [PubMed] [Google Scholar] 52. Эспозито I и др. Распределение и активация тучных клеток при хроническом панкреатите. Hum Pathol. 2001. 32 (11): 1174–83. [PubMed] [Google Scholar] 53. Kweon MN, et al. Системно полученные CD4 (+) Th3-клетки толстого кишечника играют центральную роль в STAT6-опосредованной аллергической диарее. J Clin Invest. 2000. 106 (2): 199–206. [Бесплатная статья PMC] [PubMed] [Google Scholar] 54. Меткалф Д.Д., Пиви Р.Д., Гилфиллан А.М. Механизмы передачи сигналов тучными клетками при анафилаксии. J Allergy Clin Immunol.2009. 124 (4): 639–46. викторина 647–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 55. Knol EF. Требования к эффективному сшиванию IgE на тучных клетках и базофилах. Mol Nutr Food Res. 2006. 50 (7): 620–4. [PubMed] [Google Scholar] 56. Raithel M, et al. Продукция иммуноглобулина Е при хроническом панкреатите. Eur J Gastroenterol Hepatol. 2003. 15 (7): 801–7. [PubMed] [Google Scholar] 57. Raithel M, et al. Стимуляция образования иммуноглобулина Е при хроническом панкреатите алкоголем и внешнесекреторной недостаточностью поджелудочной железы.З. Гастроэнтерол. 2001. 39 (4): 269–76. [PubMed] [Google Scholar] 58. Jyonouchi H. Не-IgE-опосредованная пищевая аллергия – последние сведения о последних достижениях иммунитета слизистых оболочек. Цели лекарств от аллергии на воспаление. 2012. 11 (5): 382–96. [PubMed] [Google Scholar] 59. Caubet JC, et al. Не IgE-опосредованные желудочно-кишечные пищевые аллергии у детей. Pediatr Allergy Immunol. 2016 [PubMed] [Google Scholar] 61. Кумар С. В., Дас М., Двиведи П. Д.. Аллергенное разнообразие пищевых белков растений и животных. Food Reviews International. 2011. 28 (3): 277–298.[Google Scholar] 62. Манохар М., В.А., Венкатешайя С.У., Мишра А. Иммунологические реакции, участвующие в развитии острого и хронического панкреатита. J Clin Immunol Res. 2017; 1: 1–8. [Google Scholar] 63. Воутерс М.М., Викарио М., Сантос Дж. Роль тучных клеток в функциональных расстройствах желудочно-кишечного тракта. Кишечник. 2016; 65 (1): 155–68. [PubMed] [Google Scholar] 64. Галли SJ, Grimbaldeston M, Tsai M. Иммуномодулирующие тучные клетки: как отрицательные, так и положительные регуляторы иммунитета. Nat Rev Immunol. 2008. 8 (6): 478–86. [Бесплатная статья PMC] [PubMed] [Google Scholar] 65.Краневельд А.Д. и др. Две стороны тучных клеток при пищевой аллергии и аллергической астме: возможная концепция Инь-Ян. Biochim Biophys Acta. 2012; 1822 (1): 93–9. [PubMed] [Google Scholar] 66. Braganza JM. Тучная клетка: ключевой игрок в лечении острого панкреатита со смертельным исходом. QJM. 2000. 93 (7): 469–76. [PubMed] [Google Scholar] 68. Диб М. и др. Роль тучных клеток в развитии полиорганной дисфункции, вызванной панкреатитом. Br J Surg. 2002. 89 (2): 172–8. [PubMed] [Google Scholar] 69. Масато Янагава К.Ю., Икемунэ Манами, Икеура Цукаса, Шиматани Масааки, Фукуи Тоширо, Такаока Макото, Нишио Акиёси, Сатои Сохей, Окадзаки Кадзуичи.Роль базофилов через передачу сигналов TLR у пациентов с аутоиммунным панкреатитом 1 типа. Панкреатология. 2016; 16 (4): S 40. [Google Scholar] 70. Стеллато С. и др. Производство нового хемокина C-C MCP-4 клетками дыхательных путей и сравнение его биологической активности с другими хемокинами C-C. J Clin Invest. 1997. 99 (5): 926–36. [Бесплатная статья PMC] [PubMed] [Google Scholar] 71. Маэшима А. и др. Эозинофильный гастроэнтерит с острым панкреатитом. J Med. 1997. 28 (3–4): 265–72. [PubMed] [Google Scholar] 72.Манохар М., ВАК, Венкатешайя С.У., Мишра А. Роль эозинофилов в инициации и прогрессировании патогенеза панкреатита. Am J Physiol Gastrointest Liver Physiol. 2017 сен 19; Принято, статья в печати. [Бесплатная статья PMC] [PubMed] [Google Scholar] 73. Wallaert B, et al. Воспаление нейтрофилов дыхательных путей у неастматических пациентов с пищевой аллергией. Аллергия. 2002. 57 (5): 405–10. [PubMed] [Google Scholar] 74. Merza M, et al. Внеклеточные ловушки нейтрофилов вызывают активацию трипсина, воспаление и повреждение тканей у мышей с тяжелым острым панкреатитом.Гастроэнтерология. 2015; 149 (7): 1920–1931 e8. [PubMed] [Google Scholar] 75. Ян З.В., Мэн XX, Сюй П. Центральная роль нейтрофилов в патогенезе тяжелого острого панкреатита. J Cell Mol Med. 2015; 19 (11): 2513–20. [Бесплатная статья PMC] [PubMed] [Google Scholar] 76. Муньос-Кано Р. и др. Механизмы анафилаксии помимо IgE. J Исследование Allergol Clin Immunol. 2016; 26 (2): 73–82. викторина 2p после 83. [PubMed] [Google Scholar] 77. Хан Дж. И др. Нейтрофилы и внеклеточные ловушки нейтрофилов организуют инициирование и разрешение воспаления.Clin Exp Rheumatol. 2016; 34 (4 Suppl 98): 6–8. [PubMed] [Google Scholar] 78. Demols A, et al. CD4 (+) Т-клетки играют важную роль в остром экспериментальном панкреатите у мышей. Гастроэнтерология. 2000. 118 (3): 582–90. [PubMed] [Google Scholar] 79. Vonlaufen A, et al. Роль воспалительных и паренхиматозных клеток при остром панкреатите. J Pathol. 2007. 213 (3): 239–48. [PubMed] [Google Scholar] 80. Ямада Т. и др. Роль Т-клеток в развитии хронического панкреатита у самцов крыс Wistar Bonn / Kobori: эффекты такролимуса.Am J Physiol Gastrointest Liver Physiol. 2001; 281 (6): G1397–404. [PubMed] [Google Scholar] 81. Frossard JL, et al. Мыши с дефицитом лиганда Cd40 защищены от церулеин-индуцированного острого панкреатита и связанного с панкреатитом повреждения легких. Гастроэнтерология. 2001. 121 (1): 184–94. [PubMed] [Google Scholar] 82. Паломарес О. Роль регуляторных Т-клеток в IgE-опосредованной пищевой аллергии. J Исследование Allergol Clin Immunol. 2013. 23 (6): 371–82. quiz 2 p перед 382. [PubMed] [Google Scholar] 83. Эйгенманн П.А., Фроссар С.П.Т-лимфоциты при расстройствах пищевой аллергии. Curr Opin Allergy Clin Immunol. 2003. 3 (3): 199–203. [PubMed] [Google Scholar]Острый панкреатит, вызванный пищевыми продуктами
Dig Dis Sci. Авторская рукопись; доступно в PMC 1 декабря 2018 г.
Опубликован в окончательной редакции как:
PMCID: PMC5718054
NIHMSID: NIHMS
4
, Ph.D, 1, $ , Ph.D, 1, $ , к.т.н., 1 , д.м.н., 2 и, к.т.н. 1, *Мурли Манохар
1 Департамент медицины, отделение легочных заболеваний, Центр эозинофильных заболеваний Тулейна, Школа медицины Тулейнского университета, Новый Орлеан, Лос-Анджелес, 70112, США
Алок К.Verma
1 Департамент медицины, Отделение легочных заболеваний, Центр эозинофильных заболеваний Тулейна, Медицинский факультет Тулейнского университета, Новый Орлеан, Лос-Анджелес, 70112, США
Сатиша Уппарахалли Венкатешайя
1 Департамент медицины, Отделение легочных заболеваний, Центр эозинофильных заболеваний Тулейна, Медицинский факультет Тулейнского университета, Новый Орлеан, Лос-Анджелес 70112, США
Хемант Гоял
2 Кафедра внутренней медицины, Медицинский факультет Университета Мерсер, 707 Pine St.Macon, GA 31201
Анил Мишра
1 Департамент медицины, Отделение легочных заболеваний, Тулейнский центр эозинофильных расстройств, Школа медицины Тулейнского университета, Новый Орлеан, Лос-Анджелес 70112, США
1 Департамент медицины, Отделение легочных заболеваний, Тулейнский центр эозинофильных расстройств, Школа медицины Тулейнского университета, Новый Орлеан, Лос-Анджелес 70112, США
2 Кафедра внутренней медицины, Медицинский факультет Университета Мерсер, 707 Pine St.Macon, GA 31201
* Автор, ответственный за переписку: Анил Мишра, доктор философии, заведующий кафедрой Шлидера, профессор и директор Тулейнского центра эозинофильных расстройств, департамент медицины, отделение легочной медицины, Медицинская школа Тулейнского университета, Новый Орлеан, LA 70112 , США. Тел: 504-988-3840; Факс: 504-988-2144; ude.enalut@arhsima$ Авторы внесли одинаковый вклад: Мурли Манохар, Алок К. Верма
Окончательная отредактированная версия этой статьи издателем доступна на Dig Dis SciSee, другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
Пищевая аллергия – широко распространенная во всем мире проблема, определяемая как неблагоприятный иммунный ответ на пищу. Множество связанных с иммунитетом эффекторных клеток, таких как тучные клетки, эозинофилы, нейтрофилы и Т-клетки, участвуют в пищевых аллергических ответах, которые классифицируются как IgE-опосредованные, не-IgE-опосредованные и смешанные (IgE и не-IgE) в зависимости от основные иммунологические механизмы. Пищевые антигены в основном нацелены на желудочно-кишечный тракт, включая поджелудочную железу, которая воспаляется из-за пищевой аллергии и приводит к острому панкреатиту.Отчеты показывают, что некоторые пищевые белки вызывают панкреатит; однако подробный механизм, лежащий в основе панкреатита, вызванного пищевыми продуктами, не изучен. Цель обзора – понять и обновить текущий сценарий пищевого панкреатита. Через PubMed был проведен всесторонний поиск литературы по соответствующим исследовательским статьям, и статьи были выбраны на основе их актуальности для панкреатита, опосредованного пищевыми аллергенами. Несколько случаев в литературе, указывающих на то, что острый панкреатит был спровоцирован после употребления горчицы, молока, яиц, бананов, рыбы и киви.Панкреатит, вызванный пищевыми продуктами, – это игнорируемая и неизученная область исследований. В обзоре подчеркивается значение пищи в развитии панкреатита и обращается внимание врачей и ученых на то, чтобы рассматривать пищевую аллергию как возможную причину инициирования патогенеза панкреатита.
Ключевые слова: Пищевая аллергия, панкреатит, эозинофилы, тучные клетки, нейтрофилы
Введение
Растущая распространенность аллергических заболеваний является тревожной проблемой во всем мире, и пищевые аллергены вносят основной вклад в развитие аллергических проявлений, включая желудочно-кишечные расстройства [ 1–4] Распространенность пищевой аллергии оценивается примерно в 3–8%, и она значительно влияет на качество жизни восприимчивых людей [5].Пищевая аллергия может быть определена как провокация неблагоприятной аллергической реакции на безвредные пищевые антигены из-за чрезмерной реакции иммунной системы на эти пищевые антигены. Признаки и симптомы пищевой аллергии могут варьироваться от легкой до тяжелой и могут включать рвоту, диарею, крапивницу, зуд, отек языка, низкое кровяное давление и затрудненное дыхание [6]. Аллергические реакции, вызванные пищевыми продуктами, обычно возникают в течение от нескольких минут до нескольких часов после воздействия, а при тяжелых симптомах они могут вызвать тяжелую анафилаксию [7].Чрезмерная реакция иммунной системы организма на пищевые антигены может поражать несколько органов, включая дыхательные и желудочно-кишечные (ЖКТ) тракты, что приводит к развитию обострения астмы, дыхательной недостаточности, эзофагита и гастроэнтерита [2, 8, 9]. аллергия считается одной из причин, способствующих развитию острого панкреатита [10–14]. Панкреатит характеризуется острым или хроническим воспалением, которое может быть вызвано различными вредными раздражителями, такими как камни в желчном пузыре, алкоголь и мутация в гене трипсиногена [15–17].Ежегодная заболеваемость острым и хроническим панкреатитом колеблется от 13 до 45 и от 4,4 до 11,9 на 100 000 человек в США соответственно [15, 18]. Более того, различные сообщения указывают на повышенную заболеваемость панкреатитом среди населения Японии по сравнению с США [15, 19, 20]. К сожалению, в текущем сценарии распространенность острого или хронического панкреатита, вызванного пищевыми продуктами, все еще недостаточно хорошо известна. С 1933 г. известно, что пищевая аллергия является причиной острого панкреатита у собак [21]; кроме того, несколько случаев острого панкреатита у человека, вызванного аллергией на горчицу [22], молоко [13, 23], икру трески [14], яйца [24], бананы [10], рыбу [25] и киви [ 26] описаны в литературе.Несколько исследований показывают, что высокая гликемическая нагрузка [27], жир, мясо, яйца и т. Д. [28] связаны с риском острого панкреатита, не связанного с желчнокаменной болезнью. В то время как другие исследования сообщают, что овощи и рыба (включая жирную и нежирную рыбу) могут быть связаны со снижением риска нежечнокаменного острого панкреатита [29, 30]. Все эти исследования показывают, что определенные продукты связаны с повышенным риском острого панкреатита, в то время как другие продукты могут быть защитными.
Согласно клиническим данным и тестам на аллергию, известны три типа пищевых аллергий: опосредованные IgE (немедленный тип, гиперчувствительность I типа), не опосредованные IgE (замедленный тип, клеточная гиперчувствительность, гиперчувствительность IV типа) и смешанные (IgE / Non-IgE) [31], но в случае пищевого панкреатита механизм неизвестен, и эта область исследований игнорируется и остается неизученной.В этом обзоре мы стремимся предоставить текущую информацию, касающуюся пищевых аллергических реакций, с особым акцентом на панкреатит, вызванный пищевыми продуктами. Текущий обзор также предоставляет исследователям и врачам платформу для понимания участия различных типов эффекторных иммунных клеток, а также действующих молекулярных механизмов, которые могут проложить путь к новым методам лечения панкреатита, вызванного пищевыми продуктами.
Аллергические расстройства, вызванные пищевыми продуктами
Аллергические расстройства, вызванные пищевыми продуктами, растут во всем мире, и некоторые продукты питания были отмечены как фактор риска развития аллергических заболеваний [32].Пищевая аллергия в основном связана с увеличением цитокинов Th3, эозинофилов и тучных клеток в ответ на аллергены [33–36]. Пищевая аллергия сообщается при нескольких аллергических заболеваниях, включая астму [33–35], аллергический ринит [37, 38], желудочно-кишечные расстройства, такие как эозинофильный гастроэнтерит [2, 39] и панкреатит [23, 24]. Здесь мы суммировали текущее понимание и имеющиеся данные о развитии эозинофильного гастроэнтерита-зависимого и независимого панкреатита.
Эозинофильный гастроэнтерит и панкреатит, вызванный пищевыми аллергенами
Эозинофильный гастроэнтерит (ЭГ) – это воспалительное заболевание, опосредованное эозинофилами, которое характеризуется инфильтрацией эозинофилов в желудке, тонком и толстом кишечнике [2, 39]. Базовые эозинофилы обычно присутствуют в желудочно-кишечном тракте [40]; но увеличение их количества наблюдалось в ответ на несколько раздражителей, таких как повреждение тканей и инфекции, включая пищевые аллергены.Эти накопленные эозинофилы активируются, что приводит к дальнейшей дегрануляции и секреции различных цитокинов, которые приводят к развитию EG [41]. Примечательно, что данные указывают на то, что 50–75% пациентов с ЭГ имеют в личном или семейном анамнезе сопутствующие аллергии или атопические расстройства [42, 43]. Было высказано предположение, что пищевая аллергия способствует стимулированию ЭГ у этих пациентов, а увеличение общего IgE и пищевого специфического IgE свидетельствует о пищевой аллергии в стимулировании ЭГ у пациентов [44]. Сообщалось, что коровье молоко вызывает эрозивный гастрит, и его исключение из рациона показало исчезновение аллергических симптомов у младенцев [45].Некоторые данные свидетельствуют о том, что пищевые антигены играют решающую роль в патогенезе эозинофильного гастроэнтерита, а также колита [46].
Впервые о пищевой аллергии и ее связи с панкреатитом сообщили в 1933 году Couvelaire и Bargeton [21], продемонстрировав экспериментальный анафилактический шок, вызванный пищевыми аллергенами, у собак. Несколько сообщений о случаях острого панкреатита, спровоцированного пищевой аллергией на горчицу [22], молоко [13, 23], яйца [24], бананы [10], рыбу [25] и киви [26], у человека были опубликованы в литература.Также сообщалось о хроническом панкреатите, сохраняющемся от 8 до 10 лет из-за употребления различных видов пищи, таких как говядина, молоко, картофель, рыба и яйца [12]. Основные симптомы этих пациентов включают острую боль в животе и повышение уровня ферментов поджелудочной железы в сыворотке крови. Однако результаты ультразвукового исследования брюшной полости и компьютерной томографии выявили отечность поджелудочной железы только у одного пациента. Уровень IgE в сыворотке был повышен у одного пациента [12]. Этих пациентов лечили путем прекращения приема провоцирующей пищи (говядины, молока, картофеля, рыбы и яиц) и одновременно с приемом препарата кромогликат, стабилизатора тучных клеток [47], который предотвращает высвобождение гистамина из тучных клеток.Также сообщалось о случае острого панкреатита, связанного с молоком, у 23-летнего пациента с повторяющимися эпизодами боли в животе, повышенными уровнями амилазы, липазы, сывороточного IgE, бета-лактоглобулина и увеличенной поджелудочной железой в ультразвуковом отчете. У пациента были рецидивирующие эпизоды острого панкреатита, сопровождавшиеся эритемой лица с инъекцией конъюнктивы, генерализованным зудом, диареей и эозинофилией после употребления молока [13]. Inamura et al. [10] опубликовали случай рецидивирующего острого панкреатита (три эпизода), вызванного аллергией на бананы, у 47-летней женщины с аллергическим ринитом в анамнезе.Пациент лечился консервативно, с легкой диетой и внутривенным введением жидкости, с исчезновением клинических симптомов в течение нескольких дней. Кроме того, повышенные уровни амилазы вернулись к нормальным значениям параллельно с клиническими симптомами. Общий уровень IgE в сыворотке составлял 644 МЕ / мл, при этом уровень специфического IgE к бананам составлял 2,18 UA / мл, что свидетельствует о значительной аллергии на бананы. Gastaminza et al. [26] представили клинический случай острого панкреатита, развившегося после употребления киви у 48-летнего мужчины с язвой двенадцатиперстной кишки и кровотечением из верхних отделов желудочно-кишечного тракта в анамнезе.Этот пациент также имел в анамнезе ринит, бронхиальную астму и аллергию на пиразолоны. Сообщалось о повышении уровня амилазы и лейкоцитоза в сыворотке крови на 835 Ед / л (N = 60–190) и 13 000 / мм 2 соответственно. Примечательно, что после 48 часов лечения легкой диетой, внутривенными жидкостями, антацидами и анальгетиками; уровни амилазы и липазы в сыворотке вернулись к норме. Поскольку пациент умеренно пил, у него изначально был диагностирован алкогольный панкреатит, но примерно через две недели он перенес еще один эпизод панкреатита после употребления в пищу киви.Позже прокол показал аллергию на киви, и ему поставили диагноз панкреатит, вызванный фруктами киви. Согласно отчету, после отказа от употребления киви в течение последних пяти лет пациент больше не страдал панкреатитом. Сводка каждого из этих отчетов о случаях острого панкреатита, связанного с пищевыми продуктами, представлена в. Более того, несколько крупных многонациональных когортных исследований показали, что высокая гликемическая нагрузка, насыщенные жиры, холестерин, красное мясо и яйца повышают риск острого панкреатита, не связанного с желчнокаменной болезнью [27, 28]; Напротив, недавние отчеты показали, что потребление овощей и рыбы (жирной и нежирной рыбы вместе) может быть связано со снижением риска нежечнокаменного острого панкреатита [29, 30].Резюме проспективных когортных исследований, связанных с острым панкреатитом, вызванным пищевыми продуктами, у человека было представлено в.
Таблица 1
Обобщенные детали отчетов о случаях острого панкреатита, вызванного пищевыми аллергенами
| S. No. | Возраст (год) | Пол | Аллергическая пища | Симптомы | s) | IgE | Другие ассоциированные заболевания | Список литературы | |
|---|---|---|---|---|---|---|---|---|---|
| 1. | 26 | F | NA | Боль в животе, аллергические симптомы | Эозинофилы | Повышенный уровень IgE в сыворотке | EP | [11] | |
| 2. | M | Говядина (дважды) Молоко Картофель Рыба Яйцо | Боль в животе, Мигрень, Зуд, Повышенная амилаза в сыворотке крови, Боль в эпигастрии, связанная с диффузной головной болью | Нормальный уровень эозинофилов | Повышенный уровень IgE 9026 у одного пациента NA | [12] | |||
| 3. | 23 | NA | Молоко | Боль в животе, эритема лица с инъекцией конъюнктивы, генерализованный зуд, диарея, эозинофилия, повышенные уровни ферментов поджелудочной железы в сыворотке крови, увеличение поджелудочной железы и отек | на сонограмме | Уровень IgE | NA | [13] | |
| 4. | 48 | M | Киви | Боль в эпигастрии, рвота, диарея, эритема лица, зуд, повышение сывороточного уровня | Повышенный уровень сывороточного аминофосфата | общий IgE 257 мкл / мл | Язвенная болезнь двенадцатиперстной кишки в анамнезе, кровотечение из верхних отделов пищеварительного тракта, аллергия на пиразолоны, ринит и бронхиальная астма | [26] | |
| 5. | 47 | F | Банан | Эпигастралгия, Тошнота, Рвота, Диарея, Повышенный уровень амилазы в сыворотке и моче, Ампула Фатера опухшая и отечная | Повышение 64 Тучных клеток, Общее количество IUE в сыворотке | увеличено и специфический IgE к бананам (2,18 UA / мл) | NA | [10] | |
| 6. | – | M | Молоко | Симптомы ЭГ, такие как тошнота, рвота, боль в животе, диспепсия, Нарушение всасывания, асцит и потеря веса, повышение ферментов поджелудочной железы в сыворотке и общий билирубин | Повышение эозинофилов | – | EG | [23] | |
| 7. | 8 | M | треска | Анафилактическая реакция, Боль в животе, Повышенный уровень ферментов поджелудочной железы в сыворотке крови, Паренхиматозный отек при УЗИ | NA | Специфический IgE для трески = 1,30 kU / л | ребенка в первый год жизни атопический дерматит и хроническая диарея с мукореей и ректальным кровотечением, соблюдение диеты без коровьего молока[25] | ||
| 8. | 25 | F | Яйцо | Рвота, боль в животе, диарея 263 | Повышенный уровень эозинофилов 2300–2500 эозиофилов / мкл | Общий IgE = 89.7 кЕд / л Уровень специфического для яиц IgE = 6,25 кЕд / л | История перемежающихся желудочно-кишечных симптомов EG | [24] |
Таблица 2
Проспективные когортные исследования, связанные с пищевым острым панкреатитом
| S. No. | Возраст, лет | Пол | Тип питания | Показатели заболеваемости | Результаты | Заключение | Ссылка |
|---|---|---|---|---|---|---|---|
| 1. | 45–84 | M Высокие гликемические факторы питания | 49 случаев на 100000 человеко-лет в наивысшем квартиле гликемической нагрузки и 33 случая на 100000 человеко-лет в самом низком | 364 случаях инцидентов, не связанных с GS-AP (236 у мужчин и 128 у женщин) | диеты с высоким гликемическим индексом связаны с повышенным риском non-GS-AP | [27] | |
| 2. | 45–84 | M-39,267 F-32,191 | Жирная и нежирная рыба | Потребление рыбы ≤2,0–3,0 порций в неделю было связано со значительным снижением риска заболевания. | 320 случаев (209 случаев у мужчин и 111 случаев у женщин) инцидентов Non-GS-AP | Потребление всей рыбы (жирная рыба и нежирная рыба вместе) может быть связано со снижением риска non-GS-AP | [30] |
| 3. | 46–84 | 80 019 женщин и мужчин, | Овощи, фрукты | Снижение риска на 17% при потреблении овощей | 320 инцидентов (216 мужчин и 104 женщин) с non-GS-AP | Потребление овощей, но не потребление фруктов, может играть роль в предотвращении non-GS-AP | [29] |
| 4. | 45–75 | 145,886 Мужчины и женщины | Факторы питания: жир, яйца, красное мясо, молоко, кофе и т. Д. | Более высокая частота ассоциаций между факторами питания и панкреатитом наблюдалась в основном для GS-AP | GS – ОП (n = 1210), AP, не связанное с камнями в желчном пузыре (n = 1222), или рецидивирующий AP, или подозрение на хронический панкреатит (n = 378). | Насыщенные жиры, источники холестерина, такие как красный цвет и яйца, положительно связаны с GS-AP. Витамин D из молока, кофе, клетчатки, защищающей от GS-AP. | [28] |
Связь ЭГ с панкреатитом также хорошо известна в литературе, и основной причиной ЭГ является пищевая аллергия [23, 24, 48]. Многочисленные сообщения о случаях показывают, что ЭГ может возникать из-за коровьего молока [23] и аллергии на яйца [24], а тяжелые симптомы ЭГ могут усугублять острый панкреатит. Судзуки и др. [23] сообщили о случае панкреатита, связанного с аллергией на молоко, который быстро улучшился после прекращения приема молока из рациона и лечения кортикостероидами.У пациента отмечено снижение сывороточных титров ферментов поджелудочной железы и общего билирубина с нормализацией количества эозинофилов в крови. Пациент не проявлял никаких симптомов в течение более 20 месяцев после исключения коровьего молока из своего рациона. Таким образом, аллергия на коровье молоко у взрослых встречается редко; но они могут вызвать серьезные осложнения, такие как анафилаксия, гастроэнтерит и панкреатит.
Tse и соавторы [24] представили первое сообщение о панкреатите, связанном с аллергией на яйца, у 25-летней женщины, не страдающей атопией, у которой в течение 30 минут после еды яйца возникла боль в животе, иррадирующая в левый подреберь и грудь.Лабораторные исследования выявили уровень липазы в сыворотке 2400 Ед / л и периферическую эозинофилию 23,3% (2300 эозинофилов / мкл), который оставался повышенным, увеличившись до 26% (2500 эозинофилов / мкл) на следующей неделе. Дальнейшая диагностическая визуализация, такая как УЗИ, КТ брюшной полости и MRCP, не выявила расширения желчных протоков или обструкции, что могло бы указывать на наличие камней в желчном пузыре. Другие частые причины панкреатита, такие как алкоголь и лекарства, также были исключены. Верхняя эндоскопия в норме. Тесты на аллергию in vitro подтвердили положительный уровень яичных специфических IgE на уровне 6.25 кЕд / л, тогда как все другие протестированные продукты были отрицательными, а общий IgE составил 89,7 кЕд / л. Однако биопсия двенадцатиперстной кишки показала 80 эозинофилов / поле высокой мощности, а анализ образца кала на яйцеклетки и паразитов был отрицательным, за исключением присутствия кристаллов Шарко-Лейдена, что указывает на лежащий в основе эозинофильный желудочно-кишечный процесс. У этого пациента ЭГ была достаточно тяжелой, чтобы вызвать острый панкреатит. Возможный механизм, предсказанный для опосредованной пищевой гиперчувствительностью и острого панкреатита, связанного с ЭГ, связан с обструкцией протока поджелудочной железы из-за местного воспаления двенадцатиперстной кишки [49].
Несмотря на то, что в большинстве случаев пищевого панкреатита наблюдались отек кишечной стенки и воспаление двенадцатиперстной кишки, компьютерная томография показала нормальную поджелудочную железу [10, 23, 24, 26]. Это указывает на то, что визуализации поджелудочной железы недостаточно для диагностики панкреатита. В пересмотренной классификации панкреатита в Атланте говорится, что для диагностики панкреатита следует рассматривать два из трех следующих критериев, например, классическую боль в животе, уровень амилазы или липазы в крови, индуцированный примерно в 3 раза, а визуализация показывает воспалительные изменения в поджелудочной железе.Кроме того, следует учитывать индекс Бальтазара и систему оценки тяжести КТ для диагностики острого панкреатита как степени А и оценки 0 соответственно, потому что панкреатит может возникать даже без каких-либо видимых морфологических изменений после компьютерной томографии [50]. Однако есть некоторые сообщения о случаях, которые указывают на боль в животе и повышение липазы более чем в 3 раза, и отсутствие панкреатита. Несмотря на то, что они соответствуют клиническим критериям острого панкреатита, у них могут быть язвы кишечника или отек стенки кишечника.В клинических условиях, когда есть сомнения в достоверности повышения липазы, клиницисты обычно проводят КТ / МРТ для подтверждения интерстициального отека / воспаления поджелудочной железы. Когда он присутствует, то нет никаких сомнений в том, что панкреатит возник. Когда он отсутствует при соблюдении клинических критериев, остается сомнительным, действительно ли возник панкреатит. Следовательно, некоторые из этих случаев могут не быть панкреатитом, но как минимум соответствуют текущим общепринятым клиническим критериям.
Механизм, связанный с пищевым панкреатитом
Inamura et al. (2005) предположили, что заброс желчи в проток поджелудочной железы из-за обструкции ампулы Фатера и неправильной активации зимогенов может быть причиной панкреатита, индуцированного пищей [10]. Они обнаружили воспалительные изменения в ампуле Фатера при эндоскопическом исследовании, а патология показала накопление большого количества тучных клеток в слизистой и подслизистой оболочке при иммуногистохимическом окрашивании против триптазы тучных клеток человека.Кроме того, тучные клетки играют ключевую роль в панкреатите [51, 52]. Этот пациент ел бананы каждый раз перед приступами рецидивирующего острого панкреатита и имел специфический IgE к бананам 2,18 МЕ / л, что является низким положительным результатом. Другой пациент с панкреатитом, связанным с аллергией на молоко, имел специфический IgE к коровьему молоку 2,17 KU / 1 [13]. Следовательно, гиперчувствительность к пищевому веществу также может привести к закупорке ампулы Фатера, вызывая рефлюкс желчи в проток поджелудочной железы и несоответствующую активацию ферментов поджелудочной железы, приводящую к приступу панкреатита.
Индуцированный пищевым аллергеном IgE играет роль в индукции панкреатита
Пищевая аллергия, опосредованная IgE, вызывается, когда антитела IgE связываются с рецепторами FcεRI (фрагмент, кристаллизующаяся область эпсилон R1), присутствующими на тучных клетках и базофилах, вызывая высвобождение биологически активные медиаторы и последующее развитие реакции гиперчувствительности в отношении съеденных пищевых белков [1]. Как правило, пищевая аллергия, опосредованная IgE, проходит в два этапа: сенсибилизацию и дегрануляцию.Первичное воздействие аллергена вызывает сенсибилизацию, а вторичное воздействие того же аллергена вызывает дегрануляцию иммунных клеток. Когда происходит первичное воздействие пищевых аллергенов, эти аллергены улавливаются и превращаются в небольшие пептидные фрагменты антигенпрезентирующими клетками (APC) с помощью протеасомного комплекса. Позже эти процессированные пептидные фрагменты были представлены вместе с основным комплексом гистосовместимости класса II (MHC-II) с помощью APC наивным CD4 + Т-клеткам. Эти наивные CD4 + Т-клетки дифференцируются в клетки Th3 в присутствии IL-4 и продуцируют специфические цитокины Th3, такие как IL-5 и IL-13 [53].Эти высвободившиеся цитокины Th3, особенно IL-4 и IL-13, были ответственны за перекрестную связь между T- и B-клетками и индуцировали дифференцировку B-клеток в плазматические клетки, продуцирующие IgE. Эти пищевые аллерген-специфические антитела IgE связываются с поверхностными рецепторами FcεRI на тучных клетках и базофилах [54]. Эта стадия обычно известна как «фаза сенсибилизации», и теперь сенсибилизированные иммунные клетки готовы спровоцировать более сильный аллергический ответ при повторном воздействии того же пищевого аллергена. Вторичное воздействие того же пищевого аллергена вызывает перекрестное связывание аллерген-специфических антител IgE с рецепторами FcεRI на тучных клетках и / или базофилах.Это событие, в свою очередь, вызывает дегрануляцию тучных клеток или базофилов, высвобождая несколько медиаторов аллергии, таких как гистамин, простагландин D2 и т. Д., Что приводит к развитию характерных симптомов аллергии [55].
Кроме того, сообщалось об IgE при панкреатите, и несколько исследований показали, что пациенты с хроническим панкреатитом имеют высокие уровни IgE в сыворотке крови, особенно во время острых воспалительных эпизодов или если пациент принимал алкоголь [56, 57]. Более того, в более раннем отчете о клиническом случае также было показано повышение уровня IgE у пациента с рецидивирующим панкреатитом, длившимся несколько лет, что предполагает пищевую аллергию как причину рецидивирующего панкреатита [12].Кроме того, аллергия на молочный белок была связана с острым панкреатитом, а сывороточные уровни IgE, специфичных к молочным белкам и бета-лактоглобулину, были повышены у пациентов с острым панкреатитом [13]. Кроме того, даже при возникновении острого панкреатита сообщалось о аллергии на фрукты, в том числе бананы [10] и киви [26]. У этих пациентов не было рецидива панкреатита после отказа от ответственной пищи [26]. Кроме того, повышенная гликемическая нагрузка [27], потребление насыщенных жиров, холестерина, красного мяса и яиц [28] повышают риск острого панкреатита, не связанного с желчными камнями.На большой выборке из 80 019 шведов (в возрасте 46–84 лет) Оскарссон и его коллеги показали, что потребление овощей может играть роль в профилактике острого панкреатита, не связанного с желчными камнями [26]. Аналогичным образом сообщалось о случае 26-летней женщины с большим количеством эозинофилов в резецированной поджелудочной железе, у которой подозревали эозинофильный панкреатит. Интересно, что у нее неоднократно было нормальное количество эозинофилов, гистологически нормальные биопсии гастродуоденальных, селезеночных и чревных лимфатических узлов.Было высказано предположение, что это могло быть связано с редким проявлением аллергических проявлений в анамнезе пациента и повышением сывороточных уровней IgE [11]. Эти исследования показывают, что некоторые продукты могут вызвать приступ панкреатита, тогда как некоторые продукты минимизируют риск развития панкреатита.
Не-IgE-опосредованный панкреатит, вызванный пищевыми аллергенами
Не-IgE-опосредованные пищевые аллергии были вызваны компонентами иммунной системы, отличными от IgE-антител. При пищевой аллергии, не опосредованной IgE, задействован клеточный иммунный ответ с преимущественным воздействием на слизистую оболочку желудочно-кишечного тракта [58].Сообщалось об эозинофильной инфильтрации и вовлечении Т-клеток при желудочно-кишечных пищевых аллергических расстройствах, не опосредованных IgE (не-IgE-EGID), таких как синдром энтероколита, индуцированного пищевым белком (FPIES) и энтеропатия, индуцированная пищевым белком (FPE) [2, 59] . Кроме того, активация и рекрутирование эозинофилов рядом цитокинов, включая IL-3, IL-5 и GM-CSF, а также хемокины, приводит к дегрануляции эозинофилов. Дегрануляция эозинофилов вызывает высвобождение нескольких провоспалительных медиаторов, в том числе катионных белков, хранящихся в гранулах, и многих цитокинов, таких как TGF-β, IL-3, IL-4, IL-5, IL-8, IL-13, IL-18 и TNF-α, которые были ответственны за повреждение тканей в месте аллергии [2, 15].В литературе цитируется несколько сообщений о случаях накопления эозинофилов у пациентов с панкреатитом, и это состояние названо «эозинофильным панкреатитом (ЭП)» [11, 60]. В совокупности можно предположить, что пищевые специфические реакции, не опосредованные IgE, могут играть решающую роль в индукции воспаления поджелудочной железы, но необходимы дальнейшие усилия, чтобы установить этот феномен.
Роль воспалительных клеток в панкреатите, опосредованном пищевыми аллергенами
Известно, что некоторые иммунные эффекторные клетки, такие как тучные клетки, базофилы, эозинофилы, нейтрофилы и Т-клетки, играют решающую роль в стимулировании пищевых аллергических реакций при панкреатите [61, 62 ].Вкратце подробности каждой ячейки представлены ниже.
Тучные клетки
Сообщалось об участии тучных клеток в желудочно-кишечных расстройствах, вызванных пищевой аллергией [63, 64]. В IgE-опосредованных реакциях происходит выработка аллерген-специфического IgE, и последующее связывание с рецепторами FcεRI на тучных клетках инициирует аллергический ответ через высвобождение нескольких медиаторов, что приводит к расширению сосудов, отеку и бронхоспазму [65]. Тучные клетки играют решающую роль в остром летальном [66], хроническом панкреатите [52, 67] и полиорганной недостаточности [68].Также было выявлено участие тучных клеток в развитии панкреатита и возможность аллергической основы заболевания [66].
Базофилы
Базофилы составляют менее 1% лейкоцитов периферической крови и участвуют в развитии IgE-опосредованных аллергических заболеваний [1]. Недавнее наблюдение, основанное на первоначальных результатах, показало, что активированные базофилы играют важную роль в патофизиологии аутоиммунного панкреатита через активацию сигнального пути TLR [69].Однако роль базофилов в индуцированном пищевыми аллергенами патогенезе острого и хронического панкреатита все еще не ясна и требует дальнейшего изучения.
Эозинофилы
Эозинофилы также играют ключевую роль в пищевых аллергических реакциях [23, 24]. Сообщалось об эозинофилии крови и тканей с выраженной дегрануляцией при ряде аллергических заболеваний, связанных с пищевыми продуктами [2]. Эотаксины являются важными молекулами и действуют как хемоаттрактант эозинофилов, который способствует накоплению эозинофилов в ткани [70].Эозинофильный панкреатит – относительно редкое заболевание, характеризующееся местной или диффузной инфильтрацией эозинофилов в поджелудочную железу [60] во время острого панкреатита, а также зарегистрированное в связи с эозинофильным гастроэнтеритом [48, 71]. Эти наблюдения предполагают, что аллергические реакции, вызванные пищевыми аллергенами, могут быть вовлечены в развитие эозинофильного панкреатита, но еще недостаточно изучены, и их необходимо изучить, чтобы лучше понять механистические аспекты индуцированного пищевыми продуктами панкреатита.Совсем недавно мы сообщили о важной роли эозинофилов в хроническом панкреатите, вызванном церулеином. Наш отчет показывает, что у мышей с дефицитом эозинофилов GATA 1 наблюдается снижение ремоделирования поджелудочной железы по сравнению с мышами дикого типа или с дефицитом гена IL-5 после 4 недель лечения церулеином [72].
Нейтрофилы
Решающая роль нейтрофилов была показана у пациентов с пищевой аллергией [73] и хорошо документирована при остром панкреатите [15, 74, 75]. Медиаторы нейтрофилов вызывают активацию трипсина, воспаление и могут способствовать патогенезу панкреатита [74] через IgE-независимые анафилактические реакции [76].Внеклеточные ловушки нейтрофилов (NET) представляют собой деконденсированную ДНК и гистоны, которые улавливают микробные патогены и организуют инициирование и разрешение воспаления [17, 77]. NET образуются в поджелудочной железе мышей во время АП, вызывают индукцию трипсина и способствуют патогенезу панкреатита [74]. На основании этих сообщений, индукция нейтрофилов, связанная с пищевыми аллергенами, может быть связана с прогрессированием острого панкреатита.
Лимфоциты
Несколько исследований показывают, что пищевые аллерген-специфические Т-лимфоциты запускают выработку ИЛ-4 и ИЛ-13, необходимых для синтеза IgE, а Т-лимфоциты хорошо документированы в патогенезе острых состояний [78, 79] и хронический панкреатит [80].CD4 + Т-клетки играют решающую роль в прогрессировании заболевания при остром экспериментальном панкреатите [78]. Лиганд CD40 (CD40L), присутствующий на Th-клетках, связывается с рецептором CD40, присутствующим на APC, и регулирует события панкреатита [81]. Кроме того, Т-клетки участвуют как в опосредованных IgE, так и в не-IgE пищевых аллергических реакциях [82, 83] и могут играть важную роль в регуляции патогенеза панкреатита. Следовательно, необходимы дальнейшие исследования для понимания глубоких молекулярных механизмов, участвующих в патогенезе пищевой аллергии и панкреатита.
В соответствии с пониманием, кажется, что могут действовать IgE-опосредованные и не-IgE-опосредованные аллергические механизмы. Таким образом, тучные клетки, базофилы, эозинофилы, нейтрофилы и Т-клетки могут играть решающую роль в панкреатите, вызванном приемом пищи, и в будущем их необходимо будет протестировать для разработки вариантов лечения. Возможный рабочий механизм острого панкреатита, вызванного пищевыми аллергенами, и участие различных типов иммунных клеток были показаны на рис.
Возможный рабочий механизм при остром панкреатите, индуцированном пищевыми аллергенамиПищевые аллергены интернализуются и обрабатываются антигенпрезентирующими клетками (APC) с помощью протеосомного комплекса и представлены основным комплексом гистосовместимости класса II (MHC-II) наивным CD4 + Т-клетки, которые дифференцируются в клетки Th3 в присутствии IL-4 и продуцируют IL-5 и IL-13, которые активируют последующие аллергические пути и вызывают острый панкреатит, связанный с пищевым аллергеном.Аллергическая реакция поджелудочной железы, вызванная пищевыми аллергенами, может быть опосредованной IgE или не-IgE. При ответе, опосредованном IgE, клетки Th3 секретируют IL-4 и IL-13, которые вызывают активацию B-клеток и переключение класса IgE. Антитела IgE связываются с поверхностными рецепторами FcεRI, присутствующими на тучных клетках и базофилах, которые приводят к дегрануляции и высвобождению нескольких медиаторов аллергии. Эти аллергические медиаторы, вероятно, вызывают активацию трипсиногена и развитие панкреатита. Однако эта гипотеза требует дальнейшего изучения для разработки стратегии лечения.Напротив, может также возникать не-IgE-опосредованная реакция, которая включает в себя роль активных хемокинов IL-5 и эозинофилов, эотаксинов, которые привлекают, активируют и высвобождают несколько медиаторов воспаления и приводят к активации трипсиногена. Повышенный уровень трипсина последовательно запускает эпизод острого панкреатита. Кроме того, нейтрофилы образуют нейтрофильные внеклеточные ловушки (NET) деконденсированной ДНК и гистонов, которых достаточно, чтобы вызвать активацию трипсина и способствовать патогенезу панкреатита.
Существуют пробелы в знаниях между острым панкреатитом, вызванным пищевыми продуктами, и патогенезом панкреатита. . Панкреатит – смертельное заболевание со значительной заболеваемостью и смертностью. Хотя острый панкреатит, вызванный пищевыми продуктами, является редким заболеванием, четкое понимание острого панкреатита, связанного с пищевыми продуктами, с этим заболеванием должно насторожить врача, чтобы он мог надлежащим образом диагностировать и лечить этих пациентов с острым панкреатитом, пораженным пищевыми продуктами.Дальнейшие исследования должны быть выполнены для понимания молекулярных механизмов острого панкреатита, вызванного пищевыми продуктами, и его клинических последствий. Кроме того, оценка аллергологом и гастроэнтерологом пищевых продуктов, обычно связанных с состоянием панкреатита, поможет установить более ранний диагноз. Ранняя диагностика может облегчить и ускорить прекращение неприятной пищи, тем самым уменьшив количество осложнений и продолжительность пребывания в больнице.
Усилия, необходимые для установления панкреатита, вызванного пищевыми аллергенами
В настоящее время очень мало сообщений о случаях причастности пищевых аллергенов к индукции панкреатита; Следовательно, медицинскому сообществу необходимо приложить больше усилий для выявления пищи, вызывающей острый панкреатит, и лучшего понимания механистических аспектов панкреатита, опосредованного пищевыми продуктами.Кроме того, необходимо тесное сотрудничество между аллергологом и гастроэнтерологом для диагностики и понимания патогенеза пищевого панкреатита путем разработки новых и эффективных подходов, таких как идентификация определенного типа пищевого аллергена для конкретного пациента.
Лечение острого панкреатита, вызванного пищевыми продуктами
Панкреатит, вызванный пищевой аллергией, можно вылечить путем исключения определенных диетических аллергенов; избегая определенного типа пищи. «Nil per Os» – это первая линия лечения наряду с агрессивной гидратацией, которая помогает поджелудочной железе отдохнуть и восстановиться [24, 26].В зависимости от основной причины панкреатита варианты лечения могут различаться в зависимости от конкретной причины. При необходимости можно использовать анальгетики и противорвотные средства. Кромоглициевая кислота (стабилизатор тучных клеток) и кортикостероиды часто используются для лечения острого панкреатита, вызванного пищевыми продуктами [12, 24, 26]. Кроме того, использование терапии микронутриентами, включая несколько витаминов, метионин и β-каротин, дает очень многообещающие результаты при лечении хронического панкреатита. В одном исследовании микронутриентная терапия была приготовлена другим способом для обеспечения метиловых и тиоловых фрагментов, которые ограничивают образование активных форм кислорода, деактивируют провоспалительные реакции и предотвращают дегрануляцию тучных клеток [51].Следовательно, препараты, стабилизирующие тучные клетки, могут стать вариантом лечения пищевого панкреатита в будущем.
Заключение
В настоящем обзоре дается всестороннее понимание механизмов пищевой аллергии и связанных с ней расстройств, включая акцент на панкреатите, вызванном пищевыми продуктами. Острый или хронический панкреатит, вызванный пищевыми продуктами, представляет собой проблему для научного сообщества, поскольку его патогенез до сих пор не ясен и как происходит развитие / прогрессирование заболевания с помощью иммунных компонентов, активируемых пищевым антигеном.Однако литературы о влиянии пищи на индукцию панкреатита очень мало. В этом обзоре мы обобщили имеющиеся отчеты о случаях панкреатита, связанного с пищевой аллергией, и его возможные механизмы. Наш обзор литературы побуждает к дальнейшим размышлениям в этом направлении, и будет интересно узнать, как и почему определенные продукты вызывают панкреатит у некоторых восприимчивых людей. Улучшение клинических исходов для пациентов остается в центре внимания обширных фундаментальных научных и клинических исследований, и многие из текущих проблем, связанных с панкреатитом, вызванным пищевыми продуктами, особенно актуальны для клинических биохимиков и поставщиков медицинских услуг.Существует необходимость в дальнейших исследованиях в этой области пищевого панкреатита, и мы настоятельно рекомендуем не игнорировать пищевой панкреатит и обследовать пациентов у аллерголога. Поэтому мы призываем клиницистов проявлять особую бдительность в отношении панкреатита, вызванного пищевыми продуктами, особенно у пациентов, у которых диагностирован идиопатический панкреатит. Расширенный диетический анамнез, включая недавно употребленные продукты, вызывающие симптомы, может привести врачей к диагнозу пищевого панкреатита.
Благодарности
Д-р Мишра – председатель совета директоров Schlieder; поэтому авторы благодарят Образовательный фонд Эдварда Г. Шлидера за поддержку.
Сноски
Конфликт интересов
Все авторы заявляют об отсутствии конфликта интересов.
Ссылки
1. Стоун К.Д., Пруссин С., Меткалф Д.Д. IgE, тучные клетки, базофилы и эозинофилы. J Allergy Clin Immunol. 2010; 125 (2 приложение 2): S73–80. [Бесплатная статья PMC] [PubMed] [Google Scholar] 2.Шукла А., М.А., Венкатешайа С.У., Манхоар М., Махадеваппа С.П., Мишра А. Элементы, участвующие в развитии эозинофильных желудочно-кишечных расстройств. J Genet Syndr Gene Ther. 2015; 6: 265. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Verma AK, MMUVSU, Blecker U, Collins MH, Mishra A. Роль вазоактивного кишечного пептида в продвижении патогенеза эозинофильного эзофагита (EoE) Cell Mol Gastroenterol Hepatol. 2017 сен; Принято, статья в печати. [Бесплатная статья PMC] [PubMed] [Google Scholar] 4. Верма А.К., Манохар М., УВС, Мишра А.Эндокринные клетки, производные хемокинового вазоактивного кишечного полипептида (VIP) при аллергических заболеваниях. Cytokine Growth Factor Rev.2017 Сентябрь; В прессе. [Бесплатная статья PMC] [PubMed] 5. Каттан Дж. Распространенность и естественная история пищевой аллергии. Curr Allergy Asthma Rep.2016; 16 (7): 47. [PubMed] [Google Scholar] 8. Вулф Дж. Л., Асевес СС. Желудочно-кишечные проявления пищевой аллергии. Pediatr Clin North Am. 2011. 58 (2): 389–405. Икс. [PubMed] [Google Scholar] 9. Verma AK, et al. Комплексный обзор аллергии на бобовые.Clin Rev Allergy Immunol. 2013. 45 (1): 30–46. [PubMed] [Google Scholar] 10. Inamura H, et al. Острый панкреатит, возможно, вызванный аллергией на бананы. J Исследование Allergol Clin Immunol. 2005. 15 (3): 222–4. [PubMed] [Google Scholar] 11. Flejou JF, Potet F, Bernades P. Эозинофильный панкреатит: редкое проявление пищеварительной аллергии? Гастроэнтерол Clin Biol. 1989. 13 (8–9): 731–3. [PubMed] [Google Scholar] 12. Маттео А., Сарлес Х. Является ли пищевая аллергия причиной острого панкреатита? Поджелудочная железа. 1990; 5 (2): 234–7.[PubMed] [Google Scholar] 13. де Диего Лоренцо А. и др. Острый панкреатит, связанный с аллергией на молоко. Int J Pancreatol. 1992. 12 (3): 319–21. [PubMed] [Google Scholar] 14. Ивата Ф., Одадзима Ю. Острый панкреатит, связанный с пищевой аллергией. Eur J Pediatr. 1997; 156 (6): 506. [PubMed] [Google Scholar] 17. Манохар М., В.А., Венкатешайя С.У., Сандерс Н.Л., Мишра А. Острая респираторная недостаточность, связанная с хроническим панкреатитом. Минюст иммунологии. 2017; 5 (2): 1–7. [Google Scholar] 19. Ян А.Л. и др. Эпидемиология связанных с алкоголем заболеваний печени и поджелудочной железы в США.Arch Intern Med. 2008. 168 (6): 649–56. [PubMed] [Google Scholar] 20. Hirota M, et al. Шестое общенациональное эпидемиологическое исследование хронического панкреатита в Японии. Панкреатология. 2012. 12 (2): 79–84. [PubMed] [Google Scholar] 21. Couvelaire RBD. Quelques résultats expérimentaux sur la génèse des oedèmes aigus et des hémorragies pancréatiques. Les pancréatites anaphylactiques. CR Soc Biol. 1933; 11: 1435–1437. [Google Scholar] 22. Каррильо Т., А.М., Гусман Т.М., Виларделл В.Ю., Гойри И.М. Панкреатит более сложный, чем анафилаксия.Rev Esp Alergol Immunol Clin. 1987; 2: 388–390. [Google Scholar] 23. Suzuki S и др. Эозинофильный гастроэнтерит, вызванный аллергией на коровье молоко, проявляющийся острым панкреатитом. Int Arch Allergy Immunol. 2012; 158 (Дополнение 1): 75–82. [PubMed] [Google Scholar] 24. Це К.Ю., Кристиансен СК. Эозинофильный гастроэнтерит, вызванный аллергией на яйца, проявляющейся как острый панкреатит. Allergy Rhinol (Providence) 2015; 6 (1): 80–1. [Бесплатная статья PMC] [PubMed] [Google Scholar] 25. Пеллегрино К. и др. Тяжелая реакция у ребенка с бессимптомной аллергией на треску: проблема с едой, реактивирующая рецидивирующий панкреатит.Ital J Pediatr. 2012; 38: 16. [Бесплатная статья PMC] [PubMed] [Google Scholar] 26. Gastaminza G, Bernaola G, Camino ME. Острый панкреатит, вызванный аллергией на киви. Аллергия. 1998. 53 (11): 1104–5. [PubMed] [Google Scholar] 27. Оскарссон В. и др. Высокая гликемическая нагрузка в питании увеличивает риск острого панкреатита, не связанного с желчнокаменной болезнью: проспективное когортное исследование. Clin Gastroenterol Hepatol. 2014. 12 (4): 676–82. [PubMed] [Google Scholar] 28. Setiawan VW и др. Факторы питания снижают риск острого панкреатита в большой многонациональной когорте.Clin Gastroenterol Hepatol. 2017; 15 (2): 257–265 e3. [Бесплатная статья PMC] [PubMed] [Google Scholar] 29. Оскарссон В. и др. Овощи, фрукты и риск острого панкреатита, не связанного с желчнокаменной болезнью: популяционное проспективное когортное исследование. Кишечник. 2013; 62 (8): 1187–92. [PubMed] [Google Scholar] 30. Оскарссон В. и др. Потребление рыбы и риск острого панкреатита, не связанного с желчнокаменной болезнью: проспективное когортное исследование. Am J Clin Nutr. 2015; 101 (1): 72–8. [PubMed] [Google Scholar] 31. Ho MH, Wong WH, Chang C. Клинический спектр пищевых аллергий: всесторонний обзор.Clin Rev Allergy Immunol. 2014. 46 (3): 225–40. [PubMed] [Google Scholar] 32. Босолей Дж. Л., Фидлер Дж., Спергель Дж. М.. Пищевая непереносимость и детская астма: какая связь? Педиатрические препараты. 2007. 9 (3): 157–63. [PubMed] [Google Scholar] 34. Brandt EB, et al. Экспериментальная желудочно-кишечная аллергия усиливает реакцию легких на специфические и неродственные аллергены. J Allergy Clin Immunol. 2006. 118 (2): 420–7. [PubMed] [Google Scholar] 35. Чо К.А. и др. IL-33 вызывает Th27-опосредованное воспаление дыхательных путей через тучные клетки у мышей, зараженных овальбумином.Am J Physiol Lung Cell Mol Physiol. 2012; 302 (4): L429–40. [PubMed] [Google Scholar] 36. Bihouée T, BG, Chesné J, Lair D, Rolland-Debord C, Braza F, Cheminant MA, Aubert P, Mahay G, Sagan C, Neunlist M, Brouard S, Bodinier M, Magnan A. Пищевая аллергия усиливает аллергическую астму у мышей . Respir Res. 2014; 30 (15): 142. [Бесплатная статья PMC] [PubMed] [Google Scholar] 37. Тарик С.М. и др. Аллергия на яйца в младенчестве предсказывает респираторное аллергическое заболевание к 4 годам. Pediatr Allergy Immunol. 2000. 11 (3): 162–7. [PubMed] [Google Scholar] 38.Джеймс Дж. М., Бернхизел-Бродбент Дж., Сэмпсон ГА. Респираторные реакции, вызванные двойным слепым приемом пищи у детей. Am J Respir Crit Care Med. 1994. 149 (1): 59–64. [PubMed] [Google Scholar] 39. Torpier G, et al. Эозинофильный гастроэнтерит: ультраструктурные доказательства избирательного высвобождения основного основного белка эозинофилов. Clin Exp Immunol. 1988. 74 (3): 404–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 40. Мишра А. и др. Основные сигналы, регулирующие возвращение эозинофилов в желудочно-кишечный тракт.J Clin Invest. 1999. 103 (12): 1719–27. [Бесплатная статья PMC] [PubMed] [Google Scholar] 41. Uppal V, Kreiger P, Kutsch E. Эозинофильный гастроэнтерит и колит: всесторонний обзор. Clin Rev Allergy Immunol. 2016; 50 (2): 175–88. [PubMed] [Google Scholar] 42. Хан С, Оренштейн СР. Эозинофильный гастроэнтерит: эпидемиология, диагностика и лечение. Педиатрические препараты. 2002. 4 (9): 563–70. [PubMed] [Google Scholar] 43. Альфадда А.А., Сторр М.А., Шаффер Е.А. Эозинофильный колит: эпидемиология, клинические особенности и текущее лечение.Therap Adv Гастроэнтерол. 2011; 4 (5): 301–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 44. Jaffe JS и др. Доказательства аномального профиля интерлейкина-4 (IL-4), IL-5 и гамма-интерферона (гамма-IFN) в Т-клетках периферической крови пациентов с аллергическим эозинофильным гастроэнтеритом. J Clin Immunol. 1994. 14 (5): 299–309. [PubMed] [Google Scholar] 45. Эль-Музан М.И., Аль-Куорайн А.А., Anim JT. Эрозивный гастрит у грудного ребенка, вызванный коровьим молоком. J Pediatr Gastroenterol Nutr. 1990. 10 (1): 111–3. [PubMed] [Google Scholar] 46.Bischoff SC. Пищевая аллергия и эозинофильный гастроэнтерит и колит. Curr Opin Allergy Clin Immunol. 2010. 10 (3): 238–45. [PubMed] [Google Scholar] 47. Валле-Дорадо М.Г. и др. Стабилизатор тучных клеток кромогликат натрия снижает высвобождение гистамина и вызванное эпилептическим статусом повреждение нейронов в гиппокампе крыс. Нейрофармакология. 2015; 92: 49–55. [PubMed] [Google Scholar] 48. Васкес Родригес Дж. Дж. И др. Панкреатит и эозинофильный гастроэнтерит. Int Surg. 1973; 58 (6): 415–9. [PubMed] [Google Scholar] 49.Caglar E, Karismaz K, Dobrucali A. Случай эозинофильного гастроэнтерита, имитирующего лимфому желудка, связанный с панкреатитом из-за поражения двенадцатиперстной кишки. Turk J Gastroenterol. 2012; 23 (5): 585–9. [PubMed] [Google Scholar] 50. Goyal H, et al. Различия в степени тяжести и исходах между гипертриглицеридемией и алкогольным панкреатитом. N Am J Med Sci. 2016; 8 (2): 82–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Браганса JM, Дорманди TL. Микронутриентная терапия хронического панкреатита: обоснование и влияние.JOP. 2010. 11 (2): 99–112. [PubMed] [Google Scholar] 52. Эспозито I и др. Распределение и активация тучных клеток при хроническом панкреатите. Hum Pathol. 2001. 32 (11): 1174–83. [PubMed] [Google Scholar] 53. Kweon MN, et al. Системно полученные CD4 (+) Th3-клетки толстого кишечника играют центральную роль в STAT6-опосредованной аллергической диарее. J Clin Invest. 2000. 106 (2): 199–206. [Бесплатная статья PMC] [PubMed] [Google Scholar] 54. Меткалф Д.Д., Пиви Р.Д., Гилфиллан А.М. Механизмы передачи сигналов тучными клетками при анафилаксии. J Allergy Clin Immunol.2009. 124 (4): 639–46. викторина 647–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 55. Knol EF. Требования к эффективному сшиванию IgE на тучных клетках и базофилах. Mol Nutr Food Res. 2006. 50 (7): 620–4. [PubMed] [Google Scholar] 56. Raithel M, et al. Продукция иммуноглобулина Е при хроническом панкреатите. Eur J Gastroenterol Hepatol. 2003. 15 (7): 801–7. [PubMed] [Google Scholar] 57. Raithel M, et al. Стимуляция образования иммуноглобулина Е при хроническом панкреатите алкоголем и внешнесекреторной недостаточностью поджелудочной железы.З. Гастроэнтерол. 2001. 39 (4): 269–76. [PubMed] [Google Scholar] 58. Jyonouchi H. Не-IgE-опосредованная пищевая аллергия – последние сведения о последних достижениях иммунитета слизистых оболочек. Цели лекарств от аллергии на воспаление. 2012. 11 (5): 382–96. [PubMed] [Google Scholar] 59. Caubet JC, et al. Не IgE-опосредованные желудочно-кишечные пищевые аллергии у детей. Pediatr Allergy Immunol. 2016 [PubMed] [Google Scholar] 61. Кумар С. В., Дас М., Двиведи П. Д.. Аллергенное разнообразие пищевых белков растений и животных. Food Reviews International. 2011. 28 (3): 277–298.[Google Scholar] 62. Манохар М., В.А., Венкатешайя С.У., Мишра А. Иммунологические реакции, участвующие в развитии острого и хронического панкреатита. J Clin Immunol Res. 2017; 1: 1–8. [Google Scholar] 63. Воутерс М.М., Викарио М., Сантос Дж. Роль тучных клеток в функциональных расстройствах желудочно-кишечного тракта. Кишечник. 2016; 65 (1): 155–68. [PubMed] [Google Scholar] 64. Галли SJ, Grimbaldeston M, Tsai M. Иммуномодулирующие тучные клетки: как отрицательные, так и положительные регуляторы иммунитета. Nat Rev Immunol. 2008. 8 (6): 478–86. [Бесплатная статья PMC] [PubMed] [Google Scholar] 65.Краневельд А.Д. и др. Две стороны тучных клеток при пищевой аллергии и аллергической астме: возможная концепция Инь-Ян. Biochim Biophys Acta. 2012; 1822 (1): 93–9. [PubMed] [Google Scholar] 66. Braganza JM. Тучная клетка: ключевой игрок в лечении острого панкреатита со смертельным исходом. QJM. 2000. 93 (7): 469–76. [PubMed] [Google Scholar] 68. Диб М. и др. Роль тучных клеток в развитии полиорганной дисфункции, вызванной панкреатитом. Br J Surg. 2002. 89 (2): 172–8. [PubMed] [Google Scholar] 69. Масато Янагава К.Ю., Икемунэ Манами, Икеура Цукаса, Шиматани Масааки, Фукуи Тоширо, Такаока Макото, Нишио Акиёси, Сатои Сохей, Окадзаки Кадзуичи.Роль базофилов через передачу сигналов TLR у пациентов с аутоиммунным панкреатитом 1 типа. Панкреатология. 2016; 16 (4): S 40. [Google Scholar] 70. Стеллато С. и др. Производство нового хемокина C-C MCP-4 клетками дыхательных путей и сравнение его биологической активности с другими хемокинами C-C. J Clin Invest. 1997. 99 (5): 926–36. [Бесплатная статья PMC] [PubMed] [Google Scholar] 71. Маэшима А. и др. Эозинофильный гастроэнтерит с острым панкреатитом. J Med. 1997. 28 (3–4): 265–72. [PubMed] [Google Scholar] 72.Манохар М., ВАК, Венкатешайя С.У., Мишра А. Роль эозинофилов в инициации и прогрессировании патогенеза панкреатита. Am J Physiol Gastrointest Liver Physiol. 2017 сен 19; Принято, статья в печати. [Бесплатная статья PMC] [PubMed] [Google Scholar] 73. Wallaert B, et al. Воспаление нейтрофилов дыхательных путей у неастматических пациентов с пищевой аллергией. Аллергия. 2002. 57 (5): 405–10. [PubMed] [Google Scholar] 74. Merza M, et al. Внеклеточные ловушки нейтрофилов вызывают активацию трипсина, воспаление и повреждение тканей у мышей с тяжелым острым панкреатитом.Гастроэнтерология. 2015; 149 (7): 1920–1931 e8. [PubMed] [Google Scholar] 75. Ян З.В., Мэн XX, Сюй П. Центральная роль нейтрофилов в патогенезе тяжелого острого панкреатита. J Cell Mol Med. 2015; 19 (11): 2513–20. [Бесплатная статья PMC] [PubMed] [Google Scholar] 76. Муньос-Кано Р. и др. Механизмы анафилаксии помимо IgE. J Исследование Allergol Clin Immunol. 2016; 26 (2): 73–82. викторина 2p после 83. [PubMed] [Google Scholar] 77. Хан Дж. И др. Нейтрофилы и внеклеточные ловушки нейтрофилов организуют инициирование и разрешение воспаления.Clin Exp Rheumatol. 2016; 34 (4 Suppl 98): 6–8. [PubMed] [Google Scholar] 78. Demols A, et al. CD4 (+) Т-клетки играют важную роль в остром экспериментальном панкреатите у мышей. Гастроэнтерология. 2000. 118 (3): 582–90. [PubMed] [Google Scholar] 79. Vonlaufen A, et al. Роль воспалительных и паренхиматозных клеток при остром панкреатите. J Pathol. 2007. 213 (3): 239–48. [PubMed] [Google Scholar] 80. Ямада Т. и др. Роль Т-клеток в развитии хронического панкреатита у самцов крыс Wistar Bonn / Kobori: эффекты такролимуса.Am J Physiol Gastrointest Liver Physiol. 2001; 281 (6): G1397–404. [PubMed] [Google Scholar] 81. Frossard JL, et al. Мыши с дефицитом лиганда Cd40 защищены от церулеин-индуцированного острого панкреатита и связанного с панкреатитом повреждения легких. Гастроэнтерология. 2001. 121 (1): 184–94. [PubMed] [Google Scholar] 82. Паломарес О. Роль регуляторных Т-клеток в IgE-опосредованной пищевой аллергии. J Исследование Allergol Clin Immunol. 2013. 23 (6): 371–82. quiz 2 p перед 382. [PubMed] [Google Scholar] 83. Эйгенманн П.А., Фроссар С.П.Т-лимфоциты при расстройствах пищевой аллергии. Curr Opin Allergy Clin Immunol. 2003. 3 (3): 199–203. [PubMed] [Google Scholar]Острый панкреатит, вызванный пищевыми продуктами
Dig Dis Sci. Авторская рукопись; доступно в PMC 1 декабря 2018 г.
Опубликован в окончательной редакции как:
PMCID: PMC5718054
NIHMSID: NIHMS
4
, Ph.D, 1, $ , Ph.D, 1, $ , к.т.н., 1 , д.м.н., 2 и, к.т.н. 1, *Мурли Манохар
1 Департамент медицины, отделение легочных заболеваний, Центр эозинофильных заболеваний Тулейна, Школа медицины Тулейнского университета, Новый Орлеан, Лос-Анджелес, 70112, США
Алок К.Verma
1 Департамент медицины, Отделение легочных заболеваний, Центр эозинофильных заболеваний Тулейна, Медицинский факультет Тулейнского университета, Новый Орлеан, Лос-Анджелес, 70112, США
Сатиша Уппарахалли Венкатешайя
1 Департамент медицины, Отделение легочных заболеваний, Центр эозинофильных заболеваний Тулейна, Медицинский факультет Тулейнского университета, Новый Орлеан, Лос-Анджелес 70112, США
Хемант Гоял
2 Кафедра внутренней медицины, Медицинский факультет Университета Мерсер, 707 Pine St.Macon, GA 31201
Анил Мишра
1 Департамент медицины, Отделение легочных заболеваний, Тулейнский центр эозинофильных расстройств, Школа медицины Тулейнского университета, Новый Орлеан, Лос-Анджелес 70112, США
1 Департамент медицины, Отделение легочных заболеваний, Тулейнский центр эозинофильных расстройств, Школа медицины Тулейнского университета, Новый Орлеан, Лос-Анджелес 70112, США
2 Кафедра внутренней медицины, Медицинский факультет Университета Мерсер, 707 Pine St.Macon, GA 31201
* Автор, ответственный за переписку: Анил Мишра, доктор философии, заведующий кафедрой Шлидера, профессор и директор Тулейнского центра эозинофильных расстройств, департамент медицины, отделение легочной медицины, Медицинская школа Тулейнского университета, Новый Орлеан, LA 70112 , США. Тел: 504-988-3840; Факс: 504-988-2144; ude.enalut@arhsima$ Авторы внесли одинаковый вклад: Мурли Манохар, Алок К. Верма
Окончательная отредактированная версия этой статьи издателем доступна на Dig Dis SciSee, другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
Пищевая аллергия – широко распространенная во всем мире проблема, определяемая как неблагоприятный иммунный ответ на пищу. Множество связанных с иммунитетом эффекторных клеток, таких как тучные клетки, эозинофилы, нейтрофилы и Т-клетки, участвуют в пищевых аллергических ответах, которые классифицируются как IgE-опосредованные, не-IgE-опосредованные и смешанные (IgE и не-IgE) в зависимости от основные иммунологические механизмы. Пищевые антигены в основном нацелены на желудочно-кишечный тракт, включая поджелудочную железу, которая воспаляется из-за пищевой аллергии и приводит к острому панкреатиту.Отчеты показывают, что некоторые пищевые белки вызывают панкреатит; однако подробный механизм, лежащий в основе панкреатита, вызванного пищевыми продуктами, не изучен. Цель обзора – понять и обновить текущий сценарий пищевого панкреатита. Через PubMed был проведен всесторонний поиск литературы по соответствующим исследовательским статьям, и статьи были выбраны на основе их актуальности для панкреатита, опосредованного пищевыми аллергенами. Несколько случаев в литературе, указывающих на то, что острый панкреатит был спровоцирован после употребления горчицы, молока, яиц, бананов, рыбы и киви.Панкреатит, вызванный пищевыми продуктами, – это игнорируемая и неизученная область исследований. В обзоре подчеркивается значение пищи в развитии панкреатита и обращается внимание врачей и ученых на то, чтобы рассматривать пищевую аллергию как возможную причину инициирования патогенеза панкреатита.
Ключевые слова: Пищевая аллергия, панкреатит, эозинофилы, тучные клетки, нейтрофилы
Введение
Растущая распространенность аллергических заболеваний является тревожной проблемой во всем мире, и пищевые аллергены вносят основной вклад в развитие аллергических проявлений, включая желудочно-кишечные расстройства [ 1–4] Распространенность пищевой аллергии оценивается примерно в 3–8%, и она значительно влияет на качество жизни восприимчивых людей [5].Пищевая аллергия может быть определена как провокация неблагоприятной аллергической реакции на безвредные пищевые антигены из-за чрезмерной реакции иммунной системы на эти пищевые антигены. Признаки и симптомы пищевой аллергии могут варьироваться от легкой до тяжелой и могут включать рвоту, диарею, крапивницу, зуд, отек языка, низкое кровяное давление и затрудненное дыхание [6]. Аллергические реакции, вызванные пищевыми продуктами, обычно возникают в течение от нескольких минут до нескольких часов после воздействия, а при тяжелых симптомах они могут вызвать тяжелую анафилаксию [7].Чрезмерная реакция иммунной системы организма на пищевые антигены может поражать несколько органов, включая дыхательные и желудочно-кишечные (ЖКТ) тракты, что приводит к развитию обострения астмы, дыхательной недостаточности, эзофагита и гастроэнтерита [2, 8, 9]. аллергия считается одной из причин, способствующих развитию острого панкреатита [10–14]. Панкреатит характеризуется острым или хроническим воспалением, которое может быть вызвано различными вредными раздражителями, такими как камни в желчном пузыре, алкоголь и мутация в гене трипсиногена [15–17].Ежегодная заболеваемость острым и хроническим панкреатитом колеблется от 13 до 45 и от 4,4 до 11,9 на 100 000 человек в США соответственно [15, 18]. Более того, различные сообщения указывают на повышенную заболеваемость панкреатитом среди населения Японии по сравнению с США [15, 19, 20]. К сожалению, в текущем сценарии распространенность острого или хронического панкреатита, вызванного пищевыми продуктами, все еще недостаточно хорошо известна. С 1933 г. известно, что пищевая аллергия является причиной острого панкреатита у собак [21]; кроме того, несколько случаев острого панкреатита у человека, вызванного аллергией на горчицу [22], молоко [13, 23], икру трески [14], яйца [24], бананы [10], рыбу [25] и киви [ 26] описаны в литературе.Несколько исследований показывают, что высокая гликемическая нагрузка [27], жир, мясо, яйца и т. Д. [28] связаны с риском острого панкреатита, не связанного с желчнокаменной болезнью. В то время как другие исследования сообщают, что овощи и рыба (включая жирную и нежирную рыбу) могут быть связаны со снижением риска нежечнокаменного острого панкреатита [29, 30]. Все эти исследования показывают, что определенные продукты связаны с повышенным риском острого панкреатита, в то время как другие продукты могут быть защитными.
Согласно клиническим данным и тестам на аллергию, известны три типа пищевых аллергий: опосредованные IgE (немедленный тип, гиперчувствительность I типа), не опосредованные IgE (замедленный тип, клеточная гиперчувствительность, гиперчувствительность IV типа) и смешанные (IgE / Non-IgE) [31], но в случае пищевого панкреатита механизм неизвестен, и эта область исследований игнорируется и остается неизученной.В этом обзоре мы стремимся предоставить текущую информацию, касающуюся пищевых аллергических реакций, с особым акцентом на панкреатит, вызванный пищевыми продуктами. Текущий обзор также предоставляет исследователям и врачам платформу для понимания участия различных типов эффекторных иммунных клеток, а также действующих молекулярных механизмов, которые могут проложить путь к новым методам лечения панкреатита, вызванного пищевыми продуктами.
Аллергические расстройства, вызванные пищевыми продуктами
Аллергические расстройства, вызванные пищевыми продуктами, растут во всем мире, и некоторые продукты питания были отмечены как фактор риска развития аллергических заболеваний [32].Пищевая аллергия в основном связана с увеличением цитокинов Th3, эозинофилов и тучных клеток в ответ на аллергены [33–36]. Пищевая аллергия сообщается при нескольких аллергических заболеваниях, включая астму [33–35], аллергический ринит [37, 38], желудочно-кишечные расстройства, такие как эозинофильный гастроэнтерит [2, 39] и панкреатит [23, 24]. Здесь мы суммировали текущее понимание и имеющиеся данные о развитии эозинофильного гастроэнтерита-зависимого и независимого панкреатита.
Эозинофильный гастроэнтерит и панкреатит, вызванный пищевыми аллергенами
Эозинофильный гастроэнтерит (ЭГ) – это воспалительное заболевание, опосредованное эозинофилами, которое характеризуется инфильтрацией эозинофилов в желудке, тонком и толстом кишечнике [2, 39]. Базовые эозинофилы обычно присутствуют в желудочно-кишечном тракте [40]; но увеличение их количества наблюдалось в ответ на несколько раздражителей, таких как повреждение тканей и инфекции, включая пищевые аллергены.Эти накопленные эозинофилы активируются, что приводит к дальнейшей дегрануляции и секреции различных цитокинов, которые приводят к развитию EG [41]. Примечательно, что данные указывают на то, что 50–75% пациентов с ЭГ имеют в личном или семейном анамнезе сопутствующие аллергии или атопические расстройства [42, 43]. Было высказано предположение, что пищевая аллергия способствует стимулированию ЭГ у этих пациентов, а увеличение общего IgE и пищевого специфического IgE свидетельствует о пищевой аллергии в стимулировании ЭГ у пациентов [44]. Сообщалось, что коровье молоко вызывает эрозивный гастрит, и его исключение из рациона показало исчезновение аллергических симптомов у младенцев [45].Некоторые данные свидетельствуют о том, что пищевые антигены играют решающую роль в патогенезе эозинофильного гастроэнтерита, а также колита [46].
Впервые о пищевой аллергии и ее связи с панкреатитом сообщили в 1933 году Couvelaire и Bargeton [21], продемонстрировав экспериментальный анафилактический шок, вызванный пищевыми аллергенами, у собак. Несколько сообщений о случаях острого панкреатита, спровоцированного пищевой аллергией на горчицу [22], молоко [13, 23], яйца [24], бананы [10], рыбу [25] и киви [26], у человека были опубликованы в литература.Также сообщалось о хроническом панкреатите, сохраняющемся от 8 до 10 лет из-за употребления различных видов пищи, таких как говядина, молоко, картофель, рыба и яйца [12]. Основные симптомы этих пациентов включают острую боль в животе и повышение уровня ферментов поджелудочной железы в сыворотке крови. Однако результаты ультразвукового исследования брюшной полости и компьютерной томографии выявили отечность поджелудочной железы только у одного пациента. Уровень IgE в сыворотке был повышен у одного пациента [12]. Этих пациентов лечили путем прекращения приема провоцирующей пищи (говядины, молока, картофеля, рыбы и яиц) и одновременно с приемом препарата кромогликат, стабилизатора тучных клеток [47], который предотвращает высвобождение гистамина из тучных клеток.Также сообщалось о случае острого панкреатита, связанного с молоком, у 23-летнего пациента с повторяющимися эпизодами боли в животе, повышенными уровнями амилазы, липазы, сывороточного IgE, бета-лактоглобулина и увеличенной поджелудочной железой в ультразвуковом отчете. У пациента были рецидивирующие эпизоды острого панкреатита, сопровождавшиеся эритемой лица с инъекцией конъюнктивы, генерализованным зудом, диареей и эозинофилией после употребления молока [13]. Inamura et al. [10] опубликовали случай рецидивирующего острого панкреатита (три эпизода), вызванного аллергией на бананы, у 47-летней женщины с аллергическим ринитом в анамнезе.Пациент лечился консервативно, с легкой диетой и внутривенным введением жидкости, с исчезновением клинических симптомов в течение нескольких дней. Кроме того, повышенные уровни амилазы вернулись к нормальным значениям параллельно с клиническими симптомами. Общий уровень IgE в сыворотке составлял 644 МЕ / мл, при этом уровень специфического IgE к бананам составлял 2,18 UA / мл, что свидетельствует о значительной аллергии на бананы. Gastaminza et al. [26] представили клинический случай острого панкреатита, развившегося после употребления киви у 48-летнего мужчины с язвой двенадцатиперстной кишки и кровотечением из верхних отделов желудочно-кишечного тракта в анамнезе.Этот пациент также имел в анамнезе ринит, бронхиальную астму и аллергию на пиразолоны. Сообщалось о повышении уровня амилазы и лейкоцитоза в сыворотке крови на 835 Ед / л (N = 60–190) и 13 000 / мм 2 соответственно. Примечательно, что после 48 часов лечения легкой диетой, внутривенными жидкостями, антацидами и анальгетиками; уровни амилазы и липазы в сыворотке вернулись к норме. Поскольку пациент умеренно пил, у него изначально был диагностирован алкогольный панкреатит, но примерно через две недели он перенес еще один эпизод панкреатита после употребления в пищу киви.Позже прокол показал аллергию на киви, и ему поставили диагноз панкреатит, вызванный фруктами киви. Согласно отчету, после отказа от употребления киви в течение последних пяти лет пациент больше не страдал панкреатитом. Сводка каждого из этих отчетов о случаях острого панкреатита, связанного с пищевыми продуктами, представлена в. Более того, несколько крупных многонациональных когортных исследований показали, что высокая гликемическая нагрузка, насыщенные жиры, холестерин, красное мясо и яйца повышают риск острого панкреатита, не связанного с желчнокаменной болезнью [27, 28]; Напротив, недавние отчеты показали, что потребление овощей и рыбы (жирной и нежирной рыбы вместе) может быть связано со снижением риска нежечнокаменного острого панкреатита [29, 30].Резюме проспективных когортных исследований, связанных с острым панкреатитом, вызванным пищевыми продуктами, у человека было представлено в.
Таблица 1
Обобщенные детали отчетов о случаях острого панкреатита, вызванного пищевыми аллергенами
| S. No. | Возраст (год) | Пол | Аллергическая пища | Симптомы | s) | IgE | Другие ассоциированные заболевания | Список литературы | |
|---|---|---|---|---|---|---|---|---|---|
| 1. | 26 | F | NA | Боль в животе, аллергические симптомы | Эозинофилы | Повышенный уровень IgE в сыворотке | EP | [11] | |
| 2. | M | Говядина (дважды) Молоко Картофель Рыба Яйцо | Боль в животе, Мигрень, Зуд, Повышенная амилаза в сыворотке крови, Боль в эпигастрии, связанная с диффузной головной болью | Нормальный уровень эозинофилов | Повышенный уровень IgE 9026 у одного пациента NA | [12] | |||
| 3. | 23 | NA | Молоко | Боль в животе, эритема лица с инъекцией конъюнктивы, генерализованный зуд, диарея, эозинофилия, повышенные уровни ферментов поджелудочной железы в сыворотке крови, увеличение поджелудочной железы и отек | на сонограмме | Уровень IgE | NA | [13] | |
| 4. | 48 | M | Киви | Боль в эпигастрии, рвота, диарея, эритема лица, зуд, повышение сывороточного уровня | Повышенный уровень сывороточного аминофосфата | общий IgE 257 мкл / мл | Язвенная болезнь двенадцатиперстной кишки в анамнезе, кровотечение из верхних отделов пищеварительного тракта, аллергия на пиразолоны, ринит и бронхиальная астма | [26] | |
| 5. | 47 | F | Банан | Эпигастралгия, Тошнота, Рвота, Диарея, Повышенный уровень амилазы в сыворотке и моче, Ампула Фатера опухшая и отечная | Повышение 64 Тучных клеток, Общее количество IUE в сыворотке | увеличено и специфический IgE к бананам (2,18 UA / мл) | NA | [10] | |
| 6. | – | M | Молоко | Симптомы ЭГ, такие как тошнота, рвота, боль в животе, диспепсия, Нарушение всасывания, асцит и потеря веса, повышение ферментов поджелудочной железы в сыворотке и общий билирубин | Повышение эозинофилов | – | EG | [23] | |
| 7. | 8 | M | треска | Анафилактическая реакция, Боль в животе, Повышенный уровень ферментов поджелудочной железы в сыворотке крови, Паренхиматозный отек при УЗИ | NA | Специфический IgE для трески = 1,30 kU / л | ребенка в первый год жизни атопический дерматит и хроническая диарея с мукореей и ректальным кровотечением, соблюдение диеты без коровьего молока[25] | ||
| 8. | 25 | F | Яйцо | Рвота, боль в животе, диарея 263 | Повышенный уровень эозинофилов 2300–2500 эозиофилов / мкл | Общий IgE = 89.7 кЕд / л Уровень специфического для яиц IgE = 6,25 кЕд / л | История перемежающихся желудочно-кишечных симптомов EG | [24] |
Таблица 2
Проспективные когортные исследования, связанные с пищевым острым панкреатитом
| S. No. | Возраст, лет | Пол | Тип питания | Показатели заболеваемости | Результаты | Заключение | Ссылка |
|---|---|---|---|---|---|---|---|
| 1. | 45–84 | M Высокие гликемические факторы питания | 49 случаев на 100000 человеко-лет в наивысшем квартиле гликемической нагрузки и 33 случая на 100000 человеко-лет в самом низком | 364 случаях инцидентов, не связанных с GS-AP (236 у мужчин и 128 у женщин) | диеты с высоким гликемическим индексом связаны с повышенным риском non-GS-AP | [27] | |
| 2. | 45–84 | M-39,267 F-32,191 | Жирная и нежирная рыба | Потребление рыбы ≤2,0–3,0 порций в неделю было связано со значительным снижением риска заболевания. | 320 случаев (209 случаев у мужчин и 111 случаев у женщин) инцидентов Non-GS-AP | Потребление всей рыбы (жирная рыба и нежирная рыба вместе) может быть связано со снижением риска non-GS-AP | [30] |
| 3. | 46–84 | 80 019 женщин и мужчин, | Овощи, фрукты | Снижение риска на 17% при потреблении овощей | 320 инцидентов (216 мужчин и 104 женщин) с non-GS-AP | Потребление овощей, но не потребление фруктов, может играть роль в предотвращении non-GS-AP | [29] |
| 4. | 45–75 | 145,886 Мужчины и женщины | Факторы питания: жир, яйца, красное мясо, молоко, кофе и т. Д. | Более высокая частота ассоциаций между факторами питания и панкреатитом наблюдалась в основном для GS-AP | GS – ОП (n = 1210), AP, не связанное с камнями в желчном пузыре (n = 1222), или рецидивирующий AP, или подозрение на хронический панкреатит (n = 378). | Насыщенные жиры, источники холестерина, такие как красный цвет и яйца, положительно связаны с GS-AP. Витамин D из молока, кофе, клетчатки, защищающей от GS-AP. | [28] |
Связь ЭГ с панкреатитом также хорошо известна в литературе, и основной причиной ЭГ является пищевая аллергия [23, 24, 48]. Многочисленные сообщения о случаях показывают, что ЭГ может возникать из-за коровьего молока [23] и аллергии на яйца [24], а тяжелые симптомы ЭГ могут усугублять острый панкреатит. Судзуки и др. [23] сообщили о случае панкреатита, связанного с аллергией на молоко, который быстро улучшился после прекращения приема молока из рациона и лечения кортикостероидами.У пациента отмечено снижение сывороточных титров ферментов поджелудочной железы и общего билирубина с нормализацией количества эозинофилов в крови. Пациент не проявлял никаких симптомов в течение более 20 месяцев после исключения коровьего молока из своего рациона. Таким образом, аллергия на коровье молоко у взрослых встречается редко; но они могут вызвать серьезные осложнения, такие как анафилаксия, гастроэнтерит и панкреатит.
Tse и соавторы [24] представили первое сообщение о панкреатите, связанном с аллергией на яйца, у 25-летней женщины, не страдающей атопией, у которой в течение 30 минут после еды яйца возникла боль в животе, иррадирующая в левый подреберь и грудь.Лабораторные исследования выявили уровень липазы в сыворотке 2400 Ед / л и периферическую эозинофилию 23,3% (2300 эозинофилов / мкл), который оставался повышенным, увеличившись до 26% (2500 эозинофилов / мкл) на следующей неделе. Дальнейшая диагностическая визуализация, такая как УЗИ, КТ брюшной полости и MRCP, не выявила расширения желчных протоков или обструкции, что могло бы указывать на наличие камней в желчном пузыре. Другие частые причины панкреатита, такие как алкоголь и лекарства, также были исключены. Верхняя эндоскопия в норме. Тесты на аллергию in vitro подтвердили положительный уровень яичных специфических IgE на уровне 6.25 кЕд / л, тогда как все другие протестированные продукты были отрицательными, а общий IgE составил 89,7 кЕд / л. Однако биопсия двенадцатиперстной кишки показала 80 эозинофилов / поле высокой мощности, а анализ образца кала на яйцеклетки и паразитов был отрицательным, за исключением присутствия кристаллов Шарко-Лейдена, что указывает на лежащий в основе эозинофильный желудочно-кишечный процесс. У этого пациента ЭГ была достаточно тяжелой, чтобы вызвать острый панкреатит. Возможный механизм, предсказанный для опосредованной пищевой гиперчувствительностью и острого панкреатита, связанного с ЭГ, связан с обструкцией протока поджелудочной железы из-за местного воспаления двенадцатиперстной кишки [49].
Несмотря на то, что в большинстве случаев пищевого панкреатита наблюдались отек кишечной стенки и воспаление двенадцатиперстной кишки, компьютерная томография показала нормальную поджелудочную железу [10, 23, 24, 26]. Это указывает на то, что визуализации поджелудочной железы недостаточно для диагностики панкреатита. В пересмотренной классификации панкреатита в Атланте говорится, что для диагностики панкреатита следует рассматривать два из трех следующих критериев, например, классическую боль в животе, уровень амилазы или липазы в крови, индуцированный примерно в 3 раза, а визуализация показывает воспалительные изменения в поджелудочной железе.Кроме того, следует учитывать индекс Бальтазара и систему оценки тяжести КТ для диагностики острого панкреатита как степени А и оценки 0 соответственно, потому что панкреатит может возникать даже без каких-либо видимых морфологических изменений после компьютерной томографии [50]. Однако есть некоторые сообщения о случаях, которые указывают на боль в животе и повышение липазы более чем в 3 раза, и отсутствие панкреатита. Несмотря на то, что они соответствуют клиническим критериям острого панкреатита, у них могут быть язвы кишечника или отек стенки кишечника.В клинических условиях, когда есть сомнения в достоверности повышения липазы, клиницисты обычно проводят КТ / МРТ для подтверждения интерстициального отека / воспаления поджелудочной железы. Когда он присутствует, то нет никаких сомнений в том, что панкреатит возник. Когда он отсутствует при соблюдении клинических критериев, остается сомнительным, действительно ли возник панкреатит. Следовательно, некоторые из этих случаев могут не быть панкреатитом, но как минимум соответствуют текущим общепринятым клиническим критериям.
Механизм, связанный с пищевым панкреатитом
Inamura et al. (2005) предположили, что заброс желчи в проток поджелудочной железы из-за обструкции ампулы Фатера и неправильной активации зимогенов может быть причиной панкреатита, индуцированного пищей [10]. Они обнаружили воспалительные изменения в ампуле Фатера при эндоскопическом исследовании, а патология показала накопление большого количества тучных клеток в слизистой и подслизистой оболочке при иммуногистохимическом окрашивании против триптазы тучных клеток человека.Кроме того, тучные клетки играют ключевую роль в панкреатите [51, 52]. Этот пациент ел бананы каждый раз перед приступами рецидивирующего острого панкреатита и имел специфический IgE к бананам 2,18 МЕ / л, что является низким положительным результатом. Другой пациент с панкреатитом, связанным с аллергией на молоко, имел специфический IgE к коровьему молоку 2,17 KU / 1 [13]. Следовательно, гиперчувствительность к пищевому веществу также может привести к закупорке ампулы Фатера, вызывая рефлюкс желчи в проток поджелудочной железы и несоответствующую активацию ферментов поджелудочной железы, приводящую к приступу панкреатита.
Индуцированный пищевым аллергеном IgE играет роль в индукции панкреатита
Пищевая аллергия, опосредованная IgE, вызывается, когда антитела IgE связываются с рецепторами FcεRI (фрагмент, кристаллизующаяся область эпсилон R1), присутствующими на тучных клетках и базофилах, вызывая высвобождение биологически активные медиаторы и последующее развитие реакции гиперчувствительности в отношении съеденных пищевых белков [1]. Как правило, пищевая аллергия, опосредованная IgE, проходит в два этапа: сенсибилизацию и дегрануляцию.Первичное воздействие аллергена вызывает сенсибилизацию, а вторичное воздействие того же аллергена вызывает дегрануляцию иммунных клеток. Когда происходит первичное воздействие пищевых аллергенов, эти аллергены улавливаются и превращаются в небольшие пептидные фрагменты антигенпрезентирующими клетками (APC) с помощью протеасомного комплекса. Позже эти процессированные пептидные фрагменты были представлены вместе с основным комплексом гистосовместимости класса II (MHC-II) с помощью APC наивным CD4 + Т-клеткам. Эти наивные CD4 + Т-клетки дифференцируются в клетки Th3 в присутствии IL-4 и продуцируют специфические цитокины Th3, такие как IL-5 и IL-13 [53].Эти высвободившиеся цитокины Th3, особенно IL-4 и IL-13, были ответственны за перекрестную связь между T- и B-клетками и индуцировали дифференцировку B-клеток в плазматические клетки, продуцирующие IgE. Эти пищевые аллерген-специфические антитела IgE связываются с поверхностными рецепторами FcεRI на тучных клетках и базофилах [54]. Эта стадия обычно известна как «фаза сенсибилизации», и теперь сенсибилизированные иммунные клетки готовы спровоцировать более сильный аллергический ответ при повторном воздействии того же пищевого аллергена. Вторичное воздействие того же пищевого аллергена вызывает перекрестное связывание аллерген-специфических антител IgE с рецепторами FcεRI на тучных клетках и / или базофилах.Это событие, в свою очередь, вызывает дегрануляцию тучных клеток или базофилов, высвобождая несколько медиаторов аллергии, таких как гистамин, простагландин D2 и т. Д., Что приводит к развитию характерных симптомов аллергии [55].
Кроме того, сообщалось об IgE при панкреатите, и несколько исследований показали, что пациенты с хроническим панкреатитом имеют высокие уровни IgE в сыворотке крови, особенно во время острых воспалительных эпизодов или если пациент принимал алкоголь [56, 57]. Более того, в более раннем отчете о клиническом случае также было показано повышение уровня IgE у пациента с рецидивирующим панкреатитом, длившимся несколько лет, что предполагает пищевую аллергию как причину рецидивирующего панкреатита [12].Кроме того, аллергия на молочный белок была связана с острым панкреатитом, а сывороточные уровни IgE, специфичных к молочным белкам и бета-лактоглобулину, были повышены у пациентов с острым панкреатитом [13]. Кроме того, даже при возникновении острого панкреатита сообщалось о аллергии на фрукты, в том числе бананы [10] и киви [26]. У этих пациентов не было рецидива панкреатита после отказа от ответственной пищи [26]. Кроме того, повышенная гликемическая нагрузка [27], потребление насыщенных жиров, холестерина, красного мяса и яиц [28] повышают риск острого панкреатита, не связанного с желчными камнями.На большой выборке из 80 019 шведов (в возрасте 46–84 лет) Оскарссон и его коллеги показали, что потребление овощей может играть роль в профилактике острого панкреатита, не связанного с желчными камнями [26]. Аналогичным образом сообщалось о случае 26-летней женщины с большим количеством эозинофилов в резецированной поджелудочной железе, у которой подозревали эозинофильный панкреатит. Интересно, что у нее неоднократно было нормальное количество эозинофилов, гистологически нормальные биопсии гастродуоденальных, селезеночных и чревных лимфатических узлов.Было высказано предположение, что это могло быть связано с редким проявлением аллергических проявлений в анамнезе пациента и повышением сывороточных уровней IgE [11]. Эти исследования показывают, что некоторые продукты могут вызвать приступ панкреатита, тогда как некоторые продукты минимизируют риск развития панкреатита.
Не-IgE-опосредованный панкреатит, вызванный пищевыми аллергенами
Не-IgE-опосредованные пищевые аллергии были вызваны компонентами иммунной системы, отличными от IgE-антител. При пищевой аллергии, не опосредованной IgE, задействован клеточный иммунный ответ с преимущественным воздействием на слизистую оболочку желудочно-кишечного тракта [58].Сообщалось об эозинофильной инфильтрации и вовлечении Т-клеток при желудочно-кишечных пищевых аллергических расстройствах, не опосредованных IgE (не-IgE-EGID), таких как синдром энтероколита, индуцированного пищевым белком (FPIES) и энтеропатия, индуцированная пищевым белком (FPE) [2, 59] . Кроме того, активация и рекрутирование эозинофилов рядом цитокинов, включая IL-3, IL-5 и GM-CSF, а также хемокины, приводит к дегрануляции эозинофилов. Дегрануляция эозинофилов вызывает высвобождение нескольких провоспалительных медиаторов, в том числе катионных белков, хранящихся в гранулах, и многих цитокинов, таких как TGF-β, IL-3, IL-4, IL-5, IL-8, IL-13, IL-18 и TNF-α, которые были ответственны за повреждение тканей в месте аллергии [2, 15].В литературе цитируется несколько сообщений о случаях накопления эозинофилов у пациентов с панкреатитом, и это состояние названо «эозинофильным панкреатитом (ЭП)» [11, 60]. В совокупности можно предположить, что пищевые специфические реакции, не опосредованные IgE, могут играть решающую роль в индукции воспаления поджелудочной железы, но необходимы дальнейшие усилия, чтобы установить этот феномен.
Роль воспалительных клеток в панкреатите, опосредованном пищевыми аллергенами
Известно, что некоторые иммунные эффекторные клетки, такие как тучные клетки, базофилы, эозинофилы, нейтрофилы и Т-клетки, играют решающую роль в стимулировании пищевых аллергических реакций при панкреатите [61, 62 ].Вкратце подробности каждой ячейки представлены ниже.
Тучные клетки
Сообщалось об участии тучных клеток в желудочно-кишечных расстройствах, вызванных пищевой аллергией [63, 64]. В IgE-опосредованных реакциях происходит выработка аллерген-специфического IgE, и последующее связывание с рецепторами FcεRI на тучных клетках инициирует аллергический ответ через высвобождение нескольких медиаторов, что приводит к расширению сосудов, отеку и бронхоспазму [65]. Тучные клетки играют решающую роль в остром летальном [66], хроническом панкреатите [52, 67] и полиорганной недостаточности [68].Также было выявлено участие тучных клеток в развитии панкреатита и возможность аллергической основы заболевания [66].
Базофилы
Базофилы составляют менее 1% лейкоцитов периферической крови и участвуют в развитии IgE-опосредованных аллергических заболеваний [1]. Недавнее наблюдение, основанное на первоначальных результатах, показало, что активированные базофилы играют важную роль в патофизиологии аутоиммунного панкреатита через активацию сигнального пути TLR [69].Однако роль базофилов в индуцированном пищевыми аллергенами патогенезе острого и хронического панкреатита все еще не ясна и требует дальнейшего изучения.
Эозинофилы
Эозинофилы также играют ключевую роль в пищевых аллергических реакциях [23, 24]. Сообщалось об эозинофилии крови и тканей с выраженной дегрануляцией при ряде аллергических заболеваний, связанных с пищевыми продуктами [2]. Эотаксины являются важными молекулами и действуют как хемоаттрактант эозинофилов, который способствует накоплению эозинофилов в ткани [70].Эозинофильный панкреатит – относительно редкое заболевание, характеризующееся местной или диффузной инфильтрацией эозинофилов в поджелудочную железу [60] во время острого панкреатита, а также зарегистрированное в связи с эозинофильным гастроэнтеритом [48, 71]. Эти наблюдения предполагают, что аллергические реакции, вызванные пищевыми аллергенами, могут быть вовлечены в развитие эозинофильного панкреатита, но еще недостаточно изучены, и их необходимо изучить, чтобы лучше понять механистические аспекты индуцированного пищевыми продуктами панкреатита.Совсем недавно мы сообщили о важной роли эозинофилов в хроническом панкреатите, вызванном церулеином. Наш отчет показывает, что у мышей с дефицитом эозинофилов GATA 1 наблюдается снижение ремоделирования поджелудочной железы по сравнению с мышами дикого типа или с дефицитом гена IL-5 после 4 недель лечения церулеином [72].
Нейтрофилы
Решающая роль нейтрофилов была показана у пациентов с пищевой аллергией [73] и хорошо документирована при остром панкреатите [15, 74, 75]. Медиаторы нейтрофилов вызывают активацию трипсина, воспаление и могут способствовать патогенезу панкреатита [74] через IgE-независимые анафилактические реакции [76].Внеклеточные ловушки нейтрофилов (NET) представляют собой деконденсированную ДНК и гистоны, которые улавливают микробные патогены и организуют инициирование и разрешение воспаления [17, 77]. NET образуются в поджелудочной железе мышей во время АП, вызывают индукцию трипсина и способствуют патогенезу панкреатита [74]. На основании этих сообщений, индукция нейтрофилов, связанная с пищевыми аллергенами, может быть связана с прогрессированием острого панкреатита.
Лимфоциты
Несколько исследований показывают, что пищевые аллерген-специфические Т-лимфоциты запускают выработку ИЛ-4 и ИЛ-13, необходимых для синтеза IgE, а Т-лимфоциты хорошо документированы в патогенезе острых состояний [78, 79] и хронический панкреатит [80].CD4 + Т-клетки играют решающую роль в прогрессировании заболевания при остром экспериментальном панкреатите [78]. Лиганд CD40 (CD40L), присутствующий на Th-клетках, связывается с рецептором CD40, присутствующим на APC, и регулирует события панкреатита [81]. Кроме того, Т-клетки участвуют как в опосредованных IgE, так и в не-IgE пищевых аллергических реакциях [82, 83] и могут играть важную роль в регуляции патогенеза панкреатита. Следовательно, необходимы дальнейшие исследования для понимания глубоких молекулярных механизмов, участвующих в патогенезе пищевой аллергии и панкреатита.
В соответствии с пониманием, кажется, что могут действовать IgE-опосредованные и не-IgE-опосредованные аллергические механизмы. Таким образом, тучные клетки, базофилы, эозинофилы, нейтрофилы и Т-клетки могут играть решающую роль в панкреатите, вызванном приемом пищи, и в будущем их необходимо будет протестировать для разработки вариантов лечения. Возможный рабочий механизм острого панкреатита, вызванного пищевыми аллергенами, и участие различных типов иммунных клеток были показаны на рис.
Возможный рабочий механизм при остром панкреатите, индуцированном пищевыми аллергенамиПищевые аллергены интернализуются и обрабатываются антигенпрезентирующими клетками (APC) с помощью протеосомного комплекса и представлены основным комплексом гистосовместимости класса II (MHC-II) наивным CD4 + Т-клетки, которые дифференцируются в клетки Th3 в присутствии IL-4 и продуцируют IL-5 и IL-13, которые активируют последующие аллергические пути и вызывают острый панкреатит, связанный с пищевым аллергеном.Аллергическая реакция поджелудочной железы, вызванная пищевыми аллергенами, может быть опосредованной IgE или не-IgE. При ответе, опосредованном IgE, клетки Th3 секретируют IL-4 и IL-13, которые вызывают активацию B-клеток и переключение класса IgE. Антитела IgE связываются с поверхностными рецепторами FcεRI, присутствующими на тучных клетках и базофилах, которые приводят к дегрануляции и высвобождению нескольких медиаторов аллергии. Эти аллергические медиаторы, вероятно, вызывают активацию трипсиногена и развитие панкреатита. Однако эта гипотеза требует дальнейшего изучения для разработки стратегии лечения.Напротив, может также возникать не-IgE-опосредованная реакция, которая включает в себя роль активных хемокинов IL-5 и эозинофилов, эотаксинов, которые привлекают, активируют и высвобождают несколько медиаторов воспаления и приводят к активации трипсиногена. Повышенный уровень трипсина последовательно запускает эпизод острого панкреатита. Кроме того, нейтрофилы образуют нейтрофильные внеклеточные ловушки (NET) деконденсированной ДНК и гистонов, которых достаточно, чтобы вызвать активацию трипсина и способствовать патогенезу панкреатита.
Существуют пробелы в знаниях между острым панкреатитом, вызванным пищевыми продуктами, и патогенезом панкреатита. . Панкреатит – смертельное заболевание со значительной заболеваемостью и смертностью. Хотя острый панкреатит, вызванный пищевыми продуктами, является редким заболеванием, четкое понимание острого панкреатита, связанного с пищевыми продуктами, с этим заболеванием должно насторожить врача, чтобы он мог надлежащим образом диагностировать и лечить этих пациентов с острым панкреатитом, пораженным пищевыми продуктами.Дальнейшие исследования должны быть выполнены для понимания молекулярных механизмов острого панкреатита, вызванного пищевыми продуктами, и его клинических последствий. Кроме того, оценка аллергологом и гастроэнтерологом пищевых продуктов, обычно связанных с состоянием панкреатита, поможет установить более ранний диагноз. Ранняя диагностика может облегчить и ускорить прекращение неприятной пищи, тем самым уменьшив количество осложнений и продолжительность пребывания в больнице.
Усилия, необходимые для установления панкреатита, вызванного пищевыми аллергенами
В настоящее время очень мало сообщений о случаях причастности пищевых аллергенов к индукции панкреатита; Следовательно, медицинскому сообществу необходимо приложить больше усилий для выявления пищи, вызывающей острый панкреатит, и лучшего понимания механистических аспектов панкреатита, опосредованного пищевыми продуктами.Кроме того, необходимо тесное сотрудничество между аллергологом и гастроэнтерологом для диагностики и понимания патогенеза пищевого панкреатита путем разработки новых и эффективных подходов, таких как идентификация определенного типа пищевого аллергена для конкретного пациента.
Лечение острого панкреатита, вызванного пищевыми продуктами
Панкреатит, вызванный пищевой аллергией, можно вылечить путем исключения определенных диетических аллергенов; избегая определенного типа пищи. «Nil per Os» – это первая линия лечения наряду с агрессивной гидратацией, которая помогает поджелудочной железе отдохнуть и восстановиться [24, 26].В зависимости от основной причины панкреатита варианты лечения могут различаться в зависимости от конкретной причины. При необходимости можно использовать анальгетики и противорвотные средства. Кромоглициевая кислота (стабилизатор тучных клеток) и кортикостероиды часто используются для лечения острого панкреатита, вызванного пищевыми продуктами [12, 24, 26]. Кроме того, использование терапии микронутриентами, включая несколько витаминов, метионин и β-каротин, дает очень многообещающие результаты при лечении хронического панкреатита. В одном исследовании микронутриентная терапия была приготовлена другим способом для обеспечения метиловых и тиоловых фрагментов, которые ограничивают образование активных форм кислорода, деактивируют провоспалительные реакции и предотвращают дегрануляцию тучных клеток [51].Следовательно, препараты, стабилизирующие тучные клетки, могут стать вариантом лечения пищевого панкреатита в будущем.
Заключение
В настоящем обзоре дается всестороннее понимание механизмов пищевой аллергии и связанных с ней расстройств, включая акцент на панкреатите, вызванном пищевыми продуктами. Острый или хронический панкреатит, вызванный пищевыми продуктами, представляет собой проблему для научного сообщества, поскольку его патогенез до сих пор не ясен и как происходит развитие / прогрессирование заболевания с помощью иммунных компонентов, активируемых пищевым антигеном.Однако литературы о влиянии пищи на индукцию панкреатита очень мало. В этом обзоре мы обобщили имеющиеся отчеты о случаях панкреатита, связанного с пищевой аллергией, и его возможные механизмы. Наш обзор литературы побуждает к дальнейшим размышлениям в этом направлении, и будет интересно узнать, как и почему определенные продукты вызывают панкреатит у некоторых восприимчивых людей. Улучшение клинических исходов для пациентов остается в центре внимания обширных фундаментальных научных и клинических исследований, и многие из текущих проблем, связанных с панкреатитом, вызванным пищевыми продуктами, особенно актуальны для клинических биохимиков и поставщиков медицинских услуг.Существует необходимость в дальнейших исследованиях в этой области пищевого панкреатита, и мы настоятельно рекомендуем не игнорировать пищевой панкреатит и обследовать пациентов у аллерголога. Поэтому мы призываем клиницистов проявлять особую бдительность в отношении панкреатита, вызванного пищевыми продуктами, особенно у пациентов, у которых диагностирован идиопатический панкреатит. Расширенный диетический анамнез, включая недавно употребленные продукты, вызывающие симптомы, может привести врачей к диагнозу пищевого панкреатита.
Благодарности
Д-р Мишра – председатель совета директоров Schlieder; поэтому авторы благодарят Образовательный фонд Эдварда Г. Шлидера за поддержку.
Сноски
Конфликт интересов
Все авторы заявляют об отсутствии конфликта интересов.
Ссылки
1. Стоун К.Д., Пруссин С., Меткалф Д.Д. IgE, тучные клетки, базофилы и эозинофилы. J Allergy Clin Immunol. 2010; 125 (2 приложение 2): S73–80. [Бесплатная статья PMC] [PubMed] [Google Scholar] 2.Шукла А., М.А., Венкатешайа С.У., Манхоар М., Махадеваппа С.П., Мишра А. Элементы, участвующие в развитии эозинофильных желудочно-кишечных расстройств. J Genet Syndr Gene Ther. 2015; 6: 265. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Verma AK, MMUVSU, Blecker U, Collins MH, Mishra A. Роль вазоактивного кишечного пептида в продвижении патогенеза эозинофильного эзофагита (EoE) Cell Mol Gastroenterol Hepatol. 2017 сен; Принято, статья в печати. [Бесплатная статья PMC] [PubMed] [Google Scholar] 4. Верма А.К., Манохар М., УВС, Мишра А.Эндокринные клетки, производные хемокинового вазоактивного кишечного полипептида (VIP) при аллергических заболеваниях. Cytokine Growth Factor Rev.2017 Сентябрь; В прессе. [Бесплатная статья PMC] [PubMed] 5. Каттан Дж. Распространенность и естественная история пищевой аллергии. Curr Allergy Asthma Rep.2016; 16 (7): 47. [PubMed] [Google Scholar] 8. Вулф Дж. Л., Асевес СС. Желудочно-кишечные проявления пищевой аллергии. Pediatr Clin North Am. 2011. 58 (2): 389–405. Икс. [PubMed] [Google Scholar] 9. Verma AK, et al. Комплексный обзор аллергии на бобовые.Clin Rev Allergy Immunol. 2013. 45 (1): 30–46. [PubMed] [Google Scholar] 10. Inamura H, et al. Острый панкреатит, возможно, вызванный аллергией на бананы. J Исследование Allergol Clin Immunol. 2005. 15 (3): 222–4. [PubMed] [Google Scholar] 11. Flejou JF, Potet F, Bernades P. Эозинофильный панкреатит: редкое проявление пищеварительной аллергии? Гастроэнтерол Clin Biol. 1989. 13 (8–9): 731–3. [PubMed] [Google Scholar] 12. Маттео А., Сарлес Х. Является ли пищевая аллергия причиной острого панкреатита? Поджелудочная железа. 1990; 5 (2): 234–7.[PubMed] [Google Scholar] 13. де Диего Лоренцо А. и др. Острый панкреатит, связанный с аллергией на молоко. Int J Pancreatol. 1992. 12 (3): 319–21. [PubMed] [Google Scholar] 14. Ивата Ф., Одадзима Ю. Острый панкреатит, связанный с пищевой аллергией. Eur J Pediatr. 1997; 156 (6): 506. [PubMed] [Google Scholar] 17. Манохар М., В.А., Венкатешайя С.У., Сандерс Н.Л., Мишра А. Острая респираторная недостаточность, связанная с хроническим панкреатитом. Минюст иммунологии. 2017; 5 (2): 1–7. [Google Scholar] 19. Ян А.Л. и др. Эпидемиология связанных с алкоголем заболеваний печени и поджелудочной железы в США.Arch Intern Med. 2008. 168 (6): 649–56. [PubMed] [Google Scholar] 20. Hirota M, et al. Шестое общенациональное эпидемиологическое исследование хронического панкреатита в Японии. Панкреатология. 2012. 12 (2): 79–84. [PubMed] [Google Scholar] 21. Couvelaire RBD. Quelques résultats expérimentaux sur la génèse des oedèmes aigus et des hémorragies pancréatiques. Les pancréatites anaphylactiques. CR Soc Biol. 1933; 11: 1435–1437. [Google Scholar] 22. Каррильо Т., А.М., Гусман Т.М., Виларделл В.Ю., Гойри И.М. Панкреатит более сложный, чем анафилаксия.Rev Esp Alergol Immunol Clin. 1987; 2: 388–390. [Google Scholar] 23. Suzuki S и др. Эозинофильный гастроэнтерит, вызванный аллергией на коровье молоко, проявляющийся острым панкреатитом. Int Arch Allergy Immunol. 2012; 158 (Дополнение 1): 75–82. [PubMed] [Google Scholar] 24. Це К.Ю., Кристиансен СК. Эозинофильный гастроэнтерит, вызванный аллергией на яйца, проявляющейся как острый панкреатит. Allergy Rhinol (Providence) 2015; 6 (1): 80–1. [Бесплатная статья PMC] [PubMed] [Google Scholar] 25. Пеллегрино К. и др. Тяжелая реакция у ребенка с бессимптомной аллергией на треску: проблема с едой, реактивирующая рецидивирующий панкреатит.Ital J Pediatr. 2012; 38: 16. [Бесплатная статья PMC] [PubMed] [Google Scholar] 26. Gastaminza G, Bernaola G, Camino ME. Острый панкреатит, вызванный аллергией на киви. Аллергия. 1998. 53 (11): 1104–5. [PubMed] [Google Scholar] 27. Оскарссон В. и др. Высокая гликемическая нагрузка в питании увеличивает риск острого панкреатита, не связанного с желчнокаменной болезнью: проспективное когортное исследование. Clin Gastroenterol Hepatol. 2014. 12 (4): 676–82. [PubMed] [Google Scholar] 28. Setiawan VW и др. Факторы питания снижают риск острого панкреатита в большой многонациональной когорте.Clin Gastroenterol Hepatol. 2017; 15 (2): 257–265 e3. [Бесплатная статья PMC] [PubMed] [Google Scholar] 29. Оскарссон В. и др. Овощи, фрукты и риск острого панкреатита, не связанного с желчнокаменной болезнью: популяционное проспективное когортное исследование. Кишечник. 2013; 62 (8): 1187–92. [PubMed] [Google Scholar] 30. Оскарссон В. и др. Потребление рыбы и риск острого панкреатита, не связанного с желчнокаменной болезнью: проспективное когортное исследование. Am J Clin Nutr. 2015; 101 (1): 72–8. [PubMed] [Google Scholar] 31. Ho MH, Wong WH, Chang C. Клинический спектр пищевых аллергий: всесторонний обзор.Clin Rev Allergy Immunol. 2014. 46 (3): 225–40. [PubMed] [Google Scholar] 32. Босолей Дж. Л., Фидлер Дж., Спергель Дж. М.. Пищевая непереносимость и детская астма: какая связь? Педиатрические препараты. 2007. 9 (3): 157–63. [PubMed] [Google Scholar] 34. Brandt EB, et al. Экспериментальная желудочно-кишечная аллергия усиливает реакцию легких на специфические и неродственные аллергены. J Allergy Clin Immunol. 2006. 118 (2): 420–7. [PubMed] [Google Scholar] 35. Чо К.А. и др. IL-33 вызывает Th27-опосредованное воспаление дыхательных путей через тучные клетки у мышей, зараженных овальбумином.Am J Physiol Lung Cell Mol Physiol. 2012; 302 (4): L429–40. [PubMed] [Google Scholar] 36. Bihouée T, BG, Chesné J, Lair D, Rolland-Debord C, Braza F, Cheminant MA, Aubert P, Mahay G, Sagan C, Neunlist M, Brouard S, Bodinier M, Magnan A. Пищевая аллергия усиливает аллергическую астму у мышей . Respir Res. 2014; 30 (15): 142. [Бесплатная статья PMC] [PubMed] [Google Scholar] 37. Тарик С.М. и др. Аллергия на яйца в младенчестве предсказывает респираторное аллергическое заболевание к 4 годам. Pediatr Allergy Immunol. 2000. 11 (3): 162–7. [PubMed] [Google Scholar] 38.Джеймс Дж. М., Бернхизел-Бродбент Дж., Сэмпсон ГА. Респираторные реакции, вызванные двойным слепым приемом пищи у детей. Am J Respir Crit Care Med. 1994. 149 (1): 59–64. [PubMed] [Google Scholar] 39. Torpier G, et al. Эозинофильный гастроэнтерит: ультраструктурные доказательства избирательного высвобождения основного основного белка эозинофилов. Clin Exp Immunol. 1988. 74 (3): 404–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 40. Мишра А. и др. Основные сигналы, регулирующие возвращение эозинофилов в желудочно-кишечный тракт.J Clin Invest. 1999. 103 (12): 1719–27. [Бесплатная статья PMC] [PubMed] [Google Scholar] 41. Uppal V, Kreiger P, Kutsch E. Эозинофильный гастроэнтерит и колит: всесторонний обзор. Clin Rev Allergy Immunol. 2016; 50 (2): 175–88. [PubMed] [Google Scholar] 42. Хан С, Оренштейн СР. Эозинофильный гастроэнтерит: эпидемиология, диагностика и лечение. Педиатрические препараты. 2002. 4 (9): 563–70. [PubMed] [Google Scholar] 43. Альфадда А.А., Сторр М.А., Шаффер Е.А. Эозинофильный колит: эпидемиология, клинические особенности и текущее лечение.Therap Adv Гастроэнтерол. 2011; 4 (5): 301–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 44. Jaffe JS и др. Доказательства аномального профиля интерлейкина-4 (IL-4), IL-5 и гамма-интерферона (гамма-IFN) в Т-клетках периферической крови пациентов с аллергическим эозинофильным гастроэнтеритом. J Clin Immunol. 1994. 14 (5): 299–309. [PubMed] [Google Scholar] 45. Эль-Музан М.И., Аль-Куорайн А.А., Anim JT. Эрозивный гастрит у грудного ребенка, вызванный коровьим молоком. J Pediatr Gastroenterol Nutr. 1990. 10 (1): 111–3. [PubMed] [Google Scholar] 46.Bischoff SC. Пищевая аллергия и эозинофильный гастроэнтерит и колит. Curr Opin Allergy Clin Immunol. 2010. 10 (3): 238–45. [PubMed] [Google Scholar] 47. Валле-Дорадо М.Г. и др. Стабилизатор тучных клеток кромогликат натрия снижает высвобождение гистамина и вызванное эпилептическим статусом повреждение нейронов в гиппокампе крыс. Нейрофармакология. 2015; 92: 49–55. [PubMed] [Google Scholar] 48. Васкес Родригес Дж. Дж. И др. Панкреатит и эозинофильный гастроэнтерит. Int Surg. 1973; 58 (6): 415–9. [PubMed] [Google Scholar] 49.Caglar E, Karismaz K, Dobrucali A. Случай эозинофильного гастроэнтерита, имитирующего лимфому желудка, связанный с панкреатитом из-за поражения двенадцатиперстной кишки. Turk J Gastroenterol. 2012; 23 (5): 585–9. [PubMed] [Google Scholar] 50. Goyal H, et al. Различия в степени тяжести и исходах между гипертриглицеридемией и алкогольным панкреатитом. N Am J Med Sci. 2016; 8 (2): 82–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Браганса JM, Дорманди TL. Микронутриентная терапия хронического панкреатита: обоснование и влияние.JOP. 2010. 11 (2): 99–112. [PubMed] [Google Scholar] 52. Эспозито I и др. Распределение и активация тучных клеток при хроническом панкреатите. Hum Pathol. 2001. 32 (11): 1174–83. [PubMed] [Google Scholar] 53. Kweon MN, et al. Системно полученные CD4 (+) Th3-клетки толстого кишечника играют центральную роль в STAT6-опосредованной аллергической диарее. J Clin Invest. 2000. 106 (2): 199–206. [Бесплатная статья PMC] [PubMed] [Google Scholar] 54. Меткалф Д.Д., Пиви Р.Д., Гилфиллан А.М. Механизмы передачи сигналов тучными клетками при анафилаксии. J Allergy Clin Immunol.2009. 124 (4): 639–46. викторина 647–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 55. Knol EF. Требования к эффективному сшиванию IgE на тучных клетках и базофилах. Mol Nutr Food Res. 2006. 50 (7): 620–4. [PubMed] [Google Scholar] 56. Raithel M, et al. Продукция иммуноглобулина Е при хроническом панкреатите. Eur J Gastroenterol Hepatol. 2003. 15 (7): 801–7. [PubMed] [Google Scholar] 57. Raithel M, et al. Стимуляция образования иммуноглобулина Е при хроническом панкреатите алкоголем и внешнесекреторной недостаточностью поджелудочной железы.З. Гастроэнтерол. 2001. 39 (4): 269–76. [PubMed] [Google Scholar] 58. Jyonouchi H. Не-IgE-опосредованная пищевая аллергия – последние сведения о последних достижениях иммунитета слизистых оболочек. Цели лекарств от аллергии на воспаление. 2012. 11 (5): 382–96. [PubMed] [Google Scholar] 59. Caubet JC, et al. Не IgE-опосредованные желудочно-кишечные пищевые аллергии у детей. Pediatr Allergy Immunol. 2016 [PubMed] [Google Scholar] 61. Кумар С. В., Дас М., Двиведи П. Д.. Аллергенное разнообразие пищевых белков растений и животных. Food Reviews International. 2011. 28 (3): 277–298.[Google Scholar] 62. Манохар М., В.А., Венкатешайя С.У., Мишра А. Иммунологические реакции, участвующие в развитии острого и хронического панкреатита. J Clin Immunol Res. 2017; 1: 1–8. [Google Scholar] 63. Воутерс М.М., Викарио М., Сантос Дж. Роль тучных клеток в функциональных расстройствах желудочно-кишечного тракта. Кишечник. 2016; 65 (1): 155–68. [PubMed] [Google Scholar] 64. Галли SJ, Grimbaldeston M, Tsai M. Иммуномодулирующие тучные клетки: как отрицательные, так и положительные регуляторы иммунитета. Nat Rev Immunol. 2008. 8 (6): 478–86. [Бесплатная статья PMC] [PubMed] [Google Scholar] 65.Краневельд А.Д. и др. Две стороны тучных клеток при пищевой аллергии и аллергической астме: возможная концепция Инь-Ян. Biochim Biophys Acta. 2012; 1822 (1): 93–9. [PubMed] [Google Scholar] 66. Braganza JM. Тучная клетка: ключевой игрок в лечении острого панкреатита со смертельным исходом. QJM. 2000. 93 (7): 469–76. [PubMed] [Google Scholar] 68. Диб М. и др. Роль тучных клеток в развитии полиорганной дисфункции, вызванной панкреатитом. Br J Surg. 2002. 89 (2): 172–8. [PubMed] [Google Scholar] 69. Масато Янагава К.Ю., Икемунэ Манами, Икеура Цукаса, Шиматани Масааки, Фукуи Тоширо, Такаока Макото, Нишио Акиёси, Сатои Сохей, Окадзаки Кадзуичи.Роль базофилов через передачу сигналов TLR у пациентов с аутоиммунным панкреатитом 1 типа. Панкреатология. 2016; 16 (4): S 40. [Google Scholar] 70. Стеллато С. и др. Производство нового хемокина C-C MCP-4 клетками дыхательных путей и сравнение его биологической активности с другими хемокинами C-C. J Clin Invest. 1997. 99 (5): 926–36. [Бесплатная статья PMC] [PubMed] [Google Scholar] 71. Маэшима А. и др. Эозинофильный гастроэнтерит с острым панкреатитом. J Med. 1997. 28 (3–4): 265–72. [PubMed] [Google Scholar] 72.Манохар М., ВАК, Венкатешайя С.У., Мишра А. Роль эозинофилов в инициации и прогрессировании патогенеза панкреатита. Am J Physiol Gastrointest Liver Physiol. 2017 сен 19; Принято, статья в печати. [Бесплатная статья PMC] [PubMed] [Google Scholar] 73. Wallaert B, et al. Воспаление нейтрофилов дыхательных путей у неастматических пациентов с пищевой аллергией. Аллергия. 2002. 57 (5): 405–10. [PubMed] [Google Scholar] 74. Merza M, et al. Внеклеточные ловушки нейтрофилов вызывают активацию трипсина, воспаление и повреждение тканей у мышей с тяжелым острым панкреатитом.Гастроэнтерология. 2015; 149 (7): 1920–1931 e8. [PubMed] [Google Scholar] 75. Ян З.В., Мэн XX, Сюй П. Центральная роль нейтрофилов в патогенезе тяжелого острого панкреатита. J Cell Mol Med. 2015; 19 (11): 2513–20. [Бесплатная статья PMC] [PubMed] [Google Scholar] 76. Муньос-Кано Р. и др. Механизмы анафилаксии помимо IgE. J Исследование Allergol Clin Immunol. 2016; 26 (2): 73–82. викторина 2p после 83. [PubMed] [Google Scholar] 77. Хан Дж. И др. Нейтрофилы и внеклеточные ловушки нейтрофилов организуют инициирование и разрешение воспаления.Clin Exp Rheumatol. 2016; 34 (4 Suppl 98): 6–8. [PubMed] [Google Scholar] 78. Demols A, et al. CD4 (+) Т-клетки играют важную роль в остром экспериментальном панкреатите у мышей. Гастроэнтерология. 2000. 118 (3): 582–90. [PubMed] [Google Scholar] 79. Vonlaufen A, et al. Роль воспалительных и паренхиматозных клеток при остром панкреатите. J Pathol. 2007. 213 (3): 239–48. [PubMed] [Google Scholar] 80. Ямада Т. и др. Роль Т-клеток в развитии хронического панкреатита у самцов крыс Wistar Bonn / Kobori: эффекты такролимуса.Am J Physiol Gastrointest Liver Physiol. 2001; 281 (6): G1397–404. [PubMed] [Google Scholar] 81. Frossard JL, et al. Мыши с дефицитом лиганда Cd40 защищены от церулеин-индуцированного острого панкреатита и связанного с панкреатитом повреждения легких. Гастроэнтерология. 2001. 121 (1): 184–94. [PubMed] [Google Scholar] 82. Паломарес О. Роль регуляторных Т-клеток в IgE-опосредованной пищевой аллергии. J Исследование Allergol Clin Immunol. 2013. 23 (6): 371–82. quiz 2 p перед 382. [PubMed] [Google Scholar] 83. Эйгенманн П.А., Фроссар С.П.Т-лимфоциты при расстройствах пищевой аллергии. Curr Opin Allergy Clin Immunol. 2003. 3 (3): 199–203. [PubMed] [Google Scholar]диетических вмешательств при панкреатите – Today’s Dietitian Magazine
Июнь / Июль 2020 Выпуск
Диетические вмешательства при панкреатите
Автор: Carrie Dennett, MPH, RDN, CD
Сегодняшний диетолог
Vol. 22, № 6, стр. 24
Питание играет ключевую роль в спасении жизней и сохранении качества жизни.
И острый, и хронический панкреатит представляют собой серьезное бремя для здоровья и системы здравоохранения. Острый панкреатит является одной из наиболее частых желудочно-кишечных причин госпитализации в США, а хронический панкреатит значительно ухудшает качество жизни1. Как в условиях неотложной помощи, так и в амбулаторных условиях питание является ключевым фактором в лечении этих состояний.
Панкреатит – это воспаление поджелудочной железы – большой железы, которая выделяет пищеварительные соки в тонкий кишечник и высвобождает гормоны инсулин и глюкагон в кровоток – которое возникает, когда пищеварительные ферменты начинают переваривать саму поджелудочную железу.И острый, и хронический панкреатит являются серьезными заболеваниями, которые иногда могут привести к опасным для жизни осложнениям.
Острый панкреатит возникает внезапно, чаще всего проявляется болью от легкой до сильной в верхней части живота, которая может распространяться на спину, грудь или бока. Интенсивность и локализация боли не коррелируют с ее тяжестью. Также могут присутствовать жар, тошнота и рвота.2
В 40–70% случаев основной причиной являются камни в желчном пузыре, которые могут вызвать воспаление, поскольку они проходят через желчный или панкреатический проток и застревают.Сильное употребление алкоголя – более 50 г в день в течение более пяти лет – составляет от 25% до 35% случаев. Острый панкреатит также может возникать у людей с уровнем триглицеридов выше 1000 мг / дл или у людей с доброкачественными или злокачественными опухолями поджелудочной железы, причем последнее особенно важно, когда панкреатит является идиопатическим, т. Е. Не имеет идентифицируемой причины2
В Соединенных Штатах ежегодно более 270 000 госпитализаций связаны с острым панкреатитом.3,4 Случаи заболевания классифицируются как легкие, средние и тяжелые, а общая смертность колеблется от 5% до 30% в зависимости от степени тяжести.3 При лечении острый панкреатит легкой степени обычно проходит в течение нескольких дней; тем не менее, от 15% до 20% случаев являются тяжелыми, для разрешения которых требуется больше времени и требуется более длительное пребывание в больнице2
Считается, что иммунная система играет роль в прогрессировании острого панкреатита – у некоторых пациентов высвобождение провоспалительных медиаторов, вызванное самовоспалительным перевариванием поджелудочной железы, может вызвать некротический панкреатит и нарушение барьера тонкой кишки. Это делает возможным бактериальную транслокацию, которая, в свою очередь, может привести к синдрому системной воспалительной реакции и синдрому полиорганной дисфункции.5
Рецидивирующие эпизоды острого панкреатита могут привести к хроническому панкреатиту, которым страдают от 42 до 73 из 100000 взрослых в США, 6 что приводит к 86000 госпитализаций в год.7 Хотя прогрессирование хронического панкреатита варьируется и может включать длительные периоды без симптомов, состояние со временем ухудшается, что приводит к необратимым повреждениям. Симптомы могут включать боль в животе, а при наличии боли она может стать постоянной и более сильной после еды. По иронии судьбы, по мере того, как состояние прогрессирует, боль может отступать.7
Другие симптомы включают тошноту, рвоту, диарею, жирный и зловонный стул и потерю веса. При обострениях лечение хронического панкреатита аналогично лечению острого панкреатита.7
Постоянные боли в животе, рубцы поджелудочной железы, диабет и рак поджелудочной железы могут быть осложнениями хронического панкреатита. Также могут возникать нарушения пищеварения, недоедания и мальабсорбции, потенциально приводящие к остеопении и остеопорозу, что, в свою очередь, может привести к переломам костей.8
Мужчины и чернокожие американцы подвергаются более высокому риску, как и люди, у которых в семейном или личном анамнезе были камни в желчном пузыре или семейный анамнез панкреатита. Помимо чрезмерного употребления алкоголя и высокого уровня триглицеридов, причины могут включать высокий уровень кальция в крови, генетические нарушения поджелудочной железы и прием некоторых лекарств.8 Наличие целиакии увеличивает риск хронического панкреатита, в частности подтипа, известного как аутоиммунный панкреатит, за счет примерно в три раза, а люди с воспалительным заболеванием кишечника и другими аутоиммунными заболеваниями также имеют повышенный риск.9
У людей с муковисцидозом может быть хронический панкреатит без боли из-за недостаточности поджелудочной железы. Токсины окружающей среды, такие как продолжающееся употребление алкоголя и табака, способствуют прогрессированию хронического панкреатита.7
Диагностика и лечение
Рекомендации Американского колледжа гастроэнтерологии утверждают, что диагноз острого панкреатита определяется наличием двух из этих трех критериев: боль в верхней части живота, уровень амилазы и / или липазы в сыворотке, превышающий верхний предел нормы и характерные результаты визуализации брюшной полости.Уровни липазы в сыворотке предпочтительнее, чем уровни амилазы в сыворотке, потому что они остаются повышенными дольше после начала заболевания2
Легкие случаи определяются отсутствием органной недостаточности и / или некроза поджелудочной железы. В умеренно тяжелых случаях наблюдаются местные осложнения, включая некроз, но без стойкой органной недостаточности. В тяжелых случаях есть две отдельные фазы. Ранняя фаза, в течение первой недели, характеризуется синдромом системной воспалительной реакции и / или органной недостаточностью, тяжесть которой определяется органной недостаточностью.Вторая фаза характеризуется местными осложнениями. Поскольку у большинства пациентов с тяжелым панкреатитом на момент госпитализации нет органной недостаточности или некроза, у них может быть неточно диагностировано легкое заболевание, что откладывает необходимое лечение.2
Не существует единого теста, который бы однозначно диагностировал хронический панкреатит. Обычно это подозревается, если у пациента есть боль в верхней части живота, постоянное употребление алкоголя или табака, острый панкреатит в анамнезе и семейный анамнез панкреатита, а затем подтверждается с помощью компьютерной томографии или МРТ.7,10 Тестирование функции поджелудочной железы часто используется в качестве дополнительной меры. Поскольку эндоскопическое ультразвуковое исследование является инвазивным и недостаточно специфичным, оно рекомендуется только в том случае, если поперечное сечение не может подтвердить диагноз.10
Лечение хронического панкреатита основано на обезболивании, лечении панкреатической недостаточности и лечении осложнений.11 Обезболивание с помощью медицинских или, реже, хирургических средств является одним из первых шагов в лечении хронического панкреатита, за которым следуют алкоголь и курение. прекращение, если применимо.6
Если продолжающегося лечения с помощью заместительной терапии ферментами поджелудочной железы (PERT) и питания недостаточно, могут быть назначены ингибиторы протонной помпы, чтобы помочь предотвратить денатурирование желудочной кислотой липазы поджелудочной железы. Более чем у половины пациентов с хроническим панкреатитом развивается диабет, известный как панкреатогенный диабет или диабет типа 3c, из-за потери массы островковых клеток в поджелудочной железе, что, в свою очередь, увеличивает риск рака поджелудочной железы. Медикаментозное лечение диабета, вторичного по отношению к панкреатиту, обычно включает прием препаратов, повышающих чувствительность к инсулину, таких как метформин, наряду с PERT.9
Лечение легкого острого панкреатита обычно включает кратковременное пребывание в больнице для внутривенного введения жидкостей, обезболивающих и антибиотиков, если есть инфекционные осложнения, но не профилактически.2,12 Тяжелый острый панкреатит требует более длительного пребывания в больнице.
Некоторым пациентам с острым панкреатитом или обострениями хронического панкреатита могут потребоваться хирургические вмешательства для удаления закупорки, включая камни в желчном пузыре, или лечения сужения протоков поджелудочной железы или желчных протоков.Некоторым пациентам требуется хирургическое удаление некротизированной ткани и, в более редких случаях, удаление желчного пузыря или поджелудочной железы.2,13 Из-за сложной этиологии и различных клинических проявлений острого панкреатита найти лекарственное лечение было непросто.5
Диетическое лечение острого панкреатита
Что составляет оптимальную нутритивную поддержку при остром панкреатите, обсуждается на протяжении десятилетий. Обычным лечением было NPO (ничего не перорально), чтобы дать поджелудочной железе отдохнуть – несмотря на отсутствие клинических данных, подтверждающих это, 2,5 с большинством руководящих принципов, рекомендующих NPO до исчезновения боли и некоторой отсрочки перорального кормления до нормализации уровня ферментов поджелудочной железы или воспаления. стихает.2
Однако это способствует возникновению множества других проблем, включая недостаточность питания и катаболизм из-за ограничения потребления энергии в то время, когда потребности организма в энергии увеличиваются.5 Фактически, новые рекомендации, представленные Европейским обществом клинического питания и метаболизма ( ESPEN) Конгресс в прошлом году заявил, что все пациенты с прогнозируемым острым панкреатитом легкой и средней степени тяжести должны проходить скрининг на предмет риска, связанного с питанием, и что пациенты с прогнозируемым тяжелым острым панкреатитом всегда должны считаться находящимися в группе риска, связанного с питанием.14
Поскольку недостаточность питания вызывает особую озабоченность при тяжелом остром панкреатите, полное парентеральное питание (ПП) стало стандартной практикой для обеспечения питания без стимуляции поджелудочной железы.15 Однако это также предотвращает стимуляцию кишечника, и этот отдых кишечника связан с атрофия слизистой оболочки кишечника, которая ухудшает барьерную функцию тонкого кишечника примерно у 60% пациентов, что приводит к потенциально серьезным осложнениям.2,5 ППП не только не способствует здоровью кишечника, но и существует риск инфекций, исходящих из центрального венозного катетера.16
У пациентов, которые не переносят пероральное кормление, энтеральное питание (ЭП) помогает защитить слизистую кишечника и предотвращает избыточный бактериальный рост за счет стимуляции перистальтики кишечника. 5,15 A 2010 Кокрановский обзор показал, что ЭП более вероятно, чем ПП снижение системных инфекций, полиорганной недостаточности и смерти15. Систематический обзор 11 рандомизированных контролируемых исследований в 2009 г. показал аналогичные результаты. Однако исследователи отметили, что, хотя ЭП приводило к лучшим результатам, чем ПП, когда нутритивная поддержка была начата в течение 48 часов после поступления, не было разницы между ЭП и ППП, когда питание откладывалось более чем на 48 часов.Предполагается, что это произошло из-за повсеместного влияния отложенного питания17.
Таким образом, хотя EN может давать лучшие результаты, чем TPN, также оказывается, что лучше проводить EN раньше, чем позже. Несколько исследований показали, что начало ЭП в течение 48 часов после госпитализации по сравнению с ожиданием более 48 часов снижает уровень серьезной инфекции и, в некоторых случаях, смертность.17-20 Это соответствует рекомендациям обществ питания в США. Государства и Европа, включая Американское общество парентерального и энтерального питания, ESPEN и журнал Journal of Parenteral and Enteral Nutrition .14,21 В этих рекомендациях рекомендуется ранняя ЭП у всех пациентов с тяжелым острым панкреатитом, использование ПП только в тех случаях, когда ЭП не переносится или неосуществимо.
При введении ЭП пациентам с панкреатитом традиционно предпочтительным является назоеюнальный путь – доставка питания к тощей кишке тонкой кишки, поскольку он резко снижает стимуляцию поджелудочной железы, но при этом способствует перистальтике кишечника2,5,15. их труднее поместить в пациентов, что требует специального персонала и увеличивает расходы.22 Недавние исследования показали, что кормление через назогастральный зонд кажется безопасным, и Международная ассоциация панкреатологов и Американская ассоциация поджелудочной железы рекомендуют использовать любой из этих методов.3
Систематический обзор и метаанализ 2014 года показали, что назогастральное кормление было эффективным у 90% пациентов с тяжелым острым панкреатитом, обеспечивая адекватное питание без увеличения частоты таких осложнений, как диарея, вздутие живота или обострение боли 22 A 2020 Обзор Cochrane показал, что имеющихся данных недостаточно, чтобы показать преимущества или недостатки любого из режимов зондового питания.23
А как насчет перорального кормления? Многоцентровое исследование 2014 года в Нидерландах рандомизировало пациентов с тяжелым острым панкреатитом с высоким риском осложнений, которые получали либо ЭП в течение 24 часов после поступления, либо пероральную диету через 72 часа. Пациенты, которым назначена пероральная диета, получали жидкости внутривенно в течение первых 72 часов, и, если пероральная диета не переносилась через 72 часа, ее снова предлагали через 96 часов; если все еще не переносился, предлагался ЭН. Исследователи не обнаружили разницы в частоте серьезных инфекций – некроза поджелудочной железы, пневмонии или бактерий в кровотоке – или смерти в течение шести месяцев после госпитализации.Они также не увидели различий в уровне воспалительной реакции16 – примечательно, потому что уменьшение этой реакции было предположено как преимущество раннего кормления согласно EN.19
.Вопрос о том, когда начинать пероральное кормление у пациентов с острым панкреатитом легкой степени, имеет более четкий ответ.24-26 Одно рандомизированное клиническое исследование показало, что немедленное пероральное кормление у пациентов с легким острым панкреатитом ускоряет выздоровление без неблагоприятных желудочно-кишечных эффектов26. Исследование показало, что твердая диета с низким содержанием жиров переносится, а также прозрачная жидкая диета у пациентов с легкими формами заболевания, но не приводит к сокращению срока пребывания в больнице, как предполагалось.24 Однако рандомизированное контролируемое исследование 2010 г. показало, что пациенты, начавшие на полностью твердую диету, имели более короткий срок пребывания в больнице, чем пациенты, начавшие на чистой жидкой диете или мягкой диете.25
Соответственно, для пациентов с прогнозируемым острым панкреатитом легкой степени новые рекомендации ESPEN, а также рекомендации Американского колледжа гастроэнтерологии рекомендуют начинать пероральное кормление с твердой диеты с низким содержанием жиров, как только она будет перенесена, поскольку это может ускорить выздоровление, с предпочтением EN, а не TPN если не терпят.14,26,27
Когда EN является подходящим вмешательством, какая формулировка лучше всего? Полимер с неповрежденным белком, углеводами и длинноцепочечными жирными кислотами? Олигомер, также известный как элементарный или полуэлементный, с пептидами и свободными аминокислотами, моносахаридами, среднецепочечными и свободными жирными кислотами? Специальная формула с противовоспалительными иммунонутриентами, такими как глутамин и омега-3 жирные кислоты, или формула с пребиотиками и пробиотиками?
A 2015 Кокрановский обзор обнаружил недостаточные доказательства, чтобы рекомендовать какой-либо конкретный тип рецептуры EN.В частности, доказательства эффективности и безопасности иммунонутриентов были низкого или очень низкого качества, а исследования пробиотиков в лечении острого панкреатита дали непоследовательные – даже противоречивые – результаты, особенно в отношении безопасности28. Соответственно, Международная ассоциация панкреатологов этого не делает. Не рекомендую использовать пробиотики для уменьшения инфекционных осложнений, отчасти потому, что существуют значительные различия в типах и дозировках пробиотических добавок. В одном рандомизированном контролируемом исследовании использование конкретной комбинации или пробиотических штаммов не предотвратило осложнений, но увеличило смертность.3 Суть? При условии, что формула не содержит пробиотиков или иммунонутриентов, выбор между полимерными и олигомерными формулами будет в значительной степени основываться на переносимости пациентом.
Диетическое лечение хронического панкреатита
Хронический панкреатит требует другого подхода к питанию с постоянным лечением, которое включает питание, дополнительные пищеварительные ферменты и отказ от табака и алкоголя. Недоедание часто встречается у пациентов с хроническим панкреатитом из-за множества факторов, в том числе следующих 14,27,29:
• повышенный расход энергии в сочетании с связанной с болью потерей аппетита и / или страхом перед едой;
• недостаточность ферментов поджелудочной железы;
• задержка опорожнения желудка; и
• продолжающееся злоупотребление алкоголем.
Низкий уровень липазы поджелудочной железы может снизить всасывание пищевых жиров и жирорастворимых питательных веществ (витаминов A, D, E, K), вызывая вздутие живота, диарею или жирный стул, что приводит к дальнейшему предотвращению жира и препятствует адекватному потреблению энергии. Недостаточный уровень протеазы поджелудочной железы может привести как к белковой недостаточности, так и к дефициту витамина B12, а хроническое воспаление может препятствовать использованию белка организмом.30
Пациенты с хроническим панкреатитом – даже те, кто не злоупотребляет алкоголем – чаще страдают дефицитом питательных микроэлементов, чем пациенты без этого заболевания.Маркеры обновления и формирования костной ткани также ниже, 30 и сообщается о специфическом дефиците кальция, магния, цинка, тиамина и фолиевой кислоты27. PERT помогает минимизировать дефицит, но некоторым пациентам необходимо будет принимать дополнительные формы питательных микроэлементов, на которые он влияет. состояние 27,30
Давний совет ограничить употребление жиров в рационе больше не рекомендуется, в основном потому, что это снижает секрецию ферментов поджелудочной железы и может снизить эффективность дополнительных ферментов поджелудочной железы.Кроме того, ограничение пищевых жиров может маскировать начало мальабсорбции жира, которое проявляется в виде жира в стуле (стеаторея) 31 и увеличивает риск обострения потери веса и дефицита жирорастворимых витаминов.9
ESPEN рекомендует употреблять пищу с высоким содержанием белка и калорий, состоящую из пяти-шести небольших приемов пищи в день, избегая при этом диет с очень высоким содержанием клетчатки, поскольку клетчатка может поглощать или блокировать действие липазы поджелудочной железы, что приводит к снижению потребления питательных веществ. Нет необходимости ограничивать потребление жиров, если только невозможно контролировать стеаторею.14,32 Потребление белка от 1 до 1,5 г / кг обычно достаточно и хорошо переносится. В более чем 80% случаев достаточно пищи, дополненной ферментами поджелудочной железы перед каждым приемом пищи и перекуса, в то время как от 10% до 15% требуют пероральных пищевых добавок – на основе цельного белка, если переносится, и на основе пептидов, если нет, а 5% нуждаются в ЭП. Пациенты с риском непреднамеренной потери веса могут принимать добавки со среднецепочечным триглицеридом (MCT), которое всасывается непосредственно в кровоток без потребности в ферментах поджелудочной железы.Масло 27 MCT содержится в кокосовом и пальмоядровом маслах, а также в виде добавок.
Заключительные мысли
Хотя медицинские, а иногда и хирургические вмешательства важны для лечения острого и хронического панкреатита, питание также играет решающую роль в предотвращении осложнений и сохранении качества жизни.
– Кэрри Деннетт, магистр здравоохранения, RDN, CD, обозреватель по вопросам питания в журнале The Seattle Times , владелец журнала Nutrition By Carrie и автор книги Healthy for Your Life: A Holistic Guide to Optimal Wellness .
Ссылки
1. Ядав Д., Ловенфельс А.Б. Эпидемиология панкреатита и рака поджелудочной железы. Гастроэнтерология . 2013; 144 (6): 1252-1261.
2. Теннер С., Бэйли Дж., ДеВитт Дж., Ведж С.С.; Американский колледж гастроэнтерологии. Рекомендации Американского колледжа гастроэнтерологии: ведение острого панкреатита. Am J Гастроэнтерол . 2013; 108 (9): 1400-1415.
3. Рекомендации Рабочей группы IAP / APA по острому панкреатиту.Рекомендации IAP / APA по лечению острого панкреатита, основанные на фактических данных. Панкреатология . 2013; 13 (4 Дополнение 2): e1-e15.
4. Forsmark CE, Vege SS, Wilcox CM. Острый панкреатит. N Engl J Med . 2016; 375 (20): 1972-1981.
5. Пан Л.Л., Ли Дж., Шамун М., Бхатиа М., Сан Дж. Последние достижения в области питания при лечении острого панкреатита. Фронт Иммунол . 2017; 8: 762.
6. Сингх В.К., Ядав Д., Гарг П.К.Диагностика и лечение хронического панкреатита: обзор. JAMA . 2019; 322 (24): 2422-2434.
7. Кетвару Г.А., Фридман С.Д., Шет С.Г. Подход к пациентам с подозрением на хронический панкреатит: всесторонний обзор. Поджелудочная железа . 2015; 44 (2): 173-180.
8. Определения и факты о панкреатите. Веб-сайт Национального института диабета, болезней органов пищеварения и почек. https://www.niddk.nih.gov/health-information/digestive-diseases/pancreatitis/definition-facts.Обновлено в ноябре 2017 г.
9. Pham A, Forsmark C. Хронический панкреатит: обзор и обновление этиологии, факторов риска и лечения. F1000Res . 2018; 7: F1000 Faculty Rev-607.
10. Гарднер Т.Б., Адлер Д.Г., Форсмарк CE, Зауэр Б.Г., Тейлор Дж. Р., Уиткомб, округ Колумбия. Клинические рекомендации АЧГ: хронический панкреатит. Am J Гастроэнтерол . 2020; 115 (3): 322-339.
11. Джалал М., Кэмпбелл Дж. А., Хоппер А. Д.. Практическое руководство по лечению хронического панкреатита. Frontline Gastroenterol . 2019; 10 (3): 253-260.
12. Крокетт С.Д., Вани С., Гарднер ТБ, Фальк-Иттер Ю., Баркун А.Н.; Комитет по клиническим рекомендациям Института Американской гастроэнтерологической ассоциации. Руководство института Американской гастроэнтерологической ассоциации по начальному ведению острого панкреатита. Гастроэнтерология . 2018; 154 (4): 1096-1101.
13. Лечение панкреатита. Веб-сайт Национального института диабета, болезней органов пищеварения и почек.https://www.niddk.nih.gov/health-information/digestive-diseases/pancreatitis/treatment. Обновлено в ноябре 2017 г.
14. Безмаревич М; Европейское общество клинического питания и метаболизма. Руководство ESPEN по нутриционной поддержке при заболеваниях поджелудочной железы (острый и хронический панкреатит). http://www.espen.org/presfile/Bezmarevic_2019.pdf. Опубликовано 2019.
15. Аль-Омран М., Альбалави Ж.Х., Ташканди М.Ф., Аль-Ансари Л.А. Энтеральное и парентеральное питание при остром панкреатите. Кокрановская база данных Syst Rev . 2010; (1): CD002837.
16. Баккер О.Дж., ван Бруншот С., ван Сантворт Х.С. и др. Раннее кормление через назоэнтерический зонд в сравнении с кормлением по требованию при остром панкреатите. N Engl J Med . 2014; 371 (21): 1983–1993.
17. Петров М.С., Пилипчук Р.Д., Учугина А.Ф. Систематический обзор сроков искусственного питания при остром панкреатите. Br J Nutr . 2009; 101 (6): 787-793.
18.Ли JY, Yu T, Chen GC и др. Энтеральное питание в течение 48 часов после поступления улучшает клинические исходы острого панкреатита за счет уменьшения осложнений: метаанализ. PLoS One . 2013; 8 (6): e64926.
19. Sun JK, Mu XW, Li WQ, Tong ZH, Li J, Zheng SY. Влияние раннего энтерального питания на иммунную функцию пациентов с тяжелым острым панкреатитом. Мир Дж. Гастроэнтерол . 2013; 19 (6): 917-922.
20. Wereszczynska-Siemiatkowska U, Swidnicka-Siergiejko A, Siemiatkowski A, Dabrowski A.Раннее энтеральное питание превосходит отложенное энтеральное питание для предотвращения инфицированного некроза и смертности при остром панкреатите. Поджелудочная железа . 2013; 42 (4): 640-646.
21. Мирталло Дж. М., Форбс А., Макклейв С. А., Дженсен Г. Л., Вайцберг Д. Л., Дэвис А. Р.. Международные согласованные рекомендации по диетотерапии при панкреатите. JPEN J Parenter Enteral Nutr . 2012; 36 (3): 284-291.
22. Нэлли Д.М., Келли Э.Г., Кларк М., Риджуэй П.Назогастральное питание эффективно при тяжелом остром панкреатите: систематический обзор и метаанализ. Br J Nutr . 2014; 112 (11): 1769-1778.
23. Датта А.К., Гоэль А., Кирубакаран Р., Чако А., Тариан П. Сравнение назогастрального и назоеюнального зондового питания при тяжелом остром панкреатите. Кокрановская база данных Syst Rev . 2020; (3): CD010582.
24. Якобсон BC, Вандер Влит МБ, Хьюз М.Д., Маурер Р., Макманус К., Бэнкс, Пенсильвания. Проспективное рандомизированное исследование прозрачных жидкостей в сравнении с твердой диетой с низким содержанием жиров в качестве начального приема пищи при легком остром панкреатите. Клин Гастроэнтерол Гепатол . 2007; 5 (8): 946-951.
25. Moraes JM, Felga GE, Chebli LA, et al. Полноценная твердая диета в качестве начального приема пищи при остром панкреатите легкой степени является безопасной и сокращает продолжительность госпитализации: результаты проспективного рандомизированного контролируемого двойного слепого клинического исследования. Дж Клин Гастроэнтерол . 2010; 44 (7): 517-522.
26. Eckerwall GE, Tingstedt BB, Bergenzaun PE, Andersson RG. Немедленное пероральное кормление у пациентов с острым панкреатитом легкой степени безопасно и может ускорить выздоровление – это рандомизированное клиническое исследование. Clin Nutr . 2007; 26 (6): 758-763.
27. Meier R, Ockenga J, Pertkiewicz M, et al. Руководство ESPEN по энтеральному питанию: поджелудочная железа. Clin Nutr . 2006; 25 (2): 275-284.
28. Поропат Г., Гиляца В., Хаузер Г., Штимац Д. Составы для энтерального питания при остром панкреатите. Кокрановская база данных Syst Rev . 2015; (3): CD010605.
29. О’Брайен С.Дж., Омер Э. Хронический панкреатит и диетотерапия. Nutr Clin Pract . 2019; 34 Приложение 1: S13-S26.
30. Грир Дж. Б., Грир П., Сандху Б. С. и др. Питание и воспалительные биомаркеры у больных хроническим панкреатитом. Nutr Clin Pract . 2019; 34 (3): 387-399.
31. Домингес-Муньос Дж. Э., Филлипс М. Нутритивная терапия при хроническом панкреатите. Гастроэнтерол Клин Норт Ам . 2018; 47 (1): 95-106.
32. Арванитакис М., Окенга Дж., Безмаревич М. и др.Руководство ESPEN по лечебному питанию при остром и хроническом панкреатите. Clin Nutr . 2020; 39 (3): 612-631.
Хронический панкреатит | MUSC Health
Что такое хронический панкреатит?
Хронический панкреатит отличается от острого панкреатита тем, что воспаление и повреждение развиваются медленнее и со временем могут ухудшаться. Поджелудочная железа покрывается рубцами и теряет способность вырабатывать достаточное количество пищеварительных ферментов и инсулина.Утолщение сока поджелудочной железы может привести к закупорке протоков поджелудочной железы и камням поджелудочной железы, что, наряду с повреждением самих протоков, может привести к обострению панкреатита из-за непроходимости.
Когда у многих членов семьи возникает хронический панкреатит, иногда начинающийся с приступов в детстве, это называется семейным панкреатитом. Подобная форма хронического панкреатита встречается в тропических странах и часто связана с тяжелым недоеданием.
Внешний вид и клинические особенности
Большинство пациентов с хроническим панкреатитом испытывают боль в верхней части живота, которая также может ощущаться в спине.Это может быть очень тяжелым и продолжительным, но чаще бывает перемежающимся и возникает при приступах, которые обычно не достаточно серьезны, чтобы требовать немедленного лечения в больнице. Некоторые пациенты с хроническим панкреатитом никогда не испытывают боли.
Недостаток ферментов из-за повреждения поджелудочной железы приводит к плохому перевариванию и усвоению пищи, особенно жиров. Таким образом, похудание характерно для хронического панкреатита. Пациенты могут заметить объемный стул с неприятным запахом из-за слишком большого количества жира (стеаторея).Иногда на туалетной воде можно увидеть «масляное пятно».
Отек и рубцевание поджелудочной железы могут повредить другие локальные структуры. Если желчный проток сужен, у пациента может развиться желтуха. Воспаление большой вены (селезеночной вены) за поджелудочной железой может вызвать повышение давления в венах в другом месте и развитие варикозного расширения вен в верхнем отделе желудка и нижнем отделе пищевода; они могут лопнуть и вызвать сильное кровотечение.
Пациенты с хроническим панкреатитом имеют несколько повышенный риск развития рака поджелудочной железы.
Распознавание и доработка
Диагноз хронического панкреатита очевиден в запущенном случае с типичными признаками: болями в верхней части живота с потерей веса; стеаторея; и диабет. Однако все эти особенности видны только тогда, когда болезнь присутствует много лет.
Большинство пациентов жалуются только на боль. Подобные боли могут быть вызваны раком поджелудочной железы (хотя обычно он не перемежается), желчными камнями и камнями желчных протоков или тяжелыми типами язвы желудка или двенадцатиперстной кишки.Необходимо учитывать все эти условия и применять соответствующие диагностические тесты.
Эндоскопическое ультразвуковое исследование – это метод, используемый для выявления тонких и ранних изменений хронического панкреатита, в то время как ERCP широко используется для оценки и лечения пациентов с известным или подозреваемым хроническим панкреатитом. Хронический панкреатит может быть подтвержден рентгенологическими исследованиями, ультрасонографией, компьютерной томографией и MRCP.
Менеджмент
Больных хроническим панкреатитом лечат:
- воздержание от алкоголя;
- лекарств для снятия боли;
- нутритивная поддержка; и,
- Восполнение (перорально) недостающих пищеварительных ферментов.
Пациентам обычно рекомендуется придерживаться диеты с низким содержанием жиров (менее 40 г в день) при наличии стеатореи. Добавки ферментов поджелудочной железы следует принимать в высоких дозах и во время еды (часто с лекарствами, снижающими кислотность желудочного сока). Они помогают переваривать жир, а также иногда могут уменьшить боль.
Обезболивание может быть проблемой у пациентов с тяжелым хроническим панкреатитом. Наркотическая зависимость – это риск. Можно заблокировать нервы, выходящие из поджелудочной железы, с помощью инъекций (блокада чревного сплетения).Однако эффект редко длится дольше нескольких месяцев.
Хирургическое лечение может быть полезным при определенных обстоятельствах, особенно для снятия обструкции протока поджелудочной железы или желчного протока или для удаления поврежденной или плохо дренированной ткани поджелудочной железы. Наиболее частыми операциями являются процедуры Пестоу и Уиппла или дистальная резекция поджелудочной железы. (Редко требуется удаление всей поджелудочной железы.) У некоторых пациентов с хроническим панкреатитом есть псевдокисты, которые иногда требуют хирургического дренирования.
МетодыERCP имеют ограниченное применение при лечении пациентов с хроническим панкреатитом, хотя иногда ERCP помогает улучшить дренаж поджелудочной железы путем удаления камней или установки стентов. Это также может помочь при подтекании жидкостей поджелудочной железы (свищах поджелудочной железы).
Свищ поджелудочной железы
Свищи – это вытекание жидкости из внутреннего органа на кожу. Это происходит, когда соки не могут стекать обычным путем. В случае свищей поджелудочной железы это происходит при закупорке протока поджелудочной железы, особенно после травмы поджелудочной железы или хирургического вмешательства на ней.
Хотя многие свищи самопроизвольно высыхают через несколько недель, этот процесс можно ускорить с помощью инъекций лекарства, снижающего выработку сока поджелудочной железы. Во многих случаях необходимо будет разблокировать поджелудочную железу хирургическим методом или различными методами ЭРХПГ.
Острый панкреатит – Американский семейный врач
1. Руссо MW, Вэй JT, Тонкий МТ, и другие. Статистика болезней органов пищеварения и печени, 2004. Гастроэнтерология .2004; 126 (5): 1448–1453 ….
2. Singla A, Чикеш Н.Г., Саймонс Дж. П., и другие. Объем общенациональных больниц при остром панкреатите: анализ общенациональной стационарной выборки за 1998–2006 гг. Е.П.Б. (Оксфорд) . 2009. 11 (5): 391–397.
3. Гарднер ТБ. Острый панкреатит. Сентябрь 2013 г. http://emedicine.medscape.com/article/181364-overview. По состоянию на 20 июня 2014 г.
4. Mitchell RM, Бирн М.Ф., Бэйли Дж.Панкреатит. Ланцет . 2003. 361 (9367): 1447–1455.
5. Уиткомб, округ Колумбия, Ядав Д, Адам С, и другие. Североамериканская группа по изучению поджелудочной железы. Многоцентровый подход к рецидивирующему острому и хроническому панкреатиту в США: Североамериканское исследование панкреатита 2 (NAPS2). Панкреатология . 2008. 8 (4–5): 520–531.
6. Паренти Д.М., Стейнберг В, Кан П. Инфекционные причины острого панкреатита. Поджелудочная железа . 1996. 13 (4): 356–371.
7. Дервенис С, Джонсон CD, Басси C, и другие. Диагностика, объективная оценка степени тяжести и лечение острого панкреатита. Консенсусная конференция Санторини. Int J Pancreatol . 1999. 25 (3): 195–210.
8. Теннер С, Бэйли Дж, Девитт Дж. Vege SS. Рекомендации Американского колледжа гастроэнтерологии: ведение острого панкреатита [опубликованная поправка опубликована в Am J Gastroenterol.2014; 109 (2): 302]. Ам Дж. Гастроэнтерол . 2013. 108 (9): 1400–1415.
9. Gerhardt RT, Нельсон Б.К., Кинан С, Кернан Л, МакКерси А, Переулок МС. Вывод клинических рекомендаций по оценке неспецифической боли в животе: Руководство по оценке боли в животе в условиях реанимации (GAPEDS), фаза 1 исследования. Am J Emerg Med . 2005. 23 (6): 709–717.
10. Спитцер А.Л., Барсия А.М., Schell MT, и другие.Применение бритвы Оккама для прогнозирования панкреатита: модель прогнозирования с четырьмя переменными. Энн Сург . 2006. 243 (3): 380–388.
11. Смоткин Я., Теннер С. Лабораторные диагностические исследования при остром панкреатите. Дж. Клин Гастроэнтерол . 2002. 34 (4): 459–462.
12. Комитет по клинической практике и экономике Института Американской гастроэнтерологической ассоциации (AGA) «Управление острым панкреатитом»; Правление Института AGA.Заявление о медицинской позиции Института AGA по поводу острого панкреатита. Гастроэнтерология . 2007; 132 (5): 2019–2021.
13. Теннер С.М., Стейнберг В. Соотношение липаза: амилаза в сыворотке крови позволяет отличить алкогольный острый панкреатит от неалкогольного. Am J Gastroenterology . 1992. 87 (12): 1755–1758.
14. Neoptolemos JP, Кемппайнен Э.А., Майер Дж. М., и другие. Раннее прогнозирование тяжести острого панкреатита с помощью пептида активации трипсиногена в моче: многоцентровое исследование. Ланцет . 2000; 355 (9219): 1955–1960.
15. Американский колледж радиологии. Критерии соответствия ACR. Острый панкреатит. http://www.acr.org/~/media/ACR/Documents/APPCriteria/Diagnostic/AcutePancreatitis.pdf. По состоянию на 24 сентября 2014 г.
16. Jeffrey RB Jr. Сонография при остром панкреатите. Радиол Клин Норт Ам . 1989. 27 (1): 5–17.
17. Боллен Т.Л., Сингх ВК, Маурер Р, и другие. Сравнительная оценка радиологической и клинической систем оценки для раннего прогнозирования тяжести острого панкреатита. Ам Дж. Гастроэнтерол . 2012. 107 (4): 612–619.
18. Стимак Д, Милетич Д, Радич М, и другие. Роль неулучшенной магнитно-резонансной томографии в ранней оценке острого панкреатита. Ам Дж. Гастроэнтерол . 2007. 102 (5): 997–1004.
19. Чак А, Хос РХ, Купер GS, и другие. Проспективная оценка полезности EUS в оценке желчнокаменного панкреатита. Гастроинтест Эндоск . 1999. 49 (5): 599–604.
20. Ган С.И., Раджан Э, Адлер Д.Г., и другие. Комитет по стандартам практики ASGE. Роль EUS. Гастроинтест Эндоск . 2007. 66 (3): 425–434.
21. Хекимоглу К, Устундаг Y, Дусак А, и другие. MRCP против ERCP в оценке патологий желчевыводящих путей: обзор современной литературы. J Dig Dis . 2008. 9 (3): 162–169.
22. Кемппайнен Э.А., Hedström JI, Пуолаккайнен П.А., и другие. Быстрое определение трипсиногена-2 в моче в качестве скринингового теста на острый панкреатит. N Engl J Med . 1997. 336 (25): 1788–1793.
23. Арванитакис М, Дели М, De Maertelaere V, и другие. Компьютерная томография и магнитно-резонансная томография в оценке острого панкреатита. Гастроэнтерология . 2004. 126 (3): 715–723.
24. Брэдли Э.Л. III. Клинически обоснованная система классификации острого панкреатита. Резюме Международного симпозиума по острому панкреатиту, Атланта, Джорджия, 11–13 сентября 1992 г. Arch Surg . 1993. 128 (5): 586–590.
25. Банков П.А., Боллен Т.Л., Дервенис С, и другие. Рабочая группа по классификации острого панкреатита. Классификация острого панкреатита – 2012: пересмотр классификации и определений Атланты на основе международного консенсуса. Кишечник . 2013. 62 (1): 102–111.
26. Банки PA; Freeman ML; Комитет по параметрам практики Американского колледжа гастроэнтерологии. Практическое руководство при остром панкреатите. Ам Дж. Гастроэнтерол . 2006. 101 (10): 2379–2400.
27. Рэнсон Дж. Х. Этиологические и прогностические факторы острого панкреатита человека: обзор. Ам Дж. Гастроэнтерол . 1982. 77 (9): 633–638.
28. Knaus WA, Дрейпер EA, Вагнер Д.П., Zimmerman JE.APACHE II: система классификации тяжести заболевания. Crit Care Med . 1985. 13 (10): 818–829.
29. Уилсон К., Хит Д.И., Имри CW. Прогнозирование исходов при остром панкреатите: сравнительное исследование APACHE II, клинической оценки и многофакторных систем балльной оценки. Br J Surg . 1990. 77 (11): 1260–1264.
30. Knaus WA, Вагнер Д.П., Дрейпер EA, и другие. Прогностическая система APACHE III.Прогнозирование риска госпитальной смертности для тяжелобольных госпитализированных взрослых. Сундук . 1991. 100 (6): 1619–1636.
31. Баррето С.Г., Родригес Дж. Сравнение систем оценки APACHE II и Imrie для прогнозирования тяжести острого панкреатита. World J Emerg Surg . 2007; 2:33.
32. Balthazar EJ, Робинсон Д.Л., Мегибоу AJ, Рэнсон Дж. Х. Острый панкреатит: значение КТ для установления прогноза. Радиология . 1990. 174 (2): 331–336.
33. Balthazar EJ, Фрини ПК, ванСонненберг Э. Визуализация и вмешательство при остром панкреатите. Радиология . 1994. 193 (2): 297–306.
34. Леунг Т.К., Ли СМ, Лин С.Ю., и другие. Индекс тяжести компьютерной томографии Balthazar превосходит критерии Рэнсона и систему баллов APACHE II в прогнозировании исхода острого панкреатита. World J Gastroenterol .2005. 11 (38): 6049–6052.
35. Chatzicostas C, Roussomoustakaki M, Вардас Э, Романос Дж, Курумалис Э.А. Индекс тяжести компьютерной томографии Balthazar превосходит критерии Рэнсона и балльные системы APACHE II и III в прогнозировании исхода острого панкреатита. Дж. Клин Гастроэнтерол . 2003. 36 (3): 253–260.
36. Vriens PW, ван де Линде П., Slotema ET, Вармердам ЧП, Breslau PJ. Индекс тяжести компьютерной томографии – ранний прогностический инструмент острого панкреатита. J Am Coll Surg . 2005. 201 (4): 497–502.
37. Теннер С. Первичное ведение острого панкреатита: критические проблемы в течение первых 72 часов. Ам Дж. Гастроэнтерол . 2004. 99 (12): 2489–2494.
38. У БУ, Conwell DL. Острый панкреатит, часть I: подход к раннему лечению. Клин Гастроэнтерол Гепатол . 2010. 8 (5): 410–416.
39. Марик ЧП, Залога ГП. Метаанализ парентерального питания в сравнении с энтеральным питанием у пациентов с острым панкреатитом. BMJ . 2004; 328 (7453): 1407.
40. Аль-Омран М, Альбалави Ж., Ташканди МФ, Аль-Ансари Л.А. Энтеральное и парентеральное питание при остром панкреатите. Кокрановская база данных Syst Rev . 2010; (1): CD002837.
41. Mazaki T, Исии Y, Такаяма Т. Метаанализ профилактического применения антибиотиков при остром некротическом панкреатите. Br J Surg . 2006. 93 (6): 674–684.
42.Villatoro E, Мулла М, Ларвин М. Антибактериальная терапия для профилактики инфекции панкреонекроза при остром панкреатите. Кокрановская база данных Syst Rev . 2010; (5): CD002941.
43. Бесселинк МГ, ван Сантворт ХК, Бускенс Э, и другие. Голландская группа по изучению острого панкреатита. Профилактика пробиотиками при прогнозируемом тяжелом остром панкреатите: рандомизированное, двойное слепое, плацебо-контролируемое исследование [опубликованные поправки опубликованы в Lancet.2008; 371 (9620): 1246]. Ланцет . 2008. 371 (9613): 651–659.
44. Qiong W, Ипин W, Цзиньлинь Y, Тао Г, Чжэнь Г, Pengcheng Z. Китайские лекарственные травы при остром панкреатите. Кокрановская база данных Syst Rev . 2005; (1): CD003631.
45. Абулиан А, Чан Т, Ягубян А, и другие. Ранняя холецистэктомия безопасно сокращает время пребывания в стационаре у пациентов с желчнокаменным панкреатитом легкой степени: рандомизированное проспективное исследование. Энн Сург . 2010. 251 (4): 615–619.
46. Шарма В.К., Хауден CW. Метаанализ рандомизированных контролируемых исследований эндоскопической ретроградной холангиографии и эндоскопической сфинктеротомии для лечения острого билиарного панкреатита. Ам Дж. Гастроэнтерол . 1999. 94 (11): 3211–3214.
47. Аюб К, Имада Р, Славин Ю. Эндоскопическая ретроградная холангиопанкреатография при остром желчнокаменном панкреатите.

 Никакой жареной пищи в питании и диете быть не должно.
Никакой жареной пищи в питании и диете быть не должно. ). Особенно диета становится строгой при обострении болезни.
). Особенно диета становится строгой при обострении болезни.
 Именно поэтому панкреатит рассматривают как один из основных факторов риска развития сахарного диабета, а погрешности в питании – как важный предрасполагающий фактор.
Именно поэтому панкреатит рассматривают как один из основных факторов риска развития сахарного диабета, а погрешности в питании – как важный предрасполагающий фактор. В целом в этот период рацион напоминает меню при хроническом панкреатите. Вводятся растительные масла, блюда становятся более разнообразными.
В целом в этот период рацион напоминает меню при хроническом панкреатите. Вводятся растительные масла, блюда становятся более разнообразными.
 До приезда врача не рекомендован прием медикаментов, пищи и напитков, за исключением небольшого количества негазированной воды.
До приезда врача не рекомендован прием медикаментов, пищи и напитков, за исключением небольшого количества негазированной воды.



 в день;
в день;

