Острый отечный панкреатит: Nie znaleziono strony – Внутренняя Mедицина
Острый панкреатит: современная классификация и общие принципы лечения
В.Е. ВОЛКОВ, Л. И. ЧЕРКЕСОВ,
С.В. ВОЛКОВ, Н.Н. ЧЕСНОКОВА
ОСТРЫЙ ПАНКРЕАТИТ: СОВРЕМЕННАЯ КЛАССИФИКАЦИЯ
И ОБЩИЕ ПРИНЦИПЫ ЛЕЧЕНИЯ
Чувашский государственный университет имени И.Н. Ульянова, Чебоксары
Представлен ретроспективный анализ лечения 461 больного острым панкреатитом за 2009-2013 гг. Отечная (интерстициальная) форма острого панкреатита установлена у 378 (82%) пациентов, некротическая форма – у 83 (18%) пациентов. Дана оценка клинических исследований по идентификации локальных жидкостных скополений с учетом международной классификации острого панкреатита (2012). Общая летальность больных острым панкреатитом составила 6, 1%, при некротической форме панкреатита – 32, 1%.
Ключевые слова: острый панкреатит, классификация, диагностика, локальные перипанкреатические жидкостные скопления, лечение.
Острый панкреатит ‒ одно из наиболее распространенных заболеваний органов брюшной полости, объединяемых термином «острый живот».
Актуальность проблемы диагностики и лечения острого панкреатита обусловлена достаточно высокой летальностью, которая при некротической форме составляет 35-40% [2, 3]. Развитие различных осложнений, утяжеляет течение и ухудшает прогноз. У 20-30% пациентов острый панкреатит, неуклонно прогрессируя, приводит к развитию некроза ткани поджелудочной железы. При этом в 40-70% случаев уже через 3 недели с момента заболевания происходит инфицирование очагов некроза, что является ведущей причиной смерти больных острым панкреатитом. Необходимо отметить, что острым панкреатитом в большинстве случаев заболевают лица трудоспособного возраста. Высокие экономические затраты на лечение госпитализированных больных свидетельствуют о практической значимости данной проблемы.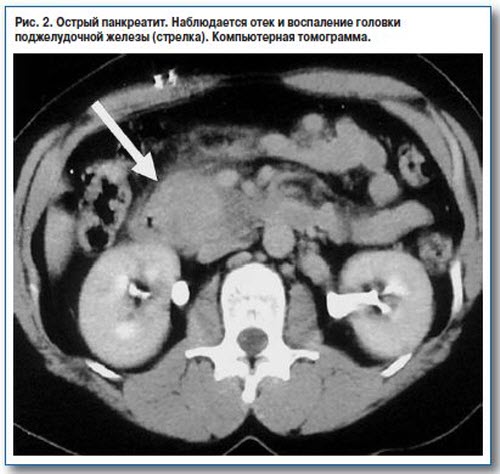
Цель: уточнить практическую значимость новой международной классификации острого панкреатита и представить критерии ранней диагностики локальных перипанкреатических жидкостных скоплений.
Материалы и методы исследования. Проведен ретроспективный анализ лечения 461 больного острым панкреатитом, находящихся на стационарном лечении в хирургическом отделении БУ «Больница скорой медицинской помощи» Минздрава Чувашии за 2009-2013 гг. Из 461 больного отечная форма острого панкреатита отмечена у 378 (82%) пациентов, некротическая форма – у 83 (18%) пациентов.
Результаты и их обсуждение.
 Другими причинами заболевания являются открытые и закрытые травмы поджелудочной железы, в том числе связанные с операциями, а также с инструментальными исследованиями. Сравнительно редко этиологическими факторами являются эндокринные заболевания, прием некоторых лекарственных средств и т.д.
Другими причинами заболевания являются открытые и закрытые травмы поджелудочной железы, в том числе связанные с операциями, а также с инструментальными исследованиями. Сравнительно редко этиологическими факторами являются эндокринные заболевания, прием некоторых лекарственных средств и т.д.Основными звеньями патогенеза острого панкреатита являются обструкция панкреатического протока с развитием внутрипротоковой гипертензии, а также активизация ферментов поджелудочной железы на фоне усиленной панкреатической секреции. Блокада большого дуоденального сосочка желчными конкрементами является фактором механической обструкции, что препятствует нормальному оттоку секрета поджелудочной железы. Употребление алкоголя приводит к спазму сфинктера Одди, отеку слизистой оболочки и усилению внешнесекреторной функции железы за счет повышенной секреции соляной кислоты. Внутрипротоковая гипертензия приводит к повреждению клеточных и субклеточных мембран, гиперсекреции и активации протеолитических ферментов, в первую очередь, трипсина, с выходом их в интерстициальное пространство и развитием аутолиза ткани поджелудочной железы.
- На основании морфологических признаков повреждения поджелудочной железы и клинических особенностей течения заболевания Рабочей Группой специалистов по изучению острого панкреатита в 2012 г. была предложена новая международная классификация острого панкреатита [5], которая включает следующие формы:
- Отечная форма (интерстициальный панкреатит).
- Асептический панкреонекроз.
- Инфицированный панкреонекроз.
- Фазы развития панкреонекроза:
- Доинфекционная;
- Инфекционная.

- Стадии панкреонекроза:
- Ранняя;
- Поздняя.
- Степень тяжести острого панкреатита:
- Легкая степень;
- Средняя степень;
- Тяжелая степень.
- Виды локальных осложнений острого панкреатита:
- Острое перипанкреатическое жидкостное скопление;
- Панкреатическая псевдокиста;
- Острое некротическое скопление;
- Отграниченный некроз.
Интерстициальный панкреатит характеризуются воспалительным отеком ткани поджелудочной железы вследствие попадания в интерстиций небольшого количества активных ферментов, тогда как при панкреонекрозе возникают очаги деструкции ткани с развитием множественных кровоизлияний. Инфицирование зон некроза приводит к развитию инфицированного панкреонекроза и возникновению инфекционных осложнений.
Острый панкреатит легкой степени тяжести характеризуется отсутствием органной недостаточности, локальных и системных осложнений.
Острый панкреатит средней тяжести характеризуется наличием транзиторной (преходящей) органной недостаточности с длительностью течения менее 48 ч или возникновением локальных и системных осложнений.
Тяжелая форма острого панкреатита характеризуется наличием персистирующей органной недостаточности с длительностью течения более 48 ч.
Локальные осложнения острого панкреатита могут возникать как в доинфекционную, так и в инфекционную фазу развития заболевания и, как правило, утяжеляют его течение.
Острое перипанкреатическое жидкостное скопление в большинстве случаев наблюдается в первые четыре недели от начала развития острого панкреатита и обычно состоит из того или иного количества экссудата без наличия некротических масс, образующегося вследствие воспалительного отека паренхимы поджелудочной железы, выхода панкреатического сока через сеть концевых панкреатических протоков. Чаще всего данный тип скопления остается стерильным и рассасывается самостоятельно на фоне проводимого лечения.
Длительность существования острого перипанкреатического жидкостного скопления (более четырех недель) и отграничение его от окружающих тканей грануляционной или фиброзной тканью завершается образованием другого локального осложнения острого панкреатита ‒ псевдокисты.
Острое некротическое скопление чаще всего возникает на фоне деструктивного процесса в поджелудочной железе. В отличие от указанных выше жидкостных образований данный тип скопления характеризуется наличием жидкости и некротического детрита. При отграничении острого некротического скопления от окружающих тканей появляется возможность формирования отграниченного некроза.
Оценивая в целом новую международную классификацию острого панкреатита (2012), следует отметить отсутствие в ней нередко встречающихся локальных гнойно-септических осложнений этого заболевания, многие из которых таят опасность развития таких опасных осложнений, как распространенный гнойный перитонит, гнойный плеврит, сепсис и септический шок, острая полиорганная недостаточность. С учетом этих данных мы различаем следующие локальные гнойно-септические осложнения острого некротического панкреатита:<> – Панкреатический гнойный инфильтрат;
С учетом этих данных мы различаем следующие локальные гнойно-септические осложнения острого некротического панкреатита:<> – Панкреатический гнойный инфильтрат;
– Абсцесс сальниковой сумки;
– Гнойно-некротическая секвестрация поджелудочной железы и забрюшинной клетчатки;
– Инфицированная псевдокиста;
– Сочетанные гнойно-септические осложнения.
Необходимо отметить, что более чем в 50% случаев отмечается сочетание локальных и распространенных гнойно-септических осложнений, утяжеляющих течение отсрого некротического панкреатита.
- Раннее распознавание острого панкреатита является залогом его эффективного лечения и благоприятного исхода. Согласно Международным рекомендациям 2012 г., диагностическими критериями острого панкреатита является триада признаков:
- Интенсивная абдоминальная боль опоясывающего характера с локализацией преимущественно в эпигастральной области;
- Увеличение уровня амилазы или липазы в 2-3 раза по сравнению с нормой;
- Характерные признаки поражения поджелудочной железы по данным УЗИ, КТ, МРТ.

Основными лабораторными признаками, свидетельствующими о вторичном инфицировании зон панкреатического некроза, являются нейтрофильный лейкоцитоз со сдвигом лейкоформулы влево, увеличение концентрации С-реактивного белка, прокальцитонина. На современном этапе целесообразно определение концентрации провоспалительных цитокинов ‒ ИЛ-1, ИЛ-6, TNF-альфа, трипсиноген-активированного белка, эластазы полиморфно-ядерных нейтрофилов, повышенный уровень которых свидетельствует о тяжелом течении острого панкреатита.
Наиболее информативными инструментальными методами диагностики острого панкреатита являются УЗИ, КТ, МРТ органов брюшной полости. УЗИ остается одним из наиболее доступных и информативных методов исследования. Эта безопасная неинвазивная методика позволяет выявить этиологический фактор острого панкреонекроза (конкременты желчевыводящих путей), отек и участки некроза поджелудочной железы, позволяет дифференцировать жидкостные образования. Но «золотым стандартом» диагностики на современном этапе является компьютерная томография органов брюшной полости. Данная методика позволяет четко визуализировать увеличение поджелудочной железы, очаги некроза, а также наличие осложнений, с высокой достоверностью разграничивать жидкостное скопление от плотных некротических масс. Наличие пузырьков газа в зоне деструкции, определяемое при КТ-исследовании, свидетельствует об инфицировании данного очага.
Данная методика позволяет четко визуализировать увеличение поджелудочной железы, очаги некроза, а также наличие осложнений, с высокой достоверностью разграничивать жидкостное скопление от плотных некротических масс. Наличие пузырьков газа в зоне деструкции, определяемое при КТ-исследовании, свидетельствует об инфицировании данного очага.
В настоящее время применяется дифференцированный подход к выбору лечебной тактики при остром панкреатите: от различных вариантов консервативного лечения в ранние сроки заболевания до разнообразных хирургических вмешательств при распространенных инфицированных формах панкреонекроза [1, 4].
Основными принципами консервативного лечения больных с острым панкреатитом являются:
‒ снижение панкреатической секреции, что достигается проведением тотального парентерального питания в течение первых 2-4 суток, декомпрессия желудка в течение 1-2 суток с помощью назогастрального зонда, назначение блокаторов Н2-рецепторов гистамина или ингибиторов протонной помпы, 5-фторурацила, соматостатина;
‒ инфузионная и дезинтоксикационная терапия с помощью введения коллоидных и кристаллоидных растворов внутривенно: от 3 до 5 литров и более в течение 3-7 дней;
‒ улучшение реологических свойств крови введением гепарина, реополиглюкина и т. д.;
д.;
‒ антибиотикотерапия с использованием препаратов широкого спектра действия (препараты выбора ‒ карбапенемы, цефалоспорины III-IV поколений или фторхинолоны II-III поколений в сочетании с метронидазолом). Показаниями к хирургическому лечению панкреонекроза являются наличие инфекционных осложнений, а также стойкая или прогрессирующая полиорганная недостаточность, сохраняющиеся симптомы системной воспалительной реакции независимо от факта инфицирования при проведении базисной консервативной терапии.
Использование консервативного и оперативного метода лечения позволило получить общую летальность у анализируемой группы больных панкреатитом в среднем 6, 1%, а при осложненных некротических формах ‒ 32, 1%.
- Литература
- Багненко С.Ф. Острый панкреатит современное состояние проблемы и нерешенные вопросы / С.Ф. Багненко, В.Р. Гольцов // Альманах института хирургии им. А.В. Вишневского, 2008. Т. 3 ‒ № 3 . ‒ С. 104-112.
- Волков В.Е. Острый некротический панкреатит / В.
 Е. Волков, С.В. Волков // Изд-во Чуваш. ун-та. 2009. ‒ 240 с.
Е. Волков, С.В. Волков // Изд-во Чуваш. ун-та. 2009. ‒ 240 с. - Волков В.Е. Ранняя диагностика и лечение локальных гнойно-септических осложнений у больных острым некротическим панкреатитом: учебное пособие / В.Е. Волков, Н.Н. Чеснокова, С.В. Волков // Чебоксары: Изд-во Чуваш. ун-та, 2015. – 60 с.
- Савельев В.С. Панкреонекрозы / В.С. Савельев, М.И. Филимонов, С.З. Бурневич // М.: Мед. Информ. Агенство, 2008. – 264 с.
- Banks P.A. Classification of acute pancreatitis – 2012 : Revision of the Atlanta classification and definitions by international consensus / P. Banks, T.L. Bollen, C. Dervenis et al. // Gut. – 2013. ‒ № 62 (1), P. 102-111.
СВЕДЕНИЯ ОБ АВТОРАХ:
Волков Владимир Егорович
заведующий кафедрой хирургических болезней ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова», доктор медицинских наук, профессор
Черкесов Леонид Ильич
профессор кафедры хирургических болезней ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова», кандидат медицинских наук
И.Н. Ульянова», кандидат медицинских наук
Волков Сергей Владимирович
профессор кафедры хирургических болезней ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова», доктор медицинских наук
Чеснокова Наталия Николаевна
аспирант кафедры хирургических болезней ФГБОУ ВО «Чувашский государственный университет им. И.Н. Ульянова»
Лечение людей с острым панкреатитом (острое воспаление поджелудочной железы)
Актуальность
Поджелудочная железа – это орган в брюшной полости (животе), который вырабатывает пищеварительные ферменты (вещества, которые обеспечивают и ускоряют химические реакции в организме) и выделяет их в систему протоков поджелудочной железы, после чего они попадают в тонкую кишку. В поджелудочной железе также есть островки Лангерганса, в которых вырабатываются несколько гормонов, включая инсулин (помогает регулировать содержание сахара в крови). Острый панкреатит – это угрожающее жизни заболевание, характеризующееся острым воспалением поджелудочной железы, которое может привести к недостаточности функции других органов, таких как легкие и почки. Существует множество исследований различных терапевтических методов лечения острого панкреатита, но не ясно, какую пользу приносит каждый из этих методов, или существует ли какое-нибудь лечение, которое оказывало бы дополнительную пользу, кроме поддерживающего лечения. Медицинская помощь при остром панкреатите включает в себя гидратацию и интенсивную терапию у людей с недостаточностью функции органов (для поддержки этих органов). Мы стремились решить эту проблему, проведя поиск существующих исследований по этой теме. Мы включили все рандомизированные контролируемые испытания (клинические исследования, в которых людей в случайном порядке распределяют в одну из двух или более групп лечения), результаты которых были опубликованы до 7 октября 2016 года.
Существует множество исследований различных терапевтических методов лечения острого панкреатита, но не ясно, какую пользу приносит каждый из этих методов, или существует ли какое-нибудь лечение, которое оказывало бы дополнительную пользу, кроме поддерживающего лечения. Медицинская помощь при остром панкреатите включает в себя гидратацию и интенсивную терапию у людей с недостаточностью функции органов (для поддержки этих органов). Мы стремились решить эту проблему, проведя поиск существующих исследований по этой теме. Мы включили все рандомизированные контролируемые испытания (клинические исследования, в которых людей в случайном порядке распределяют в одну из двух или более групп лечения), результаты которых были опубликованы до 7 октября 2016 года.
Характеристика исследований
В этот обзор мы включили 84 РКИ с 8234 участниками. В шести клинических испытаниях (658 участников) не сообщали ни об одном исходе, представляющем интерес для этого обзора. В оставшихся 78 клинических испытаниях 210 участников были исключены после рандомизации. Таким образом, всего 7366 участников из 78 клинических испытаний внесли свой вклад в один или несколько исходов для этого обзора. Не считая сравнения, в котором рассматривали, следует ли использовать антибиотики, в другие сравнения был включен лишь небольшой процент людей с панкреонекрозом (крайне тяжелая форма панкреатита, которая приводит к разрушению поджелудочной железы). Большинство клинических испытаний включали участников только с тяжелыми формами острого панкреатита, либо включали участников как с легкими, так и тяжелыми формами панкреатита.
Таким образом, всего 7366 участников из 78 клинических испытаний внесли свой вклад в один или несколько исходов для этого обзора. Не считая сравнения, в котором рассматривали, следует ли использовать антибиотики, в другие сравнения был включен лишь небольшой процент людей с панкреонекрозом (крайне тяжелая форма панкреатита, которая приводит к разрушению поджелудочной железы). Большинство клинических испытаний включали участников только с тяжелыми формами острого панкреатита, либо включали участников как с легкими, так и тяжелыми формами панкреатита.
Источники финансирования: семь клинических испытаний не получали финансирования или финансировались организациями, не заинтересованными в результатах. В двадцати одном испытании было частичное или полное финансирование от фармацевтических компаний. В остальных испытаниях не было информации об источнике финансирования.
Качество доказательств
Общее качество доказательств было низким для всех исходов из-за отсутствия ясности или высокого риска смещения в клинических испытаниях (систематическая ошибка или отклонение от истины, которые влияют на результаты в пользу одного или другого способа лечения) и небольшого числа участников в испытаниях. Таким образом, необходимы дальнейшие исследования по этой теме.
Таким образом, необходимы дальнейшие исследования по этой теме.
Основные результаты
В шестидесяти семи исследованиях с участием 6638 человек сообщали о смертности в краткосрочном периоде наблюдения. В общей сложности, в среднем 12% людей, получающих только поддерживающую терапию, умерли. Не было доказательств, что какое-либо лечение снижало смертность в краткосрочном периоде наблюдения. Были доказательства, что различные методы лечения, возможно, оказывают благоприятный эффект в отношении ряда исходов; однако, эти результаты были противоречивыми, и мы не можем сделать выводы о том, что какие-либо способы лечения могут быть полезными. Ни в одном из клинических испытаний не сообщали о качестве жизни, связанном со здоровьем.
В заключение, основываясь на доказательствах низкого качества, не существует доказательств того, что любая лекарственная терапия, добавленная к поддерживающей терапии, снижает смертность в краткосрочном периоде наблюдения. В будущих клинических испытаниях у участников с острым панкреатитом следует рассмотреть такие исходы, как качество жизни, связанное со здоровьем, затраты, возврат к работе, и период наблюдения за пациентами должен быть не менее трех месяцев (предпочтительно не менее одного года).
Острый и хронический панкреатит – гастроэнтеролог – Москва, Клиника на Садовом
Острый панкреатит
Острый панкреатит – это острый воспалительный процесс в поджелудочной железе с разнообразным вовлечением региональных тканей и/или вовлечением других органов и систем.
При остром панкреатите происходит внутрипротоковая активация ферментов (в норме ферменты находятся в поджелудочной железе в неактивном состоянии) и запуск процесса формирования панкреонекроза. В дальнейшем процесс приобретает лавинообразный характер с образованием и выбросом в сосудистое русло вторичных, агрессивных факторов – эндотоксинов, которые в свою очередь, ведут к развитию эндотоксикоза и в дальнейшем определяют клинику течения заболевания.
Основным клиническим критерием, отличающим острый панкреатит от
хронического , является восстановление нормальной функции поджелудочной
железы.
В структуре острой патологии органов брюшной полости панкреатит занимает третье место – после острого аппендицита и холецистита. Ранее он регистрировался у 9-16% больных. Но за последние 20 лет заболеваемость острым панкреатитом возросла в 40 раз, значительно увеличилась частота деструктивных форм.
При подозрении на острый панкреатит больного нужно госпитализировать в хирургическое отделение. Ввиду того, что патологический процесс в поджелудочной железе развивается чрезвычайно быстро, особенно при прогрессирующих формах заболевания, необходима госпитализация больных даже с панкреатитом легкой степени тяжести.
Немедикаментозное лечение.
При раннем энергичном и многокомпонентном консервативном лечении у
80-90% больных острым панкреатитом наступает выздоровление в течении
3-7 дней от начала лечения. Ранняя госпитализация необходима для
избегания прогрессирования острого панкреатита, предупреждения перехода
отечных форм болезни в некротические, для ограничения
распространенности некротических изменений в поджелудочной железе.
В первые дни показан холод на эпигастральную область, что подавляет экскреторную секрецию железы. С целью обеспечения функционального покоя поджелудочной железы больной должен голодать до 7 дней. При неосложненном течении после уменьшения выраженности болей прием пищи может быть возобновлен. Пищу следует принимать маленькими порциями (до 5-6 раз в сутки). Она должна содержать много углеводов, белки и жиры ограничиваются, что снижает секрецию панкреатических ферментов.
В условиях стационара применяется не только лекарственная терапия (инфузионно-дезинтоксикационная, антибактериальная терапия, обезболивание, антиферментные препараты), но в ряде случаев и хирургическое лечение.
Хронический панкреатит
Хронический панкреатит – длительное
прогрессирующее заболевание поджелудочной железы, характеризующееся
появлением во время обострения признаков острого некротизирующего
воспалительного процесса, постепенным замещением паренхимы органа
соединительной тканью и нарастанием внешнесекреторной и инкреторной
недостаточности поджелудочной железы.
За последние 30 лет в мире отмечен значительный рост числа больных острым и хроническим панкреатитом, что связывают с растущим злоупотреблением алкоголя, учащением воспалительных заболеваний ЖКТ. Чаще болеют люди 31-50 лет.
Лечение.
Комплексное лечение хронического панкреатита включает решение следующих задач:
1)необходимо убедить больного отказаться от употребления алкоголя и соблюдать диету.
2)Необходимо провести заместительную ферментную терапию с целью
компенсации внешнесекреторной недостаточности поджелудочной железы.
Лечебные мероприятия направлены на предупреждение развития осложнений и
профилактику рецидивов.
Немедикаментозное лечение.
Функциональный покой поджелудочной железы создается в первую
очередь диетой, ограничивающей секрецию панкреатического сока и
предупреждающей провоцирование миграции мелких камней. При выраженных
обострениях заболевания на 3-5 дней назначается стол 0 (голод). Через
3-5 дней больного переводят на пероральное питание. Прием пищи должен
быть частым (4-6 раз в сутки), небольшими порциями. Она должна быть
тщательно измельченной, с большим содержанием легко перевариваемых и
хорошо усваиваемых белков. Ограничивают потребление продуктов,
способных стимулировать секрецию поджелудочной железы, в первую очередь
жиров, кислых продуктов. Больному запрещается употребление алкоголя,
острой пищи, консервов, газированных напитков, кислых фруктовых соков.
Через
3-5 дней больного переводят на пероральное питание. Прием пищи должен
быть частым (4-6 раз в сутки), небольшими порциями. Она должна быть
тщательно измельченной, с большим содержанием легко перевариваемых и
хорошо усваиваемых белков. Ограничивают потребление продуктов,
способных стимулировать секрецию поджелудочной железы, в первую очередь
жиров, кислых продуктов. Больному запрещается употребление алкоголя,
острой пищи, консервов, газированных напитков, кислых фруктовых соков.
Лекарственная терапия.
Для купирования болевого синдрома при обострении хронического панкреатита применяют ненаркотические анальгетики, миотропные спазмолитики.
При лечении применяют антигистаминные препараты, подавляющие секрецию поджелудочной железы и активность гидролитических ферментов.
Для уменьшения стимулирующих влияний регулярных пептидов на
внешнюю секрецию поджелудочной железы и желудочную секрецию назначают
ингибиторы протонной помпы либо блокаторы Н2-рецепторов гистамина.
Антацидные препараты нейтрализуют HCI и способствуют снижению уровня
секретина, обеспечивают тем самым функциональный покой поджелудочной
железы.
Одновременно применяют препараты, подавляющие активность ферментов
поджелудочной железы, которые поступили в кровь. Показаниями к
назначению таких препаратов является выраженная гиперферментемия.
При обострении хронического панкреатита, сопровождающегося развитием
перипанкреатита, холангита и других осложнений, показано назначение
антибиотиков широкого спектра действия.
Заместительная терапия.
При снижении экзокринной функции поджелудочной железы, наличии признаков мальабсорбции и стеатореи с целью заместительной терапии назначаются ферментные препараты. Дозы этих препаратов зависят от степени панкреатической недостаточности.
Ферментные препараты не должны снижать рН желудочного сока или
стимулировать панкреатическую секрецию. Продолжительность лечения
зависит от состояния больного.
Продолжительность лечения
зависит от состояния больного.
После стихания обострения хронического панкреатита поддерживающую терапию необходимо проводить на протяжении 6-12 месяцев. Используют препараты, уменьшающие секрецию поджелудочной железы: антацидные препараты, антагонисты Н2-рецепторов гистамина, ИПП, холинолитики. При наличии внешнесекреторной недостаточности поджелудочной железы необходимо назначать ферментные препараты.
Профилактика.
При алкогольном панкреатите основной мерой профилактики обострения является отказ от употребления алкоголя, соблюдение диеты. Грамотная поддерживающая терапия существенно уменьшает частоту обострений у 70-80% больных.
При билиарнозависимом панкреатите необходимо проводить санацию билиарной системы. Показано проведение литолитической терапии препаратами урсодезоксихолевой кислоты.
Острый панкреатит Текст научной статьи по специальности «Клиническая медицина»
УДК 616. 37-002.4 В.А. Кубышкин
37-002.4 В.А. Кубышкин
Московский государственный медико-стоматологический университет (127030 г. Москва, Спортивный проезд, 3)
ОСТРЫЙ ПАНКРЕАТИТ
Ключевые слова: панкреонекроз, клиника, диагностика, лечение.
Лекция, посвященная современному состоянию проблемы острого панкреатита. Рассматриваются патогенез, клиника, диагностика и принципы лечения заболевания. Особое внимание уделено показаниям и противопоказаниям к консервативному и оперативному лечению панкреонекро-за в зависимости от стадии течения и тяжести заболевания. Подчеркивается, что купирование острого воспалительного процесса в железе не означает полного выздоровления и морфологического восстановления поджелудочной железы. Как правило, перенесенный панкреонекроз приводит к развитию хронического панкреатита, поэтому после выписки из стационара больные подлежат длительному восстановительному лечению, направленному на восстановление трофики ткани и функции железы.
В последние десятилетия острый панкреатит стал занимать лидирующее положение в практике неотложной абдоминальной хирургии, уступая по частоте только острому аппендициту [8, 10, 14]. Однако нам пока еще не удалось существенно улучшить результаты его лечения. Можно перечислить основные и наиболее типичные причины, которые обусловливают высокую летальность, частоту осложнений и ин-валидизации больных, препятствующие ощутимому прогрессу в лечении этого заболевания:
• несвоевременное выявление некротического панкреатита;
• несвоевременная оценка тяжести заболевания, его прогноза и несвоевременное начало адекватной интенсивной терапии;
• большая частота ранних оперативных вмешательств в связи с ошибками диагностики или прогрессирующим ухудшением состояния больного;
• использование неадекватных методов детоксикации и антибактериальной терапии;
• трудность различения системного ответа на воспаление и гнойного процесса;
• позднее выявление гнойных осложнений;
• ограниченное использование миниинвазивных методов дренирования;
• неадекватная частота планируемых санационных релапаротомий;
• отсутствие системы реабилитации больных, перенесших панкреонекроз.
Патогенез и клиника
В 1992 г. группа экспертов по проблеме острого панкреатита приняла в г. Атланта (США) классификацию острого панкреатита, которая сейчас признана и в нашей стране. В ней выделяют отечный и некроти-
Кубышкин Валерий Алексеевич — член-кор. РАМН, д-р мед. наук, профессор, заведующий кафедрой общей хирургии МГМСУ; тел.: 8 (495) 359-02-46; e-mail: [email protected].
ческий панкреатит [8, 23]. Некротический панкреатит может быть асептическим и инфицированным. Инфицированный панкреонекроз может быть представлен в виде гнойного панкреатита, забрюшинной флегмоны. В исходе острого заболевания может формироваться псевдокиста или абсцесс.
При наиболее частой и легкой форме — отечном (интерстициальном) остром панкреатите — степень активации ферментов и их системное воздействие невелики [18, 23]. Макроскопически можно отметить отек паренхимы железы, исчезновение дольчатос-ти и четких границ, появление единичных жировых некрозов и мелких кровоизлияний, а в сальниковой сумке — незначительного количества серозно-геморрагического выпота. Такие изменения нередко ошибочно расценивают как очаговый панкреонекроз.
Макроскопически можно отметить отек паренхимы железы, исчезновение дольчатос-ти и четких границ, появление единичных жировых некрозов и мелких кровоизлияний, а в сальниковой сумке — незначительного количества серозно-геморрагического выпота. Такие изменения нередко ошибочно расценивают как очаговый панкреонекроз.
При панкреонекрозе макроскопическая картина более яркая. Поджелудочная железа обычно резко увеличена в размерах и отчетливо уплотнена вследствие воспалительного отека, с множественными и сливающимися пятнами жирового некроза. Поверхность железы и даже окружающей клетчатки, корня брыжейки тонкой и толстой кишки может иметь геморрагическую имбибицию без отчетливых границ, часто черного цвета (воздействие протеолитических ферментов на компоненты крови) [24]. Важно подчеркнуть, что при наличии забрюшинной геморрагической имбибиции часто практически невозможно определить локализацию и распространение некроза, а под измененной брюшиной и окружающей клетчаткой может располагаться менее измененная поджелудочная железа. Именно поэтому заключение о масштабах поражения железы на основании лишь визуальной оценки часто не соответствует истине.
Именно поэтому заключение о масштабах поражения железы на основании лишь визуальной оценки часто не соответствует истине.
Практически во всех случаях панкреонекроз сопровождается выраженными изменениями со стороны брюшной полости и ее органов [18]. В брюшной полости может быть от 500 до 3000 мл серозного, серозно-геморрагического или насыщенно геморрагического выпота с содержанием высокого уровня панкреатических ферментов. Париетальная и висцеральная брюшина тусклая, ярко гиперемированная, в брыжейке и сальнике появляются множественные и сливающиеся очаги жирового некроза и кровоизлияний [24]. Как правило, имеется обширная серозная или геморрагическая имбибиция забрюшинной клетчатки. Петли тонкой и толстой кишки расширены, вяло перистальтируют. Желчный пузырь обычно растянут и плохо опорожняется. При панкреонекрозе возникает массивная активация ферментов поджелудочной железы (трипсина, эластазы, липазы, фосфолипазы А),
которая приводит к появлению каскада взаимосвязанных местных и общих ферментативных реакций. Так, поджелудочная железа — один из мощных источников калликреина. Активация калликреин-кинино-вой ферментной системы с мощными вазоактивными свойствами приводит к глубоким расстройствам микроциркуляции и реологии крови, а также системной гемодинамики [18]. Расстройства микроциркуляции в бассейне чревного ствола и воротной вены обусловливают дальнейшее прогрессирование аутолитического и в конечном счете некротического процесса в поджелудочной железе и окружающих тканях. Параллельно системное воздействие вазоактивных и протеолити-ческих ферментов может приводить к развитию очагов некроза практически во всех органах [24].
Так, поджелудочная железа — один из мощных источников калликреина. Активация калликреин-кинино-вой ферментной системы с мощными вазоактивными свойствами приводит к глубоким расстройствам микроциркуляции и реологии крови, а также системной гемодинамики [18]. Расстройства микроциркуляции в бассейне чревного ствола и воротной вены обусловливают дальнейшее прогрессирование аутолитического и в конечном счете некротического процесса в поджелудочной железе и окружающих тканях. Параллельно системное воздействие вазоактивных и протеолити-ческих ферментов может приводить к развитию очагов некроза практически во всех органах [24].
Системное токсическое и повреждающее воздействие активированных ферментов поджелудочной железы и продуктов ее аутолиза проявляется прежде всего в нарастающей дисфункции жизненно важных органов и систем. Со стороны центральной нервной системы наблюдаются явления токсической энцефалопатии, вплоть до развития панкреатогенно-го делирия. Отмечаются признаки дыхательной недостаточности, связанные с интерстициальным отеком легких, развитием легочного дистресс-синдрома и выпотного плеврита [3, 5, 7].
Отмечаются признаки дыхательной недостаточности, связанные с интерстициальным отеком легких, развитием легочного дистресс-синдрома и выпотного плеврита [3, 5, 7].
Наиболее рано и ярко проявляются расстройства гемодинамики и функции сердечно-сосудистой системы. На фоне снижения объема циркулирующей крови за счет нарушения проницаемости сосудов и секвестрации плазменной части крови в межклеточном пространстве, свободной брюшной полости, а также жидкости в просвете кишечника нарастает гиповолемия, снижается сердечный выброс, возникают тахикардия и отчетливые признаки расстройств периферического кровообращения — цианоз и гипотермия кожи конечностей.
На фоне гиповолемии, расстройств системной и регионарной гемодинамики развиваются и быстро прогрессируют клинико-биохимические признаки сердечно-сосудистой, дыхательной и печеночно-почечной недостаточности. Нарастают симптомы динамической кишечной непроходимости. Нарушение функций желудочно-кишечного тракта является одной из причин эндогенного инфицирования очагов некроза [10, 14]. Как показывают исследования, при панкреонекрозе уже к концу первой недели заболевания до 40% больных имеют инфицированные некрозы. К концу второй недели заболевания частота инфицирования некрозов возрастает до 80% [21, 22, 24].
Нарушение функций желудочно-кишечного тракта является одной из причин эндогенного инфицирования очагов некроза [10, 14]. Как показывают исследования, при панкреонекрозе уже к концу первой недели заболевания до 40% больных имеют инфицированные некрозы. К концу второй недели заболевания частота инфицирования некрозов возрастает до 80% [21, 22, 24].
Это важнейший фактор патогенеза панкреонекро-за. Если первично очаги аутолиза стерильны, то в процессе прогрессирования они практически неизбежно инфицируются и становятся источником местных гнойно-воспалительных осложнений [21, 24]. В связи с этим в течении панкреонекроза можно выделить и проследить две последовательные фазы: 1 фаза — ферментная токсемия с гемодинамическими и полиор-
ганными расстройствами (5—9 дней) и 2 фаза — пост-некротические и гнойные осложнения (после 7-12-го дня). В клинических проявлениях и сроках эти фазы не имеют четких границ и дополняют друг друга.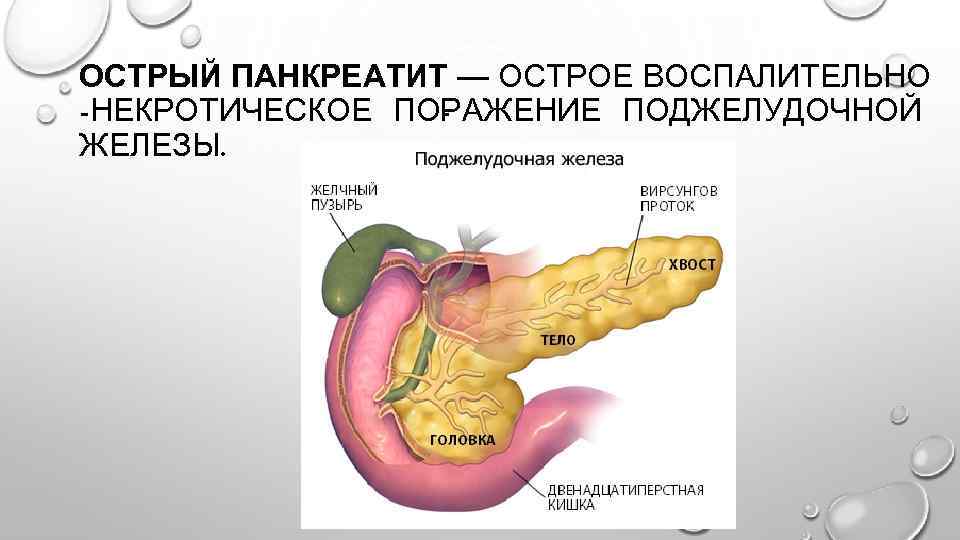
Диагностика
Важно подчеркнуть, что, помимо данных осмотра живота и даже инструментальных данных, важнейшее значение в ранней диагностике некротического панкреатита имеют малейшие признаки интоксикации и органных дисфункций.
Приоритетное значение в инструментальной диагностике панкреонекроза и оценке динамики процесса (система Бальтазара) принадлежит компьютерной томографии с внутривенным болюсным усилением, при которой возможно оценить зоны ишемии (некроза). Ультразвуковое исследование имеет преимущественно скрининговое или дифференциальнодиагностическое значение [20].
Исходя из основных макроскопических характеристик различных форм острого панкреатита, следует указать, что различия их носят не столько качественный, сколько количественный характер. Поэтому уже на ранних этапах диагностики больных острым панкреатитом следует сепарировать по какой-либо системе оценки (Ranson, APACHE, SAPS, ASA и др). на две группы течения — легкую и тяжелую. Легкой соответствует, как правило, лишь отечный панкреатит, а тяжелой — только панкреонероз [8].
на две группы течения — легкую и тяжелую. Легкой соответствует, как правило, лишь отечный панкреатит, а тяжелой — только панкреонероз [8].
Принципиально различна и динамика симптомов при отдельных формах острого панкреатита. В процессе консервативного лечения только при отечной форме уже в первые сутки наступает уменьшение болевого синдрома, снижается тахикардия, отсутствуют симптомы раздражения брюшины и желудочно-кишечных расстройств. В течение 7—14 дней наступает практически полная нормализация самочувствия, основных лабораторных показателей [9, 16]. Отечный панкреатит практически не сопровождается развитием локальных или системных осложнений.
Течение панкреонекроза на первом этапе заболевания (6—9 дней) сопровождается выраженными и прогрессирующими симптомами ферментной токсемии, которые с трудом удается купировать даже при многокомпонентной интенсивной терапии [3]. Они проявляются глубокими расстройствами гемодинамики, явлениями полиорганной недостаточности, нарастающими признаками перитонита. Любое из перечисленных осложнений может оказаться причиной смертельных исходов в эти сроки заболевания. Именно неэффективность интенсивной терапии часто служит одним из показаний к экстренному оперативному вмешательству.
Любое из перечисленных осложнений может оказаться причиной смертельных исходов в эти сроки заболевания. Именно неэффективность интенсивной терапии часто служит одним из показаний к экстренному оперативному вмешательству.
Если удается стабилизировать состояние больных панкреонекрозом, то почти у 80% из них в среднем к концу второй недели заболевания уже происходит эндогенное инфицирование очагов некроза в железе и окружающих тканях. Гнойно-воспалительный
процесс прогрессирует, и на первый план выступают симптомы интоксикации [10, 21]. Это проявляется усилением болевого синдрома, нарастанием тахикардии, появлением гипертермии, часто расстройством эвакуации из желудка и формированием воспалительного инфильтрата в эпигастральной области.
В диагностике формы острого панкреатита кроме компьютерной томографии и ультразвукового исследования часто возникает необходимость в лапароскопии, при которой возможно также осуществить дренирование брюшной полости, билиарную декомпрессию. В оценке динамики панкреонекроза и раннем выявлении инфицирования важную роль играет определение С-пептида и тонкоигольная биопсия железы. Пациенты с панкреонекрозом должны исходно получать лечение и мониторинг основных функций организма в отделении интенсивной терапии.
Лечение
Лечение острого панкреатита должно проводиться только в стационаре. Объем терапии и используемые средства различаются при разных формах заболевания. Общим принципом является максимальное воздержание от оперативных вмешательств на поджелудочной железе, полное обезболивание, создание функционального покоя органа, подавление секреции, снижение внутрипротоковой гипертензии, возмещение потерь жидкости и электролитов [28]. Необходима нейтрализация активированных ферментов поджелудочной железы и выведение токсических продуктов, поддержание функции жизненно важных органов и систем, а также профилактика гнойно-воспалительных осложнений [1, 2]. Важнейшим условием эффективности консервативной терапии является ее опережающий характер, профилактика основных системных и локальных осложнений. Каждая из этих задач может иметь несколько путей решения:
1. Обезболивание. Новокаиновая блокада паранеф-рия или круглой связки печени, внутримышечное или внутривенное введение 2% раствора промедола, эпи-дуральная блокада, внутривенная инфузия глюкозно-новокаиновой смеси [2, 4];
2. Функциональный покой поджелудочной железы. Голод, постоянная назогастральная аспирация, парентеральное введение Н2-блокаторов рецепторов гистамина [7, 12, 13];
3. Подавление внешней секреции органа. Наиболее эффективным средством в настоящее время является октреатид (сандостатин), который назначают подкожно каждые 6 часов в дозе 50—100 мг. Снижению синтеза ферментов способствует 5-фторурацил (фто-рафур) в дозе 5мл/кг в течение 5—7 дней [10, 11].
4. Снижение внутрипротоковой гипертензии. Назначают спазмолитические средства и, если это возможно технически, выполняют канюляцию вирсун-гова протока для аспирации секрета железы [17].
5. Возмещение потерь и обеспечение естественных потребностей в жидкостях и электролитах. Прово-
дят массивную инфузию изотонических растворов. Очень важно при этом регулировать объем инфу-зии по величине центрального венозного давления, сердечного выброса, гематокрита, диуреза [19]. При панкреонекрозе суточный объем инфузии должен составлять пять и более литров. Для поддержания во-лемических и гемодинамических показателей изотонические растворы комбинируют с растворами белков, препаратами с высокими онкотическими свойствами, реологически активными препаратами [9].
6. Борьба с системной ферментемией. Достигается форсированным диурезом, инфузией ингибиторов протеаз (контрикал, гордокс). Следует отметить, что назначение этих средств обосновано только при пан-креонекрозе, выраженных гемодинамических, гемо-реологических и коагуляционных расстройствах [4]. На течение процесса в поджелудочной железе эти препараты не влияют.
7. Профилактика гнойных осложнений. Парентерально вводят антибиотики широкого спектра действия, воздействующие на кокковую, неклостриди-альную и анаэробную флору [21]. Принимая во внимание важнейшую роль в развитии гнойных осложнений энтерогенной бактериальной контаминации очагов некроза, следует стремиться к раннему восстановлению функций желудочно-кишечного тракта [15]. Поэтому, помимо медикаментозной стимуляции моторики кишечника, с 4-5-го дня целесообразно начинать назоэнтеральное зондовое питание.
Объем проводимой терапии существенно различается при отечном панкреатите и панкреонекрозе. При отечном панкреатите, для которого не характерны системные нарушения, основными компонентами консервативной терапии являются обезболивание и создание функционального покоя поджелудочной железе [5]. Объем и структуру внутривенной инфузи-онной терапии определяют исходя из соображений предупреждения гиповолемии, гемодинамических расстройств и возмещения естественных потребностей организма в жидкости и электролитах. Обычно требуется 1,5—2 литра изотонических растворов.
Эти манипуляции несколько снижают внутритканевую компрессию паренхимы поджелудочной железы, а также возможность распространения ферментативного выпота по забрюшинным клетчаточным пространствам. Однако чаще всего в ранние сроки от начала заболевания такие вмешательства малоэффективны и усугубляют тяжесть состояния больных.
Оперативное лечение полностью обосновано, если имеются клинические признаки гнойного воспаления, лабораторные и инструментальные указания на гнойный очаг [22, 24]. Важным правилом оперативных вмешательств в ранние сроки заболевания должно быть воздержание от использования тампонов, которые способствуют инфицированию очагов некроза и прогрессированию гнойного процесса.
Основная цель операции во второй фазе заболевания сводится к удалению очагов некроза или свободно
расположенных тканевых секвестров. Во время этих вмешательств необходима тщательная ревизия всех возможных зон развития некроза ткани [6, 15]. Это не только поджелудочная железа и окружающая ее клетчатка, но и забрюшинная клетчатка в области корня брыжейки, клетчаточные пространства вдоль восходящей и нисходящей ободочной кишки. Такую возможность предоставляет только широкая лапаро-томия (поперечная или срединная).
Оперативные вмешательства при секвестрации ткани железы и окружающей клетчатки редко дают полный эффект при однократном выполнении, поэтому удаление некротизированных тканей часто приходится осуществлять не менее 4—5 и более раз с интервалом в 3—4 суток. Если процесс локализован только в области сальниковой сумки, то этапная некрозосеквестрэктомия может выполняться через сформированную оментобурсостому. Операция такого рода завершается наружным дренированием в зоне некроза силиконовыми дренажами, и крайне редко могут быть использованы марлевые тампоны. При наличии оментобурсостомы для последующих ревизий полости малого сальника и поджелудочной железы широко используют и лапароскопическую технику.
В последние годы приобрел широкое распространение, а в силу малой травматичности — большой лечебный эффект метод чрескожной пункции для удаления жидкости (с исследованием ее на микрофлору) или проведения дренажа при гнойном процессе под ультразвуковым наблюдением. Часто такой метод позволяет избежать оперативного вмешательства. Однако наличие множественных секвестров в очаге скопления асептической или гнойной жидкости чаще всего требует традиционной операции.
Осложнения
Острый панкреатит на всех этапах течения может сопровождаться общими и локальными осложнениями. К типичным общим осложнениям относят токсическую энцефалопатию, выпотной плеврит и легочный дистресс-синдром, острую сердечно-сосудистую недостаточность, печеночно-почечную недостаточность. В большей или меньшей степени при остром панкреатите наблюдается дисфункция всех этих органов, но только при тяжелых формах можно говорить о полиорганной недостаточности.
К местным осложнениям острого, главным образом некротического панкреатита относят ферментативный, а в последующем и гнойный перитонит, псевдокисту или абсцесс сальниковой сумки, механическую желтуху, аррозивные кровотечения, а также наружные или внутренние панкреатические свищи поджелудочной железы.
Течение панкреонекроза, как правило, проходит стадию формирования инфильтрата в эпигастральной области, которая связана с отеком связочно-клетча-точных образований в сальниковой сумке в верхнем этаже брюшной полости. Если не происходит инфи-
цирования или удается предупредить его консервативной терапией, инфильтрат может бесследно разрешиться. При инфицировании развивается гнойный оментобурсит и чаще всего формируется абсцесс сальниковой сумки.
Наиболее типичным проявлением инфицированного панкреонекроза является забрюшинная флегмона, которая может распространяться по клетчаточ-ным пространствам вплоть до малого таза. Происходит гнойное расплавление клетчатки в области корня брыжейки и обоих параколических пространств. Это тяжелое осложнение сопровождается симптоматикой быстропрогрессирующей интоксикации, усугублением дисфункции органов и обычно является одной из ведущих причин летальных исходов в поздние сроки заболевания. Поэтому симптомы повторного ухудшения состояния после временной его стабилизации в фазе ферментной токсемии всегда должны наводить на мысль о развитии гнойных осложнений.
Появление клинических признаков гнойной интоксикации и сохранение тяжелого состояния больных на фоне интенсивной терапии должно рассматриваться как безусловное показание к оперативному вмешательству. Сущность его заключается в обязательной ревизии железы и всех забрюшинных клетчаточных пространств, максимальном удалении некротизиро-ванных и секвестрирующихся тканей и дренировании зон их расположения через отдельные разрезы передней и боковых отделов брюшной стенки.
Но сама по себе эта процедура не способна купировать вялотекущий гнойно-воспалительный процесс. Поэтому необходимо особо подчеркнуть, что в лечении инфицированного панкреонекроза с обширным некрозом забрюшинной клетчатки практически никогда не удается добиться его излечения путем одно- или двухкратных санационных лапаротомий.
Одним из тяжелых осложнений панкреонекро-за может быть аррозивное кровотечение из сосудов, расположенных вблизи поджелудочной железы, — селезеночных, брыжеечных, сосудов желудочно-ободочной связки. Чаще всего это осложнение возникает после оперативных вмешательств, некрозосек-вестрэктомии. В лечении аррозивного кровотечения редко бывает эффективной тугая тампонада зоны источника кровотечения. Необходимо стремиться к поиску и лигированию поврежденного сосуда. Арро-зивные кровотечения с успехом могут быть устранены эндоваскулярными методами окклюзии сосудов.
Некроз тканей поджелудочной железы и самостоятельное или оперативное отторжение этих участков в большинстве случаев неизбежно приводит к формированию наружных панкреатических свищей по ходу дренажных каналов. При запоздалых оперативных вмешательствах или неадекватном дренировании зон некрозосеквестрэктомии могут формироваться и внутренние свищи с желудочно-кишечным трактом, свободной брюшной или плевральной полостью и даже с бронхами [15].
Купирование острого воспалительного процесса в поджелудочной железе по клинико-лабораторным признакам после консервативного и оперативного лечения не означает полного выздоровления и морфологического восстановления поджелудочной железы. В течение нескольких месяцев после перенесенного панкреонекроза могут развиваться псевдокисты и даже абсцессы вблизи поджелудочной железы или в самой ее паренхиме [25, 26]. Лечение их в большинстве случаев выполняется консервативными мерами (антибактериальная, неспецифическая противовоспалительная терапия, физиотерапевтическое лечение). При размерах кист более 5 см чаще всего приходится использовать метод чрескожной их пункции, а при плотных сформированных стенках в срок более 3—4 месяцев после панкреонекроза обычно проводится операция внутреннего дренирования кисты путем цистоэнтеростомии [27].
Как правило, перенесенный панкреонекроз приводит к развитию хронического панкреатита вследствие расстройств микроциркуляции, фиброзного замещения очагов некроза [13, 15, 25]. Поэтому после выписки из стационара больные подлежат длительному восстановительному лечению, направленному на нормализацию трофики ткани и функции железы.
Литература
1. Брискин Б.С., Рыбаков Г.С. Хирургическое лечение острого панкреатита // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2000. № 2. С. 67—74.
2. Брискин Б.С., Халидов О.Х., Багдатьев В.Е. и др. Протокол ведения больных с деструктивным панкреатитом в фазу ферментной токсемии в отделении общей реанимации и интенсивной терапии. // Акт. вопросы анестезиологии и реаниматологии: сб. научных работ. М., 2005. С. 21-23.
3. Бурневич С.З., Гельфанд Б.Р., Орлов Б.Б., Цыденжапов Е.Ц. Деструктивный панкреатит: современное состояние проблемы // Вестник хирургии им. И.И. Грекова. 2000. Т. 159, № 2. С. 116-123.
4. Губергриц Н.Б. Лечение панкреатитов. Ферментные препараты в гастроэнтерологии. М.: Медпрактика, 2003. 100 с.
5. Губергриц Н.Б. Панкреатическая боль: как помочь больному. М.: Медпрактика, 2005. 176с.
6. Итала Э. Атлас абдоминальной хирургии. Т. 1. Хирургия печени, желчных путей, поджелудочной железы и портальной системы. М.: Медлит, 2006. 508с.
7. Краткое руководство по гастроэнтерологии / под. ред. Ивашкина В.Т., Комарова Ф.И., Рапопорта С.И. М.: М-Вести, 2001. 458 с.
8. Маев И.В., Кучерявый Ю.А. Болезни поджелудочной железы. М. : ГЭОТАР-Медиа 2009. 736 с.
9. Недашковский Э.В., Бобовник С.В. Принципы интенсивной терапии острого панкреатита в стадии острой токсемии // Вестник интенсивной терапии. 2003, прил. № 5. С. 32-34.
10. Нестеренко Ю.А., Лаптев В.В., Михайлусов С.В. Диагностика и лечение деструктивного панкреатита. М.: Бином-Пресс, 2004. 304 с.
11. Острые панкреатиты: эпидемиология, патогенез, диагностика, организация лечения, хирургическое лечение, интенсивная терапия / Мальцева Л.А., Усенко Л.В., Люлько И.В. и др. Киев: Четверта хвиля, 2005. 256 с.
12. Охлобыстин А.В., Баярмаа Н. Ферментные препараты при консервативном лечении хронического панкреатита// Тер. архив. 1998. Т. 70, № 10. С. 86-88.
13. Охлобыстин А.В., Буклис Э.Р. Современные возможности терапии хронического панкреатита // Лечащий врач. 2003. № 5. С. 32-36.
14. Полушин Ю.С., Суховецкий А.В., Сурков М.В., Пащенко О.В., Широков Д.М. Острый послеоперационный панкреатит. СПб.: Фолиант, 2003. 160 с.
15. Толстой А.Д., Панов В.П., Краснорогов В.Б. и др. Парапанкреатит. СПб.: Ясный свет, 2003. 256с.
16. Фадеев Б.М., Зайцев А.В., Шамсутдинов С.М. Оптимизация интенсивной терапии острого деструктивного панкреатита // Клин. анестезиол. и реаниматол. 2004. Т. 1, № 3. С. 51-52.
17. Филимонов М.И., Гельфанд Б.Р., Бурневич С.З. Деструктивный панкреатит: комплексная диагностика и лечение //Новый медицинский журнал. 1997. № 3. С. 10-13.
18. Хендерсон Д.М. Патофизиология органов пищеварения/пер. с англ. М.; СПб.: Бином; Невский Диалект, 1997. 288 с.
19. Шалимов А.А., Крыжевский В.В., Нечитайло М.Е. Лечение острого панкреатита // Клиническая хирургия. 2000. № 4. С. 5-9.
20. Andren-Sandberg A. Theory and practice in the individualization of oral pancreatic enzyme administration for chronic pancreatitis //Int. J. Pancreatol. 1989. Vol. 5, suppl. P. 51-62.
21. Cicalese L., Sahai A., Sileri P. Acute pancreatitis and bacterial translocation //Dig. Dis. Sci., 2001. Vol. 46. P. 1127-1132.
22. Clancy T.E., Ashley S.W. Current management of necrotizing pancreatitis//Adv. Surg. 2002. Vol. 36. P. 103-121.
23. Diagnosis Criteria of Pancreatitis//Chin. J. Surg. 1997. Vol. 35, No. 12. P. 773-775.
24. Hartwig W., Werner J., Muller C.A. et al. Surgical management of severe pancreatitis including sterile necrosis // J. Hepatobiliary Pancreat. Surg. 2002. Vol. 9. P. 429-435.
25. Malesci A., Gaia E., Fioretta A. et al. No effect of long-term treatment with pancreatic extract on recurrent abdominal pain in patients with chronic pancreatitis // Scand. J. Gastroenterol. 1995. Vol. 30, No. 4. P. 392-398.
26. Nair R.J., Lawler L., Miller M.R. Chronic Pancreatitis // Am. Fam. Physician. 2007. Vol. 76. No. 11. P. 1679-1688.
27. Toskes P.P. Treatment of pain in chronic pancreatitis: inhibition of enzyme secretion // Chronic Pancreatitis. Novel Concepts in Biology and Therapy / ed. by M.W. Buchler et al.. Blackwell Wissenschafts-Verlag, 2002. P. 389-394.
28. Uhl W., Warshaw A., Imrie C. IAP guidelines for the surgical management of acute pancreatitis // Pancreatology. 2002. Vol. 2. P. 565-573.
Поступила в редакцию 10.04.2009.
ACUTE PANCREATITIS V.A. Kubyishkin
Moscow State Medicodental University (3 Sportivniy Proezd Moscow 127030 Russia)
Summary — The lecture summarises present-day issues of acute pancreatitis and discusses pathogenesis, clinical picture, diagnostics and treatment principles of this disease. Special consideration is given to indications and contraindications for conservative treatment and surgery of pancreatonecrosis, depending on the disease stage and severity. The author highlights that the rapid relief of acute inflammatory process in the gland does not result in absolute recovery and morphological recovery in the pancreas. As a rule, having pancreatonecrosis will lead to chronic pancreatitis, therefore after being discharged from the hospital, the patients should undergo long-term medical rehabilitation aimed at recovering tissue trophism and functions.
Key words: pancreatonecrosis, clinical picture, diagnostics, treatment.
Pacific Medical Journal, 2009, No. 2, p. 48—52.
Заболевания поджелудочной железы
[ Радио Свобода: Программы: Наука и медицина][17-09-05]
Заболевания поджелудочной железы
Ведущая Ольга Беклемищева: Сегодня мы говорим о заболеваниях поджелудочной железы, и, прежде всего, об остром панкреатите – наиболее распространенном и опасном из них. Клинические симптомы острого панкреатита были описаны еще 300 лет назад, а основная теория, объясняющая причины его возникновения, родилась лет 100 назад. Что же изменилось за последнее время? Изменилась частота заболевания. Из сравнительно редко встречающейся патологии панкреатит превратился в третью по частоте хирургическую патологию после аппендицита и грыжи. И шансы каждого из нас столкнуться с этой болезнью лично, к сожалению, возросли. Поэтому сегодня в студии – Александр Алексеевич Линденберг, доцент кафедры госпитальной хирургии Российского государственного медицинского университета, известный в Москве специалист по абдоминальной хирургии. А по телефону в нашем разговоре примет участие наш американский эксперт – профессор Даниил Борисович Голубев. И мы начинаем. Александр Алексеевич, что же случилось, почему панкреатиты стали встречаться так часто? Александр Линденберг: Ну, все-таки на третье место панкреатит вышел совсем недавно. И, вероятно, это связано с ростом количества заболеваний желчных путей. Я не совсем согласен с тем, что грыжа на втором месте. На втором месте заболевания желчного пузыря – острый холецистит, и все, что связано с камнеобразованием в желчных путях. Вот это одна из причин панкреатита, вероятно, двинувшая это заболевание из разряда эксквизитных в разряд часто встречающихся и, к сожалению, требующих достаточно серьезного лечения. Ольга Беклемищева: А сейчас я хочу спросить нашего американского эксперта. Профессор Голубев, а в США как обстоят дела с панкреатитами, с их частотой? Даниил Голубев: Острый и хронический панкреатиты не очень частые, но достаточно распространенные в США заболевания, нередко протекающие под маской других диагнозов. В 60-80 процентах случаев причинами развития панкреатитов является алкоголь в США, а на втором месте – желчнокаменная болезнь. Какая из этих причин лидирует, зависит от географического положения того или иного региона, а также от демографии. 10-15 процентов приходится на долю так называемого идиопатического панкреатита. То есть таких его форм, истинная причина которых остается неизвестной. Однако недавно проведенное Национальным институтом здоровья специальное исследование выявило у большинства больных этой формой микросимптоматику поражения желчевыводящих путей. Идиопатический панкреатит не проявляет ни географических, ни демографических, ни социальных предпочтений. В марте прошлого года с диагнозом “острый панкреатит” был, например, срочно госпитализирован прямо из своего кабинета в Министерстве юстиции генеральный прокурор США Джон Эшкрофт, который в силу своего крайнего ультраконсерватизма наверняка не злоупотреблял алкоголем, а судя по заявлениям его лечащих врачей, не имел до этого никаких проблем с печенью или желчными путями. Ну, другими этиологическими факторами являются травмы живота, последствия оперативных или диагностических, эндоскопических процедур в области печени, желчного пузыря и желчных протоков. Не исключена роль разного рода инфекций – микоплазм, легионелл, микобактерий туберкулеза, различных вирусов, в частности, вирусов эпидемического паротита, вирусов гепатитов и вирусов Coxsackie, ну а также паразитарных инфекций – криптококков и токсоплазм. Панкреатит может быть вызван различными лекарственными препаратами, в частности, Фуросемидом, Эстрогенами, Тетрациклином и многими другими биологически активными веществами и химикалиями. Вспомним, например, первый диагноз, с которым попал в больницу Виктор Ющенко, до того, как заговорили о его отравлении диоксином, – это был именно острый панкреатит. В общем, панкреатит в США рассматривается как полиэтиологическое заболевание, диагноз которого устанавливается на основании клинической картины, целого ряда лабораторных тестов и инструментальных методов обследования – это рентгенография брюшной полости, ультразвуковая диагностика и все более широко входящая в практику компьютерная томография. При лечении большое внимание обращается на диетотерапию и заместительную терапию ферментами поджелудочной железы. При сильных болях применяются, естественно, анальгетики, а также наркотики, при наличии бактериальных инфекций – антибиотики, в тяжелых случаях – хирургическое вмешательство, в частности, субтотальная панкреатотомия. Среди многообразных осложнений панкреатитов наиболее серьезным в США считается повышение риска развития карциномы поджелудочной железы и нередкое привыкание к наркотическим средствам при упорном болевом синдроме. Специфическая профилактика, как известно, отсутствует, а к числу профилактических мероприятий должны быть причислены: воздержание от алкоголя и, что очень важно, своевременная санация печени, желчного пузыря и желчных протоков, что доступно только людям, имеющим постоянную медицинскую страховку. Вот так обстоит дело. Ольга Беклемищева: Спасибо, Даниил Борисович. По-моему, все очень внятно объяснено. Тогда мне хотелось бы уточнить, что же происходит в самой поджелудочной железе, когда она воспаляется. Почему вообще это происходит? Александр Линденберг: Я полагаю, что все-таки надо начать с того, чтобы разграничить два понятия: есть отечные формы острого панкреатита и есть панкреонекроз – тяжелейшая форма заболевания, при которой поджелудочная железа некротизируется в той или иной степени. Почему стоит говорить о них раздельно. Вероятно, потому, что все-таки и симптоматика, и лечение, и исходы, что самое главное, у этих двух, в общем-то, однотипных заболеваний, скрывающихся под одним названием, абсолютно разные. Если отечная форма панкреатита практически сопровождается нулевой летальностью, то панкреонекроз, даже в хороших учреждениях, приводит к летальности где-то от 20 до 30 процентов. Ольга Беклемищева: А насколько часто он встречается? Александр Линденберг: Ну, он встречается приблизительно в три раза реже, чем отечная форма панкреатита. То есть четвертая часть случаев воспаления поджелудочной железы приводит к развитию тяжелых панкреонекрозов. К сожалению, статистика до сих пор у нас в России учитывает панкреатиты вообще, и поэтому на фоне общего благополучия – где-то летальность в 2-3 процента с учетом отечных форм, повторяю, от которых не погибают, летальность при панкреонекрозе в отдельных клиниках выглядит очень выгодно: 2-3 процента – это “замечательная” летальность. А вот если начинать считать только формы некротические, то это 20-30, а то и 40 процентов, как правило, погибающих больных. Ольга Беклемищева: А почему эта форма такая летальная? В чем разница? Александр Линденберг: Тяжелейшие нарушения, которые возникают при панкреонекрозе в организме, приводят к развитию недостаточности многих органов и систем. Это и дыхательная недостаточность, и сердечная недостаточность, прогрессирование синдрома эндогенной интоксикации приводит к смерти мозга и, как правило, к тяжелым формам абдоминального сепсиса и соответствующему исходу. И лечить ее значительно тяжелее, чем, скажем, тот же самый отечный панкреатит, который и особого-то лечения почти не требует. Ольга Беклемищева: Но давайте тогда сначала разберем именно вот эту более легкую форму – отечный панкреатит. Как он развивается? Что там происходит внутри нас? Александр Линденберг: Ну, отечный панкреатит, если говорить о причине заболевания, – это, как правило, достаточно легко протекающее воспаление поджелудочной железы, которое возникает в результате нарушения выделения ферментов поджелудочной железы, то есть того, что мы называем соком поджелудочной железы, из самой железы через протоки в двенадцатиперстную кишку. Причин этому много, частично они перечислялись коллегой из США. Но, в принципе, важно, что возникает рост давления в протоке. Этот рост давления может быть достаточно кратковременным. Но несмотря на его кратковременность, часть ферментов, которая выделяется в неактивных формах в просвет кишки и только там активируется, начинает активироваться непосредственно в протоках поджелудочной железы. Ну, это приводит к понятию, которое мы называем аутолизом, то есть некоторая часть клеток поджелудочной железы начинает гибнуть, самопереваривая себя. Ольга Беклемищева: Вот по этому поводу я бы хотела обратить внимание наших слушателей на то, что на самом деле поджелудочная железа – это такой технологический ответ природы на великую загадку, что если вы сделаете идеальный растворитель, то где вы его будете держать. Понятно, что когда мы перевариваем что-то, нам вот этими пищеварительными соками нужно достаточно серьезно расщеплять белки, а организм тоже создан из белков… Александр Линденберг: И жиры тоже. Ольга Беклемищева: И жиры тоже, да. И как же ему уберечься от самопереваривания? И вот природа придумала так, что ферменты, которые готовит поджелудочная железа для кишечника, они неактивны, и они активируются только в самом кишечнике под воздействием желчи. Но вот как сказал уже Александр Алексеевич, если случается обратный заброс, то поджелудочная железа беззащитна – и она начинает распадаться. Александр Линденберг: В какой-то степени. Если говорить об отечной форме, то дальше все развивается достаточно благополучно. Восстанавливается отток ферментов поджелудочной железы, и сама поджелудочная железа, перенеся только оттек – отсюда и понятие отечной формы – приходит в определенную норму. Ольга Беклемищева: Я думаю, нам нужно разграничить острый панкреатит от панкреонекрозов. Вот по тому, как мне написали на сайт наши слушатели, понятно, что у многих случаются приступы панкреатита достаточно невыраженные, когда люди, в общем-то, даже не вызывают “скорую”, не госпитализируются. Это то, о чем говорили вы, да? Александр Линденберг: Как правило, те, кто не вызывает “скорую” и не госпитализируется, они не болеют острым панкреатитом, они не придумывают себе этого диагноза. Это то, что прячется под классическим, так сказать, обывательским понятием “отравление”. Острый панкреатит никто себе сам в качестве диагноза не выставляет. Чаще всего – отравился, ну, извините, под классическим понятием “перепил”, и так далее. Вот это будет отечная форма острого панкреатита. Два-три дня лежания, холод, голод – и постепенно человек приходит в норму. К сожалению, я хочу отметить следующее, что никто и никогда не может сказать точно, не перейдет ли отечная форма острого панкреатита в панкреонекроз. Ольга Беклемищева: То есть если даже человек соблюдает покой, голод и холод, все равно может утяжелиться состояние? Александр Линденберг: Абсолютно точно. Вся неприятность этого положения в том, что мы тоже не можем сказать, в каких ситуациях острый панкреатит превращается в панкреонекроз, а в каких ситуациях он остается на уровне отечной формы острого панкреатита. Поэтому когда возникают проблемы, связанные с болями в эпигастрии… Ольга Беклемищева: Я прошу прощения, эпигастрий – это область живота в районе пупка. Александр Линденберг: Повыше немножко… с иррадиацией их в спину, с сопровождающейся тяжелой рвотой, то не надо надеяться на то, что у вас возникла легкая форма заболевания, а надо госпитализироваться, и там уже отдавать себя во власть специалистов, которые будут лечить, наблюдать, потому что этот вариант может закончиться весьма печально, ибо временной фактор в лечении панкреонекроза является чуть ли не определяющим вообще, в принципе. Чем раньше мы начинаем лечить это заболевание, тем лучшие результаты мы получаем. Ольга Беклемищева: А когда вы, врачи видите, что начинается именно панкреонекроз? Александр Линденберг: По тяжести состояния больного, как правило. Потому что отечный панкреатит, я напоминаю, это сродни острого гастрита, которым болеют процентов 70 населения. А дальше состояние ухудшается, нарастают боли, появляются признаки недостаточности разных органов и систем – одышка, учащение пульса более 120, иногда возбуждение, иногда, наоборот, признаки тяжелых форм нарушения деятельности головного мозга, живот становится резко болезненным – вот это уже признаки панкреонекроза, и лечить их уже даже не в хирургическом отделении надо, а в отделении реанимации, как правило. Ольга Беклемищева: Тогда, чтобы было понятнее, давайте перечислим сначала признаки панкреатита, то, что человек заметит у себя дома, то, что ему надо делать дома до приезда “скорой”, и вы уже перечислили признаки тяжелого состояния. Александр Линденберг: К сожалению, я вам должен ответить достаточно банально. Боли в животе являются абсолютным показанием к вызову “скорой помощи”, к обращению к врачу. И ничего до этого момента делать не надо. Потому что, как правило, старая, приснопамятная рекомендация не принимать препараты, уменьшающие боль, принимать спазмолитики, сейчас уже, по-моему, всем давно известна и не вызывает никаких сомнений. Вызвали врача, обратились за специализированной помощью. А дальше уже все решаем мы, и, в общем, для этого нас и готовят, и учат, и для этого мы лечим панкреонекрозы, собственно. Ольга Беклемищева: Александр Алексеевич, а все-таки почему не нужно принимать анальгетики при болях в животе? Дело в том, что в рекомендации, скажем, той же “скорой помощи” при остром панкреатите, я читала, что они могут ввести Анальгин, Амидопирин. Александр Линденберг: “Скорая помощь” может вводить все, что угодно, это уже специализированная помощь. Мы ведь речь ведем о приеме препаратов, когда человек еще только почувствовал боль и не обращался к врачу. Этого делать нельзя. Ну, по одной простой причине, что в свое время ведь острый панкреатит встречался тоже достаточно часто. Но где-то лет 50-60 тому назад диагноз острого панкреатита считался высшим врачебным, так сказать, пилотажем. Потому что острый панкреатит не имеет настолько специфической клинической картины, чтобы говорить, что вот это только острый панкреатит. Под ним могут прятаться “любимый” всеми острый аппендицит, холецистит, кишечная непроходимость и многое другое. Поэтому делать картинку непонятной, принимая анальгетики или спазмолитики, конечно, крайне нежелательно. Ольга Беклемищева: То есть это для облегчения дальнейшей дифференциальной диагностики? Александр Линденберг: Естественно. Ольга Беклемищева: А если очень сильно больно? Александр Линденберг: А если очень сильно больно, то никакой анальгетик, принятый в амбулаторных условиях, эти боли не уменьшит, если это боли, вызванные панкреатитом. Ольга Беклемищева: Понятно. Ну, значит, выбора нет. Ждите “скорую”. Александр Линденберг: Для того чтобы снять боли при панкреонекрозе, мы вынуждены проводить больным вещь, которая называется эпидуральная анестезия. То есть вводить препараты-анальгетики непосредственно в отдел спинного мозга. Ольга Беклемищева: А до этого, насколько я знаю, использовались атропиновые блокады, да? Александр Линденберг: Все использовалось. К счастью, прогресс медицины в отношении этого заболевания, в общем, достаточно отчетлив. И целый ряд московских клиник – клиника 31-ой городской больницы, Первая градская больница – принципиально занимаются панкреонекрозами. Поэтому в последнее время и результаты несколько стали улучшаться, хотя они остаются еще далекими от идеала. Ольга Беклемищева: И опять же из того, что мне удалось прочитать… Как раз вот вы говорите, что некоторые клиники специально им занимаются. Значит ли это, что если человек не располагает возможностью оказаться в такой специализированной клинике, то ему нужно настаивать на том, чтобы его туда перевезли? Или он все-таки может получить адекватное лечение и в другой клинике? Александр Линденберг: Нет, конечно, адекватное лечение можно получить практически в любом хирургическом стационаре города Москвы. Я говорю о клиниках, которые специализируются на разработке терапии панкреонекроза, на применении новых, современных средств, на разработке тактических вопросов. А так его достаточно неплохо лечат в любой московской клинике, но в медицинском стандарте. Ольга Беклемищева: А что такое стандарт лечения этого заболевания? Александр Линденберг: Для этого заболевания стандарт лечения довольно сложен. Потому что основная задача на первом этапе – это спасти человека от смерти, от токсического шока. Каким образом это будет делаться, ну, я не буду перечислять – это займет больше времени, чем вся передача. Но это специальные методы детоксикации, это препараты, которые снижают активность поджелудочной железы, вплоть до цитостатиков, в свое время широко применявшихся. Ольга Беклемищева: А сейчас они уже не так широко применяются? Александр Линденберг: Применяются, особенно в клиниках, где других препаратов пока нет, они применяются, остается на вооружении, они достаточно эффективны. Это применение методов экстракорпоральной детоксикации, и еще масса других препаратов, применение мощнейшей антибактериальной терапии. Это на первом этапе. На втором этапе – это консервативная терапия, направленная на то, чтобы не допустить инфицирования, то есть проникновения инфекции в обширное пространство забрюшинной клетчатки, которая при панкреонекрозе, естественно, тоже поражается. И в зависимости от положительного или отрицательного результата этой проводимой терапии наступает третий этап, где мы уже думаем, оперировать пациента или не оперировать. Если инфицирование не наступает, то, как правило, все ограничивается консервативной терапией. Если все-таки наступает период инфицирования, возникает гнойное поражение забрюшинных клетчаточных пространств, то там речь уже идет о хирургическом лечении. Выбор хирургического лечения, он тоже многообразен. Это могут быть малоинвазивные методы, когда под контролем ультразвука производится пункция вот этих пространств, гной удаляется, вставляются дренажи. Или же более массивная, агрессивная терапия, когда вскрываются уже и хирургически объемно удаляются ткани, пораженные гноем. И пациенты ведутся на массивных перевязках. То есть это уже индивидуальность поражений, индивидуальность пациента и возможности того стационара, в которой этот человек попал. Но я хочу все-таки повторить, речь идет о панкреонекрозе, тяжелых формах панкреонекроза. Ольга Беклемищева: А все-таки как врач с опытом, много раз наблюдавший такие случаи, вы можете сказать – есть какие-то признаки, вот у кого может быть такая тяжелая ситуация, а у кого, скорее всего, ее не будет? Александр Линденберг: Это все-таки из области шаманства. Ольга Беклемищева: Пошаманьте немножко. Александр Линденберг: Очень сложно сказать. Ну, все-таки, скажем так, я не буду обижать людей полноватых, но у людей толстеньких, с пораженной, скажем, алкоголем печенью – это все-таки шанс развития панкреонекроза, и в более плохом развитии, выше, чем, скажем, у людей, у которых острый панкреатит является случайной ситуацией, возникшей, предположим, на фоне злоупотребления каким-нибудь жирным продуктом. Но это все очень и очень относительно. Бывает, к сожалению, как с генеральным прокурором, который ультраконсервативно был отправлен с панкреатитом, и ничего не пил и не ел. Сложно сказать, как все-таки разовьются события. Ольга Беклемищева: То есть именно идиопатический панкреатит? Александр Линденберг: Да. В наших наблюдениях он встречается достаточно редко. Все-таки 90 процентов случаев укладывается или в спиртное, или в поражение желчного пузыря и желчевыводящей системы. Ольга Беклемищева: Вот кроме идиопатических форм, кроме того, что связано с алкоголем и поджелудочной железой, существуют ли такие заболевания, которые вызываются химическими агентами, то есть может ли это быть результатом лекарственной терапии, да или нет? Александр Линденберг: В принципе, да. Но наблюдений мало. Не видели мы этого в больших количествах, только эксквизиты. Ольга Беклемищева: То есть если у человека индивидуальная непереносимость такого или иного лекарства? Александр Линденберг: Практически невозможно ни наблюдать, ни доказать, что панкреатит развился в результате приема того или иного препарата. Ольга Беклемищева: То есть это все только гипотеза? Александр Линденберг: Абсолютно точно. Ольга Беклемищева: Александр Алексеевич, вот вы уже, наверное, убедили наших слушателей, что это серьезная болезнь и что нужно обязательно обращаться к врачу. Давайте немножко порассуждаем, что будет в случае, если они все-таки обратятся и все хорошо вылечится. Есть ли какие-то последствия перенесенного острого панкреатита? Александр Линденберг: Давайте опять разграничивать: острого отечного панкреатита или панкреонекроза? Ольга Беклемищева: Острый отечный. Александр Линденберг: Если острый отечный, то, как правило, последствий практически не остается. Колоссальный запас функциональных возможностей поджелудочной железы делает возможным перенести это заболевание и остаться ей вполне функционирующей, как здоровый орган. Ольга Беклемищева: То есть те куски – прошу прощения за ненаучный подход к делу, – железы, которые, к сожалению, некротизировались в результате… Александр Линденберг: Их будет очень мало. Ольга Беклемищева: …они восстанавливаются? Александр Линденберг: Нет, не восстанавливаются. То, что погибло, замещается соединительной тканью, то есть тканью, которая не имеет функции той ткани, из которой состоит поджелудочная железа. Соединительная ткань уплотняется. Ольга Беклемищева: То есть поджелудочная железа – это не печень, которая может… Александр Линденберг: То же самое, что и с печенью. Потому что, скажем, острый гепатит, гибель клеток печени, замещение соединительной тканью – это заболевание, которое мы называем циррозом. В данной ситуации наступает почти то же самое – цирроз поджелудочной железы. Но при отечных формах он не наступит потому, что очень небольшая зона поражения. Поэтому возможности поджелудочной железы достаточно для того, чтобы оставить этот орган здоровым. При панкреонекрозе все зависит от объема поражения. Большой объем поражения, хронические изменения приводят к выявлению недостаточности и внешнесекреторной, то есть той, о которой вы говорили, при переваривании пищи. А потом и внутрисекреторной, потому что мы забыли сказать о том, что поджелудочная железа еще и хранитель островков Лангерганса, то есть ответственна за диабет… Ольга Беклемищева: Мы отдельно поговорим о поджелудочной железе и диабете. Александр Линденберг: Хорошо. Значит, возникает недостаточность и того, и другого. Чем больше поражение, тем выше недостаточность. И, таким образом, острый панкреатит превращается в заболевание, которое мы называем хроническим панкреатитом. Ольга Беклемищева: И у нас сейчас слушатель на линии. Это Любовь Николаевна из Москвы. Здравствуйте, Любовь Николаевна. Слушатель: Здравствуйте. Я хотела бы вас спросить, какие из перечисленных вами мероприятий, которые при панкреатите проводятся, проводятся бесплатно, а какие за отдельную плату? Вот вы о медицинском стандарте говорили. И я просто подумала: по карману ли это, в принципе, достаточно бедному человеку? Ольга Беклемищева: Спасибо. Александр Алексеевич, пожалуйста. Александр Линденберг: Так как я работаю в муниципальной больнице, могу сказать, что у нас все проводится бесплатно. Ольга Беклемищева: И лекарства все есть? Александр Линденберг: И лекарства почти все, как правило, есть. Естественно, чем тяжелее случай, тем сложнее его медикаментозная терапия. Могут понадобиться разные достаточно, так сказать, редкие препараты, которых может в больнице и не быть. Но это абсолютно индивидуальная ситуация. В принципе, острый панкреатит – заболевание муниципальное. Это не уши поправить. И поэтому все, что можно для любого пациента в отделении реанимации, где лечение, в принципе, дорогое, делается абсолютно бесплатно. Ольга Беклемищева: И я обращаю внимание тех наших слушателей, кто не является жителями Москвы, на самом деле приставленное к болезни слово “острый” означает, что государство обязано ее оплатить в России. Если с вас за это требуют деньги, значит, произошло нарушение закона. И следующий слушатель – это Николай Степанович из Москвы. Здравствуйте, Николай Степанович. Слушатель: Здравствуйте. А как протекает панкреатит хронический, вернее, его обострение? И существует ли такое понятие “обострение хронического панкреатита”? То есть до поры до времени у меня не было никакой симптоматики, а потом появилась разбитость, тошнота, отрыжка и, по-видимому, как я отметил, реакция на прием фальсифицированных продуктов, всяких йогуртов и так далее. Я был помещен в больницу, диагноз не установили, давали мне в огромном количестве антибиотики тяжелые. Я думал, что у меня что-то с урологией, потому что в урологию меня поместили. А попал в хирургию по биохимическому анализу – там один показатель был превышен в несколько раз – поставили диагноз “хронический панкреатит”. И все, что мне дают, – это Панкреатин и разные ферменты. Ольга Беклемищева: Спасибо, Николай Степанович. Очевидно, показатель – амилаза в моче или в крови? Александр Линденберг: Нет. Я думаю, что речь идет… ну, случай, так сказать, достаточно стандартный, но требующий определенного разбора. Потому что все зависит от того, в каком первоначальном состоянии находится поджелудочная железа пациента. Потому что если там есть соответствующие морфологические признаки хронического панкреатита и, что самое главное, если есть ее внешнесекреторная недостаточность… Ольга Беклемищева: А как она становится очевидной? Александр Линденберг: К сожалению, необходимо проведение специальных тестов – это либо радиоизотопное исследование, либо есть такой тест секретин-панкреозиминовый, который свидетельствует о том, что в ответ на стимуляцию поджелудочная железа не выбрасывает то количество ферментов, которое необходимо ей выбросить. Грубо говоря, в ответ на кусочек жирной пищи мы недополучаем тех ферментов, которые эту пищу должны переварить. Только мы, естественно, не даем пациенту баранью ножку, а вводим специальный препарат, который стимулирует выброс этих ферментов. Поэтому если есть это, то у пациента действительно хронический панкреатит, и его надо соответствующим образом лечить. Если все это развивается по той программе, о которой говорил уважаемый радиослушатель, то, скорее всего, речь идет об остром гастрите, возможно, дуодените. Может быть, даже язве двенадцатиперстной кишки. И хроническим панкреатитом здесь и не пахнет. Ольга Беклемищева: А вообще, как выглядит хронический панкреатит? Я вот спасибо скажу Николаю Степановичу за то, что он нас подвел к следующему этапу нашего разговора, потому что мы как раз с вами начинали говорить о том, что хронический панкреатит может быть осложнением острого панкреатита. Александр Линденберг: Ну, это не осложнение, это исход. Ольга Беклемищева: Да, итог большого пути. Александр Линденберг: Итог, да. Ну, как выглядит… Я уже говорил, что… Ольга Беклемищева: Клинически. Александр Линденберг: Как правило, это уже тупые боли, возникающие в ответ на то, что мы называем погрешностями в диете. Ольга Беклемищева: Съел немножечко жирненького, выпил рюмочку – и все. Александр Линденберг: Притом эти боли иногда доводят больного вплоть до Клиники неврозов. То есть клиника болей превалирует. Второе – это неустойчивый стул. То есть нарушение перевариваемости приводит к развитию поносов, то запоров, то поносов, то запоров. Человек худеет, как правило, худеет при настоящем хроническом панкреатите. И дальнейшее уже зависит от того, в каком проценте поражена поджелудочная железа, сколько клеток погибло, сколько осталось. Как правило, это заболевание, которое прогрессирует. Ольга Беклемищева: А как остановить это прогрессирование и как его лечить? Александр Линденберг: Как правило, надо устранить причину хронического панкреатита, то есть нарушение оттока секрета поджелудочной железы из ее протоков. Потому что исходы хронического панкреатита – это и киста поджелудочной железы, это различные свищи. Но, как правило, принцип оперативного вмешательства… здесь уже речь идет о большой хирургии, здесь консервативная терапия только на ранних этапах может быть эффективна. Хронический панкреатит в форме, так сказать, запущенной, как правило, оперируется. И есть две позиции, по которым мы оперируем этих пациентов. Это тяжелейший болевой синдром постоянный – и тогда это одна группа операций, которая собственно только ликвидирует боли. И вторая – это операции, которые ликвидируют увеличенное давление, то есть гипертензию в протоках поджелудочной железы. Это, как правило, могут быть эндоскопические операции, могут быть хирургические. Но смысл их в том, чтобы эти протоки либо естественным путем начали опорожняться без напряжения… Ольга Беклемищева: Куда им положено. Александр Линденберг: Нет, куда им положено, они опорожняются, но плохо. Либо куда им не положено начали опорожняться, для того, чтобы давление все-таки в них упало до определенной зоны. К сожалению, как последний вариант – это удаление органа. Ольга Беклемищева: Дай Бог, до этого не дойдет. И у нас следующий слушатель – Константин Викторович из Москвы. Здравствуйте, Константин Викторович. Слушатель: Здравствуйте. У меня вот такой вопрос. Мне в феврале сделали брахитерапию (облучение предстательной железы). Не могло ли это спровоцировать панкреатит? Александр Линденберг: Нет, это не имеет никакого отношения к поджелудочной железе. Можете спокойно продолжать курс. Поджелудочная железа здесь не при чем. Ольга Беклемищева: И следующий слушатель – это Николай из Курска. Здравствуйте, Николай. Слушатель: Здравствуйте. Я несколько лет тому назад видел полухирургический метод, там рассказывалось, что при ослаблении функций поджелудочной железы вроде бы как шприц и игла толстая – и прямо непосредственно через брюшную полость вводились как бы донорские клетки поджелудочной железы. Вы не можете рассказать об этом методе? И при каких осложнениях этот метод применяется? И еще один момент. Все-таки воспаление поджелудочной железы и все, что с этим связано, – это ведь связано, скорее всего, и с иммунными дефицитами какими-нибудь в организме? Спасибо большое. Александр Линденберг: Начнем со второго вопроса. Есть теория, особенно, как ни странно, она относится к хроническому панкреатиту, теория, что иммунодефицит, ну, не такой грозный, как ВИЧ-инфекция, а стандартные иммунодефициты могут приводить к развитию острого панкреатита. Хотя доказательств этому достаточно мало. Но теория такая существует. А по первому вопросу, скорее всего, речь идет о пересадке клеток островков Лангерганса. Ольга Беклемищева: Это была одна из попыток в лечении диабета. Александр Линденберг: Это не панкреатит был. Ольга Беклемищева: И следующий слушатель – это Раиса Егоровна из Москвы. Здравствуйте, Раиса Егоровна. Слушатель: Здравствуйте, уважаемые собеседники. Первый вопрос. Почему не была заранее анонсирована эта программа? Ее можно было бы записать на пленку, настолько она актуальна. Второе. Скажите, пожалуйста, куда обращаться, если возникнет проблема с панкреатитом – лично к вам или к сотрудникам вашего института? И третье. Мужчина 40 лет, удален два года назад желчный пузырь. Вес у него 92 килограмма. Скажите, есть ли у него предпосылки к тому, чтобы у него был панкреатит? Ольга Беклемищева: Спасибо. Александр Линденберг: Начнем с вопроса о мужчине. О предпосылках сказать очень сложно. Для того чтобы определить, угрожаем ли он по развитию панкреатита, нужно уточнить только две вещи – является ли он любителем спиртного и в каком состоянии сейчас у него находятся желчные пути. Для того чтобы это уточнить, надо сделать достаточно приличное ультразвуковое исследование. И то, и другое дает возможность в какой-то степени прогнозировать возможность развития этого заболевания у конкретного человека. Это первое. Ольга Беклемищева: И где вас найти, как я понимаю? Александр Линденберг: Я уже говорил, что острым панкреатитом занимается целый ряд клиник Москвы. В частности, и Первая городская больница – Клиника академика Савельева, и 31-ая городская больница – это кафедра профессора Шаповальянца и Юрия Михайловича Панцырева, лаборатория эндоскопии. Ольга Беклемищева: Доцентом которой является наш гость. А по поводу того, что не было анонса, ну, извините. Исправлюсь. И вот это одно из осложнений острого панкреатита, то есть один из вариантов развития событий после острого панкреатита, когда появляется хронический панкреатит. Но есть и такая вещь, как действительно вторая половина медали, второй набор функций поджелудочной железы – это ее участие в изготовлении инсулина и в нашем внутреннем углеводном обмене. И вот насколько страдает эта функция при остром панкреатите и при панкреонекрозе? Или, наоборот, может ли диабет являться… Александр Линденберг: Начнем со второго вопроса. Диабет не является предрасполагающим фактором к развитию панкреонекроза. А что касается углеводного обмена, то при тяжелых формах панкреонекроза, как правило, возникает латентно текущий сахарный диабет. И он острый на момент развития панкреонекроза, и в дальнейшем, если пациент выписывается, как правило, он требует дополнительного обследования. И, возможно, что он и не возникнет. Все зависит от объема поражения поджелудочной железы. Но если объемы велики, то латентно текущий сахарный диабет, как правило, – это спутник первичного панкреонекроза. Ольга Беклемищева: И он останется с человеком уже потом надолго? Александр Линденберг: Я уже говорил, что если поражение небольших объемов, то может не остаться. Хотя диета определенная останется на всю жизнь – я имею в виду по сахарному диабету. Если это объемы большие, и дальше развивается осложнение, о котором мы уже говорили, то это, как правило, латентно текущий диабет, может быть, и не требующий приема инсулина. Сейчас достаточно хорошо развиты таблетированные формы лечения этой патологии. Ну и соответствующая диета. Ольга Беклемищева: Спасибо. И следующий слушатель – это Людмила Ивановна из Красногорска. Здравствуйте, Людмила Ивановна. Слушатель: Здравствуйте. Я почти год назад лежала с острым панкреотином. И вот у меня сейчас результаты УЗИ. У меня желчный пузырь деформирован в области дна, поперечник 28, полость однородна, конкрементов нет, образований нет. Александр Линденберг: Стенка желчного пузыря как изменена? Про стенку что написано? Слушатель: Стенки не изменены, истончены 2 миллиметра. Ольга Беклемищева: Спасибо, Людмила Ивановна. Александр Линденберг: Человек предрасположен к развитию панкреатита. Скорее всего, речь идет о том, что имеются как раз минимальные признаки холестаза, то есть желчь уже не такая, какая она должна быть, ее свойства, она становится более тягучей, предрасположена к камнеобразованию. Ольга Беклемищева: Но камней, насколько я понимаю, еще нет. Александр Линденберг: Нет. Камней нет видимых. Могут быть микрокристаллы. Но этого тоже достаточно для того, чтобы человек перенес панкреатит. Принимая во внимание наличие смертельно опасного осложнения, надо убирать пузырь, надо оперировать, делать холецистэктомию. Ольга Беклемищева: Людмила Ивановна, подумайте, пожалуйста. И следующий слушатель – это Михаил Яковлевич из Москвы. Здравствуйте, Михаил Яковлевич. Слушатель: Добрый день. Я болею давно. Удален пузырь у меня пять лет назад. И очень часто у меня боли в подреберье, в районе пупка, чуть выше. Ну, наблюдаюсь я у врача, лечусь. Принимал Панкреатин в основном, Креон принимал до этого. Вот и все лечение. И у меня еще язва двенадцатиперстной кишки очень часто. А состояние такое: поем… вроде бы на диете постоянно сижу, длительный период времени, а что-нибудь такое, ну, буквально минимальное… бульоны нежирные в основном, съем – и у меня боли в этом районе. Александр Линденберг: Все понятно. Вы страдаете “постхолецистэктомическим синдромом”. Не пытайтесь запомнить, название довольно сложное. Вообще вам надо ложиться в клинику, обследоваться, принимать какие-то радикальные принципы по поводу лечения язвы – и тогда можно подумать о том, как выправить ситуацию с поджелудочной железой. У вас плохо функционирует двенадцатиперстная кишка. “Постхолецистэктомический синдром”. Ольга Беклемищева: И он достаточно часто бывает после удаления желчного пузыря? Александр Линденберг: В общем, к сожалению, встречается, да, где-то в 7 процентах случаев. При колоссальных объемах холецистэктомии это, в общем, достаточно большая цифра. Ольга Беклемищева: А почему такие колоссальные объемы? Насколько та тактика, которая выбрана современным врачебным сообществом по удалению желчного пузыря, она оправдана? Александр Линденберг: Этот вопрос к панкреатиту не имеет большого отношения, но я отвечу. Тактика абсолютно верная, потому что сама операция разработана до мельчайших подробностей. А с развитием эндоскопической техники она стала еще более удобной. Наличие камней – это смертельно опасная ситуация именно по развитию целого ряда осложнений, в том числе и возвращаясь к нашей теме панкреатитов. И развития “постхолецистэктомического синдрома” можно избежать, и самое главное, на современном этапе прекрасным образом вылечить. Поэтому даже возможное его развитие не является тем препятствием, которое остановит пациента, которому надо удалять желчный пузырь с камнями. Ольга Беклемищева: И следующий слушатель – это Галина из Москвы. Здравствуйте. Слушатель: Здравствуйте. Скажите, пожалуйста, существует ли какая-то связь между герпесом второго типа, заболеваниями поджелудочной железы в общем и сахарным диабетом? Спасибо. Александр Линденберг: Ну, вопрос, конечно, непростой. В принципе, возможна связь… отрицать ее невозможно, доказать практически тоже. Да, может быть. Именно в силу того, что имеется некая иммунологическая ситуация, связанная с дефицитом в организме – собственно герпес, и поражения поджелудочной железы в этих ситуациях описаны. По крайней мере, как единичный случай это встречается. Ольга Беклемищева: Тем не менее, я напоминаю о том выступлении, которое мы слышали со стороны Даниила Борисовича Голубева. Когда он перечислял те агенты, связь которых с некоторыми панкреатитами вроде бы более очевидна, он все время упоминал именно бактерии и микробы, но не вирусы. Потому что с вирусами пока что совершенно неясно. А вот по поводу диабета мы уже говорили. Но я прошу Александра Алексеевича повторить для нашей слушательницы. Александр Линденберг: То, что диабет не является предрасполагающим фактором к развитию панкреатита, это абсолютно точно. Ольга Беклемищева: И это очень хорошо, потому что, к сожалению, диабет тоже очень распространенное заболевание. Было бы крайне обидно, если бы все это еще и накладывалось друг на друга. И у нас еще один слушатель – это Семен из Москвы. Здравствуйте, Семен. Слушатель: Здравствуйте. Вот мне проводили исследование по методу Фолля. Нашли хронический холецистит. Но я ничего не чувствую. Правда, я жирного мало ем, в общем, избегаю. И мне просто интересно, как мне быть? Александр Линденберг: Очень просто. Сделайте ультразвуковое исследование печени и поджелудочной железы. Бывают ситуации, когда клиники нет, то, что мы называем “камненосительством”. Ну, в метод Фолля я не очень верю. А вот в хороший ультразвуковой аппарат, с хорошим специалистом верю абсолютно и стопроцентно. И все ваши сомнения будут тут же разрешены. Есть камни, есть изменение в стенке желчного пузыря – значит, есть и признаки “камненосительства”, хронического холецистита. А при этом клиники может и не быть. Ольга Беклемищева: А может ли быть воспаление поджелудочной железы при отсутствии клиники? Или уж у нее клиника-то есть всегда? Александр Линденберг: Если речь идет о хроническом холецистите… Ольга Беклемищева: Я понимаю. Александр Линденберг: А у поджелудочной железы всегда будет клиника. Ольга Беклемищева: И это, в общем-то, в определенном смысле, хорошо. Александр Линденберг: То, что у нас очень часто находят уплотненную поджелудочную железу, и тут же приклеивают человеку соответствующий диагноз хронического панкреатита, это, как правило, возрастные изменения. Потому что если клиники нет у поджелудочной железы, то нет и заболевания. Ольга Беклемищева: А с возрастом она действительно может выглядеть более плотно на УЗИ-исследовании. Александр Линденберг: Естественно, как и любой орган, она стареет. Ольга Беклемищева: Ну что ж, и теперь поговорим о профилактике заболевания поджелудочной железы. Я понимаю, что вопрос действительно очень расплывчатый, потому что какой-то специфической профилактики не существует. Но я думаю, что некоторые вещи надо повторять и повторять, даже если их не очень слушают. Но я надеюсь, что наши слушатели послушаются. Так все-таки, как нужно себя вести, чтобы снизить риск заболевания поджелудочной железы? Александр Линденберг: Я боюсь оказаться вообще в субботний вечер белой вороной, потому что первое, с чего мы начинаем, – это то, что надо умеренно есть и умеренно пить. Я даже не пытаюсь говорить, что вообще не пить, но, по крайней мере, хотя бы пить умеренно. 90 процентов тяжелых панкреонекрозов все-таки связаны с нарушениями… то, что мы так стыдливо называем “нарушениями диеты”. Это первый вариант профилактики. Второй – это следить за собой в тех ситуациях, когда у вас появляются какие-либо заболевания, связанные с желчевыводящими путями и желчным пузырем, надо их лечить, хотя это чаще всего хирургическое лечение или эндоскопическое. То есть, по крайней мере, не оставлять риск развития панкреонекроза. Потому что вылечить холецистит во много раз проще, чем вылечить панкреонекроз, и пациент должен это понимать. Потому что имея угрозу развития панкреонекроза при наличии камней в желчном пузыре или протоках, они должны представлять, что они идут по очень и очень опасной тропке. Ольга Беклемищева: И нет никаких других методов, например, травы? Александр Линденберг: Нет. Никакие травы не помогут. Ольга Беклемищева: А биодобавки? Александр Линденберг: Тем более. Они могут только спровоцировать развитие панкреонекроза, а отнюдь не его профилактику. Потому что есть камни в желчном пузыре, есть нарушение обмена, которое к этим камням приводит, и никаких вариантов развития событий, кроме как хирургических, здесь не предусмотрено. Попытки дробить эти камни, выводить их с помощью различных препаратов, которые вызывают их растворение, всегда опасны именно развитием панкреонекрозов. Вот мой коллега из Америки говорил о манипуляциях. Вот как раз вот эти самые манипуляции, связанные с дроблением камней в желчном пузыре, с попытками их растворения и выведения, по аналогии с камнями в почках, то если в почках этот вариант достаточно отработан и безопасен, то тяжелейшие последствия всего этого – это, как правило, панкреонекроз с неприятными исходами, так скажем. Ольга Беклемищева: То есть дробить камни в желчном пузыре нельзя. Александр Линденберг: Ни под каким видом нельзя, или растворять их. Хотя такие попытки делаются в медицинских учреждениях. Но это всегда большой риск. И поэтому не надо этим заниматься, тем более самостоятельно, без присмотра врача. Ольга Беклемищева: И еще один вопрос, который задавал мне слушатель по интернету. Я бы хотела, чтобы вы на него ответили. Дело в том, что у мамы ребенку 4 года, и у него врожденная панкреатопатия. И чем ему это грозит в жизни? И можно ли от этого вылечиться? Александр Линденберг: Во-первых, начнем с того, что хотелось бы знать, на основании каких методов исследования ребенку был поставлен этот диагноз. Ольга Беклемищева: К сожалению, она об этом не пишет. Александр Линденберг: А она об этом не говорит. Поэтому доказательств наличия панкреатопатии детской… это очень сложно. А лечится это ферментами. Ольга Беклемищева: Большое спасибо, Александр Алексеевич. Всего вам доброго! Постарайтесь не болеть.Острый панкреатит – признаки, причины, симптомы, лечение и профилактика
Диагностика
Любой из вышеперечисленных симптомов должен стать причиной записаться на прием к врачу-гастроэнтерологу. Дополнительно необходимо получить консультацию врача-хирурга.
Для диагностики используют физикальные, лабораторные и инструментальные методы исследований:
- индикаторные и патогенетические биохимические тесты;
- УЗИ поджелудочной железы;
- рентгенография;
- КТ поджелудочной железы и МРТ поджелудочной железы;
- лапароскопия;
- ангиография;
- эндоскопия верхних отделов ЖКТ.
Лечение
Методы лечения для каждого пациента подбирается строго индивидуально. Консервативное лечение включает:
- голодание;
- дезинтоксикация организма;
- снятие спазмов гладкой мускулатуры;
- установка назогастрального зонда для декомпрессии желудка;
- антибактериальная терапия назначается для предупреждения или лечения инфекционных осложнений.
Хирургическое лечение бывает нескольких видов:
- установка дренажей и перитонеальный лаваж-диализ;
- резекция поджелудочной железы или ее отделов;
- операция Лоусона.
Основным осложнением после оперативного лечения недуга являются рецидивы, артроз сосудов, кровотечения, абсцессы.
Профилактика
К профилактическим мерам по предупреждению развития заболевания относится отказ от алкоголя, ведь именно он активирует выработку секретина, который приводит к гиперсекреции (самоперевариванию) поджелудочной железы.
Литература и источники
Видео по теме:
Лечение панкреатита. Диета при остром панкреатите.
В первой статье цикла «Панкреатит. Причины и симптомы
панкреатита» домсоветов начал знакомить читателей с особенностями такой
неприятной болезни как панкреатит. Сегодня вы узнаете, что такое острый и
хронический панкреатит, как проводится их лечение, а также какой должна быть
диета при приступе острого панкреатита.
Острый панкреатит. Лечение острого панкреатита.
Итак, острый панкреатит – это воспаление поджелудочной
железы, занимающее одно из первых мест по частоте среди болезней органов брюшины. Воспаление обычно
провоцируется перееданием либо одновременным приемом жирной, острой пищи и
алкоголя. Помимо этого приступ может быть вызван желчекаменной болезнью,
воспалением или язвенной болезнью двенадцатиперстной кишки, травмами живота, острыми
инфекциями (часто вирусным гепатитом), эндокринными сбоями.
Характерным и
наиболее ярко выраженным признаком острого панкреатита является сильнейшая приступообразная боль в
животе, которая не дает даже разогнуться. Боль нарастает и может привести к болевому
шоку, потере сознания, снижению артериального давления, учащению пульса.
Присутствует и рвота с желчью, диарея, вздутие живота, налет на языке,
наблюдается парез кишечника (не ощущается перистальтика). Повышается
температура тела, нарушается микроциркуляция крови, о чем свидетельствуют
синюшные пята около пупка и на животе. Более
60% случаев острого панкреатита списывается на острое отравление, а 15%
приступов заканчиваются летальным исходом. Диагностируется острый панкреатит не
так уж и сложно – проводится УЗИ, которое
подтверждает увеличение поджелудочной железы за счет ее воспаления и устанавливает форму болезни; в
крови и моче резко возрастает уровень амилазы; в крови – значительный рост СОЭ
и лейкоцитов.
Различают несколько форм острого панкреатита. Отечная форма
(интерстициальный панкреатит) и панкреонекроз (геморрагический, жировой и
гнойный). Наиболее благоприятный прогноз при отечном панкреатите –
поджелудочная железа воспалена, но соседние органы и ткани не измены. Сложнее
обстоят дела при геморрагическом панкреонекрозе – в поджелудочной железе
возникают очаги кровоизлияний, в брюшине скапливается жидкость. Жировая форма
характеризуется многочисленными пятнами жирового некроза, которым поражена не
только сама железа, но и органы брюшной полости. И, наконец, самый страшный –
гнойный панкреонекроз – когда очаги гнойного поражения присутствуют даже в
соседних тканях, а в брюшине скапливается гной. Думаю, даже человек, далекий от
медицины поймет, что любая форма острого панкреатита катастрофически опасна для
жизни больного, поэтому ни о каком самолечении не может быть и речи! Человека,
у которого случился приступ острого панкреатита, необходимо в экстренном
порядке госпитализировать (как правило, в хирургическое отделение или отделение
реанимации).
Лечение острого панкреатита проводится под девизом «голод,
холод и покой». В первые три-четыре дня (иногда до пяти), в период
шок-коллапса, показан строжайший постельный
режим, голод и щелочное питье не газированных вод (до одного литра в
сутки), ледяная грелка на живот. Иногда требуется промывание желудка.
Внутривенно вводятся обезболивающие и спазмолитики, с помощью специальных
препаратов приглушается секреторная функция поджелудочной железы. Помимо этого,
для предотвращения инфекционных осложнений проводится антибиотикотерапия, а также детоксикация организма.
Через три-четыре
дня больного начинают дробно кормить, при этом обязательно соблюдение
строжайшей диеты. Медикаментозная терапия продолжается. Нервное перевозбуждение
и отсутствие полноценного сна у пациентов замедляет выздоровление.
Диета при остром панкреатите.
Как уже было сказано, в первые 3-4 дня со дня приступа
рекомендован голод, после чего показан дробный и многократный прием пищи (5-6
раз в день маленькими порциями). Вся
еда должная быть теплой, ни в коем случае не горячей и не холодной. В первые
несколько недель еду не нужно солить. Пища должна быть протертой или
жидкой консистенции, категорически запрещены жареные и тушеные блюда (только
отварное или приготовленное на пару). Рекомендуются: слизистые каши или супы-пюре с
крупами (овсяная, манная,рисовая), картофельное пюре, отварное и перетертое
диетическое мясо (кролик, телятина) в виде пудингов и суфле, сухарики пшеничные. Постепенно рацион расширяется за счет
введения печеных яблок, сливочного масла (например, добавлять 5-10 г в каши), парового омлета
или яиц всмятку, пудингов из нежирного
творога, нежирных сортов рыбы. Со временем
нужно постепенно переходить на
менее щадящий для желудка режим – отказаться от протирания блюд.
Такой диеты важно придерживаться в течении 6-9 месяцев. Погрешности
питания могут спровоцировать переход панкреатита в хроническую форму. К слову,
90% успеха лечения зависит от соблюдения диеты. Помимо этого нужно полностью
исключить употребление алкогольных
напитков, рекомендуется отказ от курения.
Хронический панкреатит. Лечение хронического панкреатита.
Как уже было сказано выше, если панкреатит не лечить, не
соблюдать рекомендации врачей и диету, многократно возрастает вероятность постепенного
прогрессирования заболевания и переход его в хроническую форму. Симптомы этого заболевания идентичны с
проявлениями острого панкреатита, только не столь ярко выражены. Больной
периодически ощущает боль в животе (обычно после переедания, отклонения от
диеты, приема спиртных напитков), его постоянно подташнивает, ухудшается
аппетит, беспокоит вздутие и урчание живота, резко обозначено отвращение к
жирным блюдам, стул становится жидким, тяжело смывается с унитаза (жирный
блеск, пластилиновая консистенция), снижается масса тела. В любой момент течение хронического
панкреатита может обостриться, что приведет к приступу острого
панкреатита. Как вы понимаете, в этом
случае не обойтись без госпитализации.
В лечении хронического панкреатита вне
обострений на первый
план выходит диета и регулярный прием ферментативных препаратов. Важно
понимать, что в связи с нарушением функций поджелудочной железы, любая
нагрузка (тяжелая пища, стресс) может быть причиной острого
панкреатита. Необходимо также правильно назначить ферментативный
препарат. Дело в том, что их существует превеликое множество, и
отличаются они
не только стоимостью, но и составом. Назначение производит лечащий врач
на
основании проведенных анализов, поэтому обязательно поговорите с ним о
том, почему назначен
именно этот препарат. Со временем, и при условии отказа от жирной пищи,
дневную
дозу ферментативных препаратов можно будет варьировать. Больным
хроническим панкреатитом нельзя нервничать и поднимать тяжести.
Существует также мнение (у восточных целителей), что панкреатитом –
болезнь людей, которые очень волнуются за свою семью.
Миллионы людей живут с диагнозом хронический панкреатит.
Они
вырабатывают своеобразный стиль жизни, который базируется на соблюдении
всех
«можно» и «нельзя». Созданы целые
порталы, где люди, страдающие панкреатитом, общаются, делятся своими
«диетическими» успехами, просят советов (например сайт
панкреатиту.нет). И самое главное, там вы узнаете как люди научились
ценить
такую «трезвую и диетическую» жизнь!
В следующей статье мы поговорим о народных методах лечения
панкреатита, а также приведем рекомендуемую при хроническом панкреатите диету и
простые рецепты диетических блюд.
Что такое острый отечный панкреатит?
Telem DA, Bowman K, Hwang J, Chin EH, Nguyen SQ, Divino CM. Избирательное ведение пациентов с острым билиарным панкреатитом. Дж Гастроинтест Сург . 2009 13 декабря (12): 2183-8. [Медлайн].
Banks PA, Bollen TL, Dervenis C и др., Для Рабочей группы по классификации острого панкреатита. Классификация острого панкреатита – 2012: пересмотр классификации и определений Атланты на основе международного консенсуса. Кишечник . 2013 Январь 62 (1): 102-11. [Медлайн].
Haydock MD, Mittal A, van den Heever M и др., Для Сети поджелудочной железы Новой Зеландии. Национальное исследование инфузионной терапии при остром панкреатите: в текущей практике отсутствует надежная доказательная база. Мир J Surg . 2013 Октябрь 37 (10): 2428-35. [Медлайн].
Ai X, Qian X, Pan W. и др. Чрескожный дренаж под контролем УЗИ может снизить смертность от тяжелого острого панкреатита. Дж Гастроэнтерол . 2010. 45 (1): 77-85. [Медлайн].
Li H, Qian Z, Liu Z, Liu X, Han X, Kang H. Факторы риска и исход острой почечной недостаточности у пациентов с тяжелым острым панкреатитом. J Crit Care . 2010 июн.25 (2): 225-9. [Медлайн].
Whitcomb DC, Yadav D, Adam S, et al, для Североамериканской группы по изучению поджелудочной железы. Многоцентровый подход к рецидивирующему острому и хроническому панкреатиту в США: Североамериканское исследование панкреатита 2 (NAPS2). Панкреатология . 2008. 8 (4-5): 520-31. [Медлайн]. [Полный текст].
Эльмунцер Б.Дж., Шейман Дж.М., Леман Г.А. и др., Для Американского кооператива по исследованию исходов в эндоскопии (USCORE). Рандомизированное исследование ректального применения индометацина для профилактики панкреатита после ЭРХПГ. N Engl J Med . 2012 апр. 12, 366 (15): 1414-22. [Медлайн].
Камисава Т., Фуната Н., Хаяси Ю. и др. Новый клинико-патологический субъект аутоиммунного заболевания, связанного с IgG4. Дж Гастроэнтерол . 2003. 38 (10): 982-4. [Медлайн].
Yadav D, Lowenfels AB. Эпидемиология панкреатита и рака поджелудочной железы. Гастроэнтерология . 2013 июнь 144 (6): 1252-61. [Медлайн]. [Полный текст].
Пири А.Ф., Деллон Э.С., Лунд Дж. И др. Бремя желудочно-кишечных заболеваний в США: обновление 2012 г. Гастроэнтерология . 2012 ноябрь 143 (5): 1179-1187.e3. [Медлайн]. [Полный текст].
Singla A, Csikesz NG, Simons JP, et al.Объем общенациональной больницы при остром панкреатите: анализ общенациональной стационарной выборки за 1998-2006 гг. Е.П.Б. (Оксфорд) . 2009 11 августа (5): 391-7. [Медлайн]. [Полный текст].
Кришна С.Г., Камбодж А.К., Харт П.А., Хинтон А., Конвелл Д.Л. Изменяющаяся эпидемиология госпитализаций при остром панкреатите: десятилетие тенденций и влияние хронического панкреатита. Поджелудочная железа . 2017 Апрель 46 (4): 482-8. [Медлайн]. [Полный текст].
Банки П.А.Эпидемиология, естественное течение и предикторы исхода заболевания при остром и хроническом панкреатите. Гастроинтест Endosc . 2002 г., декабрь 56 (6 доп.): S226-30. [Медлайн].
Morinville VD, Barmada MM, Lowe ME. Рост заболеваемости острым панкреатитом в американском педиатрическом центре третичной медицинской помощи: есть ли большая осведомленность среди ответственных врачей ?. Поджелудочная железа . 2010 января 39 (1): 5-8. [Медлайн].
Ахтар А.Дж., Шахин М.Экстрапанкреатические проявления острого панкреатита у афроамериканцев и латиноамериканцев. Поджелудочная железа . 2004 29 ноября (4): 291-7. [Медлайн].
Huh JH, Jeon H, Park SM, et al. Сахарный диабет связан со смертностью при остром панкреатите. Дж Клин Гастроэнтерол . 2018 Февраль 52 (2): 178-83. [Медлайн].
Уиткомб округ Колумбия. Клиническая практика. Острый панкреатит. N Engl J Med . 2006 18 мая. 354 (20): 2142-50.[Медлайн].
Суппиа А., Малде Д., Араб Т. и др. Прогностическое значение отношения нейтрофил-лимфоциты (NLR) при остром панкреатите: определение оптимального NLR. Дж Гастроинтест Сург . 2013 Апрель 17 (4): 675-81. [Медлайн].
Mikolasevic I, Orlic L, Poropat G, et al. Безалкогольная жировая дистрофия печени и тяжесть острого панкреатита. Eur J Intern Med . 2017 Март 38: 73-8. [Медлайн].
Котари С, Калиновски М, Кобешко М, Альмуради Т.Компьютерная томография в диагностике острого неосложненного панкреатита: полезность против стоимости . Мир Дж. Гастроэнтерол . 2019 7 марта. 25 (9): 1080-7. [Медлайн]. [Полный текст].
Имамура Ю., Хирота М., Ида С. и др. Значение степени почечного края при компьютерной томографии в оценке тяжести острого панкреатита. Поджелудочная железа . 2010 января 39 (1): 41-6. [Медлайн].
Balthazar EJ, Ranson JH, Naidich DP, Megibow AJ, Caccavale R, Cooper MM.Острый панкреатит: прогностическое значение КТ. Радиология . 1985 Сентябрь 156 (3): 767-72. [Медлайн].
Бальтазар Э.Дж., Робинсон Д.Л., Мегибоу А.Дж., Рэнсон Дж. Х. Острый панкреатит: значение КТ для установления прогноза. Радиология . 1990 Февраль 174 (2): 331-6. [Медлайн].
Balthazar EJ. Стадия острого панкреатита. Радиол Клин Норт Ам . 2002 Декабрь 40 (6): 1199-209. [Медлайн].
Бадалов Н, Теннер С, Бэйли Дж.Профилактика, распознавание и лечение панкреатита после ЭРХПГ. СОП . 2009 9 марта. 10 (2): 88-97. [Медлайн].
Тестони П.А., Мариани А., Джуссани А. и др. Для группы компаний SEIFRED. Факторы риска пост-ЭРХПГ панкреатита в центрах с большим и низким объемом операций, а также среди опытных и неспециализированных операторов: проспективное многоцентровое исследование. Ам Дж. Гастроэнтерол . 2010 августа 105 (8): 1753-61. [Медлайн].
Parihar V, Ridgway PF, Conlon KC, Huggett M, Ryan BM.Роль эндоскопического вмешательства в лечении воспалительных скоплений жидкости поджелудочной железы. евро J Гастроэнтерол Hepatol . 2017 Апрель 29 (4): 371-9. [Медлайн].
Имри CW. Прогностические показатели при остром панкреатите. Банка J Гастроэнтерол . 2003 май. 17 (5): 325-8. [Медлайн].
Кришнан К. Нутритивное лечение острого панкреатита. Curr Opin Gastroenterol . 2017 марта 33 (2): 102-6. [Медлайн].
Jacobson BC, Vander Vliet MB, Hughes MD, Maurer R, McManus K, Banks PA. Проспективное рандомизированное исследование прозрачных жидкостей в сравнении с твердой диетой с низким содержанием жиров в качестве начального приема пищи при легком остром панкреатите. Клин Гастроэнтерол Гепатол . 2007 5 августа (8): 946-51; викторина 886. [Medline]. [Полный текст].
Баккер О.Дж., ван Бруншот С., ван Сантворт Х.С. и др. Для Голландской исследовательской группы по панкреатиту. Раннее кормление через назоэнтерический зонд в сравнении с кормлением по требованию при остром панкреатите. N Engl J Med . 2014 20 ноября. 371 (21): 1983-93. [Медлайн].
Марави-Пома Е., Дженер Дж., Альварес-Лерма Ф. и др., Испанская группа по изучению септических осложнений при тяжелом остром панкреатите. Раннее лечение антибиотиками (профилактика) септических осложнений при тяжелом остром некротическом панкреатите: проспективное рандомизированное многоцентровое исследование, сравнивающее две схемы лечения имипенемом-циластатином. Intensive Care Med . 2003 29 ноября (11): 1974-80.[Медлайн].
Изенманн Р., Рунци М., Крон М. и др. Для Немецкой исследовательской группы по антибиотикам при тяжелом остром панкреатите. Профилактическое лечение антибиотиками у пациентов с прогнозируемым тяжелым острым панкреатитом: плацебо-контролируемое двойное слепое исследование. Гастроэнтерология . 2004 апр. 126 (4): 997-1004. [Медлайн].
Джонсон С.Д., Кингснорт А.Н., Имри К.В. и др. Двойное слепое рандомизированное плацебо-контролируемое исследование антагониста фактора активации тромбоцитов, лексипафанта, в лечении и профилактике органной недостаточности при прогнозируемом тяжелом остром панкреатите. Кишечник . 2001, январь, 48 (1): 62-9. [Медлайн]. [Полный текст].
Абулиан А., Чан Т., Ягубиан А. и др. Ранняя холецистэктомия безопасно сокращает время пребывания в стационаре у пациентов с желчнокаменным панкреатитом легкой степени: рандомизированное проспективное исследование. Энн Сург . 2010 Апрель 251 (4): 615-9. [Медлайн].
Guadagni S, Cengeli I, Palmeri M, et al. Ранняя холецистэктомия при нетяжелом остром желчнокаменном панкреатите: легче сказать, чем сделать. Минерва Чир .2017 Апрель 72 (2): 91-7. [Медлайн].
van Santvoort HC, Besselink MG, Bakker OJ, et al, для Голландской исследовательской группы по панкреатиту. Пошаговый подход или открытая некрэктомия при некротическом панкреатите. N Engl J Med . 2010, 22 апреля. 362 (16): 1491-502. [Медлайн].
[Рекомендации] Теннер С., Бэйли Дж., ДеВитт Дж., Ведж С.С. и Американский колледж гастроэнтерологии. Рекомендации Американского колледжа гастроэнтерологии: ведение острого панкреатита. Ам Дж. Гастроэнтерол . 2013 сентябрь 108 (9): 1400-15; 1416. [Медлайн].
[Рекомендации] Crockett SD, Wani S, Gardner TB, Falck-Ytter Y, Barkun AN, Комитет клинических рекомендаций Института Американской гастроэнтерологической ассоциации. Руководство Института Американской гастроэнтерологической ассоциации по начальному ведению острого панкреатита. Гастроэнтерология . 2018 Март 154 (4): 1096-101. [Медлайн].
[Рекомендации] Веге С.С., Зиринг Б., Джайн Р., Моайеди П. и Комитет по клиническим рекомендациям Американской гастроэнтерологической ассоциации.Руководство института Американской гастроэнтерологической ассоциации по диагностике и лечению бессимптомных неопластических кист поджелудочной железы. Гастроэнтерология . 2015 апр. 148 (4): 819–22; викторина 12-3. [Медлайн].
[Рекомендации] Леппаниеми А., Толонен М., Тараскони А. и др. Рекомендации WSES 2019 по ведению тяжелого острого панкреатита. Мир J Emerg Surg . 2019. 14:27. [Медлайн]. [Полный текст].
Грейнджер Дж., Ремик Д.Острый панкреатит: модели, маркеры и медиаторы. Ударная . 2005 24 декабря, приложение 1: 45-51. [Медлайн].
Wu BU, Hwang JQ, Gardner TH, et al. Лактатный раствор Рингера уменьшает системное воспаление по сравнению с физиологическим раствором у пациентов с острым панкреатитом. Клин Гастроэнтерол Гепатол . 2011 августа, 9 (8): 710-7.e1. [Медлайн].
Ким С.Б., Ким Т.Н., Чунг Х.Х., Ким К.Х. Небольшой размер желчных камней и отсроченная холецистэктомия увеличивают риск рецидивов панкреатобилиарных осложнений после разрешения острого билиарного панкреатита. Dig Dis Sci . 2017 Март 62 (3): 777-83. [Медлайн].
Петров М.С., Ядав Д. Глобальная эпидемиология и комплексная профилактика панкреатита. Нат Рев Гастроэнтерол Гепатол . 2019 16 марта (3): 175-84. [Медлайн]. [Полный текст].
Мачикадо Дж. Д., Ядав Д. Эпидемиология рецидивирующего острого и хронического панкреатита: сходства и различия. Dig Dis Sci . 2017 Июль 62 (7): 1683-91. [Медлайн]. [Полный текст].
[Рекомендации] Веге С.С., ДиМаньо М.Дж., Форсмарк С.Е., Мартель М., Баркун А.Н.Первичное лечение острого панкреатита: Технический обзор Института Американской Гастроэнтерологической Ассоциации. Гастроэнтерология . 2018 Март 154 (4): 1103-39. [Медлайн].
Острый панкреатит: диагностика, прогноз и лечение
1. Руссо М.В., Вэй JT, Тонкий МТ, Гангароза Л.М., Коричневый А, Рингель Y, и другие. Статистика болезней органов пищеварения и печени, 2004. Гастроэнтерология .2004; 126: 1448–53 ….
2. Triester SL, Kowdley KV. Факторы прогноза при остром панкреатите. Дж Клин Гастроэнтерол . 2002; 34: 167–76.
3. Дервенис С, Джонсон CD, Басси C, Брэдли Э, Имри CW, МакМахон MJ, и другие. Диагностика, объективная оценка степени тяжести и лечение острого панкреатита. Консенсусная конференция Санторини. Инт Дж. Панкреатол . 1999; 25: 195–210.
4. Сваруп В.С., Чари СТ, Clain JE. Тяжелый острый панкреатит. ЯМА . 2004; 291: 2865–8.
5. Митчелл Р.М., Бирн М.Ф., Бэйли Дж. Панкреатит. Ланцет . 2003; 361: 1447–55.
6. Рабочая группа Британского общества гастроэнтерологов; Ассоциация хирургов Великобритании и Ирландии; Общество поджелудочной железы Великобритании и Ирландии; Ассоциация хирургов верхних отделов желудочно-кишечного тракта Великобритании и Ирландии.Руководство Великобритании по лечению острого панкреатита. Кишка . 2005; 54 (Дополнение 3): iii1–9.
7. Силен В. Острый панкреатит. В: Silen W, Cope Z, ред. Ранняя диагностика острого живота Коупом. 18 изд. Нью-Йорк, Нью-Йорк: Oxford University Press, 1999: 123–31.
8. Брисинда Дж., Мария Г, Ферранте А, Чивелло ИМ. Оценка прогностических факторов у пациентов с острым панкреатитом. Гепатогастроэнтерология . 1999; 46: 1990-7.
9. Общество хирургии пищеварительного тракта (SSAT). Лечение острого панкреатита. Манчестер, Массачусетс: Общество хирургии пищеварительного тракта (SSAT), 2004. По состоянию на 8 декабря 2006 г., по адресу: http://www.guidelines.gov/summary/summary.aspx?view_id=1″&”doc_id = 5512 # s25.
10. Clavien PA, Бурган С, Moossa AR. Ферменты сыворотки и другие лабораторные исследования при остром панкреатите. Br J Surg . 1989; 76: 1234–43.
11. Смоткин Я., Теннер С.Лабораторные диагностические исследования при остром панкреатите. Дж Клин Гастроэнтерол . 2002; 34: 459–62.
12. Frossard JL, Hadengue A, Пастор КМ. Новые сывороточные маркеры для выявления тяжелого острого панкреатита у людей. Am J Respir Crit Care Med . 2001; 164: 162–70.
13. Американский колледж радиологии (ACR). Критерии соответствия ACR. Острый панкреатит. По состоянию на 8 декабря 2006 г., по адресу: http://www.acr.org/s_acr/bin.asp? TrackID = “& amp;” SID = 1 “& amp;” DID = 11769 “& amp;” CID = 1207 & VID = 2 “& amp;” DOC = File.pdf.
14. Neoptolemos JP, Кемппайнен Э.А., Майер Дж. М., Фитцпатрик Дж. М., Рараты М.Г., Славин Ж, и другие. Раннее прогнозирование тяжести острого панкреатита с помощью пептида активации трипсиногена в моче: многоцентровое исследование. Ланцет . 2000; 355: 1955–60.
15. Теннер С. Первоначальное лечение острого панкреатита: критические проблемы в течение первых 72 часов. Ам Дж. Гастроэнтерол . 2004. 99: 2489–94.
16. Рэнсон Дж. Х. Этиологические и прогностические факторы острого панкреатита человека: обзор. Ам Дж. Гастроэнтерол . 1982; 77: 633–8.
17. Блейми С.Л., Имри CW, О’Нил Дж., Гилмор WH, Картер, округ Колумбия. Факторы прогноза при остром панкреатите. Кишка . 1984; 25: 1340–6.
18. Кнаус WA, Циммерман Дж. Э., Вагнер Д.П., Дрейпер EA, Лоуренс DE.APACHE-оценка острой физиологии и хронического здоровья: система классификации, основанная на физиологии. Crit Care Med . 1981; 9: 591–7.
19. Бальтазар Э.Дж., Робинсон Д.Л., Мегибоу AJ, Рэнсон Дж. Х. Острый панкреатит: значение КТ для установления прогноза. Радиология . 1990; 174: 331–6.
20. Леунг Т.К., Ли СМ, Лин С.Ю., Чен ХК, Ван Х.Дж., Шен Л.К., и другие.Индекс тяжести компьютерной томографии Balthazar превосходит критерии Рэнсона и систему баллов APACHE II в прогнозировании исхода острого панкреатита. Мир Дж. Гастроэнтерол . 2005; 11: 6049–52.
21. Chatzicostas C, Roussomoustakaki M, Вардас Э, Романос Дж, Курумалис Э.А. Индекс тяжести компьютерной томографии Balthazar превосходит критерии Рэнсона и балльные системы APACHE II и III в прогнозировании исхода острого панкреатита. Дж Клин Гастроэнтерол . 2003. 36: 253–60.
22. Вриенс П.В., ван де Линде П., Slotema ET, Вармердам ЧП, Breslau PJ. Индекс тяжести компьютерной томографии – ранний прогностический инструмент острого панкреатита. Дж. Ам Колл Сург . 2005; 201: 497–502.
23. Брэдли Э.Л. III. Клинически обоснованная система классификации острого панкреатита. Резюме Международного симпозиума по острому панкреатиту, Атланта, Джорджия., 11–13 сентября 1992 г. Arch Surg . 1993; 128: 586–90.
24. Chatzicostas C, Roussomoustakaki M, Влахониколис И.Г., Notas G, Музас I, Самонакис Д, и другие. Сравнение систем оценки Ranson, APACHE II и APACHE III при остром панкреатите. Поджелудочная железа . 2002; 25: 331–5.
25. Флинт Р, Виндзор JA. Ранний физиологический ответ на интенсивную терапию как клинически значимый подход к прогнозированию исхода тяжелого острого панкреатита. Arch Surg . 2004. 139: 438–43.
26. Norton SA, Олдерсон Д. Эндоскопическое ультразвуковое исследование в оценке острого идиопатического панкреатита. Br J Surg . 2000; 87: 1650–5.
27. Матос С, Cappeliez O, Winant C, Коппенс Э, Девьер Дж, Метенс Т. МРТ поджелудочной железы: обзорный тур. Рентгенография . 2002; 22: e2.
28. Fleszler F, Friedenberg F, Кревский Б, Friedel D, Брайтман Л.Е.Компьютерная томография брюшной полости увеличивает продолжительность пребывания в стационаре и часто не требуется при оценке острого панкреатита. Am J Med Sci . 2003. 325: 251–255.
29. Заявление Национального института здравоохранения по эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) для диагностики и лечения. Утверждения государственной науки NIH . 2002; 19: 1–26.
30. Аюб К, Имада Р, Славин Ю. Эндоскопическая ретроградная холангиопанкреатография при остром желчнокаменном панкреатите. Кокрановская база данных Syst Rev . 2004; (3): CD003630.
31. Лю К.Л., Lo CM, Чан Дж. К., Пун RT, Лам СМ, Вентилятор СТ, и другие. Выявление холедохолитиаза с помощью EUS при остром панкреатите: проспективная оценка у 100 последовательных пациентов. Гастроинтест Эндоск . 2001; 54: 325–30.
32. Макарий М.А., Дункан, доктор медицины, Хармон JW, Freeswick PD, Бендер Я.С., Больман М, и другие.Роль магнитно-резонансной холангиографии в лечении пациентов с желчнокаменным панкреатитом. Энн Сург . 2005; 241: 119–24.
33. Gosset J, Девьер Дж, Матос К. Магнитно-резонансная томография острого панкреатита: панкреатограмма. СОП . 2004; 5: 48–50.
34. Бариш М.А., Ючел Э.К., Ферруччи Дж. Т. Магнитно-резонансная холангиопанкреатография. N Engl J Med . 1999; 341: 258–64.
35. Муньос А, Katerndahl DA. Диагностика и лечение острого панкреатита. Ам Фам Врач . 2000; 62: 164–74.
36. Марик ЧП, Залога ГП. Метаанализ парентерального питания в сравнении с энтеральным питанием у пациентов с острым панкреатитом. BMJ . 2004; 328: 1407.
37. Изенманн Р., Рунзи М, Крон М, Каль С, Краус Д, Юнг Н, и другие., для Немецкой исследовательской группы по антибиотикам при тяжелом остром панкреатите.Профилактическое лечение антибиотиками у пациентов с прогнозируемым тяжелым острым панкреатитом: плацебо-контролируемое двойное слепое исследование. Гастроэнтерология . 2004; 126: 997–1004.
38. Шарма В.К., Хауден CW. Профилактическое введение антибиотиков снижает сепсис и смертность при остром некротическом панкреатите: метаанализ. Поджелудочная железа . 2001; 22: 28–31.
39. Малангони MA, Мартин А.С. Исход тяжелого острого панкреатита. Am J Surg . 2005. 189: 273–7.
Рекомендации WSES по ведению тяжелого острого панкреатита, 2019 г. | World Journal of Emergency Surgery
Диагностика
Вопросы:
- 1.
Каковы критерии для постановки диагноза тяжелого острого панкреатита?
- 2.
Какое визуализационное обследование необходимо при подозрении на тяжелый острый панкреатит? Какова роль магнитно-резонансной томографии (МРТ), компьютерной томографии (КТ), УЗИ (УЗИ), эндоскопического УЗИ (ЭУЗИ) и других дополнительных исследований?
- 3.
Какие лабораторные параметры следует учитывать в процессе диагностики?
- 4.
Как различная этиология влияет на диагностику?
- 5.
Какие баллы указаны для оценки риска?
- 6.
Каковы сроки и подходящий тест для ранней последующей визуализации?
Заключения (степень серьезности)
- 1.
Тяжелый острый панкреатит связан со стойкой органной недостаточностью (сердечно-сосудистой, респираторной и / или почечной) и высокой смертностью. Обе новые системы классификации, пересмотренная атлантская классификация и основанная на детерминантах классификация острого панкреатита, схожи в установлении диагноза и степени тяжести острого панкреатита (1С).
- 2.
Пациенты со стойкой органной недостаточностью с инфицированным некрозом имеют самый высокий риск смерти (1С).
- 3.
Пациенты с недостаточностью органов по возможности должны быть госпитализированы в отделение интенсивной терапии (1С).
Обсуждение
Острый панкреатит (ОП) представляет собой заболевание, характеризующееся острым воспалением поджелудочной железы и гистологическим разрушением ацинарных клеток [6].Диагноз AP требует наличия как минимум двух из трех следующих критериев: (i) боль в животе, соответствующая заболеванию, (ii) биохимические признаки панкреатита (уровень амилазы и / или липазы в сыворотке более чем в три раза превышает верхний предел нормы). ), и (iii) характерные результаты визуализации брюшной полости [2].
У большинства пациентов (80–85%) разовьется легкое течение заболевания (самоограничение, смертность <1–3%), но около 20% будут иметь умеренный или тяжелый эпизод АП с уровнем смертности от 13 до 35 % [7, 8].Таким образом, важно диагностировать (или лучше предсказать) эпизод тяжелого острого панкреатита (SAP) и выявить пациентов с высоким риском развития осложнений.
В течение почти 20 лет использовалась Атлантская классификация 1992 г., но некоторые определения и классификации вводили в заблуждение [9]. В редакции 447 статей Bollen et al. обнаружили, что альтернативные определения Атлантской классификации 1992 г. использовались более чем в половине исследований, и что определения часто используются ошибочно [9].
Важные идеи по ведению ОП, лучшее понимание патофизиологии органной недостаточности и некротического панкреатита, улучшенная диагностическая визуализация, минимально инвазивные методы и исследования, показывающие, что пациенты в тяжелой группе классификации Атланты 1992 г. составляют подгруппы с очень разными исходами. были указанием на то, что необходима более точная классификация.
В обзоре 2004 г. Johnson et al.сообщили, что стойкая органная недостаточность (ПОЯ) более 48 часов в течение первой недели тесно связана с риском смерти или местных осложнений [10]. Они использовали предыдущую базу данных о 290 пациентах с прогнозируемым SAP, набранных из 78 больниц через 18 центров в Великобритании, а также указали, что разрешение органной недостаточности в течение 48 часов предполагает хороший прогноз.
Ретроспективное исследование 759 пациентов с АП, проведенное Эдинбургским университетом, показало, что 25.4% пациентов с синдромом стойкого системного воспалительного ответа (ССВО) умерли, по сравнению с 8% с преходящим ССВО и 0,7% без ССВО [11].
Эти и другие исследования показали, что органная недостаточность занимает центральное место в определении SAP. Если органная недостаточность сохраняется более 48 часов, пациент подвергается высокому риску смерти (один из трех), и может быть установлена «тяжелая» категория. Также важно напомнить, что период заболевания с выраженной воспалительной реакцией (ССВО) предшествовал органной недостаточности, и если ССВО присутствует, у пациента есть риск прогрессирования до органной недостаточности, и необходимо предпринимать все попытки для восстановления. нормализация как можно скорее [12].
Практически одновременно в 2012 г. были опубликованы две новые системы классификации ОП: классификация степени тяжести острого панкреатита на основе детерминантов (DBC) и пересмотренная классификация Атланты 2012 г. (RAC) [2, 13]. Новый DBC был основан на глобальном интернет-опросе и специализированном международном симпозиуме с участниками из разных дисциплин: приглашения по электронной почте были доставлены 528 панкреатологам из 55 стран, и 240 панкреатологов из 49 стран приняли участие в опросе.Во время Всемирного конгресса Международной ассоциации панкреатологов 2011 г. (Кочи, Индия) около 100 участников обсудили предложенную классификацию и попытались согласовать определения [13].
RAC был создан в ходе итеративного процесса онлайн-консультаций, включающего ответы членов 11 национальных и международных обществ по лечению поджелудочной железы. В ответ на комментарии были внесены поправки, и онлайн-консультация повторилась три раза.Был пересмотрен окончательный консенсус, и были сохранены только утверждения, основанные на опубликованных доказательствах [2]. RAC представляет собой более широкий обзор, чем DBC: помимо классификации степени тяжести, он дает четкое определение диагностики AP, выделяет начало боли как важный ориентир и определяет отдельные местные осложнения, а также интерстициальный и некротический панкреатит [2, 14]. RAC делится на три категории: легкая, умеренно тяжелая и тяжелая, в зависимости от органной недостаточности и местных или системных осложнений.DBC добавил четвертую категорию: критическую, основанную на двух основных детерминантах смертности: (пери) панкреонекрозе и органной недостаточности (таблица 2).
Таблица 2 Определение степени тяжести острого панкреатитаВпоследствии Bansal et al. в когорте из 248 пациентов было обнаружено, что RAC и DBC схожи при поступлении в ОИТ, необходимости чрескожного дренирования, хирургии и внутрибольничной смертности. Критическая категория в DBC определила самое тяжелое заболевание [15]. Nawaz et al.проспективно набрали 256 пациентов и назначили категорию тяжести для всех трех классификаций: RAC, DBC и Atlanta 1992. Они обнаружили, что категории тяжести RAC и DBC точно отражают клинические исходы и превосходят Атланту 1992 г. (оценка смертности, госпитализация, длительность ICU пребывания) [16].
Два года спустя ретроспективное исследование 395 пациентов в Китае с общей госпитальной летальностью 8,9% дало аналогичные результаты. Авторы обнаружили, что все три системы классификации (RAC, BDC и Atlanta 1992) точно классифицируют степень тяжести AP.Однако RAC и DBC работали лучше, чем Atlanta 1992, и они были сопоставимы в прогнозировании долгосрочного клинического прогноза, серьезных осложнений и клинических вмешательств [17].
Choi et al. изучение 553 пациентов с ОП, госпитализированных в один центр в течение 7-летнего периода, подтвердило, что RAC хорошо коррелирует с клиническим исходом, несмотря на то, что не учитывается инфицированный некроз. Однако пациентов в тяжелой группе и с инфицированным некрозом (классифицируемым как критический в DBC) следует рассматривать отдельно от пациентов без него (уровень смертности увеличился в четыре раза: до 32%) [18].Другое исследование проанализировало 543 эпизода ОП у 459 пациентов в проспективной когорте пациентов. Они обнаружили, что разные категории тяжести для каждой системы классификации были связаны со статистически значимыми и клинически значимыми различиями в продолжительности пребывания в больнице, необходимости госпитализации в отделение интенсивной терапии, нутритивной поддержке, инвазивном лечении и внутрибольничной смертности. Кроме того, прямое сравнение категорий обеих классификаций (после объединения тяжелой и критической категории DBC) не дало существенных различий [19].
Как правило, пациенты с органной недостаточностью (точно определенные с использованием одного из установленных критериев или систем оценки) нуждаются в срочном переводе в отделение интенсивной терапии. Соответственно, может быть ненужным переводить пациентов с преходящей органной недостаточностью ни в специализированный медицинский центр, ни в отделение интенсивной терапии. Тем не менее, чтобы подтвердить стойкую органную недостаточность, ее необходимо задокументировать в течение более 48 часов.
Заявления (визуализация)
- 1.
При поступлении необходимо провести ультразвуковое исследование (УЗИ) для определения этиологии острого панкреатита (билиарного) (1С).
- 2.
Если есть сомнения, компьютерная томография (КТ) дает хорошее доказательство наличия или отсутствия панкреатита (1С).
- 3.
Всех пациентов с тяжелым острым панкреатитом необходимо обследовать с помощью компьютерной томографии с контрастным усилением (КЭ-КТ) или магнитно-резонансной томографии (МРТ). Оптимальное время для первой оценки CE-CT – 72–96 ч после появления симптомов (1C).
- 4.
Магнитно-резонансная холангиопанкреатография (MRCP) или эндоскопическое ультразвуковое исследование следует рассматривать для скрининга скрытых камней общего желчного протока у пациентов с неизвестной этиологией (1C).
Обсуждение
При поступлении следует определить этиологию ОП, чтобы спрогнозировать необходимость окончательного лечения (например, желчнокаменная болезнь) и избежать рецидива (например, употребление алкоголя, гипертриглицеридемия) [20]. Лечение и последующее наблюдение зависят от этиологии ОП. При поступлении следует провести трансабдоминальное УЗИ (для выполнения холецистэктомии при билиарном панкреатите, если это необходимо).Практически все мировые руководящие принципы AP (основанные на пересмотрах и метаанализе) рекомендуют выполнять УЗИ при поступлении или в первые 48 часов [7, 8, 20, 21, 22, 23].
Большинству пациентов с ОП КТ не требуется [24]. Распространение (пери) панкреонекроза может быть обнаружено с помощью КТ с контрастным усилением (КЭКТ) через 72 часа от начала ОП [20]. Высказывались опасения по поводу постконтрастного острого повреждения почек (ОПП). Недавний метаанализ с участием 28 обсервационных исследований и более 100 000 участников не нашел доказательств, подтверждающих связь контраста с ОПП, заместительной почечной терапией или смертностью [25].Однако сравнительных исследований у пациентов с тяжелым острым панкреатитом или сепсисом нет, поэтому следует соблюдать осторожность.
Раннее КТ не покажет некротические / ишемические области и не изменит клиническое ведение в течение первой недели болезни. Однако, если диагноз не определен, следует рассмотреть возможность проведения КТ, особенно для исключения вторичного перфорационного перитонита или мезентериальной ишемии. Он также показывает активное кровоизлияние и тромбоз, связанные с панкреатитом [21, 22].
Было показано, чтоCECT дает общий уровень раннего обнаружения 90% с чувствительностью, близкой к 100%, через 4 дня для некроза поджелудочной железы [26]. Balthazar et al. установили индекс тяжести КТ (таблица 3), который классифицировал панкреатит в зависимости от степени воспаления, наличия скоплений жидкости и степени некроза: более высокий балл связан с повышенной заболеваемостью и смертностью [26,27,28].
Таблица 3 Индекс серьезности КТ (По данным: Balthazar EJ, Robinson DL, Megibow AJ, Ranson JH.Острый панкреатит: значение КТ для установления прогноза. Радиология. 1990; 174: 331–6 [27])CECT – это метод визуализации, который выбирают для диагностики, определения стадии и обнаружения осложнений острого панкреатита, и он играет важную роль в оценке пациентов с известным или предполагаемым ОП: (i) диагноз, (ii) определение степени тяжести и (iii) выявление осложнений, в частности идентификация и количественная оценка (пери) панкреонекроза [20, 24, 26]. Однако частые повторные компьютерные томографии увеличивают общую дозу облучения и имеют ограниченный эффект при последующем принятии решений [29].
МРТ предпочтительнее КЭКТ у пациентов с аллергией на йодированный контраст, у пациентов с почечной недостаточностью / почечной недостаточностью (неусиленная МРТ), у молодых или беременных пациентов, чтобы свести к минимуму радиационное облучение с целью выявления несжиженного материала (например, мусора или некротической ткани), но менее чувствителен, чем КТ для обнаружения газа в коллекциях флюидов [24, 26]. КТ без контраста является альтернативой для первых двух групп пациентов, если МРТ недоступна.
Когда УЗИ не выявляет камни в желчном пузыре, ил или обструкцию желчевыводящих путей и при отсутствии холангита и / или аномальных функциональных тестов печени, предполагающих обструкцию желчевыводящих путей, вместо диагностической эндоскопической ретроградной холангиопанкреатографии используют магнитно-резонансную холангиопанкреатографию (MRCP) или эндоскопическое ультразвуковое исследование (EUS) (ERCP) следует использовать для скрининга скрытого холедохолитиаза, если нельзя установить другую этиологию [20, 24].В ретроспективной когорте, изучающей 221 пациента, MRCP имеет чувствительность 97,98% и специфичность 84,4% для холедохолитиаза, что позволяет избежать необходимости инвазивной визуализации у большинства пациентов с подозрением на холедохолитиаз [30].
Выписки (диагностические лабораторные показатели)
- 1.
Пороговое значение сывороточной амилазы и липазы обычно определяется как трехкратное превышение верхнего предела.
- 2.
Уровень С-реактивного белка ≥ 150 мг / л на третий день может использоваться в качестве прогностического фактора для тяжелого острого панкреатита (2A).
- 3.
Гематокрит> 44% представляет собой независимый фактор риска некроза поджелудочной железы (1B).
- 4.
Мочевина> 20 мг / дл выступает в качестве независимого предиктора смертности (2B).
- 5.
Прокальцитонин – наиболее чувствительный лабораторный тест для выявления инфекции поджелудочной железы, и низкие значения в сыворотке крови, по-видимому, являются сильными отрицательными предикторами инфицированного некроза (2A).
- 6.
При отсутствии камней в желчном пузыре или значительном употреблении алкоголя в анамнезе следует измерить уровни триглицеридов и кальция в сыворотке крови. Уровни триглицеридов в сыворотке выше 11,3 ммоль / л (1000 мг / дл) указывают на это как на этиологию (2C).
Обсуждение
Измерение ферментов поджелудочной железы в сыворотке крови является «золотым стандартом» для диагностики ОП [31].В эпизоде АП амилаза, липаза, эластаза и трипсин попадают в кровоток одновременно, но клиренс варьируется в зависимости от времени забора крови. Амилаза – это фермент, секретируемый поджелудочной железой, а также слюнными железами, тонкой кишкой, яичниками, жировой тканью и скелетными мышцами. Существует две основные изоформы амилазы: панкреатическая и слюнная, и ведущей функцией является переваривание крахмала, гликогена и родственных поли- и олигосахаридов путем гидролиза [32].При АП уровни амилазы в сыворотке обычно повышаются в течение 6–24 часов, достигают максимума через 48 часов и снижаются до нормальных или близких к нормальным уровням в течение следующих 3–7 дней [23, 32, 33].
Липаза – еще один фермент, секретируемый поджелудочной железой. AP является основной причиной увеличения липазы, и многие исследователи подчеркивают, что липаза более специфична, но может быть обнаружена повышенным также при заболеваниях, не связанных с поджелудочной железой, таких как почечная недостаточность, аппендицит, острый холецистит, хронический панкреатит, непроходимость кишечника и т.[23]. При AP липаза сыворотки остается повышенной в течение более длительного периода, чем сывороточная амилаза. Он повышается в течение 4-8 часов, достигает пика через 24 часа и снижается до нормального или близкого к нормальному уровню в течение следующих 8-14 дней [32, 33].
Трипсиноген – это зимоген трипсина фермента поджелудочной железы. При АП концентрация трипсиногена в сыворотке и моче обычно повышается до высоких уровней в течение нескольких часов и снижается через 3 дня [32, 33].
В совокупности липаза сыворотки считается более надежным диагностическим маркером AP, чем сывороточная амилаза.Ни один тест не показывает оптимальную диагностическую точность, но большинство современных руководств и рекомендаций указывают, что липаза должна быть предпочтительнее общей и p-амилазы [32]. Основные причины поддержки липазы по сравнению с обоими типами амилазы для диагностики острого панкреатита включают более высокую чувствительность и большее диагностическое окно [32]. Кокрановский пересмотр с целью сравнения диагностической точности различных ферментов поджелудочной железы при диагностике ОП показал чувствительность и специфичность 72% и 93% для сывороточной амилазы и 79% и 89% для сывороточной липазы, соответственно [33].
Chang et al. В метаанализе, включающем 13 исследований, было обнаружено, что тест-полоска на трипсиноген-2 является быстрым и неинвазивным прикроватным тестом с чувствительностью 82% и специфичностью 94% для АР [34].
Многочисленные биомаркеры были изучены как потенциальные ранние предикторы тяжести ОП, так что лечение может быть оптимально адаптировано для предотвращения осложнений [34, 35]. На данный момент практически нет лабораторных тестов для прогнозирования степени тяжести ОП [23].
При отсутствии камней в желчном пузыре или значительном употреблении алкоголя в анамнезе следует измерить уровень триглицеридов в сыворотке и принять во внимание этиологию, если значение> 11,3 ммоль / л (> 1000 мг / дл) [23].
Во многих учебниках С-реактивный белок (СРБ) рассматривается как золотой стандарт оценки тяжести заболевания [36]. Используя пороговое значение от 110 до 150 мг / л, чувствительность и специфичность варьировались от 38 до 61% и от 89 до 90%, соответственно, на момент госпитализации [36].Основным недостатком CRP является то, что пиковые уровни достигаются только через 48-72 часа.
В проспективном исследовании 175 пациентов, разделенных на легкий и нелегкий острый панкреатит в соответствии с классификацией Атланты, комбинация CRP и IL-6 продемонстрировала хорошую дискриминационную способность с площадью под кривой 0,803 [37].
Резистин – это недавно идентифицированный пептидный гормон, специфически секретируемый адипоцитами, который может вызывать ожирение и гипертриглицеридемию из-за его связи с инсулинорезистентностью.Исследования показали, что резистин также является важным цитокином при воспалительных реакциях и в регуляции других цитокинов [38]. В проспективном обсервационном исследовании уровни резистина были лучше для прогнозирования SAP, чем уровни CRP или WBC на 3-й день, и лучше, чем уровни CRP для прогнозирования развития некроза [38]. Ретроспективное когортное исследование данных 90 пациентов показало, что резистин имеет аналогичную точность с оценкой Acute Physiology and Chronic Health Evaluation II (APACHE II) при прогнозировании POF, а лептин имеет слабую корреляцию с POF [39].
Другие лабораторные данные, используемые для характеристики эпизода SAP, включают BUN> 20 мг / дл (> 7,14 ммоль / л) или повышение BUN, гематокрит (HCT)> 44% или повышение HCT, лактатдегидрогеназы (LDH) и прокальцитонина для прогнозирования инфицированный некроз у пациентов с подтвержденным панкреонекрозом [36, 40, 41, 42, 43]. Уровень прокальцитонина 3,8 нг / мл или выше в течение 96 часов после появления симптомов указывает на некроз поджелудочной железы с чувствительностью и специфичностью 93% и 79% [36, 42].Уровень лактата в сыворотке при поступлении позволяет прогнозировать тяжелую АП, смерть и поступление в ОИТ, но его следует рассматривать как субоптимальный как единственный маркер [44].
Заявления (диагностика при идиопатическом панкреатите)
- 1.
При идиопатическом панкреатите билиарную этиологию следует исключить с помощью двух ультразвуковых исследований и, при необходимости, MRCP и / или эндоскопического ультразвукового EUS, чтобы предотвратить рецидив панкреатита (2B).
Обсуждение
Идиопатический ОП определяется как панкреатит, этиология которого не установлена после первоначальных лабораторных и визуализирующих исследований. У пациентов с идиопатическим АП необходимо провести как минимум два УЗИ, чтобы исключить билиарную этиологию [31]. После этого КЭ-КТ и ЭУЗИ после окончания острой фазы являются следующими шагами для оценки микролитиаза, новообразования или хронического панкреатита.Если EUS отрицательный, необходимо выполнить МРТ для выявления морфологических аномалий [31]. Лапароскопическая холецистэктомия, по-видимому, предотвращает рецидивирующий идиопатический острый панкреатит; однако в настоящее время нет достаточных доказательств для повседневной поддержки этого подхода [45].
Заявление (оценка риска)
- 1.
Не существует «золотого стандарта» прогностической шкалы для прогнозирования тяжелого острого панкреатита.Вероятно, оценка прикроватного индекса тяжести острого панкреатита (BISAP) является одним из наиболее точных и применимых в повседневной клинической практике из-за простоты и способности прогнозировать тяжесть, смерть и органную недостаточность, а также APACHE-II (очень комплекс) и другие баллы (1B).
Обсуждение
Было разработано несколько систем оценки для прогнозирования SAP, но данные об их прогностической эффективности разнятся [46, 47].В настоящее время ни один систематический обзор не включал исследования, оценивающие точность различных систем клинической оценки, используемых для прогнозирования тяжести и смертности людей с острым панкреатитом. Кокрановская база данных систематических обзоров разрабатывает протокол для обобщения исследований, оценивающих прогностическую точность систем клинической оценки (измеряемой при поступлении и в течение 48 часов после госпитализации) [46].
Большинство оценок прогнозов в AP фокусировались на смерти как исходе.Поскольку общая смертность снижается за последние десятилетия, следует рассмотреть вопрос о том, должна ли смерть оставаться основным исходом для прогнозирования панкреатита [48].
Другой аспект заключается в том, что более или менее для всех оценок степени тяжести требуется более 24 часов для стратификации пациентов, и, вероятно, это означает потерю времени у некоторых пациентов в критическом состоянии [48]. Ретроспективное когортное исследование из Великобритании, проведенное в 159 отделениях интенсивной терапии с оценкой 2,462 пациентов, поступивших в отделение интенсивной терапии с SAP, показало, что 75% пациентов, которым требовалась интенсивная терапия, были переведены в отделение интенсивной терапии в течение первых 72 часов после поступления в больницу, со средним временем до -перенос через 24 ч после приема [49].
Со временем большинство оценок основывалось на демографических характеристиках пациента, клинических характеристиках, лабораторных параметрах или методах визуализации и оценивалось при поступлении или в течение 48 часов: критерии Рэнсона (1974), шкала Глазго-Имри (1978), острые физиологические и хронические заболевания. Оценка здоровья II (APACHE II), упрощенная оценка острой физиологии (SAPS II) (1984), оценка последовательной органной недостаточности (SOFA), индекс тяжести КТ (CTSI), оценка прикроватного индекса тяжести острого панкреатита (BISAP) (2008), Оценка серьезности по японскому языку [46].
Предикторы (или потенциальные предикторы), присутствующие почти во всех упомянутых выше системах оценки, включают возраст, органную недостаточность или иммунодефицит, предыдущую историю хронических заболеваний, температуру, артериальное давление, частоту пульса, частоту дыхания, индекс массы тела, уровень сознания, наличие перитонита, наличие острой почечной недостаточности, количество лейкоцитов в крови, гематокрит крови, количество тромбоцитов, глюкоза крови, азот мочевины крови, креатинин сыворотки, аспартаттрансаминаза сыворотки, лактатдегидрогеназа сыворотки, кальций сыворотки, электролиты сыворотки, билирубин сыворотки, плазма альбумин, насыщение кислородом, pH и дефицит оснований, а также различные методы визуализации, в основном КТ.
Оценка Apache II оценивает хронический показатель здоровья и 12 физиологических измерений, но не специфична для AP и не предназначена для повседневной оценки любого пациента. Преимущества этой партитуры заключаются в том, что это широко проверенный инструмент, и его можно сделать в любое время, но у него есть недостатки; т.е. громоздкие и не все параметры обычно собираются [48]. В исследовании 81 последовательного пациента с AP Thandassery et al. обнаружили, что независимыми предикторами возникновения инфицированного некроза были гипотония и оценка по шкале APACHE II через 24 часа после госпитализации [50].
В исследовании с участием 161 пациента оценивалась и сравнивалась ранняя предсказуемость различных параметров, наиболее широко используемых при ОП. Они обнаружили, что значимые пороговые значения для прогнозирования тяжелого AP были Ranson ≥ 3, BISAP ≥ 2, APACHE-II ≥ 8, CTSI ≥ 3 и CRP через 24 часа ≥ 21 мг / дл (> 210 мг / л). Они пришли к выводу, что разные системы оценки показали одинаковую точность прогнозирования тяжести ОП, но APACHE-II продемонстрировал наивысшую точность для прогнозирования SAP [51].
PPV по шкале Рэнсона колеблется от 28,6 до 49% (чувствительность 75–87%, специфичность 68–77,5%), для шкалы Глазго от 59 до 66% (чувствительность 61–71%, специфичность 88–89%), по шкале APACHE II – 55,6% через 48 часов (чувствительность 83,3%, специфичность 91%), а по шкале APACHE-O – 54–80% (чувствительность 69–74%, специфичность 86–90%). Все эти баллы можно оценить только через 48 часов и, таким образом, не позволяют стратифицировать риск при поступлении. Несмотря на свои недостатки, эти баллы по-прежнему полезны для подтверждения или исключения тяжелого заболевания [31].
BISAP, недавно разработанная прогностическая балльная система, была предложена в качестве простого метода прогнозирования тяжелого АД по сравнению с традиционными балльными системами. BISAP представляет собой аббревиатуру параметров, оцениваемых в баллах (Таблица 3) [48].
Оценка BISAP была получена с использованием данных, полученных для 17 992 пациентов, и подтверждена на 18 256 пациентах в США [52]. Он имеет такую же точность, что и оценка APACHE-II для прогнозирования смерти, и представляет собой очень упрощенную систему оценки, которую можно легко применить на самых ранних этапах.Одним из ключевых моментов этого исследования является то, что оно позволило выявить пациентов с повышенным риском смертности до начала органной недостаточности [52]. Ретроспективный анализ 303 пациентов показал, что BISAP предсказывает тяжесть, смерть и особенно органную недостаточность (OF) при AP так же, как APACHE-II, и лучше, чем критерии Ranson, индекс тяжести CT, CRP, гематокрит и ИМТ. Оценка BISAP, равная двум, была статистически значимым пороговым значением для диагностики тяжелого острого панкреатита, органной недостаточности и смертности [53] (таблица 4).
Таблица 4 Оценка прикроватного индекса тяжести острого панкреатита (BISAP) [48]В многочисленных исследованиях указывается, что ИМТ, ожирение и / или избыточный вес являются независимыми факторами риска развития тяжелого АП, местных осложнений или смерти [54, 55]. Исследование, проведенное в двух больницах из Нанкина, Китай, с использованием когорты из 1073 пациентов для разработки новой шкалы и 326 пациентов для ее проверки, подтвердило, что изменения внутрибрюшного давления (ВБД) и ИМТ в значительной степени связаны с тяжестью ОП. [46].Кроме того, они обнаружили, что новое моделирование с использованием ИМТ и изменений ВБД имеет лучшую чувствительность и специфичность (77,6% и 82,6%), чем APACHE-II (73,1% и 81,7%), BISAP (68,7% и 76,2%), CTSI ( 70,6% и 78,5%) и оценка Рэнсона (68,5% и 75,9%) соответственно [55].
Выписки (контрольная визуализация)
- 1.
При тяжелом остром панкреатите (индекс тяжести компьютерной томографии ≥ 3) повторное сканирование КЭКТ показано через 7–10 дней после первоначального сканирования КТ (1С).
- 2.
Дополнительные сканирования CE-CT рекомендуются только в том случае, если клинический статус ухудшается или не показывает дальнейшего улучшения, или когда рассматривается инвазивное вмешательство (1C).
Обсуждение
Пациентам с легким ОП в большинстве случаев не требуется КТ.Этим пациентам потребуется дополнительная компьютерная томография только в том случае, если есть изменение клинического статуса пациента, которое предполагает новое осложнение [20].
Плановая контрольная КТ (например, еженедельно или каждые 10 дней) рекомендуется в нескольких руководствах, но отсутствуют доказательства, оправдывающие эту практику. Подавляющее большинство осложнений у пациента с AP / SAP можно заподозрить при клинической или лабораторной оценке [20]. Следовательно, при SAP рекомендуется дополнительное последующее сканирование только в том случае, если клиническое состояние пациента ухудшается или не показывает дальнейшего улучшения [21, 31].
Разрешение КТ-проявлений (пери) воспаления поджелудочной железы практически всегда отстает от улучшения клинического статуса пациента. Таким образом, если у пациента улучшается клинический статус, дополнительные контрольные сканирования во время госпитализации рекомендуются только в том случае, если клинический статус пациента ухудшается или не показывает дальнейшего улучшения.
Лечение антибиотиками
Вопросы
- 1.
Какие показания к антимикробной терапии при тяжелом остром панкреатите?
- 2.
Эффективна ли антибиотикопрофилактика при тяжелом стерильном остром панкреатите?
- 3.
Какое правильное время для начала антимикробной терапии?
- 4.
Какой режим антимикробных препаратов следует использовать?
- 5.
Какова правильная продолжительность антимикробной терапии?
Заявление (антибиотики профилактические)
- 1.
Недавние данные показали, что профилактическое назначение антибиотиков пациентам с острым панкреатитом не связано со значительным снижением смертности или заболеваемости. Таким образом, обычные профилактические антибиотики больше не рекомендуются для всех пациентов с острым панкреатитом (1A).
Обсуждение
Использование и эффективность профилактической антибиотикотерапии при остром панкреатите долгое время были предметом споров.Профилактика относится к назначению антибиотиков пациентам при отсутствии клинической инфекции с целью предотвращения инфекции поджелудочной железы. Хотя ранние испытания предполагали, что назначение антибиотиков может предотвратить инфекционные осложнения у пациентов со стерильным некрозом [56], последующие, лучше спланированные испытания неизменно не подтверждали преимущества. Последние данные показали, что профилактическое назначение антибиотиков пациентам с острым панкреатитом не связано со значительным снижением смертности или заболеваемости [57,58,59,60,61].Таким образом, профилактическое назначение антибиотиков всем пациентам с острым панкреатитом больше не рекомендуется.
Заявление (инфицированный некроз и антибиотики)
- 1.
Антибиотики всегда рекомендуются для лечения инфицированного тяжелого острого панкреатита. Однако постановка диагноза затруднена из-за клинической картины, которую нельзя отличить от других инфекционных осложнений или от воспалительного статуса, вызванного острым панкреатитом (2A).
- 2.
Измерение прокальцитонина (ПКТ) в сыворотке может быть полезным для прогнозирования риска развития инфицированного панкреонекроза (1B).
- 3.
Тонкоигольная аспирация (FNA) под контролем КТ для окрашивания по Граму и посева может подтвердить инфицированный тяжелый острый панкреатит и начать терапию антибиотиками, но больше не используется в повседневной практике (1B).
Обсуждение
Антибиотики всегда рекомендуются для лечения инфицированного острого панкреатита. Однако диагностика инфицированного панкреатита является сложной задачей из-за клинической картины, которую нельзя отличить от других инфекционных осложнений или от воспалительного статуса, вызванного острым панкреатитом. Сроки инфицирования при панкреонекрозе изменчивы и непредсказуемы и достигают пика на второй-четвертой неделе после начала панкреатита.Клинические признаки могут быть очень чувствительными, но недостаточно специфичными [62, 63].
В ограниченном количестве небольших исследований оценивали С-реактивный белок (СРБ). Напротив, ПКТ был исследован как эффективный предиктор тяжести острого панкреатита и риска развития инфицированного панкреатита. ПКТ представляет собой неактивный пропептид из 116 аминокислот биологически активного гормона кальцитонина, который, как было впервые описано, имеет значительно повышенные концентрации у пациентов с бактериальными и грибковыми инфекциями [64].
Несколько исследований продемонстрировали, что измерение ПКТ в сыворотке может быть полезным для прогнозирования риска развития инфицированного панкреонекроза [65,66,67,68].
Предпочтительным диагностическим инструментом остается FNA поджелудочной железы под контролем некроза под контролем КТ. FNA под контролем КТ для окрашивания по Граму и посева может помочь клиницистам выбрать подходящую индивидуальную схему приема антибиотиков [69, 70]. Однако из-за большого количества ложноотрицательных результатов некоторые центры отказались от рутинного использования FNA.
Наличие газа в забрюшинной области считается признаком инфицированного панкреатита в контексте тяжелого острого панкреатита, но он присутствует только у ограниченного числа пациентов [62].
Заявление (вид антибиотиков)
- 1.
У пациентов с инфицированным некрозом следует использовать антибиотики, проникающие через панкреонекроз (1B).
- 2.
У пациентов с инфицированным некрозом спектр эмпирической схемы антибиотикотерапии должен включать как аэробные, так и анаэробные грамотрицательные и грамположительные микроорганизмы. Обычное профилактическое введение противогрибковых средств не рекомендуется пациентам с инфицированным острым панкреатитом, хотя Candida spp. часто встречаются у пациентов с инфицированным панкреонекрозом и указывают на пациентов с более высоким риском смерти (1B).
Обсуждение
Аминогликозидные антибиотики (например, гентамицин и тобрамицин) в стандартных внутривенных дозах не проникают в поджелудочную железу в тканевых концентрациях, достаточных для покрытия минимальной ингибирующей концентрации (МПК) бактерий, которые обычно встречаются при вторичных инфекциях поджелудочной железы [71].
Ацилуреидопенициллины и цефалоспорины третьего поколения имеют промежуточное проникновение в ткань поджелудочной железы, эффективны против грамотрицательных микроорганизмов и могут перекрывать МИК для большинства грамотрицательных микроорганизмов, обнаруживаемых при инфекциях поджелудочной железы [72].Среди этих антибиотиков только пиперациллин / тазобактам эффективен против грамположительных бактерий и анаэробов.
Хинолоны (ципрофлоксацин и моксифлоксацин) и карбапенемы демонстрируют хорошее проникновение в ткани поджелудочной железы, а также превосходное анаэробное покрытие [73,74,75,76]. Однако из-за высокой устойчивости к хинолонам во всем мире не рекомендуется применять хинолоны и применять их только у пациентов с аллергией на бета-лактамные агенты. Карбапенемы из-за распространения резистентного к карбапенему Klebsiella pneumoniae следует всегда оптимизировать и применять только у очень тяжелых пациентов.
Метронидазол с его бактерицидным спектром, направленным почти исключительно против анаэробов, также хорошо проникает в поджелудочную железу.
Патогенез вторичной бактериальной инфекции поджелудочной железы все еще обсуждается. Патогены могут достигать поджелудочной железы гематогенным путем, через билиарную систему, восходящую из двенадцатиперстной кишки через главный проток поджелудочной железы или через трансмуральную миграцию через толстую кишку через транслокацию бактерий толстой кишки [77].
Большинство возбудителей инфекции поджелудочной железы – это грамотрицательные бактерии желудочно-кишечного тракта ( Escherichia coli , Proteus , Klebsiella pneumonia ), которые возникают в результате нарушения кишечной флоры и повреждения слизистой оболочки кишечника. Нарушение защитных сил организма предрасполагает к перемещению желудочно-кишечных организмов и токсинов с последующей вторичной инфекцией поджелудочной железы. Однако были обнаружены грамположительные бактерии ( Staphylococcus aureus , Streptococcus faecalis , Enterococcus ), анаэробы и, иногда, грибы [78].
Грибковая инфекция – серьезное осложнение острого панкреатита, сопровождающееся увеличением заболеваемости и смертности [79]. Candida albicans является наиболее часто встречающимся организмом, за ним следуют Candida tropicalis и Candida krusei. Хотя грибковые инфекции, осложняющие острый панкреатит, обычно возникают пропорционально степени некроза поджелудочной железы, данных для профилактики грибковых инфекций недостаточно, и поэтому не рекомендуется.
Отделение интенсивной терапии
Вопросы:
- 1.
Каковы показания для поступления в отделение интенсивной терапии (ОИТ)?
- 2.
Когда показана жидкостная реанимация и какую жидкость следует использовать? Какова оптимальная скорость инфузии жидкости и измерение ответа для начальной реанимации? Какой фармакологический подход к стойкому шоку является предпочтительным?
- 3.
Каков правильный подход к обезболиванию?
- 4.
Какие показания для искусственной вентиляции легких?
- 5.
Каков медицинский подход к синдрому брюшной полости? Какова роль таких лекарств, как габексат мезилат и аналоги соматостатина?
- 6.
Энтеральное питание: по каким показаниям, какой тип питания следует использовать и какой способ энтерального питания лучше всего применять?
Заявление (мониторинг)
- 1.
При нарушении функции органов необходим постоянный мониторинг основных показателей жизнедеятельности в отделении интенсивной терапии.Стойкая органная дисфункция или возникновение органной недостаточности, несмотря на адекватную жидкостную реанимацию, является показанием для поступления в ОИТ (1С).
Обсуждение
Глобальная неоднородность отделений интенсивной и промежуточной терапии затрудняет определение универсальных путей. Не существует единого маркера, позволяющего определить степень тяжести заболевания. Для оценки степени тяжести в разных фазах, местах и пациентах следует использовать несколько систем баллов.
Интенсивное введение жидкости, адекватное обезболивание с помощью потенциально вредных стратегий и оценка функций органов во время начального лечения – вот причины, по которым постоянный мониторинг жизненно важных функций имеет решающее значение, независимо от условий. Стойкая органная дисфункция, несмотря на адекватную жидкостную реанимацию, требующую специальной поддержки органов, обычно осуществляется только в отделениях интенсивной терапии [11, 80].
Заявление(жидкостная реанимация)
- 1.
Ранняя жидкостная реанимация показана для оптимизации целевых показателей тканевой перфузии, не дожидаясь ухудшения гемодинамики. При приеме жидкости следует руководствоваться частой переоценкой гемодинамического статуса, поскольку известно, что перегрузка жидкостью имеет пагубные последствия. Изотонические кристаллоиды являются предпочтительной жидкостью (1B).
Обсуждение
Снижение смертности, наблюдаемое за последнее десятилетие, может быть связано с профилактикой панкреонекроза путем поддержания микроциркуляции за счет более обширной инфузионной реанимации.Данные о количестве жидкости, необходимой для предотвращения некроза или улучшения исхода, противоречивы, и объем должен быть скорректирован с учетом возраста, веса пациента и ранее существовавших почечных и / или сердечных заболеваний [81].
Гематокрит, азот мочевины крови, креатинин и лактат являются лабораторными маркерами волемии и адекватной тканевой перфузии, и их следует контролировать. Лактат Рингера может быть связан с противовоспалительным эффектом, но доказательства превосходства лактата Рингера надфизиологический раствор, основанный на рандомизированных исследованиях, является слабым [82,83,84]. Было бы лучше скорректировать уровень калия. Значение ранней целенаправленной терапии у пациентов с острым панкреатитом остается неизвестным [81, 85].
Заявление (обезболивание)
- 1.
Нет данных или рекомендаций об ограничении приема обезболивающих. При остром повреждении почек (ОПП) следует избегать приема нестероидных противовоспалительных препаратов (НПВП).Эпидуральная анальгезия должна быть альтернативой или агонистом внутривенной анальгезии при мультимодальном подходе. Обезболивание, контролируемое пациентом (PCA), должно быть интегрировано в каждую описанную стратегию. (1C) Дилаудид предпочтительнее морфина или фентанила у неинтубированных пациентов.
Обсуждение
Боль является основным симптомом острого панкреатита, и ее облегчение является приоритетной клинической задачей.Все пациенты с острым панкреатитом должны получить какую-либо форму анальгезии в первые 24 часа госпитализации, чтобы не ухудшить качество жизни пациента. В большинстве учреждений дилаудид предпочтительнее морфина или фентанила у неинтубированных пациентов. Эпидуральная анальгезия может быть рассмотрена для тех пациентов с тяжелым и острым критическим панкреатитом, которым требуются высокие дозы опиоидов в течение длительного периода [63].
Несмотря на некоторые данные РКИ, остается неопределенность в отношении предпочтительного анальгетика и наилучшего метода введения.Вот почему лучшая текущая рекомендация – придерживаться самых последних руководств по лечению острой боли в периоперационных условиях [63].
Заявление(ИВЛ)
- 1.
Механическая вентиляция легких должна быть применена, если подача кислорода, даже при интенсивном потоке кислорода через нос или постоянное положительное давление в дыхательных путях, стала неэффективной для коррекции тахипноэ и одышки.Могут использоваться как неинвазивные, так и инвазивные методы, но инвазивная вентиляция является обязательной, когда очистка бронхиального секрета становится неэффективной и / или пациент устает от прогнозируемой усталости. При необходимости инвазивной вентиляции легких следует использовать стратегии защиты легких (1С).
Обсуждение
Нет вопросов по лечению дыхательной недостаточности, специфичных для этой темы.Подача кислорода, даже с помощью устройств с высоким потоком или постоянным положительным давлением, может оказаться недостаточной для поддержания дыхательной недостаточности. Различные уровни тахипноэ и одышки лишь частично оправдываются гипоксией. Боль, возможная внутрибрюшная гипертензия и плевральный выпот могут вызывать эти симптомы, несмотря на адекватную оксигенацию артерий. Повышенная системная проницаемость может вызвать отек легких после жидкостной реанимации [86, 87].
Заявление (повышенное внутрибрюшное давление)
- 1.
Предлагается ограничение седативного действия, жидкости и вазоактивных препаратов для достижения реанимационных целей при более низких пределах нормы. Для ограничения внутрибрюшной гипертензии может потребоваться глубокая седация и паралич, если все другие неоперационные методы лечения, включая чрескожный дренаж внутрибрюшинной жидкости, являются недостаточными, перед выполнением хирургической абдоминальной декомпрессии (1B)
Обсуждение
Повышенная системная проницаемость, вызванная системным воспалением и терапевтическими попытками, такими как жидкостная реанимация и вазоактивные препараты, связаны с кишечной недостаточностью и ухудшением внутрибрюшного давления.Чрезмерная седация может еще больше усугубить дисфункцию кишечника с последующим повышением внутрибрюшного давления. Ограничение «обычных лекарств в ОИТ», когда побочные эффекты превосходят преимущества, имеет решающее значение [88].
Заявление (фармакологическое лечение)
- 1.
Не следует назначать какое-либо специфическое фармакологическое лечение, кроме поддержки органов и питания (1B).
Обсуждение
Несмотря на многочисленные исследования, эффективного фармакологического лечения не найдено [89].
Заявление (энтеральное питание)
- 1.
Энтеральное питание рекомендуется для профилактики кишечной недостаточности и инфекционных осложнений. Следует избегать полного парентерального питания (ПП), но следует рассмотреть возможность частичной интеграции парентерального питания для удовлетворения потребностей в калориях и белках, если энтеральное введение не переносится полностью. Можно безопасно проводить кормление как желудком, так и тощей кишкой (1A).
Обсуждение
Энтеральное питание поддерживает барьер слизистой оболочки кишечника, предотвращает нарушение и предотвращает транслокацию бактерий, вызывающих некроз поджелудочной железы. В большинстве медицинских учреждений непрерывная инфузия предпочтительнее циклического или болюсного введения. Энтеральное питание по сравнению с полным парентеральным питанием снижает инфекционные осложнения, органную недостаточность и смертность [90].В многоцентровом рандомизированном исследовании, сравнивающем раннее назоэнтериальное зондовое питание в течение 24 часов после рандомизации с пероральной диетой, начатой через 72 часа после обращения в отделение неотложной помощи с некротическим панкреатитом, раннее назоэнтеральное кормление не снизило частоту инфицирования или смерти. В группе пероральной диеты 69% пациентов переносили пероральную диету и не нуждались в питании через зонд [91].
Хирургическое и оперативное управление
Вопросы:
- 1.
Каковы показания для неотложной ЭРХПГ при тяжелом остром панкреатите?
- 2.
Какая оперативная / хирургическая тактика является правильной при тяжелом остром панкреатите?
- 3.
Какие показания для чрескожного / эндоскопического дренирования панкреатических скоплений (т.е., стерильный некроз, инфицированный некроз и др.)?
- 4.
Каковы показания к хирургическому вмешательству?
- 5.
Каковы сроки проведения операции и какая хирургическая стратегия является подходящей (т.е., лапароскопия или лапаротомия, внутрибрюшинная или внебрюшинная, ранняя или отсроченная)?
- 6.
Когда рекомендуется холецистэктомия и каковы правильные сроки?
Выписки (показания для неотложной ЭРХПГ)
- 1.
Рутинная ЭРХПГ при остром желчнокаменном панкреатите не показана (степень 1А).
- 2.
ЭРХПГ показана пациентам с острым желчнокаменным панкреатитом и холангитом (степень 1B).
- 3.
ERCP показана при остром желчнокаменном панкреатите с обструкцией общего желчного протока (степень 2B).
- 4.
ERCP у пациентов с прогнозируемым тяжелым острым желчнокаменным панкреатитом без холангита или обструкции общего желчного протока в настоящее время не может быть рекомендован (степень 2B).
Обсуждение
Систематический обзор семи рандомизированных контролируемых исследований (РКИ) с участием 757 участников не обнаружил доказательств в пользу рутинной ЭРХПГ для всех пациентов с острым желчнокаменным панкреатитом (AGP) [92].Не было никаких доказательств того, что результаты зависели от прогнозируемой тяжести AGP. Однако были высказаны опасения по поводу ограничений дизайна исследования, отсутствия объединенных выборок с прогнозируемым тяжелым AGP, а также сроков и техники ERCP. В том же метаанализе среди испытаний, в которых участвовали пациенты с холангитом, ранняя рутинная ЭРХПГ значительно снизила смертность, а также местные и системные осложнения.
У пациентов с обструкцией желчевыводящих путей ранняя рутинная ЭРХПГ была связана со значительным сокращением местных осложнений и незначительной тенденцией к снижению системных осложнений.В случае прогнозируемого тяжелого АГП рекомендации противоречивы [93]. В этом систематическом обзоре были изучены восемь метаанализов и 12 руководств и сделан вывод об отсутствии консенсуса в отношении рутинной ЭРХПГ с прогнозируемой тяжелой формой АГП. Текущее рандомизированное контролируемое исследование, исследование APEC, призвано ответить на этот вопрос [94]. Набор закончился, но результаты еще не опубликованы.
Заявление (показания к чрескожному / эндоскопическому дренированию панкреатических сборов)
- 1.
Клиническое ухудшение с признаками или сильным подозрением на инфицированный некротический панкреатит является показанием к вмешательству (чрескожное / эндоскопическое дренирование)
Через 4 недели после начала заболевания:
Продолжающаяся органная недостаточность без признаков инфицированного некроза
Продолжающаяся непроходимость выходного отверстия желудка, желчных путей или кишечника из-за большого некротического скопления, отделенного стенками
Синдром отсоединенного протока
Симптоматическая или растущая псевдокиста
Через 8 недель от начала заболевания:
(степень 1С)
Обсуждение
Доказательства показаний основаны на понимании естественного течения болезни, обосновании механизмов и нерандомизированных исследованиях.Вмешательства при некротическом панкреатите предпочтительно проводить, когда некроз перестал быть стенкой, обычно через 4 недели после начала заболевания [2].
Признаки или сильное подозрение на инфицированный некроз у пациента с симптомами требует вмешательства, хотя было показано, что небольшое количество пациентов выздоравливает только с помощью антибиотиков [1]. При ухудшении состояния пациента показан поэтапный подход, начинающийся с чрескожного или эндоскопического дренирования [20, 95, 96, 97].
Большинство пациентов со стерильным некротическим панкреатитом можно лечить без вмешательства [1]. Однако следует отметить, что почти половина пациентов, прооперированных из-за продолжающейся органной недостаточности без признаков инфицированного некроза, имеют положительную бактериальную культуру в оперативном препарате [98]. Следовательно, вмешательство следует рассматривать, если дисфункция органов сохраняется более 4 недель.
Огражденные стеной некротические скопления или псевдокисты могут вызывать симптомы и / или механическую непроходимость, и если они не исчезают после прекращения воспаления, рекомендуется повышенный подход.Симптоматическое отключение протока поджелудочной железы приводит к перипанкреатическому скоплению и является показанием для вмешательства [99, 100].
Показания (показания к оперативному вмешательству)
Показания к оперативному вмешательству являются:
Как продолжение в поэтапном подходе после чрескожной / эндоскопической процедуры с теми же показаниями
Синдром брюшной полости
Острое продолжающееся кровотечение при неудачном эндоваскулярном доступе
Ишемия кишечника или острый некротический холецистит при остром панкреатите
Кишечный свищ, переходящий в перипанкреатический сбор
(марка 1С)
Обсуждение
Доказательства показаний основаны на понимании естественного течения болезни, обосновании механизмов и нерандомизированных исследованиях.Если чрескожные или эндоскопические методы не улучшают состояние пациента, следует рассмотреть возможность дальнейшего хирургического вмешательства. Синдром брюшного отдела сначала следует лечить консервативными методами [101]. Если консервативные методы недостаточны, следует рассмотреть возможность хирургической декомпрессии с помощью лапаростомии [102].
Осложнения кровотечения при остром тяжелом панкреатите могут потребовать хирургического вмешательства, если эндоваскулярный доступ оказался безуспешным. Осложнения кишечника и другие экстрапанкреатические осложнения относительно редки, но могут потребовать хирургического вмешательства.
Заявление (сроки операции)
- 1.
Откладывание хирургических вмешательств более чем на 4 недели после начала заболевания снижает смертность (2B).
Обсуждение
Раннее хирургическое вмешательство сравнивалось с поздним хирургическим вмешательством в недавнем систематическом обзоре и метаанализе Восточной ассоциации хирургии травм [103].Исследование состояло из девяти исследований, одно из которых было рандомизированным контролируемым. Сроки оперативных вмешательств сравнивали в трех разных точках отсчета (72 часа, 12 дней и 30 дней). Во всех случаях поздняя операция привела к явному увеличению выживаемости. При отсроченной операции происходит отделение некроза от жизненно важных тканей, что приводит к меньшему повреждению жизненно важных тканей. Следовательно, на поздних сроках операции кровотечение меньше, а некрэктомия более эффективна.
Неизвестно, на какой срок можно отложить операцию, сможет ли пациент ее перенести, и приведет ли более длительная отсрочка к большему количеству осложнений, таких как учащение кишечных свищей или кишечная непроходимость.Если экстренное хирургическое вмешательство необходимо раньше по другим показаниям, таким как синдром брюшной полости или некроз кишечника, дренирование или некрэктомия обычно не рекомендуется [20, 97].
Заключения (хирургическая тактика)
- 1.
При инфицированном панкреонекрозе чрескожный дренаж в качестве первой линии лечения (поэтапный подход) откладывает хирургическое лечение до более благоприятного времени или даже приводит к полному разрешению инфекции у 25–60% пациентов и рекомендуется в качестве первая линия лечения (1А).
- 2.
Минимально инвазивные хирургические стратегии, такие как трансгастральная эндоскопическая некрэктомия или видеоассистированная ретроперитонеальная обработка (VARD), приводят к меньшему количеству случаев послеоперационной впервые возникшей органной недостаточности, но требуют большего количества вмешательств (1B).
- 3.
Что касается смертности, недостаточно доказательств в поддержку открытого хирургического, миниинвазивного или эндоскопического доступа (1B).
- 4.
В отдельных случаях с некрозом без стенок и у пациентов с отсоединением протока поджелудочной железы возможна одномоментная хирургическая трансгастральная некрэктомия (2C).
- 5.
Многопрофильная группа экспертов должна индивидуализировать хирургическое лечение с учетом местной экспертизы (2C)
Обсуждение
Систематический обзор чрескожного катетерного дренажа как основного лечения некротического панкреатита включал 11 исследований и 384 пациента [97].Инфицированный некроз был доказан у 71%, и 56% пациентов не потребовали хирургического вмешательства после чрескожного дренирования. Кроме того, чрескожный дренаж позволяет отложить возможное позднее хирургическое вмешательство на более благоприятное время.
Важный вопрос – какая стратегия предпочтительнее, если чрескожный дренаж не приводит к разрешению инфекции. Варианты лечения включают открытую хирургию, миниинвазивную хирургию, эндоскопическую хирургию и их комбинацию.Принято считать, что открытая операция вызывает более тяжелую воспалительную реакцию. Существуют различные РКИ и обзор, в котором сравниваются разные стратегии [104, 105, 106]. Таким образом, минимально инвазивные стратегии (например, минимально инвазивный пошаговый подход, санация забрюшинного пространства с помощью видео, VARD или эндоскопия) приводят к меньшему количеству впервые возникших органной недостаточности, но требуют большего количества вмешательств. Однако никаких различий в смертности обнаружено не было. Эти выводы подтверждаются систематическим обзором [107].При интерпретации результатов следует отметить значительную неоднородность пациентов, недостаточность органов и размер, а также локализацию некроза. К тому же хирургическая техника и показания к вмешательству неоднородны.
В серии из 178 отобранных случаев некроза со стенками 96% пациентов перенесли одномоментную хирургическую трансгастральную некрэктомию с послеоперационной летальностью и заболеваемостью 2% и 38% соответственно [108].Это также хороший вариант для пациентов с синдромом отсоединенного протока.
При рассмотрении смертности важно отметить, что смертность, связанная с панкреатитом, в основном не вызвана инфицированным некрозом. Следовательно, в будущих исследованиях следует рассмотреть другие критерии оценки исходов. Эти показатели результатов должны позволять определять полное исчезновение симптомов, качество жизни, время для возвращения к нормальной повседневной деятельности или работе и необходимость дальнейших вмешательств.Следует учитывать местную экспертизу различных хирургических подходов, так как только небольшой процент пациентов требует хирургического вмешательства, и даже в крупных центрах количество операций остается небольшим. Мы рекомендуем, чтобы местная многопрофильная группа экспертов разработала индивидуальную хирургическую стратегию.
Заявления (сроки холецистэктомии)
- 1.
Лапароскопическая холецистэктомия во время первичной госпитализации рекомендуется при легком остром желчнокаменном панкреатите (1A).
- 2.
При выполнении ЭРХПГ и сфинктеротомии во время первичной госпитализации риск рецидива панкреатита снижается, но холецистэктомия при госпитализации все еще рекомендуется, поскольку существует повышенный риск других осложнений со стороны желчевыводящих путей (1B).
- 3.
При остром желчнокаменном панкреатите с скоплением перипанкреатической жидкости холецистэктомию следует отложить до разрешения или стабилизации скопления жидкости и прекращения острого воспаления (2C).
Обсуждение
В двух различных систематических обзорах утверждается, что индексная холецистэктомия при приеме с легким AGP безопасна [109, 110]. Чтобы сократить продолжительность пребывания в стационаре и общие затраты, холецистэктомию можно выполнять уже на второй день госпитализации, если состояние пациента улучшается [111, 112].Рутинная интраоперационная холангиография, по-видимому, не нужна пациентам с легким желчнокаменным панкреатитом и нормализацией уровня билирубина [113]. Если ЭРХПГ выполнялась во время первичной госпитализации, риск рецидивов желчевыводящих путей, особенно рецидивов АГП, был снижен, но все же выше, чем при холецистэктомии при том же госпитализации. Многоцентровое рандомизированное контролируемое исследование с участием 266 пациентов показало, что интервальная холецистэктомия привела к увеличению числа осложнений, связанных с камнями в желчном пузыре, особенно к рецидивирующему панкреатиту и коликам, без увеличения количества осложнений, связанных с холецистэктомией [114].Существует единственное ретроспективное исследование сроков холецистэктомии у пациентов с АГП средней и тяжелой степени с скоплениями перипанкреатической жидкости [115]. В этом исследовании сообщалось о большем количестве осложнений после ранней холецистэктомии.
Открытый живот
Вопросы
- 1.
Какие показания к открытию живота при тяжелом остром панкреатите?
- 2.
Какая система временного закрытия живота лучше всего подходит для открытого живота?
- 3.
Каковы правильные сроки для смены повязки?
- 4.
Какое правильное время для закрытия живота?
Выписки (открытый живот)
- 1.
У пациентов с тяжелым острым панкреатитом, не поддающимся консервативному лечению ИАГ / ОКС, хирургическая декомпрессия и использование открытого живота эффективны при лечении синдрома брюшной полости (2C).
- 2.
Мы предлагаем клиницистам проявлять осторожность, чтобы не реанимировать пациентов с ранним SAP и регулярно измерять внутрибрюшное давление (1C).
- 3.
Мы предлагаем избегать открытого живота (ОА), если другие стратегии могут быть использованы для смягчения или лечения тяжелой внутрибрюшной гипертензии при SAP (1C).
- 4.
Мы рекомендуем не использовать ОА после некрэктомии для SAP (если только тяжелая ВБГ не требует выполнения ОА в качестве обязательной процедуры) (1С).
- 5.
Мы рекомендуем не проводить санацию или раннюю некрэктомию, если вынуждены провести ранний ОА из-за синдрома брюшной полости или висцеральной ишемии (1A).
Обсуждение
Потенциальное обоснование для потенциального использования лечения ОА у пациентов с тяжелым острым панкреатитом (SAP) исторически состояло в том, чтобы потенциально смягчить IAH / ACS, улучшить дренаж воспалительного асцита, позволить возможный лаваж поджелудочной железы и потенциально облегчить релапаротомию с повторной некрэктомией [ 116,117,118].
Однако в SAP отсутствуют доказательства уровня 1 относительно эффективности открытого живота для SAP, без рандомизированных контролируемых исследований (РКИ) и метаанализов. Был опубликован протокол такого исследования [119], но составители обзора не смогли найти доказательств того, что это исследование когда-либо проводилось.
В качестве следующего лучшего уровня доказательств существуют согласованные рекомендации Всемирного общества экстренной хирургии [120] и Международной ассоциации панкреатологов / Американской ассоциации поджелудочной железы [20], которые рекомендуют как медикаментозное, так и минимально инвазивное лечение тяжелых интраоперационных заболеваний. -абдоминальная гипертензия (ИАГ), приводящая к синдрому абдоминального компартмента (ОКС), согласно алгоритмам управления синдромом абдоминального компартмента [101].Однако, осознавая, что выявленный явный ОКС всегда фатален при отсутствии лечения, потребуется открытая декомпрессивная лапаротомия (ДКЛ), которая рекомендуется, если менее инвазивные меры неэффективны. При проведении ДКЛ забрюшинную полость и малый сальниковый мешок следует оставить нетронутыми, чтобы снизить риск инфицирования перипанкреатического и панкреонекроза [20, 121].
В связи с этой основной рекомендацией есть дополнительные утверждения, которые относятся к основным принципам, согласно которым чрезмерная инфузионная реанимация, по-видимому, тесно связана с возникновением ВБГ / ОКС при тяжелом шоке и что ранняя некрэктомия не оправдана при SAP.Теперь уже классическое исследование показало, что ранняя (<72 ч) по сравнению с поздней (> 12 дней) некрэктомия имела 56% при ранних вмешательствах и 27% при поздних операциях, а интраоперационная кровопотеря была существенно снижена за счет отсроченного подхода, результаты, которые только продолжала улучшаться благодаря постоянным усовершенствованиям в хирургии и реанимации [122, 123, 124].
Заявления (ведение открытой брюшной полости и временное закрытие живота)
- 1.
Мы рекомендуем использовать перитонеальную терапию отрицательным давлением для лечения ОА (1B).
- 2.
Мы предлагаем добавить фасциальную тракцию к методам NPWT (2B).
- 3.
Мы предлагаем провести дальнейшие контролируемые исследования внутрибрюшинной осмотической терапии при SAP (нет рекомендаций)
Обсуждение
Не было РКИ или метаанализов, которые бы прямо представляли сравнительные данные о методах ОА при SAP, поэтому все доказательства будут косвенными, связанными с изучением ОА в других связанных условиях, таких как внутрибрюшинный сепсис [125, 126] или смешанные группы травматологов [127,128,129,130] с методологическими проблемами.
Исследование Pliakos примечательно тем, что рандомизированное включение фасциальных тракционных швов в дополнение к перитонеальной вакуумной терапии было значительно связано с продемонстрированным превосходством в отношении более короткой продолжительности открытого живота, меньшего количества смен повязок, снижения частоты повторных исследований, более успешного закрытия брюшной полости частота и уменьшение энтероатмосферных свищей [125]. РКИ, в котором сравнивали активную перитонеальную терапию отрицательным давлением с более пассивным давлением, продемонстрировало улучшение смертности при повышенном перитонеальном давлении [129], подтверждая нерандомизированные результаты [130], но биологический механизм не был очевиден.Было проведено несколько метаанализов, включая данные нерандомизированных исследований, без явного превосходства какого-либо одного метода [131, 132]. Самый современный из них заключил: «Хотя наилучшие результаты с точки зрения достижения отсроченного закрытия фасции и риска энтероатмосферной фистулы были показаны для NPWT с непрерывной фасциальной тракцией, общее качество имеющихся доказательств было низким, и единообразных рекомендаций дать нельзя» [131].
Последней терапией, которую следует тщательно рассмотреть при лечении ОА, является прямая перитонеальная реанимация (DPR), внутрибрюшинная инстилляция диализирующего раствора, эффективность которой у пациентов с травмами [133].В рандомизированном контролируемом исследовании, проведенном Смитом и коллегами, интраабдоминальные осложнения (8% против 18%), частота абсцессов (3% против 14%) и 30-дневная смертность были ниже, несмотря на схожие оценки тяжести травм (13% против 28%). %; p = 0,06) (20). Поскольку нет прямых доказательств у пациентов с SAP, не было сделано никаких рекомендаций относительно DPR.
Заявление (сроки смены повязки)
- 1.
Повторное обследование открытого живота следует проводить не позднее, чем через 24–48 ч после индексации и любой последующей операции, при этом продолжительность предыдущей операции сокращается с увеличением степени неулучшения пациента и нестабильности гемодинамики (1С).
Обсуждение
Нет РКИ или метаанализов, касающихся сроков, когда пациента с открытой брюшной полостью следует вернуть в операционную, в частности, когда показанием ОА было SAP, или по каким-либо другим показаниям на самом деле. Другие руководящие принципы признанных обществ также не содержат доказательств того, когда следует проводить повторную операцию с ОА [101, 131, 134, 135]. Однако в одном обзоре повторное обследование, проведенное более чем через 48 часов после первоначальной операции, привело к значительно более высокому уровню смертности; самый низкий уровень смертности (9%) был достигнут у пациентов, перенесших повторную операцию в течение 48 часов [136].
Современные данные показывают, что существует линейная корреляция между днями остеоартрита и серьезными осложнениями, такими как развитие кожно-кишечного свища [137]. В другой проспективной серии исследований отмечалось, что, в частности, каждый час задержки возвращения в операционную через 24 часа после начальной лапаротомии наблюдалось снижение первичного фасциального закрытия на 1,1% и тенденция к увеличению внутрибрюшных осложнений через 48 часов [138].
В отсутствие каких-либо новых данных специалисты по анализу SAP OA предлагают принять предыдущее современное заявление о руководящих принципах WSES OA, чтобы поддерживать согласованность между санкционированными рекомендациями WSES до тех пор, пока новые данные не потребуют возможного пересмотра [120].Поскольку общие результаты заметно улучшаются за счет отказа от ранних и ненужных вмешательств на поджелудочной железе [124], хирурги должны сопротивляться любым искушениям «вмешаться в дела поджелудочной железы», которые могут возникнуть в ходе повторной операции по поводу остеоартроза, недоступной при менее сложные случаи SAP.
Выписки (сроки закрытия живота)
- 1.
Раннее фасциальное и / или абдоминальное окончательное закрытие должно быть стратегией ведения открытой брюшной полости после того, как исчезнут все потребности в продолжающейся реанимации, окончательно достигнут контроль источника, не останется никаких опасений относительно жизнеспособности кишечника, больше не будет повторного хирургического вмешательства. необходимо исследование, и нет никаких опасений по поводу синдрома брюшной полости (1B).
Обсуждение
Рискуя быть рассмотренным в шутку, команда авторов подчеркивает важность попытки оптимизировать превентивные стратегии ВБГ посредством тщательной и усердной реанимации, раннего внедрения медицинских и минимально инвазивных методов лечения ВБГ [101, 139, 140], чтобы попытаться чтобы избежать перехода в ACS с требованием DCL.
Отсроченное закрытие фасции определяется как формальная фасция, полученная через семь или более дней после индексной процедуры ОА [141].Стало очевидно, что количество осложнений намного выше, а первичное закрытие фасции намного ниже у тех, кто подвергается позднему закрытию по сравнению с ранним, хотя это также может быть связано с факторами пациента в неконтролируемых нерандомизированных исследованиях. Однако метаанализ показал, что по сравнению с отсроченным закрытием брюшной полости раннее ПФК было связано со снижением смертности и частоты осложнений [142]. Таким образом, бывшее Всемирное общество синдрома абдоминального отдела рекомендовало, чтобы среди пациентов ОИТ с ОА были предприняты сознательные и / или протоколированные усилия для достижения раннего или, по крайней мере, на момент госпитализации абдоминального фасциального закрытия [101].
Подобно предыдущему вопросу, до тех пор, пока не появятся новые данные об окончательном закрытии OA в SAP или любых других условиях, рецензенты предлагают принять предыдущее современное заявление руководящих принципов WSES, чтобы поддерживать согласованность между санкционированными рекомендациями WSES до тех пор, пока новые данные не потребуют возможного пересмотра [120] .
Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookieЭтот сайт использует файлы cookie для повышения производительности.Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в cookie-файлах может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Острый панкреатит – проект EMCrit
Вы здесь: Домашняя страница / IBCC / Острый панкреатит, Джош Фаркас
СОДЕРЖАНИЕбыстрый справочник
(вернуться к содержанию)
диагностика
(вернуться к содержанию)
диагностические критерии острого панкреатита
- Требуются как минимум два из следующего:
- (1) Повышение липазы> 3-кратного верхнего предела нормы (1)
- (2) Характерная боль в животе
- (3) Визуализирующие доказательства панкреатита на КТ, МРТ или УЗИ.
- Пациенты, не соответствующие этим критериям, не болеют панкреатитом и не должны лечиться от него.
- Боль:
- Обычно в эпигастральной области или левом подреберье, может излучать назад.
- При осмотре обычно присутствует болезненность в эпигастрии.
- Постоянная тошнота / рвота
- Геморрагический панкреатит может вызвать Знак Каллена и Знак Грея Тернера:
- Чувствительность и специфичность ~ 90% для острого панкреатита.
- Причины повышенной липазы включают:
- Заболевание поджелудочной железы любого вида (панкреатит, псевдокиста, рак)
- Кишечная непроходимость / псевдообструкция, перфорация, язвенная болезнь двенадцатиперстной кишки, ишемия
- Болезни желчевыводящих путей (холецистит, холангит, холедохолитиаз)
- Почечная недостаточность
- Повышение уровня липазы из-за других заболеваний, кроме панкреатита, как правило, в три раза ниже верхнего предела нормы.
- Очень высокие значения липазы более специфичны для диагностики панкреатита.
- Более высокие значения липазы не коррелируют с худшим прогнозом. Столь высокие значения липазы могут показаться пугающими, но на самом деле этого не должно быть.
- Липаза заменила амилазу в диагностике панкреатита. Нет смысла проверять уровень амилазы.
КТБоль в эпигастрии, повышение LFT и липазы. #POCUS показывает «тень эха стены» Великобритании. Вероятен желчнокаменный панкреатит.
Изображение – @PhilipsLumify. Подтверждено КТ рис.twitter.com/KTrAmdawAM– Гордон Джонсон (@pdxfutebol) 24 декабря 2017 г.
- Ранняя КТ при необходимости уточнения диагноза
- CT чувствителен и специфичен для панкреатита, а также предоставляет информацию о степени тяжести.
- Если у пациента определенно панкреатит (на основании типичного анамнеза, осмотра и лабораторных данных), то нет причин для ранней компьютерной томографии (это не повлияет на лечение).
- Пациентам, находящимся в состоянии шока, часто бывает целесообразно провести КТ для исключения очага внутрибрюшного сепсиса.
- Поздняя компьютерная томография при осложнениях
- Настоящая роль компьютерной томографии при панкреатите заключается в поиске осложнений, если состояние пациента ухудшится позже (через несколько дней). Например, компьютерная томография может помочь оценить инфицированный некроз и псевдокисту.
оценка причины панкреатита
(вернуться к содержанию)
частые причины острого панкреатита
- Желчные камни (~ 40%) 1
- Алкоголизм (~ 30%)
- Нарушения обмена веществ: гипертриглицеридемия, гиперкальциемия
- Лекарства включают: 2
- антибиотики: тетрациклины, сульфаниламиды, пентамидин, лекарства от ВИЧ, изониазид, метронидазол
- иммунодепрессанты: азатиоприн, сульфасалазин, аминосалицилаты, 6-меркаптопурин
- сердечные: амиодарон, лозартан, фуросемид, правастатин, симвастатин
- вальпроевая кислота
- полностью трансреионная кислота (ATRA)
- Муковисцидоз
- Задняя проникающая язва, травма
- Ятрогенный: ЭРХПГ, хирургия, лучевая терапия, пост АКШ
- Злокачественная опухоль поджелудочной железы
- Кальций
- Гиперкальциемия – редкая причина панкреатита
- Гипокальциемия может возникнуть из-за самого панкреатита, иногда вызывая симптоматическую гипокальциемию.
- Уровень триглицеридов (> 1000 мг / дл или 11,2 мМ предполагает гипертриглицеридемический панкреатит)
- Функциональные пробы печени
- Значительно повышенный уровень билирубина и щелочной фосфатазы указывает на обструкцию, что может вызывать опасения одновременного восходящего холангита.
- Должен быть получен у всех пациентов с панкреатитом. 3
- Камни в желчном пузыре могут указывать на желчный панкреатит.
- Самый важный результат – это размер общего желчного протока.
Когда CBD расширен, никто не должен его пропустить. Сразу перед PV. Если сомневаетесь, используйте цвет или силу. #POCUS #FOAMed pic.twitter.com/Sqdu0i2XJQ
– Мохаммед Альшамси (@EmergOmBur) 9 января 2016 г.
Стратификация риска – кому нужна ОИТ?
(вернуться к содержанию)
Большинство пациентов с панкреатитом имеют легкую форму заболевания и могут быть помещены в палату, но некоторым требуется госпитализация в ОИТ.Это сложно, потому что пациенты с панкреатитом могут сначала выглядеть нормально, но позже их состояние ухудшается.
классификация: отечный панкреатит против некротического- Панкреатит можно разделить на две категории:
- Интерстициальный отечный панкреатит (90%) – диффузное воспаление поджелудочной железы, ткань остается жизнеспособной.
- Некротический панкреатит (10%) – некротизируются участки ткани поджелудочной железы.
- Диагноз «некротический панкреатит» обычно ставится на основании контрастной компьютерной томографии, которая показывает отсутствие кровотока в некротизированных областях.Однако обратите внимание, что компьютерная томография не должна проводиться исключительно для этой цели.
- Некротический панкреатит вызывает большее беспокойство, поскольку эти пациенты подвержены риску развития полиорганной недостаточности или суперинфекции омертвевшей ткани поджелудочной железы (инфицированный панкреонекроз). Смертность от некротического панкреатита составляет 17%, что намного выше, чем смертность от интерстициального отечного панкреатита на 3%. 2
- Для прогнозирования результатов доступно около десятка систем оценки.Однако неясно, какова должна быть роль систем оценки по сравнению с оценкой клиницистов. Мне неизвестны предполагаемые доказательства того, что любая оценка лучше клинической оценки. Оценка
- APACHE-II, по-видимому, является лучшей системой оценки, при этом оценка> 7 позволяет прогнозировать тяжелый острый панкреатит. К сожалению, его эффективность далека от идеала, с чувствительностью 65% и специфичностью 76% для тяжелого панкреатита ( Калькулятор APACHE-II ).
- Оценка Рэнсона не может быть полностью рассчитана за 48 часов, поэтому она не играет значимой роли в предварительной стратификации риска.
- NLR легко рассчитывается на основе гемограммы при поступлении, как показано выше, поэтому сразу же доступен для всех ваших пациентов бесплатно.
- NLR измеряет физиологический стресс. При стрессе количество нейтрофилов имеет тенденцию повышаться, количество лимфоцитов имеет тенденцию падать, поэтому NLR увеличивается.
- Более высокие значения NLR предсказывают тяжелый панкреатит (площадь под кривой ROC ~ 0,75) 4 5 6 7 и смертность (площадь под кривой ROC ~ 0.8). 4 8 NLR кажется более точным, чем C-реактивный белок, лабораторный тест, который иногда рекомендуется для прогнозирования панкреатита. 8 9
- В таблице ниже представлено приблизительное руководство по интерпретации NLR. 4 NLR обычно уменьшается с течением времени по мере исчезновения панкреатита. Исследования преимущественно оценивали прогностическую ценность NLR при поступлении.
- Прогнозирование не должно основываться исключительно на NLR, но NLR может предоставить еще один бит информации, способствующий глобальной клинической оценке.
- Любой пациент, которому требуется агрессивная жидкостная реанимация (например, более 1-2 литров). Как обсуждается ниже, жидкостную реанимацию следует использовать только по мере необходимости для поддержки перфузии. Если пациент настолько болен, что ему требуется реанимация большого объема, его следует поместить в отделение интенсивной терапии.
- Дыхательная недостаточность (например, сильное тахипноэ или повышенная работа дыхания).
- Другие органные недостаточности (e.г. плохой диурез, повреждение почек, делирий, артериальная гипотензия).
- Гипертриглицеридемический панкреатит (триглицериды> 1000 мг / дл или 11,2 мМ) следует рассматривать для инфузии инсулина в отделении интенсивной терапии.
общий принцип – панкреатосептическая эквивалентность
(вернуться к содержанию)
Исторически панкреатит лечили как уникальную болезнь . Этого опасались реаниматологи, которые пугающе доверяли лечение гастроэнтерологам и хирургам.Панкреатит лечили с помощью большого количества жидкости, отдыха кишечника, дренажа через назогастральный зонд, парентерального питания и профилактических антибиотиков – совершенно странное попурри из методов лечения, несовместимое с основными принципами интенсивной терапии. Только недавно мы начали упорную работу по искоренению этих вредных методов лечения.
принцип панкреатосептической эквивалентности- Тяжелый панкреатит и септический шок – очень похожие процессы (оба состояния – вазодилататорный шок, включающий глубокое системное воспаление и эндотелиальную дисфункцию).
- Лечение тяжелого панкреатита должно осуществляться по тем же принципам, что и лечение септического шока.
- Пробелы в доказательствах относительно того, как лечить тяжелый панкреатит, могут быть восполнены за счет опыта, полученного при лечении септического шока.
Это может быть не на 100% точным, но это огромный прогресс по сравнению с причудливыми способами лечения панкреатита за последние несколько десятилетий.
лечение причинных факторов
(вернуться к содержанию)
гипертриглицеридемический панкреатит
- Определение гипертриглицеридемического панкреатита: Панкреатит с уровнем триглицеридов более ~ 1000 мг / дл (11.2 мМ) при отсутствии другой очевидной причины панкреатита.
- Уровень триглицеридов следует снизить, обычно с помощью инфузии инсулина. Однако перед тем, как поместить пациента в отделение интенсивной терапии для инфузии инсулина, убедитесь, что у него действительно панкреатит, как определено выше (повышенный уровень триглицеридов при отсутствии панкреатита не требует инфузии инсулина).
- Подробнее об этом здесь.
- Медикаментозное лечение : прекратить прием потенциально опасных лекарств
- Гиперкальциемия : лечите это агрессивно (например,г. с бисфосфонатом и прокальцитонином).
- Желчнокаменная болезнь : идеально холецистэктомия при госпитализации по поводу острого панкреатита
ERCP?
(вернуться к содержанию)
- Американская гастроэнтерологическая ассоциация рекомендует против плановой неотложной ЭРХПГ у пациентов с острым билиарным панкреатитом без холангита. Большинство исследований ERCP не показали положительных результатов.
- Самым сильным показанием для ЭРХПГ является явный или подозреваемый восходящий холангит (который иногда возникает одновременно с панкреатитом, служащим очагом септического шока).Признаки холангита могут включать:
- Расширение общего желчного протока
- Значительно повышенный и повышающийся билирубин
- ERCP также может быть показан пациентам с признаками холедохолитиаза (например, стойко повышенный билирубин, ретинированный камень, визуализированный рентгенологически).
- Если есть сомнения в необходимости ERCP, возможные подходы:
- Наблюдайте за пациентом клинически с последовательным мониторингом функциональных проб печени и общей картины.
- Магнитно-резонансная холангиопанкреатография (MRCP) – неинвазивный метод визуализации для лучшего определения анатомии желчных путей.
реанимация
(вернуться к содержанию)
традиционная догма: жидкостная реанимация большого объема
- Традиционно пациентов лечили с помощью массивной жидкостной реанимации (например, 250-500 мл / час, что приводит к введению ~ 8-14 литров жидкости в течение первого дня).Это безумие.
- Нет свидетельств для поддержки массового администрирования. Доступные проспективные исследования показывают, что более агрессивное введение жидкости увеличивает частоту инфекций, абдоминального синдрома, ОРДС и смерти. 10 11
- Никто не знает наилучшего подхода, для этого мало качественных перспективных данных.
- Разумный подход к реанимации, вероятно, аналогичен реанимации при септическом шоке:
- Дайте жидкость на основе гемодинамической оценки (например,г. с УЗИ). Большинству пациентов может быть полезно сначала выпить умеренного количества жидкости (например, всего 2-4 литра в течение первого дня).
- Не давайте много жидкости после первой реанимации (например, после 12-24 часов). После стабилизации, как правило, разумно установить баланс жидкости или даже (входы = выходы).
- Используйте вазопрессоры (например, норэпинефрин) на ранней стадии, если это необходимо для поддержания адекватного АД. Это может уменьшить количество вводимой жидкости, тем самым снижая риск синдрома брюшной полости (подробнее об этом ниже).
- Будьте осторожны при использовании чувствительности к жидкости у этих пациентов. Даже если пациент чувствителен к жидкости, введенная жидкость будет быстро вытекать из сосудистого пространства. Пациенты с панкреатитом часто чувствительны к жидкости независимо от того, сколько жидкости им дают.
- У пациентов часто развивается почечная недостаточность из-за острого некроза канальцев. Это не отвечает на дополнительное введение жидкости.
- Лактат Рингера, по-видимому, является предпочтительной жидкостью, учитывая одно РКИ по панкреатиту, в котором было обнаружено уменьшение воспаления при использовании LR по сравнению с физиологическим раствором. 12 В любом случае
- LR – отличная реанимационная жидкость, поэтому не нужно много доказательств, чтобы убедить нас использовать ее здесь.
питание
(вернуться к содержанию)
концепция «панкреатического покоя» опасно вводит в заблуждение догму
- Традиционно считалось, что питание стимулирует секрецию поджелудочной железы и тем самым ухудшает панкреатит.
- Это не только неправильно, но и наоборот. 13 Ранняя энтеральная нутритивная поддержка (в идеале в течение 24 часов) может улучшить результаты, например
- Улучшение функции кишечника (снижение частоты кишечной непроходимости, уменьшение бактериальной транслокации в кровоток)
- Сниженный риск инфицированного некроза поджелудочной железы.
- Сокращение продолжительности пребывания в больнице.
- Уменьшение желудочно-кишечных симптомов. 1
- Оральную диету можно начинать немедленно.
- Можно начинать с диеты с низким содержанием жиров (нет необходимости начинать с диеты с прозрачной жидкостью).
- Некоторые пациенты не могут переносить пищу (например, из-за боли или рвоты). Это можно наблюдать в течение пары дней. Если через 3-5 дней пациент все еще не ест, для обеспечения питания можно установить носовой зонд с малым диаметром отверстия. 14 Идеально разместить это в постпилорическом месте, но желудочное кормление тоже подойдет.
- Энтеральное зондовое питание следует начинать сразу после первой реанимации.Начинайте кормление с уровня тонкой струйки (10-20 мл / час) и продолжайте по мере переносимости.
- Спорно, следует ли кормить желудок (например, через назогастральный / орогастральный зонд) или использовать постпилорический зонд.
- РКИ не показали различий в результатах: подходит любой вариант.
- Среди интубированных пациентов обычно легче установить орогастральный зонд, поэтому этот способ часто используется на начальном этапе.
- Если у пациента проблемы с гастропарезом или рвотой, может оказаться полезным переход на постпилорический зонд.
- Эти пациенты должны первоначально получать строго обезжиренное энтеральное питание.
- Подробнее об этом здесь.
- РКИ по панкреатиту показали вред парентерального питания. Было показано, что это увеличивает риск инфицированного панкреонекроза и полиорганной недостаточности. 13
- Парентеральное питание следует использовать только в крайнем случае, когда энтеральное питание невозможно.
обезболивание
(вернуться к содержанию)
- Опиоиды могут способствовать развитию кишечной непроходимости, нарушать питание и потенциально повышать риск синдрома брюшной полости. Большинству пациентов потребуется некоторое количество опиоидов, но его следует свести к минимуму.
- Инфузии кетамина с обезболивающими (e.г. 0,1-0,3 мг / кг / час) может быть полезным для снятия боли при отказе от опиоидов. 15 16 17
- Не следует забывать о запланированном приеме ацетаминофена, так как он также может сберегать опиоиды (например, ацетаминофен 1 грамм каждые шесть часов). Среди пациентов с циррозом или тяжелым алкоголизмом дозу, вероятно, следует уменьшить до двух граммов в день (например, 650 мг каждые восемь часов). 18
- Следует избегать приема нестероидных противовоспалительных средств тяжелобольным пациентам (и особенно пациентам с панкреатитом), поскольку у таких пациентов повышен риск острого повреждения почек.
- При возможности можно рассмотреть вопрос об эпидуральной анальгезии.
- Подробнее об обезболивании в отделениях интенсивной терапии см. В главе здесь .
антибиотики и инфицированный панкреонекроз
(вернуться к содержанию)
избегать приема антибиотиков в первую неделю
- Как обсуждалось выше, существует много параллелей между сепсисом и панкреатитом. Это приведет к тому, что пациент с панкреатитом будет выглядеть инфицированным по прибытии (например, ).г. панкреатит обычно вызывает лихорадку, лейкоцитоз, гипотонию и сосудорасширяющий шок). Однако это, как правило, отражение стерильного воспаления, а не истинной инфекции.
- Исторически существовало представление, что профилактических антибиотика могут предотвратить развитие инфицированного панкреонекроза. Это было опровергнуто и не должно использоваться. Предварительные антибиотики отбирают устойчивые организмы, которые впоследствии вызывают проблемы (когда действительно происходит настоящая инфекция).
- Следует избегать приема антибиотиков в течение первой недели, за следующими исключениями:
- (a) Диагноз панкреатита неясен, есть опасения по поводу септического шока с очагом инфекции в другом месте.
- (b) У пациента сосуществующий восходящий холангит (который является истинной бактериальной инфекцией и требует декомпрессии и антибиотиков).
- Инфекционные осложнения панкреатита (например, инфицированный некроз) в течение первой недели возникают редко.В течение этого периода воспалительные симптомы (например, лихорадка, лейкоцитоз), вероятно, отражают стерильное воспаление поджелудочной железы.
- Пик наступает примерно через 10-14 дней после начала панкреатита. Классическим представлением является пациент, состояние которого сначала улучшается, но впоследствии ухудшается с обострением сепсиса.
- Исследование обычно начинается с повторной компьютерной томографии. Иногда диагностическими могут быть рентгенологические признаки (например,г. воздух в ткани поджелудочной железы подразумевает инфекцию).
- Тонкоигольная аспирация для определения наличия инфекции обычно используется в некоторых центрах и рекомендуется в канадских рекомендациях по лечению острого панкреатита. 19 Однако в некоторых центрах отдают предпочтение эмпирическим антибиотикам из-за опасения занести инфекцию в поджелудочную железу во время тонкоигольной аспирации. 20
- Традиционно карбапенем (например, меропенем) используется для улучшения проникновения в поджелудочную железу.Однако другие антибиотики также хорошо проникают в поджелудочную железу (например, цефепим / метронидазол, пиперациллин-тазобактам). 21 22 Учитывая, что эти пациенты часто остаются в отделении интенсивной терапии в течение нескольких недель, первоначальное использование пиперациллин-тазобактама (вместо карбапенема) может ограничить выбор устойчивых патогенов.
- Для решения этих устойчивых проблем требуется командный подход, включающий хирургов поджелудочной железы, интервенционных радиологов и инвазивных гастроэнтерологов. В идеале это должно происходить в большом центре, который предлагает ряд малоинвазивных методов обработки раны. 2
- Хотя прокальцитонин часто рассматривается как тест на бактериальный сепсис, его уровень может быть повышен и при панкреатите (что можно было ожидать, исходя из сходства между этими двумя состояниями). Прокальцитонин потенциально может использоваться для двух целей:
- (1) Стратификация риска
- Более высокий уровень прокальцитонина отражает более тяжелое воспаление, которое может предсказывать более тяжелое течение болезни.
- Повышение уровня прокальцитонина> 0,5 нг / мл предсказывает тяжелый панкреатит со средней надежностью (чувствительность 73%, специфичность 87%). 23
- (2) Диагностика инфицированного панкреонекроза
- Сам по себе панкреатит обычно не вызывает значительного повышения уровня прокальцитонина. Следовательно, заметно повышенный уровень прокальцитонина (например,> 3,5 нг / мл) указывает на инфицированный некроз поджелудочной железы. 24 25
- Другие причины повышения прокальцитонина включают почечную недостаточность и другие очаги внутрибольничной инфекции (например,г. линия инфекции, пневмония).
- Значение прокальцитонина для инфицированного панкреонекроза, вероятно, соответствует критерию , исключающему (например, низкий уровень прокальцитонина свидетельствует против инфицированного некроза, тогда как повышенное значение неспецифично). Это может быть полезно для избежания ненужных курсов антибиотиков или инвазивных процедур у пациентов с низким риском истинной инфекции. Для подтверждения этого необходимы дальнейшие проспективные доказательства.
Синдром брюшной полости
(вернуться к содержанию)
- Синдром компартмента может вызвать ухудшение состояния и полиорганную недостаточность.
- Это в основном ятрогенное осложнение из-за использования чрезмерных объемов кристаллоидов. По мере того, как мы уходим от реанимации большого объема панкреатита, это кажется меньшей проблемой.
подкаст
(назад к содержанию)
Следуйте за нами в iTunes
вопросы и обсуждения
(вернуться к содержанию)
Чтобы эта страница оставалась небольшой и быстрой, вопросы и обсуждение этого сообщения можно найти на другой странице здесь .
- Самая распространенная ошибка №1 – введение чрезмерного количества жидкости, вызывающее ОРДС и синдром брюшной полости. К сожалению, эту стратегию продолжают рекомендовать многие источники.
- Задержка начала питания из-за желания «дать отдых» поджелудочной железе.
- Вызванное страхом начало приема антибиотиков в течение первой недели терапии, когда суперинфекция встречается редко.
- Меропенему не требуется проникать в ткань поджелудочной железы, пиперациллин-тазобактам также хорошо проникает.
1.
Хаммад А., Дитилло М., Кастанон Л. Панкреатит. Surg Clin North Am . 2018; 98 (5): 895-913. [PubMed]2.
Гарбер А., Фракс С., Арора З., Чахал П. Механизмы и лечение острого панкреатита. Гастроэнтерол Рес Прак . 2018; 2018: 6218798. [PubMed]3.
Харви Р., Миллер В. Острое заболевание желчевыводящих путей: начальная КТ и последующее УЗИ по сравнению с первоначальным УЗИ и последующей КТ. Радиология .1999; 213 (3): 831-836. [PubMed]4.
Zhang Y, Wu W, Dong L, Yang C, Fan P, Wu H. Отношение нейтрофилов к лимфоцитам предсказывает стойкую органную недостаточность и внутрибольничную смертность в азиатско-китайской популяции острого панкреатита. Медицина (Балтимор) . 2016; 95 (37): e4746. [PubMed]5.
Jeon T, Park J. Клиническое значение соотношения нейтрофилов и лимфоцитов как раннего прогностического маркера неблагоприятных исходов у пациентов с острым панкреатитом. Мир Дж. Гастроэнтерол .2017; 23 (21): 3883-3889. [PubMed]6.
Хан Ч., Цзэн Дж., Лин Р. и др. Полезность соотношения нейтрофилов к лимфоцитам и секвестрации жидкости в качестве раннего предиктора тяжелого острого панкреатита. Научная репутация . 2017; 7 (1): 10704. [PubMed]7.
Wang Y, Fuentes H, Attar B, Jaiswal P, Demetria M. Оценка прогностической ценности отношения нейтрофилов к лимфоцитам у пациентов с острым панкреатитом, вызванным гипертриглицеридемией. Панкреатология . 2017; 17 (6): 893-897.[PubMed]8.
Ли Й, Чжао Й, Фэн Л., Го Р. Сравнение прогностических значений маркеров воспаления у пациентов с острым панкреатитом: ретроспективное когортное исследование. BMJ Open . 2017; 7 (3): e013206. [PubMed]9.
Cho S, Jung S, Lee K, Kim J. Отношение нейтрофилов к лимфоцитам и соотношение тромбоцитов к лимфоцитам может предсказать тяжесть желчнокаменного панкреатита. БМК Гастроэнтерол . 2018; 18 (1): 18. [PubMed]10.
Мао Э, Тан И, Фей Дж и др.Гидравлическая терапия при тяжелом остром панкреатите в стадии острой реакции. Chin Med J (англ.) . 2009; 122 (2): 169-173. [PubMed]11.
Мао Э, Фей Дж, Пэн Й, Хуанг Дж, Тан Й, Чжан С. Быстрая гемодилюция связана с повышенным сепсисом и смертностью среди пациентов с тяжелым острым панкреатитом. Chin Med J (англ.) . 2010; 123 (13): 1639-1644. [PubMed]12.
Ву Б., Хван Дж., Гарднер Т. и др. Лактатный раствор Рингера уменьшает системное воспаление по сравнению с физиологическим раствором у пациентов с острым панкреатитом. Клин Гастроэнтерол Гепатол . 2011; 9 (8): 710-717.e1. [PubMed]13.
Crockett S, Wani S, Gardner T, Falck-Ytter Y, Barkun A, American G. Руководство Института Американской гастроэнтерологической ассоциации по начальному ведению острого панкреатита. Гастроэнтерология . 2018; 154 (4): 1096-1101. [PubMed]14.
Баккер О., ван Б., ван С. и др. Раннее кормление через назоэнтерический зонд в сравнении с кормлением по требованию при остром панкреатите. N Engl J Med . 2014; 371 (21): 1983–1993.[PubMed]15.
Agerwala S, Sundarapandiyan D, Weber G. Использование кетамина для успешного разрешения пост-ERCP острой боли в животе при панкреатите. Case Rep Anesthesiol . 2017; 2017: 7845358. [PubMed]16.
Швенк Э., Вискузи Э., Буванендран А. и др. Консенсусные рекомендации по использованию внутривенных инфузий кетамина для лечения острой боли от Американского общества региональной анестезии и медицины боли, Американской академии медицины боли и Американского общества анестезиологов. Reg Anesth Pain Med . 2018; 43 (5): 456-466. [PubMed]17.
Мотов С., Драпкин Дж., Ликоурезос А. и др. Непрерывное внутривенное вливание субдиссоциативной дозы кетамина для купирования боли в отделении неотложной помощи. West J Emerg Med . 2018; 19 (3): 559-566. [PubMed]18.
Имани Ф., Мотаваф М., Сафари С., Алавиан С. Терапевтическое использование анальгетиков у пациентов с циррозом печени: обзор литературы и рекомендации, основанные на фактах. Hepat Mon .2014; 14 (10): e23539. [PubMed]19.
Гринберг Дж., Хсу Дж., Бавазир М. и др. Руководство по клинической практике: лечение острого панкреатита. Банка J Surg . 2016; 59 (2): 128-140. [PubMed]20.
Макспаррон Дж., Хейс М., Постон Дж. И др. Основной учебный план ATS 2017: Часть III. Медицина интенсивной терапии для взрослых. Энн Ам Торак Соц . 2017; 14 (Приложение_2): С182-С195. [PubMed]21.
Отто В., Коможицкий К., Кравчик М. Эффективность проникновения антибиотиков при панкреонекрозе. Е.П.Б. (Оксфорд) . 2006; 8 (1): 43-48. [PubMed]22.
Бертаццони М., Бенини А., Франко Л., Басси С., Педерзоли П. Проникновение пиперациллин-тазобактама в панкреатический сок человека. Противомикробные агенты Chemother . 2008; 52 (11): 4149-4152. [PubMed]23.
Мофиди Р., Сатти С., Патил П., Огстон С., Паркс Р. Значение прокальцитонина в прогнозировании тяжести острого панкреатита и развития инфицированного панкреонекроза: систематический обзор. Хирургия .2009; 146 (1): 72-81. [PubMed]24.
Рау Б., Кемппайнен Э., Гамбс А. и др. Ранняя оценка инфекций поджелудочной железы и общий прогноз при тяжелом остром панкреатите с помощью прокальцитонина (ПКТ): проспективное международное многоцентровое исследование. Энн Сург . 2007; 245 (5): 745-754. [PubMed]25.
Рау Б., Штайнбах Г., Баумгарт К., Гансауге Ф., Грюнерт А., Бегер Х. Клиническая ценность прокальцитонина в прогнозировании инфицированного некроза при остром панкреатите. Мед. Интенсивной терапии .2000; 26 Приложение 2: С159-64. [PubMed]26.
Скотт П., Брюс С., Скофилд Д., Шил Н., Браганса Дж., Макклой Р. Статус витамина С у пациентов с острым панкреатитом. Br J Surg . 1993; 80 (6): 750-754. [PubMed]27.
Бонэм М., Абу-Зидан Ф., Симович М. и др. Раннее истощение аскорбиновой кислоты связано с тяжестью острого панкреатита. Br J Surg . 1999; 86 (10): 1296-1301. [PubMed]28.
Sağıroğlu T, Eren E, Tunca F, Meydan B, Ertekin C. Влияние гипертонического солевого раствора, аскорбиновой кислоты и низкомолекулярного гепарина на острый некротический панкреатит у крыс. Евразийский журнал J Med . 2008; 40 (2): 53-57. [PubMed]29.
Лю X, Сонг Y, Fu Y, Si J, Цянь К. Аскорбиновая кислота облегчает повреждение поджелудочной железы, вызванное дибутилоловодихлоридом (DBTC) у крыс. Йонсей Мед Дж. . 2007; 48 (6): 1028-1034. [PubMed]30.
Du W, Yuan Z, Sun J и др. Терапевтическая эффективность высоких доз витамина С при остром панкреатите и его потенциальных механизмах. Мир Дж. Гастроэнтерол . 2003; 9 (11): 2565-2569. [PubMed]31.
Фаулер А., Сайед А., Ноулсон С. и др.Исследование безопасности фазы I внутривенного введения аскорбиновой кислоты пациентам с тяжелым сепсисом. J Transl Med . 2014; 12:32. [PubMed]32.
Забет М., Мохаммади М., Рамезани М., Халили Х. Влияние высоких доз аскорбиновой кислоты на потребность в вазопрессорах при септическом шоке. Дж. Рес Фарм Практик . 2016; 5 (2): 94-100. [PubMed]33.
Attaluri P, Castillo A, Edriss H, Nugent K. Дефицит тиамина: важное значение для тяжелобольных пациентов. Am J Med Sci .Июнь 2018 г. [PubMed]34.
Мансанарес В., Харди Г. Добавки тиамина в критически больных. Curr Opin Clin Nutr Metab Care . 2011; 14 (6): 610-617. [PubMed]35.
Woolum J, Abner E, Kelly A, Thompson B, Morris P, Flannery A. Влияние введения тиамина на клиренс лактата и смертность у пациентов с септическим шоком. Crit Care Med . 2018; 46 (11): 1747-1752. [PubMed]36.
Доннино М., Андерсен Л., Чейз М. и др. Рандомизированное, двойное слепое, плацебо-контролируемое исследование тиамина как метаболического реанимационного средства при септическом шоке: пилотное исследование. Crit Care Med . 2016; 44 (2): 360-367. [PubMed]37.
Марик П., Хангура В., Ривера Р., Хупер М., Катравас Дж. Гидрокортизон, витамин С и тиамин для лечения тяжелого сепсиса и септического шока: ретроспективное исследование до и после. Сундук . 2017; 151 (6): 1229-1238. [PubMed]38.
Барабутис Н., Хангура В., Марик П., Катравас Дж. Гидрокортизон и аскорбиновая кислота синергетически предотвращают и восстанавливают индуцированную липополисахаридами дисфункцию легочного эндотелиального барьера. Сундук . 2017; 152 (5): 954-962. [PubMed]39.
Донг Л., Лю З., Ван С. и др. Кортикостероидная терапия при тяжелом остром панкреатите: метаанализ рандомизированных контролируемых исследований. Инт Дж. Клин Эксперт Патол . 2015; 8 (7): 7654-7660. [PubMed]Интернет-книга интенсивной терапии – это онлайн-учебник, написанный Джошем Фаркасом (@PulmCrit), доцентом кафедры легочной медицины и реанимации Университета Вермонта.
Острый панкреатит – WikEM
Фон
- Острый воспалительный процесс, который может поражать окружающие ткани и системы удаленных органов [1]
- Заболевание может варьироваться от легкого воспаления до тяжелого некроза и полиорганной недостаточности
Этиология
- Желчные камни (включая микролитиаз) – 35-40% случаев в большинстве регионов мира [1]
- Алкоголь (острое и хроническое употребление) – 30% случаев в США [2]
- Гипертриглицеридемия
- ERCP
- Наиболее частое осложнение после ЭРХПГ, обычно связанное с механическим повреждением протока поджелудочной железы инструментарием или гидростатическим повреждением в результате инъекции контрастного вещества
- Лекарственные препараты (азатиоприн, цисплатин, фуросемид, тетрациклин, тиазиды, сульфа, вальпроат, диданозин, пентамидин и др.)
- Аутоиммунные заболевания (СКВ, Sjögren и др.)
- Травма живота
- Послеоперационные осложнения
- Инфекция
- Гиперкальциемия
- Гиперпаратиреоз
- Ишемия
- Задняя проникающая язва
- Яд скорпиона (вызван жанром Tityus и Leiurus , которые распространены в Центральной / Южной Америке и Северной / Восточной Африке, соответственно
- Фосфаторганический инсектицид
- Опухоль поджелудочной железы или ампулы
- Divisum поджелудочной железы с протоковым сужением на панкреатограмме
- Дисфункция сфинктера Одди
- Идиопатический (15-20% случаев)
Клинические особенности
- Боль является наиболее частым симптомом и часто характеризуется: [1]
- Постоянной
- Локализуется в эпигастральной области, вокруг талии, RUQ или иногда в LUQ
- Излучает назад
- Начало может быть менее резким, а боль плохо локализована
- Тошнота / рвота отмечаются у большинства
- Вздутие живота – частая жалоба
- Признак Каллена (экхимоз околопупочной области) – внутрибрюшное кровоизлияние
- Симптом Тернера (экхимозы боков) – забрюшинное кровоизлияние
- Результаты исследования легких
- Гипоксемия, ОРДС, тахипноэ
- Указывает на тяжелый панкреатит.
- Воспаление диафрагмы, панкреатоплевральный свищ
Дифференциальный диагноз
Боль в эпигастрии
Диффузная боль в животе
Оценка
УЗИ острого панкреатита с неоднородной гипоэхогенной областью в проекции тела / хвоста, свидетельствующей о обширном некрозе.Осложненный острый панкреатит с большим абсцессом в проекции хвоста. Острый экссудативный панкреатит на компьютерной томографии Панкреатт с кальцинированными камнями протоков поджелудочной железы с небольшим количеством свободной жидкости в брюшной полостиWork-Up
- липаза
- Амилаза менее чувствительна и специфична (чувствительность: 67-100%; специфичность: 85-98%) [3]
- CBC
- Химия
- LFT
- ? Лактат
- ? Триглицерид
Ультразвук
- Отечная, опухшая поджелудочная железа
- Камни в желчном пузыре
- Псевдокиста / абсцесс поджелудочной железы
КТ с внутривенным контрастированием
[4]- Мало пользы на ранних стадиях заболевания и вряд ли повлияет на ведение пациентов с острым панкреатитом в течение первой недели болезни
- Следует зарезервировать для пациентов с хронической органной недостаточностью, сильной болью и признаками сепсиса
Диагноз
Два из следующих:
- Характерная боль в животе
- Уровень липазы> 3x верхнего предела нормы
- Чувствительность 82-100%, специфичность 82-100% [5]
- Отрицательная липаза не исключает панкреатит при хроническом / рецидивирующем заболевании
- Абсолютное значение, не связанное с прогнозом или серьезностью
- Характерные результаты на УЗИ или КТ
Ведение
Основное лечение включает поддерживающую терапию для отдыха поджелудочной железы.Этого можно добиться, главным образом, за счет диеты.
Медицинский
Диета
- NPO (очистка, вероятно, подходит для легких / умеренных случаев)
- При возобновлении диеты ешьте небольшими порциями с низким содержанием жира и постепенно переходите к следующему этапу в течение 3–6 дней в зависимости от переносимости
- Для пациентов с легким панкреатитом, которые переносят пероральные инъекции и, скорее всего, могут быть выписаны. Необходимы инструкции относительно легкой диеты и отказа от алкоголя [1]
Внутривенные жидкости
Обезболивающие и противорвотные
Управление электролитами и другими молекулами
Антибиотики
Использование антибиотиков часто вызывает споры и обычно требуется только при наличии явных признаков или источников инфекции.В профилактических целях нет необходимости [7] [8] [9] [10] [11]
Процедурные / хирургические
Декомпрессия кишечника
- Рассматривайте установку трубки NG только при наличии SBO или кишечной непроходимости и симптоматических симптомов
ERCP
[12]- Показан пациентам с желчнокаменным панкреатитом с сохраненным камнем CBD или холангитом (рекомендуется в течение 24 часов)
- Альтернативный вариант для пациентов с желчнокаменным панкреатитом, которые не подходят для оперативного вмешательства для холецистэктомии
Холецистэктомия
- Показан пациентам с билиарным панкреатитом.Пациентам, как правило, будет полезна ранняя холецистэктомия, как только пациент выздоровеет, предпочтительно в рамках той же госпитализации. [13]
Сбор жидкости Дренаж
- Симптоматические скопления жидкости поджелудочной железы с ограниченными стенками должны быть оценены для процедуры дренирования.
Распоряжение
Разряд
- Легкий случай + отсутствие желчевыводящих путей + отсутствие системных осложнений + переносимость клирса
- Пациенты могут быть выписаны, когда пероральные анальгетики купируют их боль
Допускаются
Осложнения
местный
- Некроз поджелудочной железы
- Псевдокиста / абсцесс поджелудочной железы
- Тромбоз воротной вены
- Синдром брюшной полости
- Псевдоаневризма брюшной полости
- Внутрибрюшное кровоизлияние
Системное
Прогноз
APACHE-II
- Высочайшая чувствительность и специфичность в различении легкого панкреатита от тяжелого [14]
- Может использоваться для оценки риска смерти в отделении интенсивной терапии на основе худшего набора лабораторий в течение первых 24 часов пациента
Индекс тяжести КТ
Расширение шкалы Бальтазара со стратификацией степени тяжести на основе баллов. [15] [16]
- Классификация панкреатита по шкале Бальтазара
- A = нормальная поджелудочная железа – 0
- B = увеличение поджелудочной железы – 1
- C = воспалительные изменения поджелудочной железы и перипанкреатического жира – 2
- D = единичный сбор жидкости с плохим определением – 3
- E = два или более плохо определенных коллектора жидкости – 4
- нет – 0
- меньше / равно 30% – 2
- > 30–50% – 4
- > 50% – 6
- Максимальный балл, который можно получить, равен 10.
- 0-3: легкая
- 4-6: умеренный
- 7-10: тяжелая
Критерии Рэнсона
- Состоит из 11 параметров. Пять факторов оцениваются при поступлении, а шесть факторов оцениваются в течение следующих 48 часов. [17]
- Оценка 3 или более указывает на тяжелый острый панкреатит.
- При приеме
- Возраст> 55
- WBC> 16,000
- Глюкоза крови> 200 мг / дл
- Лактатдегидрогеназа> 350 Ед / л
- Аспартатаминотрансфераза (АСТ)> 250 Ед / л
- 48 часов
- Снижение гематокрита> 10%
- АМК увеличивается на> 5 мг / дл
- Кальций в сыворотке <8 мг / дл
- pO2 <60 мм рт. Ст.
- Базовый дефицит> 4 MEq / л
- Секвестрация жидкости> 6 л
BISAP
- Прикроватный индекс тяжести острого панкреатита [18]
- Пониженная чувствительность, но превосходит по специфичности по сравнению с Ranson и APACHE II [19] [20]
- Клинически легче получить, особенно в условиях неотложной помощи
- АМК> 25 мг / дл
- Нарушение психического статуса, определяемое как дезориентация, летаргия, сонливость
- ≥2 критерия SIRS
- Возраст> 60 лет
- Плевральный выпот
- Устный перевод
- Оценка 0-2, летальность <2%
- Оценка 3-4, смертность> 15%
- Оценка 5 дает 22% смертности
См. Также
Внешние ссылки
Список литературы
- ↑ 1.0 1,1 1,2 1,3 Уиткомб Д. Острый панкреатит. N Engl J Med 2006; 354: 2142-215
- ↑ Vege SS. Этиология острого панкреатита. Uptodate.com
- ↑ Ядав Д., Агарвал Н., Пичумони С.С. Критическая оценка лабораторных тестов при остром панкреатите. Am J Gastroenterol. 2002 июн; 97 (6): 1309-18.
- ↑ Рабочая группа Великобритании по острому панкреатиту. Руководство Великобритании по лечению острого панкреатита. Кишечник 2005; 54: iii1-iii9
- ↑ Ядав Д., Агарвал Н., Пичумони С.С.Критическая оценка лабораторных тестов при остром панкреатите. Am J Gastroenterol. 2002 июн; 97 (6): 1309-18.
- ↑ Nathens AB, Curtis JR, Beale RJ, et al. Ведение тяжелобольного пациента с тяжелым острым панкреатитом. Crit Care Med 2004; 32: 2524-2536.
- ↑ Bassi C, Larvin M, Villatoro E. Антибактериальная терапия для профилактики инфекции панкреонекроза при остром панкреатите. Кокрановская база данных Syst Rev.2003; Выпуск 4, CD002941.
- ↑ Голуб Р., Сиддики Ф., Поль Д.Роль антибиотиков при остром панкреатите: метаанализ. J Gastrointest Surg. 1998; 2: 496–503.
- ↑ Sharma VK, Howden CW. Профилактическое введение антибиотиков снижает сепсис и смертность при остром некротическом панкреатите: метаанализ. Поджелудочная железа. 2001; 22: 28–31.
- ↑ Чжоу Ю.М., Сюэ З.Л., Ли Ю.М. и др. Антибиотикопрофилактика у пациентов с тяжелым острым панкреатитом. Гепатобилиарный панкреат Dis Int. 2005; 4: 23–27.
- ↑ Manes G, Rabitti PG, Menchise A, et al. Профилактика септических осложнений при остром панкреатите меропенемом: рандомизированное контролируемое исследование по сравнению с имипенемом.Поджелудочная железа. 2003; 27: 79–83.
- ↑ Теннер, С., Бэйли, Дж., ДеВитт, Дж. И Ведж, С. (2013). Рекомендации Американского колледжа гастроэнтерологии: ведение острого панкреатита. Американский журнал гастроэнтерологии, 108 (9), стр. 1400-1415.
- ↑ Kimura Y, Takada T, Kawarada Y et al. Руководство JPN по лечению острого панкреатита: лечение острого панкреатита, вызванного желчнокаменной болезнью. J Hepatobilation Pancreat Surg. 2006; 13 (1): 56-60.
- ↑ Knaus WA, Draper EA, Wagner DP, Zimmerman JE.APACHE II: система классификации тяжести заболевания.
- ↑ Balthazar EJ, Robinson DL, Megibow AJ et al. Острый панкреатит: значение КТ для установления прогноза. Радиология. 1990; 174 (2): 331-6.
- ↑ Balthazar EJ. Острый панкреатит: оценка степени тяжести с помощью клинической и компьютерной томографии. Радиология. 2002; 223 (3): 603-13PDF.
- ↑ Ranson JH, Rifkind KM, Roses DF, Fink SD, Eng K, Spencer FC. Прогностические признаки и роль оперативного лечения при остром панкреатите.Surg Gynecol Obstet. 1974 июл; 139 (1): 69-81. PubMed PMID: 4834279
- ↑ Wu BU et al. Раннее прогнозирование смертности при остром панкреатите: крупное популяционное исследование. Кишечник. 2008 декабрь; 57 (12): 1698-703.
- ↑ Gao W et al. Значение оценки BISAP для прогнозирования смертности и тяжести острого панкреатита: систематический обзор и метаанализ. PLoS One. 2015; 10 (6): e0130412.
- ↑ Papachristou GI et al. Сравнение показателей BISAP, Ranson’s, APACHE-II и CTSI для прогнозирования органной недостаточности, осложнений и смертности при остром панкреатите.Am J Gastroenterol. 2010 февраль; 105 (2): 435-41; Виктория 442.
Управление коллекциями (пери) поджелудочной железы при остром панкреатите – FullText – Visceral Medicine 2019, Vol. 35, № 2
Аннотация
Образование скоплений (пери) панкреатической жидкости – частое местное осложнение острого панкреатита. Эти скопления классифицируются как ранние (скопление острой перипанкреатической жидкости или скопление острого некроза) или поздние (некроз со стенками или псевдокиста).Большинство скоплений жидкости поджелудочной железы рассасываются спонтанно и не требуют вмешательства. Однако инфекция может потребовать вмешательства. Вмешательства могут включать эндоскопический или чрескожный катетерный дренаж, а на следующем этапе – эндоскопическую или хирургическую некрэктомию, минимально инвазивную или открытую. Оптимальное время для первого вмешательства все еще исследуется. В то время как некоторые используют антибиотики, чтобы отложить вмешательство до стадии некроза стенок, другие дренируют раньше. Эндоскопический дренаж скоплений (пери) панкреатической жидкости в настоящее время является предпочтительным методом дренирования из-за снижения заболеваемости по сравнению с хирургическим или чрескожным дренированием.Однако к каждой коллекции необходимо подходить индивидуально. Окончательное лечение должно учитывать анатомические характеристики, предпочтения пациента, профиль сопутствующей патологии пациента и усмотрение врача. В этом обзоре обобщены текущие данные по лечению скоплений (пери) панкреатической жидкости.
Автор (ы). Опубликовано S. Karger AG, Базель
Введение
Острый панкреатит (ОП) составляет более 50% всех госпитализаций по поводу заболевания поджелудочной железы и по-прежнему представляет собой одно из самых непредсказуемых заболеваний пищеварительной системы [1].Как таковой, ОП может быть связан с различными местными или системными осложнениями, а в наиболее тяжелой форме он может привести к полиорганной недостаточности и даже смерти [1-4]. Умеренно тяжелый панкреатит определяется как ОП, который сопровождается местными осложнениями (например, некрозом) панкреатической и / или перипанкреатической ткани и преходящей органной недостаточностью, а тяжелый панкреатит определяется как местные осложнения в сочетании со стойкой органной недостаточностью [2]. Примерно у 15–20% пациентов развивается умеренно тяжелая или тяжелая форма заболевания.Почти у одной трети этой группы возникает инфекция (пери) панкреонекроза, что связано с уровнем смертности от 15% до 39% [4-8]. Примерно половина случаев смерти от AP происходит в течение первых 2 недель заболевания, в основном из-за полиорганной недостаточности в результате тяжелой системной воспалительной реакции. Остальная часть смертей наступает позже в результате вторичных осложнений инфекции (пери) панкреонекроза и последующих вмешательств [9, 10].
Эффективное лечение требует точной диагностики и лечения многопрофильной командой хирургов, гастроэнтерологов, реаниматологов и радиологов, работающих в тандеме, чтобы минимизировать заболеваемость и смертность.За последние десятилетия лечение эволюционировало от агрессивной открытой хирургии к более консервативному подходу с минимально инвазивными методами. В этом обзоре будут представлены и обобщены существующие данные по лечению скоплений (пери) панкреатической жидкости и даны комментарии по проблемам, которые ждут впереди.
Определения скоплений перипанкреатической жидкости
Одним из наиболее частых местных осложнений при АП является накопление (пери) скоплений жидкости поджелудочной железы (ПФК). В соответствии с пересмотренной классификацией Атланты 2012 года [2], ПФК можно классифицировать в зависимости от остроты зрения и содержания на четыре отличительные категории: острая перипанкреатическая жидкость (APFC), острые некротические скопления (ANC), панкреатические псевдокисты (PP) и оторванные стенки некроз (ВОН).В соответствии с этой классификацией PP определяется как четко очерченный, однородный скопление жидкости, окруженное четко определенной стенкой без связанной некротической ткани в этом скоплении, и наблюдается> 4 недель после начала интерстициального отечного панкреатита. PP будет иметь строго жидкое вещество и, следовательно, по определению никогда не будет возникать при некротическом панкреатите. До 4 недель после начала AP эти скопления жидкости называются APFC и не имеют стенки [2, 11]. APFC и PP могут возникать в результате разрыва главного протока поджелудочной железы или одной из меньших периферических боковых ветвей протоковой системы поджелудочной железы.Необязательно, чтобы все APFC и PP имели прямое сообщение с протоком поджелудочной железы, поскольку они также могут возникать в результате местного отека, вторичного по отношению к воспалению поджелудочной железы [2, 12]. Обычно эти коллекции рассасываются спонтанно [2, 13, 14].
АНК может возникнуть в результате некротического панкреатита. Эти коллекции содержат как жидкие, так и некротические компоненты. Это можно рассматривать как более неоднородное представление при визуализации брюшной полости (например, компьютерной томографии с контрастным усилением или магнитно-резонансной томографии).Некроз разовьется в первые 3-5 дней после начала заболевания, поэтому раннее сканирование может недооценить степень некроза. Поэтому рекомендуется выполнять визуализацию через 5 дней после начала заболевания. В острой фазе бывает трудно отличить APFC от ANC. После первоначального диагноза скопления жидкости может пройти 1-2 недели, чтобы провести четкое различие [2, 14]. Некротический панкреатит может проявляться некрозом паренхимы поджелудочной железы, обычно сопровождающимся перипанкреатическим некрозом.У небольшой группы пациентов будет только внепанкреатический некроз (EXPN) без некроза паренхимы. Примерно через 2–6 недель после начала ОП некротическая ткань начинает разжижаться, создавая вид как жидких, так и твердых компонентов в четко разграниченной области (WON) [15]. Следовательно, термин WON относится к зрелой АНК, которая имеет хорошо разграниченную и утолщенную стенку между некротической и жизнеспособной тканью поджелудочной железы [2].
Показания и сроки для вмешательства (пери) панкреатической жидкости и некротических скоплений
Показания для вмешательства PFC менялись с годами.Ранее [16] ПФУ рассматривались для дренирования на основании наличия симптомов и / или осложнений, таких как боль в животе, непроходимость желудочно-кишечного тракта, сдавление сосудов, непроходимость желчевыводящих путей или инфекция, а также от размера скопления. Однако в соответствии с рекомендациями дренирование необходимо только в инфицированных коллекциях или в исключительных случаях при симптоматических скоплениях жидкости после длительного консервативного лечения [17].
Как правило, вмешательство в ПФУ считается предпочтительным, если оно проводится после инкапсуляции или демаркации сбора (обычно примерно через 4 недели).Это облегчает попадание в коллекцию с более низкой вероятностью свободной перфорации и более высокой вероятностью успешного дренирования из-за большего прилегания коллекции к просвету желудочно-кишечного тракта при эндоскопическом доступе, например [18]. Кроме того, отсрочка вмешательства снизила смертность из-за снижения провоспалительного ответа у уже находящихся в критическом состоянии пациентов, уменьшила послеоперационные осложнения и технически более проста в выполнении с меньшим количеством нежелательных явлений [19, 20].Однако все эти аргументы были экстраполированы на основе прямой открытой хирургической некрэктомии. Неясно, применимо ли то же самое к текущим малоинвазивным процедурам.
PP представляет собой инкапсулированное скопление жидкости с четко выраженной воспалительной стенкой, обычно вне поджелудочной железы без некроза. Этому заболеванию обычно требуется более 4 недель после начала интерстициального отечного панкреатита для созревания [2]. ПП на КТ с контрастным усилением представляет собой четко очерченную, обычно круглую или овальную однородную жидкость плотностью без нежидкого компонента (рис.1) [2, 11, 21]. Спонтанное разрешение ПП колеблется от 8 до 70% и зависит от нескольких факторов: наличия множественных кист, расположения в хвосте поджелудочной железы, коммуникации с основным протоком поджелудочной железы и сосуществования стриктуры, а также увеличения размера во время наблюдения [22- 24]. Вмешательство следует отложить на срок до 6 недель от начала АП, чтобы дать стенке ПП созреть [3, 12, 24]. Эта задержка вмешательства способствует успеху любого типа дренажа [25]. Исключением этой задержки является возникновение опасных для жизни событий, таких как эрозия окружающих кровеносных сосудов с кровотечением с разрывом кисты или без него; однако это очень редко.ПП диаметром менее 3 см обычно протекают бессимптомно и не требуют вмешательства. Абсолютного размера, при котором требуется вмешательство, не существует; однако сообщалось о повышенном риске осложнений, связанных с кистой> 5 см в диаметре, особенно при отсутствии уменьшения размера кисты в течение 6 недель [2, 18, 24, 26]. Неосложненные и бессимптомные ПП, которые остаются стабильными или даже уменьшаются в размерах, можно лечить консервативно. ПП большего размера могут вызывать симптомы и являются относительным показанием к вмешательству.Симптомы включают стойкую боль в животе, боль в боку или спине, частичную или полную обструкцию выходного отверстия желудка или двенадцатиперстной кишки с ранним насыщением, анорексию, потерю веса, вздутие живота, рвоту или рефлюкс, непроходимость желчевыводящих путей и желтуху. Как уже упоминалось, более серьезные осложнения включают инфекцию PP, кровотечение в кисту, разрыв PP и эрозии гастродуоденальной и / или селезеночной артерии [18, 27-29], где необходимо вмешательство.
Рис. 1.
Компьютерная томография скопления жидкости поджелудочной железы у мужчины 63 лет через 56 дней после начала острого панкреатита.Для исключения наличия некроза поджелудочной железы в этом сборе требуется УЗИ или МРТ.
В течение первых 2–4 недель после возникновения АНК он либо рассасывается, либо инкапсулируется (рис. 2). Большинство ДРП бесплодны и разрешаются при консервативном лечении, но в случаях инфекции потребуется дальнейшее вмешательство [17]. Бессимптомный WON не требует вмешательства независимо от его размера, потому что он может разрешиться спонтанно с течением времени [8, 30]. Даже в больших коллекциях большинство рассосется спонтанно.Однако было показано, что больший размер WON, распространение WON до параколического желоба и распространение некроза связаны с необходимостью вмешательства [31-33]. Вмешательство в стерильную коллекцию несет риск вторичной ятрогенной инфекции со всеми связанными с ней заболеваемостью и смертностью. Симптоматический стерильный некротический сбор (например, боль в животе или механическая непроходимость) может потребовать вмешательства; однако из-за риска вторичной ятрогенной инфекции следует сосредоточить внимание на консервативном лечении, а вмешательство следует отложить на 6–8 недель или дольше [8].Почти у 30% пациентов происходит инфицирование (пери) панкреонекроза, что требует вмешательства у подавляющего большинства пациентов (рис. 3). Лишь небольшой процент пациентов можно лечить только антибиотиками [34, 35]. Поскольку ранняя открытая операция связана с высокой заболеваемостью и смертностью, ее следует по возможности избегать. Ишемия брыжейки и синдром абдоминального компартмента как прямое следствие ОП могут представлять только два абсолютных показания к раннему открытому хирургическому вмешательству [36].Неросэктомия в первые 2 недели сопряжена с высоким риском заболеваемости и смертности, поэтому ее следует избегать [19, 20, 36]. Однако чрескожное дренирование может быть выполнено на ранней стадии инфицированного некротического панкреатита. В настоящее время голландская группа по изучению панкреатита проводит исследование POINTER (http://www.isrctn.com/ISRCTN33682933), которое рандомизирует 104 пациента между немедленным дренированием катетера после диагностики инфицированного некроза и текущим стандартным лечением с отсрочкой дренирования катетера при лечении антибиотиками. (желательно до некроза от стенок).При необходимости будет выполнена некрэктомия, которая будет отложена, если это возможно, до стадии некроза стенок в обеих группах лечения. В настоящее время в это испытание набрано более 75% пациентов, и результаты ожидаются в 2020 году.
Рис. 2.
Острый некротический забор у 57-летнего мужчины через 17 дней после начала острого панкреатита.
Рис. 3.
Некроз стенок с инфекцией, подтвержденный ударным газом у 74-летней женщины через 27 дней после начала острого панкреатита.
Управление острыми скоплениями перипанкреатической жидкости и псевдокистами поджелудочной железы
Как указано выше, APFC не требует какого-либо вмешательства и может лечиться консервативно. Если есть показания к вмешательству ПП, доступно несколько методов, включая чрескожный, эндоскопический и хирургический дренаж. Эндоскопический трансмуральный дренаж по существу заменил хирургический и чрескожный дренаж.
В последние два десятилетия исследования, сравнивающие различные методы лечения, показывают значительную неоднородность включенных исследований, и нельзя сделать однозначный вывод [37–45].Адекватная техника, которую следует использовать, зависит от анатомии, локализации ПП, размера, содержимого и связи с основным протоком поджелудочной железы. В одном из крупнейших исследований по сравнению чрескожного и хирургического дренирования ПП Morton et al. [44] пришли к выводу, что хирургический подход имеет меньше осложнений, меньшую стационарную смертность и сокращает время пребывания в стационаре. Аналогичные результаты были опубликованы Heider et al. [45], которые предпочли хирургический доступ чрескожному. Только два исследования, опубликованные почти 3 десятилетия назад, отдавали предпочтение чрескожному доступу перед хирургическим с точки зрения более высокой смертности, заболеваемости [46] и повторных вмешательств [47].Что касается показателя успеха, похоже, что хирургический подход имел более высокий уровень клинического успеха, но общий показатель успеха был одинаковым для всех методов [40–45]. С другой стороны, хирургическое дренирование все же может быть предпочтительным, поскольку оно позволяет избежать использования внешнего катетера и снижает риск развития внешнего свища поджелудочной железы. При сравнении эндоскопических процедур с другими методами лечения ПП, эндоскопический трансмуральный подход показал преимущество в сокращении госпитализации, стоимости лечения и качества жизни [37–39, 41, 46].Следовательно, эндоскопический доступ предпочтителен, когда анатомия ПП позволяет прямой дренаж в желудок или двенадцатиперстную кишку. Только если киста расположена далеко от желудка или двенадцатиперстной кишки, следует рассмотреть возможность хирургического или чрескожного доступа. Кроме того, чрескожный дренаж может быть полезен в случаях слабых пациентов с тяжелыми сопутствующими заболеваниями, которые не переносят никакие другие процедуры; однако из-за риска возникновения кожно-панкреатической фистулы этот метод лечения не является предпочтительным. Важно оценить связь между ППК и основным протоком поджелудочной железы из-за снижения клинического успеха только трансмурального дренажа в случаях, когда такая связь присутствует.В таких случаях комбинированный эндоскопический трансмуральный и транспапиллярный дренаж может иметь преимущество перед методом единого доступа [48]. Однако в другом исследовании не было обнаружено каких-либо преимуществ от комбинации транспапиллярного и трансмурального дренирования по сравнению с одним только трансмуральным дренажом [49], и на данный момент использование этого комбинированного подхода остается неоднозначным.
Лечение острых некротических скоплений и некроза за стенками
Инвазивные интервенционные процедуры при остром некротическом панкреатите включают рентгенологический, эндоскопический и хирургический доступ.Раньше предпочтительным методом выбора была первичная открытая некрэктомия. Это было связано с высокими показателями смертности и заболеваемости. В настоящее время предпочтительным методом лечения является поэтапный подход, при котором в первую очередь дренируются некротические скопления, а в случае отсутствия клинического улучшения существует «шаг вперед» в направлении некрэктомии. Этот поэтапный подход снижает частоту впервые возникшей полиорганной недостаточности, заболеваемость, серьезные побочные эффекты и снижает затраты [50, 51] по сравнению с первичной открытой некрэктомией, от которой с тех пор в значительной степени отказались.
При поэтапном подходе почти половину пациентов можно лечить только с помощью дренажа, другой половине требуются дополнительные различные процедуры для окончательного лечения, включая чрескожную, эндоскопическую, открытую или минимально инвазивную хирургию [17, 50, 52 , 53]. В систематическом обзоре, включающем 10 ретроспективных серий и одно РКИ с 384 пациентами, которым было выполнено чрескожное дренирование из-за острого некротического панкреатита, чрескожного дренирования было достаточно в качестве окончательного лечения у 56% пациентов [54].Другой анализ показал, что чрескожное дренирование вместе с антибиотиками было успешным у 50% пациентов [55]. Сравнительных испытаний диаметра катетера пока нет, но катетеры с большим диаметром, кажется, реже закупориваются некротическими осколками. Увеличение диаметра дренажей до большего диаметра может быть полезным для результатов [35, 50, 54, 56]. Если пациент не выздоравливает только с помощью дренажа, требуется некрэктомия. Традиционная открытая некрэктомия в значительной степени заменена малоинвазивными методами [6, 50, 51].Из них наиболее часто используемые методы включают эндоскопию синусового тракта и ретроперитонеальную санацию с помощью видео (VARD) [57, 58]. Эти методы показали снижение заболеваемости и смертности, особенно в группах высокого риска [59].
В последние десятилетия все чаще применяется эндоскопическое трансмуральное (т.е. трансжастральное) лечение острого некротического панкреатита. Для лечения WON используются различные эндоскопические методы, все они включают трансмуральный доступ к полости с эндоскопическим ультразвуком (EUS) или без него.Дренаж и / или некрэктомия под контролем EUS имеют преимущество перед традиционным трансмуральным эндоскопическим доступом благодаря более высокому техническому успеху [40, 42, 60]. По сравнению с хирургической некрэктомией, эндоскопический подход значительно снижает провоспалительный ответ и улучшает клинический исход у пациентов с ANP [52]. Однако при использовании в качестве единого метода лечения для окончательного лечения требуется больше сеансов некрэктомии, чем в сочетании с другими интервенционными процедурами [53, 61-63]. Большой метаанализ показал, что эндоскопическая некрэктомия имеет эффективность 81% в качестве единственного метода лечения с частотой осложнений 36% [64].В крупнейшем рандомизированном контролируемом исследовании, сравнивающем эндоскопический поэтапный подход с увеличивающим хирургическим подходом [53], обе процедуры имели одинаковые показатели смертности и серьезных осложнений. Тем не менее, при хирургическом подходе повышенная частота встречаемости панкреатокожных свищей была выше [51, 53].
Заключение
Управление сбором панкреатической жидкости должно быть адаптировано для каждого пациента. Междисциплинарный подход имеет решающее значение для адекватного и своевременного лечения. Бессимптомные коллекции не требуют дренажа независимо от их размера.Зараженные коллекции могут потребовать вмешательства. Отсрочка вмешательства по крайней мере на 3–4 недели после начала ОП позволяет лучше принять решение при выборе интервенционного подхода. Минимально инвазивный пошаговый подход превосходит первичную открытую операцию с точки зрения заболеваемости для всех скоплений перипанкреатической жидкости и должен быть лечением выбора. Решение о хирургическом / чрескожном или эндоскопическом лечении должно приниматься с учетом анатомии, места сбора и местных знаний эндоскопистов, радиологов и хирургов.
Список литературы
- Диагностика и лечение панкреатита. NICE руководство. Март 2018 г. Доступно по адресу: www.nice.org.uk.
- Бэнкс П.А., Боллен Т.Л., Дервенис С., Гуззен Х.Г., Джонсон С.Д., Сарр М.Г. и др.; Рабочая группа по классификации острого панкреатита. Классификация острого панкреатита – 2012: пересмотр классификации и определений Атланты на основе международного консенсуса. Кишечник. 2013 Янв; 62 (1): 102–11.
- Рана СС, Шарма В., Шарма Р.К., Чхабра П., Гупта Р., Бхасин Д.К. Клиническое значение наличия и степени экстрапанкреатического некроза при остром панкреатите.J Gastroenterol Hepatol. 2015 Апрель; 30 (4): 794–8.
- Бэнкс PA, Freeman ML; Комитет по параметрам практики Американского колледжа гастроэнтерологии. Практическое руководство при остром панкреатите. Am J Gastroenterol. Октябрь 2006 г.; 101 (10): 2379–400.
- Траверсо Л.В., Козарек Р.А.Некрэктомия поджелудочной железы: определения и техника. J Gastrointest Surg. Март 2005 г .; 9 (3): 436–9.
- Рарати М.Г., Халлоран С.М., Додд С., Гане П., Коннор С., Эванс Дж. И др. Забрюшинная некрэктомия поджелудочной железы с минимальным доступом: снижение заболеваемости и смертности с помощью менее инвазивного подхода.Ann Surg. 2010 Май; 251 (5): 787–93.
- Тан В., Шарашон А., Леско Т., Шафай Н., Ле Балер Й., Дельшер Дж. К. и др. Сравнение эндоскопической трансгастральной некрозэктомии и хирургической некроза поджелудочной железы. Клин Рес Гепатол Гастроэнтерол. 2014 декабрь; 38 (6): 770–6.
- Фриман М.Л., Вернер Дж., Ван Сантвоорт Х.С., Барон Т.Х., Бесселинк М.Г., Виндзор Дж. А. и др.; Международная многопрофильная группа спикеров и модераторов. Вмешательства при некротическом панкреатите: резюме многопрофильной консенсусной конференции. Поджелудочная железа. 2012 ноябрь; 41 (8): 1176–94.
- Карновале А., Рабитти П.Г., Манес Дж., Эспозито П., Пачелли Л., Уомо Г. Смертность при остром панкреатите: раннее или позднее событие? JOP.2005 сентябрь; 6 (5): 438–44.
- Fu CY, Yeh CN, Hsu JT, Jan YY, Hwang TL. Сроки смертности при тяжелом остром панкреатите: опыт 643 пациентов. Мир Дж. Гастроэнтерол. 2007 Апрель; 13 (13): 1966–9.
- Thoeni RF.Пересмотренная Атланта классификация острого панкреатита: ее значение для радиолога и ее влияние на лечение. Радиология. 2012 Март; 262 (3): 751–64.
- Пан Г., Ван М. Х., Се К. Л. и др. Классификация и лечение псевдокист поджелудочной железы. Медицина (Балтимор). 2015 июн; 94 (24): e960.
- Майерле Дж., Талукдар Р., Бейер Дж. И др. Интервенционная и эндоскопическая терапия хронического панкреатита. Pancreapedia. База знаний по экзокринной поджелудочной железе; 2016. https://doi.org/10.3998/panc.2016.28.
- Сарр М.Г., Бэнкс П.А., Боллен Т.Л., Дервенис С., Гуззен Х.Г., Джонсон С.Д. и др.Новая пересмотренная классификация острого панкреатита 2012. Surg Clin North Am. 2013 июнь; 93 (3): 549–62.
- ван Гринсвен Дж., ван Бруншот С., ван Баал М.С., Бесселинк М.Г., Фокенс П., ван Гур Х. и др .; Голландская исследовательская группа по панкреатиту. Естественная история газовых конфигураций и инкапсуляции в некротических коллекциях при некротическом панкреатите.J Gastrointest Surg. 2018 Сен; 22 (9): 1557–64.
- Брэдли Э.Л. 3-й. Клинически обоснованная система классификации острого панкреатита. Резюме Международного симпозиума по острому панкреатиту, Атланта, штат Джорджия, 11–13 сентября 1992 г. Arch Surg. 1993 Май; 128 (5): 586–90.
- Рекомендации Рабочей группы IAP / APA по острому панкреатиту.Рекомендации IAP / APA по лечению острого панкреатита, основанные на фактических данных. Панкреатология. 2013; 13 (4 Suppl 2): e1–15.
- Песня TJ, Ли СС. Эндоскопический дренаж псевдокист. Clin Endosc. 2014 Май; 47 (3): 222–6.
- Миер Дж., Леон Э.Л., Кастильо А, Робледо Ф., Бланко Р.Сравнение ранней и поздней некрэктомии при тяжелом некротическом панкреатите. Am J Surg. 1997, февраль, 173 (2): 71–5.
- Besselink MG, Verwer TJ, Schoenmaeckers EJ, Buskens E, Ridwan BU, Visser MR, et al. Сроки хирургического вмешательства при некротическом панкреатите. Arch Surg. 2007 декабрь; 142 (12): 1194–201.
- Ленхарт Д.К., Бальтазар Э.Дж. МДКТ острого легкого (ненекротического) панкреатита: абдоминальные осложнения и судьба скоплений жидкости. AJR Am J Roentgenol. Март 2008 г., 190 (3): 643–9.
- Андрен-Сандберг А., Дервенис К.Псевдокисты поджелудочной железы в 21 веке. Часть II: естествознание. JOP. Март 2004 г.; 5 (2): 64–70.
- Андрен-Сандберг А., Ансорге С., Эйрикссон К., Гломсакер Т., Малецкас А. Лечение псевдокист поджелудочной железы. Scand J Surg. 2005. 94 (2): 165–75.
- Агалианос К., Пассас I, Сидерис I, Давидес Д., Дервенис К.Обзор вариантов лечения псевдокист поджелудочной железы. Перевод Гастроэнтерол Гепатол. Март 2018; 3:18.
- Парки RW, Tzovaras G, Diamond T, Rowlands BJ. Лечение псевдокист поджелудочной железы. Ann R Coll Surg Engl. 2000 ноя; 82 (6): 383–7.
- Muthusamy VR, Chandrasekhara V, Acosta RD, Bruining DH, Chathadi KV, Eloubeidi MA, et al.; Комитет по стандартам практики ASGE. Роль эндоскопии в диагностике и лечении воспалительных скоплений поджелудочной железы. Gastrointest Endosc. 2016 Март; 83 (3): 481–8.
- Дакка Н., Саманта Дж., Кочхар С., Калра Н., Аппасани С., Манрай М. и др. Сборы поджелудочной железы: каков идеальный метод визуализации? Мир Дж. Гастроэнтерол.2015 декабрь; 21 (48): 13403–10.
- Холт Б.А., Варадараджулу С. Эндоскопическое лечение псевдокист поджелудочной железы (с видео). Gastrointest Endosc. 2015 Апрель; 81 (4): 804–12.
- Зерем Э., Хаузер Г., Лога-Зец С., Куносич С., Йованович П., Црнкич Д.Малоинвазивное лечение псевдокист поджелудочной железы. Мир Дж. Гастроэнтерол. 2015 июн; 21 (22): 6850–60.
- Вронски М., Цебульский В., Павловский В., Краснодембски И.В., Слодковски М. Некроз за стеной: безопасность бдительного ожидания. Dig Dis Sci. 2015 Апрель; 60 (4): 1081–6.
- Баккер О.Дж., ван Сантвоорт Х., Бесселинк М.Г., Бурмеестер М.А., ван Эйк К., Деджонг К. и др.; Голландская исследовательская группа по панкреатиту. Экстрапанкреатический некроз без паренхиматозного некроза поджелудочной железы: отдельное явление при некротизирующем панкреатите? Кишечник. 2013 Октябрь; 62 (10): 1475–80.
- Rana SS, Bhasin DK, Sharma RK, Kathiresan J, Gupta R. Определяют ли морфологические особенности панкреонекроза без стенок при эндоскопическом УЗИ исход эндоскопического трансмурального дренажа? Эндоскопическое УЗИ.2014 Апрель; 3 (2): 118–22.
- Папахристоу Г.И., Такахаши Н., Чахал П., Сарр М.Г., барон Т.Х. Пероральный эндоскопический дренаж / санация стенок панкреонекроза. Ann Surg. 2007 июнь; 245 (6): 943–51.
- Гарг П.К., Шарма М., Мадан К., Сахни П., Банерджи Д., Гойал Р.Первичное консервативное лечение приводит к летальности, сравнимой с хирургической у пациентов с инфицированным панкреонекрозом. Clin Gastroenterol Hepatol. 2010 декабрь; 8 (12): 1089–1094.e2.
- Мули В.П., Шринивас В., Гарг П.К. Эффективность консервативного лечения инфицированного панкреонекроза без некрозэктомии: систематический обзор и метаанализ.Гастроэнтерология. 2013 февраль; 144 (2): 333–340.e2.
- Фернандес-дель Кастильо С., Раттнер Д.В., Макари М.А., Мостафави А., МакГрат Д., Уоршоу А.Л. Дебридмент и закрытая упаковка для лечения некротического панкреатита. Ann Surg. 1998 ноябрь; 228 (5): 676–84.
- Варадараджулу С., Банг Дж. Й., Саттон Б. С., Тревино Дж. М., Кристейн Дж. Д., Уилкокс С. М..Равная эффективность эндоскопической и хирургической цистогастростомии для дренирования псевдокисты поджелудочной железы в рандомизированном исследовании. Гастроэнтерология. 2013 сентябрь; 145 (3): 583–90.e1.
- Редван А.А., Хамад М.А., Омар М.А. Дилемма псевдокисты поджелудочной железы: совокупный многоцентровый опыт управления с использованием эндоскопии, лапароскопии и открытой хирургии.J Laparoendosc Adv Surg Tech A. 2017 Октябрь; 27 (10): 1022–30.
- Мелман Л., Азар Р., Беддов К., Брант Л. М., Халпин В. Дж., Игон Дж. К. и др. Первичные и общие показатели успешности клинических исходов после лапароскопической, эндоскопической и открытой панкреатической цистгастростомии по поводу псевдокист поджелудочной железы.Surg Endosc. 2009 Февраль; 23 (2): 267–71.
- Пак Д.Х., Ли С.С., Мун С.Х., Чхве С.И., Юнг С.В., Со Д.В. и др. Сравнение эндоскопического дренажа под контролем УЗИ с традиционным трансмуральным дренированием псевдокист поджелудочной железы: проспективное рандомизированное исследование. Эндоскопия. Октябрь 2009 г.; 41 (10): 842–8.
- Varadarajulu S, Lopes TL, Wilcox CM, Drelichman ER, Kilgore ML, Christein JD.EUS по сравнению с хирургической кистой-гастростомией для лечения псевдокист поджелудочной железы. Gastrointest Endosc. Октябрь 2008 г., 68 (4): 649–55.
- Varadarajulu S, Christein JD, Tamhane A, Drelichman ER, Wilcox CM. Проспективное рандомизированное исследование по сравнению EUS и EGD для трансмурального дренирования псевдокист поджелудочной железы (с видео).Gastrointest Endosc. 2008 декабрь; 68 (6): 1102–11.
- Kahaleh M, Shami VM, Conaway MR, Tokar J, Rockoff T, De La Rue SA и др. Эндоскопический ультразвуковой дренаж псевдокисты поджелудочной железы: перспективное сравнение с традиционным эндоскопическим дренированием. Эндоскопия. 2006 Апрель; 38 (4): 355–9.
- Мортон Дж. М., Браун А., Галанко Дж. А., Нортон Дж. А., Гримм И. С., Бернс К. Э.. Национальное сравнение хирургического и чрескожного дренирования псевдокист поджелудочной железы: 1997-2001 гг. J Gastrointest Surg. 2005 Янв; 9 (1): 15–20.
- Heider R, Meyer AA, Galanko JA, Behrns KE.Чрескожное дренирование псевдокист поджелудочной железы связано с более высокой частотой неудач, чем хирургическое лечение у неотобранных пациентов. Ann Surg. 1999 июнь; 229 (6): 781–7.
- Адамс ДБ, Андерсон М.С. Чрескожный катетерный дренаж по сравнению с внутренним дренажом при лечении псевдокисты поджелудочной железы.Ann Surg. 1992 июн; 215 (6): 571–6.
- Lang EK, Paolini RM, Pottmeyer A. Эффективность паллиативного и окончательного чрескожного дренирования абсцессов и псевдокист поджелудочной железы по сравнению с хирургическим дренированием: проспективное исследование с участием 85 пациентов. South Med J. 1991, январь; 84 (1): 55–64.
- Тревино Дж. М., Тамхане А., Варадараджулу С.Успешное стентирование при разрыве протока благоприятно влияет на результаты лечения пациентов, которым проводится трансмуральный дренаж скоплений перипанкреатической жидкости. J Gastroenterol Hepatol. 2010 Март; 25 (3): 526–31.
- Ян Д., Амин С., Гонсалес С., Муллади Д., Хасак С., Гаддам С. и др.Транспапиллярный дренаж не дает дополнительных преимуществ для результатов лечения у пациентов, перенесших трансмуральный дренаж псевдокист поджелудочной железы под контролем EUS: большое многоцентровое исследование. Gastrointest Endosc. 2016 Апрель; 83 (4): 720–9.
- van Santvoort HC, Besselink MG, Bakker OJ, Hofker HS, Boermeester MA, Dejong CH, et al.; Голландская исследовательская группа по панкреатиту. Пошаговый подход или открытая некрэктомия при некротическом панкреатите. N Engl J Med. 2010 апр; 362 (16): 1491–502.
- Гурусами К.С., Белгаумкар А.П., Хасвелл А., Перейра С.П., Дэвидсон Б.Р. Вмешательства при некротизирующем панкреатите. Кокрановская база данных Syst Rev.2016 Апрель; 4: CD011383.
- Баккер О.Дж., ван Сантвоорт Х.С., ван Бруншот С., Гескус Р.Б., Бесселинк М.Г., Боллен Т.Л. и др .; Голландская исследовательская группа по панкреатиту. Сравнение эндоскопической трансгастральной некрэктомии при инфицированном некротизирующем панкреатите: рандомизированное исследование. ДЖАМА. 2012 Март; 307 (10): 1053–61.
- van Brunschot S, van Grinsven J, van Santvoort HC, Bakker OJ, Besselink MG, Boermeester MA и др .; Голландская исследовательская группа по панкреатиту. Эндоскопический или хирургический подход к лечению инфицированного некротического панкреатита: многоцентровое рандомизированное исследование. Ланцет. 2018, январь; 391 (10115): 51–8.
- ван Баал М.С., ван Сантвоорт Х.С., Боллен Т.Л., Баккер О.Дж., Бесселинк М.Г., Гуззен Х.Г. Голландская исследовательская группа по панкреатиту. Систематический обзор чрескожного катетерного дренирования как основного лечения некротического панкреатита. Br J Surg. 2011 Янв; 98 (1): 18–27.
- Шенви С., Гупта Р., Канг М., Кхуллар М., Рана С.С., Сингх Р. и др.Сроки хирургического вмешательства у пациентов с инфицированным некротическим панкреатитом, не отвечающих на чрескожный катетерный дренаж. Панкреатология. 2016 сентябрь-октябрь; 16 (5): 778–87.
- ван Гринсвен Дж., Тиммерман П., ван Лиенден К.П., Хавеман Дж. В., Бурма Д., ван Эйк С.Х. и др .; Голландская исследовательская группа по панкреатиту.Превентивное и стандартное чрескожное катетерное дренирование при инфицированном некротизирующем панкреатите. Поджелудочная железа. 2017 Апрель; 46 (4): 518–23.
- Картер CR, Маккей CJ, Имри CW. Чрескожная некрэктомия и эндоскопия синусового тракта в лечении инфицированного панкреонекроза: первый опыт.Ann Surg. 2000, август; 232 (2): 175–80.
- Хорват К.Д., Као Л.С., Верри К.Л., Пеллегрини, Калифорния, Синанан Миннесота. Методика лапароскопического чрескожного дренирования инфицированных панкреонекроза и абсцесса поджелудочной железы. Surg Endosc. 2001 Октябрь; 15 (10): 1221–5.
- van Brunschot S, Hollemans RA, Bakker OJ, Besselink MG, Baron TH, Beger HG и др.Минимально инвазивная и эндоскопическая некрэктомия по сравнению с открытой некротизирующим панкреатитом: объединенный анализ индивидуальных данных для 1980 пациентов. Кишечник. 2018 Апрель; 67 (4): 697–706.
- Arvanitakis M, Dumonceau JM, Albert J, Badaoui A, Bali MA, Barthet M, et al. Эндоскопическое лечение острого некротического панкреатита: мультидисциплинарные руководящие принципы Европейского общества гастроинтестинальной эндоскопии (ESGE), основанные на фактических данных.Эндоскопия. 2018 Май; 50 (5): 524–46.
- Varadarajulu S, Phadnis MA, Christein JD, Wilcox CM. Техника множественных транслюминальных ворот для дренирования симптоматического стенозированного панкреонекроза под контролем EUS. Gastrointest Endosc. Июль 2011 г .; 74 (1): 74–80.
- Анг Т.Л., Квек А.Б., Тан СС, Ибрагим С., Фок К.М., Тео Е.К.Прямая эндоскопическая некрэктомия: минимально инвазивный эндоскопический метод лечения инфицированных стенок панкреонекроза и инфицированных псевдокист с твердым мусором. Singapore Med J. 2013, апрель; 54 (4): 206–11.
- Глюк М., Росс А., Ирани С., Лин О, Ган С.И., Фотоохи М. и др.Двойной метод дренирования при симптоматическом панкреонекрозе со стенками сокращает продолжительность госпитализации, проведения радиологических процедур и количества эндоскопий по сравнению со стандартным чрескожным дренированием. J Gastrointest Surg. 2012 февраль; 16 (2): 248–56.
- van Brunschot S, Fockens P, Bakker OJ, Besselink MG, Voermans RP, Poley JW, et al.Эндоскопическая транслюминальная некрэктомия при некротизирующем панкреатите: систематический обзор. Surg Endosc. 2014 Май; 28 (5): 1425–38.
Автор Контакты
Марк Г. Бесселинк
Отделение хирургии, Амстердам Гастроэнтерология и метаболизм
Амстердам UMC, Амстердамский университет
Meibergdreef 9, NL – 1105 AZ Амстердам (Нидерланды)
E-Mail [email protected]
Подробности статьи / публикации
Предварительный просмотр первой страницы
Поступила: 1 марта 2019 г.
Дата принятия: 15 марта 2019 г.
Опубликована онлайн: 2 апреля 2019 г.
Дата выпуска: апрель 2019 г.
Количество страниц для печати: 7
Количество рисунков: 3
Количество столов: 0
ISSN: 2297-4725 (печатный)
eISSN: 2297-475X (онлайн)
Для дополнительной информации: https: // www.karger.com/VIS
Лицензия открытого доступа / Дозировка лекарства / Отказ от ответственности
Эта статья находится под международной лицензией Creative Commons Attribution-NonCommercial 4.0 (CC BY-NC). Для использования и распространения в коммерческих целях требуется письменное разрешение. Дозировка лекарств: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор и дозировка лекарств, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации.Однако с учетом продолжающихся исследований, изменений в правительственных постановлениях и постоянного потока информации, касающейся лекарственной терапии и реакций на них, читателю рекомендуется проверять листок-вкладыш для каждого препарата на предмет любых изменений показаний и дозировки, а также дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендованным агентом является новое и / или редко применяемое лекарство. Отказ от ответственности: утверждения, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и соавторам, а не издателям и редакторам.Появление в публикации рекламы и / или ссылок на продукты не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности.


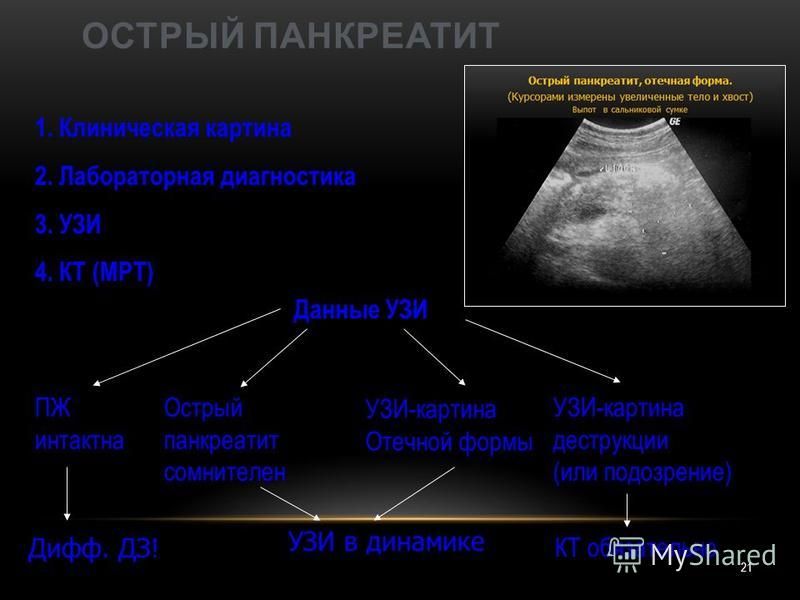
 Е. Волков, С.В. Волков // Изд-во Чуваш. ун-та. 2009. ‒ 240 с.
Е. Волков, С.В. Волков // Изд-во Чуваш. ун-та. 2009. ‒ 240 с.