13С уреазный дыхательный тест на хеликобактер пилори: 13С-уреазный дыхательный тест на Helicobacter pylori
13С-уреазный дыхательный тест (13С-УДТ, 13C-Urea Breath test, UBT). Выявление инфекции Helicobacter pylori
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, и приводимая ниже информация носит исключительно справочный характер.
13С-уреазный дыхательный тест: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.Синонимы: 13C-Urea Breath test, UBT; 13С-уреазный дыхательный тест, дыхательный тест с 13С-меченной мочевиной, 13С-УДТ.
Показания для назначения исследования
13С-уреазный дыхательный тест – лабораторный метод диагностики хеликобактериоза (инфекционного заболевания, вызванного бактерией Helicobacter pylori

Этот неинвазивный высокочувствительный и высокоспецифичный тест рекомендуется использовать в целях диагностики Helicobacter pylori, а также подтверждения ее эрадикации (уничтожения) по истечении четырех недель после окончания терапии.
Противопоказания к проведению исследования
13С-уреазный дыхательный тест не проводят людям, у которых были операции на желудке, поскольку результат исследования может быть ложноположительным.
13С-уреазный дыхательный тест имеет возрастные ограничения – его применяют только для пациентов старше 12 лет.
Безопасность проведения 13С-уреазного дыхательного теста во время беременности и в период лактации не исследовалась.
Подготовка к процедуре
- Тест необходимо проводить утром натощак или не ранее, чем через 6 часов после легкого приема пищи; воду в небольшом количестве пить можно.
- Накануне следует избегать пищевых перегрузок.
- Тест можно проводить не ранее, чем через четыре недели после окончания приема антибиотиков, препаратов висмута или сукральфата.

- После окончания приема ингибиторов протонной помпы (препаратов, снижающих образование соляной кислоты в желудке) должно пройти не менее двух недель.
- После приема 13С изотопных растворов должно пройти не менее 24 часов.
- Не следует проводить тест в один и тот же день с эндоскопическим исследованием (гастроскопией) желудка и 12-перстной кишки с биопсией.
- Рекомендуется исключить прием антацидов и блокаторов Н2-гистаминовых рецепторов за 1-2 дня до исследования.
- Исключить физические и эмоциональные перегрузки накануне исследования.
- В течение 1 часа до исследования не следует курить.
- Исключить прием алкоголя накануне исследования.
Как проходит процедура 13С-уреазный дыхательный тест
- Перед началом проведения теста пациенту предлагают выпить 200 мл апельсинового сока (в случае аллергии на апельсины можно использовать яблочный сок).
- Через 5 минут после приема кислого напитка проводится сбор выдыхаемого воздуха в специальный контейнер.

- Содержимое флакона с 13С-мочевиной растворяют в 50 мл воды (выполняется медицинским персоналом), и пациент выпивает приготовленный раствор.
- В течение 30 минут пациенту необходимо находится в спокойном состоянии, ожидая в медицинском офисе.
- Строго через 30 минут после приема раствора проводят сбор выдыхаемого воздуха во второй контейнер.
Срок исполнения
До 5 рабочих дней (указанный срок не включает день взятия биоматериала).
Что может повлиять на результаты
К ложноположительному результату (когда тест показывает, что бактерия Helicobacter pylori присутствует, а на самом деле ее нет) могут привести следующие причины:
- ахлоргидрия – атрофия слизистой оболочки желудка;
- присутствие других спиралевидных желудочных бактерий с уреазной активностью;
- нарушение правил подготовки к исследованию и процедуры проведения (в т.ч. выполнение теста вскоре после эзофагогастродуоденоскопии, повторное проведение дыхательного теста в тот же день).

- использование антибиотиков, ингибиторов протонной помпы, препаратов висмута в течение предшествующих 2 недель;
- проведение дыхательного теста ранее, чем через 4 недели после окончания терапии, направленной на эрадикацию (уничтожение)
- нарушение процедуры (проведение сбора пробы слишком рано или слишком поздно после приема тестового раствора, взятие второй пробы при неглубоком выдохе).
13С-уреазный дыхательный тест
Сдать 13С-уреазный дыхательный тест можно в ближайшем медицинском офисе ИНВИТРО. Список офисов, где принимается биоматериал для лабораторного исследования, представлен в разделе «Адреса». Референсные значения 13С-уреазного дыхательного теста представлены в таблице.Единицы измерения: DOB, ‰. При проведении 13С-уреазного дыхательного теста с применением 13С-мочевины измеряемым показателем является относительная разница между отношением 13С/12С в пробах выдыхаемого воздуха до и после приема раствора препарата (обозначается как DOB – Delta over Baseline, измеряется в промилле (‰)).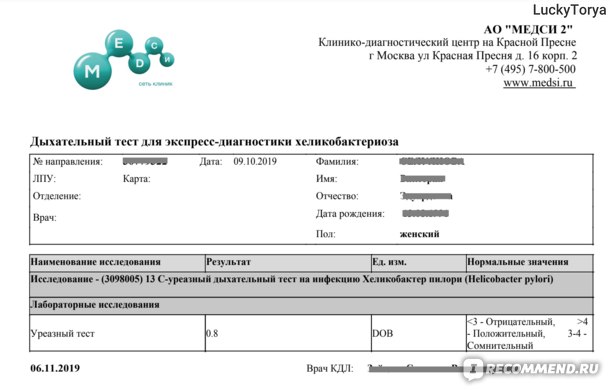
| DOB, ‰ | Результат | пояснение |
| < 3,0 | отрицательный | отсутствие Helicobacter pylori |
| 3,0-4,5 | сомнительный | рекомендуется проведение любого альтернативного дополнительного теста |
| > 4,5 | положительный | наличие Helicobacter pylori |
Положительный результат с высокой вероятностью говорит об инфицировании Helicobacter pylori, отрицательный – об отсутствии инфицирования. При получении промежуточных значений от 3,0 до 4,5 ‰ рекомендуется проведение любого альтернативного дополнительного теста, направленного на выявление

Helicobacter pylori (H. pylori) – это короткие, извитые S-образные бактерии средних размеров, подвижные, имеющие 4-5 жгутиков.
Бактерии Helicobacter pylori
H. pylori играют существенную роль в развитии острого и хронического гастритов, язвенной болезни желудка и 12-перстной кишки. Кроме того, инфицирование H. pylori является предрасполагающим фактором развития рака желудка и лимфоцитарной опухоли желудочно-кишечного тракта (мальтомы).
Постоянное присутствие H. pylori в желудке определяется рядом уникальных свойств этой бактерии, обеспечивающих ее приспособление к среде хозяина в сочетании с относительной «недосягаемостью» для иммунной системы человека.
Спиралевидная форма и наличие жгутиков позволяют бактерии, подобно штопору, ввинчиваться в слой желудочной слизи и прилепляться к эпителиальным клеткам желудка. Основным фактором, обеспечивающим выживание H. pylori в кислой среде желудка, является бактериальный фермент – уреаза, обладающий специфическим свойством – при взаимодействии с водой расщеплять мочевину с образованием диоксида углерода и аммиака. Аммиак нейтрализует ионы водорода и обеспечивает бактерии локальное поддержание комфортного для нее pH.
Аммиак нейтрализует ионы водорода и обеспечивает бактерии локальное поддержание комфортного для нее pH.
Именно это свойство Н. pylori лежит в основе 13С-уреазного дыхательного теста. Пациенту предлагают сделать выдох в специальную емкость, которую закупоривают. В этой пробе определят базовое содержание 13С (углерода 13) и 12С (углерода 12). Затем пациент выпивает специальный раствор, в котором содержится мочевина с углеродом 13С (он нерадиоактивен и безопасен). Если в желудке есть H. pylori, то бактерия расщепляет мочевину, и углерод
Источники:
- Tsachi Tsadok Perets, Rachel Gingold-Belfer et al. Optimization of 13C-urea breath test threshold levels for the detection of Helicobacter pylori infection in a national referral laboratory.
 J Clin Lab Anal. 2019;33:e22674.
J Clin Lab Anal. 2019;33:e22674. - Malfertheiner P, Megraud F, O’Morain CA, et al. Management of Helicobacter pylori infection-the Maastricht V/Florence consensus report. Gut. 2017;66:6‐30.
- Li Z‐X, Huang L‐L, Liu C, et al. Cut‐off optimization for 13C‐urea breath test in a community‐based trial by mathematic, histology and serology approach. Sci Rep. 2017;7:2072.
- Athanasios Makristathis, Alexander M. Hirschl, Francis Mégraud, Emilie Bessède, Review: Diagnosis of Helicobacter pylori infection, Helicobacter, 10.1111/hel.12641, 24, S1, (2019).
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Информация проверена экспертом
Лишова Екатерина Александровна
Высшее медицинское образование, опыт работы – 19 лет
Дыхательный тест на Хеликобактер, онлайн-запись на процедуру – сеть клиник МЕДСИ
Перед началом тестирования пациенту стоит принять 100-200 мл сока (апельсиновый, яблочный) или разведенной лимонной кислоты в качестве адъюванта.
Через 5-10 мин после приема сока проводится сбор выдыхаемого воздуха для базового замера соотношения 13СО2/12СО2 в выдохе. В этих целях пациент осуществляет выдох в пакет №1 с синей крышкой. Чтобы результаты были наиболее точными, пациент должен как можно больше выдохнуть последнюю (альвеолярную) часть воздуха. После процедуры пакет герметично закрывают крышкой.
Внимание! Перед открытием флакона с реагентом его необходимо ориентировать крышкой вверх, затем встряхнуть для полного перемешивания реагента, после чего осторожно вскрыть фиксатор и открыть крышку флакона.
Содержимое флакона растворяют в 50 мл дистиллированной воды (возможно использовать кипяченую или минеральную воду). Затем пациент выпивает его содержимое, объем которого зависит от возраста больного:
- Взрослые – весь флакон (50 мл)
- Дети в возрасте 5-12 лет – полфлакона (25 мл)
Помните! Приготовленный препарат должен быть использован в течение 5 минут после вскрытия флакона и разведения водой.
В течение 30 минут после приема препарата пациент должен находиться в спокойном состоянии, поскольку выделяемый при физической нагрузке СО2 оказывает негативное влияние на результат теста.
Через 30 минут после приема препарата больной должен сделать выдох в пакет № 2 с красной крышкой. Для обеспечения точности теста пациент должен в максимальном объеме выдохнуть последнюю (альвеолярную) часть воздуха. После выдоха пакет герметично закрывается крышкой.
13С-уреазный дыхательный тест на хеликобактер пилори (helicobacter pylori)
13С уреазный дыхательный тест на хеликобактер – наиболее доступный и простой метод контроля эффективности проведенного лечения инфекции Helicobacter pylori.
Преимущества дыхательного 13С уреазного теста на helicobacter pylori
- Неинвазивность (не требует проведения гастроскопии)
- Простота и безопасность
- Высокая чувствительность, специфичность и точность (95-100%)
Подготовка к исследованию
- Тест проводится не ранее чем через 1-1,5 месяца после завершения эрадикации хеликобактер пилори.

- За 4 недели до исследования нельзя принимать антибиотики, сукралфат (вентер) и препараты висмута (денол, улькавис).
- За 2 недели до исследования необходимо отменить лекарства, блокирующие продукцию соляной кислоты (нольпаза, омез, лосек, контролок, париет, нексиум, ранитидин и др.).
- 13С уреазный тест выполняется утром на голодный желудок или спустя 8 часов после лёгкого завтрака.
- Если дыхательному тесту предшествовала эзофагогастроскопия (ЭГДС) или значительная физическая нагрузка, то после их завершения должно пройти не менее 24 часов.
- Для проведения дыхательного 13С уреазного теста на хеликобактер пилори необходимо иметь с собой 200 мл апельсинового или грейпфрутового сока.
Проведение уреазного дыхательного теста С13 на хеликобактер пилори
Во время теста исследуются образцы выдыхаемого пациентом воздуха до и после приёма специального препарата. При наличии бактерии Helicobacter pylori, изменяется химический состав выдыхаемого воздуха, что определяется данным тестом.
Если Вы задумались, где сделать дыхательный уреазный тест на хеликобактер в Москве, обращайтесь в Клинический госпиталь на Яузе. Цену исследования можно узнать по телефону, указанному на сайте.
13С-уреазный дыхательный тест на Хеликобактер пилори
13С-уреазный дыхательный тест на Хеликобактер пилори
Хеликобактер пилори может привести к гастриту, язвенной болезни и раку желудка!
13С-уреазный дыхательный тест относится к неинвазивным безопасным методам исследования, обеспечивающим высокую чувствительность, специфичность и точность.
13С-уреазный дыхательный тест – признанное гастроэнтерологами всего мира достоверное исследование для диагностики инфекции Helicobacter pylori.
Почему необходимо провериться на наличие Хеликобактера пилори?
Бактерии Helicobacter pylori практически во всех случаях приводят к хроническому гастриту, реже – к язвенной болезни или раку желудка.
Helicobacter pylori распространена повсеместно – сегодня ей заражен каждый второй житель Земли, причем подавляющее большинство — с самого детства.
Бактерия передается контактно-бытовым путем: через загрязненную воду, продукты, общую посуду, при недостаточном уровне гигиены. Инфекция быстро распространяется внутри семьи.
Преимущества 13С-уреазного дыхательного теста:
- Безболезненность и отсутствие неприятных ощущений: не нужно проводить гастроскопию и сдавать кровь.
- Достоверность: специфичность – до 93 – 100%, чувствительность – до 97 – 100%, общая точность – 94,8 % – 100%**
- Возможность одновременного тестирования всей семьи старше 14 лет.
- Применение как для первичной диагностики инфекции Helicobacter pylori, так и для контроля лечения.
- Возможность повторять тестирование после терапии.
- Простота исследования и быстрый результат (тест выполняется в течение 30 минут, результаты можно получить в течение 3 рабочих дней, не считая день взятия биоматериала.
Показания
- диагностика Н. pylori инфекции у лиц старше 14 лет;
- контроль лечения (подтверждение эрадикации H.
 pylori инфекции) по истечении четырех недель после завершения терапии.
pylori инфекции) по истечении четырех недель после завершения терапии.
Противопоказания и ограничения: абсолютных противопоказаний к применению 13С-УДТ нет. Побочных эффектов не обнаружено. Дыхательный тест в текущей модификации предназначен для лиц старше 14 лет. Пациентам, перенесшим резекцию желудка, целесообразно применять другие методы исследования на хеликобактериоз. Безопасность применения теста при беременности и лактации не исследована. Ограничения теста см. также в разделе «Подготовка к проведению исследования».
Как проходит тест:
- В течение 30 минут пациент находится в медицинском офисе
- Перед исследованием медсестра предложит пациенту выпить 200 мл апельсинового или яблочного сока.
- Через 5 минут после приема напитка проводится сбор выдыхаемого воздуха в специальный контейнер.
- Сразу после сбора воздуха необходимо выпить 50 мл водного раствора карбамида.
- Строго через 30 минут проводится повторный сбор выдыхаемого воздуха.

Подготовка к тесту:
- Рекомендуется проводить тест натощак (не менее 6 часов и не более 14 часов после последнего приема пищи, питье – вода в небольшом количестве), накануне избегать пищевых перегрузок.
- Желательно за 72 часа исключить употребление алкогольных напитков.
- За 1 час исключить курение.
- Исключить физические и эмоциональные перегрузки накануне исследования.
- После окончания курса эрадикационной, антибактериальной терапии, приема препаратов висмута или сукральфата должно пройти не менее четырех недель.
- После окончания приема ингибиторов протонной помпы (ИПП) должно пройти не менее двух недель.
- После приема 13С-изотопных растворов должно пройти не менее 24 часов.
- Не следует проводить тест после проведения эндоскопического исследования желудка и 12-перстной кишки с биопсией в тот же день.
- За 7 дней до проведения теста необходимо исключить из пищевого рациона кукурузу
Дыхательный тест проводится с понедельника по пятницу с 8:00 до 9:00.

хеликобактер
23 марта 2018 г.
Просмотры: 3609
13С – уреазный дыхательный тест
Helicobacter pylori – бактерия, которой заражаются еще в детском возрасте. Микроб живет в слизистой оболочке желудка, желудочной слизи и вызывает развитие хронического гастрита, язвенной болезни желудка и двенадцатиперстной кишки. Длительное инфицирование Helicobacter pylori многократно повышает риск развития рака желудка. Опасность для инфицированного заключается в возможном бессимптомном носительстве микроба и выявлении инфекции уже на стадии развития осложнений (от гастрита и язвы до рака желудка).
Эксперты Всемирной Организации Здравоохранения признали микроорганизм Helicobacter pylori абсолютно доказанным канцерогеном 1 класса. Стратегия «тестируй на Helicobacter pylori и лечи» признана наиболее эффективной мерой профилактики некардиального рака желудка, лечения язвенной болезни и гастрита.
Для диагностики инфекции Нelicobacter pylori и контроля за уничтожением (оценке эффективности лечения) во всех странах мира используется стандартизованный, рекомендованный российскими, европейским, американскими и азиатскими экспертами неинвазивный (без гастроскопии и биопсии слизистой желудка) 13C-дыхательный тест с 13C меченой мочевиной. Это единственный неинвазивный тест, позволяющий количественно определять степень инфицированности.
Тест обладает самой высокой чувствительностью и специфичностью (по сравнению с другими методами диагностики хеликобактерной инфекции). Тест безопасен и может проводиться как взрослым, так и детям.
Пациент принимает препарат, содержащий 13C меченую мочевину. В течение 30 минут собираются пробы выдыхаемого воздуха в специальные фольгированные мешки объемом 100 мл в которых измеряется изотопный состав углерода при помощи медицинского высокоточного немецкого инфракрасного анализатора. При наличии в желудке обследуемого Нelicobacter pylori мочевина подвергается изменениям с выделением меченого 13C углекислого газа, который регистрируется в выдыхаемом воздухе .
Человек инфицирован бактерией хеликобактер пилори, если в выдыхаемом воздухе после приема субстрата, повышается содержание метки выше контрольного уровня. При отсутствии Нelicobacter pylori этого не происходит.
13C-дыхательный тест может использоваться как для первичной диагностики Нelicobacter pylori, так и для оценки эффективности эрадикации.
РЕЗУЛЬТАТ В ДЕНЬ ТЕСТИРОВАНИЯ!
ВАЖНО: при выявлении инфекции у пациента, важно обследовать всех членов семьи, учитывая возможность внутрисемейной передачи инфекции.
ПОДГОТОВКА К ИССЛЕДОВАНИЮ : Пациенту необходимо
–не принимать пищу за 2 часа до проведения теста,
–отменить за 2 дня прием лекарств, снижающих секрецию кислоты в желудке (ингибиторов протонной помпы (омепразол, пантопразол, рабепразол, эзомепразол, лансопразол),
-отменить и Н2-блокаторов (циметидин, ранитидин, фамотидин),
–отменить антибиотики и препараты висмута (Де-нол)
–контроль эффективности лечения Helicobacter pylori (эрадикационной терапии) стоит проводить не ранее, чем через 4 недели после его окончания
Уничтожение бактерии приводит к излечению от гастрита и способствует ремиссии язвенной болезни.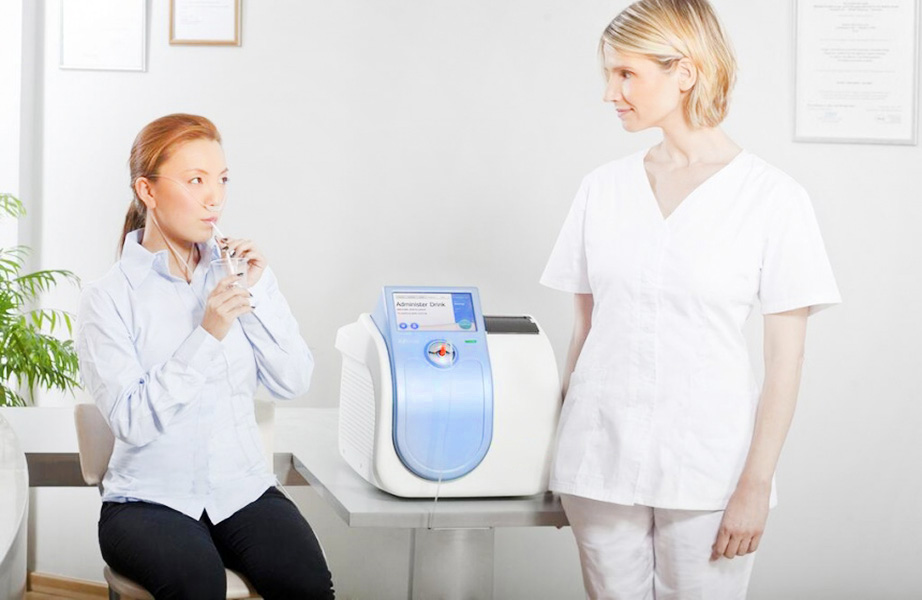 Для лечения применяют комплексные схемы с антибиотиками и антисекреторными препаратами.
Для лечения применяют комплексные схемы с антибиотиками и антисекреторными препаратами.
В клинике наши специалисты подберут для Вас схему лечения с учетом индивидуальных особенностей течения инфекции.
13С-уреазный дыхательный тест на определение Helicobacter pylori
13С-уреазный дыхательный тест на определение Helicobacter pylori – методика лабораторной диагностики инфекции, вызванной Helicobacter pylori, основанная на анализе в пробах выдыхаемого воздуха специального реагента, содержание которого изменяется под действием выделяемого бактерией фермента уреазы.
Helicobacter pylori – грамотрицательная бактерия спиралевидной формы, которая обнаруживается в различных областях желудка и двенадцатиперстной кишки человека.
Helicobacter pylori способна выживать в агрессивной кислой среде желудка, в том числе из-за интенсивной продукции специального фермента – уреазы. Уреаза расщепляет мочевину с образованием аммиака, который нейтрализует соляную кислоту желудочного сока и таким образом обеспечивает поддержание комфортного для бактерии уровня кислотности (рН).
Описание:
Среди диагностических методик определения инфицированности Helicobacter pylori в последнее время всё чаще применяется уреазный дыхательный тест. Это неинвазивное исследование (то есть без фиброгастроскопии и биопсии слизистой желудка), основанное на способности бактерии секретировать уреазу. Основным реагентом в данном тесте является 13С-мочевина, в которой 12С-атом углерода заменён на 13С-изотоп. При наличии в желудке Helicobacter pylori продуцируемая бактерией уреаза расщепляет поступившую в желудок с тестовым раствором 13С-мочевину на аммиак и 13С-углекислый газ, который затем всасывается в кровь, попадает в лёгкие и выводится с выдыхаемым воздухом.
Непосредственно перед исследованием пациенту необходимо выпить 200 мл апельсинового или грейпфрутового сока, чтобы замедлить эвакуацию из желудка. Через 5-10 минут производится взятие контрольной пробы воздуха – пациент делает выдох в специальный герметичный пакет, который затем закрывается и маркируется соответствующим образом.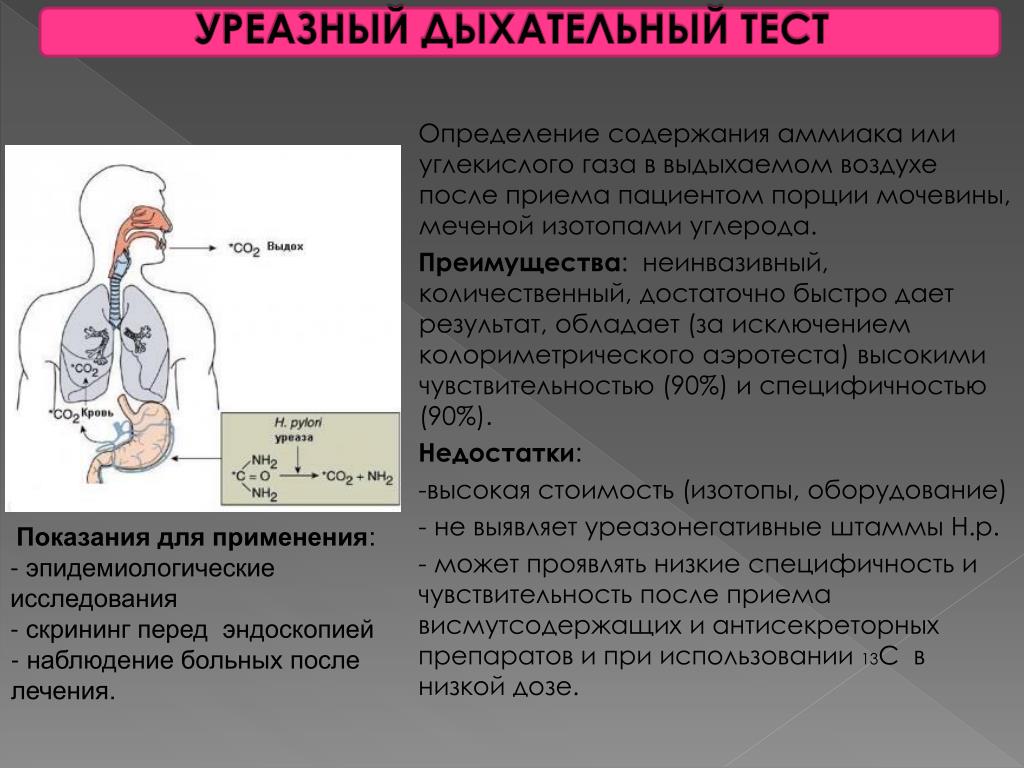 Для обеспечения точности теста особенно важно выдыхать последнюю (альвеолярную) часть воздуха. Затем пациенту дают выпить 50 мл раствора мочевины, меченной изотопом углерода 13С. Это раствор без вкуса и запаха, его прием не сопровождается никакими неприятными ощущениями. Раствор готовится непосредственно перед приемом, его необходимо выпить в течение пяти минут после приготовления. Взрослые выпивают приготовленный раствор полностью (50 мл), а дети от 5 до 12 лет – половину. Затем в течение получаса следует находиться в спокойном состоянии, чтобы на результаты исследования не повлиял углекислый газ, выделяющийся при физической нагрузке. Через 30 минут производится взятие второй пробы воздуха, пакет с которой также герметично закрывается и маркируется. Затем пробы воздуха анализируют на инфракрасном спектрометре для определения изотопного соотношения 13С/12С. Если пациент инфицирован Helicobacter pylori, то во второй пробе воздуха появится увеличенное количество 13 СО2 по сравнению с его содержанием в первой (контрольной) пробе.
Для обеспечения точности теста особенно важно выдыхать последнюю (альвеолярную) часть воздуха. Затем пациенту дают выпить 50 мл раствора мочевины, меченной изотопом углерода 13С. Это раствор без вкуса и запаха, его прием не сопровождается никакими неприятными ощущениями. Раствор готовится непосредственно перед приемом, его необходимо выпить в течение пяти минут после приготовления. Взрослые выпивают приготовленный раствор полностью (50 мл), а дети от 5 до 12 лет – половину. Затем в течение получаса следует находиться в спокойном состоянии, чтобы на результаты исследования не повлиял углекислый газ, выделяющийся при физической нагрузке. Через 30 минут производится взятие второй пробы воздуха, пакет с которой также герметично закрывается и маркируется. Затем пробы воздуха анализируют на инфракрасном спектрометре для определения изотопного соотношения 13С/12С. Если пациент инфицирован Helicobacter pylori, то во второй пробе воздуха появится увеличенное количество 13 СО2 по сравнению с его содержанием в первой (контрольной) пробе.
Подготовка:
Исключить из рациона алкоголь в течение 72 часов до исследования.
Не принимать пищу в течение 6 часов до исследования, можно пить чистую негазированную воду.
Исследование проводится не ранее чем через 6 недель после окончания последнего приема антибиотиков (по любому поводу) и препаратов висмута.
За две недели до проведения исследования необходимо прекратить (по согласованию с врачом) прием ингибиторов протонной помпы (омепразол, рабепразол, лансопразол, эзомепразол, пантопразол) и блокаторов гистаминовых рецепторов второго типа (ранитидин, фамотидин, низатидин, роксатидин).
Исследование проводится не менее чем через сутки после выполнения фиброгастроскопии (ФГДС) или до её проведения.
Литература
Гастроэнтерология: национальное руководство. Под ред. В. Т. Ивашкина, Т. Л. Лапиной. – М. : ГЭОТАР-Медиа, 2008. С. 432.
Коварный и опасный. Врач – о том, как распознать гастрит
|
В советское время диагноз «гастрит» ставили весьма часто. |
«Не спешите сами себе ставить диагноз»
«Гастрит – это воспалительное заболевание слизистой оболочки желудка. Симптомами могут быть боли в верхних отделах живота, возникающие во время или сразу после приёма пищи. Также может возникать ощущение переполнения, тяжести в желудке, тошнота, налёт на языке, снижение аппетита», – рассказывает врач.
Гастрит: «гастр» – желудок; «ит» – воспаление. Чтобы установить диагноз, обязательно нужно провести гастроскопию с биопсией. И обнаружить воспалительные клетки или признаки атрофии (дисплазии, метаплазии) в более тяжёлых случаях.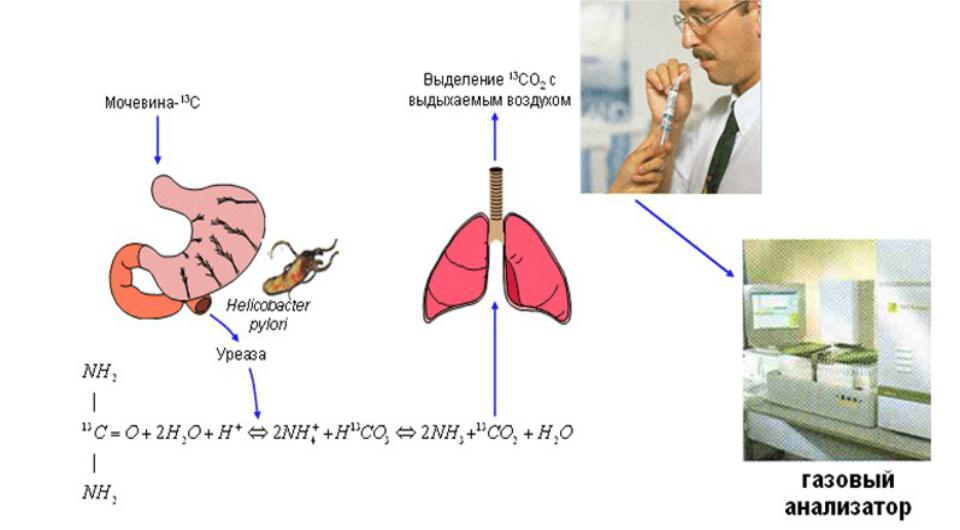
Часто у пациентов вызывает негативную реакцию само слово «биопсия», как связанное с онкологией. Но бояться не нужно. Это обычное исследование, призванное подтвердить или опровергнуть диагноз. Многие пациенты, приходя впервые на приём к гастроэнтерологу, рассказывают, что у них гастрит ещё со школьных времен. Или самостоятельно выставляют себе диагноз только на основании боли в животе.
Но в большинстве случаев гастрит при обследовании не подтвердится. До того как врач проведёт гастроскопию, диагноз будет звучать «диспепсия неуточнённая». А уже далее, если гистологически подтвердится воспаление, мы с уверенностью поставим диагноз «гастрит». Или «функциональная диспепсия», если не обнаружим никаких изменений в слизистой оболочке желудка.
Почему так важна формулировка диагноза?
Потому что в гастроэнтерологии есть такое понятие как «каскад Корреа» – длительное воспаление (хронический гастрит) – ведёт к атрофии – метаплазии – дисплазии – онкологическим заболевания желудка. Обычно на развитие этих событий уходят годы.
Обычно на развитие этих событий уходят годы.
Но теперь вы понимаете, что «гастрит» не такой безобидный диагноз. И пациент, которому установлен данный диагноз, должен находиться под наблюдением гастроэнтеролога. Поэтому мы можем только порадоваться, что «гастрит есть не у всех». И что ещё в школьные годы этот диагноз большинство получили ошибочно».
Маленькая, но очень опасная
Что же вызывает этот недуг? В преобладающем большинстве случаев болезнь возникает из-за заражения хеликобактер пилори, которая в процессе своей жизнедеятельности вызывает воспаление в слизистой оболочке желудка.
Заразиться можно через грязные руки, использование общей или недостаточно обработанной посуды, плохо обработанный эндоскоп при процедурах. Впрочем, последний путь заражения в современном мире практически нигде не встречается.
Наличие опасной бактерии в организме выявляется просто – достаточно провести 13С-уреазный дыхательный тест. Этот тест считается «золотым стандартом» в выявлении хеликобактер пилори. Также её можно определить при исследовании кала или крови или во время проведения гастроскопии.
Этот тест считается «золотым стандартом» в выявлении хеликобактер пилори. Также её можно определить при исследовании кала или крови или во время проведения гастроскопии.
«Хочу обратить внимание, что существует ещё и аммонийный дыхательный тест на хеликобактер, проводимый с помощью специального аппарата. Для медицинских клиник это экономически выгодно. Но для пациента важно знать, что метод не доказательный и часто даёт ошибочные результаты, – говорит специалист.
«Медицинский лучевой центр» на Северной, 445 – один из немногих медицинских учреждений, где проводится доказательный 13С-уреазный дыхательный тест. Наши медицинские сестры старательно, поэтапно, с соблюдением всех правил проводят данное исследование».
Что же входит в оставшиеся 10 %? Гастрит также может возникать на фоне длительного употребления медикаментов, алкоголя, курения, других бактерий, грибков, паразитов, забросов желчи в желудок и др. Самый сложный в лечении – аутоиммунный гастрит.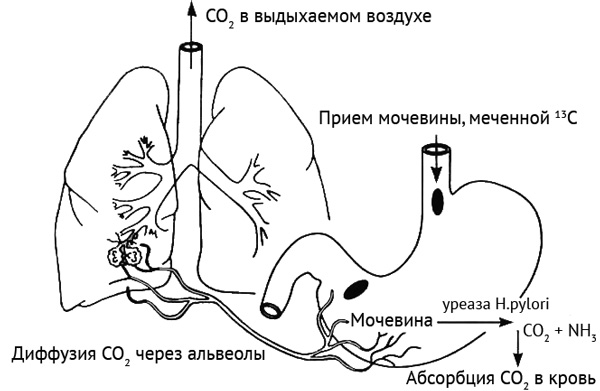 Это заболевание, при котором организм вырабатывает антитела к своим же клеткам желудка и повреждает их.
Это заболевание, при котором организм вырабатывает антитела к своим же клеткам желудка и повреждает их.
Соответственно, в зоне риска находятся те, кто пренебрегает личной гигиеной, злоупотребляет алкоголем, курением или лекарствами, неправильно питается.
На какие тревожные симптомы следует особенно обратить внимание?
Длительные, постоянные боли в верхних отделах живота. Ночные симптомы: боли, чувство переполнения, распирания в животе во сне. Необоснованное снижение массы тела. Нарушение, затруднение глотания. Повторяющаяся рвота. Повышение температуры тела. Кровь в кале или чёрный стул. Если возникают такие симптомы, визит к врачу откладывать просто опасно.
Всем лицам, достигшим возраста 50 лет, обязательно нужно пройти эзофагогастродуоденоскопию (ЭФГДС). Даже если вас ничего не беспокоит. И тем более, если вы обнаружили у себя хотя бы один из вышеперечисленных признаков.
В «МЛЦ» с первого февраля до первого апреля 2020 года действует выгодная скидка 20 % на программу «Гастроэнтерология», в которую входят:
- Первичный приём гастроэнтеролога;
- УЗИ органов брюшной полости;
- Приём гастроэнтеролога по результатам обследования.

Но, как говорят медики, всё же лучше не допустить возникновения болезни, чем лечить её потом. Соблюдайте правила личной гигиены, старайтесь правильно питаться, не употреблять слишком горячую пищу, не злоупотреблять алкоголем и лекарствами без назначения врача, не курить. А при возникновении неприятных симптомов обращайтесь к врачу.
Мазько Инна Сергеевна
Заместитель главного врача по медицинской части
Врач- гастроэнтеролог, врач-терапевт
Медицинский стаж с 2012 года
Дыхательный тест с мочевиной 13C в диагностике инфекции Helicobacter pylori
Дыхательный тест на мочевину (UBT) – один из наиболее важных неинвазивных методов выявления инфекции Helicobacter pylori. В тесте используется гидролиз перорально вводимой мочевины ферментом уреазой, который H.pylori производит в больших количествах. Мочевина гидролизуется до аммиака и углекислого газа, который диффундирует в кровь и выводится из легких. CO2, меченный изотопами, может быть обнаружен в выдыхаемом воздухе различными методами. Маркировка мочевины 13C становится все более популярной, поскольку этот нерадиоактивный изотоп безвреден и может безопасно применяться у детей и женщин детородного возраста. Образцы дыхания также можно отправить по почте или курьером в удаленные аналитические центры. Тест прост в выполнении, и его можно повторять столько раз, сколько потребуется для одного и того же пациента. Необходимо дать еду, чтобы увеличить время контакта между индикатором и уреазой H.pylori в желудке.Тест был упрощен до такой степени, что двух проб дыхания, собранных до и через 30 минут после приема мочевины в жидкой форме, достаточно для получения надежной диагностической информации. Стоимость производства 13C-мочевины высока, но возможно дальнейшее снижение дозировки путем введения ее в форме капсул. Масс-спектрометр изотопного состава (IRMS) обычно используется для измерения обогащения 13C в образцах выдыхаемого воздуха, но этот прибор дорогостоящий.
CO2, меченный изотопами, может быть обнаружен в выдыхаемом воздухе различными методами. Маркировка мочевины 13C становится все более популярной, поскольку этот нерадиоактивный изотоп безвреден и может безопасно применяться у детей и женщин детородного возраста. Образцы дыхания также можно отправить по почте или курьером в удаленные аналитические центры. Тест прост в выполнении, и его можно повторять столько раз, сколько потребуется для одного и того же пациента. Необходимо дать еду, чтобы увеличить время контакта между индикатором и уреазой H.pylori в желудке.Тест был упрощен до такой степени, что двух проб дыхания, собранных до и через 30 минут после приема мочевины в жидкой форме, достаточно для получения надежной диагностической информации. Стоимость производства 13C-мочевины высока, но возможно дальнейшее снижение дозировки путем введения ее в форме капсул. Масс-спектрометр изотопного состава (IRMS) обычно используется для измерения обогащения 13C в образцах выдыхаемого воздуха, но этот прибор дорогостоящий. Чтобы снизить эту стоимость, недавно было разработано новое и более дешевое оборудование, основанное на недисперсионной, изотопно-селективной, инфракрасной спектроскопии (NDIRS) и лазерном анализе соотношения (LARA).Это действительные альтернативы IRMS, хотя они не могут обрабатывать такое же большое количество образцов дыхания одновременно. Эти многообещающие достижения, безусловно, будут способствовать более широкому использованию 13C-UBT, который особенно полезен для эпидемиологических исследований у детей и взрослых, для скрининга пациентов перед эндоскопией и для оценки эффективности схем эрадикации.
Чтобы снизить эту стоимость, недавно было разработано новое и более дешевое оборудование, основанное на недисперсионной, изотопно-селективной, инфракрасной спектроскопии (NDIRS) и лазерном анализе соотношения (LARA).Это действительные альтернативы IRMS, хотя они не могут обрабатывать такое же большое количество образцов дыхания одновременно. Эти многообещающие достижения, безусловно, будут способствовать более широкому использованию 13C-UBT, который особенно полезен для эпидемиологических исследований у детей и взрослых, для скрининга пациентов перед эндоскопией и для оценки эффективности схем эрадикации.
Какова роль дыхательного теста с углеродом 13 с мочевиной в диагностике инфекции Helicobacter pylori (H. pylori)?
[Директива] Sugano K, Tack J, Kuipers EJ и др. Для преподавателей Киотской конференции по глобальному консенсусу.Киотский глобальный консенсусный отчет по гастриту Helicobacter pylori. Кишка . 2015 Сентябрь 64 (9): 1353-67. [Медлайн].
Кишка . 2015 Сентябрь 64 (9): 1353-67. [Медлайн].
Младенова И., Дураццо М. Передача Helicobacter pylori. Минерва Гастроэнтерол Диетол . 2018 сентябрь 64 (3): 251-4. [Медлайн].
Хорики Н., Омата Ф., Уэмура М. и др. Ежегодное изменение первичной устойчивости к кларитромицину среди изолятов Helicobacter pylori с 1996 по 2008 год в Японии. Хеликобактер .2009 14 октября (5): 86-90. [Медлайн].
Fallone CA. Эпидемиология устойчивости Helicobacter pylori к антибиотикам в Канаде. Банка Дж Гастроэнтерол . 2000 14 ноября (10): 879-82. [Медлайн].
Hage N, Renshaw JG, Winkler GS, Gellert P, Stolnik S, Falcone FH. Улучшенная экспрессия и очистка адгезина BabA Helicobacter pylori за счет включения гекса-лизиновой метки.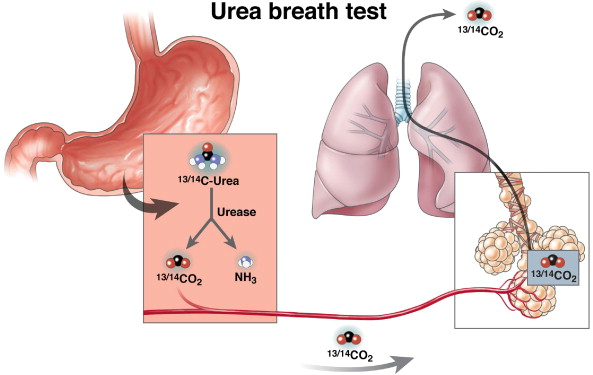 Протеин Expr Purif . 2015 фев. 106: 25-30.[Медлайн]. [Полный текст].
Протеин Expr Purif . 2015 фев. 106: 25-30.[Медлайн]. [Полный текст].
Tomb JF, White O, Kerlavage AR и др. Полная последовательность генома возбудителя желудочного сока Helicobacter pylori. Природа . 1997, 7 августа. 388 (6642): 539-47. [Медлайн].
Lowenthal AC, Hill M, Sycuro LK, et al. Функциональный анализ белков переключателей жгутиков Helicobacter pylori. Дж Бактериол . 2009 декабрь 191 (23): 7147-56. [Медлайн]. [Полный текст].
Гианнакис М., Чен С.Л., Карам С.М. и др.Эволюция Helicobacter pylori при прогрессировании хронического атрофического гастрита до рака желудка и ее влияние на стволовые клетки желудка. Proc Natl Acad Sci U S A . 2008 Март 105 (11): 4358-63. [Медлайн].
Лехур П. Фактический диагноз инфекции Helicobacter pylori..gif) Минерва Гастроэнтерол Диетол . 2018 Сентябрь 64 (3): 267-79. [Медлайн].
Минерва Гастроэнтерол Диетол . 2018 Сентябрь 64 (3): 267-79. [Медлайн].
Pullen LC. Объясняет ли эрадикация H.pylori рост ожирения? Медицинские новости Medscape от WebMD.9 июня 2014 г. Доступно по адресу http://www.medscape.com/viewarticle/826406. Доступ: 19 июня 2014 г.
Кредитор Н., Талли, штат Нью-Джерси, Энк П. и др. Обзорная статья: связь между Helicobacter pylori и ожирением – экологическое исследование. Алимент Фармакол Тер . 2014 июл. 40 (1): 24-31. [Медлайн].
[Рекомендации] Шах С.К., Айер П.Г., Мосс С.Ф. Обновление клинической практики AGA по ведению рефрактерной инфекции Helicobacter pylori: обзор экспертов. Гастроэнтерология . 2021 Апрель 160 (5): 1831-41. [Медлайн]. [Полный текст].
Колецко Л., Маке Л. , Шульц С., Малфертхайнер П. Эрадикация Helicobacter pylori при диспепсии: новые доказательства симптоматической пользы. Лучший Практик Рес Клин Гастроэнтерол . 2019 июн – август 40–1: 101637. [Медлайн].
, Шульц С., Малфертхайнер П. Эрадикация Helicobacter pylori при диспепсии: новые доказательства симптоматической пользы. Лучший Практик Рес Клин Гастроэнтерол . 2019 июн – август 40–1: 101637. [Медлайн].
Лютер Дж., Дэйв М., Хиггинс П.Д., Као Дж. Связь между инфекцией Helicobacter pylori и воспалительным заболеванием кишечника: метаанализ и систематический обзор литературы. Воспаление кишечника . 2010 июн.16 (6): 1077-84. [Медлайн].
Джексон Л., Бриттон Дж., Льюис С.А. и др. Популяционное эпидемиологическое исследование инфекции Helicobacter pylori и ее связи с системным воспалением. Хеликобактер . 2009 октября, 14 (5): 108-13. [Медлайн].
[Рекомендации] Тараскони А., Кокколини Ф., Биффл В.Л. и др. Перфорированная и кровоточащая язвенная болезнь: рекомендации WSES. Мир J Emerg Surg .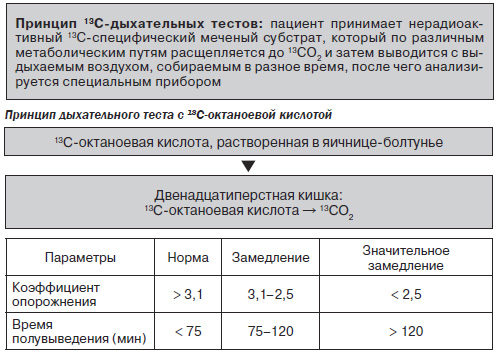 2020. 15: 3. [Медлайн]. [Полный текст].
2020. 15: 3. [Медлайн]. [Полный текст].
Hsu PI, Wu DC, Chen WC, et al. Рандомизированное контролируемое исследование, сравнивающее 7-дневную тройную, 10-дневную последовательную и 7-дневную сопутствующую терапию инфекции Helicobacter pylori. Противомикробные агенты Chemother . 2014 Октябрь 58 (10): 5936-42. [Медлайн].
Pellicano R, Zagari RM, Zhang S, Saracco GM, Moss SF. Фармакологические соображения и пошаговое предложение по лечению инфекции Helicobacter pylori в 2018 году. Минерва Гастроэнтерол Диетол . 2018 Сентябрь 64 (3): 310-21. [Медлайн].
Папастержиу В., Георгопулос С.Д., Каратапанис С. Лечение инфекции Helicobacter pylori: решение проблемы устойчивости к противомикробным препаратам. Мир Дж. Гастроэнтерол . 2014 7 августа. 20 (29): 9898-911. [Медлайн].
Лю X, Ван Х, Lv Z, и др. Спасательная терапия с ингибитором протонной помпы плюс амоксициллин и рифабутин для инфекции Helicobacter pylori: систематический обзор и метаанализ. Гастроэнтерол Рес Прак . 2015. 2015: 415648. [Медлайн]. [Полный текст].
FDA требует удаления с рынка всех продуктов ранитидина (Zantac). Пресс-релиз FDA .1 апреля 2020 г. Доступно на https://www.fda.gov/news-events/press-announcements/fda-requests-removal-all-ranitidine-products-zantac-market.
Отзыв на: Пероральный прием ранитидина увеличивает выведение N-нитрозодиметиламина с мочой. Канцерогенез . 2021 16 июля. 42 (7): 1008. [Медлайн].
Канцерогенез . 2021 16 июля. 42 (7): 1008. [Медлайн].
Флориан Дж., Матта М.К., ДеПальма Р. и др. Влияние перорального ранитидина на выведение N-нитрозодиметиламина с мочой (NDMA): рандомизированное клиническое исследование. JAMA . 2021 20 июля. 326 (3): 240-9. [Медлайн].
Дуглас Д. Использование ранитидина не приводит к увеличению выведения канцерогена NDMA с мочой. Новости Medscape от WebMD. 8 июля 2021 г. Доступно по адресу https://www.medscape.com/viewarticle/954328. Дата обращения: 20 июля 2021 г.
Сафаров Т, Киран Б, Багирова М, Аллахвердиев А.М., Абамор Э.С. Обзор основанных на нанотехнологиях подходов к лечению Helicobacter Pylori. Expert Rev Anti Infect Ther .2019 17 (10) октября: 829-40. [Медлайн].
Ниаз Т. , Ихсан А., Аббаси Р., Шаббир С., Нур Т., Имран М. Основанные на хитозане-альбумине нано-антимикробные вещества оболочки и короны для уничтожения резистентных желудочных патогенов. Инт Дж Биол Макромол . 1 октября 2019 г. 138: 1006-18. [Медлайн].
, Ихсан А., Аббаси Р., Шаббир С., Нур Т., Имран М. Основанные на хитозане-альбумине нано-антимикробные вещества оболочки и короны для уничтожения резистентных желудочных патогенов. Инт Дж Биол Макромол . 1 октября 2019 г. 138: 1006-18. [Медлайн].
Zhi X, Liu Y, Lin L и др. Устные pH-чувствительные нанозонды GNS @ ab для таргетной терапии Helicobacter pylori без нарушения микробиома кишечника. Наномедицина .20 августа 2019: 10 [Медлайн].
de Avila BE, Angsantikul P, Li J, et al. Активная доставка лекарств с помощью микромотора для лечения желудочной инфекции in vivo. Нац Коммуна . 2017 16 августа. 8 (1): 272. [Медлайн]. [Полный текст].
Гринберг Э. Р., Андерсон Г. Л., Морган Д. Р. и др. 14-дневная тройная, 5-дневная сопутствующая и 10-дневная последовательная терапия инфекции Helicobacter pylori в семи странах Латинской Америки: рандомизированное исследование. Ланцет .2011 6 августа. 378 (9790): 507-14. [Медлайн].
Ланцет .2011 6 августа. 378 (9790): 507-14. [Медлайн].
Liou JM, Lin JT, Chang CY и др. Тройная терапия на основе левофлоксацина и кларитромицина в качестве терапии первого и второго ряда при инфекции Helicobacter pylori: рандомизированное сравнительное исследование с перекрестным дизайном. Кишка . 2010 май. 59 (5): 572-8. [Медлайн].
Apostolopoulos P, Koumoutsos I, Ekmektzoglou K, et al. Сопутствующая терапия по сравнению с последовательной терапией для лечения инфекции Helicobacter pylori: греческое рандомизированное проспективное исследование. Сканд Дж Гастроэнтерол . 2016 Февраль 51 (2): 145-51. [Медлайн].
Юн Х., Ким Н., Ли Б.Х. и др. Тройная терапия, содержащая моксифлоксацин, в качестве лечения второй линии при инфекции Helicobacter pylori: влияние продолжительности лечения и устойчивости к антибиотикам на скорость эрадикации. Хеликобактер . 2009 октября, 14 (5): 77-85. [Медлайн].
Хеликобактер . 2009 октября, 14 (5): 77-85. [Медлайн].
Malfertheiner P, Bazzoli F, Delchier JC, et al. Эрадикация Helicobacter pylori с помощью капсулы, содержащей субцитрат висмута калия, метронидазол и тетрациклин, с омепразолом по сравнению с тройной терапией на основе кларитромицина: рандомизированное открытое исследование не меньшей эффективности, фаза 3. Ланцет . 2011 12 марта. 377 (9769): 905-13. [Медлайн].
Ли С.Б., Ян Дж.В., Ким К.С. Связь между MALT-лимфомой конъюнктивы и Helicobacter pylori. Br J Офтальмол . 2008 апр. 92 (4): 534-6. [Медлайн].
Aanpreung P. Предполагаемые параметры эрадикационной терапии у детей с гастритом Helicobacter pylori. J Med Assoc Thai . 2005 г., ноябрь 88, приложение 8: S21-6. [Медлайн].
Александр Г.А., Броули О.В. Связь инфекции Helicobacter pylori с раком желудка. Мил Мед . 2000, январь, 165 (1): 21-7. [Медлайн].
Ceponis PJ, Jones NL. Модуляция путей передачи сигнала клетки-хозяина инфекцией Helicobacter pylori. Банка Дж Гастроэнтерол . 2005 июля 19 (7): 415-20. [Медлайн].
Cheng TY, Lin JT, Chen LT и др. Ассоциация полиморфизмов регуляторных генов Т-клеток с предрасположенностью к лимфоме лимфоидной ткани, ассоциированной со слизистой оболочкой желудка. Дж.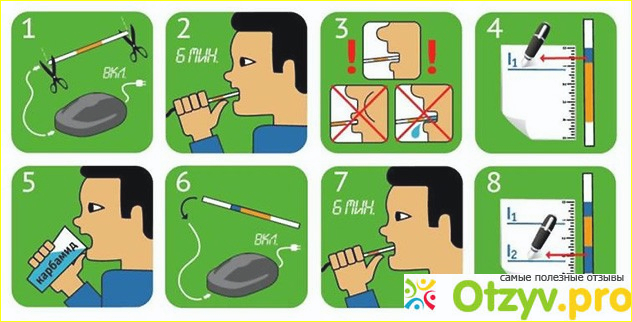 Клин Онкол . 20 июля 2006 г. 24 (21): 3483-9. [Медлайн].
Клин Онкол . 20 июля 2006 г. 24 (21): 3483-9. [Медлайн].
Краанен М.Э., Блок П., Деккер В. и др. Helicobacter pylori и ранний рак желудка. Кишка . 1994 окт. 35 (10): 1372-4. [Медлайн].
Давыдов Л, Ченг Ж. Связь инфекции и ишемической болезни сердца: обновленная информация. Заключение эксперта по расследованию наркотиков . 2000 ноября, 9 (11): 2505-17. [Медлайн].
Демирель А., Онсел С., Кейдер М., Доган А., Устен Х., Онгорен А. Инфекция Helicobacter pylori в образцах после гастрэктомии. Интернет J of Gastro . 1999. 1 (1): [Полный текст].
Данн Б.Е., Коэн Х., Блазер М.Дж. Helicobacter pylori. Clin Microbiol Ред. . 1997.10.10 (4): 720-41. [Медлайн].
Эль-Омар Э.М., Кэррингтон М., Чоу WH и др. Полиморфизм интерлейкина-1 связан с повышенным риском рака желудка. Природа . 2000 23 марта.404 (6776): 398-402. [Медлайн].
Эрджан И., Чакир Б.О., Узел Т.С. и др. Роль желудочной инфекции Helicobacter pylori в ларингофарингеальной рефлюксной болезни. Отоларингол Хирургия головы и шеи . 2006 июль 135 (1): 52-5. [Медлайн].
Фиорини Г., Вакил Н., Зулло А. и др. Селекционная терапия на основе культур для пациентов, которые не ответили на предыдущее лечение инфекции Helicobacter pylori. Клин Гастроэнтерол Гепатол . 2013 май.11 (5): 507-10. [Медлайн].
2013 май.11 (5): 507-10. [Медлайн].
Fischbach W. Первичная лимфома желудка MALT: соображения патогенеза, диагностики и лечения. Банка Дж Гастроэнтерол . 2000 14 ноября Дополнение D: 44D-50D. [Медлайн].
Фок К.М., Кателарис П., Сугано К. и др. Второе Азиатско-Тихоокеанское согласованное руководство по инфекции Helicobacter pylori. Дж Гастроэнтерол Гепатол . 2009 24 октября (10): 1587-600. [Медлайн].
Гарсия-Альтес А., Рота Р., Баренис М. и др.Экономическая эффективность стратегии «оценка и масштаб» для лечения диспепсии. Eur J Гастроэнтерол Hepatol . 2005 июл.17 (7): 709-19. [Медлайн].
Гатопулу А., Мимидис К., Гиатроманолаки А. и др. Влияние инфекции Helicobacter pylori на гистологические изменения при неэрозивной рефлюксной болезни. Мир Дж. Гастроэнтерол . 2004 15 апреля. 10 (8): 1180-2. [Медлайн].
Мир Дж. Гастроэнтерол . 2004 15 апреля. 10 (8): 1180-2. [Медлайн].
Грэм Д.Ю. Терапия Helicobacter pylori: текущее состояние и проблемы. Гастроэнтерология . 2000, февраль 118 (2 приложение 1): S2-8. [Медлайн].
Грэм Д.Ю., Лью Г.М., Лехаго Дж. Количество G-клеток и D-клеток антрального отдела при инфекции Helicobacter pylori: эффект эрадикации H. pylori. Гастроэнтерология . 1993 июн.104 (6): 1655-60. [Медлайн].
Graham DY, Lew GM, Malaty HM, et al. Факторы, влияющие на эрадикацию Helicobacter pylori при тройной терапии. Гастроэнтерология . 1992 фев.102 (2): 493-6. [Медлайн].
Graham DY, Malaty HM, Evans DG, et al. Эпидемиология Helicobacter pylori у бессимптомной популяции в США. Влияние возраста, расы и социально-экономического статуса. Гастроэнтерология . 1991 июн.100 (6): 1495-501. [Медлайн].
Гастроэнтерология . 1991 июн.100 (6): 1495-501. [Медлайн].
[Рекомендации] Howden CW, Hunt RH. Руководство по лечению инфекции Helicobacter pylori. Специальный комитет по параметрам практики Американского колледжа гастроэнтерологии. Ам Дж. Гастроэнтерол . 1998 декабрь 93 (12): 2330-8. [Медлайн].
Jia CL, Jiang GS, Li CH, Li CR. Влияние контроля зубного налета на инфекцию Helicobacter pylori в слизистой оболочке желудка. Дж Периодонтол . 2009 Октябрь 80 (10): 1606-9. [Медлайн].
Kusters JG, van Vliet AH, Kuipers EJ. Патогенез инфекции Helicobacter pylori. Clin Microbiol Ред. . 2006 июл.19 (3): 449-90. [Медлайн].
Лейнонен М., Сайкку П.Инфекции и атеросклероз. Сканд Кардиоваск J . 2000. 34 (1): 12-20. [Медлайн].
[Медлайн].
Лопес А.И., Викторино Р.М., Пальха А.М. и др. Субпопуляции лимфоцитов слизистой оболочки и экспрессия антигена HLA-DR при педиатрическом гастрите, ассоциированном с Helicobacter pylori. Clin Exp Immunol . 2006 июл.145 (1): 13-20. [Медлайн].
Мюллер А., Сайи А., Хитцлер И. Защитные и патогенные функции Т-клеток неотделимы во время взаимодействия Helicobacter-хозяин. Дисков Мед . 2009 8 августа (41): 68-73. [Медлайн].
Накадзима С., Кришнан Б., Ота Н. и др. Участие тучных клеток в гастрите с инфекцией Helicobacter pylori или без нее. Гастроэнтерология . 1997 сентябрь 113 (3): 746-54. [Медлайн].
Padol S, Yuan Y, Thabane M, et al. Влияние полиморфизма CYP2C19 на скорость эрадикации H. pylori при терапии двойным и тройным ИПП первой линии: метаанализ. Ам Дж. Гастроэнтерол .2006 июль 101 (7): 1467-75. [Медлайн].
Ам Дж. Гастроэнтерол .2006 июль 101 (7): 1467-75. [Медлайн].
Peach HG, Barnett NE. Детерминанты базального уровня гастрина в плазме в общей популяции. Дж Гастроэнтерол Гепатол . 2000 15 ноября (11): 1267-71. [Медлайн].
Pratt JS, Sachen KL, Wood HD и др. Модуляция иммунных ответов хозяина цитотоксическим токсином Helicobacter hepaticus. Заражение иммунной . 2006 г., август 74 (8): 4496-504. [Медлайн].
Reyrat JM, Rappuoli R, Telford JL.Обзор структуры цитотоксина Helicobacter. Int J Med Microbiol . 2000 Октябрь 290 (4-5): 375-9. [Медлайн].
Родригес MN, Queiroz DM, Bezerra Filho JG, et al. Распространенность инфекции Helicobacter pylori у детей из городских поселений на северо-востоке Бразилии и факторы риска инфицирования. Eur J Гастроэнтерол Hepatol . 2004 Февраль 16 (2): 201-5. [Медлайн].
Eur J Гастроэнтерол Hepatol . 2004 Февраль 16 (2): 201-5. [Медлайн].
Santacroce L, Bufo P, Latorre V и др. [Роль тучных клеток в физиопатологии поражений желудка, вызванных Helicobacter pylori]. Чир Итал . 2000 сен-окт. 52 (5): 527-31. [Медлайн].
Smoot DT, Mobley HL, Chippendale GR и др. Активность уреазы Helicobacter pylori токсична для эпителиальных клеток желудка человека. Заражение иммунной . 1990 июн. 58 (6): 1992-4. [Медлайн].
Шталер Ф.Н., Оденбрайт С., Хаас Р. и др. Новый насос для оттока металла Helicobacter pylori CznABC необходим для обеспечения устойчивости к кадмию, цинку и никелю, модуляции уреазы и колонизации желудка. Заражение иммунной . 2006 июль 74 (7): 3845-52. [Медлайн].
Цай С.Дж., Перри С. , Санчес Л. и др. Инфекция Helicobacter pylori у разных поколений латиноамериканцев в районе залива Сан-Франциско. Am J Epidemiol . 2005 15 августа. 162 (4): 351-7. [Медлайн].
, Санчес Л. и др. Инфекция Helicobacter pylori у разных поколений латиноамериканцев в районе залива Сан-Франциско. Am J Epidemiol . 2005 15 августа. 162 (4): 351-7. [Медлайн].
Tytgat GN. Обзорная статья: Helicobacter pylori: где мы и куда идем ?. Алимент Фармакол Тер . 2000, 14 октября, Дополнение 3: 55-8. [Медлайн].
Уоррен Дж. Р., Маршалл Б. Неопознанные изогнутые бациллы на эпителии желудка при активном хроническом гастрите. Ланцет . 4 июня 1983 г., 1 (8336): 1273-5. [Медлайн].
Вайра Д., Гатта Л., Риччи С. и др. Язвенная болезнь и Helicobacter pylori: обновленная информация о тестировании и лечении. Постградская медицина . 2005 июн. 117 (6): 17-22, 46. [Medline].
Ван Х, Ваттис Р., Пагглиасиа С. и др. Топология мембраны цитотоксина VacA из H.пилори. FEBS Lett . 2000, 15 сентября. 481 (2): 96-100. [Медлайн].
Топология мембраны цитотоксина VacA из H.пилори. FEBS Lett . 2000, 15 сентября. 481 (2): 96-100. [Медлайн].
Вт TL. Курение, Helicobacter pylori и пародонтит. BMJ . 24 июня 2006 г.. 332 (7556): 1513. [Медлайн].
Wotherspoon AC. Критический обзор влияния эрадикации Helicobacter pylori на MALT-лимфому желудка. Curr Gastroenterol Rep . 2000 Декабрь 2 (6): 494-8. [Медлайн].
Chao CY, Wang CH, Che YJ, Kao CY, Wu JJ, Lee GB.Интегрированная микрофлюидная система для диагностики устойчивости Helicobacter pylori к антибиотикам на основе хинолонов. Biosens Bioelectron . 2016 15 апреля. 78: 281-9. [Медлайн].
Lee YC, Chiang TH, Liou JM, Chen HH, Wu MS, Graham DY. Массовая ликвидация Helicobacter pylori для предотвращения рака желудка: теоретические и практические соображения. Печень кишечника . 2016 23 января 10 (1): 12-26. [Медлайн].
Печень кишечника . 2016 23 января 10 (1): 12-26. [Медлайн].
Kono Y, Okada H, Takenaka R, et al.Усиливает ли Helicobacter pylori повреждение слизистой оболочки желудка у пользователей нестероидных противовоспалительных препаратов? Многоцентровое ретроспективное исследование случай-контроль. Печень кишечника . 2016 23 января 10 (1): 69-75. [Медлайн].
Исаева Г.С., Фагуни С. Биологические свойства и факторы патогенности Helicobacter pylori. Минерва Гастроэнтерол Диетол . 2018 Сентябрь 64 (3): 255-66. [Медлайн].
Корреляция между количественным тестом на дыхание с 13C-мочевиной и успехом лечения Helicobacter pylori в популяционной когорте
Общие сведения .Постоянно предпринимаются попытки определить факторы, влияющие на успех терапии первой линии для инфекции Helicobacter pylori ( H. pylori ).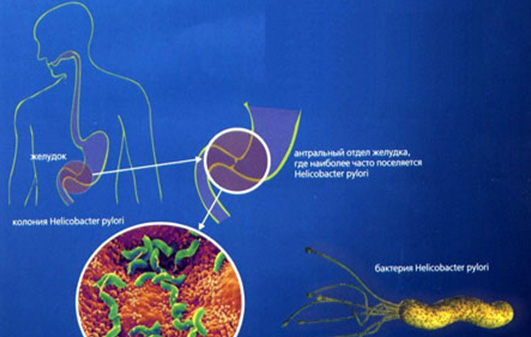 Результат дыхательного теста с мочевиной 13 (C13-UBT) использует уреазную активность H. pylori и является высокоточным диагностическим анализом. Мы стремились определить, связана ли величина результата C13-UBT с успехом лечения. Методы . Были включены взрослые пациенты, которые прошли первый дыхательный тест на 13 C-мочевину в период с января 2010 года по январь 2016 года.Чтобы изолировать наивную популяцию, проходившую тестирование и лечение, которая вряд ли прошла первоначальный эндоскопический тест H. pylori , мы исключили пациентов старше 45 лет и пациентов с предыдущим C13-UBT. Данные взяты из базы данных лаборатории Службы здравоохранения Клалит. Результатов . В исследование были включены 94 590 пациентов (36,1% мужчин, возраст 28,5 ± 6,0 лет), впервые перенесших C13-UBT в течение периода исследования. C13-UBT был положительным у 48 509 (51,3%) пациентов. Подтверждающая постобработка C13-UBT была проведена 18 375 пациентам (37.
Результат дыхательного теста с мочевиной 13 (C13-UBT) использует уреазную активность H. pylori и является высокоточным диагностическим анализом. Мы стремились определить, связана ли величина результата C13-UBT с успехом лечения. Методы . Были включены взрослые пациенты, которые прошли первый дыхательный тест на 13 C-мочевину в период с января 2010 года по январь 2016 года.Чтобы изолировать наивную популяцию, проходившую тестирование и лечение, которая вряд ли прошла первоначальный эндоскопический тест H. pylori , мы исключили пациентов старше 45 лет и пациентов с предыдущим C13-UBT. Данные взяты из базы данных лаборатории Службы здравоохранения Клалит. Результатов . В исследование были включены 94 590 пациентов (36,1% мужчин, возраст 28,5 ± 6,0 лет), впервые перенесших C13-UBT в течение периода исследования. C13-UBT был положительным у 48 509 (51,3%) пациентов. Подтверждающая постобработка C13-UBT была проведена 18 375 пациентам (37.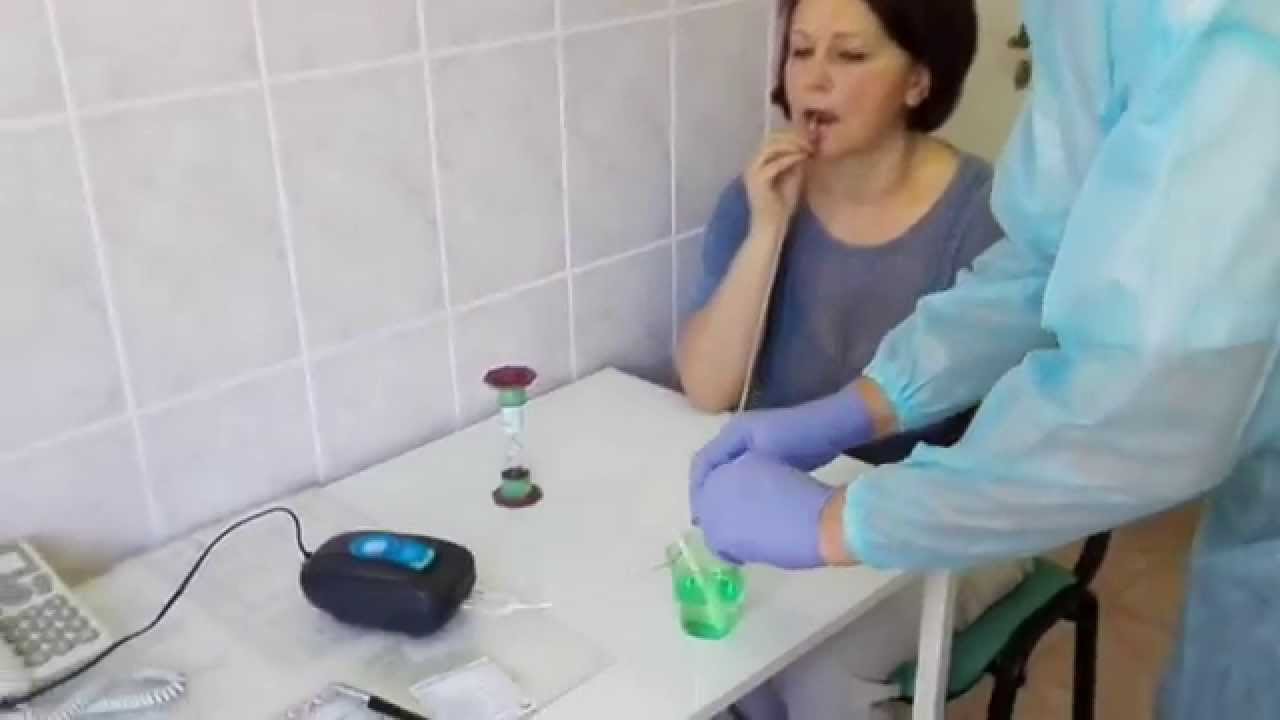 8%), а ликвидация была успешной у 12 018 (65,4%). Среднее значение C13-UBT составило 20,6 ± 16,2 DOB у субъектов с успешной эрадикацией и 19,5 ± 13,1 DOB у субъектов с неэффективным лечением (OR 1,01; 95% CI 1,00–1,01). Среди пациентов в верхнем квинтиле измерения C13-UBT эрадикация была достигнута у 67,6% по сравнению с 62,6% в нижнем квинтиле (OR 1,22; 95% CI 1,11–1,35). Субъекты в верхнем 1 процентиле (C13-UBT ≥ 70 DOB) достигли эрадикации в 75,0% по сравнению с 65,3% среди субъектов с C13-UBT <70 DOB (OR, 1.59; 95% ДИ 1,05–2,41,). Выводы . Превосходство в эрадикации H. pylori , наблюдаемое у субъектов с более высоким DOB C13-UBT, невелико, но значимо. Дальнейшие исследования должны изучить физиологическую и микробиологическую основу этого открытия.
8%), а ликвидация была успешной у 12 018 (65,4%). Среднее значение C13-UBT составило 20,6 ± 16,2 DOB у субъектов с успешной эрадикацией и 19,5 ± 13,1 DOB у субъектов с неэффективным лечением (OR 1,01; 95% CI 1,00–1,01). Среди пациентов в верхнем квинтиле измерения C13-UBT эрадикация была достигнута у 67,6% по сравнению с 62,6% в нижнем квинтиле (OR 1,22; 95% CI 1,11–1,35). Субъекты в верхнем 1 процентиле (C13-UBT ≥ 70 DOB) достигли эрадикации в 75,0% по сравнению с 65,3% среди субъектов с C13-UBT <70 DOB (OR, 1.59; 95% ДИ 1,05–2,41,). Выводы . Превосходство в эрадикации H. pylori , наблюдаемое у субъектов с более высоким DOB C13-UBT, невелико, но значимо. Дальнейшие исследования должны изучить физиологическую и микробиологическую основу этого открытия.
1. Введение
Helicobacter pylori ( H. pylori ) Инфекция поражает до 50% населения мира и является основной причиной язвенной болезни, рака желудка и лимфомы MALT [1].Наиболее доступным и точным неинвазивным тестом для диагностики H. pylori является дыхательный тест с С-мочевиной 13 (C13-UBT) [2]. Этот тест использует способность организма продуцировать уреазу и включает измерение 13 CO 2 после перорального приема 13 C-мочевины с истекшим сроком годности. Когда присутствует инфекция H. pylori , 13 C-мочевина расщепляется бактериальной уреазой до 2NH 3 и 13 CO 2 .Абсорбируется 13 CO 2 выводится через легкие и измеряется в выдыхаемом воздухе на исходном уровне и через 30 минут после приема индикатора. На положительный результат указывает увеличение 13 C с истекшим сроком действия по сравнению с исходным уровнем или дельта по сравнению с исходным уровнем (DOB) [3-5].
pylori является дыхательный тест с С-мочевиной 13 (C13-UBT) [2]. Этот тест использует способность организма продуцировать уреазу и включает измерение 13 CO 2 после перорального приема 13 C-мочевины с истекшим сроком годности. Когда присутствует инфекция H. pylori , 13 C-мочевина расщепляется бактериальной уреазой до 2NH 3 и 13 CO 2 .Абсорбируется 13 CO 2 выводится через легкие и измеряется в выдыхаемом воздухе на исходном уровне и через 30 минут после приема индикатора. На положительный результат указывает увеличение 13 C с истекшим сроком действия по сравнению с исходным уровнем или дельта по сравнению с исходным уровнем (DOB) [3-5].
На величину DOB влияет множество факторов, связанных с пациентом, включая пол, национальность, голодание, лекарства и осанку [6–9]. Характеристики теста, такие как 13 дозировка C-мочевины, пробный обед и продолжительность теста, также напрямую связаны с точностью C13-UBT и могут влиять на величину DOB [10–15].
Величина DOB также связана с серьезностью инфекции H. pylori . Было показано, что плотность H. pylori , а также гистопатологическая хроничность и индексы активности положительно коррелируют с величиной DOB [16-25]. С другой стороны, не наблюдается явной корреляции между величиной DOB и диспепсией или язвенной болезнью [21, 25, 26].
Ликвидация H. pylori остается сложной задачей, и предпринимаются постоянные усилия по выявлению факторов, влияющих на успех лечения.Взаимосвязь между гистопатологической серьезностью гастрита и вероятностью успеха лечения сложна. Несколько исследований показали, что более высокая степень хронического активного воспаления в слизистой оболочке желудка связана с успехом лечения H. pylori [27–30]. С другой стороны, высокая степень атрофии слизистой оболочки снижает вероятность успеха лечения [30]. Неясно, связана ли величина результата C13-UBT с успехом лечения. Целью этого исследования было выяснить, связан ли результат C13-UBT с вероятностью последующей успешной эрадикации H. pylori .
pylori .
2. Материалы и методы
2.1. Пациенты
Мы ретроспективно идентифицировали взрослых пациентов старше 18 лет, которые впервые прошли 13 дыхательный тест на содержание C-мочевины (C13-UBT) в период с 1 января 2010 года по 31 декабря 2015 года в Службе здравоохранения Клалит (CHS). Чтобы исключить пациентов, которые, возможно, ранее получали лечение антибиотиками от H. pylori , мы сначала исключили пациентов ≥ 45 лет, которые могли пройти первичную эндоскопию на основе H.pylori в соответствии с рекомендациями на момент включения [31]. Впоследствии мы исключили субъектов, которые прошли курс C13-UBT за 2 года до включения (1 января 2008 г. – 31 декабря 2009 г.). Наконец, мы исключили пациентов, которые прошли C13-UBT после отрицательного результата теста. Для целей этого исследования мы предположили, что лечение антибиотиками проводилось после положительного результата C13-UBT и до последующего C13-UBT.
2.2. Сбор и анализ образцов
Образцы дыхания были получены в учреждениях CHS, которые включают 14 больниц и 1300 клиник первичной медико-санитарной помощи и специализированных клиник в восьми округах. Дыхательные тесты проводились специализированными медсестрами. Пациентам давали 75 мг 13 C-меченой мочевины, смешанной с пробной едой из 100 мл апельсинового сока. Все образцы дыхания C13-UBT были транспортированы и обработаны в центральной лаборатории Медицинского центра Рабина, Петах-Тиква, Израиль. Образцы анализировали с помощью автоматического пробоотборника дыхания Gilson XL222 (Gilson, Middleton, WI, США) и масс-спектрометра изотопного отношения AP2003 (IRMS) (Analytical Precision, Phoenix, AZ, США). Соотношение 13 C и 12 C, измеренное в частях на тысячу, было получено на исходном уровне и через 30 минут после приема внутрь 13 C-мочевины (T30-T0).Конечный результат был выражен как разница между двумя оценками, дельта относительно исходного уровня (DOB). Пороговое значение 3,5 DOB использовалось в соответствии со спецификациями производителя. Повышение DOB выше 3,5 считалось положительным на наличие инфекции H. pylori .
Дыхательные тесты проводились специализированными медсестрами. Пациентам давали 75 мг 13 C-меченой мочевины, смешанной с пробной едой из 100 мл апельсинового сока. Все образцы дыхания C13-UBT были транспортированы и обработаны в центральной лаборатории Медицинского центра Рабина, Петах-Тиква, Израиль. Образцы анализировали с помощью автоматического пробоотборника дыхания Gilson XL222 (Gilson, Middleton, WI, США) и масс-спектрометра изотопного отношения AP2003 (IRMS) (Analytical Precision, Phoenix, AZ, США). Соотношение 13 C и 12 C, измеренное в частях на тысячу, было получено на исходном уровне и через 30 минут после приема внутрь 13 C-мочевины (T30-T0).Конечный результат был выражен как разница между двумя оценками, дельта относительно исходного уровня (DOB). Пороговое значение 3,5 DOB использовалось в соответствии со спецификациями производителя. Повышение DOB выше 3,5 считалось положительным на наличие инфекции H. pylori .
2.
 3. Извлечение данных
3. Извлечение данныхДемографические данные и результаты C13-UBT были извлечены из центральной компьютеризированной базы данных CHS. CHS – крупнейшая организация по поддержанию здоровья в Израиле и вторая по величине организация по поддержанию здоровья в мире, насчитывающая более 3 организаций.8 миллионов абитуриентов. Данные были получены и сохранены после одобрения Институционального наблюдательного совета Медицинского центра Рабина и в соответствии с принципами Хельсинкской декларации и надлежащей клинической практики.
2.4. Статистический анализ
Все анализы были выполнены с использованием программного обеспечения для статистического анализа SPSS версии 24.0 (IBM Inc., Чикаго, Иллинойс, США). Распределения непрерывных переменных оценивались на нормальность с помощью критерия Колмогорова-Смирнова (отсечение при) и описываются как средние значения ± стандартное отклонение (SD).Номинальные переменные сравнивались с использованием критерия хи-квадрат. Кривая оператора приемника (ROC) была построена и проанализирована с помощью индекса Юдена. В статистическом анализе использовалась многомерная модель прямой логистической регрессии для оценки отношения шансов (OR) и 95% доверительного интервала. Все тесты были двусторонними и считались значимыми при.
В статистическом анализе использовалась многомерная модель прямой логистической регрессии для оценки отношения шансов (OR) и 95% доверительного интервала. Все тесты были двусторонними и считались значимыми при.
3. Результаты
Всего было включено 94 590 субъектов (36,1% мужчин, возраст 28,5 ± 6,0 лет), которые впервые прошли C13-UBT в течение периода исследования.C13-UBT был положительным у 48 509 (51,3%) пациентов. Подтверждающая постобработка C13-UBT была проведена у 18 375 (37,8%), а эрадикация была успешной у 12 018 (65,4%).
Среди 18 375 H. pylori -положительных субъектов, перенесших второй C13-UBT, средняя начальная запись C13-UBT составила 20,6 ± 16,2 DOB среди субъектов с успешной эрадикацией и 19,5 ± 13,1 DOB у субъектов с неэффективным лечением (OR , 1.01; 95% ДИ 1.00-1.01,) (Таблица 1). ROC-анализ показал, что пороговое значение 14.9 DOB может предсказать успех лечения с чувствительностью 45,2% и специфичностью 58,5%.
Среди пациентов в верхнем квинтиле измерения C13-UBT эрадикация была достигнута у 67,6% по сравнению с 62.6% в нижнем квинтиле (OR 1,22; 95% CI 1,11–1,35) (рисунок 1). Результаты были аналогичными при использовании модели многомерной логистической регрессии с поправкой на возраст и пол (OR 1,28; 95% ДИ 1,15–1,42;) (таблица 2).
Субъекты из первого процентиля с C13-UBT ≥ 70 DOB достигли эрадикации в 75.0% по сравнению с 65,3% среди субъектов с C13-UBT <70 DOB (OR 1,59; 95% CI 1,05–2,41) (рис. 2). Результаты были аналогичными при использовании модели многомерной логистической регрессии с поправкой на возраст и пол (OR 1,62; 95% CI 1,07–2,45) (таблица 2). 4. ОбсуждениеМы обнаружили, что среди субъектов, перенесших C13-UBT, по мере увеличения DOB вероятность успешного уничтожения H. pylori также увеличивается. Величина значения DOB напрямую связана с H.pylori активность уреазы. В предыдущем исследовании изучалась взаимосвязь между величиной DOB и успехом лечения.В отличие от наших результатов, Gisbert et al. не обнаружили корреляции между величиной DOB и вероятностью успешного искоренения среди 600 субъектов [38]. Предыдущие исследования изучали связь между оценкой воспаления, измеренной по пересмотренной Сиднейской системе, и вероятностью успешного лечения [39]. Три исследования показали, что более высокая степень хронического активного воспаления связана с успехом лечения [27–29]. Дополнительное исследование показало, что высокая степень атрофии слизистой оболочки снижает вероятность успеха лечения [30].Эти исследования не включали молекулярную оценку бактериальной нагрузки или количественный анализ C13-UBT. Однако, если мы рассмотрим доказательства того, что величина DOB прямо пропорциональна инфильтрату воспалительных клеток и обратно пропорциональна атрофии, как обсуждалось, то эти исследования могут согласовываться с нашими выводами, которые предполагают, что величина DOB пропорциональна успеху лечения. Взятые вместе, кажется, что субъекты с более тяжелым воспалительным инфильтратом с большей вероятностью будут иметь высокую бактериальную нагрузку, более высокий DOB и больший успех лечения.Субъекты с атрофией слизистой оболочки и более низкой бактериальной нагрузкой с большей вероятностью будут иметь более низкую величину DOB и большую неэффективность лечения. Очевидно, что эти два сценария во многом пересекаются, и, хотя это может быть достоверным наблюдением в условиях популяции, оно мало актуально для отдельного пациента. Существует несколько возможных механизмов, почему высокий показатель DOB или оценка воспаления связаны с успехом лечения. Усиление хронического активного воспаления может вызвать благоприятный ответ хозяина, который облегчит уничтожение организма при соответствующем лечении.Labenz et al. обнаружили, что пациенты с успешной эрадикацией имели более высокий рН желудочного сока по сравнению с пациентами с неэффективным лечением. Более высокий pH может усилить действие амоксициллина за счет снижения минимальной ингибирующей концентрации, повышения стабильности препарата в просвете желудка и увеличения концентрации в просвете за счет замедления опорожнения желудка [40–42]. Тем не менее, взаимосвязь между величиной DOB и оценкой воспаления не совсем ясна, и эти механизмы могут только объяснить, почему воспаление, но не DOB, связано с успехом лечения. Ограничением нашего исследования является отсутствие данных гистопатологии для корреляции наших результатов. Еще одно ограничение – это вероятное присутствие нескольких факторов, влияющих на ситуацию, которые невозможно учесть. Во-первых, существует множество факторов, определяющих величину DOB, помимо плотности бактерий, которые могут объяснить наблюдаемую разницу в успехе лечения. К ним относятся факторы пациента, бактериальные факторы и тестовые / лабораторные факторы [6–15]. Во-вторых, существуют смешанные факторы, которые могут объяснить различия в успехе лечения.К ним относятся приверженность к лекарствам, устойчивость к антибиотикам, режим антибиотиков, лекарственные взаимодействия, полиморфизм CYP2C19 и курение. Тем не менее, учитывая большой размер выборки, маловероятно, что учет этих факторов существенно повлияет на результаты. Еще одним ограничением является относительно низкий уровень эрадикации – 65,4%. Предыдущие данные показывают, что более 90% пациентов получали тройную терапию на основе кларитромицина [43], несмотря на то, что первичная резистентность H. pylori к кларитромицину в нашем регионе составляет> 20% [44, 45].В соответствии с действующими рекомендациями по лечению тройная терапия на основе кларитромицина не рекомендуется в регионах, где первичная резистентность к кларитромицину превышает 15% [1, 46]. Тем не менее тройная терапия на основе кларитромицина остается наиболее распространенным протоколом лечения [43]. Если бы субъекты получали более эффективные схемы лечения с более высокой скоростью эрадикации, возможно, что величина DOB больше не была бы в значительной степени связана с успехом лечения. Для целей данного исследования мы предположили, что лечение антибиотиками проводилось после положительного результата C13-UBT и до последующего C13-UBT.Однако некоторые субъекты могли не получать лечения или могли пройти более одного курса лечения до повторения C13-UBT. У нас нет данных о различных протоколах лечения. Хотя мы исключили субъектов старше 45 лет, некоторые субъекты могли пройти тесты на основе эндоскопии для диагноза H. pylori и, возможно, прошли лечение до индексного теста. Наконец, наша когорта ограничена 18–45-летними. Мы исключили пациентов старше 45 лет, поскольку эти пациенты с большей вероятностью прошли эндоскопию верхних отделов желудочно-кишечного тракта в качестве первоначального теста на диспепсию.В противном случае пациенты с положительным результатом C13-UBT после положительного результата эндоскопического теста и последующего лечения были бы ошибочно классифицированы как не леченные. Поскольку мы не смогли достоверно идентифицировать пациентов, которые ранее прошли тест на основе эндоскопии на H. pylori , мы решили исключить пациентов старше 45 лет. Наши результаты могут быть неприменимы к пожилым пациентам с более длительной инфекцией, более высокими показателями атрофии желудка и, возможно, лучшим соблюдением режима лечения.Сила нашего исследования заключается в большой когорте, строгих критериях исключения и качестве используемой базы данных. В заключение мы обнаружили, что более высокая величина DOB связана с большей степенью успешной эрадикации H. pylori . Необходимы дальнейшие исследования, включающие гистопатологические и клинические переменные, для проверки и выяснения физиологической основы наших результатов. Доступность данныхНеобработанные данные, использованные для подтверждения результатов этого исследования, доступны у соответствующего автора по запросу. Конфликт интересовАвторы не заявляют о конфликте интересов. Дыхательный тест с низкими дозами 13 C-мочевины на Helicobacter pylori перспективенGatta L и др. . (2006) Точность дыхательных тестов с использованием низких доз 13C-мочевины для диагностики инфекции Helicobacter pylori : рандомизированное контролируемое исследование. Кишечник 55 : 457–462 Дыхательный тест на С-мочевину 13 (UBT) точен в диагностике и подтверждении искоренения инфекции Helicobacter pylori . Доза 13 C-мочевины, используемая в настоящее время в UBTs, колеблется от 75 до 125 мг, но 13 C-мочевина стоит дорого, и исследования показали, что можно использовать более низкие дозы 13 C- мочевина. В своем проспективном исследовании, состоящем из двух частей, Gatta et al . подтвердили, что низкие дозы 13 C-UBT могут обеспечить как точный диагноз инфекции, так и подтверждение H.pylori . Первоначально авторы случайным образом распределили 300 последовательных пациентов с диспепсией для проведения UBT с 10, 15 или 25 мг 13 C-мочевины, а затем верхней эндоскопии с биопсией. Лучшая диагностическая эффективность для инфекции H. pylori была отмечена при использовании 15 мг 13 C-мочевины: 100% специфичность (95% ДИ 92,6–100) и чувствительность 96,1% (95% ДИ 86,8–98,9). Эта доза использовалась для диагностики H. pylori у последующих пациентов. Затем авторы оценили H.pylori у 110 пациентов, получавших эрадикационную терапию и по которым были доступны полные данные последующего наблюдения. UBT с 15 мг 13 C-мочевины имели 98,9% специфичность (95% ДИ 94,3–99,8) и 100% чувствительность (95% ДИ 79,6–100) для эрадикации. Авторы предполагают, что хорошие результаты, достигаемые с низкой дозой 13 C-UBT, могут означать, что можно разработать недорогой тест, который будет иметь особое значение в развивающихся странах. Об этой статьеЦитируйте эту статьюGiles, C.Низкая доза 13 Дыхательный тест C-мочевины на Helicobacter pylori является многообещающим. Nat Rev Gastroenterol Hepatol 3, 298 (2006). https://doi.org/10.1038/ncpgasthep0476 Ссылка для скачивания Точная диагностика Helicobacter pylori: Дыхательный тест с 13C-мочевинойДыхательный тест с мочевиной является неинвазивным методом выбора для определения статуса Helicobacter pylori . Этот тест основан на уреазной активности организма, которая высвобождает диоксид углерода (CO 2 ) из мочевины и производит аммиак для буферизации ее кислой среды.Проглатывание меченой мочевины приводит к выработке меченого CO 2 , который затем может быть обнаружен в выдыхаемом воздухе. Доступны две формы меченой мочевины: одна содержит стабильный нерадиоактивный изотоп 13 C, а другая – радиоактивный изотоп 14 C. Хотя количество радиационного воздействия с помощью дыхательного теста с мочевиной 14 C невелико. , нет лучшего, и, по мнению авторов, тест противопоказан детям, беременным и, возможно, женщинам детородного возраста.Уровень радиационного воздействия приблизительно эквивалентен дневному фоновому излучению, но поскольку этикетка потенциально может быть включена в пул бикарбоната, а период полураспада большой, долгосрочные эффекты непредсказуемы. Дыхательный тест с карбамидом 13 оказался чрезвычайно надежным и дает удовлетворительные результаты; большинство возможных модификаций было испробовано. Тест представляет собой качественный анализ фермента уреазы. Концепции, лежащие в основе теста, просты, как и факторы, которые могут привести к ложноположительным или ложноотрицательным результатам, а именно:
Рекомендуемые статьиЦитирующие статьи (0) Полный текстCopyright © 2000 W. B. Saunders Company. Опубликовано Elsevier Inc. Все права защищены. Рекомендуемые статьиЦитирующие статьи13 Расчет пороговых значений дыхательного теста на C-мочевину и оценка для выявления инфекции Helicobacter pylori у детей | BMC GastroenterologyDrumm BB: Helicobacter pylori у педиатрического пациента. Гастроэнтерол Clin North Am. 1993, 22: 169-82. CAS PubMed Google Scholar Прието Г., Поланко И., Ларраури Дж., Рота Л., Лама Р., Карраско С. Инфекция Helicobacter pylori у детей: клинические, эндоскопические и гистологические корреляции. J Педиатр Гастроэнтерол Нутр. 1992, 14: 420-5. CAS Статья PubMed Google Scholar Vandenplas Y, Blecker U, Devreker T, Keppens E, Nijs J, Cadranel S, Pipeleers Marichal M, Goossens A, Lauwers S: вклад дыхательного теста с мочевиной 13 в выявление гастрита Helicobacter pylori у детей. Педиатрия. 1992, 90: 608-611. CAS PubMed Google Scholar Thijs JC, van Zwet AA, Thijs WJ, Oey HB, Karrenbeld A, Stellaard F, Luijt DS, Meyer BC, Kleibeuker JH: Диагностические тесты на Helicobacter pylori: предполагаемая оценка их точности, без выбора единый тест как золотой стандарт.Am J Gastroenterol. 1996, 91: 2125-2129. CAS PubMed Google Scholar Логан Р.П.: Дыхательные тесты на мочевину при лечении инфекции Helicobacter pylori. Кишечник. 1998, 43: S47-S50. Артикул PubMed PubMed Central Google Scholar Graham DY, Klein PD, Evans DJ, Evans DG, Alpert LC, Opekun AR, Boutton TW: Campylobacter pylori обнаруживается неинвазивно с помощью дыхательного теста 13 с С-мочевиной.Ланцет. 1987, 1: 1174-1177. 10.1016 / S0140-6736 (87) 92145-3. CAS Статья PubMed Google Scholar Klein PD, Graham DY: Минимальные требования к анализу для обнаружения инфекции Helicobacter pylori с помощью дыхательного теста 13 C-urea. Am J Gastroenterol. 1993, 88: 1865-1869. CAS PubMed Google Scholar Кляйн П., Малати Х., Мартин Р., Грэм К., Гента Р., Грэм Д.: Неинвазивное обнаружение инфекции Helicobacter pylori в клинической практике: дыхательный тест с мочевиной C 13 .Am J Gastroent. 1996, 91: 690-694. CAS PubMed Google Scholar Megraud F: Преимущества и недостатки современных диагностических тестов для обнаружения Helicobacter pylori. Scand J Gastroenterol Suppl. 1996, 215: 57-62. CAS Статья PubMed Google Scholar Mion F, Delecluse HJ, Rousseau M, Berger F, Brazier JL, Minaire Y: 13 Дыхательный тест на C-мочевину для диагностики инфекции Helicobacter pylori.Сравнение с гистологией. Гастроэнтерол Clin Biol. 1994, 18: 1106-1111. CAS PubMed Google Scholar Мион Ф., Рознер Дж., Руссо М., Минер Й .: 13 Дыхательный тест с С-мочевиной на Helicobacter pylori: определение пороговой точки с помощью кластерного анализа. Clin Sci. 1997, 93: 3-6. CAS Статья PubMed Google Scholar Катлер А.Ф., Хавстад С., Ма С.К., Блазер М.Дж., Перес Перес Г.И., Шуберт Т.Т .: Точность инвазивных и неинвазивных тестов для диагностики инфекции Helicobacter pylori.Гастроэнтерология. 1995, 109: 136-141. CAS Статья PubMed Google Scholar Эльтуми М., Брютон М.Дж., Фрэнсис Н.: Диагностика гастрита Helicobacter pylori у детей с помощью дыхательного теста с мочевиной 13 C. J Clin Gastroenterol. 1999, 28: 238-240. 10.1097 / 00004836-1990-00010. CAS Статья PubMed Google Scholar Rowland M, Lambert I, Gormally S, Daly LE, Thomas JE, Hetherington C, Durnin M, Drumm B: Carbon 13 Дыхательный тест на мочевину с меткой для диагностики инфекции Helicobacter pylori у детей. J Pediatr. 1997, 131: 815-820. CAS Статья PubMed Google Scholar Bazzoli F, Cecchini L, Corvaglia L, Dall’Antonia M, De Giacomo C, Fossi S, Casali LG, Gullini S, Lazzari R, Leggeri G, Lerro P, Valdambrini V, Mandrioli G, Marani M , Martelli P, Miano A, Nicolini G, Oderda G, Pazzi P, Pozzato P, Ricciardiello L, Roda E, Simoni P, Sottili S, Zagari RM: Валидация дыхательного теста C-мочевины 13 для диагностики Helicobacter pylori у детей: многоцентровое исследование.Am J Gastroenterol. 2000, 95: 646-650. 10.1016 / S0002-9270 (99) 00895-3. CAS Статья PubMed Google Scholar Томас Дж. Э., Дейл А., Хардинг М., Кауард В. А., Коул Т. Дж., Салливан П. Б., Кэмпбелл Д. И., Уоррен Б. Ф., Уивер Л. Т.: Интерпретация теста на дыхание с мочевиной 13 среди большой популяции детей младшего возраста из развивающейся страны. Pediatr Res. 1999, 46: 147-151. CAS Статья PubMed Google Scholar Кехрт Р., Беккер М., Брёзике Н., Крюгер Н., Хельге Х: Распространенность инфекции Helicobacter pylori у никарагуанских детей с постоянной диареей, диагностированная с помощью дыхательного теста 13 C-мочевина. J Педиатр Гастроэнтерол Нутр. 1997, 25: 84-88. 10.1097 / 00005176-199707000-00014. CAS Статья PubMed Google Scholar Caspary WF, Arnold R, Bayerdorffer E, Behrens R, Birkner B, Braden B, Domschke W, Labenz J, Koletzko S, Malfertheiner P, Menge H, Rosch W., Schepp W, Strauch M, Stolte M : Диагностика и терапия инфекции Helicobacter pylori.Рекомендации Немецкого общества пищеварительных и метаболических заболеваний. З. Гастроэнтерол. 1996, 34: 392-401. CAS PubMed Google Scholar Wand M: Выбор ширины ячейки гистограммы на основе данных. Американский статистик. 1997, 51: 59-64. Google Scholar Венейблс В., Рипли Б. Современная прикладная статистика с S-Plus. Нью-Йорк, Спрингер. 1997, 2 Google Scholar Nagelkerke NJ, Fidler V, Buwalda M: Инструментальные переменные в оценке процедур диагностических тестов, когда истинное состояние болезни неизвестно. Stat Med. 1988, 7: 739-744. CAS Статья PubMed Google Scholar Шао Дж., Дуншэн Т.: складной нож и бутстрап. Нью-Йорк, Спрингер. 1995 Google Scholar Hanley JA, McNeil BJ: Значение и использование площади под кривой рабочей характеристики приемника (ROC).Радиология. 1982, 143: 29-36. CAS Статья PubMed Google Scholar Kalach N, Briet F, Raymond J, Benhamou PH, Barbet P, Bergeret M, Senouci L, Maurel M, Flourie B, Dupont C: дыхательный тест на углекислый газ 13 для неинвазивного обнаружения Helicobacter pylori у детей: сравнение с культурой и определение минимальных требований к анализу. J Педиатр Гастроэнтерол Нутр. 1998, 26: 291-296.10.1097 / 00005176-199803000-00010. CAS Статья PubMed Google Scholar Киндерманн А, Деммельмайр Х, Колецко Б., Краусс-Эчманн С., Вибеке Б., Колецко С. Влияние возраста на 13 Результаты дыхательного теста на содержание С-мочевины у детей. J Педиатр Гастроэнтерол Нутр. 2000, 30: 85-91. 10.1097 / 00005176-200001000-00023. CAS Статья PubMed Google Scholar В Китае рекомендуется диапазон повторного тестирования для дыхательных тестов с мочевиной 13C и 14C на инфекцию Helicobacter pylori | Патогены кишечникаОбзор всего исследованияСхема экспериментальной программы показана на рис.1. Рис. 1Обзор всего исследования Развитие исследованияВо время клинической практики мы заметили, что некоторые результаты UBT противоречили результатам, определенным с помощью гистопатологического исследования, что побудило нас пересмотреть диагностическую эффективность из 13 C-UBT и 14 коммерческих наборов C-UBT, используемых для скрининга инфекции H. pylori в нашей больнице. Определение критериев исследованияСледующие критерии исключения были применены к нашим испытуемым: (i) предыдущее лечение H.pylori , (ii) получал ингибитор протонной помпы, антагонист рецептора H 2 , отхаркивающее средство или лечение антибиотиками в течение последних четырех недель до эндоскопии, (iii) хирургия желудка в анамнезе, (iv) диагностировали рак желудочно-кишечного тракта, ( v) имел тяжелое заболевание сердца, легких, печени, почек или системы крови, (vi) в возрасте до 18 или старше 70 лет и (vii) беременность. Одобрение этикиЭто исследование было одобрено комитетом по этике исследований Народной больницы Шэньчжэнь Куйчун (номер ссылки.201609) и зарегистрирован на сайте www.chictr.org.cn (Регистрационный номер ChiCTR2000041570). Каждого пациента гастроэнтеролог подробно ознакомил с целью и процессом исследования. Письменное и информированное согласие было получено от всех пациентов до их участия в исследовании. Исследуемая популяцияС января 2017 г. по ноябрь 2018 г., после применения критериев исключения, 484 пациента (18–70 лет), которые посетили Народную больницу Шэньчжэнь Куйчун (26 Kuixin N Road, Dapeng New District, Город Шэньчжэнь, Китай) для эндоскопического обследования согласились участвовать в этом исследовании. Перед сеансом эндоскопии пациенты получили либо 13 C-UBT, либо 14 C-UBT по усмотрению гастроэнтеролога с использованием метода чередования. Общая информация о состоянии здоровья пациентов была собрана клиническими медсестрами. Во время эндоскопии были собраны два образца биопсии желудка (по одному из антрального отдела и тела) для гистопатологического исследования. Гистологическое исследование было выполнено Клинической лабораторией Даань, сторонним поставщиком услуг патологии.{2} \ left ({1 – Prev} \ right)}} \) где Z, значение нормального распределения, было установлено равным 1,96, что соответствует 95% доверительному интервалу, и d , максимально допустимая ширина 95% доверительный интервал был установлен на 10%. На основании предыдущего исследования было показано, что UBT достигает значения чувствительности 96% и значения специфичности 93% [10]. Уровень распространенности (Prev) H. pylori в Шэньчжэне, Китай, составил 35,85% [11]. Исходя из вышеперечисленных критериев, для этого исследования требовалось не менее 41 H.pylori -положительных пациентов (n1) и 39 H. pylori -отрицательных пациентов (n2), что дает минимальный общий размер выборки 80 участников для каждого теста UBT. Дыхательный тест на мочевину13 C-UBTТест 13 C-UBT (Beijing Boran Pharmaceutical Co. Ltd., Китай) был выполнен в соответствии с инструкциями производителя. Вкратце, у каждого пациента после голодания в течение не менее четырех часов перед приемом капсулы, содержащей 50 мг меченой изотопом 13 C мочевины, был взят образец исходного дыхания с 80–100 мл воды.После 30 мин сидения выдыхаемый воздух снова собрался. Содержание 13 CO 2 в начальной и 30-минутной воздушной подушке выдоха анализировали с помощью инфракрасного спектрометра HG-IRIS13C (Beijing Richen-Force Science & Technology Co., Китай). После 30 минут введения значение дельта относительно исходного уровня (DOB), равное 4% или выше, рассматривалось как положительный индикатор инфекции H. pylori . 14 C-UBTМодель 14 C-UBT (Zhonghe Headway Bio-Sci & Tech Co.Ltd., Китай) выполнялась согласно инструкции производителя. Вкратце, пациентов, голодавших не менее четырех часов, просили проглотить желатиновую капсулу, содержащую 0,75 мкКи изотопа 14 C, с 20 мл воды. Через 25 минут каждого пациента просили непрерывно выдыхать в бутылку до тех пор, пока пурпурная удерживающая жидкость CO 2 внутри не станет бесцветной. Затем добавляли сцинтилляционную жидкость, и в гомогенизированном растворе измеряли количество 14 CO 2 .Показание с более чем 100 распадами в минуту (DPM) было классифицировано как H. pylori положительным. ГистопатологияДва образца биопсии желудка (по одному из антрального отдела и тела) были отправлены в Клиническую лабораторию Даань (Гуанчжоу, Китай) для гистопатологического исследования. Гистопатологи не знали результатов UBT. Присутствие микроорганизма, подобного Helicobacter-, подтверждали стандартным окрашиванием гематоксилином и эозином (HE). Окрашивание по Гимзе выполняли дополнительно, если HE не мог подтвердить присутствие H.pylori , и у тех пациентов, у которых был хронический активный гастрит, но не было обнаружено H. pylori в пятнах HE. Статистический анализЗначения чувствительности и специфичности каждого метода UBT были представлены в соответствии с рекомендованным производителем пороговым значением. Чтобы оценить диагностические возможности каждого метода UBT, была построена кривая рабочей характеристики приемника (ROC) путем нанесения истинно-положительного показателя на оси y против истинно-отрицательного показателя на оси x [12].Наш ROC-анализ был выполнен с использованием пакета R pROC (версия 1.16.2) [13]. Площадь под кривой (AUC) была рассчитана для количественной оценки общей точности каждого метода UBT для диагностики исходов инфекции H. pylori . Оптимальное значение отсечки UBT, которое дает наивысшую частоту истинных положительных результатов вместе с самой низкой частотой ложных срабатываний, было определено с использованием метода максимального индекса Юдена, где индекс Юдена = чувствительность + специфичность – 1 [14]. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||




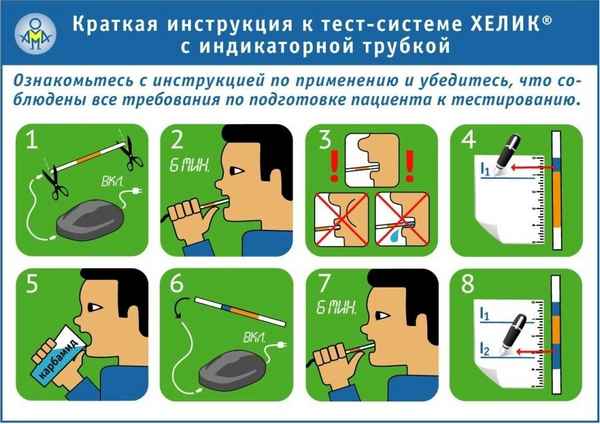 J Clin Lab Anal. 2019;33:e22674.
J Clin Lab Anal. 2019;33:e22674. pylori инфекции) по истечении четырех недель после завершения терапии.
pylori инфекции) по истечении четырех недель после завершения терапии.
 Причём только ориентируясь на симптомы. Поэтому многие пациенты, почувствовав боль в желудке, тут же приписывают себе эту болезнь. Как на самом деле распознать недуг и отличить его от других опасных заболеваний, рассказала заместитель главного врача по медицинской части федеральной сети медицинских центров «МЛЦ» в Краснодаре, врач-гастроэнтеролог, врач-терапевт Инна Мазько.
Причём только ориентируясь на симптомы. Поэтому многие пациенты, почувствовав боль в желудке, тут же приписывают себе эту болезнь. Как на самом деле распознать недуг и отличить его от других опасных заболеваний, рассказала заместитель главного врача по медицинской части федеральной сети медицинских центров «МЛЦ» в Краснодаре, врач-гастроэнтеролог, врач-терапевт Инна Мазько.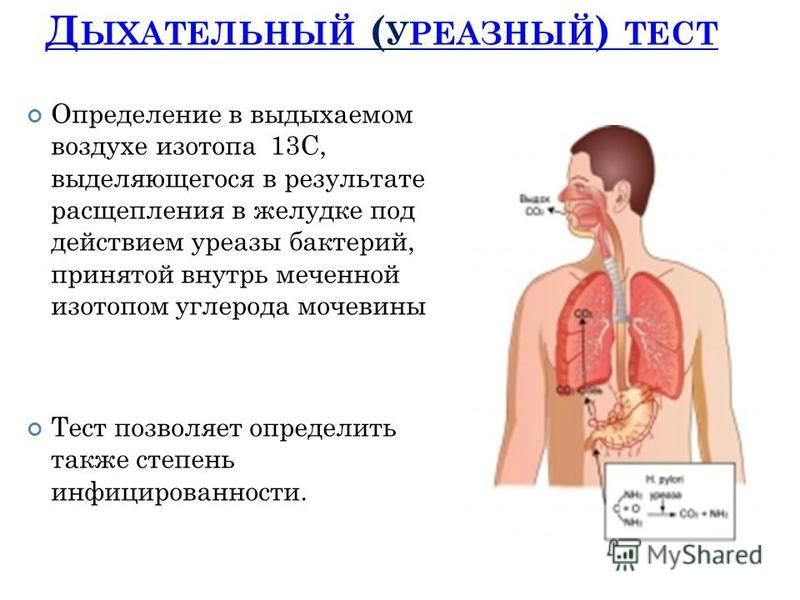
 5)
5) 28
28 Поэтому неудивительно, что величина DOB коррелировала с плотностью H. pylori , измеренной с помощью ПЦР, а также со степенью хронического активного воспаления, о чем свидетельствует инфильтрация лимфоцитов и нейтрофилов в слизистой оболочке желудка [16 –25, 32]. Величина ДОБ также коррелировала с частотой и интенсивностью диспепсии [33]. С другой стороны, атрофия слизистой оболочки желудка связана со снижением бактериальной плотности [34, 35].Отсюда следует, что пациенты с большей степенью атрофии слизистой оболочки желудка имеют более низкую величину DOB [23, 32]. Низкое соотношение PGI / II, указывающее на атрофию желудка, также коррелировало с более низкой величиной DOB [32]. Следует отметить, однако, что другие исследования не обнаружили связи между плотностью бактерий и величиной DOB, хотя эти исследования не включали оценку хронического активного воспаления [36, 37].
Поэтому неудивительно, что величина DOB коррелировала с плотностью H. pylori , измеренной с помощью ПЦР, а также со степенью хронического активного воспаления, о чем свидетельствует инфильтрация лимфоцитов и нейтрофилов в слизистой оболочке желудка [16 –25, 32]. Величина ДОБ также коррелировала с частотой и интенсивностью диспепсии [33]. С другой стороны, атрофия слизистой оболочки желудка связана со снижением бактериальной плотности [34, 35].Отсюда следует, что пациенты с большей степенью атрофии слизистой оболочки желудка имеют более низкую величину DOB [23, 32]. Низкое соотношение PGI / II, указывающее на атрофию желудка, также коррелировало с более низкой величиной DOB [32]. Следует отметить, однако, что другие исследования не обнаружили связи между плотностью бактерий и величиной DOB, хотя эти исследования не включали оценку хронического активного воспаления [36, 37].