Антибиотик убивающий хеликобактер пилори: все современные методы эрадикационной терапии
РЕЗИСТЕНТНОСТЬ HELICOBACTER PYLORI К АНТИБАКТЕРИАЛЬНЫМ ПРЕПАРАТАМ: СОВРЕМЕННОЕ СОСТОЯНИЕ ПРОБЛЕМЫ
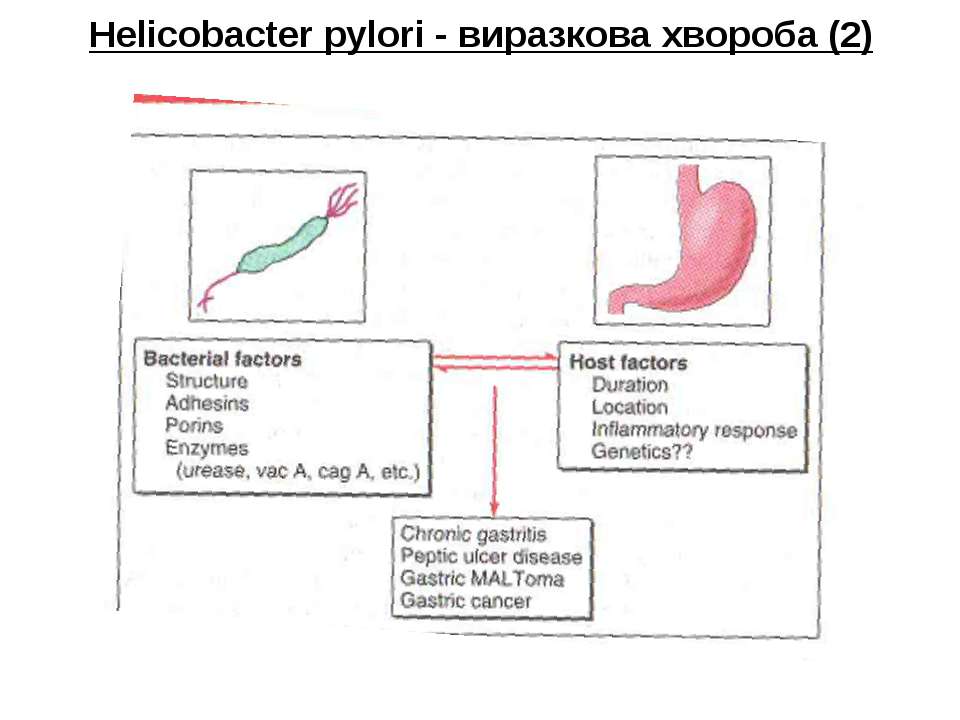
В настоящее время доказан факт определенной этиологической и патогенетической роли бактерий Helicobacter pylori (НР) в развитии распространенных заболеваний — острого и хронического гастрита, язвенной болезни желудка и двенадцатиперстной кишки, образовании некоторых видов опухолей желудка (МALT-лимфомы, аденокарциномы), диспепсии неязвенной этиологии (Hant R.N., 1994).
Наличие НР в большинстве случаев при этих заболеваниях и их влияние на организм человека дали основание считать их патогенетически связанными и получили название заболеваний, ассоциированных с НР (Noach L., Tytgat G., 1994).
Так, бактерии НР выявляют у 80—100% больных с хроническим гастритом, у 70–80% — с язвой желудка, у 90–100% — с язвой двенадцатиперстной кишки, у 100% — с МALT-лимфомой, у 80–95% — с аденокарциномой желудка, у 60% — с диспепсией неязвенной этиологии (Moran P.
Элиминация бактерий НР после проведения успешной терапии способствует полной или частичной регенерации слизистой оболочки в гастродуоденальной зоне (Axon A.T.R., 1996; Hulst R.W.M. et al., 1996; Pounder R.E., Williams M.P., 1997; Vautier G., 1997).
Общепринято, что при заболеваниях, ассоциированных с инфекцией НР, необходимо проводить антихеликобактерную терапию. В 1996–1997 гг. были предложены единые стандартные схемы антихеликобактерной терапии (Европейский Маастрихтский консенсус, Американская Интернациональная конференция фонда здоровья, Азиатский консенсус) с использованием 2 или 3 антимикробных препаратов и 1 антисекреторного (препарат висмута, антибиотики: кларитромицин, амоксициллин, тетрациклин или метронидазол и блокатор Н+/К+-АТФазы) (Consensus conference Helicobacter pylori peptic ulcer disease, 1994; The European Maastricht Consensus, 1997; Lam S.K., Talley N.J., 1998).
По усредненным данным эффективность официально рекомендованных схем лечения заболеваний органов пищеварения, ассоциированных с НР, составляет от 65 до 87%, но в большинстве случаев зависит от чувствительности НР к применяемым антибактериальным препаратам (Hant R. N., 1997; Graham D.Y., Dore M.P., 1998).
N., 1997; Graham D.Y., Dore M.P., 1998).
Резистентность патогенных микроорганизмов к применяемым антибактериальным препаратам является весьма актуальной проблемой. Это связано с неуклонным повышением резистентности, которая в последние годы приобрела глобальный характер (Glupczynski Y., 1998).
В полной мере это относится и к заболеваниям, ассоциированным с НР, базисное лечение которых по сути сводится к уничтожению возбудителей этой инфекции. В последние годы такое лечение становится все более сложным, поскольку количество штаммов НР
Резистентные штаммы НР значительно труднее поддаются эрадикации (уничтожению), что снижает на 20–50% эффективность рекомендованных лечебных схем и делает их экономически невыгодными (Иванников И.А., 1998). Так, именно с повышением резистентности НР к антибактериальным препаратам связывают рост заболеваний и осложнений, обусловленных патологией органов гастродуоденальной зоны, а следовательно — значительное увеличение затрат на лечение, что является не только медицинской, но и социально-экономической проблемой.
Установлено, что НР резистентны к антибактериальным препаратам групп нитроимидазолов, макролидов, фторхинолонов, производных рифампицина, полусинтетических пенициллинов. Известно, что развитие первичной резистентности микроорганизмов к тем или иным антибактериальным препаратам зависит от частоты их применения у населения конкретного региона. Развитие первичной резистентности НР к этим препаратам связывают с их довольно частым применением при инфекционных и респираторных заболеваниях. Вторичная резистентность бактерий развивается вследствие проведения антихеликобактерной терапии.
Распределение антибактериальных препаратов, рекомендованных для антихеликобактерной терапии в зависимости от частоты развития к ним резистентности НР
Препараты | Максимальные показатели развития резистентности |
Часто возникает резистентность | |
| Группа нитроимидазолов: метронидазол тинидазол | 100% |
| Группа макролидов: кларитромицин | |
| Группа фторхинолонов: офлоксацин норфлоксацин ципрофлоксацин | 30% |
Редко возникает резистентность | |
| Полусинтетические пенициллины: амоксициллин | 7% |
| Тетрациклины: тетрациклина гидрохлорид доксациклина гидрохлорид | 5% |
Резистентность не развивается | |
| Группа нитрофуранов: фурадонин фуразолидон | |
| Соли коллоидного висмута: висмута субцитрат висмута субгалат висмута субсалицилат | |
Таблица 2
Эффективность существующих схем антихеликобактерной терапии при разной резистентности НР к метронидазолу и кларитромицину (Tytgat G. N.J., 1998)
N.J., 1998)
Первичная резистентность | Схемы терапии | Эффективность, % |
М менее 30% | О+К+А О+К+М РВЦ/ВК+К+М | 85–95 |
M более 30% K менее 15% | O+K+A РВЦ/ВК+К+А | 85–95 |
M более 30% K более 15% | О+ВК+М+Т О+ВК+М+Т | 50–95 |
Примечание. М — метронидазол, К — кларитромицин, О — омепразол, А — амоксициллин, РВЦ — ранитидин — висмут — цитрат, ВК — коллоидный висмут, Т —тетрациклин.
Наиболее высокая резистентность НР развивается к производным нитроимидазола — метронидазолу и тинидазолу. В развитых странах первичная резистентность НР к нитроимидазолам составляет 30–35%, что связано с частым применением в гинекологии и венерологии, в развивающихся странах — 50–60%, где его также применяют при часто возникающих амебиазе, лямблиозе, трихомониазе.
Так, в странах Африки, Латинской Америки, Юго-Восточной Азии первично-резистентные к нитроимидазолу штаммы НР в популяции составляют от 50 до 100% (Lee A., Megraud F., 1996).
В странах Восточной Европы с невысоким уровнем жизни (в том числе и в странах СНГ) первично-резистентные к нитроимидазолу штаммы НР составляют 20–40%; в России к метронидазолу — почти 30%, в Москве — 36% (Кудрявцева Л.В., 1998).
В странах Западной Европы, по данным Европейского многоцентрового исследования, средний уровень первичной резистентности НР к метронидазолу составляет 25,6% (European Study Group on Antibiotic Susceptibility of Helicobacter pylori, 1992).
Вторичная резистентность НР к используемым антибиотикам, как правило, обусловлена неадекватным лечением: заниженными дозами препаратов, применением неполных схем лечения (с использованием двух препаратов), несоблюдением сроков лечения и кратности приема или неправильной оценкой эффективности эрадикации. Предполагают, что механизм развития повторной резистентности НР связан с мутациями бактерий.
Повторная резистентность к нитроимидазолам в развитых странах в 1996 р. составила 50% (Megraud F. et al., 1994), а в развивающихся — 80–100%. Так, бесконтрольное использование метронидазола при лечении пациентов с язвенной болезнью привело к повышению вторичной резистентности в Гонконге с 22 в 1991 г. до 73,2% в 1995 г. (Ling T.K.W. et al., 1996). В России вторичная резистентность к метронидазолу у больных, которым проводили антихеликобактерную терапию по поводу язвенной болезни, составила 100% (Кудрявцева Л.В., 1998).
Уровень первичной резистентности НР к макролидам, например к кларитромицину, в Европе составляет 2–15%, что, вероятно, связано с частым использованием препаратов этой группы для лечения больных с респираторными инфекциями (Versalovic G. et al., 1995).
et al., 1995).
В развивающихся странах, где кларитромицин применяют нечасто, резистентность к нему значительно ниже или еще не выявлена. По данным Российской Группы по изучению НР, первичная резистентность бактерий к этому препарату не выявлена. Вторичная резистентность НР к кларитромицину в развитых странах достигает 40%, в России — пока не обнаружена (Кудрявцева Л.В., 1998).
Первичная резистентность НР к фтoрхинолонам (ципрофлоксацину, офлоксацину, норфлоксацину) составляет в среднем 1% (Меgraud F., 1995). Наряду с этим, определена довольно высокая вторичная резистентность бактерий к фторхинолонам — 30% в развитых странах. Данных о резистентности НР к препаратам этой группы в развивающихся странах нет.
Данных о первичной резистентности НР к препаратам группы рифампицина пока нет. Имеются единичные сообщения о развитии вторичной резистентности бактерий к препаратам этой группы, составляющей 5%, что, возможно, связано с довольно редким включением их в схемы антихеликобактерной терапии (Меgraud F.
В последнее время не сообщалось о выделении в странах Западной Европы штаммов НР, резистентных к полусинтетическим пенициллинам (амоксициллину), тетрациклинам, нитрофуранам.
В 1997 г. впервые сообщалось о появлении резистентных к амоксициллину штаммов НР, составивших 7% в развитых странах. Российская Группа по изучению НР в 1998 г. сообщила о выделении резистентных к амоксициллину штаммов НР, что составило 11% (Кудрявцева Л.В., 1998).
Почти полное отсутствие или низкая резистентность бактерий к кларитромицину, амоксициллину и фторхинолонам у населения развивающихся стран связана с ограниченным применением этих средств, поскольку указанные препараты не производятся промышленностью этих стран, а стоимость экспортируемых препаратов высока.
Отмечена довольно низкая резистентность (не более 5%) НР к препаратам группы тетрациклина у населения как в развитых, так и в развивающихся странах, хотя эти средства довольно часто применяются (Hant R. N., 1997).
N., 1997).
Не определена резистентность бактерий НР к препаратам нитрофуранового ряда, а также к препаратам коллоидного висмута.
Известно, что препараты, содержащие висмут, в частности Де-нол, для лечения пациентов с язвенной болезнью применяют в течение нескольких десятилетий, однако резистентность к нему НР до сих пор не выявлена.
Распределение антибактериальных препаратов в зависимости от частоты развития резистентности к ним HР
Антибактериальные препараты, применяемые для эрадикации НР, условно можно разделить на следующие группы (табл. 1): средства, к которым резистентность НР развивается часто; редко; не возникает вовсе.
Частота резистентности НР неодинакова в разных регионах. Например, резистентность к метронидазолу в странах Европы составляет 45% — в Германии, 30% — во Франции, 80% — в Албании. Причем отмечается тенденция к неуклонному ее повышению.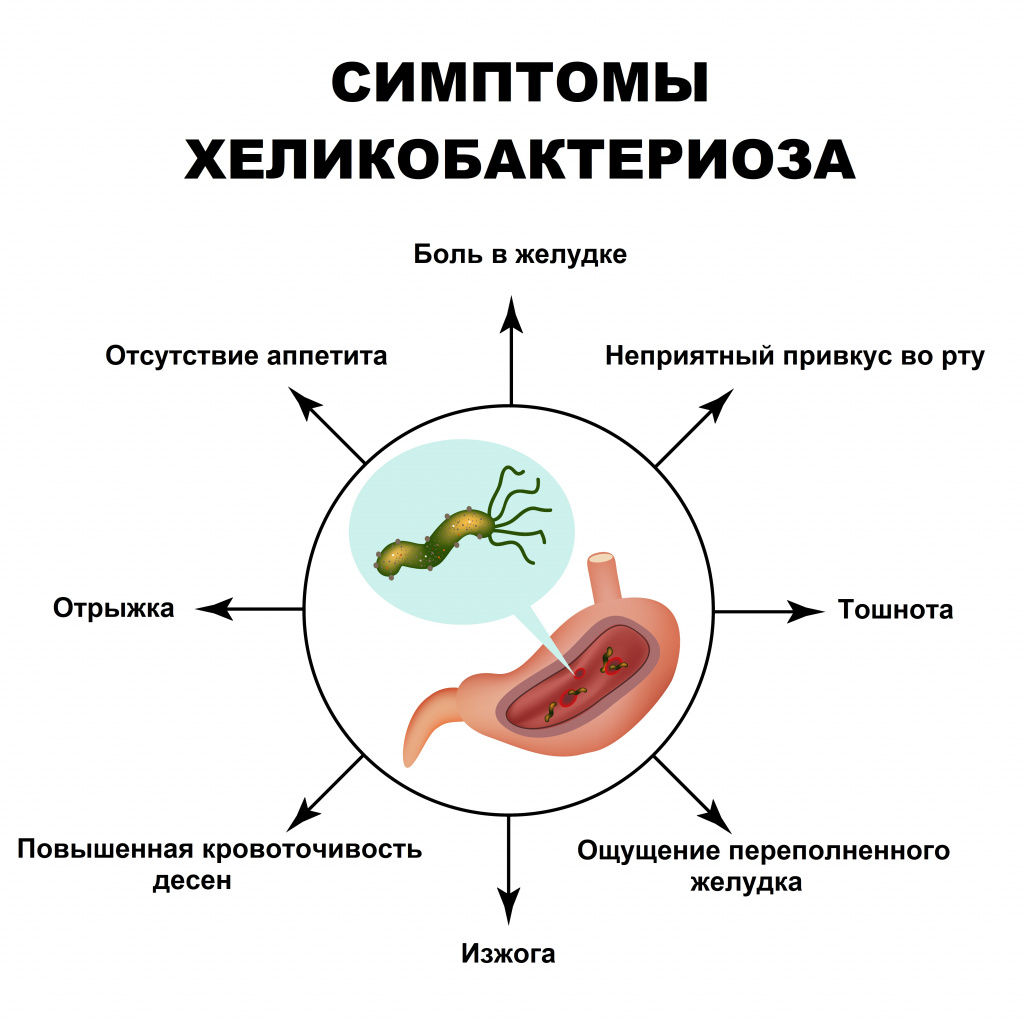 Так, в странах Западной Европы резистентность НР к метронидазолу возросла с 31,8 в 1991 г. до 46% в 1995 г., к кларитромицину — от 0 до 8,5% в 1997 г. (во Франции — 10%, в США — 7%) (Hant R.N., 1997).
Так, в странах Западной Европы резистентность НР к метронидазолу возросла с 31,8 в 1991 г. до 46% в 1995 г., к кларитромицину — от 0 до 8,5% в 1997 г. (во Франции — 10%, в США — 7%) (Hant R.N., 1997).
Пути преодоления резистентности HP к антибактериальным препаратам
Для повышения эффективности эрадикации бактерий необходим дифференцированный подход к применению существующих стандартных схем антихеликобактерной терапии. Состав препаратов, входящих в схемы терапии, необходимо изменять с учетом данных о частоте выявления резистентных штаммов бактерий в разных регионах и локальной резистентности НР к каждому из применяемых препаратов.
Так, при резистентности НР к метронидазолу более 30% в популяции в схему лечения этот препарат не включают, используют кларитромицин и амоксициллин в сочетании с препаратами коллоидного висмута. При высокой резистентности к метронидазолу (более 30%) и одновременно к кларитромицину (более 15%) рекомендуют одновременное применение четырех препаратов («квадротерапия») — блокатор Н+/К+-АТФазы+препарат висмута+метронидазол+тетрациклин (табл. 2) (Передерий В.Г., 1997).
2) (Передерий В.Г., 1997).
Необходимо отметить, что такая дифференцированная терапия допускает определение чувствительности и резистентности НР к назначаемым препаратам.
Наряду с существующими рекомендациями, идет постоянный поиск более эффективных схем антихеликобактерной терапии с учетом изменяющейся резистентности НР и создание новых антихеликобактерных средств, к которым не развивается резистентность.
Результаты исследования последних лет свидетельствуют, что повышение доз антибактериальных средств не преодолевает резистентность бактерий, а только приводит к увеличению частоты побочных эффектов.
В Украине пока не разработан единый подход к антихеликобактерной терапии. Нет единого стандарта для диагностики и лечения заболеваний, ассоциированных с НР, с учетом географических, этнических, социальных и экономических особенностей. Некоторые ученые продолжают пропагандировать устаревшие способы лечения, например язвенной болезни, без применения антибактериальных препаратов, многие специалисты продолжают назначать репаранты и М-холинолитики, а при хроническом гастрите типа В — антациды. Антихеликобактерную терапию, как правило, проводят с использованием метронидазола.
Антихеликобактерную терапию, как правило, проводят с использованием метронидазола.
Все это обусловлено в значительной мере тем, что в Украине не проводят многоцентровые исследования по изучению распространенности и выявляемости НР в популяции в целом и при заболеваниях органов гастродуоденальной зоны, в частности. Нет данных о частоте выявления инфекции НР при гастрите типа В, язвенной болезни желудка и двенадцатиперстной кишки, диспепсии неязвенной этиологии; вирулентных штаммах НР и их распространенности; локальной резистентности бактерий к антибактериальным препаратам, в том числе к метронидазолу и др.; обобщенных данных о частоте неэффективной эрадикации бактерий после применения того или другого варианта терапии. Не изучена частота рецидивов инфекции НР и реинфицирования после успешного лечения.
Результаты наших исследований, проводимых в отделе гастроэнтерологии Института терапии АМН Украины (под руководством проф. О.Я. Бабак) в течение 10 лет, свидетельствуют, что частота инфицирования НР весьма высока не только среди больных с патологией органов пищеварения, но и при других заболеваниях — атеросклерозе, гипертонической болезни, вегетососудистой дистонии и достигает 83%. При обострении воспалительных заболеваний верхних отделов пищеварительного тракта частота определения НР достигает 94%. При этом выявлена высокая частота резистентности к производным нитроимидазолов — в 98% (исследования проводили только у жителей Харьковского региона).
При обострении воспалительных заболеваний верхних отделов пищеварительного тракта частота определения НР достигает 94%. При этом выявлена высокая частота резистентности к производным нитроимидазолов — в 98% (исследования проводили только у жителей Харьковского региона).
Однако, с нашей точки зрения, вероятность формирования резистентности НР к антибактериальным препаратам может быть снижена. Этого возможно достичь путем повышения эффективности антихеликобактерной терапии.
Прежде всего необходимо исключить применение исходных нитроимидазолов в схеме тройной антихеликобактерной терапии, поскольку, очевидно, в нашей стране резистентность НР к препаратам этой группы превышает 30%.
В связи с тем что к препаратам коллоидного висмута, в частности к Де-нолу, резистентность НР не выявлена, целесообразно его включение в большинство схем антихеликобактерной терапии.
Благодаря действию Де-нола на НР (угнетение его адгезии в эпителий слизистой оболочки в гастродуоденальной зоне, нарушение метаболизма бактерий, что приводит к их гибели), и практически полному отсутствию резистентности, препарат на сегодня остается базовым, то есть основным компонентом при составлении схем антихеликобактерной терапии. Доза препарата должна составлять 240 мг при приеме 2 раза в день.
Доза препарата должна составлять 240 мг при приеме 2 раза в день.
Весьма перспективно включение в схемы лечения препаратов нитрофуранового ряда — фурадонина и фуразолидона, поскольку резистентность НР к ним также до сих пор не выявлена. Опубликованы данные (Segura A.M. et al., 1997) об успешном применении фуразолидона при лечении больных с резистентными штаммами НР к метронидазолу. Применяли висмута субцитрат в дозе 240 мг 2 раза, фуразолидон — по 100 мг 4 раза, амоксициллин — по 500 мг 4 раза в сутки, курс лечения — 2 нед). Эрадикация НР достигнута в 6% случаев. Представленная схема лечения эффективна, имеет невысокую стоимость, поэтому лечение доступно для населения стран с невысоким уровнем жизни.
Перспектива усовершенствования схем антихеликобактерной терапии и повышение частоты эрадикации НР с учетом чувствительности и резистентности бактерий к препаратам, этнических, географических особенностей каждой популяции и экономических возможностей позволяет надеяться на возможность замедления повышения резистентности НР к проводимой терапии.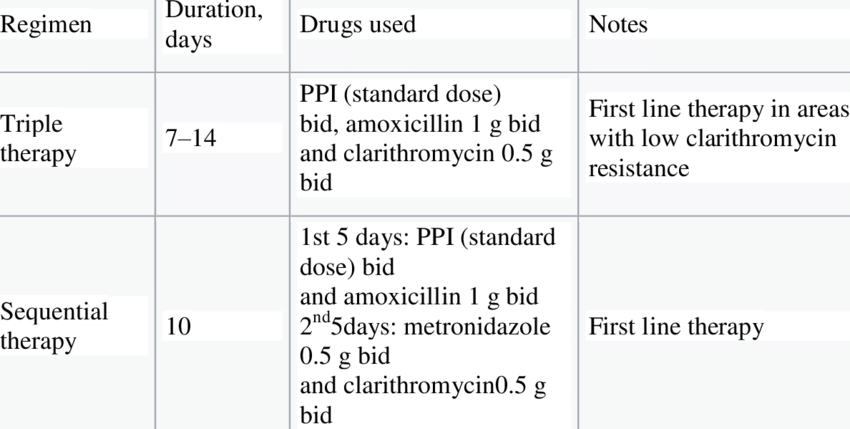
Ссылки
- 1. Иваницкий И.О. (1998) Проблема преодоления резистентности штаммов Helicobacter pylori. В кн.: Материалы 7-й сессии Российской Группы по изучению Helicobacter pylori, 27–28 мая 1998 г., Нижний Новгород, с. 34–36.
- 2. Кудрявцева Л.В. (1998) Опыт изучения антибиотикорезистентных российских штаммов Helicobacter pylori. В кн.: Материалы 7-й сессии Российской Группы по изучению Helicobacter pylori, 27–28 мая 1998 г., Нижний Новгород, с. 11–14.
- 3. Axon A.T.R. (1996) Eradication of Helicobacter pylori. Scand. J. Gastroenterol., 31 (214): 47–53.
- 4. European Study Group on Antibiotic Susceptibility of Helicobacter pylori. Results of a multicentre European Survey in 1991 of metronidasole resistance in Helicobacter pylori (1992) Eurор. J. Microbiol. Infect. Dis., 8, p. 181–185.
- 5. Glupczynski Y. (1998) Rasing antimicrobial resistance of Helicobacter pylori: A global problem Helicobacter pylori: Basic mechanisms to clinical cure. San Diego Marriott.
 Hotel & Marina, Januar 18–21, р. 43.
Hotel & Marina, Januar 18–21, р. 43. - 6. Graham D.Y., Dore M.P. (1998) Causes of variability of antimicrobial efficacy. Helicobacter pylori: Basic mechanisms to clinical cure. San Diego Marriott Hotel & Marina Januar 18–21, р. 45.
- 7. Hant R.N. (1997) Dyspepsia menagement in the year 2000 — a caseillustrated discussion. Europ. J. Clin. Res., 9: 99–103.
- 8. Helicobacter pylori. Basic Mechnisms to Clinical Cure (1994) Ed. R.N. Hant, GNJ Tytgat Kluwer Academic Publishers Lancaster, UK, 612 р.
- 9. Hulst R.W.M., Keller J., Rauws E.A.J., Tytgat G.N.J. (1996) Treatment of Helicobacter pylori infection: A Review of World Lierature. Helicobacter, 1(1): 6–19.
- 10. Lam S.K., Talley N.J. (1998) Helicobacter pylori consensus: Report of the 1997 Asia Pacific Consensus Conference on the menegement of Helicobacter pylori infection. J. Gastroenterol. Hepatol., 13: 1–12.
- 11. Lee A., Medraud F. (1996) Helicobacter pylori: techniques for clinical diagnosis and basic reseach.
 , 20–21.
, 20–21. - 12. Ling T.K.W., Cheng A.F.B., Sung J.J.Y. et al. (1996) An increase in Helicobacter pylori straint resistant to metronidasole:
- 13. A five-year study. Helicobacter, 1: 57–61.
- 14. Medraud F., Cayla R., Lamouliatte H., Bouchard S. (1994) Darmaillac Surveillance or Helicobacter pylori resistance to macrolides and nitroimidasole compounds at a national level (abstract). Amer. J. Gastroenterol., 89: 1368.
- 15. Medraud F. (1995) Rationale for the choice of antibiotics for the eradication Helicobacter pylori. Eurор. J. Gastroenterol., 1: 49–54.
- 16. National Institute of Health (1994) Consensus conference Helicobacter pylori in peptic ulcer disease. J.A.M.A., 272: 65–69.
- 17. Noach L., Tytgat G. (1994) Helicobacter pylori infection. Aspects of pathogenesis and therapy. Amsterdam, 165 p.
- 18. Pathogenesis and Host Response in Helicobacter pylori Infection Edited by Anthony P. Moran, Colm A. O’Morain (1997) NORMED, Bad Homburg, Verl.
 , p. 230–241.
, p. 230–241. - 19. Pounder R.E., Williams M.P. (1997) The treatment of Helicobacter pylori infection. Alimentary Pharmacology & Therapeutics. Apr, 11( 1): 35–41.
- 20. The European Helicobacter pylori Study Group (1997) Current European concepts in the management of Helicobacter pylori infection: The Maastricht Consensus Report. Gut, 41: 8–13.
- 21. Tytgat G.N.J. (1998) Treatment of Peptic Ulcer. Digestion, 59: 446–452.
- 22. Vautier G. (1997) Scott BBA one-week quadruple eradication regimen for Helicobacter pylori in routine clinical practice. Aliment Pharmacol Ther Feb, 11(1): 107–108.
- 23. Versalovic J., Kibler K., Smell S., Graham D.Y., Go M.F. (1995) Mutation in 23 S ribosomal RNA confer claritromycin resistance in Helicobacter pylori. Gut, 37(1): A67.
Фадеенко Галина Дмитріївна
Резюме. У статті на підставі багаторічного досвіду та аналізу сучасної літератури наведені причини розвитку первинної та вторинної резистентності Helicobacter pylori до антибактеріальних препаратів, що застосовуються. Висвітлені можливі шляхи подолання розвитку резистентності Helicobacter pylori до антибактеріальних препаратів, засоби знищення бактерій.
Висвітлені можливі шляхи подолання розвитку резистентності Helicobacter pylori до антибактеріальних препаратів, засоби знищення бактерій.
Ключові слова:Helicobacter pylori, резистентність, антигелікобактерна терапiя
Fadeуenko Galina D
Summary. Based on many years experience and analysis of modern literature the reasons of development of primary and secondary Helicobacter рylori resistance to the applied antibacterial preparations are presented. Possible ways of development overcoming of Helicobacter рylori resistance to antibacterial preparations as well as bacterias elimination are reflected.
Key words: Helicobacter pylori, resistance, antihelicobacter therapy
6 природных антибиотиков — Новости — Forbes Kazakhstan
Из-за чрезмерного употребления антибиотиков супербактерии развили к ним иммунитет, а наиболее сильные лекарства обычно имеют опасные побочные эффекты. Но мудрость природы безгранична: она создала необычайно эффективные продукты с антибактериальными, противогрибковыми и противовирусными свойствами, которые способны оградить организм от тяжёлого лечения и сохранить силы, по сведениям Наша планета.
Вам не придётся идти дальше своего холодильника или кладовки, чтобы отыскать вкусные и безопасные продукты и травы для борьбы с вирусами и самыми опасными бактериями.
1. Чеснок
Во всём мире чеснок тысячелетиями использовался в медицинских целях. Это удивительное растение лечит всё, от лёгкой боли в ухе до гриппа, золотистого стафилококка, хеликобактер пилори, пневмонии и даже чумы.
Современные исследования подтвердили, что чеснок обладает многочисленными антиоксидантами, которые уничтожают свободные радикалы и бактерий в крови, тем самым защищая и укрепляя иммунную систему.
Чеснок содержит активное вещество аллицин, способное атаковать и разрушать всевозможные вирусы, а также грибковые заболевания (в том числе кандиду) в отличие от современных антибиотиков. Употребление чеснока в целях профилактики может помочь защитить организм от различных болезнетворных микроорганизмов, препятствуя началу заболевания.
2. Эхинацея
Эхинацея столетиями используется для укрепления иммунной системы и борьбы с различными заболеваниями. Традиционно она применялась для лечения бактериальных и сифилитических поражений, заражения крови, открытых ран, целлюлита, дифтерии. Это сильное растение обладает способностью разрушать самые опасные бактерии, включая золотистый стафилококк, хотя обычно эхинацея используется для борьбы с простудой и гриппом.
Традиционно она применялась для лечения бактериальных и сифилитических поражений, заражения крови, открытых ран, целлюлита, дифтерии. Это сильное растение обладает способностью разрушать самые опасные бактерии, включая золотистый стафилококк, хотя обычно эхинацея используется для борьбы с простудой и гриппом.
3. Имбирь
Имбирь – это корнеплод, издавна используемый для лечения заболеваний дыхательных путей. Было обнаружено, что соединения, содержащиеся в этом растении, гингеролы, борются, по крайней мере, с некоторыми грамотрицательными возбудителями, а также с многочисленными болезнетворными микроорганизмами полости рта.
4. Мёд
Во всём мире мёд использовался для лечения болезней и ран задолго до того, как были разработаны искусственные антибиотики.
Мёд содержит фермент, противомикробный по своей сути, который препятствует росту отдельных видов бактерий.
В китайской медицине мёд использовался для уменьшения боли, нейтрализации токсинов, нормализации работы печени, а его антибактериальные свойства применялись в лечении бактерии хеликобактер пилори, вызывающей язву желудка.
5. Лимон
Большое количество исследований направлено на изучение антибактериальных свойств лимона.В частности было установлено, что лимон содержит тетразин и кумарин: оба соединения эффективны в борьбе с болезнетворными организмами.
Лимон, как лук и чеснок, в лечебных целях в качестве природного антибактериального продукта используется и наружно, и для внутреннего применения.
6. Ферментированные продукты
В настоящее время всё больше врачей призывают для восстановления микрофлоры (хороших бактерий), принимать в сочетании с лечением антибиотиками пробиотик. Его источником могут выступать богатые микроорганизмами квашеные овощи, которые можно приобрести в продуктовом магазине. Непастеризованная квашеная капуста, соленья и кимчи, — все эти продукты идеально подойдут, чтобы вновь обогатить ваш кишечник пробиотиками. Начинать можно с нескольких чайных ложек, постепенно увеличивая порцию.
Обнаружены новые свойства антибиотика изо рта сибирского медведя – Газета.
 Ru
RuГруппа ученых из Института биоорганической химии РАН определила перспективы использования природного аналога антибиотика амикумацина изо рта сибирского медведя и предложила оптимальный способ его массового производства. Для этого ученые использовали метод глубокого функционального профилирования (упаковки бактерий в капли), который они разрабатывали последние несколько лет. Работа опубликована в журнале Antibiotics. Исследования поддержаны Российским научным фондом (РНФ).
В современном мире наблюдается глобальное распространение устойчивости к антибиотикам: «Это возникает вследствие неграмотного и бесконтрольного использования этих препаратов. Также устойчивость может возникать у самих бактерий, что делает применение лекарств бесполезным. Например, во всем мире устойчивые к антибиотикам инфекции вызывают 31,5 миллиона случаев сепсиса, что приводит к 5,3 миллиона смертей ежегодно», — сообщает руководитель проекта по гранту РНФ Иван Смирнов, доктор химических наук, заместитель директора по науке Института биоорганической химии имени М. М. Шемякина и Ю. А. Овчинникова РАН (ИБХ РАН, Москва). Именно поэтому для медицины очень важно находить новые виды антибиотиков и проверять их эффективность против отдельных видов бактерий.
М. Шемякина и Ю. А. Овчинникова РАН (ИБХ РАН, Москва). Именно поэтому для медицины очень важно находить новые виды антибиотиков и проверять их эффективность против отдельных видов бактерий.
Амикумацин впервые описали в далеком 1981 году, но принцип и область действия антибиотика оставались неизвестными. Его применяли в основном в научных кругах. Однако несколько лет назад был обнаружен природный источник амикумацина — бактерия Bacillus pumilus, которая обитает в ротовой полости сибирского бурого медведя. Открытие возобновило интерес к этому антибиотику. В своем исследовании ученые использовали недавно изобретенный ими метод глубокого функционального профилирования, чтобы выделить наиболее эффективные штаммы Bacillus pumilus и определить спектр действия амикумацина.
«Суть метода заключается в изоляции индивидуальных бактерий в микрокаплях и их анализе на уровне единичных клеток. В отличие от стандартных методов эта технология обладает уникально высокой производительностью, что позволяет выявлять даже очень редких представителей природного или искусственного биоразнообразия. Таким образом, мы можем легко находить уникальные бактерии микробиома, обладающие антибиотической активностью по отношению к патогенам», — объясняет участник проекта по гранту РНФ Станислав Терехов, кандидат химических наук, научный сотрудник ИБХ РАН.
Таким образом, мы можем легко находить уникальные бактерии микробиома, обладающие антибиотической активностью по отношению к патогенам», — объясняет участник проекта по гранту РНФ Станислав Терехов, кандидат химических наук, научный сотрудник ИБХ РАН.
Кроме того, ученые установили наиболее благоприятные условия для широкомасштабного производства Bacillus pumilus: повышенное насыщение кислородом (аэрация), высокоуглеводная среда и микрочастицы карбоната кальция.
Дальнейшие исследования показали, что амикумацин эффективен против бактерий хеликобактер пилори, вызывающих язву желудка и гастрит, и золотистого стафилококка. Он может приводить к огромному числу заболеваний, от легких кожных инфекций до пневмонии, менингита и остеомиелита. В целом антибиотик на высоком уровне боролся со многими грамположительными бактериями. Тем не менее, у амикумацина обнаружили способность повреждать клетки тканей, которая затрудняет его использование при терапии бактериальных заболеваний. Также антибиотик не пригоден для длительного лечения из-за особенности своего строения. Он нестабилен и в физиологических условиях распадается в течение двух часов. Однако, по мнению Ивана Смирнова, нестабильность молекул не всегда является их недостатком. Для локального воздействия и снижения общей токсичности для организма быстрый «вывод из строя» высокоактивных действующих веществ более предпочтителен. Подобные стратегии все чаще находят свое практическое применение сегодня.
Он нестабилен и в физиологических условиях распадается в течение двух часов. Однако, по мнению Ивана Смирнова, нестабильность молекул не всегда является их недостатком. Для локального воздействия и снижения общей токсичности для организма быстрый «вывод из строя» высокоактивных действующих веществ более предпочтителен. Подобные стратегии все чаще находят свое практическое применение сегодня.
Не стоит забывать, что ученые работали с изначальным, природным видом антибиотика, а значит, его недостатки можно будет исправить при дальнейшем изучении.
«Очевидно, что молекула амикумацина, созданная природой, не имеет набора свойств, характерных для полусинтетических антибиотиков и цитостатических лекарственных препаратов, существующих на рынке. В то же время его структура является стартовой площадкой для создания стабильных аналогов амикумацина, направленных на уничтожение бактерий или клеток человека, позволяя перенаправить его высокий потенциал на получение новых антимикробных и противораковых препаратов. Этим и многим другим мы занимаемся совместно с нашими коллегами», — заключает Станислав Терехов.
Этим и многим другим мы занимаемся совместно с нашими коллегами», — заключает Станислав Терехов.
ᐉ 13 современных препаратов для лечения хеликобактерной инфекции (хеликобактер пилори) – Рейтинг 2020
Хеликобактер пилори: диагностика, эффективные схемы лечения и профилактика
Частые боли в животе, ощущение тяжести и отрыжка после еды, тошнота – типичные признаки заболеваний желудочно-кишечного тракта. Одной из причин плохого самочувствия может стать бактериальная инфекция «хеликобактер пилори», которая поражает желудок и двенадцатиперстную кишку и провоцирует развитие гастрита, язвы и прочих опасных заболеваний ЖКТ.
Бактерии хеликобактер пилори были выявлены сравнительно недавно – около 30 лет назад. И в 2005 году австралийские ученые Робин Уоррен и Барри Маршалл были удостоены за это открытие Нобелевской премии. Тот факт, что гастрит и язва могут иметь инфекционное происхождение, стал новой страницей в истории медицинских исследований.
Причины появления бактерии
Бактерия хеликобактер пилори не может развиваться на открытом воздухе. Передается она бытовым путем: через посуду, средства личной гигиены, а также при поцелуе. Эта бактерия устойчива к кислотной среде, поэтому она легко проникает в слизистые оболочки желудка и разрушает его ткани. Слизистая воспаляется, развиваются эрозии, гастриты, затем – язвы. Если инфекцию вовремя не вылечить, есть риск рака желудка.
Заражению способствует низкий уровень жизни и пренебрежение правилами личной гигиены. Чаще всего болеют люди, живущие в общежитиях, интернатах, детских домах, а также медработники. В странах третьего мира заболевание регистрируется чаще, чем в развитых государствах. Стоит отметить, что в России, как и в других цивилизованных странах мира, в последние годы зафиксированы случаи заболевания среди достаточно обеспеченного населения.
Симптомы хеликобактериоза
Через 6-8 дней после заражения больной начинает отмечать признаки воспаления желудочно-кишечного тракта: боли, тошноту, рвоту, отрыжку..gif) Они являются краткосрочными, и им обычно не придают значения. Болевые ощущения часто возникают натощак и снижаются после приема пищи, что также заставляет больного не воспринимать происходящее всерьез. Тем временем, бактерии остаются в организме и в любой момент могут начать свою разрушительную работу, хотя могут и никак не проявлять свое присутствие годами. Риск начала их болезнетворной активности повышается при неправильном питании, курении, злоупотреблении алкоголем, стрессах, ослаблении общего иммунитета, инфекционных заболеваниях.
Они являются краткосрочными, и им обычно не придают значения. Болевые ощущения часто возникают натощак и снижаются после приема пищи, что также заставляет больного не воспринимать происходящее всерьез. Тем временем, бактерии остаются в организме и в любой момент могут начать свою разрушительную работу, хотя могут и никак не проявлять свое присутствие годами. Риск начала их болезнетворной активности повышается при неправильном питании, курении, злоупотреблении алкоголем, стрессах, ослаблении общего иммунитета, инфекционных заболеваниях.
Открытие бактерий хеликобактер пилори и изучение их роли в развитии гастрита и язвы дали впечатляющие результаты. Частота рецидивов у больных с язвой двенадцатиперстной кишки снизилась с 67% до 6%, а у больных с язвой желудка – с 59% до 4%. Сейчас ученые не сомневаются в необходимости тестов на хеликобактер пилори при этих заболеваниях.
Диагностика
При подозрении на заражение бактериями хеликобактер пилори проводятся следующие диагностические исследования.
Неинвазивные тесты . Анализы крови и выдыхаемого воздуха. Эти методы отличаются невысокой стоимостью и быстротой получения результатов. Однако неинвазивные тесты дают большое количество ложноположительных результатов. Для повышения надежности дыхательного теста необходимо за 2 недели отказаться от приема антисекреторных средств, антибиотиков, противовоспалительных и антацидных средств. В течение 3 суток перед исследованием нельзя принимать крепкие спиртные напитки и бобовые, а за 3 часа до анализа не курить и не пользоваться жевательной резинкой.
Биопсия . Проводится во время эндоскопического обследования желудка и двенадцатиперстной кишки. На наличие бактерий исследуется образец слизистой. Биопсия дает более точные результаты при условии, что было взято несколько образцов с различных воспаленных участков.
Лечение хеликобактер пилори: современные методы и схемы
Поскольку препараты для лечения хеликобактер пилори относятся к антибиотикам, их назначают исходя из принципа наименьшего вреда для организма. Иногда становится ясно, что лечение хеликобактер пилори антибиотиками нанесет пациенту больший вред, чем сами бактерии, и тогда медикаментозный курс не назначается. Однако при наличии существенных эрозий и язв такое лечение все-таки необходимо – без него заживление не будет окончательным даже при приеме лекарств для восстановления слизистых оболочек. Обязателен курс антибиотиков и в тех случаях, когда в результате хеликобактериоза развились такие заболевания, как мальтома желудка, атрофический гастрит, язва и крайняя степень запущенности заболевания – рак. Антибиотики могут применяться не только в период обострения, но и при ремиссии болезни.
Все схемы лечения хеликобактериоза включают не менее трех лекарственных препаратов. Обычно это два индивидуально подобранных антибиотика и специальный ингибитор протонной помпы, например, париет. Длительность приема лекарств составляет четырнадцать дней. Уже в первый день приема препаратов нередко больной начинает ощущать улучшение своего состояния. Однако принципиально важно довести курс до конца, чтобы бактерии не успели адаптироваться к назначенному антибиотику и не пришлось подбирать новый.
При диагнозе «хеликобактер» курс лечения обязательно предполагает контроль над образом жизни пациента. Предполагается полный отказ от курения и спиртных напитков. Противопоказаны стрессы, неправильное питание. Из рациона исключается кислая, жареная, острая, копченая, жирная пища.
Негативные последствия отсутствия лечения
Самолечение хеликобактериоза недопустимо. Прежде всего, его симптомы сходны с симптомами целого ряда других заболеваний, которые не всегда связаны непосредственно с желудочно-кишечным трактом. Лекарства, их дозировку и длительность лечения необходимо подбирать по результатам анализов. Поэтому лечением хеликобактер пилори может заниматься только квалифицированный врач. Однако даже самая высокая квалификация может оказаться бессильна перед запущенными случаями, когда речь идет о развитии онкологических заболеваний желудка и двенадцатиперстной кишки. Поэтому при малейших симптомах желудочно-кишечной патологии необходимо пройти обследование в авторитетной клинике, где при необходимости вам предложат современное лечение хеликобактер пилори.
Профилактика
Что необходимо делать, чтобы вас не настигла эта болезнь? Лечение кого-либо из ваших близких означает, что вам тоже следует срочно обследоваться.
Чтобы хеликобактер после лечения не вернулся и не начал свою разрушительную деятельность с новой силой, через 2-6 недель по окончании курса приема медикаментов назначаются контрольные анализы. Особенного внимания требуют пациенты, у которых в результате инфекции были осложнения в виде кровотечения или перфорации слизистой оболочки желудка. Для них рецидив болезни крайне опасен и даже может привести к летальному исходу.
В случае если у вас возникли подозрения на присутствие Helicobacter pylori, следует обследоваться не только самому, но и всем членам семьи. При положительном результате анализов хотя бы у одного из домочадцев, стоит принять строгие меры для недопущения распространения болезни.
13 современных препаратов для лечения хеликобактерной инфекции (хеликобактер пилори)
*Обзор лучших по мнению редакции expertology.ru. О критериях отбора. Данный материал носит субъективный характер, не является рекламой и не служит руководством к покупке. Перед покупкой необходима консультация со специалистом.
Прочитав эту статью, человек без медицинского образования может не только понять, что представляет собой хеликобактерная инфекция, но главное — зачем её нужно лечить, и как её нужно лечить в соответствии с современными представлениями. Поэтому если врач просто предлагает вам «пропить антибиотик» чтобы избавиться от хеликобактер пилори, то после ознакомления с этой статьей, вы, конечно, убежите от такого врача, как от чумы, и будете искать настоящего специалиста. Лечение хеликобактерной инфекции дело непростое, но обо всём по порядку.
Вначале казалось невероятным, что в кислой среде желудка, которая способна растворять даже железные опилки, может жить и размножаться какой-либо микроорганизм. Потом это стало доказанным фактом. Это нежный, завернутый в спираль микроорганизм — хеликобактер пилори. Вначале их считали случайной находкой, затем – безвредными сапрофитами. Но потом эти микробы стали всё чаще встречаться у пациентов с болями в животе, с отрыжкой, изжогой и другими симптомами верхней, или желудочной диспепсии.
Но в разы возросло значение этого возбудителя инфекции, когда была установлена тесная взаимосвязь наличия хеликобактера с развитием язвенной болезни желудка и злокачественными новообразованиями этого органа у носителей хеликобактера. Специалисты-онкологи считают наличие хеликобактерной инфекции ярко выраженным канцерогеном 1-го уровня.
Важно, что выявить наличие этой инфекции в настоящее время очень просто. Существует особый уреазный дыхательный тест. Это очень эффективный и неинвазивный способ, для него нужно только лишь «подышать в трубочку». Этот тест может сделать каждый, и узнать, находится ли человек в группе риска.
Но, к сожалению, «наши люди» не придают значения профилактике, и часто попадают на операционный стол уже с осложнениями – например, язвой желудка. Поэтому в том случае, если человек старше 50-55 лет, если у него уже выявлены симптомы диспептических расстройств, и у врача есть «настороженность на онкологию», (например, есть потеря массы тела, аппетита, наличие симптомов железодефицитной анемии), то уже нужно выполнять гастроэндоскопию с биопсией.
Доказано, что наличие длительно протекающей хеликобактерной инфекции способно вызывать не только язву желудка и двенадцатиперстной кишки, а также рак желудка. Хеликобактерная инфекция может вызывать железодефицитную анемию, падение тромбоцитов в плазме крови, вызывать хронический дефицит витамина B12, который проявляется неврологическими расстройствами.
Поэтому лечение хеликобактерной инфекции дело важное, хотя и не простое. Сама процедура уничтожения этого микроорганизма называется эрадикацией, что в переводе с латинского – «искоренение». Это неслучайный термин. Просто так, путем назначения какого-либо одного лекарства, «на авось» уничтожить хеликобактерную инфекцию, для которой суровые условия желудочного сока – это норма, невозможно. Существует много схем эрадикации, которые все признаны, «работают», и применяются при наличии тех или иных показаний. Но прежде, чем переходить к лекарствам, необходимо точно определить показания к лечению.
Кому показано лечение?
В современном мире, странах с высоким уровнем медицины, существует профилактическая направленность лечения. Это означает, что какого-либо состояния лучше совсем не допускать, чем лечить потом развившуюся болезнь, затрачивая большие деньги. Поэтому в том случае, если человек, не имеющий никаких жалоб, самостоятельно решает обследоваться на хеликобактерную инфекцию и она подтверждается, то возможно проведение лечения с профилактической целью, чтобы снизить риск развития серьезных заболеваний впоследствии.
Если же у пациента уже существуют какие-либо симптомы, то в таком случае лечение тем более показано, и в первую очередь, при таких состояниях, как:
- наличие выраженных симптомов диспепсии, таких как изжога, тошнота, вздутие живота и тяжесть в желудке после еды;
- тупые, нелокализованные, блуждающие боли или дискомфорт в эпигастрии;
- подташнивание и горечь во рту;
- наличие диагностированной язвенной болезни желудка и или двенадцатиперстной кишки на фоне выявленной хеликобактерной инфекции;
- особая лимфома, или опухоль, ассоциированная со слизистой оболочкой желудка, так называемая МАLT – лимфома;
- известно, что хеликобактерная инфекция повышает риск развития эрозивного гастрита и язвенной болезни при длительном приеме нестероидных противовоспалительных средств, таких как аспирин, и особенно индометацин и диклофенак. Поэтому в том случае, если у пациента доказано наличие хеликобактерной инфекции, и он готовится длительно получать нестероидные противовоспалительные средства, например при наличии диагноза ревматоидного артрита, то ему также необходимо превентивное лечение;
- при наличии доказанной кишечной метаплазии, или атрофии эпителия, выявленной при гастродуоденоскопии;
- если у пациента — носителя хеликобактерной инфекции есть ближайшие родственники — родители, или братья и сёстры, у которых был выявлен рак желудка или в семье имелись случаи смерти от этого заболевания;
- при наличии железодефицитной анемии неясной этиологии, при исключении других причин, а также при идиопатической тромбоцитопенической пурпуре;
- ещё одним показанием для назначения схемы эрадикации является выставленный диагноз болезни Менетрие, или гипертрофического гастрита. При этом заболевании слизистая оболочка желудка увеличивается, образует складки, в ней развиваются кистозные образования и различные аденомы. Известно, что болезнь Менетрие считается факультативным (необязательным) предраковым состоянием.
Современная гастроэнтерология не стоит на месте, и постоянно подбираются наилучшие схемы эрадикации. Ведь этот микроорганизм, так, как и все другие микробы, виновные в развитие тех или иных заболеваний, постоянно совершенствуется, и резистентность, то есть устойчивость хеликобактера к антибиотикам постепенно возрастает. Поэтому основой данной статьи будет так называемый «маастрихтский консенсус V» от 2015 года.
По данным этого авторитетного собрания гастроэнтерологов, результаты которого приняты к действию во многих странах мира, в том числе и в Российской Федерации, и рекомендованы всемирной организации здравоохранения (ВОЗ), своевременное лечение хеликобактерной инфекции, или эрадикация:
- уменьшает риск развития злокачественных новообразований желудка почти на 35%;
- уже диагностированные предраковые болезни желудка перестают прогрессировать;
- если по данным гастроскопии была выявлена атрофия желудка, то такая атрофия исчезает, и слизистая оболочка желудка восстанавливается;
Наконец, своевременная эрадикация хеликобактерной инфекции выгодна экономически и пациенту и врачу, поскольку стоимость её чрезвычайно низка по сравнению со стоимостью лечения развернутого случая язвы или рака желудка, причиной которых и бывает эта инфекция.
Препараты от хеликобактер пилори: лечение антибиотиками
Терапия, направленная на изгнание Нelicobacter руlori из желудка инфицированного им человека – не самая простая задача, которую ставит перед собой доктор.
Это связано с тем, что патогенные микроорганизмы крайне неохотно покидают излюбленные места существования – эпителиальные клетки внутренней оболочки желудка или подслизистой основы, формируются устойчивые штаммы к лекарственным препаратам.
Поэтому воздействие на бактерию должно быть комплексным: медикаментозным, физиотерапевтическим, диетологическим, фитотерапевтическим. Основной точкой приложения служит лекарственная терапия.
Как и чем лечить хеликобактер пилори — медикаментозные способы
Выражение «лечить хеликобактерную инфекцию» не совсем верно с врачебной точки зрения. Доктора лечат заболевания, вызванные данным микроорганизмом, а от самой бактерии следует избавляться.
Основным направлением в медикаментозной терапии является эрадикация – способ уничтожения инфекционного агента при помощи лекарств.
Помимо эрадикационной терапии, важно скорректировать нарушенную кислотность желудочного сока, восстановить моторную и эвакуаторную функцию ЖКТ, стабилизировать ферментативную активность, унять воспалительные процессы.
Все эти функции возлагаются на конкретные препараты, которые в сочетании с правильным питанием, дают положительные результаты. Основные группы препаратов, лекарств и таблеток для лечения бактерии хеликобактер пилори (helicobacter pylori):
- Антибактериальные
- Препараты солей висмута
- Блокаторы протонной помпы
- М-холинолитики
- Блокаторы Н2-гистаминовых рецепторов
- Антациды
- Спазмалитики
- Прокинетики
Наиболее частая лекарственная форма препаратов – таблетки, антациды могут применяться в виде суспензий, порошков, требующих растворения в воде.
Какие антибиотики убивают хеликобактер пилори
Антибактериальные лекарственные средства – «тяжёлая артиллерия», заставляющая бактерию дезертировать и покидать организм пациента.
В стандартах лечения хеликобактер-ассоциированных патологий желудка указаны как минимум два антибиотика. При значительном обсеменении слизистой, выраженных клинических проявлениях болезни без них обойтись никак нельзя.
Какие антибиотики рекомендуют принимать при хеликобактер пилори:
- Амоксициллин
- Кларитромицин
- Тетрациклин
- Метронидазол
- Рифамбутин
- Левофлоксацин
Рифамбутин и левофлоксацин являются препаратами «запаса», они не входят в стандартных схемы терапии, но могут быть использованы, если у патогенных штаммов разовьётся устойчивость к распространённым, входящим в протоколы средствам.
Антибактериальные препараты имеют побочные эффекты: аллергические реакции, дисбактериоз, кандидоз, тошнота. Часто пациенты бояться пить антимикробные препараты именно по этой причине.
В случае инфицирования хеликобактер и наличия клиники желудочных заболеваний, делать этого не стоит. Приём антибиотиков в этом случае оправдан.
Без этих лекарственных средств пациент рискует заработать себе язву желудка, также отказом от лечения подвергает организм риску развития онкопатологии желудочно-кишечного тракта. Рак желудка в 3-6 раз чаще возникает у пациентов, инфицированных Н.руlori, которые не получали должной терапии.
Как лечить хеликобактер пилори антибиотиками — схемы эрадикационной терапии
На сегодняшний день разработаны и активно применяются 3-х и 4-х компонентные схемы лечения, направленные на уничтожение бактерии.
Если у пациента выявлен микроб в желудке, имеются симптомы поражения ЖКТ, ранее человек не получал лечения, начинают терапию всегда с трёхкомпонентной схемы, включающей в себя:
- Блокатор протонной помпы (омепразол, лансопразол, рабепразол, пантопразол 20 мг) 2 раза в сутки
- Амоксициллин 1000 мг 2 раза в сутки
- Кларитромицин 500 мг 2 раза в сутки
3-х компонентная схема назначается при первичном обращении пациента за лечением, пожилым, ослабленным пациентам индивидуально может проводиться корректировка дозы лекарственных средств.
Назначают данную терапию от 7 (минимум) до 14 дней. Клинические исследования показали, что в ряде случаев недельного приёма препаратов оказывается недостаточно для обеспечения эрадикации, терапия оказывается неэффективной.
После двух недель приема препаратов, напротив, эффект от лечения был на порядок выше: у гораздо большего числа пациентов эрадикация патогена достигала 80% и более.
Четырёхкомпонентная схема лечения
В случае, когда эффект от 3-хкомпонентной схемы не достигнут, уничтожения инфекционного агента не произошло, врач порекомендует спустя месяц-полтора продолжить терапию, состоящую из:
- Блокатора протонной помпы (омепразол, лансопразол, рабепразол, пантопразол 20 мг) 2 раза в сутки
- Препараты солей висмута 120 мг 4 раза в день
- Метронидахол 500 мг 3 раза в сутки
- Тетрациклин 500 мг 4 раза в сутки
Это 4-хкомпонентная схема эрадикации. Важно учесть, чтобы антибактериальные препараты, применяемые ранее, не повторялись. Если выявлена резистентность к вышеперечисленным антибиотикам, можно назначить лекарства «запаса»: левофлоксацин, рифамбутин.
Несмотря на разработанные стандарты, врач, проводя эрадикацию, должен подходить к каждому случаю и заболеванию индивидуально, с учетом возраста пациента, сопутствующих патологий, возможных аллергических реакций организма и устойчивости конкретных штаммов бактерии к препаратам.
Сколько дней пить антибиотики при хеликобактер пилори
3-компонентная схема назначается врачом на срок от 7 до 14 дней. Менее недели пить препараты нецелесообразно, эффекта от такого лечения не будет.
Бактерия с трудом поддаётся терапии, вырабатывает устойчивость к препаратам, поэтому появляется всё больше данных о том, что и недели мало для достижения положительного результата и избавления от патогена. Всё больше врачей склоняются к продлению антибиотикотерапии до 10-14 дней.
Недельный курс приема рекомендуют пожилым и ослабленным пациентам, имеющим сопутствующую полиорганную патологию, с трудом переносящим нагрузку двумя антибиотиками.
4-компонентная схема назначается сроком на две недели.
Эффективность лечения следует оценивать посредством диагностических и лабораторных методов не ранее чем через 1-1,5 месяца от окончания приёма препаратов.
Если эрадикация составляет 80% и более от первоначального уровня, либо бактерий вовсе не обнаружено в организме, можно говорить об успехе в терапии заболевания, связанного с данным патогеном.
Подробнее про препараты
Особенности приема антибиотиков для лечения хеликобактер пилори:
Это антибактериальный препарат из группы макролидов. Входит в состав терапии первой линии хеликобактерной инфекции. Успешно применяется в гастроэнтерологии, способен ингибировать синтез клеточной стенки helicobacter pylori, а значит предотвращать её размножение. Кислотоустойчив, эффективно «работает» при нормальной и повышенной кислотности, хорошо всасывается.
Некоторые штаммы бактерий проявляют резистентность к кларитромицину. В этом случае препарат необходимо заменить на другой, для достижения лучшего терапевтического эффекта.
- Амоксициллин и метронидазол
Метронидазол или трихопол – препарат оказывающий губительное или бактерицидное действие на Н.руlori. Его активность не зависит от уровня рН в желудке, препарат может применяться как при гипер-, так и при гипоацидных состояниях.
На сегодняшний день очень распространена резистентность многих штаммов хеликобактерий к метронидазолу. Если препарат назначается совместно с де-нолом, устойчивость к нему развивается медленнее.
Амоксициллин — антибиотик пенициллинового ряда, блокирующий синтез клеточной стенки микробов, хорошо всасывается слизистой оболочкой желудка. Более активен в нейтральной среде, чем в кислой. Повышение рН до 4 в 10 раз усиливает фармакологический эффект данного препарата.
Метронидазол и амоксициллин являются препаратами первой линии, но могут назначаться и в 4-хкомпонентной схеме лечения.
Ещё одно противомикробное средство, активно используемое в эрадикационной терапии helicobacter pylori. Механизм действия тетрациклина заключается в ингибировании синтеза белка микробной клетки.
Лекарство хорошо всасывается в ЖКТ. Приём молочной пищи замедляет его всасываемость.
- Блокаторы протонной помпы
Самым распространённым представителем данной группы является омепразол (омез). Существуют и другие весьма эффективные средства: лансопразол, пантопрозол, эзомепразол, рабепразол).
Лекарственные средства подавляют выработку соляной кислоты. Тем самым они воздействуют на микроб косвенно: не уничтожают его, а создают неблагоприятные условия для существования, оказывают супрессивное действие на инфекцию: приостанавливают бактериальный рост и развитие.
Омепразол и другие представители группы за счёт повышения рН желудочного содержимого способствуют лучшей работе антибактериальных препаратов, в частности амоксициллина.
Есть данные о том, что ингибиторы протонной помпы способны блокировать фермент бактерии уреазу.
Врачи рекомендуют после окончание курса лечения с антибиотиками, продолжать прием омепразола до 4-8 недель. У пациентов, продолжающих принимать блокаторы протонного насоса, лучше происходят процессы заживления слизистой, выше процент уничтожения бактерий относительно пациентов, которые прекратили приём омепразола после окончания эрадикационной схемы.
- Антациды и блокаторы Н2-рецепторов
Чаще всего кислотность желудочного сока при инфицировании Н.руlori нормальная или повышенная.
Помимо омепразола, нормализующего рН, таким действием обладают и антацидные препараты (альмагель, фосфалюгель, гефал, маалокс, ренни) и блокаторы Н2-гистаминовых рецепторов (фамотидин, ранитидин)
Механизм действия антацидов заключается в нейтрализации соляной кислоты желудка. Действующие вещества в данных препаратах – алюминия, магния гидроскиды.
Средства эффективно устраняют клинические проявления «ацидизма» – изжогу, отрыжку кислым. Принимают их через 1-2 часа после еды и на ночь. Форма выпуска – суспензии, или порошки, таблетки.
Не стоит сочетать приём антацидов с антибактериальными препаратами или солями висмута, поскольку гидроксиды алюминия и магния нарушают всасывания в ЖКТ других веществ.
Блокаторы Н2-гистаминовых рецепторов нового поколения (фамотидин, ранитидин) практически не имеют побочных эффектов. Механизм их действия: тормозят выработку НСL и продукцию пепсина, из-за чего понижается кислотность. Назначают таблетки после завтрака и перед сном.
Данная группа лекарственных средств в сочетании с антибиотиками обладает бактерицидным действием – уничтожает как кокковые штаммы, так и вегетативные формы.
Соли висмута обладают множеством эффектов, которые оказывают положительное влияние при проведении комплексного лечения заболеваний, вызванных хеликобактериями:
- Препятствуют прикреплению патогенов к эпителиальным клеткам слизистой оболочки желудка
- Нарушают синтез микробной АТФ
- Блокируют ферменты бактерии
- Способствуют разрушению клеточной стенки инфекционного агента
- Повышают синтез защитных иммуноглобулинов, простагландинов желудочного секрета
- Усиливают выделение бикарбонатов и защитной слизи
- Уменьшают всасывание антибиотиков в ЖКТ, тем самым повышая их концентрацию в желудочном содержимом
- Обеспечивают реперативный, ранозаживляющий эффект внутренней желудочной стенки
- Улучшают местное кровообращение
Данные фармакологические свойства позволили препаратом висмута занять свою нишу в терапии хеликобактериоза в сочетании с двумя антибиотиками. Одним из самых эффективных препаратов данной группы является де-нол.
Де-нол убивает хеликобактер или нет
Лишь в сочетании с противомикробными препаратами де-нол обладает бактерицидным действием. Если принимать данное лекарственное средство отдельно в качестве монотерапии, должного эффекта такое лечение не возымеет.
Но в комбинированной схеме лечения, де-нол в полной мере раскрывает свои терапевтические эффекты, одновременно усиливая свойства антибактериальных препаратов.
Комбинация «де-нол + 2 антибиотика» является чрезвычайно эффективной, и в случае чувствительности хеликобактерий, позволяет добиться исчезновения микроба при условии приема таблеток в течение 10-14 дней.
Сколько пить де-нол при хеликобактер инфекции
Препарат назначают по 1 таб 4 раза в сутки за 30 мин. до еды и на ночь на срок минимум 21 день, можно принимать лекарство до 8 недель по рекомендации врача. Следует знать, что при назначении препарата стул окрашивается в чёрный цвет.
Запивать таблетки следует стаканом кипячёной воды, нельзя молоком, поскольку молочные продукты снижают фармакологический эффект препарата. Не сочетаются таблетки и с соками.
Антациды замедляют всасывание де-нола, поэтому вместе пить их не стоит.
При появлении побочных эффектов: диареи, тошноты, аллергических реакций, рвоты, приём лекарства следует прекратить и обратиться за консультацией к врачу.
Источники:
http://www.kp.ru/guide/lechenie-khelikobakter-pilori.html
http://expertology.ru/13-sovremennykh-preparatov-dlya-lecheniya-khelikobakternoy-infektsii-khelikobakter-pilori/
http://bolvzheludke.ru/preparaty/lechenie-helikobakter-antibiotikami/
Хеликобактер пилори – симптомы и лечение
Автор Николай Ефимов На чтение 3 мин Просмотров 128 Опубликовано
За открытие хеликобактер пилори — бактерии, вызывающей язву и рак желудка, ученые получили нобелевскую премию. Однако, чтобы понять, есть ли эта бактерия в желудке и как с ней бороться надо прочитать про хеликобактер пилори, симптомы и лечение которой строго определены в медицине.
Хеликобактер пилори симптомы
Количество больных с заболеваниями, ассоциированными с хеликобактерной инфекцией (Нр), не уменьшается, а число случаев неудачной эрадикационной терапии постоянно увеличивается.
Несмотря на наличие четко установленных методов диагностики и принципов проведения эрадикационного лечения, возникают новые вопросы, связанные с уничтожением Нр, одним из которых является резистентность Нр к антибактериальным препаратам.
Как самому понять симптомы хеликобактер пилори — вы можете заподозрить наличие этой бактерии, если у вас язва, или если у вас частые рвоты и диспепсия. Просто пойдите в ближайшую лабораторию крови и сдайте кровь на наличие хеликобактер пилори.
Хеликобактер пилори — лечение
Применение эрадикационной терапии позволило существенно повысить эффективность лечения заболеваний, ассоциированных с Нр, значительно поднять качество жизни больных, но, учитывая наличие выраженной резистентности к метронидазолу и антибиотикам, увеличение случаев неудачной эрадикации, необходим поиск альтернативного лечения. Казалось бы, применив новые группы антибиотиков можно проблему Нр устранить.
Лечение от хеликобактер пилори возможно только антибиотиками.
Однако использование «резервных» антибиотиков в качестве препаратов стартовой линии приведет к потере их эффективности не только при гастроэнтерологической патологии, но и при внегоспитальных, нозокомиальных инфекциях, туберкулезе.
Орнистат
На сегодня существует современный комплексный препарат с повышенным антибактериальным воздействием – Орнистат, который за счет накопления активного радикала с атомом хлора путем пассивного транспорта проникает в бактерию.
Его мишенью в микробной клетке является ДНК, РНК и клеточные белки. Продукты восстановления образуют комплексы с ДНК, обусловливающие деградацию и нарушающие процессы репликации и транскрипции ДНК.
Доказано, что орнистат отличается высокой антихеликобактерной активностью, большей продолжительностью максимального воздействия, чем метронидазол (3 и 1-2 часа соответственно).
Что лучше метронидазол или орнистат (орнидазол)
Также у орнидазола более длительный период полувыведения, чем у метронидазола (соответственно 12-14 и 6-10 часов). Биодоступность обоих препаратов практически одинакова, но орнидазол в меньшей степени соединяется с белками плазмы (15%), чем метронидазол (20%), что вызывает значительно меньшее количество побочных явлений.
Минимальная ингибирующая концентрация для орнистата составляет 10 мкг / мл, а для метронидазола — 12 мкг / мл, что также подтверждает преимущества первого. Кроме того, среди преимуществ орнидазола следует отметить то, что он не имеет перекрестной чувствительности к метронидазолу. Так, первичная резистентность к орнидазолу не выше 17%, то есть резистентность Нр к орнидазолу возникает в 3-4 раза реже, чем к метронидазолу.
Это позволяет существенно уменьшить количество побочных явлений, повысить уровень эрадикации, что не всегда удается осуществить при применении эрадикационной схем с метронидазолом и тинидазолом.
Также дополнительное положительное влияние на приверженность больного к лечению может иметь удобная форма выпуска орнидазола, которая позволяет больному каждые сутки принимать содержимое 1 блистера Орнистат, при этом количество лекарств рассчитано на курс лечения, что, в свою очередь, увеличивает экономическую доступность данного препарата.
Теперь вы знаете что такое хеликобактер пилори симптомы и лечение вы можете составить и сами, но лучше обратиться к врачу, который выпишет вам необходимый антибактериальный препарат.
[avatar user=»autor-terapevt» size=»thumbnail» align=»center»]Статья подготовлена врачом терапевтом Николаем Ефимовым.[/avatar]Эффективность двух различных доз левофлоксацина в лечении инфекции Helicobacter pylori: проспективное одноцентровое рандомизированное клиническое исследование
Дизайн исследования
Это было проспективное рандомизированное контролируемое одноцентровое клиническое исследование. Это исследование проводилось в Шестой дочерней больнице Медицинского университета Гуанчжоу (Народная больница Цинюань) в период с апреля по сентябрь 2017 года. Пациенты с диспепсией, направленные на верхнюю эндоскопию и с диагнозом хронический гастрит с диспепсией или атрофией / эрозией слизистой оболочки, имели право на участие в исследовании, если у них был H.pylori , были в возрасте 20–60 лет и никогда ранее не получали лечения от инфекции H. pylori . Пациенты, которые соответствовали одному из следующих критериев, были исключены из исследования: пациенты, принимавшие какие-либо лекарства, которые могли повлиять на результаты исследования, такие как антибиотики, соли висмута, ИПП или блокаторы гистаминовых 2-рецепторов, в течение предыдущих 4 недель; пациенты с язвенной болезнью, злокачественными новообразованиями желудочно-кишечного тракта, перенесенными операциями на желудке или пищеводе или тяжелыми сопутствующими заболеваниями; пациенты с аллергией на какой-либо из исследуемых препаратов в анамнезе; беременные или кормящие пациентки; и пациенты, которые не могли дать информированное согласие сами или отказались участвовать в исследовании.Это исследование было одобрено институциональным наблюдательным советом Шестой дочерней больницы Медицинского университета Гуанчжоу. Перед началом процедуры исследования каждый пациент предоставил письменное информированное согласие. Дизайн и процедуры исследования были выполнены в соответствии с принципами Хельсинкской декларации. Это исследование было зарегистрировано в Китайском регистре клинических испытаний 13.01.2017 (регистрационный номер клинического исследования: ChiCTR-IPD-17010408).
Вмешательство
Отобранные пациенты были случайным образом разделены на две группы эрадикации с компьютерным случайным порядком в соотношении 1: 1, чтобы принять одну из следующих четырехкратных схем, содержащих амоксициллин, в течение 14 дней.Группа А получала эзомепразол 20 мг 2 раза / сут за 30 мин до еды, амоксициллин 1000 мг 2 раза / сут через 30 мин после еды, коллоидный пектин висмута 200 мг 2 раза / сут через 30 мин после еды и левофлоксацин 500 мг 1 раз / сут через 30 мин после еды. Группа Б получала эзомепразол 20 мг 2 раза / сут за 30 мин до еды, амоксициллин 1000 мг 2 раза / сут через 30 мин после еды, коллоидный пектин висмута 200 мг 2 раза / сут через 30 мин после еды и левофлоксацин 200 мг 2 раза / сут через 30 мин после еды.
Медицинский персонал отделения гастроэнтерологии подробно объяснил всем включенным пациентам схему лечения и возможные побочные эффекты перед началом терапии.Их также попросили записывать симптомы побочных эффектов во время лечения. Пациентам давали устные и письменные инструкции о важности регулярного приема лекарств и советовали не прекращать прием лекарств в случае легких или умеренных побочных эффектов. Пациентам рекомендовалось вызвать врачей, если побочные эффекты были серьезными. Пациентов просили вернуться в течение 3 дней после эрадикации H. pylori для оценки терапевтического соответствия и определения частоты побочных эффектов.
Обнаружение H. pylori
Пациенты прошли 13 дыхательных тестов на C-мочевину (UBT; UCBT Kit, Atom High Tech, Пекин, Китай) через 8 недель после эрадикации H. pylori для оценки терапевтического результата. Другие препараты, которые могли повлиять на результаты, были запрещены во время исследования. Антибиотики, соли висмута, ИПП и блокаторы рецепторов гистамина-2 были отменены как минимум на 4 недели до проведения 13 C-UBT. Пациентам было рекомендовано ничего не принимать внутрь за 2 часа до процедуры 13 C-UBT.Базовый образец выдыхаемого воздуха получали путем продувания через одноразовую пластиковую соломинку в контейнер емкостью 20 мл, а затем капсулу, содержащую 75 мг 13 C-мочевины, давали пациентам со 100 мл воды. Другой образец дыхания был взят через 30 минут. Базовые и 30-минутные образцы дыхания анализировали с помощью масс-спектрометра. Тест считался положительным, если разница между исходным образцом и 30-минутным образцом превышала 4,0 единицы.
Безопасность и соответствие
Побочные реакции на лекарства и соблюдение режима приема лекарств оценивались научным персоналом.Нежелательные реакции на лекарства оценивались с помощью открытых вопросов в самоотчетах пациентов и при физикальных обследованиях. Неблагоприятные лекарственные реакции были классифицированы как легкие (не мешающие распорядку дня), умеренные (влияющие на распорядок дня), тяжелые (существенно влияющие на распорядок дня и прекращение приема лекарств) и серьезные (госпитализация, инвалидность, требующая вмешательства для предотвращения необратимого повреждения или смерти). . Также учитывались лечебные препараты, которые не принимали пациенты. Комплаентность считалась низкой, если принималось менее 80% лечебных препаратов.
Сбор данных
Были собраны демографические и клинические данные. Первичной конечной точкой исследования была степень эрадикации H. pylori . Вторичными конечными точками были частота побочных реакций на лекарства и соблюдение каждого режима. Оценивались профиль безопасности (частота нежелательных реакций) и комплаентность (прием препаратов). Инфекция H. pylori определялась по разнице между исходным и 30-минутным образцами, превышающей 6.0 шт. Инфекция H. pylori считалась искорененной, если результат однократного 13 C-UBT был отрицательным.
Статистический анализ
Размер нашей выборки (N = 390) был запланирован перед исследованием, исходя из ранее сообщенной степени эрадикации при использовании четырехкратной схемы приема амоксициллина, составляющей приблизительно 90%. Расчеты основывались на предположениях a = 0,05 и 1 – β = 0,80 и ожидаемой разнице между группами 10% или больше, что считалось минимальной клинически значимой разницей.Проценты использовались для описания категориальных переменных, а средние (стандартное отклонение) или медианы (диапазон) использовались для описания непрерывных переменных. Для категориальных переменных ассоциации между 2 группами оценивались с помощью критерия хи-квадрат (при необходимости применяя поправку Фишера), а для непрерывных переменных использовался t-критерий для двух выборок или U-критерий Манна – Уитни. Все статистические анализы были выполнены с использованием программного обеспечения IBM SPSS 18.0. Все тесты проводились с параметром a-level, установленным на 0.05 (двусторонний).
Схемы на основе кларитромицина, амоксициллина и метронидазола для лечения инфекций Helicobacter Pylori в Колумбии – полный текст
Открытие Helicobacter pylori, удостоенное Нобелевской премии Уорреном и Маршаллом, и их последующая работа, которая показала, что гастрит и пептические язвы можно успешно лечить искоренение этой бактерии в конечном итоге произвело революцию в том, как врачи лечат язвенную болезнь. Однако наше предыдущее исследование показало, что большинство методов лечения H.pylori значительно менее эффективны при наличии лекарственной устойчивости, особенно в развивающихся странах, где H. pylori широко распространена. Наш недавний метаанализ, который побудил Канадскую группу консенсуса по Helicobacter изменить свои рекомендации по лечению для Канады, показал, что четырехкратная терапия кларитромицином, амоксициллином, метронидазолом (КАМ) и ингибитором протонной помпы эффективна при наличии резистентности к кларитромицину или метронидазолу. Однако этот режим еще предстоит испытать в развивающейся стране.
С момента открытия Уоррена и Маршалла H.pylori также считается фактором риска развития рака желудка и, возможно, неязвенной диспепсии (НЯД), хотя противоречивые данные свидетельствуют о том, что он может быть защитным фактором для исходов заболеваний пищевода. Считается, что атрофия желез, вызванная H. pylori, инициирует предраковый процесс, нарушая слизистый барьер, позволяя канцерогенам напрямую контактировать с клетками желудка. Атрофия сопровождается повышением pH в полости желудка.Канцерогены, мутации эпителия, быстрый оборот клеток, токсины и факторы вирулентности, такие как штаммы H. pylori, содержащие белки CagA и вакуолизирующий цитотоксин (VacA), а также гены cagA и vacA, которые кодируют эти белки, являются предполагаемыми факторами риска развития кишечного тракта. метаплазия, за которой следует дисплазия, а затем инвазивная карцинома.
Существует много споров о том, приносит ли лечение против H. pylori инфицированным пациентам неязвенную диспепсию. Метаанализ краткосрочных исследований показывает, что H.pylori является слабым фактором риска диспепсии в некоторых неустановленных группах населения. Эта информация вместе с анализом экономической эффективности привела к рекомендации Европейского Маастрихтского консенсуса 2-2000 о том, что молодых пациентов с стойкой диспепсией нужно обследовать и, в случае инфицирования, лечить от H. pylori («стратегия тестирования и лечения»). Тем не менее, без убедительных доказательств, подтверждающих эту стратегию при диспепсии, и отсутствия понимания того, как элиминация H. pylori влияет на симптомы, эта стратегия не получила широкого распространения и не является частью нынешних стандартов лечения во многих странах.Однако исследований, в которых изучается влияние H. pylori на симптомы в развивающихся странах, где встречается большинство инфекций, нет.
Хотя заболеваемость раком желудка снизилась в развитых странах, более высокие показатели наблюдаются в группах меньшинств и иммигрантов, и он по-прежнему является вторым по частоте распространением раком в мире. В Нариньо, Колумбия, заболеваемость раком желудка считается самой высокой в мире – до 150 на 100 000 в год. В 1993-94 гг. Мы провели рандомизированное клиническое исследование, направленное на краткосрочное уменьшение воспаления и повреждения эпителия в желудке H.pylori инфицировали людей НЕД из населения Пасто, столицы Нариньо («когорта пасто»). Данные этого испытания и нашего последующего метаанализа показали, что классический анти-H. pylori, которые эффективно устраняют H. pylori в Европе и Северной Америке, не были эффективны в таких популяциях, как Пасто, где широко распространена инфекция и высокая распространенность резистентности к метронидазолу.
Мы проверим эффективность многообещающих трех- и четырехкратных схем лечения на основе кларитромицина, амоксициллина и метронидазола (CAM) для эрадикации по сравнению с рекомендованными FDA 10-дневными схемами (кларитромицин, амоксициллин и омепразол).Поскольку антибактериальная терапия наиболее эффективна в определенном диапазоне pH желудочного сока, а также поскольку мутофокальная атрофия приводит к повреждению и потере продуцирующих кислоту париетальных клеток, мы проверим эффективность нашей модифицированной терапии, стратифицированной диагнозом мультифокального атрофического гастрита. Мы предполагаем, что: 1) среди инфицированных H. pylori субъектов в когорте Пасто с мультифокальным атрофическим гастритом те, кто рандомизирован на 14-дневную тройную терапию САМ, с большей вероятностью искоренит свою инфекцию H. pylori по сравнению с теми, кто рандомизирован в FDA. утвержденный режим; 2) среди H.pylori в когорте Pasto без мультифокального атрофического гастрита, которые рандомизированы на 14-дневную четырехкратную терапию CAM плюс омепразол, с большей вероятностью искоренит свою инфекцию H. pylori по сравнению с теми, кто рандомизирован на схему, одобренную FDA; и 3) среди инфицированных H. pylori субъектов в Пасто без предшествующего гистологического диагноза у тех, кто рандомизирован на 14-дневную терапию САМ, будет больше шансов искоренить H. pylori по сравнению с теми, кто рандомизирован на схему, одобренную FDA.Поэтому наша основная цель – провести рандомизированное клиническое испытание в Пасто, Колумбия, чтобы оценить диагностическую эффективность 14-дневной тройной терапии CAM и 14-дневной четырехкратной терапии кларитромицином, амоксициллином, метронидазолом и омепразолом для элиминации H. pylori по сравнению с одобренной FDA 10-дневной тройной терапией кларитромицином, амоксициллином и омепразолом у субъектов, которые никогда не лечились от инфекции H. pylori.
% PDF-1.7 % 1 0 объект > эндобдж 2 0 obj > эндобдж 3 0 obj > эндобдж 4 0 obj > эндобдж 5 0 obj > эндобдж 6 0 obj > эндобдж 7 0 объект > эндобдж 8 0 объект > эндобдж 9 0 объект > эндобдж 10 0 obj > эндобдж 11 0 объект > эндобдж 12 0 объект > эндобдж 13 0 объект > эндобдж 14 0 объект > эндобдж 15 0 объект > эндобдж 16 0 объект > эндобдж 17 0 объект > эндобдж 18 0 объект > эндобдж 19 0 объект > эндобдж 20 0 объект > эндобдж 21 0 объект > эндобдж 22 0 объект > эндобдж 23 0 объект > эндобдж 24 0 объект > эндобдж 25 0 объект > эндобдж 26 0 объект > эндобдж 27 0 объект > эндобдж 28 0 объект > эндобдж 29 0 объект > эндобдж 30 0 объект > эндобдж 31 0 объект > эндобдж 32 0 объект > эндобдж 33 0 объект > эндобдж 34 0 объект > эндобдж 35 0 объект > эндобдж 36 0 объект > эндобдж 37 0 объект > эндобдж 38 0 объект > эндобдж 39 0 объект > эндобдж 40 0 объект > эндобдж 41 0 объект > эндобдж 42 0 объект > эндобдж 43 0 объект > эндобдж 44 0 объект > эндобдж 45 0 объект > эндобдж 46 0 объект > эндобдж 47 0 объект > эндобдж 48 0 объект > / Граница [0 0 0] / Прямоугольник [507.458 702,142 569,99 714,16] / Подтип / Ссылка / Тип / Аннотация >> эндобдж 49 0 объект > / Border [0 0 0] / Rect [139.181 625.776 149.159 635.811] / Subtype / Link / Type / Annot >> эндобдж 50 0 объект > / Border [0 0 0] / Rect [216.964 55.502 230.797 63.496] / Subtype / Link / Type / Annot >> эндобдж 51 0 объект > / Border [0 0 0] / Rect [394.129 36.284 523.502 43.257] / Subtype / Link / Type / Annot >> эндобдж 52 0 объект > / Border [0 0 0] / Rect [468,283 725,669 569,99 749.707] / Подтип / Ссылка / Тип / Аннотация >> эндобдж 53 0 объект > поток x ս ے G-hc ~ QT% Uj} ʺDL2 * g | @
Пробиотики H. pylori и успех лечения
Как использовать пробиотики в качестве союзников во время лечения H. pyloriЕсли вы испытываете классические симптомы H. pylori боли, жжения в желудке или язвы, или вы пытались вылечить H. pylori, но безуспешно, вы будете рады узнать, что пробиотики – простой и эффективный помощник.
Может показаться, что обычные пробиотики не имеют большого значения против патогенных бактерий Helicobacter pylori.Но удивительная новость заключается в том, что различные штаммы пробиотиков, по-видимому, предотвращают инфекцию H. pylori [1], значительно улучшают эффективность лечения H. pylori [2 Trusted Source PubMed Перейти к источнику] и даже иногда полностью лечат ее (в меньшинство случаев) [3 Trusted Source PubMed Go to source].
Давайте посмотрим, что говорят исследования о H. pylori, о влиянии пробиотиков на H. pylori и о том, как пробиотики лучше всего подходят для лечения H. pylori.
Что такое хеликобактер пилори?Helicobacter pylori – известный как H.pylori для краткости – это патогенные бактерии со спиралевидным хвостом, которые в основном обитают в желудке, хотя они также могут жить где угодно в желудочно-кишечном тракте [4 Trusted Source PubMed Go to source].
H. pylori был обнаружен двумя австралийскими исследователями, Барри Маршаллом и Робином Уорреном, один из которых доказал, что H. pylori вызывает гастрит, заразившись бактериями [5]. В 2005 году они были удостоены Нобелевской премии за это важное открытие для гастроэнтерологии.
По оценкам, более половины населения мира имеет H.pylori, присутствующие в их кишечнике [6, 7 Trusted Source PubMed Go to source]. Только у 10-20% инфицированных людей разовьются симптомы, подобные пептической язве, и у очень небольшого процента разовьется рак желудка [8].
H. pylori проникает в слизистую оболочку желудка и вызывает воспаление, что влияет на продуцирующие кислоту париетальные клетки желудка [9]. Хроническое снижение кислотности желудочного сока из-за инфекции H. pylori является фактором риска многих заболеваний и побочных эффектов. Низкий уровень кислоты в желудке может привести к дефициту витамина B12 и железа, плохому перевариванию белка, низкой секреции желчи и ферментов и замедлению перистальтики кишечника [10 Надежный источник PubMed Перейти к источнику, 11 Надежный источник PubMed Перейти к источнику].
Ликвидация H. pylori приводит к исчезновению симптомов у людей с язвенной болезнью и предотвращает рецидив [12 Надежный источник PubMed Перейти к источнику, 13 Надежный источник PubMed Перейти к источнику, 14 Надежный источник PubMed Перейти к источнику].
Симптомы инфекции H. pyloriH. активность pylori вызывает желудочные симптомы, в том числе:
- Вздутие живота, газы и боль в животе
- Жжение в желудке
- Боль в животе натощак
- Потеря аппетита
- Тошнота
- Частая отрыжка
- Изжога, рефлюкс или ГЭРБ
- Язвы желудка или двенадцатиперстной кишки
- Гастрит (воспаление слизистой оболочки желудка)
H.pylori колонизирует эпителиальные клетки желудка. Когда бактерии расщепляют белки в стенке желудка, они вырабатывают фермент уреазу. Высокий уровень уреазы увеличивает содержание аммиака в желудке, что приводит к воспалению желудка и повреждению слизистой оболочки [15 Trusted Source PubMed Go to source].
Эрадикация Helicobacter pylori обычно устраняет эти симптомы.
Пробиотики – союзники лечения H. pyloriПробиотические бактерии были показаны в многочисленных метаанализах и систематических обзорах (данные высочайшего качества) для улучшения результатов лечения H.pylori.
В частности, было показано, что добавки с пробиотиками:
Долгосрочное использование пробиотиков также снижает риск развития расстройств, связанных с воспалением желудка, вызванных инфекцией H. pylori, таких как язвы, гастрит и т. Д. рак [20].
Не все данные совпадают. Один метаанализ пришел к выводу, что пробиотики не улучшили показатели эрадикации Helicobacter pylori, но обнаружили, что побочные эффекты, такие как диарея и тошнота, были уменьшены [21 Trusted Source PubMed Go to source].Небольшое клиническое исследование пришло к аналогичным выводам [22 Trusted Source PubMed Go to source].
Однако широкий спектр метаанализов, систематических обзоров и клинических испытаний пришел к выводу, что пробиотики имеют большое значение в лечении H. pylori. Учитывая эти данные, роль пробиотиков во время лечения должна быть заметной.
Лучшие пробиотики для лечения H. pyloriУченые изучили влияние многих различных типов пробиотиков на H.pylori. В некоторых исследованиях были протестированы отдельные штаммы, но было показано, что многие различные штаммы и комбинации эффективны для улучшения успеха лечения. Подведем итог тому, что мы знаем о лучших пробиотиках для лечения H. pylori.
Пробиотики Lactobacillus и Bifidobacteria и H. pyloriПробиотики Lactobacillus и Bifidobacteria были показаны в многочисленных метаанализах и систематических обзорах для поддержки успешного лечения H. pylori, хотя отчасти это может быть связано с тем, что они являются наиболее часто изучаемые пробиотики.
Известные исследования о лактобациллах (молочнокислых бактериях) и пробиотиках бифидобактерий (таких как Lactobacillus acidophilus и Lactobacillus reuteri) для H. pylori обнаружены:
- Lactobacillus casei был определен как лучший уровень эрадикации для H. pylori. 23 Надежный источник PubMed Перейти к источнику].
- Комбинации пробиотиков , которые включают Lactobacillus casei, L. plantarum, L. reuteri, L. salivarius, L. sporogenes, L.acidophilus, L. rhamnosus, Bifidobacterium infantis и B. longum могут помочь с побочными эффектами лечения , такими как диарея, запор, тошнота, рвота и нарушение вкуса [24 Надежный источник PubMed Перейти к источнику].
- Широкий спектр пробиотиков Lactobacillus повысил эффективность лечения H. pylori и снизил побочные эффекты [25 Надежный источник PubMed Перейти к источнику].
- Рандомизированное контролируемое исследование под руководством исследователя H. pylori Круше показало, что Lactobacillus johnsonii Li1 снижает уровень H.pylori у детей по сравнению с контрольной группой [26 Надежный источник PubMed Перейти к источнику].
- Штамм LG21 Lactobacillus gasseri , как было показано, увеличивает эрадикацию H. pylori и снижает побочные эффекты [27].
- Многообещающее пилотное исследование на мышах показало, что Lactobacillus gasseri OLL2716 снижает воспалительные цитокины и ингибирует рост устойчивых к антибиотикам H. pylori [28 Trusted Source PubMed Go to source]. Чтобы подтвердить клиническую ценность этого открытия, необходимо провести дополнительные исследования.
Saccharomyces boulardii – полезные дрожжи, обладающие пробиотическими свойствами. Он был широко изучен, и было показано, что он также способствует искоренению H. pylori.
В систематическом обзоре было показано, что только Saccharomyces boulardii устраняет инфекцию H. pylori в 12% случаев [29 Надежный источник PubMed Перейти к источнику], хотя для подтверждения необходимы дополнительные исследования этот результат.
Saccharomyces boulardii также было показано по крайней мере в двух метаанализах, чтобы повысить эффективность тройной терапии антибиотиками и уменьшить побочные эффекты [30 Надежный источник PubMed Перейти к источнику, 31 Надежный источник PubMed Перейти к источнику]
Кроме того, в систематическом обзоре было показано, что специально улучшает вздутие живота во время лечения H. pylori [32 Надежный источник PubMed Перейти к источнику].
Почвенные пробиотики (Bacillus)Исследований почвенных пробиотиков гораздо меньше по сравнению с двумя другими типами, но ограниченные исследования показывают, что почвенные пробиотики могут помочь H.pylori.
Систематический обзор пришел к выводу, что пробиотик с несколькими штаммами, включая почвенные бактерии, такие как Bacillus mesentericus и Streptococcus faecalis , улучшил потерю аппетита во время лечения. [33 Trusted Source PubMed Go to source].
Обзор доказательств использования пробиотиков Bacillus в лечении H. pylori пришел к выводу, что они были особенно эффективны для уменьшения диареи, связанной с антибиотиками [34]. В этом обзоре предполагается, что вероятный механизм связан с их способностью подавлять патогены и модулировать иммунный ответ организма.
Имея все эти данные, свидетельствующие о том, что пробиотики поддерживают лечение H. pylori, давайте посмотрим, как их лучше всего использовать.
Обследование и лечение H. pyloriЕсли у вас есть симптомы, связанные с H. pylori, такие как язвенная болезнь желудка или двенадцатиперстной кишки, стойкая и хроническая изжога или жжение в желудке, хорошей идеей может быть тестирование на H. pylori. .
Есть четыре способа проверить на инфекцию H. pylori.
Биопсия желудка во время эндоскопии – один из вариантов, но довольно инвазивный.Результаты могут отличаться в зависимости от метода отбора проб, степени распространения инфекции и того, как образец проверяется после сбора [35]. По этой причине другие методы тестирования могут дать лучшие результаты и, безусловно, будут менее дорогостоящими и инвазивными.
Тест на выдыхание мочевины ( UBT ) ищет фактор вирулентности уреазы в вашем дыхании после приема раствора для испытания. Любая лаборатория LabCorp или Quest может провести тест на дыхание мочевиной (UBT) для H.пилори.
Анализ крови на H. pylori ищет антитела к H. pylori. Положительный результат указывает на наличие инфекции в настоящем или прошлом. Этот тест наименее надежен для диагностики H. pylori [36].
S Инструментальные экраны для тестирования H. pylori . Некоторые лаборатории используют тесты ПЦР-ДНК для скрининга ДНК H. pylori в образце стула. Тест также проверяет, насколько вирулентны штаммы H. pylori, которые у вас есть, что может дать некоторые подсказки о том, насколько опасна инфекция.
Поговорите со своим врачом по поводу тестирования на H. pylori.
Следует ли лечить положительный тест на H. pylori?H. pylori определенно ассоциируется с язвой желудка и двенадцатиперстной кишки и гастритом, но есть некоторые споры о том, является ли H. pylori комменсальными (нормальными) бактериями в кишечнике или инфекционными бактериями, которые необходимо удалить.
Поскольку H. pylori широко распространен среди населения, его наличие не обязательно требует действий.Вероятно, лучший показатель того, следует ли вам лечить инфекцию H. pylori, – это наличие у вас явных симптомов H. pylori, таких как жжение в желудке, язвенная болезнь желудка или двенадцатиперстной кишки, хроническая изжога и рефлюкс.
Если у вас положительный результат на H. pylori, но нет симптомов инфекции, в лечении, скорее всего, нет необходимости. Если у вас есть симптомы, то, вероятно, стоит продолжить лечение.
Лечение H. pylori только пробиотикамиЕсли ваш тест на H.pylori, но у вас нет общих симптомов H. pylori, вам может быть просто полезно использовать пробиотики, чтобы сбалансировать свою микробиоту.
Систематический обзор действительно обнаружил, что небольшой процент инфекций H. pylori можно искоренить с помощью одних пробиотиков [37 Trusted Source PubMed Go to source]. Итак, если у вас положительный результат теста на H. pylori, и у вас ДЕЙСТВИТЕЛЬНО есть общие симптомы H. pylori, такие как гастрит, язва, боль в желудке или вздутие живота, вы также можете попробовать пробиотики в одиночку перед лечением более интенсивной терапией. .
Если ваши симптомы или тест на H. pylori не исчезают с помощью одних пробиотиков, вы можете рассмотреть возможность увеличения лечения, включив в него пробиотики и противомикробную терапию. Обязательно обсудите планы лечения со своим врачом.
Стандартное лечение H. pyloriСтандартное лечение антибиотиками первой линии от Helicobacter pylori, называемое «тройной терапией», которое длится 14 дней:
- Ингибитор протонной помпы (ИПП), такой как омепразол, за его ингибирующее действие на кислоту желудка, что способствует заживлению слизистой оболочки желудка.
- Два антибиотика вместе, такие как амоксициллин, метронидазол или кларитромицин
Однако скорость эрадикации H. pylori при этом режиме варьируется в зависимости от устойчивости штаммов H. pylori к антибиотикам [38 Надежный источник PubMed Перейти к источник]. Недавно были разработаны новые стратегии антибактериальной терапии, включая последовательную терапию [39 Trusted Source PubMed Перейти к источнику], при которой в течение курса лечения назначают серию антибиотиков, и четырехкратную терапию, при которой ИПП с несколькими антибиотиками назначают вместе с висмут [40 Надежный источник PubMed Перейти к источнику].
Среди врачей функциональной медицины и натуропатов стандартное лечение в клинической практике может включать растительные антибиотики и пробиотики в качестве анти-H. pylori подход.
Независимо от того, какой курс лечения назначит ваш врач, у многих пациентов наблюдаются побочные эффекты и побочные эффекты антибиотиков или растительных противомикробных препаратов. Вот где действительно сияют пробиотики.
Пробиотики с лечением антибиотиком H. pyloriСмешивание пробиотиков со стандартной эрадикационной терапией Helicobacter pylori увеличивает вероятность успеха лечения и уменьшает побочные эффекты, такие как диарея, связанная с антибиотиками, тошнота и вздутие живота [41 Надежный источник PubMed Перейти к источнику].
Включение пробиотиков в курс лечения против Helicobacter pylori с большой вероятностью сведет к минимуму эти побочные эффекты и увеличит вероятность успеха.
Исследования показывают, что совместное использование разнообразных пробиотиков дает лучшие результаты, чем один штамм или разновидность [42 Trusted Source PubMed Go to source, 43 Trusted Source PubMed Go to source], а исследование H. pylori поддерживает это [44 Надежный источник PubMed Перейти к источнику, 45 Надежный источник PubMed Перейти к источнику].Лучше всего использовать простой протокол, который включает по одному качественному пробиотику одновременно из каждой из трех основных категорий пробиотиков – смеси Lactobacillus-Bifidobacteria, Saccharomyces boulardii и пробиотика на почвенной основе. (Подробнее о том, как правильно использовать пробиотики, см. В нашем Руководстве по пробиотикам для начинающих.)
ИтогХотя искоренение инфекции H. pylori может быть сложной задачей из-за устойчивости к антибиотикам и побочных эффектов, пробиотики – прекрасный союзник.Было показано, что пробиотики увеличивают эрадикацию H. pylori, уменьшают неприятные побочные эффекты, такие как тошнота, диарея и вздутие живота. Испытайте пробиотическую терапию, прежде чем переходить к более традиционному лечению, а затем включите пробиотики в свой план лечения H. pylori, чтобы обеспечить успех.
Чтобы получить индивидуальную помощь с пищеварением, запишитесь на прием в Институт функциональной медицины Рушио.
➕ Ссылки
- Koga Y, Ohtsu T, Kimura K, et al.Пробиотический штамм L. gasseri (LG21) для верхних отделов желудочно-кишечного тракта, действующий за счет улучшения местной микробиоты. BMJ Open Gastro. 2019; 6: e000314. DOI: 10.1136 / bmjgast-2019-000314
- Ши X, Чжан Дж., Мо Л., Ши Дж., Цинь М., Хуанг X. Эффективность и безопасность пробиотиков в искоренении Helicobacter pylori: сетевой метаанализ. Медицина (Балтимор). 2019 апр; 98 (15): e15180. DOI: 10.1097 / MD.0000000000015180. PMID: 30985706; PMCID: PMC6485819. Надежный источник PubMed Перейти к источнику
- Losurdo G, Cubisino R, Barone M, Principi M, Leandro G, Ierardi E, Di Leo A.Монотерапия пробиотиками и ликвидация Helicobacter pylori : систематический обзор с анализом объединенных данных. Мир Дж. Гастроэнтерол. 2018 7 января; 24 (1): 139-149. DOI: 10.3748 / wjg.v24.i1.139. PMID: 29358890; PMCID: PMC5757118. Надежный источник PubMed Перейти к источнику
- Nagasawa S, Azuma T, Motani H, Sato Y, Hayakawa M, Yajima D, Kobayashi K, Ootsuka K, Iwase H. Обнаружение ДНК Helicobacter pylori (H.pylori) в пищеварительной системе от трупов методом ПЦР в реальном времени. Leg Med (Токио).2009 Апрель; 11 Приложение 1: S458-9. DOI: 10.1016 / j.legalmed.2009.03.001. Epub 2009 1 мая. PMID: 19410495. Надежный источник PubMed Перейти к источнику
- Ахмед Н. 23 года открытия Helicobacter pylori: споры окончены? Анн Клин Микробиол Антимикроб. 31 октября 2005 г .; 4:17. DOI: 10.1186 / 1476-0711-4-17. PMID: 16262889; PMCID: PMC1283743.
- Каур Б., Балгир П., Кумар Б., Гарг Н. Инфекция Helicobacter pylori: эффективность пробиотиков и роль полногеномных исследований ассоциации. Архив клинической микробиологии.Кафедра биотехнологии.
- Eusebi LH, Zagari RM, Bazzoli F. Эпидемиология инфекции Helicobacter pylori. Helicobacter. 2014 сентябрь; 19 Прил.1: 1-5. DOI: 10.1111 / hel.12165. PMID: 25167938. Надежный источник PubMed Перейти к источнику
- Marshall BJ (1994) Helicobacter pylori . Am J Gastroenterol 89: 116-118.
- Marshall BJ (1994) Helicobacter pylori . Am J Gastroenterol 89: 116-118.
- О’Коннор А., О’Мораин С. Пищеварительная функция желудка.Dig Dis. 2014; 32 (3): 186-91. DOI: 10,1159 / 000357848. Epub 2014, 10 апреля. PMID: 24732181. Надежный источник PubMed Перейти к источнику
- Ramsay PT, Carr A. Желудочная кислота и физиология пищеварения. Surg Clin North Am. 2011 Октябрь; 91 (5): 977-82. DOI: 10.1016 / j.suc.2011.06.010. PMID: 21889024. Надежный источник PubMed Перейти к источнику
- Leodolter A, Kulig M, Brasch H, Meyer-Sabellek W., Willich SN, Malfertheiner P. Метаанализ, сравнивающий частоту эрадикации, заживления и рецидивов у пациентов с Helicobacter pylori -ассоциированная язва желудка или двенадцатиперстной кишки.Алимент Pharmacol Ther. 2001 декабрь; 15 (12): 1949-58. DOI: 10.1046 / j.1365-2036.2001.01109.x. PMID: 11736726. Надежный источник PubMed Перейти к источнику
- Rauws EA, Tytgat GN. Лечение язвы двенадцатиперстной кишки, связанное с искоренением Helicobacter pylori. Ланцет. 1990 26 мая; 335 (8700): 1233-5. DOI: 10.1016 / 0140-6736 (90)
-р. PMID: 1971318. Надежный источник PubMed Перейти к источнику - Malfertheiner P, Leodolter A, Peitz U. Лечение язвенной болезни, связанной с Helicobacter pylori, путем ликвидации.Baillieres Best Pract Res Clin Gastroenterol. 2000 Февраль; 14 (1): 119-32. DOI: 10.1053 / bega.1999.0063. PMID: 10749093. Надежный источник PubMed Перейти к источнику
- Smoot DT. Как Helicobacter pylori вызывает повреждение слизистой оболочки? Прямые механизмы. Гастроэнтерология. 1997 декабрь; 113 (6 доп.): S31-4; обсуждение S50. DOI: 10.1016 / s0016-5085 (97) 80008-х. PMID: 9394757. Надежный источник PubMed Перейти к источнику
- Cremonini F, Di Caro S, Covino M, Armuzzi A, Gabrielli M, Santarelli L, Nista EC, Cammarota G, Gasbarrini G, Gasbarrini A.Влияние различных пробиотических препаратов на побочные эффекты, связанные с терапией против Helicobacter pylori: параллельное групповое, тройное слепое, плацебо-контролируемое исследование. Am J Gastroenterol. 2002 ноя; 97 (11): 2744-9. DOI: 10.1111 / j.1572-0241.2002.07063.x. PMID: 12425542. Надежный источник PubMed Перейти к источнику
- Lü M, Yu S, Deng J, Yan Q, Yang C, Xia G, Zhou X. Эффективность терапии пробиотическими добавками для эрадикации Helicobacter pylori: метаанализ Рандомизированные контролируемые испытания.PLoS One. 2016 10 октября; 11 (10): e0163743. DOI: 10.1371 / journal.pone.0163743. PMID: 27723762; PMCID: PMC5056761. Надежный источник PubMed Перейти к источнику
- Tong JL, Ran ZH, Shen J, Zhang CX, Xiao SD. Мета-анализ: влияние добавления пробиотиков на частоту эрадикации и побочные эффекты во время эрадикационной терапии Helicobacter pylori. Алимент Pharmacol Ther. 2007 15 января; 25 (2): 155-68. DOI: 10.1111 / j.1365-2036.2006.03179.x. PMID: 17229240. Надежный источник PubMed Перейти к источнику
- Koga Y, Ohtsu T, Kimura K, et al.Пробиотический штамм L. gasseri (LG21) для верхних отделов желудочно-кишечного тракта, действующий за счет улучшения местной микробиоты. BMJ Open Gastro. 2019; 6: e000314. DOI: 10.1136 / bmjgast-2019-000314
- Кога Ю., Оцу Т., Кимура К. и др. Пробиотический штамм L. gasseri (LG21) для верхних отделов желудочно-кишечного тракта, действующий за счет улучшения местной микробиоты. BMJ Open Gastro. 2019; 6: e000314. doi: 10.1136 / bmjgast-2019-000314
- Lu C, Sang J, He H, Wan X, Lin Y, Li L, Li Y, Yu C. Прием пробиотиков не улучшает скорость эрадикации инфекции Helicobacter pylori по сравнению с плацебо. по стандартной терапии: метаанализ.Sci Rep.21 марта 2016; 6: 23522. DOI: 10,1038 / srep23522. PMID: 26997149; PMCID: PMC4800733. Надежный источник PubMed Перейти к источнику
- Наварро-Родригес Т., Сильва Ф.М., Барбути Р.С., Маттар Р., Мораес-Филхо Дж. П., де Оливейра М. Н., Богсан К. С., Чинзон Д., Эйсиг Дж. Н.. Связь пробиотика со схемой эрадикации Helicobacter pylori не увеличивает эффективность и не снижает побочные эффекты лечения: проспективное, рандомизированное, двойное слепое, плацебо-контролируемое исследование. BMC Gastroenterol.2013 26 марта; 13:56. DOI: 10.1186 / 1471-230X-13-56. PMID: 23530767; PMCID: PMC3614530. Надежный источник PubMed Перейти к источнику
- Feng JR, Wang F, Qiu X, McFarland LV, Chen PF, Zhou R, Liu J, Zhao Q, Li J. Эффективность и безопасность тройной терапии с добавлением пробиотиков для искоренения Helicobacter pylori у детей: систематический обзор и сетевой метаанализ. Eur J Clin Pharmacol. 2017 Октябрь; 73 (10): 1199-1208. DOI: 10.1007 / s00228-017-2291-6. Epub 2017, 5 июля. PMID: 28681177. Надежный источник PubMed Перейти к источнику
- Feng JR, Wang F, Qiu X, McFarland LV, Chen PF, Zhou R, Liu J, Zhao Q, Li J.Эффективность и безопасность тройной терапии с добавлением пробиотиков для эрадикации Helicobacter pylori у детей: систематический обзор и сетевой метаанализ. Eur J Clin Pharmacol. 2017 Октябрь; 73 (10): 1199-1208. DOI: 10.1007 / s00228-017-2291-6. Epub 2017, 5 июля. PMID: 28681177. Надежный источник PubMed Перейти к источнику
- Shi X, Zhang J, Mo L, Shi J, Qin M, Huang X. Эффективность и безопасность пробиотиков в искоренении Helicobacter pylori: сетевая мета -анализ. Медицина (Балтимор). 2019 апр; 98 (15): e15180.DOI: 10.1097 / MD.0000000000015180. PMID: 30985706; PMCID: PMC6485819. Надежный источник PubMed Перейти к источнику
- Cruchet S, Obregon MC, Salazar G, Diaz E, Gotteland M. Влияние приема диетического продукта, содержащего Lactobacillus johnsonii La1, на колонизацию Helicobacter pylori у детей. Питание. 2003 сентябрь; 19 (9): 716-21. DOI: 10.1016 / s0899-9007 (03) 00109-6. PMID: 12921879. Надежный источник PubMed Перейти к источнику
- Koga Y, Ohtsu T, Kimura K, et al. Пробиотик L.gasseri (LG21) для верхних отделов желудочно-кишечного тракта за счет улучшения местной микробиоты. BMJ Open Gastro. 2019; 6: e000314. doi: 10.1136 / bmjgast-2019-000314
- Ushiyama A, Tanaka K, Aiba Y, Shiba T, Takagi A, Mine T, Koga Y. Lactobacillus gasseri OLL2716 в качестве пробиотика при резистентной к кларитромицину инфекции Helicobacter pylori. J Gastroenterol Hepatol. 2003 августа; 18 (8): 986-91. DOI: 10.1046 / j.1440-1746.2003.03102.x. PMID: 12859730. Надежный источник PubMed Перейти к источнику
- Losurdo G, Cubisino R, Barone M, Principi M, Leandro G, Ierardi E, Di Leo A.Монотерапия пробиотиками и ликвидация Helicobacter pylori : систематический обзор с анализом объединенных данных. Мир Дж. Гастроэнтерол. 2018 7 января; 24 (1): 139-149. DOI: 10.3748 / wjg.v24.i1.139. PMID: 29358890; PMCID: PMC5757118. Надежный источник PubMed Перейти к источнику
- Wang F, Feng J, Chen P, Liu X, Ma M, Zhou R, Chang Y, Liu J, Li J, Zhao Q. Пробиотики в терапии эрадикации Helicobacter pylori: систематический обзор и сетевой метаанализ. Клин Рес Гепатол Гастроэнтерол.2017 сентябрь; 41 (4): 466-475. DOI: 10.1016 / j.clinre.2017.04.004. Epub 2017 25 мая. PMID: 28552432. Надежный источник PubMed Перейти к источнику
- Zhou BG, Chen LX, Li B, Wan LY, Ai YW. Saccharomyces boulardii в качестве адъювантной терапии для эрадикации Helicobacter pylori: систематический обзор и метаанализ с последовательным анализом проб. Helicobacter. 2019 Октябрь; 24 (5): e12651. DOI: 10.1111 / hel.12651. Epub 2019, 14 августа. PMID: 31414551. Надежный источник PubMed Перейти к источнику
- Feng JR, Wang F, Qiu X, McFarland LV, Chen PF, Zhou R, Liu J, Zhao Q, Li J.Эффективность и безопасность тройной терапии с добавлением пробиотиков для эрадикации Helicobacter pylori у детей: систематический обзор и сетевой метаанализ. Eur J Clin Pharmacol. 2017 Октябрь; 73 (10): 1199-1208. DOI: 10.1007 / s00228-017-2291-6. Epub 2017, 5 июля. PMID: 28681177. Надежный источник PubMed Перейти к источнику
- Feng JR, Wang F, Qiu X, McFarland LV, Chen PF, Zhou R, Liu J, Zhao Q, Li J. Эффективность и безопасность Тройная терапия с добавлением пробиотиков для искоренения Helicobacter pylori у детей: систематический обзор и сетевой метаанализ.Eur J Clin Pharmacol. 2017 Октябрь; 73 (10): 1199-1208. DOI: 10.1007 / s00228-017-2291-6. Epub 2017, 5 июля. PMID: 28681177. Надежный источник PubMed Перейти к источнику
- Джаянти Н., Ратна Судха М. (2015) Bacillus clausii – лучший пробиотик в лечении диареи. J Yoga Phys Ther 5: 211. doi: 10.4172 / 2157-7595.1000211
- Pohl D, Keller PM, Bordier V, Wagner K. Обзор современных диагностических методов и достижений в диагностике Helicobacter pylori в эпоху секвенирования следующего поколения.Мир Дж. Гастроэнтерол. 2019 28 августа; 25 (32): 4629-4660. DOI: 10.3748 / wjg.v25.i32.4629. PMID: 31528091; PMCID: PMC6718044.
- Khalifehgholi M, Shamsipour F, Ajhdarkosh H, Ebrahimi Daryani N, Pourmand MR, Hosseini M, Ghasemi A, Shirazi MH. Сравнение пяти методов диагностики Helicobacter pylori. Иран J Microbiol. 2013 декабрь; 5 (4): 396-401. PMID: 25848511; PMCID: PMC4385167.
- Losurdo G, Cubisino R, Barone M, Principi M, Leandro G, Ierardi E, Di Leo A. Пробиотическая монотерапия и искоренение Helicobacter pylori : систематический обзор с анализом объединенных данных.Мир Дж. Гастроэнтерол. 2018 7 января; 24 (1): 139-149. DOI: 10.3748 / wjg.v24.i1.139. PMID: 29358890; PMCID: PMC5757118. Надежный источник PubMed Перейти к источнику
- Боянова Л., Хаджийский П., Кандиларов Н., Марковская Р., Митов И. Множественная лекарственная устойчивость Helicobacter pylori : текущее состояние и направления на будущее. Эксперт Rev Clin Pharmacol. 2019 сентябрь; 12 (9): 909-915. DOI: 10.1080 / 17512433.2019.1654858. Epub 2019, 28 августа. PMID: 31424296. Надежный источник PubMed Перейти к источнику
- ekin AH, ahintürk Y, Akbay Harmandar F, Uyar S, Yolcular BO, ekin Y.Использование пробиотиков в качестве адъюванта к последовательной эрадикационной терапии H. pylori: влияние на частоту эрадикации, резистентность к лечению, побочные эффекты, связанные с лечением, и соблюдение пациентом режима лечения. Turk J Gastroenterol. 2017 Янв; 28 (1): 3-11. DOI: 10.5152 / tjg.2016.0278. Epub 2016, 23 декабря. PMID: 28007678. Надежный источник PubMed Перейти к источнику
- Selgrad M, Bornschein J, Malfertheiner P. Рекомендации по лечению Helicobacter pylori на Востоке и Западе. Эксперт Rev Anti Infect Ther. 2011 август; 9 (8): 581-8.DOI: 10.1586 / eri.11.80. PMID: 21819326. Надежный источник PubMed Перейти к источнику
- Feng JR, Wang F, Qiu X, McFarland LV, Chen PF, Zhou R, Liu J, Zhao Q, Li J. Эффективность и безопасность тройной терапии с пробиотиками по искоренению Helicobacter pylori у детей: систематический обзор и сетевой метаанализ. Eur J Clin Pharmacol. 2017 Октябрь; 73 (10): 1199-1208. DOI: 10.1007 / s00228-017-2291-6. Epub 2017, 5 июля. PMID: 28681177. Надежный источник PubMed Перейти к источнику
- Целевая группа Американского колледжа гастроэнтерологии по синдрому раздраженного кишечника, Brandt LJ, Chey WD, Foxx-Orenstein AE, Schiller LR, Schoenfeld PS, Spiegel BM, Талли, штат Нью-Джерси, Куигли Э.М.Изложение позиции, основанной на фактах, в отношении лечения синдрома раздраженного кишечника. Am J Gastroenterol. 2009 Янв; 104 Приложение 1: С1-35. DOI: 10.1038 / ajg.2008.122. PMID: 19521341. Надежный источник PubMed Перейти к источнику
- Ford AC, Quigley EM, Lacy BE, Lembo AJ, Saito YA, Schiller LR, Soffer EE, Spiegel BM, Moayyedi P. Эффективность пребиотиков, пробиотиков и синбиотиков в синдром раздраженного кишечника и хронический идиопатический запор: систематический обзор и метаанализ. Am J Gastroenterol.2014 октябрь; 109 (10): 1547-61; quiz 1546, 1562. DOI: 10.1038 / ajg.2014.202. Epub 2014, 29 июля. PMID: 25070051. Надежный источник PubMed Перейти к источнику
- Feng JR, Wang F, Qiu X, McFarland LV, Chen PF, Zhou R, Liu J, Zhao Q, Li J. Эффективность и безопасность Тройная терапия с добавлением пробиотиков для искоренения Helicobacter pylori у детей: систематический обзор и сетевой метаанализ. Eur J Clin Pharmacol. 2017 Октябрь; 73 (10): 1199-1208. DOI: 10.1007 / s00228-017-2291-6. Epub, 5 июля 2017 г. PMID: 28681177.Надежный источник PubMed Перейти к источнику
- Ши Х, Чжан Дж, Мо Л, Ши Дж, Цинь М., Хуанг Х. Эффективность и безопасность пробиотиков в искоренении Helicobacter pylori: сетевой метаанализ. Медицина (Балтимор). 2019 апр; 98 (15): e15180. DOI: 10.1097 / MD.0000000000015180. PMID: 30985706; PMCID: PMC6485819. Надежный источник PubMed Перейти к источнику
Нужна помощь или вы хотите узнать больше?
Получить помощь
Посмотреть дополнительные ресурсы доктора РушиоУстойчивый Helicobacter pylori (H.pylori) – Центр болезней органов пищеварения
Helicobacter pylori (H. pylori) – это спиралевидная бактерия, поражающая более 30% населения мира. В некоторых странах им заражено более 50% населения 3 . Таким образом, это одна из наиболее распространенных бактериальных инфекций человека.
Обнаружение CDD
После подтверждения в 1980-х годах, что H. pylori вызывает пептические язвы, медицинский директор и основатель Центра болезней органов пищеварения доктор Томас Бороди разработал первую терапию для борьбы с H.pylori и вылечить язвенную болезнь 1,2 . Это стало золотым стандартом во всем мире.
Всемирная организация здравоохранения объявила бактерии канцерогеном класса 1 (что означает, что бактерия вызывает рак у человека). Он проникает в слизистую оболочку желудка и является причиной до 80% язв двенадцатиперстной кишки и до 60% язв желудка, а также был связан с раком желудка и лимфомой 3 .
Трансмиссия
Несмотря на тщательное расследование распространения H.pylori , точный способ передачи остается неясным. Есть некоторые свидетельства того, что H. pylori передается от человека к человеку фекально-оральным путем, но способ передачи остается неясным. На этом этапе наиболее вероятны орально-оральные или фекально-оральные пути передачи. Большинство инфекций, вызванных H. pylori , происходит в детском возрасте. Переполненные жилищные условия, плохая санитария, плохая личная гигиена и плохое водоснабжение коррелируют с более высоким уровнем инфицирования (который может достигать 80% населения в развивающихся странах).
H.pylori одинаково заражает обоих полов.
Симптомы
У большинства людей с H. pylori симптомы отсутствуют, но симптомы инфекции могут включать жгучую боль в верхней части живота, расстройство желудка, тошноту, рвоту, отрыжку, потерю аппетита.
Осложнения
- Pylori тесно связан с развитием язв желудка и двенадцатиперстной кишки. Искоренение H.pylori может предотвратить образование язв. Пациенты с язвой должны быть проверены на H. pylori и получить лечение, поскольку уничтожение этой бактерии у пациентов с уже существующими язвами не только излечивает язвенную болезнь, но и предотвращает большинство рецидивов.
В то время как присутствие H. pylori в желудке вызывает хроническое активное воспаление почти у всех инфицированных, менее чем у 10% людей, колонизированных H. pylori , развиваются серьезные заболевания или осложнения, такие как язвенная болезнь желудка, рак желудка. или лимфому, ассоциированную со слизистой оболочкой лимфоидной ткани (MALT).
Имеются убедительные доказательства того, что H. pylori способствует развитию рака желудка. Многие факторы, вероятно, вызывают рак, поскольку только у небольшой части пациентов с H. pylori развивается рак желудка. Диета с низким содержанием фруктов / овощей, курение, возраст и высокое потребление соли также увеличивают риск рака желудка независимо от инфекции H. pylori . Однако из всех этих факторов именно инфекция H. pylori наиболее тесно связана с раком желудка.Следовательно, из-за известной связи, все пациенты с H. pylori должны рассматриваться для лечения.
Инфекция H.pylori также может привести к развитию состояния, известного как лимфома, ассоциированная со слизистой оболочкой, лимфоидной ткани (MALT), разновидность рака желудка. Лечение и искоренение инфекции H. pylori может привести к регрессу злокачественного новообразования в 75% случаев.
Диагностика
Существует множество различных тестов, используемых для диагностики H.pylori инфекция. Тесты на H. pylori могут быть инвазивными, требующими эндоскопии верхних отделов желудочно-кишечного тракта (гастроскопии) и основанными на анализе образцов биопсии желудка, или неинвазивными с использованием тест-полосок и дыхательных тестов 3 .
- Гастроскопия – Гастроэнтеролог может выполнить панендоскопию (также известную как гастроскопия). Это обследование требует, чтобы пациент был седативен, прежде чем эндоскоп, оснащенный миниатюрным видеооборудованием, будет введен через рот в пищевод.Затем гастроэнтеролог может взять биопсию (образец ткани) для патологического исследования, чтобы определить наличие инфекции pylori .
Гистологический диагноз, при котором образец ткани исследуется под микроскопом, является золотым стандартом. Помимо подтверждения наличия H. pylori , патологическое состояние слизистой оболочки желудка может быть определено как острый или хронический гастрит, атрофия, аномальные клетки (метаплазия или дисплазия – предраковые изменения), пищевод Барретта или даже лимфома. / злокачественность.
Для подтверждения инфекции также можно использовать экспресс-тест на уреазу. Известно, что эти тесты достигают очень высокого уровня точности.
Культура H. pylori может быть проведена на такой биопсии ткани для определения чувствительности к конкретным антибиотикам. Это особенно важно для пациентов, которые не прошли обычное лечение и все еще являются носителями инфекции. У этих людей проверяется чувствительность H. pylori , чтобы гарантировать начало наиболее подходящего лечения.
- Дыхательные тесты на мочевину – Дыхательные тесты обеспечивают быстрый неинвазивный способ определения наличия активной инфекции и часто используются для проверки успешности ликвидации. В этом тесте для определения инфекции используется образец выдыхаемого воздуха.
Принцип этого теста основан на способности бактерий преобразовывать соединение, называемое мочевиной, в диоксид углерода. Специально меченая мочевина вводится перорально в таблетированной форме, а выдыхаемый воздух проверяется на содержание меченого углекислого газа.Эти тесты очень точны и просты в выполнении.
- Серология – кровь пациента может быть проверена на наличие антител к pylori , что указывает на иммунный ответ на бактерии. Эти тесты немного менее точны, чем другие доступные тесты, и не делают различий между текущей инфекцией и недавним контактом. У тех пациентов, у которых слизистая оболочка желудка изменилась до предраковой формы кишечной метаплазии, нельзя использовать ни биопсию, ни дыхательные тесты на мочевину, так как бактерий очень мало.Однако серийный серологический анализ концентраций антител может быть использован в качестве последующего наблюдения после лечения инфекции H. pylori .
- Тест на антиген стула – Это довольно точный тест, и он используется все чаще.
Терапия первой линии
Лечение H. pylori направлено на уничтожение бактерий из желудка с помощью комбинации антибиотиков, специфичных для организма, с кислотным супрессором и / или желудочным протектором.Использование только одного или двух препаратов для лечения H. pylori не рекомендуется. В разных странах существуют разные одобренные методы лечения H. pylori . В настоящее время доказанным и эффективным лечением в Австралии является 7-дневный курс лечения под названием Triple Therapy, включающий два антибиотика, амоксициллин и кларитромицин, для уничтожения бактерий вместе с кислотным супрессором для повышения активности антибиотика. Этот режим тройной терапии уменьшает симптомы язвы, убивает H.pylori и предотвращает рецидив язвы примерно у 70% пациентов, но его эффективность постепенно падает.
С использованием антибиотиков для лечения такого количества пациентов с различными заболеваниями стало труднее лечить H. pylori из-за увеличения числа штаммов, устойчивых к антибиотикам. В результате до 35% пациентов не проходят терапию первой линии.
Вторая линия и последующие методы лечения резистентной H. pylori
В Центре болезней органов пищеварения после неудачного лечения, а иногда и при начальном лечении, специально для пациента разрабатывают комбинированный режим, часто руководствуясь профилем чувствительности бактерий к антибиотикам.Используя эти индивидуальные методы лечения, наши гастроэнтерологи могут лечить даже резистентный H.pylori .
Исследования
В Центре болезней пищеварительной системы мы особенно заинтересованы в разработке «спасательных» или «спасательных» методов лечения, которые используются для лечения пациентов, которые не прошли другие стандартные методы лечения. В этих методах лечения используются различные комбинации трех или более препаратов против H. pylori в сочетании с лекарством для стимуляции иммунитета слизистой оболочки желудка.
Контактная информация
Если вы хотите встретиться с одним из наших гастроэнтерологов, чтобы обсудить ваше состояние и рассмотреть возможность лечения, перейдите по следующей ссылке, чтобы узнать, как стать пациентом в Центре болезней органов пищеварения: https://centrefordigestivediseases.com / Как стать пациентом / .
Ссылки и дополнительная литература
1 Бороды Т.Дж. (2016). Разработка новых методов лечения дисбиоза кишечника. Открытые публикации ученых UTS (OPUS). Идентификатор: http://hdl.handle.net/10453/52985
Ссылка на диссертацию: https://opus.lib.uts.edu.au/bitstream/10453/52985/6/01front.pdf
2 Эслик, Г.Д., Тилден, Д., Арора, Н., Торрес, М., Клэнси, Р.Л. (2020). Клиническое и экономическое влияние «тройной терапии» эрадикации Helicobacter pylori на язвенную болезнь в Австралии. Helicobacter, 25 (6) . Doi: 10.1111 / hel.12751
Ссылка на статью: https: // onlinelibrary.wiley.com/doi/epdf/10.1111/hel.12751
3 Яксли, Дж. И Чакраварти, Б. (2014). Ликвидация Helicobacter pylori – последняя информация о последних методах лечения. Австралийский семейный врач, 43 (5): 301-305.
Ссылка на статью: https://www.racgp.org.au/afp/2014/may/helicobacter-pylori-eradication/
Комбинированная лекарственная терапия при язвенной болезни
Примеры
Схемы комбинированной лекарственной терапии
Комбинированные препараты схемы терапии, обычно используемые для лечения H.пилори Инфекция включает следующие варианты:
- Ингибитор протонной помпы (ИПП) плюс кларитромицин плюс амоксициллин или метронидазол
- Ингибитор протонной помпы плюс висмут соединение плюс метронидазол плюс тетрациклин
Антибиотики
Некоторые примеры используемых антибиотиков для лечения H. pylori :
амоксициллин кларитромицин Биаксин метронидазол Flagyl тетрациклин Расфасованные комбинации лекарств
Некоторые из рекомендуемых комбинаций лекарств: упакованы вместе для удобства.
Субцитрат висмута калий и метронидазол и тетрациклин Пилера субсалицилат висмута и метронидазол и тетрациклин Helidac лансопразол (ИПП) и амоксициллин и кларитромицин Prevpac омепразол (ИПП), амоксициллин и кларитромицин Как это работает
Правильные комбинации антибиотиков обычно убивают Helicobacter pylori ( H.pylori ) бактерии, вызывающие многие пептические язвы. Используются как минимум два антибиотика, потому что комбинированное лечение работает лучше и менее эффективно. вероятно потерпит неудачу из-за устойчивость к антибиотикам.
Почему используется
Комбинированная лекарственная терапия, включает как минимум два антибиотика, восстановитель кислоты и иногда висмут соединение рекомендуется для людей, которые страдают язвенной болезнью и известны быть инфицированным Helicobacter pylori ( H.pylori ).
Насколько хорошо это работает?
Helicobacter pylori ( H. pylori ) Инфекции излечиваются от 70% до 85% времени, если используется правильное комбинированное лекарственное лечение. 1
Побочные эффекты
Все лекарства имеют побочные эффекты. Но многие люди не чувствуют побочных эффектов или могут с ними справиться. Спросите своего фармацевта о побочных эффектах каждого лекарства, которое вы принимаете. Побочные эффекты также перечислены в информации, прилагаемой к вашему лекарству.
Вот некоторые важные вещи, о которых стоит подумать:
- Обычно польза от лекарства более важна, чем любые незначительные побочные эффекты.
- Побочные эффекты могут исчезнуть через некоторое время после приема лекарства.
- Если побочные эффекты все еще беспокоят вас, и вы задаетесь вопросом, следует ли вам продолжать принимать лекарство, позвоните своему врачу . Он или она может снизить дозу или изменить лекарство. Не прекращайте прием лекарства внезапно, если только врач не сказал вам об этом.
Немедленно позвоните 911 или в другую службу экстренной помощи , если у вас:
- Проблемы с дыханием.
- Отек лица, губ, языка или горла.
Позвоните своему врачу, если у вас:
- Крапивница.
- Стул с кровью, черный или дегтеобразный.
- Сильная боль в животе или тошнота.
- Сильная диарея.
Общие побочные эффекты этого лекарства включают:
- Головная боль.
- Темный язык и темный стул, вызванные висмутом.
- Легкая диарея.
- Язвы во рту.
- Зуд или выделения из влагалища.
См. Справочник по лекарствам для получения полного списка побочных эффектов. (Ссылка на лекарства не доступно во всех системах.)
Что думать
Очень важно, чтобы вы принять все прописанные лекарства. Не прекращайте прием лекарства, даже если тебе лучше. Может показаться, что нужно принять много таблеток, но это также важно принять схему, содержащую как минимум три лекарства для лечения Helicobacter pylori ( H.pylori ). Комбинированные схемы – наиболее эффективный способ гарантировать, что Бактерии H. pylori не развивают устойчивость к антибиотики, используемые для их лечения.
Полностью избегайте употребления алкоголя (включая безрецептурные ночные лекарства от простуды, такие как NyQuil), когда вы принимаете метронидазол. Сочетание алкоголя с этим лекарством может вызвать сильную тошноту и рвоту.
Тетрациклин может сделать вашу кожу более чувствительной к солнцу.
- По возможности держитесь подальше от солнца.
- По возможности надевайте длинные брюки, рубашки с длинными рукавами и головные уборы.
- Используйте солнцезащитный крем с SPF, рекомендованным вашим врачом.
Избегайте употребления молока и других молочных продуктов, антацидов или добавок и витаминов, содержащих железо, в течение 2 часов после приема тетрациклина.
Принимая эти лекарства, запивая полным стаканом воды, можно предотвратить раздражение пищевода.
Прием лекарств
Лекарства – одно из многих инструментов, которые может иметь ваш врач для лечения проблемы со здоровьем.Прием лекарств по рекомендации врача улучшит ваше здоровье и может предотвратить проблемы в будущем. Если вы не принимаете лекарства должным образом, вы можете подвергнуть риску свое здоровье (и, возможно, свою жизнь).
Есть много причин, по которым люди не могут принимать лекарства. Но в большинстве случаев вы можете что-то сделать. Для получения рекомендаций о том, как обойти типичные проблемы, см. Раздел «Прием лекарств по назначению».
Рекомендации для женщин
Комбинации, содержащие метронидазол или тетрациклин
Не используйте это лекарство , если вы беременны или планируете забеременеть.Если вам нужно использовать это лекарство, поговорите со своим врачом о том, как вы можете предотвратить беременность.
Все другие комбинации
Если вы беременны, кормите грудью или планируете забеременеть, не принимайте никаких лекарств, если ваш врач не говорит вам об этом. Некоторые лекарства могут навредить вашему ребенку. Сюда входят лекарства, отпускаемые по рецепту и без рецепта, витамины, травы и добавки. И убедитесь, что все ваши врачи знают, что вы беременны, кормите грудью или планируете забеременеть.
Контрольные осмотры
Последующее наблюдение является ключевым элементом вашего лечения и безопасности. Обязательно приходите на все приемы и звоните своему врачу, если у вас возникли проблемы. Также неплохо знать результаты своих анализов и вести список лекарств, которые вы принимаете.
Некоторые люди, которые прошли курс лечения от инфекции H. pylori , нуждаются в последующее тестирование, чтобы убедиться, что инфекция вылечил.
Заполните новую форму информации о лекарстве (PDF) (Что такое PDF-документ?), Чтобы помочь вам разобраться в этом лекарстве.
Ссылки
Ссылки
- Chey WD, et al. (2007). Американский колледж Гастроэнтерологическое руководство по лечению инфекции Helicobacter pylori. Американский журнал гастроэнтерологии, 102 (8): 1808–1825.
Консультации по другим работам
- Ян YX и др. (2006). Долговечный протонный насос ингибиторная терапия и риск перелома шейки бедра. ДЖАМА, 296 (24): 2947–2953.
Кредиты
ByHealthwise Staff
Главный медицинский экспертГрегори Томпсон, врач-терапевт
, медицинский специалист-обозреватель Джером Б. Саймон, доктор медицины, FRCPC, FACP – гастроэнтерологияПо состоянию на 14 ноября 2014 г.
Пробиотики для лечения Helicobacter pylori | 2002-05-01
Пробиотики для лечения
Helicobacter pyloriАвтор: Джей Удани, доктор медицины, и Майлс Спар, доктор медицины, магистратура в час
Пробиотики традиционно определяются как живые микроорганизмы, принадлежащие к естественной кишечной флоре, которые оказывают положительный эффект при профилактике или лечении определенных патологических состояний при попадании в организм.Те, что используются таким образом, составляют небольшую часть из более чем 500 видов бактерий, которые симбиотически живут в кишечнике человека.
Helicobacter pylori является основным этиологическим фактором язвенной болезни и фактором риска рака желудка: этот организм вызывает шестикратный риск развития этого рака. 1 Распространенность инфекции в США оценивается в 45-52%. Этот грамотрицательный стержень обычно начинает колонизировать пищеварительный тракт в молодости, и его распространенность увеличивается на протяжении всей жизни.По оценкам, 70-80% пожилых людей являются переносчиками бактерий. 2
Доказано, что использование пробиотиков, также называемых «микробным вмешательством», эффективно при лечении многих желудочно-кишечных заболеваний, включая инфекционную диарею, воспалительное заболевание кишечника, синдром раздраженного кишечника и непереносимость лактозы. 3 Пастер и Жубер отметили, что этот тип терапии оказался успешным. еще в 1877 году, и сейчас переживает возрождение для лечения H.Инфекция Pylori , среди прочего условия.
Обычное лечение
Консенсусная конференция Национальных институтов здравоохранения в 1994 году пришла к выводу, что все пациенты с язвенной болезнью, будь то при первом обращении, рецидиве или с язвой в анамнезе, которые являются положительными на H. pylori , должны лечиться от этой инфекции. 4 Лечение антибиотиками требует 14-дневного приема нескольких лекарств. Текущий стандарт лечения включает использование ингибитора протонной помпы с двумя антибиотиками, обычно кларитромицином и амоксициллином, с висмутом или без него.Этот протокол позволяет добиться уничтожения более чем на 90%; однако он требует частого дозирования и связан с побочными эффектами. Одно исследование показало, что 25% пациентов, получавших стандартную терапию, испытывают ограничивающие работу побочные эффекты, такие как сыпь, светочувствительность, рвота, невропатия и лихорадка. 5
Идентификация пробиотиков
Наиболее изученными пробиотиками являются молочнокислые бактерии, Lactobacillus sp. И Bifidobacterium sp.Другие используемые организмы включают Escherichia coli , Streptococcus sp., Enterococcus sp., Bacteroides sp., Bacillus sp., Propionibacterium sp. И различные грибы (см. Таблицу ). 1, ниже) . Многие пробиотические препараты содержат смеси более чем одного вида бактерий.
Таблица 1
Профили избранных штаммов пробиотиков
Штамм Механизм действия Текущее использование Лактобациллы ацидофильный Подавляет привязанность; подавляет инвазию; конкурирует за питательные вещества; производит молочную кислоту и перекись водорода и натуральные антибиотики
H.пилори
Bifidobacterium bifidum Подавляет колонизацию; производит уксусную кислоту; стимулирует выработку антител; способствует усвоению кальция; помогает избавить организм от шлаков; производит молочную и уксусную кислоты Развитие иммунной системы у детей, находящихся на искусственном вскармливании; детский понос; Хеликобактер пилори
Лактобациллы болгарик Протеолитический; производит молочную кислоту; подавляет адгезию; удаляет свободные радикалы; стимулирует функцию Т-лимфоцитов
Кислотный рефлюкс; непереносимость лактозы Стрептококк термофильный Используется для производства йогурта; помогает расщеплять лактозу
Непереносимость лактозы Лактобациллы рутери Производит молочную кислоту
Детство диарея Лактобациллы GG Продукция молочная кислота синдром раздраженного кишечника; заболевание раздраженного кишечника; профилактика аллергии у новорожденных; иммунная система улучшение Механизм действия
Существует множество механизмов, с помощью которых пробиотики способствуют антимикробному действию.Они включают в себя стимуляцию иммунитета, конкуренцию за ограниченные питательные вещества, ингибирование адгезии эпителия и слизистых оболочек, ингибирование эпителиальной инвазии и производство противомикробных препаратов. вещества. 6
Для последних нескольких механизмов было показано, что Lactobacillus acidophilus , анаэробная грамположительная бактерия, оказывает ингибирующее действие на прикрепление H. pylori к эпителиальным клеткам желудка in vitro. 7 L. acidophilus также может продуцировать бактериоцины, которые представляют собой белки с антибиотико-подобными бактерицидными свойствами, 8 , а также молочную кислоту и перекись водорода, которые ограничивают рост H.pylori . 9 Исследование in vitro одного типа пробиотика, Bacillus subtilis 3, который подавляет рост H. pylori , показало, что этот вид продуцирует как минимум два антибиотических вещества. 10 Некоторые виды лактобацилл могут вырабатывать оксид азота и другие эндотоксины, убивающие патологические бактерии. 11
Исследования in vitro и на животных
В исследовании 1995 года сообщалось об ингибировании роста H. pylori L.acidophilus и Lactobacillus delbrueckii , последняя является типичной молочной бактерией, обнаруживаемой в йогуртовых культурах. 12 В другом исследовании изучалась бактерия Clostridium butyricum , обнаруженная среди нормальной флоры человека, против H. pylori in vitro и на мышах. Эта группа продемонстрировала ингибирование адгезии H. pylori к эпителиальным клеткам желудка и излечение инфекции H. pylori у мышей. 7
Клинические исследования
Особенно актуальны несколько рандомизированных контролируемых испытаний (РКИ) и две серии случаев.В трех рандомизированных контролируемых исследованиях и серии случаев изучались показатели симптомов, купирования и искоренения симптомов, а в одном испытании изучалось влияние лактобацилл на побочные эффекты стандартной тройной терапии (см. Таблицу 2, ниже) .
Таблица 2
Пробиотики против антибиотиков
Параметр Пробиотики Тройная терапия с антибиотиками Допуск Отлично Умеренный Безопасность
О нежелательных явлениях не сообщалось Лекарственные взаимодействия, нейротоксичность Побочные эффекты
Минимальный Тошнота, рвота, сыпь, светочувствительность, возможная нейропатия
Стоимость
~ 35 долл. США ~ 95 долл. США Эффективность при ликвидации
Недоказано Высокие показатели излечения в исследованиях (> 90%), ниже в клинической практике
Устойчивость к антибиотикам
,00Нет Значительное Варианты повторного лечения
Возможность продвижения к применению антибиотиков Повторить ту же терапию Текущая роль в терапии
Добавочный Первичная ликвидация Стандарт качества
Переменная Фармацевтическая В одно рандомизированное контролируемое исследование было включено 120 бессимптомных лиц, у которых обнаружено H.pylori – положительный результат во время обычного скрининга, выбравший эрадикационную терапию. 13 Их случайным образом распределили на одну неделю лечения: 1) рабепразолом (Ацифекс, 20 мг два раза в день), кларитромицином (250 мг три раза в день) и амоксициллином (500 мг три раза в день) или 2 ) по той же схеме с добавлением лиофилизированной и инактивированной культуры L. acidophilus . Доза лактобацилл составляла 5 × 10 9 инактивированных бактериальных клеток, вводимых три раза в день в течение 10 дней, включая семь дней тройной терапии плюс дополнительные три дня.Не упоминалось, давали ли лактобациллы с пищей или нет. Используя анализ намерения лечить всех пациентов, завершивших терапию, уровень эрадикации был значительно выше в группе, получавшей L. acidophilus , чем в контрольной группе (86,6% против 70%; P <0,05).
Во втором РКИ 20 субъектов с H. pylori лечили супернатантом L. acidophilus La1 на основе сыворотки (50 мл 4 раза в день) vs.омепразол (Прилосек, 20 мг 4 раза в день) плюс La1 в течение 14 дней. 14 Дыхательные тесты H. pylori показали заметное и значительное снижение значений H. pylori сразу после лечения в обеих группах в одинаковой степени. К сожалению, не было контрольной группы плацебо для лактобацилл. Исследование действительно показало снижение показателей дыхательного теста на 53-57% среди всех участников. Продолжительное подавление инфекции наблюдалось в группе, получавшей только La1 по сравнению с группой.группа комбинированной терапии через шесть недель после лечения.
Та же группа изучала использование подкисленного La1 молока (фактически, коммерчески доступного йогурта) по сравнению с плацебо среди 53 добровольцев, инфицированных H. pylori . 15 Молоко / йогурт давали по 180 мл два раза в день в течение трех недель. Все пациенты получали кларитромицин 500 мг два раза в день в течение последних двух недель терапии. Эзофагогастродуоденоскопия и биопсия были выполнены при включении и повторены через 4-8 недель после окончания лечения.Группа лактобацилл снизила плотность H. pylori на , антральное воспаление и активность антрального гастрита по сравнению с плацебо (P <0,05 в каждом случае), эффект, который сохранялся для заключительных последующих исследований. Однако лактобациллы не улучшали показатели эрадикации, полученные от антибиотика.
В 2001 году Сакамото и др. Исследовали использование Lactobacillus gasseri (LG21) в серии случаев из 31 субъекта, которые были положительными на H. pylori по результатам дыхательного теста на мочевину и серологических исследований. 16 В первой части 90 г йогурта, содержащего 1-1,4 × 10 7 колониеобразующих единиц / г LG21 потребляли дважды в день в течение восьми недель после восьми недель употребления йогурта без бактерий. Серийные дыхательные тесты с мочевиной показали значительно более низкие значения после приема йогурта LG21, но через три месяца эти уровни снова повысились у трех испытуемых. Показатели воспаления слизистой оболочки желудка были значительно ниже после восьми недель приема йогурта LG21 по сравнению с периодом после обычного йогурта.Исследование биопсий антрального отдела выявило уменьшение количества H. pylori в 2–100 раз, но ни в одном случае бактерии не были полностью уничтожены.
Наконец, Armuzzi и др. Использовали штамм Lactobacillus GG в исследовании с участием 120 пациентов для сравнения побочных эффектов от одной только тройной терапии (одна неделя пантопразола [Протоникс] 40 мг два раза в день, кларитромицин 500 мг два раза в день и тиндазол 500 мг. два раза в день) или по той же схеме с добавлением Lactobacillus GG в течение 14 дней. 17 Доза лактобацилл составляла 6 x 10 9 жизнеспособных бактерий, вводимых дважды в день, через два часа после завтрака или ужина в течение недели эрадикационной терапии и на следующей неделе. Пациенты заполняли утвержденные анкеты во время последующего наблюдения, чтобы определить тип и тяжесть побочных эффектов. Было обнаружено, что в группе лактобацилл было значительно меньше диареи (6,6% против 23,3%), вздутия живота (16,6% против 40%) и нарушений вкуса (6,6% против 26,6%), все со значениями P <0,05.
Токсичность / безопасность (побочные эффекты)
Пробиотики переносятся хорошо. Испытания более 2000 здоровых нормальных взрослых добровольцев не показали никаких вредных эффектов. 18 Исследование 1996 года, в котором было обнаружено, что лактобациллы объединяют тромбоциты, было опровергнуто. 19
Тем не менее, в некоторых сообщениях были выделены бактерии, используемые в пробиотиках, от человеческих инфекций, хотя есть мнение, что это были условно-патогенные инфекции. 20 Lactobacillus GG , в частности, не обладает инвазивными свойствами.Хотя в обзорной литературе не было обнаружено сообщений об аллергической реакции на пробиотики, многие из этих видов поставляются в препаратах, содержащих лактозу и молочные белки, которые обладают аллергическим потенциалом.
Существует несколько известных лекарственных взаимодействий при использовании пробиотиков. Однако было показано, что L. acidophilus влияет на метаболизм сульфасалазина и хлорамфеникола, разлагая эти препараты в желудке при одновременном приеме. 20
Подготовка
Помимо лиофилизированного порошка, существует множество источников пробиотиков, включая кисломолочные продукты, такие как йогурт, кефир и сыр, а также мисо и темпе. 21 Поскольку процесс пастеризации убивает эти организмы, их необходимо вводить после пастеризации.
Состав и дозировка
Исследования ДНК выявили большую генетическую изменчивость внутри штаммов L. acidophilus и других пробиотических видов. Рекомендуется использование определенных штаммов, соответствующих тем, которые используются в научных исследованиях. Кроме того, важен способ упаковки и хранения продукта, поскольку температура, влажность, свет и воздух могут отрицательно повлиять на жизнеспособность.Охлаждение продукта с момента производства до доставки и хранения имеет решающее значение для обеспечения активности штаммов, поскольку температура выше 60 ° F (15 ° C) убьет многие бактерии. 22 Продукты следует хранить в стеклянных бутылках янтарного цвета во избежание легкого повреждения, если производитель специально не разработал их для стабильной работы на полке в какой-либо другой упаковке.
Однако качество – это проблема. Одно исследование недавно сообщило, что из 30 протестированных сухих пробиотических добавок 11 не содержали жизнеспособных бактерий, семь содержали все заявленные виды, а 18 имели виды, отличные от тех, которые указаны на этикетке.Другая группа обнаружила, что 63% продуктов, протестированных в Соединенном Королевстве, не соответствовали стандартам. 23
Как правило, пробиотики следует принимать отдельно, натощак, через два-три часа после приема антибиотика, чтобы не убить пробиотические бактерии. Рекомендуется ограничить дозировку до менее 10 миллиардов жизнеспособных L. acidophilus в день, чтобы снизить любой риск возможных легких желудочно-кишечных расстройств. 8
Пациентам следует рекомендовать использовать те пробиотики, которые прошли клинические испытания.Продукты должны быть разработаны уважаемыми производителями, которые подвергают свою продукцию независимому контролю качества и гарантируют эффективность, чистоту и правильную маркировку. Пробиотики в форме инкапсулированных добавок должны быть тесно связаны с отдельными формами, изучаемыми в клинических испытаниях.
Вывод
H. pylori – один из самых распространенных патогенов в мире. В исследованиях in vitro и на животных было показано, что пробиотики, добавки или продукты, содержащие местную флору и используемые для лечения или профилактики заболеваний, ингибируют H.pylori и даже уничтожить организм. Исследования на людях начали подтверждать эти результаты, но все еще есть ограниченные доказательства контролируемых клинических испытаний и нет надежных данных, свидетельствующих о том, что пробиотическая терапия сама по себе была бы столь же эффективной, как стандартная терапия для искоренения инфекции H. pylori . Эти исследования действительно показывают, что пробиотики, особенно лактобациллы, могут уменьшать побочные эффекты и повышать эффективность традиционной эрадикационной терапии.
Рекомендация
Использование пробиотиков рекомендуется в качестве дополнения к проверенному в настоящее время стандартному лечению H.pylori инфекция. За исключением риска аллергической реакции, эти продукты имеют минимальные побочные эффекты и способны нейтрализовать некоторые побочные эффекты тройной терапии. Исследования по определению эффективности пробиотиков в искоренении инфекции H. pylori продолжаются.
Д-р Удани и д-р Спар – клинические инструкторы медицинского факультета Калифорнийского университета в Лос-Анджелесе; Д-р Удани также является медицинским директором программы интегративной медицины больницы Нортриджа, Нортридж, Калифорния.
Каталожные номера
1. Parsonnet J, et al. Риск рака желудка у людей с положительным CagA или отрицательным CagA Helicobacter pylori . Гут 1997; 40: 297-301.
2. Graham DY, et al. Эпидемиология Helicobacter pylori в бессимптомной популяции в США. Влияние возраста, расы и социально-экономического статуса. Гастроэнтерология 1991; 100: 1495-1501.
3.Marteau PR, et al. Защита от желудочно-кишечных заболеваний с помощью пробиотиков. Am J Clin Nutr 2001; 73 (2 доп.): 430S-436S.
4. Пещера, DR. Передача и эпидемиология Helico-bacter pylori . Am J Med 1996; 100 (Дополнение 5A): 17S-18S.
5. Сарди Б. Helicobacter pylori . Бактерии, вызывающие не только язвы. Новости науки о питании 2000; Май.
6. Рольфе Р.Д. Роль пробиотических культур в контроле здоровья желудочно-кишечного тракта. J Nutr 2000; 130 (2S доп.): 396С-402С.
7. Takahashi M, et al. Исследования влияния Clostridium butyricum на Helicobacter pylori на нескольких тестовых моделях, включая гнотобиотических мышей. J Med Microbiol 2000; 49: 635-642.
8. Анонимный. Lactobacillus acidophilus 96 описание. Компакт-диск HealthPlus. Группа JAG; 1998.
9. Bhatia SJ, et al. Lactobacillus acidophilus подавляет рост Campylobacter pylori in vitro. J Clin Microbiol 1989; 32: 2328-30.
10. Пинчук И.В. и др. Активность пробиотического штамма Bacillus subtilis 3 in vitro против Helicobacter pylori обусловлена секрецией антибиотиков. Противомикробные агенты Chemother 2001; 45: 3156-3161.
11. Бенгмарк С. Экологический контроль желудочно-кишечного тракта. Роль пробиотической флоры. Кишечник 1998; 42: 2-7.
12. Rasic J, et al. Противомикробный эффект Lactobacillus acidophilus и Lactobacillus delbruekii subsp.Булгарикус против Helicobacter pylori in vitro. Arch Gastroenterohepatol 1995; 14: 158-160.
13. Canducci F, et al. Лиофилизированная культура Lactobacillus acidophilus увеличивает скорость эрадикации Helicobacter pylori . Алимент Фармакол Тер 2000; 14: 1625-1629.
14. Michetti P, et al. Влияние супернатанта культуры на основе сыворотки Lactobacillus acidophilus (johnsonii) La1 на инфекцию Helicobacter pylori у людей. Пищеварение 1999; 60: 203-209.
15. Felley C, et al. Благоприятное влияние подкисленного молока (LC-1) на гастрит Helicobacter pylori у человека. Eur J Gastroenterol Hepatol 2001; 13: 25-29.
16. Сакамото I, et al. Подавляющее действие Lactobacillus gasseri OLL 2716 (LG21) на инфекцию Helicobacter pylori у людей. J Antimicrob Chemother 2001; 47: 709-710.
17. Armuzzi A, et al. Влияние добавок Lactobacillus GG на побочные эффекты со стороны желудочно-кишечного тракта, связанные с антибиотиками, во время эрадикационной терапии Helicobacter pylori : пилотное исследование. Пищеварение 2001; 63: 1-7.
18. Салимен С., Донохью Д. Оценка безопасности штамма Lactobacillus GG. Nutr Сегодня 1996; 31: 12С-15С.
19. Moilanen E, et al. Влияние Lactobacillus GG на агрегацию тромбоцитов. Nutr Сегодня 1996; 31: 43С-44С.
20. Ишибаши Н., Ямазаки С.

 Hotel & Marina, Januar 18–21, р. 43.
Hotel & Marina, Januar 18–21, р. 43. , 20–21.
, 20–21. , p. 230–241.
, p. 230–241.