Болезни толстого кишечника: Диагностика и лечение болезней толстой кишки
Заболевания кишечника – Гастроэнтерология – Отделения
1. Синдром раздраженного кишечника (СРК) определяется как функциональное заболевание кишечника, при котором боль в животе или дискомфорт связаны с дефекацией или изменением консистенции стула и характерным нарушением дефекации. Характеристика синдрома предполагает особые подходы к постановке диагноза, проведению дифференциального диагноза и осуществлению программы лечения больных.
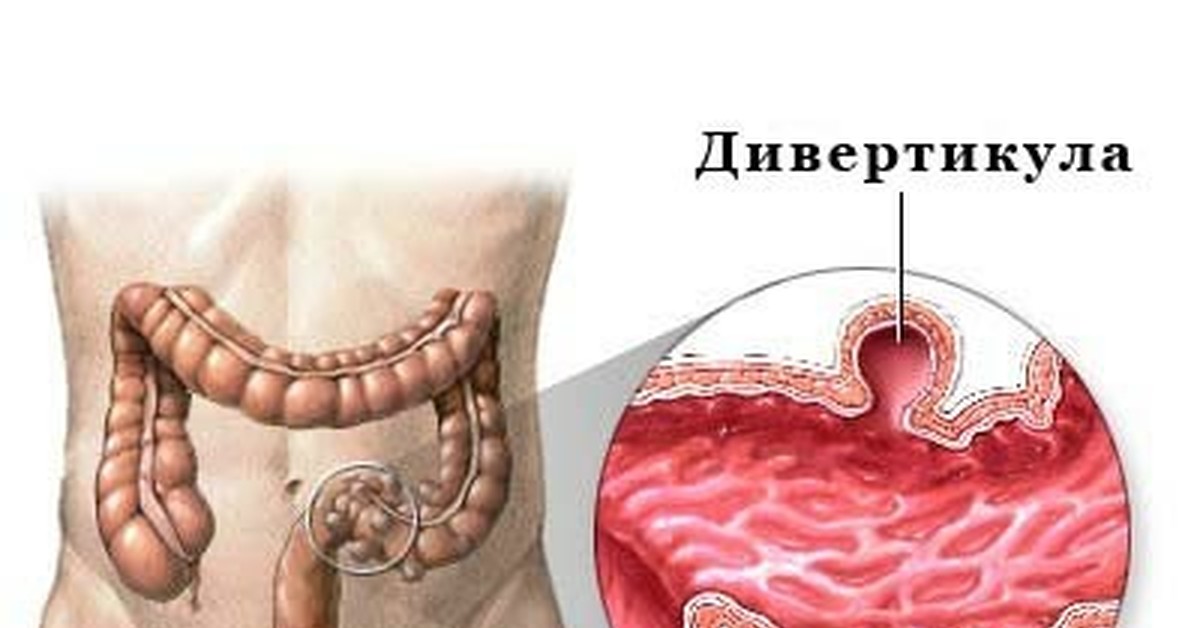
2. Дивертикулярная болезнь толстого кишечника – Дивертикулярная болезнь (дивертикулез) толстой кишки представляет собой морфо-функциональный патологический процесс, характерным отличительным признаком которого является наличие мешковидных выпячиваний стенки ободочной кишки (дивертикулов). Дивертикулы являются проявлением различных патологических состояний, среди которых ведущее значение имеют дистрофические изменения в мышечной стенке ободочной кишки, дискоординация ее моторики, врожденная или приобретенная слабость соединительной ткани, сосудистые изменения в стенке кишки.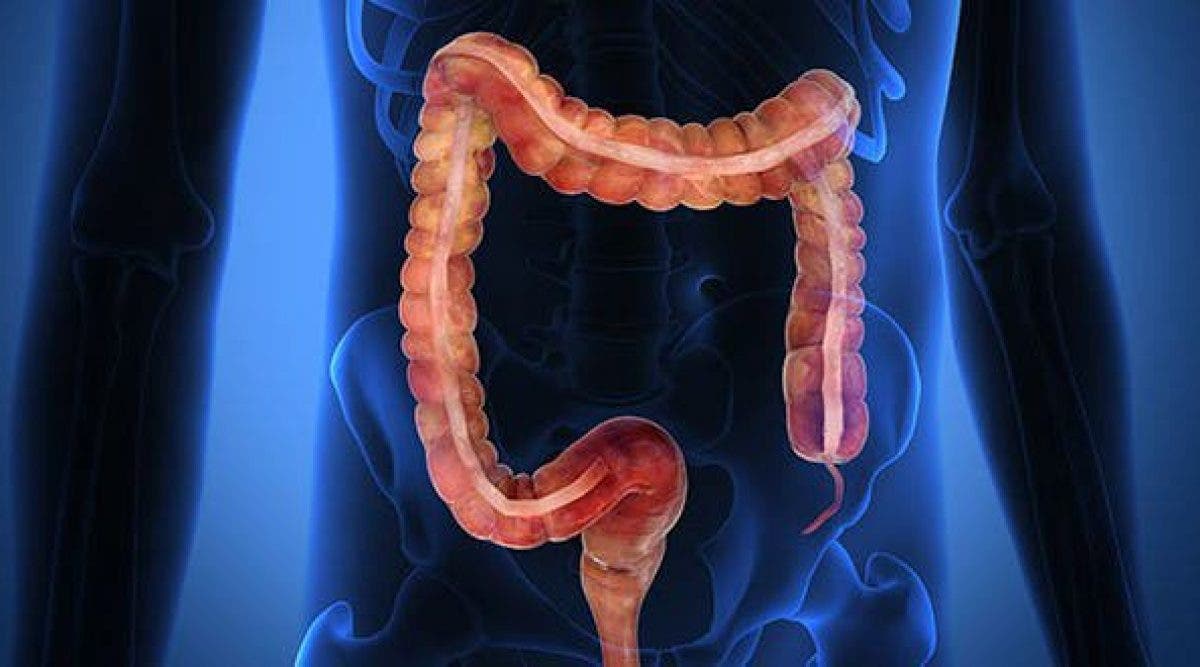
3. Дисбактериоз кишечника. Дисбактериозом кишечника считается клинико-лабораторный синдром, связанный с изменением состава микрофлоры кишечника, как качественного, так и количественного, с возможным развитием желудочно-кишечных расстройств. Основными причинами развития дисбактериоза являются длительное и бесконтрольное применение антибиотиков, химиопрепараты, гормонотерапия, радиотерапия, воздействие радиации, нерациональное питание, острые или хронические кишечные инфекции
, паразитарные заболевания кишечника (аскаридоз), состояния, сопровождающие снижением иммунитета (онкологические заболевания, сахарный диабет, цирроз печени, СПИД, и другие),старческий возраст.
4. Язвенный колит – хроническое рецидивирующее воспалительное заболевание преимущественно слизистой оболочки толстого кишечника с той или иной распространенностью процесса. Этиология (причина) заболевания до сих пор остаются неизвестными. Предполагается аутоиммунное поражение тканей стенок толстого кишечника. Данное предположение основано на том, что в большинстве случаев язвенный неспецифический колит ассоциируется с другими аутоиммунными заболеваниями (системные васкулиты, системные поражения соединительной ткани, аутоиммунный тиреоидит и пр.).
5. Болезнь Крона (БК) – хроническое рецидивирующее заболевание желудочно-кишечного тракта неизвестной этиологии, характеризующееся трансмуральным, сегментарным, гранулематозным воспалением с развитием местных и системных осложнений. В отличие от язвенного колита, при болезни Крона все слои стенки кишки вовлекаются в воспалительный процесс. Воспаление в большинстве случаев сначала возникает в подвздошной кишке, а затем переходит на другие отделы кишечника
Дивертикулярная болезнь толстого кишечника | Тамбовская областная клиническая больница имени В.
 Д. Бабенко
Д. БабенкоДивертикул – это грыжевидное выпячивание стенки полого органа.
Дивертикулёз – это наличие множественных дивертикулов полого органа.
Дивертикулярная болезнь – заболевание, обусловленное наличием дивертикула или дивертикулеза, включая воспаление (дивертикулит) и его осложнения (перидивертикулит, абсцесс, перфорация, свищ, кровотечение, перитонит).
Дивертикулярная болезнь поражает преимущественно сигмовидную кишку, и нисходящую ободочную кишку, реже правую половину поперечной ободочной кишки и правые отделы ободочной кишки.
Частота дивертикулёза увеличивается с возрастом. До 40 лет это заболевание выявляется у 5% населения, в возрасте 40-50 лет – 5-10%, в возрасте 50-60 лет – 14%, у лиц старше 60 лет – 30%, старше 80 лет – 60-65%. Среди мужчин и женщин распространённость заболевания приблизительно одинаковая.
Наиболее значимый фактор развития дивертикулярной болезни – диета, бедная растительной клетчаткой.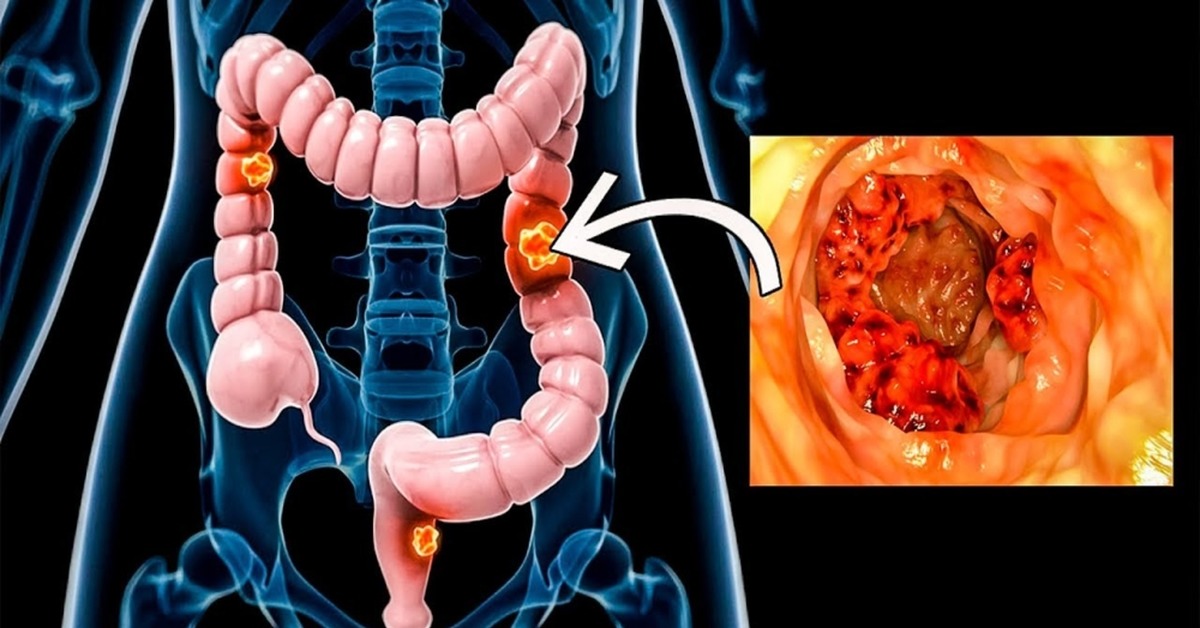 Клетчатка входит в состав овощей, фруктов и злаков, способствует размягчению стула и более легкому транзиту химуса по кишечнику. При недостатке клетчатки в пищевом рационе развивается склонность к запорам. Частые запоры способствуют повышению давления в кишечнике. В местах, где имеется ослабление кишечной стенки в результате повышения внутрикишечного давления, возникают выпячивания. Со временем, формируются постоянные выпячивания кишечной стенки, которые могут стать очагом размножения бактериальной флоры.
Клетчатка входит в состав овощей, фруктов и злаков, способствует размягчению стула и более легкому транзиту химуса по кишечнику. При недостатке клетчатки в пищевом рационе развивается склонность к запорам. Частые запоры способствуют повышению давления в кишечнике. В местах, где имеется ослабление кишечной стенки в результате повышения внутрикишечного давления, возникают выпячивания. Со временем, формируются постоянные выпячивания кишечной стенки, которые могут стать очагом размножения бактериальной флоры.
Классификация:
Дивертикулярную болезнь толстого кишечника классифицируют по клиническому течению и подразделяют на бессимптомный дивертикулез, дивертикулез, протекающий с клиническими проявлениями и дивертикулез с осложнениями.
Дивертикулярная болезнь длительное время может протекать бессимптомно и ничем не проявляться. При прогрессировании заболевания пациенты предъявляют жалобы на периодические боли разной интенсивности в левых и нижних отделах живота, нарушение стула (запоры или поносы), наличие примесей в стуле (кровь, гной, слизь), повышение температуры тела (при воспалении дивертикулов).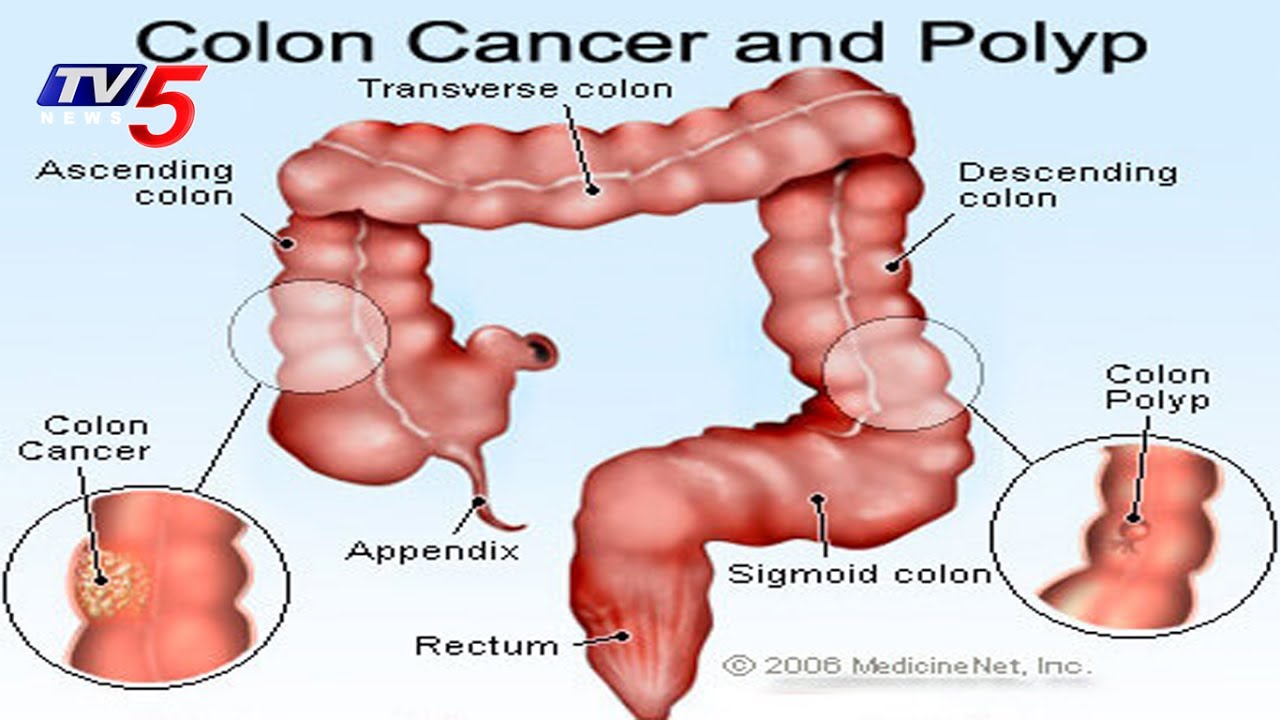
С целью диагностической верификации патологического процесса в толстом кишечнике применяются следующие исследования:
– Колоноскопия –
эндоскопический метод, при котором проводится осмотр кишки со стороны слизистой. В ходе исследования выявляются участки толстого кишечника с наличием дивертикулов, определяется их размер, степень воспаления. По показаниям выполняются лечебные мероприятия, такие как остановка кровотечения.– Ирригоскопия – рентгенологический метод, позволяющий оценить протяженность поражения ободочной кишки.
– УЗИ брюшной полости – неинвазивный метод, позволяющий оценить распространенность поражения кишки, а также выявить наличие возможных осложнений.
– Компьютерная томография – неинвазивный метод, позволяющий предельно точно оценить распространенность поражения кишки, а также выявить наличие возможных осложнений.
Развитие дивертикулита требует противовоспалительной и бактериальной терапии.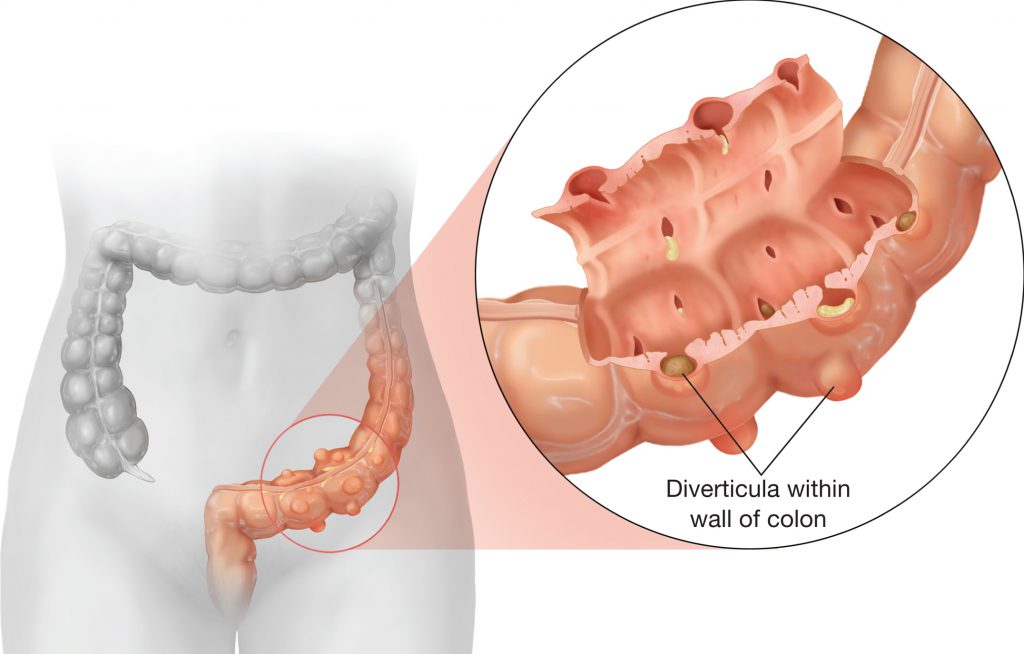 Для успешного лечения дивертикулита необходимо снятие нагрузки на толстый кишечник, чему способствуют меры по изменению рациона питания. Своевременно назначенный курс антибактериальной терапии подавляет развивающуюся инфекцию. В некоторых случаях консервативное лечение может быть безуспешным, либо развитие осложнений требует немедленного хирургического вмешательства.
Для успешного лечения дивертикулита необходимо снятие нагрузки на толстый кишечник, чему способствуют меры по изменению рациона питания. Своевременно назначенный курс антибактериальной терапии подавляет развивающуюся инфекцию. В некоторых случаях консервативное лечение может быть безуспешным, либо развитие осложнений требует немедленного хирургического вмешательства.
Абсолютными показаниями к оперативному лечению являются: перфорация толстой кишки с выходом кишечного содержимого в брюшную полость; перитонит; прогрессирующий абсцесс; полная кишечная непроходимость; массивное кровотечение; высокая вероятность роста злокачественного новообразования кишечника. Кроме того, показанием к оперативному вмешательству является: неэффективность консервативного лечения; периодические небольшие внутренние кровотечения; выраженная анемия; свищи; частые рецидивы дивертикулита.
Профилактика и прогноз
Чаще всего дивертикулярная болезнь толстого кишечника не доставляет серьезных проблем пациентам, придерживающимся диеты.
В Тамбовской областной клинической больнице на базе гастроэнтерологического и второго хирургического отделений ежегодно получают лечение 40-50 пациентов по поводу дивертикулярной болезни. Оперативные вмешательства представлены разными вариантами резекций участков толстого кишечника: резекция сигмовидной кишки, левосторонняя гемиколэктомия. Данные виды операций позволяют избавиться от дивертикулярной болезни и развития ее осложнений.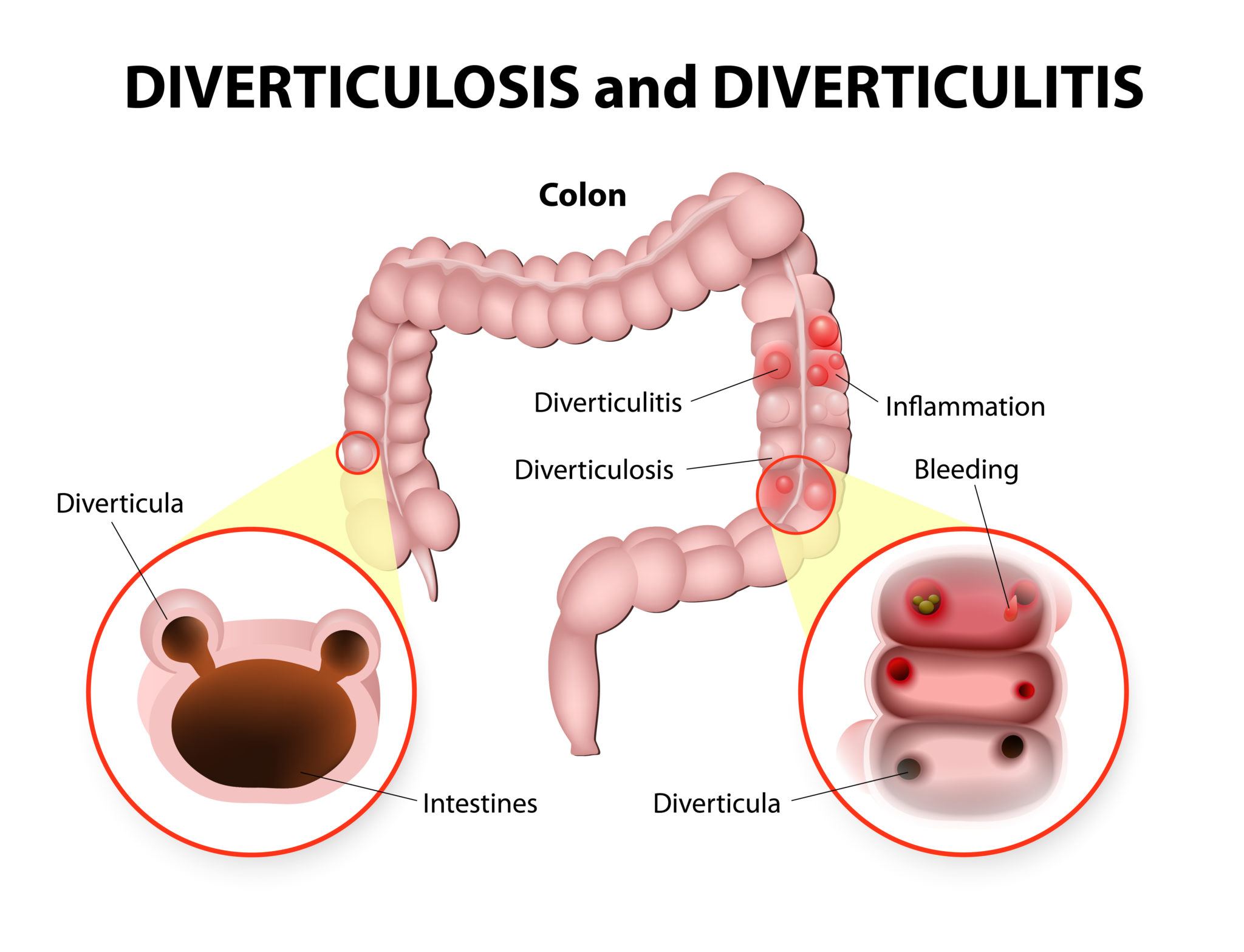
09 Марта 2021 года
Заболевания толстого кишечника | Санаторий имени 30-летия Победы
Функция толстого кишечника состоит в выведении остатков пищи из организма. Поэтому заболевание толстой кишки может повлечь за собой нарушение всего процесса пищеварения.
Воспалительные заболевания толстого кишечника
К ним относятся воспаления всего кишечного тракта или отдельных его частей. Проявлениями воспалительного процесса могут стать такие болезни как язвенный колит и болезнь Крона. Они могут протекать достаточно болезненно и привести к опасным для жизни осложнениям.
Заболевания опухолевого характера
К ним относятся такие болезни как диффузный полипоз, рак, злокачественные лимфомы, гемангиомы. Они, как правило, протекают гораздо мучительней для больного. В данном случае происходят нарушения в работе обмена веществ, функциях половых органов, замедление роста, истощение и слабость.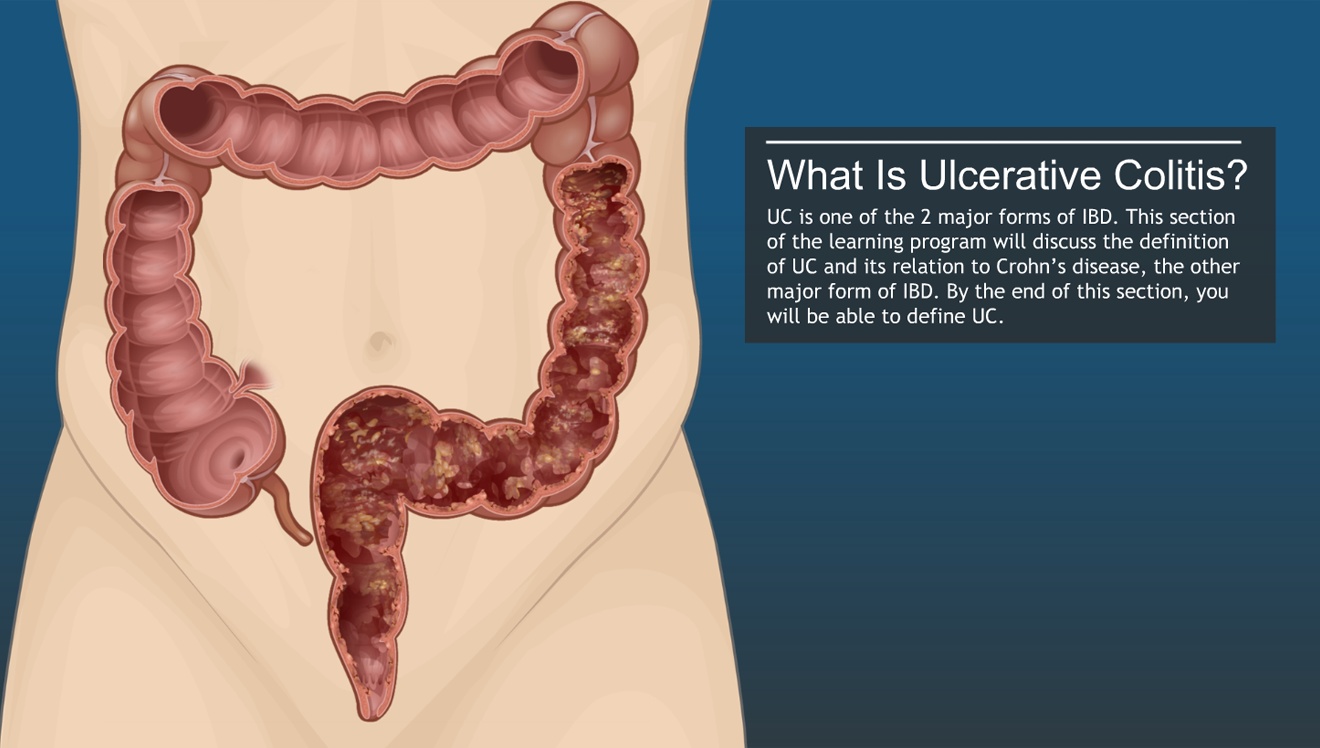
Симптомы воспалительных заболеваний толстого кишечника
- кровотечения из прямой кишки через задний проход;
- тянущая боль и спазмы в животе;
- диарея с кровью;
- боли в левой части живота;
- беспричинное уменьшение массы и веса тела;
- усталость;
- обезвоживание.
Для опухолевых заболеваний толстого кишечника характерны такие симптомы как:
- анемия;
- изменения формы или размера кала;
- запоры, поносы, вздутия живота;
- смесь крови со слизью в кале;
- заметный глазу рельеф округлой формы.
Причины заболеваний толстого кишечника
К причинам данного заболевания можно отнести достаточно большое количество недугов. Среди них выделяют:
- вирусы;
- наследственные заболевания;
- глисты;
- неправильное питание;
- радиация;
- аллергия;
- нарушение состояний слизистой оболочки;
- стрессовые состояния;
- избыток белка или углевода в организме человека;
- гибель полезных бактерий, которые участвуют в обмене веществ.

Методы лечения
Методы лечения заболеваний толстой кишки достаточно разнообразны. К лечению следует приступать на начальных стадиях, когда болезнь еще не вступила в полную силу. На запущенных стадиях в лечении помогут только хирургические вмешательства или медицинские препараты. Если обнаружились какие-нибудь симптомы из вышеперечисленных, то рекомендуется предпринять следующие меры для предотвращения дальнейшего развития болезни.
Прежде всего, необходимо пересмотреть весь рацион питания. Диета при заболевании толстого кишечника должна быть максимально сбалансированной. Ни в коем случае нельзя употреблять жирное и сладкое. Это приведет слизистую всей пищеварительной системы в возбужденное состояние.
В повседневное меню рекомендуется внести больше вареных блюд и приготовленных на пару. Пить следует компоты из клюквы и брусники. Именно эти ягоды способствуют активной работе полезных бактерий. С десертами лучше воздержаться.
Рекомендуется принимать витамины. Возможно, именно их нехватка отразилась на заболеваниях толстого кишечника. Не следует принимать препараты без рецепта врача, некоторые из них могут усугубить ситуацию.
Возможно, именно их нехватка отразилась на заболеваниях толстого кишечника. Не следует принимать препараты без рецепта врача, некоторые из них могут усугубить ситуацию.
При беспокоящих недомоганиях настоятельно рекомендуется обратиться к специалисту. Не стоит запускать болезнь до необратимого состояния.
В рамках общетерапевтической программы в санатории 30 лет Победы проводится лечение заболеваний толстого кишечника.
Профилактика рака прямой кишки — Профилактика заболеваний и ЗОЖ — Бюджетное учреждение Ханты-Мансийского автономного округа – Югры
Рак прямой кишки – злокачественная образование конечного отдела толстой кишки, занимает первое место среди онкологических заболеваний толстого кишечника, около 70% случаев. Рак прямой кишки, чаще возникает у мужчин и риск его развития повышается с возрастом. И связано это с возрастными изменениями в эпителиальных клетках кишечника. Большинство случаев рака прямой кишки диагностируется на поздних стадиях, хотя сама прямая кишка доступна к множеству исследований, самым доступным из которых является пальцевой ректальный осмотр. Связано это с тем, что пациенты стесняются обращаться к врачу с этой интимной проблемой.
Связано это с тем, что пациенты стесняются обращаться к врачу с этой интимной проблемой.
Причины рака прямой кишки
Отмечается прямая зависимость развития рака прямой кишки от особенностей пищевого поведения. Болезнь чаще встречается у людей, употребляющих жирную, жаренную и острую пищу, со скудным содержанием растительной клетчаткой. Кроме этого большое количество мясных блюд в рационе питания способствует возникновению злокачественных образований в толстой кишке.
Важными факторами, повышающими риск развития рака толстого кишечника, являются хронические воспалительные заболевания: болезнь Крона, неспецифический язвенный колит, врожденные патологии (семейный полипоз, ферментные недостаточности). Полипы толстого кишечника являются самым распространенным предраковых заболеванием, а семейный полипоз, самым малигнизирующимся. Наследственный фактор также играет не последнюю роль в заболеваемости раком прямой кишки.
Симптомы рака прямой кишки
На ранних стадиях рак прямой кишки протекает бессимптомно, что значительно затрудняет диагностирование и своевременное выявление опухоли.
Самые распространенные симптомы рака прямой кишки: нарушение дефекации (запоры или поносы), кровотечение из заднего прохода, примесь крови в кале, снижение массы тела, ноющие боли в низу живота, «ленточный» стул.
Диагностика рака прямой кишки
На сегодняшний день существуют онкомаркеры на рак толстого кишечника, самым доступным из которых является иммунохимическое исследование кала на скрытую кровь. Важно понимать, что положительный тест на скрытую кровь автоматически не означает наличие рака кишечника у исследуемого пациента, а только предполагает наличие злокачественного или предракового заболевания и возможно о воспалительных заболеваниях толстого кишечника. Основным методом диагностики рака толстого кишечника являются инструментальные методы исследования, такие как: ректороманоскопия (обследуется внутренняя стенка прямой и сигмовидной кишки), колоноскопия (эндоскопическое исследование всей толстой кишки), ирригоскопия (рентгенографическое исследование толстой кишки с контрастным веществом).
Эндоскопические методики позволяют подробно изучить состояние слизистой оболочки кишечной стенки, имеющиеся опухолевые образования, произвести биопсию для последующего гистологического и цитологического исследования. Диагностика рака прямой кишки производится только на сновании обнаружения раковых клеток при цитологическом исследовании биоптата.
Профилактика рака прямой кишки
Профилактические меры злокачественных новообразований толстой кишки включают регулярное обследование лиц, входящих в группу риска (люди старше 50 лет, больные с хроническими заболеваниями толстой кишки). Особое внимание уделяется пациентам с полипами толстой кишки.
В скрининговые мероприятия входят: ежегодный анализ кала на скрытую кровь, сигмоидоскопия каждые 5 лет, каждые 10 лет – колоноскопия.
Лица, страдающие семейным полипозом, подлежат обследованию каждые 2-3 года. Общие меры профилактики рака прямой кишки включают активный образ жизни, правильное сбалансированное питание, богатое растительной клетчаткой без перегруженности животными жирами, отказ от курения и злоупотребления алкогольными напитками, своевременное выявление и лечение заболеваний, провоцирующих развитие злокачественных опухолей.
Вторичная профилактика рака прямой кишки заключается в предотвращении болезни путем раннего обнаружения патологии, в результате чего увеличиваются шансы на успешное излечение. Диспансерное наблюдение с регулярными осмотрами рекомендовано лицам, которые находятся в группе риска. К ним относятся пациенты с полипами и полипозом, проктитами, язвами, трещинами, свищами и др. Конечно, при появлении первых симптомов следует незамедлительно отправляться к врачу. Во время регулярного профилактического осмотра можно обнаружить опухоль, когда о ее появлении пациент даже не догадывается.
При пальцевом ректальном исследовании диагностируется около 40% случаев болезни. После проведения ректороманоскопии подтверждается до 95% всех диагнозов. Следует помнить, что при вовремя начатом лечении прогноз весьма благоприятный. Благодаря раннему выявлению болезни лечение удается начать на ранней стадии болезни. В таком случае существует возможность проведения сфинктеросохраняющей операции, при которой в дальнейшем акт дефекации по-прежнему будет физиологичным.
Подготовил:
заведующий ОПСМСП – 5 Чернобай Владимир Григорьевич
Микробиом, дисбиоз толстой кишки и воспалительные заболевания кишечника: когда функция важнее таксономии | Ситкин
1. Putignani L, Del Chierico F, Vernocchi P, Cicala M, Cucchiara S, Dallapiccola B; Dysbiotrack Study Group. Gut microbiota dysbiosis as risk and premorbid factors of IBD and IBS along the childhood-adulthood transition. Inflamm Bowel Dis. 2016;22(2):487–504. doi: 10.1097/MIB.0000000000000602.
2. Gilbert JA, Blaser MJ, Caporaso JG, Jansson JK, Lynch SV, Knight R. Current understanding of the human microbiome. Nat Med. 2018;24(4): 392–400. doi: 10.1038/nm.4517.
3. Вахитов ТЯ, Ситкин СИ. Концепция суперорганизма в биологии и медицине. Экспериментальная и клиническая гастроэнтерология. 2014;(7):72–85.
Экспериментальная и клиническая гастроэнтерология. 2014;(7):72–85.
4. Bäckhed F, Ley RE, Sonnenburg JL, Peterson DA, Gordon JI. Host-bacterial mutualism in the human intestine. Science. 2005;307(5717): 1915–20. doi: 10.1126/science.1104816.
5. Clarke G, Grenham S, Scully P, Fitzgerald P, Moloney RD, Shanahan F, Dinan TG, Cryan JF. The microbiome-gut-brain axis during early life regulates the hippocampal serotonergic system in a sex-dependent manner. Mol Psychiatry. 2013;18(6):666–73. doi: 10.1038/mp.2012.77.
6. Carbonero F. Human epigenetics and microbiome: the potential for a revolution in both research areas by integrative studies. Future Sci OA. 2017;3(3):FSO207. doi: 10.4155/fsoa-2017-0046.
7. Nagao-Kitamoto H, Kitamoto S, Kuffa P, Kamada N. Pathogenic role of the gut microbiota in gastrointestinal diseases. Intest Res. 2016;14(2): 127–38. doi: 10.5217/ir.2016.14.2.127.
Nagao-Kitamoto H, Kitamoto S, Kuffa P, Kamada N. Pathogenic role of the gut microbiota in gastrointestinal diseases. Intest Res. 2016;14(2): 127–38. doi: 10.5217/ir.2016.14.2.127.
8. Ситкин СИ, Вахитов ТЯ, Ткаченко ЕИ, Орешко ЛС, Жигалова ТН, Радченко ВГ, Селиверстов ПВ, Авалуева ЕБ, Суворова МА, Комличенко ЭВ. Микробиота кишечника при язвенном колите и целиакии. Экспериментальная и клиническая гастроэнтерология. 2017;(1):8–30.
9. Lopetuso LR, Petito V, Graziani C, Schiavoni E, Paroni Sterbini F, Poscia A, Gaetani E, Franceschi F, Cammarota G, Sanguinetti M, Masucci L, Scaldaferri F, Gasbarrini A. Gut microbiota in health, diverticular disease, irritable bowel syndrome, and inflammatory bowel diseases: time for microbial marker of gastrointestinal disorders. Dig Dis. 2018;36(1):56–65. doi: 10.1159/000477205.
10. Селиверстов ПВ, Ситкин СИ, Радченко ВГ, Лазебник ЛБ, Авалуева ЕБ, Вахитов ТЯ, Демьянова ЕВ, Скворцова ТЭ, Приходько ЕМ, Суворова МА. Saccharomyces boulardii модулируют состав микробиоты кишечника у пациентов с неалкогольной жировой болезнью печени, препятствуя прогрессированию заболевания. Экспериментальная и клиническая гастроэнтерология. 2018;(2):4–18.
Селиверстов ПВ, Ситкин СИ, Радченко ВГ, Лазебник ЛБ, Авалуева ЕБ, Вахитов ТЯ, Демьянова ЕВ, Скворцова ТЭ, Приходько ЕМ, Суворова МА. Saccharomyces boulardii модулируют состав микробиоты кишечника у пациентов с неалкогольной жировой болезнью печени, препятствуя прогрессированию заболевания. Экспериментальная и клиническая гастроэнтерология. 2018;(2):4–18.
11. Opazo MC, Ortega-Rocha EM, Coronado-Arrázola I, Bonifaz LC, Boudin H, Neunlist M, Bueno SM, Kalergis AM, Riedel CA. Intestinal microbiota influences non-intestinal related autoimmune diseases. Front Microbiol. 2018;9:432. doi: 10.3389/fmicb.2018.00432.
12. Neurath MF. Cytokines in inflammatory bowel disease. Nat Rev Immunol. 2014;14(5):329–42. doi: 10.1038/nri3661.
13. Miner-Williams WM, Moughan PJ. Intestinal barrier dysfunction: implications for chronic inflammatory conditions of the bowel. Nutr Res Rev. 2016;29(1):40–59. doi: 10.1017/S0954422416000019.
Intestinal barrier dysfunction: implications for chronic inflammatory conditions of the bowel. Nutr Res Rev. 2016;29(1):40–59. doi: 10.1017/S0954422416000019.
14. Chen SJ, Liu XW, Liu JP, Yang XY, Lu FG. Ulcerative colitis as a polymicrobial infection characterized by sustained broken mucus barrier. World J Gastroenterol. 2014;20(28):9468–75. doi: 10.3748/wjg.v20.i28.9468.
15. Sartor RB, Wu GD. Roles for intestinal bacteria, viruses, and fungi in pathogenesis of inflammatory bowel diseases and therapeutic approaches. Gastroenterology. 2017;152(2): 327–39.e4. doi: 10.1053/j.gastro.2016.10.012.
16. Waldschmitt N, Metwaly A, Fischer S, Haller D. Microbial Signatures as a Predictive Tool in IBD-Pearls and Pitfalls. Inflamm Bowel Dis. 2018;24(6):1123–32. doi: 10. 1093/ibd/izy059.
1093/ibd/izy059.
17. Ситкин СИ, Вахитов ТЯ, Ткаченко ЕИ, Орешко ЛС, Жигалова ТН, Радченко ВГ, Селиверстов ПВ, Авалуева ЕБ, Суворова МА, Утсаль ВА. Дисбиоз кишечника при язвенном колите и целиакии и его терапевтическая коррекция с помощью масляной кислоты в комбинации с инулином. Экспериментальная и клиническая гастроэнтерология. 2017;(6):77–98.
18. Meisel M, Mayassi T, Fehlner-Peach H, Koval JC, O’Brien SL, Hinterleitner R, Lesko K, Kim S, Bouziat R, Chen L, Weber CR, Mazmanian SK, Jabri B, Antonopoulos DA. Interleukin-15 promotes intestinal dysbiosis with butyrate deficiency associated with increased susceptibility to colitis. ISME J. 2017;11(1):15–30. doi: 10.1038/ismej.2016.114.
19. Hodzic Z, Schill EM, Bolock AM, Good M. IL-33 and the intestine: the good, the bad, and the inflammatory. Cytokine. 2017;100:1–10. doi: 10.1016/j.cyto.2017.06.017.
Cytokine. 2017;100:1–10. doi: 10.1016/j.cyto.2017.06.017.
20. Griesenauer B, Paczesny S. The ST2/IL-33 axis in immune cells during inflammatory diseases. Front Immunol. 2017;8:475. doi: 10.3389/fimmu.2017.00475.
21. Ni J, Wu GD, Albenberg L, Tomov VT. Gut microbiota and IBD: causation or correlation? Nat Rev Gastroenterol Hepatol. 2017;14(10): 573–84. doi: 10.1038/nrgastro.2017.88.
22. Lee YK, Mazmanian SK. Has the microbiota played a critical role in the evolution of the adaptive immune system? Science. 2010;330(6012):1768–73. doi: 10.1126/science.1195568.
23. de Zoete MR, Flavell RA. Interactions between nod-like receptors and intestinal bacteria. Front Immunol. 2013;4:462. doi: 10.3389/fimmu.2013.00462.
doi: 10.3389/fimmu.2013.00462.
24. Lamas B, Richard ML, Leducq V, Pham HP, Michel ML, Da Costa G, Bridon-neau C, Jegou S, Hoffmann TW, Natividad JM, Brot L, Taleb S, Couturier-Maillard A, Nion-Larmurier I, Merabtene F, Seksik P, Bourrier A, Cosnes J, Ryffel B, Beaugerie L, Launay JM, Langella P, Xavier RJ, Sokol H. CARD9 impacts colitis by altering gut microbiota metabolism of tryptophan into aryl hydrocarbon receptor ligands. Nat Med. 2016;22(6):598–605. doi: 10.1038/nm.4102.
25. Holzapfel WH, Haberer P, Snel J, Schillinger U, Huis in’t Veld JH. Overview of gut flora and probiotics. Int J Food Microbiol. 1998;41(2): 85–101. doi: 10.1016/S0168-1605(98)00044-0.
26. Levy M, Kolodziejczyk AA, Thaiss CA, Elinav E. Dysbiosis and the immune system. Nat Rev Immunol. 2017;17(4):219–32. doi: 10.1038/nri.2017.7.
2017;17(4):219–32. doi: 10.1038/nri.2017.7.
27. Petersen C, Round JL. Defining dysbiosis and its influence on host immunity and disease. Cell Microbiol. 2014;16(7):1024–33. doi: 10.1111/cmi.12308.
28. Vangay P, Ward T, Gerber JS, Knights D. Antibiotics, pediatric dysbiosis, and disease. Cell Host Microbe. 2015;17(5):553–64. doi: 10.1016/j.chom.2015.04.006.
29. Ситкин СИ, Ткаченко ЕИ, Вахитов ТЯ. Метаболический дисбиоз кишечника и его биомаркеры. Экспериментальная и клиническая гастроэнтерология. 2015;(12):6–29.
30. Frank DN, St Amand AL, Feldman RA, Boedeker EC, Harpaz N, Pace NR. Molecular-phylogenetic characterization of microbial community imbalances in human inflammatory bowel diseases. Proc Natl Acad Sci U S A. 2007;104(34): 13780–5. doi: 10.1073/pnas.0706625104.
Proc Natl Acad Sci U S A. 2007;104(34): 13780–5. doi: 10.1073/pnas.0706625104.
31. Sartor RB. Gut microbiota: Diet promotes dysbiosis and colitis in susceptible hosts. Nat Rev Gastroenterol Hepatol. 2012;9(10):561–2. doi: 10.1038/nrgastro.2012.157.
32. Lozupone CA, Stombaugh J, Gonzalez A, Ackermann G, Wendel D, Vázquez-Baeza Y, Jansson JK, Gordon JI, Knight R. Meta-analyses of studies of the human microbiota. Genome Res. 2013;23(10):1704–14. doi: 10.1101/gr.151803.112.
33. Kriss M, Hazleton KZ, Nusbacher NM, Martin CG, Lozupone CA. Low diversity gut microbiota dysbiosis: drivers, functional implications and recovery. Curr Opin Microbiol. 2018;44:34– 40. doi: 10.1016/j.mib.2018.07.003.
34. Walujkar SA, Dhotre DP, Marathe NP, Lawate PS, Bharadwaj RS, Shouche YS. Characterization of bacterial community shift in human Ulcerative Colitis patients revealed by Illumina based 16S rRNA gene amplicon sequencing. Gut Pathog. 2014;6:22. doi: 10.1186/1757-4749-6-22.
Walujkar SA, Dhotre DP, Marathe NP, Lawate PS, Bharadwaj RS, Shouche YS. Characterization of bacterial community shift in human Ulcerative Colitis patients revealed by Illumina based 16S rRNA gene amplicon sequencing. Gut Pathog. 2014;6:22. doi: 10.1186/1757-4749-6-22.
35. Fite A, Macfarlane S, Furrie E, Bahrami B, Cummings JH, Steinke DT, Macfarlane GT. Longitudinal analyses of gut mucosal microbiotas in ulcerative colitis in relation to patient age and disease severity and duration. J Clin Microbiol. 2013;51(3):849–56. doi: 10.1128/JCM.02574-12.
36. Li KY, Wang JL, Wei JP, Gao SY, Zhang YY, Wang LT, Liu G. Fecal microbiota in pouchitis and ulcerative colitis. World J Gastroenterol. 2016;22(40):8929–39. doi: 10.3748/wjg.v22.i40.8929.
37. Halfvarson J, Brislawn CJ, Lamendella R, Vázquez-Baeza Y, Walters WA, Bramer LM, D’Amato M, Bonfiglio F, McDonald D, Gonzalez A, McClure EE, Dunklebarger MF, Knight R, Jansson JK. Dynamics of the human gut microbiome in inflammatory bowel disease. Nat Microbiol. 2017;2:17004. doi: 10.1038/nmicrobiol.2017.4.
Dynamics of the human gut microbiome in inflammatory bowel disease. Nat Microbiol. 2017;2:17004. doi: 10.1038/nmicrobiol.2017.4.
38. Yang Y, Jobin C. Novel insights into microbiome in colitis and colorectal cancer. Curr Opin Gastroenterol. 2017;33(6):422–7. doi: 10.1097/MOG.0000000000000399.
39. Gonçalves P, Araújo JR, Di Santo JP. A cross-talk between microbiota-derived short-chain fatty acids and the host mucosal immune system regulates intestinal homeostasis and inflammatory bowel disease. Inflamm Bowel Dis. 2018;24(3):558–72. doi: 10.1093/ibd/izx029.
40. Morgan XC, Tickle TL, Sokol H, Gevers D, Devaney KL, Ward DV, Reyes JA, Shah SA, LeLeiko N, Snapper SB, Bousvaros A, Korzenik J, Sands BE, Xavier RJ, Huttenhower C. Dysfunction of the intestinal microbiome in inflammatory bowel disease and treatment. Genome Biol. 2012;13(9):R79. doi: 10.1186/gb-2012-13-9-r79.
Genome Biol. 2012;13(9):R79. doi: 10.1186/gb-2012-13-9-r79.
41. Chen B, Chen H, Shu X, Yin Y, Li J, Qin J, Chen L, Peng K, Xu F, Gu W, Zhao H, Jiang L, Li L, Song J, Elitsur Y, Yu HD, Jiang M, Wang X, Xiang C. Presence of segmented filamentous bacteria in human children and its potential role in the modulation of human gut immunity. Front Microbiol. 2018;9:1403. doi: 10.3389/fmicb.2018.01403.
42. Hansen R, Thomson JM, El-Omar EM, Hold GL. The role of infection in the aetiology of inflammatory bowel disease. J Gastroenterol. 2010;45(3):266–76. doi: 10.1007/s00535-009-0191-y.
43. Timms VJ, Daskalopoulos G, Mitchell HM, Neilan BA. The association of Mycobacterium avium subsp. paratuberculosis with inflammatory bowel disease. PLoS One. 2016;11(2):e0148731. doi: 10.1371/journal.pone.0148731.
doi: 10.1371/journal.pone.0148731.
44. Peng JC, Shen J, Zhu Q, Ran ZH. The impact of Clostridum difficile on surgical rate among ulcerative colitis patients: A systemic review and meta-analysis. Saudi J Gastroenterol. 2015;21(4):208–12. doi: 10.4103/1319-3767.161644.
45. Волчкова ЕВ, Белоусова ЕА, Макарчук ПА, Русанова ЕВ, Великанов ЕВ. Частота выявления инфекции Clostridium difficile в больничных условиях. Альманах клинической медицины. 2014;33:71–6. doi: 10.18786/2072-0505-2014-33-71-76.
46. Bien J, Palagani V, Bozko P. The intestinal microbiota dysbiosis and Clostridium difficile infection: is there a relationship with inflammatory bowel disease? Therap Adv Gastroenterol. 2013;6(1):53–68. doi: 10.1177/1756283X12454590.
47. Byndloss MX, Olsan EE, Rivera-Chávez F, Tiffany CR, Cevallos SA, Lokken KL, Torres TP, Byndloss AJ, Faber F, Gao Y, Litvak Y, Lopez CA, Xu G, Napoli E, Giulivi C, Tsolis RM, Revzin A, Lebrilla CB, Bäumler AJ. Microbiota-activated PPAR-γ signaling inhibits dysbiotic Enterobacteriaceae expansion. Science. 2017;357(6351): 570–5. doi: 10.1126/science.aam9949.
Byndloss MX, Olsan EE, Rivera-Chávez F, Tiffany CR, Cevallos SA, Lokken KL, Torres TP, Byndloss AJ, Faber F, Gao Y, Litvak Y, Lopez CA, Xu G, Napoli E, Giulivi C, Tsolis RM, Revzin A, Lebrilla CB, Bäumler AJ. Microbiota-activated PPAR-γ signaling inhibits dysbiotic Enterobacteriaceae expansion. Science. 2017;357(6351): 570–5. doi: 10.1126/science.aam9949.
48. Zeng MY, Inohara N, Nuñez G. Mechanisms of inflammation-driven bacterial dysbiosis in the gut. Mucosal Immunol. 2017;10(1):18–26. doi: 10.1038/mi.2016.75.
49. Laserna-Mendieta EJ, Clooney AG, Carretero-Gomez JF, Moran C, Sheehan D, Nolan JA, Hill C, Gahan CGM, Joyce SA, Shanahan F, Claesson MJ. Determinants of Reduced Genetic Capacity for Butyrate Synthesis by the Gut Microbiome in Crohn’s Disease and Ulcerative Colitis. J Crohns Colitis. 2018;12(2):204–16. doi: 10.1093/ecco-jcc/jjx137.
50. Litvak Y, Byndloss MX, Tsolis RM, Bäumler AJ. Dysbiotic Proteobacteria expansion: a microbial signature of epithelial dysfunction. Curr Opin Microbiol. 2017;39:1–6. doi: 10.1016/j.mib.2017.07.003.
51. Sokol H, Seksik P, Furet JP, Firmesse O, Nion-Larmurier I, Beaugerie L, Cosnes J, Corthier G, Marteau P, Doré J. Low counts of Faecalibacterium prausnitzii in colitis microbiota. Inflamm Bowel Dis. 2009;15(8):1183–9. doi: 10.1002/ibd.20903.
52. Machiels K, Joossens M, Sabino J, De Preter V, Arijs I, Eeckhaut V, Ballet V, Claes K, Van Immerseel F, Verbeke K, Ferrante M, Verhaegen J, Rutgeerts P, Vermeire S. A decrease of the butyrate-producing species Roseburia hominis and Faecalibacterium prausnitzii defines dysbiosis in patients with ulcerative colitis. Gut. 2014;63(8):1275–83. doi: 10.1136/gutjnl-2013-304833.
Gut. 2014;63(8):1275–83. doi: 10.1136/gutjnl-2013-304833.
53. Takahashi K, Nishida A, Fujimoto T, Fujii M, Shioya M, Imaeda H, Inatomi O, Bamba S, Sugimoto M, Andoh A. Reduced abundance of butyrate-producing bacteria species in the fecal microbial community in Crohn’s disease. Digestion. 2016;93(1):59–65. doi: 10.1159/000441768.
54. Duboc H, Rajca S, Rainteau D, Benarous D, Maubert MA, Quervain E, Thomas G, Barbu V, Humbert L, Despras G, Bridonneau C, Dumetz F, Grill JP, Masliah J, Beaugerie L, Cosnes J, Chazouillères O, Poupon R, Wolf C, Mallet JM, Langella P, Trugnan G, Sokol H, Seksik P. Connecting dysbiosis, bile-acid dysmetabolismand gut inflammation in inflammatory bowel diseases. Gut. 2013;62(4):531–9. doi: 10.1136/gutjnl-2012-302578.
55. Rehman A, Rausch P, Wang J, Skieceviciene J, Kiudelis G, Bhagalia K, Amarapurkar D, Kupcinskas L, Schreiber S, Rosenstiel P, Baines JF, Ott S. Geographical patterns of the standing and active human gut microbiome in health and IBD. Gut. 2016;65(2):238–48. doi: 10.1136/gutjnl-2014-308341.
Geographical patterns of the standing and active human gut microbiome in health and IBD. Gut. 2016;65(2):238–48. doi: 10.1136/gutjnl-2014-308341.
56. Kang S, Denman SE, Morrison M, Yu Z, Dore J, Leclerc M, McSweeney CS. Dysbiosis of fecal microbiota in Crohn’s disease patients as revealed by a custom phylogenetic microarray. Inflamm Bowel Dis. 2010;16(12):2034–42. doi: 10.1002/ibd.21319.
57. Png CW, Lindén SK, Gilshenan KS, Zoetendal EG, McSweeney CS, Sly LI, McGuckin MA, Florin TH. Mucolytic bacteria with increased prevalence in IBD mucosa augment in vitro utilization of mucin by other bacteria. Am J Gastroenterol. 2010;105(11):2420–8. doi: 10.1038/ajg.2010.281.
58. Vigsnæs LK, Brynskov J, Steenholdt C, Wilcks A, Licht TR. Gram-negative bacteria account for main differences between faecal microbiota from patients with ulcerative colitis and healthy controls. Benef Microbes. 2012;3(4): 287–97. doi: 10.3920/BM2012.0018.
Benef Microbes. 2012;3(4): 287–97. doi: 10.3920/BM2012.0018.
59. Wrzosek L, Miquel S, Noordine ML, Bouet S, Joncquel Chevalier-Curt M, Robert V, Philippe C, Bridonneau C, Cherbuy C, Robbe-Masselot C, Langella P, Thomas M. Bacteroides thetaiotaomicron and Faecalibacterium prausnitzii influence the production of mucus glycans and the development of goblet cells in the colonic epithelium of a gnotobiotic model rodent. BMC Biol. 2013;11:61. doi: 10.1186/1741-7007-11-61.
60. Vigsnaes LK, van den Abbeele P, Sulek K, Frandsen HL, Steenholdt C, Brynskov J, Vermeiren J, van de Wiele T, Licht TR. Microbiotas from UC patients display altered metabolism and reduced ability of LAB to colonize mucus. Sci Rep. 2013;3:1110. doi: 10.1038/srep01110.
61. Fyderek K, Strus M, Kowalska-Duplaga K, Gosiewski T, Wedrychowicz A, Jedynak-Wasowicz U, Sładek M, Pieczarkowski S, Adamski P, Kochan P, Heczko PB. Mucosal bacterial microflora and mucus layer thickness in adolescents with inflammatory bowel disease. World J Gastroenterol. 2009;15(42):5287–94. doi: 10.3748/wjg.15.5287.
Mucosal bacterial microflora and mucus layer thickness in adolescents with inflammatory bowel disease. World J Gastroenterol. 2009;15(42):5287–94. doi: 10.3748/wjg.15.5287.
62. Kabeerdoss J, Jayakanthan P, Pugazhendhi S, Ramakrishna BS. Alterations of mucosal microbiota in the colon of patients with inflammatory bowel disease revealed by real time polymerase chain reaction amplification of 16S ribosomal ribonucleic acid. Indian J Med Res. 2015;142(1): 23–32. doi: 10.4103/0971-5916.162091.
63. Thorkildsen LT, Nwosu FC, Avershina E, Ricanek P, Perminow G, Brackmann S, Vatn MH, Rudi K. Dominant fecal microbiota in newly diagnosed untreated inflammatory bowel disease patients. Gastroenterol Res Pract. 2013;2013:636785. doi: 10.1155/2013/636785.
64. Lozupone CA, Stombaugh JI, Gordon JI, Jansson JK, Knight R. Diversity, stability and resilience of the human gut microbiota. Nature. 2012;489(7415):220–30. doi: 10.1038/nature11550.
Diversity, stability and resilience of the human gut microbiota. Nature. 2012;489(7415):220–30. doi: 10.1038/nature11550.
65. Ситкин СИ, Ткаченко ЕИ, Вахитов ТЯ. Филометаболическое ядро микробиоты кишечника. Альманах клинической медицины. 2015;40:12–34. doi: 10.18786/2072-0505-2015-40-12-34.
66. Salonen A, Salojärvi J, Lahti L, de Vos WM. The adult intestinal core microbiota is determined by analysis depth and health status. Clin Microbiol Infect. 2012;18 Suppl 4:16–20. doi: 10.1111/j.1469-0691.2012.03855.x.
67. Prosberg M, Bendtsen F, Vind I, Petersen AM, Gluud LL. The association between the gut microbiota and the inflammatory bowel disease activity: a systematic review and meta-analysis. Scand J Gastroenterol. 2016;51(12):1407– 15. doi: 10.1080/00365521. 2016.1216587.
2016.1216587.
68. Magnusson MK, Strid H, Isaksson S, Simrén M, Öhman L. The mucosal antibacterial response profile and fecal microbiota composition are linked to the disease course in patients with newly diagnosed ulcerative colitis. Inflamm Bowel Dis. 2017;23(6):956–66. doi: 10.1097/MIB.0000000000001130.
69. Sokol H, Jegou S, McQuitty C, Straub M, Leducq V, Landman C, Kirchgesner J, Le Gall G, Bourrier A, Nion-Larmurier I, Cosnes J, Seksik P, Richard ML, Beaugerie L. Specificities of the intestinal microbiota in patients with inflammatory bowel disease and Clostridium difficile infection. Gut Microbes. 2018;9(1):55–60. doi: 10.1080/19490976.2017.1361092.
70. Rajca S, Grondin V, Louis E, Vernier-Massouille G, Grimaud JC, Bouhnik Y, Laharie D, Dupas JL, Pillant H, Picon L, Veyrac M, Flamant M, Savoye G, Jian R, Devos M, Paintaud G, Piver E, Allez M, Mary JY, Sokol H, Colombel JF, Seksik P. Alterations in the intestinal microbiome (dysbiosis) as a predictor of relapse after infliximab withdrawal in Crohn’s disease. Inflamm Bowel Dis. 2014;20(6):978–86. doi: 10.1097/MIB.0000000000000036.
Alterations in the intestinal microbiome (dysbiosis) as a predictor of relapse after infliximab withdrawal in Crohn’s disease. Inflamm Bowel Dis. 2014;20(6):978–86. doi: 10.1097/MIB.0000000000000036.
71. Magnusson MK, Strid H, Sapnara M, Lasson A, Bajor A, Ung KA, Öhman L. Anti-TNF therapy response in patients with ulcerative colitis is associated with colonic antimicrobial peptide expression and microbiota composition. J Crohns Colitis. 2016;10(8):943–52. doi: 10.1093/ecco-jcc/jjw051.
72. Ananthakrishnan AN, Luo C, Yajnik V, Khalili H, Garber JJ, Stevens BW, Cleland T, Xavier RJ. Gut microbiome function predicts response to anti-integrin biologic therapy in inflammatorybowel diseases. Cell Host Microbe. 2017;21(5): 603–10.e3. doi: 10.1016/j.chom.2017.04.010.
73. Doherty MK, Ding T, Koumpouras C, Telesco SE, Monast C, Das A, Brodmerkel C, Schloss PD. Fecal Microbiota Signatures Are Associated with Response to Ustekinumab Therapy among Crohn’s Disease Patients. MBio. 2018;9(2). pii: e02120–17. doi: 10.1128/mBio.02120-17.
Doherty MK, Ding T, Koumpouras C, Telesco SE, Monast C, Das A, Brodmerkel C, Schloss PD. Fecal Microbiota Signatures Are Associated with Response to Ustekinumab Therapy among Crohn’s Disease Patients. MBio. 2018;9(2). pii: e02120–17. doi: 10.1128/mBio.02120-17.
74. Casén C, Vebø HC, Sekelja M, Hegge FT, Karlsson MK, Ciemniejewska E, Dzankovic S, Frøyland C, Nestestog R, Engstrand L, Munkholm P, Nielsen OH, Rogler G, Simrén M, Öhman L, Vatn MH, Rudi K. Deviations in human gut microbiota: a novel diagnostic test for determining dysbiosis in patients with IBS or IBD. Aliment Pharmacol Ther. 2015;42(1):71–83. doi: 10.1111/apt.13236.
75. Pascal V, Pozuelo M, Borruel N, Casellas F, Campos D, Santiago A, Martinez X, Varela E, Sarrabayrouse G, Machiels K, Vermeire S, Sokol H, Guarner F, Manichanh C. A microbial signature for Crohn’s disease. Gut. 2017;66(5):813–22. doi: 10.1136/gutjnl-2016-313235.
Gut. 2017;66(5):813–22. doi: 10.1136/gutjnl-2016-313235.
76. Montassier E, Al-Ghalith GA, Hillmann B, Viskocil K, Kabage AJ, McKinlay CE, Sadowsky MJ, Khoruts A, Knights D. CLOUD: a non-parametric detection test for microbiome outliers. Microbiome. 2018;6(1):137. doi: 10.1186/s40168-018-0514-4.
77. Costello EK, Lauber CL, Hamady M, Fierer N, Gordon JI, Knight R. Bacterial community variation in human body habitats across space and time. Science. 2009;326(5960):1694–7. doi: 10.1126/science.1177486.
78. Lavelle A, Lennon G, O’Sullivan O, Docherty N, Balfe A, Maguire A, Mulcahy HE, Doherty G, O’Donoghue D, Hyland J, Ross RP, Coffey JC, Sheahan K, Cotter PD, Shanahan F, Winter DC, O’Connell PR. Spatial variation of the colonic microbiota in patients with ulcerative colitis and control volunteers. Gut. 2015;64(10): 1553–61. doi: 10.1136/gutjnl-2014-307873.
Gut. 2015;64(10): 1553–61. doi: 10.1136/gutjnl-2014-307873.
79. Kralik P, Ricchi M. A Basic Guide to Real Time PCR in Microbial Diagnostics: Definitions, Parameters, and Everything. Front Microbiol. 2017;8:108. doi: 10.3389/fmicb.2017.00108.
80. Gerber GK. The dynamic microbiome. FEBS Lett. 2014;588(22):4131–9. doi: 10.1016/j.febslet.2014.02.037.
81. Schippa S, Conte MP. Dysbiotic events in gut microbiota: impact on human health. Nutrients. 2014;6(12):5786–805. doi: 10.3390/nu6125786.
82. Flores GE, Caporaso JG, Henley JB, Rideout JR, Domogala D, Chase J, Leff JW, Vázquez-Baeza Y, Gonzalez A, Knight R, Dunn RR, Fierer N. Temporal variability is a personalized feature of the human microbiome. Genome Biol. 2014;15(12):531. doi: 10.1186/s13059-014-0531-y.
Genome Biol. 2014;15(12):531. doi: 10.1186/s13059-014-0531-y.
83. Holmes I, Harris K, Quince C. Dirichlet multinomial mixtures: generative models for microbial metagenomics. PLoS One. 2012;7(2):e30126. doi: 10.1371/journal.pone.0030126.
84. Zaneveld JR, McMinds R, Vega Thurber R. Stress and stability: applying the Anna Karenina principle to animal microbiomes. Nat Microbiol. 2017;2:17121. doi: 10.1038/nmicrobiol.2017.121.
85. Gonze D, Coyte KZ, Lahti L, Faust K. Microbial communities as dynamical systems. Curr Opin Microbiol. 2018;44:41–9. doi: 10.1016/j.mib.2018.07.004.
86. Arnol’d VI. Catastrophe Theory. 3rd edition. Berlin – Heidelberg: Springer-Verlag; 1992. 150 p. doi: 10. 1007/978-3-642-58124-3.
1007/978-3-642-58124-3.
87. Gibbons SM, Kearney SM, Smillie CS, Alm EJ. Two dynamic regimes in the human gut microbiome. PLoS Comput Biol. 2017;13(2):e1005364. doi: 10.1371/journal.pcbi.1005364.
88. David LA, Materna AC, Friedman J, Campos-Baptista MI, Blackburn MC, Perrotta A, Erdman SE, Alm EJ. Host lifestyle affects human microbiota on daily timescales. Genome Biol. 2014;15(7):R89. doi: 10.1186/gb-2014-15-7-r89.
89. Sommer F, Anderson JM, Bharti R, Raes J, Rosenstiel P. The resilience of the intestinal microbiota influences health and disease. Nat Rev Microbiol. 2017;15(10):630–8. doi: 10.1038/nrmicro.2017.58.
90. Donskey CJ, Hujer AM, Das SM, Pultz NJ, Bonomo RA, Rice LB. Use of denaturing gradient gel electrophoresis for analysis of the stool microbiota of hospitalized patients. J Microbiol Methods. 2003;54(2):249–56. doi: 10.1016/S0167-7012(03)00059-9.
Use of denaturing gradient gel electrophoresis for analysis of the stool microbiota of hospitalized patients. J Microbiol Methods. 2003;54(2):249–56. doi: 10.1016/S0167-7012(03)00059-9.
91. Jernberg C, Löfmark S, Edlund C, Jansson JK. Long-term ecological impacts of antibiotic administration on the human intestinal microbiota. ISME J. 2007;1(1):56–66. doi: 10.1038/ismej.2007.3.
92. Jakobsson HE, Jernberg C, Andersson AF, Sjölund-Karlsson M, Jansson JK, Engstrand L. Short-term antibiotic treatment has differing long-term impacts on the human throat and gut microbiome. PLoS One. 2010;5(3):e9836. doi: 10.1371/journal.pone.0009836.
93. Shenderov BA. Metabiotics: novel idea or natural development of probiotic conception. Microb Ecol Health Dis. 2013;24. doi: 10. 3402/mehd.v24i0.20399.
3402/mehd.v24i0.20399.
94. Reinisch W. Fecal microbiota transplantation in inflammatory bowel disease. Dig Dis. 2017;35(1–2):123–6. doi: 10.1159/000449092.
95. Sitkin S, Pokrotnieks J. Clinical Potential of Anti-inflammatory Effects of Faecalibacterium prausnitzii and Butyrate in Inflammatory Bowel Disease. Inflamm Bowel Dis. 2018. doi: 10.1093/ibd/izy258. [Epub ahead of print].
96. Lavelle A, Lennon G, Winter DC, O’Connell PR. Colonic biogeography in health and ulcerative colitis. Gut Microbes. 2016;7(5):435–42. doi: 10.1080/19490976.2016.1216748.
97. McIlroy J, Ianiro G, Mukhopadhya I, Hansen R, Hold GL. Review article: the gut microbiome in inflammatory bowel disease-avenues for microbial management. Aliment Pharmacol Ther. 2018;47(1):26–42. doi: 10.1111/apt.14384.
Aliment Pharmacol Ther. 2018;47(1):26–42. doi: 10.1111/apt.14384.
98. Walujkar SA, Kumbhare SV, Marathe NP, Patangia DV, Lawate PS, Bharadwaj RS, Shouche YS. Molecular profiling of mucosal tissue associated microbiota in patients manifesting acute exacerbations and remission stage of ulcerative colitis. World J Microbiol Biotechnol. 2018;34(6):76. doi: 10.1007/s11274-018-2449-0.
99. Prideaux L, Kang S, Wagner J, Buckley M, Mahar JE, De Cruz P, Wen Z, Chen L, Xia B, van Langenberg DR, Lockett T, Ng SC, Sung JJ, Desmond P, McSweeney C, Morrison M, Kirkwood CD, Kamm MA. Impact of ethnicity, geography, and disease on the microbiota in health and inflammatory bowel disease. Inflamm Bowel Dis. 2013;19(13):2906–18. doi: 10.1097/01.MIB.0000435759.05577.12.
100. Fedorak RN, Ismond KP. Practical considerations and the intestinal microbiome in disease: antibiotics for IBD therapy. Dig Dis. 2016;34(1– 2):112–21. doi: 10.1159/000443014.
Fedorak RN, Ismond KP. Practical considerations and the intestinal microbiome in disease: antibiotics for IBD therapy. Dig Dis. 2016;34(1– 2):112–21. doi: 10.1159/000443014.
101. Le Bastard Q, Al-Ghalith GA, Grégoire M, Chapelet G, Javaudin F, Dailly E, Batard E, Knights D, Montassier E. Systematic review: human gut dysbiosis induced by non-antibiotic prescription medications. Aliment Pharmacol Ther. 2018;47(3):332–45. doi: 10.1111/apt.14451.
102. Marchesi JR. Shifting from a gene-centric to metabolite-centric strategy to determine the core gut microbiome. Bioeng Bugs. 2011;2(6): 309–14. doi: 10.4161/bbug.2.6.17235.
103. Wang WL, Xu SY, Ren ZG, Tao L, Jiang JW, Zheng SS. Application of metagenomics in the human gut microbiome. World J Gastroenterol. 2015;21(3):803–14. doi: 10.3748/wjg.v21.i3.803.
doi: 10.3748/wjg.v21.i3.803.
104. Ситкин СИ, Вахитов ТЯ, Ткаченко ЕИ, Лазебник ЛБ, Орешко ЛС, Жигалова ТН, Радченко ВГ, Авалуева ЕБ, Селиверстов ПВ, Утсаль ВА, Комличенко ЭВ. Нарушения микробного и эндогенного метаболизма при язвенном колите и целиакии: метаболомный подход к выявлению потенциальных биомаркеров хронического воспаления в кишечнике, связанного с дисбиозом. Экспериментальная и клиническая гастроэнтерология. 2017;(7):4–50.
105. Schirmer M, Franzosa EA, Lloyd-Price J, McIver LJ, Schwager R, Poon TW, Ananthakrishnan AN, Andrews E, Barron G, Lake K, Prasad M, Sauk J, Stevens B, Wilson RG, Braun J, Denson LA, Kugathasan S, McGovern DPB, Vlamakis H, Xavier RJ, Huttenhower C. Dynamics of metatranscription in the inflammatory bowel disease gut microbiome. Nat Microbiol. 2018;3(3):337–46. doi: 10.1038/s41564-017-0089-z.
106. Lavelle A, Sokol H. Gut microbiota: beyond metagenomics, metatranscriptomics illumi-nates microbiome functionality in IBD. Nat Rev Gastroenterol Hepatol. 2018;15(4):193–4. doi: 10.1038/nrgastro.2018.15.
Lavelle A, Sokol H. Gut microbiota: beyond metagenomics, metatranscriptomics illumi-nates microbiome functionality in IBD. Nat Rev Gastroenterol Hepatol. 2018;15(4):193–4. doi: 10.1038/nrgastro.2018.15.
107. Larsen PE, Dai Y. Metabolome of human gut microbiome is predictive of host dysbiosis. Gigascience. 2015;4:42. doi: 10.1186/s13742-015-0084-3.
108. Marchesi JR, Holmes E, Khan F, Kochhar S, Scanlan P, Shanahan F, Wilson ID, Wang Y. Rapid and noninvasive metabonomic characterization of inflammatory bowel disease. J Proteome Res. 2007;6(2):546–51. doi: 10.1021/pr060470d.
109. Huda-Faujan N, Abdulamir AS, Fatimah AB, Anas OM, Shuhaimi M, Yazid AM, Loong YY. The impact of the level of the intestinal short chain Fatty acids in inflammatory bowel disease patients versus healthy subjects.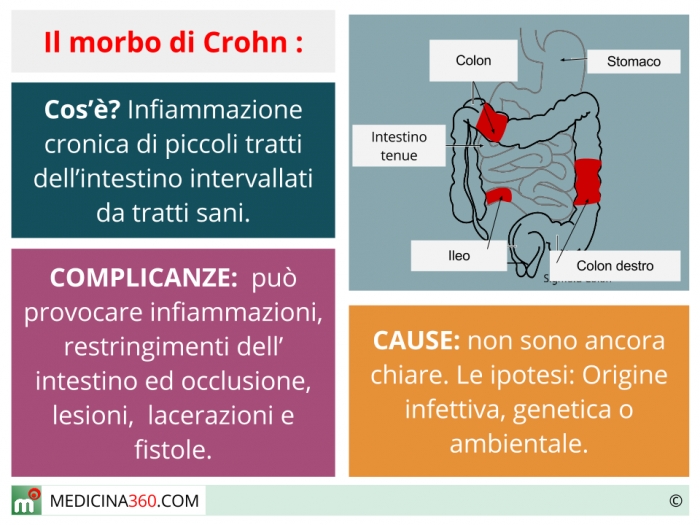 Open Biochem J. 2010;4:53–8. doi: 10.2174/1874091X01004010053.
Open Biochem J. 2010;4:53–8. doi: 10.2174/1874091X01004010053.
110. Venkatesh M, Mukherjee S, Wang H, Li H, Sun K, Benechet AP, Qiu Z, Maher L, Redinbo MR, Phillips RS, Fleet JC, Kortagere S, Mukherjee P, Fasano A, Le Ven J, Nicholson JK, Dumas ME, Khanna KM, Mani S. Symbiotic bacterial metabolites regulate gastrointestinal barrier function via the xenobiotic sensor PXR and Toll-like receptor 4. Immunity. 2014;41(2):296–310. doi: 10.1016/j.immuni.2014.06.014.
111. Agus A, Planchais J, Sokol H. Gut Microbiota Regulation of Tryptophan Metabolism in Health and Disease. Cell Host Microbe. 2018;23(6):716–24. doi: 10.1016/j.chom.2018.05.003.
112. Beloborodova N, Bairamov I, Olenin A, Shubina V, Teplova V, Fedotcheva N. Effect of phenolic acids of microbial origin on production of reactive oxygen species in mitochondria and neutrophils. J Biomed Sci. 2012;19:89. doi: 10.1186/1423-0127-19-89.
J Biomed Sci. 2012;19:89. doi: 10.1186/1423-0127-19-89.
113. Osipov GA, Verkhovtseva NV. Study of human microecology by mass spectrometry of microbial markers. Benef Microbes. 2011;2(1):63–78. doi: 10.3920/BM2010.0017.
114. Nicholson JK, Holmes E, Kinross J, Burcelin R, Gibson G, Jia W, Pettersson S. Host-gut microbiota metabolic interactions. Science. 2012;336(6086):1262–7. doi: 10.1126/science.1223813.
115. Verbeke KA, Boobis AR, Chiodini A, Edwards CA, Franck A, Kleerebezem M, Nauta A, Raes J, van Tol EA, Tuohy KM. Towards microbial fermentation metabolites as markers for health benefits of prebiotics. Nutr Res Rev. 2015;28(1):42–66. doi: 10.1017/S0954422415000037.
116. Santoru ML, Piras C, Murgia A, Palmas V, Camboni T, Liggi S, Ibba I, Lai MA, Orrù S, Blois S, Loizedda AL, Griffin JL, Usai P, Caboni P, Atzori L, Manzin A. Cross sectional evaluation of the gut-microbiome metabolome axis in an Italian cohort of IBD patients. Sci Rep. 2017;7(1):9523. doi: 10.1038/s41598-017-10034-5.
Santoru ML, Piras C, Murgia A, Palmas V, Camboni T, Liggi S, Ibba I, Lai MA, Orrù S, Blois S, Loizedda AL, Griffin JL, Usai P, Caboni P, Atzori L, Manzin A. Cross sectional evaluation of the gut-microbiome metabolome axis in an Italian cohort of IBD patients. Sci Rep. 2017;7(1):9523. doi: 10.1038/s41598-017-10034-5.
117. Ley RE, Peterson DA, Gordon JI. Ecological and evolutionary forces shaping microbial diversity in the human intestine. Cell. 2006;124(4): 837–48. doi: 10.1016/j.cell.2006.02.017.
118. Dethlefsen L, McFall-Ngai M, Relman DA. An ecological and evolutionary perspective on human-microbe mutualism and disease. Nature. 2007;449(7164):811–8. doi: 10.1038/nature06245.
119. Turnbaugh PJ, Hamady M, Yatsunenko T, Cantarel BL, Duncan A, Ley RE, Sogin ML, Jones WJ, Roe BA, Affourtit JP, Egholm M, Henrissat B, Heath AC, Knight R, Gordon JI. A core gut microbiome in obese and lean twins. Nature. 2009;457(7228):480–4. doi: 10.1038/nature07540.
A core gut microbiome in obese and lean twins. Nature. 2009;457(7228):480–4. doi: 10.1038/nature07540.
120. Moya A, Ferrer M. Functional Redundancy-Induced Stability of Gut Microbiota Subjected to Disturbance. Trends Microbiol. 2016;24(5): 402–13. doi: 10.1016/j.tim.2016.02.002.
121. Human Microbiome Project Consortium. Structure, function and diversity of the healthy human microbiome. Nature. 2012;486(7402): 207–14. doi: 10.1038/nature11234.
122. Ардатская МД, Бельмер СВ, Добрица ВП, Захаренко СМ, Лазебник ЛБ, Минушкин ОН, Орешко ЛС, Ситкин СИ, Ткаченко ЕИ, Суворов АН, Хавкин АИ, Шендеров БА. Дисбиоз (дисбактериоз) кишечника: современное состояние проблемы, комплексная диагностика и лечебная коррекция. Экспериментальная и клиническая гастроэнтерология.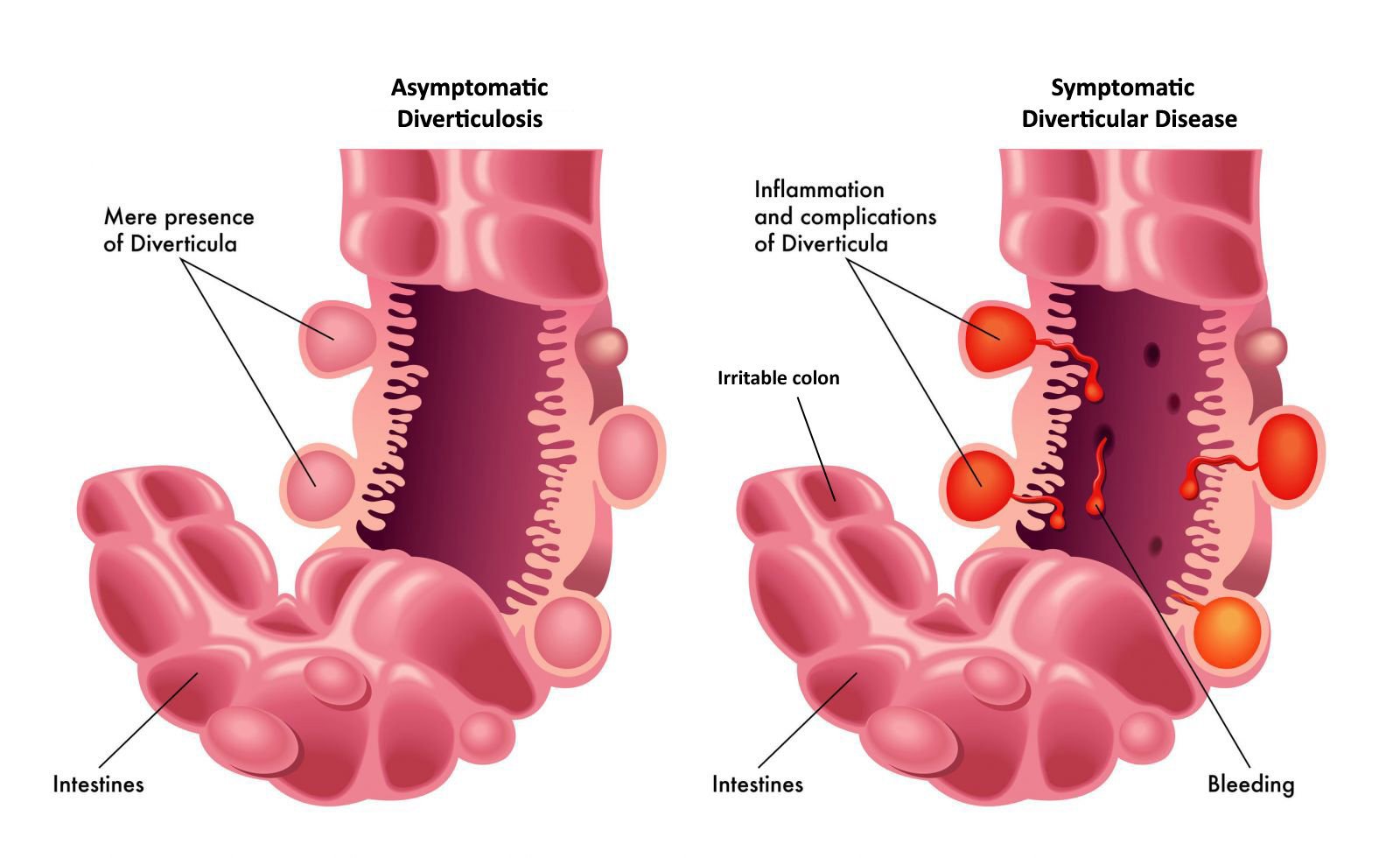 2015;(5):13–50.
2015;(5):13–50.
123. Flint HJ, Scott KP, Duncan SH, Louis P, Forano E. Microbial degradation of complex carbohydrates in the gut. Gut Microbes. 2012;3(4): 289–306. doi: 10.4161/gmic.19897.
124. Rajilić-Stojanović M, de Vos WM. The first 1000 cultured species of the human gastrointestinal microbiota. FEMS Microbiol Rev. 2014;38(5):996–1047. doi: 10.1111/1574-6976.12075.
125. Walker AW. Studying the human microbiota. Adv Exp Med Biol. 2016;902:5–32. doi: 10.1007/978-3-319-31248-4_2.
126. Tarasova E, Abdurasulova I, Matsulevich A, Skulyabin D, Bisaga G, Ermolenko E, Suvorov A, Klimenko V. Intestinal microbiota composition in patients with multiple sclerosis. Abstracts of 26th ECCMID Congress, the European Congress of Clinical Microbiology and Infectious Diseases. Amsterdam, Netherlands, 9–12 April, 2016. 2016. ESCMID eLibrary. P1001. Abstract 4608 [Internet]. Available from: https://www.researchgate.net/publication/303633786_Intestinal_microbiota_composition_in_patients_with_multiple_sclerosis.
Amsterdam, Netherlands, 9–12 April, 2016. 2016. ESCMID eLibrary. P1001. Abstract 4608 [Internet]. Available from: https://www.researchgate.net/publication/303633786_Intestinal_microbiota_composition_in_patients_with_multiple_sclerosis.
127. Sitkin S, Vakhitov T, Tkachenko E, Zhigalova T, Oreshko L, Suvorova M. P749. Not only butyrate-producing bacteria but possibly also Bacteroides thetaiotaomicron protects against ulcerative colitis. J Crohns Colitis. 2016;10(Sup-pl 1):S489. doi: 10.1093/ecco-jcc/jjw019.868.
128. Багненко СФ, Захаренко АА, Суворов АН, Шлык ИВ, Тен ОА, Джамилов ШР, Беляев МА, Трушин АА, Натха АС, Зайцев ДА, Вовин КН, Рыбальченко ВА. Периоперационные изменения кишечного микробиоценоза у больных раком толстой кишки. Вестник хирургии им. И.И. Грекова. 2016;175(6):33–7. doi: 10.24884/0042-4625-2016-175-6-33-37.
129. Sitkin S, Vakhitov T, Tkachenko E, Avalueva E, Oreshko L, Zhigalova T, Demyanova E, Shalaeva O, Utsal V, Suvorova M, Komlichenko E. P852. A metabolomics approach to discover biomarkers of chronic intestinal inflammation associated with gut microbiota dysbiosis in ulcerative colitis and Celiac Disease. J Crohns Colitis. 2018;12(Suppl 1):S547–8. doi: 10.1093/ecco-jcc/jjx180.979.
Sitkin S, Vakhitov T, Tkachenko E, Avalueva E, Oreshko L, Zhigalova T, Demyanova E, Shalaeva O, Utsal V, Suvorova M, Komlichenko E. P852. A metabolomics approach to discover biomarkers of chronic intestinal inflammation associated with gut microbiota dysbiosis in ulcerative colitis and Celiac Disease. J Crohns Colitis. 2018;12(Suppl 1):S547–8. doi: 10.1093/ecco-jcc/jjx180.979.
130. Mancabelli L, Milani C, Lugli GA, Turroni F, Cocconi D, van Sinderen D, Ventura M. Identification of universal gut microbial biomarkers of common human intestinal diseases by meta-analysis. FEMS Microbiol Ecol. 2017;93(12). doi: 10.1093/femsec/fix153.
131. Duvallet C, Gibbons SM, Gurry T, Irizarry RA, Alm EJ. Meta-analysis of gut microbiome studies identifies disease-specific and shared responses. Nat Commun. 2017;8(1):1784. doi: 10.1038/s41467-017-01973-8.
132. Rosen CE, Palm NW. Functional Classification of the Gut Microbiota: The Key to Cracking the Microbiota Composition Code: Functional classifications of the gut microbiota reveal previously hidden contributions of indigenous gut bacteria to human health and disease. Bioessays. 2017;39(12). doi: 10.1002/bies.201700032.
133. Walker AW, Duncan SH, Louis P, Flint HJ. Phylogeny, culturing, and metagenomics of the human gut microbiota. Trends Microbiol. 2014;22(5):267–74. doi: 10.1016/j.tim.2014.03.001.
134. Devlin AS, Fischbach MA. A biosynthetic pathway for a prominent class of microbiota-derived bile acids. Nat Chem Biol. 2015;11(9): 685–90. doi: 10.1038/nchembio.1864.
135. Kettle H, Louis P, Holtrop G, Duncan SH, Flint HJ. Modelling the emergent dynamics and major metabolites of the human colonic microbiota. Environ Microbiol. 2015;17(5): 1615–30. doi: 10.1111/1462-2920.12599.
Kettle H, Louis P, Holtrop G, Duncan SH, Flint HJ. Modelling the emergent dynamics and major metabolites of the human colonic microbiota. Environ Microbiol. 2015;17(5): 1615–30. doi: 10.1111/1462-2920.12599.
136. Dodd D, Spitzer MH, Van Treuren W, Merrill BD, Hryckowian AJ, Higginbottom SK, Le A, Cowan TM, Nolan GP, Fischbach MA, Sonnenburg JL. A gut bacterial pathway metabolizes aromatic amino acids into nine circulating metabolites. Nature. 2017;551(7682):648–52. doi: 10.1038/nature24661.
137. Sitkin S, Vakhitov T, Pokrotnieks J. How to increase the butyrate-producing capacity of thegut microbiome: do IBD patients really need butyrate replacement and butyrogenic therapy? J Crohns Colitis. 2018;12(7):881–2. doi: 10.1093/ecco-jcc/jjy033.
138. Donohoe DR, Garge N, Zhang X, Sun W, O’Connell TM, Bunger MK, Bultman SJ. The microbiome and butyrate regulate energy metabolism and autophagy in the mammalian colon. Cell Metab. 2011;13(5):517–26. doi: 10.1016/j.cmet.2011.02.018.
The microbiome and butyrate regulate energy metabolism and autophagy in the mammalian colon. Cell Metab. 2011;13(5):517–26. doi: 10.1016/j.cmet.2011.02.018.
139. Dumas ME. The microbial-mammalian metabolic axis: beyond simple metabolism. Cell Metab. 2011;13(5):489–90. doi: 10.1016/j.cmet.2011.04.005.
140. Wang A, Si H, Liu D, Jiang H. Butyrate activates the cAMP-protein kinase A-cAMP response element-binding protein signaling pathway in Caco-2 cells. J Nutr. 2012;142(1):1–6. doi: 10.3945/jn.111.148155.
141. Hamer HM, Jonkers D, Venema K, Vanhoutvin S, Troost FJ, Brummer RJ. Review article: the role of butyrate on colonic function. Aliment Pharmacol Ther. 2008;27(2):104–19. doi: 10.1111/j.1365-2036.2007.03562.x.
142. Louis P, Flint HJ. Diversity, metabolism and microbial ecology of butyrate-producing bacteria from the human large intestine. FEMS Microbiol Lett. 2009;294(1):1–8. doi: 10.1111/j.1574-6968.2009.01514.x.
Louis P, Flint HJ. Diversity, metabolism and microbial ecology of butyrate-producing bacteria from the human large intestine. FEMS Microbiol Lett. 2009;294(1):1–8. doi: 10.1111/j.1574-6968.2009.01514.x.
143. Vital M, Howe AC, Tiedje JM. Revealing the bacterial butyrate synthesis pathways by analyzing (meta)genomic data. MBio. 2014;5(2):e00889. doi: 10.1128/mBio.00889-14.
144. Zhou L, Zhang M, Wang Y, Dorfman RG, Liu H, Yu T, Chen X, Tang D, Xu L, Yin Y, Pan Y, Zhou Q, Zhou Y, Yu C. Faecalibacterium prausnitzii produces butyrate to maintain Th27/Treg balance and to ameliorate colorectal colitis by inhibiting histone deacetylase 1. Inflamm Bowel Dis. 2018;24(9):1926–40. doi: 10.1093/ibd/izy182.
145. Zheng L, Kelly CJ, Battista KD, Schaefer R, Lanis JM, Alexeev EE, Wang RX, Onyiah JC, Kominsky DJ, Colgan SP. Microbial-derived butyrate promotes epithelial barrier function through IL-10 receptor-dependent repression of claudin-2. J Immunol. 2017;199(8):2976–84. doi: 10.4049/jimmunol.1700105.
Microbial-derived butyrate promotes epithelial barrier function through IL-10 receptor-dependent repression of claudin-2. J Immunol. 2017;199(8):2976–84. doi: 10.4049/jimmunol.1700105.
146. Thibault R, Blachier F, Darcy-Vrillon B, de Coppet P, Bourreille A, Segain JP. Butyrate utilization by the colonic mucosa in inflammatory bowel diseases: a transport deficiency. Inflamm Bowel Dis. 2010;16(4):684–95. doi: 10.1002/ibd.21108.
147. Boesmans L, Ramakers M, Arijs I, Windey K, Vanhove W, Schuit F, Rutgeerts P, Verbeke K, De Preter V. Inflammation-induced downregulation of butyrate uptake and oxidation is not caused by a reduced gene expression. J Cell Physiol. 2015;230(2):418–26. doi: 10.1002/jcp.24725.
148. Kumar A, Alrefai WA, Borthakur A, Dudeja PK. Lactobacillus acidophilus counteracts en-teropathogenic E. coli-induced inhibition of butyrate uptake in intestinal epithelial cells. Am J Physiol Gastrointest Liver Physiol. 2015;309(7):G602–7. doi: 10.1152/ajpgi.00186.2015.
coli-induced inhibition of butyrate uptake in intestinal epithelial cells. Am J Physiol Gastrointest Liver Physiol. 2015;309(7):G602–7. doi: 10.1152/ajpgi.00186.2015.
149. Hulin SJ, Singh S, Chapman MA, Allan A, Langman MJ, Eggo MC. Sulphide-induced energy deficiency in colonic cells is prevented by glucose but not by butyrate. Aliment Pharmacol Ther. 2002;16(2):325–31. doi: 10.1046/j.1365-2036.2002.01164.x.
150. Reichardt N, Vollmer M, Holtrop G, Farquharson FM, Wefers D, Bunzel M, Duncan SH, Drew JE, Williams LM, Milligan G, Preston T, Morrison D, Flint HJ, Louis P. Specific substrate-driven changes in human faecal microbiota composition contrast with functional redundancy in short-chain fatty acid production. ISME J. 2018;12(2):610–22. doi: 10.1038/ismej.2017.196.
151. Quévrain E, Maubert MA, Michon C, Chain F, Marquant R, Tailhades J, Miquel S, Carlier L, Bermúdez-Humarán LG, Pigneur B, Lequin O, Kharrat P, Thomas G, Rainteau D, Aubry C, Breyner N, Afonso C, Lavielle S, Grill JP, Chassaing G, Chatel JM, Trugnan G, Xavier R, Langella P, Sokol H, Seksik P. Identification of an anti-inflammatory protein from Faecalibacterium prausnitzii, a commensal bacterium deficient in Crohn’s disease. Gut. 2016;65(3):415–25. doi: 10.1136/gutjnl-2014-307649.
Quévrain E, Maubert MA, Michon C, Chain F, Marquant R, Tailhades J, Miquel S, Carlier L, Bermúdez-Humarán LG, Pigneur B, Lequin O, Kharrat P, Thomas G, Rainteau D, Aubry C, Breyner N, Afonso C, Lavielle S, Grill JP, Chassaing G, Chatel JM, Trugnan G, Xavier R, Langella P, Sokol H, Seksik P. Identification of an anti-inflammatory protein from Faecalibacterium prausnitzii, a commensal bacterium deficient in Crohn’s disease. Gut. 2016;65(3):415–25. doi: 10.1136/gutjnl-2014-307649.
152. Breyner NM, Michon C, de Sousa CS, Vilas Boas PB, Chain F, Azevedo VA, Langella P, Chatel JM. Microbial Anti-Inflammatory Molecule (MAM) from Faecalibacterium prausnitzii shows a protective effect on DNBS and DSS-induced colitis model in mice through inhibition of NF-κB pathway. Front Microbiol. 2017;8:114. doi: 10.3389/fmicb.2017.00114.
153. Fernandes J, Su W, Rahat-Rozenbloom S, Wolever TM, Comelli EM. Adiposity, gut microbiota and faecal short chain fatty acids are linked in adult humans. Nutr Diabetes. 2014;4:e121. doi: 10.1038/nutd.2014.23.
Adiposity, gut microbiota and faecal short chain fatty acids are linked in adult humans. Nutr Diabetes. 2014;4:e121. doi: 10.1038/nutd.2014.23.
154. den Besten G, van Eunen K, Groen AK, Venema K, Reijngoud DJ, Bakker BM. The role of short-chain fatty acids in the interplay between diet, gut microbiota, and host energy metabolism. J Lipid Res. 2013;54(9):2325–40. doi: 10.1194/jlr.R036012.
155. Lewis SJ, Heaton KW. Increasing butyrate concentration in the distal colon by accelerating intestinal transit. Gut. 1997;41(2):245–51. doi: 10.1136/gut.41.2.245.
156. Boets E, Deroover L, Houben E, Vermeulen K, Gomand SV, Delcour JA, Verbeke K. Quantification of in vivo colonic short chain fatty acid production from inulin. Nutrients. 2015;7(11): 8916–29. doi: 10. 3390/nu7115440.
3390/nu7115440.
157. van der Beek CM, Bloemen JG, van den Broek MA, Lenaerts K, Venema K, Buurman WA, Dejong CH. Hepatic uptake of rectally ad-ministered butyrate prevents an increase in systemic butyrate concentrations in humans. J Nutr. 2015;145(9):2019–24. doi: 10.3945/jn.115.211193.
158. Louis P, Duncan SH, McCrae SI, Millar J, Jackson MS, Flint HJ. Restricted distribution of the butyrate kinase pathway among butyrate-producing bacteria from the human colon. J Bacteriol. 2004;186(7):2099–106. doi: 10.1128/JB.186.7.2099-2106.2004.
159. Vital M, Karch A, Pieper DH. Colonic butyrate-producing communities in humans: an overview using Omics data. mSystems. 2017;2(6). pii: e00130-17. doi: 10.1128/mSystems.00130-17.
160. de Sousa Moraes LF, Grzeskowiak LM, de Sales Teixeira TF, Gouveia Peluzio Mdo C. Intestinal microbiota and probiotics in celiac disease. Clin Microbiol Rev. 2014;27(3):482–9. doi: 10.1128/CMR.00106-13.
161. Costello SP, Soo W, Bryant RV, Jairath V, Hart AL, Andrews JM. Systematic review with meta-analysis: faecal microbiota transplantation for the induction of remission for active ulcerative colitis. Aliment Pharmacol Ther. 2017;46(3):213–24. doi: 10.1111/apt.14173.
162. Derwa Y, Gracie DJ, Hamlin PJ, Ford AC. Systematic review with meta-analysis: the efficacy of probiotics in inflammatory bowel disease. Aliment Pharmacol Ther. 2017;46(4): 389–400. doi: 10.1111/apt.14203.
163. Jacobi CA, Malfertheiner P. Escherichia coli Nissle 1917 (Mutaflor): new insights into an old probiotic bacterium. Dig Dis. 2011;29(6): 600–7. doi: 10.1159/000333307.
164. Zocco MA, dal Verme LZ, Cremonini F, Piscaglia AC, Nista EC, Candelli M, Novi M, Rigante D, Cazzato IA, Ojetti V, Armuzzi A, Gasbarrini G, Gasbarrini A. Efficacy of Lactobacillus GG in maintaining remission of ulcerative colitis. Aliment Pharmacol Ther. 2006;23(11):1567–74. doi: 10.1111/j.1365-2036.2006.02927.x.
165. World Gastroenterology Organisation Global Guidelines ‘Probiotics and Prebiotics’. 2017 Feb. Available from: http://www. worldgastroenterology.org/guidelines/globalguidelines/probiotics-and-prebiotics/ probiotics-and-prebiotics-english [Accessed 05 September 2018].
166. Laurell A, Sjöberg K. Prebiotics and synbiotics in ulcerative colitis. Scand J Gastroenterol. 2017;52(4):477–85. doi: 10.1080/00365521.2016.1263680.
167. Fernández-Bañares F, Hinojosa J, Sánchez-Lombraña JL, Navarro E, Martínez-Salmerón JF, García-Pugés A, González-Huix F, Riera J, González-Lara V, Domínguez-Abascal F, Giné JJ, Moles J, Gomollón F, Gassull MA. Randomized clinical trial of Plantago ovata seeds (dietary fiber) as compared with mesalamine in maintaining remission in ulcerative coli-tis. Spanish Group for the Study of Crohn’s Disease and Ulcerative Colitis (GETECCU). Am J Gastroenterol. 1999;94(2):427–33. doi: 10.1111/j.1572-0241.1999.872_a.x.
168. Sagar NM, Cree IA, Covington JA, Arasaradnam RP. The interplay of the gut microbiome, bile acids, and volatile organic compounds. Gastroenterol Res Pract. 2015;2015:398585. doi: 10.1155/2015/398585.
169. Vakhitov TY, Chalisova NI, Sitkin SI, Sall TS, Shalaeva ON, Demyanova EV, Morugina AS, Vinogradova AF, Petrov AV, Nozdrachev AD. Low-molecular-weight components of the metabolome control the proliferative activity in cellular and bacterial cultures. Dokl Biol Sci. 2017;472(1):8–10. doi: 10.1134/S0012496617010069.
170. Vernia P, Monteleone G, Grandinetti G, Villotti G, Di Giulio E, Frieri G, Marcheggiano A, Pallone F, Caprilli R, Torsoli A. Combined oral sodium butyrate and mesalazine treatment compared to oral mesalazine alone in ulcerative colitis: randomized, double-blind, placebo-controlled pilot study. Dig Dis Sci. 2000;45(5):976–81. doi: 10.1023/A:1005537411244.
171. Assisi RF; GISDI Study Group. Combined butyric acid/mesalazine treatment in ulcerative colitis with mild-moderate activity. Results of a multicentre pilot study. Minerva Gastroenterol Dietol. 2008;54(3):231–8.
172. Sitkin S, Tkachenko E, Vakhitov T, Oreshko L, Zhigalova T. P399. Oral butyrate plus inulin improve serum metabolomic profile and gut microbiota composition in ulcerative colitis and celiac disease. J Crohns Colitis. 2014;8(Suppl 1):S232. doi: 10.1016/S1873-9946(14)60519-5.
173. Chang PV, Hao L, Offermanns S, Medzhitov R. The microbial metabolite butyrate regulates intestinal macrophage function via histone deacetylase inhibition. Proc Natl Acad Sci U S A. 2014;111(6):2247–52. doi: 10.1073/pnas.1322269111.
174. Moayyedi P, Surette MG, Kim PT, Libertucci J, Wolfe M, Onischi C, Armstrong D, Marshall JK, Kassam Z, Reinisch W, Lee CH. Fecal microbiota transplantation induces remission in patients with active ulcerative colitis in a randomized controlled Trial. Gastroenterology. 2015;149(1):102–9.e6. doi: 10.1053/j.gastro.2015.04.001.
175. Vaughn BP, Vatanen T, Allegretti JR, Bai A, Xavier RJ, Korzenik J, Gevers D, Ting A, Robson SC, Moss AC. Increased intestinal microbial diversity following fecal microbiota transplant for active Crohn’s disease. Inflamm Bowel Dis. 2016;22(9):2182–90. doi: 10.1097/MIB.0000000000000893.
176. Blumstein DT, Levy K, Mayer E, Harte J. Gastrointestinal dysbiosis. Evol Med Public Health. 2014;2014(1):163. doi: 10.1093/emph/eou029.
177. Wang HG, Liu SP, Ma TH, Yan W, Zhou JF, Shi YT, Shen P, Yang XZ, Wu SN. Fecal microbiota transplantation treatment for refractory ulcerative colitis with allergy to 5-aminosalicylic acid: a case report. Medicine (Baltimore). 2018;97(19):e0675. doi: 10.1097/MD.0000000000010675.
178. Martin FP, Su MM, Xie GX, Guiraud SP, Kussmann M, Godin JP, Jia W, Nydegger A. Urinary metabolic insights into host-gut microbial interactions in healthy and IBD children. World J Gastroenterol. 2017;23(20):3643–54. doi: 10.3748/wjg.v23.i20.3643.
179. Qu D, Shen L, Liu S, Li H, Ma Y, Zhang R, Wu K, Yao L, Li J, Zhang J. Chronic inflammation confers to the metabolic reprogramming associated with tumorigenesis of colorectal cancer. Cancer Biol Ther. 2017;18(4):237–44. doi: 10.1080/15384047.2017.1294292.
180. Ip WKE, Hoshi N, Shouval DS, Snapper S, Medzhitov R. Anti-inflammatory effect of IL-10 mediated by metabolic reprogramming of macrophages. Science. 2017;356(6337): 513–9. doi: 10.1126/science.aal3535.
181. Abraham BP, Quigley EMM. A probiotic for ulcerative colitis: the culture wars continue. Dig Dis Sci. 2018;63(7):1678–80. doi: 10.1007/s10620-018-5097-1.
Диагностика кишечника – методы обследования.
Сегодня медицина имеет широкий диапазон диагностических методов для проведения высокоточного обследования целого ряда проблем с толстым кишечником, анальным каналом и промежностью, а также широкие возможности для лечения ряда заболеваний. В перчень диагностики входят инструментальные и безинструментальные ректальные способы проведения обследования, общие анализы, а также ряд исследований.
Проведение общего осмотра доктором
Колопроктолог начинает обследование с определения жалоб, осмотра общего плана и сбора информации. Осмотр играет немаловажное значение и помогает установить диагноз. При помощи первоначального осмотра можно заметить целый ряд проблем: вздутие всего живота, некоторых его участков, перистальтику, наличие опухоли, выпячивание брюшной стенки вперед и прочее.
Способы обследования кишечника?
Простукивание или перкуссия позволяет определить присутствие скопившейся жидкости в полости живота, наличие в ней газов, метеоризм, а также рассчитать примерные пределы вздутой петли кишечника.
Выслушивание шумов или аускультация позволяет услышать и оценить перистальтику, определить признаки проблем с проходимостью, а также ряд других проблем.
Прощупывание или так называемая пальпация живота считается одним из наиболее полезных первичных способов определения:
- излишнего напряжения мышц брюшной полости;
- расположения, размера, типа, подвижности опухоли, а также сокращения спастического типа петель, асцита и множества других проблем и патологий;
Когда завершается осмотр промежности, доктор начинает пальцевое исследование прямой кишки, а затем аноскопию или ректороманоскопию, зависимо от конкретной ситуации. Во время проведения осмотра перианальной зоны проводят проверку рефлексов в виде сокращения мышц сфинктера при незначительном раздражении кожи около него.
Обследование прямой кишки при помощи пальца
Его проводят, если есть жалобы на неприятные ощущения в области живота и при проблемах с органами малого таза и ЖКТ. Исследование осуществляют при помощи указательного пальца. Надев перчатку, специалист аккуратно проводит осмотр. Для расслабления мышц больному необходимо немного тужиться.
Метод ректороманоскопии (ректоскопии)
Данный метод предполагает введение ректороманоскопа через анальный проход на глубину двадцать-тридцать сантиметров. Благодаря увеличительной оптике, которая используется в ходе проведения процедуры, можно рассмотреть даже самые мелкие нарушения состояния слизистой.
В случае присутствия подозрений на недоброкачественность новообразований доктор может отобрать материал для проведения анализа тканей. Благодаря биопсии можно получить точный ответ о виде имеющейся у больного опухоли.
Если вам больше сорока лет, то лучше всего проводить ректоскопию не реже раза в год – это позволит предупредить развитие недоброкачественных новообразований кишечника.
Процедура практически не приносит боли, но в отдельных случаях может использоваться местная анестезия. Для того чтобы правильно провести ректороманоскопию, следует за день до процедуры хорошо очистить толстый кишечник от кала. Это можно сделать при помощи ослабляющих кишечник средств или с использованием клизмы.
Больным следует соблюдать особенную диету, вечером выпить только чай, а само исследование проводить не принимая перед этим никакой пищи. Грамотная подготовка к такого рода процедуре позволяет получить гарантию точного результата, потому не стоит ею пренебрегать.
Аноскопия
Аноскопия – это метод обследования кишечника путем осмотра его изнутри при помощи специального устройства аноскопа, который вводят через анальный проход вплоть до 14 сантиметров в глубину. Аноскопию проводят при наличии жалоб на болезненные ощущения в области анального прохода, кровяные выделения, нарушения стула, а также подозрениях на болезни прямого кишечника. Аноскопия дополняет обычное ректальное обследование. Подготовка к аноскопии ничем не отличается от подготовки к ректороманоскопии, а также является не менее важной и ответственной.
Биопсия
Ткани для исследования причин опухоли или полипа берут с использованием специальных эндоскопических инструментов. Существует два вида биопсии “Прицельная” или “Слепая”. Первую проводят при присутствии подозрений на опухоль или болезнь крона, а вторую при высоком риске диффузийного поражения кишечника.
Колоноскопия
Колоноскопия – это метод эндоскопической диагностики болезней толстого кишечника, который предполагает использование колоноскопа.
Зачастую для проведения колоноскопического исследования не нужно применять никакой анестезии. Пациенты с сильной болью в области заднего прохода нуждаются в местной анестезии, а при наличии существенного разрушения тканей применяется и общая анестезия.
Колоноскопия – это довольно информативный способ исследования лишь тогда, когда пациент строго выполняет предписания доктора, относящиеся к очищению кишечника. От овощей, фруктов, зелени, грибов, картофеля и бобов следует полностью отказаться.
За день до колоноскопии можно принимать исключительно жидкую и легко перевариваемую пищу. Клизмирование проводят до выхода воды в чистом виде. Не стоит недооценивать важность подготовки к процедурам исследования кишечника. Правильная подготовка – гарантия точного результата.
В ходе проведения колоноспокического исследования больные ощущают переполнение кишечника газами и позывы на дефекацию. После того как исследование завершается, введенный в кишечник воздух отсасывают через специальный канал эндоскопа. У больного могут наблюдаться кратковременные небольшие неприятные ощущения. В случае, если ощущение переполнения кишечника газами не прошло, принимают десяток таблеток активированного угля, запивая кипяченой водой комнатной температуры.
Лабораторные исследования
Общий анализ кала позволяет обнаружить кровь, пигменты желчи и паразитов. Подобный анализ позволяет обнаружить воспалительный процесс, инвазию, состав и состояние флоры, начинающиеся язвы и прочее. Анализ кала на присутствие в нем скрытой крови может помочь определить кровотечение в частях, которые располагаются выше толстой кишки.
В результате проведенного анализа можно диагностировать наличие увеличенных варикозом вен ЖКТ, пептической язвы, дизентерии и множество подобных патологических состояний. Стоит отметить, что ранняя диагностика заболеваний кишечника, ровно как и любых других, значительно повышает шансы на скорейшее восстановление и минимизирует последствия перенесенной болезни.
Диагностика онкологических болезней кишечника
Полноценные проявления онкологических болезней толстого кишечника появляются не сразу: часто пациенты жалуются на неприятные ощущения в районе живота, выраженные симптомы расстройства кишечника, постоянные запоры или понос, значительное и быстрое снижение веса тела, а также очень высокую утомляемость.
В случае активно развивающегося заболевания может появиться ухудшение кишечной проходимости, а если опухоль сильно разрослась, то пациент может чувствовать ее в животе. Данные симптомы зачастую сопровождаются значительным снижением аппетита, потерей массы тела, потерей трудоспособности и обезвоживанием, тем не менее, они не являются обязательными.
Онкологические болезни толстой кишки могут быть диагностированы целым спектром исследований и анализов, перечисленных ранее. Одним из самых высокоинформативных методов установления предрасположенности к онкологии может послужить эмбриональный раковый антиген, который считается индикатором присутствия процессов образования опухоли в кишечнике.
СА 19,9 – это онкомаркер злокачественных болезней ЖКТ и органов малого таза.
Наивысшая его чувствительность может отмечаться в случае онкологии поджелудочной железы, недоброкачественного новообразования в желчевыводящих путях, а также в печени. В случае онкологии ЖКТ и кишечника содержание онкомаркера существенно увеличивается. Незначительное повышение показателей данного онкомаркера может наблюдаться при таких неприятных болезнях, как холецистит, а также панкреатит в острой форме.
Кишечник – это очень важный орган человеческого организма. От его состояния, стабильной и бесперебойной работы, а также от состояния микрофлоры зависит здоровье не только ЖКТ, но и организма человека полностью. Потому, если вы стали замечать у себя разные симптомы патологического характера, будь то запор, понос, излишнее образование газов в кишечнике, вздутие, сыпь на коже, высокая утомляемость, ухудшение качества сна, боль в районе живота и некоторые другие – это повод обратить внимание на здоровье своего кишечника. В таком случае вам можно порекомендовать исследование комплексного плана ЖКТ.
Диагностика кишечника в клинике «Чудо Доктор»
Не стоит бояться различных методов медицинского обследования кишечника. Сейчас вы имеете информацию относительно разных методов диагностирования, об их проведении и необходимой подготовке. Надежное и качественное оборудование, а также такт и терпение наших сотрудников помогут провести максимально быстрое, безболезненное и эффективное обследование. Все, что требуется от пациента – внимательное и точное следование всем советам и рекомендациям доктора. Вместе мы сможем вернуть здоровье вашего кишечника!
Автор
флеболог, хирург, проктолог
Стаж 15 лет
+7 (495) 032-15-21Проктология: болезни и симптомы | «УРО-ПРО» Екатеринбург
Проктология — это медицинская дисциплина, которая занимается изучением, лечением и профилактикой заболеваний толстого кишечника, анального канала и параректальной области. С 1997 года в России данная специальность была переименована в колопроктологию.
Толстая кишка является конечным отделом пищеварительной системы и имеет протяженность около 1,5-2 метров. Помимо всасывания воды и электролитов, ее функцией является формирование каловых масс и удаление их из организма. Толстая кишка состоит из нескольких отделов: слепая кишка, ободочная (восходящая ободочная, поперечно-ободочная, нисходящая), сигмовидная и прямая. Конечная часть прямой кишки заканчивается анальным каналом, который окружен параректальной клетчаткой. Лечением различных заболеваний толстой и прямой кишки занимаются колопроктологи.
Причины
Основными причинами развития проктологических болезней являются:
- Особенности питания — преобладание в рационе мясных и жирных блюд, употребление большого количества острой пищи, копченостей, мучных изделий, алкоголя и др.
- Склонность к запорам. Она чаще всего развивается из-за недостатка в рационе пищевых волокон, но причиной может быть и нарушение перистальтической функции кишечника.
- Хронические диареи. Могут возникать из-за инфекционных заболеваний, нарушения режима питания, употребления некачественных продуктов, нарушения регуляции деятельности кишечной стенки.
- Малоподвижный образ жизни.
- Беременность и роды. Беременность приводит к повышению давления в брюшной полости, хроническим запорам. В результате расширяются вены геморроидального сплетения, что приводит к развитию геморроя. Роды могут осложниться разрывом мягких тканей и повреждением анального канала вплоть до разрыва сфинктера.
- Врожденные пороки развития — атрезия анального канала (заращение).
- Стрессы.
- Травматические повреждения: анальные трещины, разрывы и др.
Симптомы проктологических болезней
Главными симптомами проктологических болезней являются:
- появление следов алой крови на туалетной бумаге;
- боли в анусе при дефекации или сразу после стула;
- появление шишек синюшного цвета в районе ануса;
- выпадение из заднего прохода геморроидальных узлов при натуживании;
- выделения из заднего прохода (во время дефекации и самостоятельные): слизь, кровь, гной;
- чувство неполного опорожнения, ощущение инородного тела в прямой кишке;
- появление свищей на ягодицах (в области ануса).
Проктологические заболевания серьезно ухудшают качество жизни больных, вызывая не только физический, но и психический дискомфорт. При отсутствии лечения состояние пациента постепенно усугубляется, в процесс могут вовлекаться органы мочеполовой системы или верхние отделы пищеварительного тракта. Нередко проктологические болезни приводят к развитию злокачественных новообразований или гнойно-септических осложнений. Поэтому при наличии патологических симптомов мы рекомендуем не затягивать, а своевременно обращаться к врачу.
Диагностика проктологических заболеваний
Для диагностики заболеваний в проктологии применяются следующие методы:
- Пальцевое ректальное исследование — пальпация анального канала и терминальных отделов прямой кишки.
- Эндоскопические методы исследования — ректороманоскопия, ректосигмоидоскопия, колоноскопия. Эти методы не только позволят визуально осмотреть поверхность кишечника, но и взять биопсию, а при необходимости провести лечебные манипуляции, например, удалить полипы, остановить кровотечение и др.
- Рентгенологическое исследование — ирригоскопия. Позволяет визуализировать новообразования, определить нарушение перистальтики кишечника.
- Лабораторные методы исследования. Анализ кала на скрытую кровь, копрограмма, биопсия новообразований и патологически измененных участков кишки, общий анализ крови и др.
- Компьютерная томография или виртуальная колоноскопия. Это исследование подразумевает прием специальной капсулы, которая по мере прохождения по кишечнику будет делать большое количество снимков слизистой оболочки кишки.
Лечение
Лечение проктологических болезней носит комплексный характер. Ввиду того, что основными причинами их развития является нарушение питания, необходимо придерживаться особой диеты. Пища должна быть богатой пищевыми волокнами, витаминами и микроэлементами – это позволит нормализовать стул и устранить травматическое повреждение слизистой толстой кишки и анального канала.
Из консервативных методов применяются следующие группы препаратов:
- Противовоспалительные средства системного и местного действия (свечи, кремы, мази), антибактериальные препараты.
- Анальгетики системного и местного действия.
- Тромболизирующие препараты, например, на основе гепарина. Используются при тромбозе геморроидальных узлов.
- Кровоостанавливающие средства — гемостатические губки на основе фибриногена или альгината. Они применяются при ректальных кровотечениях на фоне геморроя или неглубоких анальных трещин.
- Трофические средства. Они обеспечивают скорейшее заживление повреждений.
В ряде случаев консервативные методы не оказывают достаточной эффективности или приводят только ко временному эффекту, тогда возникают показания к малоинвазивным манипуляциям. Современная проктология обладает большим количеством амбулаторных методик, которые позволяют провести лечение в одно посещение врача. Например, при лечении геморроя используется лигирование латексными кольцами, при удалении перианальных папиллом или бахромок применяются радиоволновые методы.
Как и в любом разделе медицины, в проктологии существует правило — чем раньше обнаружена проблема, тем проще с нею справиться. Если на ранних этапах можно обойтись консервативными или малоинвазивными методами лечения, то при запущенных случаях нередко требуются полноценные проктологические операции в условиях стационара.
В этой связи мы рекомендуем не откладывать визит к врачу при наличии проблемы. Наши специалисты понимают, что многие пациенты испытывают чувство стыда и неловкости на приеме у проктолога, поэтому приложат все усилия, чтобы лечение прошло максимально эффективно, быстро и с минимальным дискомфортом.
Воспалительное заболевание кишечника: симптомы, лечение и диагностика
Обзор
Что такое воспалительное заболевание кишечника (ВЗК)?
Воспалительное заболевание кишечника (ВЗК) – это группа заболеваний, вызывающих хроническое воспаление (боль и отек) в кишечнике. ВЗК включает болезнь Крона и язвенный колит.Оба типа влияют на пищеварительную систему. Лечение может помочь справиться с этим заболеванием на протяжении всей жизни.
Насколько распространено ВЗК?
До трех миллионов американцев страдают той или иной формой ВЗК. Заболевание поражает людей всех возрастов и полов. ВЗК чаще всего возникает в возрасте от 15 до 30 лет.
Какие бывают типы ВЗК?
Болезнь Крона и язвенный колит являются основными типами ВЗК. Типы включают:
- Болезнь Крона вызывает боль и опухоль в пищеварительном тракте.Это может повлиять на любую часть от рта до ануса. Чаще всего поражается тонкий кишечник и верхняя часть толстого кишечника.
- Язвенный колит вызывает отек и язвы (язвы) в толстой кишке (ободочной и прямой кишке).
- Микроскопический колит вызывает воспаление кишечника, которое можно обнаружить только под микроскопом.
В чем разница между воспалительным заболеванием кишечника (ВЗК) и синдромом раздраженного кишечника (СРК)?
ВЗК – болезнь; СРК – это синдром или группа симптомов.Причины и методы лечения разные.
СРК – это разновидность функционального желудочно-кишечного заболевания. Это влияет на работу кишечника, заставляя его сокращаться чаще (а иногда реже), чем обычно. СРК также известен как спастическая толстая кишка или нервный желудок.
IBS не вызывает воспаление и не повреждает кишечник, как ВЗК, поэтому визуализация не может его обнаружить и не увеличивает риск рака толстой кишки. Людям с СРК редко требуется госпитализация или хирургическое вмешательство.
Можно ли болеть ВЗК и СРК?
Да, возможно наличие как IBD, так и IBS.Хотя ВЗК может вызывать симптомы СРК, нет никаких доказательств того, что наличие СРК увеличивает риск ВЗК.
Симптомы и причины
Что вызывает ВЗК?
Исследователи все еще пытаются определить, почему у некоторых людей развивается ВЗК. Три фактора, по-видимому, играют роль:
- Генетика: Каждый четвертый человек с ВЗК имеет семейный анамнез этого заболевания.
- Ответ иммунной системы: Иммунная система обычно борется с инфекциями. У людей с ВЗК иммунная система принимает пищу за чужеродные вещества. Он высвобождает антитела (белки) для борьбы с этой угрозой, вызывая симптомы ВЗК.
- Триггеры окружающей среды: Люди с семейным анамнезом ВЗК могут заболеть этим заболеванием после воздействия триггера окружающей среды. Эти триггеры включают курение, стресс, прием лекарств и депрессию.
Каковы симптомы ВЗК?
Симптомы ВЗК могут приходить и уходить.Они могут быть легкими или тяжелыми, появляться внезапно или постепенно. Периоды симптомов ВЗК – это вспышки ВЗК. Когда у вас нет симптомов, у вас ремиссия.
Симптомы ВЗК включают:
Редко ВЗК может также вызывать:
Каковы осложнения воспалительного заболевания кишечника (ВЗК)?
Люди с ВЗК имеют более высокий риск развития рака толстой кишки (колоректального). Другие возможные осложнения включают:
- Анальный свищ (туннель, образующийся под кожей, соединяющий инфицированную анальную железу и задний проход).
- Стеноз или стриктура заднего прохода (сужение анального канала, где стул выходит из тела).
- Анемия (низкий уровень эритроцитов) или сгустки крови.
- Камни в почках.
- Заболевания печени, такие как цирроз и первичный склерозирующий холангит (воспаление желчных протоков).
- Нарушение всасывания и недостаточность питания (неспособность получать достаточное количество питательных веществ через тонкий кишечник).
- Остеопороз.
- Перфорированная кишка (отверстие или разрыв в толстой кишке).
- Токсичный мегаколон (сильное вздутие кишечника).
Диагностика и тесты
Как диагностируется ВЗК?
Болезнь Крона и язвенный колит вызывают аналогичные симптомы. Ни один тест не может диагностировать ни одно из состояний.
Чтобы поставить диагноз, ваш лечащий врач спросит о ваших симптомах.Обследование может начаться с общего анализа крови (CBC) и анализа стула для выявления признаков воспаления кишечника.
Вы также можете пройти один или несколько из следующих диагностических тестов:
- Колоноскопия для исследования толстого и тонкого кишечника.
- EUS (эндоскопическое УЗИ) для проверки пищеварительного тракта на наличие отеков и язв.
- Гибкая ректороманоскопия для исследования внутренней части прямой кишки и заднего прохода.
- Визуальное сканирование , такое как компьютерная томография или МРТ, для проверки признаков воспаления или абсцесса.
- Верхняя эндоскопия для исследования пищеварительного тракта от рта до начала тонкой кишки.
- Капсульная эндоскопия с помощью небольшой камеры, которую вы проглатываете. Камера делает снимки во время прохождения через пищеварительный тракт.
Ведение и лечение
Что такое нехирургическое лечение воспалительного заболевания кишечника (ВЗК)?
Лечение ВЗК варьируется в зависимости от конкретного типа и симптомов.Лекарства могут помочь контролировать воспаление, чтобы у вас не было симптомов (ремиссии). Лекарства для лечения ВЗК включают:
- Аминосалицилаты (противовоспалительное средство, такое как сульфасалазин, месаламин или бальсалазид) минимизируют раздражение кишечника.
- Антибиотики лечат инфекции и абсцессы.
- Biologics прерывают сигналы иммунной системы, вызывающие воспаление.
- Кортикостероиды , такие как преднизон, контролируют иммунную систему и управляют обострениями.
- Иммуномодуляторы успокаивают сверхактивную иммунную систему.
Вы также можете воспользоваться этими безрецептурными препаратами для лечения ВЗК:
Какие хирургические методы лечения болезни Крона?
Примерно 7 из 10 человек с болезнью Крона в конечном итоге нуждаются в хирургическом вмешательстве, когда лекарства больше не облегчают симптомы. Во время резекции кишечника хирург:
- Удаляет пораженный сегмент кишечника.
- Соединяет два конца здорового кишечника вместе (анастомоз).
После операции оставшаяся часть кишечника адаптируется и функционирует так же, как и раньше. Примерно у 6 из 10 человек, перенесших операцию по поводу болезни Крона, в течение 10 лет будет рецидив. Вам может подойти еще одна резекция кишечника.
Какие хирургические методы лечения язвенного колита?
После 30 с лишним лет жизни с язвенным колитом примерно 1 из 3 человек нуждается в операции.
Хирург:
- Удаляет толстую кишку (колэктомия) или толстую и прямую кишку (проктоколэктомия).
- Соединяет тонкий кишечник и задний проход.
- Создает мешочек подвздошной кишки, в который собирается кал, который затем выходит через задний проход.
В редких случаях может потребоваться илеостомия вместо подвздошной сумки. Мешок для илеостомии прикрепляется за пределами живота для сбора стула.
Проктоколэктомия является лечебной. Симптомы не вернутся после операции по удалению толстой и прямой кишки. Однако у вас могут возникнуть проблемы с илеостомией или подвздошной кишкой, например, поучит (воспаление и инфекция).
Профилактика
Как предотвратить воспалительное заболевание кишечника (ВЗК)?
Хотя нет ничего, что можно сделать для предотвращения ВЗК, определенные изменения в питании и образе жизни могут контролировать симптомы. Вы можете:
- Ешьте небольшими порциями каждые два-четыре часа.
- Найдите здоровые способы справиться со стрессом, такие как медитация, движения, такие как тай-чи, прослушивание музыки или прогулка.
- Высыпайтесь и оставайтесь физически активными.
- Вести дневник питания, чтобы определять продукты, вызывающие вспышки ВЗК. Вы можете столкнуться с пищевой непереносимостью, например непереносимостью лактозы. Если это так, вашему организму труднее переваривать определенные продукты, что вызывает расстройство желудка.
- Сократите количество продуктов, раздражающих кишечник, например, волокнистых, острых, жирных или приготовленных с молоком.Во время обострения выбирайте мягкую безвкусную пищу, которая не вызывает воспаления.
- Сократите употребление кофеиновых, газированных и алкогольных напитков. Пейте больше воды, чтобы предотвратить обезвоживание.
- Бросить курить.
Перспективы / Прогноз
Каков прогноз (перспективы) для людей с воспалительным заболеванием кишечника (ВЗК)?
IBD – это пожизненное заболевание, но оно не должно сокращать продолжительность вашей жизни.При правильном лечении вы можете предотвратить обострения и добиться длительных периодов ремиссии.
Управлять таким пожизненным заболеванием, как ВЗК, может быть непросто. Для людей с ВЗК нет ничего необычного в том, чтобы впадать в тревогу или депрессию. Посещение консультанта по психическому здоровью может помочь.
Жить с
Когда мне следует позвонить своему врачу?
Вы должны позвонить своему врачу, если у вас возникли проблемы:
- Избыточное похудание.
- Сильная боль в животе или диарея.
- Повышенная температура или признаки инфекции.
- IBD под отбортовку.
- Признаки обезвоживания.
Какие вопросы я должен задать своему врачу?
Вы можете спросить своего врача:
- Какой у меня тип ВЗК?
- Какое лечение для меня лучше всего?
- Каких продуктов или напитков мне следует избегать?
- Какие изменения в образе жизни мне следует сделать?
- Могу ли я столкнуться с другими проблемами?
- Стоит ли обращать внимание на признаки осложнений?
Записка из клиники Кливленда
Большинство людей с воспалительным заболеванием кишечника (ВЗК) ведут активный образ жизни.Тем не менее, симптомы болезни Крона и язвенного колита могут разрушить жизнь. У некоторых людей наступает ремиссия (без симптомов) после приема лекарств. Некоторым людям требуется операция, чтобы справиться с серьезными обострениями симптомов. Ваш лечащий врач может посоветовать изменения в питании и образе жизни для лечения ВЗК.
Воспалительное заболевание кишечника (ВЗК): симптомы, причины, лечение
Обзор воспалительного заболевания кишечника
Термин воспалительное заболевание кишечника (ВЗК) описывает группу заболеваний, при которых кишечник воспаляется.Его часто считают аутоиммунным заболеванием, но исследования показывают, что хроническое воспаление не может быть вызвано атакой иммунной системы на сам организм. Напротив, это результат того, что иммунная система атакует безвредный вирус, бактерии или пищу в кишечнике, вызывая воспаление, которое приводит к повреждению кишечника.
Двумя основными типами ВЗК являются язвенный колит и болезнь Крона. Язвенный колит ограничен толстой или толстой кишкой. С другой стороны, болезнь Крона может поражать любую часть желудочно-кишечного тракта от рта до заднего прохода.Однако чаще всего это поражает последнюю часть тонкой кишки или толстую кишку, или и то, и другое.
Если у вас ВЗК, вы знаете, что он обычно проходит через курс депиляции и убыли. Когда есть сильное воспаление, болезнь считается активной, и у человека наблюдается обострение симптомов. Когда воспаление слабое или отсутствует, у человека обычно отсутствуют симптомы и болезнь находится в стадии ремиссии.
Что вызывает воспалительное заболевание кишечника?
ВЗК – заболевание с неизвестной причиной.Некоторый агент или комбинация агентов – бактерии, вирусы, антигены – запускают иммунную систему организма, чтобы вызвать воспалительную реакцию в кишечном тракте. Недавние исследования показывают, что некоторая комбинация наследственных, генетических и / или экологических факторов может вызвать развитие ВЗК. Также может быть, что собственная ткань тела вызывает аутоиммунный ответ. Что бы ни было причиной, реакция продолжается бесконтрольно и повреждает стенку кишечника, что приводит к диарее и болям в животе.
Каковы симптомы воспалительного заболевания кишечника?
Как и в случае с другими хроническими заболеваниями, у человека с ВЗК обычно бывают периоды, когда болезнь обостряется и вызывает симптомы, за которыми следуют периоды, когда симптомы уменьшаются или исчезают, и хорошее здоровье возвращается.Симптомы варьируются от легких до тяжелых и обычно зависят от того, какая часть кишечного тракта поражена. Они включают:
Есть ли осложнения, связанные с ВЗК?
ВЗК может привести к нескольким серьезным осложнениям в кишечнике, включая:
- Обильное кишечное кровотечение из язв
- Перфорация или разрыв кишечника
- Сужение, называемое стриктурой, и непроходимость кишечника; обнаружен в свищах Крона
- (аномальные ходы) и перианальном заболевании, заболевании тканей вокруг заднего прохода; эти состояния чаще встречаются при болезни Крона, чем при язвенном колите.
- Токсичный мегаколон, представляющий собой крайнее расширение толстой кишки, опасное для жизни; это больше связано с язвенным колитом, чем с болезнью Крона.
- Недоедание
ВЗК, особенно язвенный колит, также увеличивает риск рака толстой кишки. ВЗК также может поражать другие органы; например, у человека с ВЗК может быть артрит, кожные заболевания, воспаление глаз, заболевания печени и почек или потеря костной массы. Из всех осложнений вне кишечника наиболее распространенным является артрит.Осложнения со стороны суставов, глаз и кожи часто возникают вместе.
Как диагностируется ВЗК?
Ваш врач ставит диагноз воспалительного заболевания кишечника на основании ваших симптомов и различных обследований и тестов:
- Исследование стула. Вам будет предложено сдать образец стула, который будет отправлен в лабораторию, чтобы исключить возможность бактериальной, вирусной или паразитарной причины диареи. Кроме того, стул будет исследован на наличие следов крови, которые не видны невооруженным глазом.
- Общий анализ крови. Медсестра или лаборант возьмут кровь, которая затем будет проверена в лаборатории. Увеличение количества лейкоцитов предполагает наличие воспаления. А если у вас сильное кровотечение, количество эритроцитов и уровень гемоглобина могут снизиться.
- Другие анализы крови. Электролиты (натрий, калий), белок и маркеры воспаления, такие как скорость оседания эритроцитов (СОЭ) и С-реактивный белок (СРБ), могут быть использованы для оценки тяжести заболевания.Уровни перинуклеарных антинейтрофильных цитоплазматических антител (pANCA) могут повышаться при язвенном колите. Кроме того, могут быть сделаны специальные тесты на заболевания, передающиеся половым путем.
- Бариевый рентгеновский снимок. Хотя он используется редко, он позволяет проверить верхние отделы желудочно-кишечного тракта – пищевод, желудок и тонкий кишечник – на предмет аномалий, вызванных болезнью Крона. Вы проглатываете мелово-белый раствор, который покрывает кишечный тракт, поэтому он будет виден на рентгеновских снимках. Если для проверки нижних отделов желудочно-кишечного тракта используется исследование с барием, вам сделают клизму, содержащую барий, и попросят подержать ее, пока делается рентгеновский снимок прямой и толстой кишки.На этих рентгеновских снимках могут обнаруживаться аномалии, вызванные болезнью Крона или язвенным колитом.
- Другие радиологические исследования. Компьютерная томография (компьютерная томография), магнитно-резонансная томография (МРТ) и ультразвук также использовались для диагностики болезни Крона и язвенного колита.
- Ригмоидоскопия. В этой процедуре врач использует сигмоидоскоп, узкую гибкую трубку с камерой и светом, чтобы визуально осмотреть последнюю треть толстой кишки, которая включает прямую и сигмовидную кишки.Сигмоидоскоп вводится через задний проход, и стенка кишечника визуально исследуется на наличие язв, воспалений и кровотечений. Врач также может взять образцы – биопсию – слизистой оболочки кишечника с помощью инструмента, вставленного через трубку. Затем они будут исследованы в лаборатории под микроскопом.
- Колоноскопия. Колоноскопия похожа на ректороманоскопию, за исключением того, что врач будет использовать колоноскоп, более длинную гибкую трубку, чтобы исследовать всю толстую кишку. Эта процедура позволяет оценить степень заболевания толстой кишки.
- Верхняя эндоскопия. Если у вас есть симптомы со стороны верхних отделов желудочно-кишечного тракта, такие как тошнота и рвота, врач будет использовать эндоскоп, узкую гибкую трубку с камерой и светом, которую вводят через рот, чтобы исследовать пищевод, желудок и двенадцатиперстную кишку, которые это первая часть вашего тонкого кишечника. Язвы в желудке и двенадцатиперстной кишке возникают примерно у одного из 10 человек с болезнью Крона.
- Капсульная эндоскопия. Этот тест может быть полезен для диагностики заболевания тонкого кишечника, например, болезни Крона.Вы проглатываете небольшую капсулу с фотоаппаратом. Снимки пищевода, желудка и тонкой кишки отправляются на приемник, который вы носите на поясе. По окончании процедуры снимки загружаются из приемника в компьютер. Камера проходит через ваше тело в унитаз.
Как лечится воспалительное заболевание кишечника?
Лечение ВЗК включает сочетание ухода за собой и медицинского лечения.
Продолжение
Самопомощь
Хотя не было показано, какая диета предотвращает или лечит ВЗК, изменения в диете могут быть полезны в управлении вашими симптомами.Важно обсудить с врачом способы изменить свой рацион и при этом убедиться, что вы получаете необходимые питательные вещества. Например, в зависимости от ваших симптомов врач может посоветовать вам уменьшить количество потребляемой клетчатки или молочных продуктов. Кроме того, лучше переносятся частые и небольшие приемы пищи. В общем, нет необходимости избегать определенных продуктов, если они не вызывают или не усугубляют ваши симптомы.
Одно из диетических вмешательств, которое может порекомендовать ваш врач, – это диета с низким содержанием остатков, очень ограниченная диета, которая снижает количество клетчатки и других непереваренных материалов, которые проходят через толстую кишку.Это поможет облегчить симптомы диареи и боли в животе. Если вы все же придерживаетесь диеты с низким содержанием остатков, убедитесь, что вы понимаете, как долго вам следует придерживаться этой диеты, потому что диета с низким содержанием остатков не обеспечивает всех необходимых вам питательных веществ. Ваш врач может порекомендовать вам принимать витаминные добавки.
Продолжение
Еще один важный аспект ухода за собой – научиться справляться со стрессом, который может ухудшить ваши симптомы. Одна вещь, которую вы можете сделать, – это составить список вещей, которые вызывают у вас стресс, а затем подумать, какие из них вы можете исключить из своей повседневной жизни.Кроме того, когда вы чувствуете приближение стресса, можно сделать несколько глубоких вдохов и медленно их выдохнуть. Обучение медитации, выделение времени для себя и регулярные упражнения – все это важные инструменты для снижения уровня стресса в вашей жизни.
Участие в группе поддержки дает вам возможность познакомиться с другими людьми, которые точно знают, какое влияние ВЗК оказывает на вашу повседневную жизнь, потому что они проходят через то же самое, что и вы. Они могут предложить поддержку и советы о том, как бороться с симптомами и их влиянием на вас.
Лечение
Цель лечения – подавить патологическую воспалительную реакцию, чтобы кишечная ткань могла зажить. При этом должны уменьшиться симптомы диареи и боли в животе. Как только симптомы будут под контролем, лечение будет сосредоточено на уменьшении частоты обострений и поддержании ремиссии.
Продолжение
Врачи часто применяют поэтапный подход к применению лекарств при воспалительных заболеваниях кишечника.При таком подходе в первую очередь используются наименее вредные лекарства или лекарства, которые принимаются только в течение короткого периода времени. Если они не приносят облегчения, используются препараты более высокой ступени.
Лечение обычно начинается с аминосалицилатов, которые представляют собой аспириноподобные противовоспалительные препараты, такие как бальсалазид (колазал), месаламин (Asacol, Apriso, Lialda, Pentasa), олсалазин (Dipentum) и сульфасалазин (азульфидин). Месаламин можно принимать перорально или вводить в виде ректальных суппозиториев или клизм для лечения язвенного колита.Поскольку они обладают противовоспалительным действием, они эффективны как для облегчения симптомов обострения, так и для поддержания ремиссии. Врач также может назначить противодиарейные средства, спазмолитики и подавители кислоты для облегчения симптомов. Не следует принимать противодиарейные средства без консультации врача.
Если у вас болезнь Крона, особенно если она сопровождается осложнением, например перианальной болезнью (поражение тканей вокруг ануса), врач может назначить антибиотик, который следует принимать вместе с другими лекарствами.Реже антибиотики используются при язвенном колите.
Продолжение
Если первые лекарства не принесут должного облегчения, врач, скорее всего, пропишет кортикостероид, который является быстродействующим противовоспалительным средством. Кортикостероиды, как правило, обеспечивают быстрое облегчение симптомов наряду со значительным уменьшением воспаления. Однако из-за побочных эффектов, связанных с их длительным применением, кортикостероиды используются только для лечения обострений и не используются для поддержания ремиссии.
Иммуномодифицирующие агенты – это следующие препараты, которые следует использовать, если кортикостероиды неэффективны или требуются в течение длительного периода времени. Эти лекарства не используются при обострениях болезни, потому что на принятие мер может уйти от 2 до 3 месяцев. Эти лекарства нацелены на иммунную систему, которая высвобождает вызывающие воспаление химические вещества в стенках кишечника. Примерами наиболее распространенных иммунодепрессантов являются азатиоприн (имуран), метотрексат (ревматрекс) и 6-меркаптопурин или 6-МП (пуринетол).
Биологические препараты – это антитела, которые нацелены на действие некоторых других белков, вызывающих воспаление. Инфликсимаб (Remicade) и инфликсимаб-abda (Renflexis) или инфликсимаб-dyyb (Inflectra), биоподобный Remicade, являются лекарствами, одобренными FDA для лечения умеренной и тяжелой болезни Крона, когда стандартные лекарства были неэффективны. Они принадлежат к классу препаратов, известных как агенты против TNF. TNF (фактор некроза опухоли) продуцируется лейкоцитами и, как полагают, отвечает за повреждение тканей, которое происходит при болезни Крона.Другими анти-TNF агентами, одобренными для лечения болезни Крона, являются адалимумаб (Хумира), адалимумаб-атто (Амджевита), биоподобный Хумире, и цертолизумаб (Цимзия). Альтернативой анти-TNF лечению болезни Крона являются биопрепараты, нацеленные на интегрин, два из которых – натализумаб (Tysabri) и ведолизумаб (Entyvio). Другой препарат, устекинумаб (Стелара), блокирует IL-12 и IL-23.
Продолжение
Адалимумаб (Хумира), адалимумаб-атто (Амджевита), цертолизумаб (Симзия), голимумаб (Симпони, Симпони Ария), Инфликсимаб (Ремикейд), инфликсимаб-абда (Ренфлексимаб) и -флексимаб (ренфлексимаб) и некоторые из препаратов против TNF, которые в настоящее время одобрены FDA для лечения язвенного колита.
Если вы не отвечаете на препараты, рекомендованные для лечения ВЗК, поговорите со своим врачом о регистрации в клиническом исследовании. Клинические испытания – это способ тестирования новых методов лечения болезни, чтобы увидеть, насколько они эффективны и как пациенты на них реагируют. Вы можете узнать о клинических испытаниях на веб-сайте Американского фонда Крона и колита.
Применялась ли когда-либо хирургия для лечения воспалительного заболевания кишечника?
Хирургическое лечение ВЗК зависит от заболевания.Например, язвенный колит можно вылечить хирургическим путем, потому что болезнь ограничивается толстой кишкой. После удаления толстой кишки болезнь больше не возвращается. Однако хирургическое вмешательство не вылечит болезнь Крона, хотя некоторые операции могут быть применены. Чрезмерное хирургическое вмешательство у людей с болезнью Крона на самом деле может привести к большему количеству проблем.
Людям с язвенным колитом доступно несколько хирургических вмешательств. Какой из них вам подходит, зависит от нескольких факторов:
- Степень вашего заболевания
- Ваш возраст
- Ваше общее состояние здоровья
Продолжение
Первый вариант называется проктоколэктомией.Он включает удаление всей толстой и прямой кишки. Затем хирург делает отверстие в брюшной полости, называемое илеостомией, которое входит в часть тонкой кишки. Это отверстие обеспечивает новый путь для выхода фекалий в мешочек, который прикрепляется к коже с помощью клея.
Другая часто используемая операция называется подвздошно-анастомозом. Хирург удаляет толстую кишку, а затем создает внутренний мешок, который соединяет тонкий кишечник с анальным каналом. Это позволяет фекалиям выходить через задний проход.
Несмотря на то, что операция не вылечит болезнь Крона, примерно 50% людей с болезнью Крона в какой-то момент нуждаются в операции. Если у вас болезнь Крона и вам требуется операция, ваш врач обсудит с вами возможные варианты. Убедитесь, что вы задаете вопросы и понимаете цель или задачи операции, ее риски и преимущества, а также то, что может случиться, если вам не сделают операцию.
Симптомы ВЗК будут появляться и исчезать в течение многих лет. Это не значит, что они контролируют вас; Управление вашим состоянием с помощью вашего поставщика медицинских услуг – лучший способ оставаться максимально здоровым в долгосрочной перспективе.
Воспалительное заболевание кишечника – NHS
Воспалительное заболевание кишечника (ВЗК) – это термин, который в основном используется для описания двух состояний: язвенного колита и болезни Крона.
Язвенный колит и болезнь Крона – это хронические заболевания, которые включают воспаление кишечника.
Язвенный колит поражает только толстую кишку. Болезнь Крона может поражать любую часть пищеварительной системы, от рта до ануса.
Люди любого возраста могут заболеть ВЗК, но обычно это диагностируется в возрасте от 15 до 40 лет.
Информация:Консультации по коронавирусу
Получите консультацию о коронавирусе и ИБК:
Симптомы ВЗК
Симптомы ВЗК включают:
- боль, спазмы или опухоль в животе
- повторяющаяся или кровавая диарея
- потеря веса
- крайняя усталость
Не у всех есть все эти симптомы, а у некоторых людей могут быть дополнительные симптомы , включая высокую температуру, тошноту (рвоту) и анемию.
Артрит, болезненные красные глаза (увеит), болезненные красные шишки на коже (узловатая эритема) и желтуха (первичный склерозирующий холангит) реже связаны с ВЗК.
Симптомы ВЗК могут появляться и исчезать. Могут быть случаи, когда симптомы тяжелые (обострение), за которыми следуют длительные периоды, когда симптомов мало или совсем нет (ремиссия).
Подробнее о симптомах язвенного колита и симптомах болезни Крона.
Лечение IBD
В настоящее время нет лекарства от язвенного колита или болезни Крона.
Если у вас язвенный колит легкой степени, вам может потребоваться минимальное лечение или его полное отсутствие, и вы будете оставаться здоровыми в течение продолжительных периодов времени.
Лечение направлено на облегчение симптомов и предотвращение их повторного появления и включает определенные диеты, изменение образа жизни, лекарства и хирургическое вмешательство.
Лекарства, используемые для лечения язвенного колита или болезни Крона, включают:
По оценкам, каждый пятый человек с язвенным колитом имеет тяжелые симптомы, которые не улучшаются с помощью лекарств. В этих случаях может потребоваться операция по удалению воспаленного участка толстой кишки (толстой кишки).
Примерно от 60 до 75% людей с болезнью Крона потребуется хирургическое вмешательство для восстановления повреждений пищеварительной системы и лечения осложнений, вызванных болезнью Крона.
Люди с язвенным колитом или болезнью Крона также подвержены повышенному риску заболевания раком кишечника. Ваш врач порекомендует вам регулярно проходить обследование кишечника (эндоскопию) для выявления рака.
Причины ВЗК
Неясно, что вызывает ВЗК, но считается, что это вызвано комбинацией факторов, включая:
- генетика – у вас больше шансов заболеть ВЗК, если у вас есть близкий родственник с заболеванием
- проблема с вашим иммунитетом system
У курящих в два раза больше шансов заболеть болезнью Крона, чем у некурящих.
Справка и поддержка
Благотворительная организация Crohn’s and Colitis UK оказывает помощь и поддержку людям с ВЗК.
Позвоните по телефону доверия 0300 222 5700 с понедельника по пятницу с 10 до 17 часов. Или вы можете использовать онлайн-форму для связи.
IBS Network – еще одна британская благотворительная организация, у которой есть полезная информация о группах поддержки.
Синдром раздраженного кишечника (СРК)
ВЗК – это не то же самое, что синдром раздраженного кишечника (СРК), который является распространенным заболеванием, вызывающим такие симптомы, как:
Последняя проверка страницы: 15 апреля 2020 г.
Срок следующей проверки: 15 апреля 2023 г.
Заболевания и лечение толстой кишки
Толстая кишка, также известная как толстая кишка или толстая кишка, начинается в области чуть ниже правой талии и продолжается от тонкой кишки до брюшной полости.Основная функция толстой кишки – поглощать воду из оставшейся неудобоваримой пищи и выводить ненужные отходы из организма.
Многие заболевания могут поражать толстую или толстую кишку, в том числе:
Признаки и симптомы заболеваний толстой кишки
Типы симптомов, которые могут возникать при заболевании толстой кишки, зависят от того, какая часть толстой кишки поражена. Эти симптомы могут варьироваться от легких до тяжелых, а также приходить и уходить с периодами обострений.Кроме того, проблемы с кишечником могут сопровождать другие симптомы, которые могут различаться в зависимости от основного заболевания, расстройства или состояния.
Некоторые из наиболее распространенных симптомов заболеваний толстой кишки включают:
- Боль в животе
- Вздутие, вздутие или вздутие живота
- Стул с кровью (кровь может быть красной, черной или дегтеобразной по текстуре)
- Запор
- Диарея
- Усталость
- Лихорадка и озноб
- Газ
- Неспособность испражняться или отводить газы
- Тошнота с рвотой или без нее
При заболевании толстой кишки могут присутствовать другие симптомы, которые могут повлиять на общее состояние здоровья и самочувствие пациента, например:
- Беспокойство
- Депрессия
- Потеря аппетита
- Недоедание
- Состояние кожи и волос
- Необъяснимая потеря веса
- Слабость (упадок сил)
Диагностика заболеваний толстой кишки
Для того, чтобы определить, какой тип расстройства толстой кишки у пациента или степень тяжести заболевания, ваш врач сначала соберет полную историю болезни и проведет физическое обследование.Диагностические тесты также могут использоваться для помощи в разработке плана лечения вашего состояния и могут включать:
- Бариевая клизма. Также известна как серия с более низким GI; в толстую кишку вводится раствор бария и делается рентген.
- Бариевая ласточка. Также известна как серия верхнего GI; раствор бария используется для покрытия внутренней оболочки пищевода, желудка и первой части тонкой кишки, а также проводятся рентгеновские снимки.
- Анализы крови
- Дыхательные пробы с лактозой. безопасный, простой и неинвазивный метод оценки абсорбции. В тесте используется питательное вещество, содержащее радиоактивный материал, который измеряется в выдыхаемом воздухе.
Колоноскопия: Тонкая гибкая трубка, называемая колоноскопом, используется для исследования внутренней оболочки толстой кишки. Этот тест помогает обнаружить язвы, полипы толстой кишки, опухоли, а также области воспаления или кровотечения. Могут быть взяты образцы тканей (биопсия) и удалены аномальные новообразования. Этот тест также можно использовать в качестве скринингового теста на рак или предраковые образования (полипы) в толстой или прямой кишке.
Малоинвазивное тестирование. Для постановки диагноза доступны анализы крови. Иммунохимический тест кала (FIT) – это новая версия анализа кала на скрытую кровь (FOBT), который обнаруживает мельчайшие следы крови в стуле.
- Капсульная эндоскопия может быть выполнена для обеспечения улучшенного обзора нижних отделов пищеварительного тракта, который может быть не виден при традиционной колоноскопии.
- Ригмоидоскопия: Процедура, используемая для осмотра внутренней части прямой кишки и области толстой кишки, ближайшей к прямой кишке.
- Визуальные тесты . Рентген, компьютерная томография (КТ), МРТ, ПЭТ ,00
- МРТ
- Радионуклеотидная визуализация: обычно используется при дивертикулите и при обнаружении желудочно-кишечного кровотечения. В вену вводят радиоактивное вещество. При кишечном кровотечении радиоактивное вещество вместе с кровью попадет в кишечник.
- Ультразвук: Хорошо для обнаружения опухолей толстой кишки.
Лечение заболеваний толстой кишки
В некоторых случаях ваш врач может предложить несколько простых мер, чтобы определить, исчезнут ли ваши симптомы, например:
- Не курить
- Избегайте продуктов, вызывающих симптомы
- Упражнение
- Увеличение количества пищевых волокон
- Поддержание здорового веса
- Лекарства (т. Е. Лекарства, отпускаемые без рецепта или по рецепту)
Некоторые состояния, такие как инфекция C. difficile , будут лечиться в сотрудничестве с другими клиницистами Summa, включая наших колоректальных хирургов и специалистов по инфекционным заболеваниям.
В качестве расширенной лечебной меры ваш специалист может порекомендовать операцию. Хирурги Summa проводят множество операций на толстой кишке, в том числе:
Чтобы записаться на прием к врачу Summa для обсуждения лечения вашего желудочно-кишечного заболевания, щелкните или позвоните по телефону 330.761.1111.
Болезнь Крона | Сидарс-Синай
Не то, что вы ищете?Что такое болезнь Крона?
Болезнь Крона возникает при покраснении, отеке (воспалении) и язвах. вдоль пищеварительного тракта.Это часть группы заболеваний, известных как воспалительные заболевание кишечника или ВЗК.
Болезнь Крона – длительное хроническое заболевание, которое может приходить и уходить в разные раз в твоей жизни. В большинстве случаев поражается тонкий кишечник, чаще всего нижний. часть называется подвздошная кишка. В некоторых случаях поражается как тонкий, так и толстый кишечник.
Иногда воспаление может распространяться по всему пищеварительному тракту.Это включает в себя ваш рот, ваш пищевод (пищевод), ваш желудок, первая часть вашего маленького кишечник или двенадцатиперстная кишка, аппендикс и задний проход.
Что вызывает болезнь Крона?
Эксперты не знают, что вызывает болезнь Крона. Возможно, вирус или бактерия влияет на систему борьбы с инфекциями организма (иммунную систему). Иммунная система может создают в стенке кишечника ненормальную воспалительную реакцию, которая не прекращается.
Многие люди с болезнью Крона имеют ненормальную иммунную систему. Но эксперты не знают, проблемы с иммунитетом вызывают болезнь. Они также не знают, может ли болезнь Крона вызывать иммунные проблемы. Стресс не вызывает болезни Крона.
Кто подвержен риску болезни Крона болезнь?
Болезнь Крона может возникнуть в любом возрасте.Чаще всего он поражает людей в возрасте от 15 до 35 лет. Это также может произойти у детей или пожилых людей. Он одинаково влияет на мужчин и женщин.
Вы могут подвергаться большему риску развития болезни Крона, если вы:
- Есть семейный анамнез болезни Крона, например, ваш отец, мать, брат, сестра или ребенок
- Имеют восточноевропейское происхождение, особенно евреи европейского происхождения
- Белые
- Жить в развитой стране, в городе или в северном климате
- Дым
Каковы симптомы болезни Крона?
Симптомы у каждого человека могут отличаться.Симптомы могут включать:
- Боль в животе или животе, часто в правом нижнем углу
- Понос, иногда с кровью
- Ректальное кровотечение
- Похудание
- Лихорадка
- Боль в суставах
- Тошнота или рвота
- Порез или разрыв заднего прохода (трещина заднего прохода)
- Сыпь
Симптомы могут отсутствовать долгое время, даже годы.Это называется ремиссией. Невозможно узнать, когда может наступить ремиссия или когда симптомы вернутся.
Симптомы болезни Крона могут быть похожи на другие проблемы со здоровьем. Всегда вижу свой поставщик медицинских услуг, чтобы быть уверенным.
Как диагностируется болезнь Крона?
Вас могут проверить на наличие признаков болезни Крона, если у вас было длительное или хроническое заболевание:
- Боль в животе или животе
- Диарея
- Лихорадка
- Похудание
- Анемия, потеря здоровых эритроцитов, из-за которой вы чувствуете усталость
Ваш лечащий врач изучит ваше прошлое здоровье и проведет медицинский осмотр.
Другие тесты на болезнь Крона могут включать следующее:
- Кровь тесты. Это делается, чтобы увидеть, меньше ли у вас здоровых эритроцитов. (анемия) из-за потери крови. Эти тесты также проверяют, есть ли у вас более высокий количество лейкоцитов. Это может означать, что у вас воспалительная проблема.
- Табурет культура. Это делается для того, чтобы увидеть, есть ли в вашем пищеварительный тракт, который может вызвать диарею или другие проблемы. Небольшой образец вашего кал собирают и отправляют в лабораторию. Через 2 или 3 дня тест покажет, есть ли у вас аномальные бактерии или если вы потеряли кровь. Он также покажет, заражена ли а паразиты или бактерии вызывают ваши симптомы.
- Другие тесты стула. Помимо табурета посев, другие анализы образцов кала, такие как калпротектин или лактоферрин, могут быть сделать, чтобы увидеть, есть ли воспаление в кишечнике.
- Верхний эндоскопия (ФГДС). Этот тест исследует внутреннюю часть вашей пищевой трубки или пищевод, желудок и верхняя часть тонкой кишки, называемая двенадцатиперстной кишкой. В этом тесте используется тонкая трубка с подсветкой, называемая эндоскопом.В трубке есть камера на один конец. Пока вы находитесь под действием седативного препарата, трубку вводят вам в рот и горло. Тогда это идет в пищевод, желудок и двенадцатиперстную кишку. Ваш лечащий врач может увидеть внутри этих органов. Они также могут взять небольшой образец ткани или биопсию, если: нужный.
- Колоноскопия. Этот тест исследует толстую кишку по всей длине.Это может помочь проверить наличие аномальных новообразований, красных или опухших тканей, язв или кровотечение. Длинная гибкая трубка с подсветкой с крошечной камерой на конце (колоноскоп). используется. Пока вы находитесь под действием седативного препарата, он вводится в прямую кишку вверх в толстую кишку. Этот трубка позволяет вашему лечащему врачу увидеть слизистую оболочку толстой кишки и извлечь ткань образец или биопсия для проверки. Они также могут решить некоторые проблемы, которые могут быть нашел.
- Биопсия. Ваш лечащий врач возьмет образец ткани или клеток слизистой оболочки вашу толстую кишку, чтобы рассмотреть ее под микроскопом.
- Верхний GI череда или бариевая ласточка. Этот тест исследует органы, составляющие верхнюю часть вашей пищеварительной системы.Он проверяет пищевод, желудок и первую часть тонкой кишки, называемой двенадцатиперстной кишкой. Вы проглотите меловую жидкость под названием барий. Барий покрывает органы так, чтобы их можно было увидеть на рентгеновском снимке. Затем рентгеновские лучи находятся приняты для проверки органов пищеварения.
- Нижний GI череда или бариевая клизма. Этот тест проверяет вашу толстую кишку, включая толстая и прямая кишка.Густая меловая жидкость, называемая барием, помещается в трубку. это вставлен в прямую кишку в виде клизмы. Барий покрывает органы, чтобы их можно было увидеть на рентген. Рентген вашего живота покажет любые суженные участки, называемые стриктурами. Это также покажет любые засоры или другие проблемы.
- Компьютерная томография. В этом тесте используются рентгеновские снимки, чтобы создать вид кишечника.Это может быть сделано с IV или оральный рентгеновский контраст.
- МРТ. В этом тесте используется магнитное поле и радиоволны для создания обзора живота. таз и кишечник. Это может быть сделано с помощью внутривенного контрастирования и, в некоторых случаях, ректального введения. контраст.
- Капсульная эндоскопия. Для этого теста вы проглотить небольшую таблетку (капсулу), являющуюся видеокамерой.Снимает маленькие кишечник, как он проходит. Капсула выводится естественным путем со стулом, и снимки с монитора оцениваются на компьютере.
Как протекает болезнь Крона обрабатывали?
Лечение будет зависеть от ваших симптомов, возраста и общего состояния здоровья. Это также будет зависеть на насколько тяжелое состояние.
Нет лекарства от болезни Крона. Но есть кое-что, что может помочь контролировать это. Лечение преследует 3 цели:
- Легкость такие симптомы, как боль в животе или животе, диарея и ректальное кровотечение
- Контроль покраснение или припухлость (воспаление)
- Справка вы получаете правильное питание
Лечение может включать:
- Медицина. Некоторые лекарства могут помочь облегчить спазмы в животе и диарею. Лекарства часто уменьшают воспаление в толстой кишке. Если у вас более серьезный случай, вам могут понадобиться лекарства, которые влияют на систему борьбы с инфекциями вашего организма (иммунная система). Эти лекарства называются биопрепаратами. Их дают в виде таблеток, инъекций, или их комбинации. Очень важно обсудить плюсы и минусы лекарства с вашим лечащим врачом и не прекращать прием лекарства без их знания.Иногда прекращение приема лекарства ограничивает его способность помочь вам. снова в будущем.
- Диета. Не было показано, что специальная диета помогает предотвратить или лечить болезнь Крона. Тем не мение, а специальная диета, называемая элементарной диетой, может в некоторых случаях лечить болезнь Крона. В некоторых случаях симптомы усугубляются молоком, алкоголем, острыми специями или клетчаткой.
- Дополнения. Ваш лечащий врач может предложить пищевые добавки или специальные, калорийные жидкие формулы. Это может быть полезно для детей, которые не растет достаточно быстро.
- IV или внутривенное питание. В редких случаях внутривенное кормление может использоваться для людей, которые нуждаются в дополнительном питании на короткий период времени.
- Хирургия. Хирургия может помочь при болезни Крона, но не вылечить ее. Опухоль или воспаление часто возвращается к тому месту, где был удален кишечник. Иногда операция является также необходимо для лечения язв вокруг ануса.
- Образ жизни
изменения. Подумайте о следующем:
- Если куришь, брось.Курение вызывает симптомы болезни Крона худший.
- Если стресс и эмоции ухудшают ваши симптомы, консультирование может помочь. Так же как и меры самопомощи, такие как упражнения, йога и медитация.
Операционные возможности
Хирургическое вмешательство может помочь уменьшить долгосрочные или хронические симптомы, которые не проходят с терапия.Хирургия также может решить некоторые проблемы, такие как закупорка кишечника, сужение область (стриктура), отверстие или перфорация, абсцесс или кровотечение.
Типы операций могут включать:
Дренирование абсцессов в свищах или около них
Абсцесс – это скопление гноя или инфекции. Лечение включает антибиотики и инъекционные препараты, например, биопрепараты, но иногда требуется хирургическое вмешательство.
Кишечник или резекция кишечника
Больной участок кишечника удален. Два здоровых участка кишечника находятся прикрепил. Эта операция укорачивает ваш кишечник.
Стома
При удалении части кишечника делается новое отверстие для удаления стула из твое тело.Операция по созданию нового отверстия называется стомой. Новое открытие называется стомой. Существуют разные виды хирургии стомы. Тип операции это будет зависеть от того, сколько и какая часть вашего кишечника будет удалена.
Операция по удалению стомы может включать:
- Илеостомия. Ободочная и прямая кишки удаляются, а нижняя часть тонкой кишки (подвздошная кишка) прикрепляется к новому отверстию или стома.
- Колостома. Эта операция открывает в вашем живот или живот. Небольшая часть толстой кишки проходит через это отверстие до поверхность кожи. В некоторых случаях может быть сделана краткосрочная колостома. Это используется, когда часть толстой кишки была удалена, а остальная часть толстой кишки должна быть лечить.
- Хирургия илеоанального резервуара. Это можно сделать вместо постоянная илеостомия. Выполняется в 2-х хирургических операциях. Во-первых, толстая и прямая кишки удаляется и выполняется кратковременная илеостомия. Затем илеостома закрывается. Часть тонкой кишки используется для создания внутреннего мешка для стула. Этот мешочек прикреплен к анусу. Мышца прямой кишки остается на месте, поэтому что стул в сумке не вытекает из заднего прохода.Люди, у которых есть это хирургия может контролировать их испражнения.
Какие возможные осложнения Болезнь Крона?
Болезнь Крона может вызывать другие проблемы со здоровьем. Сюда могут входить:
- А заблокированный (кишечная непроходимость) или суженный (стриктура) кишечник
- Типа туннеля, называемого свищом, в близлежащих тканях, который может инфицировать
- Разрывы или разрывы заднего прохода, называемые трещинами
- Рак толстой кишки, если ваша толстая кишка поражена болезнью Крона
- Проблемы с функцией печени
- Камни в желчном пузыре
- Недостаток некоторых питательных веществ, таких как калории, белки и витамины
- Слишком мало эритроцитов или слишком мало гемоглобина в крови (анемия)
- Слабость костей либо из-за хрупкости костей (остеопороз), либо из-за того, что кости мягкий (остеомаляция)
- Заболевание нервной системы, при котором ощущаются боли в ногах, называемое синдромом беспокойных ног
- Артрит
- Проблемы с кожей
- Покраснение или отек (воспаление) глаз или рта
Болезнь Крона также может приводить к состояние, называемое мальабсорбцией.Кишечник помогает переваривать и усваивать пищу. Нарушение всасывания происходит, когда пища плохо переваривается и питательные вещества не усваиваются. в тело. Это может привести к плохому росту и развитию. Нарушение всасывания может произойти, когда воспаляется пищеварительный тракт или если после операции возникает синдром короткой кишки.
Общие симптомы мальабсорбции включают следующее:
- Свободный стул или диарея
- Большой количество жира в стуле, называемое стеатореей
- Похудание или плохой рост
- Потеря жидкости или обезвоживание
- Недостаток витаминов и минералов
Это важно лечить болезнь Крона.Это означает, что нельзя прекращать прием лекарств, когда вы Чувствовать лучше. Это потому, что держать болезнь под контролем (ремиссия) – лучший способ путь к избежать осложнений спустя много лет.
Что я могу сделать, чтобы предотвратить болезнь Крона? болезнь?
Эксперты не знают, что вызывает болезнь Крона болезнь или как ее можно предотвратить.
Жизнь с болезнью Крона болезнь
Для вас важно тесно сотрудничать с вашим лечащим врачом, чтобы управлять вашим заболеванием.Убедитесь, что вы регулярно посещения вашего лечащего врача, так как постоянный мониторинг важен. Следовать все инструкции о лекарствах, диете и изменении образа жизни.
Когда мне следует позвонить своему врачу?
Позвоните своему врачу, если ваши симптомы ухудшатся или у вас появятся новые симптомы.
Ключевые сведения о болезни Крона болезнь
- Болезнь Крона – это покраснение и припухлость (воспаление), язвы или язвы пищеварительного тракта.
- Это тип воспалительного заболевания кишечника (ВЗК).
- В большинстве случаях он поражает тонкий кишечник. Но это может повлиять на весь пищеварительный тракт. тракт.
- Это длительное хроническое заболевание.
- Нет лекарства. Некоторые изменения в диете могут помочь облегчить симптомы.
- Мост людям с болезнью Крона необходимо продолжать принимать лекарства, чтобы ограничить развитие других медицинских проблем в будущем.Может потребоваться операция.
Следующие шаги
Советы, которые помогут вам получить максимальную пользу от посещения вашего врача провайдер:
- Знайте причину вашего визита и то, что вы хотите.
- Перед визитом запишите вопросы, на которые хотите получить ответы.
- Возьмите с собой кого-нибудь, кто поможет вам задать вопросы и запомнить что вам говорит ваш провайдер.
- При посещении запишите название нового диагноза и любого нового диагноза. лекарства, лечение или тесты. Также запишите все новые инструкции вашего провайдера дает тебе.
- Узнайте, почему прописано новое лекарство или лечение и как это сделать. Вам поможет. Также знайте, каковы побочные эффекты.
- Спросите, можно ли вылечить ваше состояние другими способами.
- Знайте, почему рекомендуется тест или процедура и каковы результаты может означать.
- Знайте, чего ожидать, если вы не примете лекарство или тест или процедура.
- Если у вас назначена повторная встреча, запишите дату, время, и цель этого визита.
- Знайте, как вы можете связаться со своим провайдером, если у вас есть вопросы.
Медицинский обозреватель: Jen Lehrer MD
Медицинский обозреватель: Рональд Карлин, доктор медицины
Медицинский обозреватель: Раймонд Кент Терли BSN MSN RN
© 2000-2021 Компания StayWell, LLC. Все права защищены. Эта информация не предназначена для замены профессиональной медицинской помощи. Всегда следуйте инструкциям лечащего врача.
Не то, что вы ищете?Токсичный мегаколон | Johns Hopkins Medicine
Токсичный мегаколон встречается редко, но опасен для жизни.Это осложнение тяжелой болезни или инфекции толстой кишки.
Токсичный мегаколон может быть смертельным, поскольку подвергает вас риску заражения всего тела, шока и обезвоживания. Токсический мегаколон – это опасное для жизни состояние, которое требует немедленного лечения.
Симптомы
Это признаки и симптомы, относящиеся к токсическому мегаколону:
Вздутие живота
Боль в животе
Лихорадка
Учащенный пульс
Удар
Диарея
Факторы риска
Токсичный мегаколон является осложнением этих состояний:
Язвенный колит.Это воспалительное заболевание кишечника. Обычно поражает толстую и прямую кишку.
Болезнь Крона. Это воспалительное заболевание кишечника. Это может повлиять на любую часть пищеварительного тракта.
Инфекции толстой кишки. Это может быть вызвано C. difficile . Это микроб, который может вызывать симптомы, варьирующиеся от диареи до возможно смертельного воспаления толстой кишки. Другие инфекции также могут быть причиной проблемы.
Ишемия.Низкий кровоток в толстой кишке.
В редких случаях – рак толстой кишки.
Другие факторы риска включают диабет, трансплантацию органов, почечную недостаточность, подавленный иммунитет и хроническую обструктивную болезнь легких.
Диагностика
Чтобы поставить диагноз, ваш лечащий врач сделает следующее:
Изучите свою историю болезни
Пройти медицинский осмотр
Заказать анализы крови, например, общий анализ крови
Заказать рентген кишечника или компьютерную томографию
Лечение
Лечение токсического мегаколона включает:
Лекарства.Лечение исходного состояния или инфекции может помочь уменьшить токсический мегаколон. Противовоспалительные препараты могут помочь контролировать воспаление. Антибиотики могут помочь вылечить или предотвратить инфекцию. Ваш лечащий врач может назначить другие лекарства.
Покой и декомпрессия кишечника. Эти процедуры удаляют газы и вещества, заполняющие толстую кишку.
Внутривенные жидкости. Вам могут сделать внутривенное введение жидкости и электролитов, чтобы питать ваше тело и предотвратить обезвоживание.
Хирургия. Если менее инвазивные методы лечения не уменьшают размер токсичного мегаколона в течение 2-3 дней, вам может потребоваться операция по удалению части или всей толстой кишки.
Ваш лечащий врач может попросить вас прекратить прием определенных лекарств, пока вы лечитесь от токсичного мегаколона. Некоторые лекарства, которые могут ухудшить состояние, – это опиоиды, нестероидные противовоспалительные препараты, лекарства от диареи, антидепрессанты и холинолитики.
Осложнения
При отсутствии лечения токсический мегаколон может привести к серьезным осложнениям, таким как:
Токсичный мегаколон может быть смертельным, если его не лечить.
Когда звонить поставщику медицинских услуг
Немедленно обратитесь за медицинской помощью или попросите кого-нибудь позвонить в службу 911, если у вас сильная боль в животе и следующие симптомы:
Частая диарея
Кровавый понос
Вздутие живота
Лихорадка
Учащенный пульс
Признаки шока, такие как слабый пульс, холодная или липкая кожа, расширенные глаза, спутанность сознания и учащенное или поверхностное дыхание
Хроническое воспаление кишечника: воспалительное заболевание кишечника и рак толстой кишки, связанный с колитом
Воспалительные заболевания кишечника (ВЗК), включая болезнь Крона (БК) и язвенный колит (ЯК), являются хроническими воспалительными заболеваниями кишечника.Распространенность в США превышает 200 случаев на 100 000, а общее число пациентов с ВЗК составляет от 1 до 1,5 миллиона. CD может поражать все части желудочно-кишечного тракта, от рта до ануса, но чаще всего поражает дистальную часть тонкой кишки или подвздошной кишки и толстой кишки. ЯК приводит к воспалению толстой кишки, которое может поражать только прямую кишку или может прогрессировать проксимально, поражая часть или всю толстую кишку. Клинические симптомы включают диарею, боль в животе, желудочно-кишечное кровотечение и потерю веса.Серьезным длительным осложнением хронического воспаления является развитие рака прямой кишки. Долгое время была признана генетическая основа ВЗК, основанная на повышенном семейном риске. Однако значительное несоответствие БК у близнецов и гораздо менее надежное фенотипическое соответствие ЯК предполагают, что в патогенезе заболевания играют роль дополнительные факторы, включая факторы окружающей среды. За последние несколько лет прогресс в понимании молекулярных основ ВЗК ускорился, начиная с создания моделей колита на животных и заканчивая идентификацией конкретных генетических маркеров на основе анализа генов-кандидатов, сцепления генов и анализа ассоциаций в целом.
