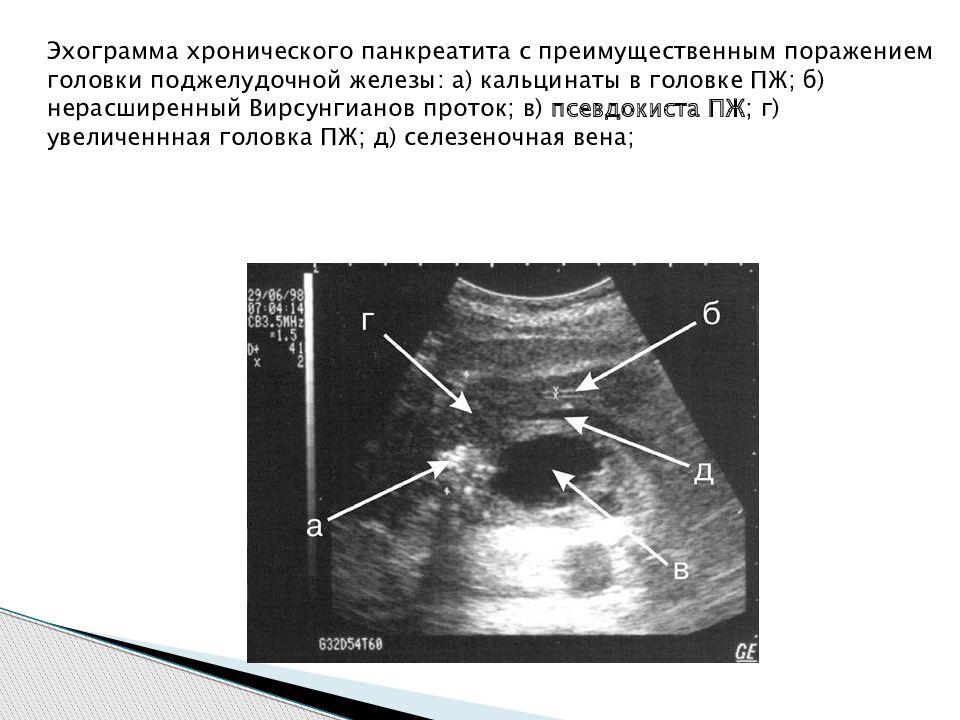
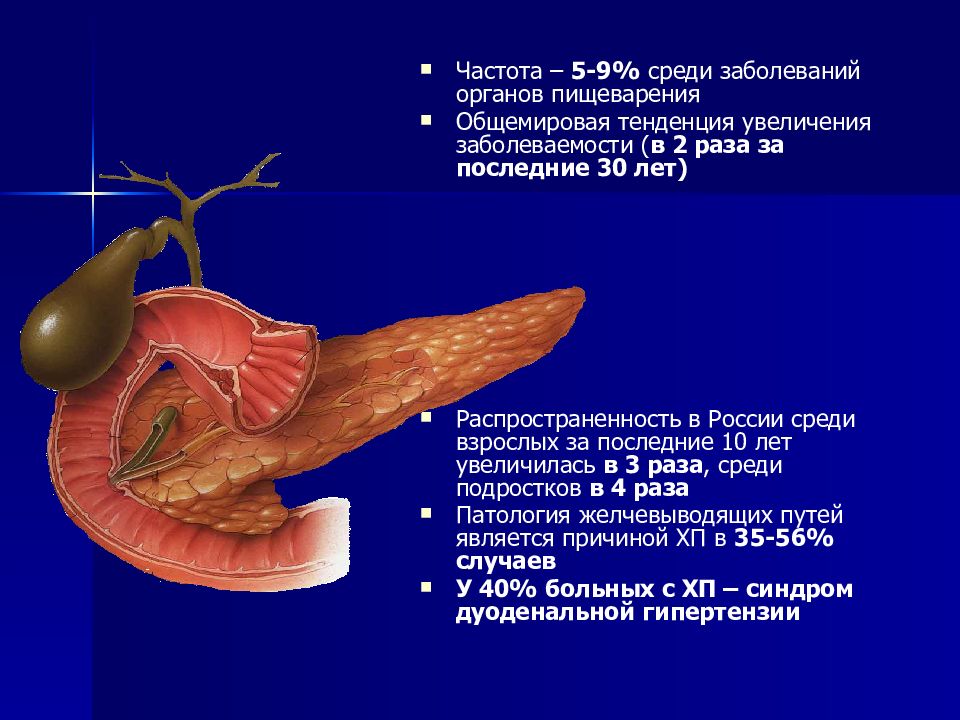
Диффузное изменение паренхимы поджелудочной железы: Лечение диффузных изменений поджелудочной железы в Москве
Диффузные изменения поджелудочной железы на УЗИ
Умеренное употребление пищи — мать здоровья.
М.В. Ломоносов
Поговорим еще об одном часто встречаемом в ультразвуковой практике заключении: «Диффузные изменения паренхимы поджелудочной железы». Причем я уверена, что большинство пациентов не понимают, что ж это такое. «Поджелудка!» — говорят они родственникам, выходя из кабинета УЗИ.
Но что ж это за орган? Зачем он нужен? Почему он у всех страдает?
Поджелудочная железа расположена, как вы догадались, под желудком. Большая её часть (хвост) находится слева, меньшая часть срединно (тело) и справа (головка). Железа примыкает вплотную к разным органам (печень, двенадцатиперстная кишка и другие отделы кишечника, желудок, селезенка, почки, сосуды, выводные желчные протоки), поэтому, если вас беспокоят боли в верхних отделах живота, не надо все валить на бедную поджелудочную железу! Лучше провериться, ведь помимо перечисленных органов, боль сюда может проецироваться даже от сердца.
Продолжим. Почему она называется железой? Железой называют орган, который может производить какие-то важные для организма вещества. Так вот, поджелудочная железа весом у взрослого человека около 60–80 г в сутки вырабатывает около 1,5–2 л панкреатического сока! Большая часть клеток, из которых она состоит, вырабатывает именно этот сок, который по протоку поступает в кишечник и там помогает переваривать белки, жиры и углеводы. У пожилых масса органа уменьшается по причине возрастных изменений, а также после всех проблем, перенесенных за жизнь, поэтому и сока вырабатывается меньше. Значит питание с возрастом должно быть в небольших объёмах, легкоусвояемое, некалорийное. «Раньше меня так не вздувало!» — слышишь от пациентов, так и сока 10–20 лет назад поджелудочная вырабатывала больше, пища переваривалась быстрее, легче.
Только около 2% клеток поджелудочной железы вырабатывает инсулин, который регулирует уровень сахара в крови, т.е. около 1,2–1,6 г клеток нам всего дано на всю жизнь, только вдумайтесь! А теперь прикиньте, сколько углеводов (сладостей) вы употребляете за жизнь? сколько покупаете «вкусняшек» вашим детям? В среднем в год человек съедает 24–28 кг сахара (в России — до 40 кг!). Прибавьте к этому около 50 тонн еды, которые в среднем съедает человек при продолжительности жизни 70 л. Ну, и не забудем про алкоголь, лекарства (которые свободно можно купить в аптеке!!!). А наша маленькая поджелудочная железа должна все это переварить!
Прибавьте к этому около 50 тонн еды, которые в среднем съедает человек при продолжительности жизни 70 л. Ну, и не забудем про алкоголь, лекарства (которые свободно можно купить в аптеке!!!). А наша маленькая поджелудочная железа должна все это переварить!
Хотелось бы еще рассказать о влиянии сна на поджелудочную железу. Недосыпание приводит к появлению неправильно свёрнутых белков и потенциально может привести к гибели клеток, особенно в пожилом возрасте. Исследование учёных из Медицинской школы Пенсильванского университета (США) как раз об этом. А также исследования жозефа Баура (Joseph Baur) и его коллег. Неправильные белки организм должен либо исправить, либо утилизировать. Ученый обнаружил, что у старых животных реакция на такой стресс ослаблена, то есть с возрастом недостаток сна может сказываться всё сильнее.
Поэтому задумайтесь, прежде чем попить чайку на ночь глядя (а тем более что-то покрепче) или посмотреть любимый фильм до часу ночи.
Так вот, при современном изобилии в питании и разнообразии в образе жизни не стоит удивляться, если начались проблемы с пищеварением (вздутие, чувство тяжести, нарушения стула и пр. ) Многие на исследовании признаются: «Так я уже ничего такого и не ем, а не помогает!» Ключевое слово здесь «уже», т.е. в течение многих десятков лет мы едим все подряд, а «садимся» на диету только тогда, когда организм уже начнет выдавать нам неприятности с пищеварением или повышенный сахар в анализах. К сожалению, здесь уже иногда сложно помочь.
) Многие на исследовании признаются: «Так я уже ничего такого и не ем, а не помогает!» Ключевое слово здесь «уже», т.е. в течение многих десятков лет мы едим все подряд, а «садимся» на диету только тогда, когда организм уже начнет выдавать нам неприятности с пищеварением или повышенный сахар в анализах. К сожалению, здесь уже иногда сложно помочь.
Что же доктор видит на УЗИ?
Обычно при первых проблемах с железой на ультразвуке может не быть изменений, и это замечательно! Хотя многим хотелось бы их увидеть, и пациенты остаются разочарованы.
Запомните! Однократные воспаления в железе могут проходить бесследно и без изменений по УЗИ.
Но если доктор все-таки находит патологию, то это уже, вероятнее всего, необратимо или оставит свой след на работе органа.
В большинстве случаев доктор описывает примерно следующую картину: контуры железы неровные, нечеткие, эхогенность повышена или высокая, размеры могут быть нормальные, увеличены или уменьшены. Редко бывает расширение протока железы и даже камни в ней. В такой ситуации доктор пишет в заключении пресловутые «Диффузные изменения», т.е. железа многократно за жизнь испытывала нагрузки и часть её клеток погибли или заместились на жир и рубцовую ткань и она уже не может работать как прежде.
Редко бывает расширение протока железы и даже камни в ней. В такой ситуации доктор пишет в заключении пресловутые «Диффузные изменения», т.е. железа многократно за жизнь испытывала нагрузки и часть её клеток погибли или заместились на жир и рубцовую ткань и она уже не может работать как прежде.
Что с этим заключением делать? Обязательно необходимо дообследование (сначала гастроэнтеролог, терапевт), чтобы определить степень нарушений пищеварения и состояние организма в целом, ведь, если страдает поджелудочная железа, значит во всем организме есть проблемы (нарушение углеводного, жирового обмена, как правило сопутствует атеросклероз, могут быть кожные проявления и пр.).
А ситуация в целом, конечно, зависит от вас самих. Доктор пропишет лечение, поможет временно нормализовать беспокоящие вас симптомы. Но контроль за питанием полностью в ваших руках. Если у вас на ультразвуке уже выявлены диффузные изменения, не нагружайте поджелудочную железу, дайте ей возможность подольше обеспечить вам комфортную жизнь!
Диффузные изменения поджелудочной железы: что это такое, узи признаки, лечение
Симптомы ДИ зависят от основного заболевания, которое привело к появлению изменений.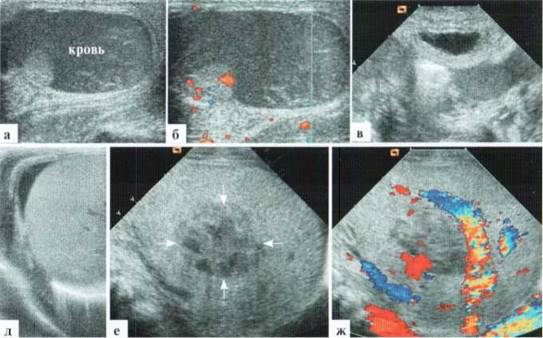
- При остром панкреатите в протоке ПЖ возникает повышенное давление, что вызывает повреждения органа и выход пищеварительных ферментов через ткани железы. Это приводит у разрушению тканей поджелудочной и вызывает интоксикацию организма. Больной ощущает ужасные боли в левом подреберье, частую рвоту и тошноту. Появляются симптомы нарастающей тахикардии и пониженного артериального давления. Состояние не улучшается, вплоть до проведения интенсивной терапии или хирургического лечения.
- При хроническом панкреатите, симптоматика ДИПЖ имеет затяжной характер. На первом этапе происходит повреждение железы, что приводит к ее отечности и небольшим кровоизлияниям. Через время, ПЖ уменьшается в размерах и склерозируется, что приводит к нарушениям выработки пищеварительных ферментов.

- Если диффузные изменения поджелудочной железы вызваны фиброзом, то на первых порах данного заболевания, симптоматика отсутствует. При фиброзном воспалении нормальные ткани железы меняются на соединительную ткань. Это приводит к пониженной выработке ферментов и гормонов, которые поддерживают обменные процессы в организме и отвечают за процесс пищеварения. Начальная симптоматика заболевания схожа с симптомами панкреатита. Больной ощущает постоянную боль в левом подреберье и тошноту. Из-за недостатка ферментов появляется тошнота, поносы, рвота, резкое похудение. В дальнейшем, из-за истощения белковых резервов начинается аллергизация организма и нарушение выработки инсулина, что приводит к сахарному диабету.
- Если изменения ПЖ вызваны липоматозом, то это необратимый процесс. Здоровая ткань железы заменяется жировой тканью. Поскольку жировые клетки не выполняют функции пищеварительных желез, то организм начинает ощущать дефицит веществ, которые необходимы для нормального функционирования.
 Степень выраженности, то есть симптоматика липоматоза, полностью зависит от степени диффузных изменений поджелудочной железы. Так, если заболевание имеет ограниченное распространение очага патологии, то процесс протекает бессимптомно. При бесконтрольном прогрессировании происходит сдавливание паренхимы массивным скоплением жировой ткани, что вызывает болезненные ощущения и приводит к нарушениям в работе ПЖ.
Степень выраженности, то есть симптоматика липоматоза, полностью зависит от степени диффузных изменений поджелудочной железы. Так, если заболевание имеет ограниченное распространение очага патологии, то процесс протекает бессимптомно. При бесконтрольном прогрессировании происходит сдавливание паренхимы массивным скоплением жировой ткани, что вызывает болезненные ощущения и приводит к нарушениям в работе ПЖ.
[11], [12]
Диффузные изменения паренхимы поджелудочной железы
Очень часто встречаются в заключении ультразвукового исследования. Это не поставленный диагноз, а всего лишь результат проведенного исследования, который свидетельствует о равномерном изменении в тканях железы, отсутствии камней, локальных очагов, кист или опухолей. То есть УЗИ говорит о том, что в тканях паренхимы наблюдаются изменения, причину которых необходимо выяснить.
Врачи выделяют следующие причины диффузных изменений в паренхиме поджелудочной железы:
- Панкреатит (острая форма) – серьезное заболевание, которое возникает в результате нарушения оттока секрета из-за воспалительного процесса в ПЖ.
 Результат вышеупомянутого процесса отражается диффузными изменениями в паренхиме железы.
Результат вышеупомянутого процесса отражается диффузными изменениями в паренхиме железы. - Хронический панкреатит – одна из форм воспаления ПЖ. Заболевание может возникать из-за патологических процессов в желчном пузыре и печени или появляться самостоятельно.
- Сахарный диабет – заболевание, при котором здоровая ткань железы заменяется жировой тканью. Как результат, на ультразвуковом исследовании видны диффузные изменения в паренхиме органа.
Кроме диффузных изменений, при исследовании паренхимы поджелудочной железы, врачи могут диагностировать повышенную эхогенность органа. Эхогенность тканей считается одним из важных показателей, которые позволяют оценить плотность внутренних органов. Если УЗИ выявило повышенную или пониженную эхогенность паренхимы поджелудочной железы, то обязательно проводятся дополнительные анализы для выяснения причины данной патологии. Как правило, повышенная эхогенность паренхимы поджелудочной железы, возникает при:
- Воспалительный процесс с образованием фиброза – соединительная ткань зарубцовывается, из-за чего участки ткани отличаются по плотности.
 На УЗИ это дает гипеорэхогенный сигнал. Заболевание может возникнуть из-за нарушения обмена веществ.
На УЗИ это дает гипеорэхогенный сигнал. Заболевание может возникнуть из-за нарушения обмена веществ. - Острый и хронический панкреатит – воспалительное заболевание приводит к отечности органа, из-за чего меняется плотность паренхимы, а значит, повышается эхогенность ткани.
[13], [14], [15], [16]
Диффузные изменения структуры поджелудочной железы
Бывают равномерного и неравномерного характера. Именно характер изменений свидетельствует о том, что процессы, происходящие в железе, имеют общую, а не локальную форму. Ткани ПЖ из-за воспалительных процессов и отечности могут становиться плотнее или наоборот терять свою плотность.
При неравномерных диффузных изменениях структуры тканей железы чаще всего обнаруживаются различные опухоли, кисты или склероз органа. Больше всего изменения касаются паренхимы железы, так как ее ткани имеют железистую структуру.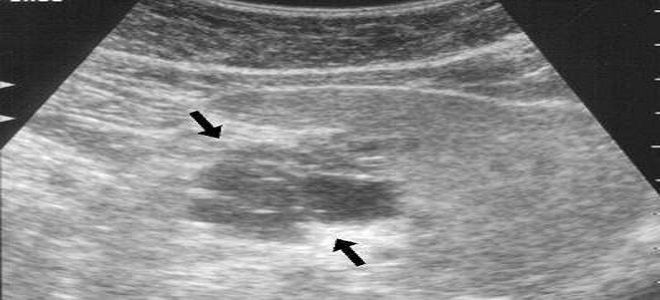 Существует множество причин, которые приводят к изменениям структуры органа. Изменения свидетельствуют о нарушениях в работе органа, что без дополнительной диагностики и лечения может привести к серьезным последствиям. Так как ПЖ отвечает не только за процесс пищеварения, но и за производство жизненно важных гормонов, таких как глюкагон и инсулин.
Существует множество причин, которые приводят к изменениям структуры органа. Изменения свидетельствуют о нарушениях в работе органа, что без дополнительной диагностики и лечения может привести к серьезным последствиям. Так как ПЖ отвечает не только за процесс пищеварения, но и за производство жизненно важных гормонов, таких как глюкагон и инсулин.
Давайте рассмотрим самые распространенные факторы, которые приводят к изменениям структуры.
- Воспалительные заболевания и другие поражения органов пищеварительной системы.
- Патологическая наследственность – очень часто заболевания ПЖ передаются детям от родителей.
- Хроническое нервное перенапряжение, стрессы, повышенная утомляемость.
- Неправильное питание, злоупотребление соленными, острыми, жирными и сладкими продуктами.
- Курение и алкоголизм.
- Возраста пациента – очень часто диффузные изменения структуры поджелудочной начинаются в позднем возрасте.
Задача врача точно определить причину изменений.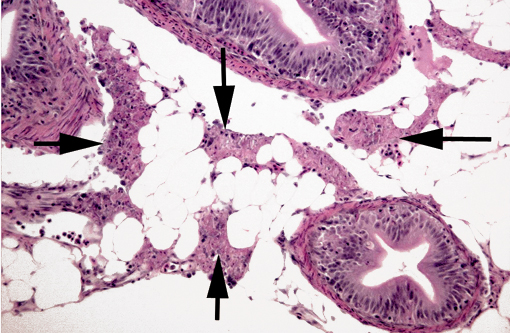 Но не стоит забывать, что изменение структуры ПЖ может быть симптоматикой множества заболеваний. То есть наличие только структурных изменений, это не повод для постановки окончательного диагноза. Врач руководствуется собранным анамнезом и результатами других исследований и анализов.
Но не стоит забывать, что изменение структуры ПЖ может быть симптоматикой множества заболеваний. То есть наличие только структурных изменений, это не повод для постановки окончательного диагноза. Врач руководствуется собранным анамнезом и результатами других исследований и анализов.
[17], [18], [19], [20]
Хронические диффузные изменения поджелудочной железы
Могут долго не проявлять себя. Хронические изменения свидетельствуют о наличие хронических заболеваний и воспалительных процессов. Причиной подобного рода изменений может быть хронический панкреатит, фиброз или липоматоз.
- Липоматоз – это заболевание, при котором здоровые ткани железы заменяются жировыми клетками. От данного заболевания чаще всего страдают люди с сахарным диабетом.
- Если кроме хронических диффузных изменений поджелудочной железы, ультразвуковое исследование обнаружило повышенную эхогенность, но нормальные размеры железы сохранены, то это фиброз. Заболевание может быть вызвано нарушением обменных процессов или появиться в результате сращивания соединительной ткани.

Хронические диффузные изменения поджелудочной железы свидетельствуют о равномерных изменениях в органе. Подобные результаты ультразвукового исследования не являются диагнозом, а выступают сигналом для врача, который должен найти причину изменений и устранить ее.
[21], [22], [23]
Диффузные реактивные изменения поджелудочной железы
Означают вторичные изменения, то есть реакцию органа на заболевание. Диффузные реактивные изменения могут возникать при любых заболеваниях органов пищеварения, поскольку функции всех органов и систем взаимосвязаны. Но чаще всего реактивные изменения свидетельствуют о проблемах с печенью или желчевыводящими путями, так как именно с ними у ПЖ самая тесная связь.
Реактивные изменения могут говорить наличие вторичного панкреатита, который возникает у пациентов с заболеваниями органов пищеварения, из-за регулярного переедания, употребления в пищу жаренного, острого, соленного. Патология возникает и при некоторых врожденных ферментативных нарушениях и из-за длительного применения лекарственных препаратов или аномалиях в развитии желчевыводящих путей.
На ультразвуковом исследовании, диффузные реактивные изменения поджелудочной железы схожи с картиной острого панкреатита. Один из участков органа увеличен, чаще всего хвост, наблюдается расширение протока железы и изменения в тканях органа. При вторичных ДИ, пациента ждет полная диагностика органов желудочно-кишечного тракта для определения настоящей причины данной патологии.
[24]
Диффузно очаговые изменения поджелудочной железы
Могут свидетельствовать о том, что в органе есть опухолевые процессы, кисты или камни. Это вызвано локальными, то есть очаговыми изменениями тканей поджелудочной железы. Подобные процессы могут возникать из-за заболеваний, как органов желудочно-кишечного тракта, так и ПЖ.
Диффузно очаговые изменения требуют дополнительных исследований и обязательного лечения. Так как свидетельствуют о патологическом процессе в организме. Пациенты, с такими результатами ультразвукового исследования, должны быть к готовы к длительному, а возможно и хирургическому лечению.
[25]
Диффузные фиброзные изменения поджелудочной железы
Это рубцевание, то есть уплотнение соединительной ткани. Данная патология может возникать из-за нарушений обмена веществ в организме, хронических воспалительных процессов, вирусной или алкогольной интоксикации или поражений гепато-билиарной системы. При проведении ультразвукового исследования, фиброзные изменения характеризуются повышенной эхогенностью и плотностью тканей органа. Не всегда наблюдается уменьшение ПЖ, так как изменение размеров органа зависит от степени распространения изменений ткани.
Фиброзные изменения могут указывать на развитие в тканях органа фибромы. Фиброма – это доброкачественная опухоль, которая образуется из соединительной ткани, не метастазирует и очень медленно растет. Заболевание не вызывает болезненной симптоматики, поэтому диагностировать его можно только с помощью ультразвукового исследования. Но если опухоль имеет большие размеры, то это приводит к сдавливанию ПЖ и органов, которые расположены рядом. В зависимости от локализации фибромы в поджелудочной железе возникает определенная симптоматика:
В зависимости от локализации фибромы в поджелудочной железе возникает определенная симптоматика:
- Боли в левом или правом подреберье, в области пупка и эпигастрии – это признак поражения поджелудочной железы.
- Если фиброма находится в головке ПЖ, то из-за пережатого желчного протока появляется симптоматика желтухи.
- Если фиброма сжимает двенадцатиперстную кишку, то у больного появляется симптоматика, схожая на кишечную непроходимость (тошнота, рвота).
Фиброзные изменениятребуют лечения. Лечение может осуществляться как консервативным, то есть медикаментозным путем, так и с помощью оперативного вмешательства. Помимо лечения, пациента ждет длительный восстановительный период, соблюдение здорового образа жизни и только диетическое питание (диета стол №5).
[26], [27], [28]
Диффузные дистрофические изменения поджелудочной железы
Это необратимый процесс, который связан с недостатком жировой ткани, что приводит к патологическим изменениям органа. Нормальные клетки ПЖ сменяются жировыми, которые неспособны стабильно функционировать и поддерживать работу органа. Диффузные дистрофические изменения – это липодистрофия.
Нормальные клетки ПЖ сменяются жировыми, которые неспособны стабильно функционировать и поддерживать работу органа. Диффузные дистрофические изменения – это липодистрофия.
Жировая дистрофия возникает из-за отмирания клеток органа, под влиянием ряда факторов (воспалительные процессы, хронический панкреатит, опухоли). Из-за таких патологий, организм не в состоянии восстановить свою целостность. Если дистрофия возникла из-за сбоя, а количество отмерших клеток не велико, то человек может даже и не знать о подобных процессах в организме. Так как поджелудочная железа будет работать исправно. Если дистрофия прогрессирует, а клетки образуют очаги, то это приводит к остановке полноценной работы ПЖ.
Точная симптоматика, которая помогла бы диагностировать диффузные дистрофические изменения, отсутствует. Как правило, проблемы обнаруживают при проведении ультразвукового исследования. Все это говорит о том, что любые нарушения в работе ПЖ должны быть поводом для глубокой диагностики, которая могла бы подтвердить или опровергнуть диффузные дистрофические изменения.
[29], [30], [31], [32], [33], [34]
Диффузные изменения поджелудочной железы хвоста
Это патологический процесс, который требует детальной диагностики. ПЖ имеет три основные части: головку, тело и хвост, который уже основной части. Хвост имеет загнутую грушевидную форму, поднимается вверх и плотно прилегает к селезенке. Оптимальная ширина хвоста поджелудочной железы – 20-30 мм. В хвосте расположен выводной проток, который имеет длину 15 см и проходит через все тело органа.
Как правило, диффузные изменения хвоста поджелудочной железы свидетельствуют о его уплотнении или расширении. Данные изменения происходят из-за нарушений проходимости селезеночной вены. На фоне данных изменений может развиться портальная гипертензия подпочечной формы.
Диффузные изменения хвоста поджелудочной железы занимают четвертую часть среди всех заболеваний органа. Исследуют хвост через селезенку или левую почку. А вот лечить патологии хвоста очень сложно. Как правило, больному проводят операцию по удалению хвоста ПЖ и преграждают кровеносные сосуды органа для сохранения его нормальной работы. При незначительных или умеренных диффузных изменениях возможна консервативная терапия и регулярное наблюдение.
При незначительных или умеренных диффузных изменениях возможна консервативная терапия и регулярное наблюдение.
[35], [36], [37], [38]
Диффузные паренхиматозные изменения поджелудочной железы
Возникают при различных заболеваниях органов желудочно-кишечного тракта, а в особенности ПЖ. Стоит отметить, что все органы человеческого организма делятся на паренхиматозные и полые. Паренхиматозные органы заполнены основной тканью, то есть паренхимой. Поджелудочная железа и печень – это паренхиматозные органы брюшной полости, так как в них находится железистая ткань, разделенная на множество долек соединительнотканными перегородками, и покрыта капсулой.
Функционирование ПЖ, желчевыводящих путей и печени взаимосвязаны, так как все эти органы имеют единый проток для вывода желчи и панкреатического сока. Любые нарушения в печени отображаются на поджелудочной железе и наоборот. Диффузные изменения паренхимы поджелудочной железы возникают из-за обменно-дистрофических заболеваний, которые приводят к замещению нормальной ткани органа на жировую или соединительную ткань.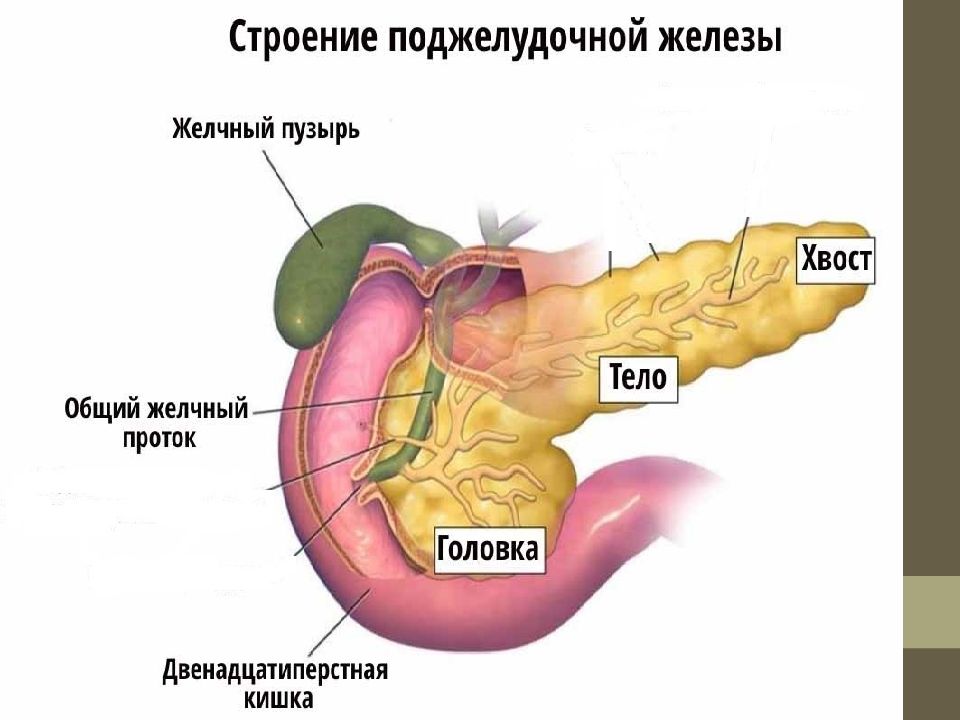
Как правило, диффузные изменения паренхимы встречаются у пациентов пожилого возраста, больных сахарным диабетом и у людей с заболеваниями сердечно-сосудистой системы и нарушениями кровообращения в ПЖ. Изменения могут быть вызваны заболеваниями печени, органов желудочно-кишечного тракта, желчевыводящих путей или длительными инфекционно-воспалительными заболеваниями, которые вызывают нарушения обмена веществ.
Паренхиматозные изменения встречаются у пациентов молодого и среднего возраста. Патология вызвана перенесенным острым панкреатитом. Изменения могут наложить отпечаток на функциональные способности ПЖ и вызывать болезненные ощущения. Для того чтобы определить последствия диффузных изменений, необходимо провести осмотр пациента и дополнительные анализы.
[39], [40], [41], [42], [43], [44]
Диффузные изменения поджелудочной железы: симптомы и классификация
Статью подготовил:
Василий Бабкинский
Врач высшей категории
Диффузные изменения в поджелудочной железе обнаруживаются при ультразвуковом исследовании. Такой метод диагностирования стандартный. Диффузное изменение поджелудочной железы – признак заболевания. По МКБ (международная классификация болезней) отклонение имеет код 87.1. Диффузное изменение может быть локальным или смешанным. Установить первопричину отклонения возможно только после комплексного исследования. Основной диагностический метод – УЗИ. Врачи также выделяют несколько степеней выраженности патологического процесса.
Такой метод диагностирования стандартный. Диффузное изменение поджелудочной железы – признак заболевания. По МКБ (международная классификация болезней) отклонение имеет код 87.1. Диффузное изменение может быть локальным или смешанным. Установить первопричину отклонения возможно только после комплексного исследования. Основной диагностический метод – УЗИ. Врачи также выделяют несколько степеней выраженности патологического процесса.
О патологии
Диффузные изменения проявляются равномерной трансформацией паренхимы поджелудочной железы на всем протяжении. Данная часть органа отвечает за выработку ферментов и гормонов. От ее функционирования зависит работоспособность всего организма.
Любые патологические изменения паренхимы влияют на ее плотность. Диффузное изменение – не конкретный диагноз, а объективный симптом, отражающий отклонение от нормальных показателей. При наличии нарушения поджелудочная железа увеличивается и уплотняется. При наличии некоторых патологий диффузия поджелудочной железы характеризуется заменой нормальных тканей на соединительную или жировую.
При наличии некоторых патологий диффузия поджелудочной железы характеризуется заменой нормальных тканей на соединительную или жировую.
Самочувствие человека напрямую зависит от количества оставшихся здоровых клеток и участков органа.
Диффузное уплотнение поджелудочной железы является вариантом нормы у детей. Со временем состояние органа нормализуется. Также у маленьких пациентов такой симптом может указывать на ранее перенесенные хронические заболевания.
Вызвать подобные патологии могут разные заболевания ЖКТОсновные причины диффузных нарушений поджелудочной железы описаны в таблице.
| Хронические заболевания пищеварительной системы | Спровоцировать диффузное нарушение могут имеющиеся заболевания пищеварительной системы, в том числе и поджелудочной. Некоторые патологии затрагивают сразу несколько участков организма. В особенности это касается железы, печени и желчного пузыря. В них патологические процессы возникают одновременно. |
| Обменно-дистрофические отклонения | В таком случае диффузное нарушение поджелудочной железы объясняется болезнями, характеризующимися заменой нормальной ткани на соединительную или жировую. |
| Сердечно-сосудистые заболевания | Патологии при длительном протекании провоцируют ухудшение кровотока в тканях поджелудочной железы. Ухудшается обмен веществ и возникает диффузное изменение в органе. |
| Инфекционные заболевания | Диффузные нарушения провоцируют отклонения, которые сопровождаются тканевым обменом. |
| Генетическая предрасположенность | Возрастает риск появления нарушений диффузного характера у людей, близкие родственники которых столкнулись с таким отклонением. |
Также существуют негативные факторы, повышающие риск формирования отклонения. К ним относят:
- погрешности в назначенной диете;
- злоупотребление спиртосодержащими напитками;
- курение;
- необдуманный прием медикаментозных препаратов;
- стрессы;
- нервные перенапряжения;
- нарушение гормонального фона.

Более подвержены формированию заболевания люди старшей возрастной категории.
Классификация по выраженности
Отклонение имеет несколько степеней выраженности. Первый тип – диффузное уменьшение плотности тканей поджелудочной. В таком случае орган увеличивается в размерах, а также повышается эхогенность. Такие изменения характерны для пациентов с острой формой панкреатита. Пищеварительный сок разрушает участки железы. Также возможно диффузное уменьшение плотности ткани. Эхогенность снижается, а орган остается в норме. Изменение характерно для хронической формы панкреатита.
При этом может наблюдаться увеличение поджелудочной железыДиффузное увеличение эхогенности без изменений размеров органа свидетельствует о течении липоматоза. В таком случае нормальные ткани сменяются жировыми. Обычно нарушение диагностируется у людей старшей возрастной категории.
Также возможно диффузное изменение поджелудочной железы, повышение плотности тканей и увеличение эхогенности. Орган остается в норме или немного уменьшен. Такое состояние характерно для фиброза железы.
Орган остается в норме или немного уменьшен. Такое состояние характерно для фиброза железы.
Незначительные диффузные изменения
Незначительные изменения не являются поводом для беспокойства. Обычно такое состояние указывает на недавнее перенесенное воспалительное заболевание. Также это происходит после сильной стрессовой ситуации или при неправильном питании.
Несущественное диффузное изменение в большинстве случаев свидетельствует о нарушении функционирования центральной нервной системы. Для нормализации поджелудочной железы достаточно всего лишь устранить основную первопричину отклонения.
Незначительные нарушения могут возникать из-за несоблюдения диетыУмеренные диффузные изменения
Умеренные диффузные изменения сопровождают начальные стадии болезней пищеварительной системы. В особенности это касается воспалительных процессов. В таком случае поджелудочная железа отекает.
Диффузные изменения умеренного типа могут указывать на течение:
- хронической формы панкреатита;
- болезней двенадцатиперстной кишки или желчного пузыря;
- фиброза.

Диагностировать умеренные изменения довольно трудно. Часто нарушение обнаруживается случайно при обследовании организма, касаемо иных отклонений.
Невыраженные диффузные изменения
Невыраженные диффузные изменения – патологические процессы, которые не влияют на функционирование организма. В таком случае здоровые ткани заменяются жировыми или соединительными.
Невыраженные изменения могут возникать на фоне болезней печениНевыраженное отклонение может указывать на:
- увеличение уровня сахара в кровотоке;
- болезни печени и желчного пузыря;
- острый или хронический панкреатит;
- сердечно-сосудистые отклонения.
Отклонения невыраженного характера часто диагностируются у пациентов старшей возрастной категории.
Выраженные изменения в поджелудочной
Выраженные нарушения свидетельствуют о течении патологического процесса в организме. При явных диффузных изменениях пациенту необходимо пройти обследование пищеварительной системы и всего тела в целом.
В большинстве случаев выраженные изменения указывают на течение панкреатита. При острой форме болезни присутствует застой панкреатического сока. Жидкость разрушает ткани поджелудочной. Это и приводит к диффузным отклонениям.
При хронической форме панкреатита диффузные изменения могут быть как явными, так и умеренно выраженными. Заподозрить течение патологии на стадии ремиссии трудно.
Симптоматика нарушения
Симптоматика нарушения напрямую зависит от степени выраженности. Иногда изменение протекает бессимптомно. Также признаки могут меняться в зависимости от основного диагноза.
Часто у больных падает аппетитК основным признакам относят:
- снижение аппетита;
- нарушение стула в виде поноса или запора;
- болезненное ощущение в брюшной полости;
- изменение массы тела;
- тошноту и рвотный рефлекс;
- упадок сил;
- повышенное газообразование;
- отрыжку;
- тяжесть в желудке;
- снижение АД;
- скачки пульса.

Все перечисленные симптомы считаются основными. Однако возможен ряд дополнительных признаков, в зависимости от основного патологического диагноза. Симптоматика проявляется при обширных поражениях поджелудочной железы. На первых стадиях обнаружить отклонение самостоятельно почти невозможно.
У некоторых падает давлениеДиагностические методы
Основной диагностический метод для выявления диффузии поджелудочной железы – УЗИ. Исследование позволяет определить структуру органов брюшной полости, их форму, размеры и контуры. Помимо этого доктор может подтвердить или опровергнуть наличие сторонних новообразований.
Врачи выделяют следующие эхопризнаки диффузных изменений железы:
- неоднородность текстуры поджелудочной железы за счет изменений эхогенности в некоторых участках;
- неравномерное увеличение эхогенности;
- неравномерное увеличение желчных протоков;
- патологическое изменение объемов поджелудочной железы;
- дополнительные эхопризнаки в виде присутствия кист и псевдокист.

Пациенту также показаны дополнительные методы исследования. К ним относят анализы крови и мочи, а также эндоскопическое обследование.
Обязательно проводится УЗИ диагностика поджелудочнойК основным показаниям к проведению УЗИ относят:
- дискомфортное ощущение в животе после приема пищи;
- частые запоры или поносы;
- повышенное газообразование;
- увеличенный уровень глюкозы в крови;
- пожелтение кожного покрова.
Описанная клиническая картина – повод заподозрить присутствие диффузных изменений.
Лечебные методы
Единого лечения диффузного изменения не существует. Нарушение не является основным и появляется только при наличии какого-либо отклонения в работе поджелудочной железы. Терапия может быть как консервативной, так и оперативной.
Лечение доктор назначает только после установления окончательного диагноза. Выяснить истинную причину изменений возможно благодаря сбору жалоб, проведению лабораторных и инструментальных методов диагностики.
Избавиться от уже появившихся изменений невозможно. Лечение в таком случае неэффективно, поскольку здоровые клетки необратимо заменены на соединительные или жировые.
При появлении нарушения на фоне сахарного диабета пациенту назначают препараты для поддержания оптимального показателя глюкозы в кровотоке. Дополнительно могут применяться травяные настойки и отвары.
Пациентам в возрасте специальное лечение не показано, достаточно соблюдать рацион питания и принципы здорового образа жизниПри возникновении диффузии поджелудочной в пожилом возрасте специальное лечение не требуется. Достаточно придерживаться простых рекомендаций доктора. Обычно они включают здоровое питание, изменение образа жизни и тщательный контроль состояния здоровья.
Диетотерапия
Вне зависимости от причин появления изменений диффузного характера поджелудочной пациент должен придерживаться особенного питания. Прием пищи должен происходить от 4 раз в сутки. Еда должна иметь теплую температуру.
Из рациона полностью исключают жирное и жареное. Помимо этого нужно воздержаться от маринованного, соленого, пряного и консервированного. Еда может отвариваться или запекаться. Категорически запрещено пить спиртосодержащие напитки.
В рационе должны присутствовать овощи, обезжиренные типы рыбы и мяса, а также каши. В первые дни может рекомендоваться лечебное голодание. Питьевой режим также необходим. В сутки нужно пить от 7 стаканов чистой воды.
Почему возникают диффузные изменения поджелудочной железы, вы сможете узнать, посмотрев этот ролик:
Прогноз
Лечение диффузных отклонений имеет благоприятный прогноз только при своевременном начале. В таком случае выздоровление наступит как можно быстрее. Прогноз неблагоприятный, если лечение было начато поздно или пациент самостоятельно подобрал медикаменты для устранения нарушения. В таком случае количество здоровых клеток значительно уменьшится. Поджелудочная не сможет нормально функционировать. Повышается риск необходимости удаления органа.
В таком случае количество здоровых клеток значительно уменьшится. Поджелудочная не сможет нормально функционировать. Повышается риск необходимости удаления органа.
При удалении поджелудочной здоровье пациента сильно усугубляется. На протяжении всей жизни больному придется пить медикаменты для поддержания самочувствия.
Профилактические меры
Диффузные нарушения легче предотвратить, чем своевременно обнаружить и устранить. В качестве профилактики врачи рекомендуют:
- отказаться от спиртосодержащих напитков;
- отказаться от потребления жирного и жареного;
- избавиться от никотиновой зависимости;
- регулярно потреблять травяные отвары и настои;
- своевременно обращаться к доктору при наличии каких-либо патологических признаков;
- ежегодно проходить комплексное обследование организма.
Все перечисленные рекомендации позволяют существенно снизить риск формирования диффузных нарушений.
Василий Бабкинский
Привет, меня зовут Василий.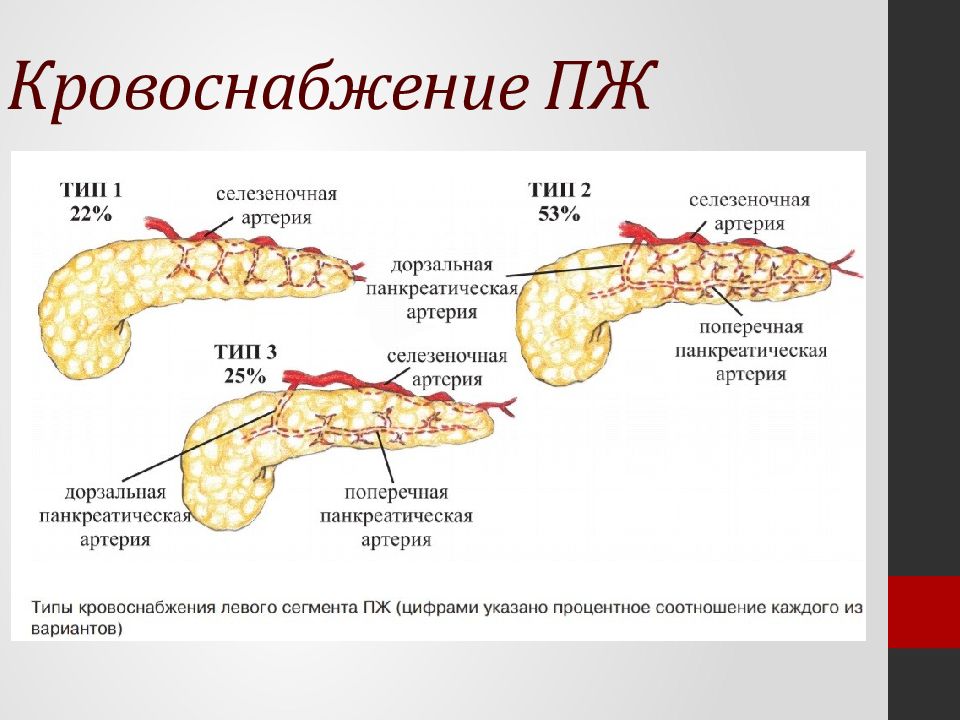 Вот уже 7 лет помогаю людям с проблемами кишечника, работая в первой частной поликлинике г. Брно. Буду рад ответить на ваши вопросы по поводу статьи в комментариях, другие вопросы можете задавать нашим врачам на этой странице.
Вот уже 7 лет помогаю людям с проблемами кишечника, работая в первой частной поликлинике г. Брно. Буду рад ответить на ваши вопросы по поводу статьи в комментариях, другие вопросы можете задавать нашим врачам на этой странице.
Незначительные диффузные изменения паренхимы поджелудочной железы – Вопрос гастроэнтерологу
Если вы не нашли нужной информации среди ответов на этот вопрос, или же ваша проблема немного отличается от представленной, попробуйте задать дополнительный вопрос врачу на этой же странице, если он будет по теме основного вопроса. Вы также можете задать новый вопрос, и через некоторое время наши врачи на него ответят. Это бесплатно. Также можете поискать нужную информацию в похожих вопросах на этой странице или через страницу поиска по сайту. Мы будем очень благодарны, если Вы порекомендуете нас своим друзьям в социальных сетях.
Медпортал 03online.com осуществляет медконсультации в режиме переписки с врачами на сайте. Здесь вы получаете ответы от реальных практикующих специалистов в своей области. В настоящий момент на сайте можно получить консультацию по 67 направлениям: специалиста COVID-19, аллерголога, анестезиолога-реаниматолога, венеролога, гастроэнтеролога, гематолога, генетика, гепатолога, гинеколога, гомеопата, дерматолога, детского гастроэнтеролога, детского гинеколога, детского дерматолога, детского инфекциониста, детского кардиолога, детского лора, детского невролога, детского нефролога, детского офтальмолога, детского психолога, детского пульмонолога, детского ревматолога, детского уролога, детского хирурга, детского эндокринолога, диетолога, иммунолога, инфекциониста, кардиолога, клинического психолога, косметолога, логопеда, лора, маммолога, медицинского юриста, нарколога, невропатолога, нейрохирурга, нефролога, нутрициолога, онколога, онкоуролога, ортопеда-травматолога, офтальмолога, паразитолога, педиатра, пластического хирурга, проктолога, психиатра, психолога, пульмонолога, ревматолога, рентгенолога, репродуктолога, сексолога-андролога, стоматолога, трихолога, уролога, фармацевта, физиотерапевта, фитотерапевта, флеболога, фтизиатра, хирурга, эндокринолога.
Мы отвечаем на 97% вопросов.
Оставайтесь с нами и будьте здоровы!
Способ верификации диагноза заболеваний поджелудочной железы
Изобретение относится к медицине и может быть использовано в клинике внутренних болезней, в гепатологии и отделениях лучевой диагностики как референтный метод верификации диагноза вместо биопсии.
В настоящее время для верификации диагноза заболеваний поджелудочной железы используют аппаратные методы исследования, а именно: трансабдоминальный ультразвук (Борсуков А.В., Иванов Ю.В., Мамошин А.В. Патент на изобретение №2280408 «Способ выявления некроза при остром деструктивном панкреатите»), эндосонографию (Дж. Шайман, Парта С. Нанди. «Эндоскопическая ультрасонография поджелудочной железы» // Ультразвуковая диагностика в хирургии: основные сведения и клиническое применение. – М.: БИНОМ. Лаборатория знаний, 2012. – с. 404-409; «Кистозные опухоли поджелудочной железы: диагностика и лечение / В. А. Кубышкин, Г.Г. Кармазановский, С.А. Гришанков. – М.: Издательский дом Видар – М. 2013. – с.101-104, с.126, с.145).
А. Кубышкин, Г.Г. Кармазановский, С.А. Гришанков. – М.: Издательский дом Видар – М. 2013. – с.101-104, с.126, с.145).
Но для верификации диагноза псевдотуморозного панкреатита и злокачественных новообразований необходимо дополнительно проводить пункционную биопсию поджелудочной железы («Малоинвазивные технологии под ультразвуковой навигацией в современной клинической практике» под редакцией А.В. Борсукова и В.Н. Шолохова, Смоленск 2009 г. – с. 87-88).
Однако пункционная биопсия обладает рядом недостатков. Это инвазивность, плохая переносимость пациентами, противопоказания к проведению данной манипуляции.
Техническим результатом использования изобретения является упрощение верификации диагноза за счет проведения компрессионной эластографии одновременно с эндосонографией.
Сущность предлагаемого способа верификации диагноза заболеваний поджелудочной железы, включающего трансабдоминальное ультразвуковое исследование и эндосонографию, состоит в том, что одновременно с эндосонографией проводят компрессионную эластографию поджелудочной железы, последовательно устанавливая конвексный датчик при диффузном характере изменений в месте проекции головки поджелудочной железы, а именно: в нисходящей части, верхушке луковицы и в луковице 12-перстной кишки, в месте проекции тела поджелудочной железы в антральном отделе и теле желудка, в месте проекции хвоста поджелудочной железы в дне желудка, при очаговом характере изменений датчик поочередно устанавливают в месте проекции головки и тела поджелудочной железы в очаговой, перифокальной и внеперифокальных зонах, рассчитываются коэффициенты разницы компрессионной эластографии SR, и при коэффициенте разницы меньше 10 у.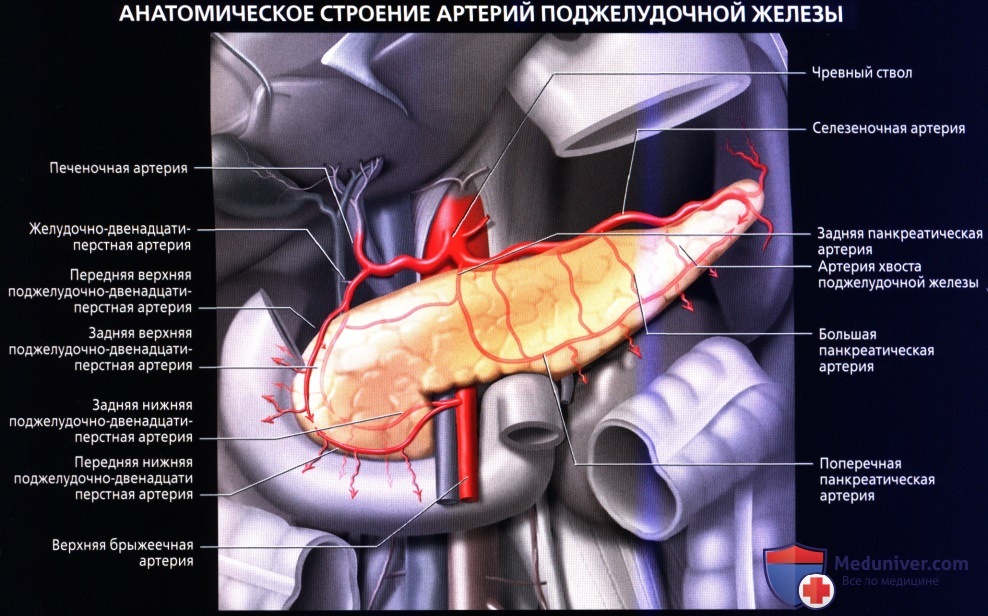 е. подтверждают диагноз хронического панкреатита, при коэффициенте разницы в пределах 11-25 у.е. – диагноз псевдотуморозного панкреатита, при коэффициенте разницы более 25 у.е. – злокачественное новообразование поджелудочной железы.
е. подтверждают диагноз хронического панкреатита, при коэффициенте разницы в пределах 11-25 у.е. – диагноз псевдотуморозного панкреатита, при коэффициенте разницы более 25 у.е. – злокачественное новообразование поджелудочной железы.
Способ осуществляют с помощью ультразвукового аппарата «HITACHI Prerius» и эндоскопа с конвексным датчиком «PENTAX EG 387OUTK».
После установки предварительного клинического диагноза проводят трансабдоминальное ультразвуковое исследование и эндосонографию поджелудочной железы, где уточняют диффузный или очаговый характер изменений в паренхиме.
При диффузном характере изменений (хроническом панкреатите и псевдотуморозном панкреатите) проводят компрессионную эластографию при эндосонографии по программе №1: в месте проекции головки поджелудочной железы, а именно: в нисходящей части, верхушке луковицы и в луковице 12-перстной кишки, в месте проекции тела поджелудочной железы в антральном отделе и теле желудка, в месте проекции хвоста поджелудочной железы – в дне желудка.
При очаговом характере изменений в паренхиме проводят компрессионную эластографию при эндосонографии по программе №2 в 3-х зонах: 1-ая зона – очаг, 2-ая – перифокальная зона, 3-я – внеперифокальная зона (зона неизмененной паренхимы органа), устанавливая конвексный датчик эндоскопа в зависимости от топографии очагового образования в область проекции головки, тела, хвоста поджелудочной железы.
По мере движения датчика от зоны к зоне рассчитываются коэффициенты разницы компрессионной эластографии SR, выдаваемые дисплеем аппарата. При коэффициенте разницы меньше 10 у.е. верифицируют диагноз хронического панкреатита, в пределах 11-25 у.е. – диагноз псевдотуморозного панкреатита, более 25 у.е. – злокачественное новообразование поджелудочной железы.
Пример №1: Больной Ф., 37 лет, история болезни № 4178
Госпитализирован в гастроэнтерологическое отделение ОГБУЗ «Клиническая больница №1» 27 сентября 2011 года с предварительным диагнозом: Обострение хроническго панкреатита. Эрозивный гастрит. В анамнезе сезонные обострения хронического гастрита, периодическое злоупотребление алкоголем.
Эрозивный гастрит. В анамнезе сезонные обострения хронического гастрита, периодическое злоупотребление алкоголем.
Жалобы: на снижение аппетита, боли ноющего характера в эпигастральной области, тошноту, слабость.
Объективно: кожные покровы телесного цвета, язык обложен белым налетом, в легких дыхание везикулярное, хрипов нет. Тоны сердца ритмичные. Живот мягкий, при пальпации болезненный в эпигастральной области. Печень по краю реберной дуги.
Общий анализ крови: умеренный лейкоцитоз.
Общий анализ мочи: без патологии.
Инфицирования гепатотропными вирусами не установлено: (HBsAg, antiHCV Ag отр.).
Биохимический анализ крови: общий белок 79 г/л, билирубин 15 мкм/л, АЛТ 44 ЕД/л, ACT 52 ЕД/л, ЩФ 98 ЕД/л, ГГТ 101 ЕД/л, α – амилаза 450 мкмоль/л, p – амилаза 155 мкмоль/л
Ультразвуковое трансабдоминальное исследование поджелудочной железы
Заключение. Размеры поджелудочной железы: головка 23 мм, тело 23 мм, хвост 19 мм. Контуры нечеткие, неровные. Выраженные диффузные изменения паренхимы поджелудочной железы. УЗ – признаки обострения хронического панкреатита? Псевдотуморозный панкреатит?
Контуры нечеткие, неровные. Выраженные диффузные изменения паренхимы поджелудочной железы. УЗ – признаки обострения хронического панкреатита? Псевдотуморозный панкреатит?
Эндосонография поджелудочной железы проводилась по стандартной методике с позиционированием конвексного датчика эндоскопа в проекции головки, тела и хвоста поджелудочной железы.
Заключение. Эндосонографические признаки выраженных диффузных изменений паренхимы поджелудочной железы. Вирсунгов проток – 5 мм (расширен) в головке и теле. Локальный панкреатостаз. Нельзя исключить формирование псевдотуморозного панкреатита.
При проведении компрессионной эластографии при эндосонографии поджелудочной железы конвексный датчик последовательно устанавливали по программе №1, а именно: в месте проекции головки поджелудочной железы, а именно в нисходящей части, верхушке луковицы и в луковице 12-перстной кишки, в месте проекции тела поджелудочной железы: в антральном отделе и теле желудка, в месте проекции хвоста поджелудочной железы – в дне желудка. При этом были получены следующие коэффициенты разницы SR: в головке поджелудочной железы 9,8 у.е., в теле – 8,2 у.е., в хвосте – 9,6 у.е., что подтвердило наличие хронического панкреатита.
При этом были получены следующие коэффициенты разницы SR: в головке поджелудочной железы 9,8 у.е., в теле – 8,2 у.е., в хвосте – 9,6 у.е., что подтвердило наличие хронического панкреатита.
Референтным методом для проверки полученных данных по эластографии поджелудочной железы явился метод пункционной биопсии поджелудочной железы с последующим гистологическим исследованием полученного биоптата.
Гистологическое исследование биоптата.
Заключение. В присланном материале из ткани поджелудочной железы (пункционная биопсия) морфологическая картина хронического панкреатита (стекло №23478). Данные морфологического исследования подтверждают диагноз хронического панкреатита.
Пример №2: Больной К., 49 лет, история болезни № 2450
Госпитализирован в хирургическое отделение ОГБУЗ «Клиническая больница №1» 18 мая 2012 года с предварительным диагнозом: Хронический панкреатит. В анамнезе имело место постоянное злоупотребление алкоголем.
Жалобы: на умеренную диспепсию, опоясывающие боли в эпигастральной области, тяжесть и ноющие боли в правом подреберье, сухость и горечь во рту, тошноту, выраженную общую слабость.
Объективно: кожные покровы бледные, в легких дыхание везикулярное, хрипов нет. Тоны сердца ритмичные, приглушены. Живот вздут, при пальпации болезненный в эпигастральной области. Печень выступает из-под края реберной дуги на 3,5 см.
Общий анализ крови: сдвиг лейкоцитарной формулы влево, умеренный лейкоцитоз.
Общий анализ мочи: без патологии.
Инфицирования гепатотропными вирусами не установлено: (HBsAg, antiHCV Ag отр.).
Биохимический анализ крови: общий белок 79 г/л, билирубин 15 мкм/л, АЛТ 58 ЕД/л, ACT 62 ЕД/л, ЩФ 100 ЕД/л, ГТТ 199 ЕД/л, α – амилаза 850 мкмоль/л, p – амилаза 190 мкмоль/л
Ультразвуковое трансабдоминальное исследование поджелудочной железы
Заключение. Размеры поджелудочной железы: головка 23 мм, тело 21 мм, хвост 22 мм. Диффузные изменения паренхимы поджелудочной железы, локальное уплотнение паренхимы поджелудочной железы. УЗ – признаки хронического панкреатита.
Диффузные изменения паренхимы поджелудочной железы, локальное уплотнение паренхимы поджелудочной железы. УЗ – признаки хронического панкреатита.
Эндосонография поджелудочной железы проводилась по стандартной методике с позиционированием конвексного датчика эндоскопа в проекции головки, тела и хвоста поджелудочной железы.
Заключение. Эндосонографические признаки диффузных изменений паренхимы поджелудочной железы, локального уплотнения головки и тела поджелудочной железы. Вероятнее, больше данных за хронический панкреатит.
При проведении компрессионной эластографии при эндосонографии поджелудочной железы конвексный датчик последовательно устанавливали по программе №1, а именно: в месте проекции головки поджелудочной железы, а именно в нисходящей части, верхушке луковицы и в луковице 12-перстной кишки, в месте проекции тела поджелудочной железы: в антральном отделе и теле желудка, в месте проекции хвоста поджелудочной железы – в дне желудка. При этом были получены следующие коэффициенты разницы SR: в головке поджелудочной железы 20 у. е., в теле – 19 у.е., в хвосте – 22 у.е. Коэффициент разницы верифицировал диагноз псевдотуморозного панкреатита.
е., в теле – 19 у.е., в хвосте – 22 у.е. Коэффициент разницы верифицировал диагноз псевдотуморозного панкреатита.
Референтным методом для проверки полученных данных по эластографии поджелудочной железы явился метод пункционной биопсии поджелудочной железы с последующим гистологическим исследованием полученного биоптата.
Гистологическое исследование биоптата.
Заключение. В присланном материале из ткани поджелудочной железы (пункционная биопсия) морфологическая картина псевдотуморозного панкреатита (стекло №295701). Данные морфологического исследования подтверждают диагноз псевдотуморозного панкреатита.
Пример №3: Больной И., 62 года, история болезни № 3642
Госпитализирован в хирургическое отделение ОГБУЗ «Клиническая больница №1» 10 августа 2013 года с предварительным диагнозом: Хронический панкреатит в стадии обострения. В анамнезе – злоупотребление алкоголем отрицает.
Жалобы: на слабость, недомогание, умеренную диспепсию, тяжесть и боли в эпигастральной области в течение дня, не связывает с приемом пищи. Аппетит снижен, тошнота.
Аппетит снижен, тошнота.
Объективно: в легких дыхание везикулярное, хрипов нет. Сердце – без особенностей. Живот мягкий, при пальпации болезненный в эпигастральной области. Печень не увеличена.
Общий анализ крови: повышено СОЭ, лейкопения.
Общий анализ мочи: без видимой патологии.
Биохимический анализ крови: общий белок 79 г/л, билирубин 15 мкм/л, АЛТ 38 ЕД/л, ACT 40 ЕД/л, ЩФ 78 ЕД/л, ГГТ 182 ЕД/л
Ультразвуковое трансабдоминальное исследование поджелудочной железы
Заключение. Размеры поджелудочной железы: головка 31 мм, тело 24 мм, хвост 20 мм. Размеры Вирсунгова протока – 4 мм. УЗ – признаки увеличения размеров головки поджелудочной железы, панкреатостаз. Выраженные диффузные изменения паренхимы поджелудочной железы, неоднородность структуры паренхимы. Панкреатостаз. Подозрение на псевдотуморозный панкреатит.
Эндосонография поджелудочной железы проводилась по стандартной методике с позиционированием конвексного датчика эндоскопа в проекции головки, тела и хвоста поджелудочной железы.
Заключение. В месте проекции головки поджелудочной железы очаговое образование до 10 мм, в теле до 11 мм эндосонографические признаки очагового образования головки поджелудочной железы, нельзя исключить очаговые образования тела. Выраженные диффузные изменения паренхимы поджелудочной железы, деформация главного панкреатического протока. Псевдотуморозный панкреатит? Злокачественное новообразование поджелудочной железы?
При проведении компрессионной эластографии при эндосонографии поджелудочной железы исследовали зону очага, перифокальную зону и внеперифокальную зону. Конвексный датчик эндоскопа в указанных зонах устанавливали в месте проекции головки и тела.
Были получены результаты: в головке поджелудочной железы 102 у.е., в теле – 98 у.е., в хвосте – 26 у.е. Коэффициент разницы подтвердил диагноз рака головки и тела поджелудочной железы.
Референтным методом для проверки полученных данных по эластографии поджелудочной железы явился метод пункционной биопсии поджелудочной железы с последующим гистологическим исследованием полученного биоптата.
Гистологическое исследование биоптата. Заключение. В присланном материале из ткани поджелудочной железы (пункционная биопсия) морфологическая картина аденокарциномы поджелудочной железы (стекло №156240). Данные морфологического исследования подтверждают диагноз рака поджелудочной железы (аденокарцинома).
В городском отделении диагностических исследований и малоинвазивных вмешательств при ОГБУЗ «Клиническая больница №1» предложенный способ верификации заболеваний поджелудочной железы применен у 27 больных.
Данные представлены в таблице.
Полученные данные проверялись референтным методом в гастроэнтерологии и хирургии: пункциями поджелудочной железы под ультразвуковым контролем у 19 пациентов. Данные имели статистически достоверную корреляционную связь между гистологическим заключением и данными компрессионной эластографии при эндосонографии выявленных изменений в поджелудочной железе.
Таким образом, проведение компрессионной эластографии одновременно с эндосонографией поджелудочной железы позволяет верифицировать злокачественные новообразования поджелудочной железы, своевременно и достоверно дифференцировать хронический и псевдотуморозный панкреатит.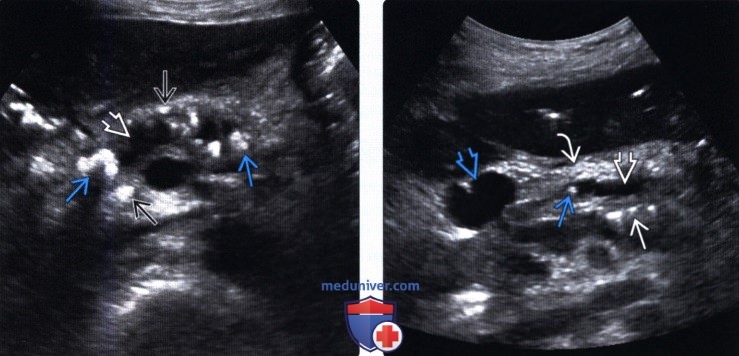 Способ отличается простотой, является малоинвазивным и достоверным, не требует дополнительных манипуляций, хорошо переносится больными и может найти широкое применение в клинической практике.
Способ отличается простотой, является малоинвазивным и достоверным, не требует дополнительных манипуляций, хорошо переносится больными и может найти широкое применение в клинической практике.
Ультразвуковое исследование
Ультразвуковое исследование (УЗИ) – неинвазивное исследование организма человека с помощью ультразвуковых волн. Ультразвуковой метод является высокоинформативным, безвредным (не несет лучевой нагрузки), доступным и точным. Метод дает возможность диагностировать большое количество заболеваний. Например: онкологические заболевания, хрофнические диффузные изменения в органах, диффузные изменения печени и поджелудочной железы, паренхимы почек, предстательной железы, визуализирует наличие конкрементов в почках и желчном пузыре, наличие аномалий внутренних органов и систем, определяет наличие свободной жидкости в брюшной полости, жидкостных образований в органах.
Противопоказания к УЗИ
Ультразвуковое исследование не имеет противопоказаний. Это всегда метод выбора для диагностики патологических состояний во время беременности. УЗИ не обладает лучевой нагрузкой, его можно повторять неограниченное число раз. С помощью УЗИ можно исследовать практически все органы и системы.
Подготовка
Исследование органов брюшной полости проводится натощак (предыдущий прием пищи не ранее чем за 6-8 часов до исследования), утром. Из рациона на 1-2 дня следует исключить продукты, содержащие клетчатку, бобовые, сырые овощи, черный хлеб, молоко. При наклонности к газообразованию рекомендован прием эспумизана, активированного угля по 1 таблетке 3 раза в день, других энтеросорбентов, фестала. Если пациент с сахарным диабетом, то допустим легкий завтрак (теплый чай, подсушенный белый хлеб). Для выполнения трансабдоминального исследования органов малого таза (мочевого пузыря, матки или предстательной железы) необходимо наполнение мочевого пузыря. Рекомендуется воздержание от мочеиспускания в течение 3-х часов до исследования или прием 300-500 мл воды за 1 час до исследования. При проведении внутриполостного исследования (через влагалище у женщин – ТВУЗИ, или через прямую кишку у мужчин – ТРУЗИ), наоборот, необходимо опорожнить мочевой пузырь. Ультразвуковые исследования сердца, сосудов, щитовидной железы не требуют специальной подготовки.
Как проходит обследование
Врач или медсестра пригласят Вас в кабинет ультразвуковой диагностики, и предложит Вам лечь на кушетку, обнажив исследуемую часть тела. Для наилучшего проведения ультразвуковых волн врач нанесет на кожу специальный гель, который не содержит никаких лекарственных средств и является абсолютно нейтральным для организма.
Во время исследования врач будет прижимать к телу в разных положениях ультразвуковой датчик. Изображения будут отображаться на мониторе и печататься на специальную термобумагу.
При исследовании сосудов будет включена функция определения скорости кровотока с помощью режима допплеровского исследования. В этом случае исследование будет сопровождать характерный звук, отражающий движение крови по сосуду.
На УЗИ мы можем исследовать:
Щитовидную железу. В настоящее время ультразвуковое исследование щитовидной железы является ведущим и позволяет выявить диффузные изменения паренхимы, визуализировать наличие кист, узловых образований, изменения размера железы.
Печень. Желчный пузырь и желчные протоки.
УЗ-исследование печени является высокоинформативным. Во время исследования врач оценивает размеры, структуры паренхимы, однородность, наличие очаговых образований. Метод позволяет выявить диффузные заболевания с высокой точностью и специфичностью (гепатит, жировая дистрофия, цирроз), очаговые образования (опухолевые образования, кисты). – выявление метастатического поражения печени при злокачественных опухолях любой локализации.
Исследование желчного пузыря и желчных путей.
Когда оценивается состояние желчного пузыря и протоков, оцениваются размеры, проходимость, толщина стенок, наличие конкрементов. УЗИ позволяет с точностью определить наличие конкрементов в полости желчного пузыря.
Поджелудочную железу.
Сложный для диагностики орган. При исследовании поджелудочной железы оцениваются размеры, форму, контуры, наличие образований, состояние паренхимы органа. – диагностика очаговых и диффузных заболеваний (опухоли, кисты, воспалительные процессы)
Также в настоящее время ультразвуковое исследование играет важную роль в постановке диагноза заболеваний внутренних органов, таких как:
Шея:
1. Исследование щитовидной железы.
2. Исследование слюнных желез.
3. Исследование лимфатических узлов.
– подозрение на их метастатическое поражение при выявленной злокачественной опухоли любого органа.
4. Неорганные образования шеи (опухоли, кисты).
Грудь:
Исследование молочных желез.
– уточнение неопределенных рентгенологических данных
– дифференциация кист и тканевых образований, выявленных при пальпации.
– оценка состояния молочных желез при увеличении подмышечных, под- и надключичных л\у.
Органы живота:
1. Исследование паренхиматозных органов пищеварительной системы (печень, поджелудочная железа)
2. Исследование почек и мочевых путей.
– диагностика различных заболеваний и выраженности изменений.
– выявление злокачественных новообразований и оценка распространенности процесса.
– изменения в анализе мочи.
Исследование лимфатических узлов.
– выявление их метастатического поражения при злокачественном процессе.
– лимфаденопатии.
Исследование органов малого таза.
1.Исследование мочевых путей (мочеточник, мочевой пузырь)
– диагностика различных заболеваний.
– определение остаточной мочи в мочевом пузыре.
2. Исследование предстательной железы (трансабдоминально)
– диагностика различных заболеваний
– определение стадии доброкачественной гиперплазии предстательной железы.
Диффузные изменения паренхимы печени и поджелудочной железы
Диффузные изменения паренхимы печени и поджелудочной железы являются частой находкой при ультразвуковой диагностике. Они представляют собой равномерное изменение плотности тканей, распространяющееся на всю поджелудочную железу и печень. Данное заключение врача ультразвуковой диагностики говорит о патологии этих органов.
Диффузные изменения паренхимы печени и поджелудочной железы нередко сочетаются и могут быть реактивными, например, при болезнях печени встречается реактивный панкреатит. Обнаружив такую «ультразвуковую картину», с большой вероятностью можно исключить у больного опухоль, кисту или камни, поскольку подобные образования «дают» локальные (очаговые) изменения плотности тканей.
Результат ультразвуковой диагностики не является диагнозом, поэтому пациент нуждается в подробнейшем обследовании у терапевта либо гастроэнтеролога. Диффузные изменения плотности и эхогенности (способности отражать эхо-сигнал) часто сочетаются с изменением размеров органов.
При уменьшении эхогенности и плотности поджелудочной в совокупности с увеличением её размеров можно подозревать острый панкреатит. Если размер печени неизмененный, то гораздо выше вероятность того, что панкреатит хронический. Когда воспаление приводит к превращению железистой ткани поджелудочной железы в фиброзную, при УЗ- исследовании обнаруживается диффузное (распространенное по всему органу) увеличение плотности при обычном либо уменьшенном размере органа.
Болезни печени (гепатиты, стеатоз, цирроз, обменные поражения) и сердечная недостаточность также сопровождаются диффузными изменениями печеночных тканей. Как и при заболеваниях поджелудочной железы, подобные изменения не являются специфичными, доктор ультразвуковой диагностики не может достоверно указать причину их появления.
Получив заключение узиста «Диффузные изменения паренхимы печени и поджелудочной железы», врач-клиницист выяснит происхождение этих изменений. Больному назначат анализы крови — общий, биохимический, дополнительные инструментальные исследования.
Так же следует отметить, что практически у всех пациентов с 20-30 лет выявляют подобные изменения, что может быть связано с несовершенностью метода или все же с тем, что наши внутренние органы существенно страдают от того, что мы едим и пьем уже смолоду.
Не стоит бить тревогу, если у вас вывили подобные изменения, но и не стоит ими пренебрегать, проконсультируйтесь с гастроэнтерологом и постройтесь питаться правильно.
Визуализация поджелудочной железы: Часть 1
Поджелудочная железа – забрюшинный орган, расположенный глубоко в брюшная полость и труднодоступна при физикальном осмотре. Поджелудочной железы патологии имеют множество проявлений, что позволяет поставить их диагноз сложно для врачей. 1 Визуализация играет важную роль в оценка заболеваний поджелудочной железы и предоставляет ценную информацию клиницистам, тем самым диктуя важные управленческие решения. Технологические достижения в мультидетекторной компьютерной томографии (МДКТ) и магнитно-резонансная томография (МРТ) в сочетании с инновациями в Возможности трехмерной (3D) визуализации революционизировали роль визуализация в ведении пациентов с заболеваниями поджелудочной железы.Визуализация больше всего часто выполняется для лечения пациентов с панкреатитом и подозрением на новообразования поджелудочной железы.
В части 2 этой статьи, доступно на www.appliedradiology.com, продолжается обсуждение визуальных проявлений различных аномалии, влияющие на поджелудочную железу, поскольку они связаны с определенными типами панкреатит, новообразования поджелудочной железы и опухоли.
Нормальная анатомия и физиология
поджелудочная железа – забрюшинный орган, расположенный в переднем отделе надпочечников. пространство кзади от желудка и ограниченное С-образной петлей двенадцатиперстной кишки на правая сторона.Поджелудочная железа делится на головку, крючковидный отросток, шея, тело и хвост. Головка расположена внутри дуоденальной С-образной петли, в то время как хвост лежит в воротах селезенки немного выше головы. Поскольку поджелудочная железа некапсулирована, происходит беспрепятственное распространение опухоль и воспаление окружающих структур. Сплено-воротная вена слияние лежит сразу кзади от шейки поджелудочной железы и кпереди от крючковатый отросток. Селезеночная вена проходит вдоль заднего прохода. части тела и хвоста поджелудочной железы, в то время как чревная артерия относящиеся черепно к шейке поджелудочной железы.Верхняя брыжеечная артерия (СМА) берет начало от аорты на уровне шейки поджелудочной железы. Голова получает артериальное кровоснабжение из общей печеночной артерии. через ветви гастродуоденальной артерии (GDA) – переднюю и заднюю верхняя панкреатико-дуоденальная ветвь и нижняя SMA панкреатико-дуоденальные ветви. Они образуют обширную артериальную сеть. вокруг головки поджелудочной железы. Тело и хвост поджелудочной железы снабжается ветвями селезеночной артерии, в том числе дорсальной поджелудочная артерия. 2
Поджелудочная железа состоит из двух функции, эндокринные и экзокринные. От восьмидесяти до 95% поджелудочной железы паренхима состоит из ацинарных клеток, которые предназначены для экзокринные функции производства и секреции пищеварительных ферментов, таких как трипсиноген, липаза. и амилаза. 3 Любопытно отметить что в то время как подавляющая часть паренхимы поджелудочной железы ацинарно-клеточная карцинома, состоящая из ацинарных клеток, встречается крайне редко. подтип рака поджелудочной железы (<1% всех опухолей поджелудочной железы). 4 Только от 5% до 20% паренхимы поджелудочной железы отвечает за эндокринная функция, состоящая из клеток, сгруппированных в островки Лангерганса, которые производят гормоны, такие как инсулин, глюкагон и соматостатин.
Развитие и варианты
Эмбриологически, поджелудочная железа возникает из дорсальной и вентральной зачатков поджелудочной железы. В более крупный спинной зачаток является предшественником передней части головы в виде а также тело и хвост, в то время как меньшая брюшная почка развивается в задняя головка и крючковидный отросток.Дорсальный и вентральный протоки соединяются в один большой проток, проток Вирсунга, который впадает в двенадцатиперстная кишка вместе с общим желчным протоком у ампулы Фатера. 1 Вариации схемы разветвления протоков поджелудочной железы являются обычным явлением. (Фигура 1). Один из распространенных вариантов – наличие аксессуара. проток поджелудочной железы, известный как проток Санторини, который впадает в двенадцатиперстная кишка отдельно от основного протока поджелудочной железы через малый сосочек, который превосходит ампулу. Другой вариант – так называемый дорсальный доминантный дренаж, где проток Вирсунга впадает в малый сосочек и проток Санторини впадают в большой сосочек.Это похоже на деление поджелудочной железы, которое присутствует примерно в 10% нормальные люди. Однако в делении поджелудочной железы наблюдается полная разделение дорсального и вентрального протоков поджелудочной железы. 5 Ан описана связь между делением поджелудочной железы и панкреатитом. и считается, что это связано с относительной обструкцией спинного протока поджелудочной железы, который переносит пищеварительные ферменты из большинства железы и опорожняется через более мелкие второстепенные сосочки. 6 Это, однако это противоречиво, и другие авторы считают, что поджелудочная железа divisum не является причиной панкреатита, а только ассоциирован с другими известными генетическими причинами острого и хронического панкреатита, такими как как мутации, связанные с CTFR, SPINK1 и PRSS1. 7 Кольцевое поджелудочной железы может возникнуть во время вращения брюшной зачатка поджелудочной железы, так как она сливается со спинным зачатком, образуя кольцо ткани поджелудочной железы окружает двенадцатиперстную кишку, вызывая закупорку выходного отверстия желудка у младенцев и панкреатит у взрослых (рис. 2).
Визуализация
Рентгенограмма простая
Рентгенография играет ограниченную роль в визуализации поджелудочной железы, но иногда может изображают кальцификаты паренхимы, что помогает в обнаружении хронический панкреатит.Однако точечные кальцификаты возле поджелудочной железы можно спутать с обызвествлением селезеночной артерии. У пациентов с панкреатит, описаны несколько простых рентгенологических признаков, включая так называемый «признак отсечения толстой кишки», характеризующийся резким прекращение газовой тени толстой кишки при изгибе селезенки.
УЗИ
УЗИ (США) также играет ограниченную роль в оценке состояния поджелудочной железы как вышележащий газ из поперечной ободочной кишки и желудка делает визуализацию панкреатической паренхима затруднена или даже невозможна.Однако США могут помочь определить камни в желчном пузыре как этиология у больных панкреатитом и желчнокаменной болезнью. расширение протоков у пациентов с опухолью головки поджелудочной железы. Самый центральный Поражения поджелудочной железы гипоэхогенны по сравнению с нормальной паренхимой. В появление эндоскопического УЗИ (EUS) добавило новое измерение, поскольку оно обеспечивает изображения сверхвысокого разрешения и изысканные детали опухолей поджелудочной железы, особенно при кистозных поражениях. Кроме того, EUS позволяет одновременно отбор образцов ткани поражений поджелудочной железы с помощью тонкой иглы под контролем EUS аспирация (FNA).Однако приобретение и интерпретация этих изображения обычно выполняются интервенционными гастроэнтерологами и выходят за рамки данной статьи.
Мультидетектор CT
MDCT – это метод выбора для оценки воспалительных и неопластических состояний поджелудочной железы. 2 дюйма воспалительные процессы, MDCT не только обеспечивает отличную визуализацию паренхиматозных аномалий, но четко показывает внепанкреатическое распространение болезни.При новообразованиях поджелудочной железы, MDCT точно отображает морфологию опухоли, анатомию протока и ее отношение к окружающим органам и сосудистым структурам. Тонкое сечение MDCT в сочетании с методами обработки изображений (многоплоскостной реконструкций и криволинейных преобразований) могут обеспечить дополнительную визуализацию детали и могут определить анатомию протока поджелудочной железы.
Техника
конкретный протокол визуализации MDCT зависит от клинического вопроса, который необходимо решить. ответил. Типичный протокол MDCT для оценки поджелудочной железы включает: введение перорального и внутривенного контраста (таблица 1).Для рутины показания, включая панкреатит, КТ брюшной полости в фазе воротной вены с положительным пероральным контрастным веществом (POCM) предоставляет наибольшую информацию. Однако для специализированного протокола КТ поджелудочной железы нейтральный пероральный контраст носители (NOCM), такие как вода, являются предпочтительными, поскольку они обеспечивают превосходное изображение реконструкция. 8 У пациентов с подозрением на новообразование поджелудочной железы a Выполняется сфокусированная протокольная КТ поджелудочной железы, которая включает панкреатическая, воротная венозная и отложенная фаза через печень для оценить метастазы в печени.Артериальная фаза может выполняться в место панкреатической фазы, если гиперваскулярное поражение поджелудочной железы, подобное подозревается нейроэндокринная опухоль. Панкреатическая фаза относится к позднему артериальная фаза (обычно 40-45 секунд после введения контрастного вещества) во время что есть максимальная дифференциация между нормальной паренхимой и гиподензивные опухоли поджелудочной железы, такие как аденокарцинома. Эта фаза также обеспечивает оптимальное помутнение артериальных и брыжеечных вен, что позволяет оценить сосудистое поражение, тем самым позволяя хирургическое вмешательство планирование путем оценки потенциальной резектабельности опухоли.Артериальный помутнение на этом этапе ограничивает потребность в отдельном выделенном артериальная фаза. Точная синхронизация контрастности для получения изображения во время различные фазы могут быть достигнуты с помощью тестового болюса или автоматического болюсный запуск.
МРТ
Магнитный появилась резонансная томография (МРТ) с холангиопанкреатографией (MRCP) как надежный инструмент для точной характеристики панкреатической патологии. Превосходное разрешение мягких тканей и контрастность. к МРТ делает его превосходным тестом для оценки морфологических особенностей опухолей поджелудочной железы, особенно кисты поджелудочной железы.MRCP обеспечивает отличное двухмерное (2D) и трехмерное (3D) изображение анатомия протока поджелудочной железы и ее аномалии у пациентов с панкреатит, а также новообразования.
Техника
Типичный Используемые последовательности изображений включают аксиальные T1-взвешенные изображения с и без насыщения жира, используя задержку дыхания или закрытое дыхание. А полная оценка паренхимы поджелудочной железы и панкреатико-билиарной системы Система протоков может выполняться в следующих последовательностях: Т1-взвешенное градиентное эхо, Т2-взвешенное (T2W) аксиальное и корональное последовательности, либо быстрое спин-эхо (FSE), либо турбо-спиновое эхо (TSE), 2D и 3D MRCP; и Т1-взвешенное трехмерное градиентное эхо до и после гадолиния.Чтобы адекватно визуализировать желчный пузырь и оценить экзокринную ответ на секретин, в идеале пациент должен голодать в течение 4 часов. Отрицательный пероральный контраст вводится для уменьшения сигнала от над желудком и двенадцатиперстной кишкой. Аксиальные и корональные Т2 изображения с и без жирового насыщения. изображения должны быть получены через 25, 70 и 120 секунд после гадолиния контрастная инъекция. В идеале напряженность поля должна быть ≥ 1,0 Тесла при быстрые последовательности изображений.Стандартный протокол лечения поджелудочной железы также включает: Изображения MRCP для дальнейшей оценки патологии протоков поджелудочной железы. Последовательность MRCP может быть двухмерной (2D) или двухмерной. Трехмерное (3D) получение. 3D MRCP создает изображения с высоким разрешением анатомии панкреатобилиарного протока в виде тонких срезов без срез 3D-техники позволяет лучше оценить мелкие камни, боковые ветви главного протока поджелудочной железы и внутрипеченочные желчные протоки. 2D MRCP можно получить либо в виде однократного однократного быстрого отжима толстых плит. эхо-последовательность T2W или многосекционная, тонкая, однократная FSE T2W последовательность.Последовательность 3D быстрого спинового эхо-сигнала может быть получена как серия задержек дыхания или во время свободного дыхания. Secretin MRCP – это модифицированная последовательность MRCP, что влечет за собой введение секретина в стимулируют экзокринную функцию поджелудочной железы. Секретин MRCP полезен при оценке сложных аномалий протоков и количественно или полуколичественно оценить экзокринную функцию поджелудочной железы.
Обычный вид
Вкл. УЗИ, поджелудочная железа немного эхогенная по сравнению с печенью и имеет однородный внешний вид.На MDCT нормальная поджелудочная железа немного выше затухание, чем параспинальные мышцы, и имеет дольчатый контур. На при введении контраста, он усиливается довольно однородно (до 100-150 HU) с небольшими различиями в затухании (<30 HU) между головками и хвост, что может быть нормальным вариантом. 9 Жировая инфильтрация поджелудочной железы может возникнуть при нормальном старении, но также наблюдается при патологические состояния, такие как ожирение, муковисцидоз и реже состояния, такие как синдром Швахмана-Даймонда и Джонсон-Близзард синдром (рисунок 3). 2
Нормальная поджелудочная железа самый высокий внутренний сигнал T1 среди всех органов брюшной полости и, следовательно, преконтрастные T1-взвешенные изображения являются наиболее чувствительной последовательностью для обнаружения очаговые поражения, которые часто гипоинтенсивны по сравнению с нормальными паренхимы и для обнаружения кровоизлияния в воспалительный коллекции. На T2-взвешенных изображениях поджелудочная железа немного гиперинтенсивны по сравнению с соседними мышцами, и они оптимально подходит для изображения анатомии протока, кистозных поражений и островковых клеток опухоли, которые являются гиперинтенсивными по сравнению с нормальной поджелудочной железой. 5
Воспалительные заболевания
Острый панкреатит
острый панкреатит – острое обратимое воспаление поджелудочной железы. паренхима. Примерно 200000 пациентов с этим заболеванием ежегодно попадает в больницу в Соединенных Штатах (США). 10 Это вызвано преждевременной активацией пищеварительных ферментов в паренхима поджелудочной железы, приводящая к перевариванию поджелудочной железы и перипанкреатические ткани. Этиология острого панкреатита включает: камни в желчном пузыре (40%), злоупотребление алкоголем (30% -35%) и идиопатические причины (20%).Другая этиология включает механическую (после ЭРХПГ, травмы), метаболическую (гиперкальциемия, гипертриглицеридемия, муковисцидоз и наследственные панкреатит) и токсическим (такие препараты, как ГХТЗ и аспаригиназа). 1 Общая смертность от панкреатита составляет от 2% до 10%, но большинство (70-80%) пациенты страдают легким или отечным панкреатитом, который обычно это самоизлечивающееся заболевание со смертностью <1%. На с другой стороны, примерно 25% пациентов испытывают тяжелые панкреатит, связанный с высокой заболеваемостью и смертностью ставка от 10% до 23%.Дихотомия между этими двумя исходами такова: сильно коррелирует с наличием или отсутствием панкреонекроза, что наблюдается почти в 20% всех случаев. 11 поджелудочной железы некроз вызван нарушением микроциркуляции через некротизацию васкулит и тромбоз и является важным прогностическим показателем. Смертность повышается со степенью панкреонекроза и смертности. частота> 50% наблюдается, когда некроз поражает> 30% панкреатической паренхима. 12 Некротическая ткань может вторично инфицироваться из-за транслокации кишечной флоры и почти всегда приводит к летальному исходу, если ее не лечить. 13 Лечение обычно включает хирургическую обработку раны или чрескожный дренаж.
Визуализация при остром панкреатите
Диагноз острый панкреатит часто основан на клинических и лабораторных данных. Визуализация поэтому проводится у пациентов с панкреатитом не для диагностики но по следующим причинам: (i) для выявления возможной этиологии (например, камни в желчном пузыре или новообразование), (ii) для оценки степени тяжести, (iii) для оценить осложнения и (iv) выявить возможные отличительные особенности визуализации при особых типах панкреатита, таких как тропический панкреатит, аутоиммунный панкреатит или желобчатый панкреатит. 2,9 Кроме того, было показано, что КТ лучше предсказывает осложнений, смертности и продолжительности пребывания в больнице, чем Критерии Рэнсона или APACHE II. 14
MDCT является предпочтительным методы визуализации и введение контрастного вещества необходимы для обнаружения осложнения, такие как некроз паренхимы, венозный тромбоз и артериальная псевдоаневризма. МДКТ брюшной полости с одной портальной венозной фазой – это выполняется в обычных случаях, но сканирование артериальной фазы обязательно при подозрении на псевдоаневрим.Диапазон показателей поджелудочной железы и классификация КТ представлена в Таблице 2. Легкий или ранний панкреатит (Степень A) является скрытым на КТ, и результаты визуализации отстают от клинических и лабораторные данные. Панкреатит степени B характеризуется диффузным или очаговое увеличение поджелудочной железы, при перипанкреатическом воспалительном процессе изменения, в том числе размытие края поджелудочной железы, скручивание прилегающий жир и незначительное снижение плотности паренхимы из-за отека Панкреатит inGrade C (рисунок 4). Утолщение передних отделов почек. фасция (фасция Героты) также видна и является ранним и чувствительным индикатор перипанкреатического воспаления.МРТ обычно выполняется при оценка этиологии, например, камней в желчном пузыре или деления поджелудочной железы. В Результаты визуализации включают потерю нормальной гиперинтенсивности Т1 с неоднородные гипоинтенсивные участки. На изображениях с подавлением жира на T2 могут быть небольшие количество перипанкреатической жидкости.
Осложнения
Некроз
Точно обнаружение некроза поджелудочной железы имеет первостепенное значение при визуализации панкреатит. Как на MDCT, так и на МРТ некроз поджелудочной железы выглядит как диффузные или очаговые паренхиматозные области без усиления (рис. 5).Кроме того, МРТ показывает области кровоизлияния в некротических очагах как нечеткие области высокого T1 и низкого T2 сигнала. На MDCT ложное срабатывание диагноз может быть результатом областей пониженного затухания из-за очагового замещение жировой ткани, отек или скопление внутрижелудочной жидкости. Ложь отрицательные результаты сканирования иногда возникают, когда визуализация выполняется на ранних этапах фаза воспаления поджелудочной железы (первые 12-24 часа после появления симптомов начало). Хотя некроз возникает рано, ложноотрицательный результат может быть уменьшается, если КТ выполняется через 72 часа после появления симптомов.В целом, MDCT сообщалось, что точность 87% и специфичность 100% обнаружение некроза с поражением> 30% железы. 9
Забор жидкости / псевдокиста
острый скопления жидкости часто возникают у пациентов с панкреатитом, и наличие скоплений жидкости увеличивает степень КТ панкреатита. Псевдокисты – наиболее частые воспалительные кистозные поражения поджелудочной железы. и содержат некротический мусор из переваренного забрюшинного жира. Пока их окончательный диагноз требует стремления содержания показать высокий уровень амилазы, предшествующий панкреатит в анамнезе с типичным особенности визуализации, такие как скопление жидкости с отчетливым волокнистым капсула, сохраняющаяся более 4 недель, позволяет уверенно предположить диагноз.Псевдокисты могут иметь множество визуальных проявлений, начиная от морфология от однокамерного до многокамерного. Увеличение стенки кисты обычно наблюдается на MDCT. На МРТ они обычно изменчивы, но низкие. сигнал на T1-взвешенных изображениях и высокий сигнал на T2-взвешенных изображениях. Кровоизлияние и инородный мусор могут вызвать атипичный вид, приводящий к увеличенный сигнал T1 и уменьшенный сигнал T2 по сравнению с простым появлением псевдокисты. Многие псевдокисты демонстрируют связь с основными проток поджелудочной железы, лучше всего виден с помощью ERCP или MRCP. 2 Псевдокисты обычно лечат консервативно, если нет осложнений, такие как массовый эффект, инфекция и разрыв, приводящий к перитониту, возникают (рисунки 6 и 7). Газ в псевдокисте не доказывает инфекционное заболевание; эта визуализация также может быть связана с кишечным свищом или недавнее вмешательство. Чрескожный, эндоскопический или открытый хирургический дренаж варианты лечения.
Сосудистые осложнения
Утечка пищеварительных ферментов поджелудочной железы может вызвать переваривание стенки окружающие артерии, приводящие к ослаблению и псевдоаневризме формация (рисунок 8).Чаще всего поражается селезеночная артерия, затем следует желудочно-дуоденальная артерия, чревная артерия или SMA. Они есть с высоким риском кровотечения и срочного хирургического или сосудистого необходима интервенционная радиологическая оценка. Поджелудочной железы и перипанкреатическое воспаление может распространяться на окружающие венозные структуры приводит к тромбозу, который проявляется дефектом наполнения пораженный сосуд во время портальной венозной фазы.
Хронический панкреатит
Пока традиционно хронический панкреатит считался отдельным субъект от острого панкреатита, учитывая, что повторяющиеся эпизоды острого панкреатит иногда приводит к хроническому панкреатиту, острому и теперь считается, что хронический панкреатит относится к спектру аналогичных болезнь. 15
Хронический панкреатит с проявлением необратимый фиброз, атрофия, внешнесекреторная и эндокринная недостаточность поджелудочной железы, клинически может проявляться мальабсорбцией и диабетом.
Результаты визуализации
MDCT является предпочтительным модальность изображения хронического панкреатита благодаря лучшей визуализации кальцинозы (рисунок 9). Кальцификаты поджелудочной железы могут быть паренхиматозными. или протокового происхождения. Железа может стать очаговой или диффузной атрофией. Расширение протока поджелудочной железы с бусинчатым видом – это характерный вид при хроническом панкреатите.Иногда хронический панкреатит может привести к воспалительной псевдомассе, вызывающей очаговую увеличение с фиброзом и гипоусилением и воспалительное сужение общего желчного протока, который может имитировать аденокарциному. Присутствие кальцификации и плавное сужение CBD позволяют дифференциация воспалительной псевдомассы от аденокарциномы, которая приводит к резкому сужению общего желчного протока. 2 МРТ результаты похожи на внешний вид MDCT. Однако поджелудочная кальцификации плохо видны на МРТ.Воспалительная псевдомасса имеет снижение интенсивности сигнала на T1-взвешенных изображениях вследствие фиброза и снижение содержания белка в железе из-за атрофии. Расширение боковые ветви поджелудочной железы более очевидны на МРТ, чем на КТ, и могут вызывать появление на МРХП так называемой «жемчужной нити» или «цепи озер». 5
Список литературы
- Хрубран Р., Виленц Р. Поджелудочная железа. В: Кумар В., Аббас А.К., Фаусто Н., ред. Роббинс и котран Патологические основы болезни 7-е изд.Филадельфия, Пенсильвания: Эльзевьер Сондерс; 2005: 939-953.
- Leyendecker JR, Олифант М. Поджелудочная железа. В: Dalrymple NC, Leyendecker JR, Oliphant M, ред. Решение проблем при визуализации брюшной полости . Филадельфия, Пенсильвания: Мосби Эльзевьер; 2009.
- Марино С., Горелик Ф. Панцирные и слюнные железы. В: Boron W, Boulpaep E eds. Медицинская физиология: клеточный и молекулярный подход . Филадельфия, Пенсильвания: Эльзевьер; 2005: 908-926.
- Mulkeen A, Yoo, P, Cha C.Реже новообразования поджелудочной железы. World J Gastroenterol. 2006; 12: 3180-3185.
- Roth CG, Deshmukh S. МРТ панкреатобилиарной системы. В: Roth CG ed. Основы МРТ тела . Филадельфия, Пенсильвания: Эльзевьер Сондерс; 2012: 129–199.
- Shanbhogue A, Fasih N, Surabhi V, et al. Клинико-рентгенологический обзор необычных типов и причин панкреатита . Рентгенография. 2009; 29: 1003-1026.
- Пеццилли Р.Делительная поджелудочная железа и острый или хронический панкреатит. JPancreas. 2012; 13: 118-119.
- Бреннан Д.Д., Замбони Дж., Раптопулос В., Крускал Дж. Компрехенисве предоперационная оценка аденокарциномы поджелудочной железы с 64-секционным объемная КТ. Рентгенография . 2007; 27: 1653-1666.
- Balthazar EJ. Острый панкреатит: оценка степени тяжести с помощью клинической и компьютерной томографии. Радиология. 2002; 223: 603-613.
- Сингла А., Чикес Н., Саймонс Дж. И др.Объем общенациональной больницы при неотложной помощи панкреатит: Анализ общенациональной стационарной выборки 1998-2006 гг. . HBP (Оксфорд) . 2009; 11: 391-397.
- Baron TH, Morgan DE. Острый некротический панкреатит. N Engl J Med . 1999; 340: 1412-1417.
- Balthazar EJ, Робинсон DL, Megibow AJ, Ransson JH. Острый панкреатит: значение КТ для установления прогноза. Радиология. 1990; 174: 331-336.
- Banks PA. Зараженный некроз: заболеваемость и терапевтические последствия. Гепатогастоэнтерология. 1991; 38: 116-119.
- Леунг Т.К., Ли С.М., Лин С.И. и др. Индекс тяжести компьютерной томографии составляет превосходит критерии Рэнсона и систему оценок APACHE II в прогнозировании исход острого панкреатита. World J Gastroenterol. 2005; 11: 6049-6052.
- Braganza J, Lee S, McCloy R, McMahon M. Хронический панкреатит. Ланцет . 2011; 377: 1184-1197.
журналов поджелудочной железы | Список проиндексированных статей
JOP – это рецензируемый журнал с открытым доступом, который два раза в месяц публикует рукописи по соответствующим темам, включая этиологию, эпидемиологию, профилактику, генетику, патофизиологию, диагностику, хирургическое и медицинское лечение заболеваний поджелудочной железы, включая рак, воспалительные заболевания, сахарный диабет, клиническую практику. панкреатология, внутренние болезни, клинические исследования, желудочно-кишечная хирургия, эндокринология, гепатология, лечение острого панкреатита, диабета, протоковой аденокарциномы поджелудочной железы и ее лечения, хронического панкреатита, нейроэндокринной опухоли, муковисцидоза и других врожденных заболеваний.
Представленные материалы включают оригинальные исследования, тематические исследования, нововведения в разработке программ, научные обзоры, теоретический дискурс и обзоры книг. Кроме того, Журнал поощряет представление ответственных предположений и комментариев. JOP. Журнал поджелудочной железы предоставляет актуальные обзоры и обновления, относящиеся к аномалиям поджелудочной железы и терапии, а также текущие аннотированные обзоры исследований, опубликованные в других местах, что делает журнал уникальным и ценным справочным ресурсом. Редакционная коллегия состоит из международных корифеев, которым поручено предоставлять читателям самую свежую информацию, которая будет иметь большое значение для всех, кто работает в области исследований поджелудочной железы.
The JOP. Journal of Pancreas следует процессу простого слепого рецензирования для проверки качества и ценности каждой полученной рукописи. Рецензирование осуществляется под эгидой членов редакционной коллегии журнала. После первичной проверки качества каждая статья рецензируется сторонними экспертами под руководством назначенного редактора. Утверждение по крайней мере двух независимых рецензентов с последующим одобрением редактора является обязательным для принятия любой заявки.
Цитирование
Журнал индексируется: EBSCO, CNKI, ICMJE, THOMSON REUTERS ESCI (EMERGING SOURCES CITATION INDEX), COSMOS, BRITISH LIBRARY и University of Zurich – UZH
Связано с
Сеть сторонников панкреатита
Греческое общество печени, поджелудочной железы и желчных путей
Белорусский панкреатический клуб
Заявление об открытом доступе
Это журнал с открытым доступом, который позволяет бесплатно получить весь контент для отдельного пользователя или любого учреждения.Пользователям разрешается читать, скачивать, копировать, распространять, распечатывать, искать или ссылаться на полные тексты статей или использовать их для любых других законных целей без предварительного разрешения издателя или автора при условии, что автор предоставлен должный кредит там, где это необходимо. Это соответствует определению открытого доступа BOAI.
Поджелудочная железа
Поджелудочная железа – это длинная плоская железа, расположенная в брюшной полости за желудком. Он производит несколько важных ферментов, которые попадают в тонкий кишечник и помогают пищеварению.Поджелудочная железа также содержит кластеры клеток, называемые островками. Клетки этих островков вырабатывают гормоны, такие как инсулин и глюкагон, которые помогают контролировать уровень глюкозы (типа сахара) в крови.
Связанные журналы поджелудочной железы
Поджелудочная железа, панкреатология, Журнал гепато-билиарно-панкреатических наук, гепатобилиарные и панкреатические заболевания International
Панкреатит
Панкреатит – это воспаление поджелудочной железы. Поджелудочная железа – это длинный ровный орган, расположенный за животом в верхней части живота.Поджелудочная железа вырабатывает ферменты, которые помогают пищеварению, и гормоны, которые помогают управлять процессом обработки сахара (глюкозы) вашим организмом. Поджелудочная железа может протекать как острый панкреатит, так и хронический панкреатит.
Связанные журналы панкреатита
Панкреатология, Медицинский журнал Новой Англии, Журнал гепато-билиарно-панкреатических наук, Международный вестник гепатобилиарных и панкреатических заболеваний
Функция поджелудочной железы
Поджелудочная железа – это две железы, которые тесно перемешаны в один орган.Первый функциональный компонент – «экзокринный», а второй функциональный компонент – «эндокринный». Экзокринные »клетки, вырабатывающие ферменты, помогающие переваривать пищу, а эндокринная поджелудочная железа состоит из небольших островков клеток, называемых островками Лангерганса.
Связанные журналы функции поджелудочной железы
Поджелудочная железа, заболевания поджелудочной железы и терапия, панкреатология, гепатобилиарные заболевания и заболевания поджелудочной железы International
Острый панкреатит
Острый панкреатит – это внезапное кратковременное воспаление поджелудочной железы.Другой термин, используемый для обозначения острого панкреатита, – это острый некроз поджелудочной железы. Несмотря на высокий уровень лечения, это может привести к серьезным осложнениям или даже смерти. В тяжелых случаях острый панкреатит приводит к кровотечению в железе, серьезному повреждению тканей, инфекции и образованию кисты. Он также может нанести вред другим жизненно важным органам, таким как сердце, легкие и почки. Острый панкреатит диагностируется клинически, но иногда требуется компьютерная томография, полный анализ крови, функциональные тесты почек, визуализация и т. Д.
Связанные журналы острого панкреатита
Гастроэнтерология, эндоскопия желудочно-кишечного тракта, Американский журнал хирургии, панкреатологии, болезней органов пищеварения и печени
Хронический панкреатит
Хронический панкреатит – это перманентное воспаление поджелудочной железы, которое не заживает и не улучшает, а изменяет нормальную структуру и функции органа.Обычно это наблюдается после приступа острого панкреатита. Еще одна серьезная причина – употребление алкоголя в больших количествах. Хронический панкреатит может проявляться как эпизоды сильного воспаления в поврежденной поджелудочной железе или как хроническое поражение с постоянной болью или нарушением всасывания. Диабет – частое осложнение, возникающее из-за хронического поражения поджелудочной железы, и требует лечения инсулином.
Связанные журналы хронического панкреатита
Гастроэнтерология, эндоскопия желудочно-кишечного тракта, Американский журнал хирургии, панкреатологии, болезней органов пищеварения и печени
Рак поджелудочной железы
Рак поджелудочной железы – злокачественное новообразование, происходящее из трансформированных клеток, возникающих в тканях, образующих поджелудочную железу.Рак поджелудочной железы (рак поджелудочной железы) в основном встречается у людей старше 60 лет. Если он диагностирован на ранней стадии, то операция по удалению рака дает некоторые шансы на излечение. В целом, чем более развит рак (чем больше он разросся и распространился), тем меньше шансов, что лечение будет излечивающим. Как экзокринные, так и эндокринные клетки поджелудочной железы могут образовывать опухоли. Но опухоли, образованные экзокринными клетками, встречаются гораздо чаще. Клетки рака поджелудочной железы не умирают программно, а вместо этого продолжают расти и делиться.
Связанные журналы рака поджелудочной железы
Гастроэнтерология, эндоскопия желудочно-кишечного тракта, Европейский журнал рака, панкреатологии, Американский журнал хирургии
Сахарный диабет
Сахарный диабет – это группа метаболических заболеваний, характеризующихся дефицитом гормона поджелудочной железы инсулина, который возникает в результате нарушения секреции или действия инсулина, либо того и другого. Сахарный диабет Диабет – это хроническое заболевание, а это означает, что, хотя его можно контролировать, он сохраняется на всю жизнь.Существует три основных типа сахарного диабета: 1. СД 1 типа; 2. Тип 2 ДМ; 3. Гестационный диабет.
Связанные журналы сахарного диабета
Исследования и клиническая практика диабета, метаболизм, гастроэнтерология, панкреатология
Хирургия поджелудочной железы
Хирургия поджелудочной железы – сложная процедура и выполняется, когда это единственный вариант, который может привести к длительному выживанию при раке поджелудочной железы и, в некоторых случаях, возможно, имеет потенциальный шанс на излечение.Применяется для лечения хронического панкреатита и других, менее распространенных доброкачественных заболеваний поджелудочной железы. Панкреатодуоденэктомия Уиппла – это операция, наиболее часто выполняемая при опухолях головки поджелудочной железы. Он включает удаление части желудка, всей двенадцатиперстной кишки, части тонкой кишки, головки поджелудочной железы, желчного протока и желчного пузыря, оставляя после себя основные кровеносные сосуды. Основная цель хирургии поджелудочной железы – снятие трудноизлечимых болей и декомпрессия соседних органов.
Связанные журналы хирургии поджелудочной железы
Гастроэнтерология, Эндоскопия желудочно-кишечного тракта, Американский журнал хирургии, Журнал детской хирургии, Панкреатология, Журнал хирургических исследований, Ланцет, Хирургия, Европейский журнал рака, болезней пищеварения и печени, Европейский журнал добавок к раку, Журнал гастроинтестинальной хирургии
Аутоиммунный панкреатит
Аутоиммунный панкреатит (АИП) – это недавно обнаруженный тип хронического панкреатита, который трудно отличить от карциномы поджелудочной железы.Установлено, что аутоиммунный панкреатит (АИП) поддается лечению кортикостероидами, особенно преднизоном. В настоящее время это считается формой гипер-IgG4-болезни. Существует две категории AIP: Тип 1 и Тип 2, каждая с разными клиническими профилями. Пациенты с AIP типа 1, как правило, были старше и имели высокую частоту рецидивов, но пациенты с AIP типа 2 не испытывали рецидивов и, как правило, были моложе. AIP не влияет на долгосрочную выживаемость.
Связанный журнал аутоиммунного панкреатита
Гастроэнтерология, эндоскопия желудочно-кишечного тракта, панкреатология, заболевания органов пищеварения и печени, клиническая гастроэнтерология и гепатология, Отчет по гастроэнтерологии, Американский журнал рентгенологии, Медицинский журнал Новой Англии
Псевдокиста поджелудочной железы
Псевдокиста поджелудочной железы – это заполненный жидкостью мешок в брюшной полости, который иногда также содержит ткани, ферменты и кровь из поджелудочной железы.Псевдокиста поджелудочной железы обычно возникает у пациентов с хроническим панкреатитом. Он также может возникать у людей с травмой поджелудочной железы или после травмы живота. Псевдокиста поджелудочной железы развивается, когда протоки поджелудочной железы повреждены воспалением, возникающим при панкреатите. В отличие от настоящих кист, псевдокисты выстланы не эпителием, а грануляционной тканью. Другие осложнения, возникающие из-за псевдокисты поджелудочной железы, включают инфекцию, кровотечение, непроходимость, разрыв, сдавление мочевыделительной системы, желчевыводящей системы и артериовенозной системы.
Связанный журнал псевдокисты поджелудочной железы
Эндоскопия желудочно-кишечного тракта, Гастроэнтерология, Американский журнал хирургии, Журнал детской хирургии, панкреатология
Островковно-клеточная карцинома
Островоклеточная карцинома – это необычный рак эндокринной поджелудочной железы. На его долю приходится примерно 1,3% случаев рака поджелудочной железы. Это также известно как или несидиобластома. Опухоли из островковых клеток поджелудочной железы могут быть доброкачественными и злокачественными. Островковые клетки производят множество различных гормонов; большинство опухолей выделяют только один гормон, который вызывает определенные симптомы.Существуют различные типы островковых опухолей, такие как: гастриномы (синдром Золлингера-Эллисона), глюкагономы, инсулиномы. Опухоли островковых клеток поддаются лечению даже после метастазирования. Симптомы включают потливость, головную боль, голод, беспокойство, двоение в глазах или нечеткое зрение, учащенное сердцебиение, диарею, язвы в желудке и тонкой кишке, рвоту с кровью и т. Д.
Реализованные журналы островково-клеточной карциномы
Гастроэнтерология, Американский журнал хирургии, Ланцет, Патология человека, Американский медицинский журнал
Трансплантация поджелудочной железы
Трансплантация поджелудочной железы – это передача здоровой поджелудочной железы от донора пациентам с диабетом.Поскольку поджелудочная железа является жизненно важным органом, родная поджелудочная железа пациента остается на месте, а пожертвованная поджелудочная железа помещается в другое место. Это делается потому, что в случае отторжения новой поджелудочной железы у пациента разовьется тяжелый диабет, и он не смог бы выжить без сохранившейся родной поджелудочной железы. Здоровая поджелудочная железа поступает от только что умершего донора или от человека с мертвым мозгом. В настоящее время трансплантация поджелудочной железы обычно проводится людям с тяжелым инсулинозависимым диабетом.
Связанные журналы трансплантации поджелудочной железы
Трансплантация, Гастроэнтерология, Панкреатология, The Lancet, Американский журнал хирургии, Журнал хирургических исследований
Муковисцидоз
Муковисцидоз (МВ) – это аутосомно-рецессивное генетическое заболевание, поражающее легкие, поджелудочную железу, печень и кишечник. Его основная характеристика – нарушенный транспорт хлоридов и натрия через эпителий, что приводит к густым вязким секретам.Он также известен как муковисцидоз. Ненормальное дыхание – самый серьезный симптом, возникающий в результате частых инфекций легких. Муковисцидоз вызывается мутацией сдвига рамки считывания в гене белка трансмембранного регулятора проводимости (CFTR). Название муковисцидоз было дано из-за образования кисты в поджелудочной железе. Густая секреция слизи, возникающая из-за муковисцидоза, блокирует путь пищеварительных и эндокринных ферментов поджелудочной железы, вызывая полное повреждение поджелудочной железы.
Связанные журналы муковисцидоза
Журнал муковисцидоза, Журнал педиатрии, гастроэнтерологии, Ланцет, Журнал детской хирургии, Журнал аллергии и клинической иммунологии, Журнал трансплантации сердца и легких, Американский журнал хирургии, респираторной медицины, Американский журнал медицины
Патофизиология
Патофизиология или физиопатология – это соединение патологии с физиологией. Патология описывает состояния во время болезненного состояния, тогда как физиология – это дисциплина, которая описывает механизмы, действующие в организме.Патология описывает ненормальное состояние, тогда как патофизиология пытается объяснить физиологические процессы, из-за которых такое состояние развивается и прогрессирует. Другими словами, патофизиология определяет функциональные изменения, связанные с заболеванием или травмой.
Связанные журналы патофизиологии
Гастроэнтерология, панкреатология, биологическая психиатрия, журнал Американского колледжа кардиологии, патофизиология
Искусственная поджелудочная железа
Искусственная поджелудочная железа – это технология, разработанная, чтобы помочь людям с диабетом автоматически контролировать уровень глюкозы в крови, обеспечивая замену инсулина здоровой поджелудочной железы.Основная цель искусственной поджелудочной железы – обеспечить эффективную заместительную инсулиновую терапию, чтобы контроль уровня глюкозы в крови был нормальным и не было осложнений гипергликемии. Искусственная поджелудочная железа облегчает лечение инсулинозависимых. Эту систему носят как инсулиновую помпу и называют «искусственной поджелудочной железой», потому что она контролирует и регулирует уровень инсулина так же, как поджелудочная железа у людей без диабета.
Связанные журналы искусственной поджелудочной железы
Гастроэнтерология, панкреатология, Медицинский журнал Новой Англии, Американский журнал хирургии, исследований диабета и клинической практики, метаболизм
Кольцо поджелудочной железы
Кольцо поджелудочной железы – редкое заболевание, при котором часть ткани поджелудочной железы разрастается и окружает двенадцатиперстную кишку.Эта дополнительная ткань возникает из головки поджелудочной железы. Это вызывает сужение двенадцатиперстной кишки, блокируя поступление пищи в оставшуюся часть кишечника. Частота возникновения кольцевидной железы поджелудочной железы составляет 1 случай на 12–15 000 новорожденных. Обычно это происходит из-за аномального или экстраэмбриологического развития. Однако также сообщалось о некоторых случаях заболевания у взрослых. Ранние признаки аномалии включают многоводие, низкий вес при рождении и непереносимость кормления сразу после рождения.
Связанные журналы кольцевидной железы поджелудочной железы
Журнал детской хирургии, Американский журнал хирургии, желудочно-кишечная эндоскопия, ультразвук в медицине и биологии, клиники и исследования в области гепатологии и гастроэнтерологии
Заболевания поджелудочной железы
Поджелудочная железа – это орган, который играет важную роль в пищеварении и производстве гормонов.Заболевания поджелудочной железы включают острый панкреатит, наследственный панкреатит и рак поджелудочной железы. В журнале собрана информация о заболеваниях поджелудочной железы, методах выявления, различных методах лечения и передовых методах лечения заболеваний поджелудочной железы.
Связанные журналы заболеваний поджелудочной железы
Pancreatic Disorders & Therapy, Journal of Hepato-Bili-Pancreatic Sciences, Международный журнал гепатобилиарных и панкреатических заболеваний, Журнал гастроэнтерологии, панкреатологии и заболеваний печени
изображений при хроническом панкреатите | Pancreapedia
Аутоиммунный панкреатит (АИП) – это необычная и отличная форма ХП, которая будет обсуждаться позже в этой главе.
3. Методы визуализации
Существуют различные методы визуализации для диагностики ХП, которые имеют свои преимущества и ограничения, и ни один из методов не предоставляет всю информацию.
Рентгенограммы брюшной полости
Десятилетия назад, до появления методов поперечного сечения, диагностическая диагностика ХП основывалась на простой рентгенографии. ХП проявляется на рентгенограммах брюшной полости в виде мультифокальных кальцинатов в эпигастральной области (рис. 1а) .Эти кальцификаты обычно видны по всему позвоночнику вдоль поджелудочной железы. Поскольку кальцификаты обычно наблюдаются в запущенных случаях и только при определенных типах ХП, рентгенограммы не чувствительны (30-70%) (38). Хотя кальцификаты специфичны, их следует отличать от кальцификатов, вызванных другими причинами и вышележащими органами. Из-за вышеуказанных ограничений рентгенограммы брюшной полости обычно не выполняются для оценки ХП. Часто кальциноз поджелудочной железы выявляется на рентгенограммах, чтобы исключить другие причины боли в животе.
ERCP
ERCP считается золотым стандартом диагностики ХП из-за его превосходного пространственного разрешения и способности отображать аномалии боковых ветвей на ранней стадии ХП. Это дает дополнительное преимущество терапевтических вмешательств, когда это необходимо. Его ограничениями являются инвазивный характер процедуры и связанные с ней осложнения. После появления MRCP популярность ERCP для диагностической оценки значительно снизилась, поскольку MRCP является неинвазивным методом (32).Однако преимущество ERCP заключается в том, что система протоков показана в растянутом состоянии, что очень помогает при обнаружении тонких поражений, таких как делитель поджелудочной железы. Диаметр нормального главного панкреатического протока (MPD) варьируется в зависимости от области поджелудочной железы (3-4 мм в голове, 2-3 мм в теле и 1-2 мм в хвостовой области) (38). Видно, что несколько боковых ответвлений попеременно соединяются с MPD под прямым углом. Самые ранние признаки ХП можно увидеть только на ЭРХПГ в виде неровностей и расширения боковых ветвей.Эти изменения могут стать более серьезными вместе с дилатацией, потерей нормального сужения и нерегулярностью MPD по мере прогрессирования заболевания (Рисунок 1b) . Чередование дилатации и стеноза MPD может давать вид цепочки озер. Внутрипротоковые камни можно рассматривать как дефекты наполнения. ЭРХПГ также помогает диагностировать другие обструктивные причины ХП, такие как ампульные поражения, внутрипротоковые новообразования и врожденные аномалии, такие как деление поджелудочной железы. Кембриджская классификация ХП, основанная на ERCP, используется для группирования пациентов по двусмысленным, легким, умеренным или выраженным типам.Состояние MPD, боковых ветвей, наличие камней и стриктур протоков учитывается в Кембриджской классификации (44).
AIP, в отличие от других форм CP, показывает фокальное, сегментарное или диффузное сужение MPD и отсутствие визуализации боковых ветвей на ERCP (45). Сужение также можно увидеть в нижнем конце общего желчного протока (CBD), вызывая расширение желчных протоков. AIP может быть связан с первичным склерозирующим холангитом, который проявляется как мультифокальное сужение в более проксимальных отделах желчных протоков.
УЗИ (США)
Сонография поджелудочной железы является сложной задачей из-за ее забрюшинного расположения и перекрытия петель кишечника. Это также зависит от телосложения пациента и навыков оператора. Для получения изображения поджелудочной железы в целом могут потребоваться различные маневры, такие как изменение положения пациента, расширение желудка водой и использование селезенки в качестве окна для визуализации хвоста поджелудочной железы. Несмотря на вышеупомянутые ограничения, УЗИ по-прежнему является методом первой линии для оценки боли в животе из-за его доступности, низкой стоимости и отсутствия ионизирующего излучения.Оценка состояния поджелудочной железы проводится натощак, чтобы газы кишечника не закрывали визуализацию.
Нормальная поджелудочная железа изо или гиперэхогенна по сравнению с нормальной печенью, и с возрастом может происходить прогрессирующее замещение жировой ткани (13). На ранней стадии ХП поджелудочная железа теряет гиперэхогенность и становится неоднородной из-за очаговых воспалительных изменений. При прогрессировании заболевания от средней до тяжелой стадии изменения становятся более выраженными и заметны почти у 70% пациентов (6, 23).На поздних стадиях заболевания изменения ЦП проявляются в виде нерегулярных расширенных MPD с панкреатическими и внутрипротоковыми камнями и связанной с ними атрофией поджелудочной железы (6, 19) (Рисунок 2a, b) . Он также может показать скопления или псевдокисты вокруг поджелудочной железы. Иногда УЗИ позволяет обнаружить очаговые поражения поджелудочной железы, которые ответственны за развитие обструктивного типа ХП.
Эластография – это новый метод оценки твердости тканей, который можно использовать для оценки степени поражения ХП, а также для оценки степени фиброза, который может быть прогностическим индикатором у пациента, подвергающегося хирургическим вмешательствам.Эластографию можно использовать вместе с трансабдоминальным и эндоскопическим ультразвуком. На рынке имеется два типа эластографии (13). Первый – это визуализация деформации, которая качественно оценивает деформацию ткани в ответ на экзогенный акустический импульс. Второй тип – это эластография сдвиговой волны, которая количественно оценивает твердость ткани на основе скорости поперечных волн в тканях. В обоих методах эластограмма представлена как цветовая карта, наложенная на изображения в B-режиме.
Компьютерная томография (КТ)
Более широкая доступность и технический прогресс за последние два десятилетия сделали компьютерную томографию предпочтительным методом визуализации для оценки ХП. Кальцификаты поджелудочной железы, которые имеют решающее значение для постановки диагноза ХП, лучше всего видны на CT (рис. 2c) . Он чувствителен даже к мелким точечным кальцификациям, которые могут быть пропущены при использовании других методов визуализации.
Липоматоз поджелудочной железы: обширный обзор изображений
Определения и справочная информация
Поджелудочная железа – это и эндокринная, и экзокринная железа.Экзокринный компонент составляет около 80 процентов от общего объема желез и в основном состоит из двух разных типов клеток: ацинарных клеток (в основном секретирующих пищеварительные ферменты) и протоковых клеток (в основном секретирующих жидкости и электролиты). Эндокринный компонент состоит из типичных островков Лангерганса, которые содержат несколько типов клеток, разбросанных по экзокринной ткани [ 1 ].
Липоматоз и замещение жира поджелудочной железы являются наиболее частыми доброкачественными патологическими состояниями поджелудочной железы взрослых [ 1 , 2 , 3 ].Классически это явление вызывает повышенную гипоплотность поджелудочной железы на КТ и типичную гиперэхогенность при ультразвуковом (УЗИ) исследовании.
Накопление жира в поджелудочной железе (липоматоз) и замещение различных частей поджелудочной железы жиром (замещение жира) имеют различные синонимы: липоматоз поджелудочной железы, замещение жировой ткани, жировая инфильтрация, жировая прослойка поджелудочной железы, липоматозная псевдогипертрофия, безалкогольный жировая болезнь поджелудочной железы и стеатоз поджелудочной железы [ 4 ].Эти синонимы вызывают путаницу.
На основе различных результатов визуализации можно было бы склониться к использованию термина «липоматозная инфильтрация», когда островки поджелудочной железы кажутся диссоциированными от жировой ткани или когда плотность (КТ), эхогенность (ультразвук) или сигнал (МРТ) ) диффузно модифицированы. Когда кажется, что панкреатические островки исчезли или были сильно замещены жиром, можно было бы более склонно предпочесть словесное «замещение жира».
Точно так же можно склониться к использованию термина «липоматозная инфильтрация», когда процесс кажется обратимым, и оставить термин «замещение жира» для случаев, демонстрирующих вероятное необратимое исчезновение островков желез [ 4 , 5 ].
Тем не менее, значительных гистопатологических исследований, чтобы доказать или опровергнуть, что липоматоз и жировое замещение поджелудочной железы являются (i) отдельными образованиями, (ii) ассоциированными образованиями в различных пропорциях в определенном случае, или (iii) выражениями та же болезнь. Поэтому, чтобы упростить лекцию этого иллюстрированного обзора, термины замещение жира и липоматоз поджелудочной железы были заменены упрощенным термином жировая инфильтрация или «FI».Это подчеркивает, что FI поджелудочной железы может быть однородным, неравномерно распределенным или ограничиваться одной областью поджелудочной железы (очаговый FI) [, 1, , , 6, ].
Этиология
ФИ – доброкачественное заболевание, не имеющее единой этиологии [ 1 , 2 , 7 , 8 , 9 ]. Сущность была связана со многими заболеваниями и состояниями. Возраст и ожирение значительно коррелируют со степенью FI [ 9 , 10 ].Как следствие, FI обычно напрямую коррелирует с индексом массы тела пациента (ИМТ). Точнее, корреляция лучше между FI и индексом висцерального жира , который, тем не менее, сложнее оценить, чем ИМТ или вес пациента. Другими словами, количество ткани висцерального жира является лучшим индикатором и предиктором FI поджелудочной железы, чем только BMI (Рисунок 1) [ 1 ].
Рисунок 1Большой диффузный ФИ (тип 2b) был обнаружен у 75-летней женщины с патологическим ожирением и хроническим сахарным диабетом (a и c).Значительный регресс глобального FI был обнаружен после 4-летнего периода (b и d). И диссоциация долек поджелудочной железы жиром, и общий объем органа уменьшились, и пациент потерял более 25 кг. Резко регрессировал стеатоз печени.
FI также коррелирует с наличием сахарного диабета, приобретенного или наследственного панкреатита [ 3 ]. Хотя ФИ ассоциируется с наличием сахарного диабета; это не связано конкретно с самой болезнью.Типичные островки Лангерганса парадоксальным образом примечательны своей устойчивостью к FI.
FI тесно связан с метаболическим синдромом [ 4 ], возникающим синдромом, состоящим из ассоциации по крайней мере трех из следующих признаков: гиперинсулинемия; гипертония; гиперхолестеринемия; ожирение; и гипергликемия. FI поджелудочной железы также наблюдалась у пациентов с алкогольным гепатитом или принимающих стероиды [ 1 ].
Большой ФИ поджелудочной железы также является наиболее частой картиной КТ у подростков и взрослых с муковисцидозом [ 11 , 12 , 13 ].
Было обнаружено множество случаев ФИ, связанных с патологиями, связанными с проницаемостью протоков поджелудочной железы или на которые она влияет. Столь выраженный FI, с атрофией желез или без нее, обычно наблюдается у взрослых пациентов, вторично по отношению к обструкции протоков поджелудочной железы внутрипротоковыми камнями или опухолями поджелудочной железы (Рисунки 2, 3 и 4) [ 7 ]. Врожденный стеноз протока поджелудочной железы также во многих случаях может приводить к ФИ паренхимы [ 14 ]. Предыдущие эксперименты на животных уже продемонстрировали, что перевязка протока поджелудочной железы может привести к атрофии и лизису ацинусов поджелудочной железы, тогда как островки Лангерганса относительно сохранились.Число протоковых клеток медленно уменьшалось, и они становились редкими из-за гибели клеток. Однако поджелудочная железа постепенно увеличивалась за счет замещения внутрилобулярной жировой ткани до 16 недель [ 15 ].
Рисунок 2Криволинейный (a), сагиттальный (b) и коронарный (c) переформатированные виды (MPR) в случае полного FI поджелудочной железы (тип 2b). Псевдогипертрофия не связана. Пациент, мужчина 50 лет, имел лишь легкую биологическую экзокринную недостаточность поджелудочной железы. Лишь небольшое количество железистых ацинусов сохраняется вдоль основной и вторичной сети протоков.Пациенту ранее была проведена хирургическая резекция нейроэндокринной опухоли двенадцатиперстной кишки, расположенной частично на сосочке, и массивный FI уже был замечен до операции (не показано). Гипотеза о хроническом препятствии оттока желчного протока или главного протока поджелудочной железы как основного причинного фактора («протоковая гипотеза») массивного диффузного ФИ подтверждается этим случаем.
Рисунок 3Старение может вызвать FI (белые стрелки на a и b), а также атрофию поджелудочной железы (черные стрелки), как показано на примере этой 100-летней женщины.Большая атрофия тела или хвоста поджелудочной железы (белые стрелки на c) более распространена, чем липоматоз, в случае хронической обструкции Вирсунга опухолью, как показано на примере этого 88-летнего мужчины с небольшой аденокарциномой тела (черный звезда). В случае истинной атрофии поджелудочной железы окружающие органы сходятся, чтобы занять ложе поджелудочной железы (белые стрелки на c).
Рис. 4Глобальный и массивный FI (тип 2b) обнаружен у 60-летней женщины в результате кальцифицирующего хронического панкреатита с хронической обструкцией главного протока большой кальцификацией (звездочка).Показаны криволинейная реконструкция (a) и осевые виды (b и c). Примитивное ложе (или объем) поджелудочной железы сохраняется (белые стрелки). Чрезвычайно похожий случай кальцифицирующего хронического панкреатита (d и e) превратился в массивную атрофию поджелудочной железы (черная стрелка) вместо FI. Причина такого различия в эволюции неизвестна.
Неравномерная жировая инфильтрация
Неравномерный ФИ поджелудочной железы является очень частым – и в действительности наиболее частым – представлением ФИ, и сообщалось о многих случаях [ 2 , 6 , 7 , 16 ].Хотя неравномерный FI поджелудочной железы может повлиять на любую часть железы, он обычно более частый и заметный в передней головке поджелудочной железы (APH). Задняя головка поджелудочной железы (PPH) поджелудочной железы и крючковидный отросток (UP) обычно щадят или, по крайней мере, более резистентны к FI [ 2 , 7 ]. Область, наиболее резистентная к FI, – это очень маленькая фокальная область вокруг общего желчного протока [ 16 ].
Это анатомическое различие между APH и PPH и UP имеет первостепенное значение с точки зрения эмбриологии.Поджелудочная железа человека развивается в результате слияния дорсальной и вентральной зачатков поджелудочной железы (рис. 5). Брюшной зачаток является общим с желчным протоком. На шестой неделе беременности он поворачивается на 270 ° по часовой стрелке и заканчивается на задней нижней стороне спинного зачатка. Таким образом, он становится анатомически кзади [ 17 , 18 ]. Дорсальный зачаток поджелудочной железы дает начало передней части головки (APH) поджелудочной железы, помимо тела и хвоста, в то время как вращающийся вентральный зачаток поджелудочной железы развивается в заднюю часть головы (PPH) и крючковидный отросток (UP ).Это слияние зачатков поджелудочной железы связано с анастомозом их соответствующих протоков (рис. 5 и 6), за исключением примерно 4–10% пациентов, у которых будет обнаружена поджелудочная железа divisum. Главный проток брюшного зачатка входит в преимущественное сообщение с основным протоком спинного зачатка. Точка слияния образуется между перешейком и головкой, что приводит к созданию доминирующего и более постоянного протока Вирсунга и объясняет его байонетный вид [ 19 ] (рис. 6).Следовательно, проток Вирсунга дренирует части поджелудочной железы различного эмбриологического происхождения: ПРК (происходящие из брюшной зачатка), а также тело и хвост (происходящие из дорсальной зачатка). Проксимальная часть главного дорсального протока поджелудочной железы частично регрессирует с образованием дополнительного протока поджелудочной железы или протока Санторини, который открывается в малый сосочек двенадцатиперстной кишки.
Рисунок 5Поджелудочная железа развивается в результате слияния дорсального (DP) и вентрального (VP) зачатков поджелудочной железы (a). ВП встречается с желчным протоком (выделено зеленым цветом).На шестой неделе беременности VP поворачивается по часовой стрелке на 270 ° (b), чтобы закончить на задне-нижней стороне DP (c). Таким образом, он становится анатомически задним. DP дает начало APH поджелудочной железы, в дополнение к телу и хвосту, в то время как вращающийся VP развивается в PPH и UP. Сращение зачатков поджелудочной железы сопровождается анастомозом протоков (г). Главный канал VP сливается с основным каналом DP и становится доминирующим и более постоянным каналом Вирсунга.Таким образом, проток Вирсунга дренирует части поджелудочной железы различного эмбриологического происхождения. Дистальная часть основного протока DP частично регрессирует с образованием добавочного протока Санторини, который открывается в малый дуоденальный сосочек.
Рисунок 6Анатомия протока поджелудочной железы. Во время развития канал телесной каудальной поджелудочной железы (дорсальный зачаток) сливается с каналом PPH (b) (вентральный зачаток), образуя главный канал Вирсунга (черная стрелка). Этот сплав выражает свою типичную байонетную форму (маленькая белая стрелка).Проток вентральной головки (а) (берущий начало от дистального дорсального зачатка) становится добавочным каналом Санторини (белая стрелка). Классическое пространственное расположение этих протоков хорошо проиллюстрировано на сагиттальной реконструкции головы (b), трехмерной объемной визуализации (d) и толстой проекции минимальной интенсивности (MIN) поджелудочной железы (c).
Неравномерный ФИ поджелудочной железы был классифицирован Мацумото в 1995 г. (рис. 7) на два типа, и каждый из них был вторично разделен на две подгруппы [ 16 ].При типе 1 (71% случаев) PPH и UP не зависят от FI. При типе 1а (35% случаев) ФИ ограничивается APH. А у типа 1б (36% случаев) ФИ АПГ связаны с ФИ тела и хвоста.
Рис. 7Схематическая классификация ФИ, предложенная Мацумото. ФИ обозначен серыми зонами. При типе 1 (71% случаев) PPH и UP не зависят от FI. При типе 1а (35% случаев) ФИ ограничивается APH. А у типа 1б (36% случаев) ФИ АПГ связаны с ФИ тела и хвоста.При типе 2 (29% случаев) FI затрагивает всю голову, за исключением очень маленькой рефрактерной очаговой области вокруг общего желчного протока. При типе 2а (11% случаев) ФИ ограничивается всей головой. А при типе 2б (18% случаев) ФИ головы ассоциируется с ФИ тела и хвоста. Таким образом, FI типа 2b представляет собой FI почти всей поджелудочной железы (за исключением очень маленькой фокальной области вокруг общего желчного протока).
При типе 2 (29% случаев) FI затрагивает всю голову, за исключением очень маленькой рефрактерной фокальной области вокруг общего желчного протока.При типе 2а (11% случаев) ФИ ограничивается всей головой. А при типе 2б (18% случаев) ФИ головы ассоциируется с ФИ тела и хвоста. Таким образом, тип 2b представляет собой FI почти всей поджелудочной железы (за исключением очень маленькой очаговой области вокруг общего желчного протока). Таким образом, неравномерные FI обнаруживаются примерно в 82% случаев FI (типы 1a, 1b и 2a).
Неравномерный FI двух разных эмбриологических частей (APH и PPH) головки головы (типы 1a и 2a), таким образом, обнаруживается в 46% случаев неравномерного FI поджелудочной железы.Причина этой разницы в возможностях FI двух наложенных друг на друга и эмбриологически различных частей головки поджелудочной железы остается неясной, но может быть частично объяснена их конституциональными гистологическими различиями в связи с их различным эмбриологическим происхождением [ 6 ]. Было доказано, что эмбриологическая вентральная поджелудочная железа, которая становится PPH и UP, имеет меньшие, плотно упакованные ацинусы, меньшие экзокринные клетки, скудные или отсутствующие внутрипаренхиматозные жировые клетки и больше межлобулярной фиброзной ткани, чем эмбриологическая дорсальная поджелудочная железа [ 6 , 16 ].
По нашему мнению, эта «гистологическая эмбриологическая гипотеза» не может сама по себе объяснить частые неравномерные FI поджелудочной железы. Действительно, эта гипотеза не принимает во внимание, что тело и хвост поджелудочной железы, которые часто учитываются FI в случаях изолированного FI APH (тип 1a) или глобального головного FI (тип 1b) – фактически, в 71% случаев при кумуляции типов 1а и 1b – имеют одинаковое эмбриологическое происхождение. Таким образом, для этих случаев должна быть найдена другая гипотеза, чем эмбриологическая гипотеза.
После слияния двух эмбриологических зачатков поджелудочной железы проксимальная часть главного дорсального протока поджелудочной железы частично регрессирует с образованием добавочного протока поджелудочной железы Санторини, который открывается в малый дуоденальный сосочек [ 19 ]. Этот второстепенный сосочек значительно меньше большого сосочка и может затем подвергаться возможной перегрузке секреторной способности [ 19 ]. Исследования недавно обнаружили значительную корреляцию между проходимостью добавочного протока поджелудочной железы и острым панкреатитом, при этом проходимость добавочного протока значительно ниже у пациентов с панкреатитом (17%), чем в контрольных случаях (43%) [ 19 ].Таким образом, проходимость добавочного протока чрезвычайно вариабельна и у многих пациентов кажется уменьшенной или отсутствует.
Более того, у пациентов с делением поджелудочной железы (от 4% до 14% населения) большая часть главного дорсального протока остается отделенной от вентральной поджелудочной железы и, следовательно, дренируется исключительно через малый сосочек [ 18 ]. Считается, что несоответствие между малым размером малого сосочка и большим количеством секрета из дорсальной части железы может привести к относительной обструкции оттока из дорсальной части поджелудочной железы, что приведет к боли или панкреатиту.Существуют противоречия, но была показана положительная корреляция между делением поджелудочной железы и панкреатитом [ 18 , 19 , 20 ].
Дополнительный проток Санторини дренирует весь APH, а именно ту часть железы, которая более склонна к FI. Частое преобладание изолированного массивного липоматоза APH породило гипотезу о том, что FI, вероятно, также вызван плохим качеством дренажа из вспомогательного канала Санторини. Эта «гипотеза протоков», вероятно, сосуществует и противоречит «эмбриологической гипотезе» в случаях неравномерного липоматоза.
Визуализация жировой инфильтрации поджелудочной железы
Неравномерный ФИ головной поджелудочной железы обычно обнаруживается не только с помощью передовых методов визуализации, но и при УЗИ поджелудочной железы [ 17 , 20 ]. Вентральная эмбриологическая поджелудочная железа, которая имеет тенденцию оставаться свободной от FI, часто оказывается более гипоэхогенной, чем дорсальная часть (Рисунок 8). Во время УЗИ всегда необходимо постоянно осознавать этот классический образец, поскольку многие патологические процессы поджелудочной железы также часто являются спонтанно гипоэхогенными, включая карциному, метастазы, лимфому и карциноидные опухоли, а также очаговые и сегментарные острые и хронические панкреатиты [ 17 ] .
Рис. 8Неравномерный ФИ головной поджелудочной железы (тип 1а) обычно обнаруживается во время УЗИ брюшной полости, особенно у женщин среднего возраста. Показаны классические поперечные виды (a, c и d) и сагиттальные виды (b и e). Желчный проток и дистальный участок Вирсунга (белая стрелка) обычно проходят в ПРК (эмбриологический вентральный зачаток), который чаще выглядит гипоэхогенным (звездочка), потому что он меньше подвержен влиянию FI.
Считается, что причиной более высокой чувствительности УЗИ для обнаружения неравномерного ФИ в головном мозге в целом является более высокая чувствительность УЗИ для обнаружения тонких различий в содержании жира в различных тканях.Это также обычное наблюдение в печени, при котором УЗИ легче обнаруживает гиперэхогенную область ограниченного стеатоза и гипоэхогенную область ткани, подверженную стеатозу, чем КТ [ 21 ].
Во время УЗИ FI поджелудочной железы оказывается гиперэхогенным, а не гипоэхогенным, как это обычно наблюдается при липоме. Причина в том, что не сам жир определяет эхогенность, а архитектурная модификация из-за развития адипоцитов внутри межлобулярных перегородок.Чередование железистых и жировых поверхностей раздела отвечает за гиперэхогенность [ 17 ].
Эхогенность поджелудочной железы постепенно увеличивается с возрастом и ожирением. Неравномерный ФИ головки поджелудочной железы редко бывает в возрасте до 25 лет и чаще всего обнаруживается у женщин среднего возраста с умеренно эхогенной поджелудочной железой [ 17 ]. Когда поджелудочная железа становится очень липоматозной и, следовательно, чрезвычайно гиперэхогенной, эффективность УЗИ для диагностики неравномерного ФИ головной головки, тем не менее, резко снижается из-за явления насыщения, а также из-за того, что резко снижается передача УЗИ через гиперэхогенную переднюю головку.Такая же ситуация наблюдается при массивном стеатозе печени.
Напротив, чем больше поджелудочная железа инфильтрируется или замещается жиром, тем лучше КТ может легко диагностировать это заболевание. Таким образом, КТ становится методом выбора при массивном ФИ поджелудочной железы.
В клинической практике ФИ поджелудочной железы обычно однозначно диагностируется с помощью КТ, когда ФИ достаточно резкий, чтобы показать типичные значения Хаунсфилда с отрицательным затуханием. Тем не менее, если степень очагового FI остается умеренной, ослабление может быть недостаточным и может имитировать кистозный или гиподенсный опухолевый процесс [, 2, , , 7, ].Более того, на постконтрастных изображениях нормальная паренхима поджелудочной железы, заключенная между областями FI, может показывать значительное усиление контраста (Рисунок 9), что может имитировать опухолевую массу [ 2 , 7 ].
Рисунок 9Типичный случай неравномерного FI (a и b), ограниченного APH (тип 1a) (черная стрелка). Однако типичная «отрицательная» плотность жира не так очевидна, потому что измерения плотности неизменно включают остаточные железистые ацинусы. Эти ацинусы также усиливаются при внутривенном контрастировании остальной части железы.Тем не менее, общее усиление контраста липоматозной области (с 7 UH (c) до 28 UH (d)) остается ниже, чем у остальной части железы (с 23-25 UH (e) до 70-90 UH (f )). Эта ситуация может имитировать рак поджелудочной железы, особенно когда отношение сигнал / шум изображения плохое или если толщина среза не соответствует требованиям. В сложных или неоднозначных случаях в дифференциальной диагностике может помочь УЗИ или МРТ.
Классически различные модели неравномерного ФИ, описанные Мацумото, обычно обнаруживаются во время клинической КТ:
Рис. 10PPH и UP исключены из FI в типе 1
Тип 1a (35% случаев), в котором FI ограничивается APH, показан на рисунках 10 и 11.
Тип 1b (36% случаев), в котором FI APH связан с FI тела и хвоста, показан на рисунке 12.
FI включает всю голову, за исключением очень маленькой рефрактерной очаговой области вокруг общего желчного протока у типа 2.
Тип 2а (11% случаев), при котором FI ограничивается всей головой, является самым редким типом.
Тип 2b (18% случаев) представляет собой ФИ почти всей поджелудочной железы (за исключением очень маленькой очаговой области вокруг общего желчного протока) (рисунки 1, 2, 4 и 121314).
На рисунках a – e показаны осевые (a и b), коронарные (c и d) и сагиттальные (e) виды поджелудочной железы 70-летней женщины с патологическим ожирением и сахарным диабетом 2 типа. FI только выборочно включает APH (черная звезда) (тип 1a). Гипоплотность липоматозной APH резко контрастирует с нормальной плотностью PPH, UP и телесной каудальной поджелудочной железы (белые стрелки).
Рисунок 11Быстрое прогрессирование диффузного FI, преимущественно поражающего APH (тип 1a), у 70-летней женщины.Пациенту сделали снимки 3 раза в течение 6 лет в связи с рецидивирующими эпизодами ишемического колита. На аксиальных срезах FI прогрессивно увеличивается во всех частях ткани (a – c), но резко преобладает на APH (c – e), где он связан с прогрессирующим увеличением головы и очаговой «псевдогипертрофией» (белые стрелки).
Рис. 12Типичные аспекты головки поджелудочной железы при FI типа 2b (a и b). И APH, и значительная часть PPH и UP инфильтрируются жиром.Только очень небольшая ограниченная овоидная область ткани поджелудочной железы вокруг желчного протока остается нетронутой (черная стрелка). Тонкий, но типичный случай FI типа 1b (рисунки c и d). APH и телесные каудальные части железы (белые звездочки) кажутся более гиподенсированными из-за липоматоза. Они контрастируют с более высокой плотностью PPH (черная звезда). Резкое изменение плотности обнаруживается как раз на уровне цефало-истмического соединения (белый кружок), хотя эти две области дренируются одним и тем же нормальным каналом Вирсунга (черные стрелки).Этот случай подтверждает эмбриологическое гистологическое объяснение неравномерного липоматоза.
Рис.13Криволинейная реконструкция (а), сагиттальная цефальная (b), а также передняя (в) и задняя (г) коронарные виды (d) коронковой части головы почти полного обширного и однородного FI (тип 2b), обнаруженного у довольно молодого пациента (60 лет) с нормальным ИМТ, без диабета и без клинических или биологических признаков внешнесекреторной недостаточности поджелудочной железы. Также присутствует дискретное увеличение органа. FI довольно однороден, за исключением дискретно меньшей инволюции задней части головы (черные стрелки) и конца хвоста (звездочка).
Рис. 14Корональная цефальная (a) и осевая косая каудальная проекции (b) демонстрируют малозаметные признаки острого каудального панкреатита, накладывающиеся на диффузный FI 75-летнего пациента (тип 2b), страдающего карциномой толстой кишки. Дискретный отек обнаруживается между долями железы (белая звездочка), а небольшой линейный выпот (черная стрелка) обнаруживается в передней околопочечной фасции. Последующие исследования – КТ без усиления на 5 день (b) и КТ с контрастным усилением на 30 день (e) – показывают воспалительную агглютинацию долек, имитирующих псевдоопухолевые узелки (белые стрелки).К счастью, интеркуррентная ПЭТ / КТ 18F-FDG, выполненная при последующем наблюдении карциномы толстой кишки на 15-й день, показала отрицательное поглощение FDG (d). Медленный регресс некротических псевдотуморальных узелков отчетливо виден через 10 месяцев (f).
Как показано в этом иллюстрированном обзоре, также могут быть обнаружены другие нетипичные и неклассифицированные проявления неравномерного FI (Рисунки 151617).
Рисунок 15Атипичные и неклассифицируемые случаи неравномерного FI. Косая коронковая (а) и криволинейная (б) реформации у пациента 81 года с массивным ФИ только хвоста (белая стрелка).Осевые косые (в) и криволинейные (г) реформации у другого 88-летнего пациента с массивным ФИ головы и тела, контрастирующим с относительной стороной хвоста (черная стрелка).
Рисунок 16Атипичный периферический неровный ФИ. Железа (a и b) окружена гиподонтической полосой, имитирующей перипанкреатический отек или тонкий выпот на изображениях КТ с контрастным усилением (белые стрелки на a и b). Эта гиподенсированная полоса отсутствовала 2 года назад, а хвост поджелудочной железы был тоньше (в).Периферическая полоса гипоинтенсивна на Т2-взвешенном изображении (d), что исключает отечный выпот (белые стрелки на d). Осевые синфазные изображения (e) показывают нормальную интенсивность сигнала в теле поджелудочной железы, более высокий сигнал в периферической железе, заметно на передней стороне (белая стрелка на e), с падением интенсивности сигнала на изображениях в противофазе ( белые стрелки на f) выявляют атипичные периферические неровные перикаудальные FI.
Рис. 17Рисунки a – e иллюстрируют необычный случай FI, поражающего исключительно дистальный конец поджелудочной железы (черный кружок).Этот атипичный ФИ ассоциируется с элективной псевдогипертрофией. Связана изолированная небольшая липома хвоста (черные стрелки на b и d). Остальная железа выглядит нормально. Этот редкий тип каудального FI был очень стабильным в течение 5-летнего периода.
В нетипичных или неоднозначных случаях МРТ с химическим сдвигом может быть полезной для дифференциальной диагностики [ 2 , 7 ]. МРТ с химическим сдвигом имеет преимущество перед КТ в подтверждении наличия очагового ФИ поджелудочной железы. Характерная потеря интенсивности сигнала на Т1-взвешенном градиентном эхо-изображении в противофазе по сравнению с соответствующим синфазным изображением подтверждает присутствие микроскопического липида в очаге поджелудочной железы [ 7 ].Это гистологическое состояние, как правило, отсутствует при раке поджелудочной железы [ 2 ]. Последовательности МРТ с подавлением жира также полезны для диагностики FI (рисунки 16, 18 и 19).
Рисунок 18МРТ поджелудочной железы, выполненная для исключения холедохолитиаза у пациента, перенесшего острый панкреатит два месяца назад. Поперечные МРТ-изображения в фазе и противофазе соответственно показывают типичную глобальную гипер- (a) и гипоинтенсивность (b) поджелудочной железы. Т1-взвешенное изображение с подавлением жира (c) подтверждает пониженную интенсивность поджелудочной железы из-за массивного FI.Т1-взвешенное изображение с подавлением жира после усиления гадолиния (d) показывает однородное усиление всей поджелудочной железы.
Рис. 19Типичные аспекты МРТ в случае диффузного ФИ поджелудочной железы. FI преобладает на APH (тип 1a) с увеличением железы (белые стрелки). На T1-взвешенных изображениях (a и b) липоматозный APH имеет типичный высокий сигнал. Резкое исчезновение сигнала обнаруживается на изображениях, взвешенных по T1, с подавлением жира (c и d).
Из-за доброкачественности и редкости тяжелой ФИ поджелудочной железы результаты эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) недостаточно документированы.При минимальном ФИ панкреатограмма в норме [ 9 ]. При тяжелой ФИ, ЭРХПГ может проявляться стенозом или резкой обструкцией в части тела и хвоста. Стенозированный главный проток поджелудочной железы обычно гладкий и имеет удлиненную форму. Обструкцию следует отличать от патологической обструкции, вызванной агенезией, хроническим панкреатитом или раком. Сегодня эти редкие находки можно предпочтительно описать с помощью магнитно-резонансной холангиопанкреатографии (MRCP).
FI поджелудочной железы также может быть осложнен острым панкреатитом (рис. 20).Другими словами, ФИ поджелудочной железы не защищает орган от эпизода панкреатита. Тем не менее, в этих случаях классические особенности визуализации воспаления могут быть изменены фоном FI, что может привести к диагностической путанице. Очаговый острый или подострый панкреатит может имитировать опухолевое образование из-за очагового увеличения плотности ранее липоматозной части (рис. 14). В этих случаях необходимо наблюдение. Точно так же диффузный панкреатит может имитировать почти нормальную поджелудочную железу в случае массивной предсуществующей ФИ, особенно если для сравнения недоступны предыдущие изображения поджелудочной железы (рис. 21).
Рисунок 20Global FI (тип 2b) у 45-летнего пациента (a и b), не страдающего ожирением, гиперметаболическим состоянием или сахарным диабетом. FI затрагивает всю поджелудочную железу, за исключением небольшой части ПРК (черная звездочка на a). Через три года у больной диффузный отечный панкреатит (c и d) неустановленного происхождения. Железа опухшая с нечеткими контурами, плотность увеличилась из-за отека (белая звездочка на c и d). Особенно поражается головная часть (c).Через четыре месяца после эпизода панкреатита морфология липоматозной поджелудочной железы вернулась к исходному состоянию (e и f).
Рисунок 2160-летняя женщина поступила с клиническим и биологическим острым эпизодом панкреатита. Неулучшенная КТ брюшной полости показала умеренно липоматозную, но почти нормальную головную (b) и каудальную (d) части поджелудочной железы. Однако на предыдущей компьютерной томографии, найденной в базе данных, поджелудочная железа выглядела чрезвычайно липоматозной (тип 2b) (a и c).Из-за отека острый панкреатит стал причиной очень необычного «повторного появления» железы. Острый панкреатит на очень липоматозной поджелудочной железе может имитировать нормальную поджелудочную железу.
В нашей практике мы сталкивались с редкими ситуациями массивного LI поджелудочной железы – особенно у пожилых людей – при которых плотность жира была чрезвычайно низкой по сравнению с остальной частью внутрибрюшного жира (рис. 22). У этих пациентов было пониженное количество внутрибрюшного жира, вероятно, из-за хронической потери веса.Тем не менее объем ложа поджелудочной железы оставался нормальным. Причина такой очень низкой плотности неизвестна, но мы предполагаем, что этот аспект представляет собой реальное гистологическое замещение жировой ткани, а не жировую инфильтрацию. Сохранение объема железы также можно объяснить тем фактом, что этот жировой заменитель более устойчив к потере веса.
Рисунок 22Два случая (a и b, случай 1; c и d, случай 2) массивного диффузного (тип 2b) панкреатического FI у пожилых пациентов. Эти пациенты были очень стройными, с очень низким количеством внутрибрюшного жира, что резко контрастировало с сохранением нормального объема липоматозного ложа поджелудочной железы.Средняя плотность жирового ложа поджелудочной железы также оказалась значительно ниже, чем у внутрибрюшного жира. Расхождение составило от 25 до 35 грн. Этот аспект, вероятно, был связан с реальным гистологическим жировым отростком (а не с жировой инфильтрацией). Сохранение объема ложа поджелудочной железы также можно объяснить тем фактом, что этот жировой заменитель более устойчив к потере веса.
Массовый панкреатит в сравнении с протоковой аденокарциномой поджелудочной железы: КТ и МРТ для дифференциации | Визуализация рака
Киркегард Дж., Мортенсен Ф.В., Кронин-Фентон Д. Хронический панкреатит и риск рака поджелудочной железы: систематический обзор и метаанализ. Am J Gastroenterol. 2017; 112: 1366–72.
PubMed Google Scholar
Биргин Э., Хаблавец П., Теуль П., Рюкерт Ф., Вильгельм Т.Дж. Хронический панкреатит и резектабельная синхронная карцинома поджелудочной железы: анализ выживаемости. Панкреатология. 2018; 18: 394–8.
PubMed Google Scholar
Эльшериф С.Б., Вираркар М., Джавади С., Ибарра-Ровира Дж.Дж., Тамм Е.П., Бхосале ПР. Панкреатит и PDAC: ассоциация и дифференциация. Abdom Radiol. 2019; 45: 1324.
Google Scholar
Braganza JM, Lee SH, McCloy RF, McMahon MJ. Хронический панкреатит. Ланцет. 2011; 377: 1184–97.
CAS PubMed Google Scholar
д Вантини I, Амодио А, Габбриелли А., Кристофори С., Фруллони Л., Бенини Л.Хронический панкреатит: клиническое течение, недостаточность поджелудочной железы и метаболические последствия. В: Testoni PA, Mariani A, Arcidiacono PG, редакторы. Острый и хронический панкреатит. Новые концепции и научно обоснованные подходы. Edizioni Minerva Medica; 2013. с. 71–82.
Google Scholar
Wolske KM, Ponnatapura J, Kolokythas O, Burke LMB, Tappouni R, et al. Хронический панкреатит или опухоль поджелудочной железы? Подход к решению проблем. Рентгенография.2019; 39: 1965–82.
PubMed Google Scholar
Beger HG, Schlosser W, Friess HM, Büchler MW. Резекция головы с сохранением двенадцатиперстной кишки при хроническом панкреатите изменяет естественное течение болезни: 26-летний опыт работы в одном центре. Ann Surg. 1999; 230: 512–9 обсуждение 519–523.
CAS PubMed PubMed Central Google Scholar
Сингх В.К., Ядав Д., Гарг П.К.Диагностика и лечение хронического панкреатита: обзор. ДЖАМА. 2019; 322: 2422–34.
Függer R, Gangl O, Fröschl U. Клинический подход к пациенту с твердым образованием поджелудочной железы. Wien Med Wochenschr. 2014; 164: 73–9.
PubMed Google Scholar
Lowenfels AB, Maisonneuve P, Cavallini G, Ammann RW, Lankisch PG, Andersen JR, et al. Панкреатит и риск рака поджелудочной железы. Международная группа по изучению панкреатита.N Engl J Med. 1993; 328: 1433–147.
CAS PubMed Google Scholar
Talamini G, Falconi M, Bassi C, Sartori N, Salvia R, Caldiron E, et al. Заболеваемость раком при хроническом панкреатите. Am J Gastroenterol. 1999; 94: 1253–60.
CAS PubMed Google Scholar
Филипс А.Е., Шах Н., Борхани А.А., Ядав Д., Бренд RE. Панкреатит в анамнезе ускоряет развитие аденокарциномы поджелудочной железы.Поджелудочная железа. 2018; 47: 1262–6.
PubMed PubMed Central Google Scholar
Сайед А., Бабич О., Таккар П., Патель А., Абдул-Баки Х., Фарах К. и др. Определение панкреатита как фактора риска рака поджелудочной железы: роль, частота и сроки развития. Поджелудочная железа. 2019; 48: 1098–101.
CAS PubMed Google Scholar
Малинка Т., Кляйн Ф., Ле Тху Т., Рёш С.С., Вундсам Х., Библ М. и др.Двухнациональный анализ 252 резекций поджелудочной железы по поводу хронического панкреатита с учетом последовательности случайной карциномы и общего послеоперационного результата. Anticancer Res. 2018; 38: 4947–52.
PubMed Google Scholar
Zheng Z, Chen Y, Tan C, Ke N, Du B, Liu X. Риск рака поджелудочной железы у пациентов, перенесших операцию по поводу хронического панкреатита. BMC Surg. 2019; 19: 83.
PubMed PubMed Central Google Scholar
Уэда Дж., Танака М., Оцука Т., Токунага С., Симосегава Т. Хирургическое лечение хронического панкреатита снижает риск рака поджелудочной железы: многоцентровый ретроспективный анализ. Операция. 2013; 153: 357–64.
PubMed Google Scholar
Ким Т., Мураками Т., Такамура М., Хори М., Такахаши С., Накамори С. Масса поджелудочной железы из-за хронического панкреатита: корреляция характеристик КТ и МРТ с патологическими данными. AJR Am J Roentgenol.2001; 177: 367–71.
CAS PubMed Google Scholar
Дутта А.К., Чако А. Масса головы при хроническом панкреатите: воспалительном или злокачественном. Мир J Gastrointest Endosc. 2015; 7: 258–64.
PubMed PubMed Central Google Scholar
Srisajjakul S, Prapaisilp P, Bangchokdee S. Функции КТ и МРТ, которые могут помочь отличить очаговый хронический панкреатит от рака поджелудочной железы.Radiol Med. 2020; 13: 1.
Google Scholar
Олесен С.С., Лисицкая М.В., Древес А.М., Новович С., Нойгаард С., Калаитцакис Э. и др. Кальцификации поджелудочной железы связаны с различными этиологическими факторами риска у пациентов с хроническим панкреатитом: многоцентровое исследование 1500 случаев. Панкреатология. 2019; 19: 922–8.
CAS PubMed Google Scholar
Campisi A, Brancatelli G, Vullierme MP, Levy P, Ruszniewski P, Vilgrain V.Специфичны ли кальцификаты поджелудочной железы для диагностики хронического панкреатита? Многорядный КТ-анализ. Clin Radiol. 2009; 64: 903–11.
CAS PubMed Google Scholar
Итикава Т., Соу Х., Араки Т., Арбаб А.С., Йошикава Т., Исигаме К. и др. Признак проницаемости протока при MRCP: полезность для дифференциации воспалительного новообразования поджелудочной железы от карциномы поджелудочной железы. Радиология. 2001; 221: 107–16.
CAS PubMed Google Scholar
Бонинсенья Э., Манфреди Р., Негрелли Р., Авесани Г., Мехраби С. и др. Стеноз протока поджелудочной железы: дифференциальная диагностика злокачественных и доброкачественных состояний при MRCP с повышенным секретином. Clin Imaging. 2017; 41: 137–43.
PubMed Google Scholar
Tirkes T. Хронический панкреатит: что клиницист хочет знать о МРТ. Магнитно-резонансная томография Clin N Am. 2018; 26: 451–61.
PubMed PubMed Central Google Scholar
Раджан Э., Клэйн Дж. Э., Леви М. Дж., Нортон И. Д., Ван К. К., Виерсема М. Дж. И др. Возрастные изменения поджелудочной железы, выявленные с помощью EUS: проспективная оценка. Gastrointest Endosc. 2005; 61: 401–6.
PubMed Google Scholar
Ядав А.К., Шарма Р., Кандасами Д., Прадхан Р.К., Гарг П.К., Бхалла А.С. и др. Перфузионная КТ – может ли она разрешить карциному поджелудочной железы по сравнению с загадкой хронического панкреатита, образующей массу? Панкреатология. 2016; 16: 979–87.
PubMed Google Scholar
Аслан С., Нурал М.С., Камлидаг И., Даначи М. Эффективность перфузионной КТ в дифференциации аденокарциномы протока поджелудочной железы от массивного хронического панкреатита и характеристика изоаттенуирующих поражений поджелудочной железы. Abdom Radiol. 2019; 44: 593–603.
Google Scholar
Zhang TT, Wang L, Liu HH, Zhang CY, Li XM, Lu JP, et al.Дифференциация карциномы поджелудочной железы и массово-очагового панкреатита: качественная и количественная оценка с помощью динамической МРТ с контрастным усилением в сочетании с диффузионно-взвешенной визуализацией. Oncotarget. 2017; 8: 1744–59.
PubMed Google Scholar
Де Робертис Р., Кардоби Н., Ортолани С., Тинацци Мартини П., Стеммер А., Гримм Р. и др. Интравоксельная МРТ-визуализация твердых образований поджелудочной железы, взвешенная по диффузии, некогерентного движения: надежность и полезность для характеристики.Abdom Radiol. 2019; 44: 131–9.
Google Scholar
Кан К.М., Ли Дж. М., Юн Дж. Х., Кифер Б., Хан Дж. К., Чой Б. И.. Интравоксельная МРТ-визуализация с диффузионно-взвешенным некогерентным движением для характеристики очаговых поражений поджелудочной железы. Радиология. 2014; 270: 444–53.
PubMed Google Scholar
Ким Б., Ли С.С., Сунг И.С., Чеонг Х., Бюн Дж. Х., Ким Х. Дж. И др. Интравоксельная визуализация поджелудочной железы с диффузионно-взвешенными движениями некогерентного движения: характеристика доброкачественных и злокачественных патологий поджелудочной железы.J. Магнитно-резонансная томография. 2017; 45: 260–9.
PubMed Google Scholar
Ruan Z, Jiao J, Min D, Qu J, Li J, Chen J, et al. Функции мультимодальной визуализации позволяют отличить карциному поджелудочной железы от хронического панкреатита головки поджелудочной железы. Oncol Lett. 2018; 15: 9735–44.
PubMed PubMed Central Google Scholar
Керстинг С., Конопке Р., Керстинг Ф., Фольк А., Дистлер М., Бергерт Н.Количественный анализ перфузии при трансабдоминальном контрастном ультразвуковом исследовании новообразований поджелудочной железы и карцином. Гастроэнтерология. 2009; 137: 1903–11.
PubMed Google Scholar
Иглесиас-Гарсия J, Линдквист B, Lariño-Noia J, Domínguez-Muñoz JE. Роль EUS по отношению к другим методам визуализации в дифференциальной диагностике между массовым хроническим панкреатитом, аутоиммунным панкреатитом и протоковой аденокарциномой поджелудочной железы.Rev Esp Enferm Dig. 2012; 104: 315–21.
PubMed Google Scholar
Д’Онофрио М., Де Робертис Р., Барби Е., Мартоне Е., Манфрин Е., Гоббо С. и др. Чрескожная тонкоигольная аспирация солидных новообразований поджелудочной железы под контролем УЗИ: 10-летний опыт более чем 2000 случаев и обзор литературы. Eur Radiol. 2016; 26: 1801–7.
PubMed PubMed Central Google Scholar
Сидху П.С., Брабранд К., Кантисани В., Корреас Дж. М., Цуй Х. С., Д’Онофрио М. и др. Руководство EFSUMB по интервенционному ультразвуку (INVUS), часть II. Диагностические интервенционные процедуры под контролем УЗИ (полная версия). Ultraschall Med. 2015; 36: E15–35.
CAS PubMed Google Scholar
Вакабаяси Т., Каваура Ю., Сатомура Ю., Ватанабе Х., Мотоу И., Окаи Т. и др. Клинические и визуальные особенности аутоиммунного панкреатита с очаговым отеком поджелудочной железы или образованием массы: сравнение с так называемым опухолевым панкреатитом и карциномой поджелудочной железы.Am J Gastroenterol. 2003. 98: 2679–87.
PubMed Google Scholar
Чой С.И., Ким С.Х., Кан Т.В., Сон К.Д., Пак Х.Дж., Чой Й. Дифференциация массообразующего аутоиммунного панкреатита от аденокарциномы протока поджелудочной железы на основе данных МРТ и DWI с контрастированием. AJR Am J Roentgenol. 2016; 206: 291–300.
PubMed Google Scholar
Kwon JH, Kim JH, Kim SY, Byun JH, Kim HJ, Lee MG, et al.Дифференциация очагового аутоиммунного панкреатита и протоковой аденокарциномы поджелудочной железы: МРТ с контрастным усилением с особым акцентом на артериальной фазе. Eur Radiol. 2019; 29: 5763–71.
PubMed Google Scholar
Найто И., Накадзава Т., Хаяси К., Окумура Ф., Миябе К., Симидзу С. и др. Клинические различия между массообразующим аутоиммунным панкреатитом и раком поджелудочной железы. Сканд Дж Гастроэнтерол. 2012; 47: 607–13.
CAS PubMed Google Scholar
Чанг В.И., Ким Б.Дж., Ли Дж.К., Кан Пи, Ли К.Х., Ли К.Т. и др. Клинико-рентгенологические характеристики очагового массово-образующего аутоиммунного панкреатита: сравнение с хроническим панкреатитом и раком поджелудочной железы. Поджелудочная железа. 2009; 38: 401–8.
PubMed Google Scholar
Мухи А., Итикава Т., Мотосуги Ю., Су Х., Сано К., Цукамото Т. и др. Массовый аутоиммунный панкреатит и карцинома поджелудочной железы: дифференциальный диагноз на основе компьютерной томографии и магнитно-резонансной холангиопанкреатографии и результатов диффузионно-взвешенной визуализации.J. Магнитно-резонансная томография. 2012; 35: 827–36.
PubMed Google Scholar
Muraki T, Kim GE, Reid MD, Mittal P, Bedolla G, Memis B, et al. Парадуоденальный панкреатит: визуализация и патологическая корреляция 47 случаев выявляют различные подтипы и факторы, участвующие в его этиопатогенезе. Am J Surg Pathol. 2017; 41: 1347–63.
PubMed Google Scholar
de Pretis N, Capuano F, Amodio A, Pellicciari M, Casetti L, Manfredi R, et al. Клинические и морфологические особенности парадуоденального панкреатита: итальянский опыт с 120 пациентами. Поджелудочная железа. 2017; 46: 489–95.
PubMed Google Scholar
Triantopoulou C, Dervenis C, Giannakou N, Papailiou J, Prassopoulos P. Панкреатит с бороздками: диагностическая проблема. Eur Radiol. 2009; 19: 1736–43.
CAS PubMed Google Scholar
Миттал П.К., Харри П., Нандвана С., Морено С.К., Мураки Т., Адсей В. и др. Парадуоденальный панкреатит: доброкачественные и злокачественные имитации на МРТ. Abdom Radiol. 2017; 42: 2652–74.
Google Scholar
Визуализация делает успехи в лечении заболеваний поджелудочной железы
Многие заболевания поджелудочной железы у педиатрических пациентов имеют характерный вид на снимках. Анализ этих состояний на УЗИ, КТ и МРТ должен помочь понять патологические процессы, влияющие на поджелудочную железу у этой популяции пациентов.
Этот анализ основан на результатах визуализации из нашей собственной базы данных детской патологии поджелудочной железы. Мы выполняли УЗИ во всех случаях и КТ и / или МРТ, когда результаты УЗИ были безрезультатными. МР-холангиопанкреатография (MRCP) использовалась для исследования протоков поджелудочной железы.
Поджелудочная железа представляет собой неинкапсулированную многодолевую железу, которая простирается от второй части двенадцатиперстной кишки до ворот селезенки. 1 Эмбриологически он образуется из брюшной зачатка, которая становится нижней головкой поджелудочной железы и крючковатым отростком, и дорсальной зачаткой, которая становится верхней панкреатической головкой, телом и хвостом.Два зачатка сливаются на седьмой неделе беременности, и более чем в 90% случаев сливаются протоки. 2
Размер поджелудочной железы зависит от возраста ребенка. Проток Вирсунга заканчивается во второй части двенадцатиперстной кишки у большого сосочка вместе с общим желчным протоком. Дополнительный проток поджелудочной железы, дренирующий малую ампулу, присутствует у 44% пациентов. 2
Ультразвук является методом выбора для первоначальной оценки подозрения на заболевание поджелудочной железы у детей, 2 из-за отсутствия жира, выступа левой доли печени и отсутствия ионизирующего излучения или необходимости седации. .Никакой специальной подготовки не требуется, кроме шести-восьми часов голодания (три часа для новорожденных).
Исследование, как правило, проводится с использованием секторного преобразователя 5 или 7,5 МГц, хотя у детей старшего возраста можно использовать секторный преобразователь 3,5 МГц. Выполняется поперечное и продольное сканирование всей поджелудочной железы. Следует измерить каждую часть органа и сравнить ее эхогенность с эхогенностью печени. Также следует проводить систематическое сканирование всей верхней части живота (рис. 1А).
МРТ поджелудочной железы показана в случаях неоптимальных или сомнительных результатов ультразвукового исследования с высоким клиническим подозрением на патологию. 3,4 Конкретные показания включают оценку острого и хронического панкреатита и характеристику сложных скоплений перипанкреатической жидкости. Полная оценка заболевания поджелудочной железы обычно требует Т1-взвешенных последовательностей с подавлением жира до и после контрастирования, а также Т2-взвешенных последовательностей, но выбор последовательностей будет зависеть от сканера.
MRCP – это неинвазивный метод визуализации панкреатобилиарного тракта. 2 Поджелудочная железа имеет более высокую интенсивность сигнала T1 на последовательностях с подавлением жира, чем любой другой внутрибрюшной орган. Интенсивность сигнала выше, чем у печени на артериально-капиллярной фазе изображений, усиленных гадолинием, и аналогична интенсивности сигнала печени на изображениях с задержкой. Интенсивность сигнала Т2 нормальной поджелудочной железы варьируется; он может быть равным печени или достигать уровня абдоминального жира (рис. 1В).
КТ не рекомендуется в качестве основного метода визуализации поджелудочной железы у детей, но она полезна, когда результаты ультразвукового исследования не являются диагностическими и МРТ недоступна. 5 CT может использоваться для диагностических и терапевтических процедур, таких как аспирационная биопсия или дренирование. Пациенты, проходящие КТ, должны по возможности получать адекватный внутривенный контраст и пероральный контраст. Мы варьируем толщину среза, шаг и интервал реконструкции в зависимости от возраста пациента, сводя дозу к минимуму. Ослабление КТ поджелудочной железы обычно аналогично ослаблению печени.
ВРОЖДЕННЫЕ АНОМАЛИИ
Истинные эпителиальные кисты поджелудочной железы встречаются редко и возникают в результате аномального развития протоков поджелудочной железы. 1 Кисты могут появляться сами по себе или в сочетании с системными заболеваниями, такими как синдром фон Гиппеля-Линдау или поликистоз почек. 6,7 При большом количестве эпителиальных кист определить их происхождение бывает сложно. Дифференциальный диагноз включает брыжеечные кисты, кисты холедоха и дупликационные кишечные кисты. 6-8
Ультразвук показывает четко выраженную безэховую массу с толстыми стенками и акустическим усилением в задней части. 1 CT показывает массу с четко очерченными стенками и низким затуханием в центре. 2 МРТ показывает массу с гладкими стенками водоподобной интенсивности сигнала на T1- и T2-взвешенных изображениях. 3,8 MRCP полезен для исключения коммуникации с протоком поджелудочной железы или желчным деревом. 2 Окончательный диагноз может быть поставлен после патологического исследования образца. 6
Pancreas divisum, наиболее частая врожденная аномалия поджелудочной железы, представляет собой неполное слияние структур дорсального и вентрального протоков, при котором более длинный дорсальный проток поджелудочной железы выходит через меньший малый сосочек. 2 Состояние может быть диагностировано с помощью компьютерной томографии, когда головка поджелудочной железы увеличена при отсутствии видимых образований поджелудочной железы или когда в поджелудочной железе видна жировая расщелина. 5 Когда MRCP показывает несвязанные вентральный и дорсальный протоки поджелудочной железы, входящие в двенадцатиперстную кишку, это подтверждает измененную анатомию протока. 9,2
Кольцевидная поджелудочная железа, вторая по частоте врожденная аномалия поджелудочной железы, 2,3 характеризуется тканью поджелудочной железы, полностью или частично окружающей нисходящую двенадцатиперстную кишку.Пациенты с полной кольцевой поджелудочной железой присутствуют в неонатальном периоде с симптоматической непроходимостью кишечника и специфическим признаком «двойного пузыря» на рентгенограмме. Пациенты с неполной или частичной кольцевой поджелудочной железой могут появиться только в зрелом возрасте. 9 КТ или МРТ могут показать утолщение передней, боковой и задней части нисходящей двенадцатиперстной кишки, вызванное интенсивностью тканевого сигнала и характеристиками усиления, которые идентичны характеристикам паренхимы поджелудочной железы. 2,3,5
Синдром фон Хиппеля Линдау – аутосомно-доминантное заболевание, которое приводит к ангиоматозу сетчатки, гемангиобластоме мозжечка и кистам различных органов. 10 Кисты обычно маленькие и множественные. Скопление множественных кист затрудняет их дифференциацию от микрокистозных аденом. Диагностическим считается наличие кист поджелудочной железы у пациента с семейным анамнезом синдрома фон Гиппеля-Линдау. 3,8 Наблюдения на УЗИ, КТ и МРТ аналогичны наблюдениям за врожденными кистами поджелудочной железы, кистами поджелудочной железы у пациентов с поликистозом почек и цистозом поджелудочной железы. Окончательный диагноз ставится на основании истории болезни и других результатов визуализации. 3
Синдром Швахмана-Даймонда – редкое аутосомно-рецессивное заболевание, которое обычно проявляется в младенчестве. Он характеризуется внешнесекреторной недостаточностью поджелудочной железы, которая приводит к нарушению всасывания (с нормальными результатами потового теста), низкому росту и дисфункции костного мозга. 11 Характерной патологической находкой является жировая инфильтрация поджелудочной железы, уменьшение ацинусов и сохранение островков. 1 Ультразвук показывает гиперэхогенную поджелудочную железу, размер которой не изменился, что помогает отличить ее от муковисцидоза, при котором поджелудочная железа меньше. 1 КТ показывает полное жировое замещение поджелудочной железы, протоковую эктазию и кальцификаты. 5 Жировая инфильтрация поджелудочной железы имеет такую же или более высокую интенсивность сигнала, чем остальная часть поджелудочной железы на T1-взвешенной МРТ. 11
Несидиобластоз представляет собой сохранение нормального состояния поджелудочной железы плода, характеризующееся диффузной пролиферацией и сохранением несидиобластов. 1,12 У пациентов может развиться гипогликемия из-за аномальной секреции инсулина фетальными клетками поджелудочной железы; несидиобластоз – наиболее частая и тяжелая причина гипогликемии у новорожденных и младенцев. 12
Ультразвук, КТ и МРТ в большинстве случаев не демонстрируют патологических изменений, хотя визуализация может показать неспецифическое увеличение размера головки, тела или хвоста поджелудочной железы (рис. 2). 1,13 Во избежание повторных операций рекомендуется почти тотальная (95%) панкреатэктомия. Остаток ткани поджелудочной железы (в основном голова) остается для защиты общего желчного протока.
Может произойти регенерация поджелудочной железы без рецидива гипогликемии после почти полной панкреатэктомии, и в таких случаях УЗИ демонстрирует нормальную поджелудочную железу.Также может произойти частичная регенерация ткани поджелудочной железы.
Муковисцидоз – наиболее серьезное аутосомно-рецессивное заболевание поджелудочной железы среди белых. 14,15 Он характеризуется дисфункциональным транспортом хлорид-иона через эпителиальные поверхности. 14 Хотя болезнь легких является преобладающей причиной заболеваемости и смерти, диагноз у детей обычно ставится на основании желудочно-кишечных симптомов. 14
Кисты, которые обычно имеют небольшой размер, скорее всего, возникают вторично из-за закупорки протока сгущенными секретами.Ультразвук показывает повышение эхогенности и уменьшение размеров поджелудочной железы. Мелкодольчатая (похожая на булыжник) эхо-картину обычно наблюдается в поджелудочной железе, 1,14 , а небольшие или сгруппированные кальцификаты можно наблюдать в любой части поджелудочной железы.
CT демонстрирует полное замещение поджелудочной железы жиром как увеличение размера поджелудочной железы с низкими значениями затухания. МРТ показывает увеличенную поджелудочную железу с высокой интенсивностью сигнала на Т1-взвешенных изображениях. Полная атрофия поджелудочной железы без жирового замещения также может быть видна, и в этом случае поджелудочная железа кажется уменьшенной в размере с ослаблением мягких тканей, но без затухания жира или высокой интенсивности сигнала.Области фиброза демонстрируют низкие значения затухания без постконтрастного усиления на КТ и низкую интенсивность сигнала на Т1- и Т2-взвешенных МРТ изображениях. Также может наблюдаться полный фиброз поджелудочной железы и кальцификаты поджелудочной железы. 4,14,15
Скопления кист до нескольких сантиметров в диаметре в редких случаях могут полностью заменить поджелудочную железу, вызывая массовый эффект в брюшной полости. Это состояние известно как цистоз поджелудочной железы (рис. 3). Ультразвук, КТ и МРТ могут визуализировать это полное замещение поджелудочной железы одно- или многоязычными кистозными массами.
Ультразвук показывает множественные сонопрозрачные, округлые, четко определенные, заполненные жидкостью поражения, простирающиеся от ворот печени до ворот селезенки и гиперэхогенную ткань поджелудочной железы, разбросанную по кистам. 1 Большинство поражений демонстрируют однородное содержание воды на КТ и, реже, немного более высокое значение затухания. 3,14 Могут быть видны небольшие кальцификации, и идентифицируемая ткань поджелудочной железы исчезает, когда макрокисты полностью замещают поджелудочную железу. 14 T1-взвешенная МРТ показывает однородный сигнал низкой интенсивности, который значительно ниже, чем у ткани поджелудочной железы. Кисты имеют очень высокую интенсивность сигнала на Т2-взвешенной МРТ. Стенки кисты выглядят как тонкие регулярные линии с низкой интенсивностью сигнала. 4,15
ПАНКРЕАТИТ
Острый панкреатит – это преимущественно диффузный воспалительный процесс. Степень поражения поджелудочной железы может широко варьироваться. 16 В педиатрии случаи острого панкреатита редки; те, что случаются, обычно вызваны травмой. 1,5,16,17 Наиболее частая находка при УЗИ – диффузное или очаговое увеличение желез и снижение эхогенности с плохо очерченными границами. 1 В некоторых случаях поджелудочная железа выглядит нормальной. КТ показывает диффузное увеличение поджелудочной железы, неоднородное ослабление, плохо очерченный контур поджелудочной железы и перипанкреатическую жидкость в переднем околопочечном пространстве и малом мешочке (рис. 4). Паттерн ослабления вызван резким уменьшением (или полным отсутствием) усиления, вызванным ишемическими и некротическими зонами. 5,16-18
Т1-взвешенная МРТ острого панкреатита выявляет очаговое или диффузное увеличение и перипанкреатические воспалительные изменения, 3,4 , в то время как Т2-взвешенная МРТ демонстрирует перипанкреатический отек и скопления жидкости. Главный проток поджелудочной железы сохраняет гладкий контур на MRCP, но может быть сдавлен окружающей отечной паренхимой. 2
Псевдокисты являются наиболее частым местным осложнением острого панкреатита и наиболее распространенным типом кисты поджелудочной железы. 7,16-18 Псевдокисты могут быть экстра- или интрапанкреатическими. 18 Ультразвук показывает псевдокисты как безэховые структуры с четко определенными границами и задним укреплением. 1 CT показывает их круглой или овальной формы, с тонкой капсулой и жидким содержимым <15 HU. Более высокие значения затухания указывают на внутрикистозное кровоизлияние. 3
Повреждения обычно однородны с интенсивностью сигнала, сопоставимой с интенсивностью сигнала воды на T1- и T2-взвешенной МРТ. 3,4 MRCP показывает сообщение с протоком поджелудочной железы или с другими соседними органами. 2 Хотя абсцессы поджелудочной железы могут выглядеть как псевдокисты, их можно отличить по анамнезу или наличию газа в коллекции. 18
Хронический панкреатит – воспалительный процесс поджелудочной железы с необратимой экзокринной и эндокринной дисфункцией, чаще всего вызываемый наследственным панкреатитом у детей. 1,19 Ультразвук показывает атрофию паренхимы с очаговым увеличением поджелудочной железы, повышенной эхогенностью, кальцификациями, расширением протоков и неправильными очертаниями поджелудочной железы.Отложения кальция, визуализируемые как эхогенный очаг, отбрасывающий акустическую тень, а также иногда видны псевдокисты. 1 КТ демонстрирует кальцификаты (сгруппированные и / или рассеянные), очаговую или диффузную атрофию паренхимы и дилатацию основных протоков поджелудочной железы и желчных протоков. 5,19 При хроническом панкреатите поджелудочная железа обычно становится атрофической. Если в таких случаях наблюдается очаговое или диффузное увеличение, дифференциальный диагноз должен включать злокачественность.
Хронический панкреатит проявляется в снижении интенсивности сигнала на Т1-взвешенной МРТ. 3,4 Изображения с немедленным постконтрастом и с отложенным улучшением показывают снижение неоднородного усиления и атрофию железы. MRCP выявляет расширение и неправильные контуры протока. 2
НОВООБРАЗОВАНИЯ, МЕТАСТАЗЫ
Злокачественные и доброкачественные новообразования поджелудочной железы у детей крайне редки. 1,5,7 Опухоли поджелудочной железы классифицируются как эпителиальные и неэпителиальные по происхождению. 5 Эпителиальные опухоли поджелудочной железы могут происходить из эндокринной или неэндокринной ткани и могут быть злокачественными или доброкачественными.Неэпителиальные опухоли поджелудочной железы, включая лимфому и рабдомиосаркому, могут быть первичными или метастатическими.
Муцинозное кистозное новообразование, наиболее распространенное кистозное новообразование поджелудочной железы, чаще всего встречается у женщин среднего возраста и редко у детей. 7,8 Эта опухоль обычно состоит из большой многоячеистой кисты, содержащей муцинозный материал или геморрагическую жидкость, и ее следует отличать от псевдокисты. 7
Микрокистозная аденома (серозная цистоаденома) – второе по распространенности кистозное новообразование поджелудочной железы.Эти доброкачественные опухоли чаще встречаются у пациентов с болезнью фон Гиппеля-Линдау 7,8 и обычно располагаются в головке поджелудочной железы. Микрокистозные аденомы обычно состоят из множества небольших кист, разделенных фиброзными перегородками, исходящими от центра.
Нейроэндокринные опухоли, которые встречаются относительно редко, возникают из клеток островков Лангерганса поджелудочной железы. 7 К пяти типам относятся инсуломы (самые распространенные), гастриномы, глюкагономы, соматостатиномы и опухоли, которые секретируют вазоактивный кишечный пептид.Все чаще возникают у взрослых среднего возраста, чем у детей.
Примерно 50% нейроэндокринных опухолей не имеют гормональной функции. Как функционирующие, так и нефункционирующие нейроэндокринные опухоли характеризуются гиперваскуляризацией. Опухоли из нефункционирующих островковых клеток обычно имеют большие размеры и иногда содержат кальцификаты. 10 У них может развиться кистозный вид вследствие дегенерации и некроза. Опухоли из функционирующих островковых клеток имеют тенденцию быть небольшими, четко очерченными, круглыми или овальными.
Панкреатобластома поражает преимущественно детей раннего возраста. В целом это редкая опухоль, но наиболее частое новообразование поджелудочной железы у детей. 7,10 Эти опухоли имеют тенденцию быть большими и одиночными и могут возникать в любой области поджелудочной железы. Ультразвук показывает твердые образования смешанной эхогенности с участками кистозного изменения или кальцификации. КТ показывает неоднородное усиление с кальцинированными очагами или без них. Опухоли имеют сигнал от низкого до среднего на Т1-взвешенной МРТ и высокую интенсивность сигнала на Т2-взвешенной МРТ. 7,10
Метастазы поджелудочной железы встречаются чаще, чем первичные новообразования. Неходжкинская лимфома, наиболее часто встречающееся опухолевое заболевание поджелудочной железы у детей, поражает поджелудочную железу вторично примерно у 30% пациентов с широко распространенным заболеванием. 1,20 Злокачественное новообразование обычно распространяется на поджелудочную железу путем прямого распространения от перипанкреатической лимфаденопатии. Первичное поражение поджелудочной железы встречается редко и поражает от 2% до 5% пациентов с экстранодальными лимфомами. Эти метастазы обычно развиваются на поздних стадиях заболевания и часто сопровождаются сопутствующими внепанкреатическими метастазами. 20
Метастазы на УЗИ проявляются как одиночные или множественные поражения. Они визуализируются как твердые, гипоэхогенные, четко определенные образования или как диффузная железистая инфильтрация. Сама поджелудочная железа кажется больше и имеет пониженную эхогенность. 1 CT показывает три картины: большое, четко очерченное яйцевидное или округлое локализованное образование, которое является либо изоденсным, либо гиподенсным (от 50% до 73% случаев), диффузное увеличение поджелудочной железы с гладким или дольчатым контуром (Рисунок 5) и множественные узелки поджелудочной железы. 20
ДОПОЛНИТЕЛЬНЫЕ РЕЗУЛЬТАТЫ
Жировую инфильтрацию поджелудочной железы может вызывать ряд факторов, включая длительное лечение кортикостероидами или цитостатиками, парентеральное питание, болезнь Кушинга и ожирение. 1,5,21 При жировой инфильтрации липид поджелудочной железы ограничен интерстициальной стромой, не затрагивает экзокринные или эндокринные паренхимные клетки и обычно имеет мало клинических последствий. 21
Распространение жировой инфильтрации варьирует, но тело и хвост поджелудочной железы являются доминирующими областями замещения жировой ткани.Ультразвук показывает гиперэхогенную поджелудочную железу без изменения размера. 1 КТ выявляет ткань с низким затуханием, перемежающуюся между нормальной паренхимой поджелудочной железы. 5 МРТ показывает более высокую интенсивность сигнала в поджелудочной железе с жировой инфильтрацией, чем в остальной части поджелудочной железы, но эта интенсивность сигнала теряется на Т1-взвешенной МРТ с градиентным эхом в противофазе. 3,21
DR. ГЕРРЕРО, ДР. БЕРРОКАЛ и ДР. LARRAURI базируются в Университетской больнице Ла-Пас в Мадриде, Испания.В подготовке этой рукописи участвовали Беатрис Родригес-Виджил, Альберто Браво и Консуэло Прието из того же отдела.
СПИСОК ЛИТЕРАТУРЫ
1. Беррокаль Т., Прието С., Игнасио П. и др. Сонография заболеваний поджелудочной железы у младенцев и детей. Радиография 1995; 15 (2): 301-313.
2. Фулчер А.С., Тернер М.А. МР-панкреатография: полезный инструмент для оценки заболеваний поджелудочной железы. Радиография 1999; 19 (1): 5-24.
3. Ито К., Коике С., Мацунага Н.МРТ заболеваний поджелудочной железы. Europ J Radiol 2001; 38 (2): 78-93.
4. Ly JN, Miller FH. МРТ поджелудочной железы: практический подход. Радиол Clin N Am 2002; 40 (6): 1289-1306.
5. Вон Д.Д., Джабра А., Фишман Э. Заболевание поджелудочной железы у детей и молодых людей: оценка с помощью компьютерной томографии. Радиография 1998; 18 (5): 1171-1187.
6. Boulanger SC, Borowitz DS, Fisher JF, Brisseau GF. Врожденные кисты поджелудочной железы у детей. J Pediatr Surg 2003; 38 (7): 1080-1082.
7.Джонсон П., Шпиц Л. Кисты и опухоли поджелудочной железы. Семин Педиатр Хирургия 2000; 9 (4): 209-215.
8. Хаммонд Н., Миллер Ф. Х., Sica GT, Гор РМ. Визуализация кистозных заболеваний поджелудочной железы. Радиол Clin N Am 2002; 40 (6): 1243-1263.
9. Беня Э. Поджелудочная железа и желчная система: визуализация аномалий развития и заболеваний, характерных только для детей. Радиол Clin N Am 2002; 40 (6): 1355-1363.
10. Mukhopadhyay B., Sahdev A, Monson JP, et al. Поражения поджелудочной железы при болезни фон Гиппеля-Линдау.Clin Endocrinol 2002; 57 (5): 603-608.
11. Smith OP. Синдром Швахмана-Даймонда. Семин Гематол 2002; 39 (2): 95-102.
12. Cretolle C, Fekete CN, Jan D, et al. Частичная плановая панкреатэктомия является излечивающей при очаговой форме постоянной гиперинсулинемической гипогликемии в младенчестве: отчет о 45 случаях с 1983 по 2000 год. J Pediatr Surg 2002; 37 (2): 155-158.
13. Рахье Дж., Гио Й., Семпу С. Стойкая гиперинсулинемическая гипогликемия младенчества: гетерогенный синдром, не связанный с несидиобластозом.Arch Dis Child Fetal Neonatal Ed 2000; 82 (2): F108-F112.
14. Agrons GA, Corse WR, Markowitz RI, et al. Желудочно-кишечные проявления муковисцидоза: лучевая и патологическая корреляция. Радиография 1996; 16 (4): 871-893.
15. King LJ, Scurr ED, Natajaran M, et al. Гепатобилиарные и панкреатические проявления муковисцидоза: МРТ. Радиография 2000; 20 (3): 767-777.
16. Balthazar EJ. Стадия острого панкреатита. Радиол Clin N Am 2002; 40 (6): 1199-1209.
17. Джексон В.Д. Панкреатит: этиология, диагностика и лечение. Curr Opin Pediatr 2001; 13 (5): 447-451.
18. Балтажар EJ. Осложнения острого панкреатита: клиника и компьютерная томография. Радиол Clin N Am 2002; 40 (6): 1211-1227.
19. Ремер Э.М., Бейкер МЭ. Визуализация хронического панкреатита. Радиол Clin N Am 2002; 40 (6): 1229-1242.
20. Скатаридж Дж. К., Хортон К. М., Шет С., Фишман Е. К.. Метастазы в паренхиму поджелудочной железы: наблюдения на спиральной компьютерной томографии. AJR 2001; 176 (3): 695-699.
21. Isserow JA, Siegelman ES, Mammone J. Фокальная жировая инфильтрация поджелудочной железы: МРТ-характеристика с визуализацией химического сдвига. AJR 1999; 173 (5): 1263-1265.
Визуализирующая диагностика и стадирование аденокарциномы протока поджелудочной железы: всесторонний обзор | Взгляд на визуализацию
Маленький и изоаттенуирующий PDAC
Обычное трансабдоминальное УЗИ может быть полезным для визуализации изоаттенуирующего новообразования поджелудочной железы на КТ [11]. При трансабдоминальном УЗИ PDAC обычно рассматривается как нерегулярная гипоэхогенная масса, связанная с резким перекрытием главного панкреатического протока (MPD) и дилатацией MPD выше по течению [12] (рис.1). Трансабдоминальное УЗИ имеет чувствительность от 75 до 89% для обнаружения PDAC в зависимости от опыта оператора, телосложения пациента и влияния кишечных газов на качество изображения [1]. Несмотря на эти ограничения, УЗИ является легкодоступным инструментом и часто используется при медицинских осмотрах. В многоцентровом исследовании аномалии УЗИ были ключом к диагностике ранней стадии PDAC у 91% и 41% пациентов с симптомами и бессимптомно, соответственно. Чаще всего сообщалось о дилатации MPD, за которой следовало образование поджелудочной железы и стриктура MPD [13].
Рис. 172-летний мужчина с изоаттенуирующим PDAC. КТ-изображение аксиальной фазы поджелудочной железы ( a ) показывает стриктуру MPD (стрелка) на теле поджелудочной железы без видимой массы. Поперечное трансабдоминальное ультразвуковое изображение ( b ) показывает гипоэхогенное образование (звездочка) в месте стриктуры MPD (стрелка). МРТ-изображения с динамическим контрастированием с использованием Т1-взвешенной последовательности с подавленным жиром в артериальной ( c ) и портальной венозной ( d ) фазах показывают стриктуру MPD (стрелка), но не демонстрируют отчетливую массу.Последующая панкреатодуоденэктомия показала PDAC
КТ считается исходным методом визуализации для оценки пациентов с подозрением на PDAC. КТ поджелудочной железы обычно выполняется с помощью двухфазного исследования с контрастным усилением, включая фазу поджелудочной железы обычно через 40–50 секунд и фазу воротной вены через 65–70 секунд. PDAC обычно имеет плотную фибробластическую строму и, следовательно, обычно выглядит как гипоаттенуирующая масса по сравнению с нормальной паренхимой поджелудочной железы во время панкреатической фазы [7, 9, 14]. PDAC можно точно диагностировать на КТ с общей чувствительностью 89% и специфичностью 90% [15].Однако небольшие и изоаттенуирующие PDAC являются сложной задачей и могут быть упущены из виду на КТ с зарегистрированной более низкой чувствительностью 58–77% для обнаружения небольших (≤ 2 см) опухолей [16,17,18]. Изоаттенуирующие опухоли имеют распространенность 5,4–11% в опухолях всех размеров и еще выше (27%) в опухолях небольшого размера (≤ 2 см) [7, 19, 20]. Примечательно, что изоаттенуирующие опухоли чаще встречаются среди хорошо дифференцированных PDAC по сравнению с низкодифференцированными [7] и связаны с лучшей выживаемостью после хирургической резекции.Изоаттенуирующий PDAC, как правило, имеет более низкую клеточность опухоли и менее частый некроз опухоли, чем гипоаттенуирующий PDAC [19]. Развивающаяся технология двухэнергетической КТ может быть полезной при обнаружении тонких, небольших опухолей за счет увеличения заметности поражения при реконструкции виртуальных моноэнергетических изображений с низким кэВ. Это преимущество основано на усилении разницы в ослаблении между гиповаскулярной опухолью и окружающей паренхимой [21].
Раннее выявление тонких PDAC можно улучшить путем выявления вторичных признаков, которые наблюдаются в большинстве (88%) небольших изоаттенуирующих опухолей.К вторичным признакам относятся следующие: (а) резкое прекращение MPD с расширением протока вверх по потоку или без него; (б) дистальная атрофия поджелудочной железы; (c) неправильный контур поджелудочной железы на месте опухоли; (d) расширенный знак MPD и CBD «двойной канал»; и (e) сосудистая оболочка или сужение [7, 22]. В исследовании Gangi et al., Фокальная стриктура и дилатация протока поджелудочной железы были ключевыми результатами КТ при тонкой PDAC. Оглядываясь назад, эти данные были обнаружены у 50 и 7% пациентов за 18 месяцев и раньше, соответственно, до фактического диагноза PDAC [23] (рис.2). Следовательно, вторичные признаки следует рассматривать как красный флаг, требующий дальнейшей оценки с помощью МРТ или EUS, а не последующего наблюдения [7].
Рис. 2Мужчина 72 лет с ОПАК. КТ-изображение аксиальной портальной фазы ( a ) показывает стриктуру MPD (стрелка) в теле поджелудочной железы с дилатацией вверх по потоку без видимой закупоривающей массы. КТ-изображения осевой воротной вены ( b и c ), полученные через 6 месяцев, показывают прогрессирование стриктуры MPD (стрелка) с усилением дилатации протока вверх по течению и атрофии поджелудочной железы.Имеется небольшая гипоаттенуирующая масса (стрелки в c ), связанная с увеличенным некротическим метастатическим портакавальным лимфатическим узлом (звездочка)
PDAC в основном выглядит гипоинтенсивным по сравнению с нормальной поджелудочной железой на T1-взвешенных изображениях с подавлением жира и гипоинтенсивным до изоинтенсивного на постконтрастном МРТ-изображения, взвешенные по T1 [24]. Сообщенная диагностическая точность МРТ эквивалентна КТ со специфичностью 89% [15]; тем не менее, он имеет дополнительную ценность при обнаружении изоаттенюирующего PDAC на CT [25].Ограниченная диффузия выявляется в PDAC на диффузионно-взвешенной визуализации (DWI) из-за уменьшения внеклеточного пространства и увеличения клеточности и фиброза внутри опухоли. DWI обладает высокой диагностической эффективностью с зарегистрированной чувствительностью и специфичностью 92–96% и 97–99% соответственно [26, 27]. Тем не менее, он имеет ограниченную диагностическую ценность в дифференциации PDAC от хронического панкреатита, образующего массу, из-за перекрытия значений ADC [28, 29].
EUS имеет особое значение для пациентов с высоким клиническим подозрением на PDAC без обнаруживаемого образования на КТ, особенно для небольших (≤ 2 см) опухолей.Сообщенные чувствительность и специфичность составили 87% и 98% соответственно. PDAC выглядит как гипоэхогенное поражение по сравнению с нормальной тканью поджелудочной железы. В отсутствие дискретной массы EUS имеет преимущество в получении биопсии ткани, нацеленной на область очаговой стриктуры поджелудочной железы или общего желчного протока [30].
Роль FDG-PET в раннем обнаружении PDAC остается спорной. Сообщается о высоких показателях обнаружения с чувствительностью 81–100% для небольших (≤ 2 см) PDAC [31, 32].Однако крупное ретроспективное исследование продемонстрировало снижение чувствительности FDG-PET до 50% для небольших опухолей, что указывает на его низкую диагностическую ценность при ранней стадии PDAC [33].
Крючковидный отросток PDAC
Крючковидный отросток представляет собой язычковое продолжение нижней части головки поджелудочной железы, которое простирается кзади за верхней брыжеечной веной (SMV) и артерией (SMA). Частота PDAC крючкового отростка составляет от 2,5% до 10,7% от всех PDAC [34]. Крючковидный отросток относительно удален от панкреатических и общих желчных протоков, но ближе к SMA, SMV и главной воротной вене (MPV) по сравнению с остальной поджелудочной железой.Благодаря этим особым анатомическим особенностям PDAC крючковидного отростка часто имеют клинические проявления и характеристики визуализации, отличные от других PDAC в головке поджелудочной железы. Боль в животе, а не желтуха, является наиболее частым симптомом при PDAC крючковидного отростка, часто приводящим к позднему клиническому проявлению и диагностике [8].
Крюковидный отросток PDAC, по сравнению с PDAC в других местах, чаще связан с сосудистой инвазией, а именно с оболочкой SMA, SMV и MPV (рис.3). Кроме того, сообщалось о более высокой частоте экстрапанкреатической периневральной инвазии [8, 35]. Инвазия двенадцатиперстной кишки также более распространена: частота составляет 68% по сравнению с 41% при других ОАП головного мозга [35]. В результате обструкция двенадцатиперстной кишки может развиться у 9% пациентов с PDAC крючковатым отростком [8]. На КТ и МРТ инвазия двенадцатиперстной кишки определяется как расширение смежной опухоли в стенке двенадцатиперстной кишки и фокальное прерывание нормального усиления стенок двенадцатиперстной кишки [35, 36] (рис.4).
Рис. 3Мужчина 63 лет с местно-распространенным ОПАП и крючковатым отростком. КТ-изображения осевой фазы поджелудочной железы ( a и b ) показывают образование (острие стрелки) в крючковом отростке, охватывающее SMA с умеренной дилатацией CBD (стрелка) и MPD (короткие стрелки) вверх по течению и связанное с умеренно растянутым желчным пузырем (GB)
Рис. 4Мужчина 63 лет с крючковатым отростком PDAC, вызывающим дуоденальную непроходимость. КТ-изображения осевой фазы поджелудочной железы ( a и b ) показывают гипоаттенуирующее образование (звездочка), возникающее из-за крючковидного отростка, инфильтрирующее третью часть двенадцатиперстной кишки (D) и упирающееся в переднюю стенку аорты.CBD (стрелка) нормальный по калибру. Поджелудочная железа (P) не имеет расширения или атрофии протоков. КТ-изображение осевой портальной фазы ( c ), полученное через 1 месяц, показывает заметное растяжение желудка (S) из-за дуоденальной непроходимости и новое гипоаттенуирующее метастатическое поражение печени (стрелка)
Ранняя стадия крючковидного процесса PDAC может легко не заметить при визуализации из-за тонкости опухоли и отсутствия вторичных признаков дилатации протока (рис. 5). Tamada et al. сообщили о 14% случаев PDAC без вторичных признаков на предоперационной КТ, из которых 50% были локализованы в крючковом отростке [11].
Рис. 5Мужчина 47 лет с крючковатым отростком PDAC. Осевые ( a ) и корональные ( b ) изображения КТ фазы поджелудочной железы показывают небольшую гипоаттенуирующую массу (стрелки) в крючковидном отростке поджелудочной железы. Из-за расположения опухоли нет дилатации CBD или MPD. Биопсия под контролем EUS выявила PDAC, и пациенту была проведена панкреатодуоденэктомия
Новые критерии визуализации для резектабельности опухоли
КТ является методом выбора для оценки сосудистой инвазии со специфичностью 82–100% и чувствительностью 70–96% [37 , 38,39,40].Двухфазная КТ поджелудочной железы, выполняемая с тонкими срезами (<3 мм, предпочтительно 0,5–1 мм, если доступно) и многоплоскостным переформатированием, является оптимальным методом для оценки перипанкреатических артерий и вен во время панкреатической и портальной венозной фаз соответственно [9 ]. Осевые, корональные и сагиттальные реконструкции следует тщательно исследовать, чтобы оценить контакт опухоли с окружностью и длинной осью сосудов. Изображения с проекциями максимальной интенсивности (MIP) и изображения с объемной визуализацией полезны для обнаружения тонких изменений в калибрах сосудов [41].МРТ, включая МР-ангиографию, является отличной альтернативой с чувствительностью и специфичностью, сравнимой с КТ [1, 15, 39, 42]. EUS имеет чувствительность 72% и специфичность 89% для предоперационной диагностики сосудистой инвазии [43] с более высокой чувствительностью (94%) и специфичностью (89%) при использовании контрастного вещества [44]. Однако ЭУЗИ обычно не рекомендуется для оценки сосудистого поражения из-за различной анатомии печеночных артерий, высокой зависимости от оператора и относительной инвазивности [45].
Опухолевый абатмент определяется как окружной контакт опухоли с сосудом под углом ≤ 180 °, а под оболочкой опухоли подразумевается контакт опухоли с сосудом под углом> 180 ° [9, 46, 47]. Знак слезы, измененная форма пораженной вены на аксиальных КТ-изображениях из-за оболочки опухоли или десмопластической реакции, тесно связан с венозной инвазией [41, 48]. Морфологические изменения артерии несут более высокий риск инвазии по сравнению с веной. Покрытие артерий опухолью на КТ имеет чувствительность до 80% и специфичность в отношении сосудистой инвазии до 98% [41, 49].
Местнораспространенные опухоли при отсутствии отдаленных метастазов обычно лечат химиолучевой терапией, тогда как резектабельные опухоли обычно лечат предварительной хирургической резекцией, которая является единственным потенциально излечивающим методом лечения PDAC [1, 2]. Пограничная резектабельная (BR) опухоль не может быть отнесена к этим двум категориям. Эта категория варьируется среди различных учреждений, особенно в определении критериев, связанных с венозной инвазией, из-за различий в операциях по реконструкции сосудов [40].В 2016 году Международная ассоциация панкреатологов (IAP) попыталась продвинуть международный консенсус по определению пограничной резектабельной PDAC (BR-PDAC) и включила (1) анатомические, (2) биологические и (3) условные критерии (Таблица 1) [ 50].
Таблица 1 Определяющие критерии пограничной резектабельности в соответствии с консенсусом Международной ассоциации панкреатологов (IAP) (2016)В консенсусе IAP 2016 года, немного отличается от рекомендаций Национальной комплексной сети рака (NCCN) в 2019 году (Таблица 2) [51 ], BR-PDAC подразделяется на венозный BR, где опухоль включает только PV / SMV, и артериальный BR, если артерии вовлечены отдельно или вместе с венами (рис.6). Кроме того, отсутствие контакта опухоли с первой ветвью тощей кишки, дренирующей в SMV, исключено из критериев IAP для BR-PDAC из-за анатомических изменений ветвей тощей кишки и трудностей идентификации на КТ. Вместо этого нижняя граница двенадцатиперстной кишки рассматривалась как анатомический ориентир для оценки степени венозной инвазии и отличия BR-PDAC от неоперабельной PDAC [50].
Таблица 2 Определяющие критерии резектабельности опухоли в соответствии с рекомендациями Национальной комплексной сети (NCCN) (2019) и консенсусом Международной ассоциации панкреатологов (IAP) (2016) Рис.6Мужчина 63 лет с PDAC. КТ-изображения осевой фазы поджелудочной железы ( a и b ) показывают гипоаттенуирующую массу (звездочка) в головке поджелудочной железы с контактом опухоли> 180 ° с замещенной правой печеночной артерией (длинная стрелка) и контактом опухоли> 180 ° с SMV ( короткая стрелка) при деформации просвета вены. Пациенту была выполнена полная панкреатэктомия и реконструкция сосудов после неоадъювантной терапии, но метастазы в печени развились через год после операции
Наличие анатомических вариантов артерий увеличивает риск интраоперационных сосудистых повреждений и послеоперационных осложнений, таких как ишемия печени, утечка билиарного анастомоза и псевдоаневризмы. .Анатомические вариации печеночной артерии встречаются у 55–79% пациентов и включают замененную правую или левую печеночную артерию, добавочную правую или левую печеночную артерию и гепатомезентериальный ствол, где общий печеночный ствол возникает из SMA [41, 48] . Предоперационная диагностика этих изменений может помочь в планировании хирургического вмешательства и выборе техники реконструкции сосудов, чтобы зарезервировать аберрантную артерию и избежать повреждения сосудов. Радиолог должен сообщить об артериальном варианте, особенно о наличии замещенной печеночной артерии или гепатомезентериального ствола, поскольку они могут определить резектабельность опухоли.В отчете также следует описать отсутствие или наличие и степень контакта опухоли с аберрантной артерией [9, 41].
PDAC считается неоперабельным, если имеется оболочка опухоли на CA / SMA, невозможная реконструкция SMV / PV или контакт опухоли с аортой, самой проксимальной ветвью SMV тощей кишки или первой ветвью SMA тощей кишки [51]. Благодаря своему расположению большой PDAC может распространяться через несколько перитонеальных и забрюшинных анатомических плоскостей и вторгаться в соседние структуры, включая желудок, селезенку, толстую кишку, почки и надпочечники.Инвазия опухоли в эти органы, если таковая имеется, должна быть описана в радиологическом отчете [9, 52]. Многоплоскостное переформатирование КТ помогает оптимально отслеживать кровеносные сосуды как анатомические ориентиры для распространения опухоли, например: (а) сосуды средней толстой кишки для поперечной ободочной кишки и мезоколон, (б) СМА и вена для брыжейки, (в) собственно печеночная артерия и PV для печеночно-двенадцатиперстной связки, (d) сосуды селезенки для селезеночной связки, селезенки и левой почки и (e) сосуды левого желудочно-сальника для большей кривизны желудка и ворот селезенки [9, 52].
Метастатическое заболевание, вызванное PDAC, обычно поражает печень, брюшину, легкие и кости. Интраоперационное обнаружение небольших метастазов в печени или перитонеальных метастазов является наиболее частой причиной (до 55%) прерванной операции у кандидатов с предоперационной КТ-диагностикой резектабельной опухоли [53, 54]. Пропущенные метастазы в печень обычно небольшие и обнаруживаются в субкапсулярной области печени, что повышает вероятность того, что это форма локорегионального перитонеального распространения, а не гематогенного метастаза [55].МРТ более чувствительна для изображения небольших метастазов в печень с чувствительностью 90─100% для МРТ с гадобенат димеглюмином или гадоксетовой кислотой по сравнению с 70─76% для КТ [56]. Кроме того, МРТ с DWI имеет большую специфичность для характеристики неопределенных поражений печени, выявленных на КТ; метастазы обычно демонстрируют промежуточную гиперинтенсивность на Т2-взвешенных МР-изображениях с ограниченной диффузией на DWI и усилением обода на динамических изображениях с контрастным усилением [55, 57]. Ранние перитонеальные метастазы часто скрыты и слишком малы, чтобы их можно было идентифицировать с помощью доступных в настоящее время методов визуализации.Следовательно, необъяснимое утолщение брюшины или асцит должны вызывать подозрение на карциноматоз брюшины. При подозрении на заболевание брюшины лапароскопическая стадия может быть рассмотрена у пациентов с операбельным PDAC [54, 56].
Результаты визуализации после неоадъювантной терапии
Неоадъювантная химиолучевая терапия (CRT) использовалась для повышения вероятности безопухолевого края резекции (R0) для пограничной резектабельной PDAC или для снижения стадии неметастатических местнораспространенных опухолей. СРТ может привести к снижению стадии примерно у 30% пациентов с последующим радиологическим и / или гистологическим ответом [58].В последнее время СРТ все чаще используется во многих онкологических учреждениях, даже для пациентов с операбельным ОАК, хотя потенциальные преимущества и недостатки еще предстоит определить [59].
Оценить ответ на СРТ на КТ сложно [60, 61]. Для оценки ответа на CRT были предложены морфологические критерии, включая размер опухоли, аттенюацию и контакт с сосудами. Однако размер опухоли может быть завышен на КТ из-за изменений, связанных с лечением, таких как некроз и отек, и изменение размера опухоли не имеет значительной корреляции с границей резекции без опухоли (R0).Точно так же изменение ослабления опухоли имеет ограниченное значение для прогнозирования резектабельности из-за неспособности дифференцировать некроз, фибровоспаление или отек от остаточной опухолевой ткани. Следовательно, изменения размера опухоли и ослабления на КТ имеют низкую точность для мониторинга ответа опухоли на лечение [10, 61]. Однако в исследовании Cassinotto et al. Уменьшение контакта опухоль-сосуд было значимо связано с резекцией R0 независимо от уменьшения размера опухоли или степени контакта опухоль-сосуд.Частичное уменьшение контакта опухоли с SMV / PV, SMA, CA или печеночной артерией было связано с резекцией R0 у 91% пациентов, что позволяет предположить, что это открытие может считаться показанием для хирургической резекции у подходящих кандидатов [10]. Поэтому изменение степени контакта опухоли с окружностью перипанкреатического сосуда может быть особенно важным (рис. 7 и 8).
Рис. 7Мужчина 64 лет с ОПП головы. Корональное Т2-взвешенное МР-изображение ( a ) показывает большую массу головки поджелудочной железы с низкой промежуточной интенсивностью сигнала (звездочка), вызывающую дилатацию CBD вверх по течению (длинная стрелка).Осевое Т1-взвешенное изображение с усиленным контрастом в фазе воротной вены ( b ) показывает гипоусиленное образование головки поджелудочной железы, прилегающее к SMV. КТ-изображения коронарной ( c ) и аксиальной ( d ) фазы воротной вены, полученные через 2 месяца после неоадъювантной терапии, показывают значительное уменьшение объема опухоли (короткие стрелки). Впоследствии пациенту была проведена панкреатодуоденэктомия, и патология выявила обширный эффект неоадъювантного лечения на PDAC с остаточной опухолью всего 1 см и отрицательной границей резекции.В течение 3 лет рецидивов не было.
Рис. 8Женщина 62 лет с ОПАП головы. КТ-изображения осевой портальной венозной фазы ( a и b ) показывают плохо выраженную гипоаттенуирующую массу, покрывающую SMA (длинная стрелка). SMV демонстрирует каплевидный знак (короткая стрелка) и полностью стирается на более высоком уровне (не показано). КТ-изображения аксиальной портальной фазы ( c и d ), полученные через 2 месяца после неоадъювантной терапии, показывают уменьшение интервала размера опухоли и контакта опухоли с SMA (длинная стрелка) и SMV (короткая стрелка).Пациенту была выполнена панкреатодуоденэктомия, и патология не выявила остаточной инвазии в SMA
. Появляется возрастающая роль DWI в восстановлении опухоли после неоадъювантной терапии при различных злокачественных новообразованиях брюшной полости, таких как рак прямой кишки и шейки матки [62, 63]. PDAC демонстрирует высокую интенсивность сигнала на DWI с высоким значением b и более низкую интенсивность сигнала на карте кажущегося коэффициента диффузии (ADC) по сравнению с нормальной паренхимой [64]. В недавнем исследовании количественные параметры DWI были оценены у пациентов с PDAC, получающих химиотерапию, и обеспечили раннее и точное различие между респондентами и неответчиками.Постепенное уменьшение объема DW наблюдалось в группе респондентов [65]. Дала и др. проанализировали изменения значений ADC после начала CRT у пациентов с операбельными и погранично операбельными PDAC. Авторы обнаружили, что значения ADC были значительно выше в пост-CRT по сравнению с pre-CRT со значительной корреляцией с патологическим ответом опухоли [66]. Следовательно, DWI может служить полезным биомаркером визуализации для прогнозирования ответа опухоли и выбора пациентов с PDAC, которым может помочь неоадъювантная терапия [64].Однако до сих пор существует ограниченное количество данных о ценности DWI. Кроме того, снижение качества изображения DWI и отсутствие воспроизводимости значений ADC могут вызвать ограничения на его клиническую применимость [67].
ФДГ-ПЭТ-КТ может быть полезным инструментом для прогнозирования результатов у пациентов, получающих СРТ. Результаты показали, что чем больше разница между максимальными стандартными значениями поглощения до и после лечения (SUVmax), тем выше показатели выживаемости и тем дольше выживаемость без прогрессирования заболевания [68].
Стеноз чревной артерии
Стеноз чревной артерии (СА) обнаружен у 2.0–7,6% пациентов, перенесших панкреатодуоденэктомию [69]. Это может быть связано с внешним сдавлением средней дугообразной связкой (MAL) или внутренним стенозом при атеросклеротическом заболевании. Клиническое лечение различается в зависимости от первопричины стеноза [70, 71]. Оценка стеноза СА особенно важна у пациентов, которые являются кандидатами на панкреатодуоденэктомию, потому что послеоперационное прекращение коллатерального потока от SMA к ответвлениям CA может подвергнуть пациента риску ишемии печеночной артерии.Оценка СА на сагиттальных переформатированных изображениях должна быть включена в контрольный список всех предоперационных КТ при панкреатодуоденэктомии [71, 72].
КТ-ангиография полезна для выявления стеноза СА, выявления основной этиологии и картирования коллатеральных путей [73, 74]. При синдроме компрессии MAL КТ-ангиография демонстрирует верхнюю выемку CA, расположенную примерно в 5 мм от ее начала, с характерным «J», «U» или крючковидным видом. Верхняя выемка CA также может быть замечена у нормальных людей, и, следовательно, выполнение КТ-ангиографии во время выдоха помогает избежать ложноположительных результатов.Дополнительные функции КТ включают постстенотическую дилатацию и увеличенные перипанкреатические коллатеральные артерии. Напротив, атеросклеротический стеноз обычно поражает устье и связан с кальцификациями интимы СА [74, 75].
При стенозе СА основные коллатеральные пути между СА и СМА включают панкреатодуоденальные дуоденальные дуги и дорсальные артерии поджелудочной железы, которые видны в 95% и 76%, соответственно. Передняя панкреатодуоденальная аркада проходит вдоль панкреатодуоденальной борозды кпереди как продолжение гастродуоденальной артерии (GDA), а задняя – кзади от дистального общего желчного протока.Дорсальная панкреатическая артерия отходит от селезеночной, чревной или общей печеночной артерии и проходит заднемедиальнее SMV [74]. КТ-ангиография полезна для оценки степени стеноза, но не может отразить его гемодинамическое значение. Следовательно, интраоперационная допплерография может использоваться для оценки кровотока в печеночной артерии после пережатия GDA. Сохраненный допплеровский сигнал указывает на эффективный коллатеральный кровоток, тогда как значительное снижение печеночного артериального кровотока оправдывает реконструкцию артерий [71, 72, 76] (рис.9).
Рис. 960-летний мужчина проходит предоперационную визуализацию для определения PDAC. Осевые ( a и b ) и сагиттальные ( c ) изображения КТ фазы поджелудочной железы показывают устный стеноз чревной артерии (стрелка) из-за атеросклеротического заболевания. У пациента установлен билиарный стент (изогнутая стрелка), а PDAC определяется как легкое гипоаттенуирующее поражение (стрелки). Осевое Т1-взвешенное МРТ-изображение с подавленным жиром ( d ) четко демонстрирует PDAC как гипоинтенсивное образование.Интраоперационное ультразвуковое исследование допплера ( e и f ) показывает значительный стеноз чревной артерии, демонстрируя каудокраниальный / обратный кровоток в гастродуоденальной артерии, что указывает на его значительный вклад в кровоснабжение печеночной артерии. Пациенту впоследствии была проведена панкреатодуоденэктомия после стентирования чревной артерии.
Имитирует PDAC
. Различные состояния могут выглядеть схожими с PDAC на визуализации, включая доброкачественные аномалии, такие как аутоиммунный панкреатит и бороздчатый панкреатит, а также очаговую жировую инфильтрацию и злокачественные образования, такие как нейроэндокринные опухоли и лимфоциты. метастаз.
Аутоиммунный панкреатит (AIP) является отличным аналогом PDAC и составляет 2–3% хирургических резекций при клинически подозрении на рак; поэтому дифференциация обоих объектов имеет решающее значение [77]. При диффузном AIP поджелудочная железа имеет диффузно увеличенную «колбасную форму» с потерей долей поджелудочной железы и капсулоподобным ободком «ореола» гипоаттенуации на КТ или гипоинтенсивности на МРТ [78]. Очаговый «массообразующий» AIP является менее распространенным типом и, как и PDAC, проявляется как нерегулярная, плохо определяемая, похожая на массу аномалия; поэтому различить обе сущности довольно сложно.Однако наличие относительно длинной стриктуры, видимого протока в новообразовании, мультифокальных стриктур и отсутствие значительного протока поджелудочной железы выше по течению больше наблюдаются при очаговом AIP, чем при PDAC [78,79,80] (рис. 10). Кроме того, сохранение контраста во время отсроченной фазы постконтрастной МР-визуализации более частое и отчетливое при AIP [80,81,82,83]. Считается, что этот паттерн усиления обусловлен сохранением ацинарных клеток с легким фиброзом, тогда как PDAC полностью заменяет нормальную ткань поджелудочной железы опухолевыми клетками с обильной фиброзной стромой [83].Сопутствующие доказательства внепанкреатического заболевания, связанного с IgG4, являются еще одним важным ключом к диагностике AIP. Могут быть поражены несколько органов, такие как вторичный склерозирующий холангит со стриктурой желчных протоков, двусторонние почечные массоподобные поражения, забрюшинный фиброз и склерозирующий мезентериит [78].
Рис. 10Мужчина 71 года с массообразующим АИП. Осевые ( a – c ) КТ-изображения в фазе поджелудочной железы показывают два плохо очерченных, массоподобных поражения (звездочка) в теле поджелудочной железы без значительной дилатации MPD (стрелки).Имеется связанное с утолщением периаортальных мягких тканей корка (стрелки), представляющая забрюшинный фиброз, связанный с IgG4
Панкреатит с бороздками (ГП) – редкое специфическое заболевание хронического панкреатита, поражающее бороздку между головкой поджелудочной железы, двенадцатиперстной кишкой и общим желчным протоком, обычно поражающее молодые мужчины и связанные со злоупотреблением алкоголем [84]. Воспаление может ограничиваться бороздой в чистой форме ГП или распространяться на головку поджелудочной железы в сегментарной форме [85].PDAC и GV довольно сложно различить из-за схожих характеристик, включая низкую интенсивность сигнала на T1-взвешенных изображениях с подавленным жиром, среднюю или высокую интенсивность сигнала на T2-взвешенных МР-изображениях и гиповаскулярность на ранней стадии КТ и МРТ с контрастным усилением. визуализация с переменной степенью отсроченного усиления во время отсроченной фазы [85, 86]. Ключевые особенности визуализации в основном отображаются на МРТ и включают: (а) кистозные изменения вокруг добавочного протока поджелудочной железы в сочетании с увеличивающейся утолщенной стенкой нисходящей двенадцатиперстной кишки; (b) гладкая длинная стриктура внутрипанкреатического CBD без заметной дилатации желчных протоков вверх по течению; и (c) смещение CBD и GDA из просвета двенадцатиперстной кишки из-за воспалительной ткани панкреатодуоденальной борозды [84, 86,87,88] (рис.11). Для окончательного отличия GP от PDAC может потребоваться биопсия ткани под контролем EUS или цитология тонкоигольной аспирации. Хотя фиброзная ткань присутствует в обоих состояниях, что увеличивает диагностическую неопределенность [84].
Рис. 11Женщина 60 лет с сегментарной формой панкреатита бороздки. КТ-изображение венозной фазы воротной вены ( a ) показывает гипоаттенуирующую пластинчатую область в панкреатодуоденальной борозде (между длинными стрелками), связанную с утолщением стенок и сужением просвета нисходящей двенадцатиперстной кишки.CBD (короткая стрелка) смещается медиально воспалительным процессом и сужается дистально. МРТ-изображения с корональной последовательностью T2 HASTE ( b ), аксиальной последовательностью T1 с подавлением жира ( c ) и последовательностью T1 с подавленным аксиальным контрастом замедленной фазы ( d ) показывают аномалию панкреатодуоденальной борозды между длинными стрелками), содержащий множественные крошечные кисты вдоль стенки двенадцатиперстной кишки с высокой интенсивностью Т2-сигнала и лист фибровоспалительной ткани с низкой интенсивностью Т1-сигнала и замедленным усилением.Отмечается неусиливающаяся крошечная псеводоциста (изогнутая стрелка). CBD (короткая стрелка) и MPD (стрелка) не расширены. Состояние пациента улучшилось при последующем наблюдении
Очаговая жировая инфильтрация паренхимы поджелудочной железы отражает неравномерное отложение жировой ткани и часто затрагивает переднюю часть головки поджелудочной железы с сохранением ее задней части и области вокруг общего желчного протока [ 89]. На УЗИ очаговая жиросберегающая область отличается от гипоэхогенной массы сохраненным курсом и калибром CBD и четкой границей с передней гиперэхогенной зоной жировой инфильтрации [90].Очаговую жировую инфильтрацию поджелудочной железы можно отличить от PDAC на КТ по наличию четкой границы между пораженной передней частью и нормальной тканью поджелудочной железы вокруг общего желчного протока, а также отсутствию обструкции протоков поджелудочной железы [91, 92]. МРТ демонстрирует падение интенсивности сигнала в противофазной последовательности, что отличает его от PDAC [91, 93] (рис. 12).
Рис. 12Женщина 39 лет с очаговой жировой инфильтрацией головки поджелудочной железы. КТ-изображение осевой портальной фазы ( a ) показывает область низкого ослабления (стрелки) в головке поджелудочной железы с язычковым расширением сразу после SMV.Нет масс-эффекта или дилатации MPD. Обратите внимание на нормальную паренхиму затухания вокруг CBD. МРТ-изображения с осевым химическим сдвигом показывают отсутствие отклонений от нормы в синфазной последовательности ( b ) и падение сигнала в той же области (стрелки) при противоположной фазовой последовательности ( c ), что соответствует микроскопическому жиру в очаговой жировой инфильтрации
Нейренэндокрин поджелудочной железы опухоли (PNET) составляют 1–3% всех новообразований поджелудочной железы, чаще всего в четвертом – шестом десятилетии жизни [94, 95]. В отличие от PDAC, PNET, как правило, демонстрируют четко очерченную массу, изо- или гипер-возрастающую по сравнению с нормальной поджелудочной железой и реже связанную с дилатацией MPD выше по течению и атрофией дистальной части поджелудочной железы [94, 96, 97] (рис.13).
Рис. 13Мужчина 53 лет с нейроэндокринной опухолью головы поджелудочной железы. Осевая артериальная фаза ( a ) и фаза воротной вены ( b ) и ( c ) КТ-изображения показывают четко выраженное образование (звездочка) с периферической гиперваскуляризацией и центральной кистозной областью. Только легкое расширение MPD (стрелка) из-за внешнего сжатия опухолью, а не протокового происхождения опухоли. Гистопатология выявила эндокринную опухоль поджелудочной железы
Метастазы в поджелудочную железу относительно редки, составляя 2–5% злокачественных образований, и большинство из них возникает из-за почечно-клеточного рака, за которым следуют рак груди, легких, толстой кишки и меланомы.Метастатическое заболевание может проявляться в виде одиночного образования в 50–75%, диффузного инфильтративного образования в 15–44% или множественных образований в 5–10% [98] (рис. 14). Метастазы из почечно-клеточной и гепатоцеллюлярной карциномы обычно гиперваскулярны и легко дифференцируются от гиповаскулярной PDAC; однако метастатические образования могут достигать большего размера и развиваться центральный некроз [99]. Напротив, гиповаскулярные метастазы рака легких, молочной железы и колоректального рака очень похожи на PDAC. Вовлечение протока не является надежным дискриминационным критерием, поскольку оно также может возникать при метастазах и вызывать дилатацию протока поджелудочной железы и атрофию дистального отдела поджелудочной железы.Перипанкреатическая сосудистая инвазия редко встречается при метастатическом поражении [100]. Наличие в анамнезе первичных злокачественных новообразований, сопутствующих внепанкреатических метастазов и множественных поражений поджелудочной железы может помочь в диагностике метастазов. В противном случае может потребоваться биопсия, если поражение остается неопределенным [99].
Рис. 1472-летний мужчина с метастазами папиллярного рака щитовидной железы с поражением поджелудочной железы. КТ-изображение в осевой фазе поджелудочной железы показывает множественные увеличивающиеся образования (звездочки), охватывающие всю поджелудочную железу
Лимфома поджелудочной железы встречается редко, составляя менее 0.


 Степень выраженности, то есть симптоматика липоматоза, полностью зависит от степени диффузных изменений поджелудочной железы. Так, если заболевание имеет ограниченное распространение очага патологии, то процесс протекает бессимптомно. При бесконтрольном прогрессировании происходит сдавливание паренхимы массивным скоплением жировой ткани, что вызывает болезненные ощущения и приводит к нарушениям в работе ПЖ.
Степень выраженности, то есть симптоматика липоматоза, полностью зависит от степени диффузных изменений поджелудочной железы. Так, если заболевание имеет ограниченное распространение очага патологии, то процесс протекает бессимптомно. При бесконтрольном прогрессировании происходит сдавливание паренхимы массивным скоплением жировой ткани, что вызывает болезненные ощущения и приводит к нарушениям в работе ПЖ. Результат вышеупомянутого процесса отражается диффузными изменениями в паренхиме железы.
Результат вышеупомянутого процесса отражается диффузными изменениями в паренхиме железы. На УЗИ это дает гипеорэхогенный сигнал. Заболевание может возникнуть из-за нарушения обмена веществ.
На УЗИ это дает гипеорэхогенный сигнал. Заболевание может возникнуть из-за нарушения обмена веществ.