Дуодено гастро рефлюкс: Дуодено-гастральный рефлюкс – что такое ДГР в гастроэнтерологии
Дуоденогастральный рефлюкс: современный взгляд на старую проблему
Авторы: С.М. Ткач, д. мед. н., профессор, Ю.Г. Кузенко, д. мед. н., профессор, Украинский научно-практический центр эндокринной хирургии, трансплантации эндокринных органов и тканей МЗ Украины, г. Киев
Статья в формате PDF
Дуоденогастральный рефлюкс (синонимы – билиарный рефлюкс, рефлюкс-гастрит, билиарный гастрит, щелочной гастрит) представляет собой ретроградное поступление желчи в желудок, которое нередко сопровождается клиническими симптомами, эндоскопическими изменениями и гистологическими признаками химического (реактивного) гастрита. Впервые дуоденогастральный рефлюкс (ДГР) был описан еще в 1833 году У. Бьюмонтом у пациента с желудочной фистулой. На протяжении более чем 100 лет ДГР рассматривался в рамках хирургических болезней как следствие операций на желудке, сопровождающихся резекцией или повреждением привратника.
ДГР обычно возникает вследствие избыточного поступления желчи из двенадцатиперстной кишки, недостаточности привратника как барьера для ретроградного тока желчи, а также/или вследствие снижения антероградной перистальтики желудка и двенадцатиперстной кишки. Факторами риска развития первичного ДГР являются дисфункция желчного пузыря и дуоденальная дисмоторика. Вторичный ДГР нередко развивается после операций на желудке (резекция привратника, пилоропластика) или желчном пузыре/желчевыводящих путях (холецистэктомия, билиарная сфинктеротомия; рис. 1). Важное значение как в предотвращении развития ДГР, так и в очищении антрального отдела желудка от желчного рефлюктата играет 3-я фаза гастродуоденальной моторики – мигрирующий моторный комплекс, представляющий собой циклическую, стереотипно повторяющуюся сократительную активность желудка и тонкой кишки в межпищеварительный период.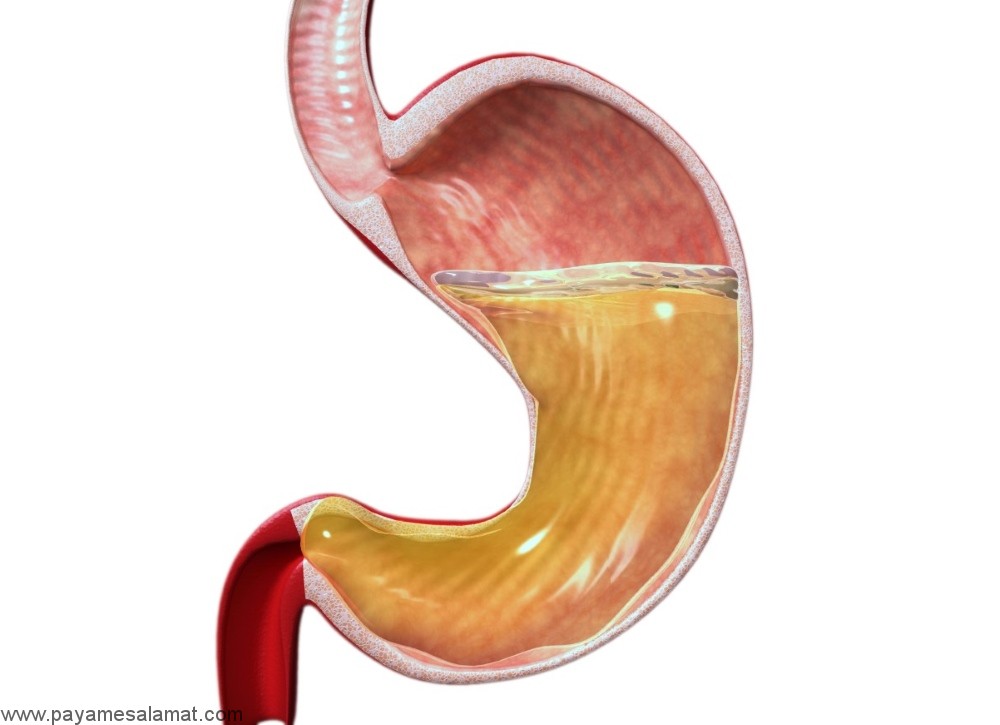
Симптоматика при ДГР, как правило, «расплывчата» и весьма вариабельна. Она может включать абдоминальную боль, диспепсию, горечь во рту, тошноту и рвоту желчью, снижение массы тела, изжогу. Хотя истинная распространенность ДГР неизвестна, она имеет тенденцию к увеличению, что связано с повышением распространенности состояний, способствующих гастродуоденальной дисмоторике, таких как сахарный диабет 2 типа, бариатрические операции, прием опиоидных аналгетиков или других препаратов, замедляющих опорожнение желудка (антихолинергические средства, антидепрессанты, леводопа и др.).
Диагностика ДГР и билиарного рефлюкс-гастрита является достаточно проблематичной, особенно в тех случаях, когда хирургические факторы риска отсутствуют. Эндоскопические и гистологические данные могут быть неспецифическими или не всегда идентифицироваться клиницистами. Хотя общепринятых критериев диагностики нет, считается, что эндоскопически подтвержденного наличия ДГР в сочетании с гистологическими признаками гастрита достаточно для установления диагноза. Методы выявления ДГР включают его визуализацию при эндоскопии, обнаружение желчных солей в желудочном соке, измерение концентрации билирубина в желудочном соке с помощью волоконно-оптического спектрофотометра или радиосцинтиграфию (последние три исследования в клинической практике обычно не выполняются, а применяются в научных целях). Эндоскопическая картина чаще всего включает эритему слизистой оболочки желудка и наличие желчи в желудке; также могут определяться утолщение складок желудка, эрозии и атрофия слизистой оболочки. При гистологическом исследовании выявляют признаки химического гастрита, включая фовеолярную гиперплазию, отек, наличие гладкомышечных волокон в собственной пластинке и скудность клеток острого или хронического воспаления.
Эндоскопические и гистологические данные могут быть неспецифическими или не всегда идентифицироваться клиницистами. Хотя общепринятых критериев диагностики нет, считается, что эндоскопически подтвержденного наличия ДГР в сочетании с гистологическими признаками гастрита достаточно для установления диагноза. Методы выявления ДГР включают его визуализацию при эндоскопии, обнаружение желчных солей в желудочном соке, измерение концентрации билирубина в желудочном соке с помощью волоконно-оптического спектрофотометра или радиосцинтиграфию (последние три исследования в клинической практике обычно не выполняются, а применяются в научных целях). Эндоскопическая картина чаще всего включает эритему слизистой оболочки желудка и наличие желчи в желудке; также могут определяться утолщение складок желудка, эрозии и атрофия слизистой оболочки. При гистологическом исследовании выявляют признаки химического гастрита, включая фовеолярную гиперплазию, отек, наличие гладкомышечных волокон в собственной пластинке и скудность клеток острого или хронического воспаления.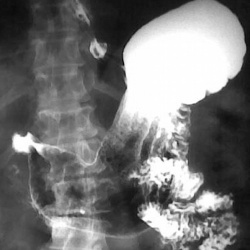
Ведение больных с ДГР и билиарным рефлюкс-гастритом включает как медикаментозное, так и хирургическое лечение. Хотя теоретически при ДГР повышается риск развития аденокарциномы желудка, что было показано на моделях у животных, у людей подобные эффекты не зафиксированы. Поэтому основной целью терапии является уменьшение выраженности симптоматики при помощи лекарственных средств. Однозначного мнения относительно необходимости проведения фармакотерапии при отсутствии симптомов в настоящее время нет.
Эффективность приема некоторых лекарственных препаратов оценивали в неконтролируемых или небольших контролируемых исследованиях с переменными результатами. Наиболее часто при ДГР применяются ингибиторы протонной помпы (ИПП), хотя механизм их действия при этой патологии не совсем ясен.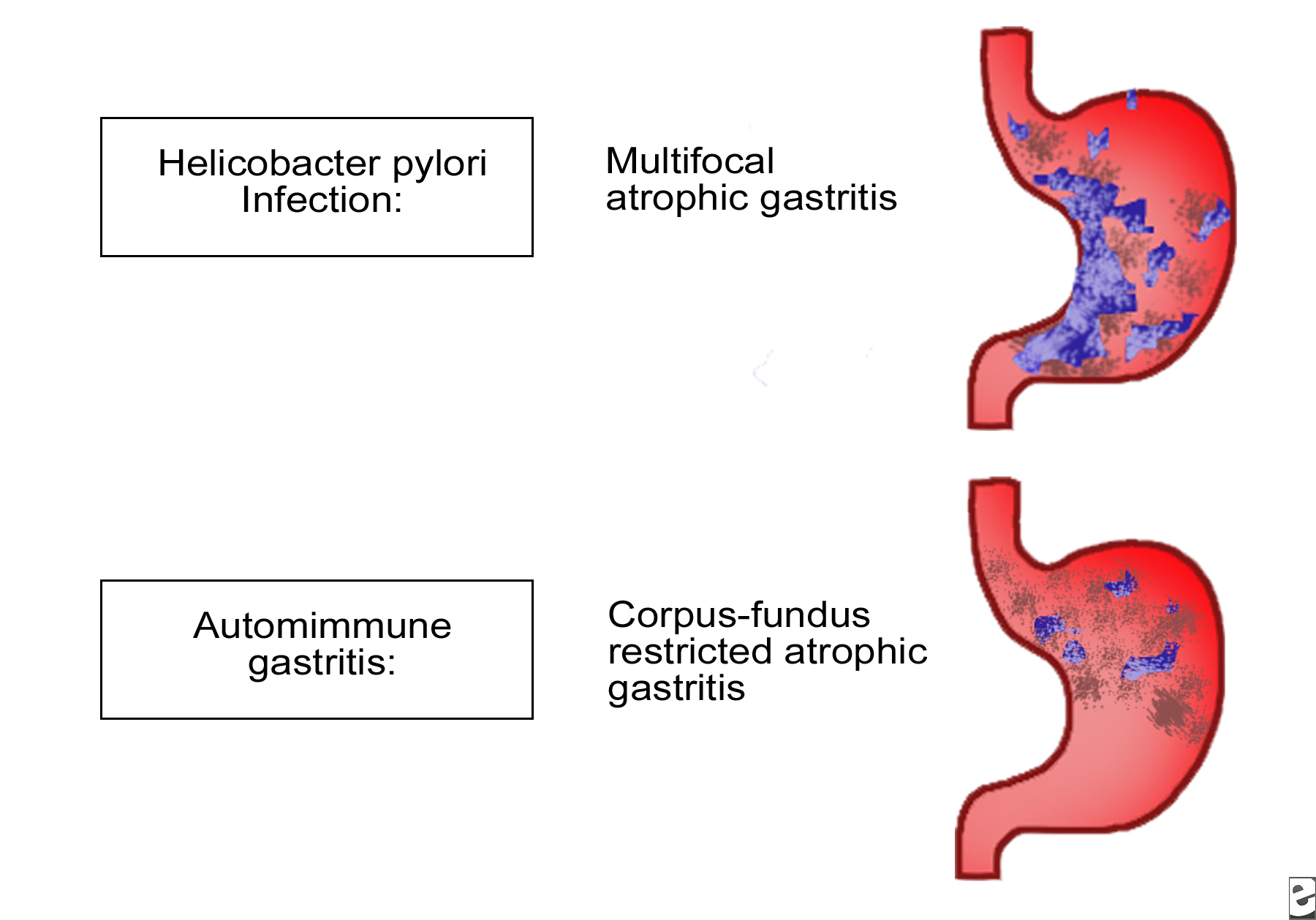 Считается, что желчные кислоты вызывают повреждение из-за своих детергентных свойств, однако при более низких значениях рН последние преципитируются, а при более высоких значениях рН способны оказывать больший повреждающий эффект на слизистую оболочку желудка. Применение ИПП сопровождается выраженным снижением рН и уменьшением повреждающего воздействия желчных кислот на слизистую оболочку желудка.
Считается, что желчные кислоты вызывают повреждение из-за своих детергентных свойств, однако при более низких значениях рН последние преципитируются, а при более высоких значениях рН способны оказывать больший повреждающий эффект на слизистую оболочку желудка. Применение ИПП сопровождается выраженным снижением рН и уменьшением повреждающего воздействия желчных кислот на слизистую оболочку желудка.
В рандомизированном исследовании с участием 60 пациентов с ДГР после холецистэктомии изучали эффективность рабепразола в дозе 20 мг в день. Боль в эпигастральной области у пациентов в группе рабепразола уменьшилась на 30%, в контрольной группе (не получали лечения) – на 10%. Соответственно, выраженность изжоги уменьшилась на 35 и 15%. Эндоскопические показатели в группе рабепразола улучшились, хотя не ясно, было ли эндоскопическое исследование контролируемым и слепым.
В Украине зарегистрировано несколько препаратов рабепразола. Одним из наиболее широко применяемых препаратов является Барол (компания «Мега Лайфсайенсиз»), который при данной патологии рекомендуется принимать в дозе 20 мг на протяжении 4 недель.
В нескольких неконтролируемых и одном контролируемом исследовании изучали эффективность сукральфата, который обеспечивал гистологическое, но не симптоматическое улучшение. Исследовали также эффективность урсодезоксихолевой кислоты (УДХК) в дозе 1000 мг/сут у 12 пациентов с ДГР после предшествующей операции на желудке. При изучении содержания желчных кислот в желудочном содержимом во время лечения имело место изменение уровня УДХК. Пять пациентов в течение 4 недель принимали плацебо, а затем на протяжении 4 недель – УДХК; на фоне приема плацебо у этих пациентов эффекта не было, но после назначения УДХК симптоматика существенно уменьшилась. Дополнительно 7 пациентов лечились УДХК с последующим назначением плацебо; у всех было отмечено клиническое улучшение, однако у 3 из них отмечался рецидив симптомов после приема плацебо. Каких-либо изменений эндоскопической и гистологической картины отмечено не было.
В Украине зарегистрированы несколько препаратов УДХК, среди которых наиболее доступным в экономическом плане является Урсолив (компания «Мега Лайфсайенсиз»). Рекомендуемая схема приема препарата – 1 г/сут на протяжении не менее 4 недель.
Рекомендуемая схема приема препарата – 1 г/сут на протяжении не менее 4 недель.
В небольших контролируемых испытаниях исследовали также эффективность применения холестирамина в сочетании с альгинатами и простагландином Е2 в лечении пациентов с ДГР, однако эти препараты оказались неэффективными. Роль прокинетиков в лечении ДГР и рефлюкс-гастрита в контролируемых исследованиях до настоящего времени детально не изучена, хотя в клинической практике при этом состоянии они применяются очень широко.
Возможность хирургического лечения может рассматриваться только у пациентов с тяжелыми симптомами, как правило, в случаях развития ДГР вследствие предшествующей операции. Обычно используемые вмешательства включают изоперистальтическую петлю тощей кишки (Хенли), энтероэнтеростомию Брауна и холедохоеюностомию по Roux-en-Y, которая может быть применена для отвода желчи непосредственно от желчевыводящих путей после холецистэктомии. Эти процедуры могут быть эффективны в уменьшении выраженности симптомов, однако несут в себе риск таких осложнений, как изъязвления, стаз, формирование безоаров.
При ведении больных первым этапом является пересмотр принимаемых больным лекарственных средств и прекращение необязательного приема любых препаратов, которые могут снижать гастродуоденальную моторику (рис. 2). Кроме того, рекомендуются общие диетические мероприятия, способствующие нормализации моторики гастродуоденальной зоны: частое дробное питание, прием пищи в одно и то же время, отказ от жирных блюд и продуктов, снижающих скорость опорожнения желудка. При необходимости медикаментозного лечения в качестве препаратов первой линии назначают ИПП, в частности рабепразол (Барол) в течение 4 недель. При отсутствии достаточного эффекта в качестве терапии второй линии назначают препараты УДХК (Урсолив) в дозе 1 г/сут в 2-3 приема в течение 4 недель. Если симптомы сохраняются, применяют сукральфат (1-2 г два раза в день) или назначают комбинацию лекарственных средств. У пациентов с выраженной симптоматикой и отсутствием эффекта от медикаментозной терапии, особенно в случаях предшествующего оперативного вмешательства, может рассматриваться возможность хирургической коррекции.
Таким образом, ДГР является частым состоянием, первично возникающим на фоне билиарной дисфункции и гастродуоденальной дисмоторики либо вследствие предшествующей операции на желудке или желчевыводящих путях. ДГР проявляется разными клиническими симптомами и снижает качество жизни больных. Классическим методом диагностики ДГР является эндоскопия. При наличии симптомов ДГР необходима нормализация режима питания, определенные диетические ограничения и назначение лекарственных средств. В качестве препаратов первой линии применяют ИПП (Барол), а при их недостаточной эффективности – препараты УДХК (Урсолив), сукральфат, прокинетики или комбинацию лекарственных средств. В отдельных случаях при наличии выраженных симптомов после предшествующего оперативного вмешательства и неэффективности медикаментозного лечения может осуществляться хирургическая коррекция.
Литература
- Beaumont W. Experiments and observations on the gastric juice, and the physiology of digestion.
 Plattsburgh: Printed by F.P. Allen, 1833. Nutr Rev. 1977 Jun; 35(6): 144-145.
Plattsburgh: Printed by F.P. Allen, 1833. Nutr Rev. 1977 Jun; 35(6): 144-145. - Testoni P.A., Fanti L., Passaretti S. et al. Interdigestive motility pattern in subjects with duodenogastric bile reflux. Scand J Gastroenterol. 1987; 22: 757-762.
- Atak I., Ozdil K., Yucel M. et al. The effect of laparoscopic cholecystectomy on the development of alkaline reflux gastritis and intestinal metaplasia. Hepatogastroenterology. 2012; 59: 59-61.
- Vere C.C., Cazacu S., Comanescu V. et al. Endoscopical and histological features in bile reflux gastritis. Rom J Morphol Embryol. 2005; 46: 269-274.
- Ritchie W.P. Alkaline reflux gastritis: a critical reappraisal. Gut. 1984; 25: 975-987.
- Madura J.A. Primary bile reflux gastritis: diagnosis and surgical treatment. Am J Surg. 2003; 186: 269-273.
- Niemela S. Duodenogastric reflux in patients with upper abdominal complaints or gastric ulcer with particular reference to reflux-associated gastritis. Scand J Gastroenterol Suppl.
 1985; 115: 1-56.
1985; 115: 1-56. - Beaumont W., Osler W. Experiments and observations on the gastric juice and the physiology of digestion / William Beaumont. Together with a biographical essay, William Beaumont: a pioneer American physiologist / by Sir William Osler. Mineola, N.Y: Dover, 1996.
- Dixon MFOcH, Axon ATR, King RFJG, et al. Reflux gastritis: distinct histopathological entity? J Clin Pathol 1986; 39: 524-530.
- Santarelli L., Gabrielli M., Candelli M. et al. Post-cholecystectomy alkaline reactive gastritis: a randomized trial comparing sucralfate versus rabeprazole or no treatment. Eur J Gastroenterol Hepatol. 2003; 15: 975-979.
- Stefaniwsky A.B., Tint G.S., Speck J. et al. Ursodeoxycholic acid treatment of bile reflux gastritis. Gastroenterology. 1985; 89: 1000-1004.
Тематичний номер «Гастроентерологія. Гепатологія. Колопроктологія» № 2 (52), травень 2019 р.
СТАТТІ ЗА ТЕМОЮ Гастроентерологія
30. 05.2021
Гастроентерологія
Онкологія та гематологія Сучасна колопроктологія через призму місяця боротьби з колоректальним раком
05.2021
Гастроентерологія
Онкологія та гематологія Сучасна колопроктологія через призму місяця боротьби з колоректальним ракомБерезень – місяць боротьби з колоректальним раком (КРР), який традиційно відзначають кожного року. У цей період активно проводять просвітницькі заходи для населення з метою зосередження уваги на проблемах, пов’язаних із КРР, провідних факторах ризику розвитку захворювання та на значенні скринінгових програм у ранній діагностиці онкопатології, що визначатиме тактику лікування й прогноз для пацієнтів. У фаховій спільноті організовують науково-практичні конференції, на яких провідні спеціалісти представляють оновлені дані доказової медицини, що стосуються ведення пацієнтів з КРР, діляться власним досвідом лікування таких хворих. …
…
Лікування гострої кишкової інфекції (ГКІ), одного з найпоширеніших у світі захворювань, ґрунтується на декількох принципах, а саме на проведенні регідратаційної терапії, призначенні антибіотиків, застосуванні допоміжних засобів, раціоналізації дієти. Незважаючи на скорочення переліку показань для призначення антибіотиків при ГКІ в дітей і дорослих, проведення протимікробної терапії необхідне за підозри на гемоколіт, шигельоз, кампілобактеріоз, холеру, амебіаз, а також у разі тяжкого перебігу інвазивної діареї. Наявність вторинних бактеріальних ускладнень, коморбідної онко- та гематологічної патології, хронічного захворювання кишечнику, супутнього імунодефіцитного стану внаслідок інфікування вірусом імунодефіциту людини, проведення хіміопроменевої / тривалої кортикостероїдної терапії також вважаються підставами для обґрунтованого застосування антибіотиків….
Наявність вторинних бактеріальних ускладнень, коморбідної онко- та гематологічної патології, хронічного захворювання кишечнику, супутнього імунодефіцитного стану внаслідок інфікування вірусом імунодефіциту людини, проведення хіміопроменевої / тривалої кортикостероїдної терапії також вважаються підставами для обґрунтованого застосування антибіотиків….
Антибіотики є однією з найширше застосовуваних груп лікарських препаратів, які використовуються в різних галузях медицини та складають до 70% від обсягу призначень ліків [1, 2]. Водночас слід розуміти, що антибіотики – важливий компонент у лікуванні багатьох захворювань, але він може зумовлювати тяжкі побічні ефекти [3-6]….
Водночас слід розуміти, що антибіотики – важливий компонент у лікуванні багатьох захворювань, але він може зумовлювати тяжкі побічні ефекти [3-6]….
Пандемія коронавірусної хвороби (COVID‑19) стала безпрецедентним викликом для лікарів усіх спеціальностей, адже, як виявилося, ця підступна інфекція здатна спричиняти поліорганні ураження та виникнення ускладнень не тільки в гострій фазі захворювання, а й у період реконвалесценції. Особливо небезпечним COVID‑19 є для тих категорій пацієнтів, які мають хронічні соматичні захворювання; саме вони закономірно потребують пріоритетної уваги фахівців на етапі реабілітації. Про практичні аспекти ведення пацієнтів із хронічними захворюваннями печінки (ХЗП), які перенесли COVID‑19, під час IX Всеукраїнського конгресу «Профілактика. Антиейджинг. Україна» (3-5 березня) докладно розповів професор кафедри клінічної фармакології та клінічної фармації Національного медичного університету ім. О. О. Богомольця (м. Київ), доктор медичних наук, професор Леонід Леонідович Пінський….
Особливо небезпечним COVID‑19 є для тих категорій пацієнтів, які мають хронічні соматичні захворювання; саме вони закономірно потребують пріоритетної уваги фахівців на етапі реабілітації. Про практичні аспекти ведення пацієнтів із хронічними захворюваннями печінки (ХЗП), які перенесли COVID‑19, під час IX Всеукраїнського конгресу «Профілактика. Антиейджинг. Україна» (3-5 березня) докладно розповів професор кафедри клінічної фармакології та клінічної фармації Національного медичного університету ім. О. О. Богомольця (м. Київ), доктор медичних наук, професор Леонід Леонідович Пінський….
Лечение рефлюкса в СПб
Рефлюкс – заболевание ЖКТ, при котором происходит обратный ток содержимого желудка или кишечника. При гастральном рефлюксе желудочный сок попадает в пищевод и становится причиной химического ожога. Если не пытаться с ним бороться, то со временем это приведет к язвенной болезни.
Если не пытаться с ним бороться, то со временем это приведет к язвенной болезни.
Классификация рефлюксов
Рефлюксы органов ЖКТ классифицируются по локализации:
- Дуодено-гастральный рефлюкс. Проникновение содержимого двенадцатиперстной кишки в желудок.
- Гастроэзофагеальный рефлюкс. Проникновение содержимого желудка в пищевод.
- Фаринголарингеальный рефлюкс. Проникновение содержимого желудка в горло.
Симптомы рефлюксов
Признаки рефлюкса различаются в зависимости от вида заболевания. Общими для всех видов рефлюксов считаются следующие симптомы:
- отрыжка;
- изжога;
- тошнота.
При дуодено-гастральном рефлюксе на языке появляется желтый налет, возможна боль в животе с неясной локализацией. Гастроэзофагеальный рефлюкс отличается кислой отрыжкой и загрудинной болью. При фаринголарингеальном рефлюксе появляется охриплость в голосе, кашель, ощущение кома в горле.
Причины рефлюксов
Основной причиной рефлюксов называют повышенное давление в желудке или в двенадцатиперстной кишке. Дуодено-гастральный рефлюкс может развиваться в результате удаления желчного пузыря или лечения язвы. Гастроэзофагеальный (гастральный) рефлюкс начинается на фоне неспособности пищевода самоочищаться. Также на это заболевание влияют ожирение, неправильное питание, стрессы. Причиной фаринголарингеального рефлюкса могут стать грыжа отверстия диафрагмы и неполное опорожнение желудка.
Лечение рефлюксов
Лечение рефлюксов заключается в медикаментозном курсе или даже в хирургическом вмешательстве.
При лечении дуодено-гастрального рефлюкса используются домперидон и другие прокинетики, уменьшающие забросы содержимого 12-перстной кишки в желудок. Для уменьшения действия желчи при рефлюксе назначают лекарства на основе урсодезоксихолевой кислоты.
При гастроэзофагеальном и фаринголарингеальном рефлюксе тоже назначаются антисекреторные средства и прокинетики. К ним добавляют антациды для нейтрализации желудочного сока. Также назначаются витамины, стимулирующие перистальтику кишечника для полного вывода содержимого желудка.
К ним добавляют антациды для нейтрализации желудочного сока. Также назначаются витамины, стимулирующие перистальтику кишечника для полного вывода содержимого желудка.
Кроме применения лекарств, врач может рекомендовать ряд профилактических мер. В первую очередь необходимо нормализовать вес и изменить привычную диету. Питаться нужно дробно, 4-5 раз в день и небольшими порциями. Исключить из рациона продукты, раздражающие слизистую пищевода и подстегивающие увеличение выработки желчи при рефлюксе. Также рекомендуется отказ от тесной одежды, усиливающей внутрибрюшное давление.
В ряде случаев, если медикаментозное лечение не дает результатов, может понадобиться вмешательство хирурга. В качестве инвазивного лечения применяются методики с использованием современного оборудования. Магнитные браслеты LINX, надеваемые на пищевод, предотвращают вбросы содержимого желудка в пищевод. Для лечения грыжи отверстия диафрагмы используются эндоскопические аппараты. Операции на желудке часто проводятся методом лапароскопии.
В нашей клинике есть отделение гастроэнтерологии, где можно пройти обследование ЖКТ с последующим лечением рефлюксов.
Наши клиники в Санкт-Петербурге
Медицентр Юго-ЗападПр.Маршала Жукова 28к2
Кировский район
- Автово
- Проспект Ветеранов
- Ленинский проспект
Получить подробную информацию и записаться на прием Вы можете по телефону +7 (812) 640-55-25
Дуоденогастральный рефлюкс как причина развития рефлюкс-гастрита Текст научной статьи по специальности «Клиническая медицина»
infants]: avtoref. t al.] // Allergy. — 2008. — Vol. 63. — P.5.
t al.] // Allergy. — 2008. — Vol. 63. — P.5.
23. Doyle, L.W. Respiratory function at age in extremely lou birthweight / very preterm children in Victoria in 1991—1992 / L.W. Doyle // Pediatr. Pulmonol. — 2006. — № 118. — P.108—113.
24. Bronchopulmonary dysplasia in very low birth weight subjects and lung function in late adolescence / L.W. Doyle, B. Faber, C. Calanan [et al.] // Pediatric. — 2006. — № 118. — P. 108—113.
25. Ellison-Loschmann, L. Socioeconomic status, asthma and chronic bronchitis in a large community-based stady / L. Ellison-Loschmann, J. Sunyer, E. Plana // Eur. Respir. J. — 2007. — Vol. 29. — P.897—905.
26. Van Gent, R. Poor perception of dyspnea in children with undiagnosed asthma / R. van Gent., L.E.M. van Essen-Zandvliet // Eur. Respir. J. — 2007. — Vol. Mon. — 2010. — № 47. — P.251—262.
Mon. — 2010. — № 47. — P.251—262.
28. Emphysema in yang adult survivors of moderate-to-severe bronchopulmonary dysplasia / P.M. Wong, A.N. Lees, N. French [et al.] // Eur. RespirY J. — 2008. — № 32. — P.321—328.
29. Alekseevskih, Yu.G. Strukturno-funkcional’nye osobennosti krupnyh i melkih bronhov i razlichiya voznikayuschih v nih vospalitel’nyh reakcii [Structural and functional features of the large and small bronchi and differences arising in these inflammatory reactions] / Yu.G. Alekseevskih, I.K. Esipova // Arhiv patologii. — 1994. — № 4. — S.6—9.
30. E p i d e m i o l o g i c h e s k i e p o d h o d y k i z u c h e n i y u rasprostranennosti recidiviruyuschih i hronicheskih bronholegochnyh zabolevanii u detei na primere Sankt-Peterburga: metod. rekomendacii [Epidemiological approaches to the study of the prevalence of recurrent and chronic bronchopulmonary diseases in children by the example of St. Petersburg: guidelines] / A.V. Bogdanova, E.V. Boicova, A.O. Karelin [i dr.]. — SPb., 2004. — 25 s.
Petersburg: guidelines] / A.V. Bogdanova, E.V. Boicova, A.O. Karelin [i dr.]. — SPb., 2004. — 25 s.
31. Zaiceva, O.V. Bronhoobstruktivnyi sindrom [Bronchial obstruction] / O.V. Zaiceva // Infekciya respiratornogo trakta u detei rannego vozrasta [In Respiratory tract infections in infants] / pod red. G.A. Samsyginoi. — M., 2006. — C.279.
32. Goloborod’ko, M.M. Rasprostranennost’ i faktory riska formirovaniya boleznei melkih bronhov u detei na primere g. Sankt-Peterburga i Leningradskoi oblasti [Prevalence and risk factors for the formation of small airways disease in children by the example of St. Petersburg and Leningrad region]: dis. … kand. med. nauk / Goloborod’ko Mariya Mihailovna — SPb., 2009. — 15 s.
33. Gosudarstvennyi doklad o sostoyanii zdorov’ya naseleniya Rossiiskoi Federacii v 2005 g. [State report on the health status of the population of the Russian Federation in 2005] // Zdravoohranenie Rossiiskoi Federacii [Health of the Russian Federation]. — 2007. — № 5. — C.3—34.
— 2007. — № 5. — C.3—34.
34. 2010 Child Asthma Data: Prevalence Tables [electronic resource] // Centers for Disease Control and Prevention. — 2010. —URL: http: www.cdc.gov/asthma/brfss/2010/child/ lifetime/tablek/htm
35. Truncova, E.S. Rasprostranennost’ hronicheskih i recidiviruyuschih nespecificheskih zabolevanii legkih v Yuzhnom regione strany (g. Astrahan’) [The prevalence of chronic and recurrent nonspecific pulmonary diseases in the Southern region of the country (Astrakhan)]: avtoref. dis. … kand. med. nauk / Truncova Evgeniya Semenovna. — SPb., 2005. — C.7—16.
36. Gaiduk, I.M. Respiratornaya allergiya u detei: epidemiologiya, sovremennyi podhod k terapii i profilaktike [Respiratory allergies in children: epidemiology, modern approach to therapy and prevention]: avtoref. dis. … d-ra med. nauk / Gaiduk Irina Mihailovna. — SPb., 2013. — 35 s.
— SPb., 2013. — 35 s.
37. Zabolevaemost’ detskogo naseleniya Rossii v 2011 g.: stat. materialy / Ministerstvo zdravoohraneniya i social’nogo razvitiya [The incidence of child population in Russia in 2011 statistics.The Ministry of Health Social Development]. — M., 2012. — ch. 5. — 144 s.
© Ш.З. Галиев, Н.Б. Амиров, 2015 УДК 616.33-002-02(048.8)
ДУОДЕНОГАСТРАЛЬНЫЙ РЕФЛЮКС КАК ПРИЧИНА РАЗВИТИЯ РЕФЛЮКС-ГАСТРИТА
ШАМИЛЬ ЗУЛЬФАРОВИЧ ГАПИЕВ, аспирант кафедры общей врачебной практики ГБОУ ВПО «Казанский государственный медицинский университет» Минздрава России, Казань, Россия, тел. 8-927-421-03-08, e-mail: [email protected]
НАИЛЬ БАГАУВИЧ АМИРОВ, докт. мед. наук, профессор кафедры общей врачебной практики ГБОУ ВПО «Казанский государственный медицинский университет» Минздрава России, Казань, Россия, тел. 8-905-313-01-11
8-905-313-01-11
Реферат. Цель исследования — проанализировать проблему дуоденогастрального рефлюкса (ДГР) у различных категорий больных, выявить последствия, к которым приводит наличие данной патологии. Материал и методы. В предложенном обзоре литературы приводятся взгляды на патофизиологические механизмы ДГР и развитие рефлюкс-гастрита (РГ). Проводится анализ работ, указывающих на взаимосвязь ДГР и развития предраковых изменений слизистой оболочки желудка (СОЖ). Приводятся данные исследований, в которых имеются несовпадающие друг с другом результаты воздействия желчного рефлюкса на Н. pylori. Результаты и их обсуждение. В клинической картине нет симптомов, специфичных для ДГР, поэтому диагностика строится главным образом на инструментальных методах исследования. Заключение. В лечении ДГР и рефлюкс-гастрита на сегодняшний день применяются различные группы препаратов, эффективность которых исследована в разной степени, а
50
ОБЗОРЫ
ВЕСТНИК СОВРЕМЕННОЙ КЛИНИЧЕСКОМ МЕДИЦИНЫ 2015 Том 8, вып. 2
2
общепринятые схемы лечения данной патологии отсутствуют. Приведена обоснованность назначения урсоде-зоксихолиевой кислоты (УДХК) при ДГР
Ключевые слова: дуоденогастральный рефлюкс, рефлюкс-гастрит, кишечная метаплазия, урсодезоксихолиевая кислота.
DUODENOGASTRiO REFLUX AS A CAUSE OF REFLUX-GASTRiTiS
SHAMIL Z. GALIEV. graduate student of Department of general practice of SBEIHPE «Kazan State Medical University»,
Kazan, Russia, tel. 8-927-421-03-08, e-mail: [email protected]
NAIL B. AMIROV, D.Med.Sci., Professor of Department of general practice of SBEI HPE «Kazan State Medical University», Kazan, Russia, tel. 8-905-313-01-11
Abstract. Aim. The purpose of the study is to look into the problem of duodenogastric reflux (DGR) among different categories of patients. And also to identify consequences of the disease. Material and methods. The literature review shows different existing positions on pathophysiological mechanisms of the DGR and development of reflux gastritis. The main attention is paid on of the articles pointing on the link between DGR and the development of precancerous changes in the gastric mucosa. Comparison of different surveys on how biliary reflux affects H. Pylori displays controversy in their data. Results. Mainly it’s because the clinical picture of DGR has no specific symptoms, so generally the diagnosis is based on instrumental methods of research. Conclusion. It is known than different groups of drugs are used in the treatment of the DGR and reflux gastritis. Nevertheless their efficiency has not been studied uniformly. And the generally accepted regimen for this illness seems has not been found yet.
Aim. The purpose of the study is to look into the problem of duodenogastric reflux (DGR) among different categories of patients. And also to identify consequences of the disease. Material and methods. The literature review shows different existing positions on pathophysiological mechanisms of the DGR and development of reflux gastritis. The main attention is paid on of the articles pointing on the link between DGR and the development of precancerous changes in the gastric mucosa. Comparison of different surveys on how biliary reflux affects H. Pylori displays controversy in their data. Results. Mainly it’s because the clinical picture of DGR has no specific symptoms, so generally the diagnosis is based on instrumental methods of research. Conclusion. It is known than different groups of drugs are used in the treatment of the DGR and reflux gastritis. Nevertheless their efficiency has not been studied uniformly. And the generally accepted regimen for this illness seems has not been found yet. It is shown the validity of UDCA prescription for DGR treatment.
It is shown the validity of UDCA prescription for DGR treatment.
Key words: duodenal reflux, reflux gastritis, intestinal metaplasia, UDCA.
Патофизиологические аспекты дуодено-гастрального рефлюкса. Дуоденальное содержимое является частым спутником и составной частью желудочного сока. Оно выявляется у 20—25% обследуемых [1], а у больных, страдающих патологией верхних отделов желудочно-кишечного тракта (ЖКТ), ретроградный заброс дуоденального содержимого через пилорический сфинктер становится постоянным явлением и обнаруживается в 45—100% случаев [2]. Одни авторы рассматривают его как защитную реакцию организма в ответ на поступление в двенадцатиперстную кишку желудочного сока с высокой кислотно-пептической активностью, подчеркивают его важную роль в регуляции желудочной секреции [8, 9, 32]. Другие исследователи отводят рефлюксу дуоденального содержимого в желудок роль патологического агента в развитии заболеваний желудка и двенадцатиперстной кишки [3].
В ходе измерений концентрации желчных кислот в желудке с помощью фиброоптической спектрофотометрии (Bilitec, 2000) было показано, что желчь в желудке у здоровых пациентов присутствует 37% от времени записи: 28% в дневное время и 47% в ночное [38]. H. Sjovall (2011), исследуя особенности работы мигрирующего моторного комплекса в зоне антрального отдела желудка и двенадцатиперстной кишки, выделяет наличие рефлюкса в содержимом двенадцатиперстной кишки, в котором отсутствует желчь, но содержатся бикарбонат и секреторный IgA. Такому рефлюксу автор отводит большую физиологическую роль в регулировании кислотности антродуоденальной зоны [32].
Основываясь на данных суточной интрагаст-ральной рН-метрии, В.С. Волков и соавт. (2010) делают вывод, что дуоденогастральный рефлюкс (ДГР) постоянно присутствует у здоровых людей, занимает около 40% времени суток и усиливается ночью. Общее число ДГР у здоровых людей составляет в среднем 60—68 раз, в то время как у
больных язвенной болезнью (ЯБ) двенадцатиперстной кишки — 27—32 раза. Обнаружено также, что у больных ЯБ двенадцатиперстной кишки средняя продолжительность рефлюкса вдвое меньше, чем у здоровых людей, для них характерно отсутствие его ночной активации и ограничение преимущественно антральным отделом [8]. Исследуя ДГР у больных хроническим гастродуоденитом, И.Ю. Колесникова и соавт. (2012) придают ему роль антиязвенного протектора. У таких больных повышенная кислотность в теле желудка сочетается с нормально функционирующим ДГР, что способствует компенсации антрального ощелачивания. В то же время у больных ЯБ двенадцатиперстной кишки по сравнению со здоровыми людьми значительно повышена кислотность в теле желудке и его антральном отделе, меньше частота и продолжительность ДГР, отсутствуют его нормальные циркадные колебания. По мнению авторов, роль ДГР в патогенезе таких кислотозависимых заболеваний, как хронический гастрит и ЯБ двенадцатиперстной кишки, до конца не изучена и является предметом дальнейших исследований [9].
Обнаружено также, что у больных ЯБ двенадцатиперстной кишки средняя продолжительность рефлюкса вдвое меньше, чем у здоровых людей, для них характерно отсутствие его ночной активации и ограничение преимущественно антральным отделом [8]. Исследуя ДГР у больных хроническим гастродуоденитом, И.Ю. Колесникова и соавт. (2012) придают ему роль антиязвенного протектора. У таких больных повышенная кислотность в теле желудка сочетается с нормально функционирующим ДГР, что способствует компенсации антрального ощелачивания. В то же время у больных ЯБ двенадцатиперстной кишки по сравнению со здоровыми людьми значительно повышена кислотность в теле желудке и его антральном отделе, меньше частота и продолжительность ДГР, отсутствуют его нормальные циркадные колебания. По мнению авторов, роль ДГР в патогенезе таких кислотозависимых заболеваний, как хронический гастрит и ЯБ двенадцатиперстной кишки, до конца не изучена и является предметом дальнейших исследований [9].
Патогенез рефлюкс-гастрита. Рефлюкс-гастрит (РГ) (щелочной рефлюкс-гастрит) рассматривается как своеобразная форма заболевания, связанная с забросом содержимого двенадцатиперстной кишки в желудок, что оказывает повреждающее действие вследствие постоянной травматизации слизистой оболочки желудка компонентами рефлюксата.
Рефлюкс-гастрит (РГ) (щелочной рефлюкс-гастрит) рассматривается как своеобразная форма заболевания, связанная с забросом содержимого двенадцатиперстной кишки в желудок, что оказывает повреждающее действие вследствие постоянной травматизации слизистой оболочки желудка компонентами рефлюксата.
В настоящее время определены следующие механизмы развития желчного рефлюкса, приводящего к патологическим изменениям слизистой оболочки желудка:
• несостоятельность сфинктерного аппарата: дуоденальное содержимое может свободно достигать желудка и пищевода через пилорический и нижний пищеводный сфинктеры;
• антродуоденальная дисмоторика — нарушение координации между антральным, пилорическим отделами желудка и двенадцатиперстной кишкой,
ВЕСТНИК СОВРЕМЕННОЙ КЛИНИЧЕСКОЙ МЕДИЦИНЫ 2015 Том 8, вып. 2
2
ОБЗОРЫ
51
которые управляют направлением тока дуоденального содержимого;
• ликвидация естественного антирефлюксного барьера (после частичной гастрэктомии и других оперативных вмешательств) [5].
В развитии ДГР наряду с антиперистальтическим механизмом участвует фактор повышения давления в двенадцатиперстной кишке и следующее за ним развитие хронической дуоденальной непроходимости (ХДН) [14]. В течении синдрома ХДН различают компенсированную, субкомпен-сированную и декомпенсированную стадии. При компенсированной (или латентной) стадии ХДН еще сохраняется замыкательная функция привратника. При субкомпенсированной стадии ХДН нарастает гипертензия в двенадцатиперстной кишке, появляются антиперистальтические сокращения, возникает застой желчи и секрета поджелудочной железы. Двенадцатиперстная кишка постепенно расширяется, истощается ее нервно-мышечный аппарат, что приводит к расслаблению привратникового жома и забросу дуоденального содержимого в желудок, развивается ДГР. Желудок расширяется, а в результате повреждения его слизистой оболочки желчными кислотами и лизолецитином формируется рефлюкс-гастрит (РГ). В стадии декомпенсации ХДН гипертензия и усиленная перистальтика двенадцатиперстной кишки сменяются гипотонией и атонией, значительной ее дилатацией, что приводит к развитию порочного круга: содержимое двенадцатиперстной кишки свободно перемещается через зияющий привратник в желудок и обратно. Длительный стаз в двенадцатиперстной кишке приводит к инфицированию содержимого и обусловливает развитие уже хронического дуоденита с прогрессирующей атрофией слизистой оболочки, появлением в ней эрозий и изъязвлений.
Двенадцатиперстная кишка постепенно расширяется, истощается ее нервно-мышечный аппарат, что приводит к расслаблению привратникового жома и забросу дуоденального содержимого в желудок, развивается ДГР. Желудок расширяется, а в результате повреждения его слизистой оболочки желчными кислотами и лизолецитином формируется рефлюкс-гастрит (РГ). В стадии декомпенсации ХДН гипертензия и усиленная перистальтика двенадцатиперстной кишки сменяются гипотонией и атонией, значительной ее дилатацией, что приводит к развитию порочного круга: содержимое двенадцатиперстной кишки свободно перемещается через зияющий привратник в желудок и обратно. Длительный стаз в двенадцатиперстной кишке приводит к инфицированию содержимого и обусловливает развитие уже хронического дуоденита с прогрессирующей атрофией слизистой оболочки, появлением в ней эрозий и изъязвлений.
Среди компонентов рефлюксата наиболее хорошо изучен механизм повреждающего действия желчных кислот, им, по-видимому, принадлежит основная роль в патогенезе повреждения пищевода и желудка при дуоденогастроэзофагеальном рефлюксе (ДГЭР). Желчные кислоты, содержащиеся в рефлюксате, обладают детергентными свойствами и способствуют солюбилизации липидов мембран поверхностного эпителия. Такой эффект зависит от концентрации, уровня конъюгации и гидроксили-рования желчных кислот и, что очень важно, от рН желудочного содержимого. При низких значениях последнего слизистую оболочку повреждают только тауриновые конъюгаты, другие конъюгаты в таких условиях преципитируют. Напротив, при высоких значениях рН, что особенно характерно для культи резецированного желудка, неконъюгированные и дигидроксильные желчные кислоты обладают значительно большими повреждающими свойствами, чем конъюгированные и тригидроксильные [5].
Желчные кислоты, содержащиеся в рефлюксате, обладают детергентными свойствами и способствуют солюбилизации липидов мембран поверхностного эпителия. Такой эффект зависит от концентрации, уровня конъюгации и гидроксили-рования желчных кислот и, что очень важно, от рН желудочного содержимого. При низких значениях последнего слизистую оболочку повреждают только тауриновые конъюгаты, другие конъюгаты в таких условиях преципитируют. Напротив, при высоких значениях рН, что особенно характерно для культи резецированного желудка, неконъюгированные и дигидроксильные желчные кислоты обладают значительно большими повреждающими свойствами, чем конъюгированные и тригидроксильные [5].
Компоненты дуоденального содержимого, повреждающие слизистую оболочку пищевода и желудка, представлены не только желчными кислотами, но и лизолецитином, и трипсином. Установлено, что конъюгированные желчные кислоты (в первую очередь, тауриновые конъюгаты) и лизолецитин об-
ладают более выраженным повреждающим эффектом на слизистую пищевода и желудка при кислом рН, что определяет их синергизм с соляной кислотой в патогенезе эзофагита и рефлюкс-гастрита. Неконъюгированные желчные кислоты и трипсин более токсичны при нейтральном и слабощелочном рН, т.е. их повреждающее действие в присутствии ДГЭР усиливается на фоне медикаментозного подавления кислого рефлюкса. Токсичность неконъюгированных желчных кислот обусловлена преимущественно их ионизированными формами, которые легче проникают через слизистую оболочку пищевода. Приведенные данные могут объяснять факт отсутствия адекватного клинического ответа на монотерапию антисекреторными препаратами у 15—20% больных воспалительными заболеваниями слизистой пищевода и желудка [12].
Неконъюгированные желчные кислоты и трипсин более токсичны при нейтральном и слабощелочном рН, т.е. их повреждающее действие в присутствии ДГЭР усиливается на фоне медикаментозного подавления кислого рефлюкса. Токсичность неконъюгированных желчных кислот обусловлена преимущественно их ионизированными формами, которые легче проникают через слизистую оболочку пищевода. Приведенные данные могут объяснять факт отсутствия адекватного клинического ответа на монотерапию антисекреторными препаратами у 15—20% больных воспалительными заболеваниями слизистой пищевода и желудка [12].
Результатом постоянного повреждения слизистой оболочки желудка кишечным содержимым являются дистрофические и некробиотические изменения желудочного эпителия. Морфологические изменения при этом стереотипны: фовеолярная гиперплазия, отек и пролиферация гладкомышечных клеток в собственной пластинке на фоне умеренного воспаления. Фовеолярную гиперплазию определяют как экспансию слизистых клеток. При РГ она охватывает исключительно поверхностный эпителий и этим отличается от гастрита типа В (хеликобактерного), для которого характерна гиперплазия не только поверхностного, но и ямочного эпителия слизистой оболочки желудка. Эпителий становится резко уплощенным базофильным, насыщенным РНК и почти не содержащим слизи. В клетках эпителия отмечаются грубая вакуолизация цитоплазмы, пик-ноз ядер, некробиоз и некроз, который считается началом образования эрозий. Со временем нарастают атрофические изменения, сопровождающиеся прогрессированием пролиферативных процессов и развитием дисплазии различной степени выраженности, что увеличивает риск малигнизации [6].
При РГ она охватывает исключительно поверхностный эпителий и этим отличается от гастрита типа В (хеликобактерного), для которого характерна гиперплазия не только поверхностного, но и ямочного эпителия слизистой оболочки желудка. Эпителий становится резко уплощенным базофильным, насыщенным РНК и почти не содержащим слизи. В клетках эпителия отмечаются грубая вакуолизация цитоплазмы, пик-ноз ядер, некробиоз и некроз, который считается началом образования эрозий. Со временем нарастают атрофические изменения, сопровождающиеся прогрессированием пролиферативных процессов и развитием дисплазии различной степени выраженности, что увеличивает риск малигнизации [6].
Информативность морфологической диагностики изменений слизистой оболочки желудка при ДГР очень высока. По причине стереотипности изменений слизистой оболочки желудка появилась возможность разработать индекс ДГР, основанный на гистологических данных. Данный индекс был введен G.M. Sobala и соавт. в 1993 г. на основании данных биопсии антрального отдела желудка или дистального отдела культи желудка. Индекс выводится на основе наличия и тяжести некоторых гистологических параметров: отек в собственной пластинке слизистой оболочки желудка (обозначенный как E в формуле ниже), кишечная метаплазия (IM), хроническое воспаление (CI в приведенной ниже формуле) и колонизация Helicobactor pylori (.H.p.) в желудке. Каждому гистологическому параметру патологоанатом присваивает оценку от 0 до 3, что соответствует уровням: отсутствие параметра, легкая, умеренная или высокая степень наличия соответственно. Формула определения индекса билиарного рефлюкса (сокращенно BRI) была выведена на основе ступенчатого логистического регрессионного анализа:
52
ОБЗОРЫ
ВЕСТНИК СОВРЕМЕННОЙ КЛИНИЧЕСКОМ МЕДИЦИНЫ 2015 Том 8, вып. 2
BRI = (7 x Е) + (3 x IM) + (4 x CI) — (6 x Н.р.).
По данным Sobala и соавт., BRI выше 14 указывает на ДГР (что соответствует уровню желчных кислот более 1 ммоль/л, т.е. выше уровня верхнего предела физиологической нормы) с 70% чувствительности и 85% специфичности. Основываясь на этих данных, а также на том, что другие методы диагностики ДГР не обладают на сегодняшний день высокой точностью, данный индекс используется рядом авторов в качестве диагностического критерия в клинических исследованиях [40, 45 и др.].
Вторичный билиарный рефлюкс-гастрит. Наверное, самой многочисленной группой пациентов, у которых развивается вторичный рефлюкс-гастрит (РГ), являются пациенты, перенесшие холецистэктомию (ХЭ). Все больше данных появляется о том, что ХЭ, которая является золотым стандартом лечения желчнокаменной болезни (ЖКБ), связана с высоким риском развития различной патологии слизистой оболочки желудка. У пациентов после ХЭ с удлинением времени после операции увеличивается риск развития РГ [26], кишечной метаплазии и даже рака желудка [33]. Предыдущие исследования [35] показали, что от 51 до 89% пациентов после ХЭ имеют патологический ДГР, имеется значительная корреляция между уровнем внутрижелудочных желчных кислот и тяжестью ДГР. G. Aprea и соавт. (2012) исследовали пациентов после проведенной ХЭ на протяжении 6 мес послеоперационного периода. Обнаружилось, что у 58% таких пациентов возникает РГ, для диагностики которого использовался гистологический BRI. Причем клиническая симптоматика в послеоперационном периоде не соответствует гистологическим данным: в то время как BRI был положительный у 58% пациентов после ХЭ, клинические симптомы в виде диспепсии были обнаружены только у 41,9% из них. При этом уровень инфицированности Н. pylory у таких пациентов оставался неизменным как до, так и после операции, несмотря на высокий уровень показателей ДГР [45].
Другой вид операций, при котором высок процент изменений слизистой оболочки желудка по причине желчного рефлюкса, — это резекции желудка или операции на тонкой кишке [24, 30]. S. Kuran и соавт. (2008) изучали пациентов, которым проводились различные манипуляции на желчевыводящих путях, такие как эндоскопическая папиллосфинктеротомия, эндоскопическое стентирование или холедоходуоде-ностомия при патологиях, не связанных со злокачественными новообразованиями. Оказалось, что все указанные выше процедуры связаны с повышенным риском развития ДГР. Наиболее высокий процент ДГР возникает у больных после холедоходуодено-стомии. При этом, если у пациентов, которые не были прооперированы, ДГР в основном оказывает влияние на антральный отдел желудка, то у пациентов, перенесших перечисленные выше операции на желчных путях, в том числе и после ХЭ, ДГР воздействует как на антральный отдел, так и на тело желудка [46]. Таким образом, по мере проведения новых исследований появляется все больше данных
о возникновении послеоперационных осложнений, причиной которых выступает ДГР.
Дуоденогастральный рефлюкс и предраковые изменения слизистой оболочки желудка. В
связи с тем общим положением, что хроническое воспаление является предрасполагающим фактором в развитии рака, а также с доказанным фактом, что в желудке воспаление, вызванное Helicobacter pylori, связано с развитием рака желудка, возникает вопрос о взаимосвязи гастрита, вызванного ДГР, с канцерогенезом. До настоящего времени нет прямых доказательств, что ДГР является причиной развития рака желудка. В «скандинавском исследовании» изучалась взаимосвязь ДГР и рака желудка у пациентов после ХЭ. Для того чтобы изучить вопрос, является ли длительное неинфекционное воспаление, каковым является ДГР, предиктором канцерогенеза, K. Fall и соавт. (2007) провели масштабное исследование большой когорты населения после проведенной ХЭ. Как известно, после такой операции с высокой частотой возникают ДГР и реактивный гастрит. Были исследованы данные 251 672 пациентов Шведского национального регистра госпитализированных больных, которые перенесли ХЭ с 1970 по 1997 г. При этом все случаи заболевания раком желудка были выявлены через взаимосвязь со Шведским регистром заболеваемости раком. В качестве сравнения использовались показатели заболеваемости раком среди всего населения Швеции. Для обеих групп были высчитаны стандартизированные коэффициенты заболеваемости. В результате было выявлено, что у больных после ХЭ на 11% возрастает риск возникновения рака дистального отдела желудка. Причем такая взаимосвязь была найдена только у мужчин и в течение 10 лет после операции. У женщин не было выявлено изменения риска заболеваемости, кроме того, у мужчин со сроком операции более 10 лет такая связь также не наблюдалась. Тот факт, что взаимосвязь изменялась в зависимости от пола и затрагивала сравнительно короткий период, а с течением времени ослабевала, то, по мнению авторов, она ослабляет причинноследственную связь между ХЭ и раком желудка на протяжении долгого периода времени [35].
В ряде исследований изучались патогенетические механизмы воздействия билиарного рефлюкса на слизистую оболочку желудка и определялось, может ли ДГР быть фактором канцерогенеза. Так как при ДГР наблюдается усиление пролиферации слизистых клеток, это увеличивает вероятность возникновения опухолевого клона эпителиальных клеток. Такие клоны возникают, в частности, в тех случаях, когда хронические повреждения эпителия связаны с рефлюксом желчи [36].
В ряде других исследований изучались факторы, которые способствуют развитию кишечной метаплазии слизистой оболочки желудка, так как кишечная метаплазия также может быть фактором канцерогенеза. Ранее уже было показано, что такая метаплазия связана с хроническим воспалением, вызванным или желудочно-пищеводным рефлюксом, или гастроэзофагеальной рефлюксной болезнью (ГЭРБ), или хеликобактерной инфекцией.
ВЕСТНИК СОВРЕМЕННОЙ КЛИНИЧЕСКОЙ МЕДИЦИНЫ 2015 Том 8, вып. 2
ОБЗОРЫ
53
Другим этиологическим фактором является рефлюкс желчи. Было показано, что рефлюкс желчи является независимым фактором риска в развитии кишечной метаплазии как на уровне кардиального отдела слизистой оболочки желудка [41], так и в других отделах желудка. Причем такие изменения слизистой оболочки желудка наблюдались, по некоторым данным, уже на протяжении 6 мес после операции [47], в то время как другие исследователи [45] считают такой срок слишком коротким для развития метаплазии на фоне патологического ДГР и РГ
В большом исследовании T Matsuhisa и соавт. (2013) было обнаружено наличие взаимосвязи между риском возникновения атрофического гастрита и кишечной метаплазии и рефлюксом желчных кислот в желудок, а также наличие хеликобактерной инфекции. В исследовании приняло участие 2 283 пациента с наличием желчных кислот в содержимом желудка натощак. Пациенты были разделены на группы по уровню концентрации желчных кислот. При этом оказалось, что риск развития атрофического гастрита не связан с наличием ДГР ни у Н. pylori-позитивных, ни у Н. pylori-негативных пациентов. В то время как риск развития кишечной метаплазии связан с наличием повышенных концентраций желчных кислот в желудке у Н. pylori-негативных пациентов [42]. В исследованиях последних лет было обнаружено, что воздействие желчных кислот на слизистую оболочку желудка, в частности хеноде-зоксихолевой кислоты (ХДК), имеет свой, не связанный с H. pylori, механизм действия. В эксперименте in vitro на культуре клеток было показано, что ХДК приводит к кишечной метаплазии клеток слизистой оболочки желудка путем экспрессии генов Cdx2 и MUC2, вызывающих подобные изменения. Причем эффект воздействия ХДК на экспрессию этих генов был дозозависимым [43]. Такие же данные были получены in vivo при исследовании воздействия желчных кислот на слизистую оболочку желудка у пациентов, инфицированных H. pylori. Несмотря на то что при воздействии желчных кислот уровень воспалительных изменений слизистой оболочки желудка, вызванных H. pylori, снижался, на фоне ДГР развивались атрофия и кишечная метаплазия и повышался риск возникновения рака желудка [44].
H. pylori и дуоденогастральный рефлюкс в патогенезе гастрита. Вопрос о взаимодействии таких патогенных факторов, как H. pylori и желчи в развитии рефлюкс-гастрита, ставится уже давно. Известны данные об ингибирующем воздействии желчных кислот на H. pylori, это было продемонстрировано в работе M.L. Hanninen (1991), где под действием хенодезоксихолевой и дезоксихолевой кислот (основных компонентов желчи) происходило разрушение этого микроорганизма in vitro [25]. Однако в клинических исследованиях имеются различные данные по этому вопросу.
У пациентов после ХЭ исследования различных авторов показали разные результаты по уровню обсемененности H. pylori слизистой оболочки желудка. Имеются исследования, в которых количественные показатели обсемененности H. pylori снижались в послеоперационном периоде [47].
В других исследованиях обсемененность H. pylori не изменялась [33] или даже увеличивалась [26] и в послеоперационном периоде. Во многих случаях авторы отмечают синергизм этих двух патогенных факторов в возникновении патологических изменений в слизистой оболочке желудка у пациентов после ХЭ.
При исследовании пациентов, перенесших резекцию желудка или прооперированных на кишечнике, также нет однозначных данных по влиянию Н. pylori на течение рефлюкс-гастрита. Исследования, проведенные у таких больных, выявили, что частота гастрита культи, вызванного Н. pylori возрастает после резекции желудка и снижается после операций на желчевыводящих путях [30]. У тех больных, у которых операция выполнена таким способом, который защищает культю желудка от желчного рефлюкса (резекция желудка по Бильрот-2), были более высокие показатели обсемененности H. pylori и более низкие показатели воспаления слизистой оболочки желудка, по данным эндоскопического исследования. И, наоборот, у больных, которым была проведена резекция желудка по Бильрот-1, показатели воспаления слизистой оболочки желудка были выше, а уровень обсемененности H. pylori — ниже [24].
В более позднем исследовании X.B. Li и соавт. (2008) показатели хронического воспаления, его активность, атрофия и кишечная метаплазия слизистой оболочки желудка у пациентов после резекции дистальной части желудка на фоне присутствия H. pylori были значительно более высокими, чем у H. pylori-негативных пациентов. На основании этих данных авторы делают вывод о том, что и ДГР, и инфицированность H. pylori утяжеляют течение гастрита [31].
В исследованиях пациентов с первичным билиарным рефлюксом было также отмечено взаимное влияния рефлюкса и H. pylori на состояние слизистой оболочки желудка. При оценке влияния билиарного рефлюкса на выраженность повреждений слизистой оболочки желудка у пациентов с диспепсией и хроническим гастритом было выявлено, что как степень изменений слизистой оболочки, так и колонизация инфекцией H. pylori коррелировали с длительностью билиарного рефлюкса [22]. В другом исследовании было найдено, что у пациентов с хроническим каль-кулезным холециститом, инфицированных H. pylori, желчный рефлюкс встречается достоверно чаще, чем у здоровых лиц и у неинфицированных больных [27]. В одном из ранних исследований, посвященных этой проблеме, при исследовании пациентов с билиарным рефлюксом было обнаружено, что это не только два независимых фактора в развитии гастрита. При наличии инфицированности H. pylori количество рефлюксов в желудок возрастает [34]. Однако в последующих исследованиях не было найдено подтверждения такой взаимосвязи.
Можно предположить комплексный механизм воздействия ДГР и H. pylori на слизистую оболочку желудка. Так, абсорбция рефлюктанта желчи на поверхности слизистой оболочки желудка оказывает прямой повреждающий эффект, а также усиливает
54
ОБЗОРЫ
ВЕСТНИК СОВРЕМЕННОЙ КЛИНИЧЕСКОМ МЕДИЦИНЫ 2015 Том 8, вып. 2
действие пепсина и соляной кислоты; повреждение слизистой оболочки желудка в свою очередь способствует колонизации Н. pylori от антрального отдела до тела желудка. В отсутствие инфицирования Н. pylori вследствие забросов щелочного содержимого из ДПК и изменения рН возможна бактериальная контаминация микрофлорой нижележащих отделов пищеварительного тракта, что также приводит к более выраженному повреждению слизистой оболочки желудка.
Клиническая картина. В «чистом» виде ДГР встречается редко, в большинстве случаев он диагностируется на фоне других заболеваний ЖКТ, прежде всего гастродуоденальной патологии, что накладывает отпечаток на клиническую симптоматику рефлюкса, в значительной степени маскируя ее. Клинические проявления ДГР характеризуются преобладанием диспептических симптомов — отрыжкой воздухом или кислым, тошнотой, изжогой, рвотой желчью, горечью во рту, часто не проходящей или усиливающейся на фоне приема ингибиторов протонной помпы (ИПП).
Боли в животе носят периодический характер, чаще схваткообразный, иногда провоцируются физической нагрузкой, стрессовыми ситуациями. В отличие от «классического» кислого рефлюкса, проявляющегося изжогой, регургитацией и дисфагией, ассоциация ДГР с соответствующей симптоматикой выражена слабее, однако чаще, чем при кислом рефлюксе, выявляются симптомы диспепсии. Пациенты могут предъявлять жалобы на боль в эпига-стрии, усиливающуюся после приема пищи, иногда достигающую значительной интенсивности [15].
Чаще всего указанные выше симптомы возникают как следствие развившегося на фоне ДГР гастрита. Несостоятельность сфинктерного аппарата, антродуоденальная дискоординация (нарушение координации между антральным, пилорическим отделами желудка и двенадцатиперстной кишки), а также резекции части желудка, приводящая к ликвидации естественного антирефлюксного барьера, являются причиной формирования желчного рефлюкса и служат важными факторами анамнеза, выявление которых может привести к правильной постановке диагноза [11].
В связи с тем, что нет клинических симптомов, специфичных для ДГР, его диагностика в большей степени проводится на основании инструментальных методов исследования.
Диагностика дуоденогастрального рефлюкса. Наиболее распространенным на сегодняшний день методом диагностики, при котором устанавливается диагноз ДГР, является эндоскопическая эзофагогастродуоденоскопия. Среди изменений, определяемых при ЭГДС, наблюдаются наличие очаговой гиперемии, отек слизистой оболочки желудка, окрашивание содержимого желудка в желтый цвет. Привратник, из которого в желудок порционно поступает желчь, зияет [4, 5]. Наиболее распространенными эндоскопическими изменениями при ДГР являются: эритема слизистой оболочки желудка, наличие желчи в желудке, утолщение складок желудка, эрозии, атрофия слизистой оболочки желудка, пе-
техии, кишечная метаплазия и полипы желудка [29]. Причем, по данным авторов, после операций на желудке, таких как резекция желудка, пилоропластика и наложение желудочно-кишечного анастомоза при возникновении рефлюкс-гастрита, наиболее часто возникали такие изменения слизистой оболочки желудка, как острое воспаление, наличие хеликобак-терной инфекции, образование желудочных полипов и пептических язв. В то время как у пациентов после операций на желчевыводящих путях, таких как ХЭ или наложение холедоходуоденального анастомоза, более частыми были изменения в виде отека и дисплазии слизистой оболочки желудка.
рН-метрия как кратковременная, так и суточная позволяет оценить профиль внутрижелудочной рН и высоту рефлюкса. Более достоверным методом является суточная рН-метрия. При этом определяется рН в теле желудка и антральном отделе. За ДГР принимается «зазубренное» ощелачивание или быстрое повышение рН в антральном отделе выше 4,0, не связанное с приемом пищи или поступлением слюны [17].
В связи с тем, что указанные выше методы диагностики ДГР являются недостаточно точными, они часто дополняются другими методами. Среди них можно отметить аспирацию содержимого желудка, выполняемую совместно с ФЭГДС или рН-метрией, которые позволяют провести биохимический анализ находящихся в желудке желчных кислот и определить их концентрацию [4].
При ультразвуковой диагностике (эхография с водной нагрузкой) в случае заброса щелочного содержимого двенадцатиперстной кишки в кислую среду желудка, т.е. при ДГР, на эхограммах периодически, соответственно забросу в желудок дуоденального содержимого, регистрируется ретроградное движение пузырьков газа (эхогенных участков) и жидкости от привратника к телу желудка [18, 19].
При рентгеноскопии желудка характерным признаком ДГР является регургитация бария из двенадцатиперстной кишки в желудок.
Из методов диагностики билиарного рефлюкса наиболее точной, по мнению ряда авторов [28, 47, 56], является фиброоптическая спектрофотометрия (Bilitec, 2000), основанная на определении абсорбционного спектра билирубина. В отличие от диагностики аппаратом Bilitec, изолированное мони-торирование рН внутри пищевода или желудка признано неудовлетворительным, так как нет возможности с точностью определить, когда заканчивается постпрандиальный период. Кроме того, по мнению ряда авторов, фиброоптическая спектрофотометрия является наиболее удобным диагностическим методом для пациента. Однако более поздние исследования показали, что если для измерения концентрации желчи в пищеводе фиброоптическая спектрофотометрия является достаточно точной методикой, то для измерений уровня билирубина в желудке методика не так точна. K.H. Fuchs и соавт. (1999) [37] при исследовании пищевода и желудка с помощью Biliteс и рН-мониторинга обнаружили несоответствие этих двух методов в регистрации ДГР. Так, в щелочной среде регистрируется повышение
ВЕСТНИК СОВРЕМЕННОЙ КЛИНИЧЕСКОЙ МЕДИЦИНЫ 2015 Том 8, вып. 2
ОБЗОРЫ
55
уровня билирубина более часто при постоянном рН (43%), а увеличение рН — при неизменном уровне билирубина (37%). Другие авторы показали, что данные по концентрации билирубина, измеренные с помощью Bilitec, не совсем точны в кислой среде желудка [38, 39].
Радионуклидная билиарная сцинтиграфия с HIDA меченым радиоизотопом технеция применяется в условиях стационара, однако до настоящего времени имеет ряд преимуществ перед другими методами, так как является неинвазивным и физиологическим методом определения ДГР Исследования, проведенные в последние годы, показали наличие корреляции между тяжестью гистологических изменений на слизистой оболочке желудка и наличием ДГР на сцинтиграфии. Будучи физиологической методикой с хорошей воспроизводимостью результатов, гепатобилиарная сцинтиграфия подходит для рутинного клинического применения в диагностике ДГР [47]. Для косвенного определения уровня ДГР широко используется индекс, основанный на гистологических изменениях слизистой оболочки желудка, о котором говорилось выше.
Лечение. Лечение ДГР и РГ представляет сложную задачу и включает назначение прокинетиков, антацидов, препаратов урсодезоксихолевой кислоты (УДХК), ингибиторов протонной помпы (ИПП), сорбентов и цитопротекторов.
Терапия ДГР направлена на нейтрализацию раздражающего действия компонентов дуоденального содержимого на слизистую оболочку желудка и пищевода (в случае УДХК, сорбентов и цитопротекторов), на нормализацию пропульсивной способности ЖКТ (прокинетики). Терапия, подавляющая кислотопродукцию, может быть эффективна в снижении повреждающего действия соляной кислоты и желчи. Подавление кислотопродукции с применением ИПП эффективно снижает как кислотный, так и желчный рефлюкс [49]. Возможный механизм, который задействован в подавлении желчного рефлюкса, связан с тем, что ИПП увеличивают длительность III фазы активности антрального отдела желудка и двенадцатиперстной кишки в межпищеварительный период. Удлинение данной фазы, названной мигрирующим моторным комплексом, может приводить к ускорению продвижения содержимого желудка по антруму и двенадцатиперстной кишки, что, в свою очередь, должно уменьшить число ДГР и объем как кислотного, так и желчного заброса в желудок. Данный факт был обнаружен L. Vinter-Jensen и соавт. (1989) при исследовании воздействия омепразола на мигрирующий моторный комплекс у здоровых добровольцев [51].
Помимо рабепразола у больных РГ применяется антацид местного действия — гидротальцит. Достоинством этого антацида является его специфическая слоисто-сетчатая структура, которая создает механизм для оптимального рН-контроля, создаваемого препаратом. Механизм действия данной структуры состоит в том, что когда гидротальцит взаимодействует с кислотой, активны только поверхностные слои таблетки, включающие в себя окись алюминиевого и магниевого гидратата. Как только показатель
рН становится больше 5, реакция останавливается. Оставшиеся слои решетки, представленные прослойками воды и анионов углекислой кислоты, сохраняются до тех пор, пока секреция кислоты вновь не возрастет. Далее включается в действие следующий слой гидротальцита. Благодаря этому препарат не только быстро избавляет от изжоги, боли, тяжести в желудке, но и дольше, чем другие антациды, удерживает рН на уровне 3, не нарушая при этом процесса пищеварения [21]. Помимо поддержания рН у гидротальцита имеется также свойство адсорбента, благодаря чему адсорбируются желчь и лизолецитин. В исследовании H. Chen и соавт. (2010) при применении рабепразола или гидротальцита в монотерапии уровень купирования симптомов при ДГР был недостаточен. Исследование показало, что при применении комбинированной терапии (рабепразол плюс гидротальцит) снижались все показатели ДГР, которые исследовались авторами: диспептическая симптоматика, эндоскопические и гистологические данные ДГР, количество желчных рефлюксов, количество желчных рефлюксов длительностью более 5 мин и процент времени, в течение которого обнаруживался билирубин в содержимом желудка. Таким образом, комбинированная терапия рабепразолом плюс гидротальцитом наиболее эффективна по сравнению с группой пациентов без терапии и по сравнению с монотерапией каждым препаратом у больных ДГР [50].
К препаратам, которые применяются для восстановления ЖКТ и устранения ДГР, относятся антагонисты дофаминовых рецепторов (метокло-прамид, домперидон), агонисты 5-НТ4 серотонино-вых рецепторов (мосаприд, тегасерод), препараты комбинированного действия: антагонисты периферических дофаминовых D2-рецепторов и блокаторы ацетилхолинэстеразы (итоприда гидрохлорид), агонисты мотилиновых рецепторов (эритромицин), агонисты опиоидных периферических рецепторов (тримебутина малеат), неселективные блокаторы синтеза NO и др.2-антагонист) связаны с блокадой дофаминовых рецепторов. Антагонисты дофаминовых рецепторов повышают тонус нижнего пищеводного сфинктера, усиливают сократительную способность желудка и препятствуют его релаксации, ускоряют эвакуацию из желудка и улучшают антродуоденальную координацию, способствуя тем самым устранению ДГР. Из препаратов этой группы чаще применяется домпери-дон в связи с тем, что метоклопрамид проникает через гематоэнцефалический барьер и может вызывать большое количество побочных эффектов: мышечный гипертонус, гиперкинезы, сонливость, беспокойство, депрессию, а также эндокринные нарушения (гиперпролактинемия, галакторея).
56
ОБЗОРЫ
ВЕСТНИК СОВРЕМЕННОЙ КЛИНИЧЕСКОМ МЕДИЦИНЫ 2015 Том 8, вып. 2
Препарат комбинированного действия итоприда гидрохлорид является одновременно антагонистом дофаминовых рецепторов и блокатором ацетилхолинэстеразы. Он усиливает пропульсивную моторику желудка и ускоряет его опорожнение, оказывает противорвотный эффект в результате взаимодействия с D2-рецепторами триггерной зоны (эффективность препарата 57—81%). Антагонист периферических опиоидных рецепторов тримебу-тина малеат является универсальным регулятором моторики, оказывает спазмолитическое (антагонист NMDA-рецепторов) или прокинетическое действие в зависимости от исходного состояния моторики ЖКТ (эффективность 83%). Тримебутин оказывает стимулирующее влияние на III фазу активности антрального отдела желудка и двенадцатиперстной кишки в межпищеварительный период, что приводит к улучшению пропульсивной перистальтики ЖКТ и доказанному уменьшению ДГР [15].
Кроме прокинетиков при наличии билиарного рефлюкса применяются, как было показано выше, антациды и цитопротекторы, сорбенты для нейтрализации соляной кислоты и адсорбции желчных кислот и лизолецитина, а также с целью повышения устойчивости слизистой оболочки желудка к действию повреждающих агрессивных факторов.
Основанием для применения УДХК при гастрите и эзофагите, обусловленных ДГР, служит ее цитопротекторный эффект. УДХК способствует переходу желчных кислот, содержащихся в забрасываемом содержимом, в водорастворимую форму, что уменьшает агрессивные свойства рефлюксата. Вытеснение пула гидрофобных желчных кислот и предотвращение индуцированного ими апоптоза эпителиоцитов ведут к редукции клинической симптоматики и эндоскопических признаков повреждения слизистой оболочки желудка и слизистой пищевода.
Эффективность УДХК в лечении желчного рефлюкс-гастрита была показана в экспериментальных научных исследованиях.
Т. Kawamura и соавт. (1989) вызывали у экспериментальных крыс стрессовое повреждение желудка. Предварительное назначение УДХК защищало желудок экспериментального животного от ульцерации, при этом уровень каталазы в сыворотке крови и ткани желудка был существенно ниже, чем у животных из группы контроля. Кроме того, УДХК в данном эксперименте продемонстрировала антиоксидантный эффект [55]. В 2008 г. группой ученых были опубликованы результаты эксперимента по применению УДХК у мышей, инфицированных H. pylori. Мыши с H. pylori-позитивным гастритом были разделены на две группы: 1-я получала УДХК, а 2-я — плацебо. Результаты эксперимента показали уменьшение колонизации H. pylori на слизистой оболочке желудка. Это повлияло на степень выраженности гастрита, которая оценивалась по активности миелопероксидазы, свидетельствующей о наличии полиморфно-ядерных лейкоцитов в ткани желудка. Данный показатель определялся на 4, 6 и 8-й нед приема УДХК, при этом отмечалось его снижение на 60, 40 и 37,5% соответственно. В
этом же исследовании было показано, что УДХК при гастрите снижает уровень малатдегидрогеназы и кислородных радикалов, что может предотвратить апоптоз при H. pylori-позитивном гастрите. Таким образом, на экспериментальной модели была показана эффективность применения УДХК не только при поражениях, вызванных ДГР, но и при гастритах, причиной которых является H. pylori [54]. Это важный аспект применения УДХК в силу того, что, как было отмечено выше, в патогенезе рефлюксгастритов желчные кислоты и H. pylori обладают синергизмом в повреждающем воздействии на слизистую оболочку желудка и пищевода.
A.B. Stefaniwsky и соавт. (1985) применяли УДХК у больных после операций на желудке в дозе 1000 мг/сут в течение месяца. У больных присутствовали эпигастральная боль, тошнота и рвота желчью. В плацебоконтролируемом исследовании оценивалось влияние УДХК на клиническую симптоматику и гистологические показатели слизистой оболочки желудка. В результате лечения с помощью УДХК значительно уменьшились интенсивность и частота болей, почти исчезли тошнота и рвота. За период терапии доля УДХК в желчи, полученной из желудочного содержимого, выросла до 50% от общего количества желчных кислот [52].
Эффективность лечения РГ с помощью УДХК, подтвержденная эндоскопическим исследованием, была отмечена и у больных после ХЭ. M. Ozkaya и соавт. (2002) исследовали воздействие УДХК на уровень эпидермального фактора роста в слизистой оболочке желудка. Данный индуктор пролиферации эпителиальных клеток слизистой оболочки желудка секретируется в ответ на повреждение слизистой, а также является фактором защиты и заживления слизистой оболочки желудка у больных с билиарным РГ после проведенной ХЭ. В исследовании участвовал 31 пациент с ДГР и различными степенями гастрита. После 6-недельного курса лечения УДХК у 29% пациентов наблюдалось полное исчезновение эндоскопических симптомов заболевания, а у остальных пациентов излечение было частичным. Однако уровень эпидермального фактора роста значительно снижался у всех пациентов на фоне лечения УДХК. Низкий уровень высвобождения фактора роста эпидермиса можно объяснить заживлением слизистой оболочки желудка после курса лечения. Однако авторы считают, что необходимы дальнейшие исследования для того, чтобы выяснить, имеет ли УДХК прямое влияние на эпидермальный фактор роста или эта взаимосвязь опосредованная [53].
Таким образом, ДГР как патологический рефлюкс осложняет течение многих функциональных и органических заболеваний ЖКТ, является одним из факторов, способствующих канцерогенезу в слизистой оболочке желудка, а его клинические проявления не позволяют своевременно диагностировать ДГР и предотвратить его последствия. Одновременно с этим методы диагностики и лечения ДГР нуждаются в дальнейшей доработке и нахождении оптимальных и общепринятых схем и алгоритмов.
ВЕСТНИК СОВРЕМЕННОЙ КЛИНИЧЕСКОЙ МЕДИЦИНЫ 2015 Том 8, вып. 2
ОБЗОРЫ
57
ЛИТЕРАТУРА
1. Пиманов, С.И. Гастрит, эзофагит и язвенная болезнь / С.И. Пиманов. — Н. Новгород: Изд-во НГМА. — 2000. — 380 с.
2. Михаськив, И.Н. Роль рефлюкса дуоденального содержимого в генезе рака культи желудка после резекции желудка / И.Н. Михаськив // Хирургия. — 1980. — № 2. — С.44—51.
3. Вахрушев, Я.М. Комплексное изучение патогенетических механизмов эрозивного поражения желудка и двенадцатиперстной кишки / Я.М. Вахрушев, Е.В. Никишина // Pocсийский гастроэнтерологический журнал. — 1998. — № 3. — С.22—29.
4. Санников, О.Р Оптимизация диагностики дуодено-гастрального рефлюкса после холецистэктомии: авто-реф. дис. … канд. мед. наук / О.Р Санников. — Пермь, 2007. — 22 с.
5. Бабак, О.Я. Желчный рефлюкс: современные взгляды на патогенез и лечение / О.Я. Бабак // Сучасна гастроэнтеролога. — 2003. — № 1(11). — С.28—30.
6. Аруин, Л.И. Морфологическая диагностика болезней желудка и кишечника / Л.И. Аруин, Л.Л. Капуллер,
В.А. Исаков. — М.: Триада-Х, 1998. — 496 с.
7. Гончарик, И.И. Клиническая гастроэнтерология / И.И. Гончарик. — Минск: Интерпрессервис, 2002. — 334 с.
8. Волков, В.С. Дуоденогастральный рефлюкс и язвенная болезнь двенадцатиперстной кишки — расставим точки над «i» / В.С. Волков, И.Ю. Колесникова // Верхневолжский медицинский журнал. — 2010. — Т. 8, № 1. — С.26—29.
9. Колесникова, И.Ю. Почему не возникает язва двенадцатиперстной кишки у больных хроническим гастродуоденитом? / И.Ю. Колесникова, В.С. Волков,
Е.К. Лукашева // Российские медицинские вести. — 2012. — Т XVII., № 3. — С.69—72.
10. Колесникова, И.Ю. Особенности дуоденогастрального рефлюкса при язвенной болезни двенадцатиперстной кишки и его динамика после эрадикации Helicobacter pylori / И.Ю. Колесникова, В.С. Волков, Л.А. Любская // Экспериментальная и клиническая гастроэнтерология. — 2011. — № 5. — С.16—19.
11. Панько, С.В. Значение суточного рН-мониторирования в диагностике рефлюксной патологии желудочнокишечного тракта / С.В. Панько, Г.А. Журбенко, А.С. Карпицкий [и др.] // Биологические ритмы: материалы Междунар. науч.-практ. конф. 11—12 окт. 2012 г. — Брест, 2012. — С.147—149.
12. Осипенко, М.Ф. Подходы к диагностике и терапии гастрита, ассоциированного с рефлюксом желчи / М.Ф. Осипенко, М.А. Ливзан // Лечащий врач. — 2012. — № 2. — С.50—53.
13. Буеверов, А.О. Дуоденогастроэзофагеальный рефлюкс как причина рефлюкс-эзофагита / А.О. Буеверов, Т.Л. Лапина // Фарматека. — 2006. — № 1. — С.1—5.
14. Звягинцева, Т.Д. Хроническая дуоденальная непроходимость и принципы консервативной терапии / Т.Д. Звягинцева, И.И. Шаргород // Новости медицины и фармации. Гастроэнтерология (тематический номер). — 2011. — № 367 (газета). — URL: http://www. mif-ua.com (дата обращения 26.10.2014).
15. Звягинцева, ТД. Дуоденогастральный рефлюкс в практике врача-гастроэнтеролога: очевидные опасности и скрытая угроза / Т.Д. Звягинцева, А.И. Чернобай // Здоровье Украины. — 2012. — № 3. — С.11.
16. Юрченко, И.Н. Дуоденогастральный рефлюкс при гастроэзофагеальной рефлюксной болезни / И.Н. Юрченко, Н.А. Каширина, Н.А. Власова // Материалы XVII Российской гастронедели // РЖГГК. — 2011. — № 5, прил. 38. — C.19.
17. Селезнева, Э.Я. Внутрижелудочная рН-метрия в оценке секреторных и моторных нарушений желудка /
Э.Я. Селезнева // Российский гастроэнтерологический журнал. — 1998. — № 4 — С.69—72.
18. Гибадулина, И.О. Возможности ультразвуковой оценки функциональных результатов хирургической коррекции дуоденогастрального рефлюкса / И.О. Гибадулина,
Н.В. Гибадулин // SonoAce-Ultrasound. — 2011. — № 22 (мед. журнал). — URL: http://www.medison.ru/si/
19. Руководство по ультразвуковой диагностике заболеваний пищевода, желудка и двенадцатиперстной кишки / под ред. ГК. Жерлова, С.А. Соколова. — Новосибирск: Наука, 2005. — 208 с.
20. Белоусов, С.С. Гастроэзофагеальная рефлюксная болезнь и дуоденогастральный рефлюкс / С.С. Белоусов,
C. В. Муратов, А.М. Ахмад. — Н. Новгород: Изд-во Нижегородской гос. мед. академии, 2005. — 120 с.
21. Лапченко, Е.С. Состояние слизистой оболочки желудка у больных с дуоденогастральным рефлюксом / Е.С. Лапченко, Т.М. Преображенская, Е.В. Галаева, И.Д. Лоранская // Экспериментальная и клиническая гастроэнтерология. — 2010. — № 9. — С.25—29.
22. Ивашкин, В.Т. Место антацидов в современной терапии язвенной болезни / В.Т. Ивашкин, Е.К. Баранская,
O. С. Шифрин, Е.Ю. Юрьева // Русский медицинский журнал. Болезни органов пищеварения. — 2002. — Т 4, № 2. — URL: http://www.rmj.ru/
23. Chen, S.L. Effects of bile reflux on gastric mucosal lesions in patients with dyspepsia or chronic gastritis / S.L. Chen,
J.Z. Mo, Z.J. Cao [et al.] // World J. Gastroenterol. — 2005. — Vol. 11, № 18. — P.2834—2847.
24. Abe, H. Influence of bile reflux and Helicobacter pylori infection on gastritis in the remnant gastric mucosa after distal gastrectomy / H. Abe, K. Murakami, S. Satoh [et al.] // J. Gastroenterol. — 2005. — Vol. 40, № 6. —
P. 563—569.
25. Hanninen, M.L. Sensitivity of Helicobacter pylori to different bile salts / M.L. Hanninen // Eur. J. Clin. Microbiol. Infect. Dis. — 1991. — Vol. 10. — P.515—518.
26. Caldwell, M.T.P. Helicobacter pylori infection increases following cholecystectomy / M.T.P. Caldwell, M. McDermott, S. Jazrawi [et al.] // Ir. J. Med. Sci. — 1995. — Vol. 164. — P52—55.
27. Chen, D.F. H. pylori exist in the gallbladder mucosa of patients with chronic cholecystitis / D.F. Chen, L. Hu, P Yi,
D. C. Fang [et al.] // World J. Gastroenterol. — 2007. — Vol. 13, № 10. — P1608—1611.
28. Bechi, P. Are there alternative methods for measuring «bile» reflux? / P Bechi, F. Pucciani, F. Baldini [et al.] // Dig. Dis. Sci. — 1993. — Vol. 38, № 7. — P1297—1306.
29. Lin, J.K. A study of diagnosis of primary biliary reflux gastritis / J.K. Lin, PJ. Hu, C.J. Li [et al.] // Zhonghua Nei Ke Za Zhi. — 2003. — Vol. 42, № 2. — P.81—83.
30. Vere, C.C. Endoscopical and histological features in bile reflux gastritis / C.C. Vere, S. Cazacu, V. Comanescu [et al.] // Rom. J. Morphol. Embryol. — 2005. — Vol. 46, № 4. — P269—274.
31. Li, X.B. Role of bile reflux and Helicobacter pylori infection on inflammation of gastric remnant after distal gastrectomy / X.B. Li, H. Lu, H.M. Chen [et al.] // J. Dig. Dis. — 2008. — Vol. 9, № 4 — P.208—212.
32. Sjovall, H. Meaningful or redundant complexity — mechanisms behind cyclic changes in gastroduodenal pH in the fasting state / H. Sjovall // Acta Physiol (Oxf). — 2011. — Vol. 201, № 1. — P127—131.
33. Zullo, A. Gastric Pathology in Cholecystectomy Patients: Role of Helicobacter pylori and Bile Reflux / A. Zullo, V. Rinaldi, C. Hassan [et al.] // Journal of Clinical Gastroenterology. — 1998. — Vol. 27, № 4. — P335— 338.
58
ОБЗОРЫ
ВЕСТНИК СОВРЕМЕННОЙ КЛИНИЧЕСКОМ МЕДИЦИНЫ 2015 Том 8, вып. 2
34. Ladas, S.D. Helicobacter pylori may induce bile reflux: link between H. pylori and bile induced injury to gastric epithelium / S.D. Ladas, J. Katsogridakis, H. Malamou [et al.] // Gut. — 1996. — Vol. 38, № 1. — P. 15—18.
35. Fall, K. Risk for Gastric Cancer After Cholecystectomy / K. Fall, W. Ye, O. Nyren // The American Journal of Gastroenterology. — 2007. — Vol. 102, № 6. — P.1180— 1184.
36. Mac Dowall, J.E. Cell proliferation in type C gastritis affecting the intact stomach / J.E. Mac Dowall, P. Willis,
R. Prescott [et al.] // Clin. Pathol. — 2000. — Vol. 53. — P.784—787.
37. Fuchs, K.H. The role of 24-hr gastric pH-monitoring in the interpretation of 24-hr gastric bile monitoring for duodenogastric reflux / K.H. Fuchs, M. Fein, J. Maroske [et al.] // Hepatogastroenterology. — 1999. — Vol. 46, № 25. — P.60—65.
38. Tibbling, G.L. Gastric bile monitoring: an in vivo and in vitro study of Bilitec reliability / G.L. Tibbling, L. Blackadder, T. Franzen, E. Kullman // Scand. J. Gastroenterol. — 2002. — Vol. 37, № 11. — P.1334—1337.
39. Bechi, P. Technical aspects and clinical indications of 24-hour intragastric bile monitoring / P. Bechi, F. Cianchi // Hepatogastroenterology. — 1999. — Vol. 46, № 25. — P.54—59.
40. Sobala, G.M. Bile reflux and intestinal metaplasia in gastric mucosa / G.M. Sobala, H.J. O’Connor, E.P. Dewar [et al.] // J. Clin. Pathol. — 1993. — Vol. 46. — P.235—240.
41. Dixon M.F. Bile reflux gastritis and intestinal metaplasia at the cardia / M.F. Dixon, N.P. Mapstone, P.M. Neville [et al.] // Gut. — 2002. — Vol. 51. — P.351—355.
42. Matsuhisa, T. Relation between bile acid reflux into the stomach and the risk of atrophic gastritis and intestinal metaplasia: a multicenter study of 2283 cases / T. Matsuhisa, T. Arakawa, T. Watanabe [et al.] // Dig. Endosc. — 2013. — Vol. 25, № 5. — P.519—525.
43. Xu, Y. Bile Acids Induce Cdx2 Expression Through the Farnesoid X Receptor in Gastric Epithelial Cells / Y Xu, T. Watanabe, T. Tanigawa [et al.] // J. Clin. Biochem. Nutr. — 2010. — Vol. 46, № 1. — P.81—86.
44. Tatsugami, M. Bile acid promotes intestinal metaplasia and gastric carcinogenesis. / M. Tatsugami, M. Ito, S. Tanaka [et al.] // Cancer Epidemiol Biomarkers Prev. — 2012. — Vol. 21, № 11. — P.2101—2107.
45. Aprea, G. Morpho-functional gastric pre-and post-operative changes in elderly patients undergoing laparoscopic cholecystectomy for gallstone related disease / G. Aprea, A. Canfora, A. Ferronetti [et al.] // BMC Surg. — 2012. — Vol. 12, № 1. — P.5.
46. Kuran, S. Bile reflux index after therapeutic biliary procedures / S. Kuran, E. Parlak, G. Aydog [et al.] // BMC Gastroenterol. — 2008. — Vol. 8. — P.4.
47. Atak, I. The effect of laparoscopic cholecystectomy on the development of alkaline reflux gastritis and intestinal metaplasia / I. Atak, K. Ozdil, M. Yucel [et al.] // Hepatogastroenterology. — 2012. — Vol. 59, № 113. — P.59—61.
48. Chen, T.-F. Comparative evaluation of intragastric bile acids and hepatobiliary scintigraphy in the diagnosis of duodenogastric reflux / T.-F. Chen, P.K. Yadav, R.-J. Wu [et al.] //World J. Gastroenterol. — 2013. — Vol. 19, № 14. — P.2187—2196.
49. Menges, M. Increased acid and bile reflux in Barrett’s oesophagus compared to reflux oesophagitis, and effect of proton pump inhibitor therapy / M. Menges, M. Muller,
M. Zeitz // Am. J. Gastroenterol. — 2001. — Vol. 96. — P.331—337.
50. Chen, H. Rabeprazole combined with hydrotalcite is effective for patients with bile reflux gastritis after
cholecystectomy / H. Chen, X. Li, Z. Ge [et al.] // Can. J. Gastroenterol. — 2010. — Vol. 24, № 3. — P.197—201.
51. Vinter-Jensen, L. A double-blind placebo-controlled trial of omeprazole on characteristics of the migrating motor complex in healthy volunteers / L. Vinter-Jensen,
K. Kraglund, S.A. Pedersen // Aliment. Pharmacol. Ther. — 1989. — Vol. 3, № 6. — P.615—620.
52. Stefaniwsky, A.B. Ursodeoxycholic acid treatment of bile reflux gastritis. / A.B. Stefaniwsky, G.S. Tint, J. Speck [et al.] // Gastroenterology. — 1985. — Vol. 89, № 5. — P.1000—1004.
53. Ozkaya, M. The effect of ursodeoxycholic acid treatment on epidermal growth factor in patients with bile reflux gastritis / M. Ozkaya, A. Erten, I. Sahin [et al.] // Turk. J. Gastroenterol. — 2002. — Vol. 13, № 4. — P.198—202.
54. Thao, T.D. Antibacterial and anti-atrophic effects of a highly soluble, acid stable UDCA formula in Helicobacter pylori-induced gastritis / T.D. Thao, H.C. Ryu, S.H. Yoo [et al.] // Biochem. Pharmacol. — 2008. — Vol. 75, № 11. — P.2135—2146.
55. Kawamura, T. Effect of ursodeoxycholic acid on water immersion restraint stress ulcer of rats / T. Kawamura,
F. Koizumi, A. Ishimori // Nihon Shokakibyo Gakkai Zasshi. — 1989. — Vol. 86, № 10. — P.2373—2378.
56. Kawiorski, W. Current diagnosis of gastroduodenal reflux and biliary gastritis / W. Kawiorski, R.M. Herman, J. Legut-ko // Przegl. Lek. — 2001. — Vol. 58, № 2. — P.90—94.
REFERENCES
1. Pimanov, S.I. Gastrit, ezofagit i yazvennaya bolezn’ [Gastritis, esophagitis and peptic ulcer] / S.I. Pimanov. —
N. Novgorod: Izd-vo NGMA. — 2000. — 380 s.
2. Mihas’kiv, I.N. Rol’ reflyuksa duodenal’nogo soderzhimogo v geneze raka kul’ti zheludka posle rezekcii zheludka [The role of reflux of duodenal contents in the genesis of cancer of the gastric stump after gastrectomy] / I.N. Mihas’kiv // Hirurgiya [Surgery]. — 1980. — № 2. — S.44—51.
3. Vahrushev, Ya.M. Kompleksnoe izuchenie patogene-ticheskih mehanizmov erozivnogo porazheniya zheludka i dvenadcatiperstnoi kishki [Comprehensive study of pathogenetic mechanisms of erosive lesions of the stomach and duodenum] / Ya.M. Vahrushev, E.V. Nikishina // Pocsiiskii gastroenterologicheskii zhurnal [Russian Journal of Gastroenterology]. — 1998. — № 3. —
S.22—29.
4. Sannikov, O.R. Optimizaciya diagnostiki duodeno-gastral’nogo reflyuksa posle holecistektomii [Optimizing the diagnosis of duodenal reflux after cholecystectomy]: avtoref. dis. … kand. med. nauk / O.R. Sannikov. — Perm’, 2007. — 22 s.
5. Babak, O.Ya. Zhelchnyi reflyuks: sovremennye vzglyady na patogenez i lechenie [Bile reflux: current views on the pathogenesis and treatment] / O.Ya. Babak // Suchasna gastroenterologiya [Modern Gastroenterology]. — 2003. — № 1(11). — S.28—30.
6. Aruin, L.I. Morfologicheskaya diagnostika boleznei zheludka i kishechnika [Morphological diagnosis of diseases of the stomach and intestines] / L.I. Aruin,
L. L. Kapuller, V.A. Isakov. — M.: Triada-H, 1998. — 496 s.
7. Goncharik, I.I. Klinicheskaya gastroenterologiya [Clinical Gastroenterology] / I.I. Goncharik. — Minsk: Interpresservis, 2002. — 334 s.
8. Volkov, V.S. Duodenogastral’nyi reflyuks i yazvennaya bolezn’ dvenadcatiperstnoi kishki — rasstavim tochki nad «i» [Duodenal reflux and duodenal ulcer — dot the «i»] / V.S. Volkov, I.Yu. Kolesnikova // Verhnevolzhskii medicinskii zhurnal [Verhnevolzhskiy Medical Journal]. —
2010. — T 8, № 1. — S.26—29.
ВЕСТНИК СОВРЕМЕННОЙ КЛИНИЧЕСКОЙ МЕДИЦИНЫ 2015 Том 8, вып. 2
ОБЗОРЫ
59
9. Kolesnikova, I.Yu. Pochemu ne voznikaet yazva dvenadcatiperstnoi kishki u bol’nyh hronicheskim gastroduodenitom? [Why is not there a duodenal ulcer in patients with chronic gastroduodenitis?] / I.Yu. Kolesnikova, V.S. Volkov, E.K. Lukasheva // Rossiiskie medicinskie vesti [Russian Medical News]. — 2012. — T. XVII., № 3. —
S. 69—72.
10. Kolesnikova, I.Yu. Osobennosti duodenogastral’nogo reflyuksa pri yazvennoi bolezni dvenadcatiperstnoi kishki i ego dinamika posle eradikacii Helicobacter pylori [Features of duodenogastric reflux with duodenal ulcer and its dynamics after Helicobacter pylori eradication] / I.Yu. Kolesnikova, V.S. Volkov, L.A. Lyubskaya // Eksperimental’naya i klinicheskaya gastroenterologiya [Experimental and Clinical Gastroenterology ]. — 2011. — № 5. — S.16—19.
11. Pan’ko, S.V. Znachenie sutochnogo rN-monitorirovaniya v diagnostike reflyuksnoi patologii zheludochno-kishechnogo trakta [Meaning of daily pH monitoring in diagnosing reflux diseases of the gastrointestinal tract] / S.V. Pan’ko,
G.A. Zhurbenko, A.S. Karpickii [i dr.] // Biologicheskie ritmy: materialy Mezhdunar. nauch.-prakt. konf. 11—12 okt. 2012 g. [Biological rhythms: Materials intern. scientific and practical. conference]. — Brest, 2012. — S.147—149.
12. Osipenko, M.F. Podhody k diagnostike i terapii gastrita, associirovannogo s reflyuksom zhelchi [Approaches to diagnosis and treatment of gastritis associated with bile reflux] / M.F. Osipenko, M.A. Livzan // Lechaschii vrach [Treating physician]. — 2012. — № 2. — S.50—53.
13. Bueverov, A.O. Duodenogastroezofageal’nyi reflyuks kak prichina reflyuks-ezofagita [Duodenogastroesophageal reflux as a reason of reflux oesophagitis] / A.O. Bueverov,
T. L. Lapina // Farmateka. — 2006. — № 1. — S.1—5.
14. Zvyaginceva, T.D. Hronicheskaya duodenal’naya neprohodimost’ i principy konservativnoi terapii [Chronic duodenal obstruction and principles of conservative therapy] / T.D. Zvyaginceva, I.I. Shargorod // Novosti mediciny i farmacii. Gastroenterologiya (tematicheskii nomer) [News of medicine and pharmacy. Gastroenterology]. — 2011. — № 367 (gazeta). — URL: http://www.mif-ua.com (data obrascheniya 26.10.2014).
15. Zvyaginceva, T.D. Duodenogastral’nyi reflyuks v praktike vracha-gastroenterologa: ochevidnye opasnosti i skrytaya ugroza [Duodenogastric reflux in practice of Gastroenterologist: obvious dangers and hidden threat] / T.D. Zvyaginceva, A.I. Chernobai // Zdorov’e Ukrainy. — 2012. — № 3. — S.11.
16. Yurchenko, I.N. Duodenogastral’nyi reflyuks pri gastroezofageal’noi reflyuksnoi bolezni [Duodenogastric reflux with gastroesophageal reflux disease] /
I.N. Yurchenko, N.A. Kashirina, N.A. Vlasova // Materialy XVII Rossiiskoi gastronedeli [Materials XVII Russian gastro week] // RZHGGK. — 2011. — № 5, pril. 38. — C.19.
17. Selezneva, E.Ya. Vnutrizheludochnaya rN-metriya v ocenke sekretornyh i motornyh narushenii zheludka [Intragastric pH-metry in the evaluation of secretory and motor disorders of the stomach] / E.Ya. Selezneva // Rossiiskii gastroenterologicheskii zhurnal [Russian Journal of Gastroenterology]. — 1998. — № 4 — S.69—72.
18. Gibadulina, I.O. Vozmozhnosti ul’trazvukovoi ocenki funkcional’nyh rezul’tatov hirurgicheskoi korrekcii duodenogastral’nogo reflyuksa [Ultrasound evaluation of the functional capabilities of the results of surgical correction of duodenogastric reflux] / I.O. Gibadulina, N.V. Gibadulin // SonoAce-Ultrasound. — 2011. — № 22 (med. zhurnal). — URL: http://www.medison.ru/si/
19. Rukovodstvo po ul’trazvukovoi diagnostike zabolevanii pischevoda, zheludka i dvenadcatiperstnoi kishki [Guide to the ultrasound diagnosis of diseases of the esophagus,
stomach and duodenum] / pod red. G.K. Zherlova, S.A. Sokolova. — Novosibirsk: Nauka, 2005. — 208 s.
20. Belousov, S.S. Gastroezofageal’naya reflyuksnaya bolezn’ i duodenogastral’nyi reflyuks [Gastroesophageal reflux disease and duodenogastric reflux] / S.S. Belousov, S.V. Muratov, A.M. Ahmad. — N. Novgorod: Izd-vo Nizhegorodskoi gos. med. akademii, 2005. — 120 s.
21. Lapchenko, E.S. Sostoyanie slizistoi obolochki zheludka u bol’nyh s duodenogastral’nym reflyuksom [Condition of the gastric mucosa in patients with duodeno-gastric reflux] / E.S. Lapchenko, T.M. Preobrazhenskaya,
E.V. Galaeva, I.D. Loranskaya // Eksperimental’naya i klinicheskaya gastroenterologiya [Experimental and Clinical Gastroenterology]. — 2010. — № 9. — S.25— 29.
22. Ivashkin, V.T. Mesto antacidov v sovremennoi terapii yazvennoi bolezni [The place of antacids in modern therapy of peptic ulcer] / V.T. Ivashkin, E.K. Baranskaya,
O. S. Shifrin, E.Yu. Yur’eva // Russkii medicinskii zhurnal. Bolezni organov pischevareniya [Russian Medical Journal. Diseases of the digestive]. — 2002. — T. 4, № 2. — URL: http://www.rmj.ru/
23. Chen, S.L. Effects of bile reflux on gastric mucosal lesions in patients with dyspepsia or chronic gastritis / S.L. Chen,
J.Z. Mo, Z.J. Cao [et al.] // World J. Gastroenterol. — 2005. — Vol. 11, № 18. — P.2834—2847.
24. Abe, H. Influence of bile reflux and Helicobacter pylori infection on gastritis in the remnant gastric mucosa after distal gastrectomy / H. Abe, K. Murakami, S. Satoh [et al.] // J. Gastroenterol. — 2005. — Vol. 40, № 6. —
P. 563—569.
25. Hanninen, M.L. Sensitivity of Helicobacter pylori to different bile salts / M.L. Hanninen // Eur. J. Clin. Microbiol. Infect. Dis. — 1991. — Vol. 10. — P.515—518.
26. Caldwell, M.T.P Helicobacter pylori infection increases following cholecystectomy / M.T.P. Caldwell, M. McDermott, S. Jazrawi [et al.] // Ir. J. Med. Sci. — 1995. — Vol. 164. — P.52—55.
27. Chen, D.F. H. pylori exist in the gallbladder mucosa of patients with chronic cholecystitis / D.F. Chen, L. Hu, P. Yi, D.C. Fang [et al.] // World J. Gastroenterol. — 2007. — Vol. 13, № 10. — P.1608—1611.
28. Bechi, P. Are there alternative methods for measuring «bile» reflux? / P. Bechi, F. Pucciani, F. Baldini [et al.] // Dig. Dis. Sci. — 1993. — Vol. 38, № 7. — P.1297—1306.
29. Lin, J.K. A study of diagnosis of primary biliary reflux gastritis / J.K. Lin, P.J. Hu, C.J. Li [et al.] // Zhonghua Nei Ke Za Zhi. — 2003. — Vol. 42, № 2. — P.81—83.
30. Vere, C.C. Endoscopical and histological features in bile reflux gastritis / C.C. Vere, S. Cazacu, V. Comanescu [et al.] // Rom. J. Morphol. Embryol. — 2005. — Vol. 46, № 4. — P.269—274.
31. Li, X.B. Role of bile reflux and Helicobacter pylori infection on inflammation of gastric remnant after distal gastrectomy / X.B. Li, H. Lu, H.M. Chen [et al.] // J. Dig. Dis. — 2008. — Vol. 9, № 4 — P.208—212.
32. Sjovall, H. Meaningful or redundant complexity — mechanisms behind cyclic changes in gastroduodenal pH in the fasting state / H. Sjovall // Acta Physiol (Oxf). —
2011. — Vol. 201, № 1. — P.127—131.
33. Zullo, A. Gastric Pathology in Cholecystectomy Patients: Role of Helicobacter pylori and Bile Reflux / A. Zullo, V. Rinaldi, C. Hassan [et al.] // Journal of Clinical Gastroenterology. — 1998. — Vol. 27, № 4. — P.335— 338.
34. Ladas, S.D. Helicobacter pylori may induce bile reflux: link between H. pylori and bile induced injury to gastric epithelium / S.D. Ladas, J. Katsogridakis, H. Malamou [et al.] // Gut. — 1996. — Vol. 38, № 1. — P.15—18.
61
ОБЗОРЫ
ВЕСТНИК СОВРЕМЕННОЙ КЛИНИЧЕСКОМ МЕДИЦИНЫ 2015 Том 8, вып. 2
35. Fall, K. Risk for Gastric Cancer After Cholecystectomy / K. Fall, W. Ye, O. Nyren // The American Journal of Gastroenterology. — 2007. — Vol. 102, № 6. — P.1180— 1184.
36. Mac Dowall, J.E. Cell proliferation in type C gastritis affecting the intact stomach / J.E. Mac Dowall, P. Willis,
R. Prescott [et al.] // Clin. Pathol. — 2000. — Vol. 53. — P.784—787.
37. Fuchs, K.H. The role of 24-hr gastric pH-monitoring in the interpretation of 24-hr gastric bile monitoring for duodenogastric reflux / K.H. Fuchs, M. Fein, J. Maroske [et al.] // Hepatogastroenterology. — 1999. — Vol. 46, № 25. — P.60—65.
38. Tibbling, G.L. Gastric bile monitoring: an in vivo and in vitro study of Bilitec reliability / G.L. Tibbling, L. Blackadder, T. Franzen, E. Kullman // Scand. J. Gastroenterol. — 2002. — Vol. 37, № 11. — P.1334—1337.
39. Bechi, P. Technical aspects and clinical indications of 24-hour intragastric bile monitoring / P. Bechi, F. Cianchi // Hepatogastroenterology. — 1999. — Vol. 46, № 25. — P.54—59.
40. Sobala, G.M. Bile reflux and intestinal metaplasia in gastric mucosa / G.M. Sobala, H.J. O’Connor, E.P. Dewar [et al.] // J. Clin. Pathol. — 1993. — Vol. 46. — P.235—240.
41. Dixon M.F. Bile reflux gastritis and intestinal metaplasia at the cardia / M.F. Dixon, N.P. Mapstone, P.M. Neville [et al.] // Gut. — 2002. — Vol. 51. — P.351—355.
42. Matsuhisa, T. Relation between bile acid reflux into the stomach and the risk of atrophic gastritis and intestinal metaplasia: a multicenter study of 2283 cases / T. Matsuhisa, T. Arakawa, T. Watanabe [et al.] // Dig. Endosc. — 2013. — Vol. 25, № 5. — P.519—525.
43. Xu, Y. Bile Acids Induce Cdx2 Expression Through the Farnesoid X Receptor in Gastric Epithelial Cells / Y Xu, T. Watanabe, T. Tanigawa [et al.] // J. Clin. Biochem. Nutr. — 2010. — Vol. 46, № 1. — P.81—86.
44. Tatsugami, M. Bile acid promotes intestinal metaplasia and gastric carcinogenesis. / M. Tatsugami, M. Ito,
S. Tanaka [et al.] // Cancer Epidemiol Biomarkers Prev. —
2012. — Vol. 21, № 11. — P.2101—2107.
45. Aprea, G. Morpho-functional gastric pre-and postoperative changes in elderly patients undergoing laparoscopic cholecystectomy for gallstone related disease / G. Aprea, A. Canfora, A. Ferronetti [et al.] // BMC Surg. — 2012. — Vol. 12, № 1. — P.5.
46. Kuran, S. Bile reflux index after therapeutic biliary procedures / S. Kuran, E. Parlak, G. Aydog [et al.] // BMC Gastroenterol. — 2008. — Vol. 8. — P.4.
47. Atak, I. The effect of laparoscopic cholecystectomy on the development of alkaline reflux gastritis and intestinal metaplasia / I. Atak, K. Ozdil, M. Yucel [et al.] // Hepatogastroenterology. — 2012. — Vol. 59, № 113. — P.59—61.
48. Chen, T.-F. Comparative evaluation of intragastric bile acids and hepatobiliary scintigraphy in the diagnosis of duodenogastric reflux / T.-F. Chen, P.K. Yadav, R.-J. Wu [et al.] //World J. Gastroenterol. — 2013. — Vol. 19, № 14. — P.2187—2196.
49. Menges, M. Increased acid and bile reflux in Barrett’s oesophagus compared to reflux oesophagitis, and effect of proton pump inhibitor therapy / M. Menges, M. Muller,
M. Zeitz // Am. J. Gastroenterol. — 2001. — Vol. 96. — P.331—337.
50. Chen, H. Rabeprazole combined with hydrotalcite is effective for patients with bile reflux gastritis after cholecystectomy / H. Chen, X. Li, Z. Ge [et al.] // Can.
J. Gastroenterol. — 2010. — Vol. 24, № 3. — P.197— 201.
51. Vinter-Jensen, L. A double-blind placebo-controlled trial of omeprazole on characteristics of the migrating motor complex in healthy volunteers / L. Vinter-Jensen,
K. Kraglund, S.A. Pedersen // Aliment. Pharmacol. Ther. — 1989. — Vol. 3, № 6. — P.615—620.
52. Stefaniwsky, A.B. Ursodeoxycholic acid treatment of bile reflux gastritis. / A.B. Stefaniwsky, G.S. Tint, J. Speck [et al.] // Gastroenterology. — 1985. — Vol. 89, № 5. — P.1000—1004.
53. Ozkaya, M. The effect of ursodeoxycholic acid treatment on epidermal growth factor in patients with bile reflux gastritis / M. Ozkaya, A. Erten, I. Sahin [et al.] // Turk. J. Gastroenterol. — 2002. — Vol. 13, № 4. — P.198—202.
54. Thao, T.D. Antibacterial and anti-atrophic effects of a highly soluble, acid stable UDCA formula in Helicobacter pylori-induced gastritis / T.D. Thao, H.C. Ryu, S.H. Yoo [et al.] // Biochem. Pharmacol. — 2008. — Vol. 75, № 11. — P.2135—2146.
55. Kawamura, T. Effect of ursodeoxycholic acid on water immersion restraint stress ulcer of rats / T. Kawamura, F. Koizumi, A. Ishimori // Nihon Shokakibyo Gakkai Zasshi. — 1989. — Vol. 86, № 10. — P.2373— 2378.
56. Kawiorski, W. Current diagnosis of gastroduodenal reflux and biliary gastritis / W. Kawiorski, R.M. Herman, J. Legutko // Przegl. Lek. — 2001. — Vol. 58, № 2. — P.90—94.
© В.Д. Менделевич, 2015 УДК 613.84(048.8)
ПОЛЬЗА И ВРЕД ЭЛЕКТРОННЫХ СИГАРЕТ СКВОЗЬ ПРИЗМУ
разных терапевтических методологий
ВЛАДИМИР ДАВЫДОВИЧ МЕНДЕЛЕВИЧ, докт. мед. наук, профессор, зав. кафедрой медицинской и общей психологии ГБОУ ВПО «Казанский государственный медицинский университет» Минздрава России,
Казань, Россия, тел. +7-843-238-60-74, e-mail: [email protected]
Реферат. Цель исследования. В статье приводится аналитический обзор современных исследований по оценке пользы и вреда использования электронных сигарет (ЭС) при никотиновой зависимости. Материал и методы. Изучены результаты исследования нескольких десятков работ, выполненных в дизайне доказательных исследований. Результаты и их обсуждение. Делается вывод о том, что оценка эффективности зависит от того, какой терапевтической парадигмы придерживается исследователь — стратегии «нулевой толерантности» или «снижения вреда». В первом случае позитивное влияние оценивается исключительно на основании полного отказа от курения (как обычных, так и электронных сигарет), во втором — используются критерии уменьшения вредных последствий курения. Обращается внимание на то, что медики имеют отношения с реальными пациентами, значительная часть которых не желает бросать курить и будет продолжать курить, несмотря на очевидные риски
ВЕСТНИК СОВРЕМЕННОЙ КЛИНИЧЕСКОЙ МЕДИЦИНЫ 2015 Том 8, вып. 2
ОБЗОРЫ
61
Дуодено-гастральный рефлюкс: причины, лечение, прогноз
Дуодено-гастральным рефлюксом, то есть забросом содержимого двенадцатиперстной кишки в желудок, страдает, по меньшей мере, половина гастроэнтерологических больных. Редко эта патология носит изолированный характер; чаще она возникает на фоне прочих нарушений работы ЖКТ или становится причиной этих нарушений.
Почему возникают проблемы?
Дуодено-гастральный рефлюкс может развиваться по причине:
- анатомических особенностей двенадцатиперстной кишки;
- хронического нарушения дуоденальной проходимости на фоне рубцовых изменений связочного аппарата, спаек в зоне тонкого кишечника;
- хирургического удаления привратника;
- функциональной несостоятельности пилорического сфинктера;
- расстройства моторики ЖКТ, в частности, нарушения координации между желудком и двенадцатиперстной кишкой.
Все это приводит к тому, что пищевой комок или желчь поступает из тонкого кишечника в желудок, откуда может забрасываться и в вышерасположенные отделы – пищевод, глотку. Кислоты, входящие в состав желчи, повреждают слизистую оболочку желудка и пищевода. Это сопровождается развитием гастрита и эзофагита. Очень часто у пациентов с дуодено-гастральным рефлюксом диагностируются:
- функциональная диспепсия;
- рефлюкс-гастрит;
- гастрит с пониженной кислотностью;
- язвенная болезнь желудка;
- пищевод Баррета.
Хроническое повреждение слизистой запускает процесс ее метаплазии, то есть перерождения. На поврежденных участках образуются нетипичные для этой зоны клетки. В тяжелых случаях это приводит к развитию плоскоклеточного рака пищевода.
Повреждение слизистой глотки может сопровождаться катаральным фарингитом и пароксизмальным ларингоспазмом. Нередки также жалобы пациентов на боли в области грудной клетки (проекции сердца), кашель, поражение органов дыхания. Их появление может быть вызвано раздражением ветвей блуждающего нерва.
Каким должно быть лечение?
Лечение дуодено-гастрального рефлюкса начинается с консервативных мероприятий: диеты и медикаментозной терапии. В том случае, если эти меры не позволяют достичь желаемого результата, симптоматика сохраняется, а болезнь прогрессирует, выполняется хирургическое вмешательство. Основная цель операции – укрепить пилорический сфинктер, то есть создать механическое препятствие для заброса дуоденального содержимого в желудок, и устранить имеющиеся препятствия для продвижения пищевого комка и желчи.
В настоящее время ведущие хирурги страны – в частности, Константин Пучков – проводят хирургическое лечение этой патологии методом лапароскопии. После такой операции на брюшной стенке пациента остается несколько незаметных рубцов, а восстановительный период протекает очень быстро.
В первый день после операции они начинают пить, на второй принимают жидкую пищу. Уже на вторые-третьи сутки большинство пациентов выписывается из стационара. К работе они могут приступить уже через две-три недели после операции. В течение полугода им рекомендуется соблюдение мягкой диеты, в дальнейшем пациент возвращается к привычному рациону и не нуждается в приеме лекарственных средств.
Примечательно, что сегодня в рамках одного хирургического вмешательства можно провести хирургическое лечение нескольких заболеваний. Такой подход позволяет полностью наладить работу желудочно-кишечного тракта с минимальными временными затратами и ущербом для здоровья пациента.
Желудочно-пищеводный рефлюкс: причины, симптомы, лечение
Желудочно-пищеводным рефлюксом называют патологический обратный заброс части содержимого желудка в вышележащий отдел пищеварительной системы – пищевод. Это состояние, имеющее также название гастроэзофагеального рефлюкса, в норме почти не наблюдающееся у здоровых людей, часто служит фоном для воспалительно-дистрофических процессов пищевода и дыхательных путей.
Желудочное содержимое (химус с соком желудка) на всех этапах пищеварения отличается высокой кислотностью (рН 1-4) из-за присутствия соляной кислоты. При его попадании в пищевод (желудочно-пищеводный рефлюкс), в просвете которого чаще бывает нейтральная реакция, наблюдается повреждение слизистой оболочки в виде покраснений (гиперемий), эрозий. При вовлечении глублежащих отделов пищевода, а также при длительном воздействии агрессивного фактора, в ряде случаев, могут образовываться язвы пищевода и даже наблюдаться опухолевая трансформация (развитие рака пищевода).
Причины желудочно-пищеводного рефлюкса
Причиной дуоденогастрального рефлюкса может стать дисбаланс в работе желудочно-пищеводного сфинктера (гладкой мышцы, не дающей в норме содержимому желудка попадать в пищевод), нарушение нервной регуляции указанного мышечного образования вследствие заболеваний желудка, других смежных органов, сбой в вегетативной иннервации. К желудочно-пищеводному рефлюксу нередко приводит хронический гастрит, воспаление 12-перстной кишки, опухолевые процессы в кардиальной части пищевода, желудка, язвенная болезнь различных локализаций.
Работа, связанная с длительным и регулярным подъёмом тяжестей, может способствовать повышению внутрибрюшного давления и сформировать пищеводную грыжу диафрагмы (растяжение диафрагмального отверстия), а это, в свою очередь, может привести к дуоденогастральному рефлюксу.
С возрастом происходит ослабление всей мышечной системы, сфинктеров, в том числе и желудочно-пищеводного. Поэтому дуоденогастральный рефлюкс у пожилых людей – нередкое явление, особенно на фоне регулярного переедания, сахарного диабета, гипотиреоза и ожирения.
Патология других отделов пищеварительной системы может отражаться на течении заболевания и вызывать желудочно-пищеводный рефлюкс. Например, хронический панкреатит с явлениями метеоризма (вздутие живота), колит с хроническими запорами, повышают внутрибрюшное давление и способствуют прогрессированию заброса в пищевод содержимого желудка.
Хронические запоры, хронический гипомоторный колит, долихосигма, замедление транзита содержимого толстой кишки может способствовать рефлюксу при наличии других факторов. Запоры вызывают повышение давления в брюшной полости, что при длительном анамнезе заболевания, особенно в сочетании с избыточным весом, способствует забросу кислого содержимого из зоны желудка в пищевод.
Постоянное ношение тяжестей, выраженные силовые нагрузки с вовлечением брюшного пресса способны потенциировать патологические процессы, приводящие к рефлюксу.
Симптомы желудочно-пищеводного рефлюкса
Желудочно-пищеводный (дуоденогастральный) рефлюкс проявляется ощущением изжоги, или мучительного жжения по ходу всего пищевода, в области грудины, тошнотой, снижением аппетита, периодически кислой рвотой. Иногда наблюдается отрыжка горьким (при сопутствующем дуодено-гастральном рефлюксе). Беспокоит тяжесть в подложечной (эпигастральной) зоне, боль после еды, часто натощак. Со временем болевые симптомы могут становиться постоянными. Больные для облегчения дискомфорта вынуждены часто принимать антациды (альмагель, фосфалюгель), соду.
При длительном течении рефлюкса и остром (или хроническом) раздражении эпителиальной ткани пищевода развивается эзофагит (воспалительный процесс в пищеводе), иногда формируются язвы. Пищеводная язва характеризуется постоянным болевым синдромом, более длительным, чем при эрозиях.
Заброс кислоты в просвет пищевода, а также полость рта ночью во время сна, может приводить к раздражению гортани и даже трахеи. Постоянное воздействие кислоты способствует хроническим процессам в лёгких (бронхит, астма, ларингит). Аспирация, особенно у ослабленных больных, может привести к пневмонии.
Для диагностики дуоденогастрального рефлюкса чаще используется метод эндоскопии (ЭФГДС), позволяющий в деталях рассмотреть все дефекты слизистой, взять биопсию подозрительного участка.
Принципы лечения гастродуоденального рефлюкса
Больным, страдающим пищеводным рефлюксом, назначают строгое соблюдение рациона питания, с исключением кофе, какао, жареной, богатой экстрактивными веществами и специями, жирной пищи, газированных напитков, алкоголя, концентрированных соков, кислых блюд.
Особенности образа жизни, неблагоприятно сказывающиеся на течении рефлюкса желательно модифицировать. Рациональным советом для уменьшения выраженности дуоденогастрального рефлюкса может стать снижение лишнего веса, борьба с гиподинамией, запорами.
Не рекомендуется принимать горизонтальное положение сразу после еды (3-4 часа не ложиться), поднимать тяжести, использовать тугие пояса, спать советуют с приподнятым изголовьем.
Для купирования воспаления применяют антисекреторные средства и антациды, по назначению врача проводят противоязвенное лечение. В ряде случаев, для уменьшения степени заброса из желудка применяют прокинетические лекарственные средства.
При появлении симптомов рефлюкса и изжоги самостоятельный приём лекарств часто оказывается неэффективным, так как успех терапии зависит от своевременности постановки точного диагноза и лечения собственно болезни, а не только его симптомов. Также за симптомами изжоги и боли за грудиной могут скрываться многие заболевания, не имеющие прямого отношения к пищеводу (например, болезни сердца, лёгких).
Бесплатные консультации врачей онлайн
Вопрос создается. Пожалуйста, подождите…
Только зарегистрированные пользователи могу задавать вопрос.
Зарегистрируйтесь на портале, задавайте вопросы и получайте ответы от квалифицированных специалистов!
Напоминаем, что стоимость публикации вопроса — 10 бонусов.
Зарегистрироваться Как получить бонусы
К сожалению, у вас недостаточно бонусов для оплаты вопроса.
Напоминаем, что стоимость публикации вопроса — 10 бонусов.
Как получить бонусы
Раздел медицины*: — Не указано —КоронавирусАкушерствоАллергология, иммунологияАнестезиологияВенерологияВертебрологияВетеринарияГастроэнтерологияГематологияГепатологияГериатрияГинекологияГирудотерапияГомеопатияДерматологияДиетологияИглотерапия и РефлексотерапияИнфекционные и паразитарные болезниКардиологияКардиохирургияКосметологияЛабораторная и функциональная диагностикаЛечение травмЛогопедияМаммологияМануальная терапияМРТ, КТ диагностикаНаркологияНеврологияНейрохирургияНетрадиционные методы леченияНефрологияОбщая хирургияОнкологияОстеопатияОториноларингологияОфтальмологияПедиатрияПлазмаферезПластическая хирургияПодологияПроктологияПсихиатрияПсихологияПсихотерапияПульмонология, фтизиатрияРадиология и лучевая терапияРеабилитологияРеаниматология и интенсивная терапияРевматологияРепродукция и генетикаСексологияСомнологияСпортивная медицинаСтоматологияСурдологияТерапияТравматология и ортопедияТрансфузиологияТрихологияУЗИУльтразвуковая диагностикаУрология и андрологияФармакологияФизиотерапияФлебологияЧелюстно-лицевая хирургияЭндокринологияЗатрудняюсь выбрать (будет выбрана терапия)
Кому адресован вопросВопрос адресован: ВсемКонсультантам
Консультант, которому задается вопрос: Всем…Агабекян Нонна Вачагановна (Акушер, Гинеколог)Айзикович Борис Леонидович (Педиатр)Акмалов Эдуард Альбертович (Аллерголог, Врач спортивной медицины)Александров Павел Андреевич (Венеролог, Гепатолог, Инфекционист, Паразитолог, Эпидемиолог)Александрова Анна Михайловна (Педагог, Психолог, Психотерапевт)Али Мохамед Гамал Эльдин Мансур (Педиатр)Аристова Анастасия Михайловна (Андролог, Уролог, Хирург)Армашов Вадим Петрович (Хирург)Афанасьева Дарья Львовна (Кардиолог, Терапевт)Беляева Елена Александровна (Гинеколог, Невролог, Рефлексотерапевт)Бушаева Ольга Владимировна (Пульмонолог, Терапевт)Врублевская Елена (Педиатр)Гензе Ольга Владимировна (Генетик, Педиатр)Горохова Юлия Игоревна (Венеролог, Врач общей практики, Дерматолог)Григорьева Алла Сергеевна (Врач общей практики, Терапевт)Демидова Елена Леонидовна (Психолог, Психотерапевт)Денищук Иван Сергеевич (Андролог, Уролог)Дибиров Магомед Гусейнович (Стоматолог)Димина Тамара Олеговна (Акушер, Аллерголог, Ангиохирург)Довгаль Анастасия Юрьевна (Маммолог, Онколог, Радиолог)Долгова Юлия Владимировна (Педиатр)Дьяконова Мария Алексеевна (Гериатр, Терапевт)Жердакова Дарья Владимировна (Акушер, Гинеколог)Загумённая Анна Юрьевна (Врач спортивной медицины, Гирудотерапевт, Диетолог, Косметолог, Терапевт)Зверев Валентин Сергеевич (Ортопед, Травматолог)Згоба Марьяна Игоревна (Окулист (Офтальмолог))Зинченко Вадим Васильевич (Рентгенолог, Хирург)Зорий Евген Владимирович (Невролог, Психолог, Терапевт, Хирург)Извозчикова Нина Владиславовна (Гастроэнтеролог, Дерматолог, Иммунолог, Инфекционист, Пульмонолог)Илона Игоревна (Врач общей практики, Гастроэнтеролог, Терапевт, Эндокринолог)Калявина Светлана Николаевна (Акушер, Гинеколог)Калягина Екатерина (Другая специальность)Карпенко Алик Викторович (Ортопед, Травматолог)Касимов Анар Физули оглы (Онколог, Хирург)Киреев Сергей Александрович (Психиатр, Психолог, Психотерапевт)Кирнос Марина Станиславовна (Стоматолог, Стоматолог детский, Стоматолог-терапевт)Копежанова Гульсум (Акушер, Гинеколог)Кравцов Александр Васильевич (Нарколог, Психиатр)Красильников Андрей Викторович (Врач ультразвуковой диагностики, Медицинский директор, Флеболог, Хирург)Кряжевских Инна Петровна (Терапевт, Гастроэнтеролог)Кудряшова Светлана Петровна (Эндокринолог)Куртанидзе Ираклий Малхазович (Окулист (Офтальмолог))Кущ Елена Владимировна (Диетолог, Терапевт)Лазарева Татьяна Сергеевна (ЛОР (Оториноларинголог))Лаптева Лариса Ивановна (Невролог)Лебединская Татьяна Александровна (Психолог, Психотерапевт)Ледник Максим Леонидович (Венеролог, Дерматолог)Леонова Наталья Николаевна (Детский хирург)Литвиненко Станислав Григорьевич (Ортопед, Травматолог)Лямина Ирина Алексеевна (Акушер)Максименко Татьяна Константиновна (Инфекционист)МАЛЬКОВ РОМАН ЕВГЕНЬЕВИЧ (Диетолог, Остеопат, Реабилитолог)Мамедов Рамис (ЛОР (Оториноларинголог))Мартиросян Яков Ашотович (Детский хирург, Проктолог, Травматолог, Уролог, Хирург)Маряшина Юлия Александровна (Акушер, Венеролог, Врач ультразвуковой диагностики, Гинеколог, Педиатр)Матвеева Ярослава Дмитриевна (Педиатр)Мершед Хасан Имадович (Вертебролог, Нейрохирург)Миллер Ирина Васильевна (Невролог)Мильдзихова АЛЬБИНА Бексолтановна (Врач общей практики, Гинеколог, ЛОР (Оториноларинголог), Педиатр, Терапевт)Муратова Наталья Сергеевна (Врач общей практики, Диетолог)Мухорин Виктор Павлович (Нефролог)Наумов Алексей Алексеевич (Мануальный терапевт)Никитина Анна Алексеевна (Окулист (Офтальмолог))Ольга Викторовна (Невролог, Неонатолог, Педиатр, Реабилитолог, Терапевт)Павлова Мария Игоревна (Стоматолог, Стоматолог-хирург, Челюстно-лицевой хирург)Панигрибко Сергей Леонидович (Венеролог, Дерматолог, Косметолог, Массажист, Миколог)Пантелеева Кристина Алексеевна (Невролог)Пастель Владимир Борисович (Ортопед, Ревматолог, Травматолог, Хирург)Паунок Анатолий Анатольевич (Андролог, Уролог)Першина Наталия Сергеевна (Невролог)Прокофьева Анастасия Михайловна (ЛОР (Оториноларинголог))Прохоров Иван Алексеевич (Нейрохирург, Хирург)Пушкарев Александр Вольдемарович (Гинеколог, Психотерапевт, Реабилитолог, Репродуктолог (ЭКО), Эндокринолог)Пьянцева Екатерина Вячеславна (Педиатр)Радевич Игорь Тадеушевич (Андролог, Венеролог, Сексолог, Уролог)Сапрыкина Ольга Александровна (Невролог)Свечникова Анастасия Евгеньевна (Стоматолог, Стоматолог детский, Стоматолог-ортопед, Стоматолог-терапевт, Стоматолог-хирург)Семений Александр Тимофеевич (Врач общей практики, Реабилитолог, Терапевт)Сергейчик Никита Сергеевич (Анестезиолог, Гомеопат)Силуянова Валерия Викторовна (Акушер, Врач ультразвуковой диагностики, Гинеколог)Соболь Андрей Аркадьевич (Кардиолог, Нарколог, Невролог, Психиатр, Психотерапевт)Сошникова Наталия Владимировна (Эндокринолог)Степанова Татьяна Владимировна (ЛОР (Оториноларинголог))Степашкина Анастасия Сергеевна (Гематолог, Пульмонолог, Терапевт)Сурова Лидия (Гирудотерапевт, Невролог, Терапевт)Суханова Оксана Александровна (Клинический фармаколог, Психолог)Сухих Данил Витальевич (Психиатр)Тумарец Кирилл Михайлович (Врач лечебной физкультуры, Врач спортивной медицины, Кинезитерапевт, Реабилитолог, Физиотерапевт)Турлыбекова Венера Равильевна (Врач общей практики, Педиатр)Устимова Вера Николаевна (Гематолог, Терапевт, Трансфузиолог)Фатеева Анастасия Александровна (Гастроэнтеролог, Диетолог, Психотерапевт, Эндокринолог)Федотова Татьяна Владимировна (Врач ультразвуковой диагностики, Гематолог, Терапевт)Фоминов Олег Эдуардович (Сексолог)Фоминов Олег Эдуардович (Сексолог)Фурманова Елена Александровна (Аллерголог, Иммунолог, Инфекционист, Педиатр)Хасанов Эльзар Халитович (Андролог, Врач ультразвуковой диагностики, Онколог, Уролог, Хирург)Хасанова Гульнара Сунагатулловна (Акушер, Врач ультразвуковой диагностики)Чупанова Аида (Акушер, Гинеколог)Чупанова Аида Идаятовна (Акушер, Гинеколог, Репродуктолог (ЭКО))Швайликова Инна Евненьевна (Окулист (Офтальмолог))Шибанова Мария Александровна (Нефролог, Терапевт)Щепетова Ольга Александровна (Терапевт)Ягудин Денар Лукманович (ЛОР (Оториноларинголог))Ярвела Марианна Юрьевна (Психолог)
Описание проблемы:
Пол: —укажите пол—ЖенщинаМужчина
Возраст:
Рефлюкс-эзофагит I степени, дуодено-гастральный рефлюкс, эритоматозная гастропатия. I need help. | Пацан будь здоров | Do4a.com
Фаренгоф сказал(а): ↑Всем привет.Жила с такой штукой долго.Вот такие страшные слова написали мне в результатах проверки ФГДС (трубка в горло и глотать). + указали что есть 2 линейные циркулярные эрозии в желудке и натощак умеренное кол-во желчи, и повсюду “очаги гиперемии”.
Скажите если кто -то живёт с подобным букетом, поделитесь опытом, историей, возможно наставлением или конкретными пунктами действий от режима, до питания, до возвращения к спорту т.к. мне сказали что мне нельзя даже утром делать зарядку на пресс…
Спасибо друзья.
Нажмите, чтобы раскрыть…
Хеликобактер тут ни при чем. На западе ее вообще полезной считают. По статистике чаще болеют ГЕРБ те, у кого нет хеликобактер. Те у кого есть – в меньшем количестве.
Нужно лечить ГЭРБ и желчный, причем к последнему нужен комплексный медицинский подход – хороший врач, который проведет комплексное лечение.
То что “проходило в течении дней или пары недель” называется гастро дэуденальным приступом – первый признак дэуденита, который провоцируется внезапным, несвоевременным выбросом желчи. После болей в желудке как правило еще и блюют до желчи, а потом отпускает. Лечите желчный. Без него плохо.
Если кратко:
Медикаменты для ГЭРБ – из ИПП : париет, из прокинетиков: итомед, тримедат. Можно гевискон через пол часа после еды поживать ( на 15 минут изжогу суспокаивает при обострениях)
Питание по часам – 5-6 раз в день с перерывом в 2,5 – 3 часа
Еду не запивать (пить за 10 минут до еды, не раньше чем через час после еды)
Потреблять больше белка (нежирная птица, рыба, мясо)
Обязательно сьедать не менее 1 столовой ложки растительного масла с каждой порцией пищи (для работы желчного)
Супы исключить ( если только вы их в блендере не перемалываете)
Кисло-молочку исключить
Продукты вызывающие брожение исключить: дрожжи и продукты с ними, все кисло-молочные продукты, свежие овощи и фрукты, томаты, белокачанную капусту, лук, специи и соусы, орехи, бобовые, соки, сахарные продукты, конфеты и печенье из магазина (если только там не мука и вода, а не +100500 ингредиентов разного гавна), кофе, какао, шоколад
Тертая морковь и сухой вчерашний хлеб неплохо помогают смыть кислоту с пищевода
Спать на кровати с уклоном, оптимально на левом боку
Избегать внутрибрюшного давления ( приседания со штангой, качание пресса, наклоны, узкая одежда, затянутый пояс)
Травку не курить, мышечные релаксанты и спазмолитики не принимать
+ за все советы от zamyslenysh
Через пол года будет существенно лучше. Главное быть настойчивым, последовательным, упорным, пить таблетки и правильно кушать. Поправитесь будете суши трескать.
Дуодено-желудочно-пищеводный рефлюкс – что такое патологический? Сравнение пациентов с пищеводом Барретта и добровольцев того же возраста
Резюме
Введение
Целью исследования был анализ данных мониторинга pH и желчи у пациентов с пищеводом Барретта и в контрольной группе, сопоставимой по возрасту и полу.
Субъекты и методы
Двадцать четыре последовательных пациента Барретта (8 женщин, 16 мужчин, средний возраст 57 лет), 21 пациент с эзофагитом (10 женщин, 11 мужчин, средний возраст 58 лет) и 19 здоровых пациентов контрольной группы (8 женщин). , 11 мужчин, средний возраст 51 год).Только пациентам проводилась эндоскопия с биопсией. Все группы были исследованы с помощью манометрии, 24-часового pH желудка и пищевода и одновременного мониторинга желчи в соответствии со стандартизованным протоколом. Абсорбция билирубина> 0,25 была определена как вредный желчный рефлюкс. Метод характеристики оператора приемника (ROC) был применен для определения оптимального порогового значения уровней патологического билирубина.
Результаты
Из пациентов Барретта у 79% был патологический кислый желудочный рефлюкс (pH <4> 5% от общего времени измерения).Однако у 32% здоровых людей из контрольной группы также был кислотный рефлюкс ( p <0,05) без каких-либо симптомов. Медиана рефлюкса желчи из пищевода составила 7,8% (нижний квартиль (LQ) - верхний квартиль (UQ) = 1,6–17,8%) у пациентов с болезнью Барретта, у пациентов с эзофагитом - 3,5% (LQ – UQ = 0,1–13,5) и контраст с 0% (LQ – UQ = 0–1,0%) в контроле, p = 0,001. ROC-анализ показал оптимальное значение деления для пациентов с рефлюксом желчи более 1% в течение 24 часов (чувствительность 75%, специфичность 84%).
Заключение
Оптимальный порог для различения нормального и патологического рефлюкса желчи в пищевод составляет 1% (24-часовой мониторинг желчи с поглощением> 0.25).
Ключевые слова: Референтное значение bilitec, Рефлюкс желчи, кислотный рефлюкс, слизистая оболочка Барретта, пищевод, спектрофотометрия
Введение
Уровень заболеваемости аденокарциномой (АК) пищевода и кардии желудка в западных промышленно развитых странах быстро вырос1. Помимо никотина и злоупотребления алкоголем, факторы питания, высокий индекс массы тела, кислотный желудочный рефлюкс и пищевод Барретта считаются критическими факторами канцерогенеза.2–4 Недавние исследования показали, что наличие желчного рефлюкса в сочетании с кислотным желудочным рефлюксом повреждает слизистой пищевода и вызывает осложнения гастроэзофагеальной рефлюксной болезни (ГЭРБ), e.g., развитие слизистой оболочки Барретта (BM) .5,6 Дуодено-желудочный рефлюкс в пищевод (DGER), в частности, по-видимому, важен для патогенеза пищевода Барретта (7). пациенты с тяжелым эзофагитом и пищеводом Барретта.8 Восемьдесят процентов пациентов с пищеводом Барретта, принимающих ингибиторы протонной помпы, демонстрируют нормальный профиль pH пищевода, но 60% демонстрируют ненормальное воздействие желчи через пищевод по данным Bilitec 2000.9
В прошлом прямое и продолжительное количественное определение дуоденоэзофагеального рефлюкса было труднодостижимым. Теперь концентрацию билирубина можно напрямую измерить спектрофотометрией на основе удельного поглощения на длине волны 453 нм. Билиарный рефлюкс можно измерить с помощью амбулаторного фиброоптического зонда, проходящего через нос (Bilitec 2000), который регистрирует всасывание желчи. Уже опубликован ряд работ по обнажению пищевода10–13 и желудка24–16 с использованием этой техники.Однако в этих исследованиях возраст контрольной группы составлял от 25 до 35 лет. В клинической практике пациенты со слизистой оболочкой Барретта обычно старше. Кроме того, авторы каждого исследования использовали различные контрольные значения для измерения билиарного рефлюкса в пищеводе, что затрудняло сравнение измеренных значений.
Целью настоящего исследования был анализ данных мониторинга pH и желчи в группе здоровых лиц из контрольной группы, соответствующих возрасту и полу, и пациентов с пищеводом Барретта.
Субъекты и методы
Субъекты
Отбор контролей проводился в соответствии со строгим протоколом. В исследование были включены здоровые добровольцы, лечившиеся с 1999 по 2000 год, в возрасте от 40 до 60 лет. Никто из контрольных не принимал препараты, подавляющие кислоту или перистальтику кишечника, не имел в анамнезе заболеваний верхних отделов желудочно-кишечного тракта, не подвергался хирургическим вмешательствам на верхних отделах брюшной полости или обширным операциям на брюшной полости, а также не подвергался терапевтическим эндоскопическим процедурам верхних отделов желудочно-кишечного тракта.Диагностическая эндоскопия и проглатывание бария не проводились, но желчнокаменная болезнь была исключена на УЗИ.
С 1999 по 2002 год в исследование были включены 24 пациента с гистологически подтвержденной слизистой оболочкой Барретта. Для дополнительного сравнения мы включили группу пациентов с эзофагитом (стадия I – III по Савари и Миллеру) без пищевода Барретта, которым перед плановой лапароскопической фундопликацией были выполнены те же диагностические процедуры. В течение вышеупомянутого периода для этого исследования был доступен 21 пациент в возрасте старше 40 лет.Критериями исключения были хирургия пищевода, желудка или желчевыводящих путей в анамнезе, лучевая терапия брюшной или грудной клетки в анамнезе или наличие язвенной болезни, активное желудочно-кишечное кровотечение, варикозное расширение вен пищевода или дна, хроническое заболевание пищевода или верхних отделов тонкой кишки или опухолевые заболевания. Все препараты, потенциально влияющие на перистальтику желудочно-кишечного тракта и секрецию, были отменены по крайней мере за 1 неделю до исследования.
Эндоскопия верхних отделов желудочно-кишечного тракта
Всем пациентам была выполнена классическая эндоскопия верхних отделов желудочно-кишечного тракта.Если была необходима седация, обычно применяли внутривенное введение пропофола (до 200 мг) или изредка применяли мидазолам (до 5 мг). Во время эндоскопии было отмечено наличие и степень эзофагита, пищевода Барретта и грыжи пищеводного отверстия диафрагмы. Биопсии были взяты со слизистой оболочки Барретта.
Амбулаторный мониторинг pH пищевода / желудка и желчи
Все группы прошли манометрию пищевода и 24-часовой мониторинг pH и одновременный мониторинг желчи с использованием стандартизованного протокола.Амбулаторный мониторинг pH выполнялся с использованием трансназально введенного сурьмяного pH-электрода с отдельным кожным электродом сравнения (Synetics Medical, Стокгольм, Швеция). Данные сохранялись на портативном цифровом записывающем устройстве (Digitrapper MkIII, Synectics Medical Stockholm, Швеция). Перед каждым исследованием зонд pH калибровали в буферных растворах с pH 7 и 1. Эпизод кислотного рефлюкса определялся как снижение pH пищевода до менее 4 в течение более 10 с.
Для количественной оценки дуодено-пищеводного рефлюкса использовался амбулаторный фиброоптический спектрофотометр, переданный через нос (Bilitec 2000, Synectics, Швеция).Система состоит из миниатюрного зонда диаметром 1,5 мм, который передает световые сигналы в пищевод и обратно через пластиковую волоконно-оптическую связку. Перед каждым исследованием зонд калибровали в воде. В соответствии с текущей литературой, абсорбция билирубина> 0,25 использовалась в качестве эталона для вредного билиарного рефлюкса.14
Зонды желчи и pH были скреплены вместе и прошли трансназально в пищевод и желудок, как подробно описано в другом месте.17 Верхняя часть кончики зондов были расположены на 5 см выше верхней границы нижнего сфинктера пищевода, как определено манометрией пищевода.Дистальный pH-электрод и оптоволоконный датчик помещали на дно желудка на 10 см дистальнее нижнего сфинктера пищевода (рис.). Контрольной группы и пациентов просили следовать строгому протоколу трехразового питания без жидкости между приемами пищи. Лежачие фазы записи разрешались только ночью. Пациентов просили вести дневник, фиксируя точный характер приема пищи, фазы измерения в положении лежа на спине и прямо, а также ощущения изжоги и срыгивания.
Расположение датчиков pH и билирубина в желудке и пищеводе.(UES = верхний сфинктер пищевода; LES = нижний сфинктер пищевода).
Одновременный мониторинг желчных протоков и pH проводился с применением бесцветной «белой диеты» (WD), включающей жидкую и твердую пищу с максимальным поглощением желчи in vitro 0,25 [шкала поглощения от 0 (обычная вода) до 1 (общая экран)]. Еда включала воду, молоко, тосты, картофель, курицу, сухое печенье и рыбу.
Сбор и интерпретация данных
После завершения измерений зонды у пациентов извлекались, и данные сохранялись через интерфейс на IBM-совместимом компьютере, оснащенном программным обеспечением Polygram® (Medtronic).Для анализа использовались данные каждой секунды 24-часовых измерений. Чтобы оценить наличие желудочного или пищеводного билиарного рефлюкса, был рассчитан процент времени, когда абсорбция была больше 0,25 для следующих периодов: всего в положении лежа на спине, в вертикальном положении и после приема пищи. Постпрандиальный период определялся как 2 ч после окончания приема пищи. Процент времени с pH пищевода ниже 4 и медианным pH желудка и процент времени с pH желудка, измеряющим 1, 2, 3–7 и> 7, также был рассчитан для вышеуказанных периодов.Средняя продолжительность амбулаторного мониторингового исследования pH и Bilitec составляла 22 часа 40 минут у пациентов и 23 часа 44 минуты в контрольной группе.
Статистический анализ
Для анализа результатов использовалась программа SPSS (версия 11.0, Чикаго, Иллинойс). Для графического представления использовалась программа MedCalc для Windows (версия 9.0, MedCalc Software, Бельгия). Были установлены медианы, значения межквартильного размаха (IQR или 25–75 перцентиль). Непараметрические тесты (анализ Манна – Уитни и Краскела – Уоллиса) использовались для оценки взаимосвязи между переменными.Для представления некоторых данных использовались графики Box и Whisker. На этих графиках прямоугольник представляет IQR, а усы – самые высокие и самые низкие значения. Также нанесены выбросы, определенные как более чем в 1,5 раза превышающие IQR от 75-го центиля. Экстремальные значения были определены как более чем трехкратный IQR от 75-го центиля.
Кривая характеристики оператора приемника (ROC) использовалась для определения порогового значения для оптимальной чувствительности и специфичности согласно Цвейгу и Кэмпбеллу18. Площадь под кривой (AUC) использовалась как измерение диагностической эффективности теста.Результаты представлены в виде точек с доверительным интервалом 95% (95% ДИ) и графически для представления всех данных. В качестве положительной группы мы использовали пациентов со слизистой оболочкой Барретта, а отрицательную тестовую группу определяли здоровыми добровольцами. Предполагалось непараметрическое распределение площади под кривой.
Предположения для расчета требуемого размера выборки были альфа = 0,05, бета = 0,80, и что тест действителен для ежедневного использования только в том случае, если менее 20% здоровых контролей и не менее 80% пациентов имеют положительный результат теста. полученные результаты.Расчетный размер выборки для каждой группы составил 20.
Этика
Протокол исследования был одобрен этическим комитетом Кельнского университета. Каждый субъект дал письменное информированное согласие.
Результаты
В исследование были включены 24 пациента с пищеводом Барретта (средний возраст: 58 лет), 21 пациент с эзофагитом (средний возраст: 57 лет) и 19 здоровых людей контрольной группы со средним возрастом 51 год. У пациентов с БМ выявлен эзофагит 0 степени (4 случая), I степени (12 случаев) и II степени (8 случаев).В контрольной группе пациентов с эзофагитом было девять случаев с I степенью, восемь случаев со II степенью и три случая с III степенью. Демографические данные пациентов и добровольцев представлены в таблице (данные одного добровольца не были использованы из-за технических проблем).
Таблица 1
Демографические данные пациентов с слизистой оболочкой Барретта или эзофагитом и здоровых добровольцев
| Параметры | Пациенты с пищеводом Барретта ( n = 24) | Пациенты с эзофагитом ( n = 21) | Контроли ( n = 19) | Значение Пат.с Barrett vs Controls |
|---|---|---|---|---|
| Возраст (средний) | 57 лет | 58 лет | 51 год | – |
| Мин. 39–62 года | ||||
| Пол м: ж | 16: 8 | 11:10 | 11: 8 | нс |
| ИМТ (медиана) мин – макс | 27,0 кг / м 2 (18,6–33,1) | 26.9 кг / м 2 (17,9–31,5) | 24,1 кг / м 2 (19,62–27,34) | p = 0,003 |
| Курильщики (%) | n = 5 (20,8 ) | n = 4 (19,0) | n = 6 (31,6) | нс |
| Без спирта% | n = 3 (12,5) | n = 5 (23,8) | n = 5 (26,3) | n.s. |
Кислый желудочный рефлюкс (AGR)
Пациенты с пищеводом Барретта, 19 из 24 (79%) и 20 из 21 контрольных пациентов с эзофагитом (95%) имели патологические AGR [pH <4 в> 5% от общего числа измерения времени (TMT)], но также у 6 из 19 здоровых контролей (32%) наблюдались патологические AGR без каких-либо симптомов ( p = 0.002). Во время TMT средний AGR составил 10,6% для пациентов Barrett и 3,2% для контрольной группы ( p <0,01). В частности, измерения длительного кислотного рефлюкса (LAR), определяемого как pH рефлюкса <4, длящегося более 5 минут, показали значительные различия между пациентами и контрольной группой. Патологический AGR был обнаружен у пациентов в период измерения натощак как в положении лежа на спине, так и в вертикальном положении. Напротив, патологические AGR у здоровых людей наблюдались только в вертикальном положении (таблица).
Таблица 2
Медиана кислотного желудочного рефлюкса в пищевод у пациентов с BM или с эзофагитом и в здоровой контрольной группе
| Параметры | Пациенты с пищеводом Барретта ( n = 24) [медиана (LQ-UQ )] | Пациенты с эзофагитом ( n = 21) [медиана (LQ-UQ)] | Контрольная группа ( n = 19) [медиана (LQ-UQ)] | Значение Пат.с Barrett vs Controls |
|---|---|---|---|---|
| Процент от общего времени измерения pH <4 (%) | 10,6 (6,2–38,3) | 19,9 (1,6–71,7) | 3,2 (0,9–5,5) | p = 0,01 |
| Процент времени измерения в вертикальном положении pH <4 (%) | 11,7 (6,03–6,4) | 18,9 (8,7–60,8) | 2,4 (0,9–6,1) | p <0,05 |
| Процент времени измерения в положении лежа на спине pH <4 (%) | 10.9 (0,4–27,1) | 6,3 (0,0–13,3) | 0,3 (0,0–4,2) | p = 0,004 |
24-часовой мониторинг внутрижелудочного pH и желчи
Мониторинг pH желудка не показал значимых различия между пациентами и контрольной группой для всех периодов измерения (таблица). Воздействие желудочного билирубина, указывающее на билиарный рефлюкс, было значительно более частым у пациентов, чем в контрольной группе, в течение всех периодов измерения (таблица). Воздействие желчных путей в положении лежа на спине обычно происходило в ранние утренние часы во время сна, что выражалось увеличением абсорбции в течение 2–3 часов с быстрым возвращением к исходным значениям примерно в то время, когда субъект снова возвращался в вертикальное положение.За тот же период времени мониторинг pH желудка показал повышение уровня pH до более чем 2 (рис.).
Таблица 3
Результаты 24-часового внутрижелудочного мониторинга pH и желчи у пациентов с пищеводом Барретта и здоровой контрольной группы
| Параметры | Пациенты ( n = 24) [медиана (LQ – UQ)] | Контроли ( n = 19) [Медиана (LQ – UQ)] | Значимость |
|---|---|---|---|
| Медиана внутрижелудочного pH во время TMT | 1.3 (1,0–1,4) | 1,4 (1,1–1,7) | н.с. |
| Процент воздействия билирубина (%) TMT | 7,8 (1,6–17,8) | 0,0 (0,0–1,0) | p = 0,001 |
| Процент воздействия билирубина (%) в прямом эфире | 6,9 (0,1–12,9) | 0,0 (0,0–1,3) | p <0,01 |
| Процент воздействия билирубина (%) во время пребывания на спине | 2,0 (0,0–28,6) | 0.0 (0,0–0,0) | p = 0,001 |
24-часовой внутрижелудочный мониторинг pH и желчи у пациента с пищеводом Барретта, демонстрирующего дуоденогастральный рефлюкс ранним утром. а. Bilitec®-мониторинг, б. pH-мониторинг.
Воздействие билирубина на пищевод
По результатам TMT медиана желчного рефлюкса пищевода составила 7,8% для пациентов с пищеводом Барретта (LQ – UQ = 1,6–17,8%) и 3,5 (LQ – UQ = 0,1–13,5) для контроля пациентов, в отличие от 0% для контроля (LQ – UQ = 0–1.0%), р = 0,001). На рисунке показано, что мониторинг желчи пищевода у пациентов с пищеводом Барретта и здоровых людей в контрольной группе варьировался в течение всего периода измерения и периода лежа на спине.
Результаты мониторинга желчи в пищеводе у 24 пациентов с пищеводом Барретта, 21 пациента с эзофагитом и 19 здоровых людей из контрольной группы а) общий период измерения (тест Краскела-Уоллиса = 0,01) б) период лежа на спине (тест Краскала-Уоллиса p = 0,01) .
Рабочая кривая приемника, отображающая процент истинных положительных результатов (пациенты с пищеводом Барретта, идентифицированные по воздействию билирубина) в зависимости от частоты ложных срабатываний (здоровые контроли с высоким уровнем воздействия билирубина), показана на рис.. С площадью под кривой 0,78 (95% ДИ = 0,56–0,89) ROC-анализ мониторинга желчевыводящих путей показал оптимальное значение для пациентов при 1% TMT [чувствительность 75% (95% ДИ = 53–90%). , Специфичность 84% (95% ДИ = 60–96%)]. Следовательно, пороговое значение для различения нормального и патологического билиарного рефлюкса с использованием 24-часового мониторинга желчевыводящих путей в пищеводе (порог поглощения> 0,25) должно быть зафиксировано на уровне 1% от TMT.
ROC-кривая с 95% доверительным интервалом для патологического мониторинга желчи у пациентов с пищеводом Барретта по сравнению со здоровыми контрольными пациентами, соответствующими возрасту и полу.
пациентов Барретта, 18 из 24 (75%), 15 из 21 контрольного пациента с эзофагитом (71%) и 3 из 19 контрольных (16%) показали билирийный рефлюкс в пищевод более 1,1% TMT ( p <0,001). Используя это пороговое значение, ни у одного из контрольных пациентов, у 10 из контрольных пациентов (48%) и у 11 из 24 пациентов с болезнью Барретта (46%) не было патологического воздействия билирубина во время сна.
Обсуждение
Результаты нашего исследования подтверждают, что пациенты с пищеводом Барретта имеют значительно более частый дуоденогастральный рефлюкс в пищевод, чем здоровые люди из контрольной группы того же возраста и пола.Кроме того, этот рефлюкс, измеряемый воздействием кислоты и билирубина, дольше остается в пищеводе, особенно во время сна.
Роль кислотного и некислотного рефлюкса в пищевод как причинного фактора симптомов и поражений слизистой оболочки рассматривалась в ряде исследований. Не только продолжительность, но, возможно, и состав рефлюкса, играет важную роль в развитии таких поражений.13 Круглосуточный внутрижелудочный мониторинг желчи предоставил клиницисту однозначные доказательства чрезмерного дуоденогастрального рефлюкса (DGR) у 41% пациентов. с эндоскопическим эзофагитом, симптомами гастроэзофагеального рефлюкса (ГЭР) и желудочными симптомами, указывающими на ДГР.19 Рефлюкс двенадцатиперстной кишки в желудок, особенно после еды, является физиологическим явлением; 20 тем не менее, билиарный рефлюкс вносит значительный вклад в поражение слизистой оболочки всего желудка 21
В нашем исследовании контрольная группа пациентов с различными степенями тяжести. При эзофагите не было выявлено значительных различий в показателях кислотного или желчного рефлюкса в желудок или пищевод по сравнению с пациентами Барретта. Это может быть вызвано отбором пациентов с эзофагитом, которые были кандидатами на фундопликацию, но обе группы пациентов значительно различались по сравнению со здоровым контролем.Поэтому наши результаты имеют большое клиническое значение, особенно для предоперационной диагностики.
Marshall et al. сравнивали здоровую контрольную группу с пациентами с различными степенями рефлюкс-эзофагита и пищевода Барретта в отношении измерения желчи в желудке.22 В этом исследовании средний возраст контрольных пациентов составлял 25 лет, а пациентов групп I, II , а III – 42, 50 и 60 лет соответственно. Билитек-зонд располагался на 10 см ниже нижнего сфинктера пищевода (LES).Порог поглощения билирубина составлял 0,14, и хотя не было обнаружено различий между группами по ТМТ, воздействие билирубина желудка было выше в положении лежа на спине, чем в вертикальном положении. В текущем исследовании контрольная группа была старше, чем в исследовании Маршалла. Больше дуодено-желудочного рефлюкса было зарегистрировано как у исследуемых, так и у контрольных пациентов во все периоды измерения. Эти результаты могут быть связаны с улучшением условий исследования.
Мы использовали пищеводный порог поглощения билирубина 0,25.Fein et al. [14] в исследовании in vitro абсорбции различных белых блюд показали, что наименьшее влияние пищи во время мониторинга желчи было измерено при абсорбции> 0,25.
Tack et al. сообщили о влиянии консистенции еды на результаты измерений Bilitec у здоровых субъектов.23 Они сравнили две группы молодых людей из контрольной группы. Испытуемые принимали либо только жидкую пищу, не поглощающую свет той же длины волны, что и билирубин, либо твердую пищу, избегая диет, которые влияют на поглощение билирубина.Авторы обнаружили существенные различия между двумя группами, используя порог поглощения билирубина> 0,14 со средним процентным соотношением (межквартильный диапазон) над TMT 10,9% (6,7–19,3) для твердой пищи и 0,3% (0,0–2,8) для жидкой пищи. Основные артефакты приема пищи присутствовали у субъектов, получавших твердую пищу из двух блюд (10%) и без жидкости. В нашем исследовании мы обнаружили такой артефакт приема пищи у одного пациента и одного контроля, но значения поглощения билирубина были ниже 0,25 и, следовательно, не соответствовали нашим результатам.
Гастроэзофагеальный рефлюкс нередко содержит секреции желчи, двенадцатиперстной кишки и поджелудочной железы. Использование спектрофотометрического зонда Bilitec продемонстрировало более высокую распространенность аномального воздействия билирубина пищевода у пациентов с метаплазией Барретта по сравнению с пациентами с эрозивным повреждением или без признаков эзофагита (6,8,10,13). добровольцы включены в контрольную группу. Однако другие исследования показали повышенную распространенность гастроэзофагеального рефлюкса с возрастом.24 По этим причинам мы изучали здоровых людей из контрольной группы по возрасту и полу и пациентов с пищеводом Барретта или с эзофагитом. Мы обнаружили патологическую кислотность и желчный рефлюкс пищевода у одной трети контрольной. Возможно, это может быть вызвано артефактами или нарушением протокола волонтерами. Но в предыдущем опубликованном исследовании мы смогли показать, что у более молодых здоровых людей такого патологического рефлюкса не было.17 Возможно, эти явления вызваны расслаблением, которое чаще встречается у пожилых людей.Напротив, почти все пациенты с пищеводом Барретта (87%) и все пациенты с эзофагитом (100%) показали патологический кислотный рефлюкс и / или желчный рефлюкс, измеренные с помощью комбинированного мониторинга pH и желчи. В частности, рефлюкс желчи в пищевод во время сна был обнаружен только у пациентов с BM или с эзофагитом.
В нашем исследовании мы измерили внутрижелудочный pH и рефлюкс желчи из двенадцатиперстной кишки в желудок (DGR). Медиана внутрижелудочного pH была одинаковой в обеих группах.Но пациенты с пищеводом Барретта имели значительно более длительный дуоденогастральный рефлюкс в течение 24-часового периода измерения, чем контрольная группа. Ночью было продемонстрировано больше ДГР, чем днем, в обеих группах исследуемых пациентов и в контрольной здоровой группе. Согласно ранее опубликованным исследованиям, это могло быть связано с щелочным сдвигом pH. Точный механизм, с помощью которого происходит ночной DGR, и роль, которую играет поза, остаются неясными.
Bowrey et al. не смогли установить ни гастроэзофагеальный, ни дуоденогастральный рефлюкс как преобладающую причину воспаления в слизистой оболочке сердца желудка с использованием прибора Bilitec 2000.16 Это понятно, поскольку количество рефлюкса в желудок (DGR) не обязательно коррелирует с DGER в пищевод. В этом исследовании авторы продемонстрировали больше DGR у женщин в период лежа на спине, в то время как у мужчин было больше DGER. При этом корреляции между уровнями желчи в желудке и пищеводе не было. Однако контрольная группа была намного моложе пациентов. Мы обнаружили значительные различия в измерениях желчи желудка и пищевода между пациентами с BM и контрольной группой.В отличие от Bowrey et al., Мы наблюдали больше DGER у женщин в период лежа на спине и больше DGR у пациентов-мужчин.
Напротив, Banki сообщил об аналогичном воздействии на пищевод рефлюксной кислоты и билирубина у женщин и мужчин со слизистой оболочкой Барретта.28 Pfaffenbach et al. (29) изучали желчь пищевода и кислотный рефлюкс у пациентов с длинным сегментом пищевода Барретта (LSBE) и коротким сегментом пищевода Барретта. пищевода (SSBE) и пациентов с гастроэзофагеальной рефлюксной болезнью (GERD). Субъекты прошли манометрию пищевода и одновременный 24-часовой мониторинг pH и желчи (Bilitec 2000) со значением абсорбции> 0.2 на 10,9% от общего периода. GER не отличался между группами. Однако DGER различалась у пациентов с LSBE (14,7%), SSBE (2,1%) и GERD (2,1%).
Таким образом, анализ эталонных значений показателей кислотности пищевода и рефлюкса желчи в группе здоровых, сопоставимых по возрасту и полу контролей по сравнению с пациентами с BM привел к следующим выводам:
Хотя около 30% здоровых контролей показали кислотный рефлюкс при мониторинге pH, пациенты с BM имели значительно более высокий кислотный рефлюкс в течение всех периодов измерения.
У здоровых людей не было значимого дуодено-желудочно-пищеводного рефлюкса, измеренного по абсорбции билирубина. Особенно в период лежа на спине не было рефлюкса желчи.
Оптимальный порог патологического рефлюкса желчи составляет 1,1% (мониторинг желчи с оптической плотностью 0,25).
Дуодено-желудочно-пищеводный рефлюкс – что такое патологический? Сравнение пациентов с пищеводом Барретта и добровольцев того же возраста
Резюме
Введение
Целью исследования был анализ данных мониторинга pH и желчи у пациентов с пищеводом Барретта и в контрольной группе, сопоставимой по возрасту и полу.
Субъекты и методы
Двадцать четыре последовательных пациента Барретта (8 женщин, 16 мужчин, средний возраст 57 лет), 21 пациент с эзофагитом (10 женщин, 11 мужчин, средний возраст 58 лет) и 19 здоровых пациентов контрольной группы (8 женщин). , 11 мужчин, средний возраст 51 год). Только пациентам проводилась эндоскопия с биопсией. Все группы были исследованы с помощью манометрии, 24-часового pH желудка и пищевода и одновременного мониторинга желчи в соответствии со стандартизованным протоколом. Поглощение билирубина> 0.25 был определен как вредный желчный рефлюкс. Метод характеристики оператора приемника (ROC) был применен для определения оптимального порогового значения уровней патологического билирубина.
Результаты
Из пациентов Барретта у 79% был патологический кислый желудочный рефлюкс (pH <4> 5% от общего времени измерения). Однако у 32% здоровых людей из контрольной группы также был кислотный рефлюкс ( p <0,05) без каких-либо симптомов. Медиана рефлюкса желчи из пищевода составила 7,8% (нижний квартиль (LQ) – верхний квартиль (UQ) = 1).6–17,8%) у пациентов с болезнью Барретта, у пациентов с эзофагитом - 3,5% (LQ – UQ = 0,1–13,5) и, в отличие от 0% (LQ – UQ = 0–1,0%) в контроле, p = 0,001 . ROC-анализ показал оптимальное значение деления для пациентов с рефлюксом желчи более 1% в течение 24 часов (чувствительность 75%, специфичность 84%).
Заключение
Оптимальный порог для различения нормального и патологического рефлюкса желчи в пищевод составляет 1% (24-часовой мониторинг желчи с поглощением> 0,25).
Ключевые слова: Референтное значение bilitec, Рефлюкс желчи, Кислотный рефлюкс, слизистая оболочка Барретта, пищевод, спектрофотометрия
Введение
Уровень заболеваемости аденокарциномой (АК) пищевода и кардии желудка в западных промышленно развитых странах быстро вырос.1 Помимо злоупотребления никотином и алкоголем, факторы питания, высокий индекс массы тела, кислый желудочный рефлюкс и пищевод Барретта считаются критическими факторами канцерогенеза. 2–4 Недавние исследования показали, что наличие желчного рефлюкса в сочетании с кислым желудочным рефлюксом. повреждает слизистую оболочку пищевода и вызывает осложнения гастроэзофагеальной рефлюксной болезни (ГЭРБ), например, развитие слизистой оболочки Барретта (ВМ) .5,6 Дуодено-желудочный рефлюкс в пищевод (ДГЭР), в частности, важен для патогенез пищевода Барретта.7 Продолжительные исследования аспирации пищевода документально подтвердили повышение уровня желчных кислот у пациентов с тяжелым эзофагитом и пищеводом Барретта. 8 Восемьдесят процентов пациентов с пищеводом Барретта, принимающим ингибиторы протонной помпы, демонстрируют нормальный профиль pH пищевода, но 60% показывают аномальное воздействие желчи в пищевод, как измерено. by Bilitec 2000.9
В прошлом прямая и продолжительная количественная оценка дуоденоэзофагеального рефлюкса была труднодостижимой. Теперь концентрацию билирубина можно напрямую измерить спектрофотометрией на основе удельного поглощения на длине волны 453 нм.Билиарный рефлюкс можно измерить с помощью амбулаторного фиброоптического зонда, проходящего через нос (Bilitec 2000), который регистрирует всасывание желчи. Уже опубликован ряд работ по обнажению пищевода10–13 и желудка24–16 с использованием этой техники. Однако в этих исследованиях возраст контрольной группы составлял от 25 до 35 лет. В клинической практике пациенты со слизистой оболочкой Барретта обычно старше. Кроме того, авторы каждого исследования использовали различные контрольные значения для измерения билиарного рефлюкса в пищеводе, что затрудняло сравнение измеренных значений.
Целью настоящего исследования был анализ данных мониторинга pH и желчи в группе здоровых лиц из контрольной группы, соответствующих возрасту и полу, и пациентов с пищеводом Барретта.
Субъекты и методы
Субъекты
Отбор контролей проводился в соответствии со строгим протоколом. В исследование были включены здоровые добровольцы, лечившиеся с 1999 по 2000 год, в возрасте от 40 до 60 лет. Никто из контрольных не принимал препараты, подавляющие кислоту или перистальтику кишечника, не имел в анамнезе заболеваний верхних отделов желудочно-кишечного тракта, не подвергался хирургическим вмешательствам на верхних отделах брюшной полости или обширным операциям на брюшной полости, а также не подвергался терапевтическим эндоскопическим процедурам верхних отделов желудочно-кишечного тракта.Диагностическая эндоскопия и проглатывание бария не проводились, но желчнокаменная болезнь была исключена на УЗИ.
С 1999 по 2002 год в исследование были включены 24 пациента с гистологически подтвержденной слизистой оболочкой Барретта. Для дополнительного сравнения мы включили группу пациентов с эзофагитом (стадия I – III по Савари и Миллеру) без пищевода Барретта, которым перед плановой лапароскопической фундопликацией были выполнены те же диагностические процедуры. В течение вышеупомянутого периода для этого исследования был доступен 21 пациент в возрасте старше 40 лет.Критериями исключения были хирургия пищевода, желудка или желчевыводящих путей в анамнезе, лучевая терапия брюшной или грудной клетки в анамнезе или наличие язвенной болезни, активное желудочно-кишечное кровотечение, варикозное расширение вен пищевода или дна, хроническое заболевание пищевода или верхних отделов тонкой кишки или опухолевые заболевания. Все препараты, потенциально влияющие на перистальтику желудочно-кишечного тракта и секрецию, были отменены по крайней мере за 1 неделю до исследования.
Эндоскопия верхних отделов желудочно-кишечного тракта
Всем пациентам была выполнена классическая эндоскопия верхних отделов желудочно-кишечного тракта.Если была необходима седация, обычно применяли внутривенное введение пропофола (до 200 мг) или изредка применяли мидазолам (до 5 мг). Во время эндоскопии было отмечено наличие и степень эзофагита, пищевода Барретта и грыжи пищеводного отверстия диафрагмы. Биопсии были взяты со слизистой оболочки Барретта.
Амбулаторный мониторинг pH пищевода / желудка и желчи
Все группы прошли манометрию пищевода и 24-часовой мониторинг pH и одновременный мониторинг желчи с использованием стандартизованного протокола.Амбулаторный мониторинг pH выполнялся с использованием трансназально введенного сурьмяного pH-электрода с отдельным кожным электродом сравнения (Synetics Medical, Стокгольм, Швеция). Данные сохранялись на портативном цифровом записывающем устройстве (Digitrapper MkIII, Synectics Medical Stockholm, Швеция). Перед каждым исследованием зонд pH калибровали в буферных растворах с pH 7 и 1. Эпизод кислотного рефлюкса определялся как снижение pH пищевода до менее 4 в течение более 10 с.
Для количественной оценки дуодено-пищеводного рефлюкса использовался амбулаторный фиброоптический спектрофотометр, переданный через нос (Bilitec 2000, Synectics, Швеция).Система состоит из миниатюрного зонда диаметром 1,5 мм, который передает световые сигналы в пищевод и обратно через пластиковую волоконно-оптическую связку. Перед каждым исследованием зонд калибровали в воде. В соответствии с текущей литературой, абсорбция билирубина> 0,25 использовалась в качестве эталона для вредного билиарного рефлюкса.14
Зонды желчи и pH были скреплены вместе и прошли трансназально в пищевод и желудок, как подробно описано в другом месте.17 Верхняя часть кончики зондов были расположены на 5 см выше верхней границы нижнего сфинктера пищевода, как определено манометрией пищевода.Дистальный pH-электрод и оптоволоконный датчик помещали на дно желудка на 10 см дистальнее нижнего сфинктера пищевода (рис.). Контрольной группы и пациентов просили следовать строгому протоколу трехразового питания без жидкости между приемами пищи. Лежачие фазы записи разрешались только ночью. Пациентов просили вести дневник, фиксируя точный характер приема пищи, фазы измерения в положении лежа на спине и прямо, а также ощущения изжоги и срыгивания.
Расположение датчиков pH и билирубина в желудке и пищеводе.(UES = верхний сфинктер пищевода; LES = нижний сфинктер пищевода).
Одновременный мониторинг желчных протоков и pH проводился с применением бесцветной «белой диеты» (WD), включающей жидкую и твердую пищу с максимальным поглощением желчи in vitro 0,25 [шкала поглощения от 0 (обычная вода) до 1 (общая экран)]. Еда включала воду, молоко, тосты, картофель, курицу, сухое печенье и рыбу.
Сбор и интерпретация данных
После завершения измерений зонды у пациентов извлекались, и данные сохранялись через интерфейс на IBM-совместимом компьютере, оснащенном программным обеспечением Polygram® (Medtronic).Для анализа использовались данные каждой секунды 24-часовых измерений. Чтобы оценить наличие желудочного или пищеводного билиарного рефлюкса, был рассчитан процент времени, когда абсорбция была больше 0,25 для следующих периодов: всего в положении лежа на спине, в вертикальном положении и после приема пищи. Постпрандиальный период определялся как 2 ч после окончания приема пищи. Процент времени с pH пищевода ниже 4 и медианным pH желудка и процент времени с pH желудка, измеряющим 1, 2, 3–7 и> 7, также был рассчитан для вышеуказанных периодов.Средняя продолжительность амбулаторного мониторингового исследования pH и Bilitec составляла 22 часа 40 минут у пациентов и 23 часа 44 минуты в контрольной группе.
Статистический анализ
Для анализа результатов использовалась программа SPSS (версия 11.0, Чикаго, Иллинойс). Для графического представления использовалась программа MedCalc для Windows (версия 9.0, MedCalc Software, Бельгия). Были установлены медианы, значения межквартильного размаха (IQR или 25–75 перцентиль). Непараметрические тесты (анализ Манна – Уитни и Краскела – Уоллиса) использовались для оценки взаимосвязи между переменными.Для представления некоторых данных использовались графики Box и Whisker. На этих графиках прямоугольник представляет IQR, а усы – самые высокие и самые низкие значения. Также нанесены выбросы, определенные как более чем в 1,5 раза превышающие IQR от 75-го центиля. Экстремальные значения были определены как более чем трехкратный IQR от 75-го центиля.
Кривая характеристики оператора приемника (ROC) использовалась для определения порогового значения для оптимальной чувствительности и специфичности согласно Цвейгу и Кэмпбеллу18. Площадь под кривой (AUC) использовалась как измерение диагностической эффективности теста.Результаты представлены в виде точек с доверительным интервалом 95% (95% ДИ) и графически для представления всех данных. В качестве положительной группы мы использовали пациентов со слизистой оболочкой Барретта, а отрицательную тестовую группу определяли здоровыми добровольцами. Предполагалось непараметрическое распределение площади под кривой.
Предположения для расчета требуемого размера выборки были альфа = 0,05, бета = 0,80, и что тест действителен для ежедневного использования только в том случае, если менее 20% здоровых контролей и не менее 80% пациентов имеют положительный результат теста. полученные результаты.Расчетный размер выборки для каждой группы составил 20.
Этика
Протокол исследования был одобрен этическим комитетом Кельнского университета. Каждый субъект дал письменное информированное согласие.
Результаты
В исследование были включены 24 пациента с пищеводом Барретта (средний возраст: 58 лет), 21 пациент с эзофагитом (средний возраст: 57 лет) и 19 здоровых людей контрольной группы со средним возрастом 51 год. У пациентов с БМ выявлен эзофагит 0 степени (4 случая), I степени (12 случаев) и II степени (8 случаев).В контрольной группе пациентов с эзофагитом было девять случаев с I степенью, восемь случаев со II степенью и три случая с III степенью. Демографические данные пациентов и добровольцев представлены в таблице (данные одного добровольца не были использованы из-за технических проблем).
Таблица 1
Демографические данные пациентов с слизистой оболочкой Барретта или эзофагитом и здоровых добровольцев
| Параметры | Пациенты с пищеводом Барретта ( n = 24) | Пациенты с эзофагитом ( n = 21) | Контроли ( n = 19) | Значение Пат.с Barrett vs Controls |
|---|---|---|---|---|
| Возраст (средний) | 57 лет | 58 лет | 51 год | – |
| Мин. 39–62 года | ||||
| Пол м: ж | 16: 8 | 11:10 | 11: 8 | нс |
| ИМТ (медиана) мин – макс | 27,0 кг / м 2 (18,6–33,1) | 26.9 кг / м 2 (17,9–31,5) | 24,1 кг / м 2 (19,62–27,34) | p = 0,003 |
| Курильщики (%) | n = 5 (20,8 ) | n = 4 (19,0) | n = 6 (31,6) | нс |
| Без спирта% | n = 3 (12,5) | n = 5 (23,8) | n = 5 (26,3) | n.s. |
Кислый желудочный рефлюкс (AGR)
Пациенты с пищеводом Барретта, 19 из 24 (79%) и 20 из 21 контрольных пациентов с эзофагитом (95%) имели патологические AGR [pH <4 в> 5% от общего числа измерения времени (TMT)], но также у 6 из 19 здоровых контролей (32%) наблюдались патологические AGR без каких-либо симптомов ( p = 0.002). Во время TMT средний AGR составил 10,6% для пациентов Barrett и 3,2% для контрольной группы ( p <0,01). В частности, измерения длительного кислотного рефлюкса (LAR), определяемого как pH рефлюкса <4, длящегося более 5 минут, показали значительные различия между пациентами и контрольной группой. Патологический AGR был обнаружен у пациентов в период измерения натощак как в положении лежа на спине, так и в вертикальном положении. Напротив, патологические AGR у здоровых людей наблюдались только в вертикальном положении (таблица).
Таблица 2
Медиана кислотного желудочного рефлюкса в пищевод у пациентов с BM или с эзофагитом и в здоровой контрольной группе
| Параметры | Пациенты с пищеводом Барретта ( n = 24) [медиана (LQ-UQ )] | Пациенты с эзофагитом ( n = 21) [медиана (LQ-UQ)] | Контрольная группа ( n = 19) [медиана (LQ-UQ)] | Значение Пат.с Barrett vs Controls |
|---|---|---|---|---|
| Процент от общего времени измерения pH <4 (%) | 10,6 (6,2–38,3) | 19,9 (1,6–71,7) | 3,2 (0,9–5,5) | p = 0,01 |
| Процент времени измерения в вертикальном положении pH <4 (%) | 11,7 (6,03–6,4) | 18,9 (8,7–60,8) | 2,4 (0,9–6,1) | p <0,05 |
| Процент времени измерения в положении лежа на спине pH <4 (%) | 10.9 (0,4–27,1) | 6,3 (0,0–13,3) | 0,3 (0,0–4,2) | p = 0,004 |
24-часовой мониторинг внутрижелудочного pH и желчи
Мониторинг pH желудка не показал значимых различия между пациентами и контрольной группой для всех периодов измерения (таблица). Воздействие желудочного билирубина, указывающее на билиарный рефлюкс, было значительно более частым у пациентов, чем в контрольной группе, в течение всех периодов измерения (таблица). Воздействие желчных путей в положении лежа на спине обычно происходило в ранние утренние часы во время сна, что выражалось увеличением абсорбции в течение 2–3 часов с быстрым возвращением к исходным значениям примерно в то время, когда субъект снова возвращался в вертикальное положение.За тот же период времени мониторинг pH желудка показал повышение уровня pH до более чем 2 (рис.).
Таблица 3
Результаты 24-часового внутрижелудочного мониторинга pH и желчи у пациентов с пищеводом Барретта и здоровой контрольной группы
| Параметры | Пациенты ( n = 24) [медиана (LQ – UQ)] | Контроли ( n = 19) [Медиана (LQ – UQ)] | Значимость |
|---|---|---|---|
| Медиана внутрижелудочного pH во время TMT | 1.3 (1,0–1,4) | 1,4 (1,1–1,7) | н.с. |
| Процент воздействия билирубина (%) TMT | 7,8 (1,6–17,8) | 0,0 (0,0–1,0) | p = 0,001 |
| Процент воздействия билирубина (%) в прямом эфире | 6,9 (0,1–12,9) | 0,0 (0,0–1,3) | p <0,01 |
| Процент воздействия билирубина (%) во время пребывания на спине | 2,0 (0,0–28,6) | 0.0 (0,0–0,0) | p = 0,001 |
24-часовой внутрижелудочный мониторинг pH и желчи у пациента с пищеводом Барретта, демонстрирующего дуоденогастральный рефлюкс ранним утром. а. Bilitec®-мониторинг, б. pH-мониторинг.
Воздействие билирубина на пищевод
По результатам TMT медиана желчного рефлюкса пищевода составила 7,8% для пациентов с пищеводом Барретта (LQ – UQ = 1,6–17,8%) и 3,5 (LQ – UQ = 0,1–13,5) для контроля пациентов, в отличие от 0% для контроля (LQ – UQ = 0–1.0%), р = 0,001). На рисунке показано, что мониторинг желчи пищевода у пациентов с пищеводом Барретта и здоровых людей в контрольной группе варьировался в течение всего периода измерения и периода лежа на спине.
Результаты мониторинга желчи в пищеводе у 24 пациентов с пищеводом Барретта, 21 пациента с эзофагитом и 19 здоровых людей из контрольной группы а) общий период измерения (тест Краскела-Уоллиса = 0,01) б) период лежа на спине (тест Краскала-Уоллиса p = 0,01) .
Рабочая кривая приемника, отображающая процент истинных положительных результатов (пациенты с пищеводом Барретта, идентифицированные по воздействию билирубина) в зависимости от частоты ложных срабатываний (здоровые контроли с высоким уровнем воздействия билирубина), показана на рис.. С площадью под кривой 0,78 (95% ДИ = 0,56–0,89) ROC-анализ мониторинга желчевыводящих путей показал оптимальное значение для пациентов при 1% TMT [чувствительность 75% (95% ДИ = 53–90%). , Специфичность 84% (95% ДИ = 60–96%)]. Следовательно, пороговое значение для различения нормального и патологического билиарного рефлюкса с использованием 24-часового мониторинга желчевыводящих путей в пищеводе (порог поглощения> 0,25) должно быть зафиксировано на уровне 1% от TMT.
ROC-кривая с 95% доверительным интервалом для патологического мониторинга желчи у пациентов с пищеводом Барретта по сравнению со здоровыми контрольными пациентами, соответствующими возрасту и полу.
пациентов Барретта, 18 из 24 (75%), 15 из 21 контрольного пациента с эзофагитом (71%) и 3 из 19 контрольных (16%) показали билирийный рефлюкс в пищевод более 1,1% TMT ( p <0,001). Используя это пороговое значение, ни у одного из контрольных пациентов, у 10 из контрольных пациентов (48%) и у 11 из 24 пациентов с болезнью Барретта (46%) не было патологического воздействия билирубина во время сна.
Обсуждение
Результаты нашего исследования подтверждают, что пациенты с пищеводом Барретта имеют значительно более частый дуоденогастральный рефлюкс в пищевод, чем здоровые люди из контрольной группы того же возраста и пола.Кроме того, этот рефлюкс, измеряемый воздействием кислоты и билирубина, дольше остается в пищеводе, особенно во время сна.
Роль кислотного и некислотного рефлюкса в пищевод как причинного фактора симптомов и поражений слизистой оболочки рассматривалась в ряде исследований. Не только продолжительность, но, возможно, и состав рефлюкса, играет важную роль в развитии таких поражений.13 Круглосуточный внутрижелудочный мониторинг желчи предоставил клиницисту однозначные доказательства чрезмерного дуоденогастрального рефлюкса (DGR) у 41% пациентов. с эндоскопическим эзофагитом, симптомами гастроэзофагеального рефлюкса (ГЭР) и желудочными симптомами, указывающими на ДГР.19 Рефлюкс двенадцатиперстной кишки в желудок, особенно после еды, является физиологическим явлением; 20 тем не менее, билиарный рефлюкс вносит значительный вклад в поражение слизистой оболочки всего желудка 21
В нашем исследовании контрольная группа пациентов с различными степенями тяжести. При эзофагите не было выявлено значительных различий в показателях кислотного или желчного рефлюкса в желудок или пищевод по сравнению с пациентами Барретта. Это может быть вызвано отбором пациентов с эзофагитом, которые были кандидатами на фундопликацию, но обе группы пациентов значительно различались по сравнению со здоровым контролем.Поэтому наши результаты имеют большое клиническое значение, особенно для предоперационной диагностики.
Marshall et al. сравнивали здоровую контрольную группу с пациентами с различными степенями рефлюкс-эзофагита и пищевода Барретта в отношении измерения желчи в желудке.22 В этом исследовании средний возраст контрольных пациентов составлял 25 лет, а пациентов групп I, II , а III – 42, 50 и 60 лет соответственно. Билитек-зонд располагался на 10 см ниже нижнего сфинктера пищевода (LES).Порог поглощения билирубина составлял 0,14, и хотя не было обнаружено различий между группами по ТМТ, воздействие билирубина желудка было выше в положении лежа на спине, чем в вертикальном положении. В текущем исследовании контрольная группа была старше, чем в исследовании Маршалла. Больше дуодено-желудочного рефлюкса было зарегистрировано как у исследуемых, так и у контрольных пациентов во все периоды измерения. Эти результаты могут быть связаны с улучшением условий исследования.
Мы использовали пищеводный порог поглощения билирубина 0,25.Fein et al. [14] в исследовании in vitro абсорбции различных белых блюд показали, что наименьшее влияние пищи во время мониторинга желчи было измерено при абсорбции> 0,25.
Tack et al. сообщили о влиянии консистенции еды на результаты измерений Bilitec у здоровых субъектов.23 Они сравнили две группы молодых людей из контрольной группы. Испытуемые принимали либо только жидкую пищу, не поглощающую свет той же длины волны, что и билирубин, либо твердую пищу, избегая диет, которые влияют на поглощение билирубина.Авторы обнаружили существенные различия между двумя группами, используя порог поглощения билирубина> 0,14 со средним процентным соотношением (межквартильный диапазон) над TMT 10,9% (6,7–19,3) для твердой пищи и 0,3% (0,0–2,8) для жидкой пищи. Основные артефакты приема пищи присутствовали у субъектов, получавших твердую пищу из двух блюд (10%) и без жидкости. В нашем исследовании мы обнаружили такой артефакт приема пищи у одного пациента и одного контроля, но значения поглощения билирубина были ниже 0,25 и, следовательно, не соответствовали нашим результатам.
Гастроэзофагеальный рефлюкс нередко содержит секреции желчи, двенадцатиперстной кишки и поджелудочной железы. Использование спектрофотометрического зонда Bilitec продемонстрировало более высокую распространенность аномального воздействия билирубина пищевода у пациентов с метаплазией Барретта по сравнению с пациентами с эрозивным повреждением или без признаков эзофагита (6,8,10,13). добровольцы включены в контрольную группу. Однако другие исследования показали повышенную распространенность гастроэзофагеального рефлюкса с возрастом.24 По этим причинам мы изучали здоровых людей из контрольной группы по возрасту и полу и пациентов с пищеводом Барретта или с эзофагитом. Мы обнаружили патологическую кислотность и желчный рефлюкс пищевода у одной трети контрольной. Возможно, это может быть вызвано артефактами или нарушением протокола волонтерами. Но в предыдущем опубликованном исследовании мы смогли показать, что у более молодых здоровых людей такого патологического рефлюкса не было.17 Возможно, эти явления вызваны расслаблением, которое чаще встречается у пожилых людей.Напротив, почти все пациенты с пищеводом Барретта (87%) и все пациенты с эзофагитом (100%) показали патологический кислотный рефлюкс и / или желчный рефлюкс, измеренные с помощью комбинированного мониторинга pH и желчи. В частности, рефлюкс желчи в пищевод во время сна был обнаружен только у пациентов с BM или с эзофагитом.
В нашем исследовании мы измерили внутрижелудочный pH и рефлюкс желчи из двенадцатиперстной кишки в желудок (DGR). Медиана внутрижелудочного pH была одинаковой в обеих группах.Но пациенты с пищеводом Барретта имели значительно более длительный дуоденогастральный рефлюкс в течение 24-часового периода измерения, чем контрольная группа. Ночью было продемонстрировано больше ДГР, чем днем, в обеих группах исследуемых пациентов и в контрольной здоровой группе. Согласно ранее опубликованным исследованиям, это могло быть связано с щелочным сдвигом pH. Точный механизм, с помощью которого происходит ночной DGR, и роль, которую играет поза, остаются неясными.
Bowrey et al. не смогли установить ни гастроэзофагеальный, ни дуоденогастральный рефлюкс как преобладающую причину воспаления в слизистой оболочке сердца желудка с использованием прибора Bilitec 2000.16 Это понятно, поскольку количество рефлюкса в желудок (DGR) не обязательно коррелирует с DGER в пищевод. В этом исследовании авторы продемонстрировали больше DGR у женщин в период лежа на спине, в то время как у мужчин было больше DGER. При этом корреляции между уровнями желчи в желудке и пищеводе не было. Однако контрольная группа была намного моложе пациентов. Мы обнаружили значительные различия в измерениях желчи желудка и пищевода между пациентами с BM и контрольной группой.В отличие от Bowrey et al., Мы наблюдали больше DGER у женщин в период лежа на спине и больше DGR у пациентов-мужчин.
Напротив, Banki сообщил об аналогичном воздействии на пищевод рефлюксной кислоты и билирубина у женщин и мужчин со слизистой оболочкой Барретта.28 Pfaffenbach et al. (29) изучали желчь пищевода и кислотный рефлюкс у пациентов с длинным сегментом пищевода Барретта (LSBE) и коротким сегментом пищевода Барретта. пищевода (SSBE) и пациентов с гастроэзофагеальной рефлюксной болезнью (GERD). Субъекты прошли манометрию пищевода и одновременный 24-часовой мониторинг pH и желчи (Bilitec 2000) со значением абсорбции> 0.2 на 10,9% от общего периода. GER не отличался между группами. Однако DGER различалась у пациентов с LSBE (14,7%), SSBE (2,1%) и GERD (2,1%).
Таким образом, анализ эталонных значений показателей кислотности пищевода и рефлюкса желчи в группе здоровых, сопоставимых по возрасту и полу контролей по сравнению с пациентами с BM привел к следующим выводам:
Хотя около 30% здоровых контролей показали кислотный рефлюкс при мониторинге pH, пациенты с BM имели значительно более высокий кислотный рефлюкс в течение всех периодов измерения.
У здоровых людей не было значимого дуодено-желудочно-пищеводного рефлюкса, измеренного по абсорбции билирубина. Особенно в период лежа на спине не было рефлюкса желчи.
Оптимальный порог патологического рефлюкса желчи составляет 1,1% (мониторинг желчи с оптической плотностью 0,25).
Дуодено-желудочно-пищеводный рефлюкс – что такое патологический? Сравнение пациентов с пищеводом Барретта и добровольцев того же возраста
Резюме
Введение
Целью исследования был анализ данных мониторинга pH и желчи у пациентов с пищеводом Барретта и в контрольной группе, сопоставимой по возрасту и полу.
Субъекты и методы
Двадцать четыре последовательных пациента Барретта (8 женщин, 16 мужчин, средний возраст 57 лет), 21 пациент с эзофагитом (10 женщин, 11 мужчин, средний возраст 58 лет) и 19 здоровых пациентов контрольной группы (8 женщин). , 11 мужчин, средний возраст 51 год). Только пациентам проводилась эндоскопия с биопсией. Все группы были исследованы с помощью манометрии, 24-часового pH желудка и пищевода и одновременного мониторинга желчи в соответствии со стандартизованным протоколом. Поглощение билирубина> 0.25 был определен как вредный желчный рефлюкс. Метод характеристики оператора приемника (ROC) был применен для определения оптимального порогового значения уровней патологического билирубина.
Результаты
Из пациентов Барретта у 79% был патологический кислый желудочный рефлюкс (pH <4> 5% от общего времени измерения). Однако у 32% здоровых людей из контрольной группы также был кислотный рефлюкс ( p <0,05) без каких-либо симптомов. Медиана рефлюкса желчи из пищевода составила 7,8% (нижний квартиль (LQ) – верхний квартиль (UQ) = 1).6–17,8%) у пациентов с болезнью Барретта, у пациентов с эзофагитом - 3,5% (LQ – UQ = 0,1–13,5) и, в отличие от 0% (LQ – UQ = 0–1,0%) в контроле, p = 0,001 . ROC-анализ показал оптимальное значение деления для пациентов с рефлюксом желчи более 1% в течение 24 часов (чувствительность 75%, специфичность 84%).
Заключение
Оптимальный порог для различения нормального и патологического рефлюкса желчи в пищевод составляет 1% (24-часовой мониторинг желчи с поглощением> 0,25).
Ключевые слова: Референтное значение bilitec, Рефлюкс желчи, Кислотный рефлюкс, слизистая оболочка Барретта, пищевод, спектрофотометрия
Введение
Уровень заболеваемости аденокарциномой (АК) пищевода и кардии желудка в западных промышленно развитых странах быстро вырос.1 Помимо злоупотребления никотином и алкоголем, факторы питания, высокий индекс массы тела, кислый желудочный рефлюкс и пищевод Барретта считаются критическими факторами канцерогенеза. 2–4 Недавние исследования показали, что наличие желчного рефлюкса в сочетании с кислым желудочным рефлюксом. повреждает слизистую оболочку пищевода и вызывает осложнения гастроэзофагеальной рефлюксной болезни (ГЭРБ), например, развитие слизистой оболочки Барретта (ВМ) .5,6 Дуодено-желудочный рефлюкс в пищевод (ДГЭР), в частности, важен для патогенез пищевода Барретта.7 Продолжительные исследования аспирации пищевода документально подтвердили повышение уровня желчных кислот у пациентов с тяжелым эзофагитом и пищеводом Барретта. 8 Восемьдесят процентов пациентов с пищеводом Барретта, принимающим ингибиторы протонной помпы, демонстрируют нормальный профиль pH пищевода, но 60% показывают аномальное воздействие желчи в пищевод, как измерено. by Bilitec 2000.9
В прошлом прямая и продолжительная количественная оценка дуоденоэзофагеального рефлюкса была труднодостижимой. Теперь концентрацию билирубина можно напрямую измерить спектрофотометрией на основе удельного поглощения на длине волны 453 нм.Билиарный рефлюкс можно измерить с помощью амбулаторного фиброоптического зонда, проходящего через нос (Bilitec 2000), который регистрирует всасывание желчи. Уже опубликован ряд работ по обнажению пищевода10–13 и желудка24–16 с использованием этой техники. Однако в этих исследованиях возраст контрольной группы составлял от 25 до 35 лет. В клинической практике пациенты со слизистой оболочкой Барретта обычно старше. Кроме того, авторы каждого исследования использовали различные контрольные значения для измерения билиарного рефлюкса в пищеводе, что затрудняло сравнение измеренных значений.
Целью настоящего исследования был анализ данных мониторинга pH и желчи в группе здоровых лиц из контрольной группы, соответствующих возрасту и полу, и пациентов с пищеводом Барретта.
Субъекты и методы
Субъекты
Отбор контролей проводился в соответствии со строгим протоколом. В исследование были включены здоровые добровольцы, лечившиеся с 1999 по 2000 год, в возрасте от 40 до 60 лет. Никто из контрольных не принимал препараты, подавляющие кислоту или перистальтику кишечника, не имел в анамнезе заболеваний верхних отделов желудочно-кишечного тракта, не подвергался хирургическим вмешательствам на верхних отделах брюшной полости или обширным операциям на брюшной полости, а также не подвергался терапевтическим эндоскопическим процедурам верхних отделов желудочно-кишечного тракта.Диагностическая эндоскопия и проглатывание бария не проводились, но желчнокаменная болезнь была исключена на УЗИ.
С 1999 по 2002 год в исследование были включены 24 пациента с гистологически подтвержденной слизистой оболочкой Барретта. Для дополнительного сравнения мы включили группу пациентов с эзофагитом (стадия I – III по Савари и Миллеру) без пищевода Барретта, которым перед плановой лапароскопической фундопликацией были выполнены те же диагностические процедуры. В течение вышеупомянутого периода для этого исследования был доступен 21 пациент в возрасте старше 40 лет.Критериями исключения были хирургия пищевода, желудка или желчевыводящих путей в анамнезе, лучевая терапия брюшной или грудной клетки в анамнезе или наличие язвенной болезни, активное желудочно-кишечное кровотечение, варикозное расширение вен пищевода или дна, хроническое заболевание пищевода или верхних отделов тонкой кишки или опухолевые заболевания. Все препараты, потенциально влияющие на перистальтику желудочно-кишечного тракта и секрецию, были отменены по крайней мере за 1 неделю до исследования.
Эндоскопия верхних отделов желудочно-кишечного тракта
Всем пациентам была выполнена классическая эндоскопия верхних отделов желудочно-кишечного тракта.Если была необходима седация, обычно применяли внутривенное введение пропофола (до 200 мг) или изредка применяли мидазолам (до 5 мг). Во время эндоскопии было отмечено наличие и степень эзофагита, пищевода Барретта и грыжи пищеводного отверстия диафрагмы. Биопсии были взяты со слизистой оболочки Барретта.
Амбулаторный мониторинг pH пищевода / желудка и желчи
Все группы прошли манометрию пищевода и 24-часовой мониторинг pH и одновременный мониторинг желчи с использованием стандартизованного протокола.Амбулаторный мониторинг pH выполнялся с использованием трансназально введенного сурьмяного pH-электрода с отдельным кожным электродом сравнения (Synetics Medical, Стокгольм, Швеция). Данные сохранялись на портативном цифровом записывающем устройстве (Digitrapper MkIII, Synectics Medical Stockholm, Швеция). Перед каждым исследованием зонд pH калибровали в буферных растворах с pH 7 и 1. Эпизод кислотного рефлюкса определялся как снижение pH пищевода до менее 4 в течение более 10 с.
Для количественной оценки дуодено-пищеводного рефлюкса использовался амбулаторный фиброоптический спектрофотометр, переданный через нос (Bilitec 2000, Synectics, Швеция).Система состоит из миниатюрного зонда диаметром 1,5 мм, который передает световые сигналы в пищевод и обратно через пластиковую волоконно-оптическую связку. Перед каждым исследованием зонд калибровали в воде. В соответствии с текущей литературой, абсорбция билирубина> 0,25 использовалась в качестве эталона для вредного билиарного рефлюкса.14
Зонды желчи и pH были скреплены вместе и прошли трансназально в пищевод и желудок, как подробно описано в другом месте.17 Верхняя часть кончики зондов были расположены на 5 см выше верхней границы нижнего сфинктера пищевода, как определено манометрией пищевода.Дистальный pH-электрод и оптоволоконный датчик помещали на дно желудка на 10 см дистальнее нижнего сфинктера пищевода (рис.). Контрольной группы и пациентов просили следовать строгому протоколу трехразового питания без жидкости между приемами пищи. Лежачие фазы записи разрешались только ночью. Пациентов просили вести дневник, фиксируя точный характер приема пищи, фазы измерения в положении лежа на спине и прямо, а также ощущения изжоги и срыгивания.
Расположение датчиков pH и билирубина в желудке и пищеводе.(UES = верхний сфинктер пищевода; LES = нижний сфинктер пищевода).
Одновременный мониторинг желчных протоков и pH проводился с применением бесцветной «белой диеты» (WD), включающей жидкую и твердую пищу с максимальным поглощением желчи in vitro 0,25 [шкала поглощения от 0 (обычная вода) до 1 (общая экран)]. Еда включала воду, молоко, тосты, картофель, курицу, сухое печенье и рыбу.
Сбор и интерпретация данных
После завершения измерений зонды у пациентов извлекались, и данные сохранялись через интерфейс на IBM-совместимом компьютере, оснащенном программным обеспечением Polygram® (Medtronic).Для анализа использовались данные каждой секунды 24-часовых измерений. Чтобы оценить наличие желудочного или пищеводного билиарного рефлюкса, был рассчитан процент времени, когда абсорбция была больше 0,25 для следующих периодов: всего в положении лежа на спине, в вертикальном положении и после приема пищи. Постпрандиальный период определялся как 2 ч после окончания приема пищи. Процент времени с pH пищевода ниже 4 и медианным pH желудка и процент времени с pH желудка, измеряющим 1, 2, 3–7 и> 7, также был рассчитан для вышеуказанных периодов.Средняя продолжительность амбулаторного мониторингового исследования pH и Bilitec составляла 22 часа 40 минут у пациентов и 23 часа 44 минуты в контрольной группе.
Статистический анализ
Для анализа результатов использовалась программа SPSS (версия 11.0, Чикаго, Иллинойс). Для графического представления использовалась программа MedCalc для Windows (версия 9.0, MedCalc Software, Бельгия). Были установлены медианы, значения межквартильного размаха (IQR или 25–75 перцентиль). Непараметрические тесты (анализ Манна – Уитни и Краскела – Уоллиса) использовались для оценки взаимосвязи между переменными.Для представления некоторых данных использовались графики Box и Whisker. На этих графиках прямоугольник представляет IQR, а усы – самые высокие и самые низкие значения. Также нанесены выбросы, определенные как более чем в 1,5 раза превышающие IQR от 75-го центиля. Экстремальные значения были определены как более чем трехкратный IQR от 75-го центиля.
Кривая характеристики оператора приемника (ROC) использовалась для определения порогового значения для оптимальной чувствительности и специфичности согласно Цвейгу и Кэмпбеллу18. Площадь под кривой (AUC) использовалась как измерение диагностической эффективности теста.Результаты представлены в виде точек с доверительным интервалом 95% (95% ДИ) и графически для представления всех данных. В качестве положительной группы мы использовали пациентов со слизистой оболочкой Барретта, а отрицательную тестовую группу определяли здоровыми добровольцами. Предполагалось непараметрическое распределение площади под кривой.
Предположения для расчета требуемого размера выборки были альфа = 0,05, бета = 0,80, и что тест действителен для ежедневного использования только в том случае, если менее 20% здоровых контролей и не менее 80% пациентов имеют положительный результат теста. полученные результаты.Расчетный размер выборки для каждой группы составил 20.
Этика
Протокол исследования был одобрен этическим комитетом Кельнского университета. Каждый субъект дал письменное информированное согласие.
Результаты
В исследование были включены 24 пациента с пищеводом Барретта (средний возраст: 58 лет), 21 пациент с эзофагитом (средний возраст: 57 лет) и 19 здоровых людей контрольной группы со средним возрастом 51 год. У пациентов с БМ выявлен эзофагит 0 степени (4 случая), I степени (12 случаев) и II степени (8 случаев).В контрольной группе пациентов с эзофагитом было девять случаев с I степенью, восемь случаев со II степенью и три случая с III степенью. Демографические данные пациентов и добровольцев представлены в таблице (данные одного добровольца не были использованы из-за технических проблем).
Таблица 1
Демографические данные пациентов с слизистой оболочкой Барретта или эзофагитом и здоровых добровольцев
| Параметры | Пациенты с пищеводом Барретта ( n = 24) | Пациенты с эзофагитом ( n = 21) | Контроли ( n = 19) | Значение Пат.с Barrett vs Controls |
|---|---|---|---|---|
| Возраст (средний) | 57 лет | 58 лет | 51 год | – |
| Мин. 39–62 года | ||||
| Пол м: ж | 16: 8 | 11:10 | 11: 8 | нс |
| ИМТ (медиана) мин – макс | 27,0 кг / м 2 (18,6–33,1) | 26.9 кг / м 2 (17,9–31,5) | 24,1 кг / м 2 (19,62–27,34) | p = 0,003 |
| Курильщики (%) | n = 5 (20,8 ) | n = 4 (19,0) | n = 6 (31,6) | нс |
| Без спирта% | n = 3 (12,5) | n = 5 (23,8) | n = 5 (26,3) | n.s. |
Кислый желудочный рефлюкс (AGR)
Пациенты с пищеводом Барретта, 19 из 24 (79%) и 20 из 21 контрольных пациентов с эзофагитом (95%) имели патологические AGR [pH <4 в> 5% от общего числа измерения времени (TMT)], но также у 6 из 19 здоровых контролей (32%) наблюдались патологические AGR без каких-либо симптомов ( p = 0.002). Во время TMT средний AGR составил 10,6% для пациентов Barrett и 3,2% для контрольной группы ( p <0,01). В частности, измерения длительного кислотного рефлюкса (LAR), определяемого как pH рефлюкса <4, длящегося более 5 минут, показали значительные различия между пациентами и контрольной группой. Патологический AGR был обнаружен у пациентов в период измерения натощак как в положении лежа на спине, так и в вертикальном положении. Напротив, патологические AGR у здоровых людей наблюдались только в вертикальном положении (таблица).
Таблица 2
Медиана кислотного желудочного рефлюкса в пищевод у пациентов с BM или с эзофагитом и в здоровой контрольной группе
| Параметры | Пациенты с пищеводом Барретта ( n = 24) [медиана (LQ-UQ )] | Пациенты с эзофагитом ( n = 21) [медиана (LQ-UQ)] | Контрольная группа ( n = 19) [медиана (LQ-UQ)] | Значение Пат.с Barrett vs Controls |
|---|---|---|---|---|
| Процент от общего времени измерения pH <4 (%) | 10,6 (6,2–38,3) | 19,9 (1,6–71,7) | 3,2 (0,9–5,5) | p = 0,01 |
| Процент времени измерения в вертикальном положении pH <4 (%) | 11,7 (6,03–6,4) | 18,9 (8,7–60,8) | 2,4 (0,9–6,1) | p <0,05 |
| Процент времени измерения в положении лежа на спине pH <4 (%) | 10.9 (0,4–27,1) | 6,3 (0,0–13,3) | 0,3 (0,0–4,2) | p = 0,004 |
24-часовой мониторинг внутрижелудочного pH и желчи
Мониторинг pH желудка не показал значимых различия между пациентами и контрольной группой для всех периодов измерения (таблица). Воздействие желудочного билирубина, указывающее на билиарный рефлюкс, было значительно более частым у пациентов, чем в контрольной группе, в течение всех периодов измерения (таблица). Воздействие желчных путей в положении лежа на спине обычно происходило в ранние утренние часы во время сна, что выражалось увеличением абсорбции в течение 2–3 часов с быстрым возвращением к исходным значениям примерно в то время, когда субъект снова возвращался в вертикальное положение.За тот же период времени мониторинг pH желудка показал повышение уровня pH до более чем 2 (рис.).
Таблица 3
Результаты 24-часового внутрижелудочного мониторинга pH и желчи у пациентов с пищеводом Барретта и здоровой контрольной группы
| Параметры | Пациенты ( n = 24) [медиана (LQ – UQ)] | Контроли ( n = 19) [Медиана (LQ – UQ)] | Значимость |
|---|---|---|---|
| Медиана внутрижелудочного pH во время TMT | 1.3 (1,0–1,4) | 1,4 (1,1–1,7) | н.с. |
| Процент воздействия билирубина (%) TMT | 7,8 (1,6–17,8) | 0,0 (0,0–1,0) | p = 0,001 |
| Процент воздействия билирубина (%) в прямом эфире | 6,9 (0,1–12,9) | 0,0 (0,0–1,3) | p <0,01 |
| Процент воздействия билирубина (%) во время пребывания на спине | 2,0 (0,0–28,6) | 0.0 (0,0–0,0) | p = 0,001 |
24-часовой внутрижелудочный мониторинг pH и желчи у пациента с пищеводом Барретта, демонстрирующего дуоденогастральный рефлюкс ранним утром. а. Bilitec®-мониторинг, б. pH-мониторинг.
Воздействие билирубина на пищевод
По результатам TMT медиана желчного рефлюкса пищевода составила 7,8% для пациентов с пищеводом Барретта (LQ – UQ = 1,6–17,8%) и 3,5 (LQ – UQ = 0,1–13,5) для контроля пациентов, в отличие от 0% для контроля (LQ – UQ = 0–1.0%), р = 0,001). На рисунке показано, что мониторинг желчи пищевода у пациентов с пищеводом Барретта и здоровых людей в контрольной группе варьировался в течение всего периода измерения и периода лежа на спине.
Результаты мониторинга желчи в пищеводе у 24 пациентов с пищеводом Барретта, 21 пациента с эзофагитом и 19 здоровых людей из контрольной группы а) общий период измерения (тест Краскела-Уоллиса = 0,01) б) период лежа на спине (тест Краскала-Уоллиса p = 0,01) .
Рабочая кривая приемника, отображающая процент истинных положительных результатов (пациенты с пищеводом Барретта, идентифицированные по воздействию билирубина) в зависимости от частоты ложных срабатываний (здоровые контроли с высоким уровнем воздействия билирубина), показана на рис.. С площадью под кривой 0,78 (95% ДИ = 0,56–0,89) ROC-анализ мониторинга желчевыводящих путей показал оптимальное значение для пациентов при 1% TMT [чувствительность 75% (95% ДИ = 53–90%). , Специфичность 84% (95% ДИ = 60–96%)]. Следовательно, пороговое значение для различения нормального и патологического билиарного рефлюкса с использованием 24-часового мониторинга желчевыводящих путей в пищеводе (порог поглощения> 0,25) должно быть зафиксировано на уровне 1% от TMT.
ROC-кривая с 95% доверительным интервалом для патологического мониторинга желчи у пациентов с пищеводом Барретта по сравнению со здоровыми контрольными пациентами, соответствующими возрасту и полу.
пациентов Барретта, 18 из 24 (75%), 15 из 21 контрольного пациента с эзофагитом (71%) и 3 из 19 контрольных (16%) показали билирийный рефлюкс в пищевод более 1,1% TMT ( p <0,001). Используя это пороговое значение, ни у одного из контрольных пациентов, у 10 из контрольных пациентов (48%) и у 11 из 24 пациентов с болезнью Барретта (46%) не было патологического воздействия билирубина во время сна.
Обсуждение
Результаты нашего исследования подтверждают, что пациенты с пищеводом Барретта имеют значительно более частый дуоденогастральный рефлюкс в пищевод, чем здоровые люди из контрольной группы того же возраста и пола.Кроме того, этот рефлюкс, измеряемый воздействием кислоты и билирубина, дольше остается в пищеводе, особенно во время сна.
Роль кислотного и некислотного рефлюкса в пищевод как причинного фактора симптомов и поражений слизистой оболочки рассматривалась в ряде исследований. Не только продолжительность, но, возможно, и состав рефлюкса, играет важную роль в развитии таких поражений.13 Круглосуточный внутрижелудочный мониторинг желчи предоставил клиницисту однозначные доказательства чрезмерного дуоденогастрального рефлюкса (DGR) у 41% пациентов. с эндоскопическим эзофагитом, симптомами гастроэзофагеального рефлюкса (ГЭР) и желудочными симптомами, указывающими на ДГР.19 Рефлюкс двенадцатиперстной кишки в желудок, особенно после еды, является физиологическим явлением; 20 тем не менее, билиарный рефлюкс вносит значительный вклад в поражение слизистой оболочки всего желудка 21
В нашем исследовании контрольная группа пациентов с различными степенями тяжести. При эзофагите не было выявлено значительных различий в показателях кислотного или желчного рефлюкса в желудок или пищевод по сравнению с пациентами Барретта. Это может быть вызвано отбором пациентов с эзофагитом, которые были кандидатами на фундопликацию, но обе группы пациентов значительно различались по сравнению со здоровым контролем.Поэтому наши результаты имеют большое клиническое значение, особенно для предоперационной диагностики.
Marshall et al. сравнивали здоровую контрольную группу с пациентами с различными степенями рефлюкс-эзофагита и пищевода Барретта в отношении измерения желчи в желудке.22 В этом исследовании средний возраст контрольных пациентов составлял 25 лет, а пациентов групп I, II , а III – 42, 50 и 60 лет соответственно. Билитек-зонд располагался на 10 см ниже нижнего сфинктера пищевода (LES).Порог поглощения билирубина составлял 0,14, и хотя не было обнаружено различий между группами по ТМТ, воздействие билирубина желудка было выше в положении лежа на спине, чем в вертикальном положении. В текущем исследовании контрольная группа была старше, чем в исследовании Маршалла. Больше дуодено-желудочного рефлюкса было зарегистрировано как у исследуемых, так и у контрольных пациентов во все периоды измерения. Эти результаты могут быть связаны с улучшением условий исследования.
Мы использовали пищеводный порог поглощения билирубина 0,25.Fein et al. [14] в исследовании in vitro абсорбции различных белых блюд показали, что наименьшее влияние пищи во время мониторинга желчи было измерено при абсорбции> 0,25.
Tack et al. сообщили о влиянии консистенции еды на результаты измерений Bilitec у здоровых субъектов.23 Они сравнили две группы молодых людей из контрольной группы. Испытуемые принимали либо только жидкую пищу, не поглощающую свет той же длины волны, что и билирубин, либо твердую пищу, избегая диет, которые влияют на поглощение билирубина.Авторы обнаружили существенные различия между двумя группами, используя порог поглощения билирубина> 0,14 со средним процентным соотношением (межквартильный диапазон) над TMT 10,9% (6,7–19,3) для твердой пищи и 0,3% (0,0–2,8) для жидкой пищи. Основные артефакты приема пищи присутствовали у субъектов, получавших твердую пищу из двух блюд (10%) и без жидкости. В нашем исследовании мы обнаружили такой артефакт приема пищи у одного пациента и одного контроля, но значения поглощения билирубина были ниже 0,25 и, следовательно, не соответствовали нашим результатам.
Гастроэзофагеальный рефлюкс нередко содержит секреции желчи, двенадцатиперстной кишки и поджелудочной железы. Использование спектрофотометрического зонда Bilitec продемонстрировало более высокую распространенность аномального воздействия билирубина пищевода у пациентов с метаплазией Барретта по сравнению с пациентами с эрозивным повреждением или без признаков эзофагита (6,8,10,13). добровольцы включены в контрольную группу. Однако другие исследования показали повышенную распространенность гастроэзофагеального рефлюкса с возрастом.24 По этим причинам мы изучали здоровых людей из контрольной группы по возрасту и полу и пациентов с пищеводом Барретта или с эзофагитом. Мы обнаружили патологическую кислотность и желчный рефлюкс пищевода у одной трети контрольной. Возможно, это может быть вызвано артефактами или нарушением протокола волонтерами. Но в предыдущем опубликованном исследовании мы смогли показать, что у более молодых здоровых людей такого патологического рефлюкса не было.17 Возможно, эти явления вызваны расслаблением, которое чаще встречается у пожилых людей.Напротив, почти все пациенты с пищеводом Барретта (87%) и все пациенты с эзофагитом (100%) показали патологический кислотный рефлюкс и / или желчный рефлюкс, измеренные с помощью комбинированного мониторинга pH и желчи. В частности, рефлюкс желчи в пищевод во время сна был обнаружен только у пациентов с BM или с эзофагитом.
В нашем исследовании мы измерили внутрижелудочный pH и рефлюкс желчи из двенадцатиперстной кишки в желудок (DGR). Медиана внутрижелудочного pH была одинаковой в обеих группах.Но пациенты с пищеводом Барретта имели значительно более длительный дуоденогастральный рефлюкс в течение 24-часового периода измерения, чем контрольная группа. Ночью было продемонстрировано больше ДГР, чем днем, в обеих группах исследуемых пациентов и в контрольной здоровой группе. Согласно ранее опубликованным исследованиям, это могло быть связано с щелочным сдвигом pH. Точный механизм, с помощью которого происходит ночной DGR, и роль, которую играет поза, остаются неясными.
Bowrey et al. не смогли установить ни гастроэзофагеальный, ни дуоденогастральный рефлюкс как преобладающую причину воспаления в слизистой оболочке сердца желудка с использованием прибора Bilitec 2000.16 Это понятно, поскольку количество рефлюкса в желудок (DGR) не обязательно коррелирует с DGER в пищевод. В этом исследовании авторы продемонстрировали больше DGR у женщин в период лежа на спине, в то время как у мужчин было больше DGER. При этом корреляции между уровнями желчи в желудке и пищеводе не было. Однако контрольная группа была намного моложе пациентов. Мы обнаружили значительные различия в измерениях желчи желудка и пищевода между пациентами с BM и контрольной группой.В отличие от Bowrey et al., Мы наблюдали больше DGER у женщин в период лежа на спине и больше DGR у пациентов-мужчин.
Напротив, Banki сообщил об аналогичном воздействии на пищевод рефлюксной кислоты и билирубина у женщин и мужчин со слизистой оболочкой Барретта.28 Pfaffenbach et al. (29) изучали желчь пищевода и кислотный рефлюкс у пациентов с длинным сегментом пищевода Барретта (LSBE) и коротким сегментом пищевода Барретта. пищевода (SSBE) и пациентов с гастроэзофагеальной рефлюксной болезнью (GERD). Субъекты прошли манометрию пищевода и одновременный 24-часовой мониторинг pH и желчи (Bilitec 2000) со значением абсорбции> 0.2 на 10,9% от общего периода. GER не отличался между группами. Однако DGER различалась у пациентов с LSBE (14,7%), SSBE (2,1%) и GERD (2,1%).
Таким образом, анализ эталонных значений показателей кислотности пищевода и рефлюкса желчи в группе здоровых, сопоставимых по возрасту и полу контролей по сравнению с пациентами с BM привел к следующим выводам:
Хотя около 30% здоровых контролей показали кислотный рефлюкс при мониторинге pH, пациенты с BM имели значительно более высокий кислотный рефлюкс в течение всех периодов измерения.
У здоровых людей не было значимого дуодено-желудочно-пищеводного рефлюкса, измеренного по абсорбции билирубина. Особенно в период лежа на спине не было рефлюкса желчи.
Оптимальный порог патологического рефлюкса желчи составляет 1,1% (мониторинг желчи с оптической плотностью 0,25).
Дуодено-желудочно-пищеводный рефлюкс – что такое патологический? Сравнение пациентов с пищеводом Барретта и добровольцев того же возраста
Резюме
Введение
Целью исследования был анализ данных мониторинга pH и желчи у пациентов с пищеводом Барретта и в контрольной группе, сопоставимой по возрасту и полу.
Субъекты и методы
Двадцать четыре последовательных пациента Барретта (8 женщин, 16 мужчин, средний возраст 57 лет), 21 пациент с эзофагитом (10 женщин, 11 мужчин, средний возраст 58 лет) и 19 здоровых пациентов контрольной группы (8 женщин). , 11 мужчин, средний возраст 51 год). Только пациентам проводилась эндоскопия с биопсией. Все группы были исследованы с помощью манометрии, 24-часового pH желудка и пищевода и одновременного мониторинга желчи в соответствии со стандартизованным протоколом. Поглощение билирубина> 0.25 был определен как вредный желчный рефлюкс. Метод характеристики оператора приемника (ROC) был применен для определения оптимального порогового значения уровней патологического билирубина.
Результаты
Из пациентов Барретта у 79% был патологический кислый желудочный рефлюкс (pH <4> 5% от общего времени измерения). Однако у 32% здоровых людей из контрольной группы также был кислотный рефлюкс ( p <0,05) без каких-либо симптомов. Медиана рефлюкса желчи из пищевода составила 7,8% (нижний квартиль (LQ) – верхний квартиль (UQ) = 1).6–17,8%) у пациентов с болезнью Барретта, у пациентов с эзофагитом - 3,5% (LQ – UQ = 0,1–13,5) и, в отличие от 0% (LQ – UQ = 0–1,0%) в контроле, p = 0,001 . ROC-анализ показал оптимальное значение деления для пациентов с рефлюксом желчи более 1% в течение 24 часов (чувствительность 75%, специфичность 84%).
Заключение
Оптимальный порог для различения нормального и патологического рефлюкса желчи в пищевод составляет 1% (24-часовой мониторинг желчи с поглощением> 0,25).
Ключевые слова: Референтное значение bilitec, Рефлюкс желчи, Кислотный рефлюкс, слизистая оболочка Барретта, пищевод, спектрофотометрия
Введение
Уровень заболеваемости аденокарциномой (АК) пищевода и кардии желудка в западных промышленно развитых странах быстро вырос.1 Помимо злоупотребления никотином и алкоголем, факторы питания, высокий индекс массы тела, кислый желудочный рефлюкс и пищевод Барретта считаются критическими факторами канцерогенеза. 2–4 Недавние исследования показали, что наличие желчного рефлюкса в сочетании с кислым желудочным рефлюксом. повреждает слизистую оболочку пищевода и вызывает осложнения гастроэзофагеальной рефлюксной болезни (ГЭРБ), например, развитие слизистой оболочки Барретта (ВМ) .5,6 Дуодено-желудочный рефлюкс в пищевод (ДГЭР), в частности, важен для патогенез пищевода Барретта.7 Продолжительные исследования аспирации пищевода документально подтвердили повышение уровня желчных кислот у пациентов с тяжелым эзофагитом и пищеводом Барретта. 8 Восемьдесят процентов пациентов с пищеводом Барретта, принимающим ингибиторы протонной помпы, демонстрируют нормальный профиль pH пищевода, но 60% показывают аномальное воздействие желчи в пищевод, как измерено. by Bilitec 2000.9
В прошлом прямая и продолжительная количественная оценка дуоденоэзофагеального рефлюкса была труднодостижимой. Теперь концентрацию билирубина можно напрямую измерить спектрофотометрией на основе удельного поглощения на длине волны 453 нм.Билиарный рефлюкс можно измерить с помощью амбулаторного фиброоптического зонда, проходящего через нос (Bilitec 2000), который регистрирует всасывание желчи. Уже опубликован ряд работ по обнажению пищевода10–13 и желудка24–16 с использованием этой техники. Однако в этих исследованиях возраст контрольной группы составлял от 25 до 35 лет. В клинической практике пациенты со слизистой оболочкой Барретта обычно старше. Кроме того, авторы каждого исследования использовали различные контрольные значения для измерения билиарного рефлюкса в пищеводе, что затрудняло сравнение измеренных значений.
Целью настоящего исследования был анализ данных мониторинга pH и желчи в группе здоровых лиц из контрольной группы, соответствующих возрасту и полу, и пациентов с пищеводом Барретта.
Субъекты и методы
Субъекты
Отбор контролей проводился в соответствии со строгим протоколом. В исследование были включены здоровые добровольцы, лечившиеся с 1999 по 2000 год, в возрасте от 40 до 60 лет. Никто из контрольных не принимал препараты, подавляющие кислоту или перистальтику кишечника, не имел в анамнезе заболеваний верхних отделов желудочно-кишечного тракта, не подвергался хирургическим вмешательствам на верхних отделах брюшной полости или обширным операциям на брюшной полости, а также не подвергался терапевтическим эндоскопическим процедурам верхних отделов желудочно-кишечного тракта.Диагностическая эндоскопия и проглатывание бария не проводились, но желчнокаменная болезнь была исключена на УЗИ.
С 1999 по 2002 год в исследование были включены 24 пациента с гистологически подтвержденной слизистой оболочкой Барретта. Для дополнительного сравнения мы включили группу пациентов с эзофагитом (стадия I – III по Савари и Миллеру) без пищевода Барретта, которым перед плановой лапароскопической фундопликацией были выполнены те же диагностические процедуры. В течение вышеупомянутого периода для этого исследования был доступен 21 пациент в возрасте старше 40 лет.Критериями исключения были хирургия пищевода, желудка или желчевыводящих путей в анамнезе, лучевая терапия брюшной или грудной клетки в анамнезе или наличие язвенной болезни, активное желудочно-кишечное кровотечение, варикозное расширение вен пищевода или дна, хроническое заболевание пищевода или верхних отделов тонкой кишки или опухолевые заболевания. Все препараты, потенциально влияющие на перистальтику желудочно-кишечного тракта и секрецию, были отменены по крайней мере за 1 неделю до исследования.
Эндоскопия верхних отделов желудочно-кишечного тракта
Всем пациентам была выполнена классическая эндоскопия верхних отделов желудочно-кишечного тракта.Если была необходима седация, обычно применяли внутривенное введение пропофола (до 200 мг) или изредка применяли мидазолам (до 5 мг). Во время эндоскопии было отмечено наличие и степень эзофагита, пищевода Барретта и грыжи пищеводного отверстия диафрагмы. Биопсии были взяты со слизистой оболочки Барретта.
Амбулаторный мониторинг pH пищевода / желудка и желчи
Все группы прошли манометрию пищевода и 24-часовой мониторинг pH и одновременный мониторинг желчи с использованием стандартизованного протокола.Амбулаторный мониторинг pH выполнялся с использованием трансназально введенного сурьмяного pH-электрода с отдельным кожным электродом сравнения (Synetics Medical, Стокгольм, Швеция). Данные сохранялись на портативном цифровом записывающем устройстве (Digitrapper MkIII, Synectics Medical Stockholm, Швеция). Перед каждым исследованием зонд pH калибровали в буферных растворах с pH 7 и 1. Эпизод кислотного рефлюкса определялся как снижение pH пищевода до менее 4 в течение более 10 с.
Для количественной оценки дуодено-пищеводного рефлюкса использовался амбулаторный фиброоптический спектрофотометр, переданный через нос (Bilitec 2000, Synectics, Швеция).Система состоит из миниатюрного зонда диаметром 1,5 мм, который передает световые сигналы в пищевод и обратно через пластиковую волоконно-оптическую связку. Перед каждым исследованием зонд калибровали в воде. В соответствии с текущей литературой, абсорбция билирубина> 0,25 использовалась в качестве эталона для вредного билиарного рефлюкса.14
Зонды желчи и pH были скреплены вместе и прошли трансназально в пищевод и желудок, как подробно описано в другом месте.17 Верхняя часть кончики зондов были расположены на 5 см выше верхней границы нижнего сфинктера пищевода, как определено манометрией пищевода.Дистальный pH-электрод и оптоволоконный датчик помещали на дно желудка на 10 см дистальнее нижнего сфинктера пищевода (рис.). Контрольной группы и пациентов просили следовать строгому протоколу трехразового питания без жидкости между приемами пищи. Лежачие фазы записи разрешались только ночью. Пациентов просили вести дневник, фиксируя точный характер приема пищи, фазы измерения в положении лежа на спине и прямо, а также ощущения изжоги и срыгивания.
Расположение датчиков pH и билирубина в желудке и пищеводе.(UES = верхний сфинктер пищевода; LES = нижний сфинктер пищевода).
Одновременный мониторинг желчных протоков и pH проводился с применением бесцветной «белой диеты» (WD), включающей жидкую и твердую пищу с максимальным поглощением желчи in vitro 0,25 [шкала поглощения от 0 (обычная вода) до 1 (общая экран)]. Еда включала воду, молоко, тосты, картофель, курицу, сухое печенье и рыбу.
Сбор и интерпретация данных
После завершения измерений зонды у пациентов извлекались, и данные сохранялись через интерфейс на IBM-совместимом компьютере, оснащенном программным обеспечением Polygram® (Medtronic).Для анализа использовались данные каждой секунды 24-часовых измерений. Чтобы оценить наличие желудочного или пищеводного билиарного рефлюкса, был рассчитан процент времени, когда абсорбция была больше 0,25 для следующих периодов: всего в положении лежа на спине, в вертикальном положении и после приема пищи. Постпрандиальный период определялся как 2 ч после окончания приема пищи. Процент времени с pH пищевода ниже 4 и медианным pH желудка и процент времени с pH желудка, измеряющим 1, 2, 3–7 и> 7, также был рассчитан для вышеуказанных периодов.Средняя продолжительность амбулаторного мониторингового исследования pH и Bilitec составляла 22 часа 40 минут у пациентов и 23 часа 44 минуты в контрольной группе.
Статистический анализ
Для анализа результатов использовалась программа SPSS (версия 11.0, Чикаго, Иллинойс). Для графического представления использовалась программа MedCalc для Windows (версия 9.0, MedCalc Software, Бельгия). Были установлены медианы, значения межквартильного размаха (IQR или 25–75 перцентиль). Непараметрические тесты (анализ Манна – Уитни и Краскела – Уоллиса) использовались для оценки взаимосвязи между переменными.Для представления некоторых данных использовались графики Box и Whisker. На этих графиках прямоугольник представляет IQR, а усы – самые высокие и самые низкие значения. Также нанесены выбросы, определенные как более чем в 1,5 раза превышающие IQR от 75-го центиля. Экстремальные значения были определены как более чем трехкратный IQR от 75-го центиля.
Кривая характеристики оператора приемника (ROC) использовалась для определения порогового значения для оптимальной чувствительности и специфичности согласно Цвейгу и Кэмпбеллу18. Площадь под кривой (AUC) использовалась как измерение диагностической эффективности теста.Результаты представлены в виде точек с доверительным интервалом 95% (95% ДИ) и графически для представления всех данных. В качестве положительной группы мы использовали пациентов со слизистой оболочкой Барретта, а отрицательную тестовую группу определяли здоровыми добровольцами. Предполагалось непараметрическое распределение площади под кривой.
Предположения для расчета требуемого размера выборки были альфа = 0,05, бета = 0,80, и что тест действителен для ежедневного использования только в том случае, если менее 20% здоровых контролей и не менее 80% пациентов имеют положительный результат теста. полученные результаты.Расчетный размер выборки для каждой группы составил 20.
Этика
Протокол исследования был одобрен этическим комитетом Кельнского университета. Каждый субъект дал письменное информированное согласие.
Результаты
В исследование были включены 24 пациента с пищеводом Барретта (средний возраст: 58 лет), 21 пациент с эзофагитом (средний возраст: 57 лет) и 19 здоровых людей контрольной группы со средним возрастом 51 год. У пациентов с БМ выявлен эзофагит 0 степени (4 случая), I степени (12 случаев) и II степени (8 случаев).В контрольной группе пациентов с эзофагитом было девять случаев с I степенью, восемь случаев со II степенью и три случая с III степенью. Демографические данные пациентов и добровольцев представлены в таблице (данные одного добровольца не были использованы из-за технических проблем).
Таблица 1
Демографические данные пациентов с слизистой оболочкой Барретта или эзофагитом и здоровых добровольцев
| Параметры | Пациенты с пищеводом Барретта ( n = 24) | Пациенты с эзофагитом ( n = 21) | Контроли ( n = 19) | Значение Пат.с Barrett vs Controls |
|---|---|---|---|---|
| Возраст (средний) | 57 лет | 58 лет | 51 год | – |
| Мин. 39–62 года | ||||
| Пол м: ж | 16: 8 | 11:10 | 11: 8 | нс |
| ИМТ (медиана) мин – макс | 27,0 кг / м 2 (18,6–33,1) | 26.9 кг / м 2 (17,9–31,5) | 24,1 кг / м 2 (19,62–27,34) | p = 0,003 |
| Курильщики (%) | n = 5 (20,8 ) | n = 4 (19,0) | n = 6 (31,6) | нс |
| Без спирта% | n = 3 (12,5) | n = 5 (23,8) | n = 5 (26,3) | n.s. |
Кислый желудочный рефлюкс (AGR)
Пациенты с пищеводом Барретта, 19 из 24 (79%) и 20 из 21 контрольных пациентов с эзофагитом (95%) имели патологические AGR [pH <4 в> 5% от общего числа измерения времени (TMT)], но также у 6 из 19 здоровых контролей (32%) наблюдались патологические AGR без каких-либо симптомов ( p = 0.002). Во время TMT средний AGR составил 10,6% для пациентов Barrett и 3,2% для контрольной группы ( p <0,01). В частности, измерения длительного кислотного рефлюкса (LAR), определяемого как pH рефлюкса <4, длящегося более 5 минут, показали значительные различия между пациентами и контрольной группой. Патологический AGR был обнаружен у пациентов в период измерения натощак как в положении лежа на спине, так и в вертикальном положении. Напротив, патологические AGR у здоровых людей наблюдались только в вертикальном положении (таблица).
Таблица 2
Медиана кислотного желудочного рефлюкса в пищевод у пациентов с BM или с эзофагитом и в здоровой контрольной группе
| Параметры | Пациенты с пищеводом Барретта ( n = 24) [медиана (LQ-UQ )] | Пациенты с эзофагитом ( n = 21) [медиана (LQ-UQ)] | Контрольная группа ( n = 19) [медиана (LQ-UQ)] | Значение Пат.с Barrett vs Controls |
|---|---|---|---|---|
| Процент от общего времени измерения pH <4 (%) | 10,6 (6,2–38,3) | 19,9 (1,6–71,7) | 3,2 (0,9–5,5) | p = 0,01 |
| Процент времени измерения в вертикальном положении pH <4 (%) | 11,7 (6,03–6,4) | 18,9 (8,7–60,8) | 2,4 (0,9–6,1) | p <0,05 |
| Процент времени измерения в положении лежа на спине pH <4 (%) | 10.9 (0,4–27,1) | 6,3 (0,0–13,3) | 0,3 (0,0–4,2) | p = 0,004 |
24-часовой мониторинг внутрижелудочного pH и желчи
Мониторинг pH желудка не показал значимых различия между пациентами и контрольной группой для всех периодов измерения (таблица). Воздействие желудочного билирубина, указывающее на билиарный рефлюкс, было значительно более частым у пациентов, чем в контрольной группе, в течение всех периодов измерения (таблица). Воздействие желчных путей в положении лежа на спине обычно происходило в ранние утренние часы во время сна, что выражалось увеличением абсорбции в течение 2–3 часов с быстрым возвращением к исходным значениям примерно в то время, когда субъект снова возвращался в вертикальное положение.За тот же период времени мониторинг pH желудка показал повышение уровня pH до более чем 2 (рис.).
Таблица 3
Результаты 24-часового внутрижелудочного мониторинга pH и желчи у пациентов с пищеводом Барретта и здоровой контрольной группы
| Параметры | Пациенты ( n = 24) [медиана (LQ – UQ)] | Контроли ( n = 19) [Медиана (LQ – UQ)] | Значимость |
|---|---|---|---|
| Медиана внутрижелудочного pH во время TMT | 1.3 (1,0–1,4) | 1,4 (1,1–1,7) | н.с. |
| Процент воздействия билирубина (%) TMT | 7,8 (1,6–17,8) | 0,0 (0,0–1,0) | p = 0,001 |
| Процент воздействия билирубина (%) в прямом эфире | 6,9 (0,1–12,9) | 0,0 (0,0–1,3) | p <0,01 |
| Процент воздействия билирубина (%) во время пребывания на спине | 2,0 (0,0–28,6) | 0.0 (0,0–0,0) | p = 0,001 |
24-часовой внутрижелудочный мониторинг pH и желчи у пациента с пищеводом Барретта, демонстрирующего дуоденогастральный рефлюкс ранним утром. а. Bilitec®-мониторинг, б. pH-мониторинг.
Воздействие билирубина на пищевод
По результатам TMT медиана желчного рефлюкса пищевода составила 7,8% для пациентов с пищеводом Барретта (LQ – UQ = 1,6–17,8%) и 3,5 (LQ – UQ = 0,1–13,5) для контроля пациентов, в отличие от 0% для контроля (LQ – UQ = 0–1.0%), р = 0,001). На рисунке показано, что мониторинг желчи пищевода у пациентов с пищеводом Барретта и здоровых людей в контрольной группе варьировался в течение всего периода измерения и периода лежа на спине.
Результаты мониторинга желчи в пищеводе у 24 пациентов с пищеводом Барретта, 21 пациента с эзофагитом и 19 здоровых людей из контрольной группы а) общий период измерения (тест Краскела-Уоллиса = 0,01) б) период лежа на спине (тест Краскала-Уоллиса p = 0,01) .
Рабочая кривая приемника, отображающая процент истинных положительных результатов (пациенты с пищеводом Барретта, идентифицированные по воздействию билирубина) в зависимости от частоты ложных срабатываний (здоровые контроли с высоким уровнем воздействия билирубина), показана на рис.. С площадью под кривой 0,78 (95% ДИ = 0,56–0,89) ROC-анализ мониторинга желчевыводящих путей показал оптимальное значение для пациентов при 1% TMT [чувствительность 75% (95% ДИ = 53–90%). , Специфичность 84% (95% ДИ = 60–96%)]. Следовательно, пороговое значение для различения нормального и патологического билиарного рефлюкса с использованием 24-часового мониторинга желчевыводящих путей в пищеводе (порог поглощения> 0,25) должно быть зафиксировано на уровне 1% от TMT.
ROC-кривая с 95% доверительным интервалом для патологического мониторинга желчи у пациентов с пищеводом Барретта по сравнению со здоровыми контрольными пациентами, соответствующими возрасту и полу.
пациентов Барретта, 18 из 24 (75%), 15 из 21 контрольного пациента с эзофагитом (71%) и 3 из 19 контрольных (16%) показали билирийный рефлюкс в пищевод более 1,1% TMT ( p <0,001). Используя это пороговое значение, ни у одного из контрольных пациентов, у 10 из контрольных пациентов (48%) и у 11 из 24 пациентов с болезнью Барретта (46%) не было патологического воздействия билирубина во время сна.
Обсуждение
Результаты нашего исследования подтверждают, что пациенты с пищеводом Барретта имеют значительно более частый дуоденогастральный рефлюкс в пищевод, чем здоровые люди из контрольной группы того же возраста и пола.Кроме того, этот рефлюкс, измеряемый воздействием кислоты и билирубина, дольше остается в пищеводе, особенно во время сна.
Роль кислотного и некислотного рефлюкса в пищевод как причинного фактора симптомов и поражений слизистой оболочки рассматривалась в ряде исследований. Не только продолжительность, но, возможно, и состав рефлюкса, играет важную роль в развитии таких поражений.13 Круглосуточный внутрижелудочный мониторинг желчи предоставил клиницисту однозначные доказательства чрезмерного дуоденогастрального рефлюкса (DGR) у 41% пациентов. с эндоскопическим эзофагитом, симптомами гастроэзофагеального рефлюкса (ГЭР) и желудочными симптомами, указывающими на ДГР.19 Рефлюкс двенадцатиперстной кишки в желудок, особенно после еды, является физиологическим явлением; 20 тем не менее, билиарный рефлюкс вносит значительный вклад в поражение слизистой оболочки всего желудка 21
В нашем исследовании контрольная группа пациентов с различными степенями тяжести. При эзофагите не было выявлено значительных различий в показателях кислотного или желчного рефлюкса в желудок или пищевод по сравнению с пациентами Барретта. Это может быть вызвано отбором пациентов с эзофагитом, которые были кандидатами на фундопликацию, но обе группы пациентов значительно различались по сравнению со здоровым контролем.Поэтому наши результаты имеют большое клиническое значение, особенно для предоперационной диагностики.
Marshall et al. сравнивали здоровую контрольную группу с пациентами с различными степенями рефлюкс-эзофагита и пищевода Барретта в отношении измерения желчи в желудке.22 В этом исследовании средний возраст контрольных пациентов составлял 25 лет, а пациентов групп I, II , а III – 42, 50 и 60 лет соответственно. Билитек-зонд располагался на 10 см ниже нижнего сфинктера пищевода (LES).Порог поглощения билирубина составлял 0,14, и хотя не было обнаружено различий между группами по ТМТ, воздействие билирубина желудка было выше в положении лежа на спине, чем в вертикальном положении. В текущем исследовании контрольная группа была старше, чем в исследовании Маршалла. Больше дуодено-желудочного рефлюкса было зарегистрировано как у исследуемых, так и у контрольных пациентов во все периоды измерения. Эти результаты могут быть связаны с улучшением условий исследования.
Мы использовали пищеводный порог поглощения билирубина 0,25.Fein et al. [14] в исследовании in vitro абсорбции различных белых блюд показали, что наименьшее влияние пищи во время мониторинга желчи было измерено при абсорбции> 0,25.
Tack et al. сообщили о влиянии консистенции еды на результаты измерений Bilitec у здоровых субъектов.23 Они сравнили две группы молодых людей из контрольной группы. Испытуемые принимали либо только жидкую пищу, не поглощающую свет той же длины волны, что и билирубин, либо твердую пищу, избегая диет, которые влияют на поглощение билирубина.Авторы обнаружили существенные различия между двумя группами, используя порог поглощения билирубина> 0,14 со средним процентным соотношением (межквартильный диапазон) над TMT 10,9% (6,7–19,3) для твердой пищи и 0,3% (0,0–2,8) для жидкой пищи. Основные артефакты приема пищи присутствовали у субъектов, получавших твердую пищу из двух блюд (10%) и без жидкости. В нашем исследовании мы обнаружили такой артефакт приема пищи у одного пациента и одного контроля, но значения поглощения билирубина были ниже 0,25 и, следовательно, не соответствовали нашим результатам.
Гастроэзофагеальный рефлюкс нередко содержит секреции желчи, двенадцатиперстной кишки и поджелудочной железы. Использование спектрофотометрического зонда Bilitec продемонстрировало более высокую распространенность аномального воздействия билирубина пищевода у пациентов с метаплазией Барретта по сравнению с пациентами с эрозивным повреждением или без признаков эзофагита (6,8,10,13). добровольцы включены в контрольную группу. Однако другие исследования показали повышенную распространенность гастроэзофагеального рефлюкса с возрастом.24 По этим причинам мы изучали здоровых людей из контрольной группы по возрасту и полу и пациентов с пищеводом Барретта или с эзофагитом. Мы обнаружили патологическую кислотность и желчный рефлюкс пищевода у одной трети контрольной. Возможно, это может быть вызвано артефактами или нарушением протокола волонтерами. Но в предыдущем опубликованном исследовании мы смогли показать, что у более молодых здоровых людей такого патологического рефлюкса не было.17 Возможно, эти явления вызваны расслаблением, которое чаще встречается у пожилых людей.Напротив, почти все пациенты с пищеводом Барретта (87%) и все пациенты с эзофагитом (100%) показали патологический кислотный рефлюкс и / или желчный рефлюкс, измеренные с помощью комбинированного мониторинга pH и желчи. В частности, рефлюкс желчи в пищевод во время сна был обнаружен только у пациентов с BM или с эзофагитом.
В нашем исследовании мы измерили внутрижелудочный pH и рефлюкс желчи из двенадцатиперстной кишки в желудок (DGR). Медиана внутрижелудочного pH была одинаковой в обеих группах.Но пациенты с пищеводом Барретта имели значительно более длительный дуоденогастральный рефлюкс в течение 24-часового периода измерения, чем контрольная группа. Ночью было продемонстрировано больше ДГР, чем днем, в обеих группах исследуемых пациентов и в контрольной здоровой группе. Согласно ранее опубликованным исследованиям, это могло быть связано с щелочным сдвигом pH. Точный механизм, с помощью которого происходит ночной DGR, и роль, которую играет поза, остаются неясными.
Bowrey et al. не смогли установить ни гастроэзофагеальный, ни дуоденогастральный рефлюкс как преобладающую причину воспаления в слизистой оболочке сердца желудка с использованием прибора Bilitec 2000.16 Это понятно, поскольку количество рефлюкса в желудок (DGR) не обязательно коррелирует с DGER в пищевод. В этом исследовании авторы продемонстрировали больше DGR у женщин в период лежа на спине, в то время как у мужчин было больше DGER. При этом корреляции между уровнями желчи в желудке и пищеводе не было. Однако контрольная группа была намного моложе пациентов. Мы обнаружили значительные различия в измерениях желчи желудка и пищевода между пациентами с BM и контрольной группой.В отличие от Bowrey et al., Мы наблюдали больше DGER у женщин в период лежа на спине и больше DGR у пациентов-мужчин.
Напротив, Banki сообщил об аналогичном воздействии на пищевод рефлюксной кислоты и билирубина у женщин и мужчин со слизистой оболочкой Барретта.28 Pfaffenbach et al. (29) изучали желчь пищевода и кислотный рефлюкс у пациентов с длинным сегментом пищевода Барретта (LSBE) и коротким сегментом пищевода Барретта. пищевода (SSBE) и пациентов с гастроэзофагеальной рефлюксной болезнью (GERD). Субъекты прошли манометрию пищевода и одновременный 24-часовой мониторинг pH и желчи (Bilitec 2000) со значением абсорбции> 0.2 на 10,9% от общего периода. GER не отличался между группами. Однако DGER различалась у пациентов с LSBE (14,7%), SSBE (2,1%) и GERD (2,1%).
Таким образом, анализ эталонных значений показателей кислотности пищевода и рефлюкса желчи в группе здоровых, сопоставимых по возрасту и полу контролей по сравнению с пациентами с BM привел к следующим выводам:
Хотя около 30% здоровых контролей показали кислотный рефлюкс при мониторинге pH, пациенты с BM имели значительно более высокий кислотный рефлюкс в течение всех периодов измерения.
У здоровых людей не было значимого дуодено-желудочно-пищеводного рефлюкса, измеренного по абсорбции билирубина. Особенно в период лежа на спине не было рефлюкса желчи.
Оптимальный порог патологического рефлюкса желчи составляет 1,1% (мониторинг желчи с оптической плотностью 0,25).
Дуодено-желудочно-пищеводный рефлюкс – что такое патологический? Сравнение пациентов с пищеводом Барретта и добровольцев того же возраста
Резюме
Введение
Целью исследования был анализ данных мониторинга pH и желчи у пациентов с пищеводом Барретта и в контрольной группе, сопоставимой по возрасту и полу.
Субъекты и методы
Двадцать четыре последовательных пациента Барретта (8 женщин, 16 мужчин, средний возраст 57 лет), 21 пациент с эзофагитом (10 женщин, 11 мужчин, средний возраст 58 лет) и 19 здоровых пациентов контрольной группы (8 женщин). , 11 мужчин, средний возраст 51 год). Только пациентам проводилась эндоскопия с биопсией. Все группы были исследованы с помощью манометрии, 24-часового pH желудка и пищевода и одновременного мониторинга желчи в соответствии со стандартизованным протоколом. Поглощение билирубина> 0.25 был определен как вредный желчный рефлюкс. Метод характеристики оператора приемника (ROC) был применен для определения оптимального порогового значения уровней патологического билирубина.
Результаты
Из пациентов Барретта у 79% был патологический кислый желудочный рефлюкс (pH <4> 5% от общего времени измерения). Однако у 32% здоровых людей из контрольной группы также был кислотный рефлюкс ( p <0,05) без каких-либо симптомов. Медиана рефлюкса желчи из пищевода составила 7,8% (нижний квартиль (LQ) – верхний квартиль (UQ) = 1).6–17,8%) у пациентов с болезнью Барретта, у пациентов с эзофагитом - 3,5% (LQ – UQ = 0,1–13,5) и, в отличие от 0% (LQ – UQ = 0–1,0%) в контроле, p = 0,001 . ROC-анализ показал оптимальное значение деления для пациентов с рефлюксом желчи более 1% в течение 24 часов (чувствительность 75%, специфичность 84%).
Заключение
Оптимальный порог для различения нормального и патологического рефлюкса желчи в пищевод составляет 1% (24-часовой мониторинг желчи с поглощением> 0,25).
Ключевые слова: Референтное значение bilitec, Рефлюкс желчи, Кислотный рефлюкс, слизистая оболочка Барретта, пищевод, спектрофотометрия
Введение
Уровень заболеваемости аденокарциномой (АК) пищевода и кардии желудка в западных промышленно развитых странах быстро вырос.1 Помимо злоупотребления никотином и алкоголем, факторы питания, высокий индекс массы тела, кислый желудочный рефлюкс и пищевод Барретта считаются критическими факторами канцерогенеза. 2–4 Недавние исследования показали, что наличие желчного рефлюкса в сочетании с кислым желудочным рефлюксом. повреждает слизистую оболочку пищевода и вызывает осложнения гастроэзофагеальной рефлюксной болезни (ГЭРБ), например, развитие слизистой оболочки Барретта (ВМ) .5,6 Дуодено-желудочный рефлюкс в пищевод (ДГЭР), в частности, важен для патогенез пищевода Барретта.7 Продолжительные исследования аспирации пищевода документально подтвердили повышение уровня желчных кислот у пациентов с тяжелым эзофагитом и пищеводом Барретта. 8 Восемьдесят процентов пациентов с пищеводом Барретта, принимающим ингибиторы протонной помпы, демонстрируют нормальный профиль pH пищевода, но 60% показывают аномальное воздействие желчи в пищевод, как измерено. by Bilitec 2000.9
В прошлом прямая и продолжительная количественная оценка дуоденоэзофагеального рефлюкса была труднодостижимой. Теперь концентрацию билирубина можно напрямую измерить спектрофотометрией на основе удельного поглощения на длине волны 453 нм.Билиарный рефлюкс можно измерить с помощью амбулаторного фиброоптического зонда, проходящего через нос (Bilitec 2000), который регистрирует всасывание желчи. Уже опубликован ряд работ по обнажению пищевода10–13 и желудка24–16 с использованием этой техники. Однако в этих исследованиях возраст контрольной группы составлял от 25 до 35 лет. В клинической практике пациенты со слизистой оболочкой Барретта обычно старше. Кроме того, авторы каждого исследования использовали различные контрольные значения для измерения билиарного рефлюкса в пищеводе, что затрудняло сравнение измеренных значений.
Целью настоящего исследования был анализ данных мониторинга pH и желчи в группе здоровых лиц из контрольной группы, соответствующих возрасту и полу, и пациентов с пищеводом Барретта.
Субъекты и методы
Субъекты
Отбор контролей проводился в соответствии со строгим протоколом. В исследование были включены здоровые добровольцы, лечившиеся с 1999 по 2000 год, в возрасте от 40 до 60 лет. Никто из контрольных не принимал препараты, подавляющие кислоту или перистальтику кишечника, не имел в анамнезе заболеваний верхних отделов желудочно-кишечного тракта, не подвергался хирургическим вмешательствам на верхних отделах брюшной полости или обширным операциям на брюшной полости, а также не подвергался терапевтическим эндоскопическим процедурам верхних отделов желудочно-кишечного тракта.Диагностическая эндоскопия и проглатывание бария не проводились, но желчнокаменная болезнь была исключена на УЗИ.
С 1999 по 2002 год в исследование были включены 24 пациента с гистологически подтвержденной слизистой оболочкой Барретта. Для дополнительного сравнения мы включили группу пациентов с эзофагитом (стадия I – III по Савари и Миллеру) без пищевода Барретта, которым перед плановой лапароскопической фундопликацией были выполнены те же диагностические процедуры. В течение вышеупомянутого периода для этого исследования был доступен 21 пациент в возрасте старше 40 лет.Критериями исключения были хирургия пищевода, желудка или желчевыводящих путей в анамнезе, лучевая терапия брюшной или грудной клетки в анамнезе или наличие язвенной болезни, активное желудочно-кишечное кровотечение, варикозное расширение вен пищевода или дна, хроническое заболевание пищевода или верхних отделов тонкой кишки или опухолевые заболевания. Все препараты, потенциально влияющие на перистальтику желудочно-кишечного тракта и секрецию, были отменены по крайней мере за 1 неделю до исследования.
Эндоскопия верхних отделов желудочно-кишечного тракта
Всем пациентам была выполнена классическая эндоскопия верхних отделов желудочно-кишечного тракта.Если была необходима седация, обычно применяли внутривенное введение пропофола (до 200 мг) или изредка применяли мидазолам (до 5 мг). Во время эндоскопии было отмечено наличие и степень эзофагита, пищевода Барретта и грыжи пищеводного отверстия диафрагмы. Биопсии были взяты со слизистой оболочки Барретта.
Амбулаторный мониторинг pH пищевода / желудка и желчи
Все группы прошли манометрию пищевода и 24-часовой мониторинг pH и одновременный мониторинг желчи с использованием стандартизованного протокола.Амбулаторный мониторинг pH выполнялся с использованием трансназально введенного сурьмяного pH-электрода с отдельным кожным электродом сравнения (Synetics Medical, Стокгольм, Швеция). Данные сохранялись на портативном цифровом записывающем устройстве (Digitrapper MkIII, Synectics Medical Stockholm, Швеция). Перед каждым исследованием зонд pH калибровали в буферных растворах с pH 7 и 1. Эпизод кислотного рефлюкса определялся как снижение pH пищевода до менее 4 в течение более 10 с.
Для количественной оценки дуодено-пищеводного рефлюкса использовался амбулаторный фиброоптический спектрофотометр, переданный через нос (Bilitec 2000, Synectics, Швеция).Система состоит из миниатюрного зонда диаметром 1,5 мм, который передает световые сигналы в пищевод и обратно через пластиковую волоконно-оптическую связку. Перед каждым исследованием зонд калибровали в воде. В соответствии с текущей литературой, абсорбция билирубина> 0,25 использовалась в качестве эталона для вредного билиарного рефлюкса.14
Зонды желчи и pH были скреплены вместе и прошли трансназально в пищевод и желудок, как подробно описано в другом месте.17 Верхняя часть кончики зондов были расположены на 5 см выше верхней границы нижнего сфинктера пищевода, как определено манометрией пищевода.Дистальный pH-электрод и оптоволоконный датчик помещали на дно желудка на 10 см дистальнее нижнего сфинктера пищевода (рис.). Контрольной группы и пациентов просили следовать строгому протоколу трехразового питания без жидкости между приемами пищи. Лежачие фазы записи разрешались только ночью. Пациентов просили вести дневник, фиксируя точный характер приема пищи, фазы измерения в положении лежа на спине и прямо, а также ощущения изжоги и срыгивания.
Расположение датчиков pH и билирубина в желудке и пищеводе.(UES = верхний сфинктер пищевода; LES = нижний сфинктер пищевода).
Одновременный мониторинг желчных протоков и pH проводился с применением бесцветной «белой диеты» (WD), включающей жидкую и твердую пищу с максимальным поглощением желчи in vitro 0,25 [шкала поглощения от 0 (обычная вода) до 1 (общая экран)]. Еда включала воду, молоко, тосты, картофель, курицу, сухое печенье и рыбу.
Сбор и интерпретация данных
После завершения измерений зонды у пациентов извлекались, и данные сохранялись через интерфейс на IBM-совместимом компьютере, оснащенном программным обеспечением Polygram® (Medtronic).Для анализа использовались данные каждой секунды 24-часовых измерений. Чтобы оценить наличие желудочного или пищеводного билиарного рефлюкса, был рассчитан процент времени, когда абсорбция была больше 0,25 для следующих периодов: всего в положении лежа на спине, в вертикальном положении и после приема пищи. Постпрандиальный период определялся как 2 ч после окончания приема пищи. Процент времени с pH пищевода ниже 4 и медианным pH желудка и процент времени с pH желудка, измеряющим 1, 2, 3–7 и> 7, также был рассчитан для вышеуказанных периодов.Средняя продолжительность амбулаторного мониторингового исследования pH и Bilitec составляла 22 часа 40 минут у пациентов и 23 часа 44 минуты в контрольной группе.
Статистический анализ
Для анализа результатов использовалась программа SPSS (версия 11.0, Чикаго, Иллинойс). Для графического представления использовалась программа MedCalc для Windows (версия 9.0, MedCalc Software, Бельгия). Были установлены медианы, значения межквартильного размаха (IQR или 25–75 перцентиль). Непараметрические тесты (анализ Манна – Уитни и Краскела – Уоллиса) использовались для оценки взаимосвязи между переменными.Для представления некоторых данных использовались графики Box и Whisker. На этих графиках прямоугольник представляет IQR, а усы – самые высокие и самые низкие значения. Также нанесены выбросы, определенные как более чем в 1,5 раза превышающие IQR от 75-го центиля. Экстремальные значения были определены как более чем трехкратный IQR от 75-го центиля.
Кривая характеристики оператора приемника (ROC) использовалась для определения порогового значения для оптимальной чувствительности и специфичности согласно Цвейгу и Кэмпбеллу18. Площадь под кривой (AUC) использовалась как измерение диагностической эффективности теста.Результаты представлены в виде точек с доверительным интервалом 95% (95% ДИ) и графически для представления всех данных. В качестве положительной группы мы использовали пациентов со слизистой оболочкой Барретта, а отрицательную тестовую группу определяли здоровыми добровольцами. Предполагалось непараметрическое распределение площади под кривой.
Предположения для расчета требуемого размера выборки были альфа = 0,05, бета = 0,80, и что тест действителен для ежедневного использования только в том случае, если менее 20% здоровых контролей и не менее 80% пациентов имеют положительный результат теста. полученные результаты.Расчетный размер выборки для каждой группы составил 20.
Этика
Протокол исследования был одобрен этическим комитетом Кельнского университета. Каждый субъект дал письменное информированное согласие.
Результаты
В исследование были включены 24 пациента с пищеводом Барретта (средний возраст: 58 лет), 21 пациент с эзофагитом (средний возраст: 57 лет) и 19 здоровых людей контрольной группы со средним возрастом 51 год. У пациентов с БМ выявлен эзофагит 0 степени (4 случая), I степени (12 случаев) и II степени (8 случаев).В контрольной группе пациентов с эзофагитом было девять случаев с I степенью, восемь случаев со II степенью и три случая с III степенью. Демографические данные пациентов и добровольцев представлены в таблице (данные одного добровольца не были использованы из-за технических проблем).
Таблица 1
Демографические данные пациентов с слизистой оболочкой Барретта или эзофагитом и здоровых добровольцев
| Параметры | Пациенты с пищеводом Барретта ( n = 24) | Пациенты с эзофагитом ( n = 21) | Контроли ( n = 19) | Значение Пат.с Barrett vs Controls |
|---|---|---|---|---|
| Возраст (средний) | 57 лет | 58 лет | 51 год | – |
| Мин. 39–62 года | ||||
| Пол м: ж | 16: 8 | 11:10 | 11: 8 | нс |
| ИМТ (медиана) мин – макс | 27,0 кг / м 2 (18,6–33,1) | 26.9 кг / м 2 (17,9–31,5) | 24,1 кг / м 2 (19,62–27,34) | p = 0,003 |
| Курильщики (%) | n = 5 (20,8 ) | n = 4 (19,0) | n = 6 (31,6) | нс |
| Без спирта% | n = 3 (12,5) | n = 5 (23,8) | n = 5 (26,3) | n.s. |
Кислый желудочный рефлюкс (AGR)
Пациенты с пищеводом Барретта, 19 из 24 (79%) и 20 из 21 контрольных пациентов с эзофагитом (95%) имели патологические AGR [pH <4 в> 5% от общего числа измерения времени (TMT)], но также у 6 из 19 здоровых контролей (32%) наблюдались патологические AGR без каких-либо симптомов ( p = 0.002). Во время TMT средний AGR составил 10,6% для пациентов Barrett и 3,2% для контрольной группы ( p <0,01). В частности, измерения длительного кислотного рефлюкса (LAR), определяемого как pH рефлюкса <4, длящегося более 5 минут, показали значительные различия между пациентами и контрольной группой. Патологический AGR был обнаружен у пациентов в период измерения натощак как в положении лежа на спине, так и в вертикальном положении. Напротив, патологические AGR у здоровых людей наблюдались только в вертикальном положении (таблица).
Таблица 2
Медиана кислотного желудочного рефлюкса в пищевод у пациентов с BM или с эзофагитом и в здоровой контрольной группе
| Параметры | Пациенты с пищеводом Барретта ( n = 24) [медиана (LQ-UQ )] | Пациенты с эзофагитом ( n = 21) [медиана (LQ-UQ)] | Контрольная группа ( n = 19) [медиана (LQ-UQ)] | Значение Пат.с Barrett vs Controls |
|---|---|---|---|---|
| Процент от общего времени измерения pH <4 (%) | 10,6 (6,2–38,3) | 19,9 (1,6–71,7) | 3,2 (0,9–5,5) | p = 0,01 |
| Процент времени измерения в вертикальном положении pH <4 (%) | 11,7 (6,03–6,4) | 18,9 (8,7–60,8) | 2,4 (0,9–6,1) | p <0,05 |
| Процент времени измерения в положении лежа на спине pH <4 (%) | 10.9 (0,4–27,1) | 6,3 (0,0–13,3) | 0,3 (0,0–4,2) | p = 0,004 |
24-часовой мониторинг внутрижелудочного pH и желчи
Мониторинг pH желудка не показал значимых различия между пациентами и контрольной группой для всех периодов измерения (таблица). Воздействие желудочного билирубина, указывающее на билиарный рефлюкс, было значительно более частым у пациентов, чем в контрольной группе, в течение всех периодов измерения (таблица). Воздействие желчных путей в положении лежа на спине обычно происходило в ранние утренние часы во время сна, что выражалось увеличением абсорбции в течение 2–3 часов с быстрым возвращением к исходным значениям примерно в то время, когда субъект снова возвращался в вертикальное положение.За тот же период времени мониторинг pH желудка показал повышение уровня pH до более чем 2 (рис.).
Таблица 3
Результаты 24-часового внутрижелудочного мониторинга pH и желчи у пациентов с пищеводом Барретта и здоровой контрольной группы
| Параметры | Пациенты ( n = 24) [медиана (LQ – UQ)] | Контроли ( n = 19) [Медиана (LQ – UQ)] | Значимость |
|---|---|---|---|
| Медиана внутрижелудочного pH во время TMT | 1.3 (1,0–1,4) | 1,4 (1,1–1,7) | н.с. |
| Процент воздействия билирубина (%) TMT | 7,8 (1,6–17,8) | 0,0 (0,0–1,0) | p = 0,001 |
| Процент воздействия билирубина (%) в прямом эфире | 6,9 (0,1–12,9) | 0,0 (0,0–1,3) | p <0,01 |
| Процент воздействия билирубина (%) во время пребывания на спине | 2,0 (0,0–28,6) | 0.0 (0,0–0,0) | p = 0,001 |
24-часовой внутрижелудочный мониторинг pH и желчи у пациента с пищеводом Барретта, демонстрирующего дуоденогастральный рефлюкс ранним утром. а. Bilitec®-мониторинг, б. pH-мониторинг.
Воздействие билирубина на пищевод
По результатам TMT медиана желчного рефлюкса пищевода составила 7,8% для пациентов с пищеводом Барретта (LQ – UQ = 1,6–17,8%) и 3,5 (LQ – UQ = 0,1–13,5) для контроля пациентов, в отличие от 0% для контроля (LQ – UQ = 0–1.0%), р = 0,001). На рисунке показано, что мониторинг желчи пищевода у пациентов с пищеводом Барретта и здоровых людей в контрольной группе варьировался в течение всего периода измерения и периода лежа на спине.
Результаты мониторинга желчи в пищеводе у 24 пациентов с пищеводом Барретта, 21 пациента с эзофагитом и 19 здоровых людей из контрольной группы а) общий период измерения (тест Краскела-Уоллиса = 0,01) б) период лежа на спине (тест Краскала-Уоллиса p = 0,01) .
Рабочая кривая приемника, отображающая процент истинных положительных результатов (пациенты с пищеводом Барретта, идентифицированные по воздействию билирубина) в зависимости от частоты ложных срабатываний (здоровые контроли с высоким уровнем воздействия билирубина), показана на рис.. С площадью под кривой 0,78 (95% ДИ = 0,56–0,89) ROC-анализ мониторинга желчевыводящих путей показал оптимальное значение для пациентов при 1% TMT [чувствительность 75% (95% ДИ = 53–90%). , Специфичность 84% (95% ДИ = 60–96%)]. Следовательно, пороговое значение для различения нормального и патологического билиарного рефлюкса с использованием 24-часового мониторинга желчевыводящих путей в пищеводе (порог поглощения> 0,25) должно быть зафиксировано на уровне 1% от TMT.
ROC-кривая с 95% доверительным интервалом для патологического мониторинга желчи у пациентов с пищеводом Барретта по сравнению со здоровыми контрольными пациентами, соответствующими возрасту и полу.
пациентов Барретта, 18 из 24 (75%), 15 из 21 контрольного пациента с эзофагитом (71%) и 3 из 19 контрольных (16%) показали билирийный рефлюкс в пищевод более 1,1% TMT ( p <0,001). Используя это пороговое значение, ни у одного из контрольных пациентов, у 10 из контрольных пациентов (48%) и у 11 из 24 пациентов с болезнью Барретта (46%) не было патологического воздействия билирубина во время сна.
Обсуждение
Результаты нашего исследования подтверждают, что пациенты с пищеводом Барретта имеют значительно более частый дуоденогастральный рефлюкс в пищевод, чем здоровые люди из контрольной группы того же возраста и пола.Кроме того, этот рефлюкс, измеряемый воздействием кислоты и билирубина, дольше остается в пищеводе, особенно во время сна.
Роль кислотного и некислотного рефлюкса в пищевод как причинного фактора симптомов и поражений слизистой оболочки рассматривалась в ряде исследований. Не только продолжительность, но, возможно, и состав рефлюкса, играет важную роль в развитии таких поражений.13 Круглосуточный внутрижелудочный мониторинг желчи предоставил клиницисту однозначные доказательства чрезмерного дуоденогастрального рефлюкса (DGR) у 41% пациентов. с эндоскопическим эзофагитом, симптомами гастроэзофагеального рефлюкса (ГЭР) и желудочными симптомами, указывающими на ДГР.19 Рефлюкс двенадцатиперстной кишки в желудок, особенно после еды, является физиологическим явлением; 20 тем не менее, билиарный рефлюкс вносит значительный вклад в поражение слизистой оболочки всего желудка 21
В нашем исследовании контрольная группа пациентов с различными степенями тяжести. При эзофагите не было выявлено значительных различий в показателях кислотного или желчного рефлюкса в желудок или пищевод по сравнению с пациентами Барретта. Это может быть вызвано отбором пациентов с эзофагитом, которые были кандидатами на фундопликацию, но обе группы пациентов значительно различались по сравнению со здоровым контролем.Поэтому наши результаты имеют большое клиническое значение, особенно для предоперационной диагностики.
Marshall et al. сравнивали здоровую контрольную группу с пациентами с различными степенями рефлюкс-эзофагита и пищевода Барретта в отношении измерения желчи в желудке.22 В этом исследовании средний возраст контрольных пациентов составлял 25 лет, а пациентов групп I, II , а III – 42, 50 и 60 лет соответственно. Билитек-зонд располагался на 10 см ниже нижнего сфинктера пищевода (LES).Порог поглощения билирубина составлял 0,14, и хотя не было обнаружено различий между группами по ТМТ, воздействие билирубина желудка было выше в положении лежа на спине, чем в вертикальном положении. В текущем исследовании контрольная группа была старше, чем в исследовании Маршалла. Больше дуодено-желудочного рефлюкса было зарегистрировано как у исследуемых, так и у контрольных пациентов во все периоды измерения. Эти результаты могут быть связаны с улучшением условий исследования.
Мы использовали пищеводный порог поглощения билирубина 0,25.Fein et al. [14] в исследовании in vitro абсорбции различных белых блюд показали, что наименьшее влияние пищи во время мониторинга желчи было измерено при абсорбции> 0,25.
Tack et al. сообщили о влиянии консистенции еды на результаты измерений Bilitec у здоровых субъектов.23 Они сравнили две группы молодых людей из контрольной группы. Испытуемые принимали либо только жидкую пищу, не поглощающую свет той же длины волны, что и билирубин, либо твердую пищу, избегая диет, которые влияют на поглощение билирубина.Авторы обнаружили существенные различия между двумя группами, используя порог поглощения билирубина> 0,14 со средним процентным соотношением (межквартильный диапазон) над TMT 10,9% (6,7–19,3) для твердой пищи и 0,3% (0,0–2,8) для жидкой пищи. Основные артефакты приема пищи присутствовали у субъектов, получавших твердую пищу из двух блюд (10%) и без жидкости. В нашем исследовании мы обнаружили такой артефакт приема пищи у одного пациента и одного контроля, но значения поглощения билирубина были ниже 0,25 и, следовательно, не соответствовали нашим результатам.
Гастроэзофагеальный рефлюкс нередко содержит секреции желчи, двенадцатиперстной кишки и поджелудочной железы. Использование спектрофотометрического зонда Bilitec продемонстрировало более высокую распространенность аномального воздействия билирубина пищевода у пациентов с метаплазией Барретта по сравнению с пациентами с эрозивным повреждением или без признаков эзофагита (6,8,10,13). добровольцы включены в контрольную группу. Однако другие исследования показали повышенную распространенность гастроэзофагеального рефлюкса с возрастом.24 По этим причинам мы изучали здоровых людей из контрольной группы по возрасту и полу и пациентов с пищеводом Барретта или с эзофагитом. Мы обнаружили патологическую кислотность и желчный рефлюкс пищевода у одной трети контрольной. Возможно, это может быть вызвано артефактами или нарушением протокола волонтерами. Но в предыдущем опубликованном исследовании мы смогли показать, что у более молодых здоровых людей такого патологического рефлюкса не было.17 Возможно, эти явления вызваны расслаблением, которое чаще встречается у пожилых людей.Напротив, почти все пациенты с пищеводом Барретта (87%) и все пациенты с эзофагитом (100%) показали патологический кислотный рефлюкс и / или желчный рефлюкс, измеренные с помощью комбинированного мониторинга pH и желчи. В частности, рефлюкс желчи в пищевод во время сна был обнаружен только у пациентов с BM или с эзофагитом.
В нашем исследовании мы измерили внутрижелудочный pH и рефлюкс желчи из двенадцатиперстной кишки в желудок (DGR). Медиана внутрижелудочного pH была одинаковой в обеих группах.Но пациенты с пищеводом Барретта имели значительно более длительный дуоденогастральный рефлюкс в течение 24-часового периода измерения, чем контрольная группа. Ночью было продемонстрировано больше ДГР, чем днем, в обеих группах исследуемых пациентов и в контрольной здоровой группе. Согласно ранее опубликованным исследованиям, это могло быть связано с щелочным сдвигом pH. Точный механизм, с помощью которого происходит ночной DGR, и роль, которую играет поза, остаются неясными.
Bowrey et al. не смогли установить ни гастроэзофагеальный, ни дуоденогастральный рефлюкс как преобладающую причину воспаления в слизистой оболочке сердца желудка с использованием прибора Bilitec 2000.16 Это понятно, поскольку количество рефлюкса в желудок (DGR) не обязательно коррелирует с DGER в пищевод. В этом исследовании авторы продемонстрировали больше DGR у женщин в период лежа на спине, в то время как у мужчин было больше DGER. При этом корреляции между уровнями желчи в желудке и пищеводе не было. Однако контрольная группа была намного моложе пациентов. Мы обнаружили значительные различия в измерениях желчи желудка и пищевода между пациентами с BM и контрольной группой.В отличие от Bowrey et al., Мы наблюдали больше DGER у женщин в период лежа на спине и больше DGR у пациентов-мужчин.
Напротив, Banki сообщил об аналогичном воздействии на пищевод рефлюксной кислоты и билирубина у женщин и мужчин со слизистой оболочкой Барретта.28 Pfaffenbach et al. (29) изучали желчь пищевода и кислотный рефлюкс у пациентов с длинным сегментом пищевода Барретта (LSBE) и коротким сегментом пищевода Барретта. пищевода (SSBE) и пациентов с гастроэзофагеальной рефлюксной болезнью (GERD). Субъекты прошли манометрию пищевода и одновременный 24-часовой мониторинг pH и желчи (Bilitec 2000) со значением абсорбции> 0.2 на 10,9% от общего периода. GER не отличался между группами. Однако DGER различалась у пациентов с LSBE (14,7%), SSBE (2,1%) и GERD (2,1%).
Таким образом, анализ эталонных значений показателей кислотности пищевода и рефлюкса желчи в группе здоровых, сопоставимых по возрасту и полу контролей по сравнению с пациентами с BM привел к следующим выводам:
Хотя около 30% здоровых контролей показали кислотный рефлюкс при мониторинге pH, пациенты с BM имели значительно более высокий кислотный рефлюкс в течение всех периодов измерения.
У здоровых людей не было значимого дуодено-желудочно-пищеводного рефлюкса, измеренного по абсорбции билирубина. Особенно в период лежа на спине не было рефлюкса желчи.
Оптимальный порог патологического рефлюкса желчи составляет 1,1% (мониторинг желчи с оптической плотностью 0,25).
Дуоденогастральный рефлюкс – обзор
Желчь
У многих людей желчь часто попадает в желудок в результате дуоденогастрального рефлюкса. Компоненты желчи, особенно желчные кислоты, холевая, таурохолевая и гликохолевая кислота и их деоксигенированные метаболиты, считаются важными в возникновении тяжелых повреждений пищевода, включая эрозивный эзофагит, стриктуры и пищевод Барретта (52).
Кроме того, было показано, что метаболиты желчных солей обладают способностью проникать в эпителиальные клетки и связываться с клеточными рецепторами в клетках-предшественниках пищевода, чтобы активировать многие метаболические пути в экспериментальных моделях с использованием клеточных линий. Jaiswal et al. (53) показали, что конъюгированная соль желчных кислот гликохенодезоксихолевая кислота была высокоэффективной в активации пути передачи сигналов киназы P13 / Akt в клеточной линии аденокарциномы Барретта. Известно, что этот путь способствует пролиферации клеток и подавляет апоптоз.Jaiswal et al. (54) изучали влияние солей желчных кислот на нормальные плоские клетки пищевода и неопухолевые клетки Барретта. Нормальные плоские клетки пищевода, подвергшиеся воздействию солей желчных кислот в течение 5 минут, не увеличивали количество клеток. В эпителиальных клетках Барретта воздействие солей желчных кислот увеличивало количество клеток на 31%, увеличивало уровни фосфорилированного p38 и ERK в два-три раза, увеличивало включение BrdU на 30% и уменьшало апоптоз, индуцированный УФ-излучением, на 15-20%. Авторы пришли к выводу, что воздействие солей желчных кислот вызывает пролиферацию неопухолевой клеточной линии Барретта за счет активации путей ERK и p38 MAPK, и предположили, что это может быть потенциальным механизмом, посредством которого рефлюкс желчи может способствовать неопластической прогрессии пищевода Барретта.
Влияние солей желчных кислот на активацию эпителиальных клеток Барретта путем изменения генетических путей было также показано на экспериментальных животных. Stamp (55) показал, что у крыс, которым была сделана гастрэктомия и еюностомия, чтобы позволить желчным кислотам рефлюкс в пищевод, за 50 недель развилось много карцином, в то время как другие модификации, удерживающие желчь из пищевода, не вызывали рака. Авторы пришли к выводу, что желчные кислоты, рефлюксные в пищевод людей, также должны вызывать рак, особенно в западных обществах с их диетами с высоким содержанием жиров, которые обеспечивают обильное поступление желчи.Они показали, что желчные кислоты могут проникать в клетки модели OE33 и активировать онкоген c-myc при pH 4, генный комплекс NF-kappaB при pH 6,5 и вызывать пролиферацию клеток. В своем обсуждении авторы предположили, что кислотосупрессивная терапия, используемая для лечения пациентов с пищеводом Барретта, солюбилизирует свободные желчные кислоты и некоторые конъюгаты глицина, позволяя им проникать в эпителиальные клетки. Эти внутриклеточные желчные кислоты обладают способностью вызывать клеточные изменения, вызывающие канцерогенез.Таким образом, авторы пришли к выводу, что методы предотвращения попадания желчных кислот в желудок или предотвращения их реакции должны быть разработаны, но до тех пор кислотоподавляющая терапия должна быть ограничена, а не продвигаться.
Проникновение метаболитов солей желчных кислот в эпителиальные клетки пищевода является критическим фактором канцерогенеза, поскольку оно, по-видимому, является предпосылкой для активации желчными кислотами различных метаболических путей, которые приводят к повышенной пролиферации клеток. Изучение метаболизма солей желчных кислот показывает, что существует критический диапазон pH от 3 до 6, в котором желчные кислоты существуют в своей растворимой, неионизированной форме, могут проникать через клеточные мембраны и накапливаться в клетках слизистой оболочки (рис.10.24). При более низком pH желчные кислоты осаждаются, а при более высоком pH желчные кислоты существуют в не повреждающей ионизированной форме (56).
РИСУНОК 10.24. Влияние pH желудочного сока на желчные кислоты, попавшие в желудок в результате дуоденогастрального рефлюкса. У нормального человека с pH желудочного сока в диапазоне от 1 до 3 (а) желчные кислоты инактивируются осаждением. В состоянии частичного подавления кислоты, обычно имеющемся у пациентов, принимающих препараты, подавляющие кислоту (b), pH желудочного сока находится в диапазоне от 3 до 6, а метаболиты желчных кислот находятся в растворимом, неионизированном состоянии, где они, как было показано, попадают в эпителиальный клетки и вызывают канцерогенез.У пациентов с полным подавлением кислотности (c) желчные кислоты находятся в растворимом ионизированном состоянии, где они не активны как канцерогены.
Эти экспериментальные данные о метаболизме желчных кислот и клеточной активности представляют собой пугающий сценарий. Попадание желчи в желудок при дуоденогастральном рефлюксе – очень частое, если не универсальное явление. У пациента с нормальной кислотностью желудочного сока в диапазоне pH от 1 до 3 желчные кислоты осаждаются в безвредные нерастворимые молекулы (рис. 10.25). При pH выше 6 желчные кислоты остаются в ионизированной форме, что препятствует их проникновению в клетки.При pH от 3 до 6 желчные кислоты и их метаболиты превращаются в неионизированные растворимые молекулы, которые могут проникать через клеточные мембраны и проникать в эпителиальные клетки.
РИСУНОК 10.25. Эффект частичного подавления кислоты ( справа, ), когда pH желудочного сока находится в диапазоне от 2 до 6 по сравнению с неэффективным (т.е. pH желудка в диапазоне от 1 до 3) подавлением кислоты ( слева, ). Повышенный pH рефлюксата вызывает усиление кишечной метаплазии у пациентов с пониженной кислотностью.Превращение желчных кислот в канцерогены увеличивает вероятность превращения кишечной метаплазии в рак. Обратите внимание, что эти два пациента являются типичными пациентами Paull et al. (31) и Chandrasoma et al. (10), предполагая, что эти различия могут объяснить повышенную заболеваемость аденокарциномой, которая произошла в этот период.
Подавление кислотности, особенно когда оно неполное, как у подавляющего большинства пациентов, принимающих эти лекарства, как без рецепта, так и по рецепту, приводит к увеличению pH желудка до критического диапазона pH от 3 до 6, где это способствует генерации канцерогенные молекулы из эндогенных желчных кислот, когда они присутствуют в желудке.Даже в условиях строгого контроля с применением ингибиторов протонной помпы в высоких дозах редко удается достичь полного подавления кислоты, при котором pH желудочного сока постоянно остается выше 6. Поэтому весьма вероятно, что большинство пациентов, принимающих кислотосупрессивную терапию, имеют повышенное количество канцерогенных производных желчных кислот в желудке. Эти производные желчных кислот не являются канцерогенными по отношению к эпителиальным клеткам желудка, плоскоклеточным клеткам пищевода и метапластическим цилиндрическим эпителиальным клеткам пищевода в сердечных и оксинтокардиальных слизистых оболочках.Однако эти молекулы проникают в клетки кишечного эпителия пищевода, вызывая трансформации, которые, вероятно, вызывают канцерогенез.
Исследования импеданса пищевода показывают, что подавление кислоты существенно не снижает ни количество эпизодов рефлюкса, ни их объем. Он только увеличивает pH в достаточной степени, чтобы предотвратить симптомы, вызванные кислотой в пищеводе. Поскольку он вызывает симптоматическое улучшение, мы предположили в главах 8 и 9, что он увеличивает преобразование метапластической слизистой оболочки сердца в кишечную метаплазию и ингибирует преобразование слизистой оболочки сердца в оксинтокардиальную слизистую оболочку (рис.9.24). Это резко увеличивает популяцию клеток-мишеней, поскольку кишечная метаплазия увеличивается как по распространенности, так и по количеству в сегменте пищевода, выстланном столбчатыми стенками. Повышенная щелочность желудочно-пищеводного рефлюкса, который стал канцерогенным в результате подавления кислоты, одновременно создала в пищеводе благоприятную среду для его действия.
У пациента с кишечной метаплазией продолжающийся рефлюкс способствует проникновению этих растворимых метаболитов желчных кислот и, по-видимому, вызывает изменения в генетических и метаболических путях, которые приводят к пролиферации этих клеток и ингибируют апоптоз.Хотя точный путь, вызывающий канцерогенез, неизвестен, вполне вероятно, что это механизм канцерогенеза в пищеводе Барретта.
Цикл, в котором подавление кислоты увеличивает вероятность рака у пациента с пищеводом Барретта, завершен. Повышение эффективности кислотного подавления также могло бы объяснить рост числа случаев аденокарциномы, вызванной рефлюксом, с середины 1970-х годов (рис. 10.25).
Дуоденогастральный рефлюкс: клинические и терапевтические аспекты
Дуоденогастральный рефлюкс (рефлюкс желчи) может вызвать воспаление и / или изъязвление слизистой оболочки желудка, 1–5 кишечную метаплазию в желудке 6 и повышенный риск рака желудка.7 Рефлюкс желчи является результатом нарушения моторики антродуоденальной области (спонтанный рефлюкс) 8. 9 У взрослых это также может быть осложнением частичной гастрэктомии, 4 5 10 11, но эта операция у детей проводится очень редко. Диагноз дуоденогастрального рефлюкса – сложный. У взрослых нет патогномоничных клинических симптомов, указывающих на рефлюкс желчи.4 Обычно это обнаруживается во время эндоскопии, но было замечено, что процесс введения эндоскопа генерирует ретропульсивные волны и приводит к рефлюксу желчи.4 12 Морфологические изменения слизистой оболочки желудка также не могут подтвердить диагноз. 12 Таким образом, было разработано несколько дополнительных методов, таких как измерение концентраций желчных кислот13 и натрия в содержимом желудка, 14 pH-метрия, 15 и допплеровское ультразвуковое исследование16. 17 Динамическая холесцинтиграфия, которая успешно использовалась в течение нескольких лет, позволяет оценить степень рефлюкса (индекс рефлюкса), и модификация метода, предложенного Mackie и др. , 18 с молоком в качестве пробного завтрака, кажется особенно полезно.
Дуоденогастральный рефлюкс также может возникать во время эндоскопии верхних отделов желудочно-кишечного тракта у детей, и обычно диагноз не подтверждается другими методами. Также отсутствуют данные о частоте возникновения рефлюкса желчи и о том, как часто он является причиной повторяющихся болей в животе у детей.19 Корреляция между тяжестью рефлюкса и воспалительными поражениями слизистой оболочки желудка не анализировалась, и существует очень мало исследований, посвященных роли прокинетических препаратов для ограничения рефлюкса желчи у детей.20 21 год
В нашем исследовании мы стремились: (1) определить частоту дуоденогастрального рефлюкса у детей, страдающих хронической повторяющейся болью в животе; (2) оценить возможную связь между степенью рефлюкса и тяжестью воспалительных поражений слизистой оболочки желудка и двенадцатиперстной кишки; (3) наблюдать, соответствуют ли области наибольшего накопления изотопов на холесцинтиграфии участкам наиболее сильного воспаления в желудке; и (4) наблюдать, улучшают ли прокинетические препараты в сочетании с противовоспалительными средствами симптомы и признаки у пациентов с гастритом и дуоденитом, страдающих рефлюксом желчи.
Материалы и методы
Мы изучили 1120 детей, у которых была диагностирована рецидивирующая боль в животе и которые поступили в отделение педиатрии, детской гастроэнтерологии и онкологии Медицинского университета Гданьска с 1993 по 1996 год включительно. Всем детям было проведено эндоскопическое исследование верхних отделов желудочно-кишечного тракта с помощью эндоскопа Olympus GIF-PQ 20 или GIF-PQ 10. Мы обследовали пищевод, желудок и чашечку двенадцатиперстной кишки и визуально оценивали степень воспаления слизистой оболочки желудка по Сиднейской шкале.22 Учитывались следующие признаки: наличие нормальных кровеносных сосудов, наличие отека, эритемы, экссудата, эрозии, гипертрофии или атрофии складки слизистой оболочки желудка. Степень прогрессирования оценивали по шкале от I до IV (I степень – без изменений; II степень – легкие изменения; III степень – умеренные изменения; IV степень – тяжелые изменения). В двенадцатиперстной кишке мы оценивали степень визуального воспаления как легкую, умеренную или тяжелую. Учитывали наличие отека, эритемы, экссудата, эрозии и гипертрофии слизистой оболочки двенадцатиперстной кишки.Мы провели уреазный тест (CLO-тест) у всех пациентов, чтобы исключить или подтвердить инфекцию Helicobacter pylori . Мы взяли два биоптата желудка (тела и антрального отдела) и один – из колпачка двенадцатиперстной кишки для морфологической оценки у всех детей. В образцах желудка оценивали гистологическое воспаление по Сиднейской шкале. Мы учитывали следующие особенности: интенсивность и активность воспаления, степень атрофии желудочных желез и наличие метаплазии.Мы оценивали степень прогрессирования по шкале от I до IV (как указано выше). В двенадцатиперстной кишке учитывались следующие особенности: интенсивность и активность воспаления и наличие метаплазии. Мы оценивали степень прогрессирования как легкую, среднюю и тяжелую.
У детей с эндоскопическим подозрением на рефлюкс желчи мы провели динамическую холесцинтиграфию для подтверждения диагноза рефлюкса желчи.
По результатам эндоскопического обследования изначально диагностирован желчный рефлюкс у 92 детей.Детей перед холесцинтиграфией не давали. Мы вводили радиофармпрепарат (технеций-99m; HEPIDA) внутривенно в дозе 3-4 мКи (111–148 МБк) на дозу, и сборы проводились каждые пять минут, каждое продолжалось одну минуту. После пятого измерения давали выпить детям 150–200 мл сгущенного коровьего молока. После 12-го измерения мы перорально дали 2 мКи (74 МБк) 99m Tc для определения желудочного поля.
Оценка результатов холесцинтиграфии была основана на: морфологических характеристиках (кривые время-активность по желудочному полю) и индексе рефлюкса, рассчитанном путем деления количества желудочных подсчетов, полученных во время воздействия, на сумму желудочных и кишечных подсчетов.
Мы случайным образом выбрали контрольную группу из 50 человек из группы детей без эндоскопических признаков желчного рефлюкса. Некоторые пациенты с рефлюксом желчи, подтвержденным сцинтиграфией, получали прокинетический препарат (цизаприд) в дополнение к противовоспалительным средствам (трикалия дицитратобисмутат и амоксициллин и метронидазол у детей с H pylori ). Чтобы оценить эффективность цизаприда, мы случайным образом разделили пациентов на две группы: группу детей, получавших цизаприд, и группу детей, которые не получали цизаприд.На рисунке 1 показано распределение детей по различным группам. Мы давали цизаприд в течение шести недель, трикалия дицитратобисмутат в течение четырех недель, амоксициллин в течение семи дней и метронидазол в течение 14 дней. Повторная сцинтиграфия была проведена через три недели после окончания лечения.
фигура 1Критерии включения детей с хронической абдоминальной болью в наше исследование дуоденогастрального рефлюкса.
Мы проанализировали результаты с помощью критерия χ 2 и критерия Манна-Уитни.
Наше исследование было одобрено исследовательским консультативным комитетом Медицинского университета Гданьска.
Результаты
Из 1120 детей у 92 (8,21%) выявлен рефлюкс желчи при эндоскопии. Наличие рефлюкса подтверждено сцинтиграфией (группа А) у 59 пациентов, что составляет 5,27% детей с болями в животе. Диапазон индекса рефлюкса составлял 2–20% (медиана 5,6%).
Группа B состояла из 50 пациентов, выбранных случайным образом из пациентов, у которых не было рефлюкса желчи при эндоскопии.В группе А было 43 девочки и 16 мальчиков, а в группе Б – 22 девочки и 28 мальчиков. В группе А возраст детей варьировался от 4 до 17 лет со средним значением (SD) 12,25 (2,58) года. В группе B возраст детей составлял от 5 до 17 лет (средний возраст 11,58 года; стандартное отклонение 3,08). Не было обнаружено никаких симптомов, достаточно характерных для выявления симптомов рефлюкса желчи из группы пациентов с повторяющейся болью в животе.
В таблице 1 приведены результаты эндоскопического и гистологического исследования желудка.Эндоскопически в теле желудка у пациентов группы А наблюдались более тяжелые поражения, чем в группе В (p <0,01). Однако частота тяжелых поражений антрального отдела в обеих группах была одинаковой. Степень гистологического воспаления также была сходной в двух группах (таблица 1). Инфекция Helicobacter pylori была выявлена у 15 детей из группы А и у 27 из группы B. Дети, у которых не было рефлюкса желчи, были значительно чаще инфицированы H pylori по сравнению с детьми с рефлюксом желчи (p <0.005). В таблице 2 представлены результаты эндоскопической и гистологической оценки двенадцатиперстной кишки. Не было значительной разницы в распределении тяжести поражений между двумя группами. В группе А (дети с рефлюксом) мы также проанализировали сцинтиграфические изображения. Было три типа распределения радиофармацевтического агента: (1) изотоп равномерно распределялся в желудке; (2) изотоп, накопленный в антральном отделе; и (3) изотоп, накопленный в сердечной области.
Таблица 1Результаты эндоскопической и гистологической оценки слизистой оболочки желудка по наличию или отсутствию рефлюкса желчи
Таблица 2Результаты эндоскопической и гистологической оценки слизистой оболочки двенадцатиперстной кишки в зависимости от наличия или отсутствия рефлюкса желчи
Статистический анализ (тест χ 2 ) не показал корреляции между областями накопления радиофармпрепарата и локализацией гистологически оцененных воспалительных поражений в желудке (таблица 3).
Таблица 3Области накопления радиофармпрепарата и локализация воспалительных поражений в желудке
Мы обнаружили, что интенсивность воспаления в желудке и двенадцатиперстной кишке не зависела от степени рефлюкса (таблица 4).
Таблица 4Индекс рефлюкса (Ri) и воспалительные изменения желудка
В нашем исследовании не было обнаружено корреляции между областями накопления изотопов и локализацией гистологически оцененных воспалительных поражений в желудке.Чтобы объяснить это явление, мы провели следующий эксперимент. Мы выполнили холесцинтиграфию трем взрослым добровольцам мужского пола так же, как и детям в нашем исследовании. Содержимое желудка, содержащее 200 мл сгущенного коровьего молока в качестве тестовой еды и радиофармацевтический агент, откачивали и помещали в стеклянную чашу для искажения. Чашки искажения исследовали с помощью γ-камеры. Снимки, сделанные сразу после помещения в стеклянную чашку для искажения, и снимки, сделанные позже, показывают тенденцию радиофармацевтического агента собираться наверху.Анализ распределения изотопов показал, что изотопные частицы, связанные с переваренным молоком, накапливаются в верхней части чашки (рис. 2). Это явление является артефактом сцинтиграфического исследования и вызвано использованием молока в качестве пробной еды.
фигура 2Распределение радиофармпрепарата в чаше для искажения, заполненной содержимым желудка и рефлюксным материалом. (A) сразу после приема содержимого желудка, (B) через 15 минут после приема содержимого желудка. Красный, низкая радиоактивность; желтый, высокая радиоактивность.
Детям группы А, перенесшим гастрит и рефлюкс желчи, вводили противовоспалительные препараты. Первоначально 36 из 59 пациентов дополнительно получали цизаприд, но шесть из них были потеряны при последующем наблюдении, поэтому здесь сообщается только о 30.
Оценка лечения цизапридом была основана на двух показателях: клиническое улучшение и изменение индекса рефлюкса. Поскольку большинство пациентов не согласились на дальнейшую эндоскопию, анализ изменений слизистой оболочки желудка и двенадцатиперстной кишки в процессе лечения был невозможен.
У тех, кто получал цизаприд, начальный индекс рефлюкса варьировал от 2% до 20% (медиана, 5,9%), а соответствующие результаты у тех, кто не получал цизаприд, варьировались от 2,2% до 18% (медиана, 6,4%). После лечения цизапридом у 18 детей не было признаков желчного рефлюкса (в среднем 0%). У пяти детей, не получавших цизаприд, не было желчного рефлюкса (в среднем 6%). Статистический анализ (тест Манна-Уитни) показал, что лечение цизапридом снижает частоту желчного рефлюкса (U = 192.5; р <0,01).
Клиническое улучшение было отмечено у 28 детей, получавших цизаприд, и у 18 детей, которые не получали цизаприд.
Цизаприд хорошо переносился большинством пациентов; только двое детей пожаловались на усиление болей в животе, что заставило нас исключить препарат из схемы лечения этих пациентов. Других побочных эффектов не отмечалось.
Обсуждение
Эндоскопические критерии рефлюкса желчи у детей такие же, как у взрослых.Как было показано в других статьях, их недостаточно для установления диагноза. Другие методы позволяют верифицировать эндоскопический диагноз в 30–40% случаев4. Аналогичные результаты были получены в нашем исследовании (верификация эндоскопического диагноза в 64,1% случаев).
Особый интерес представляет влияние рефлюкса желчи на слизистую желудка. Хотя многие авторы наблюдали корреляцию между наличием рефлюкса желчи и интенсивностью воспалительных поражений, 1-4 6 также есть много работ, в которых такие корреляции не были обнаружены.12 23 24 Ранее упоминалось, что концентрация желчных кислот у пациентов с рефлюксом желчи очень редко бывает такой высокой, как в экспериментальных условиях.4 Высокие концентрации желчных кислот и лизолецитина наблюдаются в основном у пациентов, перенесших операцию на дистальных отделах желудка. , и в наше исследование таких случаев не было. Индекс рефлюкса также был довольно низким у обследованных нами детей. В некоторых исследованиях сообщалось о показателях рефлюкса до 1–70% 4, и они определенно выше у пациентов, перенесших частичную гастрэктомию (обычно индекс рефлюкса> 20%).25 У детей степень рефлюкса сравнительно низкая, и, вероятно, поэтому он не имеет решающего влияния на индукцию поражения слизистой оболочки. Следовательно, должны быть некоторые другие факторы, которые ответственны за воспалительные поражения желудка и двенадцатиперстной кишки у детей. Некоторые из них широко известны, например, генетическая предрасположенность, психологические факторы и инфекция H pylori . В нашем исследовании, кажется, доминируют первые два фактора. В семейном анамнезе заболевания верхних отделов желудочно-кишечного тракта были очень распространены.В 42,4% семей мы обнаружили в анамнезе язву желудка или двенадцатиперстной кишки. Наша статья подтверждает важность психологических факторов в развитии гастрита и дуоденита.
Инфекция Helicobacter pylori значительно меньше влияет на развитие воспалительных поражений у детей с рефлюксом желчи. Эти пациенты были значительно реже инфицированы бактерией, чем дети без рефлюкса. Вероятно, это связано с защелачиванием содержимого желудка у детей с рефлюксом желчи, что может затруднить колонизацию H. pylori .Другие авторы также отмечали это явление у взрослых. 26
При сцинтиграфической верификации желчного рефлюкса у детей мы отметили, что области накопления изотопов не соответствуют областям наиболее тяжелого воспаления, диагностированного эндоскопически и морфологически. Было показано, что модификация Маки18 холесцинтиграфии приводит к появлению артефактов, что затрудняет интерпретацию. Необходимы дальнейшие исследования, чтобы найти другой тестовый обед, чтобы этот полезный диагностический метод можно было применить более широко.Схемы лечения детей с рефлюксом желчи еще не установлены. В нашем исследовании мы добавили прокинетический препарат к противовоспалительному агенту при лечении. Цизаприд был выбран потому, что у него очень мало побочных эффектов и он эффективен для улучшения координации гастродуоденальной зоны.20 27 28 Как отмечалось в других отчетах, препарат хорошо переносился. Наше исследование доказало его эффективность в устранении рефлюкса желчи.
Остается ответить на один вопрос: следует ли и в каких ситуациях давать прокинетические препараты.Наше исследование не позволяет нам сделать клинические выводы, которые помогли бы врачу принять решение о лечении. Тот факт, что эти препараты также используются при так называемой функциональной диспепсии, гастрите или язве желудка, делает проблему еще более сложной. Обычно в этих случаях причиной расстройства является нарушение эвакуации содержимого желудка, а прокинетические препараты помогают поддерживать правильную эвакуацию оставшейся пищи. По этой причине многие авторы предлагают назначать прокинетические препараты при лечении гастрита и / или язвы желудка и при так называемой функциональной диспепсии.29-32 Эта проблема, несомненно, требует дальнейшего изучения.
ВЫВОДЫ
Гастродуоденальный рефлюкс был диагностирован эндоскопически у 92 из 1120 детей с рецидивирующими болями в животе, холесцинтиграфия подтвердила его наличие у 59 из этих детей. Это говорит о необходимости верификации эндоскопического диагноза другими методами
Не было достоверной разницы в интенсивности воспалительных поражений слизистой оболочки желудка и двенадцатиперстной кишки между детьми с желчным рефлюксом и детьми без этого заболевания.Это говорит о том, что могут быть другие факторы, которые важны для детей, такие как генетическая предрасположенность и психогенные факторы
Изотопный метод, применяемый для подтверждения эндоскопического диагноза, несет потенциальную ошибку из-за использования молока в качестве пробной еды. Это вызывает несоответствие между областями наиболее интенсивного накопления изотопа и локализацией воспалительного поражения в желудке
Введение прокинетического препарата (цизаприда) имеет большое влияние на снижение индекса рефлюкса.

 Plattsburgh: Printed by F.P. Allen, 1833. Nutr Rev. 1977 Jun; 35(6): 144-145.
Plattsburgh: Printed by F.P. Allen, 1833. Nutr Rev. 1977 Jun; 35(6): 144-145. 1985; 115: 1-56.
1985; 115: 1-56.