Кишечная железа: Желудок. Кишечник. Пищеварительные железы — урок. Биология, 9 класс.
Желудок. Кишечник. Пищеварительные железы — урок. Биология, 9 класс.
Желудок — расширенная часть пищеварительной трубки, в которой накапливается и переваривается пища.
Слизистая оболочка желудка включает несколько миллионы мелких желёз, вырабатывающих желудочный сок (2,0 – 2,5 л в сутки).
Одни железы вырабатывают пищеварительный фермент пепсин, который необходим для расщепления белков, другие соляную кислоту, активирующую работу пепсина и убивающую бактерии, которые проникают в желудочно-кишечный тракт с пищей.
Также клетки слизистой оболочки желудка выделяет слизистое вещество, защищающее оболочку желудка от механических и химических раздражений (самопереваривания).
Пищевой комок из желудка переходит в двенадцатиперстную кишку.
Тонкая кишка
Тонкий кишечник имеет длину 5-6 м. Он подразделяется на двенадцатиперстную кишку (длинной около 30 см), тощую кишку и подвздошную кишку.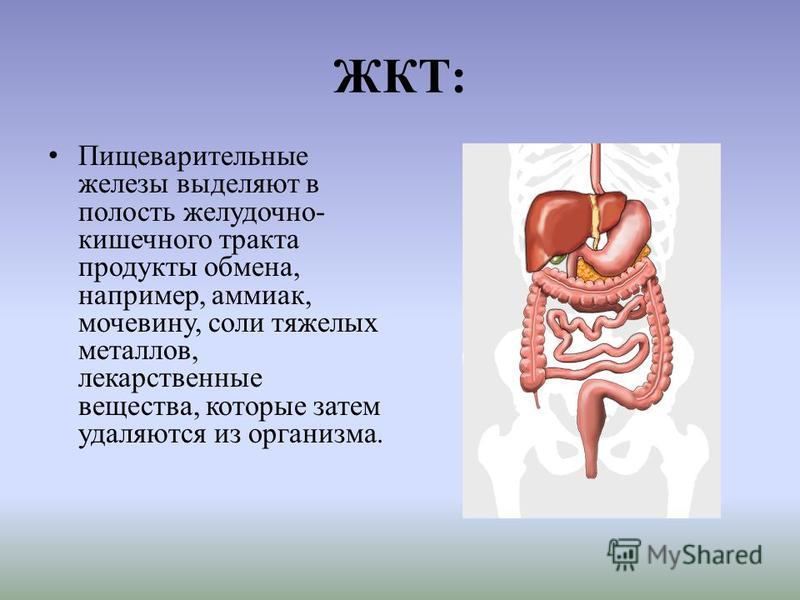
Пищеварение происходит как в полости кишки (полостное), так и на клеточных мембранах (пристеночное), образующих огромное количество ворсинок, выстилающих тонкий кишечник.
Слизистая оболочка тонкой содержится огромное число мелких желёз, выделяющих кишечный сок.
В двенадцатиперстную кишку по желчному протоку поступает желчь (вырабатываемая в печени). Туда же открывается проток поджелудочной железы, по которому в кишечник поступает поджелудочный (панкреатический) сок. Все эти вещества обеспечивают окончательное расщепление питательных веществ.
Печень и поджелудочная железа являются основными пищеварительными железами.
Печень
Печень — самый большой внутренний орган человека (её масса у взрослого человека около 1,5 кг). Она расположена в правой части брюшной полости, под диафрагмой.
Печень состоит из долек, которые образованы печеночными клетками — гепатоцитами. Печень обильно снабжается кровью и желчными капиллярами.
Печень обильно снабжается кровью и желчными капиллярами.
В печени постоянно вырабатывается желчь (горькую зеленовато-жёлтую жидкость), которая накапливается в желчном пузыре. Из него желчь по особому протоку поступает в двенадцатиперстную кишку.
Желчь состоит из воды, желчных кислот и желчных пигментов (имеет щелочную реакцию).
Пищеварительных ферментов в желчи нет, но она активирует действие других пищеварительных ферментов (особенно фермент — липазу, расщепляющую жиры), эмульгирует жиры (способствует механическому дроблению пищевых жиров на мельчайшие капельки), создает щелочную среду в тонкой кишке, усиливает сокоотделение поджелудочной железы.
Печень выполняет так же защитную (барьерную) функцию. Вся кровь, оттекающая от кишечника, проходит через печень. В печени обезвреживается до 95% ядовитых веществ, образующихся в процессе пищеварения (например, продукты распада белков).
Печень также является хранилищем глюкозы (главного источника энергии для всего организма). В печени часть глюкозы превращается в сложный углевод — гликоген и запасается. Если уровень глюкозы в плазме крови понижается, гликоген снова превращается в глюкозу и поступает в кровь.
Поджелудочная железа
Поджелудочная железа имеет гроздевидную форму и расположена в левой части брюшной полости, ниже и несколько сзади желудка, в петле двенадцатиперстной кишки.
Это железа смешанной секреции, выделяющая в своей экзокринной части панкреатический сок, а в эндокринной — гормоны глюкагон и инсулин.
Сок поджелудочной железы (2,0 – 2,5 л в сутки) имеет щелочную реакцию.
Толстый кишечник
Толстый кишечник образован слепой, ободочной и прямой кишками. Его длина 1,5—2 м. Слепая кишка имеет червеобразный отросток — аппендикс.

В толстом кишечнике всасываются вода, продукты расщепления клетчатки. Железы толстой кишки вырабатывают слизь, необходимую для формирования и выведения кала. Пищевые остатки скапливаются в прямой кишке и удаляются через анальное отверстие.
Источники:
Пасечник В.В., Каменский А.А., Швецов Г.Г./Под ред. Пасечника В.В. Биология. 8 класс.– М.: Просвещение
Любимова З.В., Маринова К.В. Биология. Человек и его здоровье. 8 класс – М.: Владос
Лернер Г.И. Биология: Полный справочник для подготовки к ЕГЭ: АСТ, Астрель
http://school-collection.edu.ru
кишечная железа – это… Что такое кишечная железа?
- кишечная железа
1) Medicine: enteraden
2) Fishery: intestinal gland
Универсальный русско-английский словарь. Академик.ру. 2011.
- кишечная диспепсия
- кишечная инвагинация
Смотреть что такое “кишечная железа” в других словарях:
ПОДЖЕЛУДОЧНАЯ ЖЕЛЕЗА — ПОДЖЕЛУДОЧНАЯ ЖЕЛЕЗА.
 Содержание: I. Эмбриология, анатомия и гистология … 16 II. Биохимия………………. 22 III. Патологическая анатомия ……… 2 2 IV. Патологическая физиология……… 28 V. Функциональная диагностика…….. 30 VІ.… … Большая медицинская энциклопедия
Содержание: I. Эмбриология, анатомия и гистология … 16 II. Биохимия………………. 22 III. Патологическая анатомия ……… 2 2 IV. Патологическая физиология……… 28 V. Функциональная диагностика…….. 30 VІ.… … Большая медицинская энциклопедияПоджелу́дочная железа́ — (pancreas) железа пищеварительной системы, обладающая экзокринной и эндокринной функциями. Анатомия и гистология Поджелудочная железа расположена забрюшинно на уровне I II поясничных позвонков, имеет вид уплощенного постепенно суживающегося тяжа … Медицинская энциклопедия
КИШЕЧНИК — КИШЕЧНИК. Сравнительно анатомические данные. Кишечник (enteron) представляет собой б. или м. длинную трубку, начинающуюся ротовым отверстием на переднем конце тела (обычно с брюшной стороны) и кончающуюся у большинства животных особым, анальным… … Большая медицинская энциклопедия
Ободочная кишка — (colon) окаймляет петли тонкой кишки и подразделяется на восходящую, поперечную, нисходящую и сигмовидную.
 Восходящая ободочная кишка (colon ascendens) (рис. 151, 159, 171) является продолжением слепой. Ее задняя поверхность не покрыта брюшиной и … Атлас анатомии человека
Восходящая ободочная кишка (colon ascendens) (рис. 151, 159, 171) является продолжением слепой. Ее задняя поверхность не покрыта брюшиной и … Атлас анатомии человекаБрюшина — (peritoneum) состоит из переходящих друг в друга висцерального (внутренностного) и париетального (пристеночного) листов, между которыми располагается полость брюшины (cavum peritonei) (рис. 158), представляющая собой сложную систему щелевидных… … Атлас анатомии человека
Вода́ — (Н2О) жидкость без запаха, вкуса, цвета; самое распространенное природное соединение. По физико химическим свойствам В. отличается аномальным характером констант, которые определяют многие физические и биологические процессы на Земле. Плотность В … Медицинская энциклопедия
ПИТАТЕЛЬНЫЕ СРЕДЫ — ПИТАТЕЛЬНЫЕ СРЕДЫ, искусственные среды того или иного состава, предназначенные для культивирования микробов и простейших в лабораторных условиях. Впервые были введены для изолирования отдельных видов бактерий Р.

ПЕРИТОНИТ — (peritonitis), воспаление брюшины; П. наблюдается б. ч. как осложнение при заболевании какого либо органа брюшной или смежной с ней полости, но иногда развивается вследствие заноса инфекции кровяным током и из более отдаленных органов. Первичное… … Большая медицинская энциклопедия
Анеми́и — (anaemiae; греч. отрицательная приставка an + haima кровь; синоним малокровие) уменьшение количества гемоглобина в крови, сопровождающееся, как правило, эритроцитопенией. А. распространенное патологическое состояние, возникающее чаще как синдром… … Медицинская энциклопедия
ГРУДНОЙ РЕБЕНОК — ГРУДНОЙ РЕБЕНОК. Общая характеристика особенностей грудного возраста. Грудной возраст в современной педиатрии играет особо важную роль. Мощное развитие знаний о грудном ребенке заставило даже некоторых авторов говорить о выделении… … Большая медицинская энциклопедия
МАТКА — (uterus), орган, являющийся источником менструальной крови (см.
 Менструация) и местом развития плодного яйца (см. Беременность, Роды), занимает центральное положение в половом аппарате женщины и в тазовой полости; лежит в геометрическом центре… … Большая медицинская энциклопедия
Менструация) и местом развития плодного яйца (см. Беременность, Роды), занимает центральное положение в половом аппарате женщины и в тазовой полости; лежит в геометрическом центре… … Большая медицинская энциклопедия
Обоснованный подход к лечению железодефицитной анемии
Если в анализе крови наблюдается понижение гемоглобина, но при этом эритроцитарные индексы повышены, речь идет о макроцитарной анемии. В таком случае дополнительно необходимо назначить анализ на уровень ферритина сыворотки крови, фолатов и витамина В12, чтобы исключить железодефицитную анемию и В12 и фолиеводефицитную анемию. Соответственно, если уровень В12 и фолатов снижен, пациенту ставится диагноз В12 и фолиеводефицитная анемия. В обратном случае (когда В12 и фолаты в норме, а гемоглобин у пациента снижен), это говорит о наличии сопутствующего хронического заболевания (ХОБЛ, гипотериоз, длительные интоксикации, алкоголизм и т.д.). В последнем случае сывороточный ферритин может быть повышен (100-800 нг/мл).
Если в анализе крови наблюдается понижение гемоглобина, но при этом эритроцитарные индексы в норме, это говорит о нормоцитарной анемии, картина которой характерна для гемолитических реакций (гемолитическая анемия), хронической болезни почек или дефицита пищевых факторов (алиментарная анемия).
Эпидемиология дефицита железа (ВОЗ, 2009)
Железодефицитные анемии составляют 70-80% среди всех анемий, при этом около 1,7 млрд. человек в мире страдает железодефицитной анемией (ЖДА), а людей со скрытым дефицитом железа, когда уровень гемоглобина остается еще нормальным, а запасы железа снижены — в 2 раза больше. До 35% населения Земли имеет латентный дефицит железа (50% из них – женщины). 41,8% беременных женщин имеют ЖДА, 12% женщин детородного возраста имеют ЖДА, 47,4% детей дошкольного возраста имеют ЖДА.
Причины ЖДА
1. Потеря крови. К обеднению организма железом могут привести как однократная потеря крови, так и повторные кровотечения. У девушек основным фактором являются обильные, длительные месячные. Считается, что критической в отношении развития дефицита железа является кровопотеря равная 40-60 мл крови за цикл. Желудочно-кишечные кровотечения, вследствие эрозий, язвенной болезни, полипов, онкопатологии. Глистные инвазии в связи с постоянными кровопотерями. Донорство.
У девушек основным фактором являются обильные, длительные месячные. Считается, что критической в отношении развития дефицита железа является кровопотеря равная 40-60 мл крови за цикл. Желудочно-кишечные кровотечения, вследствие эрозий, язвенной болезни, полипов, онкопатологии. Глистные инвазии в связи с постоянными кровопотерями. Донорство.
2. Нарушение резорбции железа при частичном желудочно-кишечном иссечении, синдромах мальабсорбции (спру, болезнь Крона), при наличии факторов, тормозящих резорбцию.
3. Повышение потребностей – в периоде усиленного роста (первые 2 года жизни) и полового созревания, увеличение физической массы при систематических занятиях спортом, при частых инфекциях, беременности, лактации.
4. Роль питания.
Симптомы дефицита железа с или без анемии у взрослых
1. Анемический синдром:
– Усталость
– Снижение толерантности к физической нагрузке и выносливости
– Понижение концентрации внимания, нервозность, забывчивость
– Депрессия, психическая лабильность
– Головная боль по утрам
– Повышение восприимчивости к инфекциям
– Бледный цвет кожи
2. Тканевой гипоксический синдром:
Тканевой гипоксический синдром:
– Ломкость волос и ногтей, койлонихия
– Сухость кожи
– Долго незаживающие «заеды», глоссит, ангулярный стоматит
– Прихоти вкуса, извращенный аппетит (мел, уголь)
– Нарушение глотания, эзофагит
Симптомы дефицита железа у беременных
– Задержка внутриутробного развития плода вследствие дисфункции плаценты
– Риск внутриутробной гибели плода
– Риск преждевременных родов
– Риск пиелонефрита
– Снижение толерантности к родовой кровопотере
– Фактор повышающий риск материнской смертности
Этапы ведения больных с ЖДА представлены ниже.
Анемия и хроническая сердечная недостаточность ,
18 марта 2021 г.
Большинство проблем, связанных с диагностикой, лечением и реабилитацией пожилых больных хронической сердечной недостаточностью (ХСН), по-прежнему приходится решать врачу-терапевту и врачу общей практики. ХСН на сегодняшний день вполне возможно рассматривать как заболевание пожилого возраста, поскольку в течение последних двух десятилетий существенно изменился «фенотип» больных ХСН: увеличилось число больных старшего возраста, число больных с сохраненной и промежуточной фракцией выброса левого желудочка (ФВЛЖ), количество сопутствующих заболеваний и принимаемых лекарственных препаратов.
Сопутствующие заболевания могут взаимно провоцировать прогрессирование друг друга, включая декомпенсацию сердечной деятельности, приводя к госпитализациям или летальному исходу. Среди сопутствующих заболеваний особый интерес представляют анемия и железодефицитное состояние (дефицит железа).
Анемия — это патологическое состояние, которое характеризуется абсолютным снижением концентрации гемоглобина и количества эритроцитов в единице объема крови за счет их уменьшения в организме. Эксперты ВОЗ (2001) рекомендуют использовать значения гемоглобина 13,0 г/дл и ниже у мужчин и 12,0 г/дл и ниже у женщин в качестве диагностических критериев анемии, осложнившей течение ХСН.
Дефицит железа (сидеропения, гипосидероз
) — это состояние здоровья, при котором доступное количество железа в организме недостаточно для удовлетворения его потребностей, и может наблюдаться как на фоне анемии, так и без нее [3].Железодефицитная анемия (ЖДА) представляет собой клинико-гематологический синдром, возникающий при развитии дефицита железа вследствие патологических (или физиологических) процессов, и характеризуется снижением концентрации гемоглобина в сочетании с клиническими признаками сидеропении: трофические нарушения кожи (шелушение, трещины кожных покровов), изменение слизистых оболочек, повышенная ломкость ногтей, выпадение волос, гипотрофический глоссит, гастрит, энтерит, сидеропеническая дисфагия.
Анемия выявляется приблизительно у 30% амбулаторных пациентов со стабильным течением ХСН и у 50% пациентов, получающих лечение в госпитальных условиях, независимо от характера ФВЛЖ. В отличие от популяции пациентов с ХСН, анемия регистрируется у 10% всего населения, и ее частота нарастает с возрастом, достигая 20% у лиц 85 лет и старше [4]. По сравнению с пациентами с ХСН без анемии пациенты с ХСН и анемией обычно старше, среди них чаще встречаются женщины, лица с хронической болезнью почек (ХБП), сахарным диабетом, отечным синдромом, у них более тяжелое течение заболевания, более низкий функциональный статус и уровень артериального давления, более высокая частота назначения диуретиков и более высокий уровень нейрогуморальной, провоспалительной цитокиновой активности и неблагоприятных исходов заболевания [5].
Результаты крупного исследования RED-HF trial (Reduction of Events With Darbepoetin Alfa in Heart Failure) показали, что сама по себе анемия, возможно, не является предиктором летального исхода у больных ХСН, но выступает маркером тяжелого течения сердечной недостаточности [6].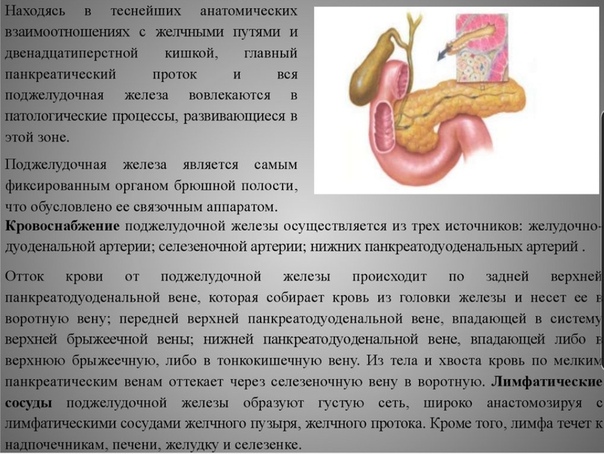
При выявлении у пациента пожилого возраста с ХСН анемии перед врачом, особенно в первичном звене, встает ряд вопросов:
Какова причина анемии?
Каков минимум диагностических мероприятий, требуемых для выявления характера анемии?
Как правильно назначить лечение?
Согласно общепринятой точке зрения анемия у пожилых больных не связана с возрастными изменениями кроветворной системы, а является в большинстве случаев проявлением сопутствующих заболеваний, которые чаще встречаются в более старшем возрасте (ХБП, неопластические процессы, нарушение питания, в основном за счет снижения употребления продуктов, содержащих железо), а другие могут быть не связаны с инволютивными изменениями (эрозивно-язвенные поражения желудочно-кишечного тракта (ЖКТ), прием аспирина, антикоагулянтов, хронические воспалительные заболевания, сердечная кахексия, обусловленная компенсаторной гиподинамией и неполноценным питанием, уменьшение всасывания железа в ЖКТ из-за застоя слизистой и др.
Патогенетические основы коморбидности
Практически у каждого 3-го пациента пожилого возраста анемия развивается без очевидной причины (гипопролиферативная анемия на фоне низкой активности эритропоэтина) [4].
Регуляция эритропоэза является сложным и комплексным процессом c участием разных представителей цитокинов. Для окончательной дифференцировки эритроидных клеток необходим эритропоэтин — гликопротеид, первичный медиатор нормальной физиологической реакции на гипоксию, стимулирующий митоз и являющийся гормоном дифференцировки, который способствует образованию эритроцитов из стволовых клеток. Эритропоэтин вырабатывается преимущественно в почках (в основном в перитубулярных интерстициальных фибробластах коры и внешней области мозгового слоя) и в меньшей степени (до 15%) — в печени (гепатоцитами и фибробластоподобными клетками печени — Ito-клетками).
ХСН способствует гипоперфузии почек, перераспределению кровотока в них, вазоконстрикции, что приводит к нарушению функции почек практически у каждого 2-го пациента пожилого возраста [10]. Анемия, развивающаяся у больных с ХСН и патологией почек, определяется дефицитом эндогенной продукции эритропоэтина вследствие необратимого уменьшения количества клубочков почек или их относительной ишемии из-за снижения сердечного выброса. По мере снижения функциональной активности почек структуры, продуцирующие эритропоэтин, замещаются фиброзной тканью и утрачивают гормонпродуцирующие свойства. В результате гипоперфузии почек нарастает ишемия эндотелиоцитов перитубулярных капилляров и фибробластов, локализующихся в тубулоинтерстиции, и уменьшается продукция эритропоэтина. Помимо этого, протеинурия при ХСН усиливает потерю эритропоэтина, трансферрина, ионизированного железа с мочой и может приводить к развитию железодефицитного состояния.
Анемия, развивающаяся у больных с ХСН и патологией почек, определяется дефицитом эндогенной продукции эритропоэтина вследствие необратимого уменьшения количества клубочков почек или их относительной ишемии из-за снижения сердечного выброса. По мере снижения функциональной активности почек структуры, продуцирующие эритропоэтин, замещаются фиброзной тканью и утрачивают гормонпродуцирующие свойства. В результате гипоперфузии почек нарастает ишемия эндотелиоцитов перитубулярных капилляров и фибробластов, локализующихся в тубулоинтерстиции, и уменьшается продукция эритропоэтина. Помимо этого, протеинурия при ХСН усиливает потерю эритропоэтина, трансферрина, ионизированного железа с мочой и может приводить к развитию железодефицитного состояния.
Подавление костномозговой функции с формированием анемии при ХСН может реализоваться и через воспалительные реакции, т. к. при данном заболевании увеличивается уровень и активность провоспалительных цитокинов, в частности ФНО-α и ИЛ-6. Повышение цитокинов ассоциируется с угнетением пролиферации и дифференцировки эритроидных клеток-предшественников, с неадекватной гипоксией, выработкой эндогенного эритропоэтина и повышением синтеза гепсидина. Последний высвобождается в печени в ответ на воспаление и подавляет абсорбцию железа в тонком кишечнике и выход железа из ретикулоэндотелиальной макрофагальной системы вследствие снижения активности ферропортина, что приводит к неэффективному эритропоэзу.
Последний высвобождается в печени в ответ на воспаление и подавляет абсорбцию железа в тонком кишечнике и выход железа из ретикулоэндотелиальной макрофагальной системы вследствие снижения активности ферропортина, что приводит к неэффективному эритропоэзу.
Показано, что низкий уровень гепсидина, наряду с нормальными значениями показателей воспалительного ответа и отсутствием связи между ними, а также отсутствием корреляции между уровнем гепсидина и концентрацией гемоглобина, свидетельствует о том, что гепсидин не играет роли в развитии анемии у больных старшего возраста с ХСН и ЖДА. И наоборот, высокие уровни гепсидина, показателей воспаления, положительные корреляции между ними и отрицательная корреляция между уровнем гепсидина и концентрацией гемоглобина указывают на воспаление как причину повышения уровня гепсидина, который обусловливает развитие анемии при ХСН в пожилом и старческом возрасте [11].
Возможной причиной развития анемии при ХСН является применение ингибиторов ренин-ангиотензин-альдостероновой системы, в частности иАПФ и АРА, особенно в высоких дозах, что замедляет выработку эритропоэтина в почках и снижает его активность в костном мозге. К примеру, обсуждается роль ингибитора гематопоэза N-ацетил-серил-аспартил-лизил-пролина (AсSDKP), который разрушается под действием АПФ, роль уменьшения циркулирующего ангиотензина II — митогенного фактора для предшественников эритропоэтина [12, 13].
К примеру, обсуждается роль ингибитора гематопоэза N-ацетил-серил-аспартил-лизил-пролина (AсSDKP), который разрушается под действием АПФ, роль уменьшения циркулирующего ангиотензина II — митогенного фактора для предшественников эритропоэтина [12, 13].
Сахарный диабет также играет немаловажную роль в развитии анемии, т. к. в процессе гликозилирования на ранних этапах повреждаются продуцирующие эритропоэтин клетки в почках [14].
У большинства пациентов с ХСН, помимо истинной анемии, может встречаться и гемодилюционная анемия, при которой снижение гемоглобина и гематокрита становится результатом повышенного объема плазмы[15]. Сниженный кровоток в почках и усиленная канальцевая реабсорбция натрия при ХСН способствуют увеличению объема плазмы, который обычно повышен даже при отсутствии застойных явлений. Еще в 2003 г. А. Androne et al. [16] показали неблагоприятный прогноз у пациентов с ХСН и гемодилюцией в отличие от пациентов с истинной анемией, и возможным объяснением этого факта выдвинули перегрузку объемом, приводящую к дилатации ЛЖ, увеличению длины саркомеров и перерастяжению миофибрилл, что в итоге приводит к эксцентрической гипертрофии миокарда — независимого предиктора неблагоприятного исхода. На сегодняшний день существует мнение, что гемодилюция предшествует клиническим проявлениям накопления жидкости и играет немаловажную роль в развитии анемии при ХСН. Помимо этого у пациентов со стабильной ХСН и низкой ФВЛЖ при оптимальной медикаментозной терапии объем плазмы в целом нормальный, но неоднородно распределенный, а встречаемость анемии при ХСН гораздо выше, чем когда ее оценивают только по уровню гемоглобина (поскольку методы измерения внеклеточного объема жидкости не всегда доступны, особенно в рутинной клинической практике) [17].
На сегодняшний день существует мнение, что гемодилюция предшествует клиническим проявлениям накопления жидкости и играет немаловажную роль в развитии анемии при ХСН. Помимо этого у пациентов со стабильной ХСН и низкой ФВЛЖ при оптимальной медикаментозной терапии объем плазмы в целом нормальный, но неоднородно распределенный, а встречаемость анемии при ХСН гораздо выше, чем когда ее оценивают только по уровню гемоглобина (поскольку методы измерения внеклеточного объема жидкости не всегда доступны, особенно в рутинной клинической практике) [17].
При ХСН дефицит железа рассматривается как сопутствующая патология и встречается у 37–61% пациентов [18]. Данные исследования NHANES III свидетельствуют о наличии дефицита железа у 61,3% из 574 взрослых пациентов с ХСН (уровень ферритина менее 100 или 100–199 при уровне трансферрина <20%) [19]. Согласно E. Jankowska et al. дефицит железа имел место у 37% из 546 пациентов с ХСН (включая 32% пациентов без анемии) [20].
Результаты проспективного обсервационного регистра PReP registry (Prävalenz des Eisenmangels bei Patienten mit Herzinsuffizienz) с участием амбулаторных пациентов с ХСН и ФВЛЖ ≤45% из Германии показали встречаемость дефицита железа у 42,5% пациентов (до включения в регистр никто из пациентов не знал о наличии этого состояния у них), анемии — у 18,9% (4,8% пациентов знали о наличии у них анемии). Средний возраст пациентов составил 69,0±10,6 года, среди них было 25,3% женщин, ФВЛЖ отмечена у 35,3±7,2%. Дефицит железа ассоциировался с женским полом, более низкой массой тела и низким уровнем гемоглобина, более высоким функциональным классом (ФК) ХСН и высоким уровнем натрийуретического пептида (при всех показателях p<0,05) [21].
Средний возраст пациентов составил 69,0±10,6 года, среди них было 25,3% женщин, ФВЛЖ отмечена у 35,3±7,2%. Дефицит железа ассоциировался с женским полом, более низкой массой тела и низким уровнем гемоглобина, более высоким функциональным классом (ФК) ХСН и высоким уровнем натрийуретического пептида (при всех показателях p<0,05) [21].
Железо играет центральную роль в поглощении, транспорте, хранении и метаболизме кислорода, эритропоэзе и клеточном иммунном ответе. Регуляция баланса железа, определяемого комбинацией абсорбции алиментарного железа, использования и его выведения, необходима для поддержания основных клеточных функций, особенно в клетках с высокими энергетическими потребностями — скелетных миоцитах и кардиомиоцитах [22, 23]. Дефицит железа может приводить к дисфункции митохондрий, нарушению активности ферментов, активации апоптоза, нарушению синтеза и функции белков. Последствия дефицита железа выражаются в ремоделировании тканей организма, в снижении работоспособности и изменении когнитивно-эмоциональной cферы.
Дефицит железа как на фоне анемии, так и независимо от нее может ухудшать течение самой ХСН и заболеваний, лежащих в ее основе, значительно снижать качество жизни, физическую активность и увеличивать риск летального исхода [24, 25]. К тому же дефицит железа повышает вероятность госпитализаций пациентов с ХСН [26].
- Moliner et al. полагают, что дефицит железа возможно рассматривать не только в качестве одного из сопутствую-щих состояний, но и как ключевой элемент в патофизиологической последовательности изменений, способствующий развитию и прогрессированию ХСН [28].
Дефицит железа может быть абсолютным, когда общее количество железа в организме снижается, или функциональным, когда общее количество железа в организме нормальное или повышенное, но достаточное количество железа не поступает из депо (происходит неравномерное распределение железа). При абсолютном дефиците железа снижаются и общие запасы железа, и запасы функционального железа, тогда как при функциональном дефиците железа снижается лишь пул функционального железа. Оба состояния могут возникать независимо друг от друга или сосуществовать у отдельного пациента.
Абсолютный дефицит железа при сердечной недостаточности может быть вызван снижением потребления железа из-за анорексии, кахексии, нарушенного всасывания железа в результате отека слизистой кишечника, а также индуцированным гепсидином подавлением активности переносчиков железа (например, ферропортина). Другие причины абсолютного дефицита железа включают желудочно-кишечные кровотечения, связанные с использованием аспирина, антиагрегантов или антикоагулянтов или вызванные сопутствующими заболеваниями, такими как злокачественные новообразования ЖКТ или мочеполовой системы.
Функциональный дефицит железа при ХСН вызван механизмами, аналогичными тем, которые ответственны за анемию хронического заболевания или воспаления, обусловленных повышением уровня воспалительных цитокинов, включая ИЛ-1, ИЛ-6, ИЛ-18 и ФНО-α, которые, в свою очередь (особенно ИЛ-6), повышают уровень гепсидина в печени. Пролиферация эритробластов напрямую ингибируется повышенными уровнями гепсидина, что еще более ухудшает синтез гемоглобина (рис. 2) [9].
Принципы дифференциальной диагностики
Ранними проявлениями ХСН в пожилом возрасте могут быть утомляемость, слабость, тяжесть в ногах, часто проявляющиеся во время повседневной физической нагрузки и не всегда ассоциирующиеся с выраженностью одышки и отечного синдрома. Пациенты могут жаловаться на головокружение, пресинкопальные и синкопальные состояния, раздражительность, нарушение сна. Как правило, эти симптомы малоспецифичны, поскольку могут присутствовать и при других заболеваниях, в частности при анемии. Клиническая картина анемического синдрома включает в себя 3 субъективных симптома: усталость, одышку и сердцебиение. При осмотре пациента с ХСН следует обращать внимание не только на эти симптомы, являющиеся неотъемлемой частью клинической картины сердечной недостаточности, но и помнить об анемическом синдроме и не игнорировать роль гемодилюции, особенно у лиц пожилого возраста.
Затруднения в дифференциальной диагностике ХСН возникают, как правило, вследствие мультиморбидности. У пожилых больных с анемией также нередко приходится исключать или подтверждать наличие ХСН. Диагностическими критериями в этом случае является совокупность анамнестических данных (в частности, ишемическая болезнь сердца, инфаркт миокарда), клинических симптомов и признаков (смещение верхушечного толчка влево, повышенная ЧСС), данных объективных методов исследования. С учетом атипичности клинических проявлений и малосимптомности заболевания в пожилом возрасте большое значение приобретает контроль уровня натрийуретического пептида.
При постановке диагноза ЖДА решающее значение имеют данные комплекса лабораторных исследований — подтверждение факта анемии и дефицита железа. Анализ крови характеризуется наличием признаков гипохромной микроцитарной анемии со снижением концентрации гемоглобина и цветового показателя. Гипохромия — уменьшение средней концентрации Hb в эритроцитах (<24 пг), микроцитоз — уменьшение размеров эритроцитов (<75 нм). В мазках крови преобладают небольшие по размеру гипохромные эритроциты, аннулоциты (эритроциты в виде колец с отсутствием Hb в центре), отмечаются пойкилоцитоз и анизоцитоз. В пользу дефицита железа свидетельствуют уровень сывороточного железа <12,5 мкмоль/л, ферритина сыворотки <30 мкг/л, сатурация трансферрина <17%) [29].
При анемии, развившейся на фоне кровопотери, непосредственно после кровотечения отмечается повышение количества ретикулоцитов. Количество лейкоцитов имеет тенденцию к снижению, но лейкоцитарная формула не меняется. Количество тромбоцитов обычно нормальное, с тенденцией к увеличению при кровотечении. Наблюдается снижение уровня сывороточного железа и повышение общей железосвязывающей способности плазмы крови. Около 33% всего количества трансферрина сыворотки связано с железом (показатель насыщения трансферрина железом). Остальное количество трансферрина остается свободным и характеризует скрытую железосвязывающую способность сыворотки крови. При дефиците железа снижается уровень трансферрина до 10–20 мг/л, но при этом увеличивается скрытая железосвязывающая способность плазмы.
На сегодняшний день эксперты рекомендуют проводить скрининг дефицита железа у всех пациентов, независимо от уровня гемоглобина, с впервые поставленным диагнозом ХСН (класс рекомендаций I, уровень доказанности С), а также при наличии уже существующей ХСН с клиническими проявлениями. Лабораторные параметры обмена железа рекомендовано определять хотя бы однократно в год (табл. 3) [1, 29].
Таким образом, дефицит железа у пациентов с ХСН диагностируется при снижении уровня ферритина <100 мкг/л или при уровне ферритина 100–299 мкг/л при условии, что сатурация трансферрина <20%.
Следует отметить, что ферритин не обладает диагностической ценностью, поскольку достаточно изменчив, является белком острой фазы, а его увеличение, которое наблюдается при ХСН и других воспалительных заболеваниях, не всегда отражает высокие уровни запаса железа, что следует принимать во внимание. К тому же показано, что именно низкий уровень сатурации трансферрина, а не ферритина ассоциируется с высоким риском летальности [30]. Кроме этого, у пациентов с уровнем сатурации трансферрина 20,1% не наблюдалось улучшения выживаемости при приеме железосодержащих препаратов [31].
Насыщение трансферрина железом является биологическим маркером доставки железа клеткам. Трансферрин — это специфический транспортный белок плазмы
крови, который обеспечивает доставку железа к клеткам через рецепторы трансферрина. Поскольку концентрация трансферрина зависит от многих факторов, в практике его в изолированном виде не используют для определения дефицита железа в организме. Степень насыщения трансферрина железом (СНТЖ) рассчитывается методом деления сывороточной концентрации железа на сывороточную концентрацию трансферрина и отражает то количество железа, которое доступно для эритробластов и других клеток, нуждающихся в нем. СНТЖ не зависит от степени воспаления в организме, а его уровень менее 20% свидетельствует о недостаточном эритропоэзе [32].
Авторы последних исследований полагают, что лечение ЖДА само по себе может быть благоприятно, но сохраняется ряд пробелов в вопросах понимания, когда, как и насколько длительно необходимо лечить текущую анемию или железодефицитное состояние при ХСН, а также понимания механизмов, лежащих в основе лечебных эффектов.
Основные принципы лечения ЖДА, в т. ч. у лиц пожилого возраста с ХСН
Установить причину кровопотери и провести лечение основного заболевания.
Нельзя только одной диетой вылечить ЖДА!
Возместить дефицит железа без железосодержащих лекарственных средств невозможно!
Терапию препаратами железа необходимо проводить длительно.
Терапия ЖДА не должна прекращаться после нормализации уровня гемоглобина и количества эритроцитов.
Гемотрансфузии при ЖДА должны проводиться строго по жизненным показаниям.
Парентеральное назначение препаратов показано только при определенных обстоятельствах.
Целью лечения ЖДА при ХСН является достижение уровня Hb ≥120 г/л за счет перорального или парентерального введения необходимого количества железа.
Терапевтические возможности в отношении улучшения функциональной способности человека очень ограничены, и целевое выявление нарушений, препятствующих транспортировке кислорода и/или его использованию, может достичь функциональных преимуществ. Эти гипотезы были подтверждены во всех 5 рандомизированных контролируемых исследованиях по изучению парентерального введения железа с участием пациентов с ХСН.
К примеру, исследование FAIR-HF (The Ferinject Assessment in Patients with Iron Deficiency and Chronic Heart Failure) продемонстрировало улучшение самочувствия, функциональной и физической работоспособности пациентов с ХСН и дефицитом железа (средний возраст 67 лет, ФВЛЖ <40%) при применении карбоксимальтозата железа [33]. Результаты многоцентрового, двойного слепого плацебо-контролируемого рандомизированного исследования CONFIRM-HF (Ferric CarboxymaltOse evaluatioN on perFormance in patients with IRon deficiency in coMbination with chronic Heart Failure) с участием 304 амбулаторных пациентов с клинически выраженной ХСН, ФВЛЖ ≤45%, повышенным уровнем НУП и дефицитом железа (ферритин <100 нг/мл или 100–300 нг/мл при уровне сатурации трансферрина <20%) также подтвердили положительное действие парентерального введения железа на функциональный статус, выраженность клинических симптомов и качество жизни пациентов [34]. Рандомизированное контролируемое исследование EFFECT-HF (Effect of Ferric Carboxymaltose on Exercise Capacity in Patients With Iron Deficiency and Chronic Heart Failure) с участием 172 пациентов с ХСН и железодефицитом показало увеличение VO2 max у пациентов, которым парентерально вводился препарат железа, по сравнению с группой контроля [35].
Результаты исследования FAIR-HF2 (Intravenous Iron in Patients With Systolic Heart Failure and Iron Deficiency to Improve Morbidity & Mortality) с участием пациентов с систолической дисфункцией ЛЖ и дефицитом железа ожидаются в 2020 г. [36].
Благоприятный эффект препаратов железа, оказываемый на пациентов с ХСН, подтвержден и в метаанализе, проведенном в 2018 г. S. Anker et al., согласно которому парентеральное введение железа способствовало снижению частоты повторных госпитализаций в связи с декомпенсацией ХСН (ОШ 0,53; 95% ДИ 0,33–0,86; р=0,011) и повторных госпитализаций по сердечно-сосудистым причинам (ОШ 0,60; 95% ДИ 0,41–0,88; р=0,009) [31].
Вышепредставленные данные позволяют рассматривать терапию железосодержащими препаратами как полезное дополнение к общепринятому медикаментозному лечению пациентов с ХСН.
Имеющаяся на сегодняшний день доказательная база по лечению пациентов пожилого и старческого возраста с ХСН и анемией не позволяет однозначно рассматривать вышепредставленные подходы как целесообразные и безопасные. К тому же нет данных об эффективности и безопасности терапии препаратами железа у пациентов с ХСН с сохраненной и промежуточной ФВЛЖ, большинство из которых и являются лицами старшего возраста.
В связи с этим эксперты Общества специалистов по сердечной недостаточности акцентируют внимание на необходимости выявления и коррекции причин, приводящих к развитию железодефицита у пациентов с ХСН (алиментарные нарушения, желудочно-кишечные кровотечения, прием нежелательных лекарственных препаратов и др.).
Пероральные железосодержащие средства могут быть препаратами выбора при ЖДА в комплексном лечении пациентов c ХСН вследствие их достаточно высокой эффективности и низкой стоимости. Лекарственные препараты железа могут быть в виде ионизированного (Fe2+) в составе органических или неорганических солей (фумарат, лактат, сульфат, хлорид) и неионного — в составе комплексов, содержащих окисное железо (Fe3+), — протеин-сукцинилат, полимальтозат или сахарозный комплекс. Препараты ионизированного железа используются только перорально, препараты комплексов окисного железа — парентерально.
Эффективность лечения пациентов с ЖДА определяется суточной дозой и формой элементарного железа, входящего в состав лекарственного препарата. При этом темп нарастания уровня гемоглобина зависит от выраженности анемического синдрома. Выбор между препаратами железа — Fe2+ или Fe3+ — определяется в первую очередь клинической целью: быстрое достижение эффекта (предпочтение отдается препарату Fe2+) или хорошая переносимость на фоне длительного приема (предпочтение отдается препарату Fe3+).
Железа (III) гидроксид полимальтозат показан для лечения латентного железодефицита и ЖДА. Этот препарат имеет несколько лекарственных форм, в частности форму жевательных таблеток, содержащих 400 мг железополимальтозного комплекса (100 мг элементарного железа), что позволяет пациенту принимать препарат по 1 таблетке 2 р./день с хорошим клиническим эффектом. Данное действие препарата обусловлено, во‑первых, структурой комплекса, которая имеет железо (III) гидроксидное ядро и углеводную оболочку, что напоминает белок запаса железа — ферритин, и, во‑вторых, контролируемой диссоциацией ионов железа из этого лекарственного комплекса. Помимо вышесказанного, полимальтозная оболочка обеспечивает стабильность и растворимость комплекса в достаточно широком диапазоне pH, что и определяет его терапевтическую эффективность и хорошую переносимость с последующим улучшением клинического состояния и качества жизни, что важно в старшем возрасте, особенно при невозможности устранения основной причины заболевания.
Адекватный ответ на терапию железосодержащими препаратами включает [37, 38]:
увеличение количества ретикулоцитов через 7 дней;
увеличение уровня гемоглобина на ≈2 г/дл через 1–2 нед. после начала приема препаратов железа;
нормализацию содержания гемоглобина через 6–8 нед.
Следует обращать внимание на динамику эритроцитарных индексов, нормализация которых отражает адекватность терапии: средний объем эритроцита, среднее содержание гемоглобина в эритроците, среднюю концентрацию гемоглобина в эритроците. Анализы периферической крови проводят 1 раз в 1–2 нед. в начале лечения, а затем 1 раз в 2–4 нед.
Поскольку не вполне корректно расценивать любое снижение гемоглобина ниже нормы у больных ХСН как анемию, то у большинства больных ХСН, помимо истинной анемии, может быть диагностирована и гемодилюция [39, 40], лечение которой должно фокусироваться на коррекции дозы диуретиков. Очевидно, что стратегия лечения возрастной категории пациентов, помимо патогенетической терапии анемии, предусматривает воздействие на нейрогуморальную активацию — применение ингибиторов АПФ и блокаторов рецепторов к ангиотензину II, антагонистов минералокортикоидных рецепторов, бета-адреноблокаторов, а также петлевых диуретиков. Поскольку в развитии отечного синдрома задействованы сложные нейрогуморальные механизмы, бездумная дегидратация вызывает побочные эффекты и рикошетную задержку жидкости, что может приводить к необоснованной терапии.
Блокирование гепсидина может быть эффективной терапевтической стратегией, особенно в отношении функционального железодефицита. Как перспективные меры могут рассматриваться прямая блокада экспрессии гепсидина с помощью анти-гепсидин-1-олигорибонуклеотида (lexaptepid), подавление активности гепсидина с помощью препаратов человеческих антител к гепсидину, блокирование передачи сигнала с гепсидина с помощью низкомолекулярного ингибитора (LDN-193189) или неантикоагулянтные гепарины. Спиронолактон, обычно используемый в качестве основного лекарственного средства у пациентов с сердечной недостаточностью, подавляет экспрессию гепсидина у мышей [41, 42].
Заключение
Таким образом, анемия и дефицит железа являются часто встречающимися сопутствующими ХСН состояниями у лиц пожилого возраста. Дефицит железа как на фоне анемии, так и независимо от анемии может ухудшать течение ХСН и заболеваний, лежащих в основе ее развития, снижать качество жизни, физическую активность пациентов и увеличивать риск неблагоприятных событий. Принципиально важным является скрининг дефицита железа у всех пациентов с ХСН, особенно при впервые возникшей, а при постановке диагноза ЖДА решающее значение имеют данные лабораторных исследований — подтверждение факта анемии и дефицита железа. На сегодняшний день однозначных рекомендаций по лечению пациентов пожилого и старческого возраста с ХСН и анемией не существует. В связи с этим необходимо выявлять и корректировать причины дефицита железа у пациентов с ХСН, воздействовать на нейрогуморальную активацию и разумно подходить к лечению отечного синдрома. Требуется тесное сотрудничество нефрологов, кардиологов, терапевтов для эффективной коррекции терапии ХСН и анемии в соответствии с современными достижениями и требованиями. Только в условиях активного регулярного врачебного наблюдения возможно улучшить качество и увеличить продолжительность жизни больным ХСН.
Отделение абдоминальной хирургии – ФГБУ «Национальный медицинский исследовательский центр хирургии имени хирургии им. А.В. Вишневского»
В отделении абдоминальной хирургии проводятся диагностика заболеваний органов брюшной полости, плановое и срочное хирургическое лечение пациентов с онкологическими и неопухолевыми заболеваниями органов брюшной полости (заболеваниями поджелудочной железы, внепеченочных желчных протоков, желчного пузыря, селезенки, тонкой и толстой кишки, неорганными опухолями).
Значительная часть наших пациентов – больные, которых в Центр хирургии им. А.В. Вишневского направляют из других медицинских учреждений страны из-за сложности требующегося оперативного вмешательства и необходимости оказания самой современной высокотехнологичной помощи.
В настоящее время абдоминальное отделение Центра хирургии им. А.В. Вишневского занимает лидирующее положение в хирургическом лечении опухолей поджелудочной железы и хронического панкреатита. На протяжении года у нас выполняется более 150 различных операций на поджелудочной железе.
В отделении накоплен самый большой в Российской Федерации опыт хирургического лечения больных хроническим панкреатитом, кистами поджелудочной железы, злокачественными и доброкачественными опухолями поджелудочной железы. Отделение является лидером в области хирургического лечения органического гиперинсулинизма (инсулиномы).
Научные и клинические достижения специалистов отделения неоднократно отмечены высокими наградами. За разработку новых методов хирургического лечения больных хроническим панкреатитом руководитель отделения, доктор медицинских наук, профессор А.Г. Кригер удостоен Премии Правительства РФ за 2015 год. А за разработку методов диагностики и лечения больных с нейроэндокринными опухолями поджелудочной железы проф. А.Г. Кригеру в 2017 году вручена Премия Правительства Москвы.
Специалисты отделения являются авторами национальных клинических рекомендаций по хирургическому лечению хронического панкреатита, которыми в настоящее время пользуются все профильные клиники России.
Сотрудники отделения абдоминальной хирургии разработали и внедрили в клиническую практику технику резекций (панкреатодуоденальной и дистальной) и полного удаления поджелудочной железы (панкреатэктомии) в сочетании с сосудистой резекцией и протезированием артериальных и венозных стволов, расширенной лимфодиссекцией при раке поджелудочной железы.
Здесь внедрены органосберегающие методики изолированных резекций головки поджелудочной железы с сохранением двенадцатиперстной кишки при доброкачественных кистозных опухолях и хроническом панкреатите. Данный подход позволяет надежно излечить пациента и обеспечить хорошее качество жизни.
В отделении активно применяются малотравматичные хирургические технологии – робот-ассистированные и лапароскопические операции при заболеваниях органов брюшной полости. Именно в нашем отделении впервые в России в 2009 году начали выполнять робот-ассистированные операции на органах брюшной полости.
Подробнее
Научная работа отделения
Опубликованные научные работы отделения абдоминальной хирургии за 2017-2020 годы
- Кригер А.Г., Трошина Е.А., Кармазановский Г.Г., Горин Д.С., Калинин Д.В., Калдаров А.Р., Дугарова Р.С., Чекмарева И.А., Лебедева А.Н., Демидова В.С., Платонова Н.М., Юкина М.Ю. Робот-ассистированная дуоденопанкреатэктомия при множественных нейроэндокринных опухолях. Анналы хир. гепатологии. 2017; 22;4:102-108.
- А.Г. Кригер, А.О. Гуща, Д.С. Горин, А.Р. Калдаров. Шваннома малого таза и ягодичной области. Хирургия. Журнал им. Н.И. Пирогова. 2017; 10:88-90.
- Кригер А.Г.,Смирнов А.В., Горин Д.С., Ратникова Н.К., Икрамов Р.З. Клиническое наблюдение ошибочной хирургической тактики у больного хроническим панкреатитом. Анналы хир. гепатологии. 2017; 22;3:77-81.
- Глотов А.В., Калинин Д.В., Смирнов А.В., Кригер А.Г. Стадирование нейроэндокринной опухоли поджелудочной железы (обзор литературы) Анналы хир. гепатологии. 2017; 2.2; 3:70-76
- Е.Н. Гордиенко, И.А. Чекмарева, О.В. Паклина, А.Р. Калдаров, И.В. Ларичева. Ультраструктурные особенности межклеточных контактов в инсулиномах поджелудочной железы. Гены&Клетки 2017; 12;2:104-109.
- Кригер А.Г., Горин Д.С., Гоев А.А., Варава А.Б., Берелавичус С.В., Ахтанин Е.А. Послеоперационное кровотечение в хирургии поджелудочной железы. Анналы хир. гепатологии. 2017; 22; 2:36-44
- Кригер А.Г., Кармазановский Г.Г., Смирнов А.В. Лучевая диагностика и тактика хирургического лечения хронического панкреатита. Хирургия. Журнал им. Н.И. Пирогова. 2017; 5:4-13
- Кригер А.Г. Технические аспекты операций при острой спаечной кишечной непроходимости. Хирургия. Журнал им. Н.И. Пирогова. 2017; 4:81-84.
- Кригер А.Г., Калдаров А.Р., Гогия Б.Ш., Горин Д.С., Матушевская В.Н., Аляутдинов Р.Р. Кишечный свищ после грыжесечения с пластикой брюшной стенки композитным протезом. Хирургия. Журнал им. Н.И. Пирогова. 2017; 4:77-80.
- Кригер А.Г. Размышления об остром аппендиците. Хирургия. Журнал им. Н.И. Пирогова. 2017; 4:43-44.
- Кригер А.Г., Нерестюк Я.И, Кармазановский Г.Г., Кубышкин В.А., Хайриева А.В. Трехмерная реконструкция компьютерных томограмм в выборе оперативного вмешательства при протоковой аденокарциноме поджелудочной железы. Хирургия. Журнал им. Н.И. Пирогова. 2017; 4:36-40.
- Кригер А.Г., Берелавичус С.В., Титова Н.Л., Калдаров А.Р., Смирнов А.В. Робот-ассистированные операции на поджелудочной железе (обзор литературы). Анналы хир.гепатологии. 2017; 22;1:55-63
- Кригер А.Г. Комментарий к статье Степан Е.В., Ермолова А.С., Рогаль Е.В. и соавт. «Принципы лечения больных с наружными панкреатическими свищами». Хирургия. Журнал им. Н.И. Пирогова. 2017; 3:48-49
- Кригер А.Г., Берелавичус С.В., Поляков И.С., Варава А.Б., Сон А.И., Ахмедов Б.Г., Гальчина Ю.С.
- Плексиформная нейрофиброма малого таза при болезни фон Реклингхаузена. Хирургия. Журнал им. Н.И. Пирогова. 2017; 3:90-93.
- Кригер А.Г. Комментарий к статье С.А. Будзинского и соавт. «Эндоскопическое транспапиллярное панкреатическое стентирование в лечении свищей поджелудочной железы». Хирургия. Журнал им. Н.И. Пирогова. 2017; 2:44.
- А.Г. Кригер, И.С. Поляков, Д.С.Горин, А.В. Смирнов. Редкое сочетание осложнений хронического панкреатита. Хирургия. Журнал им. Н.И. Пирогова. 2017; 2:77-79
- А.Г. Кригер, С.В. Берелавичус, А.И. Сон, Д.С.Горин, А.Р.Калдаров, А.В. Смирнов. Хирургическое лечение неорганных забрюшинных опухолей. Хирургия. Журнал им. Н.И. Пирогова. 2017; 1: 15-21
- Belousova E., Karmazanovsky G., Kriger A. Mannelli L., Glotov A, Karelskaya N., Paklina O., Kaldarov A. Contrast-enhanced MDCT in patients with pancreatic neuroendocrine tumors: correlation with histological findings and diagnostic performance in differentiation between tumor grades. Clin Radiol. 2017;72(2):150-158. doi: 10.1016/j.crad.2016.10.021
- Ревишвили А.Ш., Кригер А.Г., Вишневский В.А., Смирнов А.В., Берелавичус С.В., Горин Д.С., Ахтанин Е.А., Калдаров А.Р., Раевская М.Б., Захарова М.А. Актуальные вопросы хирургии поджелудочной железы. Хирургия. Журнал им. Н.И. Пирогова. 2018;(9):5-14. doi: 10.17116/hirurgia20180915
- Ахтанин Е.А., Гоев А.А., Кригер A.Г., Жарский С.Л. Кольцевидная поджелудочной железа с внутрипанкреатическим расположением воротной вены. Хирургия. Журнал им. Н.И. Пирогова. 2018; 12:126-128
- Кригер А.Г.,Кармазановский Г.Г., Смирнов А.В., Харазов А.Ф., Горин Д.С., Раевская М.Б., Галкин Г.В., Ревишвили А.Ш. Диагностика и лечение рака головки поджелудочной железы, прорастающего мезентерико-портальный сегмент вен. Хирургия. Журнал им. Н.И. Пирогова. 2018; 12: 21-29
- А.Г. Кригер, С.А. Будзинский, М.А. Захарова, Д.С. Горин. Комплексное лечение больного хроническим панкреатитом. Хирургия. Журнал им. Н.И. Пирогова. 2018; 11: 68-70.
- Ахтанин Е.А., Гоев А.А., Давыденко П.И., Кригер А.Г. Интрапанкреатическое расположение воротной вены. Анналы хир. гепатологии. 2018; 23 (3): 64-68.
- А.В. Смирнов, М.А. Захарова С.В.Берелавичус, А.Б. Варава, А.Г.Кригер. Вирсунгоррагия при кистозной муцинозной опухоли поджелудочной железы. Хирургия. Журнал им. Н.И. Пирогова. 2018; 9: 74-76.
- А.Ш. Ревишвили, А.Г. Кригер, В.А. Вишневский, А.В. Смирнов, С.В. Берелавичус, Д.С. Горин, А.Р. Калдаров, Е.А. Ахтанин, М.Б. Раевская, М.А. Захарова. Актуальные вопросы хирургии поджелудочной железы. Хирургия. Журнал им. Н.И. Пирогова. 2018; 9: 5-14
- Кригер А.Г. Комментарий. Хирургия. Журнал им. Н.И. Пирогова. 2018; 5:33.
- А.Г.Кригер, Д.С.Горин, А.Р. Калдаров, С.В.Берелавичус, Е.А. Ахтанин. Добавочная селезенка в паренхиме поджелудочной железы. Хирургия. Журнал им. Н.И. Пирогова. 2018; 8:68-71
- A.G.Kriger, A.R. Kaldarov, D.S. Gorin, S.V. Berelavichus. Surgical approuach for solid pseudopapillary neoplasm of pancreas. Single-centre experience. J. Pancreas (Onlinе) 2018 Mar; 30(2):70-74.
- А.Ш. Ревишвили, А.Г. Кригер, Д.С.Горин, А.Б. Варава, А.А. Гоев, С.В. Берелавичус, А.В. Смирнов, Е.А. Ахтанин. Эндоваскулярные вмешательства в хирургии поджелудочной железы. Хирургия. Журнал им. Н.И. Пирогова. 2018; 4:4-10.
- Кригер А.Г., Берелавичус С.В., Калдаров А.Р., Горин Д.С., Смирнов А.В., Ахтанин Е.А. Робот-ассистированные операции в хирургии поджелудочной железы. Анналы хир. гепатологии. 2018; 23; 1:19-24.
- С.А Совцов, А.Г.Кригер, О.В. Прибыткова, А.В.Смирнов. Возможна ли консервативная терапия острого аппендицита? Хирургия. Журнал им. Н.И. Пирогова. 2018; 2:96-99.
- Дугарова Р.С., Берелавичус С.В., Калдаров А.Р., Горин Д.С. Физические миниинвазивные методы лечения больных с инсулиномами поджелудочной железы. Хирургия. 2018;(4):94-97. doi: 10.17116/hirurgia2018494-97
- Kriger A, Gorin D, Kaldarov A, Berelavichus S, Galkin G, Pletneva V, Karmazanovsky G. A rare case of chronic pancreatitis complicated by internal pancreatic fistula and pancreatogenic ascites. International Journal of Medical Reviews and Case Reports. 2018; 2(4): 115-118. doi: 10.5455/IJMRCR.pancreatic-fistula
- G.Karmazanovsky, E. Belousova, W. Schima, A. Glotov, D. Kalinin, A.Kriger. Nonhypervascular pancreatic neuroendocrine tumors: spectrum of MDCT imagings and differentiation from pancreatic duct adenocarcinoma. Europ. J.of Radiology. 2018; 110: 66-73
- М.А. Захарова, Д.С. Горин, Л.А. Маринова, А.Г. Кригер. Рентгенонегативный вирсунголитиаз у больных хроническим панкреатитом. Хирургия. Журнал им. Н.И. Пирогова. 2019; 12: 137-140.
- А.Г.Кригер, Г.Г. Кармазановский, С.В. Берелавичус, Д.С. Горин, А.Р. Калдаров, В.И. Пантелеев, Д.В. Калинин, М.В. Двухжилов, А.В. Глотов, В.Ю. Зекцер. Дуоденопанкреатэктомия при опухолях поджелудочной железы – pro et contra. Хирургия. Журнал им. Н.И. Пирогова. 2019; 12: 28-36.
- S.V. Berelavichus, A.E. Zotikov, A.G. Kriger, V.I. Panteleev, A.R. Kaldarov. Two-stage combined treatment of leiomyosarcoma of iliac vein using robotic surgery. Journal of vascular Surgery cases and innovative techniques. 2019; 5 (4): 586-588.
- В.И. Пантелеев, Д.С. Горин, А.Р.Калдаров, А.Г. Кригер. Внутрипротоковая папиллярная муцинозная опухоль поджелудочной железы. Хирургия. Журнал им. Н.И. Пирогова. 2019; 11: 81-85.
- М.А. Захарова, А.В. Смирнов, Д.С. Горин, Е.А. Воробьева, А.Г. Кригер. Качество жизни как показатель эффективности хирургического лечения хронического панкреатита. Хирургия. Журнал им. Н.И. Пирогова. 2019; 11: 42-51.
- Ю.И. Патютко, А.Г. Котельников, А.Г. Кригер, И.С. Проскуряков, Г.В. Галкин, А.Н. Поляков, И.А. Файнштейн. Метастазы рака почки в поджелудочной железе: опыт хирургического лечения. Хирургия. Журнал им. Н.И. Пирогова. 2019; 9: 25-31.
- Чекмарева И.А., Паклина О.В., Гордиенко Е.Н., Калдаров А.Р. Ультраструктурная сравнительная характеристика нейроэндокринных неоплазий поджелудочной железы. Гены & Клетки. 2019; 01(14): 62-67
- Kriger A.G., Berelavichus S.V., Kaldarov A.R., Panteleev V.I., Gorin D.S., Dugarova R.S., Yukina M.Y. Proinsulin-Secreting Neuroendocrine Tumors of the Pancreas: A Single-Centre Experience. Gastrointest Tumors 2019. doi: 10.1159/000501455
- Берелавичус С.В., Стручков В.Ю., Сон. А.И., Кригер А.Г. Хирургическое лечение нейрофиброматоза 1 типа с опухолевым поражением забрюшинного пространства. Хирургия. Журнал им. Н.И. Пирогова. 2019; 3: 5-14.
- Д.С. Горин, М.А. Захарова, А.В. Смирнов, А.Г. Кригер. Ошибки диагностики внутрипротоковой папиллярно-муцинозной опухоли поджелудочной железы. Хирургия. Журнал им. Н.И. Пирогова. 2019; 2:96-100.
- А.Г. Кригер, Д.С. Горин, В.И. Пантелеев, А.Р. Калдаров. Диагностика и хирургическое лечение опухолей двенадцатиперстной кишки. Хирургия. Журнал им. Н.И. Пирогова. 2019; 1:5-13.
- Kriger AG, Gorin DS, Kaldarov AR, Berelavichus SV, Marinova LA, Galkin GV. Combination of laparoscopy and endoscopy as an option for treatment patients with gastric neuroendocrine tumors. J. Surgical Case Reports, 2019; 1, 1-3.
- Тюнибабян А.И., Блохин И.А., Чернина В.Ю., Калдаров А.Р., Кармазановский Г.Г. Ошибки в диагностике новообразований поджелудочной железы: интрапанкреатическая долька селезенки. Медицинская визуализация. 2018;(3):70-80. Doi: 10.24835/1607-0763-2018-3-70-80
- Юкина М, Нуралиева Н, Трошина Е, Калдаров А, Солдатова Т, Воронцов А. Инсулинпродуцирующая опухоль поджелудочной железы у пациента молодого возраста: поиск герминальной мутации. Клинический случай. Consilium Medicum. 2019; 21 (4): 70–74 Doi: 10.26442/20751753.2019.4.190335
- G. Karmazanovsky, E. Belousova, W. Schima, A. Glotov, D. Kalinin, A. Kriger. Nonhypervascular pancreatic neuroendocrine tumors: Spectrum of MDCT imagings and differentiation from pancreatic ductal adenocarcinoma. Europ. J. Radiology 110 (2019) 66-73.
- S. Berelavichus, A. Kriger, R. Dugarova, A. Kaldarov. Treatment of insulinomas with minimally invasive physical procedure. Literature review. SN Comprehensive Medicine.2019; 1:104-112.
- A.G. Kriger, D.S. Gorin, S.V. Berelavichus, R.S. Dugarova, O.V. Paklina, V. Panteleev. Multiple functional neuroendocrine tumors of pancreas and duodenum managed by robotic totally duodenumpancreatectomy. SN Compr.Clin.Med. (2020) DOI: 10.1007/s42399-020-00272-6
- Чернина В.Ю., Блохин И.А., Марапов Д.И., Кригер А.Г., Калинин Д.В., Шима В., Кармазановский Г.Г. Новый и простой онлайн-инструмент для дифференциации нейроэндокринных и солидных псевдопапиллярных опухолей поджелудочной железы. Мед.визуализация. 2020; 24 (1): 13-28
- Гальчина Ю.А., Кармазановский Г.Г., Калинин Д.В., Кондратьев Е.В., Горин Д.С., Галкин Г.В., Кригер А.Г. Панкреатический свищ при проксимальной резекции поджелудочной железы: корреляция компьютерно-томографических и морфологических предикторов. Мед.визуализация. 2020; 24 (1):29-38.
- Кригер А.Г. Оптимизация лечения гнойных осложнений в абдоминальной хирургии. В кн. «Оптимизация диагностики и лечения гнойно-воспалительных заболеваний. Инновационные технологии: практическое руководство» / под ред. А.Ш. Ревишвили, В.М. Земскова, А.М. Земскова. – Санкт-Петербург: Спецлит 2020. – 319 с. Стр. 36 – 51.
- Кригер А.Г., Кармазановский Г.Г., Пантелеев В.И., Горин Д.С., Ветшева Н.Н., Берелавичус С.В., Калдаров А.Р., Глотов А.В. Диагностика и лечение внутрипротоковой папиллярной муцинозной опухоли поджелудочной железы. Хирургия. Журнал им. Н.И. Пирогова. 2020;01:14-24. https://doi.org/10.17116/hirurgia202001114.
- Д.С. Горин, А.Г. Кригер, Г.В. Галкин, Д.В. Калинин, А.В. Глотов, А.Р. Калдаров, Ю.С. Гальчина, С.В. Берелавичус. Прогнозирование возникновения панкреатического свища после панкреатодуоденальной резекции. Хирургия. Журнал им. Н.И. Пирогова. 2020;(7):61-67. https://doi.org/10.17116/hirurgia202007161
- Berelavichus S., Kriger A., Kaldarov A., Panteleev V., Raevskaya M. Robotic surgery in treatment of retroperitoneal tumors. Comparative single center study [published online ahead of print, 2020 Jun 29]. J Robot Surg. 2020;10.1007/s11701-020-01114-2. doi:10.1007/s11701-020-01114-2
- A. Kriger, S. Berelavichus, A. Kaldarov, D. Gorin, V. Zekster. Robot-Assisted Pancreatic Surgery — the Russian Experience. Indian J Surg(2020). DOI: 10.1007/s12262-020-02298-5
Показать все
Железо сыворотки (Fe serum, Iron serum)
Исследуемый материал Сыворотка крови
Метод определения Колориметрический тест с феррозином.
Жизненно важный микроэлемент, участвующий в процессе связывания, переноса и передачи кислорода в ткани и в процессах тканевого дыхания.
Железо входит в состав дыхательных пигментов (преимущественно – гемоглобина, и частично – миоглобина), цитохромов, железосодержащих ферментов (каталазы, миелопероксидазы). Это, так называемое гемовое железо, которое обратимо связывает кислород и участвует в транспорте кислорода, ряде окислительно-восстановительных реакций, играет важную роль в процессах кроветворения. Железо принимает участие в метаболизме порфирина, синтезе коллагена, работе иммунной системы.
В организм железо поступает с пищей. В пищевых продуктах железо присутствует или в виде составной части гема (мясо, рыба) или как негемовое железо (овощи, фрукты). Из пищи усваивается около 10 – 15% железа, всасывание происходит в 12-типерстной кишке. Общее содержание железа в организме – 4 – 5 г. Около 70% железа входит в состав гемоглобина, 5% – миоглобина, 20% находится в депо (печени, селезёнке, костном мозге) в виде растворимого ферритина и нерастворимого гемосидерина.
Всасывание железа регулируется клетками кишечника: оно возрастает при дефиците железа и неэффективном эритропоэзе и блокируется при избытке железа в организме. Транспорт железа от кишечной стенки до предшественников эритроцитов и клеток-депо (макрофагов) осуществляется плазменным белком – трансферрином. В организме железо не встречается в виде свободных катионов, только в связи с белками.
Концентрация железа в сыворотке зависит от резорбции в желудочно-кишечном тракте, накоплений в кишечнике, селезёнке и костном мозге, от синтеза и распада гемоглобина и его потери организмом. Уровень железа в сыворотке изменяется в течение суток (наиболее высок он утром), зависит от пола и возраста. У новорожденных в течение нескольких часов после родов отмечается падение уровня железа. Средние показатели железа у женщин ниже, чем у мужчин, но и у тех и у других с возрастом показатель железа падает. Концентрация железа у женщин также связана с менструальным циклом (максимальное содержание – в лютеиновую фазу, самое низкое – после менструации). Недостаток сна и стрессы, выраженная физическая нагрузка также вызывают снижение этого показателя.
При беременности содержание железа в организме уменьшается, особенно во второй половине беременности (повышение потребности в железе в этот период связано с формированием депо железа у плода). Несмотря на нестабильность уровня Fe в сыворотке, исследование этого параметра важно для скрининга, дифференциальной диагностики железодефицитных и других анемий, а также оценки эффективности лечения больных железодефицитными анемиями. Выраженный дефицит железа сопровождается снижением уровня гемоглобина и цветного показателя. Выраженное снижение концентрации железа в сыворотке крови может быть отмечено при дефиците железа в организме, но для диагностики латентной анемии недостаточно определения содержания железа в сыворотке крови. Для более точной оценки баланса железа в организме необходимо провести дополнительные исследования (ферритин, трансферрин, ЛЖСС).
Метод исследования: расчетный (ОЖСС рассчитывается как сумма железа сыворотки и латентной железосвязывающей способности).
Единицы измерения и коэффициенты пересчета:мкмоль/ л или мкг/100 мл
Единицы измерения в ИНВИТРО: мкмоль/л
Альтернативные единицы: мг/100 мл
Пересчет единиц: мкг/100 мл * 0,179 => мкмоль/ л
Референсные значения: 44,8 – 76,3 мкмоль/л
Интерпретация результата:
Повышение:
- Гипохромные анемии.
- Острый гепатит.
- Поздние сроки беременности.
- Прием эстрогенов, пероральных контрацептивов.
Понижение:
- Анемия (не железодефицитная).
- Хронические инфекции.
- Гемохроматоз.
- Цирроз.
- Неопластические заболевания.
- Заболевания почек.
- Талассемия.
- Применение прапаратов: аспарагиназа, хлорамфеникол, кортикотропин, кортизол, тестостерон.
Литература: Энциклопедия клинических лабораторных тестов / Под ред. Н.У. Тица. − М.: «ЮНИМЕД – пресс», 2003, (с. 960)
Анемия у детей | Детская городская больница
Что такое анемия
Анемия – это снижение общей концентрации красных кровяных телец и гемоглобина в крови. Задача эритроцитов – доставлять кислород к тканям организма. Поэтому при уменьшении их численности, организм страдает от так называемой гипоксии – нехватки кислорода. Особенно чувствительны к снижению гемоглобина дети.
По статистике, анемия наблюдается у 15% детей. Анемии бывают самыми разными – одни связаны с нехваткой витаминов группы В, другие – с недостаточностью фолиевой кислоты. Но преимущественное большинство анемий развивается вследствие дефицита железа. Эти анемии называются железодефицитными, и именно они наиболее распространены (около 90% всех анемий). О железодефицитных анемиях сегодня и поговорим.
Причины и симптомы анемии
Причины железодефицитных анемии делятся на три группы.
Первая – это ситуации, связанные с потерей крови. Сюда относятся и кровотечения из желудочно-кишечного тракта, менструальные кровотечения, любые другие кровопотери.
Ко второй группе отнесем недополучение железа. И хотя такое возможно только при голодании, такое случается у детей. Например, когда родители-вегетарианцы намеренно лишают ребенка мясной пищи – основного источника гемного железа.
Следующая группа причин – нарушение всасывания железа. При некоторых заболеваниях желудка или кишечника, после полостных операций на ЖКТ. Дело в том, что железо всасывается в основном в 12-перстной кишке и в верхних отделах тонкой кишки. Поэтому любые проблемы с этими отделами ЖКТ способны спровоцировать анемию.
Анемия может также возникнуть и при недостаточной выработке эритроцитов, нарушении их функционирования и преждевременном разрушении красных кровяных телец.
Ваш ребенок бледен, быстро устает, жалуется на мышечную слабость, головокружения. Это первые признаки анемии. Такие ситуации характерны и для школьников, и для деток-дошколят. Внимательные родители сазу отправятся на прием к доктору. Если же анемию запустить, то вскоре ваше чадо станет малоподвижным, в уголках рта появятся трещины, язык станет гладким и глянцевым, перед глазами будут мелькать «мушки». Появятся извращения в пищевых желаниях, особенно – желание лизать гвозди и другие металлические предметы.
Ваше задание, как родителей, а также вашего лечащего врача – выявить ее вид, причины и устранить дефицит железа.
Диагностика и лечение анемии
Для того чтобы подтвердить диагноз «анемия», нужно сдать элементарный общий анализ крови (из пальца). По его результатам будет видно насколько критично состояние ребенка. Если гемоглобин (HGB) в пределах от 90 до 110 – это легкая анемия; 90-70 – анемия средней тяжести; показатель ниже 70 – тревожный сигнал тяжелой анемии. Обратить внимание нужно и на количество эритроцитов в крови (RBC). Их норма для детей 4,0-7х1012 (в зависимости от возраста).
Очень важным индикатором анемии служит цветовой показатель крови. В норме он должен быть равен единице. Если его значение выше 1,05 – становится ясным, что анемия вызвана дефицитом витаминов группы В либо фолиевой кислоты. Если же ЦП меньше 0,85, подозревается железодефицитная анемия. Существуют и другие критерии, исходя из которых, ставится диагноз ЖДА, но их анализ предоставим знающему доктору.
После постановки диагноза доктор должен установить причину анемии, и вы должны ему в этом помочь. Обязательно сообщите лечащему врачу, если вдруг ваш ребенок не ест мясо или рыбу, если у него есть заболевания ЖКТ (язвенные и предязвенные состояния кишечника). Очень важно выяснить и ликвидировать именно первопричину анемии, иначе никакое лечение не даст результатов, и уже через несколько месяцев анемия появится вновь. Лечение анемии должно быть комплексным. Диетой возможно устранить лишь небольшой недостаток железа, более серьезные ситуации требуют комплексного лечения, сочетающего в себе как специальную диету, так и лекарственные препараты. Но об этом позже.
Лечение должен назначать ТОЛЬКО врач. И лучше, если это будет квалифицированный гематолог. Избыток железа также опасен для детского организма, как и его недостаток. Поэтому, занимаясь самолечением, вы рискуете увидеть симптомы передозировки – судороги, рвоту и понос.
Современные препараты железа производятся в удобных для приема формах – в виде сиропов, капель и даже жевательных таблеток. При легкой анемии достаточно перорального приема лекарств. Причем, запивать их лучше соком, а принимать обязательно вне еды! Если анемия носит характер тяжелой,показано лечение в стационаре, парентеральное введение препаратов, а иногда даже переливание крови. Поэтому не рискуйте здоровьем детей и при малейших подозрениях обращайтесь за врачебной помощью.
Питание при анемии. Профилактика анемии
Для формирования правильных принципов питания ребенка важно понимать механизм всасывания железа из различных источников. Дело в том, то в красном мясе, печени и яйцах железо содержится в быстро усваиваемом виде – так называемое гемовое (гемное) железо. Растительная пища (бобовые, гречневая крупа, гранаты) – это кладезь негемового (негемного) железа, которое всасывается хуже. Поэтому в меню ребенка обязательно должно присутствовать мясо (говядина, кролик – 30 грамм в сутки), морская рыба, яйца (1-2 штуки), ягоды и соки, богатые аскорбиновой кислотой. Именно аскорбинка и животный белок улучшают всасываемость железа (при одновременном применении в 3 раза!). В то время как цельное молоко и молочные продукты должны употребляться в пищу раздельно от мяса, рыбы и яиц.
Ранее бытовало мнение, что много железа содержится в яблоках. Это не верно, так как в яблоках железа ровно столько, сколько и в гречневой крупе. Просто в яблоках содержится аскорбиновая кислота, которая улучшает всасываемость железа. Поэтому не нужно насильно кормить ребенка яблоками, а если он не любит ягоды и соки, лучше дать старую добрую витаминку-аскорбинку. Кстати, мало кто знает, что рекордсменом по содержанию железа являются сушенные белые грибы (35 мг на 100 г), морская капуста (16 мг на 100 г), какао-порошок (15 мг в 100 г), печень (9 мг на 100 г).
Не болейте!
Кишечная железа – обзор
Гистологические и гистохимические характеристики
Ободочная и слепая кишка человека и лабораторных животных выстлана довольно однородной слизистой оболочкой, лишенной ворсинок. Столбчатые клетки двух основных типов покрывают поверхностный эпителий. Это абсорбирующие и слизистые клетки, подобные тем, которые обнаруживаются в тонком кишечнике. Кишечные железы или крипты простираются вниз от поверхности, как правило, в виде простых неразветвленных канальцев, выстланных преимущественно слизистыми клетками с меньшими популяциями абсорбирующих, эндокринных и недифференцированных клеток.
Слизистая оболочка человека и лабораторных животных имеет слегка волнистый или неровный рисунок, который меняется в зависимости от конкретного участка толстой кишки. На гистологических срезах толстой кишки у людей этот гофрированный узор выглядит как гимноподобные структуры крипт, напоминающие греческую архитектурную особенность. 500 Это также наблюдается у более крупных лабораторных животных. У крыс и мышей крипты слизистой оболочки слепой кишки шире около просвета, чем в основании крипты, и крипты могут быть разветвленными, что может быть связано с абсорбционной функцией этой зоны. 597
Зона пролиферации толстой кишки обычно располагается в нижней части железы. Как и в тонкой кишке, мультипотентные недифференцированные стволовые клетки, расположенные в основании железы, дают начало основным типам клеток, которые мигрируют на поверхность клетки с последующей дифференцировкой и изменением их ферментативной активности и морфологических характеристик. 603 В исследованиях с химерами агрегации мышей было продемонстрировано, что весь эпителий каждой взрослой железы произошел от одной клетки-предшественника. 604 Один предшественник сам может дать начало нескольким стволовым клеткам, которые ответственны за обновление клеток в полной крипте.
Абсорбирующие клетки чаще всего обнаруживаются в поверхностном эпителии, но также в меньшей степени в железистом эпителии. Они морфологически сходны с таковыми в тонком кишечнике, каждая из которых обладает апикальными плазматическими мембранами с однородными микроворсинками и хорошо сформированным гликокаликсом.
Существуют видовые и региональные различия в гликоконъюгатах, обнаруженных в щеточной кайме толстой кишки, хотя обычно они содержат преимущественно кислые слизистые вещества.У мышей и крыс обнаружены сиаломуцины с некоторыми нейтральными муцинами. У хомяков, собак, приматов, не относящихся к человеку, и человека в кайме могут быть обнаружены как сульфомуцины, так и сиаломуцины. 256 Некоторые соединения могут вызывать качественные и количественные изменения содержания муцина в слизистой оболочке толстой кишки без заметных морфологических изменений. Пример этого явления был описан у крыс, получавших резерпин в течение семи дней. Слизистая оболочка толстой кишки показала увеличение сульфомуцина (положительный диамин с высоким содержанием железа), содержащих бокаловидные клетки в поверхностном эпителии. 586 Гликокаликс играет важную роль в защитной функции слизистой оболочки толстой кишки, поскольку было показано, что ее нарушение такими агентами, как салицилаты, увеличивает абсорбцию ксенобиотиков слизистой оболочкой прямой кишки крыс. 605
Ободочная кишка, как и многие другие ткани, также обладает активностью метаболизма лекарств, хотя и намного меньшей, чем в печени, в то время как у людей наблюдается значительная индивидуальная изменчивость. 606–608
Собственная пластинка толстой кишки устроена аналогично тонкой кишке.Благодаря наличию лимфоцитов, плазматических клеток, макрофагов и дендритных клеток, а также разбросанных мелких лимфоидных агрегатов или участков, он является неотъемлемой и важной частью системы иммунной защиты слизистой оболочки. Было показано, что большинство лимфоцитов в собственной пластинке слизистой оболочки толстой кишки человека, как и в подвздошной кишке, являются Т-лимфоцитами, а количество Т-хелперов превышает фенотип Т-супрессоров. 476,478 Это контрастирует с интраэпителиальными лимфоцитами слизистой оболочки толстой кишки человека, которые также являются Т-клетками, но более 80% из них обладают характеристиками супрессорного / цитотоксического фенотипа и только 10–20% являются Т-хелперами.Распределение субпопуляций лимфоцитов в толстой кишке крысы также показывает присутствие Т-лимфоцитов в собственной пластинке, и большинство из них относятся к хелперному фенотипу CD4. 489 Некоторые Т-лимфоциты в собственной пластинке имеют супрессор / цитотоксический (CD8) тип, в отличие от большей доли в эпителии толстой кишки. Зрелые маленькие В-лимфоциты относительно редко встречаются в собственной пластинке толстой кишки людей и лабораторных животных, хотя собственная пластинка содержит большое количество плазматических клеток, в основном подтипа IgA.
Особенностью слизистой оболочки толстой кишки является наличие лимфоидных агрегатов, также называемых лимфоидными узелками, пятнами, лимфоидно-железистыми комплексами или микробурсами. 483 Они похожи на бляшки Пейера тонкой кишки, поскольку состоят в основном из лимфоидных клеток серии В-клеток, расположенных в фолликулах с зародышевыми центрами с межфолликулярными и перифолликулярными зонами, состоящими из Т-клеток. 476 Они распределены по всей длине слизистой оболочки толстой кишки, хотя обычно меньше, чем пятна Пейера.У крыс Sprague-Dawley лимфоидные агрегаты обычно имеют диаметр около 5 мм, за исключением дистального отдела толстой кишки, где они достигают размеров до 10 мм в диаметре. 486
В отличие от пятен Пейера, которые обычно не связаны с криптами или ворсинками, лимфоидные агрегаты толстой кишки часто содержат нерегулярные атипичные слизистые железы, которые могут проникать глубоко в лимфоидную ткань и проникать под мышечную слизистую оболочку как у людей, так и у лабораторных животных. 609,610 Эти железистые структуры, которые тесно связаны с лимфоидной тканью, могут играть важную роль в иммунной защите слизистой оболочки толстой кишки, возможно, действуя как особый локальный рецептор для антигенов.Карциномы толстой кишки, вызванные диметилгидразином у крыс, также, по-видимому, чаще развиваются в лимфоидных агрегатах, чем в других зонах. 486
Пищеварительные ферменты, секретируемые кишечными железами | Здоровое питание
Стефани Чендлер Обновлено 17 декабря 2018 г.
Большинство людей едят, даже не задумываясь о том, что на самом деле происходит с едой, когда они ее проглатывают. Еда – это больше, чем просто приятное социальное занятие, это необходимо для жизни.Пища, которую вы потребляете, обеспечивает ваше тело энергией и питательными веществами, которые необходимы ему для функционирования. Процесс пищеварения расщепляет пищу с помощью специализированных белков, называемых ферментами. Тонкий кишечник содержит кишечные железы, называемые криптами Либеркуна, которые секретируют пищеварительные ферменты.
Пептидаза
Пища, которую вы едите, состоит из трех основных типов макроэлементов, обеспечивающих организм калориями для получения энергии: углеводов, жиров и белков. Белки представляют собой сложные цепи аминокислот.Ферменты, выделяемые во рту и желудке, расщепляют белки на более короткие аминокислотные цепи, но они все еще слишком велики для поглощения клетками, выстилающими тонкий кишечник. Кишечные железы выделяют ферменты пептидазы, которые разбивают эти цепи на отдельные аминокислоты, которые кишечник может усвоить.
Мальтаза
Углеводы служат основным источником энергии для вашего тела. Хотя существует много различных форм углеводов, все они содержат цепочки молекул сахара.Ферменты во рту начинают расщеплять углеводы на более мелкие молекулы, называемые дисахаридами, которые состоят из двух связанных вместе молекул сахара. Но ваше тело может поглощать только отдельные молекулы сахара, поэтому кишечные железы выделяют мальтазу, фермент, который расщепляет дисахарид мальтозу на две отдельные молекулы глюкозы.
Сахараза
При распаде углеводов образуется еще одна молекула дисахарида, называемая сахарозой. Сахароза, также известная как столовый сахар, состоит из двух простых сахаров, глюкозы и фруктозы, связанных вместе.Кишечные железы выделяют фермент сахарозу, который разрывает связь и высвобождает простые сахара, которые может усвоить ваш организм.
Лактаза
Молоко и молочные продукты содержат углеводную лактозу, дисахарид, состоящий из простых сахаров, глюкозы и галактозы. Кишечные железы выделяют фермент лактазу, который расщепляет лактозу на две отдельные молекулы сахара. Без лактазы ваше тело не может расщепить лактозу, поэтому она остается с отходами и попадает в толстый кишечник, где бактерии пытаются ее расщепить.Это вызывает состояние, называемое непереносимостью лактозы, симптомы которого включают боль в животе, вздутие живота, газы, диарею и рвоту. По данным Центра здоровья Университета Джорджии, 80 процентов азиатских и коренных американцев, 75 процентов афроамериканцев, 51 процент испаноязычных американцев и 21 процент кавказских американцев страдают от непереносимости лактозы.
Документ без названия
Документ без названияЗакрыть
Слайд №DMS 131 (Обезьяна; двенадцатиперстная кишка). Вы смотрите на тонкий срез пластика, окрашенный методом H&E.В качество сохранности и окрашивания этой ткани делает ее отличной для изучения цитологическая деталь.
Начиная со слизистой оболочки, обратите внимание на большие ворсинки, которые содержат нити гладких мышц, большие центральные лимфатические сосуды (млечные сосуды) и кровеносные капилляры. Обратите внимание, что эпителиальные клетки бывают двух типов; большинство из них являются абсорбирующими клетками и меньше – бокаловидными клетками. Определите кишечные железы ( крипта Либеркюн ). Обратите внимание, что они ограничены собственной пластинкой.Какие клетки образуют выстилающий эпителий желез? Определите многочисленные митотические фигуры в эпителиальных клетках в основании крипт.
Обратите внимание, что собственная пластинка более многочисленна, чем в желудке, и содержит диффузные скопления лимфоцитов и плазматических клеток. Местами можно увидеть лимфоциты, проходящие через эпителий в просвет кишечника. В других местах есть лимфоидные узелки, некоторые из них содержат зародышевые центры. Некоторые из этих узелков проходят через слизистую мышечной ткани в подслизистую оболочку.Определите двенадцатиперстную кишку ( Brunner’s ) в подслизистой оболочке. Они открываются в базальные части кишечных желез в собственной пластинке после проникновения в мышечную слизистую оболочку. Эти железы являются важным отличительным признаком двенадцатиперстной кишки. Обратите внимание, что подслизистая основа содержит относительно мало лимфоцитов. Между двумя слоями muscularis externa идентифицируют миэнтерическое сплетение. Он состоит из нервных волокон, тел нервных клеток и ядер шванновских клеток. С одной стороны двенадцатиперстной кишки к наружной мышце прилегает большое количество синеватой ткани.Это поджелудочная железа? Также обратите внимание на фиброзно-жировую ткань, окружающую двенадцатиперстную кишку, которая по большей части имеет адвентицию, а не серозную оболочку.
Используйте большую мощность, чтобы детально изучить особенности ворсинок. Если вы никогда не видели микроворсинчатых краев щеток, клеммных колодок и паутины, теперь твой шанс. Также посмотрите на содержимое сердцевины собственной пластинки. ворсинки и кишечные железы. Обратите внимание на множество плазматических клеток, лимфоцитов, иногда тучные клетки и др.Все появляются на удивление хорошо.
Это срез двенадцатиперстной кишки в очень малом увеличении. Признавая, что это участок желудочно-кишечного тракта, со слизистой оболочкой, подслизистой оболочкой, собственной мышечной оболочкой и адвентицией / серозной оболочкой, можно даже при таком малом увеличении определить его как двенадцатиперстную кишку из-за наличия подслизистых желез Бруннера вместе с ворсинчатой архитектурой. слизистой оболочки. Также обратите внимание на выступы подслизистой оболочки и слизистой оболочки, создающие макроскопические складки или складки на слизистой оболочке кишечника, один из механизмов увеличения площади поверхности кишечника.
На этом изображении двенадцатиперстной кишки с малым увеличением определите слизистую оболочку, включая ее самый внешний компонент, мышечную слизистую оболочку. Подслизистая основа с резидентными железами Бруннера, а также два слоя гладких мышц (внутренний круговой и внешний продольный) собственной мышечной ткани также хорошо различимы. Обратите внимание на характерную особенность всего тонкого кишечника – пальцеобразные выступы слизистой оболочки, называемые ворсинками (в единственном числе: ворсинки). Эпителий, покрывающий ворсинки, является продолжением эпителия кишечных желез (крипта Либеркуна), в который эпителий погружается, образуя таким образом ось крипта-ворсинка.
Это изображение слизистой оболочки двенадцатиперстной кишки в среднем увеличении. Поскольку подслизистые железы Бруннера не видны на этом изображении, более сложно распознать это как двенадцатиперстную кишку, а не какую-либо другую часть тонкой кишки. Однако относительное количество бокаловидных клеток в эпителии указывает на то, что они взяты из проксимальной части тонкой кишки. Обратите внимание на структуру ворсинки, которая покрыта эпителием и поддерживается в своей сердцевине очень клеточной собственной пластинкой.Также обратите внимание, что хотя эпителий действительно сплошной от основания кишечных желез (крипт) до верхушки ворсинок (ось крипта-ворсинка), в большинстве случаев обычно видны только профили желез в поперечном сечении.
Изображение ворсинки кишечника с большим увеличением показывает простой столбчатый эпителий, состоящий из абсорбирующих клеток с щеточной каймой, а также случайных бокаловидных клеток, хотя на этом конкретном изображении их не видно. Собственная пластинка, заполняющая сердцевину ворсинок, содержит различные типы клеток (например,грамм. лимфоциты, плазматические клетки, клетки гладкой мускулатуры), а также содержит мелкие кровеносные сосуды и лимфатический канал или млечный канал, размер которых зависит от абсорбционной активности в кишечнике. Иногда можно также увидеть внутриэпителиальные лимфоциты, сдавленные между столбчатыми эпителиальными клетками.
С помощью масляной иммерсии можно просто разрешить тонкую структуру щеточной каймы, обнаруженной на апикальной области абсорбирующих клеток кишечника. При внимательном рассмотрении можно различить многочисленные микроворсинки, вся популяция которых вместе с нижележащим конечным веб-доменом составляет щеточную кайму.Здесь также можно увидеть часть одной бокальной клетки.
Возвращаясь к более низкому изображению кишечных ворсинок и кишечных желез (крипт), обязательно обратите внимание на то, что кишечный эпителий подвергается постоянному обновлению, при этом стволовые клетки пролиферируют в криптах, мигрируют вверх по оси крипта-ворсинка, а затем отслаивание кончика ворсинки. Из-за быстрого оборота клеток в кишечных железах обычно обнаруживаются многочисленные митотические фигуры. Лучше всего это видно на следующем изображении.
Обратите внимание на митотические фигуры, обнаруженные в кишечных железах (криптах). Стволовые клетки представляют собой самообновляющуюся популяцию, которая также может дифференцироваться в основные типы клеток кишечного эпителия: абсорбирующие, бокаловидные, клетки Панета, энтероэндокринные и М-клетки.
Глядя на внешние стенки двенадцатиперстной кишки, обратите внимание на подслизистую основу и находящиеся в ней железы Бруннера. Muscularis propria (externa) состоит из внутреннего кругового слоя и внешнего продольно ориентированного слоя гладкой мускулатуры.Расположенные между двумя слоями мышц, можно найти разбросанные ганглии миэнтериального сплетения (сплетения Ауэрбаха) (лучше видно на следующем изображении). Периферически к собственной мышце находится соединительная ткань адвентиции, типичная для этого забрюшинного сегмента двенадцатиперстной кишки.
При большом увеличении можно увидеть несколько нейронов, образующих ганглий миэнтериального сплетения (сплетения Ауэрбаха), находящегося между двумя слоями гладкой мускулатуры собственной мышцы. Аналогичное сплетение находится в подслизистой оболочке (сплетение Мейснера).
Закрыть
Кишечная эндокринная система
Кишечная эндокринная система
Вторая из двух систем, контролирующих пищеварительную функцию, – это эндокринная система, которая регулирует функцию путем секреции гормонов. Напомним, что гормоны – это секретируемые в кровь химические вещества, которые изменяют физиологию клеток-мишеней. Клетка-мишень для определенного гормона – это клетка, которая имеет рецепторы для этого гормона и, таким образом, может реагировать на него.
На пищеварительную функцию влияют гормоны, вырабатываемые многими эндокринными железами, но наиболее глубокий контроль осуществляется гормонами, вырабатываемыми в желудочно-кишечном тракте.Желудочно-кишечный тракт – это самый большой эндокринный орган в организме, и эндокринные клетки в нем в совокупности называются кишечной эндокринной системой . Три наиболее изученных кишечных гормона:
- Гастрин: Выделяется из желудка и играет важную роль в контроле секреции кислоты желудочного сока.
- Холецистокинин: Гормон тонкого кишечника, стимулирующий секрецию ферментов поджелудочной железы и желчи.
- Секретин: Другой гормон, секретируемый эпителиальными клетками тонкого кишечника; стимулирует секрецию жидкости, богатой бикарбонатом, из поджелудочной железы и печени.
В отличие от эндокринных желез, таких как передняя доля гипофиза, в которых практически все клетки вырабатывают гормоны, кишечная эндокринная система является диффузной: отдельные гормон-секретирующие клетки разбросаны среди других типов эпителиальных клеток в слизистой оболочке желудка и тонкой кишки. .
Например, большинство эпителиальных клеток желудка выделяют слизь, соляную кислоту или профермент, называемый пепсиногеном, в просвет желудка. Среди этих секреторных эпителиальных клеток разбросаны G-клетки, которые являются эндокринными клетками, которые синтезируют и секретируют гормон гастрин.Гастрин, как гормон, выделяется в кровь, а не в просвет желудка. Точно так же другие гормоны, вырабатываемые эндокринной системой кишечника, синтезируются и секретируются клетками эпителия тонкой кишки.
Как и все эндокринные клетки, клетки эндокринной системы кишечника не просто непрерывно секретируют свой гормон, что было бы не очень полезно в качестве системы контроля. Скорее, они секретируют гормоны в ответ на довольно специфические стимулы и прекращают секретировать свой гормон, когда эти стимулы больше не присутствуют.Что стимулирует эндокриноциты в эндокринной системе кишечника? Как вы могли догадаться, в большинстве случаев эти эндокринные клетки реагируют на изменения в окружающей среде в просвете пищеварительной трубки. Поскольку эти клетки являются частью эпителия, их апикальная граница контактирует с содержимым просвета, что позволяет им постоянно «пробовать» или пробовать среду просвета и реагировать соответствующим образом.
Чтобы проиллюстрировать, как осуществляется контроль через эндокринную систему кишечника, рассмотрим важный пример предотвращения сгорания эпителия тонкой кишки желудочной кислотой:
- Загрязненная кислотой пища выходит из желудка в тонкий кишечник.
- Кислота в тонком кишечнике стимулирует секрецию гормона секретина эндокринными клетками кишечного эпителия.
- Secretin стимулирует поджелудочную железу сбрасывать богатую бикарбонатом жидкость в просвет кишечника.
- Бикарбонат нейтрализует кислоту, что устраняет стимул для секреции дополнительной секреции.
- При отсутствии секретинового стимула поджелудочная железа перестает секретировать бикарбонат.
Отправить комментарий Ричарду[email protected]
Аденокарцинома – виды и варианты лечения
Аденокарцинома может возникать практически в любом месте тела, начиная с желез, выстилающих внутреннюю часть органов. Аденокарцинома образуется в железистых эпителиальных клетках, которые выделяют слизь, пищеварительные соки или другие жидкости. Это подтип карциномы, наиболее распространенной формы рака, обычно образующей солидные опухоли.
Ваши железы помогают вашему телу нормально функционировать и поддерживают влажность внутренних органов. Если железистые клетки начинают бесконтрольно расти из-за мутаций, происходящих в процессе репликации ДНК в организме, они могут образовывать опухоли.Некоторые опухоли железистых клеток не являются злокачественными. Их называют аденомами. Злокачественные опухоли представляют собой аденокарциномы, которые захватывают здоровую ткань внутри органа и могут распространяться на другие части тела.
По данным Национального института рака, аденокарциномы обычно сначала представляют собой утолщенную, похожую на бляшку белую слизистую оболочку. Они часто легко распространяются через мягкие ткани в том месте, где они возникают.
Рак аденокарциномы
Многие органы имеют железистые клетки.Аденокарциному часто идентифицируют по ее конкретному типу, например, экзокринный рак поджелудочной железы, инвазивный протоковый рак молочной железы или рак эндометрия в матке. Аденокарцинома чаще всего встречается при следующих заболеваниях:
Аденокарцинома может появиться в головном мозге, как правило, из-за рака, метастазирующего из других частей тела. Аденокарцинома также может развиваться в других частях тела.
При таком большом количестве различных типов рака под заголовком аденокарциномы – и возможных метастазах – существует множество различных факторов риска и симптомов, в зависимости от конкретного заболевания.Курение является одним из факторов риска, который, по-видимому, применим ко всем аденокарциномам.
Факторы риска аденокарциномы
Факторы риска аденокарциномы зависят от типа рака. Важно помнить, что факторы риска не гарантируют диагноз рака; скорее, они увеличивают шансы на его развитие. Вы можете изменить некоторые факторы риска, например, факторы образа жизни.
Рак легкого: Аденокарцинома легкого – это тип немелкоклеточного рака легкого (НМРЛ) и основная причина смерти от рака в Соединенных Штатах.Как и в случае других видов рака легких, курение является самым большим фактором риска.
Другие факторы риска включают:
- Воздействие пассивного курения
- Загрязнение воздуха или химические раздражители, такие как асбест, радон, кремнезем, тяжелые металлы и пары дизельного топлива
- Семейный анамнез аденокарциномы легких
Некоторые исследования показали, что прием добавок бета-каротина и воздействие мышьяка с питьевой водой может увеличить риск рака легких.Использование талька или талька и курение марихуаны или электронных сигарет считаются недоказанными факторами риска.
Рак простаты: По данным Американского онкологического общества (ACS), риск рака простаты увеличивается после 50 лет, при этом большинство случаев обнаруживается у мужчин старше 65 лет. Мужчины африканского происхождения подвергаются повышенному риску.
Семейная история болезни или наследственные генетические мутации, такие как гены BRCA1 или BRCA2, являются ассоциированными факторами риска, как и наследственный неполипозный колоректальный рак (HNPCC), также известный как синдром Линча.
Рак поджелудочной железы: Риск рака поджелудочной железы повышается с возрастом, большинство случаев выявляется у пациентов старше 65 лет. Мужчины заболевают раком поджелудочной железы чаще, чем женщины, и расовая принадлежность также играет определенную роль, причем афроамериканцы подвергаются несколько более высокому риску. .
Другие факторы риска включают:
- Семейный анамнез болезни
- Унаследованные генные мутации, вызывающие хронический панкреатит
- Наследственные генетические синдромы
Рак пищевода. Мужчины чаще, чем женщины, заболевают раком пищевода.Как и в случае с некоторыми другими видами рака, риск увеличивается с возрастом. По данным ACS, большинство случаев выявляется у пациентов старше 55 лет.
Другие факторы риска включают:
- Диета с высоким содержанием обработанного мяса
- Частое употребление очень горячих жидкостей
- Употребление табака (жевательный табак, сигареты и сигары)
- Употребление алкоголя
- Ожирение
- Семейная история
- Рак легких, рта или горла в анамнезе
- Инфекция, вызванная вирусом папилломы человека (ВПЧ)
- Травма пищевода
- Гастроэзофагеальная рефлюксная болезнь (ГЭРБ)
- Пищевод Барретта, состояние, при котором хронический кислотный рефлюкс повреждает слизистую оболочку пищевода.
- Ахалазия, состояние, при котором нижний сфинктер пищевода не функционирует должным образом, вызывая раздражение слизистой оболочки пищевода.
- Тилоз, генетическое заболевание, которое может вызывать небольшие новообразования на пищеводе
- Синдром Пламмера-Винсона, синдром, вызывающий образование паутины в верхнем отделе пищевода, что может вызвать закупорку, сужение или хроническое раздражение
Колоректальный рак: Наибольшими факторами риска колоректального рака являются возраст, пол и семейный анамнез.Мужчины чаще, чем женщины, заболевают этим заболеванием.
Другие факторы риска включают:
- Диета с низким содержанием клетчатки и высоким содержанием жира и обработанное мясо
- Отсутствие физической активности
- Ожирение
- Употребление алкоголя
- Употребление табака
- Воспалительное заболевание кишечника (болезнь Крона или язвенный колит)
- Колоректальный полип
Рак груди: Семейная история болезни, а также наследственные генетические мутации (такие как BRCA1 и BRCA2) повышают риск рака груди.По данным Центров США по контролю и профилактике заболеваний, на семейную наследственность приходится от 5 до 10 процентов случаев рака груди.
Другие факторы риска включают:
- Возраст (чаще всего диагностируется у женщин в возрасте 55 лет и старше)
- Ранние менструации (особенно до 12 лет)
- Менопауза после 55 лет
- Плотная ткань груди
- История рака груди или яичников
- Предварительная лучевая терапия в области грудной клетки
- Употребление алкоголя
- Ожирение после менопаузы
- Отсутствие физической активности
Женщины, которые принимали заместительную гормональную терапию или противозачаточные средства, никогда не вынашивали доношенной беременности, не имели первого ребенка после 30 лет или не кормили грудью, подвергаются повышенному риску, равно как и женщины, принимавшие препарат диэтилстильбестрол ( DES), или чьи матери принимали препарат.
Рак желудка: У мужчин больше шансов заболеть раком желудка, и этот риск увеличивается с возрастом. Большинство пациентов получают диагноз в возрасте старше 60 лет. По данным Американского онкологического общества, рак желудка чаще встречается у латиноамериканцев, афроамериканцев, коренных американцев и жителей островов Азиатско-Тихоокеанского региона, чем у белых в Соединенных Штатах.
Другие факторы включают:
- Длительная инфекция Helicobacter pylori (H. pylori) (может привести к предраковым изменениям слизистой оболочки желудка)
- Избыточный вес или ожирение
- Диета с высоким содержанием обработанного мяса
- Употребление алкоголя и табака
- Предыдущие операции на желудке
- Полипы желудка, известные как аденомы
- Болезнь Менетрие (при которой избыточный рост слизистой оболочки желудка вызывает низкий уровень кислоты в желудке; точная связь с раком желудка неизвестна)
- Кровь типа А
- Общий вариабельный иммунный дефицит (ОВИН) (при котором иммунная система не может вырабатывать достаточное количество антител)
- Перенесенная вирусная инфекция Эпштейна-Барра
Следующие наследственные состояния также могут повышать риск рака желудка:
- Наследственный диффузный рак желудка (HDGC)
- Наследственный неполипозный колоректальный рак (HNPCC; синдром Линча)
- Семейный аденоматозный полипоз (ФАП)
- Аденома желудка и проксимальный полипоз желудка (GAPPS)
- Синдром Ли-Фраумени (LFS)
- Синдром Пейтца-Егерса (PJS)
Симптомы аденокарциномы
Рак легкого
Ранние симптомы аденокарциномы легкого включают:
- Усталость
- Постоянный кашель
- Кровянистая мокрота
- Одышка
- Охриплость
- Потеря аппетита
- Похудание
- Слабость
- Боль в груди
- Свистящее дыхание
- Хронические или повторяющиеся инфекции (например, бронхит и пневмония)
Рак простаты
Признаки аденокарциномы простаты включают:
- Частое мочеиспускание (особенно ночью)
- Затруднение при полном опорожнении мочевого пузыря
- Слабый отток мочи
- Кровь в моче
- Эректильная дисфункция
- Увеличенная простата, вызывающая боль при сидении
- Болезненность или жжение при мочеиспускании
Рак поджелудочной железы
Симптомы аденокарциномы поджелудочной железы часто не проявляются, пока болезнь не прогрессирует.Когда это происходит, у пациента может возникнуть следующее:
- Желтуха (пожелтение кожи и глаз)
- Темная или коричневая моча
- Светлый или серый жирный стул
- Зуд
- Боль в животе или спине
- Похудание
- Потеря аппетита
- Тошнота Рвота
- Увеличенная печень или желчный пузырь
- Тромбы
- Диабет, но редко
Рак пищевода
Симптомы аденокарциномы пищевода включают:
- Затруднения при проглатывании некоторых видов пищи
- Боль или удушье при глотании
- Давление в груди / жжение
- Изжога или несварение желудка
- Рвота
- Кашель
- Охриплость
- Боль за грудиной или в горле
- Похудание
Колоректальный рак
Симптомы аденокарциномы толстой или прямой кишки включают:
- Изменения привычек кишечника, такие как диарея, суженный стул или запор
- Постоянные позывы к дефекации
- Ректальное кровотечение или кровавый стул
- Боль или спазмы в животе
- Усталость
- Слабость
- Похудание
Рак груди
Симптомы аденокарциномы груди включают:
- Шишка в груди или под мышкой
- Утолщение груди
- Набухание груди
- Раздражение кожи груди
- Ямочка на коже груди
- Красная или шелушащаяся кожа вокруг соска
- Выделения из сосков
- Изменения формы и / или размера груди
- Боль в груди
Рак желудка
Симптомы аденокарциномы желудка включают:
- Снижение аппетита
- Похудание
- Боль или дискомфорт в животе
- Сытость после употребления небольшого количества пищи
- Изжога или несварение желудка
- Тошнота
- Рвота (возможно кровью)
- Вздутие живота или задержка жидкости
- Кровавый стул
- Анемия (может вызывать слабость и усталость)
- Желтуха
Диагностика аденокарциномы
Поскольку аденокарцинома может развиваться в очень многих различных областях тела, типы используемых диагностических тестов также различаются.
Рак груди часто обнаруживается на ранних стадиях во время маммографии. Рак простаты часто обнаруживают с помощью анализа крови на простатоспецифический антиген (ПСА) или пальцевого ректального исследования (DRE). Колоноскопия может использоваться для диагностики рака толстой кишки, а бронхоскопия может использоваться для обнаружения аденокарциномы легкого.
В общем, типы выполняемых тестов могут включать:
Биопсия : Эта процедура используется для удаления образца аномальной ткани из тела.Затем патолог исследует ткань под микроскопом, чтобы определить, присутствует ли рак. Биопсия также может использоваться для определения того, возник ли рак на месте биопсии или он метастатический, то есть развился в другой части тела.
Компьютерная томография : Компьютерная томография – это процедура визуализации, при которой выполняются подробные трехмерные рентгеновские снимки аномальных тканей тела. КТ также может использоваться для определения реакции аденокарциномы на лечение.
MRI : Магнитно-резонансная томография использует радиочастотные волны для создания подробных изображений поперечного сечения различных частей тела.
Анализы крови : Эти лабораторные тесты используются для обнаружения в крови определенных химических веществ, которые могут быть связаны с различными аденокарциномами.
В Центрах лечения рака Америки ® (CTCA) нашу диагностическую группу онкологов возглавляют онкологи и другие врачи, прошедшие подготовку по широкому кругу медицинских специальностей, включая радиологию, патологию, генетику и расширенное геномное тестирование.Они используют сложные тесты и процедуры для измерения стадии и прогрессирования заболевания и определения типа, размера и местоположения опухоли.
Варианты лечения
Лечение аденокарциномы также зависит от того, где она растет в организме. Процедуры могут включать:
Хирургия : Часто в качестве первой линии лечения аденокарциномы используется операция по удалению раковой железистой ткани и некоторых окружающих тканей. Если возможно, можно использовать минимально инвазивные хирургические процедуры, чтобы сократить время заживления и риск послеоперационной инфекции.
Химиотерапия : Химиотерапия использует лекарства для уничтожения раковых клеток. Химиопрепараты можно использовать по всему телу или в определенной области.
Лучевая терапия : Часто используемые в сочетании с хирургией и / или химиотерапией, передовые методы лучевой терапии используют визуализацию до и во время лечения для нацеливания на опухоли аденокарциномы и сохранения здоровых тканей и окружающих органов.
Таргетная терапия : В отличие от химиотерапии, которая убивает здоровые и раковые клетки, это лечение напрямую нацелено на раковые клетки.Терапия предназначена для воздействия на генетические особенности, регулирующие рост и деление клеток.
Иммунотерапия : вместо того, чтобы напрямую атаковать раковые клетки, иммунотерапия предупреждает иммунную систему организма о наличии аномальных клеток. Это, в свою очередь, запускает собственный иммунный ответ организма на поражение рака.Повреждение слизистой оболочки двенадцатиперстной кишки связано с пролиферативной активностью гамартомы железы Бруннера: клинический случай | BMC Gastroenterology
Гамартома железы Бруннера, как правило, представляет собой полип на ножке, состоящий из гиперпластических желез Бруннера с различным количеством протоков, гладкой мускулатуры, фиброзной ткани, жировой ткани и лимфоцитов.Это поражение взаимозаменяемо называется аденомой железы Бруннера, однако некоторые спорят об использовании последнего, поскольку это поражение обычно представляет собой примесь нормальных тканей без цитологической атипии.
Гамартома железы Бруннера встречается преимущественно у людей в возрасте от пятидесяти до шестидесяти лет. Было зарегистрировано несколько случаев в возрасте от двадцати лет с описанием размера поражения или без него, и, насколько нам известно, только в двух случаях (23- и 20-летние женщины) были зарегистрированы упоминания об их необычно большом размере полипа [5].5 см при гистологическом исследовании и 7 см при эндоскопии [5, 6].
Основным недостатком большого полипа является то, что доброкачественное поражение может быть неправильно диагностировано и лечиться как злокачественное. Ранее сообщалось о 60-летнем мужчине, который лечил гиперплазию железы Бруннера с образованием полипа 5,5 см на луковице двенадцатиперстной кишки с помощью дуоденоцефалопанкреатэктомии [7]. При обнаружении большого полипа в двенадцатиперстной кишке для клиницистов важно установить гамартому железы Бруннера в качестве дифференциального диагноза, даже при редкости заболевания.
В нашем иммуногистохимическом исследовании пролиферативная активность желез Бруннера была высокой под эпителием, показывая фовеолярную метаплазию желудка. Фовеолярная метаплазия желудка, по-видимому, часто встречается при гамартоме железы Бруннера [2], а также связана с диспластическими изменениями при гиперплазии железы Бруннера [8, 9]. Одним из заболеваний двенадцатиперстной кишки, часто сопровождающимся фовеолярной метаплазией желудка, является язва двенадцатиперстной кишки. При язве двенадцатиперстной кишки механизм восстановления слизистой оболочки сначала формирует эпителий с фовеолярной метаплазией желудка, а затем увеличивает железы Бруннера [10].Хотя неясно, как растет гамартома железы Бруннера, разумно предположить, что повторяющиеся повреждения слизистой активируют механизм восстановления слизистой оболочки, способствуя пролиферации желез Бруннера, сопровождаемой поверхностной фовеолярной метаплазией желудка.
Ким, и др. , недавно сообщалось о гистологии и экспрессии муцина в гамартоме и гиперплазии железы Бруннера [2]. Они показали, что очаги гамартомы / гиперплазии железы Бруннера, как правило, больше с поверхностными эпителиальными изменениями, такими как эрозия, язва и фовеолярная метаплазия желудка, что согласуется с нашей гипотезой о том, что повреждение слизистой оболочки способствует пролиферации железы Бруннера.Хотя пролиферативная активность приповерхностного эпителия желез Бруннера не была описана в их исследовании, сообщалось о незначительном увеличении пролиферативной активности в атипичных железах и склеротических железистых очагах с индексом маркировки MIB-1 3% и 2%, соответственно. Склеротические железистые очаги, вероятно, являются старыми поражениями в процессе репарации слизистой оболочки, поскольку очаги были обнаружены в 63,2% случаев с поверхностными эпителиальными изменениями, но не в случаях без поверхностных эпителиальных изменений [2].
Учитывая возможные причины повреждения слизистой оболочки, были предложены механические раздражители, инфекция Helicobacter pylori и гиперацидная среда в двенадцатиперстной кишке.Предполагается, что последние два участвуют в развитии гамартомы железы Бруннера [11, 12]. Инфекция Helicobacter pylori наблюдалась в некоторых случаях гамартомы железы Бруннера [3], но не наблюдалась в других случаях [4]. Маловероятно, что инфекция является существенной для гамартоматозного разрастания желез Бруннера. Повышенная кислотность может вызвать гиперпластические изменения желез Бруннера, которые выделяют щелочной муцин для буферизации желудочной кислоты. Franzin, et al. ., Продемонстрировали гиперацидное состояние у пациентов с гамартомой железы Бруннера [12].Интересно, что фовеолярная метаплазия желудка рассматривается как защитное изменение слизистой оболочки двенадцатиперстной кишки от повышенной кислотности [13].
Таким образом, мы сообщаем о случае большой гамартомы железы Бруннера у молодого (26-летнего) пациента. Наши иммуногистохимические результаты показывают, что повреждение слизистой лежит в основе гамартоматозной пролиферации желез Бруннера.
Протеом человека в кишечнике
Кишечник является основным местом расщепления пищи и всасывания питательных веществ.Он охватывает двенадцатиперстную, тощую, подвздошную, толстую и прямую кишки. Он получает химус (полужидкую массу) из желудка и желчных и панкреатических жидкостей из панкреатобилиарного протока в двенадцатиперстной кишке, чтобы начать разложение липидов и углеводов, чтобы обеспечить их поглощение в тощей и подвздошной кишке. В толстой кишке всасывается оставшаяся вода, электролиты и витамины, после чего кал попадает в прямую кишку, где они хранятся до выхода через анальный канал. Анализ транскриптома показывает, что 79% (n = 15609) всех белков человека (n = 19670) экспрессируются в кишечнике, а 764 из этих генов демонстрируют повышенную экспрессию в кишечнике по сравнению с другими типами тканей.
- 764 повышенных гена
- 122 обогащенных гена
- 200 групповых обогащенных генов
- Кишечник имеет наибольшую групповую экспрессию генов, общих с печенью
Расшифровка кишечника
Анализ транскриптома кишечника может быть визуализирован в отношении специфичности и распределения транскрибируемых молекул мРНК (рис. 1). Специфичность показывает количество генов с повышенной или не повышенной экспрессией в кишечнике по сравнению с другими тканями.Повышенное выражение включает три подкатегории типа повышенного выражения:
- Ткань обогащена: уровень мРНК в кишечнике по крайней мере в четыре раза выше по сравнению с любыми другими тканями.
- Обогащенная группа: по крайней мере, в четыре раза выше средний уровень мРНК в группе из 2-5 тканей по сравнению с любой другой тканью.
- Улучшенная ткань: по крайней мере, в четыре раза выше уровень мРНК в кишечнике по сравнению со средним уровнем во всех других тканях.
Распределение, с другой стороны, визуализирует, сколько генов имеет или не имеет обнаруживаемых уровней (NX≥1) транскрибированных молекул мРНК в кишечнике по сравнению с другими тканями.Как видно из таблицы 1, все гены с повышенным содержанием в кишечнике классифицируются как:
- Обнаружен в одиночном: обнаружен в отдельной ткани
- Обнаружен в некоторых: Обнаружен более чем в одной, но менее чем в одной трети тканей
- Обнаружен во многих: обнаружен по крайней мере в трети, но не во всех тканях
- Обнаружен во всех: Обнаружен во всех тканях
Рис. 1. (A) Распределение всех генов по пяти категориям на основе специфичности транскрипта в кишечнике, а также во всех других тканях.(B) Распределение всех генов по шести категориям на основе обнаружения транскриптов (NX≥1) в кишечнике, а также во всех других тканях.
Как показано на рисунке 1, 764 гена демонстрируют некоторый уровень повышенной экспрессии в кишечнике по сравнению с другими тканями. Три категории генов с повышенной экспрессией в кишечнике по сравнению с другими органами показаны в таблице 1. В таблице 2 определены 12 генов с наибольшим обогащением в кишечнике.
Таблица 1.Количество генов в подразделенных категориях повышенной экспрессии в кишечнике.
Таблица 2. 12 генов с наивысшим уровнем экспрессии в кишечнике. «Тканевое распределение» описывает обнаружение транскрипта (NX≥1) в кишечнике, а также во всех других тканях. «мРНК (ткань)» показывает уровень транскрипта в кишечнике в виде значений NX. «Оценка тканевой специфичности (TS)» соответствует кратному изменению между уровнем экспрессии в кишечнике и ткани со вторым по величине уровнем экспрессии.
| Джин | Описание | Распределение тканей | мРНК (ткань) | Оценка тканевой специфичности |
|---|---|---|---|---|
| ALPI | щелочная фосфатаза кишечная | Обнаружен в одиночном | 133,2 | 406 |
| C17orf78 | открытая рамка считывания 17 хромосомы 78 | Обнаружен в одиночном | 83.8 | 401 |
| MUC17 | муцин 17, ассоциированный с клеточной поверхностью | Обнаружен в одиночном | 125,2 | 299 |
| DEFA5 | дефенсин альфа 5 | Обнаружен в некоторых | 574,2 | 231 |
| RBP2 | ретинол-связывающий белок 2 | Обнаружен в некоторых | 333,2 | 198 |
| DEFA6 | дефенсин альфа 6 | Обнаружен в некоторых | 316.3 | 189 |
| MLN | мотилин | Обнаружен в одиночном | 76,0 | 175 |
| MEP1B | бета-субъединица меприна А | Обнаружен в некоторых | 241,5 | 167 |
| ЛСТ | лактаза | Обнаружен в некоторых | 255,5 | 133 |
| SI | сахароза-изомальтаза | Обнаружен в некоторых | 181.4 | 123 |
| TM4SF20 | трансмембранный 4 л из шести членов семьи 20 | Обнаружен в некоторых | 147,8 | 86 |
| FABP6 | белок, связывающий жирные кислоты 6 | Обнаружен в некоторых | 299,2 | 68 |
Повышенная экспрессия белков в кишечнике
Углубленный анализ повышенных генов в кишечнике с использованием профилей белков на основе антител позволил нам визуализировать паттерны экспрессии этих белков в различных функциональных компартментах, включая белки, участвующие в организации микроворсинок, и белки, участвующие в расщеплении и поглощении питательных веществ.
Белки, участвующие в организации микроворсинок
Несколько генов с повышенной экспрессией в кишечнике кодируют белки, связанные с организацией микроворсинок. (VIL1) представляет собой регулируемый кальцием актин-связывающий белок, который покрывает, отсекает, а также связывает актиновые филаменты в щеточной кайме кишечника. Микроворсинки прикреплены друг к другу посредством гетерофильных комплексов между (CDHR2) и (CDHR5). Тем самым контролируется упаковка микроворсинок на апикальной мембране.
VIL1
CDHR2
CDHR5
Белки, участвующие в пищеварении
Кишечник отвечает за поглощение множества различных питательных веществ, таких как жирные кислоты, аминокислоты и углеводы.Поглощению, метаболизму и транспорту жирных кислот способствуют белки, связывающие жирные кислоты (FABP). Например, считается, что FABP2 участвует в синтезе богатых триглицеридами липопротеинов. С другой стороны, сложные углеводы, такие как крахмал, расщепляются SI, локализованным на щеточной границе кишечника. Простые углеводы транспортируются через просветную мембрану через SLC5A1, натрий-зависимый переносчик глюкозы. Для глюкозы и галактозы SLC5A1 является основным переносчиком, мутации в этом гене были связаны с мальабсорбцией глюкозы-галактозы.
FABP2
SI
SLC5A1
Гены, общие для кишечника и других тканей
В кишечнике экспрессируется 200 генов, обогащенных группами. Обогащенные группы гены определяются как гены, показывающие в 4 раза более высокий средний уровень экспрессии мРНК в группе из 2-5 тканей, включая кишечник, по сравнению со всеми другими тканями.
Чтобы проиллюстрировать отношение ткани кишечника к другим типам тканей, был создан сетевой график, отображающий количество генов с общей экспрессией между различными типами тканей.
Рис. 2. Интерактивный сетевой график обогащенных и обогащенных группами генов кишечника, связанных с их соответствующими обогащенными тканями (серые кружки). Красные узлы представляют количество генов, обогащенных кишечником, а оранжевые узлы представляют количество генов, обогащенных группой. Размеры красных и оранжевых узлов связаны с количеством генов, отображаемых в узле. На каждый узел можно щелкнуть, и в результате отображается список всех обогащенных генов, связанных с выделенными краями.Сеть ограничена группами обогащенных генов в комбинациях до 2 тканей, но полученные списки показывают полный набор групповых обогащенных генов в конкретной ткани.
Кишечник разделяет наибольшую экспрессию генов, обогащенных группой, с печенью. Одним из примеров гена, экспрессируемого как в кишечнике, так и в печени, является SLC2A2, мембранный белок, который участвует в двунаправленном транспорте глюкозы. Другой белок, обнаруженный в обоих органах, – это NPC1L1, переносчик, способный переносить свободный холестерин, а также витамин Е посредством везикулярного эндоцитоза.Считается, что открытая рамка считывания C6orf58 участвует в раннем развитии печени, однако ее функция неизвестна. C6orf58 экспрессируется в подслизистой оболочке желез Бруннера в двенадцатиперстной кишке, желудке и слюнной железе. Кишечный тракт также разделяет экспрессию нескольких генов с почками. Фермент DDC экспрессируется в почках и кишечнике, удаляет карбоксильные группы предшественников молекул дофамина, серотонина и триптамина.
SLC2A2 – двенадцатиперстная кишка
SLC2A2 – тонкий кишечник
SLC2A2 – печень
NPC1L1 – двенадцатиперстная кишка
NPC1L1 – тонкий кишечник
NPC1L1 – печень
C6orf58 – двенадцатиперстная кишка
C6orf58 – желудок
C6orf58 – слюнная железа
DDC – двенадцатиперстная кишка
DDC – тонкий кишечник
DDC – почка
Самая проксимальная и самая широкая часть тонкой кишки – двенадцатиперстная кишка.Он начинается у привратника желудка, заканчивается у дуоденоеюнального перехода и имеет длину около 25 см. Он получает частично переваренную пищу (химус) из желудка и желчных и панкреатических жидкостей из панкреатобилиарного протока. После попадания в двенадцатиперстную кишку кислотное содержимое желудка нейтрализуется секрецией кишечника и поджелудочной железы. Ферменты, секретируемые поджелудочной железой, инициируют расщепление липидов, углеводов и белков, обеспечивая всасывание.
Как и во всем кишечнике, слизистая оболочка образует пальцевидные выступы, называемые ворсинками, которые проходят в просвет кишечника.Это эпителиальные складки, выстланные клетками двух типов: энтероцитами и бокаловидными клетками. Энтероциты представляют собой простые столбчатые клетки с удлиненными базальными ядрами и апикальной щеточной каймой. Кайма-кисть представляет собой микроскопическое изображение небольших выступов клеточной мембраны, микроворсинок, которые значительно увеличивают площадь поверхности клетки, увеличивая поглощающую способность. Другой тип клеток – это бокаловидные клетки, секретирующие слизь, которые можно распознать по наличию апикальной слизистой оболочки. Ядро ворсинки является частью собственной пластинки.Самыми многочисленными клетками собственной пластинки являются иммунные клетки, большинство из которых – лимфоциты. Поскольку ворсинки являются местом всасывания пищи, они имеют богатое кровоснабжение, каждая ворсинка снабжается центральными артериолами и дренируется центральными венулами и центральным лимфатическим сосудом.
В основе ворсинок находятся кишечные железы, также называемые криптами Либеркуна. Эти железы выстланы многочисленными относительно недифференцированными столбчатыми клетками, которые обычно проходят два раунда митоза, прежде чем дифференцироваться либо в абсорбирующие клетки, либо в бокаловидные клетки.Энтероциты, бокаловидные клетки, клетки панета, которые секретируют антибактериальные ферменты (распознаваемые эозинофильными гранулами в их апикальной цитоплазме) и энтероэндокринные клетки, также выстилают крипту. Тонкий слой гладкой мускулатуры отмечает конец слизистой оболочки, muscularis mucosae. В подслизистой оболочке присутствуют многочисленные бледно окрашенные железы, а именно железы Бруннера. Это разветвленные трубчатые или альвеотубулярные железы, выстланные столбчатым секреторным эпителием. Они выделяют большое количество щелочной слизи, которая нейтрализует кислотное содержимое желудка.
Гистологию двенадцатиперстной кишки человека, включая подробные изображения и информацию, можно просмотреть в гистологическом словаре белкового атласа.
Тонкая кишка (тощая кишка и подвздошная кишка) составляет около 6 метров и поглощает пищу, воду и электролиты. По гистологии и составу похож на двенадцатиперстную кишку. Постоянная поперечная подслизистая складка, проходящая в просвет кишечника, называется круговой складкой. Круговая складка состоит из слизистой, а также подслизистой оболочки.Ядро – это подслизистая основа, состоящая из рыхлой соединительной ткани, кровеносных сосудов, нервов и рассредоточенной лимфоидной ткани. Отличительной особенностью тощей и подвздошной кишок является отсутствие желез в подслизистой основе.
Слизистая оболочка характеризуется многочисленными пальцевидными ворсинками, которые выступают в просвет кишечника. Энтероциты, которые представляют собой столбчатые эпителиальные клетки с базально расположенными овальными ядрами и апикальной щеткой, граничащей с ворсинками. Энтероциты, расположенные у ворсинок, в основном выполняют абсорбционную функцию.Между энтероцитами вкраплены бокаловидные клетки, которые распознаются по содержимому большой слизистой глобулы, напоминающей небольшой «пустой пузырь» в эпителиальной выстилке. Бокаловидные клетки соединены с базальной мембраной тонкой цитоплазматической цепью, которую трудно различить при окраске гематоксилином и эозином. В основе кишечных ворсинок лежат кишечные железы. Это прямые трубчатые железы, слегка расширенные внизу. Стволовые клетки кишечника выстилают проксимальную часть желез.Стволовые клетки дают начало всем клеткам эпителия, которыми являются клетки панета, энтероциты, бокаловидные клетки и энтероэндокринные клетки. Клетки Панета секретируют антибактериальные ферменты и расположены в нижней части кишечных желез. Клетки Панета распознаются эозинофильными гранулами в цитоплазме.
Гистологию тонкой кишки человека, включая подробные изображения и информацию, можно просмотреть в гистологическом словаре белкового атласа.
Ободочная кишка делится на четыре части: восходящая, поперечная, нисходящая и сигмовидная кишка в среднем составляет 1.5 метров в длину. Его основная функция – восстановление жидкости, электролитов и витаминов. Поскольку толстая кишка не имеет ворсинок или круговой складки, слизистая оболочка гладкая. Простые трубчатые кишечные железы (крипты Либеркуна) проходят через всю толщу слизистой оболочки. Поверхностный столбчатый эпителий и клетки, выстилающие крипты, представляют собой энтероциты с овальным базальным ядром и апикальной щеточной каймой, микроскопическим представлением микроворсинок. Есть также многочисленные слизистые, секретирующие бокаловидные клетки, распознаваемые по их содержанию в большом слизистом шарике.Собственная пластинка с соединительной тканью и воспалительными клетками окружает крипты. Тонкий гладкий мышечный слой, lamina muscularis mucosae, отмечает границу между слизистой оболочкой и подслизистой оболочкой. Подслизистая основа состоит из рыхлой соединительной ткани с сосудами и нервами. Также видны отдельные лимфатические фолликулы. Мышечный слой (muscularis externa) состоит из внутреннего круглого гладкомышечного слоя, внешний продольный мышечный слой не является непрерывным, как в остальной части желудочно-кишечного тракта.Он разделен на три утолщенные мышечные полосы, называемые teniae coli.
Гистологию толстой кишки человека, включая подробные изображения и информацию, можно просмотреть в гистологическом словаре белкового атласа.
Здесь описаны и охарактеризованы гены, кодирующие белок, экспрессируемые в кишечнике, вместе с примерами иммуногистохимически окрашенных срезов ткани, которые визуализируют соответствующие паттерны экспрессии белков генов с повышенной экспрессией в кишечнике.
Профилирование транскриптов было основано на комбинации трех наборов данных транскриптомики (HPA, GTEx и FANTOM5), что соответствует в общей сложности 9332 образцам из 113 различных типов нормальных тканей человека.Окончательное согласованное значение нормализованной экспрессии (NX) для каждого типа ткани использовалось для классификации всех генов в соответствии с тканеспецифической экспрессией на две разные категории на основе специфичности или распределения.
Uhlén M et al., Тканевая карта протеома человека. Science (2015)
PubMed: 25613900 DOI: 10.1126 / science.1260419
Yu NY et al., Дополнительная характеристика ткани путем интеграции профилей транскриптомов из Атласа белков человека и консорциума FANTOM5. Nucleic Acids Res. (2015)
PubMed: 26117540 DOI: 10.1093 / nar / gkv608
Fagerberg L et al., Анализ тканеспецифической экспрессии человека путем полногеномной интеграции транскриптомики и протеомики на основе антител.

 Содержание: I. Эмбриология, анатомия и гистология … 16 II. Биохимия………………. 22 III. Патологическая анатомия ……… 2 2 IV. Патологическая физиология……… 28 V. Функциональная диагностика…….. 30 VІ.… … Большая медицинская энциклопедия
Содержание: I. Эмбриология, анатомия и гистология … 16 II. Биохимия………………. 22 III. Патологическая анатомия ……… 2 2 IV. Патологическая физиология……… 28 V. Функциональная диагностика…….. 30 VІ.… … Большая медицинская энциклопедия Восходящая ободочная кишка (colon ascendens) (рис. 151, 159, 171) является продолжением слепой. Ее задняя поверхность не покрыта брюшиной и … Атлас анатомии человека
Восходящая ободочная кишка (colon ascendens) (рис. 151, 159, 171) является продолжением слепой. Ее задняя поверхность не покрыта брюшиной и … Атлас анатомии человека
 Менструация) и местом развития плодного яйца (см. Беременность, Роды), занимает центральное положение в половом аппарате женщины и в тазовой полости; лежит в геометрическом центре… … Большая медицинская энциклопедия
Менструация) и местом развития плодного яйца (см. Беременность, Роды), занимает центральное положение в половом аппарате женщины и в тазовой полости; лежит в геометрическом центре… … Большая медицинская энциклопедия