Кровотечение из пищевода при циррозе печени: Цирроз, портальная гипертензия, кровотечение – разорви порочный круг заболеваний!
Варикозное кровотечение
Варикозное кровотечение
Внимание! Многие операции при циррозе печени, портальной гипертензии и варикозном расширении вен пищевода входят в перечень ВМП и финансируются из федерального бюджета. Узнайте больше на консультации специалиста:КРОВОТЕЧЕНИЯ ПРИ ЦИРРОЗЕ ПЕЧЕНИ И ПОРТАЛЬНОЙ ГИПЕРТЕНЗИИ. НОВЕЙШИЕ МЕТОДИКИ ДИАГНОСТИКИ И ЛЕЧЕНИЯ.
Возможным этапом развития хронических гепатитов является формирование цирроза печени и синдрома портальной гипертензии. Кровотечение из вен пищевода является наиболее драматичным осложнением портальной гипертензии. В отсутствии квалифицированного лечения летальность превышает 70%, а иногда вообще не оставляет шансов на выживание.
Источники кровотечений портального генеза
В соответствии с анатомической локализацией источников кровотечения можно выделить пищеводные и желудочные геморрагии, а также кровотечения из «эктопических вариксов».
Основной механизм развития кровотечения портального генеза связан с повышением портального давления. Источник кровотечения может быть связан с разрывом относительно крупного венозного сосуда в подслизистом слое пищевода, что представляет собой наиболее частый вариант геморрагии.
Варикозное расширение вен пищевода
ВРВ пищевода являются наиболее частой причиной кровотечений. Высокая частота пищеводных кровотечений обусловлена анатомическими особенностями нижней трети пищевода (поверхностное расположение вен, повышение сосудистого сопротивления на этом уровне, наличие нескольких венозных уровней, соединенных коммуникантами).
Эндоскопическая картина продолжающегося кровотечения из ВРВ пищевода
Варикозное расширение вен желудка
Проблемы эндоскопической диагностики варикозной трансформации желудочных вен связаны с их более глубоким расположением. ВРВ желудка могут являться как продолжением пищеводных вен, так и располагаться изолированно в своде желудка. Последний вариант чаще наблюдается при внепеченочном блоке.
Последний вариант чаще наблюдается при внепеченочном блоке.
Эндоскопическая картина ВРВ свода желудка с использованием методики инверсионного осмотра
Несмотря на то, что факт выявления ВРВ желудка в целом не влияет на выживаемость пациентов, желудочное кровотечение является потенциально более опасным. Это обусловлено низкой лечебной эффективностью эндоскопических методов. Именно поэтому четкое клиническое разграничение пищеводных и желудочных кровотечений присутствует в большинстве современных лечебно-диагностических алгоритмов.
Эктопические вариксы
Эктопические вариксы — варикозное расширение вен в органах, кроме желудка и пищевода. Выявление эктопических вариксов чаще наблюдается при внепеченочной форме портальной гипертензии. Иногда их появление связывают с последствиями эндоскопической облитерации вен пищевода. Эктопические ВРВ встречаются преимущественно в желудочно-кишечном тракте.
ВРВ тощей кишки (эктопический варикс),
диагностировано методом видеокапсульной эндоскопии
Эктопический варикс со стигмами состоявшего кровотечения
Кровотечение из эктопических варикозных вен — довольно редкое явление. Эта локализация варикозных вен является источником кровотечения приблизительно в 5 % случаев при внутрипеченочной портальной гипертензии и до 20 % при внепеченочной форме. Одна треть кровотечений из эктопических вариксов приходится на двенадцатиперстную кишку, одна треть — на тонкую кишку и одна треть — на ободочную кишку, из них 50 % — сигмовидная кишка.
Эндоскопическое лигирование
Быстрое и успешное внедрение метода лигирования ВРВ пищевода и желудка в программу профилактики и лечения варикозных кровотечений обусловлено рядом его преимуществ по сравнению со склеротерапией. Эндоскопическое лигирование быстрее позволяет достичь желаемого эффекта, более безопасно и легче переносится пациентами.
При остром кровотечении выполняют прямое лигирование кровоточащего участка варикозной вены.
Методика прямого/прецизионного лигирования ВРВ пищевода
Для решения этой задачи эндоскоп подводят к зоне дефекта варикозной вены. Лигатура накладывается непосредственно на этот участок. В случае если не удается четко установить участок повреждения вены, проводится «спиральное» лигирование, когда эластичные кольца (лигатурные петли) накладываются последовательно по спирали на каждый варикозный ствол. На каждый ствол используют от 2 до 4 колец до полной остановки кровотечения.
Профилактическое лигирование изначально предполагает спиральный метод аппликации. Начиная от гастроэзофагеального перехода, лигатуры накладываются таким образом, чтобы в одной плоскости располагалась лишь одна лигатура. Соблюдение данной методики предотвращает развитие стенозов в пищеводе. Возможно наложение до 10 лигатур за один сеанс.
Облитерация варикозных вен тканевыми клеями
Эндоскопическая склеротерапия и лигирование не лишены целого ряда недостатков. В настоящее время используются преимущественно два цианакрилатных полимера: гистоакрил (n-бутил-2-цианакрилат) и букрилат (изобутил-1-цианакрилат). К особенностям тканевых клеев относится их замедленная полимеризация в физиологическом растворе в течение 20 сек. Введение гистоакрила в кровоточащий варикозный узел обеспечивает эффективную остановку кровотечения, так как образующийся полимер, приобретая в просвете сосуда твердую консистенцию в виде «слепка» вены, надежно прекращает в ней кровоток.
В настоящее время используются преимущественно два цианакрилатных полимера: гистоакрил (n-бутил-2-цианакрилат) и букрилат (изобутил-1-цианакрилат). К особенностям тканевых клеев относится их замедленная полимеризация в физиологическом растворе в течение 20 сек. Введение гистоакрила в кровоточащий варикозный узел обеспечивает эффективную остановку кровотечения, так как образующийся полимер, приобретая в просвете сосуда твердую консистенцию в виде «слепка» вены, надежно прекращает в ней кровоток.
Из всех эндоскопических методов облитерация тканевыми клеями является технически наиболее сложной. При выполнении облитерации велика роль фактора времени в успехе лечения. Все манипуляции должны выполняться быстро, что требует специальной подготовки и взаимопонимания персонала.
Существуют рекомендации при проведении облитерирующего лечения смешивать гистоакрил с 0,5—0,8 мл масляного контрастного вещества липиодола с целью предупреждения быстрого затвердевания препарата и возможности последующего рентгенологического контроля.
Методика интравазального введения склерозанта (гистакрил + липиодол)
Использование интравазального введения клеевых композиций позволяет добиться гемостаза в 90—100 % случаев. В связи с технической сложностью данного метода, которая определяется необходимостью обязательной четкой визуализацией источника геморрагии и строгого интравазального введения препарата, использование клеевых композиций при любом кровотечении из ВРВ пищевода и желудка нецелесообразно. Рационально использование цианакрилатов для остановки кровотечения из ВРВ желудка, когда стандартные склерозанты малоэффективны, при массивных кровотечениях из ВРВ пищевода, а также в случае ранних рецидивов кровотечений.
Самораскрывающийся металлический стент
В клинике был разработан модифицированный вариант — стент Элла-Дениша, который позволяет выполнить лечебную манипуляцию без рентгенологического или эндоскопического контроля. Стент Дениша сделан в форме, которая соответствует анатомической конфигурации пищевода и варикозно расширенных вен, особенно его дистальной части — 4—6 см.
Стент Дениша в просвете пищевода (эндоскопический контроль и оценка эффективности установки)
При установке СМРС были выявлены следующие преимущества:
– стент не может быть удален или смещен самим пациентом в состоянии возбуждения;
– просвет стента обеспечивает физиологический дренаж слюны. Возможен прием жидкости и пищи через рот;
– тщательный повторный осмотр пищевода, кардии, желудка и 12-перстной кишки, а также эвакуация желудочного содержимого возможна сразу же после введения стента.
Установка стента для прекращения кровотечения из варикозно расширенных вен пищевода является инновационной методикой, которая была применена у пациентов в чрезвычайных ситуациях, связанных с высоким риском для жизни. Процедура не вызвала осложнений и привела к быстрой остановке кровотечения у всех больных. Конечно, необходимы дальнейшие исследования, чтобы подтвердить эти первоначальные положительные данные.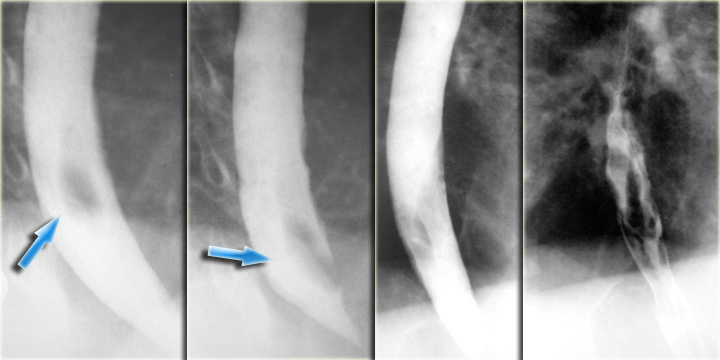
Хирургические вмешательства
По основной патогенетической направленности выделяют операции портосистемного шунтирования и портоазигального разобщения.
Снижение портального давления методом портосистемного шунтирования устраняет один из решающих патогенетических факторов возникновения кровотечений из ВРВ пищевода и желудка.
Бурное развитие хирургической техники и совершенствование анестезиологического обеспечения создали в начале 1940-х гг. предпосылки для развития операций портосистемного шунтирования. Применение сосудистых портосистемных шунтов в клинической практике выдвинуло целый ряд проблем. Операционная травма зачастую становится непереносимой для большинства декомпенсированных больных циррозом печени. Синдром портосистемной энцефалопатии усугублялся у большинства оперированных больных. В 1970-е гг. период увлечения декомпрессивными операциями сменился более сдержанным к ним отношением. Были обобщены отдаленные результаты, показывающие отсутствие увеличения продолжительности жизни пациентов после операций портосистемного шунтирования.
После портосистемного шунтирования снижаются процессы регенерации печени. В выборе типа шунта существуют своеобразные «ножницы»: чем больше диаметр шунта, тем выраженнее декомпрессивный эффект вмешательства, но при этом выше послеоперационная летальность, чаще возникает энцефалопатия, меньше продолжительность и ниже качество жизни пациентов. И наоборот, малый диаметр шунта сопровождается меньшей летальностью, энцефалопатией, умеренным угнетением печеночной регенерации, но при этом часто оказывается неэффективным в снижении портального давления. Ряд исследователей находят, что практически любой тип сосудистых портосистемных анастомозов способствует прогрессированию дистрофических процессов в печени и часто осложняется развитием печеночной энцефалопатии. Главный недостаток портосистемных анастомозов связан с существенным снижением портальной перфузии печени и увеличением объема шунтирующейся крови.
В настоящее время больше внимание уделяется не селективности шунтирования, а степени портальной декомпрессии. Доминирующую позицию занимает концепция парциальной (дозированной, частичной) портальной декомпрессии. Оптимальным считается диаметр анастомоза 6—8 мм. При этом существенно снижается риск кровотечения, а снижение функции печени и усугубление портосистемной энцефалопатии не выражены.
Процедура чрезъяремного внутрипеченочного портосистемного шунтирования является одной из последних новаторских технологий, позволяющей выполнить эффективную декомпрессию портальной системы. В англоязычной научной литературе для обозначения этого вмешательства общепринято использовать аббревиатуру TIPS — Transjugular intrahepatic portosystemic shunt.
Идея создания портальной декомпрессии путем чрескожного формирования внутрипеченочного соустья между крупными печеночными и воротной венами впервые была сформулирована и осуществлена в эксперименте Josef Rosch (1969). Разработка компактных металлических сосудистых эндопротезов в конце 80-х гг. позволила вывести процедуру TIPS на клиническую сцену и обеспечила техническую основу успешного формирования венозно-венозной фистулы в паренхиме печени. Первое клиническое использование процедуры было выполнено G. Richter [et al.] (1990). Начиная с этого времени, началось повсеместное внедрение методики TIPS в клиническую практику.
позволила вывести процедуру TIPS на клиническую сцену и обеспечила техническую основу успешного формирования венозно-венозной фистулы в паренхиме печени. Первое клиническое использование процедуры было выполнено G. Richter [et al.] (1990). Начиная с этого времени, началось повсеместное внедрение методики TIPS в клиническую практику.
Процедура внутрипеченочного портоситемного шунтирования
«Технический успех» TIPS (т. е. успешное вмешательство и выживаемость пациентов в течение 30 дней) достигает высоких значений и составляет 93—100 %. Отсутствие рецидива кровотечения в течение 1 мес. наблюдается в 83 % случаев. Наибольшее число осложнений отмечается среди пациентов Child С и при наличии асцита, свидетельствующего о декомпенсированной функции печени.
Профилактика и лечение некоторых осложнений при циррозе печени uMEDp
Лечение больных циррозом печени остается одной из ключевых проблем современной медицины в целом и гастроэнтерологии и гепатологии в частности. Это связано, во-первых, с высокой частотой госпитализации таких больных. По данным Центрального научно-исследовательского института гастроэнтерологии, в 2011–2013 гг. число пациентов с циррозом печени в среднем составило 44–51% от общего числа пациентов, пролеченных в отделении хронических заболеваний печени (табл. 1). Во-вторых, для цирроза печени характерны быстрая инвалидизация и высокая смертность (по разным данным, уровень смертности в течение 5 лет после постановки диагноза составляет от 45 до 86%). В-третьих, следует учитывать недостаточный на сегодняшний день объем трансплантаций печени в России – до 100 в год при потребности в несколько тысяч подобных вмешательств.
Это связано, во-первых, с высокой частотой госпитализации таких больных. По данным Центрального научно-исследовательского института гастроэнтерологии, в 2011–2013 гг. число пациентов с циррозом печени в среднем составило 44–51% от общего числа пациентов, пролеченных в отделении хронических заболеваний печени (табл. 1). Во-вторых, для цирроза печени характерны быстрая инвалидизация и высокая смертность (по разным данным, уровень смертности в течение 5 лет после постановки диагноза составляет от 45 до 86%). В-третьих, следует учитывать недостаточный на сегодняшний день объем трансплантаций печени в России – до 100 в год при потребности в несколько тысяч подобных вмешательств.
 В мире сегодня активно ведутся поиски альтернативных методов лечения в двух направлениях. Первое – создание генно-инженерных препаратов, активно влияющих на структурные изменения печени при циррозе. Второе – использование стволовых клеток крови и клеток-предшественников клеток печени, позволяющих восстановить поврежденные при цирротической трансформации функции печени. Кроме того, продолжаются исследования по изучению антифибротических свойств известных противовирусных препаратов (аналоги нуклеоти(зи)дов, интерфероны) и гепатопротекторов, по поиску новых антифибротических агентов.
У больных циррозом печени необходимо уточнять функциональные резервы печени и прогноз выживаемости, чтобы своевременно выявлять тех, кто нуждается в трансплантации [1]. Кроме того, оценка прогностических факторов как исходно, так и в динамике позволяет проанализировать эффективность проводимых лечебно-профилактических мероприятий. Степень тяжести цирроза печени в зависимости от печеночно-клеточной недостаточности можно определить по классификации Чайлда – Пью (Child – Pugh) (табл.
В мире сегодня активно ведутся поиски альтернативных методов лечения в двух направлениях. Первое – создание генно-инженерных препаратов, активно влияющих на структурные изменения печени при циррозе. Второе – использование стволовых клеток крови и клеток-предшественников клеток печени, позволяющих восстановить поврежденные при цирротической трансформации функции печени. Кроме того, продолжаются исследования по изучению антифибротических свойств известных противовирусных препаратов (аналоги нуклеоти(зи)дов, интерфероны) и гепатопротекторов, по поиску новых антифибротических агентов.
У больных циррозом печени необходимо уточнять функциональные резервы печени и прогноз выживаемости, чтобы своевременно выявлять тех, кто нуждается в трансплантации [1]. Кроме того, оценка прогностических факторов как исходно, так и в динамике позволяет проанализировать эффективность проводимых лечебно-профилактических мероприятий. Степень тяжести цирроза печени в зависимости от печеночно-клеточной недостаточности можно определить по классификации Чайлда – Пью (Child – Pugh) (табл. 2). Для оценки риска летального исхода у пациентов с алкогольным гепатитом обычно применяется индекс Маддрея (Maddrey’s Discriminant Function, DF, – дискриминантная функция Маддрея) [2]. Индекс Маддрея рассчитывается по формуле: DF = 4,6 × (разность показателей протромбинового времени у больного и в контроле) + уровень сывороточного билирубина (мг%). Индекс Маддрея, превышающий 32 (DF > 32), указывает на 30–50%-ную вероятность летального исхода в течение ближайшего месяца.
Шкала оценки тяжести пациентов с заболеваниями печени MELD (Model for end-stage liver disease) позволяет уточнить жизненный прогноз пациентов с циррозом печени с использованием формулы: R = 0,957 × Log (креатинин мг/дл) + 0,378 × Log (билирубин мг/дл) + 1,120 × Log (международное нормализованное отношение) + 0,643. Жизненный прогноз пациентов со значением индекса MELD > 18 оценивается как неблагоприятный. При МELD > 11 вероятность смертельного исхода в течение 30 дней составляет 22% [3].
Главной причиной смерти при циррозе печени являются осложнения, основными среди которых следует считать кровотечение из варикозно-расширенных вен пищевода как проявление портальной гипертензии, спонтанный бактериальный перитонит, гепаторенальный синдром, печеночную недостаточность и портосистемную энцефалопатию.
2). Для оценки риска летального исхода у пациентов с алкогольным гепатитом обычно применяется индекс Маддрея (Maddrey’s Discriminant Function, DF, – дискриминантная функция Маддрея) [2]. Индекс Маддрея рассчитывается по формуле: DF = 4,6 × (разность показателей протромбинового времени у больного и в контроле) + уровень сывороточного билирубина (мг%). Индекс Маддрея, превышающий 32 (DF > 32), указывает на 30–50%-ную вероятность летального исхода в течение ближайшего месяца.
Шкала оценки тяжести пациентов с заболеваниями печени MELD (Model for end-stage liver disease) позволяет уточнить жизненный прогноз пациентов с циррозом печени с использованием формулы: R = 0,957 × Log (креатинин мг/дл) + 0,378 × Log (билирубин мг/дл) + 1,120 × Log (международное нормализованное отношение) + 0,643. Жизненный прогноз пациентов со значением индекса MELD > 18 оценивается как неблагоприятный. При МELD > 11 вероятность смертельного исхода в течение 30 дней составляет 22% [3].
Главной причиной смерти при циррозе печени являются осложнения, основными среди которых следует считать кровотечение из варикозно-расширенных вен пищевода как проявление портальной гипертензии, спонтанный бактериальный перитонит, гепаторенальный синдром, печеночную недостаточность и портосистемную энцефалопатию. Учитывая недостаточное количество операций по трансплантации печени в России и пока еще отсутствие фармакоагентов для лечения собственно цирроза и фиброза печени, чрезвычайную актуальность приобретают мероприятия по профилактике и лечению осложнений при циррозе печени. От эффективности применяемых мер зависит продолжительность жизни больных. Кровотечение из варикозно-расширенных вен пищевода
Наиболее распространенным осложнением синдрома портальной гипертензии является варикозное расширение вен пищевода и желудка, которое во многих случаях может сопровождаться кровотечением и приводить к смерти больного. Варикозное расширение вен пищевода и желудка обусловлено образованием портокавальных анастамозов, направленных на декомпрессию воротной системы [4]. Среди портосистемных коллатералей пищеводные имеют наибольшую клиническую значимость из-за их склонности к кровотечениям – примерно в 1/3 случаев [5].
Существует множество классификаций варикозного расширения вен пищевода, которые учитывают расположение и диаметр венозных стволов, наличие деструкции сосудистой стенки.
Учитывая недостаточное количество операций по трансплантации печени в России и пока еще отсутствие фармакоагентов для лечения собственно цирроза и фиброза печени, чрезвычайную актуальность приобретают мероприятия по профилактике и лечению осложнений при циррозе печени. От эффективности применяемых мер зависит продолжительность жизни больных. Кровотечение из варикозно-расширенных вен пищевода
Наиболее распространенным осложнением синдрома портальной гипертензии является варикозное расширение вен пищевода и желудка, которое во многих случаях может сопровождаться кровотечением и приводить к смерти больного. Варикозное расширение вен пищевода и желудка обусловлено образованием портокавальных анастамозов, направленных на декомпрессию воротной системы [4]. Среди портосистемных коллатералей пищеводные имеют наибольшую клиническую значимость из-за их склонности к кровотечениям – примерно в 1/3 случаев [5].
Существует множество классификаций варикозного расширения вен пищевода, которые учитывают расположение и диаметр венозных стволов, наличие деструкции сосудистой стенки.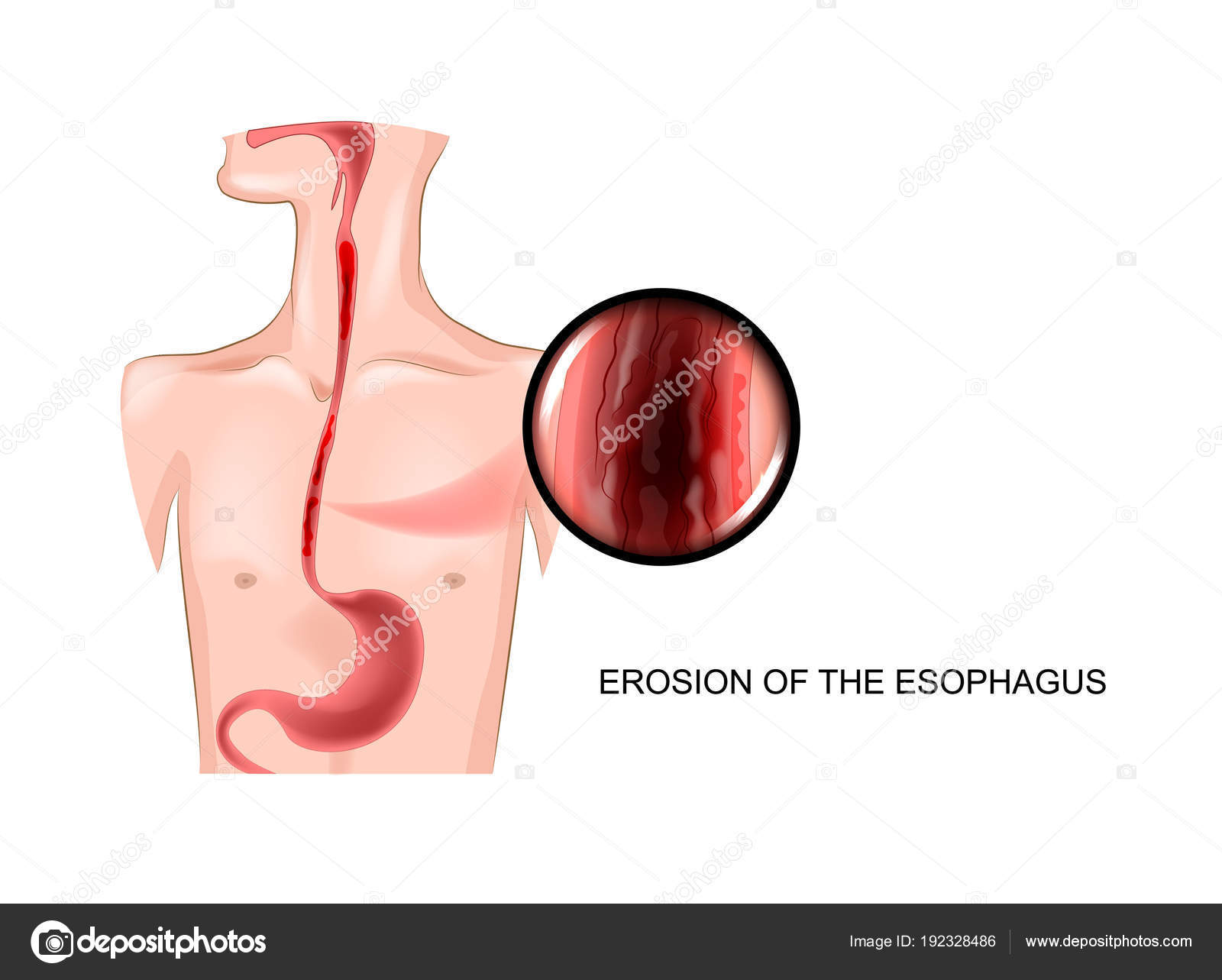 Однако самой распространенной является классификация, предложенная К.J. Paquet (1983) (табл. 3) [6]. От степени варикозного расширения вен пищевода по классификации К.J. Paquet зависит дальнейшая тактика ведения больного. Так, при I и II степени в отсутствие «красных маркеров» рекомендуется постоянный прием неселективных бета-блокаторов и/или карведилола (альфа-1- и бета-блокатор), а также проведение диагностической эзофагогастроскопии 1 раз в 6 месяцев. При III и IV степени помимо консервативной терапии показана эндоскопическая (чаще всего эндоскопическое лигирование варикозного расширения вен пищевода), а в ряде случаев – трансъюгулярное внутрипеченочное шунтирование в связи с высоким риском развития кровотечения.
Любопытным представляется алгоритм по оценке прогноза риска кровотечения на основании индекса, предложенного Североитальянским эндоскопическим клубом (North Italian Endoscopic Club, NIEC) (1988) (табл. 4, 5).
Существует несколько методов (терапевтический, эндоскопический, хирургический) остановки кровотечения, каждый из которых имеет свои показания и точки приложения (табл.
Однако самой распространенной является классификация, предложенная К.J. Paquet (1983) (табл. 3) [6]. От степени варикозного расширения вен пищевода по классификации К.J. Paquet зависит дальнейшая тактика ведения больного. Так, при I и II степени в отсутствие «красных маркеров» рекомендуется постоянный прием неселективных бета-блокаторов и/или карведилола (альфа-1- и бета-блокатор), а также проведение диагностической эзофагогастроскопии 1 раз в 6 месяцев. При III и IV степени помимо консервативной терапии показана эндоскопическая (чаще всего эндоскопическое лигирование варикозного расширения вен пищевода), а в ряде случаев – трансъюгулярное внутрипеченочное шунтирование в связи с высоким риском развития кровотечения.
Любопытным представляется алгоритм по оценке прогноза риска кровотечения на основании индекса, предложенного Североитальянским эндоскопическим клубом (North Italian Endoscopic Club, NIEC) (1988) (табл. 4, 5).
Существует несколько методов (терапевтический, эндоскопический, хирургический) остановки кровотечения, каждый из которых имеет свои показания и точки приложения (табл. 6).
В одном из последних консенсусов по портальной гипертензии (2010) представлены основные подходы к диагностике, прогнозированию исходов, лечебно-профилактическим мероприятиям (терапевтические, эндоскопичекие, хирургические) [7]. За последние несколько лет указанные стандарты претерпели некоторые изменения, ряд положений получил подтверждение с позиции доказательной медицины (рис. 1).
6).
В одном из последних консенсусов по портальной гипертензии (2010) представлены основные подходы к диагностике, прогнозированию исходов, лечебно-профилактическим мероприятиям (терапевтические, эндоскопичекие, хирургические) [7]. За последние несколько лет указанные стандарты претерпели некоторые изменения, ряд положений получил подтверждение с позиции доказательной медицины (рис. 1).В настоящее время оказание помощи больным циррозом печени при остром кровотечении из варикозно-расширенных вен пищевода необходимо начинать с назначения вазоактивных препаратов. Препаратом выбора является терлипрессин (Реместип, Ферринг).
 Накоплена достаточная доказательная база применения терлипрессина при развитии острого кровотечения из варикозно-расширенных вен пищевода у больных циррозом печени. Терлипрессин в таких случаях не только быстро останавливает кровотечение, но и, что более важно, снижает смертность. Так, было показано, что уже через 5 минут после внутривенного струйного введения 2 мг терлипрессина достоверно (на 30%) снижаются градиент венозного давления в печени (hepatic venous pressure gradient, HVPG) и кровоток в воротной вене (portal venous flow, PVF). При этом указанный эффект терлипрессина сохраняется длительно в отличие от такового октреотида, который снижает HVPG уже через 1 минуту на 45% [8], однако через 5 минут показатели HVPG практически возвращаются к исходным значениям (рис. 2).
Кроме того, в плацебоконтролируемых исследованиях было показано, что применение терлипрессина позволяет остановить кровотечение при варикозном расширении вен пищевода в течение 12 часов у 70% больных циррозом печени.
Накоплена достаточная доказательная база применения терлипрессина при развитии острого кровотечения из варикозно-расширенных вен пищевода у больных циррозом печени. Терлипрессин в таких случаях не только быстро останавливает кровотечение, но и, что более важно, снижает смертность. Так, было показано, что уже через 5 минут после внутривенного струйного введения 2 мг терлипрессина достоверно (на 30%) снижаются градиент венозного давления в печени (hepatic venous pressure gradient, HVPG) и кровоток в воротной вене (portal venous flow, PVF). При этом указанный эффект терлипрессина сохраняется длительно в отличие от такового октреотида, который снижает HVPG уже через 1 минуту на 45% [8], однако через 5 минут показатели HVPG практически возвращаются к исходным значениям (рис. 2).
Кроме того, в плацебоконтролируемых исследованиях было показано, что применение терлипрессина позволяет остановить кровотечение при варикозном расширении вен пищевода в течение 12 часов у 70% больных циррозом печени. Коэффициент выживаемости через 1 месяц после острого кровотечения при варикозном расширении вен пищевода по сравнению с группой плацебо был достоверно выше – 90 и 62% соответственно [9]. Наряду с назначением вазоактивных препаратов с первых дней рекомендуется проводить антибактериальную терапию для профилактики портосистемной энцефалопатии.
Следующий этап медицинской помощи, который часто совпадает с поступлением пациента в стационар, – эндоскопическое исследование. Во время данного исследования не только делается общее заключение (например, состояние после кровотечения при варикозном расширении вен пищевода, картина состоявшегося кровотечения из язвы желудка и т.д.), но и, что имеет значение для определения последующей тактики лечения, уточняется степень варикозного расширения вен пищевода. Если есть возможность, выполняется эндолигирование варикозного расширения вен пищевода. Далее следует динамическое наблюдение, лабораторно-инструментальное обследование, в ходе которого оцениваются предикторы неблагоприятного прогноза контроля за кровотечением из варикозно-расширенных вен пищевода: степень тяжести цирроза печени (класс по Чайлду – Пью), количество баллов по шкале MELD, при возможности определяется HVPG (табл.
Коэффициент выживаемости через 1 месяц после острого кровотечения при варикозном расширении вен пищевода по сравнению с группой плацебо был достоверно выше – 90 и 62% соответственно [9]. Наряду с назначением вазоактивных препаратов с первых дней рекомендуется проводить антибактериальную терапию для профилактики портосистемной энцефалопатии.
Следующий этап медицинской помощи, который часто совпадает с поступлением пациента в стационар, – эндоскопическое исследование. Во время данного исследования не только делается общее заключение (например, состояние после кровотечения при варикозном расширении вен пищевода, картина состоявшегося кровотечения из язвы желудка и т.д.), но и, что имеет значение для определения последующей тактики лечения, уточняется степень варикозного расширения вен пищевода. Если есть возможность, выполняется эндолигирование варикозного расширения вен пищевода. Далее следует динамическое наблюдение, лабораторно-инструментальное обследование, в ходе которого оцениваются предикторы неблагоприятного прогноза контроля за кровотечением из варикозно-расширенных вен пищевода: степень тяжести цирроза печени (класс по Чайлду – Пью), количество баллов по шкале MELD, при возможности определяется HVPG (табл. 7).
7).Факторами, приводящими к развитию кровотечения из варикозно-расширенных вен пищевода у больных циррозом печени, являются:
- градиент давления между давлением в воротной и давлением в печеночных венах: минимальный уровень, при котором возможно кровотечение, составляет 12 мм рт. ст.;
- размеры варикозного узла: чем они больше, тем выше риск кровотечения;
- наличие деструкции сосудистой стенки варикозно-расширенного венозного ствола и/или расширение интра- и субэпителиальных вен («красные маркеры»).
 В последние годы получена доказательная база достоверно лучшего прогноза выживаемости при проведении трансъюгулярного внутрипеченочного шунтирования в комбинации с эндолигированием варикозно-расширенных вен пищевода в ранние сроки по сравнению с эндолигированием и консервативной терапией – 86 и 50% соответственно. Гепаторенальный синдром
Еще одним грозным осложнением цирроза печени, которое может приводить к летальному исходу, является гепаторенальный синдром. Что касается темпов и распространенности гепаторенального синдрома, он развивается примерно в 18 и 39% случаев в течение 1 года и 5 лет после выявления асцита у больного циррозом печени. Кроме того, смертность больных с гепаторенальным синдромом через 12 дней достигает 50%, а через 3 месяца – почти 90%. Средняя продолжительность жизни после диагностики составляет несколько недель.
По своей сути гепаторенальный синдром – это острая почечная недостаточность преренального типа, вызванная выраженной почечной вазоконстрикцией у больных c хроническими заболеваниями печени, тяжелой печеночной недостаточностью и портальной гипертензией.
В последние годы получена доказательная база достоверно лучшего прогноза выживаемости при проведении трансъюгулярного внутрипеченочного шунтирования в комбинации с эндолигированием варикозно-расширенных вен пищевода в ранние сроки по сравнению с эндолигированием и консервативной терапией – 86 и 50% соответственно. Гепаторенальный синдром
Еще одним грозным осложнением цирроза печени, которое может приводить к летальному исходу, является гепаторенальный синдром. Что касается темпов и распространенности гепаторенального синдрома, он развивается примерно в 18 и 39% случаев в течение 1 года и 5 лет после выявления асцита у больного циррозом печени. Кроме того, смертность больных с гепаторенальным синдромом через 12 дней достигает 50%, а через 3 месяца – почти 90%. Средняя продолжительность жизни после диагностики составляет несколько недель.
По своей сути гепаторенальный синдром – это острая почечная недостаточность преренального типа, вызванная выраженной почечной вазоконстрикцией у больных c хроническими заболеваниями печени, тяжелой печеночной недостаточностью и портальной гипертензией.
В настоящее время подходы к ведению пациентов с гепаторенальным синдромом 1-го типа отработаны, что нашло отражение в рекомендациях Европейской ассоциации по изучению заболеваний печени (European Association for the Study of the Liver, EASL) 2010 г. [10]. Перечислим основные положения при лечении пациентов с гепаторенальным синдромом 1-го типа.
- Отмена диуретиков (уровень доказательности А1).
- Применение бета-блокаторов. В настоящее время нет убедительных данных о преимуществах как в случае продолжения применения препаратов указанной группы для профилактики кровотечения из варикозно-расширенных вен пищевода, так и при их отмене (уровень доказательности С1).
- Применение объемного парацентеза. Целесообразно только при напряженном асците для снижения дискомфорта (уровень доказательности В1).
- Медикаментозная терапия. Терлипрессин в комбинации с альбумином следует считать препаратами первой линии.
 Альтернативное направление – назначение комбинации октреотида и норадреналина (или мидодрина).
Альтернативное направление – назначение комбинации октреотида и норадреналина (или мидодрина). - Трансъюгулярное внутрипеченочное шунтирование. Данные по применению трансъюгулярного внутрипеченочного шунтирования ограниченны из-за частых противопоказаний у больных циррозом печени и гепаторенальным синдромом. При этом представлены данные об эффективности по улучшению функции почек и контроля за асцитом при гепаторенальном синдроме 2-го типа.
- Заместительная терапия. При гепаторенальном синдроме 1-го типа могут использоваться гемодиализ или продленная гемофильтрация. Однако до настоящего времени не представлено данных о сравнительной эффективности медикаментозных и заместительных методов лечения.
- Трансплантация печени. Считается методом выбора при гепаторенальном синдроме 1-го и 2-го типа (выживаемость составляет примерно 65%).
 Так, в 2013 г. был опубликован метаанализ, включавший 8 исследований (n = 377) влияния терлипрессина на выживаемость при гепаторенальном синдроме [11]. Было показано, что применение терлипрессина достоверно снижает летальность у пациентов с гепаторенальным синдромом на 15%, а в долгосрочном периоде (в течение 3 месяцев) – на 9%. Кроме того, длительное использование низких доз терлипрессина (менее 4 мг/сут) в комбинации с альбумином приводит к увеличению показателя выживаемости у таких пациентов.
Так, в 2013 г. был опубликован метаанализ, включавший 8 исследований (n = 377) влияния терлипрессина на выживаемость при гепаторенальном синдроме [11]. Было показано, что применение терлипрессина достоверно снижает летальность у пациентов с гепаторенальным синдромом на 15%, а в долгосрочном периоде (в течение 3 месяцев) – на 9%. Кроме того, длительное использование низких доз терлипрессина (менее 4 мг/сут) в комбинации с альбумином приводит к увеличению показателя выживаемости у таких пациентов. Терлипрессин рекомендуется назначать в дозе 1–2 мг (каждые 4–6 часов) внутривенно струйно. При этом лечение должно продолжаться до тех пор, пока не нормализуется уровень креатинина в плазме (менее 130 мкмоль/л), на что в среднем требуется 10 дней. Если креатинин не снижается более чем на 25% в течение 3 дней, введение терлипрессина прекращается. Терлипрессин противопоказан при ишемической болезни сердца. Необходимо следить за состоянием пациентов, получающих терлипрессин, на предмет развития аритмий или признаков ишемии внутренних органов.
 Рецидивы гепаторенального синдрома 1-го типа после отмены терлипрессина достаточно редки, в то же время его повторное назначение является эффективным (уровень доказательности А1).
При изучении эффектов терлипрессина при гепаторенальном синдроме 1-го типа P. Solanki и соавт. (2003) показали, что в группе с терлипрессином частота разрешения гепаторенального синдрома 1-го типа была достоверно выше по сравнению с плацебо и составила 42 и 0% соответственно (p
Большой интерес представляет использование терлипрессина в комбинации с альбумином. Как было показано в работе J. Uris и соавт. (2000), комбинированное применение терлипрессина и альбумина в течение 9 суток при гепаторенальном синдроме 1-го типа улучшает почечную функцию (достоверно снижает уровень креатинина сыворотки крови в 3 раза, р
Недавнее проспективное исследование с участием 18 больных с гепаторенальным синдромом подтвердило эффективность применения терлипрессина в сочетании с альбумином у больных декомпенсированным циррозом печени, гепаторенальным синдромом и сепсисом [14].
Рецидивы гепаторенального синдрома 1-го типа после отмены терлипрессина достаточно редки, в то же время его повторное назначение является эффективным (уровень доказательности А1).
При изучении эффектов терлипрессина при гепаторенальном синдроме 1-го типа P. Solanki и соавт. (2003) показали, что в группе с терлипрессином частота разрешения гепаторенального синдрома 1-го типа была достоверно выше по сравнению с плацебо и составила 42 и 0% соответственно (p
Большой интерес представляет использование терлипрессина в комбинации с альбумином. Как было показано в работе J. Uris и соавт. (2000), комбинированное применение терлипрессина и альбумина в течение 9 суток при гепаторенальном синдроме 1-го типа улучшает почечную функцию (достоверно снижает уровень креатинина сыворотки крови в 3 раза, р
Недавнее проспективное исследование с участием 18 больных с гепаторенальным синдромом подтвердило эффективность применения терлипрессина в сочетании с альбумином у больных декомпенсированным циррозом печени, гепаторенальным синдромом и сепсисом [14].
Бактериальные инфекции
Этиология и клинические проявления спонтанного бактериального перитонита Спонтанный бактериальный перитонит – тяжелое полиэтиологическое осложнение декомпенсированного цирроза печени, развивающееся в результате транслокации кишечной флоры на фоне избыточного бактериального роста, сопровождающееся воспалением брюшины, контаминацией асцитической жидкости, синдромом системной воспалительной реакции с последующим развитием сепсиса и полиорганной недостаточности [15]. Основным патогенетическим механизмом спонтанного бактериального перитонита считается транслокация бактерий из просвета кишечника в регионарные лимфоузлы, лимфу и кровоток. Кроме того, в развитии спонтанного бактериального перитонита большую роль играют такие факторы, как портальная и внутрибрюшная гипертензия, избыточный бактериальный рост в просвете тонкой кишки, повышение проницаемости кишечной стенки, замедление кишечного транзита, снижение местного иммунного ответа, нарушение фагоцитарной активности ретикуло-эндотелиальной системы печени и снижение защитных свойств асцитической жидкости. Спонтанный бактериальный перитонит характеризуется высокой смертностью, поздней выявляемостью и остается до настоящего времени часто встречающимся, но редко диагностируемым осложнением цирроза печени [16]. Клиническая картина спонтанного бактериального перитонита, как правило, смазана. Основными симптомами являются разлитая абдоминальная боль различной интенсивности, лихорадка, рвота, диарея, признаки пареза кишечника, в ряде случаев отмечают быстро нарастающую печеночную энцефалопатию и гепаторенальный синдром.
Спонтанный бактериальный перитонит характеризуется высокой смертностью, поздней выявляемостью и остается до настоящего времени часто встречающимся, но редко диагностируемым осложнением цирроза печени [16]. Клиническая картина спонтанного бактериального перитонита, как правило, смазана. Основными симптомами являются разлитая абдоминальная боль различной интенсивности, лихорадка, рвота, диарея, признаки пареза кишечника, в ряде случаев отмечают быстро нарастающую печеночную энцефалопатию и гепаторенальный синдром.У многих больных заболевание проявляется синдромом системной воспалительной реакции, который диагностируется при наличии по крайней мере 2 из 4 клинико-лабораторных параметров:
- температура > 38 ºC или
- частота сердечных сокращений > 90 уд/мин;
- частота дыхательных движений > 20 дыхательных движений в минуту или РаСО2
- лейкоциты периферической крови > 12 × 109/л или 10 [10, 15, 16].

Разработаны диагностические критерии, включение которых в алгоритм обследования позволяет значительно чаще выявлять спонтанный бактериальный перитонит (табл. 8). Частота выявления спонтанного бактериального перитонита с помощью данных критериев составила 21% по сравнению с 10%, когда учитывались только классические признаки проявления спонтанного бактериального перитонита [12, 17].
Антибиотикотерапия В соответствии с рекомендациями Международного клуба по изучению асцита (International Ascetic Club, IAC) 2000 г. до получения результатов посева асцитической жидкости всем больным при превышении числа нейтрофилов более 250 кл/мм3 рекомендуется проводить эмпирическую антибактериальную терапию [17]. С этой целью используются цефалоспорины III–IV поколения (цефотаксим, цефтриаксон, цефтазидим, цефоперазон, цефоперазон/сульбактам, цефепим) [16]. Цефотаксим, наиболее изученный и часто применяемый препарат из этой группы, назначается каждые 12 часов в течение 5 дней внутривенно, минимальная разовая доза – 2 г [18]. В настоящее время выбор антимикробных препаратов первой линии терапии – процесс сложный и неоднозначный. Это связано с ростом резистентности микроорганизмов к антибиотикам, продолжительностью жизни тяжелых больных. Итальянские ученые во главе с S. Angeloni провели ряд исследований эффективности схем терапии спонтанного бактериального перитонита, рекомендованных IAC. Лечение цефотаксимом 32 больных с классическими проявлениями спонтанного бактериального перитонита было успешным в 59% случаев. Остальным пациентам пришлось через 48 часов сменить антибиотик, что привело к разрешению инфекции в 87% случаев. Анализируя эффективность цефотаксима в группе больных спонтанным бактериальным перитонитом, в которой удалось получить рост бактериальной культуры, авторы получили хороший результат только в 44% случаев. Такую низкую эффективность авторы связывают с резистентностью микроорганизмов к данному антибиотику. Учеными был сделан вывод о необходимости поиска и других антибиотиков первой линии в лечении спонтанного бактериального перитонита [19].
В настоящее время выбор антимикробных препаратов первой линии терапии – процесс сложный и неоднозначный. Это связано с ростом резистентности микроорганизмов к антибиотикам, продолжительностью жизни тяжелых больных. Итальянские ученые во главе с S. Angeloni провели ряд исследований эффективности схем терапии спонтанного бактериального перитонита, рекомендованных IAC. Лечение цефотаксимом 32 больных с классическими проявлениями спонтанного бактериального перитонита было успешным в 59% случаев. Остальным пациентам пришлось через 48 часов сменить антибиотик, что привело к разрешению инфекции в 87% случаев. Анализируя эффективность цефотаксима в группе больных спонтанным бактериальным перитонитом, в которой удалось получить рост бактериальной культуры, авторы получили хороший результат только в 44% случаев. Такую низкую эффективность авторы связывают с резистентностью микроорганизмов к данному антибиотику. Учеными был сделан вывод о необходимости поиска и других антибиотиков первой линии в лечении спонтанного бактериального перитонита [19]. Больным неосложненным спонтанным бактериальным перитонитом (при отсутствии шока, гастроинтестинального кровотечения, выраженной печеночной энцефалопатии или повышении сывороточного креатинина), не получавшим ранее профилактически фторхинолоны, может быть рекомендован офлоксацин внутрь в дозе не менее 400 мг каждые 12 часов. По мнению турецких исследователей Измирского университета, внутривенное введение в течение 2 дней каждые 12 часов по 200 мг офлоксацина с последующим переходом на пероральный прием по 200 мг 2 раза в сутки в течение еще 5 дней эффективнее внутривенного введения цефотаксима по 1,0 г каждые 12 часов в течение 7 дней [18]. I. Tuncer и соавт. считают, что ципрофлоксацин по 500 мг каждые 12 часов перорально не уступает цефотаксиму и цефтриксону и даже превосходит их по эффективности в лечении спонтанного бактериального перитонита [20, 21]. Аминогликозиды при спонтанном бактериальном перитоните применять не рекомендуется в связи с более низкой эффективностью и высокой нефротоксичностью [17].
Больным неосложненным спонтанным бактериальным перитонитом (при отсутствии шока, гастроинтестинального кровотечения, выраженной печеночной энцефалопатии или повышении сывороточного креатинина), не получавшим ранее профилактически фторхинолоны, может быть рекомендован офлоксацин внутрь в дозе не менее 400 мг каждые 12 часов. По мнению турецких исследователей Измирского университета, внутривенное введение в течение 2 дней каждые 12 часов по 200 мг офлоксацина с последующим переходом на пероральный прием по 200 мг 2 раза в сутки в течение еще 5 дней эффективнее внутривенного введения цефотаксима по 1,0 г каждые 12 часов в течение 7 дней [18]. I. Tuncer и соавт. считают, что ципрофлоксацин по 500 мг каждые 12 часов перорально не уступает цефотаксиму и цефтриксону и даже превосходит их по эффективности в лечении спонтанного бактериального перитонита [20, 21]. Аминогликозиды при спонтанном бактериальном перитоните применять не рекомендуется в связи с более низкой эффективностью и высокой нефротоксичностью [17]. В соответствии с рекомендациями IAC эффективность проведения адекватной антибактериальной терапии достигает 90% и оценивается по снижению содержания нейтрофилов в асцитической жидкости менее 250 клеток/мл, исчезновению местных и системных проявлений инфекции. Оптимальным критерием эффективности считается снижение числа нейтрофилов в асцитической жидкости через двое суток от начала антибактериальной терапии по сравнению с исходными показателями [17]. В этой связи в ходе терапии рекомендуется проводить хотя бы один повторный парацентез через 48 часов от начала терапии.
В соответствии с рекомендациями IAC эффективность проведения адекватной антибактериальной терапии достигает 90% и оценивается по снижению содержания нейтрофилов в асцитической жидкости менее 250 клеток/мл, исчезновению местных и системных проявлений инфекции. Оптимальным критерием эффективности считается снижение числа нейтрофилов в асцитической жидкости через двое суток от начала антибактериальной терапии по сравнению с исходными показателями [17]. В этой связи в ходе терапии рекомендуется проводить хотя бы один повторный парацентез через 48 часов от начала терапии.Критериями неэффективности считается ухудшение состояния в течение первых часов антибактериальной терапии, а также снижение числа нейтрофилов в асцитической жидкости менее чем на 25%. При отсутствии результата рекомендуется смена антибиотика с учетом чувствительности микрофлоры или эмпирически.
Применение альбуминаПарацентез с возмещением объема плазмы альбумином часто применяется при лечении рефрактерных асцитов. Эффективность и безопасность этой методики у пациентов со спонтанным бактериальным перитонитом остаются спорными. C.H. Choi и соавт. (2005) провели исследование эффективности внутривенного введения альбумина больным со спонтанным бактериальным перитонитом, развившимся на фоне цирроза печени. Когорта из 42 больных была рандомизирована на 2 группы: пациенты 1-й группы (n = 21) получали стандартную терапию, 2-й группы (n = 21) – альбумин и диуретики. Кроме того, всем пациентам была назначена стандартная терапия с использованием антибактериальных средств. Общие показатели выживаемости были низкими и составили 42,5 и 22,5% через 6 месяцев и 12 месяцев после лечения соответственно. Авторы отметили, что обе схемы продемонстрировали одинаковую эффективность в лечении спонтанного бактериального перитонита. Тем не менее исследователи считают целесообразным применение большеобъемного парацентеза с замещающей внутривенной инфузией альбумина в комплексной терапии напряженного или рефрактерного асцита и общепринятой терапии асцита у пациентов с циррозом печени и спонтанным бактериальным перитонитом [18–22].
Эффективность и безопасность этой методики у пациентов со спонтанным бактериальным перитонитом остаются спорными. C.H. Choi и соавт. (2005) провели исследование эффективности внутривенного введения альбумина больным со спонтанным бактериальным перитонитом, развившимся на фоне цирроза печени. Когорта из 42 больных была рандомизирована на 2 группы: пациенты 1-й группы (n = 21) получали стандартную терапию, 2-й группы (n = 21) – альбумин и диуретики. Кроме того, всем пациентам была назначена стандартная терапия с использованием антибактериальных средств. Общие показатели выживаемости были низкими и составили 42,5 и 22,5% через 6 месяцев и 12 месяцев после лечения соответственно. Авторы отметили, что обе схемы продемонстрировали одинаковую эффективность в лечении спонтанного бактериального перитонита. Тем не менее исследователи считают целесообразным применение большеобъемного парацентеза с замещающей внутривенной инфузией альбумина в комплексной терапии напряженного или рефрактерного асцита и общепринятой терапии асцита у пациентов с циррозом печени и спонтанным бактериальным перитонитом [18–22]. Рекомендуется проведение коротких курсов бактериальной терапии с последующим переходом на длительный прием пребиотиков (лактулозы).
Рекомендуется проведение коротких курсов бактериальной терапии с последующим переходом на длительный прием пребиотиков (лактулозы).
Методы профилактики
Профилактику спонтанного бактериального перитонита рекомендуется проводить всем больным циррозом печени, осложненным асцитом и высоким риском развития тяжелых бактериальных инфекций, с применением фторхинолонов (норфлоксацин, ципрофлоксацин, офлоксацин) 400 мг внутрь каждые 12 часов в течение не менее 7 дней. В качестве альтернативных схем предлагаются комбинации фторхинолонов (ципрофлоксацин или офлоксацин) в сочетании с амоксициллин/клавулановой кислотой. (Применение невсасывающихся антибиотиков (полусинтетические производные рифамицина – рифаксимин) целесообразно на более ранних этапах до появления резистентного асцита.) В настоящее время фторхинолоны рассматриваются как важная самостоятельная группа химиотерапевтических препаратов в составе класса хинолонов – ингибиторов ДНК-гиразы, которые характеризуются высокой клинической эффективностью, разнообразными показаниями к применению и представляют собой серьезную альтернативу бета-лактамным антибиотикам широкого спектра действия. Основными особенностями фторхинолонов являются высокая биодоступность при приеме внутрь, большой объем распределения, низкое связывание с сывороточными белками, хорошее проникновение в органы, ткани и клетки макроорганизма, длительная циркуляция в организме, элиминация почечными и внепочечными механизмами.
Больные циррозом печени класса В и С по классификации Чайлда – Пью, перенесшие спонтанный бактериальный перитонит в анамнезе, относятся к группе риска повторного развития спонтанного бактериального перитонита. В настоящее время крупные рандомизированные исследования показали высокую эффективность непрерывной антибиотикопрофилактики у больных циррозом печени, перенесших спонтанный бактериальный перитонит. В соответствии с международными рекомендациями профилактика возвратного бактериального перитонита проводится непрерывно препаратами фторхинолонового ряда (норфлоксацин по 400 мг/сут). Появление резистентной микрофлоры в этом случае остается важной проблемой. В связи с низкой выживаемостью после первого эпизода спонтанного перитонита, которая в течение первого года составляет 30–50%, а в течение второго года – всего 25–30%, рекомендуется рассматривать таких пациентов в качестве кандидатов на трансплантацию печени.
Основными особенностями фторхинолонов являются высокая биодоступность при приеме внутрь, большой объем распределения, низкое связывание с сывороточными белками, хорошее проникновение в органы, ткани и клетки макроорганизма, длительная циркуляция в организме, элиминация почечными и внепочечными механизмами.
Больные циррозом печени класса В и С по классификации Чайлда – Пью, перенесшие спонтанный бактериальный перитонит в анамнезе, относятся к группе риска повторного развития спонтанного бактериального перитонита. В настоящее время крупные рандомизированные исследования показали высокую эффективность непрерывной антибиотикопрофилактики у больных циррозом печени, перенесших спонтанный бактериальный перитонит. В соответствии с международными рекомендациями профилактика возвратного бактериального перитонита проводится непрерывно препаратами фторхинолонового ряда (норфлоксацин по 400 мг/сут). Появление резистентной микрофлоры в этом случае остается важной проблемой. В связи с низкой выживаемостью после первого эпизода спонтанного перитонита, которая в течение первого года составляет 30–50%, а в течение второго года – всего 25–30%, рекомендуется рассматривать таких пациентов в качестве кандидатов на трансплантацию печени. Рандомизированные исследования эффективности норфлоксацина, проведенные J. Fernández и соавт., подтвердили его эффективность для профилактики спонтанного бактериального перитонита [23].
Рандомизированные исследования эффективности норфлоксацина, проведенные J. Fernández и соавт., подтвердили его эффективность для профилактики спонтанного бактериального перитонита [23]. Исследование особенностей течения спонтанного бактериального перитонита, анализ множества разрозненных трудов по этому заболеванию, а также литературы по проблемам синдрома системной воспалительной реакции, синдрома полиорганной недостаточности, разрабатываемым иммунологами и специалистами по сепсисологии, позволяют:
- определить тесную взаимосвязь между спонтанным бактериальным перитонитом, синдромом системной воспалительной реакции, синдромом полиорганной недостаточности и сепсисом;
- рассматривать спонтанный бактериальный перитонит как один из этапов в эволюции сложного инфекционного процесса, вызванного, как правило, индигенной флорой и развивающегося у больных с декомпенсированным циррозом печени. Итогом этого процесса может стать сепсис, полиорганная недостаточность и гибель больного.

Все это подтверждает необходимость своевременной профилактики и лечения осложнений цирроза печени.
КРОВОТЕЧЕНИЕ ИЗ ВАРИКОЗНО-РАСШИРЕННЫХ ВЕН ПИЩЕВОДА ПРИ ЦИРРОЗЕ ПЕЧЕНИ | ХУРУМ
1. Авдеева М. Г., Городин В. Н., Редько Е. Н., Стриханов С. Н., Моренец Т. М. Вирусные гепетиты: стратегия и тактика терапии, организация медицинской помощи, пособие для врачей. – Краснодар, 2009. – 262с.
2. Авдеева М. Г., Кулбужева М. И., Хурум З. Ю., Маслова Е. А., Кириченко Р. Р., Эзугбая Б. С. Анализ летальных случаев больных с циррозом печени вследствие кровотечения из вен пищевода// Актуальные вопросы инфекционной патологии юга России. Материалы X Научно–практической конференции ЮФО с международным участием. – Краснодар, 2015. – С. 11–14.
3. Анисимов А. Ю., Богуславский В. А., Кузнецов М. В. Диагностическая и лечебная тактика при кровотечениях из варикозно-расширенных вен пищевода и желудка у больных циррозом печени // Казанский медицинский журнал. – 2008. – Т. 89. – № 3. – С. 335–340.
Анисимов А. Ю., Богуславский В. А., Кузнецов М. В. Диагностическая и лечебная тактика при кровотечениях из варикозно-расширенных вен пищевода и желудка у больных циррозом печени // Казанский медицинский журнал. – 2008. – Т. 89. – № 3. – С. 335–340.
4. Богомолов П. О., Буеверов А. О., Мациевич М. В., Петраченкова М. Ю., Коблов С. В., Кокина К. Ю. Возможности этиотропной терапии вирусного цирроза печени // Инфекционные болезни. – 2014. – Т.12. – № 4. – С. 75-83.
5. Гарбузенко Д. В. Методы прогнозирования риска и мониторинг эффективности терапии кровотечений из варикозно-расширенных вен пищевода у больных циррозом печени // Гастроэнтерология. Гепатология. – 2010. – № 6. – С. 11–20.
6. Ханевич М. Д., Хрупкин В. И., Жерлов Г. К., Чепур С. В., Кошевой А. П. Кровотечения из хронических гастродуоденальных язв у больных с внутрипеченочной портальной гипертензией. – Новосибирск: Наука, 2003. – 198 с.
Кровотечения из хронических гастродуоденальных язв у больных с внутрипеченочной портальной гипертензией. – Новосибирск: Наука, 2003. – 198 с.
7. Blachir M, Leleu H, Peck-Radosavljevic M, Valla DC, Roudot-Thoraval F. The burden of liver disease in Europa: a review of available epidemioloqical data. J Hepatol. – 2013. – Vol.58(3). – Р. 593–608.
8. Hoert DL, Xu J. Deaths: preliminary data for 2011. Natl Vital Stat Rep. – 2012. – Vol. 61(6). – Р. 1-51.
ПРОФИЛАКТИКА КРОВОТЕЧЕНИЙ ИЗ ВАРИКОЗНО РАСШИРЕННЫХ ВЕН ПИЩЕВОДА ПРИ ЦИРРОЗЕ ПЕЧЕНИ | Заривчацкий
1. Ерамишанцев А. К. Развитие проблемы хирургического лечения кровотечений из варикозно расширенных вен пищевода и желудка. Анналы хирургической гепатологии, 2007, Т.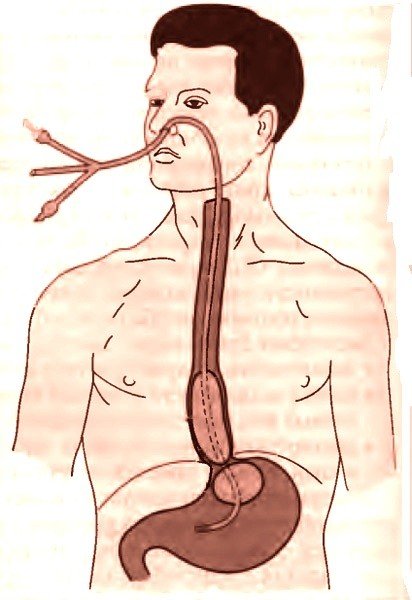 12, № 2, С. 8-15.
12, № 2, С. 8-15.
2. Жигалова С. Б., Мелкумов А. Б., Манукьян В. Г., Шерцингер А. Г. Варикозное расширение вен желудка у больных портальной гипертензией: диагностика и лечение. Анналы хирургической гепатологии, 2010, Т. 15, № 3, С. 84-94.
3. Пациора М. Д. Хирургия портальной гипертензии. – М.: Медицина, 1984. – 319 с.
4. Ерамишанцев А. К., Шерцингер А. Г., Киценко Е. А. Портальная гипертензия // Савельев В. С., Кириенко А. И. Клиническая хирургия: национальное руководство. Т. 2 – М.: ГЭОТАР-Медиа, 2008, С. 626-665.
5. Заривчацкий М. Ф., Каменских Е.Д., Мугатаров И. Н. Оценка эффективности применения ремаксола у больных циррозом печени. Хирургия. Журнал им. Н. И. Пирогова, 2013, № 3, С. 79-83.
79-83.
6. Котив Б. Н., Дзидзава И. И., Алентьев С. А. Портокавальное шунтирование в лечении больных циррозом печени с синдромом портальной гипертензии. Анналы хирургической гепатологии, 2008, Т. 13, № 2, С. 76-84.
7. Garcia-Tsao G, Bosch J. Management of varices and variceal hemorrhage in cirrhosis. N. Engl. J. Med., 2010, Vol.362, no.5, pp. 823-832.
8. Мошарова А. А., Верткин А. Л. Лечение и профилактика кровотечения из варикозно расширенных вен пищевода. Неотложная терапия, 2012, № 1-2, С. 12-19.
9. Pomier-Layrargues G., Bouchard L., Lafortune M. et al. The Transjugular Intrahepatic Portosystemic Shunt in the Treatment of Portal Hypertension: Current Status. International J. of Hepatology, 2012, vol.12, no.6, pp. 352-358.
of Hepatology, 2012, vol.12, no.6, pp. 352-358.
10. Gluud L., Klingenberg S., Nikolova D., Gluud C. Banding ligation versus b-blockers as primary prophylaxis in esophageal varices: systematic review of randomized trials. Am. J. Gastroenterol., 2007, vol.102, no.7, pp. 2842-2848.
11. Gonzalez R., Zamora J., Gomez-Camarero J. et al. Meta-analysis: Combination endoscopic and drug therapy to prevent variceal rebleeding in cirrhosis. Ann. Intern. Med., 2008, vol.149, no.8, pp.109-122.
12. Шерлок Ш., Дули Дж. Заболевания печени и желчных путей. – М.: ГЭОТАР Медицина, 1999, 864 с.
13. Bosch J., Abraldes J. G., Berzigotti A., Garcia-Pagan J. C. Portal hypertension and gastrointestinal bleeding. Semin. Liver Dis., 2008, vol.28, no.5, pp.3-25.
Semin. Liver Dis., 2008, vol.28, no.5, pp.3-25.
14. De Franchis R. Revising consensus in portal hypertension: report of the Baveno V consensus workshop on methodology of diagnosis and therapy in portal hypertension. J. Hepatol., 2010, vol.53, pp.762-768.
15. Даян З. А., Хохлов А. В. Эндовидеохирургические методы лечения синдрома портальной гипертензии. Вестник хирургии им. И. И. Грекова, 2008, Т. 167, № 2, С. 67-71.
16. Ware J. E., Kosinski M., Keller S. K. Sf-36 Health Survey. Manuel and Interpretation Guide. Lincoln, RI: QualityMetric Incorporated, 2000, 150 р.
ХИРУРГИЧЕСКИЕ МЕТОДЫ ПРОФИЛАКТИКИ КРОВОТЕЧЕНИЙ ИЗ ВАРИКОЗНО-РАСШИРЕННЫХ ВЕН ПИЩЕВОДА У БОЛЬНЫХ С ЦИРРОЗОМ ПЕЧЕНИ | Заривчацкий
1. Гранов Д. А. Трансплантация печени при гепатоцеллюлярном раке // Практ. онкол. 2008. № 4. С. 237-240.
Гранов Д. А. Трансплантация печени при гепатоцеллюлярном раке // Практ. онкол. 2008. № 4. С. 237-240.
2. Ерамишанцев А. К., Шерцингер А. Г., Киценко Е. А. Портальная гипертензия // Клиническая хирургия: национальное руководство / Под ред. В. С. Савельева, А. И. Кириенко. М.: ГЭОТАР-Медиа, 2009. Т. II. С. 626-666.
3. Жигалова С. Б., Мелкумов А. Б., Манукьян В. Г., Шерцингер А. Г. Варикозное расширение вен желудка у больных портальной гипертензией: диагностика и лечение // Анн. хир. гепатол. 2010. № 3. С. 84-94.
4. Котив Б. Н., Дзидзава И. И., Солдатов С. А., Кашкин Д. П. и др. Результаты селективного и парциального портокавального шунтирования и прогностические факторы долгосрочной выживаемости больных циррозом печени // Анн. хир. гепатол. 2015. № 2. С. 46-58.
46-58.
5. Назыров Ф. Г., Девятов А. В., Бабаджанов А. Х. Результаты и перспективы портосистемного шунтирования у больных циррозом печени // Анн. хир. гепатол. 2015. № 2. С. 31-39.
6. Павлов А. И., Хазанов А. И., Плюснин С. В., Игонин В. А. и др. Этиология предраковых заболеваний печени у больных с гепатоцеллюлярной карциномой и некоторое расширение группы риска // Росс. журн. гастроэнтерол., гепатол., колопроктол. 2008. № 6. С. 51-56.
7. Руководство по хирургии печени и желчевыводящих путей / Под ред. А. Е. Борисова. СПб.: Скифия, 2003. Т. 1. 488 с.
8. Шерцингер А. Г., Жигалова С. Б., Семенова Т. С., Мартиросян Р. А. Роль эндоскопии в выборе лечения больных портальной гипертензией // Анн. хир. гепатол. 2015. № 2. С. 20-30.
хир. гепатол. 2015. № 2. С. 20-30.
9. Bosch J. Prevention of variceal rebleeding: endoscopes, drugs, and more // Hepatology. 2000. Vol. 32. P. 660-662.
10. Helmy A., Salama I. A., Schwaitzberg S. D. Laparoscopic esophago gastric devascularization in bleeding varices // Surg. Endosc. 2003. Vol. 17. P. 1614-1619.
11. Ware J. E. Sf-36 Health Survey: Manuel and interpretation guide. Lincoln, RI: Quality Metric Incorporated, 2000. P. 150.
Опыт лечения больных циррозом печени с кровотечениями из варикозно расширенных вен пищевода и желудка Текст научной статьи по специальности «Клиническая медицина»
БМЕН ОПЫТОМ
© С. Б. Сангаджиев, А.Ф. Якупов, РР Мустафин, А.Ю. Анисимов, 2013 УДК 616.36-004.7-089:616.329/.33-005.1
Б. Сангаджиев, А.Ф. Якупов, РР Мустафин, А.Ю. Анисимов, 2013 УДК 616.36-004.7-089:616.329/.33-005.1
Опыт ЛЕЧЕНИЯ БОЛЬНЫХ ЦИРРОЗОМ ПЕЧЕНИ С КРОВОТЕЧЕНИЯМИ ИЗ ВАРИКОЗНО РАСШИРЕННЫХ ВЕН ПИЩЕВОДА И ЖЕЛУДКА
САвр Борисович сангаджиев, канд. мед. наук, врач-хирург отделения хирургии ГАУЗ «Межрегиональный клинико-диагностический центр» Министерства здравоохранения Республики Татарстан, Казань, Россия тел. 8-927-404-40-30, e-mail: [email protected]
АСкАр ФАйрузовиЧ Якупов, канд. мед. наук, врач-хирург отделения хирургии ГАУЗ «Межрегиональный клинико-диагностический центр» Министерства здравоохранения Республики Татарстан, Казань, Россия тел. 8-927-037-28-82, e-mail: [email protected]
раиС роБЕртовиЧ Мустафин, канд. мед. наук, зав. приемным отделением ГАУЗ «Городская клиническая больница № 7» г. Казани, ассистент кафедры скорой медицинской помощи ГБОУ ДПО «Казанская государственная медицинская академия» Минздрава России, тел. 8-927-240-93-02, e-mail: [email protected] Андрей Юрьевич Анисимов, докт. мед. наук, профессор кафедры скорой медицинской помощи ГБОУ ДПО «Казанская государственная медицинская академия» Минздрава России, главный внештатный специалист-хирург Министерства здравоохранения Республики Татарстан, зам. главного врача по медицинской части ГАУЗ «Городская клиническая больница № 7» г. Казани, e-mail: [email protected]
Казани, ассистент кафедры скорой медицинской помощи ГБОУ ДПО «Казанская государственная медицинская академия» Минздрава России, тел. 8-927-240-93-02, e-mail: [email protected] Андрей Юрьевич Анисимов, докт. мед. наук, профессор кафедры скорой медицинской помощи ГБОУ ДПО «Казанская государственная медицинская академия» Минздрава России, главный внештатный специалист-хирург Министерства здравоохранения Республики Татарстан, зам. главного врача по медицинской части ГАУЗ «Городская клиническая больница № 7» г. Казани, e-mail: [email protected]
Реферат. В основу работы положен анализ результатов лечения 105 больных циррозом печени с синдромом внутрипеченочной портальной гипертензии за период с 1999 по 2012 г В 1-ю группу (сравнения) вошли 77 больных с циррозом печени (ЦП), осложненным кровотечением из варикозно расширенных вен пищевода и желудка (ВРВПЖ), лечебная программа которых предусматривала выжидательную консервативную тактику с использованием хирургических методов только в качестве «операции отчаяния». Во 2-ю группу (основная) — 28 больных с ЦП, осложненным кровотечением из ВРВПЖ, комплексная лечебная программа которых предусматривала активную хирургическую тактику с использованием усовершенствованной операции М.Д. Пациора. Местные осложнения, связанные с инфекционным процессом в мягких тканях брюшной стенки, развились у 5 (6,5% наблюдений) больных в группе сравнения и у 1 (3,6% наблюдений) в основной группе.У 35 (46,7% наблюдений) пациентов группы сравнения и 2 (7,1% наблюдений) основной было сочетание как местных, так и общих осложнений. Использование предлагаемой активной хирургической тактики позволяет уменьшить общее количество осложнений с 97,4 до 25,0%, частоту развития печеночной недостаточности — с 16,9 до 14,3%, снизить послеоперационную летальность с 100 до 35,7%, госпитальную летальность с 76,6 до 35,7%.
Во 2-ю группу (основная) — 28 больных с ЦП, осложненным кровотечением из ВРВПЖ, комплексная лечебная программа которых предусматривала активную хирургическую тактику с использованием усовершенствованной операции М.Д. Пациора. Местные осложнения, связанные с инфекционным процессом в мягких тканях брюшной стенки, развились у 5 (6,5% наблюдений) больных в группе сравнения и у 1 (3,6% наблюдений) в основной группе.У 35 (46,7% наблюдений) пациентов группы сравнения и 2 (7,1% наблюдений) основной было сочетание как местных, так и общих осложнений. Использование предлагаемой активной хирургической тактики позволяет уменьшить общее количество осложнений с 97,4 до 25,0%, частоту развития печеночной недостаточности — с 16,9 до 14,3%, снизить послеоперационную летальность с 100 до 35,7%, госпитальную летальность с 76,6 до 35,7%.
Ключевые слова: цирроз печени, кровотечение.
EXPERiENOE OF TREATING PATiENTS WiTH LiVER CiRRHOSiS WiTH BLEEDiNG VARiCES ESOPHAGUS AND THE STOMACH
SAvR B. SANCADzHiYEv. the candidate of medical sciences, the doctor the surgeon of office of surgery of GAUZ «Interregional Clinic Diagnostic Center» of Ministry of Health of the Republic of Tatarstan, Kazan,
SANCADzHiYEv. the candidate of medical sciences, the doctor the surgeon of office of surgery of GAUZ «Interregional Clinic Diagnostic Center» of Ministry of Health of the Republic of Tatarstan, Kazan,
8-927-404-40-30, e-mail: [email protected]
ASKAR F. YAKUPOV, the candidate of medical sciences, the doctor the surgeon of office of surgery of GAUZ «Interregional Clinic Diagnostic Center» of Ministry of Health of the Republic of Tatarstan, Kazan,
8-927-037-28-82, e-mail: [email protected]
RAiS R. MUSTAFiN, the candidate of medical sciences, the manager of a reception of GAUZ «City Clinical Hospital № 7»
of Kazan, the assistant to chair of an emergency medical service of GBOU DPO «Kazan State Medical Academy»
of Ministry of Health of the Russian Federation, 8-927-240-93-02, e-mail: rai-mustafin@yandex. ru
ru
ANDREY YU. ANiSiMOV, the doctor of medical sciences, the professor, the chief non-staff specialist the surgeon
of Ministry of Health of the Republic of Tatarstan, the deputy chief physician by medical part of GAUZ «City Clinical Hospital № 7»
of Kazan, the professor of chair of an emergency medical service of GBOU DPO «Kazan State Medical Academy»
of Ministry of Health of the Russian Federation, Kazan, e-mail: [email protected]
Abstract. Group I (comparison) — 77 in patients with liver cirrhosis (LC), complicated by bleeding from esophageal varices and gastric (VRVPZH) treatment program that included a waiting conservative tactics using surgical methods only as the «operation of despair». Group II (basic) — 28 patients with liver cirrhosis complicated by bleeding from VRVPZH, a comprehensive treatment program that included an active surgical approach using an improved operation, MD Patsiora. Using the proposed active surgical approach to reduce the total number of complications from 97,4% to 25,0%, the incidence of liver failure — from 16,9% to 14,3%, lower postoperative mortality from 100% to 35,7%, inhospital mortality from 76,6% to 35,7%.
Using the proposed active surgical approach to reduce the total number of complications from 97,4% to 25,0%, the incidence of liver failure — from 16,9% to 14,3%, lower postoperative mortality from 100% to 35,7%, inhospital mortality from 76,6% to 35,7%.
Key words: cirrhosis of the liver, bleeding.
Введение. Ахиллесовой пятой современной хирургической гепатологии является лечение больных циррозом печени (ЦП) в момент остро возникшего пищеводно-желудочного кровотечения [1, 7, 15].
Затруднение тока крови в системе воротной вены у больных ЦП в 25—35% случаев приводит к кровотечениям из варикозно расширенных вен пищевода и желудка (ВРВПЖ) [11].
В Республике Татарстан с числом населения 3 млн 779,3 тыс. человек удельный вес желудочно-кишечных кровотечений в структуре острых хирургических заболеваний органов брюшной полости составляет 6,8%, уступая лишь острому аппендициту (42,9%), острому холециститу (18,6%), острому панкреатиту (17,1%). Причем 20—25% от числа больных с желудочнокишечным кровотечением составляют пациенты с пищеводно-желудочным кровотечением портального генеза [8].
Причем 20—25% от числа больных с желудочнокишечным кровотечением составляют пациенты с пищеводно-желудочным кровотечением портального генеза [8].
Кровотечения из ВРВПЖ у больных ЦП отличаются особой тяжестью клинических проявлений, серьезными последствиями и высокой вероятностью летального исхода [12]. Риск возникновения кровотечения в первые два года после постановки диагноза составляет 30%. Летальность при первом пищеводно-желудочном кровотечении достигает 50%. Еще более пессимистичным выглядит прогноз для пациентов, перенесших кровотечения из ВРВПЖ в прошлом. В течение первого года у 60% из них возникает рецидив. От него погибает еще 70—80% больных [3].
Оценка тенденции показателя смертности в различных возрастных группах населения Республики Татарстан показала ее выраженный рост у всех пациентов с алкогольным ЦП (от +5,2% в группе от 30 до 39 лет, до +11,14% в группе старше 70 лет).
У пациентов с вирусным ЦП в целом по группе отмечена умеренная тенденция к росту показателя смертности (от +1,5% в группе от 60 до 69 лет до +10,58% в группе от 20 до 29 лет). Однако в наиболее трудоспособных возрастных группах имеет место выраженная тенденция к росту показателя смертности (от +7,2% в группе от 30 до 39 лет и +10,58% в группе от 20 до 29 лет).
Таким образом, кровотечения из ВРВПЖ являются основным, но, как правило, запоздалым показанием к хирургическому лечению синдрома ПГ при ЦП [4, 19].
Данные мировой литературы свидетельствуют о различных подходах к лечению острых кровотечений из ВРВПЖ у больных ЦП. Так, одни авторы отдают предпочтение эндоскопическим методам гемостаза [6, 16], другие — использованию медикаментозных препаратов соматостатина или сандостатина [18], третьи — эндоваскулярной эмболизации варикозных вен желудка [2].
По-прежнему широко используются экстренные оперативные вмешательства, среди которых как различные виды портокавальных анастомозов [10, 20], так и прямые вмешательства на венах эзофагокардиаль-ной области [5, 9, 14, 17].
Таким образом, сегодня абсолютно ясно, что больного ЦП на высоте кровотечения из ВРВПЖ нельзя лечить шаблонно. Однако единой программы лечения подобных больных до сих пор не выработано. Приведенный в отдельных работах алгоритм лечебных действий при кровотечениях из ВРВПЖ дискутабелен
прежде всего в аспекте очередности и объема гемоста-тических пособий. В связи с этим улучшение результатов лечения больных ЦП с острыми кровотечениями из ВРВПЖ, связанное как с дальнейшим совершенствованием методик гемостаза и их рационального сочетания, так и с усовершенствованием лечебной программы в целом, включающей в себя раннее оперативное вмешательство и адекватные меры по коррекции нарушенных функций больного организма, являются исключительно актуальными.
Цель работы — улучшение результатов хирургического лечения больных циррозом печени, осложненным кровотечением из варикозно расширенных вен пищевода и желудка, путем применения новых тактических принципов и современных методов оперативных вмешательств.
Материал и методы. В основу работы положен анализ результатов лечения 105 больных ЦП с синдромом внутрипеченочной ПГ за период с 1999 по 2012 г.
Первую исследуемую клиническую группу сравнения составили 77 больных с ЦП, осложненным кровотечением из ВРВПЖ, лечебная программа которых предусматривала выжидательную консервативную тактику с использованием хирургических методов только в качестве «операции отчаяния».
Во вторую (основную) исследуемую клиническую группу вошли 28 больных с ЦП, осложненным кровотечением из ВРВПЖ, комплексная лечебная программа которых предусматривала активную хирургическую тактику с использованием усовершенствованной операции М.Д. Пациора.
Из них мужчин было 68 (64,8%), женщин — 37 (35,2%). В возрасте от 15 до 39 лет было 49 (46,7%), от 40 до 59 лет — 41 (39,0%), от 60 и старше — 15 (14,3%) больных. Таким образом, среди наблюдаемых нами пациентов преобладали лица молодого и среднего, т.е. трудоспособного, возраста.
Среди этиологических факторов ЦП у 27 (25,7% наблюдений) из 105 больных было выявлено алкогольное поражение печени, у 23 (21,9% наблюдений) — вирусный гепатит С, у 22 (21% наблюдений) — вирусный гепатит В, у 15 (14,3% наблюдений) — поражение печени гепатотоксичными соединениями, у 18 (17,1%) — ЦП неутонченной этиологии.
Тяжесть кровопотери оценивали по классификации А.И. Горбашко (1974). У 22 (21,0% наблюдений) человек была кровопотеря легкой, у 48 (45,7% наблюдений) человек была кровопотеря средней и у 35 (33,3% наблюдений) человек была кровопотеря тяжелой степени. На тяжесть состояния больных оказывала влияние поздняя обращаемость за медицинской помощью. В первые 24 ч от начала заболевания в хирургический стационар поступили 29 (27,6% наблюдений) человек. От 24 до 72 ч были доставлены 51 (48,6% наблюдений), в более поздние сроки — 25 (23,8% наблюдений) пациентов.
Тяжесть заболевания больных ЦП находилась в прямой зависимости от активности патологического процесса. У 60 (57,1% наблюдений) пациентов была диагностирована гиперферментемия (по Reitman, Frankel) средней степени, у 45 (42,9% наблюдений) — гиперферментемия высокой степени.
Концентрация билирубина в плазме крови у
12 (11,4% наблюдений) пациентов не превышала 25 ммоль/л, у 52 (49,5% наблюдений) она составила
от 25 до 50 ммоль/л и у 41 (39,1% наблюдений) превысила 50 ммоль/л.
Концентрация альбумина в плазме крови превышала 35 г/л у 12 (11,4% наблюдений), находилась в промежутке от 30 до 35 г/л у 32 (30,5% наблюдений) и была ниже 30 г/л у 61 (58,1% наблюдений) больного.
Протромбиновый индекс у 14 (13,3% наблюдений) человек составил от 80 до 100%, у 54 (51,4% наблюдений) — от 79 до 60%, у 37 (35,3% наблюдений) — менее 60%.
У 99 (94,3% наблюдений) пациентов при объективном исследовании была обнаружена жидкость в брюшной полости. У 34 (34,3% наблюдений) из них асцит носил транзиторный характер и легко контролировался назначением диуретиков. У 65 (65,7% наблюдений) больных асцит был диуретикорезистентным.
Все пациенты имели психоневрологические нарушения. У 14 (13,3% наблюдений) больных с помощью теста связи чисел выявлена латентная форма энцефалопатии. У 91 (86,7% наблюдений) печеночная энцефалопатия проявлялась клинически, в том числе у 41 (39,1% наблюдений) — I степени, у 36 (34,3% наблюдений) — II степени, у 14 (13,3% наблюдений) — III степени.
По критериям Чайлда—Пью (1973) все больные были разделены на три прогностические группы. В класс А (компенсированный ЦП) вошли 10 (9,5% наблюдений), в класс В (субкомпенсированный ЦП) — 44 (41,9% наблюдений) и в класс С (декомпенсированный ЦП) — 51 (48,6% наблюдений) пациент.
Всем больным с ЖКК по экстренным показаниям была выполнена ЭГДС. У 77 (73,3% наблюдений) больных со стабильными показателями центральной гемодинамики и сохраненным сознанием исследование проводили в эндоскопическом кабинете хирургического отделения. 28 (26,7% наблюдений) больным с нестабильной гемодинамикой, срыгиванием свежей крови и неадекватным поведением ЭГДС на фоне интенсивных реанимационных мероприятий выполняли непосредственно в операционной.
У 76 (72,4% наблюдений) больных с пищеводножелудочным кровотечением во время ЭГДС были обнаружены ВРВП, у 29 (27,6% наблюдений) — ВРВП и кардиального отдела желудка. Из 76 больных с ВРВП у 65 (85,5% наблюдений) они локализовались в нижней трети пищевода, у 11 (14,5% наблюдений) — в нижней и средней его трети. У 30 (28,6% наблюдений) больных была обнаружена II, а у 75 (71,4% наблюдений) — III степень выраженности ВРВП по А.Г. Шерцингеру (1986).
Локализация источника кровотечения во время проведения экстренной ЭГДС была установлена у 67 (63,8% наблюдений) больных. Это были эрозии слизистой оболочки, перфорировавшие стенку ВРВ. Последняя была расположена у 54 (80,6% наблюдений) пациентов в дистальной трети пищевода, у 13 (19,4% наблюдений) — в области кардиального отдела желудка. У 38 (36,2% наблюдений) больных имели место эндоскопические признаки состоявшегося кровотечения, однако установить точно локализацию его источника не удалось.
При проведении УЗИ печеночной паренхимы у 41 (39,1% наблюдений) пациента размеры печени были увеличены, у 16 (15,2% наблюдений) — уменьшены,
у 48 (45,7% наблюдений) не выходили за пределы возрастной нормы. У 18 (17,1% наблюдений) больных обнаружена деформация контуров печени. У 96 (91,4% наблюдений) выявлено обеднение сосудистого рисунка паренхимы печени с диффузным расположением в ней эхоструктур различной плотности и размеров. У 85 (81,0% наблюдений) больных селезенка была увеличена в размерах. Структура ее имела неоднородный характер за счет диффузного или очагового уплотнения паренхимы.
У 33 (33,3% наблюдений) из 99 больных транссудат в брюшной полости определялся в виде эхосвободной зоны в подпеченочном пространстве. У 63 (63,6% наблюдений) асцитическая жидкость занимала всю брюшную полость. У 3 (3,1% наблюдений) человек асцит, не выявленный при клиническом обследовании, был обнаружен сонографически.
У всех больных было выявлено расширение воротной и селезеночной вен.
Статистическую обработку результатов исследования проводили методом вариационной статистики путем расчета средней арифметической (М), среднеквадратичного отклонения (а) и средней ошибки (т). Достоверность различий показателей оценивали по коэффициенту Стьюдента [13].
Результаты и их обсуждение. У всех больных лечебные мероприятия начинали с установки зонда-обтуратора Сенгстакена—Блэкмора, рассматривая его как обязательный механический фактор для достижения гемостаза. Сроки нахождения зонда-обтуратора у больных группы сравнения выбирали произвольно. При этом длительность пребывания составила (3,5±1,5) сут У больных основной группы сроки зависели от степени компенсации цирроза печени и составили в классе А (12±2,0) ч, в классе В (18±6,0) ч, в классе С (70±2,5) ч.
13 (16,9% наблюдений) пациентам группы сравнения было выполнено прошивание варикозно расширенных вен пищевода и желудка в качестве «операции отчаяния», когда не оставалось никакой надежды на консервативный гемостаз, а тяжесть состояния прогрессивно нарастала. Три пациента из 13 были прооперированы через 3, шесть через 5 и четыре через 7 сут с момента поступления в стационар. Все эти больные имели кровопотерю тяжелой степени, более 4 рецидивов кровотечения в анамнезе, высокую степень гиперферментемии. На фоне длительного консервативного лечения, рецидивов кровотечения и позднего оперативного пособия у всех этих пациентов мы наблюдали прогрессирование декомпенсации функции печени. Именно поэтому все оперированные в группе сравнения пациенты имели декомпенсированный (класс С) цирроз печени и III степень варикозно расширенных вен пищевода и желудка по А.Г Шерцингеру.
В основной группе все 28 (100% наблюдений) пациентов были оперированы как можно раньше, до наступления декомпенсации функции печени. В том числе семь человек прооперированны через 12, двенадцать — через 24 и девять через 48 ч от момента поступления в хирургический стационар.
Анализ ближайших результатов лечения больных циррозом печени с кровотечениями из варикозно расширенных вен пищевода и желудка под влиянием различных вариантов лечебной программы показал, что в группе сравнения осложнения возникли у 75 (97,4%
наблюдений), а в основной у 7 (25,0% наблюдений) пациентов. У 24 (31,2% наблюдений) больных группы сравнения, несмотря на проводимую медикаментозную гемостатическую терапию, после удаления зонда-обтуратора наступил рецидив пищеводно-желудочного кровотечения. Это привело к прогрессированию печеночной недостаточности и переходу цирроза печени из субкомпенсированного (класс В) в декомпенсиро-ванный (класс С).
У больных основной группы рецидив кровотечения в послеоперационном периоде возник у 2 (7,1% наблюдений) пациентов. Его причиной были острые язвы желудка на фоне общего тяжелого состояния. Печеночная недостаточность в группе сравнения прогрессировала у 69 (89,6% наблюдений), а в основной группе — у 10 (35,7% наблюдений) человек. Местные осложнения, связанные с инфекционным процессом в мягких тканях брюшной стенки, развились у 5 (6,5% наблюдений) больных в группе сравнения и у 1 (3,6% наблюдений) в основной группе. У 35 (46,7% наблюдений) пациентов группы сравнения и у 2 (7,1% наблюдений) основной было сочетание как местных, так и общих осложнений.
Таким образом, выжидательная консервативная тактика у больных циррозом печени, осложненным пищеводно-желудочным кровотечением, не позволяет избежать большого количества осложнений и существенно уменьшить показатели летальности.
Включение в лечебную программу больных компенсированным (класс А) и субкомпенсированным (класс В) циррозом печени, осложненным кровотечением из варикозно расширенных вен пищевода и желудка, активной хирургической тактики эффективно уменьшает число послеоперационных осложнений, сокращает сроки стационарного лечения и летальность.
У больных декомпенсированным (класс С) циррозом печени операционный риск летального исхода от полиорганной недостаточности очень высок. В связи с этим при наличии симптомов декомпенсации функции печени от операции следует воздержаться.
Послеоперационная летальность в группе сравнения составила 100% (13 пациентов), в основной — 35,7% (10 пациентов). Госпитальная летальность в группе сравнения составила 76,6% (класс А — 0%, класс В — 30,5%, класс С — 69,5%), в основной — 35,7% (0%; 0%; 35,7% соответственно).
Длительность лечения больных с благоприятным исходом в группе сравнения составила в классе А — (18,1±3,0) сут, в классе В — (22,0±2,0) сут, в основной группе (13,0±2,0) и (17,25±1,0) сут соответственно.
Итак, наш клинический опыт свидетельствует о том, что активная хирургическая тактика с использованием усовершенствованного варианта операции М.Д. Пациора позволяет достичь стойкой ремиссии гастроэзофагеального кровотечения как основного симптома болезни.
Таким образом, ни в коей мере не претендуя на абсолютную завершенность, мы надеемся, что результаты проведенного исследования окажутся полезными практическим хирургам и помогут наметить пути для дальнейшего прогресса этого направления хирургической гепатологии.
Заключение
1. Выжидательная консервативная тактика у больных циррозом печени, осложненным пищеводно-
желудочным кровотечением, не позволяет избежать большого количества осложнений и существенно уменьшить показатели летальности.
2. Включение в лечебную программу больных компенсированным (класс А) и субкомпенсированным (класс В) циррозом печени, осложненным кровотечением из варикозно расширенных вен пищевода и желудка, предлагаемой активной хирургической тактики позволяет уменьшить общее количество осложнений с 97,4 до 25,0%, в том числе число рецидивов кровотечений — с 12,9 до 7,1%, частоту развития печеночной недостаточности — с 16,9 до 14,3%, нагноений срединной раны — с 6,5 до 3,6%, снизить послеоперационную летальность с 100 до 35,7%, госпитальную летальность — с 76,6 до 35,7%, сократить сроки стационарного лечения у пациентов с благоприятным исходом в классе А с (18,1 ±3,0) до (13,0±2,0) сут, в классе В — с (22,0±2,0) до (17,25±1,0) сут.
3. У больных декомпенсированным (класс С) циррозом печени операционный риск летального исхода от полиорганной недостаточности очень высок. В связи с этим при наличии симптомов декомпенсации функции печени от операции следует воздержаться.
ЛИТЕРАТУРА
1. Борисов, А.Е. Кровотечения портального генеза / А.Е. Борисов, М.И. Кузьмин-Крутецкий, В.А. Кащенко [и др.]. — СПб., 2001. — 149 с.
2. Боур, А.В. Сочетанное применение эндоваскулярной эмболизации и эндоскопического склерозирования вен пищевода и желудка у больных портальной гипертензией /
A.В. Боур, А.Г. Шерцингер, В.А. Черкасов, А.К. Ерамишан-цев // Анналы хирургической гепатологии. — 1999. — Т. 4, № 1. — С.17—21.
3. Ерамишанцев, А.К. Диагностическая и лечебная тактика при кровотечениях из варикозно расширенных вен пищевода и желудка / А.К. Ерамишанцев, А.Г. Шерцингер,
B.М. Лебезев, Е.А. Киценко [и др.] // Анналы хирургической гепатологии. — 1996. — Т. 1, № 1. — С.52—54.
4. Ерамишанцев, А.К. Эволюция хирургии синдрома портальной гипертензии / А.К. Ерамишанцев // Вестник РНЦХ РАМН. — 2002. — № 15. — С.56—61.
5. Ерамишанцев, А.К. Портокавальное шунтирование или прошивание варикозно расширенных вен пищевода и желудка. Что выбрать? / А.К. Ерамишанцев, РА. Мусин, Е.Д. Любивый // Анналы хирургической гепатологии. — 2005. — Т. 10, № 2. — С.76.
6. Жигалова, С.Б. Эндоскопическое склерозирование и эндоваскулярная эмболизация в комплексном лечении кровотечений из варикозно расширенных вен пищевода и желудка у больных с портальной гипертензией: автореф. дис. … канд. мед. наук/ С.Б. Жигалова. — М.,
1993. — 20 с.
7. Зубарев, П.Н. Хирургическая тактика при пищеводножелудочных кровотечениях у больных циррозом печени / П.Н. Зубарев, Б.Н. Котив, И.И. Дзидзава [и др.] // Анналы хирургической гепатологии. — 2005. — Т. 10, № 2. —
C.78.
8. Зыятдинов, К.Ш. Статистика здоровья населения и здравоохранения (по материалам Республики Татарстан за 2001—2005 годы): учеб.-метод. пособие / Казан. гос. мед. акад., Респуб. мед. информ.-аналит. центр МЗ РТ; К.Ш. Зыятдинов, А.А. Гильманов, В.Г. Шерпутовский [и др.]; под ред. И.Г. Низамова. — Казань, 2006. — 276 с.
9. Киценко, Е.А. Результаты операции М.Д. Пациоры у больных циррозом печени и портальной гипертензией / Е.А. Ки-
ценко, Е.К. Заворотная, И.Ч. Абдуллаев // Анналы хирургической гепатологии. — 2005. — Т. 10, № 2. — С.80.
10. Котив, Б.Н. Портокавальное шунтирование. Проблемы и перспективы / Б.Н. Котив, И.И. Дзидзава, С.А. Ален-тьев // Первая международная конференция по торако-абдоминальной хирургии. — М., 2008. — С.179.
11. Назыров, Ф.Г Хирургия портальной гипертензии у больных циррозом печени в Центрально-Азиатском регионе / Ф.Г. Назыров, Х.А. Акилов, А.В. Девятов // Анналы хирургической гепатологии. — 2003. — Т. 8, № 1. —
С.19—28.
12. Пациора, М.Д. Хирургия портальной гипертензии / М.Д. Па-циора. — 2-е изд., доп. — Ташкент, 1984. — 319 с.
13. Реброва, О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA / О.Ю. Реброва. — М.: Медиа Сфера, 2006. — 305 с.
14. Шерцингер, А.Г Ближайшие и отдаленные результаты прошивания варикозно расширенных вен пищевода и желудка у больных с портальной гипертензией / А.Г. Шерцингер, Е.А. Киценко // Анналы хирургической гепатологии. — 1998. — Т. 3, № 3. — С.172—182.
15. Шерцингер, А.Г. Тактика при острых кровотечениях из варикозно расширенных вен пищевода и желудка / А.Г. Шерцингер // Российский гастроэнтерологический журнал. — 2001. — № 3. — С.40—42.
16. Шерцингер, А.Г. Тактика лечения пищеводно-желудочных кровотечений у больных с портальной гипертензией / А.Г. Шерцингер, С.Б. Жигалова, З.Ш. Маргиани, А.Б. Гамидов // Анналы хирургической гепатологии. — 2005. — Т. 10, № 2. — С.93.
17. Idezuki, Y. Sugiura Procedure for Management of Variceal Bleeding in Japan / Y. Idezuki, N. Kokudo, K. Sanjo [et al.] // World J. Surg. — 1994. — Р216.
18. Jenkins, S.A. Somatostatin in acute bleeding esophageal varices / S.A. Jenkins // Drugs. — 2000. — Vol. 44,№ 12. — P.36—55.
19. Rikkers, L.F. Surgical Management of Acute Variceal Hemorrhage / L.F. Rikkers, G. Jin // World J. Surg. — 1994. — Р193.
20. Warren, W.D. Resent Advances in the Management of Variceal Bleeding / W.D. Warren, J.B. Whilfhead // Jap. J. Surg. — 1986. — Р.77.
REFERENCES
1. Borisov, A.E. Krovotecheniya portal’nogo geneza / A.E. Borisov,
M.I. Kuz’min-Kruteckii, V.A. Kaschenko [i dr.]. — SPb.,
2001. — 149 s.
2. Bour, A.V. Cochetannoe primenenie endovaskulyarnoi
embolizacii i endoskopicheskogo sklerozirovaniya ven pischevoda i zheludka u bol’nyh portal’noi gipertenziei / A.V. Bour, A.G. SHercinger, V.A. CHerkasov, A.K. Eramishancev // Annaly hirurgicheskoi gepatologii. — 1999. — T 4, № 1. — S.17—21.
3. Eramishancev, A.K. Diagnosticheskaya i lechebnaya
taktika pri krovotecheniyah iz varikozno rasshirennyh ven pischevoda i zheludka / A.K. Eramishancev, A.G. SHercinger, V.M. Lebezev, E.A. Kicenko [i dr.] // Annaly hirurgicheskoi gepatologii. — 1996. — T. 1, № 1. — S.52—54.
4. Eramishancev, A.K. Evolyuciya hirurgii sindroma portal’noi
gipertenzii / A.K. Eramishancev // Vestnik RNCH RAMN. —
2002. — № 15. — S.56—61.
5. Eramishancev, A.K. Portokaval’noe shuntirovanie ili
proshivanie varikozno rasshirennyh ven pischevoda i
zheludka. Chto vybrat’? / A.K. Eramishancev, R.A. Musin, E.D. Lyubivyi // Annaly hirurgicheskoi gepatologii. — 2005. — T 10, № 2. — S.76.
6. Zhigalova, S.B. Endoskopicheskoe sklerozirovanie
i endovaskulyarnaya embolizaciya v kompleksnom le-chenii krovotechenii iz varikozno rasshirennyh ven pischevoda i zheludka u bol’nyh s portal’noi gipertenziei: avtoref. dis. … kand. med. nauk/ S.B. Zhigalova. — M.,
1993. — 20 s.
7. Zubarev, P.N. Hirurgicheskaya taktika pri pischevodno-
zheludochnyh krovotecheniyah u bol’nyh cirrozom pecheni / P.N. Zubarev, B.N. Kotiv, I.I. Dzidzava [i dr.] // Annaly hirurgicheskoi gepatologii. — 2005. — T 10, № 2. — S.78.
8. Zyyatdinov, K.Sh. Statistika zdorov’ya naseleniya i
zdravoohraneniya (po materialam Respubliki Tatarstan za 2001—2005 gody): ucheb.-metod. posobie / Kazan. gos. med. akad., Respub. med. inform.-analit. centr MZ RT; K.Sh. Zyyatdinov, A.A. Gil’manov, V.G. SHerputovskii [i dr.]; pod red. I.G. Nizamova. — Kazan’, 2006. — 276 s.
9. Kicenko, E.A. Rezul’taty operacii M.D. Paciory u bol’nyh
cirrozom pecheni i portal’noi gipertenziei / E.A. Kicenko, E.K. Zavorotnaya, I.CH. Abdullaev // Annaly hirurgicheskoi gepatologii. — 2005. — T 10, № 2. — S.80.
10. Kotiv, B.N. Portokaval’noe shuntirovanie. Problemy i
perspektivy / B.N. Kotiv, I.I. Dzidzava, S.A. Alent’ev // Pervaya mezhdunarodnaya konferenciya po torako-abdominal’noi hirurgii. — M., 2008. — S.179.
11. Nazyrov, F.G. Hirurgiya portal’noi gipertenzii u bol’nyh cirrozom
pecheni v Central’no-Aziatskom regione / F.G. Nazyrov, X.A. Akilov, A.V. Devyatov // Annaly hirurgicheskoi gepatologii. — 2003. — T. 8, № 1. — S.19—28.
12. Paciora, M.D. Hirurgiya portal’noi gipertenzii / M.D. Paciora. —
2-e izd., dop. — Tashkent, 1984. — 319 s.
13. Rebrova, O.Yu. Statisticheskii analiz medicinskih
dannyh. Primenenie paketa prikladnyh programm STATISTICA / O.Yu. Rebrova. — M.: Media Sfera, 2006. — 305 s.
14. Shercinger, A.G. Blizhaishie i otdalennye rezul’taty proshivaniya
varikozno rasshirennyh ven pischevoda i zheludka u bol’nyh s portal’noi gipertenziei / A.G. Shercinger, E.A. Kicenko // Annaly hirurgicheskoi gepatologii. — 1998. — T 3, № 3. — S.172—182.
15. Shercinger, A.G. Taktika pri ostryh krovotecheniyah iz varikozno
rasshirennyh ven pischevoda i zheludka / A.G. Shercinger // Rossiiskii gastroenterologicheskii zhurnal. — 2001. — № 3. — S.40—42.
16. Shercinger, A.G. Taktika lecheniya pischevodno-zheludochnyh
krovotechenii u bol’nyh s portal’noi gipertenziei / A.G. SHercinger, S.B. Zhigalova, Z.Sh. Margiani, A.B. Gamidov // Annaly hirurgicheskoi gepatologii. — 2005. — T. 10, № 2. — S.93.
17. Idezuki, Y. Sugiura Procedure for Management of Variceal
Bleeding in Japan / Y. Idezuki, N. Kokudo, K. Sanjo [et al.] // World J. Surg. — 1994. — P216.
18. Jenkins, S.A. Somatostatin in acute bleeding esophageal
varices / S.A. Jenkins // Drugs. — 2000. — Vol. 44,№ 12. — P.36—55.
19. Rikkers, L.F. Surgical Management of Acute Variceal
Hemorrhage / L.F. Rikkers, G. Jin // World J. Surg. —
1994. — P193.
20. Warren, W.D. Resent Advances in the Management of Variceal
Bleeding / W.D. Warren, J.B. Whilfhead // Jap. J. Surg. — 1986. — P77.
Распространенность кровотечений из варикозно расширенных вен пищевода
Библиографическое описание:Плаченова, Т. С. Распространенность кровотечений из варикозно расширенных вен пищевода / Т. С. Плаченова, В. А. Халявина, С. О. Зибаев. — Текст : непосредственный // Молодой ученый. — 2017. — № 10 (144). — С. 154-158. — URL: https://moluch.ru/archive/144/40507/ (дата обращения: 05.06.2021).
Кровотечение из вен пищевода является опасным и во многих случаях жизнеугрожающим осложнением различных заболеваний. Причиной данного осложнения в основном служат два серьезных заболевания: варикозно расширенные вены пищевода (далее: ВРВП) и повреждение стенки пищевода при синдроме Мэллори-Вейса. Более подробно мы остановимся на ВРВП, так как данная патология стоит на первом месте по встречаемости среди двух перечисленных. Наиболее частым предрасполагающим фактором в обоих случаях является хронический алкоголизм. Алкогольный рынок в России занимает лидирующие позиции среди других рынков продовольственных товаров и по продажам, и по темпам развития. Россия занимает уже 4 место среди стран мира по уровню употребления алкоголя, что ведет к увеличению показателей алкогольного цирроза печени. Именно поэтому данная проблема является очень актуальной.
Целью нашего исследования явилось изучение распространенности данного осложнения в хирургическом отделении 1 Республиканской больницы и выявление контингента наиболее подверженного данной патологии.
Нашими задачами являлись:
1) Обработка историй болезни пациентов за период с 2014 по начало 2017 года хирургического отделения 1 Республиканской больницы.
2) Сортировка историй болезни, удовлетворяющих критериям поиска.
3) Анализ полученных результатов
4) И обоснование заключения.
Теоретическая часть
Флебэктазия, или варикозное расширение вен пищевода — это патология эзофагеальных вен, характеризующаяся их извитостью и мешотчатым расширением за счет формирования флебоэктазов.
Эндоскопическая классификация варикозного расширения вен пищевода:
1 степень: Единичные эктазии вен (рентгенологически не определяются).
2 степень: Единичные хорошо отграниченные стволы вен (чаще в нижней трети пищевода). Сужение пищевода отсутствует. Истончения эпителия на венах не наблюдается.
3 степень: Отчетливое сужение пищевода стволами варикозно расширенных вен, расположенных в нижней и средней трети пищевода. На верхушках вариксов выявляются единичные красные маркеры или ангиоэктазии.
4 степень: Просвет пищевода полностью закрыт варикозными узлами. Эпителий над венами истончен. На верхушках вариксов определяются множественные эрозии и/или ангиоэктазии.
Этиология ипатогенез: Наиболее часто причина варикоза пищевода связана с повышением давления в системе портальной вены, что происходит в связи с заболеваниями печени (цирроз, хронический гепатит, опухоли, туберкулез, эхинококкоз и др.).
Портальная гипертензия и варикозные поражения пищевода обусловлены внутрипеченочной блокадой. Выраженное изменение морфологического строения печени вызывает перестройку ее ангиоархитектоники, что приводит к повышению сопротивления оттоку крови из воротной вены и повышению давления в ее системе, из-за чего начинают функционировать естественные портокавальные анастомозы. При затрудненном оттоке, вены пищевода, имеющие слабую опору в виде рыхлого подслизистого слоя, начинают расширяться, извиваться и удлиняться, образуя узлы — вариксы. Чаще всего они локализуются в дистальных сегментах пищевода (в отличие от вариксов при сердечно-сосудистой патологии, располагающихся равномерно на всем протяжении органа). Если в норме портальное давление колеблется в пределах 5 -14 см вод. ст., то при варикозе пищевода давление обычно превышает норму в 2–4 раза. Давление 25–27 см вод. ст. является критическим, поэтому выше этих цифр во всех случаях развиваются флебэктазии пищевода с реальной угрозой разрыва.
Клинические проявления: Первым симптомом болезни зачастую и бывает само кровотечение из вариксов пищевода. В виду того, что вены начинают располагаться близко к слизистой оболочке, она также становится рыхлой, легко повреждается твердой пищей и воспаляется, что в ряде случаев способствует развитию эзофагита. При этом пациента может беспокоить чувство жжения, изжога и отрыжка кислым, затруднения при глотании плотной пищи.
В зависимости от величины давления в эзофагеальных венах можно выделить незначительное и массивное кровотечения из ВРВП.
Незначительные кровотечения чаще всего возникают после физической нагрузки, переедания и во сне из-за колебаний системного давления. Постоянные незначительные кровопотери могут не проявляться выраженной симптоматикой, но приводить к истощению и железодефицитной анемии. Такие кровотечения сопровождаются тошнотой, рвотой с прожилками крови, меленой, слабостью, головокружением, снижением веса, жаждой и сухостью во рту, холодным липким потом. Артериальное же давление может оставаться без изменений, либо незначительно понижаться.
Если же кровотечение массивное, а оно встречается примерно у 60 %, то у пациента возникает обильная кровавая рвота, сильная слабость, потливость, головокружение, возможна кратковременная потеря сознания, артериальное давление понижается одновременно с повышением частоты сердечных сокращений. Падение артериального давления указывает на наличие значительной кровопотери и требует немедленного восполнения объема циркулирующей крови
Практическая часть.
В ходе исследования было обработано 100 историй болезни пациентов хирургического отделения 1 Республиканской больницы города Ижевска. Результаты исследований показали, что за период 2014-начала 2017 гг. с диагнозом «Цирроз печени. ВРВП» на лечении в 1 РКБ находилось 55 больных. 33 (60 %) случая были осложнены кровотечением из варикозно-расширенных вен пищевода, остальные 22 (40 %) не сопровождались этим осложнением.
Важно отметить, что из всех случаев подавляющую часть- 80 % составляют мужчины и всего лишь 20 %- пациентки женского пола.
Проанализировав возраст больных с диагнозом «Цирроз печени. ВРВП. Состоявшееся кровотечение» мы пришли к следующим результатам:
Как видно из диаграммы, большее количество случаев заболевания приходится на людей трудоспособного возраста. Проведя более детальный разбор случаев данного осложнения за 2014–2017 гг, мы пришли к выводу, что с каждым годом заболевание возникает у более молодой группы лиц и имеет тенденцию к «молодению». Это объясняется главными этиологическими факторами, способствующими развитию хронического воспалительного процесса в тканях печени: гепатита, который в последствии может привести к циррозу печени. По данным исследований, проводимых на кафедре «Факультетской хирургии» Ижевской государственной медицинской академии, главной причиной развития гепатитов является злоупотребление алкоголем (65 %), второе место отводится вирусной этиологии (20 %) и другие причинные факторы занимают 15 % всех случаев регистрации гепатитов.
Заключение: вконце нашего исследования мы пришли к нескольким выводам:
1) Основной причиной возникновения ВРПВ является злоупотребление алкоголем (65 %)
2) Чаще данная патология возникает у лиц мужского пола (80 %), трудоспособного возраста (75,8 %)
3) Осложнения варикозно расширенных вен пищевода в виде кровотечений возникают в 60 % случаев.
На основе проведенных исследований на базе кафедры под руководством Стяжкиной С. Н., было выявлено, что в структуре летальности в хирургическом отделении 1 Республиканской больницы г. Ижевска на первом месте находятся циррозы печени с осложнениями в виде кровотечения из варикозно расширенных вен пищевода. В связи с тяжестью этого осложнения крайне важна ранняя диагностика и профилактика, которая заключается в социально-гигиеническом воспитании населения в виде пропаганды здорового образа жизни, проведении лекций о вреде алкоголя и целесообразности ведения адекватной половой жизни. Что касается лечения, следует упомянуть новые перспективные препараты, такие как: ронколейкин, гепатопротекторы, транексамовая кислота.
Литература:
- Кровотечение из варикозно расширенных вен пищевода при портальной гипертензии — учебно-методическое пособие. Автор: М. В. Варганов. Ижевск, 2008 год.
- Хирургические болезни. М. И. Кузин, О. С. Шкроб, Н. М. Кузин. — издательство «Медицина», 2002 год.
- Гастроэнтерология: Справочник. Под ред. Барановский А. Ю. Санкт-Петербург, 2011 год.
- Инфекционные болезни. Авторы: Е. П. Шувалова, Е. С. Белозеров, Т. В. Беляева, Е. И. Змушко. Санкт-Петербург, 2015 год.
- Хирургия печени и желчевыводящих путей. Авторы: А. А. Шалимов, С. А. Шалимов, М. Е. Ничитайло, Б. В. Доманский. Москва, 1993 год.
Основные термины (генерируются автоматически): хирургическое отделение, цирроз печени, осложнение, расширенная вена пищевода, Республиканская больница, артериальное давление, варикозное расширение вен пищевода, вена пищевода, россия, трудоспособный возраст.
Кровотечение из варикозно расширенных вен пищевода: MedlinePlus Medical Encyclopedia
Цель лечения – как можно скорее остановить острое кровотечение. Кровотечение необходимо контролировать быстро, чтобы предотвратить шок и смерть.
В случае обильного кровотечения человеку может потребоваться включить аппарат искусственной вентиляции легких, чтобы защитить дыхательные пути и предотвратить попадание крови в легкие.
Чтобы остановить кровотечение, врач может ввести эндоскоп (трубку с маленьким светом на конце) в пищевод:
- В варикозные узлы можно ввести лекарство для свертывания крови.
- Вокруг кровоточащих вен можно наложить резиновую ленту (это называется перевязкой).
Другие методы лечения для остановки кровотечения:
- Через вену можно вводить лекарство для сужения кровеносных сосудов. Примеры включают октреотид или вазопрессин.
- В редких случаях зонд вводят через нос в желудок и надувают воздухом. Это создает давление на кровоточащие вены (баллонная тампонада).
После остановки кровотечения другие варикозные узлы можно лечить лекарствами и медицинскими процедурами, чтобы предотвратить кровотечение в будущем.К ним относятся:
- Лекарства, называемые бета-блокаторами, такие как пропранолол и надолол, которые снижают риск кровотечения.
- Во время процедуры EGD вокруг кровоточащих вен можно наложить резиновую ленту. Кроме того, некоторые лекарства можно вводить в варикозные узлы во время ФГДС, чтобы вызвать их свертывание.
- Трансъюгулярный внутрипеченочный портосистемный шунт (TIPS). Это процедура для создания новых связей между двумя кровеносными сосудами в печени. Это может снизить давление в венах и предотвратить повторение эпизодов кровотечения.
В редких случаях для лечения людей может использоваться экстренная хирургия, если другое лечение не помогает. Портакавальное шунтирование или операция по снижению давления в варикозно расширенных венах пищевода являются вариантами лечения, но эти процедуры рискованны.
Людям с кровотечением из варикозно расширенных вен при заболевании печени может потребоваться дополнительное лечение заболевания печени, включая трансплантацию печени.
Варикозное расширение вен пищевода; Причины, симптомы, диагностика и лечение
Обзор
Варикозное расширение вен пищеводаЧто такое варикозное расширение вен пищевода?
Варикозное расширение вен – это увеличенные или опухшие вены.Пищевод – это трубка, соединяющая горло с желудком. Когда на слизистой оболочке пищевода возникают расширенные вены, они называются варикозным расширением вен пищевода.
Кто подвержен риску разрыва и кровотечения варикозного расширения вен пищевода?
Не у всех, у кого развивается варикоз пищевода, будет кровотечение. Факторы, повышающие риск кровотечения, включают:
- Высокое кровяное давление в воротной вене : Чем выше давление в воротной вене, тем выше риск кровотечения.
- Большой варикозный узел : Риск кровотечения увеличивается с увеличением размера варикозного узла.
- Тяжелое заболевание печени : Серьезный цирроз или печеночная недостаточность повышают риск.
- Постоянное употребление алкоголя : У пациентов с варикозным расширением вен, вызванным алкоголем, продолжение употребления алкоголя увеличивает риск кровотечения.
Симптомы и причины
Что вызывает варикозное расширение вен пищевода?
Печень – это орган, очищающий кровь от токсинов (ядов).По воротной вене кровь доставляется в печень. Варикозное расширение вен пищевода обычно возникает у людей с заболеваниями печени. У людей с заболеваниями печени кровоток через печень замедляется. Когда это происходит, давление в воротной вене повышается.
Высокое кровяное давление в воротной вене (портальная гипертензия) толкает кровь в окружающие кровеносные сосуды, включая сосуды пищевода. Эти кровеносные сосуды имеют тонкие стенки и расположены близко к поверхности. Излишняя кровь заставляет их расширяться и набухать.Варикозное расширение вен также может развиваться в мелких кровеносных сосудах в верхней части желудка.
Если давление, вызванное дополнительной кровью, становится слишком высоким, варикозное расширение вен может открыться и кровоточить. Кровотечение – это неотложная ситуация, требующая срочного лечения. Неконтролируемое кровотечение может быстро привести к шоку и смерти.
Тромбоз (сгусток крови) в воротной вене или селезеночной вене, которая соединяется с воротной веной, может вызвать варикозное расширение вен пищевода.
Двумя редкими состояниями, которые могут вызывать варикозное расширение вен пищевода, являются синдром Бадда-Киари (закупорка определенных вен в печени) и инфицирование паразитарным шистосомозом.
Какие заболевания печени могут привести к варикозному расширению вен пищевода?
Любое серьезное заболевание печени может вызвать варикозное расширение вен пищевода. Цирроз – наиболее распространенный вид заболеваний печени. Более чем у 90% этих пациентов когда-нибудь в жизни разовьется варикозное расширение вен пищевода, и примерно у 30% начнется кровотечение.
У пациентов с циррозом печени по всей печени образуются большие участки рубцовой ткани, что приводит к замедлению кровотока. Цирроз может быть вызван алкогольной болезнью печени, жировой болезнью печени, вирусным гепатитом или другими заболеваниями печени.
Каковы симптомы варикозного расширения вен пищевода?
Большинство людей не знают, что у них варикоз пищевода, пока варикоз не начнет кровоточить. Когда кровотечение является внезапным и сильным, человека рвет большим количеством крови. Когда кровотечение менее сильное, человек может проглотить кровь, что может вызвать черный дегтеобразный стул. Если кровотечение не остановить, у человека могут развиться признаки шока, включая бледную липкую кожу, нерегулярное дыхание и потерю сознания.
Диагностика и тесты
Как диагностируется варикозное расширение вен пищевода?
Людям с запущенным заболеванием печени рекомендуется регулярное обследование на наличие варикозного расширения вен пищевода.Скрининг проводится с помощью эндоскопии. Эндоскоп – это тонкая гибкая трубка с фонариком и крошечной камерой на конце. Врач проводит эндоскоп по пищеводу, и камера отправляет изображения внутренней части пищевода на монитор. Врач смотрит на изображения, чтобы обнаружить увеличенные вены и классифицировать их по размеру. Красные линии на венах – признак кровотечения.
Врач может также использовать эндоскоп для исследования желудка и верхней части тонкой кишки. Это называется эзофогастродуоденоскопией (ЭГДС).
Визуализация с помощью КТ или МРТ также используется для диагностики варикозного расширения вен пищевода, часто в сочетании с эндоскопией. На снимках, сделанных с помощью КТ или МРТ, видны пищевод, печень, портальные и селезеночные вены. Они дают врачу больше информации о здоровье печени, чем только эндоскопия.
Ведение и лечение
Как лечат варикоз пищевода?
Цели лечения:
- Предотвратить дальнейшее повреждение печени.
- Предотвратить кровотечение из варикозно расширенных вен.
- Остановите кровотечение, если оно произойдет.
Профилактика поражения печени
Людям с заболеваниями печени необходимо избегать токсинов, которые вызывают дополнительную нагрузку на печень и наносят ей больший ущерб. Вот несколько советов по поддержанию здоровья печени:
- Избегайте любых алкогольных напитков.
- Ограничьте использование бытовых чистящих средств и химикатов.
- Придерживайтесь более здоровой диеты с низким содержанием жиров и высоким содержанием фруктов и овощей, цельнозерновых и нежирных белков.
- Поддерживайте здоровую массу тела (избыток жира оказывает нагрузку на печень).
Предотвращение кровотечения
Лекарства для снижения артериального давления в воротной вене могут снизить риск кровотечения. Чаще всего используются препараты из группы, называемой бета-блокаторами. К ним относятся пропранолол (Inderal®), надолол (Corgard®) и карведилол (Coreg®).
Пациенты с высоким риском кровотечения могут проходить профилактическое лечение с использованием тех же методов, которые используются для остановки кровотечения.Чаще всего используется метод перевязки варикозно расширенных вен.
Остановка кровотечения
Кровотечение из варикозно расширенных вен пищевода – это неотложная ситуация, требующая немедленного лечения. В больнице пациенты получают большое количество жидкости и крови, чтобы восполнить утраченное.
Для остановки кровотечения из варикозно расширенных вен доступны два различных нехирургических метода лечения – перевязка варикозно расширенных вен, выполняемая с помощью эндоскопа, и трансъюгулярное внутрипеченочное портосистемное шунтирование (TIPS), выполняемое радиологом с использованием рентгеновского излучения.
- Перевязка варикозно расширенных вен : В этой процедуре крошечные эластичные ленты оборачиваются вокруг варикозных вен, чтобы перекрыть кровоток через варикозные узлы. Это можно сделать на любом количестве вен за один сеанс. После того, как кровотечение остановлено, пациентам может быть назначен препарат для предотвращения повторного кровотечения. Перевязку варикозно расширенных вен следует повторять каждые 4 недели до тех пор, пока кровотечение из варикозно расширенных вен не прекратится. После этого верхнюю эндоскопию следует повторять каждые 6–12 месяцев, чтобы убедиться, что варикозное расширение вен не появилось повторно.Осложнения, связанные с перевязкой варикозно расширенных вен, включают потерю крови, прокол пищевода, затрудненное глотание, аномальное сердцебиение, инфекцию, лихорадку и пониженную или поверхностную частоту дыхания. Все эти осложнения редки.
- Трансъюгулярное внутрипеченочное портально-системное шунтирование (TIPS) : это процедура для снижения портального кровяного давления, которую можно использовать у пациентов с варикозным расширением вен пищевода, кровоточащими из-за тяжелого цирроза. Небольшая тонкая трубка, называемая катетером, вводится в вену на шее.Катетер вводят через тело в печень, где находятся печеночная и воротная вены. (Печеночная вена переносит кровь от печени обратно к сердцу.) Затем через катетер пропускают проволоку. Он используется, чтобы протыкать печеночную вену к воротной вене. Проволока удаляется, и стент (крошечная проволочная катушка) пропускается через катетер к месту соединения. Стент помещается в новый канал между воротной и печеночной венами. Стент удерживает место соединения открытым, чтобы кровь могла легче течь из воротной вены в печеночную вену и выходить из печени.Это снижает давление в воротной вене, что снижает давление в варикозных узлах, что снижает риск кровотечения. TIPS могут быть очень эффективными для предотвращения кровотечений, но они также могут вызывать серьезные осложнения, особенно у пациентов с запущенным заболеванием печени, включая спутанность сознания и печеночную недостаточность.
Перспективы / Прогноз
Каков долгосрочный прогноз для людей с кровотечением из варикозно расширенных вен пищевода?
Кровотечение из варикозно расширенных вен пищевода является опасным для жизни состоянием и может быть смертельным у 50% пациентов.Люди, у которых был эпизод кровотечения из варикозно расширенных вен пищевода, подвергаются риску повторного кровотечения.
Лечение с помощью перевязки варикозно расширенных вен эффективно купирует эпизоды первого кровотечения примерно у 90% пациентов. Однако примерно у половины пациентов, которым была проведена перевязка варикозно расширенных вен, будет еще один эпизод кровотечения в течение 1-2 лет. Прием лекарств и изменение образа жизни могут помочь снизить риск рецидива (возобновления кровотечения).
Пересадка печени может быть вариантом для пациентов с тяжелым циррозом печени и / или повторяющимися эпизодами кровотечения из варикозно расширенных вен.Трансплантация печени выполняется только в избранных центрах по всей стране, которые соответствуют очень строгим критериям.
варикозно расширенных вен пищевода; Причины, симптомы, диагностика и лечение
Обзор
Варикозное расширение вен пищеводаЧто такое варикозное расширение вен пищевода?
Варикозное расширение вен – это увеличенные или опухшие вены.Пищевод – это трубка, соединяющая горло с желудком. Когда на слизистой оболочке пищевода возникают расширенные вены, они называются варикозным расширением вен пищевода.
Кто подвержен риску разрыва и кровотечения варикозного расширения вен пищевода?
Не у всех, у кого развивается варикоз пищевода, будет кровотечение. Факторы, повышающие риск кровотечения, включают:
- Высокое кровяное давление в воротной вене : Чем выше давление в воротной вене, тем выше риск кровотечения.
- Большой варикозный узел : Риск кровотечения увеличивается с увеличением размера варикозного узла.
- Тяжелое заболевание печени : Серьезный цирроз или печеночная недостаточность повышают риск.
- Постоянное употребление алкоголя : У пациентов с варикозным расширением вен, вызванным алкоголем, продолжение употребления алкоголя увеличивает риск кровотечения.
Симптомы и причины
Что вызывает варикозное расширение вен пищевода?
Печень – это орган, очищающий кровь от токсинов (ядов).По воротной вене кровь доставляется в печень. Варикозное расширение вен пищевода обычно возникает у людей с заболеваниями печени. У людей с заболеваниями печени кровоток через печень замедляется. Когда это происходит, давление в воротной вене повышается.
Высокое кровяное давление в воротной вене (портальная гипертензия) толкает кровь в окружающие кровеносные сосуды, включая сосуды пищевода. Эти кровеносные сосуды имеют тонкие стенки и расположены близко к поверхности. Излишняя кровь заставляет их расширяться и набухать.Варикозное расширение вен также может развиваться в мелких кровеносных сосудах в верхней части желудка.
Если давление, вызванное дополнительной кровью, становится слишком высоким, варикозное расширение вен может открыться и кровоточить. Кровотечение – это неотложная ситуация, требующая срочного лечения. Неконтролируемое кровотечение может быстро привести к шоку и смерти.
Тромбоз (сгусток крови) в воротной вене или селезеночной вене, которая соединяется с воротной веной, может вызвать варикозное расширение вен пищевода.
Двумя редкими состояниями, которые могут вызывать варикозное расширение вен пищевода, являются синдром Бадда-Киари (закупорка определенных вен в печени) и инфицирование паразитарным шистосомозом.
Какие заболевания печени могут привести к варикозному расширению вен пищевода?
Любое серьезное заболевание печени может вызвать варикозное расширение вен пищевода. Цирроз – наиболее распространенный вид заболеваний печени. Более чем у 90% этих пациентов когда-нибудь в жизни разовьется варикозное расширение вен пищевода, и примерно у 30% начнется кровотечение.
У пациентов с циррозом печени по всей печени образуются большие участки рубцовой ткани, что приводит к замедлению кровотока. Цирроз может быть вызван алкогольной болезнью печени, жировой болезнью печени, вирусным гепатитом или другими заболеваниями печени.
Каковы симптомы варикозного расширения вен пищевода?
Большинство людей не знают, что у них варикоз пищевода, пока варикоз не начнет кровоточить. Когда кровотечение является внезапным и сильным, человека рвет большим количеством крови. Когда кровотечение менее сильное, человек может проглотить кровь, что может вызвать черный дегтеобразный стул. Если кровотечение не остановить, у человека могут развиться признаки шока, включая бледную липкую кожу, нерегулярное дыхание и потерю сознания.
Диагностика и тесты
Как диагностируется варикозное расширение вен пищевода?
Людям с запущенным заболеванием печени рекомендуется регулярное обследование на наличие варикозного расширения вен пищевода.Скрининг проводится с помощью эндоскопии. Эндоскоп – это тонкая гибкая трубка с фонариком и крошечной камерой на конце. Врач проводит эндоскоп по пищеводу, и камера отправляет изображения внутренней части пищевода на монитор. Врач смотрит на изображения, чтобы обнаружить увеличенные вены и классифицировать их по размеру. Красные линии на венах – признак кровотечения.
Врач может также использовать эндоскоп для исследования желудка и верхней части тонкой кишки. Это называется эзофогастродуоденоскопией (ЭГДС).
Визуализация с помощью КТ или МРТ также используется для диагностики варикозного расширения вен пищевода, часто в сочетании с эндоскопией. На снимках, сделанных с помощью КТ или МРТ, видны пищевод, печень, портальные и селезеночные вены. Они дают врачу больше информации о здоровье печени, чем только эндоскопия.
Ведение и лечение
Как лечат варикоз пищевода?
Цели лечения:
- Предотвратить дальнейшее повреждение печени.
- Предотвратить кровотечение из варикозно расширенных вен.
- Остановите кровотечение, если оно произойдет.
Профилактика поражения печени
Людям с заболеваниями печени необходимо избегать токсинов, которые вызывают дополнительную нагрузку на печень и наносят ей больший ущерб. Вот несколько советов по поддержанию здоровья печени:
- Избегайте любых алкогольных напитков.
- Ограничьте использование бытовых чистящих средств и химикатов.
- Придерживайтесь более здоровой диеты с низким содержанием жиров и высоким содержанием фруктов и овощей, цельнозерновых и нежирных белков.
- Поддерживайте здоровую массу тела (избыток жира оказывает нагрузку на печень).
Предотвращение кровотечения
Лекарства для снижения артериального давления в воротной вене могут снизить риск кровотечения. Чаще всего используются препараты из группы, называемой бета-блокаторами. К ним относятся пропранолол (Inderal®), надолол (Corgard®) и карведилол (Coreg®).
Пациенты с высоким риском кровотечения могут проходить профилактическое лечение с использованием тех же методов, которые используются для остановки кровотечения.Чаще всего используется метод перевязки варикозно расширенных вен.
Остановка кровотечения
Кровотечение из варикозно расширенных вен пищевода – это неотложная ситуация, требующая немедленного лечения. В больнице пациенты получают большое количество жидкости и крови, чтобы восполнить утраченное.
Для остановки кровотечения из варикозно расширенных вен доступны два различных нехирургических метода лечения – перевязка варикозно расширенных вен, выполняемая с помощью эндоскопа, и трансъюгулярное внутрипеченочное портосистемное шунтирование (TIPS), выполняемое радиологом с использованием рентгеновского излучения.
- Перевязка варикозно расширенных вен : В этой процедуре крошечные эластичные ленты оборачиваются вокруг варикозных вен, чтобы перекрыть кровоток через варикозные узлы. Это можно сделать на любом количестве вен за один сеанс. После того, как кровотечение остановлено, пациентам может быть назначен препарат для предотвращения повторного кровотечения. Перевязку варикозно расширенных вен следует повторять каждые 4 недели до тех пор, пока кровотечение из варикозно расширенных вен не прекратится. После этого верхнюю эндоскопию следует повторять каждые 6–12 месяцев, чтобы убедиться, что варикозное расширение вен не появилось повторно.Осложнения, связанные с перевязкой варикозно расширенных вен, включают потерю крови, прокол пищевода, затрудненное глотание, аномальное сердцебиение, инфекцию, лихорадку и пониженную или поверхностную частоту дыхания. Все эти осложнения редки.
- Трансъюгулярное внутрипеченочное портально-системное шунтирование (TIPS) : это процедура для снижения портального кровяного давления, которую можно использовать у пациентов с варикозным расширением вен пищевода, кровоточащими из-за тяжелого цирроза. Небольшая тонкая трубка, называемая катетером, вводится в вену на шее.Катетер вводят через тело в печень, где находятся печеночная и воротная вены. (Печеночная вена переносит кровь от печени обратно к сердцу.) Затем через катетер пропускают проволоку. Он используется, чтобы протыкать печеночную вену к воротной вене. Проволока удаляется, и стент (крошечная проволочная катушка) пропускается через катетер к месту соединения. Стент помещается в новый канал между воротной и печеночной венами. Стент удерживает место соединения открытым, чтобы кровь могла легче течь из воротной вены в печеночную вену и выходить из печени.Это снижает давление в воротной вене, что снижает давление в варикозных узлах, что снижает риск кровотечения. TIPS могут быть очень эффективными для предотвращения кровотечений, но они также могут вызывать серьезные осложнения, особенно у пациентов с запущенным заболеванием печени, включая спутанность сознания и печеночную недостаточность.
Перспективы / Прогноз
Каков долгосрочный прогноз для людей с кровотечением из варикозно расширенных вен пищевода?
Кровотечение из варикозно расширенных вен пищевода является опасным для жизни состоянием и может быть смертельным у 50% пациентов.Люди, у которых был эпизод кровотечения из варикозно расширенных вен пищевода, подвергаются риску повторного кровотечения.
Лечение с помощью перевязки варикозно расширенных вен эффективно купирует эпизоды первого кровотечения примерно у 90% пациентов. Однако примерно у половины пациентов, которым была проведена перевязка варикозно расширенных вен, будет еще один эпизод кровотечения в течение 1-2 лет. Прием лекарств и изменение образа жизни могут помочь снизить риск рецидива (возобновления кровотечения).
Пересадка печени может быть вариантом для пациентов с тяжелым циррозом печени и / или повторяющимися эпизодами кровотечения из варикозно расширенных вен.Трансплантация печени выполняется только в избранных центрах по всей стране, которые соответствуют очень строгим критериям.
варикозно расширенных вен пищевода; Причины, симптомы, диагностика и лечение
Обзор
Варикозное расширение вен пищеводаЧто такое варикозное расширение вен пищевода?
Варикозное расширение вен – это увеличенные или опухшие вены.Пищевод – это трубка, соединяющая горло с желудком. Когда на слизистой оболочке пищевода возникают расширенные вены, они называются варикозным расширением вен пищевода.
Кто подвержен риску разрыва и кровотечения варикозного расширения вен пищевода?
Не у всех, у кого развивается варикоз пищевода, будет кровотечение. Факторы, повышающие риск кровотечения, включают:
- Высокое кровяное давление в воротной вене : Чем выше давление в воротной вене, тем выше риск кровотечения.
- Большой варикозный узел : Риск кровотечения увеличивается с увеличением размера варикозного узла.
- Тяжелое заболевание печени : Серьезный цирроз или печеночная недостаточность повышают риск.
- Постоянное употребление алкоголя : У пациентов с варикозным расширением вен, вызванным алкоголем, продолжение употребления алкоголя увеличивает риск кровотечения.
Симптомы и причины
Что вызывает варикозное расширение вен пищевода?
Печень – это орган, очищающий кровь от токсинов (ядов).По воротной вене кровь доставляется в печень. Варикозное расширение вен пищевода обычно возникает у людей с заболеваниями печени. У людей с заболеваниями печени кровоток через печень замедляется. Когда это происходит, давление в воротной вене повышается.
Высокое кровяное давление в воротной вене (портальная гипертензия) толкает кровь в окружающие кровеносные сосуды, включая сосуды пищевода. Эти кровеносные сосуды имеют тонкие стенки и расположены близко к поверхности. Излишняя кровь заставляет их расширяться и набухать.Варикозное расширение вен также может развиваться в мелких кровеносных сосудах в верхней части желудка.
Если давление, вызванное дополнительной кровью, становится слишком высоким, варикозное расширение вен может открыться и кровоточить. Кровотечение – это неотложная ситуация, требующая срочного лечения. Неконтролируемое кровотечение может быстро привести к шоку и смерти.
Тромбоз (сгусток крови) в воротной вене или селезеночной вене, которая соединяется с воротной веной, может вызвать варикозное расширение вен пищевода.
Двумя редкими состояниями, которые могут вызывать варикозное расширение вен пищевода, являются синдром Бадда-Киари (закупорка определенных вен в печени) и инфицирование паразитарным шистосомозом.
Какие заболевания печени могут привести к варикозному расширению вен пищевода?
Любое серьезное заболевание печени может вызвать варикозное расширение вен пищевода. Цирроз – наиболее распространенный вид заболеваний печени. Более чем у 90% этих пациентов когда-нибудь в жизни разовьется варикозное расширение вен пищевода, и примерно у 30% начнется кровотечение.
У пациентов с циррозом печени по всей печени образуются большие участки рубцовой ткани, что приводит к замедлению кровотока. Цирроз может быть вызван алкогольной болезнью печени, жировой болезнью печени, вирусным гепатитом или другими заболеваниями печени.
Каковы симптомы варикозного расширения вен пищевода?
Большинство людей не знают, что у них варикоз пищевода, пока варикоз не начнет кровоточить. Когда кровотечение является внезапным и сильным, человека рвет большим количеством крови. Когда кровотечение менее сильное, человек может проглотить кровь, что может вызвать черный дегтеобразный стул. Если кровотечение не остановить, у человека могут развиться признаки шока, включая бледную липкую кожу, нерегулярное дыхание и потерю сознания.
Диагностика и тесты
Как диагностируется варикозное расширение вен пищевода?
Людям с запущенным заболеванием печени рекомендуется регулярное обследование на наличие варикозного расширения вен пищевода.Скрининг проводится с помощью эндоскопии. Эндоскоп – это тонкая гибкая трубка с фонариком и крошечной камерой на конце. Врач проводит эндоскоп по пищеводу, и камера отправляет изображения внутренней части пищевода на монитор. Врач смотрит на изображения, чтобы обнаружить увеличенные вены и классифицировать их по размеру. Красные линии на венах – признак кровотечения.
Врач может также использовать эндоскоп для исследования желудка и верхней части тонкой кишки. Это называется эзофогастродуоденоскопией (ЭГДС).
Визуализация с помощью КТ или МРТ также используется для диагностики варикозного расширения вен пищевода, часто в сочетании с эндоскопией. На снимках, сделанных с помощью КТ или МРТ, видны пищевод, печень, портальные и селезеночные вены. Они дают врачу больше информации о здоровье печени, чем только эндоскопия.
Ведение и лечение
Как лечат варикоз пищевода?
Цели лечения:
- Предотвратить дальнейшее повреждение печени.
- Предотвратить кровотечение из варикозно расширенных вен.
- Остановите кровотечение, если оно произойдет.
Профилактика поражения печени
Людям с заболеваниями печени необходимо избегать токсинов, которые вызывают дополнительную нагрузку на печень и наносят ей больший ущерб. Вот несколько советов по поддержанию здоровья печени:
- Избегайте любых алкогольных напитков.
- Ограничьте использование бытовых чистящих средств и химикатов.
- Придерживайтесь более здоровой диеты с низким содержанием жиров и высоким содержанием фруктов и овощей, цельнозерновых и нежирных белков.
- Поддерживайте здоровую массу тела (избыток жира оказывает нагрузку на печень).
Предотвращение кровотечения
Лекарства для снижения артериального давления в воротной вене могут снизить риск кровотечения. Чаще всего используются препараты из группы, называемой бета-блокаторами. К ним относятся пропранолол (Inderal®), надолол (Corgard®) и карведилол (Coreg®).
Пациенты с высоким риском кровотечения могут проходить профилактическое лечение с использованием тех же методов, которые используются для остановки кровотечения.Чаще всего используется метод перевязки варикозно расширенных вен.
Остановка кровотечения
Кровотечение из варикозно расширенных вен пищевода – это неотложная ситуация, требующая немедленного лечения. В больнице пациенты получают большое количество жидкости и крови, чтобы восполнить утраченное.
Для остановки кровотечения из варикозно расширенных вен доступны два различных нехирургических метода лечения – перевязка варикозно расширенных вен, выполняемая с помощью эндоскопа, и трансъюгулярное внутрипеченочное портосистемное шунтирование (TIPS), выполняемое радиологом с использованием рентгеновского излучения.
- Перевязка варикозно расширенных вен : В этой процедуре крошечные эластичные ленты оборачиваются вокруг варикозных вен, чтобы перекрыть кровоток через варикозные узлы. Это можно сделать на любом количестве вен за один сеанс. После того, как кровотечение остановлено, пациентам может быть назначен препарат для предотвращения повторного кровотечения. Перевязку варикозно расширенных вен следует повторять каждые 4 недели до тех пор, пока кровотечение из варикозно расширенных вен не прекратится. После этого верхнюю эндоскопию следует повторять каждые 6–12 месяцев, чтобы убедиться, что варикозное расширение вен не появилось повторно.Осложнения, связанные с перевязкой варикозно расширенных вен, включают потерю крови, прокол пищевода, затрудненное глотание, аномальное сердцебиение, инфекцию, лихорадку и пониженную или поверхностную частоту дыхания. Все эти осложнения редки.
- Трансъюгулярное внутрипеченочное портально-системное шунтирование (TIPS) : это процедура для снижения портального кровяного давления, которую можно использовать у пациентов с варикозным расширением вен пищевода, кровоточащими из-за тяжелого цирроза. Небольшая тонкая трубка, называемая катетером, вводится в вену на шее.Катетер вводят через тело в печень, где находятся печеночная и воротная вены. (Печеночная вена переносит кровь от печени обратно к сердцу.) Затем через катетер пропускают проволоку. Он используется, чтобы протыкать печеночную вену к воротной вене. Проволока удаляется, и стент (крошечная проволочная катушка) пропускается через катетер к месту соединения. Стент помещается в новый канал между воротной и печеночной венами. Стент удерживает место соединения открытым, чтобы кровь могла легче течь из воротной вены в печеночную вену и выходить из печени.Это снижает давление в воротной вене, что снижает давление в варикозных узлах, что снижает риск кровотечения. TIPS могут быть очень эффективными для предотвращения кровотечений, но они также могут вызывать серьезные осложнения, особенно у пациентов с запущенным заболеванием печени, включая спутанность сознания и печеночную недостаточность.
Перспективы / Прогноз
Каков долгосрочный прогноз для людей с кровотечением из варикозно расширенных вен пищевода?
Кровотечение из варикозно расширенных вен пищевода является опасным для жизни состоянием и может быть смертельным у 50% пациентов.Люди, у которых был эпизод кровотечения из варикозно расширенных вен пищевода, подвергаются риску повторного кровотечения.
Лечение с помощью перевязки варикозно расширенных вен эффективно купирует эпизоды первого кровотечения примерно у 90% пациентов. Однако примерно у половины пациентов, которым была проведена перевязка варикозно расширенных вен, будет еще один эпизод кровотечения в течение 1-2 лет. Прием лекарств и изменение образа жизни могут помочь снизить риск рецидива (возобновления кровотечения).
Пересадка печени может быть вариантом для пациентов с тяжелым циррозом печени и / или повторяющимися эпизодами кровотечения из варикозно расширенных вен.Трансплантация печени выполняется только в избранных центрах по всей стране, которые соответствуют очень строгим критериям.
варикозно расширенных вен пищевода; Причины, симптомы, диагностика и лечение
Обзор
Варикозное расширение вен пищеводаЧто такое варикозное расширение вен пищевода?
Варикозное расширение вен – это увеличенные или опухшие вены.Пищевод – это трубка, соединяющая горло с желудком. Когда на слизистой оболочке пищевода возникают расширенные вены, они называются варикозным расширением вен пищевода.
Кто подвержен риску разрыва и кровотечения варикозного расширения вен пищевода?
Не у всех, у кого развивается варикоз пищевода, будет кровотечение. Факторы, повышающие риск кровотечения, включают:
- Высокое кровяное давление в воротной вене : Чем выше давление в воротной вене, тем выше риск кровотечения.
- Большой варикозный узел : Риск кровотечения увеличивается с увеличением размера варикозного узла.
- Тяжелое заболевание печени : Серьезный цирроз или печеночная недостаточность повышают риск.
- Постоянное употребление алкоголя : У пациентов с варикозным расширением вен, вызванным алкоголем, продолжение употребления алкоголя увеличивает риск кровотечения.
Симптомы и причины
Что вызывает варикозное расширение вен пищевода?
Печень – это орган, очищающий кровь от токсинов (ядов).По воротной вене кровь доставляется в печень. Варикозное расширение вен пищевода обычно возникает у людей с заболеваниями печени. У людей с заболеваниями печени кровоток через печень замедляется. Когда это происходит, давление в воротной вене повышается.
Высокое кровяное давление в воротной вене (портальная гипертензия) толкает кровь в окружающие кровеносные сосуды, включая сосуды пищевода. Эти кровеносные сосуды имеют тонкие стенки и расположены близко к поверхности. Излишняя кровь заставляет их расширяться и набухать.Варикозное расширение вен также может развиваться в мелких кровеносных сосудах в верхней части желудка.
Если давление, вызванное дополнительной кровью, становится слишком высоким, варикозное расширение вен может открыться и кровоточить. Кровотечение – это неотложная ситуация, требующая срочного лечения. Неконтролируемое кровотечение может быстро привести к шоку и смерти.
Тромбоз (сгусток крови) в воротной вене или селезеночной вене, которая соединяется с воротной веной, может вызвать варикозное расширение вен пищевода.
Двумя редкими состояниями, которые могут вызывать варикозное расширение вен пищевода, являются синдром Бадда-Киари (закупорка определенных вен в печени) и инфицирование паразитарным шистосомозом.
Какие заболевания печени могут привести к варикозному расширению вен пищевода?
Любое серьезное заболевание печени может вызвать варикозное расширение вен пищевода. Цирроз – наиболее распространенный вид заболеваний печени. Более чем у 90% этих пациентов когда-нибудь в жизни разовьется варикозное расширение вен пищевода, и примерно у 30% начнется кровотечение.
У пациентов с циррозом печени по всей печени образуются большие участки рубцовой ткани, что приводит к замедлению кровотока. Цирроз может быть вызван алкогольной болезнью печени, жировой болезнью печени, вирусным гепатитом или другими заболеваниями печени.
Каковы симптомы варикозного расширения вен пищевода?
Большинство людей не знают, что у них варикоз пищевода, пока варикоз не начнет кровоточить. Когда кровотечение является внезапным и сильным, человека рвет большим количеством крови. Когда кровотечение менее сильное, человек может проглотить кровь, что может вызвать черный дегтеобразный стул. Если кровотечение не остановить, у человека могут развиться признаки шока, включая бледную липкую кожу, нерегулярное дыхание и потерю сознания.
Диагностика и тесты
Как диагностируется варикозное расширение вен пищевода?
Людям с запущенным заболеванием печени рекомендуется регулярное обследование на наличие варикозного расширения вен пищевода.Скрининг проводится с помощью эндоскопии. Эндоскоп – это тонкая гибкая трубка с фонариком и крошечной камерой на конце. Врач проводит эндоскоп по пищеводу, и камера отправляет изображения внутренней части пищевода на монитор. Врач смотрит на изображения, чтобы обнаружить увеличенные вены и классифицировать их по размеру. Красные линии на венах – признак кровотечения.
Врач может также использовать эндоскоп для исследования желудка и верхней части тонкой кишки. Это называется эзофогастродуоденоскопией (ЭГДС).
Визуализация с помощью КТ или МРТ также используется для диагностики варикозного расширения вен пищевода, часто в сочетании с эндоскопией. На снимках, сделанных с помощью КТ или МРТ, видны пищевод, печень, портальные и селезеночные вены. Они дают врачу больше информации о здоровье печени, чем только эндоскопия.
Ведение и лечение
Как лечат варикоз пищевода?
Цели лечения:
- Предотвратить дальнейшее повреждение печени.
- Предотвратить кровотечение из варикозно расширенных вен.
- Остановите кровотечение, если оно произойдет.
Профилактика поражения печени
Людям с заболеваниями печени необходимо избегать токсинов, которые вызывают дополнительную нагрузку на печень и наносят ей больший ущерб. Вот несколько советов по поддержанию здоровья печени:
- Избегайте любых алкогольных напитков.
- Ограничьте использование бытовых чистящих средств и химикатов.
- Придерживайтесь более здоровой диеты с низким содержанием жиров и высоким содержанием фруктов и овощей, цельнозерновых и нежирных белков.
- Поддерживайте здоровую массу тела (избыток жира оказывает нагрузку на печень).
Предотвращение кровотечения
Лекарства для снижения артериального давления в воротной вене могут снизить риск кровотечения. Чаще всего используются препараты из группы, называемой бета-блокаторами. К ним относятся пропранолол (Inderal®), надолол (Corgard®) и карведилол (Coreg®).
Пациенты с высоким риском кровотечения могут проходить профилактическое лечение с использованием тех же методов, которые используются для остановки кровотечения.Чаще всего используется метод перевязки варикозно расширенных вен.
Остановка кровотечения
Кровотечение из варикозно расширенных вен пищевода – это неотложная ситуация, требующая немедленного лечения. В больнице пациенты получают большое количество жидкости и крови, чтобы восполнить утраченное.
Для остановки кровотечения из варикозно расширенных вен доступны два различных нехирургических метода лечения – перевязка варикозно расширенных вен, выполняемая с помощью эндоскопа, и трансъюгулярное внутрипеченочное портосистемное шунтирование (TIPS), выполняемое радиологом с использованием рентгеновского излучения.
- Перевязка варикозно расширенных вен : В этой процедуре крошечные эластичные ленты оборачиваются вокруг варикозных вен, чтобы перекрыть кровоток через варикозные узлы. Это можно сделать на любом количестве вен за один сеанс. После того, как кровотечение остановлено, пациентам может быть назначен препарат для предотвращения повторного кровотечения. Перевязку варикозно расширенных вен следует повторять каждые 4 недели до тех пор, пока кровотечение из варикозно расширенных вен не прекратится. После этого верхнюю эндоскопию следует повторять каждые 6–12 месяцев, чтобы убедиться, что варикозное расширение вен не появилось повторно.Осложнения, связанные с перевязкой варикозно расширенных вен, включают потерю крови, прокол пищевода, затрудненное глотание, аномальное сердцебиение, инфекцию, лихорадку и пониженную или поверхностную частоту дыхания. Все эти осложнения редки.
- Трансъюгулярное внутрипеченочное портально-системное шунтирование (TIPS) : это процедура для снижения портального кровяного давления, которую можно использовать у пациентов с варикозным расширением вен пищевода, кровоточащими из-за тяжелого цирроза. Небольшая тонкая трубка, называемая катетером, вводится в вену на шее.Катетер вводят через тело в печень, где находятся печеночная и воротная вены. (Печеночная вена переносит кровь от печени обратно к сердцу.) Затем через катетер пропускают проволоку. Он используется, чтобы протыкать печеночную вену к воротной вене. Проволока удаляется, и стент (крошечная проволочная катушка) пропускается через катетер к месту соединения. Стент помещается в новый канал между воротной и печеночной венами. Стент удерживает место соединения открытым, чтобы кровь могла легче течь из воротной вены в печеночную вену и выходить из печени.Это снижает давление в воротной вене, что снижает давление в варикозных узлах, что снижает риск кровотечения. TIPS могут быть очень эффективными для предотвращения кровотечений, но они также могут вызывать серьезные осложнения, особенно у пациентов с запущенным заболеванием печени, включая спутанность сознания и печеночную недостаточность.
Перспективы / Прогноз
Каков долгосрочный прогноз для людей с кровотечением из варикозно расширенных вен пищевода?
Кровотечение из варикозно расширенных вен пищевода является опасным для жизни состоянием и может быть смертельным у 50% пациентов.Люди, у которых был эпизод кровотечения из варикозно расширенных вен пищевода, подвергаются риску повторного кровотечения.
Лечение с помощью перевязки варикозно расширенных вен эффективно купирует эпизоды первого кровотечения примерно у 90% пациентов. Однако примерно у половины пациентов, которым была проведена перевязка варикозно расширенных вен, будет еще один эпизод кровотечения в течение 1-2 лет. Прием лекарств и изменение образа жизни могут помочь снизить риск рецидива (возобновления кровотечения).
Пересадка печени может быть вариантом для пациентов с тяжелым циррозом печени и / или повторяющимися эпизодами кровотечения из варикозно расширенных вен.Трансплантация печени выполняется только в избранных центрах по всей стране, которые соответствуют очень строгим критериям.
Осложнения цирроза: кровотечение из варикозно расширенных вен | Детская больница CS Mott
Обзор темы
У людей с циррозом высокое кровяное давление в венах, которые переносят кровь из кишечника в печень (портальная гипертензия), вызывает множество проблем. Одним из серьезных осложнений портальной гипертензии является кровотечение из варикозно расширенных вен.
Когда артериальное давление повышается в системе воротной вены, вены пищевода, желудка и прямой кишки расширяются, чтобы обеспечить блокировку кровотока через печень.Наличие расширенных вен (варикозного расширения вен) обычно не вызывает никаких симптомов. (Их можно найти во время эндоскопического исследования пищевода.) Варикозное расширение вен пищевода развивается у примерно 50-60 из 100 людей с циррозом. сноска 1
По мере того, как кровяное давление в системе воротной вены продолжает расти, стенки этих расширенных вен становятся тоньше, что приводит к разрыву вен и кровотечению. Это называется кровотечением из варикозно расширенных вен.
- Чем серьезнее повреждение печени и чем больше варикозное расширение вен, тем выше риск кровотечения из варикозно расширенных вен.
- Примерно 30 из 100 людей, у которых развивается варикозное расширение вен, имеют эпизод кровотечения в течение 2 лет после установления диагноза варикозного расширения вен. сноска 2
Варикозное кровотечение может быть опасным для жизни. После однократного кровотечения из варикозно расширенных вен существует высокий риск повторного кровотечения. Вероятность повторного кровотечения наиболее высока сразу после остановки первого кровотечения и постепенно снижается в течение следующих 6 недель. Если варикозное расширение вен не лечить, кровотечение может привести к летальному исходу.
Лечение кровотечения из варикозно расширенных вен может быть сложной задачей и может включать в себя лекарственные препараты, а также эндоскопическую терапию (эндоскопическое бандажирование или склеротерапию).Для получения дополнительной информации см .:
Американский колледж гастроэнтерологии рекомендует эндоскопический скрининг варикозного расширения вен всем, у кого был диагностирован цирроз печени. Если ваш первый тест не обнаружит варикозного расширения вен, вы можете пройти повторное обследование через 2–3 года. сноска 2 Вам может потребоваться более частое обследование, если у вас большие варикозные узлы или уже был эпизод кровотечения из варикозно расширенных вен, даже если вы лечите варикозные узлы бета-адреноблокаторами или варикозным бандажом. Рецидивирующее кровотечение является обычным явлением.
Ссылки
Ссылки
- Шах В.Х., Камат П.С. (2010). Портальная гипертензия и желудочно-кишечные кровотечения. В M Feldman et al., Eds., , «Болезни желудочно-кишечного тракта и печени» Слейзенгера и Фордтрана , 9-е изд., Том. 2. С. 1489–1516. Филадельфия: Сондерс.
- Garcia-Tsao G, et al. (2007). Профилактика и лечение варикозно расширенных вен желудочно-кишечного тракта и кровотечения из варикозно расширенных вен при циррозе печени. Американский журнал гастроэнтерологии , 102 (9): 2086–2102.
Шах В.Х., Камат П.С. (2010). Портальная гипертензия и желудочно-кишечные кровотечения. В M Feldman et al., Eds., , «Болезни желудочно-кишечного тракта и печени» Слейзенгера и Фордтрана , 9-е изд., Том. 2. С. 1489-1516. Филадельфия: Сондерс.
Garcia-Tsao G, et al. (2007). Профилактика и лечение варикозно расширенных вен желудочно-кишечного тракта и кровотечения из варикозно расширенных вен при циррозе печени. Американский журнал гастроэнтерологии , 102 (9): 2086-2102.
Симптомы варикозного расширения вен пищевода и эндоскопическое лечение цирроза
Варикозное расширение вен – это расширенные кровеносные сосуды пищевода или желудка, вызванные портальной гипертензией. Они не вызывают никаких симптомов, если не разрываются и не кровоточат, что может быть опасно для жизни.
Лицам с симптомами кровотечения из варикозно расширенных вен следует немедленно обратиться за лечением.Врачи могут остановить кровотечение и предотвратить повторное появление варикозного расширения вен.
Симптомы кровотечения из варикозно расширенных вен
Симптомы включают:
Кровотечение из варикозно расширенных вен требует неотложной медицинской помощи. Если кровотечение не остановить быстро, человек может впасть в шок или умереть.
Даже после остановки кровотечения могут возникнуть серьезные осложнения, такие как пневмония, сепсис, печеночная недостаточность, почечная недостаточность, спутанность сознания и кома.
Причина кровотечения из варикозно расширенных вен
Портальная гипертензия – это повышение давления в воротной вене (вене, по которой кровь от органов пищеварения поступает в печень).Часто это происходит из-за рубцевания печени или цирроза.
Это повышенное давление в воротной вене заставляет кровь отталкиваться от печени к более мелким кровеносным сосудам, которые не могут справиться с увеличенным количеством крови. Это приводит к развитию больших опухших вен (варикозного расширения вен) в пищеводе, желудке, прямой кишке и пупочной области (вокруг пупка). Варикозное расширение вен хрупкое и может легко разорваться, что приводит к большой кровопотере.
Лечение кровотечения из варикозно расширенных вен
В тяжелых случаях человеку может потребоваться временно поставить дыхательный аппарат, чтобы предотвратить наполнение легких кровью.Немедленно назначают антибиотики, чтобы снизить риск сепсиса, опасной для жизни инфекции крови.
Помимо острой необходимости остановить кровотечение, лечение также направлено на предотвращение повторного кровотечения. Процедуры, которые помогают лечить кровотечение из варикозного узла, включают:
- Бандаж. Гастроэнтеролог накладывает маленькие резинки прямо на варикозные узлы. Это остановит кровотечение и избавит от варикозного расширения вен.
- Склеротерапия. Гастроэнтеролог вводит в варикозные узлы раствор для свертывания крови, вместо того, чтобы перевязать их.
- Трансъюгулярный внутрипеченочный портосистемный шунт (TIPS). Радиологическая процедура, при которой стент (трубчатое устройство) помещается в середину печени. Стент соединяет печеночную вену с воротной веной. Эта процедура выполняется путем введения катетера через вену на шее. Это делается для того, чтобы снизить высокое кровяное давление в воротной вене и печени.
- Дистальный спленоренальный шунт (DSRS). Хирургическая процедура, при которой селезеночная вена соединяется с веной левой почки, чтобы снизить давление в варикозных узлах и остановить кровотечение.
- Трансплантат печени . Трансплантация печени может быть сделана в случае терминальной стадии заболевания печени.
- Деваскуляризация. Хирургическая процедура по удалению кровотечения из варикозно расширенных вен. Эта процедура выполняется, когда TIPS или хирургическое шунтирование невозможно или не удается остановить кровотечение.
- Перерезка пищевода. Хирургическая процедура, при которой пищевод рассекают, а затем снова сшивают скобами после того, как будут перевязаны варикозные узлы.Иногда кровотечение по линии скрепления.
Можно ли предотвратить кровотечение из варикозно расширенных вен?
Лечение основной причины кровотечения из варикозно расширенных вен может помочь предотвратить их возвращение. Раннее лечение заболеваний печени может предотвратить их развитие.
Некоторые лекарства, включая класс сердечных препаратов, называемых «бета-блокаторами», могут снизить повышенное давление в воротной вене и снизить вероятность кровотечения.

 Альтернативное направление – назначение комбинации октреотида и норадреналина (или мидодрина).
Альтернативное направление – назначение комбинации октреотида и норадреналина (или мидодрина).