Личинка трихинеллы: Что такое Трихинеллез
Что такое Трихинеллез
Трихинеллез (trichinellosis; синоним: трихиноз) – острый гельминтоз человека и млекопитающих, важное медико-социальное значение которого обусловлено тяжестью клинических проявлений, нередко потерей трудоспособности, а в отдельных случаях летальным исходом. Для инвазии характерна лихорадка, мышечные боли, отек лица, кожные высыпания, высокая эозинофилия, а при тяжелом течении – поражение миокарда, легких, центральной нервной системы.
Что провоцирует / Причины Трихинеллеза:
Трихинеллы – мелкие, почти нитевидные гельминты (thrix – волос), покрытые поперечно-исчерченной кутикулой. Тело Т. spiralis округлое, несколько суженное к переднему концу. Длина половозрелого самца 1,2-2 мм при ширине 0,04-0,05 мм. Длина половозрелой самки до оплодотворения 1,5-1,8 мм, после оплодотворения длина ее увеличивается до 4,4 мм.
Установлено существование двух типов очагов трихинеллеза: природных и синантропных.
Существует прямая и обратная связь между природными и синантропными очагами. Инвазия из природных очагов заносится в синантропные двумя путями: человеком, который добывает на охоте инвазированных диких животных и скармливает их остатки домашним животным, и дикими синантропными (крысы, мыши), которые мигрируют весной в природные очаги, а осенью возвращаются назад.
В мышцах животных личинки сохраняют инвазионность годами, а в трупном материале они погибают под воздействием очень высокой или низкой температуры (-40, -50°С), могут переносить условия арктической зоны.
Источником инвазии для человека служат пораженные трихинеллезом домашние и дикие животные. Чаще всего это свиньи, дикий кабан, бурый и белый медведь, нутрия, барсук, лиса, для некоторых народностей – собаки.
Механизм заражения пероральный. Восприимчивость людей к трихинеллезу очень велика. Для того чтобы получить тяжелое заболевание, достаточно съесть 10-15 г трихинеллезного мяса. Заражение происходит обычно при употреблении в пищу сырого или недостаточно проваренного мяса пораженных трихинеллезом животных, чаще всего мяса, сала, окорока, бекона корейки, грудинки, колбасы, изготовленных из инвазированной свинины, а также пораженного трихинеллами мяса диких животных (медведя, дикого кабана, барсука).
Заболеваемость трихинеллезом обычно носит групповой характер. Заболевают члены одной семьи, лица, участвующие в одном праздничном застолье, охотничьей трапезе, использовавшие в питание мясо одного и того же трихинеллезного животного, не прошедшего предварительного санитарно-ветеринарного контроля.
Личинки трихинелл погибают при достижении температуры внутри куска мяса не менее 80°С. Соление и копчение мяса на инкапсулированные личинки не действует.
Установлен сезонный характер групповых вспышек. В синантропных очагах они в большинстве случаев связаны с осенним периодом – периодом забоя свиней и заготовки мясных продуктов.
Вспышки трихинеллеза в природных очагах связаны с сезоном охоты – осенне-зимним периодом. В связи с существующим браконьерством они могут возникать в любое время года.
Формированию очагов трихинеллеза способствует неправильное ведение свиноводства: свободное содержание свиней, их бродяжничество, доступ в свинарники грызунов, кошек, собак.
Жизненный цикл трихинелл
Трихинеллы являются живородящими гельминтами. Важной биологической особенностью является также то, что один и тот же организм становится сначала окончательным, а затем промежуточным хозяином. Трихинеллы имеют самых разных хозяев, кроме человека. Они паразитируют у многих млекопитающих – свиней, кабанов, медведей, волков, лисиц, барсуков, собак, кошек, а также у грызунов, насекомоядных и морских млекопитающих.
В половозрелой стадии гельминты паразитируют в стенке тонкого кишечника, а в личиночной – в поперечно-полосатой мускулатуре, кроме мышцы сердца.
Человек заболевает трихинеллезом при употреблении в пищу зараженной инкапсулированными личинками свинины или мяса диких животных. В процессе пищеварения личинки освобождаются из капсул и уже через час внедряются в слизистую оболочку, достигая подслизистого слоя тонкого кишечника.
Через сутки они превращаются в самцов и самок. Половозрелые особи с помощью головного стилета прикрепляются к слизистой оболочке кишок, где затем и копулируют.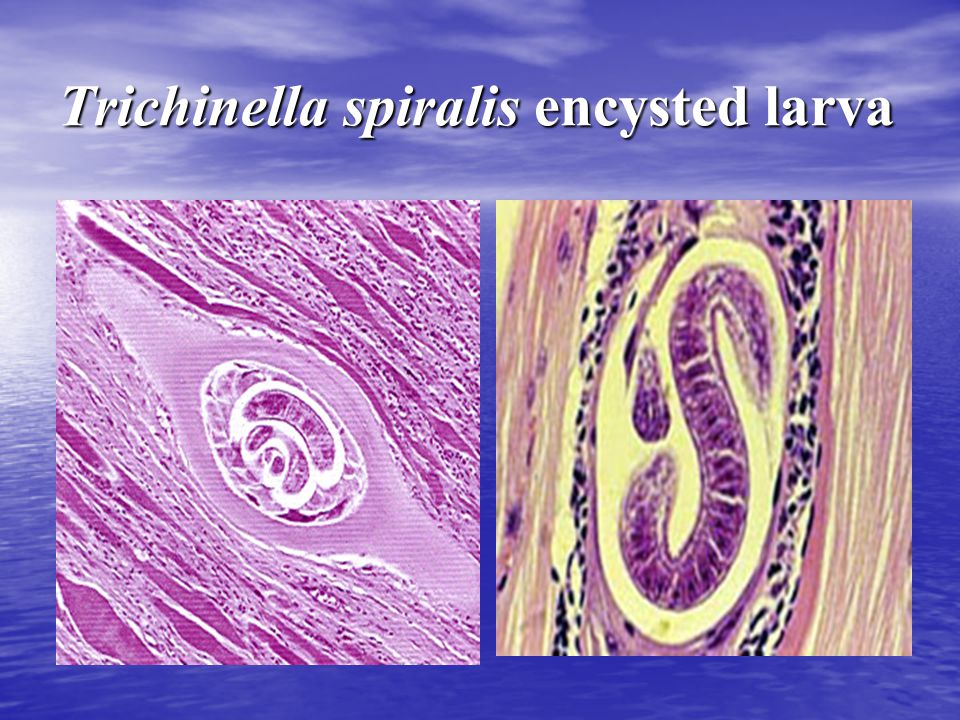
В организме разных животных самка трихинелл паразитирует от 10 до 56 дней, рожая от 200 до 2000 живых личинок. В течение всего периода паразитирования в кишечнике человека (не более 42-56 дней) одна самка рожает в среднем 1500 личинок.
Личинки проникают через слизистую оболочку кишечника в лимфатические, затем кровеносные сосуды и током крови разносятся по организму хозяина. На 5-8-й день личинки попадают в скелетную поперечно-полосатую мускулатуру. При помощи выделяемой ими гиалуронидазы они проникают в сарколемму мышечного волокна, где происходит их дальнейшее развитие, уже в организме, который стал для возбудителя промежуточным хозяином. Через 18-20 дней после заражения личинка в мышцах удлиняется до 0,8 мм, достигает инвазионной стадии и начинает свертываться спиралью.
Патогенез (что происходит?) во время Трихинеллеза:
Патогенез трихинеллеза сложен, представляя комплекс патологических реакций, пусковым механизмом которых является возбудитель.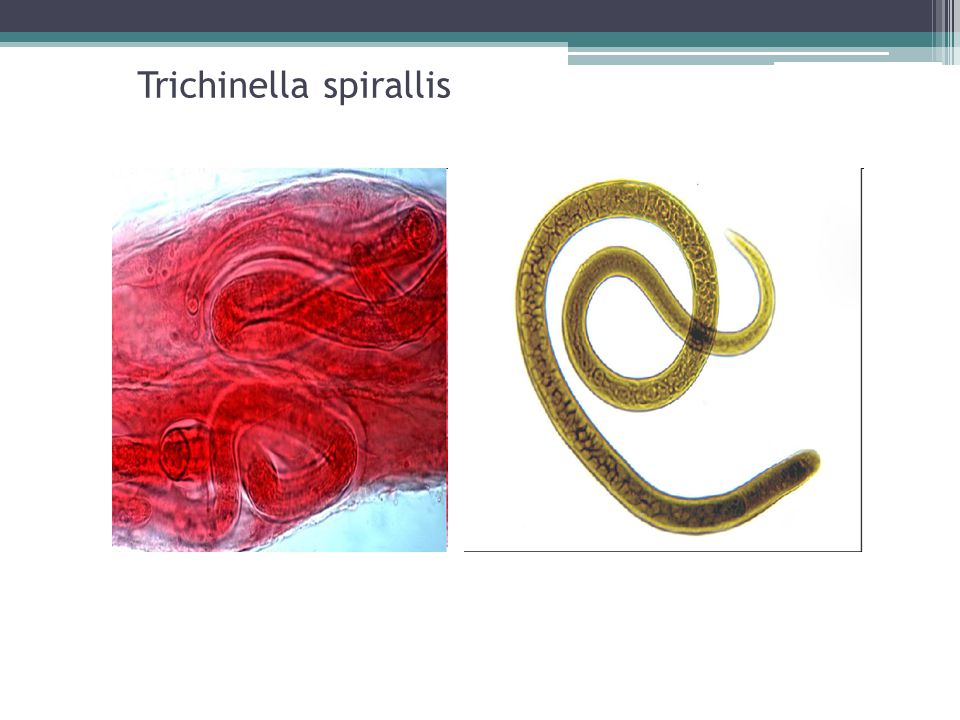
Как известно, весь биологический цикл трихинеллы проходит в организме одного хозяина, в данном случае, – человека, в котором последовательные стадии роста гельминта имеют разную локализацию: инвазионная личинка в просвете, а затем в слизистой оболочке тонкого кишечника; растущая, а затем взрослая особь в ткани тонкого кишечника; мигрирующая личинка – в кровеносном русле и лимфе; мышечная личинка – в поперечнополосатых мышцах. В результате – продукты метаболизма и частичного распада, особенно личиночных и растущих особей попадают непосредственно в ткани. Они представляют собой паразитарные антигены, обладающие высокой сенсибилизирующей активностью.
Аллергическая природа трихинеллеза лежит в основе его патогенеза. Н. Н. Озерецковская выделяет три фазы развития патологического процесса: ферментативно-токсическую (1-2 неделя после заражения), аллергическую (с конца 2-ой -3-4 недели после заражения) и иммунопатологическую.
Ферментативно-токсическая фаза связана с проникновением инвазионных личинок трихинелл в слизистую кишечника и образованием взрослых гельминтов, под воздействием ферментов и метаболитов которых в кишечнике развивается воспалительная реакция.
Вторая – аллергическая фаза трихинеллеза – характеризуется возникновением общих аллергических проявлений в виде лихорадки, миалгий, отеков, кожных высыпаний, конъюнктивита, катарального легочного синдрома и др. Уже к концу первой недели сформировавшиеся взрослые трихинеллы начинают отрождать юных личинок, которые через лимфу и кровь мигрируют в поперечно-полосатую мускулатуру. Подавленная защитная реакция хозяина в связи с иммуносупрессивным действием взрослых паразитов не препятствует активной циркуляции личинок.
Однако к концу второй – на третьей неделе болезни в сыворотке инвазированного нарастает уровень специфических антител и развивается бурная аллергическая реакция.
Бурное аллергическое воспаление в тонком кишечнике способствует гибели взрослых трихинелл, формированию гранулем вокруг личинок трихинелл в мышцах, из которых впоследствии образуются фиброзные капсулы, препятствующие поступлению антигенов паразита в организм хозяина.
Степень выраженности иммунологических реакций зависит от дозы антигена и иммунореактивности организма хозяина, от степени адаптации паразита к хозяину. Увеличение дозы заражения обусловливает нарастание интенсивности кишечной и мышечной инвазии, что в свою очередь приводит к усилению тяжести болезни, угнетению иммунологических процессов. Это сопровождается системным поражением органов и тканей в результате сенсибилизации организма не только продуктами метаболизма гельминтов, но и продуктами распада поврежденных или разрушенных тканей хозяина. Эта фаза проявляется лихорадкой, мышечными болями, отеками, конъюнктивитом, респираторными нарушениями.
Иммунопатологическая фаза
трихинеллеза, как правило, связанная с интенсивным заражением, характеризуется появлением аллергических системных васкулитов и тяжелых органных поражений.В миокарде, мозге, легких, печени и в других органах возникают узелковые инфильтраты. Трихинеллез осложняется тяжелым аллергическим диффузно-очаговым миокардитом, менингоэнцефалитом, очаговой пневмонией и другими не менее тяжелыми органными поражениями, которые могут сочетаться друг с другом, сопровождаясь высокой лихорадкой, сильными мышечными болями, кожными высыпаниями, распространением отеков.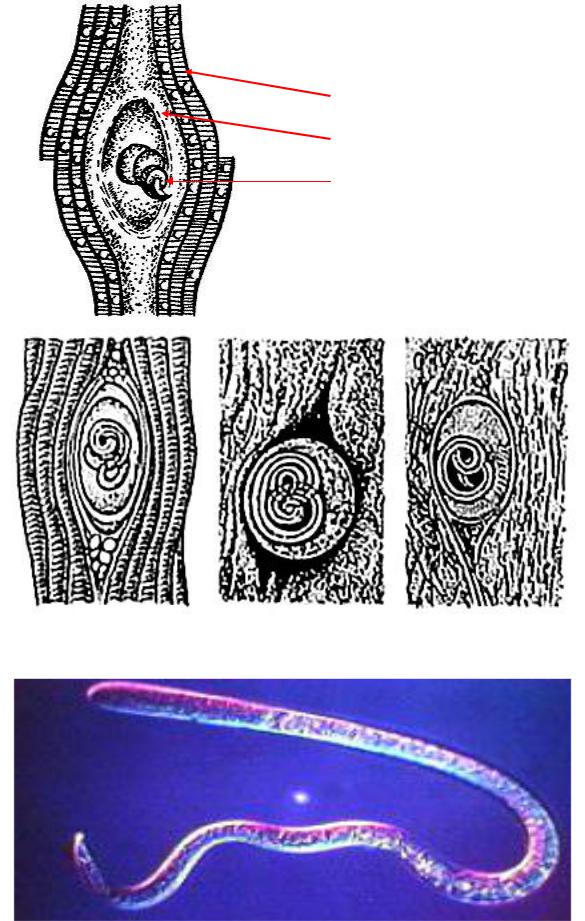
К 5-6-й неделям после заражения воспалительный процесс в паренхиматозных органах сменяется дистрофическими нарушениями, которые восстанавливаются медленно, на протяжении 6-12 месяцев.
Симптомы Трихинеллеза:
Характерными клиническими проявлениями трихинеллеза являются лихорадка, преимущественно ремиттирующего типа, отеки лица, мышечные боли, кожные высыпания, высокая эозинофилия.
При низкой интенсивности инвазии возможно субклиническое, бессимптомное ее течение, когда единственным признаком, свидетельствующим о заражении, является эозинофильная реакция крови.
Клинически выраженные варианты трихинеллеза различны по тяжести течения, длительности инкубационного периода продолжительности лихорадки и исходу. В соответствии с этим в общепринятой клинической классификации выделены следующие четыре формы инвазии: стертая, легкая, средней тяжести и тяжелая.
В течении инвазии выделяют периоды: инкубационный, острых проявлений, осложнений, реконвалесценции и рецидивов.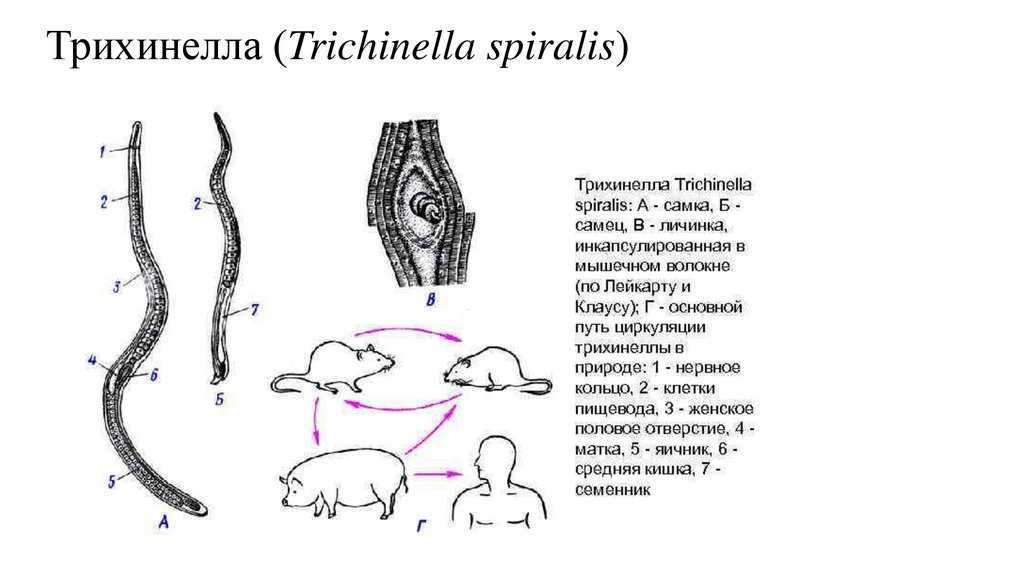
Инкубационный период трихинеллеза в среднем составляет 10 – 25 дней. Однако при заражении природными штаммами возбудителя инкубационный период удлиняется до 40 – 45 суток. Установлено, что продолжительность инкубации обратно пропорциональна тяжести течения болезни: при тяжелом течении она составляет 7-10 дней, а при особо злокачественном сокращается до 3 – 1.
При стертой форме трихинеллеза инкубационный период продолжается от 4-х до 5-ти недель. Эта форма инвазии протекает без ярко выраженных симптомов и трудна для диагностики. Основные симптомы болезни: субфебрильная лихорадка, легкие мышечные боли, пастозность лица, недомогание. В периферической крови эозинофилия до 7 – 12% на фоне нормального содержания лейкоцитов. Продолжительность болезни не более одной недели, за это время все проявления, кроме эозинофилии, проходят.
Стертое и субклиническое течение инвазии регистрируется у 20 – 30% заразившихся трихинеллезом в каждой вспышке.
При легкой форме трихинеллеза инкубационный период продолжается 4 – 5 недель.
Заболевание начинается остро с повышения температур до 38 – 39° С, головной боли, недомогания. Температура быстра снижается до субфебрильной и сохраняется на протяжении 1 недели. Боли в икроножных, поясничных, жевательных мышцах, отек век, одутловатость лица («одутловатка») появляются с первых дней болезни и более выражены. Эозинофилия пepиферической крови в пределах 10 – 20%.
Все болезненные явления могут пройти самостоятельно в течение 1- 2 недель. Умеренная эозинофилия крови сохраняется до 1 – 3 месяцев.
При средней тяжести трихинеллеза инкубационный период продолжается от 2 до 3 недель. Эта форма инвазии отличается более выраженной симптоматикой, соответствующей синдрому общих аллергических проявлений.
Характерно острое начало болезни с повышения температуры до 39 – 40° С. На высоком уровне она сохраняется несколько часов, затем на уровне 38 – 38,5° С держится на протяжении первой недели, переходя в субфебрильную на второй.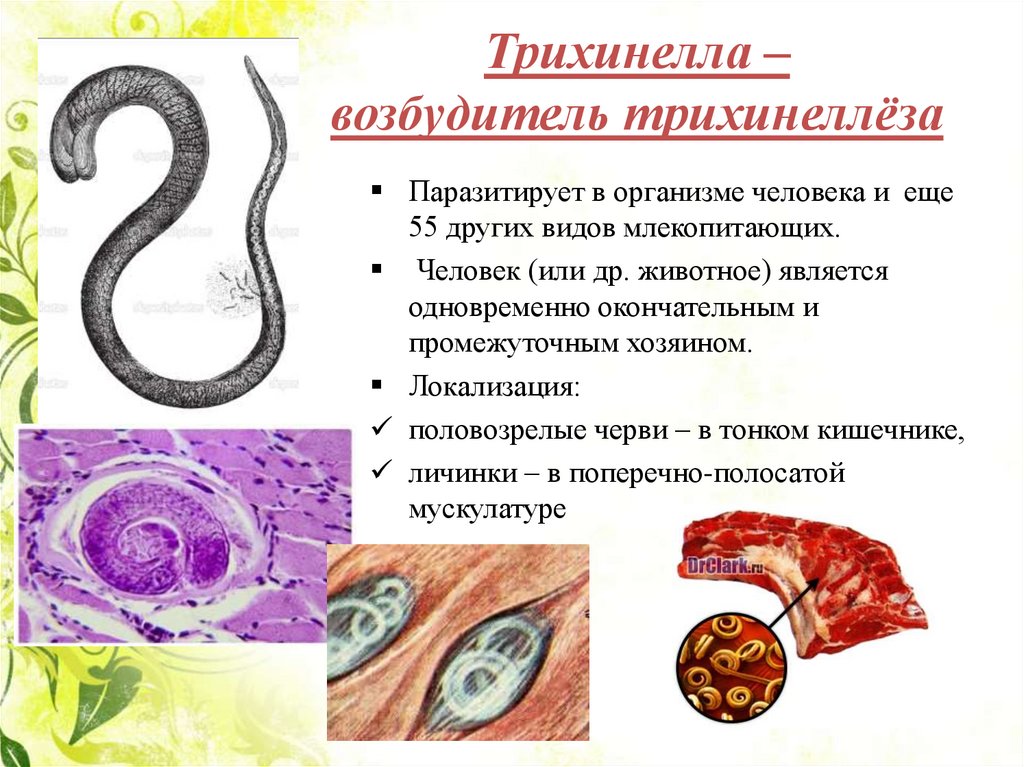
Лихорадочный период сопровождается интенсивными болями в икроножных, поясничных, затылочных, жевательных мышцах.
В качестве характерных симптомов отмечены выраженные отеки век лица, одутловатость, конъюнктивиты. У части больных на фоне лихорадки появляются кожные высыпания макуло-папулезного или геморрагического характера.
Примерно у 1/3 больных возникает бронхолегочная патология. Клиническая симптоматика у таких больных проявляется воспалением верхних дыхательных путей, бронхитом, пневмонией, плевритом. Особенностью легочной патологии при трихинеллезе, как и при других гельминтозах, является мигрирующий характер «летучих» инфильтратов при рентгенологическом и аускультативном обследованиях.
Во время лихорадки нарастают симптомы поражения сердечно-сосудистой системы: тахикардия, глухость сердечных тонов, систолический шум на верхушке. На ЭКГ определяются изменения, отражающие нарушения обменного или дистрофического характера. Больные жалуются на сердцебиение и одышку, появляющиеся при любом физическом напряжении.
У некоторых больных заболевание сопровождается симптомами поражения желудочно-кишечного тракта. Боли в животе, тошноту, рвоту, поносы отмечают 20 – 25% больных.
Увеличение лимфатических узлов, селезенки, чаще наблюдаемые у детей, подтверждает вовлечение в процесс ретикулоэндотелиальной системы.
Выявляется диспротеинемия: с одной стороны, отмечается общая гипопротеинемия и гипоальбуминемия, с другой – повышение альфа-2-глобулинов и гамма-глобулинов. Характерным симптомом является альдолаземия до 25 – 40 Е, СОЭ, замедленная в начальном периода болезни, на высоте лихорадки нарастает эозинофилия до 25 – 40% на фоне лейкоцитоза.
Клинические проявления при трихинеллезе средней тяжести достигают максимума к концу первой недели, заканчивается болезнь за 3-4 недели. Остаточные явления в виде астенизации мышечных болей могут сохраняться на протяжении 1-2 месяцев, а эозинофилия еще длительнее. После лечения глюкокортикоидными гормонами длительность острой фазы сокращается, но период выздоровления затягивается до 4 – 6 месяцев.
Легкое и средней тяжести течение трихинеллеза регистрируется у 50-60% заразившихся в каждой вспышке.
При тяжелой форме трихинеллеза инкубационный период короткий – 7-10 дней, при особо тяжелом течении сокращается до 3-1 суток.
Болезнь нередко начинается нетипично, напоминая грипп, ОРЗ, пищевое отравление, сыпной или брюшной тиф. С первых дней болезни выражены явления общей интоксикации, поражения центральной нервной системы. Температура, постепенно повышаясь до 40-41 °С, держится на протяжении 2-3 недель. Сильные головные боли, бред, возбуждение, бессонница, явления менингизма на фоне нарастающих мышечных болей и выраженных отеков сопровождают лихорадку.
Мышечные боли приобретают распространенный характер. Они возникают в икроножных, глазных, жевательных мышцах, а далее распространяются на мышцы поясницы, плечевого пояса, приобретают интенсивный характер и нередко в этих случаях сопровождаются контрактурами, ограничением подвижности до полного обездвижения больного.
Отеки распространяются на туловище и конечности, а также рыхлую клетчатку внутренних органов, оболочки мозга и паренхиму. Это приводит к функциональным нарушениям центральной нервной системы, хемозу, экзофтальму, диплопии и другим проявлениям.
На коже лица, туловища, разгибательных поверхностей нечностей появляются полиморфные сыпи эритематозно-папулезного характера, а в особо тяжелых случаях – геморрагичего по типу геморрагического васкулита.
Для этой формы трихинеллеза характерна разнообразная, тяжелая, нередко с плохим прогнозом органная и системная патологии.
Часто возникает сердечно-сосудистая патология, что проявляется гипотонией, тахикардией и нарушением ритма. Отмечается приглушение тонов сердца, признаки сердечной недостаточности – картина миокардита. ЭКГ почти у всех больных показывает диффузные изменения миокарда, коронарные нарушения с развитием недостаточности кровообращения.
Страдают органы дыхания: бронхиты с астматическим компонентом, очаговые бронхопневмонии с летучим характером инфильтратов и другие нарушения выявляются у таких больных довольно часто.
Одним из вариантов тяжелого течения трихинеллеза является абдоминальный синдром, при котором на фоне лихорадки и других проявлений болезни возникают боли в животе, тошнота, рвота, жидкий стул со слизисто-кровянистыми примесями.
Язвенно-некротические поражения желудка и кишечника с перфорацией и кровотечением могут стать причиной смерти. Дистрофические нарушения печени носят доброкачественный характер, они бесследно проходят при коррегирующей терапии.
Функция почек, как правило, не нарушена, выявляется протеинурия и цилиндрурия как реакция на лихорадку.
Нередко возникают симптомы поражения центральной нервной системы, характерные для менингоэнцефалита, энцефаломиелита. Больных беспокоят сильные головные боли, бессонница, в тяжелых случаях бред, судороги, психические расстройства, эпилептические припадки.
Органные и системные поражения могут быть причиной смерти. Главной причиной летального исхода при трихинеллезе является острый аллергический миокардит. В этих случаях. У больного внезапно возникают приступы острого нарушения сердечной деятельности с тахикардией, аритмией, гипотонией, и ЭКГ отражает диффузное поражение миокарда и коронарную патологию.
В этих случаях. У больного внезапно возникают приступы острого нарушения сердечной деятельности с тахикардией, аритмией, гипотонией, и ЭКГ отражает диффузное поражение миокарда и коронарную патологию.
На втором месте среди причин летальности при трихинеллезе стоит пневмония, иногда сопровождающаяся астмоидным бронхитом, плевритом. Инфильтраты резистентны к антибиотикам, но быстро исчезают при назначении глюкокортикоидных гормонов.
Грозным осложнением, занимающим третье место среди причин смерти больных трихинеллезом, является поражение центральной нервной системы. Это осложнение, как и легочный синдром, чаще встречается у мужчин. Психозы, тяжелые истерии, эпилептиформные приступы, парезы и параличи свидетельствуют о глубоких диффузно-очаговых поражениях головного и спинного мозга, связанных с развитием неспецифического васкулита, реже с тромбозами крупных сосудов.
У некоторых больных в результате нарушений гемостаза, системы свертываемости, внутрисосудистой коагуляции возникают флебиты, тромбозы сосудов конечностей.
Органные поражения чаще развиваются на 3-4-й, реже на 2-5-й неделях после заражения.
Эозинофилия достигает 25-40% на фоне лейкоцитоза. Однако при очень тяжелых формах в терминальном периоде резко снижается до анэозинофилии. Тяжелое течение трихинеллеза регистрируется у 10-30% заразившихся в каждой вспышке.
Клинические и лабораторные данные свидетельствуют о более легком течении трихинеллеза у детей, о меньшей выраженности у них аллергических проявлений, меньшем поражении сердечно-сосудистой системы.
Инкубационный период трихинеллеза у детей, как правило, длительнее, чем у взрослых. Температурная реакция выражена слабее, короткая – до двух недель – лихорадка встречается чаще, чем длительная ремиттирующая.
Основные клинические проявления трихинеллеза – отечный, мышечный и болевой синдромы – у детей выражены также слабее, чем у взрослых. Преобладают легкие формы болезни, чаще стертая и субклиническая.
Лабораторные показатели у детей характеризуются меньшей эозинофилией, более низким процентом положительного С-реактивного белка. Существует мнение, что более легкое течение трихинеллеза у детей по сравнению со взрослыми обусловлено выраженной иммунологической активностью организма ребенка и как следствие – ограничением развития иммунопатологических проявлений, с чем нельзя не согласиться. Кроме того, имеет значение, как правило, меньшая интенсивность заражения детей.
Существует мнение, что более легкое течение трихинеллеза у детей по сравнению со взрослыми обусловлено выраженной иммунологической активностью организма ребенка и как следствие – ограничением развития иммунопатологических проявлений, с чем нельзя не согласиться. Кроме того, имеет значение, как правило, меньшая интенсивность заражения детей.
Однако ни в коей мере нельзя исключить возможность злокачественного течения инвазии у детей с развитием тяжелого аллергического миокардита, менингоэнцефалита, даже с неблагополучным исходом.
Существуют клинические наблюдения, которые свидетельствуют о более легком течении трихинеллеза у беременных. Такие клинические критерии тяжести, как высота и продолжительность лихорадки, интенсивность и длительность мышечных болей, распространенность, локализация и время сохранения отеков, менее выражены. Осложнения встречаются реже и они выражены также слабее.
Таким образом, приведенные наблюдения свидетельствуют о том, что трихинеллез не нарушает течения беременности и не отражается на развитии плода.
Профилактика трихинеллеза
Не следует покупать мясопродукты без клейма на тушах и окороках!
Трихинеллёз | Департамент ветеринарии Томской области
Трихинеллёз – остро или хронически протекающее инвазионное заболевание человека и животных с ярко выраженными аллергическими явлениями, вызываемое круглыми червями – нематодами семейства трихинелла. В настоящее время различают следующие виды: Trichinella spiralis, Trichinella nativa , Trichinella pseudospiralis. Данный гельминтоз представляет большую опасность для человека и животных: заболевание людей протекает очень тяжело, плохо поддается лечению и часто оканчивается смертельным исходом.
Взрослые трихинеллы паразитируют в тонком отделе кишечника животных и человека, а личинки – в поперечнополосатых мышцах этих же организмов. В настоящее время зарегистрировано более 100 видов млекопитающих, которые являются хозяевами трихинелл. Наиболее часто трихинеллёз встречается у свиней, медведей, собак, волков, лисиц, кошек, крыс, мышей. К нему восприимчивы дикие кабаны, барсуки, песцы, норки, горностаи, хорьки, ежи и многие другие дикие плотоядные животные и грызуны.
Наиболее часто трихинеллёз встречается у свиней, медведей, собак, волков, лисиц, кошек, крыс, мышей. К нему восприимчивы дикие кабаны, барсуки, песцы, норки, горностаи, хорьки, ежи и многие другие дикие плотоядные животные и грызуны.
Человек заражается трихинеллёзом при употреблении в пищу сырого или недостаточно термически обработанного мяса или сала животных с мясными прожилками, чаще всего свинины, а также мяса кабана, барсука, бурого и белого медведя, мяса морских млекопитающих, содержащих личинки трихинелл. Личинки сохраняются в мышцах заражённых животных на протяжении их жизни. Могут длительное время сохраняться в трупах животных, при замораживании – десятки лет. Передача возбудителя болезни происходит между свиньями, а также между домовыми (и дикими) грызунами, собаками, кошками. Занос трихинеллёза из дикой природы связан с охотой, браконьерством, скармливанием домашним животным отбросов охоты, выпасом свиней в дикой природе.
Развитие трихинелл у человека и животных происходит однотипно и включает: кишечную фазу, миграционную фазу, мышечную фазу.
Кишечная фаза. Заражение происходит при поедании мяса, содержащего инкапсулированные личинки трихинелл. В процессе пищеварения в желудке и двенадцатиперстной кишке капсулы разрушаются. Молодые трихинеллы, находясь в просвете двенадцатиперстной кишки, созревают в течение 3-4 суток, после чего самки начинают откладывать личинки. Этот процесс длится от 10 до 45 дней, и после его окончания самки вскоре погибают. Срок кишечной стадии 42-56 дней. Самка откладывает от 1500 до 10000 личинок.
Миграционная фаза. Личинки по лимфатическим путям попадают в ток крови и разносятся по всему организму. Миграция их начинается примерно на 6 день от момента заражения.
Мышечная фаза. Оседание личинок происходит в поперечнополосатых мышцах. Первые, пока еще немногочисленные личинки появляются там уже на 6-7 день. Они распределяются неравномерно, предпочитая мимическую, дыхательную, жевательную мускулатуру, диафрагму, сгибатели конечностей. В мышцах личинки увеличиваются в размерах примерно в 10 раз, свиваются в спираль и к 17-18 дню становятся способны заражать следующего хозяина. К 3-4 неделе вокруг личинок формируются капсулы, стенка которых спустя год покрывается известью.
В мышцах личинки увеличиваются в размерах примерно в 10 раз, свиваются в спираль и к 17-18 дню становятся способны заражать следующего хозяина. К 3-4 неделе вокруг личинок формируются капсулы, стенка которых спустя год покрывается известью.
Перед употреблением мяса обязательному исследованию на трихинеллёз подлежат туши, полутуши, четвертины свиней (кроме поросят до 3-недельного возраста), кабанов, барсуков, медведей, всеядных и плотоядных животных, а также нутрий. Для исследования отбираются пробы из ножек диафрагмы, при их отсутствии – части межреберных, шейных, жевательных, поясничных, икроножных мышц, а также мышцы языка, пищевода, гортани.
Важнейшей задачей профилактики трихинеллёза является недопущение заноса инвазии из основного резервуара – природных очагов. Основное правило состоит в том, чтобы тушки несъедобных зверей и птиц, остатки съедобных хищных животных, добытые на охоте, а также погибшие от трихинеллёза домашние животные были уничтожены сжиганием.
Важную роль в системе профилактических мероприятий имеет обеспечение стойлового содержания свиней и обязательное проведение трихинеллоскопии при их убое. В случае обнаружения хотя бы одной трихинеллы в 24 мышечных срезах мясо уничтожается сжиганием или отправляется на техническую утилизацию, наружный жир перетапливается в течение 20 минут при температуре 100°С, а внутренний – может быть использован без термической обработки.
Поступившие в реализацию мясо и мясопродукты в магазинах и на рынках проходят трихинеллоскопию и не представляют опасности. Как правило, заболевания трихинеллёзом возникают вследствие использования мяса свиней, забитых в домашних условиях, кабанов, медведей, добытых на охоте и не прошедших ветеринарно-санитраную оценку в лаборатории.
В населенных пунктах должны быть оборудованы убойные пункты и биотермические ямы для утилизации отходов убоя и трупов животных, должен быть организован отлов и уничтожение бродячих собак и кошек, должны проводиться дератизационные мероприятия. Запрещается подворный убой животных без ветеринарно-санитарного контроля, а также продажа свинины, мяса диких животных без клейма ветеринарно-санитарной экспертизы.
Запрещается подворный убой животных без ветеринарно-санитарного контроля, а также продажа свинины, мяса диких животных без клейма ветеринарно-санитарной экспертизы.
Личная профилактика человека от заболевания трихинеллёзом состоит в том, чтобы употреблять в пищу только обследованное на трихинеллёз мясо свиней и диких животных. Нельзя покупать мясо этих животных или мясопродукты на случайных рынках при отсутствии ветеринарно-санитарной справки.
ВНИМАНИЕ – ТРИХИНЕЛЛЁЗ! — Информация — Новости — Главная — Официальный сайт Департамент ветеринарии Свердловской области
3 октября 2014
ВНИМАНИЕ – ТРИХИНЕЛЛЁЗ!
.
ВНИМАНИЕ – ТРИХИНЕЛЛЁЗ!
По информации ГБУСО Каменская ветеринарная станция по борьбе с болезнями животных при проведении трихинеллоскопии в пробах мяса от барсука, добытого на территории Маминского охотничьего хозяйства общественной организации “Союз охотников и рыболовов Свердловской области” (Каменский городской округ) были обнаружены личинки трихинелл. Департамент ветеринарии Свердловской области напоминает:
Трихинеллез – опасное заболевание человека и животных, вызываемое паразитированием
трихинелл – мелких червей.
Трихинеллы паразитируют у широкого круга плотоядных млекопитающих животных (как минимум 70 видов), включая домашних свиней, собак, кошек, мышевидных грызунов, а так же диких кабанов, медведей, волков, лис, барсуков, рысей, енотовидных собак и пушных зверей, являющихся источником распространения инвазии.
Домашние свиньи заражаются при поедании не обезвреженных мясных боенских отходов, павших плотоядных животных и мышевидных грызунов, дикие плотоядные при хищничестве и поедании падали.
Человек заражается при употреблении в пищу пораженного личинками трихинелл и не прошедшего достаточную термическую обработку мяса восприимчивых плотоядных животных – диких кабанов, медведей, барсуков и др. Так же известны случаи заражения трихинеллезом при употреблении сала с прожилками мышц.
Департамент ветеринарии Свердловской области напоминает:
Трихинеллез – опасное заболевание человека и животных, вызываемое паразитированием
трихинелл – мелких червей.
Трихинеллы паразитируют у широкого круга плотоядных млекопитающих животных (как минимум 70 видов), включая домашних свиней, собак, кошек, мышевидных грызунов, а так же диких кабанов, медведей, волков, лис, барсуков, рысей, енотовидных собак и пушных зверей, являющихся источником распространения инвазии.
Домашние свиньи заражаются при поедании не обезвреженных мясных боенских отходов, павших плотоядных животных и мышевидных грызунов, дикие плотоядные при хищничестве и поедании падали.
Человек заражается при употреблении в пищу пораженного личинками трихинелл и не прошедшего достаточную термическую обработку мяса восприимчивых плотоядных животных – диких кабанов, медведей, барсуков и др. Так же известны случаи заражения трихинеллезом при употреблении сала с прожилками мышц.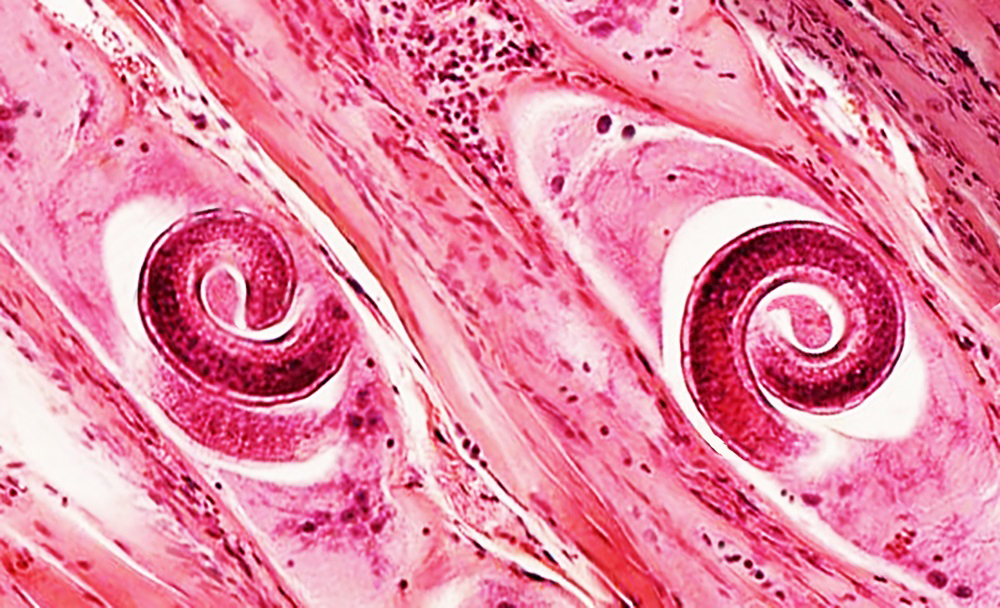 Длительность инкубационного периода с момента употребления в пищу зараженного мяса до появления первых признаков заболевания составляет от 3 до 40 дней. После попадания в кишечник через 45-60 дней личинки превращаются в половозрелых трихинелл, вновь продуцирующих личинки, которые разносятся с кровью и лимфой по организму, попадают в мышцы, в которых сохраняют жизнеспособность годами.
У человека первыми признаками болезни являются внезапный подъем
температуры, лихорадка, отек лица, боли в мышцах и суставах, расстройство пищеварения, аллергическая сыпь на коже, кровоизлияния на конъюнктиве глаз, тяжелое течение сопровождается поражением внутренних органов и центральной нервной системы. Тяжесть клинических проявлений болезни зависит от количества личинок попавших в организм.
Следует помнить, что личинки трихинелл обладают большой устой-чивостью и способны сохранять жизнеспособность при замораживании, жарке, копчении и засолке мяса.
Меры профилактики: — все туши восприимчивых к трихинеллезу животных (диких кабанов, медведей, барсуков и др.
Длительность инкубационного периода с момента употребления в пищу зараженного мяса до появления первых признаков заболевания составляет от 3 до 40 дней. После попадания в кишечник через 45-60 дней личинки превращаются в половозрелых трихинелл, вновь продуцирующих личинки, которые разносятся с кровью и лимфой по организму, попадают в мышцы, в которых сохраняют жизнеспособность годами.
У человека первыми признаками болезни являются внезапный подъем
температуры, лихорадка, отек лица, боли в мышцах и суставах, расстройство пищеварения, аллергическая сыпь на коже, кровоизлияния на конъюнктиве глаз, тяжелое течение сопровождается поражением внутренних органов и центральной нервной системы. Тяжесть клинических проявлений болезни зависит от количества личинок попавших в организм.
Следует помнить, что личинки трихинелл обладают большой устой-чивостью и способны сохранять жизнеспособность при замораживании, жарке, копчении и засолке мяса.
Меры профилактики: — все туши восприимчивых к трихинеллезу животных (диких кабанов, медведей, барсуков и др. ),
мясо которых может употребляется в пищу, подлежат обязательному диагностическому исследованию – трихинеллоскопии, в лаборатории ветеринарно-санитарной экспертизы на рынках или
в государственных ветеринарных учреждениях; — утилизация мяса, зараженного личинками трихинелл, проводится владельцем по решению
специалистов государственной ветеринарной службы; — исключается употребление в пищу не подвергавшегося трихинеллоскопии мяса диких животных, без термической обработки; — следует помнить, что любая термическая обработка мяса зараженных животных (включая проварку, прожаривание, пропекание, копчение) не гарантирует обезвреживание личинок трихинелл; — употреблять в пищу только мясо, прошедшее ветеринарно-санитарную экспертизу; — не допускают скармливания свиньям и пушным (клеточным) зверям туш убитых на охоте лисиц, волков, енотовидных собак, мелких хищников и других животных, включая птиц, восприимчивых к трихинеллезу; — территорию звероводческих хозяйств и населенных пунктов необходимо систематически очищать
от мусора и трупов мелких животных, проводить дератизацию, а также снижать популяцию бродячих плотоядных;
При обнаружении описанных симптомов после употребления в пищу свинины или
медвежатины, не подвергавшихся ветеринарно-санитарной экспертизе необходимо немедленно обратиться к врачу!
),
мясо которых может употребляется в пищу, подлежат обязательному диагностическому исследованию – трихинеллоскопии, в лаборатории ветеринарно-санитарной экспертизы на рынках или
в государственных ветеринарных учреждениях; — утилизация мяса, зараженного личинками трихинелл, проводится владельцем по решению
специалистов государственной ветеринарной службы; — исключается употребление в пищу не подвергавшегося трихинеллоскопии мяса диких животных, без термической обработки; — следует помнить, что любая термическая обработка мяса зараженных животных (включая проварку, прожаривание, пропекание, копчение) не гарантирует обезвреживание личинок трихинелл; — употреблять в пищу только мясо, прошедшее ветеринарно-санитарную экспертизу; — не допускают скармливания свиньям и пушным (клеточным) зверям туш убитых на охоте лисиц, волков, енотовидных собак, мелких хищников и других животных, включая птиц, восприимчивых к трихинеллезу; — территорию звероводческих хозяйств и населенных пунктов необходимо систематически очищать
от мусора и трупов мелких животных, проводить дератизацию, а также снижать популяцию бродячих плотоядных;
При обнаружении описанных симптомов после употребления в пищу свинины или
медвежатины, не подвергавшихся ветеринарно-санитарной экспертизе необходимо немедленно обратиться к врачу!
Назад к списку
Trichinella, IgG
Тест выявляет титр антител IgG против паразитических круглых червей Trichinella, которые вызывают у человека трихинеллез.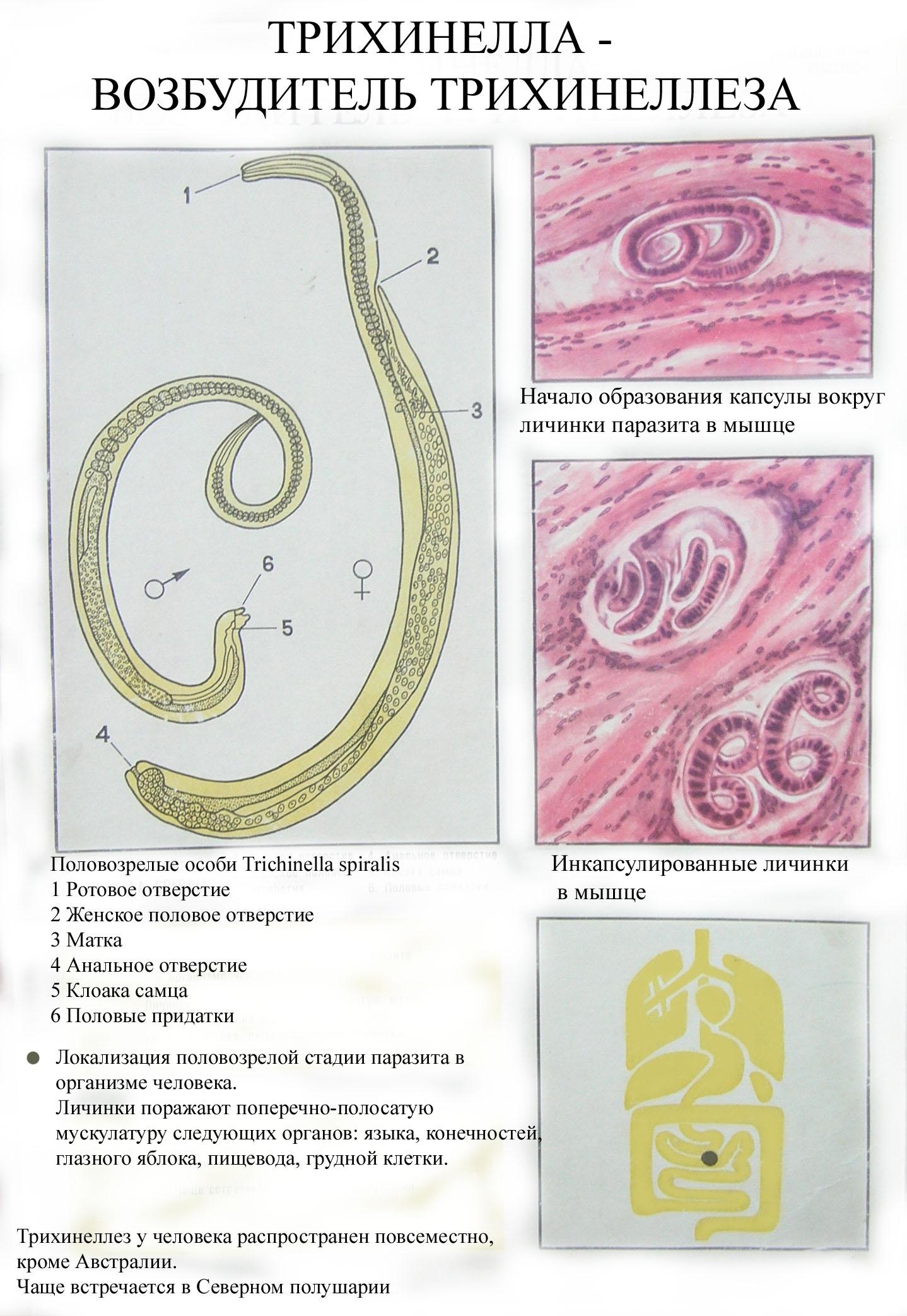
Синонимы русские
Антитела класса IgG к Trichinella, иммуноглобулины класса G к антигенам трихинелл.
Синонимы английские
Anti-Trichinella IgG, Tr. antibodies, IgG.
Метод исследования
Иммуноферментный анализ (ИФА).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Trichinella (трихинеллы) – это род паразитических круглых червей. Несколько их видов опасны для человека.
Трихинеллы паразитируют на человеке и на многих животных (свиньях, медведях, крысах, лисицах и др.). При этом в мышцах инфицированного животного присутствуют личинки трихинелл (в виде цист). Если человек съест такое мясо, то может заразиться трихинеллезом. Как правило, наиболее опасна свинина и мясо диких животных.
Чтобы предотвратить заражение, необходимо тщательно готовить мясо. При температуре кипения воды, 100 °C, трихинеллы гарантированно погибают. Однако важно следить, чтобы продукты прогревались целиком (и снаружи, и внутри).
Животные тоже инфицируются, поедая мясо. Поэтому трихинеллез в основном встречается у хищников. Свиньи часто заражаются, контактируя с крысами.
Личинки трихинелл в мясе окружены плотной капсулой, которая называется циста. Когда цисты попадают в желудок, под действием желудочного сока их оболочки растворяются. Личинки освобождаются, проникают в тонкий кишечник и через 1-2 дня превращаются во взрослых половозрелых червей.
После спаривания самки производят новое поколение личинок, которые проходят через стенку кишки и разносятся по всему организму. Внутри скелетных мышц личинки окружаются капсулой, которая потом пропитывается солями кальция и затвердевает (превращается в цисту). Тогда уже цисты сохраняются в мышцах неограниченно долго и ждут следующего хозяина.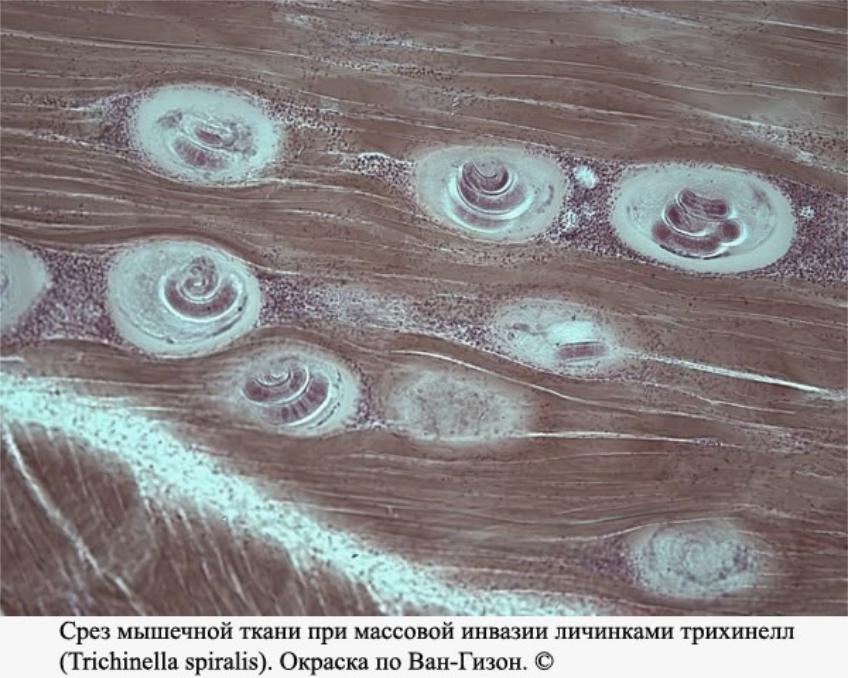
Сами взрослые особи не живут в кишечнике постоянно. Самцы погибают после спаривания, а самки исчезают через 3-5 недель после заражения (благодаря иммунному ответу организма).
Тяжесть заболевания зависит от количества трихинелл, которые попали в организм человека. Часто, если паразитов было немного, проявляется мало симптомов.
Трихинеллез протекает в две стадии. Для первой характерны признаки кишечного расстройства: умеренные боли в животе, тошнота, диарея. Они появляются в первые дни после заражения и исчезают через 10 дней (или раньше). Именно в это время в тонком кишечнике начинается развитие личинок трихинелл.
Симптомы второй стадии появляются через 2-3 недели после заражения и сохраняются несколько недель. В это время личинки разносятся по всему телу, что нарушает работу сосудов и мышц. Это может сопровождаться мышечными болями, повышенной температурой, слабостью, отеками (на лице, в частности вокруг глаз), красными точками под ногтями или в глазах.
Иногда трихинеллы повреждают сердечную мышцу, что вызывает боли в сердце, тахикардию.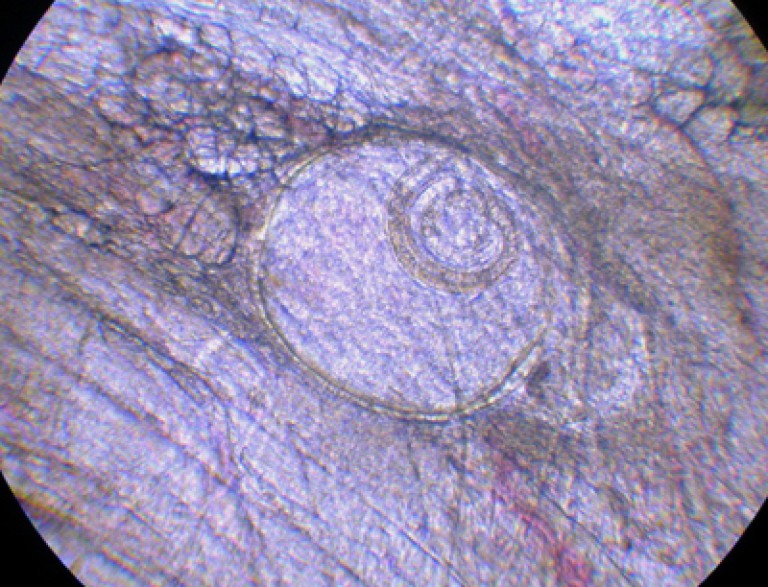 Нарушение работы нервной системы возникает в редких случаях, при сильном заражении.
Нарушение работы нервной системы возникает в редких случаях, при сильном заражении.
Со второй недели после заражения в крови увеличивается число эозинофилов (эозинофильных лейкоцитов) и повышается концентрация ферментов мышечной ткани (креатинкиназы, лактатдегидрогеназы).
В некоторых случаях для диагностики трихинеллеза используют биопсию мышц. Если трихинелл много, под микроскопом можно обнаружить их цисты.
После того как трихинеллы попадают в организм человека, он начинает с ними бороться. Один из способов борьбы – выработка антител (специальных белков иммуноглобулинов). Существует пять основных типов иммуноглобулинов: IgG, IgM, IgE, IgA и IgD.
IgE – это антитела, которые участвуют в иммунном ответе против паразитических червей. Они появляются на ранней стадии после заражения трихинеллами. Однако отмечены случаи трихинеллеза, когда анализ на IgE оказывался отрицательным. Поэтому антитела этого типа не годятся для диагностики.
Самыми подходящими антителами являются IgG.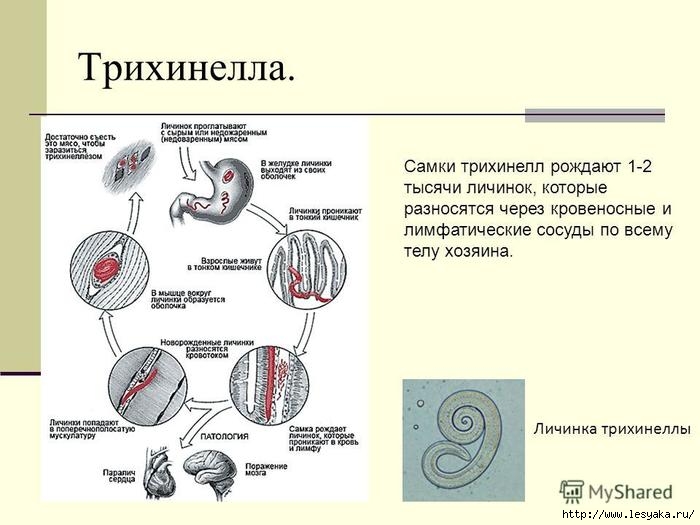 Они присутствуют в крови в наибольшем количестве (по сравнению с другими типами иммуноглобулинов). При трихинеллезе IgG можно обнаружить в крови через 12-60 дней после заражения (чем сильнее заражение, тем раньше появляются антитела). Уровень IgG остается высоким долгое время (месяцы и годы).
Они присутствуют в крови в наибольшем количестве (по сравнению с другими типами иммуноглобулинов). При трихинеллезе IgG можно обнаружить в крови через 12-60 дней после заражения (чем сильнее заражение, тем раньше появляются антитела). Уровень IgG остается высоким долгое время (месяцы и годы).
Для чего используется исследование?
Чтобы установить, был ли человек инфицирован трихинеллами.
Когда назначается исследование?
Тест назначается, если:
- проявляются симптомы болезни,
- повышено количество эозинофилов,
- повышен уровень некоторых мышечных ферментов,
- заболевший человек употреблял в пищу полусырое мясо.
Симптомы заболевания в первые 10 дней:
- боли в животе,
- тошнота,
- диарея.
Симптомы трихинеллеза через 2-3 недели после заражения:
- мышечные боли,
- повышенная температура, слабость,
- отеки (на лице, в частности вокруг глаз),
- красные точки под ногтями или на поверхности глаз.

Что означают результаты?
Референсные значения
Результат: отрицательный.
КП (коэффициент позитивности): 0 – 0,84.
Отрицательный результат
- Трихинеллеза нет.
- Недавняя инфекция. Если заражение произошло недавно (1-2 недели назад), то уровень антител может быть еще слишком низким, так что их не удалось обнаружить. В этом случае нужно повторить анализ позднее. Если и при повторном анализе IgG отсутствуют, то диагноз “трихинеллез” следует исключить.
Положительный результат
- Трихинеллез.
- Ложноположительный результат. К нему могут приводить другие паразитарные инфекции. При необходимости диагноз уточняют с помощью других методов (иммуноблота, биопсии мышц).
Что может влиять на результат?
Ложноположительному результату способствуют токсоплазмоз и некоторые другие инфекции.
Скачать пример результатаТакже рекомендуется
- Скрининговое обследование на гельминтозы (Opistorchis IgG, Toxocara IgG, Trichinella IgG, Echinococcus IgG)
Кто назначает исследование?
Врач общей практики, терапевт, инфекционист, паразитолог.
Внимание! Трихинеллез!
Трихинеллёз – болезнь человека и животных, вызываемая трихинеллами – мелкими невидимыми невооруженным глазом личинками круглого гельминта.
Заражение человека происходит при употреблении в пищу мяса и мясных продуктов (сырого фарша, сыровяленых домашней колбасы и окорока, шашлыков, жареного мяса и других), зараженных личинками трихинелл.
Заражение диких животных происходит в результате хищничества, а также поедания трупов павших животных. Домашние животные заражаются при поедании продуктов убоя, пищевых отбросов, трупов павших животных.
В трупах трихинеллезных животных личинки сохраняют жизнеспособность от 4 до 10 месяцев; при засолке мяса (в глубоких слоях) – в течение года. Трихинеллы хорошо переносят копчение, жарение, варку, обработку в микроволновой печи и замораживание.
Человек заражается трихинеллёзом при употреблении в пищу мяса животных, заражённых трихинеллами (как правило, домашние свиньи, дикие кабаны).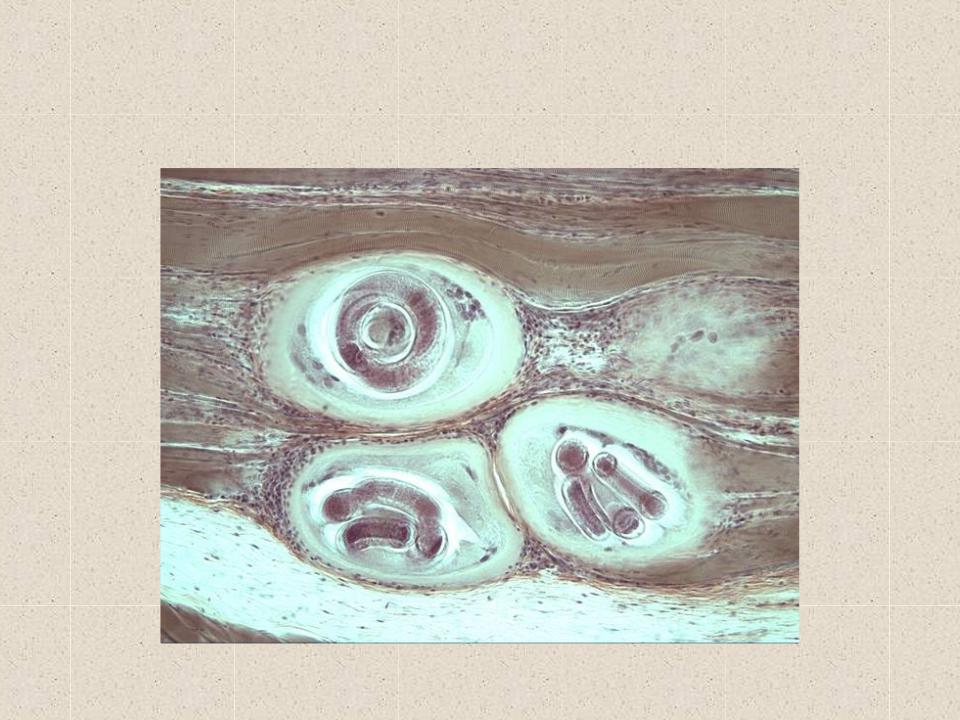 Массовое заболевание людей чаще всего наблюдаются при употреблении в пищу не прошедшего ветеринарной экспертизы мяса. Большинство таких случаев, к сожалению, случается, когда граждане забивают животных самостоятельно (дома или во время охоты) и употребляют мясо без лабораторного исследования. Нередко заражение людей происходит на свадьбах или во время других массовых мероприятий.
Массовое заболевание людей чаще всего наблюдаются при употреблении в пищу не прошедшего ветеринарной экспертизы мяса. Большинство таких случаев, к сожалению, случается, когда граждане забивают животных самостоятельно (дома или во время охоты) и употребляют мясо без лабораторного исследования. Нередко заражение людей происходит на свадьбах или во время других массовых мероприятий.
Трихинеллы отличаются большой устойчивостью к различным методам их обеззараживания. Не убивает их копчение и засолка. Остаются они живыми даже в жаренном и варёном мясе. Известны случаи заражения людей при употреблении сала (с прожилками мяса), ветчины, варёной колбасы, сосисок, пельменей, шашлыков. В кишечнике человека или животных личинки трихинелл превращаются в половозрелых самцов и самок, а те в свою очередь производят личинки, которые мигрируют через лимфатическую систему в кровь и попадают в мышцы. Взрослые трихинеллы в кишечнике живут 45-60 дней, а в мышцах – в течение многих лет.
Длительность инкубационного периода (с момента попадания в организм мяса до первых признаков заболевания) – от 3 до 40 дней.
Заболевание у человека начинается остро, обычно через 10-25 дней после заражения: повышается температура тела (иногда до 400), отмечается отёчность лица, век. Возникают боли в мышцах, появляется аллергическая сыпь. Болезнь может продолжаться до нескольких недель. Поражение сердечной мышцы в виде миокардита сопровождает все случаи тяжёлого течения и является главной причиной смерти. Кроме миокардита, заболевание может осложниться воспалением лёгких, поражением сосудов, нервов, головного мозга.
Всё мясо, поступающее в торговую сеть, в том числе реализуемое на рынках, проходит обязательную ветеринарно-санитарную экспертизу, в том числе и исследование на трихинеллёз. Для этого имеются лаборатории ветеринарно-санитарной экспертизы на всех мясоперерабатывающих предприятиях (цехах) и на рынках, где реализуется мясо. После проведения исследования выдается заключение о результатах экспертизы, на туше обязательно ставиться клеймо, без которого реализация мяса покупателю категорически запрещена.
Ошибочным является мнение, что если хорошо проварить или прожарить мясо, даже не проверенное на трихинеллёз, то не заболеешь. Личинки трихинелл, находящиеся в мышцах, образуют соединительнотканную капсулу, поэтому они устойчивы к варке, копчению, жарке, обработке в микроволновой печи и замораживанию.
Меры профилактики
– приобретайте и употребляйте в пищу только мясо, прошедшее ветеринарно-санитарную экспертизу. По действующему санитарно -ветеринарному законодательству все туши свиней, диких кабанов и других диких животных – естественных носителей трихинеллеза до выпуска в пищу должны обязательно подвергаться исследованию.
– следует помнить, что даже после тщательной термической обработки, при замораживании, посоле и копчении личинки трихинелл не погибают.
– при обнаружении хотя бы одной трихинеллы мясо, внутренние органы животных, зараженных личинками трихинелл, подлежат только утилизации, которая проводится силами ветеринарной службы.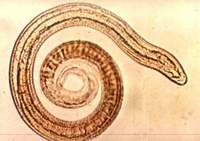
Итак, если вы или ваши родные употребляли в пищу свинину и другие перечисленные выше мясные продукты, не прошедшую ветеринарно-санитарную экспертизу, и обнаружили появление описанных симптомов, немедленно обратитесь к врачу!
От этого зависит Ваше здоровье и здоровье Ваших близких.
Авторы: Зайцева М. М. – врач – педиатр,
Михальченко Г.Н.-фельдшер-валеолог
Ответственный за выпуск: Дечко Е.В.
Диагностика трихинеллеза – сдать анализ в СЗЦДМ
Трихинеллез (трихиноз, биогельминтоз) ― это поражение внутренних органов и центральной нервной системы трихинеллой, круглыми червями, паразитирующими в тонкой кишке. Среди характерных признаков аллергические реакции, лихорадка, отечность, сильные мышечные боли.
Определение заболевания
Возбудитель трихинеллеза был открыт в 1835 году.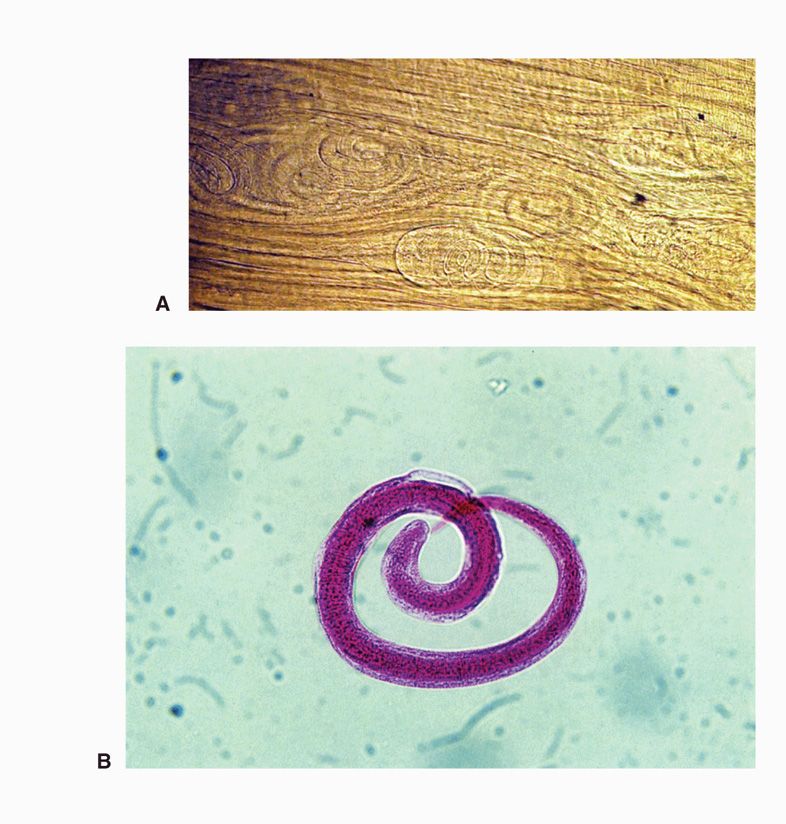 Это трихинеллы, паразитические круглые черви класса Enoplea. Спустя 2 суток после инвазии особи становятся половозрелыми. После оплодотворения самцы погибают, а самки через 48 часов начинают производить личинки. Этот процесс может занимать до 6 недель.
Это трихинеллы, паразитические круглые черви класса Enoplea. Спустя 2 суток после инвазии особи становятся половозрелыми. После оплодотворения самцы погибают, а самки через 48 часов начинают производить личинки. Этот процесс может занимать до 6 недель.
Рождается большое количество личинок. В истории есть случаи, когда на 1 кг мышечной ткани приходилось до 15 тысяч паразитов. Они проникают через слизистые в кровеносные и лимфатические сосуды. Это позволяет им мигрировать по организму. Личинки попадают во все ткани, но способны выжить только в скелетной, поперечнополосатой мускулатуре. Средой обитания могут стать жевательные, глазодвигательные и мышцы диафрагмы.
Проникая в мышечную ткань, личинки частично разрушают ее волокна, вызывая клеточный инфильтрат. В нем скапливаются клеточные элементы, включающие кровь и лимфу. Спустя несколько недель в этом месте образуется фиброзная капсула. Ее стенки постепенно уплотняются, но обмен питательными веществами между паразитом и хозяином не прекращается. Капсулу питают кровеносные сосуды, поэтому личинки могут так жить многие годы.
Капсулу питают кровеносные сосуды, поэтому личинки могут так жить многие годы.
Замкнется жизненный цикл только тогда, когда паразита вместе с мясом хозяина съест другой хищник. В этом случае личинки попадут в кишечник, достигнут половозрелости и все начнется сначала.
Заболеть трихинеллезом можно съев зараженное мясо плотоядного животного. В первую очередь это дикие звери, но встречаются больные животные среди сельскохозяйственного скота, как правило, свиньи. Они всеядны, например, могут съесть зараженную мышь, пропавшую в свинарник. Встречаются среди них и случаи каннибализма. Травоядные технически могут быть заражены, что было проверено экспериментальным путем, но в реальной жизни такого не бывает.
Наиболее частая причина заражения человека ― поедание свиного сала с прослойками мяса. Заболевание не зависит от сезона, однако количество больных возрастает в сезон охоты и в начале зимы, когда происходит забой домашнего скота. К группе риска относят охотников, работников животноводческих ферм, скотобоен, предприятий мясоперерабатывающей промышленности.
К группе риска относят охотников, работников животноводческих ферм, скотобоен, предприятий мясоперерабатывающей промышленности.
Трихинеллы выдерживают температуру до -20 С. Сохраняют жизнеспособность в замороженном мясе до 20 месяцев. Капсула настолько прочна, что личинке не страшна засолка и копчение. Паразиты способны погибнуть лишь при температуре от +63 С и выше воздействующей в течении 15 – 20 секунд. При этом, такой температуры необходимо достигнуть в середине куска.
КлассификацияПо клиническому течению трихинеллез делиться на:
По степени тяжести течения различают:
Заболевание может протекать без осложнений и со следующими осложнениями:
-
тромбозы артерий и вен;
-
менингоэнцефалит;
-
пневмония;
-
гепатит;
-
миокардит и другое.

Критерием служить выраженность симптомов интоксикации, отечности, мышечных болей, повышение температуры тела. При легкой форме симптоматика выражена слабо. Среднетяжелая характеризуется лихорадкой, отеком лица, миалгией. Тяжелая форма ― генерализованной отечностью и другими ярко выраженными симптомами, вплоть до полной обездвиженности больного.
Инкубационный период. Длиться с момента заражения до проявления первых симптомов от 10 до 40 дней. Более короткий при массивных паразитических инвазиях, длинный при легкой форме.
Аллергическая фаза. В этот период происходит активное размножение и гибели паразитов. Из-за продуктов их жизнедеятельности активизируется иммунная система, что выражается в аллергических реакциях. Внедряющиеся личинки поражаю сосуды, возникает аллергический миозит (воспаление скелетной мускулатуры).
Острое течение трихинеллеза выражается следующими симптомами:
-
Повышение температуры от субфебрилитета до +40 С.

-
Общая интоксикация (тошнота, повышенная утомляемость, головные боли).
-
Отечность, затрагивающая лицо, веки, надбровные дуги. В особых случаях отекает шея, туловище, конечности. Это считается тревожным признаком.
-
Конъюнктивит (воспалительный процесс слизистой оболочки глаза, выражающийся в покраснение белка глаза, слезотечении).
Мышечные боли начинаются чаще с икроножных. Затем боль возникает в ягодицах, спине, брюшине, и поднимаясь, доходит до языка, внутриглазных и жевательных мышц. Боли часто интенсивные, усиливаются при движении и пальпации.
Также могут наблюдаться диспепсические расстройства и аллергические реакции в виде полиморфной сыпи на всем теле. Отмечается высокая эозинофилия в крови (до 80%). Количество эозинофилов (разновидность лейкоцитов, борющихся с многоклеточными паразитами) возрастает постепенно. Резкое повышения ― плохой признак.
Резкое повышения ― плохой признак.
Фаза органных поражений. Наступает примерно на 4 неделю после заражения, характеризуется проявлением системного васкулита. Органные поражения могут стать причиной летального исхода.
В среднем заболевание с выраженной симптоматикой длиться при легкой форме до 15 дней, при среднетяжелой ― 6 недель. При тяжелом течении болезни лечение может затянуться до полугода.
ОсложненияВо время фаза органных поражений могут развиться следующие осложнения:
-
Поражение миокарда, а также тахикардия (увеличение частоты сердечных сокращений), артериальная гипотензия (снижение артериального давления на 20% и более от обычного), сосудистая недостаточность.
-
Поражение легких ― пневмонии (воспаления, ишемии и некроз легочной ткани), связанные с системным васкулитом.
-
Поражение ЦНС ― менингоэнцефалит (воспаление головного мозга), энцефаломиелит (поражение спинного и головного мозга).

-
Поражение печени и почек (гепатит и нефрит).
-
ДВС-синдром ― образование диссеминированных тромбов.
Спрогнозировать как наличие осложнений, так и их форму невозможно. Все зависит от того, куда проникнут личинки. Если не будет проведено своевременное лечение, поражение жизненно-важных органов может привести к летальному исходу. Усугубляет ситуацию то, что не всегда легкие формы болезни можно вовремя обнаружить.
На основании клинических проявлений ставиться предварительный диагноз. Необходимо выяснить факт употребления зараженного, недостаточно термически обработанного мяса (свинины или диких животных).
Подтвердить диагноз ― трихинеллез можно на основе лабораторных анализов самого мяса (если есть остатки), и в результате исследования пациента. Для этого проводят следующие мероприятия:
-
Трихинеллоскопия ― изучение мяса животных, употребленных человеком.
 Исследование направлено на обнаружение личинок трихинелл.
Исследование направлено на обнаружение личинок трихинелл.
-
Серологическая диагностика (иммуноферментный анализ). Тест может быть положителен через 2 недели с начала заболевания
-
Кожные пробы. Проводятся также через 14 дней с начала болезни. Положительный результат можно получать на протяжении многих лет.
-
Инструментальное диагностирование. УЗИ мышечной ткани, суставов, органов брюшной полости. Также проводят ЭКГ для исключения миокардита, рентгенографию при подозрении на поражение легких
На ранней стадии, когда анализы крови и мышечной биопсии не могут дать точного результата. Врач проводит дифференциальную диагностику для исключения псевдотуберкулеза, описторхоза, брюшного тифа и других схожих по проявлениям заболеваний. Инструментальные методы позволяют полностью изучить состояние больного, исключить или вовремя обнаружить органные поражения.
Руководит диагностированием и лечением врач-паразитолог, также требуется обследование у гастроэнтеролога, кардиолога, аллерголога, иммунолога и у других специалистов.
Терапия состоит из двух направлений: этиотропной и патогенетической.
В рамках этиотропного лечения уничтожаются трихинеллы, прекращается продуцирование личиной. В ряде случаев удается нарушить процесс капсуляции, убить часть мышечных паразитов. к
Больший результат этиотропная терапия дает во время инкубационного периода. Позволяет предотвратить клинические проявления трихинеллеза. Эффективность снижается пропорционально увеличению срока с начала инвазии.
Патогенетическая терапия направлена на устранение симптоматики. Основные препараты ― антигистаминные средства. При тяжелых формах назначают гормональные средства. Также назначают жаропонижающие, обезболивающие и противовоспалительные средства.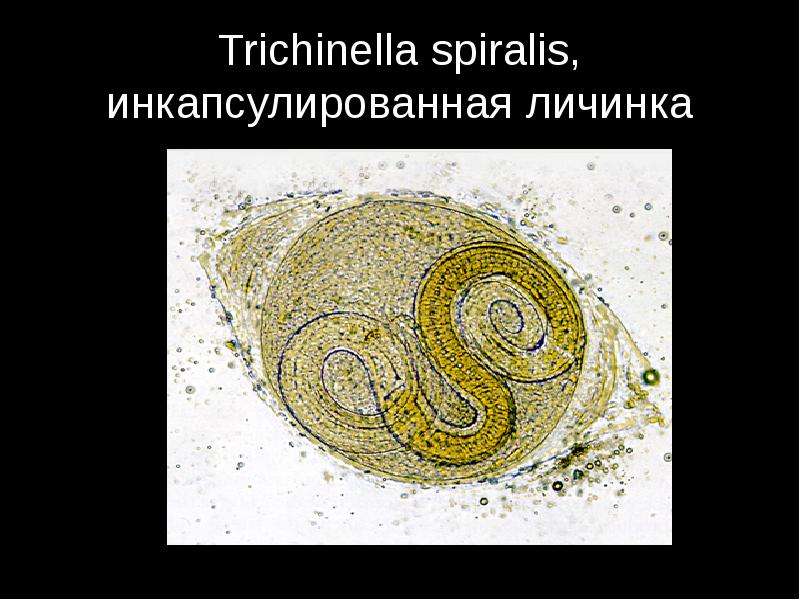
Контроль состояния пациента и эффективности лечения необходимо проводить через 6 и 12 месяцев.
ПрогнозПри легкой и среднетяжелой форме трихинеллеза прогноз благоприятный. Своевременное лечение позволяет достигнуть условно полного выздоровления в течении 1,5 – 2 месяцев. Личинки обызвествляются и остаются в теле навсегда.
При тяжелой форме болезнь может затянуться на 6 и более месяцев. Возможны рецидивы заболевания на протяжении всей жизни человека. Они выражаются в миалгиях (выраженная боль в мышцах), остаточной астенизации (повышенная утомляемость, нарушение сна, утрата способности к длительному умственному и физическому напряжению) и мышечных контрактурах (ограничение пассивных движений в суставе).
Вакцина против трихинеллеза не разработана. Летальность составляет – 5%.
Профилактика
Поскольку единственный способ инфицирование ― употребление зараженного мяса, важно обращать особое внимание на продукт.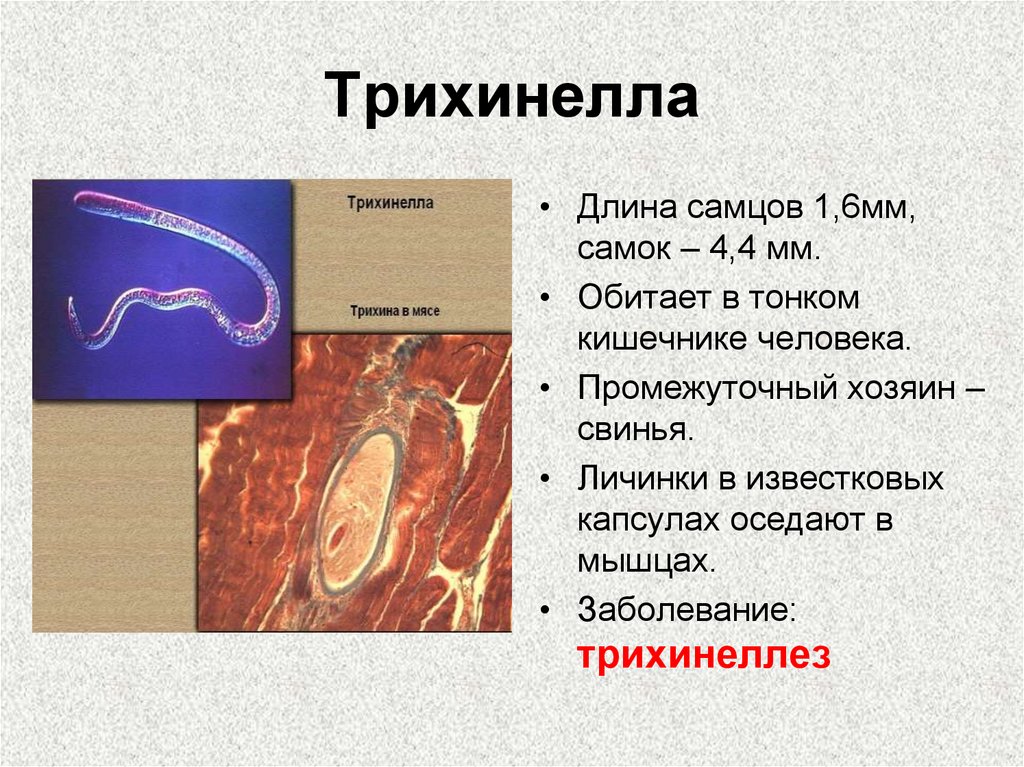 Приобретать мясо, мясные полуфабрикаты и солено-копченые изделия следует только в магазинах. Поскольку они проходят санитарную экспертизу. Стоит отказаться от употребления диких животных. Процент зараженных особей чрезвычайно высок:
Приобретать мясо, мясные полуфабрикаты и солено-копченые изделия следует только в магазинах. Поскольку они проходят санитарную экспертизу. Стоит отказаться от употребления диких животных. Процент зараженных особей чрезвычайно высок:
При обширных инвазиях капсулы личинок в волокнах поперечно-полосатых мышцах можно обнаружить визуально без сторонних приборов. Однако, при малой инвазии можно пропустить зараженный продукт даже при исследовании ― трихинеллоскопии. Стоит учесть и человеческий фактор, поскольку исследование мяса на трихинеллез проводит лаборант под специальным микроскопом. Более надежен биохимический метод переваривания, но он затратен по времени. Эффективна также прижизненная диагностика методом ИФА, которую можно провести перед забоем.
Зараженные туши подлежит утилизации. Просто выбросить их нельзя, поскольку они могут быть съедены бродячими животными и грызунами, а это продолжит распространение трихинеллеза.
Мясо диких зверей и свинина, успешно прошедшие трихинеллоскопию, все равно должны проходить тепловую обработку на протяжении не менее 6 часов.
В подразделениях АО “СЗЦДМ” можно сдать анализы на трихинеллез и другие лабораторные исследования.
К преимуществам стоит отнести удобное расположение лабораторных терминалов. Выбраны места с хорошей транспортной доступностью. Можно легко доехать как на личном автомобиле, так и на общественном транспорте. Медицинские центры и лабораторные терминалы находятся в Санкт-Петербурге, Ленинградской обл., Великом Новгороде, Новгородской обл., а также в Пскове и Калининграде.
перейти к анализам
Внимание: трихинеллез! / Россельхознадзор
Управление Россельхознадзора по Томской области неоднократно информировало население о возможности заражения трихинеллезом. И вот, в октябре 2017 года на территории Верхнекетского района Томской области зафиксировано 16 случаев заражения людей трихинеллезом.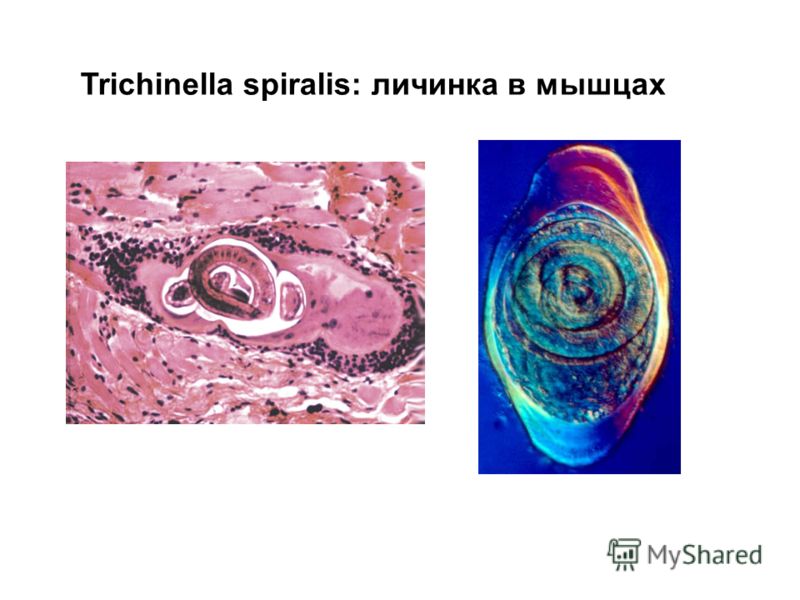 Заболевшие употребляли в пищу мясо добытого медведя. Такие случаи заболеваемости трихинеллезом на территории области регистрируется практически ежегодно в виде небольших вспышек: в 2012 году – 7 человек (Верхнекетский район), в 2008 – 36 (Каргасокский район), в 2007 – 5 (Верхнекетский район), в 2005 г – 2 (г. Кедровый), в 2002 г – 9 человек (Александровский район – 6, г. Стрежевой – 1 и завозных случаев – 2 из Кемеровской области).
Заболевшие употребляли в пищу мясо добытого медведя. Такие случаи заболеваемости трихинеллезом на территории области регистрируется практически ежегодно в виде небольших вспышек: в 2012 году – 7 человек (Верхнекетский район), в 2008 – 36 (Каргасокский район), в 2007 – 5 (Верхнекетский район), в 2005 г – 2 (г. Кедровый), в 2002 г – 9 человек (Александровский район – 6, г. Стрежевой – 1 и завозных случаев – 2 из Кемеровской области).
Источником заражения чаще всего является мясо бурого медведя. Но следует помнить, что болезнь регистрируется более чем у 100 видов животных (в т.ч. собак, кошек, свиней, медведей, пушных зверей, грызунов, насекомоядных, птиц). В последние годы на первое место выходит заражение от мяса диких животных (кабан, медведь, реже енотовидная собака и др. хищные). В качестве источников заражения могут выступать и травоядные животные. В Западной Европе в последние годы отмечался ряд вспышек, связанных с употреблением конины.
Управление Россельхознадзора по Томской области напоминает, что трихинеллез опасная болезнь, как для животных, так и для людей. Причиной ее являются мелкие нитевидные гельминты – трихинеллы. Заражение людей происходит при употреблении в пищу сырого или недостаточно термически обработанного мяса. Мясо, пораженное трихинеллами, внешне ничем не отличается от незараженного. Размеры личинок очень малы, увидеть их можно лишь с помощью трихинеллоскопа. Личинки трихинелл обладают высокой устойчивостью, переносят воздействие поваренной соли, употребляемой для консервации (при посоле сохраняются в глубине куска до 1 года), не боятся относительно высокой температуры и значительного ее понижения, поэтому в морозильных камерах холодильников не погибают (в замороженном мясе при минус 10о С личинки выживают неопределенно долго).
Кроме того, в мясе зараженных животных накапливаются токсины, вызывающие серьезные заболевания людей. Вот почему пораженные туши подлежат обязательному уничтожению.
Известны случаи заражения людей при употреблении сала (с прожилками мяса), ветчины, вареной колбасы, сосисок, пельменей, шашлыков.
К сожалению, отнюдь не каждый перед употреблением отправит добычу на экспертизу. И напрасно. Вероятность наступления клинических проявлений и их тяжесть у человека зависят от количества съеденного мяса, его обсемененности, числа поступивших в организм жизнеспособных трихинелл.
В кишечнике человека личинки трихинелл превращаются в половозрелых самцов и самок, а те в свою очередь производят личинки, которые мигрируют через лимфатическую систему в кровь и попадают в мышцы. Взрослые трихинеллы в кишечнике живут 45-60 дней, а в мышцах – в течение многих лет.
Протекает трихинеллез у человека тяжело. Спустя 5 (в некоторых случаях – 45) дней после употребления пораженного трихинеллами мяса у человека повышается температура тела, появляются: отек лица, мышечные и суставные боли, боли в животе, понос, могут быть высыпания на коже и кровоизлияния в конъюнктиву глаз. Заболевание может осложняться миокардитом, пневмонией, менингоэнцефалитом, гепатитом, нефритом. Возможен и летальный исход.
Заболевание может осложняться миокардитом, пневмонией, менингоэнцефалитом, гепатитом, нефритом. Возможен и летальный исход.
Заболевшие трихинеллезом подлежат госпитализации. Мясо и мясные продукты, подозреваемые в качестве факторов передачи трихинеллеза, изымаются и направляются для исследования в лабораторию. После подтверждения диагноза все лица, употреблявшие зараженное мясо, обследуются амбулаторно с использованием клинических и лабораторных тестов. За ними устанавливается наблюдение продолжительностью в один месяц со дня последнего употребления инвазированного мяса.
Чтобы остеречься заражения, все туши животных, как домашних, так и диких, подвергают исследованию на трихинеллез.
Во избежание заражения трихинеллезом рекомендуется не покупать мясо и мясопродукты вне установленных мест торговли. В ходе приобретения мясных продуктов на рынках, ярмарках выходного дня необходимо спрашивать у продавца справку о проведенной ветеринарной экспертизе, обращать внимание на наличие овального клейма на тушах.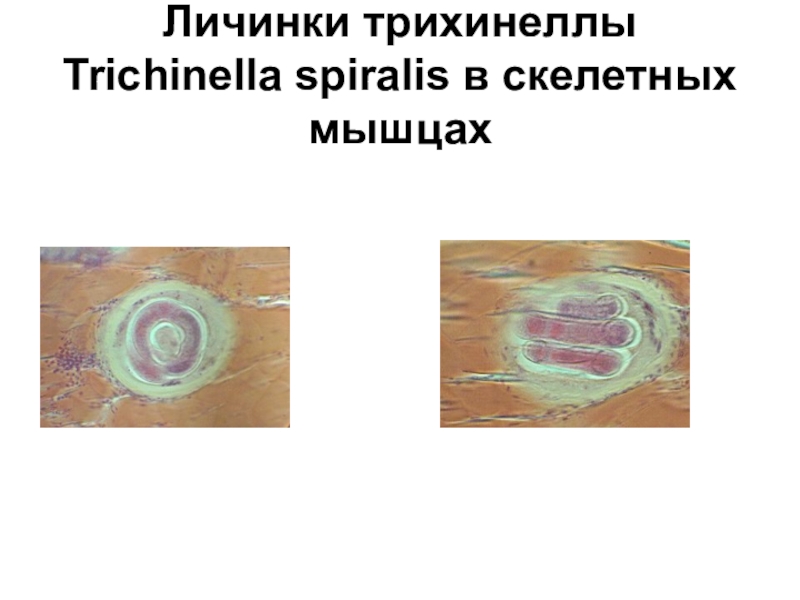 Помните, что без заключения лаборатории ветеринарно-санитарной экспертизы о проведении исследований на трихинеллез, вы рискуете заразить и себя, и близких вам людей, серьезным заболеванием.
Помните, что без заключения лаборатории ветеринарно-санитарной экспертизы о проведении исследований на трихинеллез, вы рискуете заразить и себя, и близких вам людей, серьезным заболеванием.
Источник: Управление Федеральной службы по ветеринарному и фитосанитарному надзору по Томской области
CDC – Трихинеллез – Биология
Возбудители:
Трихинеллез (трихинеллез) вызывается нематодами (круглыми червями) рода Trichinella . Помимо классического возбудителя T. spiralis (обнаруженного во всем мире у многих плотоядных и всеядных животных) в настоящее время распознаются несколько других видов Trichinella , в том числе T. pseudospiralis (млекопитающие и птицы во всем мире), T. nativa (арктические медведи), т.nelsoni (африканские хищники и падальщики), T. britovi (хищники Европы и Западной Азии) и T. papuae (дикие и домашние свиньи Папуа-Новой Гвинеи и Таиланда).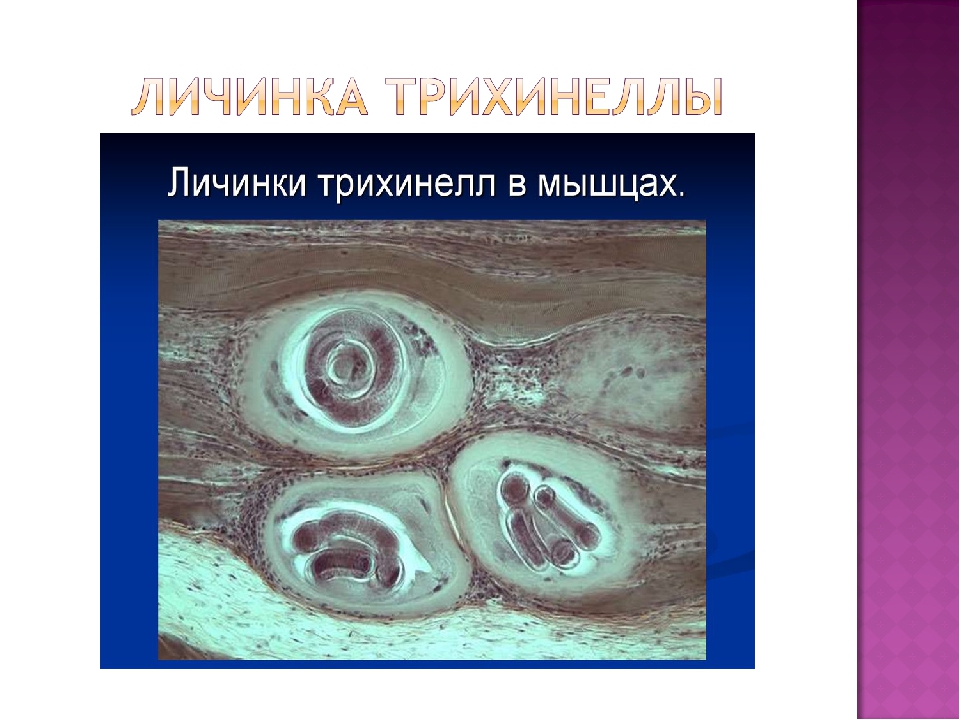 Trichinella zimbabwensis встречается у крокодилов в Африке, но на сегодняшний день нет известных ассоциаций этого вида с болезнями человека.
Trichinella zimbabwensis встречается у крокодилов в Африке, но на сегодняшний день нет известных ассоциаций этого вида с болезнями человека.
Жизненный цикл:
В зависимости от используемой классификации существует несколько видов Trichinella : T. spiralis , T.pseudospiralis , T. nativa , T. murelli , T. nelsoni , T. britovi , T. papuae и T. zimbabwensis , все, кроме последнего, были замешаны в болезнь человека. Взрослые черви и инцистированные личинки развиваются в пределах одного позвоночного-хозяина, а инфицированное животное служит окончательным хозяином и потенциальным промежуточным хозяином. Второй хост необходим для сохранения жизненного цикла Trichinella . В домашнем цикле чаще всего участвуют свиньи и антропофильные грызуны, но могут быть задействованы и другие домашние животные, например лошади.В лесном цикле диапазон инфицированных животных велик, но наиболее часто источниками заражения человека являются медведь, лось и кабан.
Трихинеллез вызывается употреблением в пищу недоваренного мяса, содержащего инцистированные личинки (за исключением T. pseudospiralis и T. papuae , которые не инцистируются) видов Trichinella . После воздействия кислоты желудочного сока и пепсина личинки выходят из цист и проникают в слизистую оболочку тонкой кишки, где развиваются во взрослых червей.Самки 2,2 мм в длину; самцы 1,2 мм. Продолжительность жизни в тонкой кишке составляет около четырех недель. Через 1 неделю самки выпускают личинок, которые мигрируют в поперечнополосатые мышцы, где инцизируются. Диагноз обычно ставится на основании клинических симптомов и подтверждается серологией или идентификацией инцистированных или неинцистированных личинок в биопсийных или аутопсийных образцах.
Изображение жизненного цикла и информация любезно предоставлены DPDx.
Trichinella spiralis – обзор
Trichinella spiralis
Trichinella spiralis – это внутриклеточная паразитическая нематода поперечнополосатой мускулатуры млекопитающих, встречающаяся во всем мире у многих плотоядных и всеядных животных.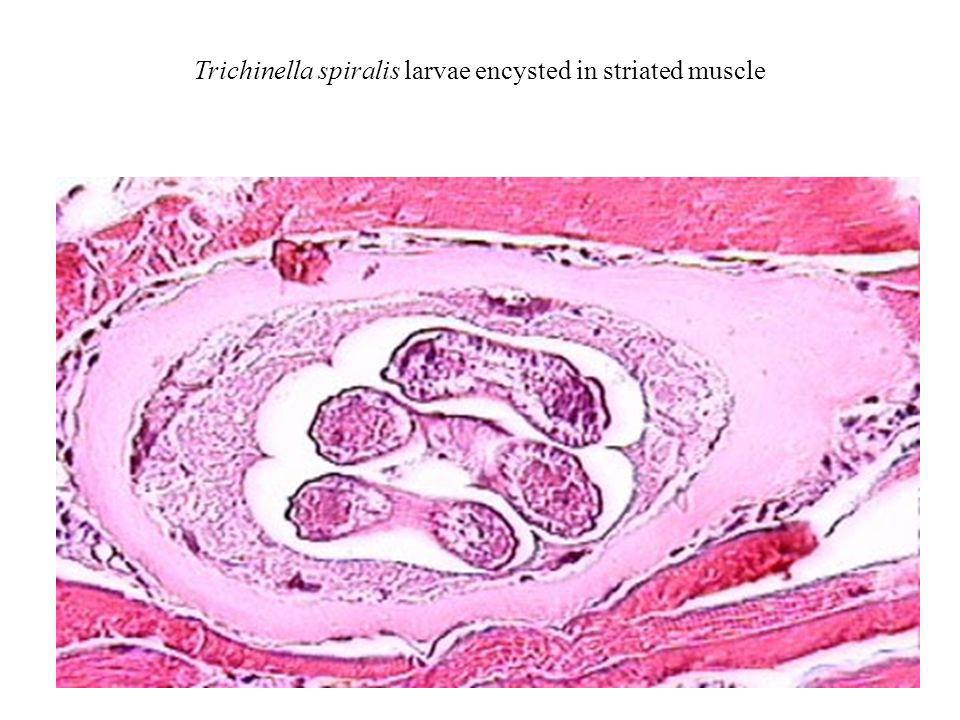 В жизненном цикле нет стадии, которая была бы внешней по отношению к хосту (в окружающей среде), и передача происходит исключительно в результате проглатывания другого зараженного хоста. Инфекции человека в основном связаны с потреблением недоваренной свинины, а паразиты являются эндемичными в свиноводческих / свиноводческих предприятиях ряда стран Восточной Европы, России (некоторые области), Китая (различные провинции), Юго-Восточной Азии (Лаос и США). Таиланд) и Южная Америка (кроме Бразилии). Другие виды Trichinella также заразны для людей и часто особенно связаны с конкретными географическими регионами или видами диких животных.
В жизненном цикле нет стадии, которая была бы внешней по отношению к хосту (в окружающей среде), и передача происходит исключительно в результате проглатывания другого зараженного хоста. Инфекции человека в основном связаны с потреблением недоваренной свинины, а паразиты являются эндемичными в свиноводческих / свиноводческих предприятиях ряда стран Восточной Европы, России (некоторые области), Китая (различные провинции), Юго-Восточной Азии (Лаос и США). Таиланд) и Южная Америка (кроме Бразилии). Другие виды Trichinella также заразны для людей и часто особенно связаны с конкретными географическими регионами или видами диких животных.
Жизненный цикл начинается с попадания инцистированных личинок в поперечнополосатую мышечную ткань другого инфицированного хозяина. После воздействия кислоты желудочного сока и пепсина личинки выходят из цист и проникают в слизистую оболочку тонкого кишечника, где развиваются во взрослых червей длиной всего пару миллиметров. Производятся сотни новых личинок, которые вместе с кровью распространяются по телу, оседая в мышечных клетках, где они инкапсулируются в тканевые кисты.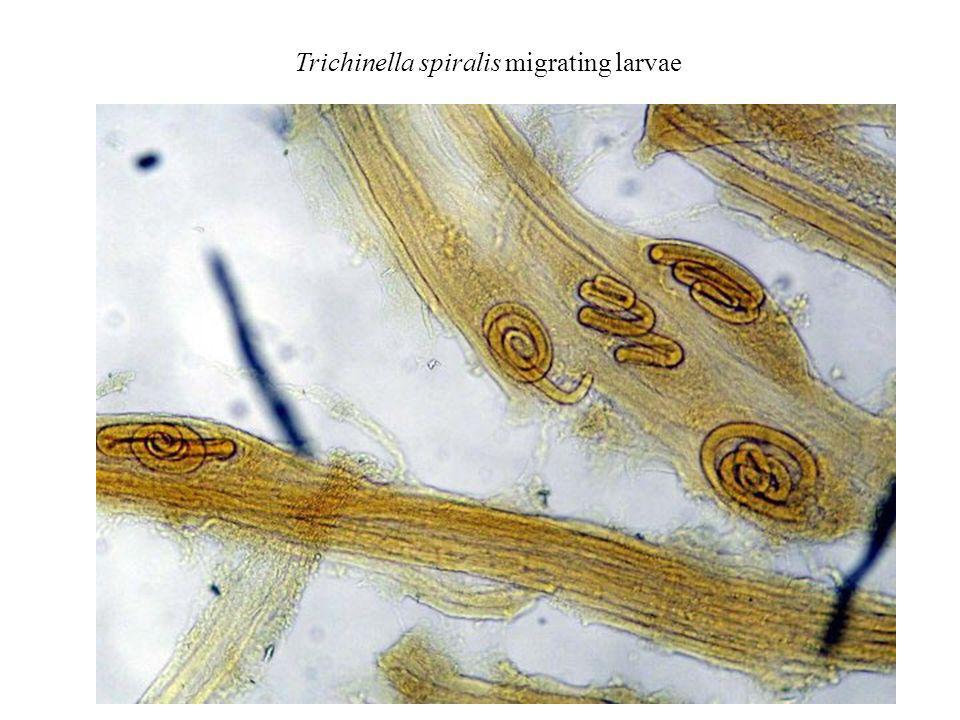 Эти инфекционные инцистированные личинки могут годами выживать в тканях, а также оставаться заразными в течение нескольких недель у мертвых животных, что позволяет инфицировать мясоедов.
Эти инфекционные инцистированные личинки могут годами выживать в тканях, а также оставаться заразными в течение нескольких недель у мертвых животных, что позволяет инфицировать мясоедов.
Хотя заражение животных T. spiralis считается бессимптомным, инфицирование человека вызывает серьезное клиническое заболевание, трихинеллез, которое может причинять много страданий и может быть смертельным. Симптомы трихинеллеза связаны с этапами жизненного цикла, с кишечной, миграционной и мышечной фазами. Во время инвазии кишечного эпителия могут возникнуть боли в животе, диарея и рвота.Во время миграции личинок симптомы могут включать лихорадку, отек лица, миалгию, сыпь и тахикардию. Появление личинок в мышечных клетках и инцистирование мышечных личинок связано с такими симптомами, как миалгия и тяжелая астения. Наиболее часто поражаются мышцы шейки матки, туловища, а также верхних и нижних конечностей. Сила мышечной боли отражает интенсивность инфекции, и подвижность может быть ограничена.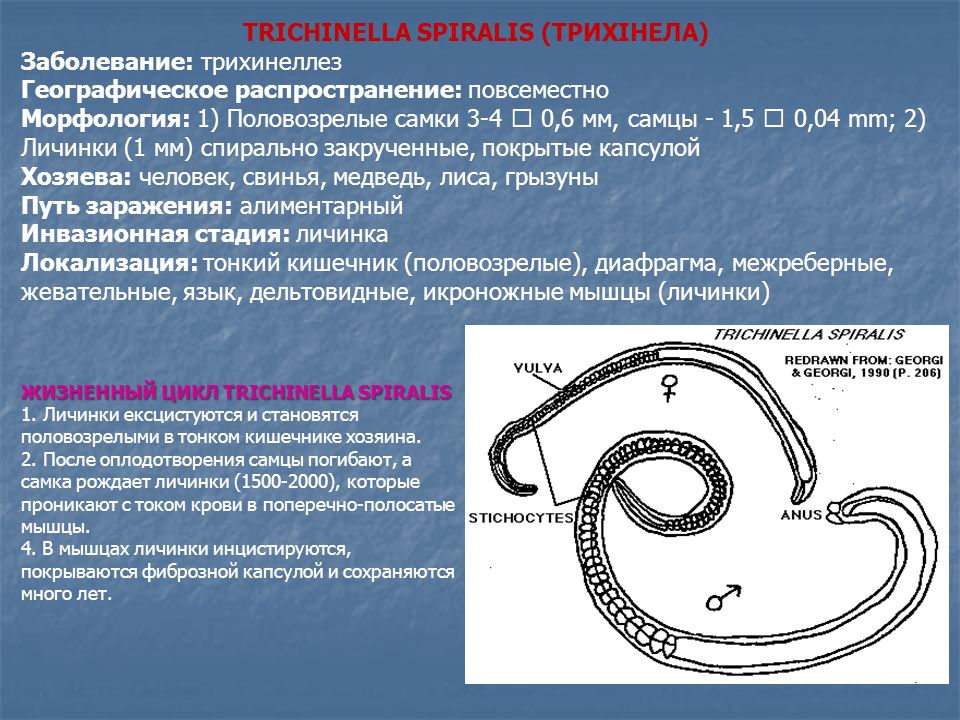 Тяжелая миалгия обычно длится 2–3 недели. Хотя инфекция носит постоянный характер, что диктуется жизненным циклом, только несколько случаев становятся «клинически хроническими» с повторяющимися мышечными болями.Сообщалось также о нарушениях работы мозга. Хотя смертность от случаев заболевания низкая, при тяжелой инфекции без лечения она может возрасти до более 10%.
Тяжелая миалгия обычно длится 2–3 недели. Хотя инфекция носит постоянный характер, что диктуется жизненным циклом, только несколько случаев становятся «клинически хроническими» с повторяющимися мышечными болями.Сообщалось также о нарушениях работы мозга. Хотя смертность от случаев заболевания низкая, при тяжелой инфекции без лечения она может возрасти до более 10%.
Заражение T. spiralis может происходить только через продукты питания, и свиньи проходят обязательный ветеринарный контроль, чтобы гарантировать, что мясо не содержит Trichinella . Нормы ЕС требуют, чтобы пробы свиней систематически отбирались на бойнях, пробы отбирались с участков, где они были заражены, и исследовались рекомендуемым методом, «методом магнитной мешалки для разложения объединенных проб», который считается наиболее чувствительным (постановление Комиссии ЕС EC 2075/2005; Рекомендации Международной комиссии по трихинеллезу).В этом методе личинки идентифицируются после искусственного переваривания образцов мышц от туш.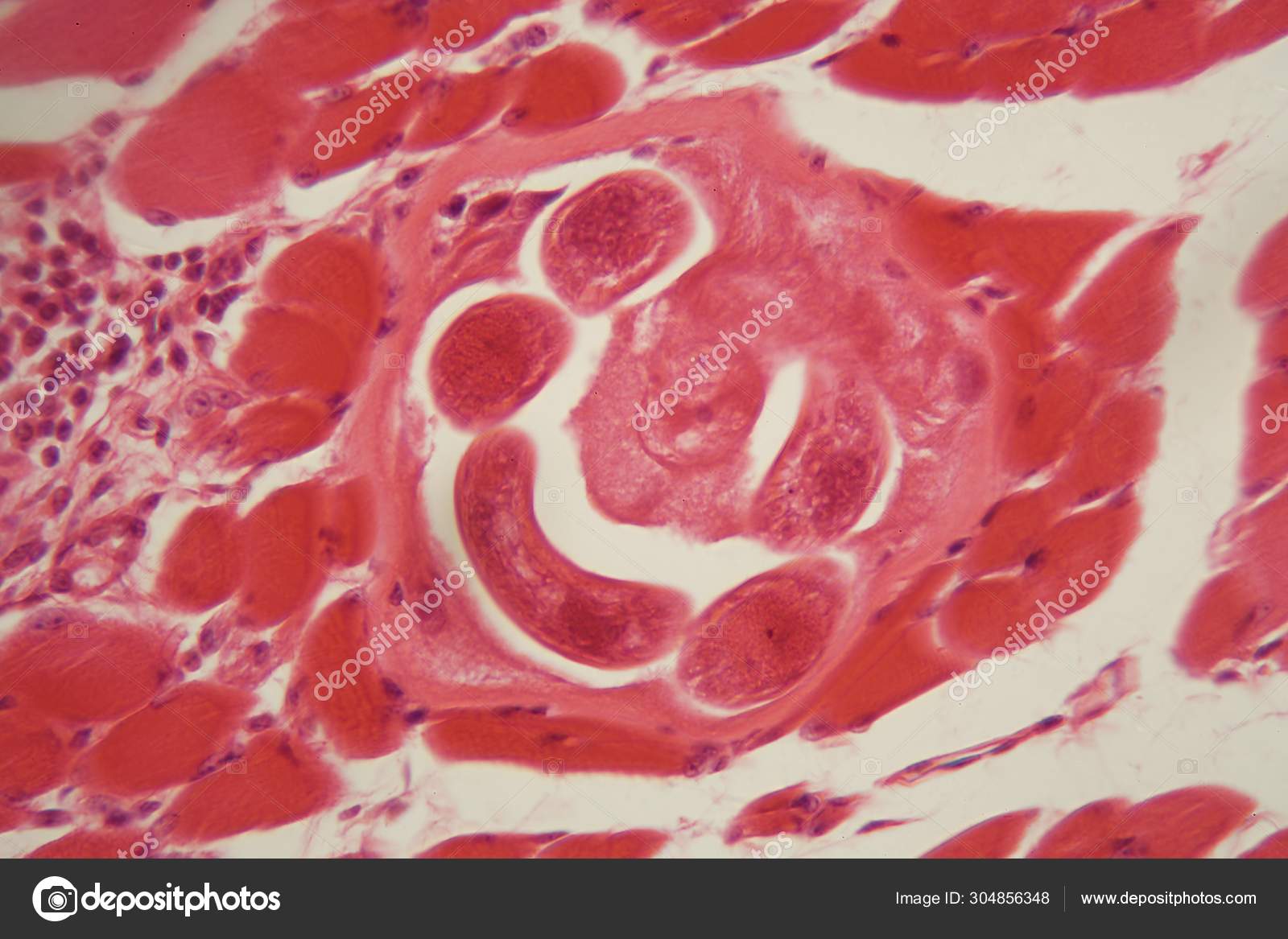 Отступления от испытаний возможны в отношении мяса домашних свиней, если свинофермы официально признаны компетентными органами как свободные от Trichinella . Это требует соблюдения немалого количества правил. В индустриальных странах большинство продаваемых свиней выращивают на фермах с высоким уровнем содержания и, следовательно, не содержат Trichinella , но свиньи на подворье, которые больше контактируют с окружающей средой, с большей вероятностью будут инфицированы, а “ органическая ” свинина также с большей вероятностью заразится. быть зараженным.Мясо домашних свиней, замороженное под надзором компетентных органов, также может быть освобождено от проверки Trichinella .
Отступления от испытаний возможны в отношении мяса домашних свиней, если свинофермы официально признаны компетентными органами как свободные от Trichinella . Это требует соблюдения немалого количества правил. В индустриальных странах большинство продаваемых свиней выращивают на фермах с высоким уровнем содержания и, следовательно, не содержат Trichinella , но свиньи на подворье, которые больше контактируют с окружающей средой, с большей вероятностью будут инфицированы, а “ органическая ” свинина также с большей вероятностью заразится. быть зараженным.Мясо домашних свиней, замороженное под надзором компетентных органов, также может быть освобождено от проверки Trichinella .
Профилактика заражения людей осуществляется путем инспекции мяса, переработки мяса и предотвращения контакта пищевых животных с инфицированным мясом. Хотя замораживание может убить личинок T. spiralis , другие виды Trichinella устойчивы к замораживанию. Тщательное приготовление свинины перед употреблением в пищу гарантирует от заражения как T.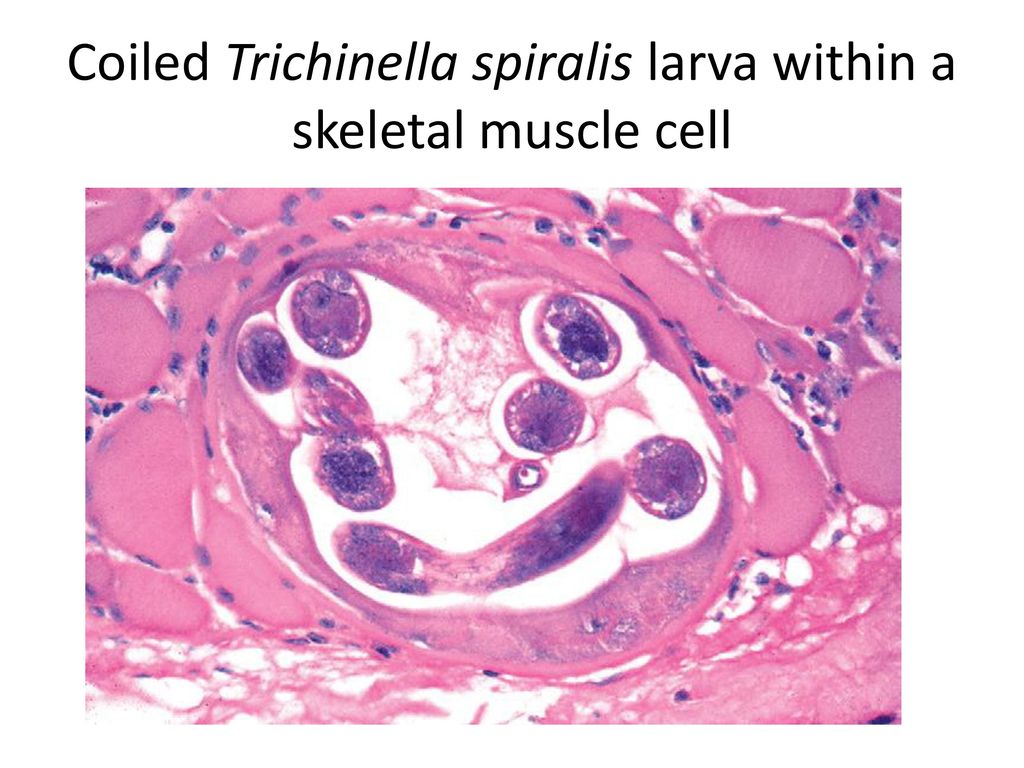 spiralis и Taenia solium .
spiralis и Taenia solium .
Trichinella Spiralis – StatPearls – NCBI Bookshelf
Непрерывное обучение
Трихинеллез, также называемый трихинеллезом, представляет собой паразитарную инфекцию, вызываемую круглыми червями (нематодами) из рода Trichinella. Это вызвано употреблением недоваренного или сырого мяса (обычно свинины). Виды Trichinella spiralis являются частой причиной болезней человека, и заражение происходит после употребления в пищу сырой или недоваренной свинины. Симптомы разнообразны и могут включать общую лихорадку, боль в животе, диарею, тошноту, рвоту или миалгию.Презентация также может включать миокардит и энцефалит. В этом упражнении описывается оценка и лечение трихинеллеза, а также подчеркивается роль межпрофессиональной команды в уходе за пациентами с этим заболеванием.
Цели:
Опишите патофизиологию трихинеллеза.
Обрисуйте типичное представление пациента с трихинеллезом.

Обобщите рекомендации по лечению пациентов с трихинеллезом.
Оцените важность сотрудничества и общения между членами межпрофессиональной команды для улучшения оказания помощи пациентам, страдающим трихинеллезом.
Введение
Трихинеллез, также называемый трихинеллезом, возникает от круглых червей (нематод) из рода Trichinella . Это паразитарная инфекция. Это вызвано употреблением недоваренного или сырого мяса (обычно свинины). Trichinella spiralis видов – частая причина болезней человека в результате употребления в пищу сырой или недоваренной свинины. Другие млекопитающие, такие как дикие хищники и лошади, могут быть резервуарами инфекции. Он может вызывать симптомы, варьирующиеся от общей лихорадки, боли в животе, диареи, тошноты, рвоты, миалгии до более серьезных, таких как миокардит и энцефалит.
Этиология
Trichinella spiralis – паразит нематод (аскариды). [1] Он обладает способностью заражать широкий спектр млекопитающих, включая свиней, лошадей, рептилий и птиц, но вызывает заболевание только у людей.Люди заражаются инфекцией, употребляя в пищу неправильно приготовленную или сырую свинину, конину или другое мясо домашних животных, а также мясо диких животных, таких как медведь. В некоторых сообщениях упоминается случайное заражение этим заболеванием при употреблении в пищу мяса рептилий, в том числе ящериц и черепах. [2] Сообщений о передаче от человека к человеку нет.
[1] Он обладает способностью заражать широкий спектр млекопитающих, включая свиней, лошадей, рептилий и птиц, но вызывает заболевание только у людей.Люди заражаются инфекцией, употребляя в пищу неправильно приготовленную или сырую свинину, конину или другое мясо домашних животных, а также мясо диких животных, таких как медведь. В некоторых сообщениях упоминается случайное заражение этим заболеванием при употреблении в пищу мяса рептилий, в том числе ящериц и черепах. [2] Сообщений о передаче от человека к человеку нет.
Эпидемиология
Трихинеллез встречается во всем мире, и, по оценкам, ежегодно происходит около 10 000 случаев [3]. Случаи обычно возникают в группах среди групп людей, употреблявших инфицированное мясо обычного животного.[4] Существует девять видов трихинеллы , и на данный момент существуют сообщения о двенадцати генотипах трихинеллы . [5] Наиболее распространенным видом трихинеллы, который может вызывать заболевание человека, является Trichinella spiralis , хотя есть другие виды . Трихинелла , вызывающая заболевание человека: T. nativa , T. nelson , T. britovi , T. pseudospiralis , T. murelli , T. papuae . [5] [6] По данным Центров по контролю и профилактике заболеваний, в 1940-х годах ежегодно регистрировалось около 400 случаев трихинеллеза, но теперь количество зарегистрированных случаев значительно снизилось и составляло около 20 случаев ежегодно с 2008 по 2010 год.В группу риска входят охотники и другие люди, которые едят мясо диких животных.
Трихинелла , вызывающая заболевание человека: T. nativa , T. nelson , T. britovi , T. pseudospiralis , T. murelli , T. papuae . [5] [6] По данным Центров по контролю и профилактике заболеваний, в 1940-х годах ежегодно регистрировалось около 400 случаев трихинеллеза, но теперь количество зарегистрированных случаев значительно снизилось и составляло около 20 случаев ежегодно с 2008 по 2010 год.В группу риска входят охотники и другие люди, которые едят мясо диких животных.
Наибольшее количество заболевших зарегистрировано в Китае, где потребление свиней является самым высоким в мире. В Арктике белые медведи, тюлени и моржи были идентифицированы как переносчики Trichinella . В последние годы предпочтение потребителями мяса без антибиотиков также привело к увеличению количества Trichinella в Европе.
Патофизиология
Проглатывание недоваренного или сырого мяса домашних или лесных животных, содержащих инцистированные личинки видов Trichinella , может привести к трихинеллезу. T. spiralis является результатом употребления в пищу неадекватно приготовленной или сырой свинины домашних свиней. [7]
T. spiralis является результатом употребления в пищу неадекватно приготовленной или сырой свинины домашних свиней. [7]
Кишечная или желудочно-кишечная фаза: После употребления человеком инфицированного мяса ферменты пепсин и соляная кислота действуют в желудке и вызывают высвобождение личинок первой стадии. Эти личинки проникают в тонкий кишечник. Инвазия может протекать бессимптомно или иногда сопровождаться болью в животе, диареей, тошнотой и рвотой. Затем личинки превращаются во взрослых особей и спариваются.Самки червей трихинеллы производят личинок, которые завершают желудочно-кишечную или кишечную фазу.
Системная (парентеральная) фаза: личинки попадают в лимфатическую систему, а затем в кровь, достигая скелетных мышц, миокарда и головного мозга с высоким содержанием кислорода. Эта фаза приводит к системным симптомам, таким как лихорадка, миозит, миалгии, периорбитальный отек и даже может вызвать миокардит и энцефалит.
Личинки вызывают значительную эозинофилию, особенно у пациентов, у которых развивается сердечная дисфункция и дисфункция ЦНС.
Жизненный цикл: [3]
- Жизненный цикл трихинеллеза делится на две стадии: 1) домашний цикл и 2) лесной цикл.
Домашний цикл: влияет на домашних животных, особенно свиней, грызунов и лошадей
Сильватический цикл: влияет на диких животных, таких как медведь, кабан и лось
История и физическое состояние
Результаты заражения в результате потребления сырого или недоваренного мяса (особенно свинины).Инкубационный период от 1 до 6 недель. У людей тяжесть инфекции связана с количеством проглоченных личинок [8]. Желудочно-кишечные симптомы – первые симптомы трихинеллеза. Обычно они возникают через 2-7 дней после употребления сырого или недоваренного мяса. Симптомы включают боль в животе, диарею, тошноту и рвоту. Мышечная боль – обычная жалоба, главным образом в средней части живота, лице (жевательные мышцы) и груди (межреберные мышцы). В некоторых случаях боль может быть настолько сильной, что человек становится инвалидом и не может выполнять повседневные дела.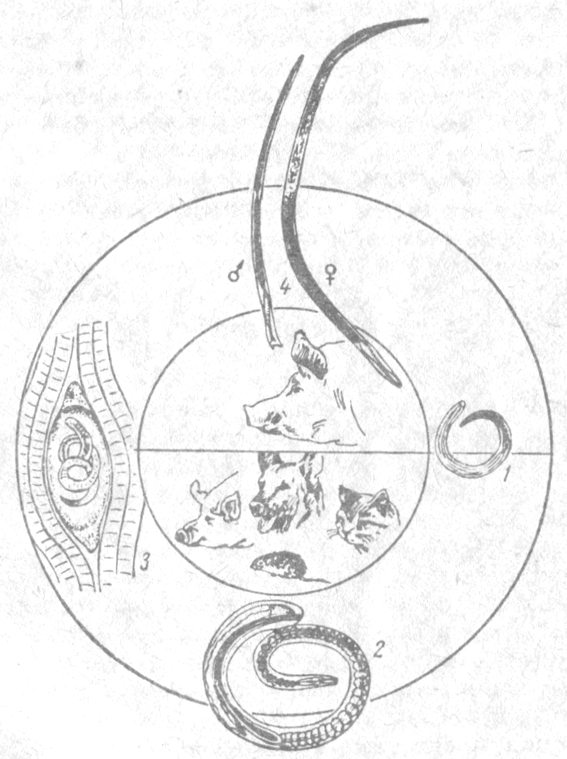
Классические симптомы трихинеллеза обычно проявляются через 2 недели после употребления сырого или недоваренного мяса и могут длиться до 8 недель. Симптомы включают лихорадку, озноб, миалгию, периорбитальный или лицевой отек, слабость и утомляемость. Также существуют сообщения о продолжительной диарее [9]. Другими распространенными симптомами являются конъюнктивит и субконъюнктивальные кровоизлияния, наблюдаемые примерно у 50% пациентов. [10] Также могут возникать осколочные кровоизлияния в ногтевые ложа (подногтевые) и кровоизлияния в сетчатку. Сыпь чаще всего имеет форму крапивницы, но может проявляться кровотечением из осколков и петехиями.Ключевой находкой является отек век, который часто связан с проптозом и хемозом. Другие менее распространенные проявления включают головную боль, кашель, сыпь, головную боль, одышку и дисфагию. Иногда также может возникать гепатомегалия. [11] К серьезным осложнениям относятся миокардит, опасные для жизни аритмии, менингит, энцефалит, респираторный миозит, вторичная бактериальная пневмония, гематурия и почечная недостаточность. [12] [13] [14] [15]
[12] [13] [14] [15]
Оценка
Первоначальный диагноз обычно ставится на основании клинических признаков и симптомов.Диагностическое подтверждение подтверждается серологией или иногда может потребоваться биопсия мышцы.
Общий анализ крови может показать лейкоцитоз и эозинофилию, что коррелирует с количеством гельминтов, вызывающих инфекцию. [3] Креатинкиназа, лактатдегидрогеназа, альдолаза и аминотрансферазы могут быть повышены из-за вторжения паразитов в скелетные мышцы, вызывающего разрушение мышц. У пациентов также может быть гипокалиемия, гипоальбуминемия и повышенный уровень IgE в сыворотке крови. Все эти тесты неспецифичны, поскольку их можно увидеть при других паразитарных заболеваниях и аутоиммунных заболеваниях.[16]
Доступны серологические тесты: ELISA (иммуноферментный анализ), непрямой IF (иммунофлуоресценция) и тест латекс-агглютинации. Подтверждение серологического теста может быть выполнено с помощью вестерн-блоттинга. [17] Иногда серологический анализ оказывается ненадежным, главным образом на раннем этапе заболевания (в течение первых 3 недель и более). Заражение другими организмами, такими как нематоды или другие гельминты, а также аутоиммунные заболевания могут вызвать ложноположительную серологическую реакцию.
Заражение другими организмами, такими как нематоды или другие гельминты, а также аутоиммунные заболевания могут вызвать ложноположительную серологическую реакцию.
Обычный рентгеновский снимок может показать плотность кальцина в мышцах.Компьютерная томография (КТ) проводится для исключения других причин неврологической дисфункции.
Электрокардиограмма (ЭКГ) может показать признаки перикардита, ишемии или миокардита. Могут быть преждевременные сокращения желудочков (ЖЭ), удлинение интервала PR, блокада проводимости или предсердные аритмии.
Окончательный метод диагностики – биопсия мышцы. [10] Чувствительность высокая, если биопсия проводится через 4 недели после заражения. Если его выполнить на ранней стадии заболевания, он может быть отрицательным.
Лечение / ведение
Клиническое течение трихинеллеза в большинстве случаев самоограничено и не вызывает осложнений. Легкие инфекции лечат симптоматически жаропонижающими и противовоспалительными средствами.
Инфекция Trichinella с системными осложнениями лечится противопаразитарными средствами и кортикостероидами. [18] Противопаразитарные средства, которые можно использовать, включают альбендазол 500 мг два раза в день перорально в течение 10-14 дней, мебендазол 200-400 мг три раза в день в течение 3 дней, затем от 400 до 500 мг трижды в день в течение 10 дней.В тяжелых случаях может потребоваться одновременный прием с преднизоном в дозе от 30 до 60 мг в день в течение в общей сложности от 10 до 14 дней.
Альбендазол и мебендазол не считаются безопасными для беременных женщин и детей младше 2 лет. В этих случаях и в таких случаях необходима консультация специалиста, а перед назначением этих лекарств необходимо взвесить риски и преимущества. Всемирная организация здравоохранения рекомендует беременным женщинам принимать противоглистные препараты (мебендазол, альбендазол, пирантел или левамизол) после первого триместра.[19]
Пациентам с поражением сердца может потребоваться кардиологический мониторинг.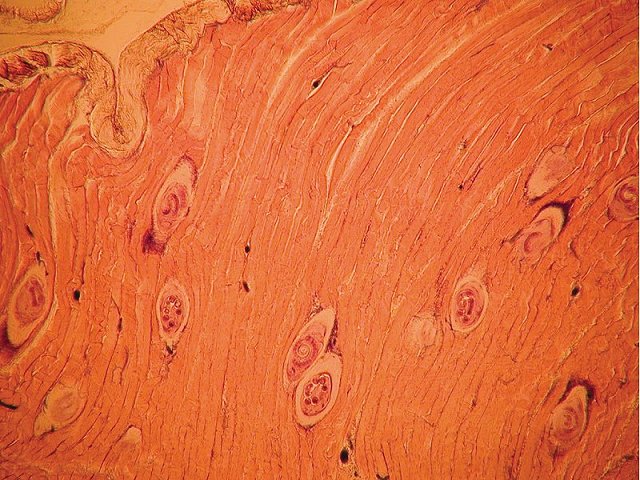
Постконтактная профилактика мебендазолом, если ее вводить в течение 6 дней после контакта, может быть эффективной [20].
Дифференциальный диагноз
Гастроэнтерит – вирусный или бактериальный
Полимиозит и дерматомиозит (аутоиммунный)
Периорбитальный целлюлит
Миалминофилический синдром, другие инфекции, связанные с эозинозинофилией фасциола, шистосомоз, токсокароз, цистицеркоз, мигрирующая висцеральная личинка и саркоцистоз.
Прогноз
Трихинеллез обычно имеет доброкачественное течение и проходит самостоятельно. Ожидается полное выздоровление пациентов в течение 2-6 месяцев после заражения. Однако некоторые случаи могут быть тяжелыми, и даже возможна смерть. Смерть наступает редко, если сердце и ЦНС остаются не задействованными. У некоторых людей с поражением ЦНС в долгосрочной перспективе может быть остаточный дефицит. Прогноз заболевания пропорционально коррелирует с паразитарной нагрузкой.

Сдерживание и просвещение пациентов
Трихинеллез вызывается употреблением сырого или недоваренного мяса инфицированных животных.Пациенты должны получить информацию о риске передачи инфекции при употреблении в пищу необработанного или сырого мяса. Сообщений о передаче от человека к человеку нет. Случаи могут возникать в группах среди групп людей из одной общины или одной семьи, которые употребляли инфицированное мясо обычного животного. Пациентов следует научить нагревать мясо до температуры не менее 77 градусов по Цельсию, что убивает личинок Trichinella . Пациентам также следует проконсультироваться по вопросам соблюдения правил безопасности пищевых продуктов.
Улучшение результатов команды здравоохранения
Лечение и профилактика трихинеллеза требует усилий межпрофессиональной команды.Сотрудничество и эффективное общение между медицинскими работниками имеют решающее значение для обеспечения безупречного ухода за пациентами. При необходимости следует обращаться за консультацией по поводу инфекционных заболеваний, чтобы выбрать наилучшие варианты лечения для пациента.
 Медсестры должны информировать пациентов о рисках передачи инфекции при употреблении недоваренного или сырого мяса. Фармацевты, медсестры и клиницисты должны знать о потенциальных побочных эффектах противоглистных препаратов, используемых при лечении трихинеллеза, и должны объяснять пациентам связанные с ними побочные эффекты.Когда пациенту ставится диагноз трихинелла, команда должна общаться, чтобы обеспечить стандарт лечения.
Медсестры должны информировать пациентов о рисках передачи инфекции при употреблении недоваренного или сырого мяса. Фармацевты, медсестры и клиницисты должны знать о потенциальных побочных эффектах противоглистных препаратов, используемых при лечении трихинеллеза, и должны объяснять пациентам связанные с ними побочные эффекты.Когда пациенту ставится диагноз трихинелла, команда должна общаться, чтобы обеспечить стандарт лечения.Рисунок
Trichinella Spiralis в скелетных мышцах. Изображение любезно предоставлено S Bhimji MD
Рисунок
Trichinella. Предоставлено CDC
Рисунок
Трихинелла. Предоставлено CDC.
Рисунок
Личинки трихинеллы. Предоставлено CDC.
Рисунок
Жизненный цикл трихинеллы.Предоставлено CDC
Ссылки
- 1.
- Blaxter ML, De Ley P, Garey JR, Liu LX, Scheldeman P, Vierstraete A, Vanfleteren JR, Mackey LY, Dorris M, Frisse LM, Vida JT, Thomas WK . Молекулярная эволюционная структура для филума Nematoda.
 Природа. 1998 5 марта; 392 (6671): 71-5. [PubMed: 9510248]
Природа. 1998 5 марта; 392 (6671): 71-5. [PubMed: 9510248] - 2.
- Lo YC, Hung CC, Lai CS, Wu Z, Nagano I, Maeda T., Takahashi Y, Chiu CH, Shyong Jiang DD. Трихинеллез человека после употребления в пищу черепах с мягким панцирем, Тайвань.Emerg Infect Dis. 2009 декабрь; 15 (12): 2056-8. [Бесплатная статья PMC: PMC3044530] [PubMed: 19961701]
- 3.
- Gottstein B, Pozio E, Nöckler K. Эпидемиология, диагностика, лечение и борьба с трихинеллезом. Clin Microbiol Rev.2009, январь; 22 (1): 127-45, Содержание. [Бесплатная статья PMC: PMC2620635] [PubMed: 1
- 37]
- 4.
- Capó V, Despommier DD. Клинические аспекты заражения Trichinella spp. Clin Microbiol Rev.1996, январь; 9 (1): 47-54. [Бесплатная статья PMC: PMC172881] [PubMed: 8665476]
- 5.
- Мюррелл К.Д., Позио Е. Трихинеллез: зооноз, который не пройдет спокойно. Int J Parasitol. 2000 ноя; 30 (12-13): 1339-49. [PubMed: 11113259]
- 6.
- Ортега-Пьерс М.Г., Арриага С.
 , Епес-Мулиа Л. Эпидемиология трихинеллеза в Мексике, Центральной и Южной Америке. Vet Parasitol. 2000 декабрь 01; 93 (3-4): 201-25. [PubMed: 11099838]
, Епес-Мулиа Л. Эпидемиология трихинеллеза в Мексике, Центральной и Южной Америке. Vet Parasitol. 2000 декабрь 01; 93 (3-4): 201-25. [PubMed: 11099838] - 7.
- Moorhead A, Grunenwald PE, Dietz VJ, Schantz PM. Трихинеллез в США, 1991–1996 годы: снижение, но не исчезновение.Am J Trop Med Hyg. 1999 Янв; 60 (1): 66-9. [PubMed: 9988325]
- 8.
- Teunis PF, Koningstein M, Takumi K, van der Giessen JW. Люди очень восприимчивы к низким дозам Trichinella spp. Epidemiol Infect. 2012 февраль; 140 (2): 210-8. [PubMed: 21489335]
- 9.
- MacLean JD, Poirier L, Gyorkos TW, Proulx JF, Bourgeault J, Corriveau A, Illisituk S, Staudt M. Эпидемиологическое и серологическое определение первичного и вторичного трихинеллеза в Арктике. J Infect Dis.1992 Май; 165 (5): 908-12. [PubMed: 1569342]
- 10.
- Bruschi F, Murrell KD. Новые аспекты трихинеллеза человека: влияние новых видов трихинелл. Postgrad Med J. 2002 Янв; 78 (915): 15-22. [Бесплатная статья PMC: PMC1742236] [PubMed: 11796866]
- 11.
- Негина Р., Негина А.М. Отзывы о трихинеллезе (IV): поражение печени. Foodborne Pathog Dis. 2011 сентябрь; 8 (9): 943-8. [PubMed: 21524198]
- 12.
- Негина Р., Негина А.М., Маринку И. Отзывы о трихинеллезе (III): поражение сердечно-сосудистой системы.Foodborne Pathog Dis. 2011 август; 8 (8): 853-60. [PubMed: 21438766]
- 13.
- Мохортер С.Д., Казура Дж. У. Трихинеллез центральной нервной системы. Semin Neurol. 1993 июн; 13 (2): 148-52. [PubMed: 8356348]
- 14.
- Комптон С.Дж., Селум К.Л., Ли С.Томпсон Д., Суми С.М., Фриче Т.Р., Кумбс Р.В. Трихинеллез с дыхательной недостаточностью и стойким миокардитом. Clin Infect Dis. 1993 Апрель; 16 (4): 500-4. [PubMed: 8513055]
- 15.
- Негина Р., Негина А.М., Маринку И., Якобичу И.Отзывы о трихинеллезе (I): поражение почек. Foodborne Pathog Dis. 2011 Февраль; 8 (2): 179-88. [PubMed: 21034231]
- 16.
- Ватанабе Н., Бруски Ф., Коренага М. IgE: вопрос защитного иммунитета при инфекции Trichinella spiralis. Trends Parasitol. 2005 Апрель; 21 (4): 175-8. [PubMed: 15780839]
- 17.
- Taher EE, Méabed EMH, El Akkad DMH, Kamel NO, Sabry MA. Модифицированный точечный ELISA для диагностики трихинеллеза человека. Exp Parasitol. 2017 июн; 177: 40-46. [PubMed: 28438521]
- 18.
- Watt G, Saisorn S, Jongsakul K, Sakolvaree Y, Chaicumpa W. Слепое плацебо-контролируемое испытание противопаразитарных препаратов при трихинеллезном миозите. J Infect Dis. 2000 Июль; 182 (1): 371-4. [PubMed: 10882628]
- 19.
- Gyorkos TW, Larocque R, Casapia M, Gotuzzo E. Отсутствие риска неблагоприятных исходов родов после дегельминтизации у беременных женщин. Pediatr Infect Dis J. 2006 Сентябрь; 25 (9): 791-4. [PubMed: 16940835]
- 20.
- Faber M, Schink S, Mayer-Scholl A, Ziesch C, Schönfelder R, Wichmann-Schauer H, Stark K, Nöckler K.Вспышка трихинеллеза из-за мяса кабана и оценка эффективности постконтактной профилактики, Германия, 2013 г. Clin Infect Dis. 2015 15 июня; 60 (12): e98-e104. [PubMed: 25770171]
Спиральная инкапсулированная личинка трихинеллы
Am J Trop Med Hyg. 2020 ноя; 103 (5): 1754.
Медицинский колледж Бейлора, Хьюстон, Техас
Автор, ответственный за переписку. * Адресная корреспонденция Джилл Э. Уэзерхед, Медицинский колледж Бейлора, 1102 Бейтс, офис 1120, Хьюстон, Техас 77030.Адреса авторов: Юлика Каплан, кафедра педиатрии, Медицинский колледж Бейлора, Хьюстон, Техас, и кафедра внутренней медицины, Медицинский колледж Бейлора, Хьюстон, Техас, электронная почта: ude.mcb @ nalpak.akiluj. Кристи Дж. Финч, отделение патологии, Медицинский колледж Бейлора, Хьюстон, Техас, электронная почта: ude.mcb@hcnifc. Джилл Э. Уэзерхед, кафедра педиатрии, Медицинский колледж Бейлора, Хьюстон, Техас, электронная почта: ude.mcb@hrehtaew.Поступила в редакцию 29 апреля 2020 г .; Принята в печать 14 июля 2020 г.
Авторские права © Американское общество тропической медицины и гигиены Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution (CC-BY), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии, что автор оригинала. и источник указаны.У мужчины 51 года с метастатическим папиллярным раком щитовидной железы была проведена модифицированная диссекция шеи с иссечением поясничной мышцы. Помимо злокачественности, гистопатология продемонстрировала инкапсулированную кисту размером 275 мкм, содержащую личинку диаметром 27 мкм с бациллярными полосами (стрелка) в скелетных мышцах, соответствующими видам Trichinella ().Бациллярные тяжи представляют собой ряды отдельных железистых клеток, пересекающих длину личинки, и описаны у нематод Trichinella , Trichuris и Capillaria . 1 Несколько инкапсулированных кист с интактными личинками, в дополнение к множественным дегенерирующим очагам аналогичного размера, были замечены по всей мышце рядом со злокачественными образованиями. Пациент был родом из Мехико, Мексика, и переехал в Хьюстон, штат Техас, за 17 лет до обращения без дальнейших поездок.Он ел сырую свинину 10 лет назад, находясь в Техасе, но отрицал употребление диких животных. На момент презентации количество лейкоцитов составляло 6900 клеток / мкл, абсолютное количество эозинофилов составляло 360 клеток / мкл, а креатинкиназа сыворотки составляла 149 единиц / л. Исследование кала на яйца и паразитов было отрицательным, сывороточные антитела Strongyloides были отрицательными, а сывороточные антитела Toxocara были положительными. Больной протекал бессимптомно. Хотя у пациента, скорее всего, был хронический трихинеллез, который менее чувствителен к антигельминтной терапии, он все же получил альбендазол, и абсолютное количество эозинофилов снизилось до 180 клеток / мкл после лечения. Trichinella передается человеку при употреблении в пищу сырого или недоваренного мяса инфицированных животных. 2 С 2011 по 2015 год в США было зарегистрировано 80 случаев трихинеллеза; 9–10 произошли в Техасе и были связаны с потреблением мяса медведя. 3 Трихинеллез от домашней свинины редко встречается в Соединенных Штатах из-за обширного законодательства и кампаний в области общественного здравоохранения. 2 Обычно трихинеллез диагностируется на основании наличия классических признаков и симптомов, включая лихорадку, миалгию, отек и диарею, после недавнего употребления сырого или недоваренного мяса в сочетании с последующим положительным серологическим анализом.Серологические анализы нацелены на IgG к экскреторному / секреторному продукту Trichinella с использованием ELISA, который может быть положительным через 12–60 дней после заражения. Ложноотрицательные тесты могут произойти, если инфекционная нагрузка минимальна или если анализ проводится через годы после первоначального заражения. Следует также отметить, что серологические анализы могут давать ложноположительные результаты из-за перекрестной реактивности с другими паразитарными инфекциями. Биопсия мышц реже используется в качестве диагностического инструмента, но при положительном результате имеет высокую специфичность. 4
Киста, инкапсулированная трихинеллой в скелетных мышцах. Этот рисунок представлен в цвете на сайте www.ajtmh.org.
СПИСОК ЛИТЕРАТУРЫ
1. Kozek WJ, 2005. Ответственны ли бациллярные полосы за изгнание Trichinella spiralis ? Ветеринарный паразитол 132: 69–73. [PubMed] [Google Scholar] 4. Pozio E, Gomez Morales MA, Dupouy-Camet J, 2003. Клинические аспекты, диагностика и лечение трихинеллеза. Exp Rev Anti Infect Ther 1: 471–482.[PubMed] [Google Scholar]The WBG – служба онлайн-публикаций WormBook
Wadim J. Kapulkin 1, 2, 3
1 Отделение вирусологии и иммунопатологии, Национальный институт общественного здравоохранения-PZH, Chocimska 24, 00-791 Варшава, Польша
2 Отделение инфекционных болезней, микробиологии и паразитологии, факультет ветеринарной медицины, Grochowska 272, 03-849 Варшава, Польша
3 || Нынешний адрес: Veterinary Consultancy, Conrada 01-922 Варшава, ПольшаРНК-интерференция (Fire et al.1998) – популярная стратегия скрининга «обратной генетики». В частности, проглоченный вариант РНКи (Timmons et al. 1999) приобрел популярность для скрининга всего генома, когда бактериально экспрессируемая дцРНК вводится per os с использованием модифицированных плазмид и E. coli в качестве питающего вектора (Timmons et al. 2001 ). Полногеномный скрининг РНКи в настоящее время осуществляется с использованием библиотек для кормления РНКи.
В настоящее время доступны два типа «питающих библиотек» РНКи по всему геному, влекущих за собой ПЦР-амплифицированные целевые области: библиотека предсказанных перекрывающихся сегментов генов (Kamath et al.2003) и амплифицированную библиотеку кДНК (Rual et al. 2004). Однако доступные библиотеки рекомбинантных РНКи на основе ПЦР по всему геному – ресурсы, состоящие из плазмид, продуцирующих дцРНК, – в значительной степени зависят от предсказаний генов, отсюда и смещение в сторону определенных богатых экзонами участков генов или определенных кДНК. Здесь я сообщаю о дополнительном ресурсе, способствующем подходу к скринингу РНКи, основанному на беспристрастной стратегии «прямой генетики».
Эксперименты, основанные на этом подходе, начались с конструирования библиотеки геномных сегментов, включенных в вектор конвергентной плазмиды сайтов связывания полимеразы Т7 (PBS) (плазмида L4440), который был лигирован со стандартной мелкомасштабной жидкой ДНК червя, предварительно расщепленной с помощью EcoRI . и HindIII * и преобразован в HT115 (DE3) E.coli (Тиммонс и др., 2001). Полученная конвергентная библиотека T7 PBS была оценена как ~ 95% рекомбинантная. Конвергентные клоны библиотеки T7 скармливались индивидуально по стандартному протоколу (как описано ранее, Kapulkin et al. 2005) червям, полученным из N2, для подтверждения очевидного летального / стерильного фенотипа, встречающегося с частотой 1-2 на 24 протестированных клона.
Основываясь на вышеупомянутом эксперименте, я считаю, что прямой скрининг РНК-интерференции полезен и осуществим, с сильным ожиданием, что представленный режим скрининга дополнит и расширит существующие, доступные в настоящее время, общегеномные ресурсы РНКи.
* Другие варианты эксперимента, исследованные в другом месте, включают фрагментированную ДНК, лигированную с другими ферментами и / или линкерами .
Список литературы
Fire A, Xu S, Montgomery MK, Kostas SA, Driver SE, Mello CC. Сильная и специфическая генетическая интерференция двухцепочечной РНК у Caenorhabditis elegans. Природа. 1998 19 февраля; 391 (6669): 806-11.
Kamath RS, Fraser AG, Dong Y, Poulin G, Durbin R, Gotta M, Kanapin A, Le Bot N, Moreno S, Sohrmann M, Welchman DP, Zipperlen P, Ahringer J.Систематический функциональный анализ генома Caenorhabditis elegans с использованием РНКи. Природа. 2003 16 января; 421 (6920): 231-7.
Капулкин В.Дж., Hiester BG, Ссылка CD. Компенсаторная регуляция среди шаперонов ER у C. elegans. FEBS Lett. 6 июня 2005 г .; 579 (14): 3063-8. Ошибка в: FEBS Lett. 2007 22 декабря; 581 (30): 5952. Капулкин, Вадим [исправлено на Капулкина, Вадима Дж.].
Rual JF, Ceron J, Koreth J, Hao T, Nicot AS, Hirozane-Kishikawa T., Vandenhaute J, Orkin SH, Hill DE, van den Heuvel S, Vidal M.На пути к улучшению картирования феномена Caenorhabditis elegans с помощью библиотеки РНКи на основе ORFeome. Genome Res. 2004 Октябрь; 14 (10B): 2162-8.
Timmons L, Court DL, Fire A. Проглатывание экспрессируемых бактериями дцРНК может вызывать специфическое и сильное генетическое вмешательство в Caenorhabditis elegans. Ген. 2001 24 января; 263 (1-2): 103-12.
Timmons L, Fire A. Специфическое вмешательство проглоченной дцРНК. Природа. 1998 29 октября; 395 (6705): 854.
ADW: Trichinella spiralis: ИНФОРМАЦИЯ
Географический диапазон
Trichinella spiralis распространена в Мексике, северном полушарии, некоторых частях южной Азии, Африке, Южной Америке и на Ближнем Востоке.Этот вид также встречается в других тропических регионах. (Olsen, 1974; Робертс, Джанвой, 1996)
Среда обитания
Trichinella spiralis имеет чрезвычайно широкий круг хозяев; практически любой вид млекопитающих может заразиться. Взрослые черви живут вокруг столбчатых эпителиальных клеток тонкой кишки, а личинки живут в поперечно-полосатых мышечных клетках одного и того же млекопитающего.
Существует три различных экологических типа жизненных циклов: городской цикл, лесной цикл и морской цикл.В городском цикле крысы и свиньи служат хозяевами и резервуарами паразита. Люди могут заразиться глистом, если съесть не тщательно приготовленную свинину. В лесном цикле хозяевами T. spiralis являются хищники и падальщики. Тюлени, моржи, киты и белые медведи – все они являются хозяевами морского цикла. (Lapage, 1957; Olsen, 1974; Roberts, Janvoy, 1996; Wassom, 1988)
Физическое описание
Trichinella spiralis – самый мелкий из известных нематодных паразитов человека.Самцы имеют длину от 1,4 до 1,6 мм, а самки вдвое больше самцов. Тело червя на переднем конце более тонкое, чем на заднем. У самок матка находится в задней части червя и заполнена развивающимися яйцами. На переднем конце самки вылупляются молодые особи.
Эта нематода имеет кутикула с тремя или более основными внешними слоями из коллагена и других соединений.Внешние слои неклеточные и секретируются эпидермисом. Слой кутикулы защищает нематод, поэтому они могут проникать в пищеварительный тракт животных.
Нематоды имеют продольные мышцы вдоль стенки тела. Мышцы расположены косо полосами. Дорсальные, вентральные и продольные нервные тяжи связаны с основным телом мышцы. (Barnes, 1987; Olsen, 1974; Roberts, Janvoy, 1996)
- самка крупнее
- полы сформированы по-разному
- Длина диапазона
- 1.От 4 до 3,2 мм
- от 0,06 до 0,13 дюйма
Разработка
Жизненный цикл этого вида начинается после поедания молоди первой стадии от промежуточного хозяина. В течение первых тридцати часов червь линяет четыре раза, а затем спаривается. Эти личинки выходят через стенку кишечника и попадают в систему крови через ветви воротной вены печени или через лимфатическую систему.Они переносятся по всему телу и поселяются в произвольных мышцах, проникая в отдельные мышечные клетки. Личинки растут внутри мышц, и вокруг них создается покрытие, вызывающее кисту. После образования кисты червь не может мигрировать дальше. Единственный способ, которым этот вид может продолжить свой жизненный цикл, – это попадание в организм другого хозяина в результате взаимодействия хищника и жертвы. Когда новый хозяин ест мышечную ткань, содержащую кисту, пищеварительные соки разрушают капсулу и высвобождают червя.(Lapage, 1957; Olsen, 1974; Read, 1972; Wassom, 1988)
Репродукция
Жизненный цикл этого вида начинается после поедания молоди первой стадии от промежуточного хозяина. В течение первых тридцати часов червь линяет четыре раза, а затем спаривается.
Самки могут производить фермомоны для привлечения самцов. Мужчина Обвивается вокруг самки своей изогнутой областью над женскими половыми органами. Губернакулум, сделанный из ткани кутикулы, направляет спикулы, которые проходят через клоаку и задний проход.Самцы используют спикулы, чтобы удерживать самку во время совокупления. Сперма нематод амебовидная, без жгутиков.
Самка яйцекладущая. Это означает, что она производит яйца, но не откладывает их, пока они не вылупятся в ее матке. Она откладывает живых личинок в тонком кишечнике на пятый или шестой день после заражения. (Barnes, 1987; Lapage, 1957; Olsen, 1974; Read, 1972; Wassom, 1988)
- предварительное оплодотворение
- до вылупления / рождения
Поведение
Trichinella spiralis – распространенный паразит хищных и всеядных млекопитающих, включая человека.Существует три различных экологических типа жизненных циклов: городской цикл, лесной цикл и морской цикл. В городском цикле крысы и свиньи служат хозяевами и резервуарами паразита. Люди могут заразиться глистом, если съесть не тщательно приготовленную свинину. В лесном цикле хозяевами T. spiralis являются хищники и падальщики. Тюлени, моржи, киты и белые медведи – все они являются хозяевами морского цикла. (Olsen, 1974; Робертс, Джанвой, 1996)
Коммуникация и восприятие
Нематоды в целом имеют сосочки, щетинки и амфиды как главные органы чувств.Щетинки обнаруживают движение (механорецепторы), а амфиды – химические вещества (хеморецепторы). (Барнс, 1987)
Привычки к еде
Взрослые особи питаются кишечным эпителием хозяина. Молодь проникает в отдельные волокна скелетных мышц и питается там.
Глоточные железы и эпителий кишечника вырабатывают пищеварительные ферменты, которые питаются жидкостями организма хозяина. Внеклеточное пищеварение начинается в просвет и заканчивается внутриклеточно.(Барнс, 1987; Робертс, Дженвой, 1996)
Хищничество
Эти паразиты обычно не становятся жертвами напрямую, а переходят от одного хозяина к другому. Смертность личинок высока, поскольку большинство паразитов не достигают подходящих хозяев.
Роли экосистемы
Люди обычно заражаются от инфицированных свиней, однако заболеваемость среди свиней составляет всего 0,37% (Лукашенко, 1966). Этот вид легче найти у кошек с заболеваемостью 71.23%, крысы – 6,43% или даже мыши – 3,38%. (Лукашенко, 1966; Робертс, Жанвой, 1996)
Экономическое значение для людей: положительный результат
Проведенное исследование приводит к выводу, что нет никаких известных экономических выгод от Trichinella spiralis для человека.
Экономическое значение для людей: отрицательно
Люди могут узнать этого паразита чаще по вызываемой им болезни.Это заболевание известно как трихинеллез, трихинеллез или трихинеллиоз. Люди могут заразиться этим паразитом, поедая уже инфицированное мясо. Обычно человек заражается недоваренной свининой. Сырая колбаса является деликатесом во многих регионах мира, поэтому трихинеллез становится хронической проблемой для здоровья. Симптомы этого заболевания могут включать:
- Слабость и мышечные подергивания из-за того, что детеныш откладывается самкой червя.
- Отек вокруг глаз, сильная мышечная боль, нарушение мышечной функции, затрудненное дыхание и постоянная лихорадка – это симптомы, которые соответствуют миграции подростка и проникновению в мышечную ткань.
- Лицо опухает. Отек конечностей, поражение сердца, нервной системы и других органов, отечность лица и пневмония – это симптомы, которые могут возникнуть при проникновении глистов в мышечную ткань.
Неизвестно хорошее средство для избавления организма от этого паразита. Лечение анальгетиками и кортикостероидами просто облегчает симптомы трихинеллеза. Заболеваемость инфекцией неуклонно снижается во всем мире.Заболеваемость в Соединенных Штатах снизилась с более чем 400 случаев в год в 1940-х годах до 30-40 случаев в год в 1987–1989 годах. (Lapage, 1957; Read, 1972; Roberts, Janvoy, 1996)
Trichinella spiralis – крупнейший внутриклеточный паразит в мире.
Кальцинированные гранулы, которые образуются в мышцах хозяина, в конечном итоге привели к открытию этого вида в 1835 году. Джеймс Пэджет, изучавший медицину в Лондоне, заметил, что его скальпели тускнеют из-за песчаных частиц в мышцах. трупа, над которым он работал.Он заметил их червеобразную природу и показал их анатому Ричарду Оуэну, который в конечном итоге дал им научное название. Двадцать пять лет спустя они определили, что эти животные вызывали болезнь. (Робертс и Дженвой, 1996)
Авторы
Рене Шерман Малкроне (редактор).
Джинджер Хартвелл (автор), Мичиганский университет в Анн-Арборе, Тереза Фридрих (редактор), Мичиганский университет в Анн-Арборе.
Глоссарий
- эфиопский
живут в Африке к югу от Сахары (к югу от 30 градусов северной широты) и на Мадагаскаре.
- Неарктика
человек проживает в Неарктической биогеографической провинции, северной части Нового Света.Это включает Гренландию, канадские арктические острова и всю Северную Америку вплоть до юга до высокогорья центральной Мексики.
- Неотропический
проживает в южной части Нового Света. Другими словами, Центральная и Южная Америка.
- Палеарктика
проживает в северной части Старого Света.Другими словами, Европа и Азия и Северная Африка.
- сельское хозяйство
человек живут на ландшафтах, где преобладает сельское хозяйство.
- двусторонняя симметрия
, имеющий такую симметрию тела, что животное можно разделить в одной плоскости на две зеркальные половины.У животных с двусторонней симметрией есть спинная и вентральная стороны, а также передний и задний концы. Синапоморфия билатериев.
- плотоядное животное
животное, которое в основном ест мясо
- вызывает заболевание у людей
животное, которое непосредственно вызывает заболевание у человека.Например, заболевания, вызванные заражением нитчатыми нематодами (слоновость и речная слепота).
- вызывает или переносит болезнь домашних животных
либо напрямую вызывает, либо косвенно передает заболевание домашнему животному
- чапараль
Обитает в прибрежных районах между 30 и 40 градусами широты, в районах со средиземноморским климатом.В растительности преобладают густые колючие кустарники с жесткими (твердыми или восковидными) вечнозелеными листьями. Может поддерживаться периодическим огнем. В Южной Америке он включает экотон кустарника между лесом и парамо.
- химический
использует запахи или другие химические вещества для общения.
- пустыня или дюны
в пустынях низкие (менее 30 см в год) и непредсказуемые осадки приводят к тому, что в ландшафтах преобладают растения и животные, адаптированные к засушливости.Растительность обычно редкая, хотя после дождя может наблюдаться эффектное цветение. Пустыни могут быть холодными или теплыми, а дневная температура обычно колеблется. В дюнных районах растительность также скудна, и условия здесь сухие. Это связано с тем, что песок плохо удерживает воду, поэтому растениям доступно мало. В дюнах у морей и океанов это усугубляется влиянием соли в воздухе и почве. Соль ограничивает способность растений впитывать воду корнями.
- экзотермический
животных, которые должны использовать тепло, полученное из окружающей среды, и поведенческие адаптации для регулирования температуры тела
- удобрения
союз яйцеклетки и сперматозоида
- лес
- В
лесных биомах преобладают деревья, в противном случае лесные биомы могут сильно различаться по количеству осадков и сезонности.
- гетеротермический
имеет температуру тела, которая колеблется в зависимости от температуры окружающей среды; не имеющий механизма или плохо развитый механизм регулирования внутренней температуры тела.
- внутреннее оплодотворение
оплодотворение происходит в теле женщины
- подвижный
, имеющий возможность перемещаться с одного места на другое.
- горы
Этот наземный биом включает вершины высоких гор, либо без растительности, либо покрытые низкой растительностью, напоминающей тундру.
- восточный
найдено в восточном регионе мира.Другими словами, Индия и Юго-Восточная Азия.
- яйцекладущие
размножение, при котором яйца развиваются внутри материнского тела без дополнительного питания от родителя и вылупляются внутри родителя или сразу после кладки.
- паразит
организм, который получает питательные вещества от других организмов вредным способом, не вызывающим немедленной смерти
- феромоны
химических веществ, выбрасываемых в воздух или воду, которые обнаруживаются другими животными того же вида и реагируют на них
- полярный
области Земли, которые окружают северный и южный полюсы, от северного полюса до 60 градусов северной широты и от южного полюса до 60 градусов южной широты.
- тропический лес
- В
тропических лесах, как умеренных, так и тропических, преобладают деревья, часто образующие закрытый навес с небольшим количеством света, достигающего земли. Обильны также эпифиты и вьющиеся растения. Количество осадков, как правило, не ограничено, но может быть сезонным.
- кустарник
кустарниковых лесов развиваются в районах с засушливым сезоном.
- малоподвижный
остается в том же районе
- сидячий
неподвижный; постоянно прикреплен к основанию.
Прикреплен к субстрату и мало или совсем не движется.Синапоморфия Anthozoa
- половой
воспроизводство, включающее сочетание генетического вклада двух особей, мужчины и женщины
- пригород
проживающих в спальных районах на окраинах крупных городов.
- тактильный
использует прикосновение для связи
- тайга
Хвойные или бореальные леса, расположенные полосой в северной части Северной Америки, Европы и Азии.Этот наземный биом также находится на больших высотах. Длинная холодная зима и короткое влажное лето. Присутствуют несколько видов деревьев; Это в первую очередь хвойные породы, которые растут густыми насаждениями с небольшим подлеском. Также могут присутствовать некоторые лиственные деревья.
- умеренный
, этот регион Земли между 23,5 градусом северной широты и 60 градусом северной широты (между тропиком Рака и полярным кругом) и между 23.5 градусов южной широты и 60 градусов южной широты (между тропиком Козерога и Северным полярным кругом).
- наземные
Проживает на земле.
- тропический
регион Земли, окружающий экватор, начиная с 23.От 5 градусов северной широты до 23,5 градусов южной широты.
- тропическая саванна и луга
Наземный биом. Саванны – это луга с разбросанными отдельными деревьями, которые не образуют закрытого полога. Обширные саванны встречаются в некоторых частях субтропической и тропической Африки и Южной Америки, а также в Австралии.
- саванна
Пастбище с разбросанными деревьями или разбросанными группами деревьев, тип сообщества, занимающий промежуточное положение между пастбищами и лесами.См. Также Тропическая саванна и биом пастбищ.
- пастбища умеренного пояса
Наземный биом, обнаруженный в умеренных широтах (> 23,5 ° северной или южной широты). Растительность состоит в основном из злаков, высота и видовое разнообразие которых во многом зависят от количества доступной влаги. Пожары и выпас скота важны для долгосрочного ухода за пастбищами.
- тундра
Наземный биом с низкой, кустарниковой или похожей на циновку растительностью, встречающийся на очень высоких широтах или возвышенностях, почти на пределе роста растений.Почвы обычно подвержены вечной мерзлоте. Разнообразие растений обычно невелико, а вегетационный период короткий.
- городской
живут в городах и крупных поселках, в ландшафтах преобладают человеческие структуры и деятельность.
Список литературы
Барнс, Р.1987. Зоология беспозвоночных. Орландо, Флорида: Драйден Пресс.
Lapage, G. 1957. Животные-паразиты. Кембридж в University Press.
Лукашенко Н. 1966. Эпизоотология трихинеллеза. Стр. 371-375 в А. Петрова, изд. Вклад в гельминтологию. Иерусалим: Израильская программа научных переводов, Ltd.
Государственный университет Огайо, 2001 г. «Trichinella spiralis (трихинеллез или трихинеллез)» (Онлайн).Паразиты и паразитологические ресурсы. Доступно 07 октября 2004 г. на http://www.biosci.ohio-state.edu/~parasite/trichinella.html.
Олсен, О. 1974. Парастики животных: их жизненные циклы и экология. University Park Press.
Рид, С. 1972. Паразитизм животных. Нью-Джерси: Prentice-Hall, Inc ..
Робертс, Л., Дж. Жанвой. 1996. Основы паразитологии, 6 изд.. McGraw-Hill Companies, Inc ..
Wassom, D. 1988. Генетический контроль иммунитета к паразитарным инфекциям: исследования мышей, инфицированных трихинеллой. Стр. 329-346 в P Englund, A Sher, eds. Биология паразитизма. MBL Лекции по биологии Vol. 9. Нью-Йорк: Alan R. Liss Inc.,
Липидный профиль личинок Trichinella papuae на мышечной стадии
- 1.
Bruschi, F. & Murrell, K. Новые аспекты трихинеллеза человека: влияние новых видов Trichinella. Аспирантура. Med. J. 78 , 15–22 (2002).
CAS PubMed PubMed Central Статья Google ученый
- 2.
Хумджуй, К. и др. . Вспышка трихинеллеза, вызванная Trichinella papuae, Таиланд, 2006 г. Emerg. Заразить. Дис. 14 , 1913–1915 (2008).
PubMed PubMed Central Статья Google ученый
- 3.
Кусолсук Т. и др. . Вторая вспышка трихинеллеза, вызванная Trichinella papuae, в Таиланде. Пер. R. Soc. Троп. Med. Hyg. 104 , 433–437 (2010).
PubMed Статья Google ученый
- 4.
Фейдас, Х., Куам, М.К., Канцура, В. и Теодоропулос, Г. Глобальное географическое распространение видов и генотипов трихинелл. Заражение. Genet. Evol. 26 , 255–266 (2014).
PubMed Статья Google ученый
- 5.
Gottstein, B., Pozio, E. & Nöckler, K. Эпидемиология, диагностика, лечение и борьба с трихинеллезом. Clin. Microbiol. Ред. 22 , 127–145 (2009).
CAS PubMed PubMed Central Статья Google ученый
- 6.
Дэвид Дж. И Петри В. Маркелл и медицинская паразитология Voge.Эльзевьер Сондерс (2006).
- 7.
Watt, G., Saisorn, S., Jongsakul, K., Sakolvaree, Y. & Chaicumpa, W. Ослепленное, плацебо-контролируемое испытание противопаразитарных препаратов при трихинеллезном миозите. J. Infect. Дис. 182 , 371–374 (2000).
CAS PubMed Статья Google ученый
- 8.
Pozio, E., Sacchini, D., Sacchi, L., Tamburrini, A. & Alberici, F. Неэффективность мебендазола при лечении людей с инфекцией Trichinella spiralis на стадии инкапсулированных личинок. Clin. Заразить. Дис. 32 , 638–642 (2001).
CAS PubMed Статья Google ученый
- 9.
Вт, тГ. И Силахамрун, У. Области неопределенности в управлении трихинеллезом человека: клиническая перспектива. Эксперт. Rev. Anti Infect. Ther. 2 , 649–652 (2004).
Артикул Google ученый
- 10.
Saïdani, N., Grando, D., Valadié, H., Bastien, O. & Maréchal, E. Возможности и ограничения открытия in silico мишеней – тематическое исследование поиска новых противомалярийных химиотерапевтических мишеней. Заражение. Genet. Evol. 9 , 359–367 (2009).
PubMed Статья CAS Google ученый
- 11.
Карраско-Панкорбо, А., Навас-Иглесиас, Н. и Куадрос-Родригес, Л. От анализа липидов к липидомике – новый вызов аналитической химии 21 века. Trends Anal. Chem. 28 , 393–403 (2009).
Артикул CAS Google ученый
- 12.
Zheng, L. et al. . Профилирование липидов Leishmania donovani с использованием хроматографии гидрофильных взаимодействий в сочетании с масс-спектрометрией с преобразованием Фурье. Rapid Commun. Масс-спектрометр. 24 , 2074–2082 (2010).
объявления CAS PubMed Статья Google ученый
- 13.
Бестейро, С., Бертран-Мишель, Дж., Лебрен, М., Виаль, Х. и Дубремец, Дж. Ф. Липидомный анализ тахизоитов Toxoplasma gondii rhoptries: дальнейшее понимание роли холестерина. Biochem. J. 415 , 87–96 (2008).
CAS PubMed Статья Google ученый
- 14.
Ван, Т. и др. . Липидом развития Haemonchus contortus. Внутр. J. Parasitol. 48 , 887–895 (2018).
CAS PubMed Статья Google ученый
- 15.
Ботте, К. и др. . Субклеточная локализация и динамика дигалактолипидоподобного эпитопа у Toxoplasma gondii. J. Lipid Res. 49 , 746–762 (2008).
PubMed Статья CAS Google ученый
- 16.
Debierre-Grockiego, F. et al . Связывание гликозилфосфатидилинозитов Toxoplasma gondii с галектином-3 необходимо для их распознавания макрофагами. J. Biol. Chem. 285 , 32744–32750 (2010).
CAS PubMed PubMed Central Статья Google ученый
- 17.
Бутлис К.С. и др. . Антитела к гликозилфосфатидилинозитам Plasmodium falciparum: обратная связь с толерантностью к паразитемии у детей и взрослых Папуа-Новой Гвинеи. Заражение. Иммун. 70 , 5052–5057 (2002).
CAS PubMed PubMed Central Статья Google ученый
- 18.
Caldarelli, S.A. и др. . Изучение потенциального пролекарства солей бис-тиазолия Т3 и Т4 для пероральных противомалярийных препаратов. Bioorg Med. Chem. Lett. 20 , 3953–3956 (2010).
CAS PubMed Статья Google ученый
- 19.
Ракотоманга, М., Сен-Пьер-Шазале, М. и Луазо, П. М. Изменение метаболизма жирных кислот и стеролов у устойчивых к милтефозину промастигот Leishmania donovani и последствия для лекарственного взаимодействия с мембраной. Антимикробный. Агенты Chemother. 49 , 2677–2686 (2005).
CAS PubMed PubMed Central Статья Google ученый
- 20.
Сен-Пьер-Шазале, М. и др. . Истощение мембранных стеринов ухудшает действие милтефозина у промастигот Leishmania donovani дикого типа и устойчивых к милтефозину. J. Antimicrob. Chemother. 64 , 993–1001 (2009).
CAS PubMed Статья Google ученый
- 21.
Hac-Wydro, K., Dynarowicz-atka, P. & Zuk, R. Langmuir Монослойное исследование комбинированной антилейшмановской терапии с использованием амфотерицина B и эдельфозина. J. Phys. Chem. B 113 , 14239–14246 (2009).
CAS PubMed Статья Google ученый
- 22.
López-Martín, C., Pérez-Victoria, J. M., Carvalho, L., Castanys, S. & Gamarro, F. Чувствительность к ситамахину у видов Leishmania не опосредуется накоплением лекарства в ацидокальцисомах. Антимикробный. Агенты Chemother. 52 , 4030–4036 (2008).
PubMed PubMed Central Статья CAS Google ученый
- 23.
Wishart, D. S., Feunang, Y. D., Marcu, A., Guo, A. C. & Liang, K. HMDB 4.0 – База данных человеческого метаболизма за 2018 г. Nucleic Acids Res. 46 , D608–617 (2018).
CAS PubMed Статья Google ученый
- 24.
Han, X. & Gross, R. W. Масс-спектроскопический анализ с ионизацией электрораспылением фосфолипидов плазматической мембраны эритроцитов человека. Proc. Natl Acad. Sci. США 91 , 10635–10639 (1994).
объявления CAS PubMed Статья Google ученый
- 25.
Хан, X. и Гросс, Р. В. Липидомика дробовика: масс-спектрометрический анализ с ионизацией электрораспылением и количественное определение клеточных липидомов непосредственно из неочищенных экстрактов биологических образцов. Масс-спектр. Ред. 24 , 367–412 (2005).
объявления CAS PubMed Статья Google ученый
- 26.
Херманссон, М., Хокынар, К. и Сомерхарью, П. Механизмы гомеостаза глицерофосфолипидов в клетках млекопитающих. Prog. Lipid Res. 50 , 240–257 (2011).
CAS PubMed Статья Google ученый
- 27.
Патнаик, П. К. и др. . Молекулярно-видовой анализ фосфолипидов из кровотока Trypanosoma brucei и проциклических форм. Mol. Biochem. Паразитол. 58 , 97–105 (1993).
CAS PubMed Статья Google ученый
- 28.
Giera, M. et al. . Липидом Schistosoma mansoni: ведет к иммуномодуляции. Анал. Чим. Acta 11 , 107–118 (2018).
Артикул CAS Google ученый
- 29.
Вевер, В. и др. . Липидный профиль филяриальных нематод Onchocerca volvulus, Onchocerca ochengi и Litomosoides sigmodontis показывает накопление специфичных для нематод эфирных фосфолипидов в организме хозяина. Внутр. J. Parasitol. 47 , 903–912 (2017).
CAS PubMed PubMed Central Статья Google ученый
- 30.
Янг, Б. В. и Подеста, Р. Б. Основные фосфолипиды и синтез фосфатидилхолина у взрослых Schistosoma mansoni. Mol. Biochem. Паразитол. 5 , 165–172 (1982).
CAS PubMed Статья Google ученый
- 31.
Гоберт, Г. Н., Стензел, Д. Дж., МакМанус, Д. П. и Джонс, М. К. Ультраструктурная архитектура тегумента взрослой Schistosoma japonicum. Внутр. J. Parasitol. 33 , 1561–1575 (2003).
PubMed Статья Google ученый
- 32.
Wharton, D. A., Petrone, L., Duncan, A. & McQuillan, A. J. Поверхностный липид может контролировать падение проницаемости, связанное с вступлением в ангидробиоз у паразитической нематоды растений Ditylenchus dipsaci. J. Exp. Биол. 211 , 2901–2908 (2008).
CAS PubMed Статья Google ученый
- 33.
Гудридж, Х.С. и др. . Фосфорилхолин имитирует эффекты ES-62 на макрофаги и дендритные клетки. Parasite Immunol. 29 , 127–137 (2007).
CAS PubMed Статья Google ученый
- 34.
Болл Д. Х., Аль-Риями Л., Харнетт В. и Харнет М. М. Передача сигналов IL-33 / ST2 и перекрестные помехи с FcεRI и TLR4 нацелены на продукт паразитического червя, ES-62. Sci.Отчет 8 , 4497 (2018).
объявления PubMed PubMed Central Статья CAS Google ученый
- 35.
Al-Riyami, L. et al. . Разработка противовоспалительных препаратов от паразитических червей: синтетический низкомолекулярный аналог продукта ES-62 Acanthocheilonema viteae предотвращает развитие коллаген-индуцированного артрита. J. Med. Chem. 56 , 9982–10002 (2013).
CAS PubMed PubMed Central Статья Google ученый
- 36.
Берри, К. А. и Мерфи, Р. С. Анализ аминофосфолипидов клеточных мембран как производных, меченных изотопами. J. Lipid Res. 46 , 1038–1046 (2005).
PubMed Статья CAS Google ученый
- 37.
Colombo, S. et al . Модуляция воспалительного ответа иммунных клеток периферической крови человека окисленными арахидоноиламинофосфолипидами. Arch. Biochem. Биофиз. 15 , 64–71 (2018).
Артикул CAS Google ученый
- 38.
Smith, T. K. et al. . Пути биосинтеза GPI паразитов и млекопитающих можно различить, используя синтетические аналоги субстрата. EMBO J. 16 , 6667–6675 (1997).
CAS PubMed PubMed Central Статья Google ученый
- 39.
Фергюсон, М.А. и др. . Молекулы гликозил-фосфатидилинозитола паразита и хозяина. Паразитология 108 , S45–54 (1994).
PubMed Статья Google ученый
- 40.
Naik, R. S., Krishnegowda, G., Ockenhouse, C. F. & Gowda, D. C. Естественно вызванные антитела к гликозилфосфатидилинозитам (GPI) Plasmodium falciparum требуют интактных структур GPI для связывания и направлены в первую очередь против консервативной части гликана. Заражение. Иммун. 74 , 1412–1415 (2006).
CAS PubMed PubMed Central Статья Google ученый
- 41.
Ferguson, M. A. Биосинтез гликозилфосфатидилинозитола утвержден как лекарственная мишень для лечения африканской сонной болезни. Proc. Natl Acad. Sci. США 97 , 10673–10675 (2000).
объявления CAS PubMed Статья Google ученый
- 42.
Киношита Т. и Иноуэ Н. Рассечение и изменение пути биосинтеза гликозилфосфатидилинозитол-якоря. Curr. Opin. Chem. Биол. 4 , 632–638 (2000).
CAS PubMed Статья Google ученый
- 43.
de Macedo, C. S., Shams-Eldin, H., Smith, T. K., Schwarz, R. T. & Azzouz, N. Ингибиторы биосинтеза гликозил-фосфатидилинозитового якоря. Biochimie 85 , 465–472 (2003).
PubMed Статья CAS Google ученый
- 44.
Quittnat, F. et al . О биогенезе липидных тел у древних эукариот: синтез триацилглицеринов ферментом, родственным DGAT1 Toxoplasma. Mol. Biochem. Паразитол. 138 , 107–122 (2004).
CAS PubMed Статья Google ученый
- 45.
Bisanz, C. и др. . Метаболизм ацил-липидов Toxoplasma gondii: синтез de novo из жирных кислот, генерируемых апикопластом, по сравнению с очисткой предшественников клеток-хозяев. Biochem. J. 394 , 197–205 (2006).
CAS PubMed PubMed Central Статья Google ученый
- 46.
Чжан К., Бангс, Дж. Д. и Беверли, С. М. Сфинголипиды у паразитических простейших. Adv. Exp. Med. Биол. 688 , 238–248 (2010).
CAS PubMed PubMed Central Статья Google ученый
- 47.
Номура, К. Х. и др. . Церамид глюкозилтрансфераза нематоды Caenorhabditis elegans участвует в образовании ооцитов и в раннем делении эмбриональных клеток. Гликобиология 21 , 834–848 (2011).
CAS PubMed Статья Google ученый
- 48.
Sonda, S., Stefanic, S. & Hehl, A. B. Ингибитор сфинголипидов вызывает остановку цитокинеза и блокирует дифференцировку стадий у Giardia lamblia. Антимикробный. Агенты Chemother. 52 , 563–569 (2008).
CAS PubMed Статья Google ученый
- 49.
van der Kleij, D. et al. . Новый липидный диалог между хозяином и паразитом. Шистосомный лизофосфатидилсерин активирует толл-подобный рецептор 2 и влияет на поляризацию иммунной системы. J. Biol. Chem. 277 , 48122–48129 (2002).
PubMed Статья Google ученый
- 50.
Баумрукер Т., Биллих А. и Бринкманн В. FTY720, иммуномодулирующий миметик сфинголипидов: перевод нового механизма в клиническую пользу при рассеянном склерозе. Эксперт. Opin. Расследование. Наркотики 16 , 283–289 (2007).
CAS PubMed Статья Google ученый
- 51.
Барретт-Би К. и Райдер Н. Биохимические аспекты ингибирования биосинтеза эргостерола. J Sutcliffe и N.H. Georgopapadakou 410–436 (1992).
- 52.
Урбина Дж. А. и др. . Мевинолин (ловастатин) усиливает антипролиферативные эффекты кетоконазола и тербинафина против трипаносомы (Schizotrypanum) cruzi: in vitro и in vivo исследования. Антимикробный. Агенты Chemother. 37 , 580–591 (1993).
CAS PubMed PubMed Central Статья Google ученый
- 53.
Мондал, М., Кунду, Дж. К. и Мисра, К. К. Различия в поглощении липидов и жирных кислот среди нематод и паразитов-цестод и их хозяев. домашняя птица: взаимодействие хозяин – паразит. 40 , 1494–1518 (2016).
Google ученый
- 54.
Гарофало А. и др. .Семейство белков FAR нематод. J. Biol. Chem. 278 , 8065–8074 (2003).
CAS PubMed Статья Google ученый
- 55.
Macieira, S., Zhang, J., Velarde, M., Buckel, W. & Messerschmidt, A. Кристаллическая структура 4-гидроксибутират-КоА-трансферазы из Clostridium aminobutyricum. Biol. Chem. 390 , 1251–1263 (2009).
CAS PubMed Статья Google ученый
- 56.
Ларри, Р. С. и Яновей, Дж. Основы паразитологии (7-е изд.). McGraw-Hill 405–407 (2005).
- 57.
Суреш, К. Г. и др. . Кристаллическая структура ацилазы пенициллина V обнаруживает новые члены семейства Ntn-гидролаз. Nat. Struct. Мол. Биол. 6 , 414–416 (1999).
CAS Статья Google ученый
- 58.
Берридж М. Дж., Липп П. и Бутман М. Д. Универсальность и универсальность передачи сигналов кальция. Nat. Rev. Mol. Cell Biol. 1 , 11–21 (2000).
CAS PubMed Статья Google ученый
- 59.
Ghannoum, M. A. Внеклеточные фосфолипазы как универсальный фактор вирулентности патогенных грибов. Nihon Ishinkin Gakkai Zasshi 39 , 55–59 (1998).
CAS PubMed Статья Google ученый
- 60.
Hänel, H., Кирш, Р., Шмидтс, Х. Л. и Коттманн, Х. Новые систематически активные антимикотики из категории бета-блокаторов. Микозы 38 , 251–264 (1995).
PubMed Статья Google ученый
- 61.
Ху, Ф. и др. . Молекулярная характеристика новой секреторной фосфолипазы A Clonorchis sinensis (2) и исследование ее потенциального вклада в фиброз печени. Mol. Biochem.Паразитол. 167 , 127–134 (2009).
CAS PubMed Статья Google ученый
- 62.
Singh, P. et al. . Роль пататин-подобной фосфолипазы в гаметогенезе Plasmodium falciparum и передаче малярии. Proc. Natl Acad. Sci. США 116 , 17498–17508 (2019).
CAS PubMed Статья Google ученый
- 63.
Фернандес, А.С.С. и др. . Эндоцитоз и экзоцитоз у Leishmania amazonensis модулируются броменоловым лактоном. Микробиол фронтальных клеточных инфекций . 10–39 (2020).
- 64.
Burda, P.C. et al. . Фосфолипаза плазмодия участвует в разрушении мембраны паразитофорной вакуоли на стадии печени. PLoS Pathog . 11 (2015)
- 65.
Kong, A. M. et al. . Клонирование и характеристика инозитол-полифосфат-5-фосфатазы массой 72 кДа, локализованной в сети Гольджи. J. Biol. Chem. 275 , 24052–24064 (2000).
CAS PubMed Статья Google ученый
- 66.
Блай, Э. Г. и Дайер, У. Дж. Быстрый метод экстракции и очистки общих липидов. банка. J. Biochem. Physiol. 37 , 911–917 (1959).
CAS PubMed Статья Google ученый
- 67.
Tipthara, P. и др. . C2., Бем Б.



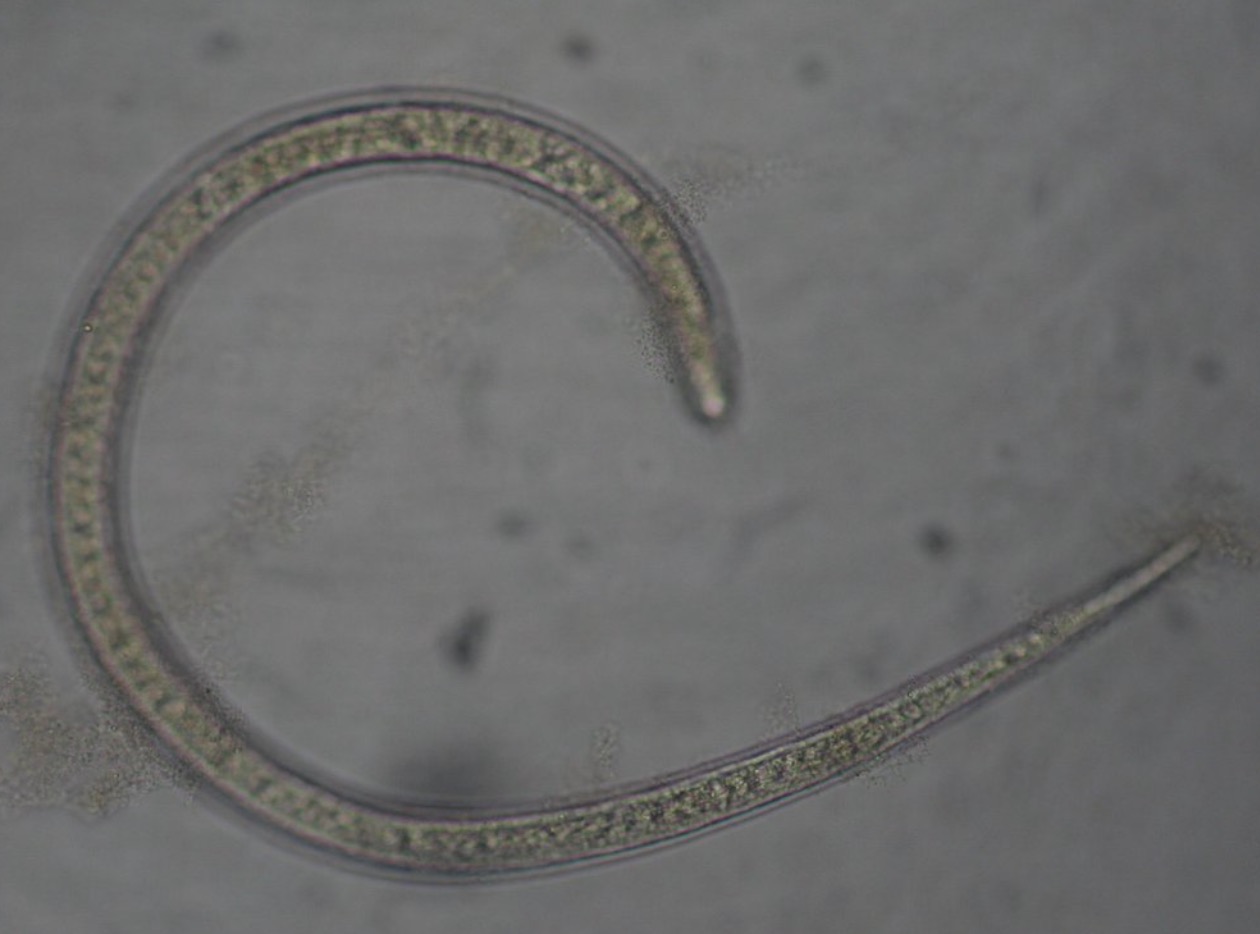
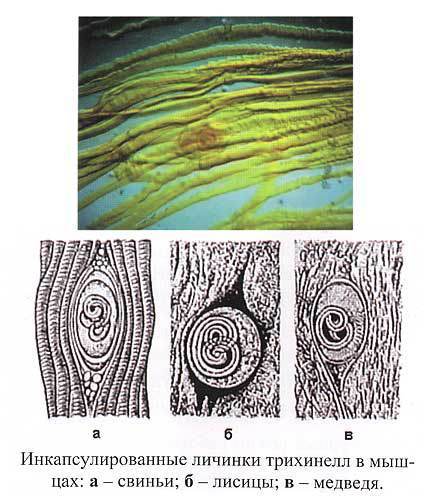
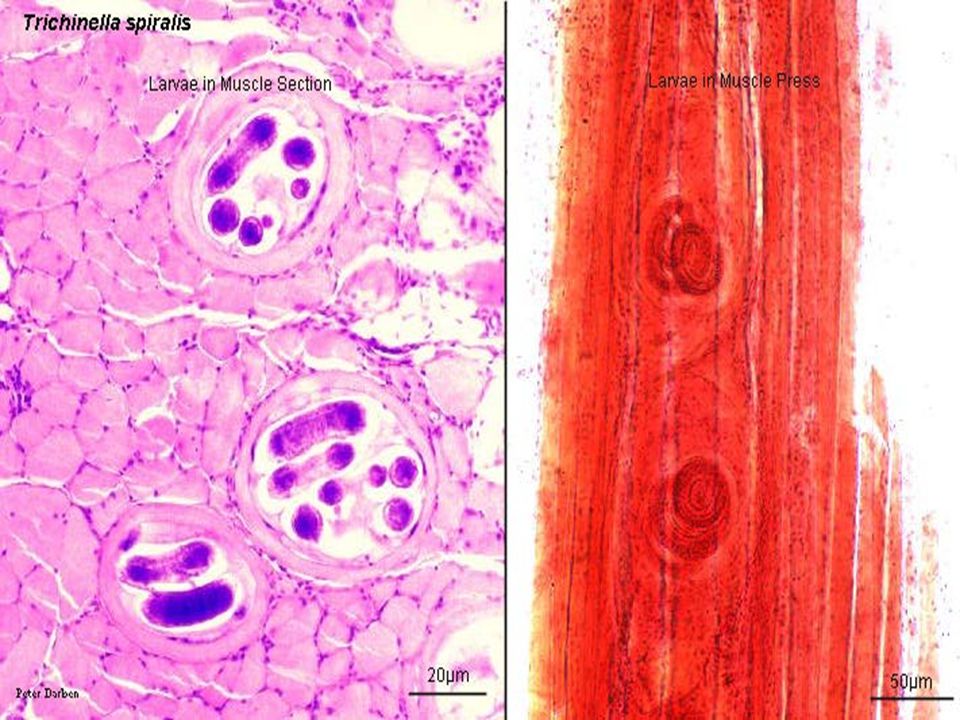 Исследование направлено на обнаружение личинок трихинелл.
Исследование направлено на обнаружение личинок трихинелл.
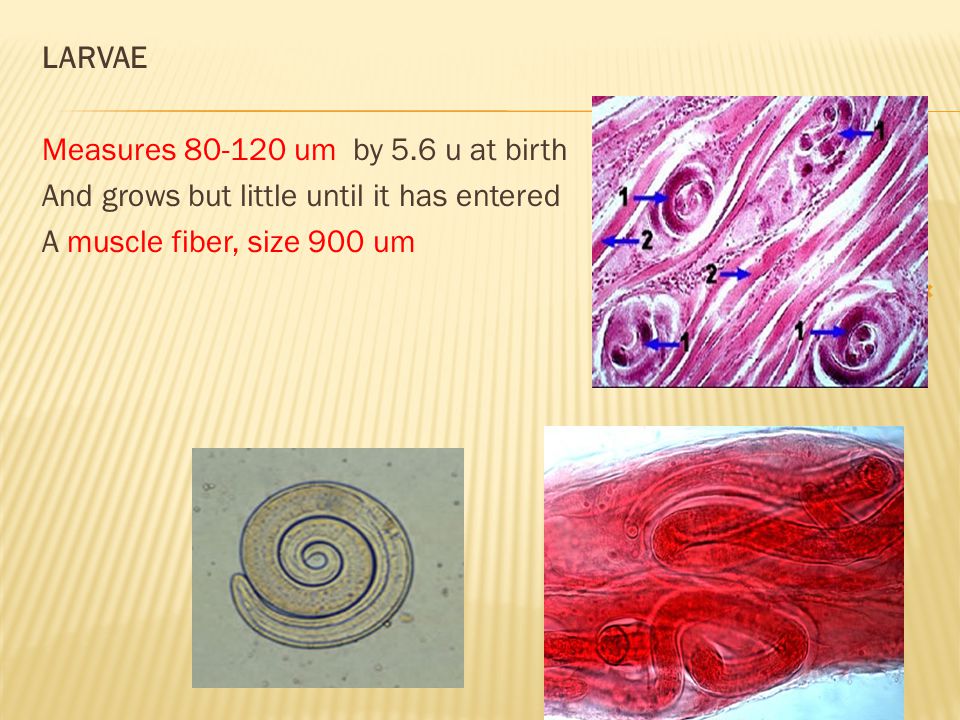

 Медсестры должны информировать пациентов о рисках передачи инфекции при употреблении недоваренного или сырого мяса. Фармацевты, медсестры и клиницисты должны знать о потенциальных побочных эффектах противоглистных препаратов, используемых при лечении трихинеллеза, и должны объяснять пациентам связанные с ними побочные эффекты.Когда пациенту ставится диагноз трихинелла, команда должна общаться, чтобы обеспечить стандарт лечения.
Медсестры должны информировать пациентов о рисках передачи инфекции при употреблении недоваренного или сырого мяса. Фармацевты, медсестры и клиницисты должны знать о потенциальных побочных эффектах противоглистных препаратов, используемых при лечении трихинеллеза, и должны объяснять пациентам связанные с ними побочные эффекты.Когда пациенту ставится диагноз трихинелла, команда должна общаться, чтобы обеспечить стандарт лечения. Природа. 1998 5 марта; 392 (6671): 71-5. [PubMed: 9510248]
Природа. 1998 5 марта; 392 (6671): 71-5. [PubMed: 9510248]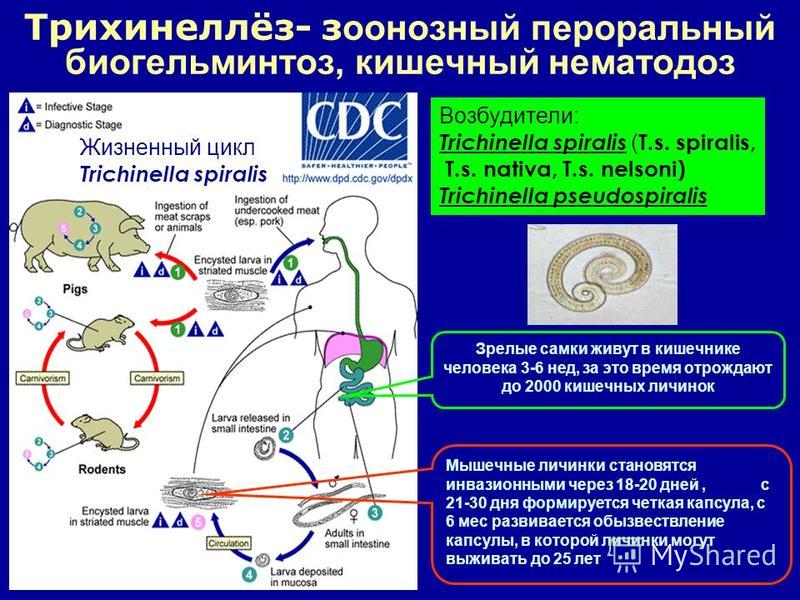 , Епес-Мулиа Л. Эпидемиология трихинеллеза в Мексике, Центральной и Южной Америке. Vet Parasitol. 2000 декабрь 01; 93 (3-4): 201-25. [PubMed: 11099838]
, Епес-Мулиа Л. Эпидемиология трихинеллеза в Мексике, Центральной и Южной Америке. Vet Parasitol. 2000 декабрь 01; 93 (3-4): 201-25. [PubMed: 11099838]