Мэллори вейса синдром причины: 404 Cтраница не найдена
Синдром Мэллори-Вэйса
Дата публикации: .
Хирургическое отделение №2
(городской центр гастродуоденальных
кровотечений язвенной этиологии)
врач-хирург Палеев C. А.
Синдром Мэллори-Вэйса («банкетный пищевод») представляет собой острое хирургическое заболевание, проявляющееся надрывом стенки желудка или пищевода.
ПРИЧИНЫ РАЗВИТИЯ СИНДРОМА МЭЛЛОРИ-ВЭЙСА
Основной причиной описываемой болезни считают сильную многократную рвоту при переполненном желудке. Создается избыточное давление, оказывающее действие на одну и ту же часть желудка и пищевода, вследствие чего стенка органа перерастягивается. Данное состояние при наличии располагающих условий может привести к частичному или полному ее разрыву.
Чаще всего при синдроме Мэллори-Вэйса наблюдается разрыв только слизистой – внутренней оболочки органа. Иногда может разрываться и средний – мышечный – слой, а в наиболее тяжелом случае наступает полный разрыв стенки органа с выходом его содержимого в брюшную полость либо (редко) в средостение, с развитием перитонита или медиастенита.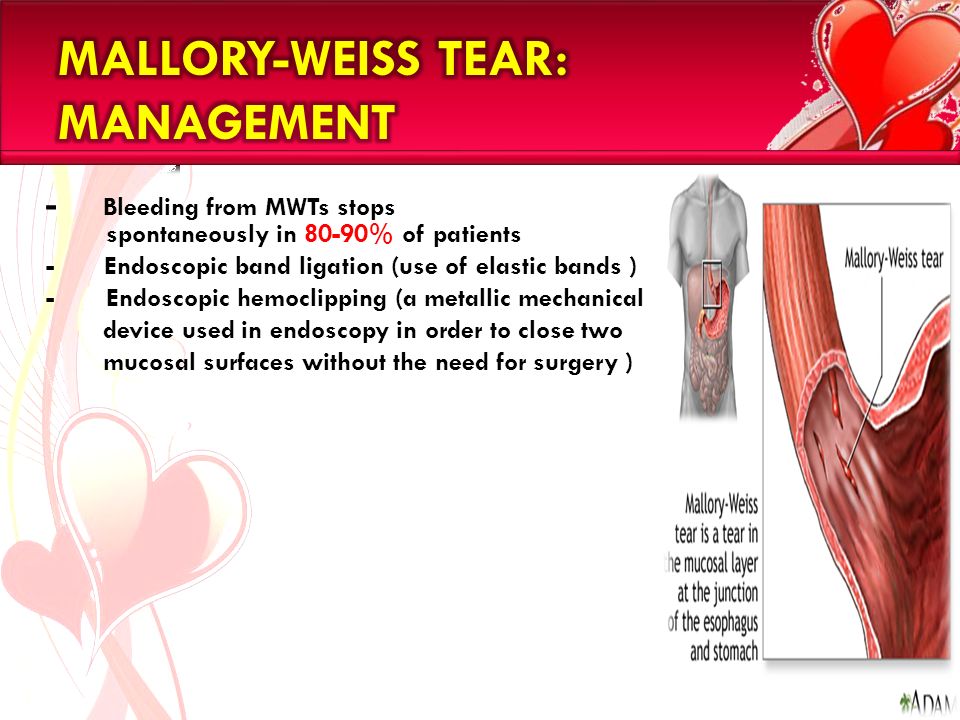
Иногда непосредственной причиной появления описываемого синдрома может стать кашель или подъем тяжести.
Очень часто (у 80% больных) предрасполагающим фактором развития данной болезни становится регулярное употребление спиртных напитков. Это связано с тем, алкоголь провоцирует развитие гастрита, что приводит к истончению слизистой. Это означат, что слизистая становится менее устойчивой к разрыву.
ПРИЗНАКИ СИНДРОМА МЭЛЛОРИ-ВЭЙСА
Клиническая картина данного синдрома зависит от количества и глубины разрывов стенки желудка и/или пищевода, интенсивности и длительности сопутствующего кровотечения и некоторых других факторов.
В наиболее типичном случае на фоне многократной рвоты (наступившей после переедания и/или употребления алкоголя) на пике очередного рвотного позыва возникает резкая боль в области желудка. При полном разрыве стенки органа боль достаточно интенсивная и постепенно распространяется по всему животу. Последующая рвота происходит с выделением того или иного количества крови (как правило, свежей, несвернувшейся) вместе с рвотными массами.
При поверхностных разрывах, которые сопровождаются незначительным кровотечением, примесь крови может быть не видна.
Если рвотные массы по цвету напоминают кофейную гущу, это может быть признаком старого кровотечения.
ДИАГНОСТИРОВАНИЕ СИНДРОМА МЭЛЛОРИ-ВЭЙСА
Для диагностики описываемого синдрома в первую очередь применяют эндоскопическое исследование (эзофагогастроскопию). Данное обследование дает возможность четко увидеть локализацию и глубину дефекта стенки органа.
Для оценки величины кровопотери при синдроме Мэллори-Вэйса проводят лабораторное исследование крови.
При подозрении на полный разрыв стенки делается обзорная рентгенография органов брюшной полости.
МЕТОДЫ ЛЕЧЕНИЯ СИНДРОМА МЭЛЛОРИ-ВЭЙСА
В подавляющем большинстве случаев данный синдром лечится консервативно.
Кровотечение останавливают эндоскопическим методом, а при значительной кровопотере проводят медикаментозное лечение для поддержания деятельности сердечно-сосудистой системы.
Важный элемент лечения синдрома – угнетение желудочной секреции для скорейшего заживления образовавшегося дефекта.
При неэффективности консервативного лечения, глубоких дефектах или полном разрыве стенки проводится хирургическое лечение описываемого синдрома.
ПРОФИЛАКТИКА СИНДРОМА МЭЛЛОРИ-ВЭЙСА
Мерами профилактики развития синдрома считается отказ от злоупотребления спиртными напитками, недопущение переедания, а также своевременное выявление и лечение заболеваний пищеварительного тракта.
Лечение синдрома меллори-вейса. Список клиник, рейтинг, отзывы, цены
О заболевании
При синдроме Мэллори-Вэйсса происходит разрыв слизистой оболочки в месте соединения желудка и пищевода. Пищевод несет ответственность за транспортировку пищи и жидкости с ротовой полости в желудок. Практически это трубка. Чаще всего разрыв пищевода возникает в результате продолжительной и хронической рвоты. Такая рвота может появляться после длительной болезни, булимии и чрезмерного употребления алкоголя. Синдром Мэллори-Вэйса также может возникать в результате травмы желудка или операции на желудке, грыжи пищеводного отверстия диафрагмы, а также острого гастрита. Постоянное деформирование желудка также может вызвать синдром Мэллори-Вейсса в долгосрочной перспективе. По данным Национальной организации редких заболеваний это условие чаще встречается у людей в возрасте от 40 – 60 лет. Мужчины более склонны к этой болезни..
Синдром Мэллори-Вэйса также может возникать в результате травмы желудка или операции на желудке, грыжи пищеводного отверстия диафрагмы, а также острого гастрита. Постоянное деформирование желудка также может вызвать синдром Мэллори-Вейсса в долгосрочной перспективе. По данным Национальной организации редких заболеваний это условие чаще встречается у людей в возрасте от 40 – 60 лет. Мужчины более склонны к этой болезни..
Симптомы
- Продолжительная сильная рвота
- Боли в желудке и верхней части живота
- Кровь рвотных массах
- Черный стул
- Усталость
- Головокружение
- Уменьшение аппетита
- Потеря веса
Кровь в рвотных массах может быть темно-красного или почти черного цвета. Это показатель, который требует немедленной неотложной помощи. Синдром Мэллори-Вэйсса имеет схожие симптомы с язвой, но эти два заболевания должны быть дифференцированы, поскольку они требуют различных методов лечения.
Диагностика
- ЭГДС (эзофагогастродуоденоскопия) – это процедура, которая позволяет доктору осмотреть пищевод и определить, была ли его слизистая разорвана или изношена.
 Для осмотра, тонкая трубка, оборудована эндоскопом, осторожно проталкивается в пищевод. Врач будет иметь возможность видеть все части пищевода с помощью камеры, подключенной к эндоскопу.
Для осмотра, тонкая трубка, оборудована эндоскопом, осторожно проталкивается в пищевод. Врач будет иметь возможность видеть все части пищевода с помощью камеры, подключенной к эндоскопу. - Анализ крови проводится, чтобы определить количество красных кровяных телец в крови, так как оно отличается у больных с синдромом Мэллори-Вэйсса.
- Ультразвук желудка выполняется, чтобы определить, был ли вызван синдром Мэллори-Вэйсса смещением стенок желудка.
Виды лечения
- Склеротерапия – это инъекционная терапия, когда некоторые лекарственные препараты вводятся, чтобы остановить кровотечение из разрывов слизистой и остановить кровотечение кровеносных сосудов.
- Коагуляция – это еще один вид терапии для разорванного кровеносного сосуда, во время которой тепло направлено на остановку кровотечения и блокирования сосуда.
- Пластическая хирургия нижнего пищеводного сфинктера – это удаление поврежденной ткани и имплантация пластикового, чтобы восстановить пищеварительную функцию и остановить рвоту.

В 80-90% лечение приносит хорошие результаты и Вы сможете вылечить синдром Мэллори-Вэйсса в течение нескольких недель. Необходимо будет придерживаться определенных ограничений в еде после операции в целях предупреждения осложнений таких, как язва или гастрит.
Автор: Доктор Надежда Иванисова
Эффективность применения эндоскопических технологий при синдроме Маллори-Вейсса
Синдром Маллори—Вейсса (СМВ) — состояние, при котором возникает развитие острых различной степени выраженности продольных разрывов слизистой оболочки абдоминального отдела пищевода или кардии желудка, проявляющееся выраженным пищеводно-желудочным кровотечением. Данная нозология занимает 3—4-е место среди причин кровотечения из верхних отделов желудочно-кишечного тракта [1] и характеризуется высоким риском развития рецидива, наблюдающимся, по данным различных авторов, в 20—35% случаев; общая летальность при этом составляет 5—10% [1, 2]. Эти данные отражают нерешенную проблему лечения больных с данной патологией, актуальность которой остается значимой наряду с другими причинами кровотечений из верхних отделов желудочно-кишечного тракта, такими как гастродуоденальные язвы и синдром портальной гипертензии.
Основной причиной, предрасполагающей к возникновению разрывов пищеводно-желудочного перехода, является злоупотребление алкоголем с последующей рвотой [3]. Тяжесть кровотечения зависит от глубины разрывов стенки этих органов, когда могут быть повреждены различные по диаметру сосуды подслизистого сплетения, а также сосуды мышечного и субсерозного слоев пищевода и желудка [4].
Хирургическое лечение больных с СМВ включает остановку кровотечения путем применения широкой лапаротомии, гастротомии и ушивания разрывов. В наши дни благодаря широкому внедрению малоинвазивных технологий и применению эндоскопического оборудования открылись новые возможности лечения таких больных путем комбинированного воздействия на очаг кровотечения различных способов эндоскопического гемостаза с одновременным применением общих мероприятий, направленных на остановку кровотечения, подавление секреции желудочного сока и кровезамещение [5, 6]. Успешность применения эндоскопических методов во многом зависит от применения грамотного и обоснованного алгоритма действий с использованием критериев оценки возможностей эндоскопического гемостаза, учета прогноза возможного рецидива, сопутствующей патологии и динамического состояния у каждого пациента.
Целью исследования явилась оценка эффективности лечения СМВ в условиях стационара неотложной помощи при преимущественном использовании эндоскопических способов гемостаза.
Материал и методы
Для решения поставленных задач был проведен анализ лечения 549 пациентов с кровотечением из зоны разрыва пищеводно-желудочного перехода, поступивших в хирургическую клинику в экстренном порядке в период с 2000 по 2011 г.
Нами ретроспективно были проанализированы истории болезней 207 пациентов с СМВ, пролеченных до широкого применения эндоскопии, с 2000 по 2004 г. При этом 156 пациентов с клинической картиной кровотечения легкой и средней степени кровопотери лечили консервативно. В экстренном порядке на фоне неэффективности консервативных методик, с признаками нестабильной гемодинамики и с тяжелой кровопотерей традиционно прооперирован 51 пациент.
С 2005 по 2011 г. одновременно с внедрением лечебной эндоскопической практики мы изучили 342 случая СМВ. Все эндоскопические исследования выполнены в пределах 3 ч после поступления больных в стационар. Всех их помещали в блок критических состояний, размещенный на уровне приемного отделения, с целью подготовки верхних отделов пищеварительного тракта к эндоскопическим манипуляциям (промывание желудка и пищевода холодным изотоническим раствором натрия хлорида до светлых вод, введение прокинетиков для быстрого опорожнения желудка), введения седативных средств неспокойным пациентам, восполнения объема циркулирующей крови и одновременного дополнительного обследования с осмотром необходимых специалистов, нивелирования последствий алкогольного опьянения. Все исследования проводили под адекватным обезболиванием в условиях палаты интенсивной терапии под наблюдением реанимационной бригады.
Все эндоскопические исследования выполнены в пределах 3 ч после поступления больных в стационар. Всех их помещали в блок критических состояний, размещенный на уровне приемного отделения, с целью подготовки верхних отделов пищеварительного тракта к эндоскопическим манипуляциям (промывание желудка и пищевода холодным изотоническим раствором натрия хлорида до светлых вод, введение прокинетиков для быстрого опорожнения желудка), введения седативных средств неспокойным пациентам, восполнения объема циркулирующей крови и одновременного дополнительного обследования с осмотром необходимых специалистов, нивелирования последствий алкогольного опьянения. Все исследования проводили под адекватным обезболиванием в условиях палаты интенсивной терапии под наблюдением реанимационной бригады.
При первичной эндоскопии выявить источник кровотечения удалось в 73,4%. Эндоскопические вмешательства продолжались от 10 до 40 мин в зависимости от перечисленных выше факторов. Продолжающееся кровотечение было выявлено у 177 (51,8%) больных, при этом струйное — у 84 (24,6%) и диффузное — у 93 (27,2%). Продолжающееся кровотечение отсутствовало у 165 (48,2%) больных.
Продолжающееся кровотечение отсутствовало у 165 (48,2%) больных.
Эндоскопический гемостаз посредством инъекционного метода (0,005% раствор адреналина, изотонический раствор натрия хлорида) осуществлен у 171 пациента, у 83 — термические (диатермокоагуляция и аргоноплазменная коагуляция) и у 26 — механические методы (эндоскопическое клипирование кровоточащего сосуда и эндоскопическое лигирование зоны разрыва латексными кольцами). Комбинированные методы эндоскопического гемостаза применили у 62 больных (инъекционный метод и механический, инъекционный и термический).
В случае отсутствия продолжающегося кровотечения (165 больных) при эндоскопии выполняли профилактические аппликации в виде инъекционного метода либо диатермокоагуляции.
Эффективность того или иного способа эндоскопического гемостаза оценивали по таким показателям, как устойчивость гемостаза и отсутствие рецидивов в раннем периоде (рис. 1).Рисунок 1. Частота возникновения рецидивов синдрома Маллори—Вейсса после применения эндоскопических методов лечения (%).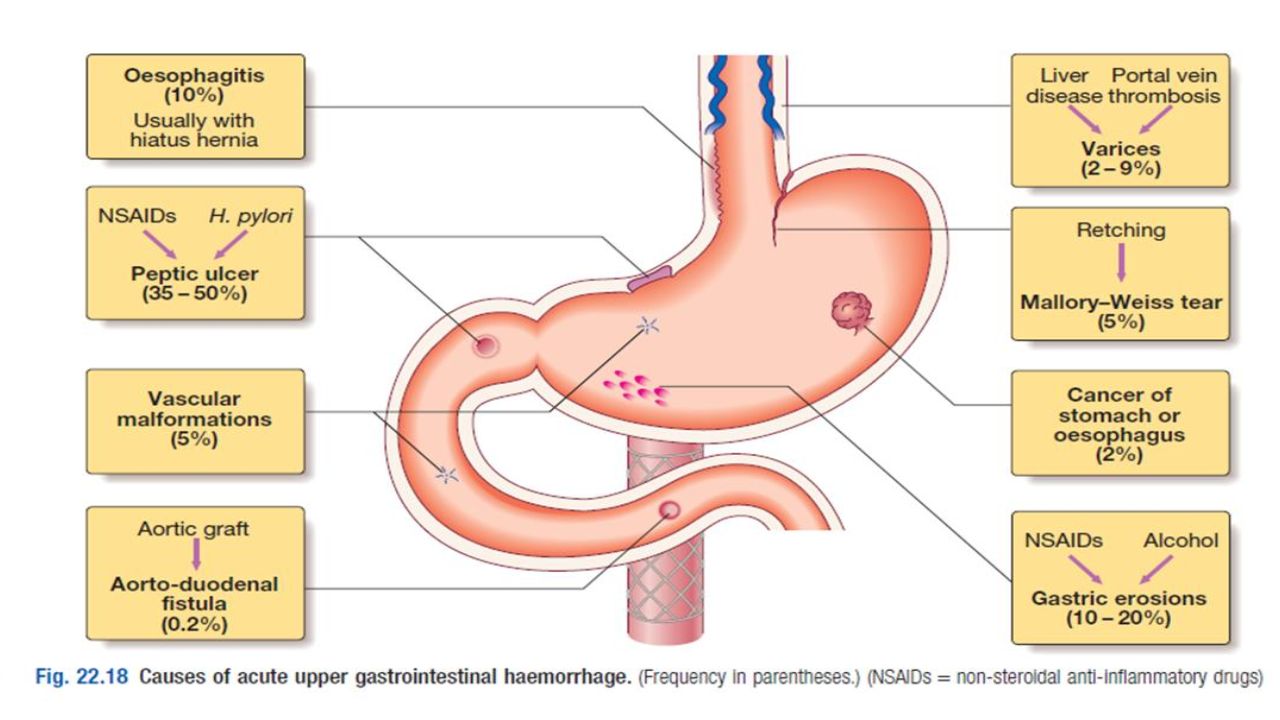
Как показал наш опыт, наиболее эффективными и дающими мало рецидивов методами эндоскопического гемостаза при СМВ оказались механические и комбинированные виды аппликаций. Менее эффективными были моновариантные методы эндоскопического гемостаза, инъекционный и термический, при которых рецидивы кровотечения возникали чаще.
Размеры выявленных повреждений варьировали от 5 до 50 мм, ширина от 2 до 10 мм, глубина разрывов от 2 до 7 мм. Для оценки степени глубины разрывов использовали классификацию H. Bellmann, основанную на оценке глубины разрывов: I степень выявлена у 211 (61,7%) больных, II степень — у 129 (37,7%), III степень — у 4 (1,2%).
Статистический анализ полученных результатов проведен методом вариационной статистики. Достоверность различий оценивали при помощи параметрических и непараметрических критериев. Различия считали достоверными при значении р≤0,05.
Результаты и обсуждение
У больных 1-й группы, пролеченных за 2000—2004 гг.
С 2005 г. лечебную эндоскопию выполняли всем больным, даже в отсутствие признаков продолжающегося кровотечения. У 39 (11,4%) больных выявлен рецидив кровотечения, в связи с чем выполняли повторный эндоскопический гемостаз, при этом, как правило, использовали комбинированные способы гемостаза. Традиционным способом прооперированы 5 больных. Умерли 2 больных с алкогольным циррозом печени и печеночной недостаточностью. Общая летальность составила 0,58% (рис. 2).Рисунок 2. Летальность в сравниваемых группах больных.
Оперативная активность в 1-й группе составила 24,6%, во 2-й — 1,5%. Стоит отметить, что во 2-й группе больных практически во всех случаях удавалось добиться гемостаза при помощи эндоскопических методик, и хирургические вмешательства выполняли при выявлении глубоких разрывов III степени в связи с опасностью перфорации желудка, а также при развитии рецидивов кровотечения, не подвергшемуся остановке повторным применением эндоскопического метода.
Эндоскопические методы позволяют добиться устойчивого гемостаза при СМВ, а в случае развития рецидивов хорошие результаты дает применение комбинированных эндоскопических методик.
Внедрение эндоскопических технологий способствует снижению оперативной активности и общей летальности при СМВ.
Эндоскопические методы помогают произвести оценку степени разрыва СМВ и темпа кровотечения и, в случае глубоких разрывов, помогают добиться временного контролируемого гемостаза с целью адекватного проведения предоперационной подготовки. 2009
2009
© Ш.В.Тимербулатов, В.М.Тимербулатов, 2009 УДК 616.33-005.1-02-039.42
Ш.В.Тимербулатов, В.М.Тимербулатов
РЕДКИЕ ПРИЧИНЫ СИНДРОМА МАЛЛОРИ-ВЕЙССА
Кафедра хирургии с курсом эндоскопии ИПО (зав. — чл.-кор. РАМН проф. В.М.Тимербулатов) Башкирского государственного медицинского университета, г. Уфа
Ключевые слова: синдром Маллори-Вейсса, редкие причины.
Синдром гастроэзофагеального разрыва, синдром гас-троэзофагеального разрыва с кровотечением, рвотный синдром с эрозией впервые описан H.Quincke в 1879 г. [46]. G.K.Mallory, S.Weiss в 1929 г. описали 15 случаев синдрома, показав различие между разрывами и эрозией [36]. Для выяснения причины перфорации пищевода авторы закупоривали привратник и пищевод, под давлением наполняли частично раздутый желудок у трупов. Перед разрывом пищевода обнаруживались вертикальные длинные трещины. В литературу данное заболевание как синдром Маллори-Вейсса (СМВ) ввели J.P.Decker и соавт. в 1953 г. [21]. Первое успешное хирургическое лечение СМВ было выполнено в 1955 г. Whiting [14].
Перед разрывом пищевода обнаруживались вертикальные длинные трещины. В литературу данное заболевание как синдром Маллори-Вейсса (СМВ) ввели J.P.Decker и соавт. в 1953 г. [21]. Первое успешное хирургическое лечение СМВ было выполнено в 1955 г. Whiting [14].
На 11 000 патологоанатомических вскрытий в 1% случаев причиной смерти были кровотечения в результате СМВ [3]. На 5160 секционных исследований, произведенных у умерших детей, в 12% случаев установлена спонтанная перфорация желудка [McCormick W.F., 1959]. Частота СМВ на материале 13 531 секционного исследования составила 2,96% [9].
СМВ составляет 4-15% среди причин желудочно-кишечных кровотечений верхних отделов пищеварительного тракта [4, 11, 47, 49, 50].
Широкое применение эндоскопии привело к увеличению выявляемости СМВ [8]. Чаще СМВ выявляется у людей 30-50 лет, хотя описаны случаи у детей 3-недельного возраста [13, 24, 42]. В литературе сообщения о СМВ у детей единичны [44, 48, 52]. L.Bak-Romaniszyn и соавт. [8] обследовали 2720 детей от 5 мес до 18 лет (гастроинтестинальная эндоскопия), и СМВ обнаружили у 8 (0,3%), в основном с локализацией разрывов слизистой оболочки выше гастроэзо-фагеального соединения. Признаков кровотечения в момент осмотра не было ни в одном случае.
В литературе сообщения о СМВ у детей единичны [44, 48, 52]. L.Bak-Romaniszyn и соавт. [8] обследовали 2720 детей от 5 мес до 18 лет (гастроинтестинальная эндоскопия), и СМВ обнаружили у 8 (0,3%), в основном с локализацией разрывов слизистой оболочки выше гастроэзо-фагеального соединения. Признаков кровотечения в момент осмотра не было ни в одном случае.
Число рецидивов при СМВ достигает 20-30%, послеоперационная летальность — 10-15% [1, 5], а общая летальность — 1,8% [2]. Послеоперационная летальность составила 17%, а при сочетании хирургического лечения с диотермокоагуляцией — 4,5% [3]. После оперативного лечения — лапаротомии с прошиванием кровоточащих сосудов, летальность составила 8% [6]. Послеоперационная летальность после гастротомии с прошиванием разрывов и сосудов составила 13%, после консервативной терапии — 3% [23].
Клинической причиной пролонгированной рвоты является алкоголизм.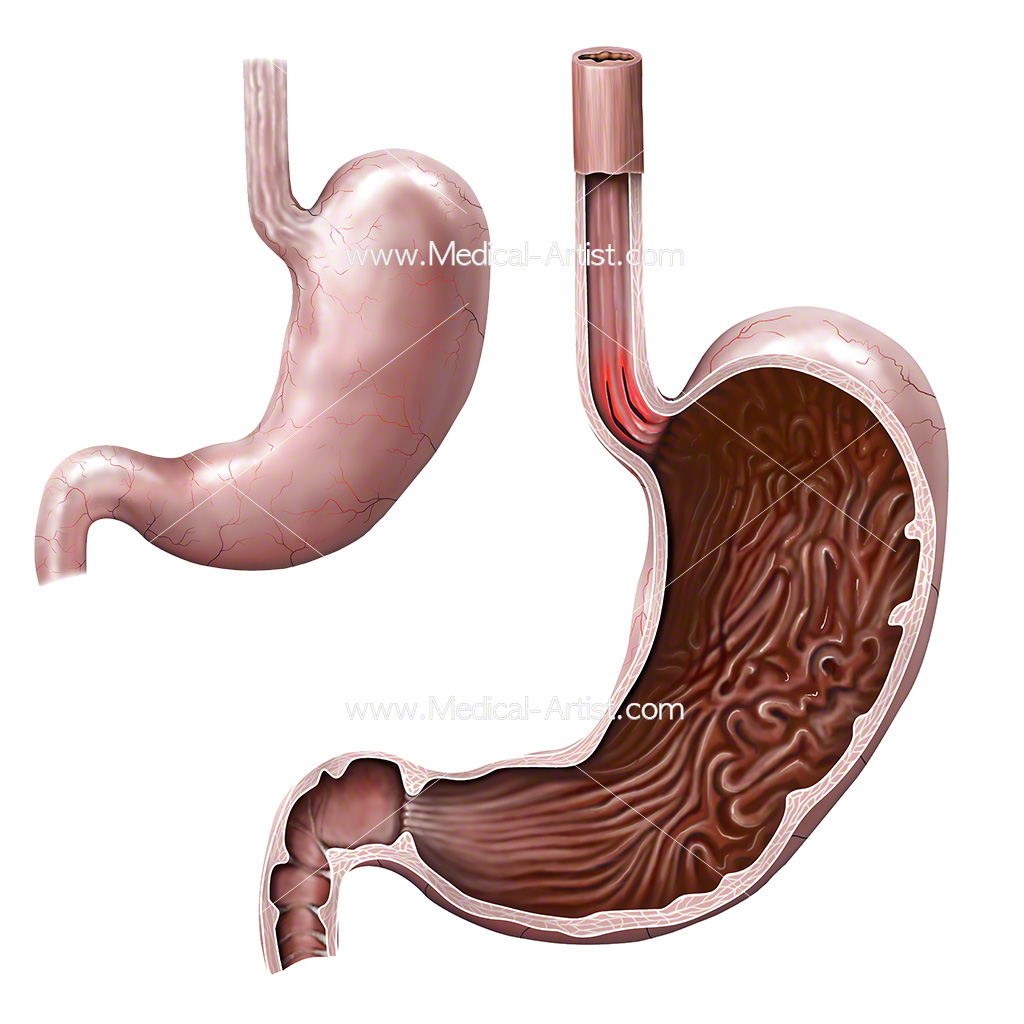 Также описаны другие причины СМВ: мигрень, беременность, грыжа пищеводного отверстия диафрагмы, язва желудка, заболевания печени и желчных путей,
Также описаны другие причины СМВ: мигрень, беременность, грыжа пищеводного отверстия диафрагмы, язва желудка, заболевания печени и желчных путей,
прием лекарств (полиэтиленгликоль для подготовки кишечника к исследованию) [26, 43].
Наиболее часто сообщаемая причина СМВ — сильная рвота от передозировки алкоголя с типичным разрывом (разрывами) гастроэзофагеального соединения, но причиной может быть рвота, например при химиотерапии [25]. У 4 из 8 наблюдаемых детей СМВ сопровождается гастритом и дуоденитом, были выявлены по одному случаю язвы двенадцатиперстной кишки, ассоциированной с Helicobacter pylori, бронхиальной астмы, гастроэзофагеального рефлюк-са, отравления carbon monoxide [8].
Описан случай СМВ при герпетическом эзофагите [31]. При эндоскопическом исследовании в средней и нижней трети пищевода выявлены множественные эрозии слизистой оболочки, разрывы в пищеводно-желудочном переходе с кровотечением. В последующем при гистологическом, имму-ногистохимическом и серологическом исследованиях диагноз был уточнён — обнаружен герпетический вирус (HSV-1) в ядрах эпителиальных клеток пищевода. Авторы считают, что причиной СМВ у данного больного были плохо поддающиеся терапии дисфагия и упорная рвота. Герпетический эзофагит впервые описан в 1940 г. H.N.Johnson [30]. Обычно возникает у иммунодефицитных больных (AIDS) [51], при злокачественных новообразованиях [38], при проведении иммуносупрессивной терапии [41]. Герпетический эзофагит редко встречается при отсутствии нарушений иммунитета [29, 40]. Есть сообщения о перфорации пищевода при герпетическом эзофагите [19]. В литературе имеются два сообщения о желудочно-кишечном кровотечении при герпетическом эзофагите [7, 18].
В последующем при гистологическом, имму-ногистохимическом и серологическом исследованиях диагноз был уточнён — обнаружен герпетический вирус (HSV-1) в ядрах эпителиальных клеток пищевода. Авторы считают, что причиной СМВ у данного больного были плохо поддающиеся терапии дисфагия и упорная рвота. Герпетический эзофагит впервые описан в 1940 г. H.N.Johnson [30]. Обычно возникает у иммунодефицитных больных (AIDS) [51], при злокачественных новообразованиях [38], при проведении иммуносупрессивной терапии [41]. Герпетический эзофагит редко встречается при отсутствии нарушений иммунитета [29, 40]. Есть сообщения о перфорации пищевода при герпетическом эзофагите [19]. В литературе имеются два сообщения о желудочно-кишечном кровотечении при герпетическом эзофагите [7, 18].
Эзофагеальный интрамуральный псевдодивертикулёз (ЭИПД) — редкое заболевание, диагностируемое при рентгенографии пищевода. Так, в Японии с 1975 по 2002 г. описаны 36 наблюдений данного заболевания [28, 32, 53]. Авторы привели описание данного заболевания у больного 62 лет, осложнённого СМВ. Диагноз ЭИПД был установлен в последующем, после оперативного вмешательства при проведении бариевой эзофагографии. При поступлении у больного с явлениями массивного кровотечения при гастро-интестинальной эндоскопии выявлено два разрыва слизистой оболочки с распространением в мышечный слой. Проведены инъекции этанола, орошение спреем тромбина, ввиду безуспешности проведенных мероприятий решено было провести ушивание разрывов после лапаротомии. Авторы, как и другие специалисты, подтверждают редкость осложнения псевдоди-вертикулёза пищевода СМВ, типичным же осложнением являются стриктуры.
описаны 36 наблюдений данного заболевания [28, 32, 53]. Авторы привели описание данного заболевания у больного 62 лет, осложнённого СМВ. Диагноз ЭИПД был установлен в последующем, после оперативного вмешательства при проведении бариевой эзофагографии. При поступлении у больного с явлениями массивного кровотечения при гастро-интестинальной эндоскопии выявлено два разрыва слизистой оболочки с распространением в мышечный слой. Проведены инъекции этанола, орошение спреем тромбина, ввиду безуспешности проведенных мероприятий решено было провести ушивание разрывов после лапаротомии. Авторы, как и другие специалисты, подтверждают редкость осложнения псевдоди-вертикулёза пищевода СМВ, типичным же осложнением являются стриктуры.
ЭИПД впервые описан K.Mendi и соавт. в 1960 г. [39], а M.S.Levine и соавт. [35] выявили его у 21 (0,15%) из 14 350
Том 168 • № 2
Синдром Маллори-Вейсса
больных, прошедших рентгенологическое исследование пищевода. СМВ был описан, включая наблюдение [53], у 2 больных с ЭИПД. Авторы полагают, что причиной слабости подслизистого слоя пищевода является хроническое воспаление, а при соответствующих причинах возникают разрывы.
СМВ был описан, включая наблюдение [53], у 2 больных с ЭИПД. Авторы полагают, что причиной слабости подслизистого слоя пищевода является хроническое воспаление, а при соответствующих причинах возникают разрывы.
В литературе описан так называемый механический гастрит, как причина массивных кровотечений из верхних отделов желудочно-кишечного тракта. Считается, что кровотечения возникают из-за позывов на рвоту и рвоты у больных с грыжей пищеводного отверстия диафрагмы [17]. Клинические проявления механического гастрита и СМВ могут быть схожи. Автор считает, что во время рвоты или позывов на рвоту слизистая оболочка желудка продавливается через суженное кольцо диафрагмы в пищеводную грыжу, что вызывает механическую травму слизистой оболочки желудка, далее вызывая гастрит, эрозии, кровотечение.
АХР1кагеку и соавт. [45] описали случай СМВ у мужчины 32 лет после длительного периода плавания и последующего длительного перелета на самолете (13 ч). Причинами развития СМВ авторы считают централизацию гемодинамики при плавании и снижение давления (на 0,3 атм) при полете. Поэтому воздушные путешествия и атлетические нагрузки должны считаться потенциальными факторами в оценке вновь возникшего желудочно-кишечного кровотечения. Описанный больной ранее не болел, алкоголь не употреблял. Кровотечение появилось во время полета и уменьшилось после внутриартериального введения вазопрессина (через левую желудочную артерию после предварительной ангиографии).
Причинами развития СМВ авторы считают централизацию гемодинамики при плавании и снижение давления (на 0,3 атм) при полете. Поэтому воздушные путешествия и атлетические нагрузки должны считаться потенциальными факторами в оценке вновь возникшего желудочно-кишечного кровотечения. Описанный больной ранее не болел, алкоголь не употреблял. Кровотечение появилось во время полета и уменьшилось после внутриартериального введения вазопрессина (через левую желудочную артерию после предварительной ангиографии).
AJ.De Упе8 и соавт. [22] сообщили о фатальном гастро-интестинальном кровотечении от СМВ после чреспищеводной эхокардиографии (ЧПЭхоКГ) во время операции на сердце. После ЧПЭхоКГ больному установили назогастральный зонд, через который поступала яркая красная кровь, в конечном итоге общая кровопотеря составила 9 л крови. Авторами не была установлена точная причина развития СМВ — за счет эхопробы или введения назогастрального зонда.
Чреспищеводная эхокардиография все чаще применяется в кардиологии и кардиохирургии с довольно редкими осложнениями. В кардиологической практике ЧПЭхоКГ считается кратковременной полуинвазивной процедурой с риском осложнений 0,5-1% в больших сериях исследований [15, 20]. Хотя большинство осложнений транзиторные (аритмии, гипотензия, дисфагия, ларингоспазм), гастроин-тестинальные кровотечения потенциально опасны, особенно в условиях кардиохирургии с проведением антикоагулянтной терапии на фоне различных коагулопатий, связанными также с кардиопульмонарным шунтированием [22]. Продолжительный контакт пищевода с датчиком эхозонда у больного под наркозом во время операции и нахождения датчика в изогнутом состоянии для постоянного мониторинга функции левого желудочка может спровоцировать повреждение слизистой оболочки пищевода. В то же время случаи выраженного (явного) пищеводно-желудочного кровотечения вслед за ЧПЭхоКГ описаны редко [23, 33].
В кардиологической практике ЧПЭхоКГ считается кратковременной полуинвазивной процедурой с риском осложнений 0,5-1% в больших сериях исследований [15, 20]. Хотя большинство осложнений транзиторные (аритмии, гипотензия, дисфагия, ларингоспазм), гастроин-тестинальные кровотечения потенциально опасны, особенно в условиях кардиохирургии с проведением антикоагулянтной терапии на фоне различных коагулопатий, связанными также с кардиопульмонарным шунтированием [22]. Продолжительный контакт пищевода с датчиком эхозонда у больного под наркозом во время операции и нахождения датчика в изогнутом состоянии для постоянного мониторинга функции левого желудочка может спровоцировать повреждение слизистой оболочки пищевода. В то же время случаи выраженного (явного) пищеводно-желудочного кровотечения вслед за ЧПЭхоКГ описаны редко [23, 33].
В последнее время отмечается увеличение сообщений о ятрогенных повреждениях пищевода (перфорациях) при использовании инструментальных методов исследования [34, 37]. Хотя ЧПЭхоКГ считается безопасной процедурой [16, 20], она может представлять риск во время операции при проведении датчика больному в условиях наркоза. Исследование может длиться несколько часов, со сдавлением слизистой оболочки пищевода и термальными повреждениями, что увеличивает вероятность повреждения пищевода [27]. Следует
Хотя ЧПЭхоКГ считается безопасной процедурой [16, 20], она может представлять риск во время операции при проведении датчика больному в условиях наркоза. Исследование может длиться несколько часов, со сдавлением слизистой оболочки пищевода и термальными повреждениями, что увеличивает вероятность повреждения пищевода [27]. Следует
иметь в виду, что больные с сердечно-легочными заболеваниями часто принимают антикоагулянты.
S.R.Massey и соавт. [37] описали случай перфорации пищевода вслед за введением зонда-датчика для чреспищеводной эхокардиографии у больной с кардиомегалией. По мнению авторов, увеличенное сердце повышает риск перфорации пищевода ввиду деформации последнего.
При трудностях введения эходатчика-зонда и его удалении следует иметь в виду возможность повреждения пищевода, поскольку симптомы перфорации пищевода проявляются не сразу [8] или они не являются специфическими для данного осложнения [34]. Задержка в проведении дополнительных методов исследования, диагностике и особенно лечении увеличивают смертность и число дополнительных осложнений [8, 10, 12].
Задержка в проведении дополнительных методов исследования, диагностике и особенно лечении увеличивают смертность и число дополнительных осложнений [8, 10, 12].
У ребенка 4,5 лет после эфирно-кислородного наркоза через катетер Нелатона наступила перфорация желудка с образованием 4 продольных дефектов по малой кривизне желудка длиной от 1,5 до 5,5 см [9].
Таким образом, причиной, предрасполагающими факторами СМВ могут быть заболевания пищевода, карди-оэзофагеального перехода, некоторые инструментальные методы исследования, проводимые через пищевод, о чем необходимо помнить при диагностике данного синдрома и особенно при проведении чреспищеводных методов исследования.
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
1. Галлингер Ю.И., Годжелло Э.А. Проблемы и перспективы внутрипросветной эндоскопической хирургии и пищевода // IV Московский международный конгресс по эндоскопической хирургии. —М., 2000.—С. 58-60.
—М., 2000.—С. 58-60.
2. Дуданов И.П., Шаршавицкий Г.А., Меженин А.М. и др. Хирургическая тактика при синдроме Маллори-Вейсса // Вестн. хир.—1998.—№ 3.—С. 67-69.
3. Курыгин А.А., Баранчук В.Н., Манышев В.Г. Лечение синдрома Маллори-Вейсса эндоскопической диатермокоагуляцией // Хирургия.—1991.—№ 9.—С. 63-66.
4. Магниех М.М. Выбор лечебной тактика при синдроме Mallory-Weiss: Автореф. дис. …канд. мед. наук.—СПб., 1999.—23 с.
5. Ревякин В.И., Оганесян Л.Е. Эффективные эндоскопические методы лечения больных с синдромом Маллори-Вейсса // IV Московский международный конгресс по эндоскопической хирургии.—М., 2000.—С. 248-249.
6. Хунафин С.Н., Гибадуллин А.Х., Абдуллина Г.А. Диагностика и лечение синдрома Маллори-Вейсса // Актуальные вопросы медицинской помощи: Материалы научно-практической кон-ференции. —Уфа, 1999.—С. 131-132.
—Уфа, 1999.—С. 131-132.
7. Ashenburg C., Rothstein F.C., Dahms B.B. Herpes esophagitis in the immunocompetent child // J. Pediatr.—1986.—Bd. 108.— S. 584-587.
8. Bak-Romaniszyn L., Matecka-Panas E., Czkwianianc E. Mallory-Weiss syndrome in children // Diseases Esophagus.—1999.— № 12.—P. 65-67.
9. Bellmann B., Wohlgemuth B., Kothe W. Об этиологии и патогенезе синдрома Маллори-Вейсса // Хирургия.—1974.—№ 2.— P. 14-19.
10. Bladergroen M.R., Lowe J.E., Postlethwait R.W. Diagnosis and recommended management of esophageal perforation // Ann. Thorac. Surg.—1986.—Vol. 42.—P. 235-239.
11. Bubrick M.P., Lundeen J.W., Onstad G.R., Hitchcock C.R. Mallory-Weiss syndrome: analysis of fifty-nine cases // Surgery.—1980.— Vol. 88.—P. 400-405. 2009
2009
12. Bufkin B.L., Miller J.I., Mansour K.A. Esophageal perforation: emphasis on management // Ann. Thorac. Surg.—1996.— Vol. 61.—P. 1447-1452.
13. Cannon R., Lee G., Cox K. Gastrointestinal hemorrhage due to Mallory-Weiss syndrome in infant // J. Pediatr. Gastroenterol. Nutr.—1985.—№ 4.—P. 323-325.
14. Carr J.C. The Mallory-Weiss syndrome // Clin. Radiol.—1973.— Vol. 24.—P. 107-112.
15. Chan K.L., Cohen G.I., Suchowski R.A., Baird M.G. Complications of transesophageal echocardiography in ambulatory adult patiens: analysis of 1500 consecutive examinations // J. Am. Soc. Echocardiogr.—1991.—№ 4.—P. 577-582.
16. Chee T.S., Quek S.S.S., Ding Z.P., Chua S.M. Clinical utility, safety, acceptability and complications of transesophageal echocardiography (TEE) in 901 patients // Singapore Med. J.— 1995.—Vol. 38.—P. 479-483.
J.— 1995.—Vol. 38.—P. 479-483.
17. Chen YL. Mechanical gastritis as cause of upper gastrointestinal hemorrhage // Scand. J. Gastroenterol.—1993.—Vol. 28.— P. 512-514.
18. Chien R.N., Chen P.C., Lin P.Y, Wu C.S. Herpes esophagitis: a cause of upper gastrointestinal bleeding in an immunocompetent patient // J. Formos Med. Assoc.—1992.—Vol. 91.—P. 11121114.
19. Cronstedt J.L., Bouchama A., Hainau B. et al. Spontaneous esophageal perforation in herpes simplex esophagitis // Am. J. Gastroenterol.—1992.—Vol. 87.—P. 124-127.
20. Daniel W.G., Erbel R., Kasper W. et al. Safety of transesophageal echocardiography: a multicenter survey of 10419 examinations // Circulation.—1991.—Vol. 83.—P. 817-821.
21. Decker J.P., Zamcheck N., Mallory G. K. Mallory-Weiss syndrome. Hemorrhage from gastroesophageal lacerations at the cardiac orifice of the stomach // N. Engl. J. Med.—1953.—Vol. 249.— P. 957-963.
K. Mallory-Weiss syndrome. Hemorrhage from gastroesophageal lacerations at the cardiac orifice of the stomach // N. Engl. J. Med.—1953.—Vol. 249.— P. 957-963.
22. De Vries A.J., van der Maaten J.M.A.A., Laurens R.R.P. Mallory-Weiss tear following cardiac surgery: transoesophageal echoprobe or nasogastric tube? // Br. J. Anaest.—2000.—Vol. 84.—P. 646649.
23. Dewhirst W.E., Stragand J.J., Fleming B.M. Mallory-Weiss tear complicating intraoperative transesophageal echocardiography in a patient undergoing aortic valve replacement // Anesthesiology.— 1990.—Vol. 73.—P. 777-778.
24. Di Felice G. The current role of endoscopy in Mallory-Weiss syndrome // Surg. Endosc.—1991.—Vol. 5.—P. 24-27.
25. Fishman M., Thirwell M.P., Daly D.S. Mallory-Weiss tear: a complication of cancer chemotherapy // Cancer. —1983.— Vol. 52.—P. 2031-2032.
—1983.— Vol. 52.—P. 2031-2032.
26. Foster D.N., Miloszewski K., Losowsky M.S. Diagnosis of Mallory-Weiss lesions: A common cause of upper gastrointestinal bleeding // Lancet.—1976.—Vol. 11.—P. 483-484.
27. Flynn A.E., Verrier E.D., Way L.W. et al. Esophageal perforation // Arch. Surg.—1989.—Vol. 124.—P. 1211-1215.
28. I guchi Y, Ohmoto K., Shibata N. et al. A case of esophageal intramural pseudodiverticulosis complicated with primary biliary cirrhosis and mixed connective tissue disease (in Japanese) // Jpn. J. Gastroenterol.—1997.—Vol. 94.—P. 180-185.
29. Itoh T., Takahashi T., Kusaka K. et al. Herpes simplex esophagitis from 1307 autopsy cases // J. Gastroenterology.—2003.— Vol. 18.—P. 1407-1411.
30. Johnson H.N. Visceral lesions associated with varicella // Arch. Pathol.—1940.—Vol. 30.—P. 292.
Johnson H.N. Visceral lesions associated with varicella // Arch. Pathol.—1940.—Vol. 30.—P. 292.
31. Kato S., Yamamoto R., Yoshimitsu S. Herpes simplex esophagitis in the immunocompetent host // Diseases of the Esophagus.— 2005.—Vol. 18.—P. 340-344.
32. Kusakari K. Esophageal web and Schatzaki’s ring (in Japanese with English summary) // Clin. Gastroenterol.—1998.—Vol. 13.— P. 493-498.
33. Latham P., Hodgins L.R. A gastric laceration after transesophageal echocardiography in a patient undergoing aortic valve replacement // Anesth. Analg.—1995.—Vol. 81.—P. 641-642.
34. Lawrence D.R., Ohri S.K., Moxon R.E. et al. Iatrogenic oesophageal perforations: a clinical review // Ann. R. Coll. Surg. Engl.—1998.— Vol. 80.—P. 115-118.
35. Levine M.S., Moolten D.N., Herlinger H. et al. Esophageal intramural pseudodiverticulosis: a reevaluation // A.J.R.—1986.— Vol. 47.—P. 1165-1170.
Levine M.S., Moolten D.N., Herlinger H. et al. Esophageal intramural pseudodiverticulosis: a reevaluation // A.J.R.—1986.— Vol. 47.—P. 1165-1170.
36. Mallory K., Weiss S. Hemorrhage from laceration of the cardiac orifice of the stomach due to vomiting // Am. J. Med. Sci.— 1929.—Vol. 178.—P. 506-515.
37. Massey S.R., Pitsis A., Mehta D., Callaway M. Oesophageal perforation following perioperative transesophageal echocardiography // Br. J. Anaesth.—2000.—Vol. 84.—P. 643646.
38. Marsumoto J., Sumiyoshi A. Herpes simplex esophagitis. A study in autopsy series // Am. J. Clin. Pathol.—1985.—Vol. 84.— P. 96-99.
39. Mendi K., McKay J.M., Tanner C.H. Intramural diverticulosis of the oesophagus and Rokitansky-Aschoff sinuses in the gall-bladder // Br. J. Radiol.—1960.—Vol. 33.—P. 496-501.
40. McBane R., Gross J.B. Jr. Herpes esophagitis: clinical syndrome, endoscopic appearance, and diagnosis in 23 patients // Gastrointest. Endosc.—1991.—Vol. 37.—P. 600-603.
41. McDonald G.B., Sharma P., Hackman R.C. et al. Esophageal infections in immunosuppressed patients after marrow transplantation // Gastroenterology.—1985.—Vol. 88.—P. 11111117.
42. Orlowski W., Gibinski K., Konturek S. Nauka o chorobach wewnetrznych.—Warszawa: PZWL, 1989.—P. 652-655.
43. Pagel J., Lindkaer-Jensen S., Nielsen O.V. The Mallory-Weiss syndrome // Acta. Chir. Scand.—1975.—Vol. 141.—P. 532-535.
44. Penston J.G., Royd E.J., Wormsley K.G. Mallory-Weiss tears occurring during endoscopy: a report of seven cases // Endoscopy. —1992.—Vol. 24.—P. 762-765.
—1992.—Vol. 24.—P. 762-765.
45. Pikarsky A.J., Zamir G., Belzberg H. Mallory-Weiss syndrome: possible link to water immersion and subsequent air flight // Am. Surgeon.—2000.—Vol. 66.—P. 1083-1084.
46. Quincke H. Ulcus oesophagi ex digestione // Dtsch. Arch. klin. Med.—1879.—Bd. 24.—S. 72.
47. Rataller R. Endoscopics sclerotheraphy in upper gastrointestinal bleeding duet of the Mallory-Weiss syndrome // Am. J. Gastroenterol.—1994.—Vol. 89.—P. 2147-2150.
48. Sinev I.V., Luzhnikov E.A., Sordiia D.G. Sindrom Mallory-Weissa pri ostrykh otrawleniakh neprizhigaiuschimi wesheststvami // Klin. Med. Mosc.—1990.—Vol. 68.—P. 77-79.
49. Srhuman R.M., Threadgill S.T. The influence of the liver disease and portal hypertension on bleeding in Mallory-Weiss syndrome // J. Clin. Gastroenterol.—1994.—Vol. 18.—P. 10-12.
Clin. Gastroenterol.—1994.—Vol. 18.—P. 10-12.
50. Sugawa C., Steffes C.P., Nakamura R. et al. Upper Gl bleeding in an urban hospital etiology, recurrence and prognosis // Ann. Surg.—1990.—Vol. 212.—P. 521-527.
51. Wilcox C.M., Schwartz D.A., Clark W.S. Esophageal ulceration in human immunodeficiency virus infection. Causes, response to therapy, and long-term outcome // Ann. Intern. Med.—1995.— Vol. 123.—P. 143-149.
52. Wos H., Grzybowska-chlebowczyk U. Mallory-Weiss syndrome in 11 years boy // Przegl. Ped.—1994.—Vol. 24.—P. 99-101.
53. Yamamoto N., Nakamura M., Tachilana S. Esophageal intramural pseudodiverticulosis with Mallory-Weiss syndrome: report of a case // Surg. Today.—2002.—Vol. 32.—P. 519-522.
Поступила в редакцию 04. 09.2008 г.
09.2008 г.
Пищеводные геморрагические синдромы | Белобородов
1. Белобородов В.А., Кельчевская Е.А. Рецидивы кровотечения из острых язв и эрозий верхних отделов пищеварительного тракта. Acta Biomedica Scientifica.2012; (4-1): 21-24.
2. Зубарев П.Н., Трофимов В.М. Хирургические болезни пищевода и кардии. Руководство для врачей. СПб.: Фолиант; 2005.
3. Петров В.П., Ерюхин И.А., Шемякин И.С. Кровотечения при заболеваниях пищеварительного тракта. М.: Медицина; 1987.
4. Черноусов А.Ф., Богопольский П.М., Курбанов Ф.С. Хирургия пищевода: руководство для врачей.М.: Медицина; 2000.
5. Синельников Р.Д., Синельников Я.Р. Атлас анатомии человека. В 4 томах. М.: Медицина; 1996.
Синельников Р.Д., Синельников Я.Р. Атлас анатомии человека. В 4 томах. М.: Медицина; 1996.
6. Шалимов А.А. Полупан В.Н. Атлас операций на пищеводе, желудке и двенадцатиперстной кишке. М.: Медицина; 1975.
7. Горпинич А.Б., Мангилев С.В. Опыт диагностики и лечения синдрома Маллори-Вейсса. Здоровье и образование в XXI веке. 2016; 18(11): 32-35.
8. Панцирев Ю.М., Федоров В.Д., Тимофеев М.Е., Михалев А.И. Эндоскопическое лечение кровотечений, обусловленных синдромом Меллори-Вейсса. Хирургия. 2003; (10): 35-40.
9. Тимербулатов Ш.В., Тимербулатов В.М., Мустафин Т.И., Ямалов Р.А. Этиопатогенетические аспекты синдрома Меллори-Вейса. Медицинский вестник Башкортостана. 2010: 5(3): 24-27.
10. Чередников Е.Ф., Мареев Ю.Ф., Черных А.В., Литовкина Т.Е., Бондаренко А.А., Чередников Е.Е., и др. Современные взгляды на диагностику, лечение и про-филактику разрывно-геморрагического синдрома (синдрома Меллори-Вейса). Вестник новых медицинских технологий. 2016; 23(4): 161-172.
11. Forrest JA, Finlayson ND, Shearman DJ. Endoscopy in gastrointestinal bleeding. Lancet. 1974; 304(7877): 394-397. doi: 10.1016/S0140-6736(74)91770-X
12. Mallory GK, Weiss S. Hemorrhages from lacerations of the cardiac orifice of the stomach due to vomiting. American Journal of the Medical Sciences,1929; 178: 506-515.
13. Борисов А.Е. (ред.) Руководство по хирургии печени и желчевыводящих путей. Т. 1.СПб.: Предприятие ЭФА; 2002.
Т. 1.СПб.: Предприятие ЭФА; 2002.
14. Дашацыренова Д.Б., Гаврилова А.К., Твердохлебов П.О. Эндоскопическое лигирование как метод первичной и вторичной профилактики пищеводных кровотечений при варикозно расширенных венах пищевода Acta Biomedica Scientifica. 2017; 2(5-2): 151-153. doi: 10.12737/article_5a3a0ead02b258.50539404
15. Жерлов Г.К., Рудая Н.С., Кошевой А.П., Карпович А.В., Жерлова Т.Г., Чирков Д.Н., и др. Оптимизация прогноза и хирургической профилактики кровотечений из варикозно-расширенных вен пищевода. Хирургия. 2006; (7): 27-33.
16. Ивашкин В.Т., Маевская М.В., Павлов Ч.С., Федосьина Е.А., Бессонова Е.Н., Пирогова И.Ю., и др. Клинические рекомендации Российского общества по изучению печени и Российской гастроэнтерологической ассоциации по лечению осложнений цирроза печени. Российский журнал гастроэнтерологии, гепатологии, колопроктологии.2016; 26(4): 71-102. doi: 10.22416/1382-4376-2016-26-4-71-102
Российский журнал гастроэнтерологии, гепатологии, колопроктологии.2016; 26(4): 71-102. doi: 10.22416/1382-4376-2016-26-4-71-102
17. Лебезев В.М., Шерцингер А.Г., Гунзынов Г.Д., Укоев А.Д. Основные показатели хирургического лечения с внепеченочной портальной гипертензией. Acta Biomedica Scientifica.2009; (3): 341-342.
18. Мошарова А.А., Соснин П.С., Алисов В.А., Верткин А.Л. Лечение и профилактика кровотечения из варикозно расширенных вен пищевода. Врач скорой помощи.2012; (9): 44-50.
19. Шаповалов А.М., Коробка В.Л., Черкасов М.Ф. Способ хирургического лечения и профилактики кровотечений из варикозных вен пищевода и желудка. Медицинский вестник Юга России. 2015; (3): 112-114.
20. Шерцингер А.Г. Чжао А.В., Ивашкин В.Т. Лечение кровотечений из варикозно расширенных вен пищевода и желудка. Анналы хирургической гепатологии. 2013; 18(3): 110-129.
Шерцингер А.Г. Чжао А.В., Ивашкин В.Т. Лечение кровотечений из варикозно расширенных вен пищевода и желудка. Анналы хирургической гепатологии. 2013; 18(3): 110-129.
21. Albillos AM. Survival of patients with cirrhosis after acute variceal bleeding. Revista Española de Enfermedades Digestivas. 2009; 101(4): 231-235.
22. Rosemurgy АS, Zervos EE. Management of variceal hemorrhage. Current Problems in Surgery, 2003; 40(6): 255-343. doi: 10.1016/s0011-3840(03)00012-1
23. Berzigotti A, García-Pagán JC. Prevention of recurrent variceal bleeding. Digestive and Liver Disease.2008; 40(5), 337-342. doi: 10.1016/j.dld.2007.12.003
24. Berzigotti A, Seijo S, Reverter E, Bosch J. Assessing portal hypertension in liver diseases. Expert Review of Gastroenterology & Hepatologyl. 2013; 7(2), 141-155. doi: 10.1586/egh.12.83
Expert Review of Gastroenterology & Hepatologyl. 2013; 7(2), 141-155. doi: 10.1586/egh.12.83
25. Crisan D, Tantau M, Tantau A. Endoscopic management of bleeding gastric varices-an updated overview. Current Gastroenterology Reports. 2014;16(10): 413. doi: 10.1007/s11894-014-0413-1
26. Franco MC, Gomes GF, Nakao FS, de Paulo GA, Ferrari AP Jr, Libera ED Jr. Efficacy and safety of endoscopic prophylactic treatment with undiluted cyanoacrylate for gastric varices. World Journal of Gastrointestinal Endoscopy. 2014; 6(6): 254-259. doi: 10.4253/wjge.v6.i6.254
27. Emori K, Toyonaga A, Oho K, Kumamoto M, Haruta T, Inoue H, et al. Balloon-occluded retrograde transvenous obliteration versus endoscopic injection sclerotherapy for isolated gastric varices: a comparative study. The Kurume Medical Journal.2014; 60(3.4): 105-113. doi: 10.2739/kurumemedj.ms63009
The Kurume Medical Journal.2014; 60(3.4): 105-113. doi: 10.2739/kurumemedj.ms63009
28. Biecker E. Portal hypertension and gastrointestinal bleeding: diagnosis, prevention and management. World Journal of Gastroenterology.2013; 19(31): 5035-5050. doi: 10.3748/wjg.v19.i31.5035
29. Агеенко В.А., Кельчевская Е.А., Нетесин Е.С. Эрозивно-язвенный эзофагит, осложненный кровотечением. Сибирский медицинский журнал (Иркутск).2009; 85(2): 105-108.
30. Байжанов С.Ш., Меньшикова И.Л., Байжанов А.С., Болотова О.Г., Ердалиева Л.К., Рысбек Т.Б., и др. Эндоско-пический гемостаз при эрозивно-язвенных поражениях верхних отделов желудочно-кишечного тракта. Вестник КазНМУ.2013; (2): 218-220.
31. Волков С.В. Химические ожоги пищевода: эндоскопическая диагностика и лечение. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2002; 12(1): 58-61.
Волков С.В. Химические ожоги пищевода: эндоскопическая диагностика и лечение. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2002; 12(1): 58-61.
32. Годжелло Э.А. Галлингер Ю.И. Пищевод Баррета, аденокарцинома пищевода и задачи современной гастроэнтерологии. Российский журнал гастроэнтерологии, гепатологии, колопроктологии.2001; 11(6): 71-75.
33. Годжелло Э.А. Пищевод Баррета: эндоскопическая диагоностика, стратегия наблюдения и лечения. Российский журнал гастроэнтерологии, гепатологии, колопроктологии.2002; (5): 67.
34. Геллер Л.И., Бессонова Г.А., Петренко В.Ф. Эрозивный рефлюкс-эзофагит и его лечение. Терапевтический архив. 1991; 63(1): 81-84.
35. Касумов Н. А. Рефлюкс-эзофагит: современное состояние проблемы (обзор литературы). Хирургия. Журнал им. Н.И. Пирогова.2007; (4): 62-65.
А. Рефлюкс-эзофагит: современное состояние проблемы (обзор литературы). Хирургия. Журнал им. Н.И. Пирогова.2007; (4): 62-65.
36. Райхлин Н.Т., Рапопорт С.И., Лаптева О.Н., Расулов М.И., Хуцишвили М.Б., Смирнова Е.А. Гастроэзофагеальная рефлюксная болезнь, новые данные по механизму заживления эрозивно-язвенных поражений пищевода. Клиническая медицина. 2000; (8): 31-37.
37. Трухманов А.С. Пищевод Баррета: эпидемиология, патогенез, клиническое течение и профилактика. Российский журнал гастроэнтерологии, гепатологии, колопроктологии.2002; (5): 59-62.
38. Сотников В.Н., Дубинская Т.К., Разживина А.А. Эндоскопическая диагностика острых кровотечений из верхних отделов пищеварительного тракта: Учебное пособие. М.: РМАПО; 2000.
39. Эфендиев В.М., Алиев Т.М., Алиев Ф.Г., Велиев М.А., Касумов Н.А., Кязимов А.К. Ваготомия в лечении кровоточащего рефлюкс-эзофагита и гастродуоденальных кровотечений. Хирургия. 2004; (6): 24-26.
Эфендиев В.М., Алиев Т.М., Алиев Ф.Г., Велиев М.А., Касумов Н.А., Кязимов А.К. Ваготомия в лечении кровоточащего рефлюкс-эзофагита и гастродуоденальных кровотечений. Хирургия. 2004; (6): 24-26.
40. Baker CR, Forshaw MJ, Gossage JA, Ng R, Mason RC. Long-term outcome and quality of life after supercharged jejunal interposition for oesophageal replacement. Surgeon. 2015; 13(4): 187-193. doi: 10.1016/j.surge.2014.01.004
41. DeMeester SR. Colon interposition following esophagectomy. Diseases of the Esophagus.2001; 14(3-4): 169-172. doi: 10.1046/j.1442-2050.2001.00180.x
42. Orringer MB, Marshall B, Iannettoni MD. Transhiatal esophagectomy: clinical experience and refinements. Annals of Surgery. 1999; 230(3): 392-403. doi: 10.1097/00000658-199909000-00012
Синдром Меллори-Вейса – причины, симптомы, диагностика и лечение
Синдром Меллори-Вейса — линейные разрывы слизистой кардиоэзофагеальной зоны, возникшие на фоне рвоты, позывов на рвоту, икоты. Проявляется наличием крови в рвотных массах, эпигастральными или загрудинными болями, артериальной гипотензией, тахикардией. Диагностируется с помощью эзофагогастроскопии, обзорной рентгенографии брюшной полости. Для лечения применяется гемостатическая, кровезаместительная терапия, противорвотные препараты, сердечные аналептики, ингибиторы протонной помпы, Н2-гистаминоблокаторы, антациды. При необходимости выполняется эндоскопический гемостаз, терапевтическая эмболизация, гастротомия для ушивания повреждений.
Проявляется наличием крови в рвотных массах, эпигастральными или загрудинными болями, артериальной гипотензией, тахикардией. Диагностируется с помощью эзофагогастроскопии, обзорной рентгенографии брюшной полости. Для лечения применяется гемостатическая, кровезаместительная терапия, противорвотные препараты, сердечные аналептики, ингибиторы протонной помпы, Н2-гистаминоблокаторы, антациды. При необходимости выполняется эндоскопический гемостаз, терапевтическая эмболизация, гастротомия для ушивания повреждений.
Общие сведения
Впервые клиника разрывно-геморрагического синдрома была описана в 1929 году американскими патологами Дж.К. Меллори и С. Вейсом. В настоящее время заболевание является одной из ведущих причин неязвенных кровотечений из верхних отделов пищеварительного тракта. Распространенность патологии достигает 5-10%. Болезнь Меллори-Вейса выявляется преимущественно у 45-60-летних пациентов, злоупотребляющих спиртными напитками. У мужчин разрывы желудочной и пищеводной слизистой возникают в 7 раз чаще, чем у женщин. У 79-80% больных поражается эзофагогастральный переход, у 16-17% — стенка пищевода, у 3-5% — кардиальная оболочка. Длина разрывов обычно составляет 0,4-4,5 см. В 77-78% случаев повреждения являются единичными, в 22-23% — множественными.
Синдром Меллори-Вейса
Причины синдрома Меллори-Вейса
Продольные разрывы слизистой в области пищеводно-желудочного перехода возникают при локальном повышении давления у пациентов со сниженной резистентностью эпителиального слоя. Предпосылками к развитию разрывно-геморрагического гастроэзофагеального синдрома служат патологические процессы, при которых повреждаются эпителиоциты или наблюдается повышенное кровенаполнение сосудов верхних отдела ЖКТ: асептическое воспаление слизистой при частом употреблении спиртных напитков, воспалительные заболевания ЖКТ (эзофагиты, гастриты), длительный прием НПВС, кортикостероидов, скользящая грыжа пищеводного отверстия диафрагмы, расширение пищеводных вен при портальной гипертензии у больных с гепатитами, жировым гепатозом, фиброзом, циррозом печени. Непосредственными причинами болезни Меллори-Вейса являются:
- Рвота, неукротимая икота. У 80-85% пациентов развитие рвоты связано с алкогольным опьянением. Провоцирующими факторами также становятся рвота беременных, диспепсические расстройства при патологии пищеварительного тракта (язвенной болезни, панкреатите, холецистите), отравления, уремия.
- Длительный интенсивный кашель. В редких случаях разрывно-геморрагический синдром провоцируется острыми и хроническими респираторными заболеваниями. Линейное повреждение слизистой пищевода, верхних отделов желудка может осложнить коклюш, ОРВИ, хронический бронхит, бронхиальную астму.
- Ятрогенные воздействия. Повреждение стенки пищевода, желудка возможно при грубом выполнении эндоскопических манипуляций (гастроскопии, эзофагогастродуоденоскопии), введении желудочного зонда. Иногда разрывы слизистой возникают при проведении сердечно-легочной реанимации.
В спорадических случаях повышение давления, приводящее к разрыву эпителиального слоя, вызывается другими факторами — подъемом тяжестей, интенсивными физическими нагрузками с резким напряжением мышц брюшного пресса, тупой травмой живота. Крайне редко заболевание осложняет течение судорожного синдрома при эпилепсии, опухолях головного мозга, энцефалопатиях, менингите, энцефалите, эклампсии.
Патогенез
Пусковым моментом разрыва пищеводно-желудочной слизистой обычно становится многократная рвота, резкое повышение абдоминального давления при переполненном желудке или кардиоэзофагеальном спазме, реже — прямые механические воздействия. Возникновение избыточного давления в кардиальном отделе желудка способствует перерастяжению стенки органа. При морфологической несостоятельности эпителия, вызванной воспалительными процессами, растянутая слизистая желудка, пищевода разрывается в наиболее истонченном или патологически измененном участке. Обычно разрыв распространяется не глубже эпителиального и подслизистого слоя. В тяжелых случаях повреждается мышечная, серозная желудочная либо адвентициальная пищеводная оболочки с выходом агрессивного содержимого в средостение или брюшную полость.
Классификация
Систематизация клинических форм синдрома Меллори-Вейса основана на протяженности и глубине дефектов оболочек поврежденных органов, от размеров которых напрямую зависит тяжесть патологии. Разрывы бывают малыми (до 1 см) — наиболее частый вариант повреждения, выявляемый у 88-90% пациентов, средними (1-3 см), большими (более 3 см). С учетом глубины деструкции стенки пораженного отдела ЖКТ специалисты в сфере гастроэнтерологии и общей хирургии различают 4 стадии гастроэзофагеального разрывного синдрома:
- I стадия. Повреждение слизистой желудочно-пищеводного перехода и дистальной трети пищевода. Встречается у 36-37% пациентов. В большинстве случаев кровотечение прекращается спонтанно.
- II стадия. Дефекты расположены в той же зоне, однако их глубина достигает подслизистого слоя. Выявляется у 52-53% больных. Обычно проводится консервативная гемостатическая терапия.
- III стадия. Глубокие зияющие разрывы с вовлечением мышечной оболочки и интенсивным кровотечением. Наблюдаются в 9-11% случаев. Необходим эндоскопический или хирургический гемостаз.
- IV стадия. Редко диагностируемое тяжелое повреждение с разрушением всех оболочек гастроэзофагеального участка ЖКТ. Осложняется медиастинитом, перитонитом, пневмотораксом.
Симптомы синдрома Меллори-Вейса
Клинические проявления заболевания обычно развиваются на фоне многократной рвоты. Основным признаком синдрома является выделение ярко-красной крови с рвотными массами (гематемезис), которое может иметь различную интенсивность – от нескольких капель до профузного кровотечения. Возникает резкая боль в эпигастральной области или за грудиной. Вследствие кровопотери у больного формируется острый анемический синдром, для которого характерны головокружение, бледность кожных покровов, мелькание «мушек» перед глазами, падение артериального давления, значительное учащение сердцебиения. При массивном кровотечении возможна потеря сознания.
Осложнения
Острая кровопотеря при симптомокомплексе Меллори-Вейса может привести к развитию геморрагического шока с тяжелыми нарушениями микроциркуляции, изменениями реологических свойств крови, прогрессирующей гипоксией. При отсутствии лечения шок переходит в декомпенсированную стадию, сопровождающуюся полиорганной недостаточностью. Наиболее тяжелым осложнением синдрома является тотальный разрыв стенки брюшного отдела пищевода, распространяющийся выше уровня диафрагмы. При этом у пациента возникает приступ одышки, цианоз кожи, сильнейшие боли в грудной клетке. Такое осложнение, известное как синдром Бурхаве, в 20-40% случаев заканчивается летальным исходом. Попадание содержимого желудка в средостение, полость брюшины провоцирует развитие медиастинита, перитонита.
Диагностика
Постановка диагноза при синдроме Мэллори-Вейса может быть затруднена, что обусловлено стремительным нарастанием клинической картины и необходимостью оказания пациенту экстренной медицинской помощи. Диагностика заболевания предполагает комплексное инструментальное обследование пищеварительного тракта для выявления первопричины кровавой рвоты. Наиболее информативными являются:
- Эзофагогастроскопия. Введение гибкого эндоскопа через ротовую полость позволяет оценить состояние эпителиальной оболочки верхних отделов ЖКТ и обнаружить линейные разрывы, которые обычно локализованы в области перехода пищевода в желудок. С помощью визуального осмотра удается установить глубину поражения стенки пищевода или желудка.
- Обзорная рентгенография брюшной полости. Проведение рентгенологического исследования информативно при подозрении на разрыв полого органа. Основной признак перфорации – наличие свободного газа в полости брюшины (симптом «серпа»). На рентгенограмме также можно обнаружить другие болезни ЖКТ, которые являются первопричиной патологии Меллори-Вейса.
В клиническом анализе крови определяются изменения, характерные для анемического синдрома — уменьшения содержания эритроцитов и гемоглобина, снижение показателя гематокрита. Для исключения хронического кишечного кровотечения проводится реакция Грегерсена, позволяющая обнаружить скрытую кровь в кале. При выраженном диспепсическом синдроме может выполняться бактериологический посев кала для выявления патогенных микроорганизмов.
Дифференциальная диагностика синдрома осуществляется с легочным кровотечением, отеком легких, сердечной астмой, кровотечением из язвы желудка, варикозным расширением пищеводных вен, острым гастроэнтеритом, кишечными инфекциями, распадом опухоли желудка или пищевода, синдромом Рандю-Ослера. Кроме осмотра хирурга и гастроэнтеролога пациенту могут потребоваться консультации гематолога, инфекциониста, пульмонолога, кардиолога, гематолога, гепатолога.
Лечение синдрома Меллори-Вейса
Пациент подлежит неотложной госпитализации в хирургический стационар. На начальном этапе больному обеспечивается покой, холод на область желудка, при позывах на рвоту применяются блокаторы дофаминовых и серотониновых рецепторов с противорвотным эффектом. Назначается консервативное лечение и малоинвазивные манипуляции, направленные на остановку кровотечения, восполнение объема циркулирующей крови. При резком падении АД терапию дополняют введением средств для поддержания гемодинамики. Пациентам с болезнью Меллори-Вейса показаны:
- Инфузионная терапия. При умеренной кровопотере проводятся внутривенные вливания коллоидных и кристаллоидных растворов. При массивном кровотечении переливается эритроцитарная масса или взвесь, нативная и свежезамороженная плазма, реже — донорская кровь.
- Гемостатические препараты. Для медикаментозного гемостаза используют стимуляторы свертывающей системы крови. Эффективность кровоостанавливающей терапии повышается при парентеральном введении препаратов кальция, синтетических аналогов витамина К.
- Эндоскопический гемостаз. При продолжающемся кровотечении с помощью эндоскопа обкалывают место повреждения средствами с сосудосуживающим эффектом, вводят склерозанты, лигируют или клипируют сосуды. Возможно выполнение аргоноплазменной или электрокоагуляции.
- Терапевтическая эмболизация. Для прекращения кровотечения из поврежденных сосудов в них под контролем ангиографии вводят смесь эмболов с физиологическим раствором. Альтернативным методом является редко применяемое внутриартериальное вливание жировых суспензий.
Баллонная зондовая тампонада используется ограниченно из-за возможного усугубления разрывов. Важным условием быстрого восстановления поврежденной стенки является угнетение желудочной секреции при помощи ингибиторов протонной помпы, блокаторов Н2-гистаминорецепторов. Прием секретолитиков дополняют назначением невсасывающихся антацидов, препаратов коллоидного висмута. Хирургические методы лечения геморрагического разрывного синдрома показаны при неостанавливающихся или рецидивирующих кровотечениях, глубоких дефектах, полном разрыве пищеводной или желудочной стенки. Рекомендованным вмешательством является гастротомия с прошиванием надрывов, кровоточащих сосудов, ушиванием дефектов, иногда — перевязкой левой желудочной артерии.
Прогноз и профилактика
Исход патологического состояния зависит от величины кровопотери и тяжести основного заболевания пациента. В 90% случаев кровотечение останавливается самопроизвольно или консервативными способами. Прогноз синдрома относительно неблагоприятный при потере больше 10% ОЦК и наличии сопутствующей патологии. Меры профилактики при заболевании Меллори-Вейса заключаются в отказе от злоупотребления алкоголем, своевременном устранении провоцирующих факторов, выявлении и лечении болезней желудочно-кишечного тракта, соблюдении техники проведения инвазивных медицинских манипуляций на пищеводе, желудке.
Синдром Маллори Вейса при диффузных поражениях печени Текст научной статьи по специальности «Клиническая медицина»
Вестник КазНМУ, №1 – 2013
УДК 617-089 (075.8)
Б.К. ИДРИСОВ
«Городская поликлиника 10», г.Алматы
СИНДРОМ МАЛЛОРИ ВЕЙСА ПРИ ДИФФУЗНЫХ ПОРАЖЕНИЯХ ПЕЧЕНИ
Пищеводно-желудочное кровотечение является одним из часто встречающихся осложнений заболеваний желудочно-кишечного тракта, обусловленное патологией печени с развитием портальной гипертензии. Варикозное расширение вен пищевода и желудка не всегда является единственным источником кровотечения при портальной гипертензии. В связи с этим, при проведении экстренного эндоскопического
исследования необходимо исключить геморрагию другой этиологии. По данным ряда авторов (Sutton G 1987; Андреев Г.Н. 2002) У больных с портальной гипертензией в 10 -28% случаев источник кровотечения не связан с варикозным расширением вен пищевода и желудка. Одной из причин эзофагально-гастрального кровотечения является синдром Маллори – Вейса, описанный впервые в 1929г. и занимает около 10% среди всех причин кровотечения желудочно-кишечного тракта. При синдроме Маллори – Вейса источником кровотечения являются, линейные разрывы слизистой оболочки в области желудочно-пищеводного перехода, а так же стенки желудка в кардиальном отделе. Разрыву слизистой оболочки пищеводно-желудочного перехода способствуют физическое перенапряжение, чаще рвота, принятие грубой пищи. Изменение кровоснабжения слизистой оболочки пищевода и желудка, рыхлость подслизистого слоя, образование трещин и множественных эрозий слизистой непосредственно связано с портальной гипертензией на фоне цирроза печени.
Принято считать, что желудочные кровотечения при портальной гипертензии возникают в результате разрыва флебэктазии, развивающиеся при этом эзофагиты с вовлечением в воспалительный процесс стенок расширенных венозных стволов, способствуют еще большему уменьшению сопротивляемости стенок сосудов и может произойти спонтанный разрыв вены. Однако, результаты эндоскопического исследования показали, что для возникновения острого кровотечения не обязателен разрыв крупных венозных стволов в подслизистом слое пищевода. Нередко, на аутопсии умерших от пищеводного кровотечения не удается обнаружить место разрыва венозного сосуда, а у 50% на секции обнаружено изъязвления слизистой оболочки нижней части пищевода, что дает предположение, что истонченные стенки слизистой оболочки пищевода подвергаются “агрессивному действию желудочного сока”, в результате чего образуются изъязвления. Клинические наблюдения показывают, что при циррозе
печени могут возникать тяжелые пищеводно-желудочные кровотечения, не связанные с разрывом пищеводных и кардиальных флэбэктазий. Установить диагноз цирроз печени на фоне острого кровотечения из варикозно – расширенных вен пищевода и кардии или из трещин слизистой оболочки весьма проблематично. Это обусловлено тем, что кровотечение чаще наблюдается в сравнительно ранних стадиях заболевания, как проявление раннего симптома цирроза печени. Правильная оценка функционального состояния печени, уровня компенсаторных возможностей организма, дифференциальная диагностика, выбор метода и тактики лечения являются основополагающими для исхода данной патологии. Патология печени с декомпенсацией портального кровотока ведет к системным нарушениям: портальная гипертензия, нарушение реологических свойств крови, значительным морфофункциональным изменениям, а в следствии этого и прилегающей слизистой пищевода и желудка.
Проанализировано 25 историй болезни, больных с синдромом Меллори-Вейса за 2011 год. Всем больным проведено эндоскопическое исследование ЭФГДС в первые часы после поступления в клинику. У 15 больных выявлено трещина абдоминального отдела и нижней трети пищевода, у 10 больных трещина нижней трети пищевода и кардии желудка, интенсивность кровотечения от легкой до тяжелой степени. Показатели красной крови колебались от 2,1 ± 0,8 до 4,5 * 1012/л и гемоглобин от 76 ± 6,0 до 120-130 гр/л. У 12 больных на УЗИ выявлены диффузные изменения в печени, умеренная гепатомегалия, у 2 больных спленомегалия. При дальнейшем исследовании биохимических показателей у больных с диффузными поражениями печени выявлены умеренная билирубинемия до 36 ммоль/л, Снижение белковообразовательной функции печени (55гр/л), повышение уровня трансаминаз в 1,2 раза, коагулограмма в сторону гиперкоагуляции. мeлшерiн толтыруга багытталып, гепатотропты жэне гепатопротекторлы дэрi-дэрмектердi мiндеттi турде ;осуымен бiрге журу керек.
B.K. IDRISOV
СИНДРОМ МАЛЛОРИ ВЕЙСА ПРИ ДИФФУЗНЫХ ПОРАЖЕНИЯХ ПЕЧЕНИ
Resume: Syndrome Mallory – Weiss may occur in patients with diffuse liver disease with portal hypertension of erosive and ulcerative lesions of the esophagus and gastric mucosa.
Treatment of patients with bleeding due to syndrome Mallory – Weiss should be complex, aimed at hemostasis, replenishing CBV with the mandatory inclusion of hepatotropic and hepatoprotector drugs.
1ll
Слеза Мэллори-Вайса | Johns Hopkins Medicine
Что такое слеза Мэллори-Вайса?
Пищевод – это трубка, по которой пища проходит из горла в желудок. Он играет жизненно важную роль в пищеварении. Иногда сильный кашель или рвота могут разорвать ткань нижнего отдела пищевода, и из него может начаться кровотечение. Это состояние называется слезой Мэллори-Вейсса.
Что вызывает слезу Мэллори-Вайса?
Слеза Мэллори-Вейсса чаще всего возникает в результате сильного кашля или рвоты.Менее распространенными причинами являются грыжа пищеводного отверстия диафрагмы или роды, которые могут повышать давление в брюшной полости.
Каковы симптомы слезы Мэллори-Вейсса?
Трудно сказать, что у вас есть слеза Мэллори-Вейсса и что у вас внутри идет кровь. Но у вас могут быть некоторые из этих признаков и симптомов:
- Рвота, ярко-красная или похожая на кофейную гущу
- Стул черный или смолистый
- Стул с кровью
- Слабость, головокружение, дурнота
- Короткость дыхания
- Диарея
- Бледность
- Боль в животе или груди
Как диагностируется слеза Мэллори-Вейсса?
Если у вас есть симптомы слезы Мэллори-Вейсса, ваш лечащий врач может проверить ваш стул на кровь.Ваш врач может также провести эндоскопию. Для этого теста ваш врач вводит гибкую трубку через рот в пищевод. Камера на конце трубки позволяет врачу увидеть разрыв внутри пищевода.
Как лечится слеза Мэллори-Вайса?
Слеза Мэллори-Вайса в большинстве случаев останавливает кровотечение и начинает заживать сама по себе. Иногда вам понадобится лечение. Эндоскоп может быть использован для инъекции или тепловой обработки, чтобы остановить кровотечение, или для вставки зажима, который закрывает разрыв и останавливает кровотечение.
Каковы осложнения слезы Мэллори-Вайса?
В редких случаях разрыв Мэллори-Вейса приводит к сильному внутреннему кровотечению. У вас учащенный пульс, падение артериального давления, проблемы с выделением мочи и шок. Если кровотечение не лечить, оно может привести к анемии с утомляемостью и одышкой.
Можно ли предотвратить разрыв Мэллори-Вайсса?
Вы мало что можете сделать, чтобы предотвратить разрыв Мэллори-Вайсса. Избегание ситуаций, вызывающих сильную рвоту (например, желудочный грипп) или кашель (например, курение), может помочь снизить риск.
Когда мне следует позвонить своему врачу?
Кровь в рвоте или стуле – серьезный симптом, требующий неотложной медицинской помощи. Если вы заметили какие-либо симптомы слезы Мэллори-Вейсса, немедленно обратитесь к своему врачу.
Ключевые моменты
- Слеза Мэллори-Вейсса – это разрыв ткани нижней части пищевода.
- Чаще всего это вызвано сильным кашлем или рвотой.
- Слезу Мэллори-Вейсса можно диагностировать и лечить во время эндоскопической процедуры.
- Если разрыв не лечить, это может привести к анемии, усталости, одышке и даже к шоку.
Дальнейшие действия
Советы, которые помогут вам получить максимальную пользу от посещения вашего поставщика медицинских услуг:
- Перед визитом запишите вопросы, на которые вы хотите получить ответы.
- Возьмите с собой кого-нибудь, кто поможет вам задать вопросы и запомнить, что вам говорит поставщик.
- Во время посещения запишите названия новых лекарств, методов лечения или тестов, а также все новые инструкции, которые дает вам поставщик.
- Если вам назначена повторная встреча, запишите дату, время и цель этого визита.
- Узнайте, как можно связаться со своим провайдером, если у вас возникнут вопросы.
Синдром Мэллори Вейсса – NORD (Национальная организация по редким заболеваниям)
УЧЕБНИКИ
Beers MH, Berkow R., eds. Руководство Merck, 17-е изд. Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк; 1999: 234.
Берков Р., изд. Руководство Merck – домашнее издание, 2-е изд. Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк; 2003: 710.
Ямада Т., Альперс Д.Х., Овьянг С. и др. Ред. Учебник гастроэнтерологии. 2-е изд. Компания Дж. Б. Липпинкотт. Филадельфия, Пенсильвания; 1995: 1295-96.
Sleisinger MH, et al. Ред. Заболевания желудочно-кишечного тракта. 4-е изд. Компания Сондерс. Филадельфия, Пенсильвания; 1989: 410.
ОБЗОР СТАТЬИ
Church NI, Palmer KR. Язвы и кровотечение из не варикозно расширенных вен. Эндоскопия. 2003; 35: 22-26.
Ямамото Н., Накамура М., Татибана С. и др. Оценка эндоскопического гемостаза при синдроме Мэллори-Вейсса, связанном с кровотечением из верхних отделов желудочно-кишечного тракта.Хирург сегодня. 2002; 32: 519-22.
Юнес З., Джонсон Д.А. Спектр спонтанных и ятрогенных повреждений пищевода: перфорации, слезы Мэллори-Вейсса и гематомы. J Clin Gastroenterol. 1999; 29: 306-17.
СТАТЬИ ИЗ ЖУРНАЛА
Fujii H, Suehiro S, Shibata T, et al. Слеза Мэллори-Вейсса, осложняющая интраоперационную чреспищеводную эхокардиография. Circ J. 2003; 32: 233-34.
Моралес П., Баум А.Е. Терапевтические альтернативы слезе Мэллори-Вейсса. Варианты лечения Curr Gastroenterol.2003; 6: 75-83.
Чунг И.К., Ким Э.Дж., Хван К.Й. и др. Оценка эндоскопического гемостаза при кровотечении из верхних отделов желудочно-кишечного тракта, связанном с синдромом Мэллори-Вейсса. Эндоскопия. 2002; 34: 474-79.
Хуанг С.П., Ван Х.П., Ли Ю.С. и др. Эндоскопическая установка гемоклипса и инъекция адреналина при синдроме Мэллори-Вейсса с активным кровотечением. Gastrointest Endosc. 2002; 55: 842-46.
Ганешрам К.Н., Харриссон П. Два случая подслизистой гематомы пищевода и слезы Мэллори-Вейсса. Int J Clin Pract.2002; 56: 225-26.
Gunay K, Cabioglu N, Barbaros U, et al. Эндоскопическая перевязка у пациентов с активным кровотечением слезы Мэллори-Вейсса. Surg Endosc. 2001: 15: 1305-07.
Llach J, Elizalde JI, Guevara MC, et al. Эндоскопическая инъекционная терапия при синдроме Мэллори-Вейсса при кровотечении: рандомизированное контролируемое исследование. Gastrointest Endosc. 2001; 54: 679-81.
Кортас Д.Ю., Хаас Л.С., Симпсон В.Г. и др. Слеза Мэллори-Вейсса: предрасполагающие факторы и предикторы осложненного течения. Am J Gastroenterol.2001; 96: 2863-65.
Тверада Р., Ито С., Акама Ф. и др. Синдром Мэллори-Вейса с сильным кровотечением: лечение эндоскопической перевязкой. Am J Emerg Med. 2000; 18: 812-15.
ИЗ ИНТЕРНЕТА
Слеза Мэллори-Вайса. MedlinePlus. Медицинская энциклопедия. Дата обновления: 13.01.2003. 3 стр.
www.nlm.nih.gov/medlineplus/ency/article/000269.htm
Синдром Мэллори-Вейсса. эмедицина. Последнее обновление: 3 января 2003 г. 9pp.
www.emedicine.com/ped/topic1359.htm
Слеза Мэллори-Вайса.эмедицина. Последнее обновление: 16 апреля 2002 г. 11pp.
www.emedicine.com/med/topic3428.htm
Синдром Мэллори-Вейсса. nd. 1шт.
www.cedars-sinai.edu/5687.html
Слеза Мэллори-Вайса | Сидарс-Синай
Не то, что вы ищете?Что такое слеза Мэллори-Вайса?
Ваш пищевод – это трубка, по которой пища переносится из горла в желудок. Играет а жизненно важная роль в пищеварении.Иногда резкий кашель или рвота могут разорвать ткань. из ваш нижний отдел пищевода, и он может начать кровоточить. Это состояние называется синдромом Мэллори-Вейсса. рвать.
Что вызывает слезу Мэллори-Вайса?
А Слеза Мэллори-Вейсса чаще всего возникает в результате сильного кашля или рвоты. Менее употребителен Причины – грыжа пищеводного отверстия диафрагмы или роды, которые могут увеличить давление в брюшной полости.Употребление алкоголя может повысить вероятность рвоты и слезы.
Каковы симптомы слезы Мэллори-Вейсса?
Это может быть трудно сказать, что у вас есть слеза Мэллори-Вейсса и что у вас внутри идет кровь. Но у вас могут быть некоторые из этих симптомов:
- Рвота ярко-красного цвета или похожая на кофейную гущу
- Табуреты черные или смолистые
- Табуреты с кровью в них
- Слабость, головокружение, дурнота
- Одышка
- Диарея
- Бледность
- Боль в животе или груди, иногда переходящая в спину
Как диагностируется слеза Мэллори-Вейсса?
Если у вас есть симптомы слезы Мэллори-Вейсса, ваш лечащий врач может проверить ваш табурет для крови.Ваш лечащий врач также может провести эндоскопию. Для этого теста гибкий трубка вводится через рот и опускается в пищевод. Камера в конце из трубка позволяет врачу увидеть разрыв внутри пищевода.
Как лечится слеза Мэллори-Вайса?
А Слеза Мэллори-Вайса в большинстве случаев останавливает кровотечение и начинает заживать самостоятельно.Иногда вам понадобится лечение. Если необходимо лечение, можно использовать эндоскоп. к сделают вам инъекцию или тепловую обработку, чтобы остановить кровотечение. Или это может быть использовано к вставьте зажим, закрывающий разрыв и останавливающий кровотечение. Часто ваше здравоохранение Врач также пропишет лекарства, снижающие кислотность желудка и помогающие вылечить Если вы принимаете лекарства для разжижения крови, узнайте у своего врача, когда ты следует остановить и перезапустить разжижитель крови.
Какие возможные осложнения слеза Мэллори-Вайса?
В В редких случаях слеза Мэллори-Вейса приводит к сильному внутреннему кровотечению. Вы получаете быстрый пульс, падение артериального давления, нарушение мочеиспускания и шок. Если кровотечение легкое остается без лечения, это может привести к анемии с утомляемостью и одышкой.
Можно ли предотвратить разрыв Мэллори-Вайса?
Вы мало что можете сделать, чтобы предотвратить слезу Мэллори-Вайсса.Держаться подальше от ситуации, которые вызывают сильную рвоту, например, употребление слишком большого количества алкоголя или кашель, например, курение, может помочь снизить риск.
Когда мне следует позвонить своему врачу?
Кровь в рвоте или стуле – серьезный симптом, требующий неотложной медицинской помощи. Если вы заметили какие-либо симптомы слезы Мэллори-Вейсса, позвоните своему врачу. сразу.
Ключевые моменты о Мэллори-Вайсе рвать
- Слеза Мэллори-Вейсса – это разрыв ткани нижней части пищевода.
- Чаще всего это вызвано сильным кашлем или рвотой.
- Слезу Мэллори-Вейсса можно диагностировать и лечить во время эндоскопической процедуры.
- Если разрыв не лечить, это может привести к анемии, утомляемости, одышке и даже шок.
Следующие шаги
Советы, которые помогут вам получить максимальную пользу от посещения вашего врача провайдер:
- Знайте причину вашего визита и то, что вы хотите.
- Перед визитом запишите вопросы, на которые хотите получить ответы.
- Возьмите с собой кого-нибудь, кто поможет вам задать вопросы и запомнить что вам говорит ваш провайдер.
- При посещении запишите название нового диагноза и любого нового диагноза. лекарства, лечение или тесты. Также запишите все новые инструкции вашего провайдера дает тебе.
- Узнайте, почему прописано новое лекарство или лечение и как это сделать. Вам поможет. Также знайте, каковы побочные эффекты.
- Спросите, можно ли вылечить ваше состояние другими способами.
- Знайте, почему рекомендуется тест или процедура и каковы результаты может означать.
- Знайте, чего ожидать, если вы не примете лекарство или тест или процедура.
- Если у вас назначена повторная встреча, запишите дату, время, и цель этого визита.
- Знайте, как вы можете связаться со своим провайдером, если у вас есть вопросы.
Медицинский обозреватель: Джен Лерер, доктор медицины
Медицинский обозреватель: Рональд Карлин, доктор медицины
Медицинский обозреватель: Раймонд Кент Терли BSN MSN RN
© 2000-2021 Компания StayWell, LLC. Все права защищены. Эта информация не предназначена для замены профессиональной медицинской помощи. Всегда следуйте инструкциям лечащего врача.
Не то, что вы ищете?Синдром Мэллори-Вейсса | Сидарс-Синай
Не то, что вы ищете?Обзор
Синдром Мэллори-Вейсса – это состояние, при котором внутренняя оболочка пищевода разрывается в месте соединения с желудком или рядом с ним.
Симптомы
У человека с этим заболеванием будет рвота кровью или черный липкий стул после периодов рвоты, рвоты или кашля.
При наличии этих симптомов следует немедленно обратиться за медицинской помощью.
Причины и факторы рискаСиндром Мэллори-Вейсса может быть вызван сильным кашлем, рвотой или рвотой.
Диагностика
Для постановки диагноза врач обычно выполняет эндоскопию верхних отделов ЖКТ, чтобы увидеть место кровотечения.
Лечение
В большинстве случаев это состояние останавливает кровотечение и излечивается без специальной терапии. Если кровотечение не прекращается, для его лечения можно использовать:
- Инъекционная терапия проводится путем введения иглы через эндоскоп в точку рядом с местом кровотечения. Чтобы остановить кровотечение, вводят адреналин, который закрывает кровеносные сосуды.
- Коагуляционная терапия проводится путем пропускания специального зонда, который нагревается через эндоскоп, к участку, чтобы остановить кровотечение.
- Артериография – это специальный рентгеновский тест, который позволяет врачам увидеть артерии. Тонкий катетер вводится в артерию, где предполагается кровотечение. Во время рентгена в него вводят специальный краситель. После выявления кровоточащей артерии кровотечение останавливают. Это делается путем инъекции ваопрессина, препарата, который закрывает кровеносные сосуды, или вещества, закупоривающего артерию.
В редких случаях для лечения этих слез может потребоваться хирургическое вмешательство.
© 2000-2021 Компания StayWell, LLC.Все права защищены. Эта информация не предназначена для замены профессиональной медицинской помощи. Всегда следуйте инструкциям лечащего врача.
Не то, что вы ищете?Синдром Мэллори-Вейсса: история вопроса, патофизиология, эпидемиология
Автор
Кармен Каффари, доктор медицины Доцент кафедры педиатрии, отделение гастроэнтерологии / питания, Медицинская школа университета Джона Хопкинса
Кармен Каффари, доктор медицины, является членом следующих медицинских обществ: Американский колледж гастроэнтерологии, Американская гастроэнтерологическая ассоциация, Североамериканское общество детской гастроэнтерологии, гепатологии и питания, Королевский колледж врачей и хирургов Канады
Раскрытие информации: получил гонорары от лабораторий Прометея за выступления и обучение; Получал гонорары от Abbott Nutritionals за выступления и преподавание.для: Abbott Nutritional, Abbvie, спикеры.
Специальная редакционная коллегия
Мэри Л. Виндл, PharmD Адъюнкт-профессор фармацевтического колледжа Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: нечего раскрывать.
B UK Li, MD Профессор педиатрии, отделение гастроэнтерологии, гепатологии и питания, Медицинский колледж Висконсина; Лечащий гастроэнтеролог, директор программы циклической рвоты, Детская больница Висконсина
B Великобритания Ли, доктор медицинских наук, является членом следующих медицинских обществ: Alpha Omega Alpha, Американская гастроэнтерологическая ассоциация, Североамериканское общество детской гастроэнтерологии, гепатологии и питания
Раскрытие информации : Нечего раскрывать.
Главный редактор
Кармен Каффари, доктор медицины Доцент кафедры педиатрии, отделение гастроэнтерологии / питания, Медицинская школа университета Джона Хопкинса
Кармен Каффари, доктор медицины, является членом следующих медицинских обществ: Американский колледж гастроэнтерологии, Американская гастроэнтерологическая ассоциация, Североамериканское общество детской гастроэнтерологии, гепатологии и питания, Королевский колледж врачей и хирургов Канады
Раскрытие информации: получил гонорары от лабораторий Прометея за выступления и обучение; Получал гонорары от Abbott Nutritionals за выступления и преподавание.для: Abbott Nutritional, Abbvie, спикеры.
Дополнительные участники
Эрик С. Маллер, доктор медицины
Эрик С. Маллер, доктор медицины, является членом следующих медицинских обществ: Американской ассоциации по изучению заболеваний печени, Американской гастроэнтерологической ассоциации, Американского общества хирургов-трансплантологов, Североамериканского общества детской гастроэнтерологии, Гепатология и питание
Раскрытие информации: раскрывать нечего.
Благодарности
Авторы и редакторы Medscape Reference выражают признательность предыдущему автору Крису Льякурасу, доктору медицины, за вклад в первоначальное написание и разработку этой статьи.
Синдром Мэллори-Вейсса – StatPearls
Непрерывное образование
Синдром Мэллори-Вейсса является одной из частых причин острого кровотечения из верхних отделов желудочно-кишечного тракта и характеризуется наличием продольных поверхностных разрывов слизистой оболочки (слезы Мэллори-Вейсса).Эти разрывы возникают в основном в области пищеводно-желудочного перехода и могут распространяться проксимально, затрагивая нижнюю и среднюю часть пищевода, или дистально, затрагивая проксимальную часть желудка. В этом упражнении рассматриваются этиология, патогенез, оценка и лечение синдрома Мэллори-Вейсса, а также подчеркивается роль межпрофессиональной группы в оценке и лечении пациентов с этим состоянием.
Цели:
Определить этиологию синдрома Мэллори-Вейсса.
Опишите результаты обследования, соответствующие синдрому Мэллори-Вейсса.
Опишите доступные варианты лечения и ведения при синдроме Мэллори-Вейсса.
Объясните стратегии межпрофессиональной команды для улучшения координации помощи и коммуникации для улучшения результатов для пациентов, страдающих синдромом Мэллори-Вейсса.
Введение
Синдром Мэллори-Вейсса (MWS) – одна из частых причин острого кровотечения из верхних отделов желудочно-кишечного тракта (ЖКТ), характеризующаяся наличием продольных поверхностных разрывов слизистой оболочки (слезы Мэллори-Вейсса).Эти разрывы возникают в основном в области пищеводно-желудочного перехода; они могут распространяться проксимально, затрагивая нижнюю или даже среднюю часть пищевода, и иногда распространяться дистально, затрагивая проксимальную часть желудка.
Хотя Альберс впервые сообщил об изъязвлении нижних отделов пищевода в 1833 году, Кеннет Мэллори и Сома Вайс в 1929 году более точно описали это состояние как разрывы нижних отделов пищевода (а не язвы), возникающие у пациентов с повторяющейся сильной рвотой и рвотой после чрезмерного употребления алкоголя.[1]
Диагноз MWS обычно подтверждается с помощью эндоскопии. Есть только разрыв слизистой оболочки около соединения ГЭ. Средняя длина разрыва составляет около 2–4 см, и у большинства пациентов имеется только одна разрыва. разрыв находится прямо под соединением GE на малой кривизне.
Этиология
Употребление большого количества алкоголя считается одним из наиболее важных предрасполагающих факторов, поскольку примерно от 50% до 70% пациентов с диагнозом синдрома Мэллори-Вейсса имеют такую же историю.[2] Сообщается, что тяжесть кровотечения из верхних отделов ЖКТ при синдроме Мэллори-Вейсса выше при одновременном наличии портальной гипертензии и варикозного расширения вен пищевода.
Взаимосвязь между грыжей пищеводного отверстия диафрагмы (выпячивание органа, обычно верхней части желудка в грудную полость через пищеводное отверстие диафрагмы) и синдромом Мэллори-Вейсса до сих пор остается предметом дискуссий. Грыжа пищеводного отверстия диафрагмы была обнаружена в значительном количестве случаев с синдромом Мэллори-Вейсса, в то время как исследование случай-контроль, проведенное в клинике Мэйо во Флориде, не обнаружило разницы в частоте возникновения грыжи пищеводного отверстия диафрагмы между пациентами с синдромом Мэллори-Вейсса и контрольной группой. группа.[3]
К другим факторам риска относятся нервная булимия, гиперемезис беременных и гастроэзофагеальная рефлюксная болезнь (ГЭРБ). Все эти состояния включают регургитацию желудочного содержимого в пищевод. Однако у значительного числа пациентов (около 25% случаев) ни один из перечисленных выше факторов риска не был выявлен.
Состояние усугубляется повторяющимися актами внезапного повышения внутрибрюшного давления, такими как рвота, рвота, натуживание, кашель, сердечно-легочная реанимация (СЛР) или тупые травмы живота.
Ятрогенный синдром Мэллори-Вейсса обычно встречается редко. Однако это может произойти как осложнение инвазивных процедур, таких как эндоскопия верхних отделов желудочно-кишечного тракта или трансэзофагеальная эхокардиография (TEE). [4] Эндоскопия верхних отделов желудочно-кишечного тракта как таковая имеет лишь от 0,07% до 0,49% осложнений, приводящих к развитию синдрома Мэллори-Вейсса, и, следовательно, риск невелик.
Эпидемиология
MWS составляет от 1% до 15% причин кровотечений из верхних отделов ЖКТ у взрослых и менее 5% у детей в США.Возраст наибольшей заболеваемости – от 40 до 60 лет [5]. Вероятность развития синдрома Мэллори-Вейсса у мужчин в 2-4 раза выше, чем у женщин, по неясным причинам. Гиперемезис является частой этиологией синдрома Мэллори-Вейсса у молодых женщин, поэтому у таких пациенток следует рассмотреть возможность тестирования на беременность.
Патофизиология
Точный механизм, с помощью которого возникают слезы Мэллори-Вейсса, до сих пор неизвестен. Предлагаемая теория заключается в том, что когда внутрибрюшное давление внезапно и резко увеличивается (как в случаях сильной рвоты и рвоты), содержимое желудка под давлением устремляется проксимально в пищевод.Это избыточное давление содержимого желудка приводит к продольным разрывам слизистой оболочки, которые могут проникать глубоко в подслизистые артерии и вены, что приводит к кровотечению из верхних отделов желудочно-кишечного тракта. Эти разрывы имеют тенденцию быть продольными, а не окружными, возможно, из-за цилиндрической формы пищевода и желудка. [6]
Анамнез и физическое состояние
В легких случаях заболевание может протекать бессимптомно. В 85% случаев проявляющимся симптомом является гематемезис. Количество крови варьируется; от слизи с прожилками крови до массивного ярко-красного кровотечения.
В случае сильного кровотечения могут проявиться другие симптомы, такие как мелена, головокружение или обморок. Боль в эпигастрии обычно присутствует и указывает на наличие предрасполагающего фактора, такого как гастроэзофагеальная рефлюксная болезнь (ГЭРБ).
Нет никаких физических признаков, специфичных для синдрома Мэллори-Вейсса, и признаки аналогичны любым другим геморрагическим состояниям или шоку. Во время медицинского осмотра врачи должны проверить признаки сильного кровотечения и шока, включая, помимо прочего, тахикардию, нитевидный пульс, гипотонию, обезвоживание, снижение тургора кожи и время наполнения капилляров, и немедленно вмешаться, если они есть.При ректальном исследовании обнаружены признаки мелены.
Оценка
При обращении все пациенты с гематемезисом должны получить немедленное внимание и надлежащую помощь. После сбора анамнеза и проведения физикального обследования их следует отсортировать по степени тяжести кровотечения. У некоторых пациентов может быть значительное внутреннее кровотечение, поэтому жизненно важны надлежащий сбор анамнеза и обследование на предмет признаков шока. Лабораторные тесты включают полный анализ крови (CBC), гемоглобин и гематокрит, профиль коагуляции (время кровотечения, протромбиновое время, частичное тромбопластиновое время и количество тромбоцитов).Хронический алкоголизм приводит к снижению количества тромбоцитов.
Лабораторные тесты должны также включать функции почек, чтобы распознать почечную недостаточность путем измерения азота мочевины крови (АМК) и креатинина. Наличие почечной недостаточности, скорее всего, связано с преренальной азотемией, если у пациента ранее не было сопутствующего хронического заболевания почек. Также важно исключить ишемию или инфаркт миокарда путем измерения сердечных ферментов и выполнения прикроватной электрокардиограммы (ЭКГ).
Эндоскопия верхних отделов желудочно-кишечного тракта – это золотой стандарт для окончательной диагностики слезы Мэллори Вейсса и лечения простого активного кровотечения из пищевода.Это может свидетельствовать об активном кровотечении, сгустке или фибриновой корке над слезой. В большинстве случаев одиночный линейный разрыв, обнаруживаемый в проксимальной части малой кривизны желудка чуть ниже кардии, подтверждает диагноз. Эндоскопия верхних отделов желудочно-кишечного тракта также полезна для выявления других причин кровотечения, в том числе варикозного расширения вен пищевода, язвы желудка или двенадцатиперстной кишки. Большинство слез Мэллори Вайсс имеют длину около дюйма.
Следует избегать исследований бария из-за их низкой диагностической ценности и их влияния на эндоскопический диагноз.
Ангиография показана при активно кровоточащих слезах в случае неудачи или недоступности эндоскопии для определения места кровоточащей слезы и остановки кровотечения.
Лечение / ведение
Поскольку синдром Мэллори-Вейсса в основном купируется самостоятельно и рецидивы редки, первоначальное лечение направлено на стабилизацию общего состояния пациента, и для большинства пациентов будет уместен консервативный подход.
Немедленная реанимация пациентов с активным кровотечением должна быть начата при поступлении.Мы оцениваем гемодинамическую стабильность, проверяя дыхательные пути, дыхание и кровообращение (протокол ABC). Создание хорошего центрального или периферического внутривенного (IV) доступа (обычно 2 линии) вместе с восполнением жидкости может спасти жизнь пациентам с тяжелым кровотечением. Инфузия упакованных эритроцитов показана, если уровень гемоглобина ниже 8 г / дл, или если у пациента есть признаки шока или сильного кровотечения.
Назогастральная декомпрессия с использованием назогастрального зонда может быть выполнена, особенно у пациентов с подозрением на сопутствующее варикозное расширение вен пищевода, перед промыванием желудка.Электролитный дисбаланс, если он присутствует, следует исправить соответствующим образом. Перед проведением эндоскопии необходимо оптимизировать факторы свертывания крови. Большинство пациентов, которым ведется консервативное лечение, обычно госпитализируются до тех пор, пока не будет достигнут гемостаз и не исчезнут симптомы.
Фармакологическое лечение
Ингибиторы протонной помпы (ИПП) и блокаторы h3 назначаются для снижения кислотности желудочного сока, поскольку повышенная кислотность препятствует восстановлению слизистой оболочки желудка и пищевода. Первоначально внутривенные ИПП вводятся пациентам, которым предстоит пройти эндоскопическое обследование.Для контроля тошноты и рвоты назначают противорвотные средства, такие как прометазин и ондансетрон.
Эндоскопическое лечение
Эзофагогастроскопия – это исследование выбора во всех случаях кровотечения из верхних отделов ЖКТ [7]. Если кровотечение уже остановилось на момент эндоскопии, дальнейшее вмешательство, как правило, не требуется. В ситуациях с продолжающимся активным или повторяющимся кровотечением существуют разные методы эндоскопического лечения. Местная инъекция адреналина (разведение от 1: 10 000 до 1: 20 000) останавливает кровотечение из-за сужения сосудов.[8] [9] Мультиполярная электрокоагуляция (MPEC), инъекция склерозирующего агента, аргоноплазменная коагуляция (APC) или эндоскопическая перевязка – это другие варианты в таких ситуациях.
Ангиотерапия
Ангиография с инъекцией сосудосуживающего агента, такого как вазопрессин, или транскатетерная эмболизация с гелевой пеной для облитерации левого желудка или верхней брыжеечной артерии рассматривается, когда эндоскопия недоступна или не удалась [10].
Хирургическое лечение
Хирургическое вмешательство требуется редко и считается необходимым после неудачи эндоскопических процедур или ангиотерапии для остановки кровотечения.Лапароскопическое ушивание разрыва под эндоскопическим контролем было выполнено с отличными результатами. [11]
Сжатие трубки Сенгстакена-Блейкмора является последним средством лечения кровоточащей слезы Мэллори-Вейсса у ослабленных пациентов. [5] Это наименее предпочтительный вариант, поскольку кровотечение в основном артериальное и давления в баллоне недостаточно для преодоления давления в кровоточащей артерии.
Дифференциальный диагноз
Синдром Мэллори Вейсса следует дифференцировать от других причин кровотечения из верхних отделов ЖКТ;
Синдром Бурхааве: Тяжелое состояние, которое имеет те же предрасполагающие факторы, что и синдром Мэллори-Вейсса, но патологией является перфорация пищевода
Язвенная болезнь: Язвенная болезнь является наиболее частой причиной кровотечение из верхних отделов ЖКТ.Он имеет характерную клиническую картину и окончательно диагностируется при эндоскопии.
Новообразование пищевода или желудка
Варикозное расширение вен пищевода: Расширенные извилистые сосуды вокруг нижней части пищевода, в основном как осложнение портальной гипертензии. Варикозное расширение вен пищевода также может сосуществовать с синдромом Мэллори Вейсса.
Артериовенозные мальформации
Прогноз
Для большинства пациентов результаты хорошие.У большинства пациентов кровотечение обычно прекращается самопроизвольно, и слеза заживает в течение 72 часов. Степень кровопотери варьируется, но переливание крови не является обычным явлением.
Осложнения
Осложнения связаны со степенью кровопотери, например гиповолемический шок, метаболические нарушения и инфаркт миокарда. [12] Смерть наступает, если кровотечение не остановить. Перфорация пищевода и рецидивы при синдроме Мэллори Вейсса – редкие осложнения.
Сдерживание и обучение пациентов
Хотя это состояние не очень распространено, пациенты должны знать об опасностях чрезмерного употребления алкоголя, включая слезы Мэллори Вайса.Важно консультировать пациентов с предыдущими эпизодами гематемезиса, чтобы избежать провоцирующих факторов, которые приводят к разрыву пищевода, несмотря на редкость рецидивов.
Улучшение результатов команды здравоохранения
Слеза Мэллори Вайсс – не редкость, и ее диагностика может быть затруднена без эндоскопии. Состояние может быть пугающим из-за крови, но большинству пациентов требуется только консервативный уход.
Сотрудничество и эффективное общение с другими вспомогательными медицинскими бригадами имеют решающее значение для обеспечения безупречного обслуживания пациентов.При необходимости следует надлежащим образом получать консультации гастроэнтеролога, интервенционной радиологии и хирурга, чтобы выбрать наилучшие варианты лечения и обеспечить стабильность гемодинамики. Лучший подход, который приведет к наиболее благоприятным результатам, включает скоординированную межпрофессиональную команду, состоящую из медсестер, первичного звена и специалистов. Медсестры должны внимательно следить за этими пациентами, так как у некоторых может развиться гипотензия, продолжающееся кровотечение и шок. Ключ к успеху – агрессивная гидратация. Пациенты нуждаются в тщательном наблюдении, поскольку в редких случаях может наблюдаться перфорация желудка, что требует хирургического вмешательства.Тесное общение между членами команды жизненно важно для достижения лучших результатов.
Состояние, как правило, купируется самостоятельно, и примерно в 90% случаев требуется только консервативное лечение. [5] Заживление слезы происходит спонтанно при консервативном лечении в течение 48-72 часов. Рецидив маловероятен. Смертность от синдрома Мэллори Вейсса значительно снизилась благодаря недавним достижениям в лечении острого кровотечения и шока.
Дополнительное образование / Контрольные вопросы
Рисунок
Слеза Мэллори Вайс.Изображение предоставлено S Bhimji MD
Рисунок
Слеза Мэллори Вайсс. Предоставлено Викимедиа Пользователь: Самир (CC BY-SA 3.0 https://creativecommons.org/licenses/by-sa/3.0/)
Ссылки
- 1.
- Carr JC. Синдром Мэллори-Вейсса. Clin Radiol. 1973 Январь; 24 (1): 107-12. [PubMed: 4579296]
- 2.
- Кортас Д.Ю., Хаас Л.С., Симпсон В.Г., Никл, штат Нью-Джерси, Гейтс Л.К. Слеза Мэллори-Вейсса: предрасполагающие факторы и предикторы осложненного течения. Am J Gastroenterol.2001 Октябрь; 96 (10): 2863-5. [PubMed: 11693318]
- 3.
- Corral JE, Keihanian T., Kröner PT, Dauer R, Lukens FJ, Sussman DA. Синдром Мэллори Вейсса не связан с грыжей пищеводного отверстия диафрагмы: согласованное исследование случай-контроль. Сканд Дж Гастроэнтерол. 2017 Апрель; 52 (4): 462-464. [PubMed: 28007004]
- 4.
- Montalvo RD, Lee M. Ретроспективный анализ ятрогенных разрывов Мэллори-Вейсса, возникающих во время эндоскопии верхних отделов желудочно-кишечного тракта. Гепатогастроэнтерология. 1996 январь-февраль; 43 (7): 174-7.[PubMed: 8682458]
- 5.
- Sugawa C, Benishek D, Walt AJ. Синдром Мэллори-Вейсса. Обследовано 224 пациента. Am J Surg. 1983 Янв; 145 (1): 30-3. [PubMed: 6600377]
- 6.
- Чередников Е.Ф., Кунин А.А., Чередников Е.Е., Моисеева Н.С. Роль этиопатогенетических аспектов в прогнозировании и профилактике прерывисто-геморрагического синдрома (Мэллори-Вейсса). EPMA J. 2016; 7: 7. [Бесплатная статья PMC: PMC4799841] [PubMed: 26998186]
- 7.
- Hastings PR, Peters KW, Cohn I.Синдром Мэллори-Вейсса. Рассмотрение 69 дел. Am J Surg. 1981 ноя; 142 (5): 560-2. [PubMed: 7304810]
- 8.
- Ллах Дж., Элизальде Дж. И., Гевара М. С., Пеллисе М., Кастелло А., Жинес А., Сориа М. Т., Бордас Дж. М., Пике Дж. М.. Эндоскопическая инъекционная терапия при синдроме Мэллори-Вейсса при кровотечении: рандомизированное контролируемое исследование. Gastrointest Endosc. 2001 декабрь; 54 (6): 679-81. [PubMed: 11726841]
- 9.
- Gawrieh S, Shaker R. Лечение активно кровоточащего синдрома Мэллори-Вейсса: инъекция адреналина или перевязка бандажа? Curr Gastroenterol Rep.2005 июн; 7 (3): 175. [PubMed: 15913474]
- 10.
- Pezzulli FA, Purnell FM, Dillon EH. Синдром Мэллори-Вейсса. Отчет о клиническом случае и обновленная информация об эмболизации по сравнению с результатами внутриартериального вазопрессина. N Y State J Med. 1986 июнь; 86 (6): 312-4. [PubMed: 3461335]
- 11.
- Китано С., Уэно К., Хашизуме М., Охта М., Томикава М., Сугимачи К. Лапароскопическое ушивание кровоточащей слезы Мэллори-Вейсса под эндоскопическим контролем. Surg Endosc. 1993 сентябрь-октябрь; 7 (5): 445-6. [PubMed: 8211627]
- 12.
- Стивенс П.Д., Лебволь О. Неотложная гипертоническая болезнь и желудочковая тахикардия после эндоскопической инъекции адреналина слезе Мэллори-Вейсса. Gastrointest Endosc. 1994, январь-февраль; 40 (1): 77-8. [PubMed: 8163143]
Синдром Мэллори-Вейсса | Рвота кровью
Что такое синдром Мэллори-Вейсса?
Синдром Мэллори-Вейса (также называемый слезой Мэллори-Вейсса) – это название, данное кровотечению и другим симптомам, вызванным разрывом слизистой оболочки верхней части кишечника (желудочно-кишечного тракта).Верхняя кишка состоит из пищевода, желудка и двенадцатиперстной кишки.
Разрыв обычно происходит в одном из двух конкретных мест верхней кишки:
- Гастроэзофагеальное соединение – часть верхней кишки, где пищевод соединяется с желудком; или
- Внутри слизистой оболочки верхней части желудка.
Синдром Мэллори-Вейсса впервые был описан в 1929 году двумя докторами по имени Мэллори и Вайс. Они заметили это у людей, у которых рвота и тошнота (рвота) после употребления алкоголя.
Что вызывает синдром Мэллори-Вейсса и у кого он возникает?
Разрыв слизистой оболочки кишечника, возникающий при синдроме Мэллори-Вейсса, может быть вызван чем угодно, что приводит к внезапному повышению давления в желудке или нижней части пищевода (пищевода). У большинства людей это вызвано повторяющейся рвотой и тошнотой (рвотой) по какой-либо причине. Реже это происходит из-за сильного кашля, икоты, чрезмерного натуживания или подъема тяжестей. Иногда очевидную причину разрыва не удается найти.
Проблема, как правило, затрагивает людей в возрасте от 30 до 50 лет, хотя может возникнуть в любом возрасте. Это чаще встречается у мужчин, чем у женщин, а также у людей с грыжей пищеводного отверстия диафрагмы. (Грыжа пищеводного отверстия диафрагмы возникает, когда часть желудка проталкивается вверх в нижнюю часть грудной клетки из-за слабости диафрагмы – большой плоской мышцы, которая находится между легкими и областью живота. Более подробную информацию см. В отдельной брошюре под названием Hiatus Hernia.)
Повторяющаяся рвота и рвота после запоя, из-за тяжелого утреннего недомогания во время беременности или из-за нервной булимии (эпизоды переедания с последующей самоиндуцированной рвотой) являются одними из наиболее частых причин синдрома Мэллори-Вейсса.Однако любое состояние, вызывающее рвоту или кашель, может вызвать появление слезы.
Каковы симптомы синдрома Мэллори-Вейсса?
У большинства людей с синдромом Мэллори-Вейса возникает рвота с выделением ярко-красной крови. Это часто происходит после приступа обычной рвоты или рвоты. Количество кровотечений (и, как следствие, рвоты кровью) варьируется от человека к человеку. У большинства людей кровотечение незначительное, но иногда может быть потеряно много крови.
Реже стул (фекалии) может стать темно-черным или дегтеобразным по цвету и иметь сильный запах. Это вызвано тем, что кровь из разрыва в верхней части кишечника проходит через нижнюю часть кишечника и выводится вместе со стулом. Когда кровь проходит через кишечник, она частично переваривается, поэтому цвет меняется с ярко-красного на черный. Если сильное кровотечение происходит в верхней части кишечника, ярко-красная кровь может проходить через задний проход (прямую кишку). У крови нет времени на переваривание, поэтому цвет не меняется.
Некоторые люди с синдромом Мэллори-Вейсса испытывают боль в верхней части живота (живота). Они также могут чувствовать головокружение и головокружение из-за потери крови. В случае сильного кровотечения человек может сильно заболеть и потерять сознание.
Примечание : есть много других состояний, которые могут привести к рвоте с кровью. Например, язва желудка, воспаление желудка (гастрит) или воспаление пищевода (пищевода). См. Дополнительную информацию в отдельной брошюре «Рвота кровью (гематемезис)».Синдром Мэллори-Вейсса является причиной кровотечения из верхней части кишечника примерно в 5 из 100 случаев. Если вы испытываете какие-либо из вышеперечисленных симптомов, важно срочно обратиться за медицинской помощью.
Как диагностируется синдром Мэллори-Вейсса?
Синдром Мэллори-Вейсса обычно диагностируется при гастроскопии (эндоскопии).
Гастроскопия – это тест, при котором оператор (врач или медсестра) изучает верхнюю часть кишечника с помощью эндоскопа. Поэтому обследование иногда называют эндоскопией.Эндоскоп – это тонкий гибкий телескоп. Толщина его примерно с мизинец. Эндоскоп вводится через рот в пищевод (пищевод) вниз по направлению к желудку и двенадцатиперстной кишке. Наконечник эндоскопа содержит свет и крошечную видеокамеру, чтобы оператор мог видеть внутреннюю часть кишечника. Эндоскоп также имеет боковой канал, по которому могут проходить различные инструменты. С ними может работать оператор.
Для получения дополнительной информации см. Отдельную брошюру «Гастроскопия (эндоскопия)».
Гастроскопия позволяет оператору увидеть, присутствует ли разрыв Мэллори-Вейсса в слизистой оболочке кишечника, а также его местоположение. Они также смогут увидеть, кровоточит ли по-прежнему слеза.
Эндоскопическое изображение слезы Мэллори-Вейсса
Самир [CC BY-SA 3.0 (https://creativecommons.org/licenses/by-sa/3.0)], через Wikimedia Commons
Что такое лечение Мэллори- Синдром Вайса?
Первое, что сделают врачи и медсестры при подозрении на синдром Мэллори-Вейсса, – это убедиться, что состояние пациента стабильно.Если было потеряно много крови, жидкость можно вводить в вены (внутривенно). Иногда может потребоваться переливание крови. Будет внимательно наблюдаться артериальное давление и частота пульса, чтобы медицинский персонал мог проверить реакцию на любое лечение.
Обычно будут сданы анализы крови. Например, чтобы проверить наличие анемии (чтобы узнать, сколько крови было потеряно из-за кровотечения) и проверить, нормально ли свертывается кровь. Могут быть назначены лекарства для облегчения симптомов плохого самочувствия (тошнота) или тошноты (рвота).
Иногда люди, у которых нет признаков продолжающегося кровотечения и состояние которых стабильно, могут не быть госпитализированы. Вместо этого они могут наблюдаться амбулаторно.
Что произойдет дальше, будет зависеть от того, будет ли по-прежнему кровоточить слеза Мэллори-Вейсса при проведении гастроскопии. Примечание : во многих случаях кровотечение останавливается к моменту проведения гастроскопии.
Если слеза Мэллори-Вейсс все еще кровоточит
Если слеза все еще кровоточит, лечение для остановки кровотечения обычно проводится во время гастроскопии.Доступен ряд различных процедур. Например:
- Разрыв можно исправить или закрыть с помощью специальных металлических зажимов, пропущенных через боковой канал, чтобы остановить кровотечение. Это называется кровотечением.
- Повязку можно использовать для перевязки кровоточащего кровеносного сосуда. Это называется перевязкой.
- Нагревательный зонд можно пропустить по боковому каналу эндоскопа, чтобы направить источник тепла на кровоточащие кровеносные сосуды и остановить кровотечение.
- Адреналин (адреналин) можно ввести вокруг точки кровотечения.Это лекарство вызывает закрытие (сужение) кровоточащих кровеносных сосудов. Таким образом можно остановить кровотечение. Опять же, для этого используется боковой канал эндоскопа.
Иногда используется комбинация методов лечения.
Очень редко вышеуказанные методы лечения не останавливают кровотечение. В этом случае может использоваться процедура, известная как ангиография с эмболизацией. В кровоток вводится специальный краситель и делается рентген. Эти рентгеновские лучи показывают кровеносные сосуды (так называемая ангиография).Таким образом, врачи могут увидеть, откуда исходит кровотечение. Затем в кровоточащий кровеносный сосуд вводится вещество, чтобы остановить кровотечение или вызвать закупорку (сгусток), чтобы он закрылся (так называемая эмболизация).
В редких случаях для лечения синдрома Мэллори-Вейсса требуется хирургическое вмешательство, если другие методы лечения не смогли остановить кровотечение. Разрыв зашивается (закрывается) хирургом.
Если слезы Мэллори-Вейсса перестали кровоточить
Если обнаруживается, что кровотечение из слезы прекратилось к моменту проведения гастроскопии, то специального лечения может не потребоваться.Слеза должна зажить сама по себе. За человеком можно наблюдать в больнице в течение определенного периода времени, чтобы врачи и медсестры могли внимательно следить за ним, чтобы гарантировать, что кровотечение не вернется (не возобновится). Для заживления слезы могут быть назначены лекарства, подавляющие кислотность желудка.
Каковы перспективы синдрома Мэллори-Вейсса?
Перспективы (прогноз) в целом очень хорошие.

 Для осмотра, тонкая трубка, оборудована эндоскопом, осторожно проталкивается в пищевод. Врач будет иметь возможность видеть все части пищевода с помощью камеры, подключенной к эндоскопу.
Для осмотра, тонкая трубка, оборудована эндоскопом, осторожно проталкивается в пищевод. Врач будет иметь возможность видеть все части пищевода с помощью камеры, подключенной к эндоскопу.