Неоплазия желудка: Опухоль желудка: симптомы доброкачественной и злокачественной
Полный текст статьи:
Парижская классификация опухолевых поражений
В предлагаемом фрагменте Парижской эндоскопической классификации (перевод Ефимовой Е.И.), представлены основные положения, терминология, формулировки и принципы эндоскопической диагностики поверхностных эпителиальных опухолей желудочно-кишечного тракта.
В 2002 году в Париже прошел рабочий семинар международной группы эндоскопистов, хирургов, и патологоанатомов по изучению клинической значимости и пользы японской эндоскопической классификации поверхностных опухолевых поражений желудочно-кишечного тракта.
В пищеводе, желудке и толстой кишке опухолевые поражения предложено называть «поверхностными» при эндоскопическом выявлении ранних раков или неинвазивных опухолевых поражений (дисплазия/ аденома).
При инвазивных поражениях «поверхностной» опухоли соответствует стадия T1 TNM классификации, в которой инвазия ограничена СО и подслизистым слоем.
«Поверхностные» опухоли не вызывают обструкции органа, как правило, протекают бессимптомно, и часто обнаруживаются случайно или при проведении скрининга.
В Японии опухолевые поражения желудка, имеющие эндоскопический внешний вид «поверхностных», классифицируются как подтип «типа 0». Термин «тип 0» был выбран для выделения классификации «поверхностных» поражений из классификации Borrmann, предложенной в 1926 году для «прогрессирующих» опухолей желудка (включает типы 1–4).
В типе 0 различают полиповидный и неполиповидный подтипы (рис. 1):
Неполиповидный подтип включает поражения
- с небольшими изменениями поверхности (слегка приподнятые (0-IIa), плоские (0-IIb), слегка вдавленные – углубленные (0-IIc)) и
- подрытые (язвенные) поражения (0-III).
Японская ассоциация рака желудка (JGCA) также добавила тип 5 для неклассифицируемых прогрессирующих опухолей.
В итоге полная модификация эндоскопической классификации для опухоли желудка выглядит следующим образом:
- тип 0 – поверхностные полиповидные, плоские/углубленные или подрытые опухоли;
- тип 1 – полиповидный рак, как правило, на широком основании;
- тип 2 – язвенная форма рака с четкими границами и приподнятыми краями;
- тип 3 – язвенно-инфильтративная форма рака без определенных границ;
- тип 4 – неязвенная, диффузная инфильтративная форма рака;
- тип 5 – неклассифицируемый прогрессирующий рак.
Таким образом, макроскопические формы РЖ делятся в классификации JGCA
Классификация «поверхностных» неоплазий желудка была адаптирована к опухолям пищевода, а позже, когда частота колоректального рака в Японии увеличилась, и для опухолей толстой кишки.
Многие эндоскописты, особенно на Западе, считают японскую классификацию с ее делением для пищевода, желудка и толстой кишки, «ботаническим хобби», слишком сложной для практического применения. Западные эндоскописты основой для принятия решения о лечении считают размер и расположение опухоли, а также гистологическое исследование биопсийного материала.
Тем не менее, японские эндоскописты установили, что данная классификация может быть определяющим фактором в возможности применения эндоскопического лечения.
Для оценки глубины инвазии опухолевого поражения при эндоскопии и выборе тактики дальнейшего лечения может быть использована EUS, а для получения большого образца ткани – EMR. У пациентов с повышенным операционным риском EMR может быть первичным лечением, дополненным по мере необходимости другими методами абляции, такими как электрокоагуляция или фотодинамическая терапия.
Скептицизм в отношении эндоскопической классификации поверхностных неопластических образований поддерживался и различиями в восточной и западной классификациях внутрислизистых поражений. Последняя Венская классификация в некоторой степени разрешила эти различия в использовании терминов «дисплазия», «аденома», «ранний рак» и «распространенный рак». Обратная связь с гистологическими исследованиями имеет решающее значение для развития эндоскопической диагностики в Японии и помогает в непрерывном усовершенствовании эндоскопического исследования.
В отличие от японских специалистов, западным эндоскопистам, как правило, не хватает внимания к деталям в полученной эндоскопической картинке и описании поверхностных поражений. Западные эндоскописты иногда недооценивают значимость и в недостаточной степени используют уточняющие эндоскопические методы, которое могут иметь большое значение в оценке глубины инвазии и принятии решения о методе лечения.
Отличия восточной и западной точки зрения на важность эндоскопического описания возникли во второй половине ХХ века. В Японии высокая частота рака желудка поддерживается его ранним выявлением эндоскопически и двойным контрастным рентгенологическим исследованием. Поскольку плоские образования играют почти исключительную роль в желудочном канцерогенезе, раннее эндоскопическое выявление их нуждается в повышенном внимании и тщательности выполнения эндоскопической процедуры. Дополнительные методы, такие как хромоэндоскопия и увеличение, также были разработаны как вспомогательные для выявления мельчайших поражений.
В Японии подход к ранней диагностике опухолевых поражений пищевода и толстой кишки продолжают по аналогии с желудочным раком. В то время когда японцы были сосредоточены на РЖ, во многих других странах приоритетной была канцер-превенция колоректального рака. И здесь полиповидные образования играют гораздо большую роль в последовательности «полип – рак», установленной Muto, Bussey и Morson в 1975г. Хромоскопия реже используется для полиповидных поражений и детальный эндоскопический анализ внешнего вида полипов менее информативен для прогноза злокачественной инвазии, чем грубая оценка размера или расширения ножки. Таким образом, рутинная хромоэндоскопия при колоноскопии, проводимая для обнаружения аденом, часто считается на Западе малоинформативной. Следовательно, малые неполиповидные (плоские) аденомы (неинвазивная неоплазия) или даже рак могут остаться незамеченными.
В настоящее время точки зрения Востока и Запада сблизились.
Азиатские, европейские и американские патологи внесли предложение о согласительной гистопатологической классификации в трех основных группах внутрислизистых неоплазий:
- неинвазивная низкой степени,
- неинвазивная высокой степени и
- рак с инвазией в собственную пластинку.
Этот консенсус, принятый в Вене, был опубликован в последнем дополнении эндоскопии ЖКТ. Слияние эндоскопической и патологической терминологии позволит использовать преимущества каждой из них. Венская классификация, адаптированная (в частности) к последней классификации распространенных опухолей ВОЗ, была несколько изменена, с улучшенными согласованными оценками и терапевтической значимостью.
ТЕРМИНЫ И ФОРМУЛИРОВКИ
Поверхностные неоплазии при эндоскопии.
Опухолевые поражения называются поверхностными, если по их внешнему виду мы можем предполагать, что инвазия в стенку органа распространяется не глубже подслизистого слоя и нет инфильтрации мышечного слоя.
«Поверхностные»’ неоплазии включают опухолевые поражения без инвазии в собственную пластинку и рак с инвазией в собственную пластинку, ограничивающейся СО (желудок и пищевод) или в подслизистую оболочку (толстая кишка).
Термин «ранний рак» предполагает локализованные опухоли с потенциальной возможностью полного излечения после резекции и низкий риск метастазирования в лимфоузлы.
Неопухолевые поражения толстокишечного эпителия (ювенильные или гиперпластические полипы) также относятся к «поверхностным».
Гиперпластические полипы практически не имеют потенциала для перехода в неопластическое поражение, но зубчатые аденомы являются исключением среди неинвазивных опухолевых поражений, сочетая в себе опухолевые клетки с зубчатой структурой.
В пищеводе неоплазии развиваются в многослойном плоском эпителии или в метаплазированном цилиндрическом эпителии (пищевод Барретта, эктопированные участки железистой СО). Дистальнее пищевода неоплазия развивается в железистой СО желудка. Разделяют опухоли, расположенные в кардии, и опухоли дистальнее кардии (субкардиальные опухоли). Опухоли области пищеводно-желудочного перехода включают аденокарциномы дистальной части пищевода и кардии.
Полиповидные и неполиповидные опухолевые поражения.
Полиповидные опухолевые поражения при эндоскопии выступают над окружающей поверхностью (см. рис. 1). На операционном материале высота образования в два и более раза превышает толщину окружающей СО. У полипов на ножке основание узкое, у сидячих полипов основание и верхушка имеют одинаковый размер (рис. 2).
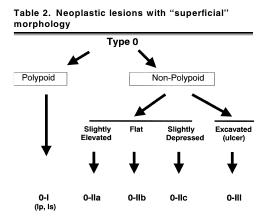
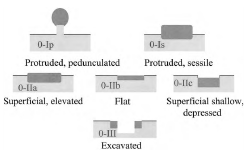 Рисунок 1. Варианты типа 0 опухолевых поражений ЖКТ: полиповидные (Ip и Is), неполиповидные (IIa, IIb и IIc) и подрытые (III).
Рисунок 1. Варианты типа 0 опухолевых поражений ЖКТ: полиповидные (Ip и Is), неполиповидные (IIa, IIb и IIc) и подрытые (III). 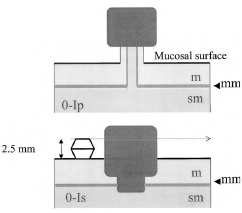
Рисунок 2. Тип 0-I: на ножке (Ip) или сидячие (Is) в поперечном сечении.
Невыступающие, или неполиповидные опухолевые поражения включают язвы и так называемые плоские поражения. В последнем случае поражения находятся на одном уровне с окружающей СО, либо слегка приподняты или углублены (депрессированы) (рис. 3).
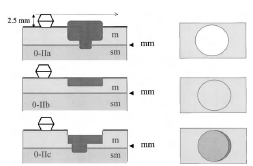
Рисунок 3. Тип 0-II приподнятый (IIa), абсолютно плоский (IIb), углубленный
При эндоскопии слегка приподнятое поражение иногда неправильно классифицируется как сидячее (полиповидный подтип). Это различие выявляется при исследовании операционного материала, в котором можно сравнить высоту образования с толщиной нормальной СО. Некоторые приподнятые поражения могут достигать большого (> 10 мм) диаметра без увеличения их высоты или протрузии над СО. В случае углубленных поражений толщина СО в зоне поражения меньше, чем у окружающей СО. Приподнятые поражения могут иметь центральное углубление. Когда есть незначительное углубление в верхней части приподнятого поражения, которое все же выше, чем окружающая нормальная СО, углубленная часть поражения называется «относительным углублением».
Метаплазия – трансформация эпителия одного типа в эпителий другого типа с отличными морфологическими и функциональными характеристиками.
Кишечная метаплазия в пищеводе и желудке классифицируется как полная (тип I) или неполная (тип II или III).
- Кишечная метаплазия I типа в основном состоит из поглощающих клеток с четко определенными ворсинчатыми границами, некоторого количества бокаловидных клеток, а иногда клеток Панета.
- Для кишечной метаплазии II и III типа характерны цилиндрические промежуточные клетки и бокаловидные клетки, которые выделяют сиаломуцин (тип II) или сульфомуцин (тип III).
В дистальном отделе пищевода метаплазия включает три различных типа эпителия, распространенного мозаично:
кардиальный или переходный тип эпителия, где железы состоят почти полностью из слизеобразующих клеток, кислотопродуцирующего типа эпителия, где преобладают париетальные и главные клетки, и кишечного типа эпителия, который часто называют «специализированной кишечной метаплазией».
В желудке кишечная метаплазия ассоциирована с хроническим гастритом и хеликобактерной инфекцией. В обоих случаях также может быть панкреатическая метаплазия.
Аденома и дисплазия.
В западных странах неинвазивные опухоли и доброкачественные поражения цилиндрического эпителия называются «аденома» при выступающих (полиповидных) поражениях и «дисплазия» при плоских или углубленных поражениях (неполиповидных), хотя термины «плоская аденома» и «углубленная аденома» общеприняты и применимы в большинстве случаев и для дискретных поражений. Неоплазии низкой или высокой степени без инвазии в собственную пластинку также называются аденоматозным или диспластическим эпителием.
В азиатских странах оба вида поражения в желудке или толстой кишке называются «аденома», с разделением на полиповидные, плоские, и углубленные аденомы.
В классификации внутрислизистых неоплазий Венского консенсуса, термины «аденома» и «дисплазия» заменяет термин «интраэпителиальная неоплазия». Внешний вид зоны внутриэпителиальной неоплазии влияет на прогноз; высокий риск развития рака связан с углубленными поражениями.
Термин «рак De Novo» применяется к малым (часто менее 5 мм) плоским или углубленным раковым поражениям, когда нет аденоматозных желез в операционном материале. При этом предполагается, что рак развился не из аденоматозных или диспластических предшественников.
Гистологическая классификация неоплазий.
Согласительная классификация прогрессирующих опухолей в СО пищеварительного тракта была предложена после Венского симпозиума и пересмотрена недавно. Классификация применяется к многослойному плоскому эпителию и железистому эпителию (пищевод Барретта, желудок, толстая кишка). При отсутствии инвазии в собственную пластинку СО неинвазивные опухолевые поражения классифицируются по степени интраэпителиальной неоплазии (ИЭН) на две группы: низкой и высокой степени.
Пересмотренная Венская классификация эпителиальных неоплазий для пищевода, желудка и толстой кишки:
- Отрицательная ИЭН;
- Неопределенная ИЭН;
- ИЭН низкой степени
- Аденома/дисплазия
- ИЭН высокой степени (внутриэпителиальная или внутрислизистая)
- Аденома/дисплазия
- Неинвазивный рак
- Подозрение на инвазивный рак
- Внутрислизистая карцинома (инвазия в собственную пластинку)
- Подслизистый рак
Расхождений в оценке различий между дисплазией низкой степени и неопределенной дисплазией/интраэпителиальной неоплазией, а также между «отрицательной» и «неопределенной» дисплазией/интраэпителиальной неоплазией много, но их гораздо меньше в диагнозе дисплазия высокой степени. Интраэпителиальная неоплазия высокой степени с тяжелыми ядерными изменениями и сложной архитектоникой, соответствующей карциноме, также была названа «рак in situ».
Место разновидностей в терминологии.
В многослойном плоском эпителии пищевода термины «интраэпителиальная неоплазия высокой степени», «интраэпителиальная карцинома» и «рак in situ» эквивалентны. Когда есть инвазия в собственную пластинку СО, повреждение называют микроинвазивным или внутрислизистым раком.
В цилиндрическом эпителии пищевода Барретта, желудка, и толстой кишки, поражения с ИЭН высокой степени и без инвазии в собственную пластинку были названы внутрислизистым раком в Японии и дисплазией высокой степени в западных странах. Большинство этих расхождений исчезает, когда используется Венская согласительная классификация. В пересмотренном варианте классификации поражения, называемые «внутрислизистый рак» на Востоке и тяжелая дисплазия на Западе, стали подразделением одной группы.
Согласительная терминология делает различие между ИЭН высокой степени без инвазии в собственную пластинку и ИЭН высокой степени с инвазией в собственную пластинку. Последняя называется «внутрислизистая карцинома пищевода или желудка». В толстой кишке риск узловой инвазии в этой ситуации равен нулю, и на Западе имеет место тенденция избегать термина «карцинома» для поражений без инвазии в подслизистую оболочку, так как они полностью излечимы при помощи локальной эксцизии. Свыше этой стадии, все неопластические поражения с инвазией в подслизистый слой называются инвазивным раком.
Классификация TNM.
- До начала лечения с помощью диагностических тестов и процедур опухоль стадируется в соответствии с классификацией TNM; глубина инвазии опухоли в стенке кишечника соответствует Т классификации.
- В пищеводе, желудке, и толстой кишке эндоскопист классифицирует изменения «поверхностных» опухолевых поражений (интраэпителиальной неоплазии и рака) как варианты типа 0.
- Патологоанатом классифицирует гистологию опухоли по группам Венской классификации неоплазии.
- Когда доступен оперативный материал, глубина инвазии классифицируется морфологом в соответствии с T- по р-TNM классификации («р» – послеоперационный).
- В пищеводе и желудке интраэпителиальная опухоль без инвазии в собственную пластинку (р-Tis) называется «рак in situ» и не включается в реестры опухоли.
- Интраэпителиальная карцинома с инвазией в собственную пластинку СО называется р-T1m;
- Карцинома с инвазией в подслизистую оболочку – р-T1sm.
В толстой кишке терминов р-Tm и р-Tis, как правило, избегают на Западе, так как они не имеют клинической значимости в отношении выживания, и классифицируются как ИЭН высокой степени.
- Когда есть инвазия в подслизистую оболочку, опухоль определяется как р-T1sm.
Эта двойная гистологическая и TNM классификация представлена в последнем издании ВОЗ.
Таким образом, поверхностный рак в слизистой оболочке ЖКТ будет классифицироваться как
- р-Tis, р-Tm (пищевод, желудок) или
- р-Tsm (пищевод, желудок, толстая кишка).
МЕТОДОЛОГИЯ КЛАССИФИКАЦИИ
Эндоскопический поиск и хромоэндоскопия.
Последние модели видеоэндоскопов отвечают требованиям для получения высококачественного цифрового изображения с соответствующим разрешением, цветопередачей, а также увеличением структуры.
Первый шаг диагностики – выявление областей СО со слегка измененной окраской (более бледной или более красной), нерегулярной микрососудистой сетью или небольших возвышенных или углубленных участков.
Второй шаг диагностики основан на хромоскопии, позволяющей детально описать поражение. Хромоскопия должна быть доступна и выполняться при обнаружении поражения. Рутинное использование эндоскопических красителей для улучшения визуализации очаговых поражений не означает, что окрашивание всей поверхности СО должно быть выполнено в каждом случае. Диффузное (тотальное) окрашивание рекомендовано в случаях высокого риска развития новообразований (например, при семейном колоректальном раке или неспецифическом язвенном колите).
Основным красителем, используемым для многослойного плоского эпителия пищевода, является водный раствор Люголя (1-2%). Опухолевые области остаются неокрашенными (отрицательная окраска), в отличие от темно-коричневой (положительной окраски) нормального эпителия.
Наиболее часто применяемый краситель на измененных участках СО желудка и толстой кишки – индигокармин (0,5% -1% раствор), контрастирует рельеф СО, выделяя повреждения ее целостности, неровности рельефа, нарушения архитектоники.
Хромоскопия с индигокармином помогает различить неопухолевые (гиперпластические) и опухолевые поражения в толстой кишке.
Хромоскопия метиленовым синим обнаруживает очаги КМ в пищеводе и желудке и используется в толстой кишке путем распыления 0,1% раствора посегментно.
В недавнем рандомизированном исследовании эта процедура была применена для наблюдения у пациентов с язвенным колитом. Повысить выявляемость неполипозных опухолевых поражений удалось в группе пациентов, обследованных с применением хромоскопии и увеличительной эндоскопии. Оптическое увеличение было расценено как основной фактор повышения эффективности.
Эндоскопическое применение разбавленной уксусной кислоты предложено в качестве красителя при изучении метапластической слизистой пищевода Барретта.
Видео- и фоторегистрация образований, обнаруженных при эндоскопии, стала доступной с переходом на цифровое оборудование, использующейся в современной эндоскопии. Такие записи оказались полезными при последующих наблюдениях. Выбор наиболее показательных изображений для каждого поражения – обычная практика в Японии. Рутинные записи изображений для всех процедур недавно были включены в руководящие принципы Европейского общества гастроинтестинальной эндоскопии и практикуются во многих учреждениях во всем мире.
Эндоскопическая классификация типа 0.
Во время эндоскопии оценка поверхностных опухолевых поражений СО ЖКТ основывается на количественных и качественных критериях.
Во-первых, размер поражения и его диаметр измеряются настолько точно, насколько это возможно, предпочтительно с использованием градуированного измерительного инструмента.
После чего поражение классифицируется по одному из 5 типов модифицированной японской классификации Borrmann для распространенного рака или типу 0, если внешний вид поражения соответствует поверхностному поражению (слизистая оболочка или подслизистый слой). На данном этапе макроскопическая классификация определяется «внешним видом». Классификация не должна зависеть от какой-либо предшествующей информации и не должна меняться по данным патологоанатома. Это означало бы, что полученная картина при эндоскопии может быть признана недействительной по результатам гистологического заключения.
Поражение, выглядящее как тип 0 при эндоскопическом исследовании, может оказаться распространенным раком при морфологической классификации по р-TNM или наоборот.
В японских исследованиях большинство поверхностных эндоскопических поражений классифицируются в соответствии с подтипами типа 0; это относится к плоскоклеточным ракам пищевода, аденокарциномам кардиального и дистального отделов желудка, толстой кишки и прямой кишки. Японская классификация иногда используется западными исследователями для опухолевых поражений в пищеводе Барретта, а также толстой кишки (в сотрудничестве с японскими экспертами).
Тип 0 поражений делится на 3 основные группы:
• тип 0-I, полиповидный
• тип 0-II, неполиповидный и неуглубленный
• тип 0-III, неполиповидный с явной язвой
Тип 0-I подразделяется на 2 варианта:
• на ножке (0-Iр)
• сидячий (0-IS)
Тип 0-II подразделяется на 3 варианта:
• слегка приподнятое (0-IIа)
• абсолютно плоское (0-IIв)
• слегка углубленное (0-IIс)
Различие между углубленным (0-IIc) и подрытым (язвенным) поражениями (0-III) легко определить в оперативном образце.
Подрытые поражения характеризуются значительным нарушением эпителиального слоя и мышечной пластинки СО.
Смешанные варианты связывают два различных типа опухоли. Приподнятые (IIa) и углубленные (IIc) варианты опухоли довольно легко диагностируется при эндоскопическом исследовании. Тем не менее, определение типа опухоли согласно японской классификации требует максимально точной оценки макроскопической картины, что является областью разногласий, так как поверхность каждого типа не единственный значимый фактор для прогноза.
Углубленные поражения с приподнятыми границами или возвышением в центре классифицируются как тип 0-IIc + IIa (рис. 4).
Приподнятые поражения с центральным углублением на их верхушке классифицируются как тип 0-IIa + IIc. Этот вариант включает в себя относительно углубленные поражения, в которых депрессивные участки не ниже уровня нормальной слизистой. Как правило, поражения типа IIa + IIc имеют менее благоприятный прогноз, с большим риском инвазии в подслизистый слой, чем все остальные типы повреждений, имеющие структуру IIa.
Рекомендации по применению классификации
• В прагматичном и простом подходе, обязательном для классификации поверхностных поражений, присутствует, по крайней мере, один из 5 основных типов: 0-I, 0-IIa, 0-IIb, 0-IIc, 0-III. Относительные пропорции каждого типа отличаются в пищеводе, желудке и толстой кишке.
• Полиповидные поражения 0-I мож
как предотвратить рецидив неоплазии в кишечнике?

Неоплазии кишечника – это группа доброкачественных или злокачественных новообразований, которые могут располагаться в разных отделах толстой кишки. Чаще всего развиваются они развиваются из слизистой оболочки кишечника, но источником роста может стать и другая ткань.
Доброкачественные новообразования довольно распространены. По некоторым данным частота их встречаемости достигает 40% у людей старше 50 лет. Как правило, они никак не беспокоят человека. Главная их опасность заключается в злокачественном перерождении и возникновении рака, поэтому необходима их своевременная диагностика и удаление.
Злокачественные опухоли занимают третье место в структуре онкопатологии и представляет серьезную проблему для экономически развитых стран. Заболевания могут приводить к инвалидизации и гибели больного, а результаты лечения не всегда удовлетворительны.
Причины неоплазии кишечника
На данный момент принято считать, что неоплазии кишечника – это полиэтиологичное заболевание. К их развитию может привести несколько причин:
- Особенности питания: переедание, употребление в пищу большого количества мяса, пряных, маринованных, копченых и соленых блюд, злоупотребление алкоголем, недостаток в рационе пищевых волокон, растительной клетчатки и витаминов.
- Воспалительные заболевания кишечника – неспецифический язвенный колит, болезнь Крона.
- Наследственная предрасположенность – описано несколько синдромов, при которых развиваются множественные новообразования кишечника, которые склонны к малигнизации.
- Возраст. Чем старше человек, тем выше вероятность развития у него неоплазии.
Доброкачественные опухоли кишечника
Полипы. Это относительно доброкачественные новообразования, произрастающие из слизистой оболочки кишечника. Выглядят как шаровидные, грибовидные или ветвистые разрастания. Некоторые полипы располагаются на тонкой ножке, другие – на широком основании. Главной опасностью данных новообразований является их возможная малигнизация (злокачественное перерождение), поэтому их рекомендуют своевременно удалять.
Липома кишечника. Это очень редкое новообразование, встречается в 0,035-0,4% случаев всех доброкачественных новообразований кишки. Обычно липома представлена единичным новообразованием, но могут быть варианты мультифокального поражения.
Диагностика данных новообразований на дооперационном этапе является сложной задачей. Как правило, ее обнаруживают при морфологическом исследовании материала, удаленного во время операции по поводу других заболеваний кишечника.
Морфологически липома представлена хорошо дифференцированной жировой тканью с фиброзной стромой. Обычно поверхность гладкая и покрыта неизмененной слизистой оболочкой. При больших размерах опухоли на слизистой могут быть эрозии и язвы (их связывают с ишемическими поражениями и травматизацией каловыми массами).

Гемангиомы кишечника. Строго говоря, гемангиома не является опухолевым образованием. По сути это результат изменений кровеносных сосудов (мальформация). Условно ее можно разделить на две категории:
- Капиллярная, представленная сетью кровеносных сосудов наименьшего калибра – капилляров, выстланных гиперплазированным эпителием.
- Кавернозная – образована более крупными кровеносными сосудами, которые располагаются между соединительнотканной стромой.
Основным симптомом гемангиомы является кровотечение. При крупных новообразованиях возможна обтурация просвета кишки с развитием кишечной непроходимости.
Злокачественные образования кишечника
Злокачественные новообразования кишечника делят на опухоли эпителиального и неэпителиального происхождения. Эпителиальные опухоли развиваются из эпителия слизистой оболочки кишки (колоректальный рак). Чаще всего, это аденокарциномы, плоскоклеточный рак, реже встречается мелкоклеточный, перстневидноклеточный, медуллярный и недифференцированный рак. Раку всегда предшествуют доброкачественные неоплазии или хронические воспалительные процессы – полипы, болезнь крона, неспецифический язвенный колит.
Из неэпителиальных опухолей встречаются лейомиосаркома, ангиосаркома и саркома Капоши.
По характеру роста злокачественного новообразования выделяют:
- Экзофитные опухоли – растут в просвет кишки.
- Диффузно-инфильтративные опухоли – распространяются внутри стенки кишки.
- Аннулярные новообразования – охватывают стенку кишки по ее окружности.
Запись на консультацию круглосуточно
Симптоматика
Симптомы новообразования зависит от его вида, размера и локализации. Мелкие новообразования, не превышающие 2-3 см, никак себя не проявляют клинически. И только при их увеличении появляются признаки:
- Боль в животе неясной локализации.
- Кишечная непроходимость. Она может развиваться на фоне обтурации или инвагинации кишечной стенки из-за нарушения ее перистальтики.
- Полипы, гамангиомы и рак кишечника могут кровоточить. При профузных кровотечениях из заднего прохода будет выделяться алая кровь или мелена. При незначительной кровоточивости могут быть прожилки крови в кале, при скрытых кровотечениях развиваются железодефицитные анемии.
- Выделение слизи из заднего прохода – ворсинчатые полипы, рак.
- Диспепсические расстройства: запоры, диареи, вздутие живота.
- Чувство инородного тела в прямой кишке.
Стадии опухолевого процесса
При диагностике злокачественной неоплазии кишечника большое значение имеет стадия распространения опухоли. От этого зависит прогноз течения заболевания и схема его лечения. Здесь выделяют следующие стадии:
Рак in situ – злокачественные клетки обнаруживаются только в слизистой оболочке кишки.
1 стадия – опухоль прорастает подслизистый слой.
2 стадия – опухоль распространяется на мышечный слой кишечной стенки.
3 стадия – опухоль прорастает всю толщину кишечной стенки, может распространяться на висцеральную брюшину и жировую клетчатку. Обнаруживаются метастазы в регионарных лимфатических узлах.
4 стадия – опухоль любых размеров с отдаленными метастазами (печень, легкие, головной мозг).
Диагностика
Для обнаружения неоплазии кишечника применяются следующие методы диагностики:
- Эндоскопическое обследование кишки – тотальная колоноскопия (осмотр всей поверхности толстой кишки) и ее сокращенный вариант – ректоскопия и ректосигмоскопия – осмотр прямой и сигмовидной кишки. Этот метод позволяет визуализировать новообразования на ранних стадиях, еще до развития симптомов, провести их удаление, а если это невозможно, выполнить биопсию. В настоящее время колоноскопия является золотым стандартом диагностики неоплазий толстой кишки.
- Анализ кала на скрытую кровь. Этот метод применяется для обнаружения полипов и опухолей, которые имеют изъязвленную поверхность и кровоточат. Как правило, речь идет о достаточно крупных новообразованиях. Это обследование проводят в рамках скрининга колоректального рака. При положительном результате показана дальнейшая колоноскопия.
- Ирригоскопия – рентгенологическое исследование толстой кишки. В первую очередь позволяет обнаружить экзофитные новообразования и опухоли, деформирующие просвет кишки и кишечную стенку.
При обнаружении злокачественной неоплазии кишечника проводится дополнительное обследование для определения стадии заболевания. Сюда входят УЗИ, КТ, МРТ, ряд лабораторных анализов.

Лечение
Новообразования кишечника подлежат удалению, независимо от того, злокачественное оно или доброкачественное.
При небольших размерах неоплазии ее удаляют во время колоноскопии, и полученный материал отправляют на морфологическое исследование. При злокачественных опухолях кишечника проводят обширные операции, направленные на радикальное удаление опухоли. Это может быть резекция фрагмента кишки или удаление кишки (колэктомия). В ряде случаев требуется наложение колостомы – выведение надопухолевого отдела кишки на переднюю брюшную стенку.
При распространенных опухолях лечение дополняют химиотерапией, а для проксимальных отделов кишечника и лучевой терапией.
Прогностические данные
Прогноз будет определяться видом неоплазии кишечника. Например, липомы и ангиосаркомы не склонны к малигнизации, но удалять их нужно, чтобы предотвратить развитие осложнений – кишечной непроходимости и кровотечений. С полипами ситуация иная. Рекомендуют проводить полипэктомию, поскольку есть риск злокачественного перерождения. Наибольший риск малигнизации наблюдается в следующих случаях:
- Ворсинчатые полипы.
- Полипы более 1 см.
- Полипы на широком основании.
- Множественный полипоз.
Прогноз при раке кишечника определяется стадией заболевания. При начальных этапах прогноз благоприятный, есть вероятность полного выздоровления, 5-летняя выживаемость достигает 90%. На второй стадии – 50-70%, на третьей – 50%, и при метастатической форме рака пятилетний рубеж переживают только 10% больных.
Профилактика неоплазий кишечника
Снизить риски развития неоплазии кишечника помогут следующие рекомендации:
- Нормализация питания. Необходимо употреблять в пищу достаточное количество витаминов, клетчатки и пищевых волокон. Не переедайте, ограничьте употребление канцерогенных продуктов: копчености, маринады, легкоусвояемые углеводы, жирные сорта мяса, жареные блюда, пряности, алкоголь.
- Соблюдайте режим физической активности.
- Не допускайте возникновения хронических запоров и диарей, своевременно лечите заболевания ЖКТ.
Учитывая то, что рак кишечника развивается из полипов, необходимо их своевременное удаление. С этой целью всем людям старше 50 лет рекомендуют проводить колоноскопию хотя бы раз в десятилетие. Эта процедура позволит осмотреть слизистую кишки и одновременно удалить обнаруженные новообразования.
Запись на консультацию круглосуточно
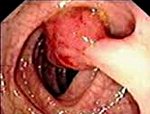
Доброкачественные опухоли желудка – это группа новообразований эпителиального и неэпителиального гистогенеза, исходящих из разных слоев желудочной стенки, характеризующихся медленным развитием и относительно благоприятным прогнозом. Могут проявляться болями в эпигастрии, симптомами желудочного кровотечения, тошнотой, рвотой. Основными методами диагностики являются рентгенография желудка и фиброгастроскопия, гистологическое исследование опухолевой ткани. Лечение заключается в удалении неоплазий эндоскопическим методом или хирургическим путем.
Общие сведения
Доброкачественные опухоли желудка составляют в современной гастроэнтерологии 2-4% от общего числа всех опухолевых новообразований органа. Опухоли желудка могут исходить из его слизистого, подслизистого, мышечного или подсерозного слоя; из эпителиальных, нервных, сосудистых, жировых структур. По типу роста различают эндогастральные новообразования (растущие в сторону просвета желудка), экзогастральные (растущие в сторону соседних органов) и интрамуральные (с внутристеночным ростом).
Причины
Причины развития доброкачественных опухолей желудка окончательно не выяснены. С точки зрения дисрегенераторной теории, развитие полипов может быть связано с нарушением регенерации слизистой оболочки желудка, дискоординацией процессов пролиферации и дифференцировки ее клеток при хроническом гастрите. Аденомы желудка возникают на фоне атрофического гастрита в результате перестройки желез и покровного эпителия, появления кишечной метаплазии.
Гиперпластические полипы развиваются при нарушении обновления и увеличения продолжительности жизни клеток, из-за избыточной регенерации покровно-ямочного эпителия. Также отмечено, что чаще всего полипы желудка возникают в зонах со сниженной секрецией соляной кислоты (нижняя треть желудка), у больных с гипо- и ахлоргидрией. Источником неэпителиальных опухолей может быть гетеротопированная эмбриональная ткань, сохранившаяся в слизистой оболочке при нарушении внутриутробного развития.
Классификация
В зависимости от происхождения доброкачественные новообразования желудка разделяются на эпителиальные и неэпителиальные. Среди эпителиальных опухолей встречаются единичные или множественные аденоматозные и гиперпластические полипы, диффузный полипоз. Полипы представляют собой опухолевидные эпителиальные выросты в просвете желудка с ножкой или широким основанием, шаровидной и овальной формы, с гладкой или грануляционной поверхностью, плотной или мягкой консистенцией.
Полипы желудка чаще всего возникают у лиц мужского пола в возрасте 40-60 лет, обычно располагаются в пилороантральном отделе. Ткани полипа представлены разросшимся покровным эпителием желудка, железистыми элементами и соединительной тканью, богатой сосудами. Аденоматозные полипы желудка – истинные доброкачественные опухоли из железистого эпителия состоят из папиллярных и/или тубулярных структур с выраженной клеточной дисплазией и метаплазией.
Аденомы опасны в плане малигнизации и часто приводят к развитию рака желудка. До 75% доброкачественных эпителиальных опухолей желудка составляют гиперпластические (опухолеподобные) полипы, возникающие вследствие очаговой гиперплазии покровного эпителия, имеющие относительно низкий риск озлокачествления (около 3%). При диффузном полипозе желудка выявляются и гиперпластические, и аденоматозные полипы.
Редко встречающиеся неэпителиальные доброкачественные опухоли формируются внутри желудочной стенки – в ее подслизистом, мышечном или подсерозном слое из различных элементов (мышечной, жировой, соединительной тканей, нервов и сосудов). К ним относятся миомы, невриномы, фибромы, липомы, лимфангиомы, гемангиомы, эндотелиомы и их смешанные варианты.
Также в желудке могут наблюдаться дермоиды, остеомы, хондромы, гамартомы и гетеротопии из тканей поджелудочной железы, дуоденальных желез. Неэпителиальные доброкачественные неоплазии чаще возникают у женщин и иногда могут достигать значительных размеров. Они имеют четкие контуры, обычно округлую форму, гладкую поверхность.
Лейомиомы – наиболее часто встречающиеся доброкачественные неэпителиальные опухоли могут оставаться в мышечном слое, расти в направлении серозной оболочки или прорастать сквозь слизистую желудка, приводя к изъязвлению и желудочному кровотечению. Неэпителиальные новоообразования желудка предрасположены к малигнизации.
Симптомы
В половине случаев полипы желудка протекают без клинических проявлений. Симптомы в основном определяются фоновым заболеванием (хроническим гастритом) и осложнениями (изъязвлением верхушки полипа, кровотечением, пролапсом полипа в двенадцатиперстную кишку и непроходимостью привратника). Боли при полипах желудка обусловлены воспалительным процессом в окружающей его слизистой оболочке, локализуются в эпигастральной области и имеют тупой, ноющий характер. Сначала они возникают после приема пищи, затем становятся постоянными.
Могут наблюдаться жалобы на горечь во рту, тошноту и отрыжку. При развитии непроходимости привратника – появляется рвота, при ущемлении полипа – начинаются схваткообразные боли в подложечной области и по всему животу. Изъязвление полипа приводит к умеренному желудочному кровотечению; при этом может выявляться кровь в рвотной массе, дегтеобразный стул, недомогание, бледность кожных покровов, анемия. Малигнизация полипов, как правило, происходит незаметно, поэтому подозрение должны вызвать отсутствие аппетита, похудание, нарастание общей слабости, диспепсические расстройства.
Клинические признаки неэпителиальных опухолей зависят от их локализации, характера и скорости роста, наличия изъязвления поверхности. Чаще всего неэпителиальные опухоли желудка сопровождаются кратковременными и постоянными болями, возникающими натощак, после приема пищи, при изменении положения тела. При невриномах болевой синдром сильный, жгучего характера. Изъязвление опухоли (особенно, гемангиомы) может вызывать скрытые или обильные желудочные кровотечения с угрозой для жизни больного.
При большом размере опухоли могут пальпироваться через переднюю брюшную стенку. Доброкачественные неэпителиальные неоплазии могут осложняться перитонитом при некрозе новообразований; острой или хронической непроходимостью привратника в случае ущемления в нем опухоли и ее злокачественным перерождением.
Диагностика
Диагностировать опухоли позволяют данные анамнеза, рентгенологического и эндоскопического исследований. На наличие полипов при рентгенографии желудка может указывать дефект наполнения, повторяющий очертания опухоли: четкие, ровные контуры, круглую или овальную форму, его смещаемость при наличии ножки или неподвижность – при полипе с широким основанием.
В случае полипоза желудка выявляют большое число разных по величине дефектов наполнения. Перистальтика стенок желудка при этом сохраняется. Признаки отсутствия перистальтики, увеличение размера, изменение формы, появление нечеткости контуров дефекта наполнения при динамическом наблюдении могут говорить о малигнизации полипа.
Диагноз уточняется при фиброгастродуоденоскопии (ФГДС), которая позволяет провести визуальный осмотр состояния слизистой оболочки желудка, распознавание и дифференциацию полипов от других заболеваний. Визуальная дифференциация доброкачественного полипа от малигнизированного затруднена. Обычно об озлокачествлении могут свидетельствовать наличие полипа размером более 2 см, с бугристой дольчатой поверхностью, неправильными изъеденными контурами. Для точного определения характера полипа во время ФГДС выполняется биопсия подозрительных участков с морфологическим исследованием биоптатов.
Диагноз неэпителиальной неоплазии в большинстве случаев можно установить только после операции и морфологического исследования данного новообразования. Наличие клинических проявлений (например, кровотечения) указывает на возможность опухолевого процесса. ФГДС более информативна при эндогастральном росте неэпителиальных опухолей. При интрамурально или экзогастрально расположенных новоообразованиях при эндоскопическом исследовании определяется сдавление желудка извне.
Рентгенография желудка при неэпителиальных объемных процессов помогает обнаружить округлые или неправильные контуры дефекта наполнения с сохранением перистальтики и складок на подслизистом слое; экзогастральный рост новообразования с оттягиванием стенки желудка; изъязвление с образованием ниши на верхушке опухоли и др. Для обнаружения экзогастральных опухолей могут быть использованы УЗИ и КТ брюшной полости.
Лечение доброкачественных опухолей желудка
Лечение патологии только хирургическое; метод оперативного вмешательства зависит от вида, характера опухоли и ее локализации. В отсутствии надежных критериев малигнизации необходимо проводить удаление всех выявленных новообразований. Основными методами удаления доброкачественных опухолей в настоящее время являются малоинвазивная эндоскопическая электроэксцизия (или электрокоагуляция), энуклеация, резекция желудка, редко – гастрэктомия.
Эндоскопическая полипэктомия проводится при небольших одиночных полипах, локализующихся в различных отделах желудка: при размере менее 0,5 см – прижиганием с помощью точечного коагулятора, при размере от 0,5 до 3 см – методом электроэксцизии. При крупных одиночных полипах на широком основании выполняют хирургическую полипэктомию (иссечение в пределах слизистой оболочки или со всеми слоями стенки желудка) с предварительной гастротомией и ревизией желудка.
При множественных полипах или подозрении на малигнизацию выполняют ограниченную или субтотальную резекцию желудка. После полипэктомии и резекции существует риск неполного удаления, рецидива и малигнизации опухоли, возможно развитие послеоперационных осложнений и функциональных расстройств. Гастрэктомия может быть показана при диффузном полипозе желудка.
Во время удаления неэпителиальных неоплазий проводится срочное гистологическое исследование опухолевых тканей. Небольшие новообразования, растущие в направлении просвета желудка, удаляют эндоскопически; инкапсулированные опухоли вылущивают методом энуклеации. Большие, труднодоступные эндо- и экзогастральные неоплазии удаляют методом клиновидной или парциальной резекции, при подозрении на малигнизацию – резекцию производят с соблюдением онкологических принципов. После операций показано динамическое наблюдение врача-гастроэнтеролога с обязательным эндоскопическим и рентгенологическим контролем.
виды, причины, симптомы, лечение и прогнозы
Опухоль желудка – является патологическим новообразованием, несмотря на то, что помимо злокачественного течения, также может иметь доброкачественную природу. В независимости от своего характера она всегда начинает развитие с одного слоя этого органа, но склонна к поражению всех структурных тканей. Довольно часто имеет бессимптомное течение и отличается медленным ростом.
Новообразования могут развиваться у абсолютно каждого человека в независимости от возраста и пола. Это означает, что стать причиной развития может большое количество различных предрасполагающих факторов, начиная от отягощённой наследственности и заканчивая неправильным питанием.
Клиническая картина полностью диктуется разновидностью опухоли. Опасность заключается в том, что зачастую болезнь протекает бессимптомно или выражается в неспецифических признаках.
Поставить правильный диагноз, а также установить гистологическое строение образования, можно только после осуществления широкого спектра инструментально-лабораторных обследований пациента.
Лечение опухоли желудка зачастую хирургическое, а консервативные способы терапии играют вспомогательную роль.
Международная классификация болезней МКБ-10 не выделяет для новообразований желудка отдельного значения. Злокачественные опухоли имеют код – С16, а доброкачественные относятся к категории другие образования, имеющие код – D10-D36.
Этиология
На сегодня остаются до конца неизвестны механизмы того, почему ткани желудка изменяются и происходит формирование опухолей. Тем не менее специалистам из области гастроэнтерологии удалось выделить ряд наиболее вероятных предрасполагающих факторов, которые в значительной степени повышают вероятность появления злокачественного или доброкачественного образования.

Причины, провоцирующие формирование опухолей
Стоит отметить, что причины будут одинаковыми для формирования любой разновидности опухоли. Таким образом, в качестве провокатора недуга могут выступать:
- хроническая форма протекания гастрита любой природы;
- отрицательное влияние такой бактерии, как Хеликобактер пилори, которая может спровоцировать развитие широкого спектра патологий ЖКТ, в частности язвенной болезни;
- диагностирование аналогичных новообразований у ближайших родственников;
- злоупотребление вредными привычками;
- любые состояния, приводящие к снижению сопротивляемости иммунитета;
- влияние неблагоприятной экологической обстановки;
- неправильное питание, а именно потребление человеком большого количества жирной, острой и пересоленной пищи. Сюда также стоит отнести недостаток в меню клетчатки и витаминов, которые содержатся в свежих овощах и фруктах;
- перенесённое ранее хирургическое вмешательство, направленное на иссечение части желудка;
- пернициозная анемия;
- протекание синдрома Менетрие;
- неблагоприятные условия труда, при которых человек постоянно вынужден контактировать с химическими, токсическими и ядовитыми веществами.
В основную группу риска входят люди трудоспособного возраста. Примечательно то, что любые опухоли зачастую диагностируются у представителей мужского пола, нежели у женщин.
Классификация
Существует множество разновидностей болезни, но основное разделение новообразований делит их на:
- злокачественные опухоли желудка – представляют собой самые частые образования, для которых характерен неблагоприятный исход. Высокий процент летальности обуславливается тем, что они длительное время протекают совершенно бессимптомно или выражаются в неспецифических клинических признаках. Это приводит к тому, что человек слишком поздно обращается за квалифицированной помощью. Диагностика на раннем этапе развития осуществляется крайне редко и в основном случайно;
- доброкачественные опухоли желудка – характеризуются медленным ростом и относительно благоприятным исходом, потому что некоторые из них могут трансформироваться в рак. Стоит отметить, что среди всех образований, доброкачественные встречаются примерно в 5% случаев.
Каждая из разновидностей имеет собственную классификацию. Таким образом, злокачественные новообразования дна желудка или любой другой локализации могут быть представлены:
- аденокарциномой желудка – среди клиницистов считается самой распространённой формой, поскольку диагностируется практически в 95% случаев злокачественных опухолей. Второе название патологии – железистый рак желудка;
- лейомиобластомами – состоят из гладкомышечных тканей;
- злокачественными лимфомами – исходя из названия, становится понятно, что в их составе присутствуют лимфатические ткани;
- карциноидной опухолью желудка – сформирована из клеток нервной системы. В медицинской сфере также известна под другим названием – нейроэндокринная опухоль желудка;
- лейомиосаркомами.
Также стоит выделить категорию наиболее редких разновидностей образований, имеющих злокачественное течение:
- фибропластическая или ангиопластическая саркома;
- ретиносаркома;
- гастроинтестинальная стромальная опухоль желудка;
- злокачественна невринома.
Среди доброкачественных опухолей стоит выделить:
- полипы желудка – такая форма диагностируется в подавляющем большинстве случаев. Подобные образования могут быть как единичными, так и множественными. В последнем случае говорят про полипоз желудка. Делятся на аденоматозные, гиперпластические и фиброматозные. Первый тип наиболее часто трансформируется в онкологию;
- фиброму – сформирована из соединительной ткани и считается самой частой среди мезенхимальных опухолей;
- лейомиому – в своём составе имеет мышечную ткань;
- липому – считается подслизистой опухолью желудка;
- невриному – включает в себя нервные ткани;
- ангиому – состоит из кровеносных сосудов.
Те доброкачественные новообразования, которые развиваются из элементов стенок этого органа, составляют группу неэпителиальных опухолей желудка.
Категория мезенхимальных опухолей состоит из образований, происходящих из:
- соединительной и жировой ткани;
- мышечной и сосудистой ткани.
Также существует классификация в зависимости от локализации того или иного образования, но наиболее часто подвергается патологии кардиальный отдел желудка. Это обуславливается тем, что он близко расположен с пищеводом, заболевания которого могут привести к развитию злокачественной или доброкачественной опухоли.
Стоит отметить, что все образования имеют не экзофитный, а эндофитный рост, при котором опухоль прорастает вглубь стенок этого органа.
Симптоматика
Симптоматическая картина будет отличаться не только от характера поражения желудка, но и от таких факторов:
- разновидность опухоли;
- размеры и количество образования;
- наличие или отсутствие изъязвлений.
Наиболее часто доброкачественные новообразования протекают без выражения какой-либо симптоматики, отчего являются диагностической неожиданностью. Обнаружить их можно лишь во время прохождения планового инструментального обследования или при диагностировании совершенно другого недуга.
Тем не менее доброкачественная опухоль желудка имеет следующие симптомы:
- болевой синдром, возникающий во время трапезы или через несколько часов после употребления пищи;
- приступы тошноты, редко приводящие к рвотным позывам. Рвота зачастую приводит к облегчению состояния пациента. Тревожным признаком считается присутствие кровавых примесей в рвотных массах;
- отрыжка, сопровождающаяся неприятным кислым запахом;
- изжога и снижение аппетита;
- повышенное газообразование и вздутие живота;
- появление характерного урчания;
- слабость и разбитость;
- головные боли и головокружение;
- расстройство стула;
- понижение массы тела и снижение работоспособности;
- бледность кожного покрова.
Подобные проявления не могут с точностью указывать на развитие доброкачественных образований, отчего во время диагностики нецелесообразно опираться лишь на клиническую картину.
Признаки опухоли желудка злокачественной формы отличаются тем, что могут сопровождаться симптоматикой базового недуга, которым зачастую выступает гастрит и язва.
По причине того, что такая категория образований зачастую представлена онкологией, то за основу проявлений берутся симптомы именно такой патологии.
На ранней стадии течения симптомы могут быть следующими:
- переполненность и дискомфорт в желудке;
- изменение пристрастий в еде;
- боли и тяжесть – склонны к обострению после потребления блюд;
- снижение аппетита;
- утрата веса.

Признаки рака желудка
По мере прогрессирования онкологии вышеуказанная симптоматика будет дополняться:
- общей слабостью и быстрой утомляемостью;
- частой сменой настроения и депрессией;
- головными болями различной интенсивности и головокружениями;
- расстройством сна;
- бледностью или синюшностью кожных покровов;
- повышением температуры;
- сухостью слизистых;
- обильным потоотделением и слюнотечением;
- тошнотой с многократной рвотой.
Диагностика
Чтобы дифференцировать злокачественную опухоль от доброкачественного образования, необходим комплексный диагностический подход, который основывается на ряде лабораторных и инструментальных исследований.
Однако, в первую очередь, гастроэнтеролог должен:
- изучить историю болезни не только пациента, но и его ближайших родственников;
- собрать и проанализировать анамнез жизни больного;
- провести тщательный физикальный осмотр;
- детально опросить пациента – для составления полной симптоматической картины.
Лабораторно-инструментальная диагностика опухоли желудка будет включать в себя:
- общеклинический анализ крови;
- биохимию крови;
- микроскопические изучения каловых масс;
- специфические дыхательные тесты;
- общий анализ урины;
- анализ крови на онкомаркеры;
- ЭКДС и УЗИ;
- КТ и МРТ;
- биопсию – для гистологического изучения;
- рентгенодиагностику с использованием контрастного вещества.
Лечение
Тактика устранения новообразования диктуется его классификацией, но зачастую обращаются к хирургическому вмешательству.
Полиповидная и другие доброкачественные опухоли лечатся путём полного или частичного иссечения желудка. После операции пациентам показано:
- медикаментозная терапия, направленная на приём ингибиторов протонного насоса и антибактериальных веществ;
- физиотерапевтические процедуры;
- диетотерапия;
- использование народных средств, но только после консультирования с лечащим врачом.

Резекция желудка
Лечение злокачественной опухоли тела желудка или иной локализации состоит из:
- лапароскопической или лапаротомической операции – при этом удалению подлежит не только поражённый орган, но и близлежащие ткани. Это делают для избегания рецидива;
- химиотерапии;
- лучевой терапии.
Последние две терапевтические методики могут выполняться как до, так и после вмешательства. После операции назначают вышеуказанные консервативные способы терапии.
Возможные осложнения
Специфика протекания доброкачественной или злокачественной желудочной опухоли может привести к опасным для жизни человека осложнениям.
Последствиями доброкачественных образований могут служить:
- частые рецидивы;
- трансформация в онкологию;
- перфорация и стеноз;
- изъязвление поверхности опухоли;
- скрытие кровоизлияния в ЖКТ;
- анемия и перитонит.
Злокачественное течение новообразований чревато:
- близкими и отдалёнными метастазами;
- сильными кровотечениями;
- истощением больного;
- ущемлением;
- стенозом и появлением отверстия в желудке.
Профилактика и прогноз
Для полного избегания или снижения вероятности формирования того или иного новообразования, необходимо придерживаться общих несложных рекомендаций:
- полный отказ от пагубных привычек;
- укрепление иммунной системы;
- сбалансированное и правильное питание;
- соблюдение правил безопасности при работе с ядовитыми веществами;
- недопущение эмоционального и физического перенапряжения;
- ранее выявление и лечение любых патологий ЖКТ;
- регулярное прохождение осмотра у гастроэнтеролога.
Прогноз будет индивидуальным для каждого пациента, но в любом случае благоприятный прогноз обеспечивает своевременная диагностика и полноценное лечение.
Все ли корректно в статье с медицинской точки зрения?
Ответьте только в том случае, если у вас есть подтвержденные медицинские знанияПоделиться статьей:
Читать нас на Яндекс.Дзен
Заболевания со схожими симптомами:
Желтуха (совпадающих симптомов: 14 из 20)Желтуха – патологический процесс, на формирование которого влияет большая концентрация в крови билирубина. Диагностировать недуг могут как у взрослых, так и у детей. Вызвать такое патологическое состояние способно любое заболевание, и все они абсолютно разные.
…Не секрет, что в организме каждого человека при различных процессах, в том числе, переваривании пищи, задействованы микроорганизмы. Дисбактериоз – это заболевание, при котором нарушается соотношение и состав населяющих кишечник микроорганизмов. Это способно привести к серьёзным нарушениям работы желудка и кишечника.
…Интоксикация организма – возникает из-за продолжительного воздействия на организм человека различных токсических веществ. Это может быть производственное отравление ядами или химическими элементами, продолжительное употребление медикаментов, например, при лечении онкологии или туберкулёза. Влияние токсинов может быть как внешнее, так и внутреннее, производимое самим организмом.
…Гастроэнтероколит (пищевая токсикоинфекция) — заболевание воспалительного характера, приводящее к поражению желудочно-кишечного тракта, локализованному преимущественно в тонком или толстом кишечнике. Он представляет большую опасность, вызываемую возможным обезвоживанием организма при отсутствии достаточного контроля. Характеризуется стремительным началом и быстрым течением. Как правило, на 3–4 сутки при соблюдении рекомендаций врача, а также назначении адекватного лечения, симптомы болезни отступают.
…Гименолепидоз (син. карликовый цепень) – представляет собой паразитарное заболевание, которое в подавляющем большинстве случаев диагностируется у детей от 4 до 14 лет. При протекании такой болезни преимущественно страдают органы пищеварительной системы.
…Различного типа новообразования, поражающие желудок и негативно влияющие на здоровье пациента, встречаются довольно часто. Доброкачественные опухоли неопасны, но они составляют не более 5% всех опухолевых образований. Чаще всего встречается рак желудка, составляющий примерно 10% от всех онкологических патологий. Большинство больных – это люди старше 50 лет. Причем у мужчин рак желудка встречается в два раза чаще. Смертность от этой патологии на втором месте среди всех онкологических заболеваний. Проблема в том, что на начальных этапах обнаружить опухоль желудка сложно, поэтому смертность от этого заболевания довольно высокая. Но в последнее время ученые заметили уменьшение числа заболевших. Сейчас в России встречается рак желудка у 35 больных из 100 тысяч населения.
Классификация
Среди всех опухолей желудка подавляющее большинство составляют злокачественные новообразования – более 95%. Доброкачественные опухоли встречаются редко, и во многих случаях они перерождаются в рак. Но выявляются на ранней стадии они редко, так как почти не имеют специфических симптомов. Проявление патологии, тяжесть течения и прогноз для пациента зависит от места локализации опухоли и ее вида. Чаще всего классифицируют такие образования по типу тканей, из которых они образованы. Различия бывают также в размерах опухоли, ее локализации.
Быстрее диагностируются большого размера образования, которые мешают перевариванию пищи и ее продвижению по пищеварительному тракту.
В основном это те, что расположены в области привратника желудка или на границе с пищеводом. Причем в этом месте могут быть опасны не только злокачественные, но и доброкачественные образования. Они затрудняют питание пациента, поэтому чем раньше будут удалены, тем благоприятнее для него прогноз.
Доброкачественные
Такие новообразования встречаются довольно редко, примерно 4–5% среди всех опухолей желудка. Причем подавляющее большинство из них составляют полипы. Это опухоль желудка, представляющая собой разросшуюся железистую ткань. Полип – это округлое образование, часто на ножке, но иногда он имеет широкое основание. Растут эти опухоли только внутрь тела желудка, не прорастая в окружающие органы. Бывают одиночные полипы, множественные или полипоз, когда больше количество новообразований поражает всю слизистую оболочку пищеварительного тракта.
Кроме того, классификация опухолей желудка проводится по типу тканей, месту их локализации и причине появления. Большинство из них – гиперпластические полипы, возникающие на фоне атрофического гастрита. Они составляют около 80% всех доброкачественных опухолей и почти никогда не перерождаются в рак. Остальные полипы чаще всего представляют собой перерожденную железистую ткань слизистой желудка. Они могут преобразовываться в злокачественное новообразование, то есть малигнизироваться. Кроме того, к полипам относят инфильтративные опухоли, возникающие из соединительной ткани при воспалительном процессе.
Остальные доброкачественные новообразования могут быть разными в зависимости от тканей, из которых они образуются. Это может быть опухоль сосудов – ангиома, нервных клеток – неврома, мышечной ткани – лейомиома, липома или подслизистая опухоль. Кроме того, к таким новообразованиям относят болезнь Менетрие или полиаденоматозный гастрит. Эту патологию считают предраковым состоянием, так как она характеризуется поражением слизистой множеством небольших образований.
Злокачественые
Виды злокачественных опухолей более разнообразны. Их классификация тоже зависит от типа тканей и локализации. Большинство из них – около 95% – карциноидные. Чаще всего встречается аденокарцинома, представляющая собой опухоль, растущую из эпителиальной ткани стенок желудка. Немного реже встречается карциноид. Это эндокринная опухоль, поэтому она способна производить гормоны.
Чаще всего в желудке встречаются опухоли, растущие на его стенках.
Еще реже диагностируют лейомиобластомы, которые состоят из разных клеток – эпителиальных и мышечных. Все остальные злокачественные новообразования являются неэпителиальными. Они могут расти из тканей гладких мышц – лейомиосаркома, лимфатической ткани – лимфома или из соединительной ткани – так называемы стромальные опухоли. Реже всего встречаются ретиносаркомы, ангиомы, невриномы.
По месту локализации различают диффузный рак и интестинальный или кишечный. Первая форма встречается чаще у женщин. Больше количество раковых клеток локализуется в основном в верхней части желудка. Развивается стремительно, дает много метастаз.
Гастроинтестинальная опухоль захватывает не только желудок, но и кишечник. Распространена в основном среди мужчин пожилого возраста. Эта форма патологии прогрессирует медленно, хорошо поддается лечению. Одной из разновидностей ее является ГИСТ или ГИСО. Это самая распространенная опухоль желудка. Она представляет собой саркому или новообразование из соединительной ткани.
Кроме того, такие образования различаются по степени распространения и характеру. Если они имеют четкие границы и растут только в просвет желудка, это экзофитные опухоли. Но бывает инфильтративный рак, когда новообразования не имеют границ и растут во все стороны.
Стадии злокачественных опухолей
Только в 10% раковая опухоль выявляется на ранней стадии. Связано это с тем, что развивается она обычно практически бессимптомно. А большинство людей не придают значения несильным ноющим болям в животе, тяжести и тошноте, принимая их за расстройство пищеварения. Такое состояние может продолжаться несколько лет, причем заболевание постоянно прогрессирует.
Важно: по мере прогрессирования опухоль обнаружить все легче, но вылечить сложнее. Только на начальных стадиях прогноз для больного может быть благоприятным.
Сейчас выделяют четыре стадии рака желудка:
- Нулевая стадия или предраковое состояние характеризуется только поражением слизистой желудка. Избавиться от небольших новообразований можно без операции с помощью эндоскопии. Процедура проводится под наркозом и в 90% случаев приводит к полному выздоровлению.
- Первая стадия рака обнаруживается редко. Опухоль при этом растет, но поражает пока только слизистую желудка, иногда начинает прорастать в окружающие лимфатические узлы. Если начать лечение на этой стадии, прогноз будет благоприятным. Около 70% больных полностью выздоравливают.
- На второй стадии опухоль разрастается, захватывает лимфоузлы. Ее нет только в мышечной ткани желудка. Поэтому лечение рака уже затруднено, выживаемость больных в течение 5 лет составляет всего немногим больше 50%.
- Патология на 3 стадии выявляется чаще всего, так как она проявляется уже явно заметными симптомами. Опухоль прорастает во все стенки желудка, потому даже при адекватном лечении выживаемость больных составляет менее 40%.
- 4 стадия рака практически неизлечима. Только 5% больных могут выжить при диагностировании патологии на этом этапе. Ведь опухоль на этой стадии обычно уже неоперабельная. Она прорастает сквозь стенки желудка и распространяется на окружающие органы. Но беда в том, что именно на этой стадии рак обнаруживается у 80% больных.
Причины
Ученым до сих пор неясны причины появления опухолей желудка. Но известны факторы, которые провоцируют перерождение нормальных тканей.
Нужно знать, что у человека со здоровым пищеварительным трактом, который не имеет вредных привычек и правильно питается, подобные новообразования не появляются.
Правда, есть еще генетическая предрасположенность. Если среди родственников был рак желудка, а также при выявлении у человека гена ИЛ-1 велика вероятность появления опухоли.
В последнее время ученые обнаружили роль бактерий Хеликобактер Пилори в развитии новообразований. Это единственный микроорганизм, который выживает в кислой среде желудка. Бактерия поселяется в слизистой оболочке, повреждая ее. Она повышает кислотность желудочного сока, из-за чего на стенках образуются эрозии и язвы. Слизистая атрофируется и становится благоприятной средой для роста раковых клеток. Из-за длительного течения хеликобактерной инфекции часто возникает язвенная болезнь. А она при недостаточном лечении может перерастать в рак. Предшествует появлению опухолей также атрофический гастрит, который часто протекает почти бессимптомно и не лечится вовремя.
Кроме того, есть много других провоцирующих факторов, которые при регулярном воздействии на организм могут привести к образованию опухолей в желудке:
- употребление алкогольных напитков;
- курение;
- частое употребление жирного, жареного, острого, копченостей и солений;
- переедание, питание всухомятку;
- отравление нитратами и нитритами, которые часто содержатся в овощах;
- длительный прием антибиотиков, нестероидных противовоспалительных препаратов, кортикостероидов;
- работа или проживание в экологически неблагополучных условиях;
- сниженный иммунитет;
- тяжелое течение анемии из-за дефицита витамина В12;
- оперативные вмешательства на органах желудочно-кишечного тракта.
Симптомы
Прогноз выздоровления и улучшения качества жизни больного сильно зависит от того, на каком этапе патологии начато лечение. Но проблема в том, что сначала почти не заметно никаких признаков роста опухоли. Особенно часто бессимптомно проходит наличие доброкачественных образований. Полипы и другие подобные опухоли в просвете желудка обычно никак себя не проявляют. И только если опухоль большая, могут наблюдаться боли после еды, тошнота, изжога, отрыжка, нарушения стула. Эти типичные симптомы большинства патологий ЖКТ, поэтому чаще всего такие образования обнаруживаются случайно.
Только при повреждении некоторых из них может возникнуть внутреннее кровотечение, которое проявляется слабостью, побледнением кожи, наличием крови в каловых и рвотных массах. При этом также может появиться головокружение, слабость, быстрая утомляемость, анемия.
Появление любых опухолей со временем приведет к сильным болям в животе и нарушению пищеварения.
Симптомы опухолей желудка злокачественного характера более разнообразны. Они могут появиться внезапно у абсолютно здорового человека.
Внимание: часто злокачественные новообразования образуются на фоне гастритов, язвенной болезни или других патологий. Поэтому многие больные продолжают лечить эти заболевания, не обращая внимания на небольшое ухудшение своего состояния.
Обычно проявления злокачественных опухолей различаются в зависимости от стадии патологии, вида опухоли и ее локализации. Сначала это может быть просто небольшое снижение аппетита, тяжесть в животе, тошнота, метеоризм. Потом появляются несильные ноющие боли, в основном после еды, но постепенно они возникают в любое время. По мере прогрессирования патологии больной ощущает изменение вкуса и чувствует отвращение к некоторым знакомым продуктам. Из-за этого он начинает меньше есть и сильно худеет.
При локализации новообразования в области кардиального отдела желудка, то есть при его соединении с пищеводом, часто наблюдается затруднение в глотании. Могут появиться боли в грудной клетке. Тошнота бывает редко, но при принятии горизонтального положения может появиться отрыжка и сильная рвота.
 Как распознать рак желудка
Как распознать рак желудка
На поздних стадиях появляются другие симптомы:
- ноющие боли в животе, не зависящие от приема пищи;
- рвота съеденной несколько дней назад пищей;
- изжога;
- темный стул с кровью;
- чередование поносов и запоров;
- боли в области печени, механическая желтуха;
- увеличение лимфоузлов.
Часто развиваются различные осложнения, которые могут появиться даже при доброкачественных опухолях. При их быстром росте они могут перекрыть просвет желудка, а при локализации в антральном отделе, то есть в нижней части желудка, опухоли затрудняют эвакуацию пищи. Полипы, которые имеют тонкую ножку, могут перекручиваться или мигрировать в двенадцатиперстную кишку, перекрывая ее. Возможно также ущемление такой опухоли или ее изъязвление, что приводит к некрозу тканей, распаду опухоли и внутреннему кровотечению.
Злокачественные новообразования чаще всего осложняются появлением метастаз. Они прорастают через стенки желудка, приводя к их перфорации. Это может привести к появлению перитонита. Кроме того, раковые клетки распространяются на другие ткани и органы. Чаще всего это лимфатические узлы и печень. Поражаться может также поджелудочная железа, кишечник, яичники.
Диагностика
Для обнаружения опухоли необходимо провести комплексное обследование. Для этого делается рентгенография органов брюшной полости. Она позволяет обнаружить изменение контуров желудка, смещение соседних органов. Более точную информацию можно получить при рентгенографии с контрастированием. При этом обнаруживается нарушение заполнения желудка и дефекты слизистой оболочки.
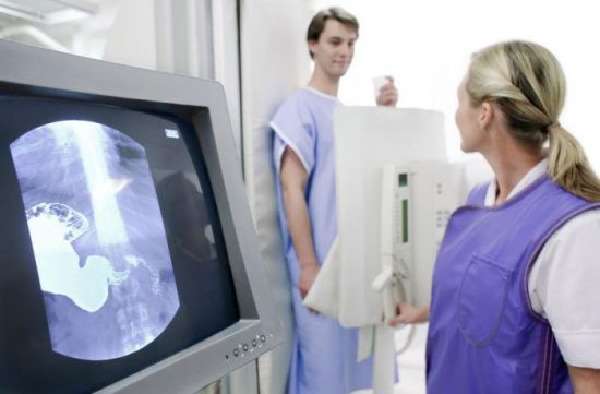
Рентгенография – самый распространенный метод обнаружения опухолей.
Но в последнее время эти методы используются реже. Ведь более информативным является эндоскопическое обследование. ФЭГДС помогает выявить опухоль даже на начальной стадии. Часто для этого требуется провести гистологическое исследование тканей, взятых во время эндоскопической биопсии. Дополнительно могут быть назначены УЗИ, КТ или МРТ органов брюшной полости. А общий и биохимический анализы крови выявляют степень интоксикации организма, низкий уровень гемоглобина и изменения в белковом обмене.
Лечение
Консервативное лечение при любых видах опухолей не применяется. Для избавления от них необходима операция. Опухоль удаляют, часто вместе с частью желудка. В сложных случаях проводят тотальную гастрэктомию, то есть, полное удаление желудка. Могут быть удалены также селезенка, часть кишечника, печени. Если опухоль удалить невозможно или она дала множество метастазов, проводится паллиативное лечение. Его цель – облегчить страдания больного и улучшить качество его жизни. Для этого применяется радиотерапия и лучевая терапия, а также специальные лекарственные препараты.
Оперативное лечение применяется даже при доброкачественных опухолях, так как консервативная терапия неэффективна. Но после обследования врач может принять решение отложить операцию, если опухоль небольшая и нет опасности ее перерождения в злокачественную. Такие операции чаще всего выполняются лапараскопическими методами без разреза брюшины.
Профилактика
Даже своевременное удаление опухоли не защитит больного от осложнений и рецидивов заболевания. Поэтому очень важно соблюдать профилактические меры, которые могут защитить от рака. Особенно это необходимо для людей с наследственной предрасположенностью и различными заболеваниями желудочно-кишечного тракта. При хроническом гастрите, язвенной болезни и других патологиях необходимо ежегодно проходить эндоскопическое обследование и тщательно соблюдать все рекомендации врача. Кроме того, очень важно следить за питанием, избегать алкоголя, не курить.
Выводы
От появления опухоли желудка никто не застрахован. Это одна из самых тяжелых патологий. Даже доброкачественные опухоли сильно снижают качество жизни больного. А излечение возможно только в том случае, если удаление опухоли было сделано на начальном этапе. Поэтому важно не игнорировать малейший дискомфорт в желудке и вовремя проходить обследование.
 Загрузка…
Загрузка…
Доброкачественная опухоль желудка – это новообразование, которое не имеет признаков злокачественного процесса. В некоторых случаях остается небольшой риск перерождения при отсутствии соответствующего лечения. Доброкачественные новообразования желудка составляют до 5% от числа всех опухолевых заболеваний желудка, могут развиваться из эпителия, нервной ткани, жировых структур или сосудистых. Рост может быть быстрый или замедленный. По направлению роста выделяют опухоли, движущиеся в сторону просвета желудка, в сторону органов брюшной полости и новообразования, которые разрастаются внутри стенки. По локализации они с одинаковой частотой возникают в теле желудка, антральном отделе или в других местах.
В ЦЭЛТ вы можете получить консультацию хирурга.
- Первичная консультация – 2 700
- Повторная консультация – 1 800
Разновидности и особенности желудочных опухолей
По происхождению все новообразования, локализованные в области желудка, разделяют на две большие группы: эпителиальные и неэпителиальные.
Среди первой группы встречаются аденомы и полипы (одиночные или группами). Разница в том, что полипы – это выросты в просвет органа, они обычно округлой формы и имеют широкое основание, могут располагаться на ножке. Развитие полипов ассоциировано с возрастными изменениями – чаще встречаются в возрасте после 40 лет, болезнь поражает мужчин чаще, чем женщин. Гистологически полип представляет собой разросшиеся железистые и эпителиальные ткани с соединительнотканными элементами и развитой сетью сосудов.
Аденомы – это истинные доброкачественные новообразования, состоящие преимущественно из железистой ткани. В отличие от полипов, аденома может чаще перерождаться. Но встречаются реже, чем полипы.
Неэпителиальные опухоли встречаются редко. Они формируются в стенке желудка и могут состоять из самых разных тканей.
К неэпителиальным новообразованиям относят:

- Миому – формируется из мышечной ткани.
- Невриному – формируется из клеток, составляющих миелиновую оболочку нервных волокон.
- Фиброму – развивается из соединительной ткани.
- Липому – состоит из жировой ткани.
- Лимфангиомы – клетки опухоли происходят из стенок лимфатических сосудов.
- Гемангиомы – из клеток, выстилающих кровеносные или лимфатические сосуды.
- и другие варианты, в том числе опухоли смешанной природы.
В отличие от полипов, которые чаще встречаются у мужчин, опухоли неэпителиальной природы чаще диагностируют у женщин. У всех подобных новообразований есть отличительные особенности: как правило, они имеют четкий контур, гладкую поверхность, округлую форму. Могут разрастаться до значительных размеров.
Особо выделяют неэпителиальную опухоль лейомиому – она встречается с более высокой частотой, чем другие новообразования из этой группы. Эта опухоль может вызывать желудочные кровотечения или потенцировать образование язв за счет прорастания в слизистую оболочку желудка. Все неэпителиальные новообразования отличаются достаточно высоким риском онкологического перерождения – малигнизации.
Симптомы
Симптомы опухоли желудка, как правило, слабо выражены. Если новообразование не растет, то практически не проявляется и никак не наблюдается. Очень часто доброкачественные опухоли определяют по косвенным признакам или выявляют случайно при эндоскопическом обследовании.
Клиническая картина включает в себя:
- Проявления, характерные для гастрита, но без достаточных диагностических признаков для постановки диагноза гастрит.
- Кровоизлияние в желудок.
- Снижение аппетита, утомляемость, колебания веса – общие нарушения, которые можно ассоциировать с болезнями пищеварительной системы.
- Диспепсия.
- При частых кровоизлияниях – анемия.
При абсолютно спокойном течении могут наблюдаться боли тупого и ноющего характера, локализованные, как правило, в эпигастрии. Боль нередко возникает после приема пищи. Достаточно часто больные ассоциируют эти симптомы с гастритом.
При опухолях достаточно большого размера могут наблюдаться более выраженные проявления. Появляется тяжесть, возникают приступы тошноты, появляется частая отрыжка. В рвотных массах и стуле больные обнаруживают примеси крови. В лабораторных анализах определяют пониженный гемоглобин. Пациенты испытывают слабость и головокружения. Вне зависимости от сохранности нормального аппетита начинается потеря веса. Всего различают более сотни видов доброкачественных новообразований – с разным течением и клинической картиной. Выраженность симптомов зависит от локализации, размера и скорости роста опухоли. Классической клинической картиной, позволяющей заподозрить опухоль, считается кровотечение, сопровождаемое общими нарушениями работы ЖКТ.
Причины
На сегодняшний день все причины образования доброкачественных опухолей желудка неизвестны. Поэтому правильно говорить о факторах риска – факторах, которые провоцируют патологические процессы, приводящие к появлению новообразований. В их числе наличие других заболеваний ЖКТ.
Наиболее актуальная теория гласит, что полипы появляются в результате нарушений естественной регенерации слизистой желудка. Поэтому полипы часто развиваются на фоне гастрита. Аденомы чаще сопровождаются атрофическим гастритом. При этом отмечено, что более 70% всех новообразований развивается в нижней трети желудка – то есть в зоне с пониженной концентрацией соляной кислоты.
Причиной развития неэпителиальной опухоли могут быть эмбриональные нарушения или наличие хронических заболеваний. Так как конкретных причин выявить не удается, не существует и специфической профилактики доброкачественных опухолей. Нельзя забывать и о наследственной предрасположенности – пациентам, чьи родственники имели новообразования желудка, необходимо даже при отсутствии каких-либо симптомов заболевания желудка выполнять эндоскопическое исследование. В любом случае, при подозрении на наличие полипа или полиповидного образования желудка следует обратиться к хирургу.
Наши врачи

Главный хирург ЦЭЛТ, заслуженный врач РФ, главный специалист ДЗ г. Москвы по эндохирургии и эндоскопии, членкор РАН, заведующий кафедрой факультетской хирургии № 1 ГБОУ БПО МГМСУ, доктор медицинских наук, врач высшей категории, профессор
Стаж 41 год
Записаться на прием
Врач-хирург, заведующий хирургической службой ЦЭЛТ, кандидат медицинских наук, врач высшей категории
Стаж 31 год
Записаться на приемДиагностика

Диагностика опухолей желудка состоит из трех основных этапов: сбор анамнеза, осмотр, рентгенографическое и эндоскопическое исследование. Также назначают анализ крови, который позволяет выявить снижение уровня гемоглобина, то есть анемию, характерную для опухолей, вызывающих кровотечение. Доброкачественность новообразования определяют по таким признакам: размер, наличие перистальтики (при инструментальном исследовании), форма. Нечеткие контуры, быстрый рост и отсутствие перистальтики свидетельствуют о том, что полип малигнизируется.
Для уточнения диагноза используют ЭГДС – эзофагогастродуоденоскопию, которая позволяет визуально оценить состояние слизистой и в режиме реального времени увидеть форму и размер опухолей, локализованных на слизистой. Этот метод позволяет оценить риск малигнизации – визуально невозможно отличить злокачественную опухоль ранней стадии от доброкачественной, требуется биопсия. При подозрении на онкологию при проведении ФГДС берут пробу для гистологического исследования в лаборатории – биопсия позволяет точно определить характер новообразования.
Так как неэпителиальные опухоли бывают самые разнообразные, то нередко поставить окончательный диагноз удается только после операции.
Исследование опухолей, расположенных вне слизистой, возможно теми же средствами: на рентгенографии видны контуры, а эндоскопическое исследование в сочетании с ультразвуковым метолом (эндо-УЗИ) позволяет определить зоны сдавливания, которые появляются при росте опухолей внутри стенок желудка или в сторону внутренних органов.
Лечение
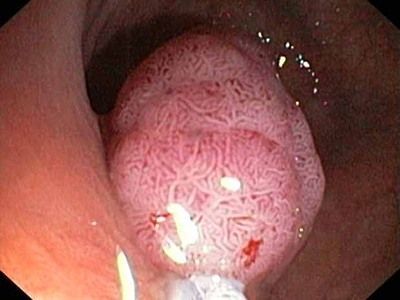
Лечение доброкачественной опухоли желудка бывает только хирургическое. Консервативные методы неэффективны. Операцию могут отложить при небольшом размере опухоли и отсутствии опасности озлокачествления. Но в большинстве случаев показано хирургическое удаление – с помощью современных технологий операция безопасна. Раннее удаление особенно важно провести в случае, когда не удается достоверно определить характер опухоли – злокачественные новообразования необходимо убрать на ранней стадии.
Существует несколько методов удаления доброкачественной опухоли, которые применяются в настоящее время:
- Эндоскопическая электроэксцизия – так называется малоинвазивная операция, которая подразумевает электрокоагуляцию через эндоскопический доступ. Таким способом удаляют полипы.
- Энуклеация – позволяет снизить кровопотерю, выполняется через эндоскопический или лапароскопический доступ (в зависимости от локализации образования).
- Лапароскопическая резекция желудка – операция с доступом через проколы передней брюшной стенки и разрез стенки желудка, при которой часть желудка удаляют, а затем восстанавливают непрерывный пищеварительный тракт с помощью аппаратного шва.
- Гастрэктомия – полное удаление желудка. Практически не применяют при доброкачественных опухолях.
Эндоскопическая операция показана при обнаружении полипов, которые видны при диагностике и расположены одиночно. Если полип небольшой, достаточно коагуляции. Для новообразований размером более 5 мм применяют электроэксцизию – полип затягивают за ножку, а затем удаляют электрокоагулятором. При полипах более крупного размера проводят подслизистую резекцию образования (через эндоскоп).
Резекцию желудка проводят при множественных полипах или при высоком риске озлокачествления. Гастрэктомию проводят при некоторых случаях диффузного полипоза.
В клинике ЦЭЛТ можно пройти обследование и начать лечение – современные технологии на страже крепкого здоровья.
Наши услуги
Администрация АО “ЦЭЛТ” регулярно обновляет размещенный на сайте клиники прейскурант. Однако во избежание возможных недоразумений, просим вас уточнять стоимость услуг по телефону: +7 (495) 788 33 88
симптомы, классификация, причины и лечение
Различного типа новообразования, поражающие желудок и негативно влияющие на здоровье пациента, встречаются довольно часто. Доброкачественные опухоли неопасны, но они составляют не более 5% всех опухолевых образований. Чаще всего встречается рак желудка, составляющий примерно 10% от всех онкологических патологий. Большинство больных – это люди старше 50 лет. Причем у мужчин рак желудка встречается в два раза чаще. Смертность от этой патологии на втором месте среди всех онкологических заболеваний. Проблема в том, что на начальных этапах обнаружить опухоль желудка сложно, поэтому смертность от этого заболевания довольно высокая. Но в последнее время ученые заметили уменьшение числа заболевших. Сейчас в России встречается рак желудка у 35 больных из 100 тысяч населения.
Классификация
Среди всех опухолей желудка подавляющее большинство составляют злокачественные новообразования – более 95%. Доброкачественные опухоли встречаются редко, и во многих случаях они перерождаются в рак. Но выявляются на ранней стадии они редко, так как почти не имеют специфических симптомов. Проявление патологии, тяжесть течения и прогноз для пациента зависит от места локализации опухоли и ее вида. Чаще всего классифицируют такие образования по типу тканей, из которых они образованы. Различия бывают также в размерах опухоли, ее локализации.
Быстрее диагностируются большого размера образования, которые мешают перевариванию пищи и ее продвижению по пищеварительному тракту.
В основном это те, что расположены в области привратника желудка или на границе с пищеводом. Причем в этом месте могут быть опасны не только злокачественные, но и доброкачественные образования. Они затрудняют питание пациента, поэтому чем раньше будут удалены, тем благоприятнее для него прогноз.
Доброкачественные
Такие новообразования встречаются довольно редко, примерно 4–5% среди всех опухолей желудка. Причем подавляющее большинство из них составляют полипы. Это опухоль желудка, представляющая собой разросшуюся железистую ткань. Полип – это округлое образование, часто на ножке, но иногда он имеет широкое основание. Растут эти опухоли только внутрь тела желудка, не прорастая в окружающие органы. Бывают одиночные полипы, множественные или полипоз, когда больше количество новообразований поражает всю слизистую оболочку пищеварительного тракта.
Кроме того, классификация опухолей желудка проводится по типу тканей, месту их локализации и причине появления. Большинство из них – гиперпластические полипы, возникающие на фоне атрофического гастрита. Они составляют около 80% всех доброкачественных опухолей и почти никогда не перерождаются в рак. Остальные полипы чаще всего представляют собой перерожденную железистую ткань слизистой желудка. Они могут преобразовываться в злокачественное новообразование, то есть малигнизироваться. Кроме того, к полипам относят инфильтративные опухоли, возникающие из соединительной ткани при воспалительном процессе.
Остальные доброкачественные новообразования могут быть разными в зависимости от тканей, из которых они образуются. Это может быть опухоль сосудов – ангиома, нервных клеток – неврома, мышечной ткани – лейомиома, липома или подслизистая опухоль. Кроме того, к таким новообразованиям относят болезнь Менетрие или полиаденоматозный гастрит. Эту патологию считают предраковым состоянием, так как она характеризуется поражением слизистой множеством небольших образований.
Злокачественые
Виды злокачественных опухолей более разнообразны. Их классификация тоже зависит от типа тканей и локализации. Большинство из них – около 95% – карциноидные. Чаще всего встречается аденокарцинома, представляющая собой опухоль, растущую из эпителиальной ткани стенок желудка. Немного реже встречается карциноид. Это эндокринная опухоль, поэтому она способна производить гормоны.
Чаще всего в желудке встречаются опухоли, растущие на его стенках.
Еще реже диагностируют лейомиобластомы, которые состоят из разных клеток – эпителиальных и мышечных. Все остальные злокачественные новообразования являются неэпителиальными. Они могут расти из тканей гладких мышц – лейомиосаркома, лимфатической ткани – лимфома или из соединительной ткани – так называемы стромальные опухоли. Реже всего встречаются ретиносаркомы, ангиомы, невриномы.
По месту локализации различают диффузный рак и интестинальный или кишечный. Первая форма встречается чаще у женщин. Больше количество раковых клеток локализуется в основном в верхней части желудка. Развивается стремительно, дает много метастаз.
Гастроинтестинальная опухоль захватывает не только желудок, но и кишечник. Распространена в основном среди мужчин пожилого возраста. Эта форма патологии прогрессирует медленно, хорошо поддается лечению. Одной из разновидностей ее является ГИСТ или ГИСО. Это самая распространенная опухоль желудка. Она представляет собой саркому или новообразование из соединительной ткани.
Кроме того, такие образования различаются по степени распространения и характеру. Если они имеют четкие границы и растут только в просвет желудка, это экзофитные опухоли. Но бывает инфильтративный рак, когда новообразования не имеют границ и растут во все стороны.
Стадии злокачественных опухолей
Только в 10% раковая опухоль выявляется на ранней стадии. Связано это с тем, что развивается она обычно практически бессимптомно. А большинство людей не придают значения несильным ноющим болям в животе, тяжести и тошноте, принимая их за расстройство пищеварения. Такое состояние может продолжаться несколько лет, причем заболевание постоянно прогрессирует.
Важно: по мере прогрессирования опухоль обнаружить все легче, но вылечить сложнее. Только на начальных стадиях прогноз для больного может быть благоприятным.
Сейчас выделяют четыре стадии рака желудка:
- Нулевая стадия или предраковое состояние характеризуется только поражением слизистой желудка. Избавиться от небольших новообразований можно без операции с помощью эндоскопии. Процедура проводится под наркозом и в 90% случаев приводит к полному выздоровлению.
- Первая стадия рака обнаруживается редко. Опухоль при этом растет, но поражает пока только слизистую желудка, иногда начинает прорастать в окружающие лимфатические узлы. Если начать лечение на этой стадии, прогноз будет благоприятным. Около 70% больных полностью выздоравливают.
- На второй стадии опухоль разрастается, захватывает лимфоузлы. Ее нет только в мышечной ткани желудка. Поэтому лечение рака уже затруднено, выживаемость больных в течение 5 лет составляет всего немногим больше 50%.
- Патология на 3 стадии выявляется чаще всего, так как она проявляется уже явно заметными симптомами. Опухоль прорастает во все стенки желудка, потому даже при адекватном лечении выживаемость больных составляет менее 40%.
- 4 стадия рака практически неизлечима. Только 5% больных могут выжить при диагностировании патологии на этом этапе. Ведь опухоль на этой стадии обычно уже неоперабельная. Она прорастает сквозь стенки желудка и распространяется на окружающие органы. Но беда в том, что именно на этой стадии рак обнаруживается у 80% больных.
Причины
Ученым до сих пор неясны причины появления опухолей желудка. Но известны факторы, которые провоцируют перерождение нормальных тканей.
Нужно знать, что у человека со здоровым пищеварительным трактом, который не имеет вредных привычек и правильно питается, подобные новообразования не появляются.
Правда, есть еще генетическая предрасположенность. Если среди родственников был рак желудка, а также при выявлении у человека гена ИЛ-1 велика вероятность появления опухоли.
В последнее время ученые обнаружили роль бактерий Хеликобактер Пилори в развитии новообразований. Это единственный микроорганизм, который выживает в кислой среде желудка. Бактерия поселяется в слизистой оболочке, повреждая ее. Она повышает кислотность желудочного сока, из-за чего на стенках образуются эрозии и язвы. Слизистая атрофируется и становится благоприятной средой для роста раковых клеток. Из-за длительного течения хеликобактерной инфекции часто возникает язвенная болезнь. А она при недостаточном лечении может перерастать в рак. Предшествует появлению опухолей также атрофический гастрит, который часто протекает почти бессимптомно и не лечится вовремя.
Кроме того, есть много других провоцирующих факторов, которые при регулярном воздействии на организм могут привести к образованию опухолей в желудке:
- употребление алкогольных напитков;
- курение;
- частое употребление жирного, жареного, острого, копченостей и солений;
- переедание, питание всухомятку;
- отравление нитратами и нитритами, которые часто содержатся в овощах;
- длительный прием антибиотиков, нестероидных противовоспалительных препаратов, кортикостероидов;
- работа или проживание в экологически неблагополучных условиях;
- сниженный иммунитет;
- тяжелое течение анемии из-за дефицита витамина В12;
- оперативные вмешательства на органах желудочно-кишечного тракта.
Читайте также:
Симптомы
Прогноз выздоровления и улучшения качества жизни больного сильно зависит от того, на каком этапе патологии начато лечение. Но проблема в том, что сначала почти не заметно никаких признаков роста опухоли. Особенно часто бессимптомно проходит наличие доброкачественных образований. Полипы и другие подобные опухоли в просвете желудка обычно никак себя не проявляют. И только если опухоль большая, могут наблюдаться боли после еды, тошнота, изжога, отрыжка, нарушения стула. Эти типичные симптомы большинства патологий ЖКТ, поэтому чаще всего такие образования обнаруживаются случайно.
Только при повреждении некоторых из них может возникнуть внутреннее кровотечение, которое проявляется слабостью, побледнением кожи, наличием крови в каловых и рвотных массах. При этом также может появиться головокружение, слабость, быстрая утомляемость, анемия.
Появление любых опухолей со временем приведет к сильным болям в животе и нарушению пищеварения.
Симптомы опухолей желудка злокачественного характера более разнообразны. Они могут появиться внезапно у абсолютно здорового человека.
Внимание: часто злокачественные новообразования образуются на фоне гастритов, язвенной болезни или других патологий. Поэтому многие больные продолжают лечить эти заболевания, не обращая внимания на небольшое ухудшение своего состояния.
Обычно проявления злокачественных опухолей различаются в зависимости от стадии патологии, вида опухоли и ее локализации. Сначала это может быть просто небольшое снижение аппетита, тяжесть в животе, тошнота, метеоризм. Потом появляются несильные ноющие боли, в основном после еды, но постепенно они возникают в любое время. По мере прогрессирования патологии больной ощущает изменение вкуса и чувствует отвращение к некоторым знакомым продуктам. Из-за этого он начинает меньше есть и сильно худеет.
При локализации новообразования в области кардиального отдела желудка, то есть при его соединении с пищеводом, часто наблюдается затруднение в глотании. Могут появиться боли в грудной клетке. Тошнота бывает редко, но при принятии горизонтального положения может появиться отрыжка и сильная рвота.
На поздних стадиях появляются другие симптомы:
- ноющие боли в животе, не зависящие от приема пищи;
- рвота съеденной несколько дней назад пищей;
- изжога;
- темный стул с кровью;
- чередование поносов и запоров;
- боли в области печени, механическая желтуха;
- увеличение лимфоузлов.
Часто развиваются различные осложнения, которые могут появиться даже при доброкачественных опухолях. При их быстром росте они могут перекрыть просвет желудка, а при локализации в антральном отделе, то есть в нижней части желудка, опухоли затрудняют эвакуацию пищи. Полипы, которые имеют тонкую ножку, могут перекручиваться или мигрировать в двенадцатиперстную кишку, перекрывая ее. Возможно также ущемление такой опухоли или ее изъязвление, что приводит к некрозу тканей, распаду опухоли и внутреннему кровотечению.
Злокачественные новообразования чаще всего осложняются появлением метастаз. Они прорастают через стенки желудка, приводя к их перфорации. Это может привести к появлению перитонита. Кроме того, раковые клетки распространяются на другие ткани и органы. Чаще всего это лимфатические узлы и печень. Поражаться может также поджелудочная железа, кишечник, яичники.
Диагностика
Для обнаружения опухоли необходимо провести комплексное обследование. Для этого делается рентгенография органов брюшной полости. Она позволяет обнаружить изменение контуров желудка, смещение соседних органов. Более точную информацию можно получить при рентгенографии с контрастированием. При этом обнаруживается нарушение заполнения желудка и дефекты слизистой оболочки.
Рентгенография – самый распространенный метод обнаружения опухолей.
Но в последнее время эти методы используются реже. Ведь более информативным является эндоскопическое обследование. ФЭГДС помогает выявить опухоль даже на начальной стадии. Часто для этого требуется провести гистологическое исследование тканей, взятых во время эндоскопической биопсии. Дополнительно могут быть назначены УЗИ, КТ или МРТ органов брюшной полости. А общий и биохимический анализы крови выявляют степень интоксикации организма, низкий уровень гемоглобина и изменения в белковом обмене.
Лечение
Консервативное лечение при любых видах опухолей не применяется. Для избавления от них необходима операция. Опухоль удаляют, часто вместе с частью желудка. В сложных случаях проводят тотальную гастрэктомию, то есть, полное удаление желудка. Могут быть удалены также селезенка, часть кишечника, печени. Если опухоль удалить невозможно или она дала множество метастазов, проводится паллиативное лечение. Его цель – облегчить страдания больного и улучшить качество его жизни. Для этого применяется радиотерапия и лучевая терапия, а также специальные лекарственные препараты.
Оперативное лечение применяется даже при доброкачественных опухолях, так как консервативная терапия неэффективна. Но после обследования врач может принять решение отложить операцию, если опухоль небольшая и нет опасности ее перерождения в злокачественную. Такие операции чаще всего выполняются лапараскопическими методами без разреза брюшины.
Профилактика
Даже своевременное удаление опухоли не защитит больного от осложнений и рецидивов заболевания. Поэтому очень важно соблюдать профилактические меры, которые могут защитить от рака. Особенно это необходимо для людей с наследственной предрасположенностью и различными заболеваниями желудочно-кишечного тракта. При хроническом гастрите, язвенной болезни и других патологиях необходимо ежегодно проходить эндоскопическое обследование и тщательно соблюдать все рекомендации врача. Кроме того, очень важно следить за питанием, избегать алкоголя, не курить.
Выводы
От появления опухоли желудка никто не застрахован. Это одна из самых тяжелых патологий. Даже доброкачественные опухоли сильно снижают качество жизни больного. А излечение возможно только в том случае, если удаление опухоли было сделано на начальном этапе. Поэтому важно не игнорировать малейший дискомфорт в желудке и вовремя проходить обследование.
Множественная эндокринная неоплазия, тип 1
Что такое множественная эндокринная неоплазия, тип 1?
Множественная эндокринная неоплазия типа 1 (MEN1) – это наследственное заболевание, связанное с опухолями эндокринных (вырабатывающих гормон) желез. MEN1 был первоначально известен как синдром Вермера. Наиболее распространенные опухоли, наблюдаемые у MEN1, включают паращитовидную железу, островковые клетки поджелудочной железы и гипофиз. Другие эндокринные опухоли, наблюдаемые у MEN1, включают опухоли коры надпочечников, нейроэндокринные опухоли (ранее называвшиеся карциноидными опухолями) и редкие феохромоцитомы, а также опухоли в других частях пищеварительного тракта.
Неэндокринные опухоли также наблюдаются у мужчин1. Эти опухоли могут включать в себя:
ангиофиброма лица, представляющая собой опухоль кровеносных сосудов и фиброзной ткани
коллагенома, которая представляет собой опухоль телесного цвета на коже
липома, которая является жировой опухолью
лейомиома, которая является опухолью гладких мышц
менингиома, которая является опухолью из ткани нервной системы; необычный
эпендимома, которая является опухолью из ткани нервной системы; необычный
Большинство опухолей у людей с MEN1 являются доброкачественными (неопухолевыми).Однако приблизительно 1 из 3 нейроэндокринных опухолей поджелудочной железы и нейроэндокринных опухолей средостения являются злокачественными, что означает, что опухоль может распространиться на другие части тела. Эти опухоли могут также вызвать проблемы, производя большое количество гормонов. Существует большое разнообразие симптомов, которые могут возникнуть из-за увеличения выработки гормонов этим типом опухоли. К ним относятся увеличение производства:
Пролактин, который вызывает неправильную выработку молока грудью, отсутствие менструаций у женщин и снижение выработки тестостерона у мужчин
гормон роста, который вызывает чрезмерный рост челюсти и других мягких тканей
адренокортикотропный гормон, который вызывает чрезмерную выработку кортизола надпочечниками
гастрин, который вызывает язву желудка
глюкагон, вызывающий сахарный диабет и кожную сыпь
вазоактивный кишечный пептид, вырабатываемый нейроэндокринной опухолью поджелудочной железы, вызывающей сильную водянистую диарею
гормон паращитовидной железы, вырабатываемый опухолями околощитовидной железы, вызывающими повышенное содержание кальция в крови (гиперкальциемия) и камни в почках
Что вызывает MEN1?
MEN1 – это генетическое заболевание.Это означает, что риск заболевания раком и другие особенности MEN1 могут передаваться из поколения в поколение в семье. Ген, связанный с MEN1, также называется , MEN1, . Мутация (изменение) в гене MEN1 дает человеку повышенный риск развития эндокринных опухолей и других симптомов MEN1. У более чем 90% людей, которые наследуют мутацию MEN1, развивается 1 или более симптомов MEN1. У небольшого процента людей без генетических изменений MEN1 были обнаружены мутации зародышевой линии (изменения в яйцеклетке или сперматозоидах организма, которые встраиваются в ДНК каждой клетки посредством наследования) в классе белков, называемых ингибиторами циклинзависимой киназы (CDKI), которые регулируют рост и деление клеток.Исследования продолжаются, чтобы узнать больше о MEN1.
Как наследуется MEN1?
Обычно каждая клетка имеет 2 копии каждого гена: 1 унаследована от матери и 1 от отца. MEN1 следует аутосомно-доминантному типу наследования, в котором мутация происходит только в 1 копии гена. Это означает, что родитель с мутацией гена может передать копию своего нормального гена или копию гена с мутацией. Следовательно, любой ребенок от одного из родителей с генетической мутацией имеет 50% шансов унаследовать эту мутацию.Однако, если родители дают отрицательный результат на мутацию, риск для братьев и сестер значительно снижается, но их риск все же может быть выше, чем средний риск.
Существуют варианты для людей, заинтересованных в том, чтобы завести ребенка, когда предполагаемый родитель несет мутацию гена, которая увеличивает риск развития этого синдрома наследственного рака. Для получения дополнительной информации, поговорите со специалистом по вспомогательной репродукции в клинике репродукции.
Как часто встречается MEN1?
По оценкам, примерно 1 из 30 000 человек имеет МЭ1.Около 10% людей с MEN1 не имеют семейной истории этого заболевания; у них есть de novo (новая) мутация в гене MEN1 .
Как диагностируется MEN1?
MEN1 подозревается, когда у человека есть по крайней мере 2 из наиболее распространенных опухолей, перечисленных ниже:
Если у человека семейный анамнез MEN1, он или она подозреваются на наличие MEN1, если у него диагностирована опухоль околощитовидной железы, поджелудочной железы или гипофиза. Генетическое тестирование мутаций в гене MEN1 доступно для людей с подозрением на наличие MEN1.Мутация в гене MEN1 обнаруживается примерно в 80-90% семей с диагнозом MEN1. Приблизительно 65% людей с 2 или более опухолями, связанными с MEN1, но без семейной истории, будут иметь мутацию в гене MEN1 .
Каковы предполагаемые риски рака, связанные с MEN1?
Приблизительно 1 из 3 нейроэндокринных опухолей поджелудочной железы являются злокачественными. Если рак распространился за пределы того места, где он начался, наиболее распространенным местом распространения является печень.Небольшой процент нейроэндокринных опухолей средостения являются злокачественными и распространяются на локальные (близлежащие) лимфатические узлы или на печень, легкие или другие места.
Какие варианты скрининга для MEN1?
Текущий рекомендуемый скрининг для людей, которые, как известно или подозревают, имеют MEN1, включает:
Генетическое тестирование
Генетическое тестирование доступно. Следует подумать о детях или молодых людях, которые являются членами семьи с диагнозом MEN1 и выявленной мутацией гена MEN1 , чтобы определить, какие дети и молодые люди должны проходить скрининговые исследования, описанные ниже.В семье с идентифицированной мутацией гена MEN1 детям с генетическим тестом, не обнаружившим мутации (ожидается, что это будет 50% детей, рожденных от человека, пораженного MEN1), могут не понадобиться скрининговые тесты, описанные ниже.
Диагностические исследования
Регулярные анализы крови каждые 1-3 года на пролактин, инсулиноподобный фактор роста 1 (IGF-1), глюкозу натощак, инсулин и проинсулин, начиная с 5-10 лет.
Ежегодный ионизированный или альбумин-скорректированный тест уровня кальция, начиная с 8 лет
Регулярные анализы крови на голодный гастрин и натощак и стимуляцию приема пищи панкреатического полипептида (РР), VIP натощак и глюкагона, начиная с 20 лет.
Сканирование головного мозга методом магнитно-резонансной томографии (МРТ) каждые 3–5 лет, начиная с 5–10 лет или в любое время, результаты анализов на сывороточный пролактин или инсулиноподобный фактор роста являются ненормальными.
МРТ или компьютерная томография (CT) Сканирование грудной клетки и живота каждые 2–4 года, начиная с 20 лет или когда отмечается аномалия сывороточного гастрина, ПП или VIP.
Рекомендации по проверке могут со временем меняться по мере разработки новых технологий и получения дополнительной информации о MEN1.Важно поговорить с врачом о соответствующих скрининговых тестах.
Какие варианты лечения эндокринных опухолей?
Большинство из этих опухолей лечат хирургическим путем или принимают лекарства, которые подавляют рост или функцию опухоли. Опухоли паращитовидной железы, которые почти всегда доброкачественные, должны быть удалены хирургическим путем, если уровень кальция в сыворотке крови с поправкой на альбумин превышает 12 мг / дл, имеется значительная потеря костной массы, повреждение почек или камни. Существуют сложные вопросы лечения, связанные с удалением нейроэндокринных опухолей поджелудочной железы.Помимо своей роли в нормальном пищеварении, поджелудочная железа регулирует уровень глюкозы в крови за счет выработки инсулина. Удаление поджелудочной железы вызовет сахарный диабет, состояние, которое может привести к серьезным проблемам со здоровьем, и необходимо будет принимать добавки ферментов поджелудочной железы, чтобы способствовать пищеварению. Врачи должны сбалансировать преимущества удаления поджелудочной железы у человека с MEN1, такие как предотвращение развития рака, с риском развития сахарного диабета. Пациентов с нейроэндокринной опухолью поджелудочной железы, которая распространилась на печень, можно лечить аналогом соматостатина или лекарственным средством, регулирующим передачу сигналов в островковых клетках поджелудочной железы, эверолимусом.Другие нейроэндокринные опухоли обычно удаляются хирургическим путем, и могут быть рекомендованы другие методы лечения.
Опухоли гипофиза, продуцирующие гормон пролактин, чаще всего управляются с помощью агонистов дофамина, которые являются препаратами, которые имитируют действие дофамина, вещества природного происхождения, продуцируемого в мозге. Опухоли, которые продуцируют гормон роста или адренокортикоптропин или нефункциональные опухоли, чаще всего лечат хирургическим путем. Существует 2 гормональных метода лечения, аналог соматостатина и антагонист гормона роста, которые успешно используются для лечения слишком большого количества гормона роста у пациентов, которые не вылечены хирургическим путем.Узнайте больше о лечении опухолей гипофиза.
Узнайте больше о том, что ожидать при проведении общих тестов, процедур и сканирований.
Вопросы, которые следует задавать команде здравоохранения
Если вы беспокоитесь о риске эндокринной опухоли, проконсультируйтесь с врачом. Может быть полезно пригласить кого-то на ваши встречи, чтобы делать заметки. Подумайте о том, чтобы задать вашей медицинской команде следующие вопросы:
Каков риск развития нейроэндокринной опухоли?
Что я могу сделать, чтобы уменьшить риск других типов опухолей?
Какие у меня варианты скрининга?
Если вас беспокоит история вашей семьи и вы думаете, что у вас или других членов семьи может быть MEN1, подумайте над тем, чтобы задать следующие вопросы:
Увеличивает ли моя семейная история риск развития рака?
Это предполагает необходимость оценки риска рака?
Будете ли вы направить меня к генетическому консультанту или другому специалисту по генетике?
Должен ли я рассмотреть генетическое тестирование?
Связанные ресурсы
Генетика рака
Генетическое тестирование
Чего ожидать при встрече с генетическим консультантом
Сбор вашей семьи История рака
Обмен результатами генетического теста с вашей семьей
Семейное генетическое тестирование Q & A
Дополнительная информация
Американская поддержка множественной эндокринной неоплазии
http: // amensupport.org /
Ассоциация по поводу множественных эндокринных нарушений неоплазии (AMEND)
www.amend.org.uk
Национальный институт рака
www.cancer.gov
Чтобы найти генетического консультанта в вашем районе, спросите своего врача или посетите этот веб-сайт:
Национальное общество генетических консультантов
www.nsgc.org
1. Введение
Нейроэндокринные опухоли желудочно-кишечного тракта составляют группу гетерогенных новообразований с несколько непредсказуемым биологическим и клиническим поведением. Эти опухоли возникают в основном в пищеварительном тракте, но могут возникать в других органах, в которых находятся нейроэндокринные клетки. Они считаются сложными опухолями и имеют непредсказуемую клиническую эволюцию из-за разнообразия признаков, которыми они обладают в качестве потенциальной способности секреции большого разнообразия пептидов.
Хотя они могут появляться доброкачественные опухоли в течение определенного периода времени, они могут вызывать инфильтрацию тканей и давать метастазы. Все эти патофизиологические признаки нейроэндокринных опухолей, которые могут проявляться с различной степенью интенсивности у разных пациентов, вызывают общий интерес, и поэтому они изучаются профессионалами из разных областей знаний. В этой главе мы обратимся к изучению некоторых соответствующих аспектов этих опухолей, которые возникают в желудке. Однако, поскольку эти новообразования являются частью большого семейства опухолей желудочно-кишечного тракта, мы проведем краткий обзор основных признаков этого семейства, которые должны быть полезны для лучшего понимания некоторых нюансов этих опухолей, возникающих в желудке.
2. Общие аспекты нейроэндокринной желудочно-кишечной системы
Термины «нейроэндокринные опухоли», «карциноидные опухоли» и «эндокринные опухоли» широко используются применительно к опухолям пищеварительного тракта. Эти обозначения могут быть найдены одновременно даже как часть одной и той же классификации. Нейроэндокринные опухоли были впервые названы «карциноидными опухолями» немецким патологом Оберндорфером в 1907 году [1]. И до сих пор термин карциноид использовался якобы, в разговорной речи и даже почти во всех современных классификациях [2, 3].
Термин «апудома» также может рассматриваться как синоним карциноидной опухоли. Наименование «клетки APUD» было предложено Пирсом в конце 1960-х годов как аббревиатура от поглощения предшественника амина и декарбоксилирования [4]. Термин APUD суммирует некоторые из наиболее важных характеристик этих клеток, которые включают (а) высокое содержание амина и / или поглощение предшественника амина, (б) активность декарбоксилазы аминокислот и (в) характерный ультраструктурный характер. Первоначально термин «апудома» использовался главным образом с клинической точки зрения для обозначения этих опухолей у пациентов с симптомами, обусловленными патологической секрецией биоактивных продуктов, а затем и для клинически бессимптомных опухолей, происходящих из клеток APUD [5–7].Как мы видим, в отличие от корней других обозначений этих опухолей, термин «апудома» был получен из последовательной морфологической и биохимической основы.
Апудомы происходят из клеточной линии APUD и поэтому имеют характерный ультраструктурный паттерн, распознаваемый благодаря наличию в опухолевых клетках секреторных гранул, где расположены регуляторные пептиды, а также биогенных аминов, которые они продуцируют [8, 9]. Обычно клетки APUD богаты аминокислотной декарбоксилазой, которая дает им возможность захватывать 5-гидрокситриптофан и дигидроксифенилаланин и продуцировать, соответственно, серотонин и дофамин.Хотя это свойство не было продемонстрировано во всех клетках, морфологически характерных для этой системы, эта биохимическая связь может встречаться во всех из них независимо от их специфической функции. Это дает этим клеткам семейную, морфологическую и биохимическую связь, которая в большей или меньшей степени распространяется на апудомы. Кроме того, эти морфологические и биохимические характеристики придают термину «APUD» биологически более конкретное обозначение по сравнению с другими конфессиями. Таким образом, термин «апудома» менее подвержен временным изменениям, чем используемые в настоящее время, а именно «карциноид», «эндокринная опухоль» и «нейроэндокринная опухоль».Последнее наименование принимается в этой статье из-за его широкого использования в современных классификациях, а также во всей индексации медицинской литературы.
2.1. Места опухолей и окрашивание
Одним из первых шагов, как в патологии, так и в клиниках, когда мы сталкиваемся с возможностью поставить диагноз апудома желудочно-кишечного тракта, является знание его возможного первичного расположения (таблица 1). Это может показаться незначительной деталью, но это может быть очень полезным в качестве первого шага для лучшего понимания биологии опухоли [10, 11].
| Foregut | Midgut | Hindgut | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Пищевод | Тощей кишки / подвздошной кишки | Дистальная кишка | ||||||||||||
| Желудок | Приложение |
Таблица 1.
Первичные участки желудочно-кишечных апудом.
Апудомы могут возникнуть в любом регионе желудочно-кишечного тракта.Эти области известны как передняя кишка, средняя кишка и задняя кишка. Апудомы из этих разных сайтов часто представляют различное клиническое поведение.
Иногда мы имеем дело с неизвестным первичным участком метастазирования. Но знание того, какой сегмент пищеварительного тракта образует опухоль, может быть полезным, поскольку эта информация дает представление о возможном развитии апудомы. Что касается желудочных апудом, это важное знание, как мы увидим позже. Кроме того, патолог приобретает уверенность в изучении диагностических возможностей, в том числе для оценки того, какие методы окрашивания или какой нейроэндокринный маркер следует использовать [12].Большинство желудочных апудом не продуцирует серотонин и отрицательно влияет на окрашивание аргентаффином; с другой стороны, они обычно положительны для окрашивания аргирофильным и хромограниновым (рис. 1). Эти свойства апудомы по отношению к определенным методам окрашивания часто зависят от места их происхождения (таблица 2) [13–15].
Рисунок 1.
Хотя это неспецифическое окрашивание клеток APUD и апудом, аргентафиновые и аргирофильные пятна могут быть полезны для демонстрации этих элементов [13].
| Желудочно-кишечные апудомы и окрашивающие свойства серебра | |||
|---|---|---|---|
| Foregut | Midgut | Hindgut | |
| Аргирофильные новообразования | +++ | +++ | +++ |
| Аргентафиновые опухоли | + | +++ | + |
Таблица 2.
Почти все апудомы желудка демонстрируются с помощью аргирофильного окрашивания и / или методами аргентаффин.
++, редко положительный; ++, иногда отрицательный; +++, очень часто положительный
В настоящее время методы иммуногистохимии используются в качестве инструментов выбора для специфической гистологической диагностики апудом. С помощью этой методологии, он стремится отметить наличие антигенных продуктов, типичных для клеток APUD, а также часто присутствующих в апудомах (Рисунки 2 и 3). Нейрон-специфическая енолаза (NSE) была первым иммуногистохимическим маркером для гистологической диагностики апудом [16].До открытия этого маркера наиболее распространенными методами были окрашивание серебром. Синаптофизин также является нейроэндокринным маркером, расположенным на мембране синаптических везикул и присутствующим в нейронах, нейроэндокринных клетках и во многих нейроэндокринных опухолях [17, 18]. Хромогранины включают группу кислых полипептидов, которые составляют около 40–50% содержания растворимого белка в надпочечных медуллярных гранулах. Хромогранин А является наиболее распространенным; он присутствует в различных количествах в гранулах секреции нейроэндокринных клеток и в нейроэндокринных опухолях [15, 18].Если опухоль менее дифференцирована и с меньшим количеством секреторных гранул в цитоплазме, окрашивание может дать сомнительные результаты или даже ложноотрицательную реакцию. Хромогранин является одним из основных маркеров, используемых для гистологической диагностики желудочных апудом, характеризующихся высоким показателем чувствительности и специфичности. Он также предположительно используется в качестве серологического маркера развития апудомы [19]. Всегда уместно помнить, что антитела, используемые против антигенов апудомы, получены из разных клонов и поставляются разными компаниями.Это может привести к различиям в чувствительности и специфичности каждого набора реагентов, и эти различные свойства должны находиться под контролем каждой лаборатории.
Рисунок 2.
Некоторые нейроэндокринные маркеры разбросаны по цитоплазме клеток апудомы, такие как PGP 9.5, синаптофизин и нейрон-специфическая енолаза. Хромогранин и регуляторные пептиды хранятся в секреторных гранулах. Количество этих гранул в опухолевых клетках будет определять более слабое или более сильное окрашивание опухоли.
Рисунок 3.
(A) G-клетка слизистой оболочки желудка, окрашенная специфически антителом против гастрина. Окрашивание является очень специфичным, наблюдая, что фоновые элементы, то есть другие клетки и окружающие ткани, являются полностью отрицательными. Очень сильный контраст между положительными и отрицательными элементами ткани придает уверенность в конечном результате в отношении специфичности реакции окрашивания. (B) Контраст окрашивания не всегда очень четкий в отношении апудом, которые могут проявлять клетки с различной степенью дифференцировки.Переменное количество опухолевых клеток с низкой плотностью секреторных гранул может вызывать сомнительную или полностью отрицательную реакцию. В результате у данной гастриномы могут проявляться клетки, сильно реагирующие на антитело к гастрину, наряду с другими, полностью отрицательными.
2.2. Общий взгляд на патологию желудочно-кишечных апудом
Мы сейчас достигли точки, которая более касается непосредственно лечащего врача. Поскольку апудомы часто представляют непредсказуемую клиническую эволюцию, как гистопатология может помочь в этом вопросе? Фактически, все факторы, показанные в Таблице 3, важны для оценки возможного клинического поведения данной желудочно-кишечной апудомы.Однако две первые, то есть степень гистологической дифференцировки опухоли и пролиферативная активность опухолевых клеток, зависят исключительно от интерпретации патолога. И маловероятно, что последние четыре параметра, показанные в Таблице 3, зависят от мнения разных специалистов-специалистов, чтобы сделать более надежные выводы о клиническом течении опухоли.
Таблица 3.
Основные критерии определения злокачественного потенциала апудомы.
При общей патологии степень дифференцировки данной эпителиальной опухоли, оцениваемая по гистологии, всегда была и остается критерием, который вместе с другими дает представление о степени злокачественности, которой должна обладать конкретная карцинома. : менее агрессивная эволюция, более распространенная среди хорошо дифференцированных или более агрессивная эволюция, более распространенная у плохо дифференцированных (рис. 4).Этот гистопатологический критерий продолжает применяться в основном в отношении неэндокринных карцином. Что касается апудом, этот параметр, как изолированный элемент, имеет мало значения. Иными словами, хорошо дифференцированная апудома может представлять непредсказуемое клиническое поведение. Однако, когда опухоль гистологически слабо дифференцирована, прогноз часто ухудшается. В этом отношении этот критерий клеточной дифференцировки может быть полезным. Кроме того, в апудомах присутствуют различные плотности мембранных рецепторов для различных регуляторных пептидов, включая соматостатин.И высокая плотность этих рецепторов в клетках апудомы приобретает современное медицинское значение для лечения пациентов. Некоторые данные указывают на то, что плотность рецепторов соматостатина будет зависеть от степени опухоли [20].
Рисунок 4.
Желудочно-дифференцированные апудомы типа 1 (А) и плохо дифференцированные типы 2 (В). Хотя степень дифференцировки опухоли может иметь некоторое значение в отношении степени злокачественности, пролиферативная активность остается лучшим гистопатологическим показателем для этой цели.
С точки зрения гистопатологического диагноза потенциал злокачественности конкретной апудомы основывается главным образом на степени пролиферации опухолевых клеток. Этот критерий может применяться ко всем апудомам независимо от их происхождения. Существует два гистопатологических инструмента для оценки степени пролиферации клеток: (i) число наблюдаемых митозов в обычных препаратах, окрашенных гематоксилином и эозином , и (ii) индекс иммунореактивности клеток для антитела Ki-67.Реактивный белок Ki-67 экспрессируется только в ядре клеток, находящихся в различных фазах цикла активной репликации клеток. Этот белок не экспрессируется в покоящихся клетках, то есть клетках, которые еще не вступили в активный митотический цикл. Более того, не всегда существует какое-либо соответствие между степенью дифференцировки данной апудомы и степенью пролиферации клеток [21, 22].
Что касается пролиферативной активности, то опухоли низкой степени (G1) имеют очень небольшое количество митозов при обычной подготовке HE или иным образом менее 3% опухолевых клеток, окрашенных антителом Ki-67.В опухолях высокой степени (G3) должно быть более 20 митозов на 10 микроскопических мощных полей (hpf) или более 20% опухолевых клеток, позитивных к антителу Ki-67. Наконец, опухоли с промежуточной степенью пролиферации клеток, которые лежат между этими двумя крайностями, считаются G2.
2.3. Желудочные апудомы
Почти все апудомы желудка происходят из эндокринных клеток слизистой оболочки тела и реже из эндокринных клеток слизистой оболочки антрального отдела. Они составляют примерно 2–4% всех желудочных новообразований и 7.2% всех апудом желудочно-кишечного тракта [10].
В последние десятилетия появились свидетельства того, что мы верим в увеличение частоты возникновения желудочных апудом. В значительной степени это увеличение должно происходить из-за технологического развития инструментов, связанных с эндоскопией верхних отделов пищеварительного тракта, потому что эти опухоли чаще всего обнаруживаются случайно во время эндоскопии. Однако нельзя исключать реального увеличения распространенности этих опухолей [11, 23, 24].
Апудомы желудка обычно делятся на три различные группы в зависимости от их клинических и физиопатологических характеристик: тип 1 – апудомы желудка, связанные с атрофическим гастритом тела (ABG), с пернициозной анемией или без нее; тип 2 – апудомы желудка, связанные с синдромом Золлингера-Эллисона, спорадические или семейные; и тип 3 – спорадическая апудома, не связанная с известным предрасполагающим заболеванием [25].
2.4. Желудочная апудома типа 1
Это наиболее частые нейроэндокринные опухоли желудка.Они характерно связаны с атрофическим гастритом тела (ABG) и являются наиболее частыми из желудочных апудом, составляющих около 70–80% из них. Критерием, принятым для классификации этих опухолей по типу 1, является признание наличия установленного хронического аутоиммунного гастрита с пернициозной анемией или без нее или просто наличие атрофического гастрита тела, подтвержденного гистопатологией. Этот тип опухоли, как представляется, является более распространенным среди женщин, а также распространенность основного заболевания (рис. 5).
Рисунок 5.
Распределение 196 пациентов с атрофическим гастритом тела в зависимости от возраста и пола. Пациенты находились в больнице общего профиля в Белу-Оризонти, Бразилия [26].
Следовательно, можно предположить, что этот тип опухоли является прямым следствием атрофического гастрита организма. Согласно этому диагностическому критерию, мы можем заключить, что различные типы апудом желудка не могут быть диагностированы, основываясь только на их эндоскопической и гистопатологической структуре.Следовательно, для включения или исключения желудочной апудомы как типа 1 необходимо, чтобы в дополнение к гистологическим образцам самой опухоли у нас также были образцы слизистой оболочки желудка антрального отдела и областей тела желудка, чтобы подтвердить или исключить возможность атрофического гастрита тела. Признание эндокринной опухоли как типа 1 открывает ряд возможностей для лучшего понимания ряда патофизиологических изменений, которые могут происходить у пациента:
Апудома желудка типа 1 встречается в слизистой оболочке глазного дна или в желудке в целом как множественные узелки размером менее 1 см в большинстве случаев.Поскольку они, как правило, являются множественными, они могут возникать в соответствии с нерегулярным распределением в теле желудка, на глазном дне желудка или в двух областях одновременно (таблица 4). Обычно эти узелки проецируются в просвет желудка и часто с помощью эндоскопии диагностируются как «полипы желудка». Этот диагноз не всегда неверен, потому что в АБГ гиперпластические полипы встречаются относительно часто.
Неоплазия обычно состоит из хорошо дифференцированных нейроэндокринных клеток с низким индексом Ki-67 (G1), указывающим на низкие уровни пролиферации клеток.Эта характеристика согласуется с ленивой эволюцией этих опухолей; только небольшое количество из них имеет метастазы при постановке диагноза и редко приводит пациента к смерти (Таблица 4).
Из-за атрофии слизистой оболочки у этих пациентов наблюдается гипохлоргидрия или ахлоргидрия.
Поскольку слизистая оболочка желудка тела атрофична и слизистая оболочка антрального отдела желудка сохраняется, G-клетки обычно гиперфункционируют, и у этих пациентов часто наблюдается гипергастринемия (таблица 4 и рисунок 6).
Даже без высокого уровня сывороточного гастрина постоянные трофические стимулы этого гормона приводят к гиперплазии эндокринных клеток желудочного организма. Эти гиперпластические клетки, как полагают, являются энтерохромаффиноподобными (ECL) клетками. Однако в этом гиперпластическом процессе могут участвовать другие типы нейроэндокринных клеток, в том числе клетки, продуцирующие грелин [26]. Области гиперплазии нейроэндокринных клеток можно обнаружить почти во всех случаях хорошо известного атрофического гастрита тела (рис. 7–9).Как мы уже говорили, эти области эндокринной гиперплазии встречаются вдоль атрофической слизистой оболочки и в соответствии с их морфологическим аспектом могут быть классифицированы как (i) диффузные, (ii) линейные и (iii) узловые [27].
Основываясь на этих общих аспектах атрофического гастрита тела, можно сделать вывод, что области нейроэндокринной гиперплазии, вероятно, являются предшественником поражения желудочной апудомы типа 1. Тем не менее, нет гистологических признаков, которые подчеркивают, где заканчивается гиперплазия и где начинается новообразование.В связи с этим, крупные, слившиеся гиперпластические узелки диаметром около 300-500 мкм, связанные с инфильтрацией тканей слизистой оболочки, уже будут классифицироваться как признак появления новообразования (рис. 9). Просто для сравнения, 500 мкм эквивалентны в среднем половине толщины нормальной оксинитной слизистой оболочки в фиксированных формалином гистологических срезах.
Проникновение в подслизистую оболочку гиперпластических эндокринных клеток уже является признаком злокачественного поведения. Тем не менее, по большей части, эти желудочные апудомы типа 1 демонстрируют индолентную эволюцию, и лишь немногие из них имеют метастазы на момент постановки диагноза (Таблица 4).
| Тип 1 | Тип 2 | Тип 3 | ||
|---|---|---|---|---|
| Частота (%) | 70–80 | 5–10 | 10–15 | |
| Эндоскопический обзор | Множественные и малые | Множественные и малые | Одиночный (> 2 см) | |
| Зона | Тело желудка / глазное дно | Тело желудка / глазное дно | Любой регион | |
| Индекс клеточной пролиферации | G1 | G1 / G2 | G3 | |
| Гастринемия | Обычно высокое | Обычно высокое | Нормальное | |
| Метастазирование (%) | 2–5 | 10–30 | 50–100 |
Таблица 4.
Дифференциальные профили между тремя группами желудочных апудом.
Рисунок 6.
Рисунок, показывающий патогенетические механизмы желудочных апудом типа 1 и типа 2. Центральным патофизиологическим механизмом, связанным с этими двумя типами опухолей, является возникновение гипергастринемии или персистирующей надбазальной гастринемии.
Рисунок 7.
Диффузный и линейный типы гиперплазии эндокринных клеток при атрофическом гастрите тела. Гиперпластические клетки окрашиваются на хромогранин.
Рисунок 8.
Узловой тип гиперплазии эндокринных клеток при атрофическом гастрите тела. Гиперпластические клетки образуют небольшие узелки в собственной пластинке. Окрашивание хромогранином.
Рисунок 9.
Эндокринная клетка, образующая крупные гиперпластические узелки в собственной пластинке. Этот тип поражений может свидетельствовать о появлении апудомы желудка. Поскольку эти опухоли могут быть многоцентровыми, возможно, что более сильные подозрения поражения встречаются в других областях слизистой оболочки желудка.Окрашивание хромогранином.
2.5. Желудочная апудома типа 2
Желудочная апудома типа 2 – это те, которые связаны со спорадическим или семейным синдромом Золлингера-Эллисона. На их долю приходится всего 5–6% желудочных апудом. Почти всегда эти опухоли встречаются у пациентов с множественной эндокринной неоплазией (MEN) типа 1. Редко, также существует синдром Золлингера-Эллисона (ZES), не связанный с множественной эндокринной неоплазией (MEN), которая приводит к развитию желудочной апудомы. В этом случае ZES может быть обусловлено наличием спорадической гастриномы, основным местом которой, как полагают, является хвост поджелудочной железы.Таким образом, чаще всего пациент, страдающий желудочной апудомой типа 2, может быть носителем генетической передачи синдрома MEN. MEN-1 – это наследственный аутосомно-доминантный синдром, вызванный инактивирующей мутацией гена MEN-1, который является геном-супрессором опухоли. Синдром MEN-1 может включать развитие первичного гиперпаратиреоза, опухолей островков поджелудочной железы и аденом гипофиза. Кроме того, у некоторых пациентов могут развиться другие новообразования, такие как опухоли щитовидной железы, аденомы надпочечников, феохромоцитомы и нейроэндокринные опухоли, в основном из области гастродуоденальной зоны.
2.6. Желудочная апудома типа 3
Желудочные апудомы типа 3 известны как спорадические опухоли желудка, на которые приходится около 10–15% всех желудочных апудом, и развиваются независимо от гипергастринемии, а также от гиперплазии эндокринных клеток желудка (Таблица 4). Чаще всего они представляют собой одну полипоидную опухоль, обычно размером более 2 см [28]. Эти опухоли состоят в основном из энтерохромаффиноподобных клеток и, в отличие от других апудом желудка, имеют агрессивную клиническую эволюцию.Эти опухоли имеют гистопатологические признаки, соответствующие клинической эволюции худшего прогноза, такого как ангиоинвазия, быстрый рост, митотическая активность и высокий индекс Ki-67.
Множественная эндокринная неоплазия типа 1
Что такое множественная эндокринная неоплазия типа 1 (MEN1)?
MEN1 является наследственным заболеванием, которое вызывает опухоли в эндокринных железах и двенадцатиперстной кишке, первой части тонкой кишки. MEN1 иногда называют множественным эндокринным аденоматозом или синдромом Вермера, после того, как один из первых врачей узнал его. MEN1 встречается редко, встречается примерно у одного из 30000 человек. 1 Расстройство затрагивает оба пола в равной степени и не имеет никаких географических, расовых или этнических предпочтений.
Эндокринные железы выделяют гормоны в кровоток. Гормоны – это мощные химические вещества, которые путешествуют по крови, контролируя и инструктируя функции различных органов. Как правило, гормоны, выделяемые эндокринными железами, тщательно сбалансированы для удовлетворения потребностей организма.
У MEN1 сверхактивные железы могут включать околощитовидные железы, поджелудочную железу или гипофиз.У людей с MEN1 множественные эндокринные железы образуют опухоли и становятся гормонально гиперактивными, часто в одно и то же время.Гиперактивные железы могут включать околощитовидные железы, поджелудочную железу или гипофиз. Большинство людей, у которых развивается гиперактивность только одной эндокринной железы, не имеют MEN1.
Как MEN1 влияет на эндокринные железы и двенадцатиперстную кишку?
Паращитовидные железы
Паращитовидные железы – эндокринные железы, наиболее ранние и наиболее часто поражаемые MEN1. Тело обычно имеет четыре околощитовидные железы, которые расположены близко к щитовидной железе в передней части шеи. Паращитовидные железы выпускают в кровоток химическое вещество под названием гормон паращитовидной железы (ПТГ), которое помогает поддерживать нормальный запас кальция в крови, костях и моче.
Гиперпаратиреоз
У мужчин1 все четыре околощитовидные железы имеют тенденцию к повышенной активности, вызывая гиперпаратиреоз. Паращитовидные железы образуют опухоли, которые выделяют слишком много ПТГ, что приводит к избытку кальция в крови. Высокий уровень кальция в крови, известный как гиперкальциемия, может существовать в течение многих лет, прежде чем он будет обнаружен случайно или в результате скрининга MEN1. Нераспознанная гиперкальциемия может вызвать избыток кальция в моче, что приведет к камням в почках или повреждению почек. Кроме того, кости могут терять кальций и ослабевать.
Почти у каждого, кто наследует восприимчивость к MEN1, развивается гиперпаратиреоз к 50 годам, но расстройство часто можно обнаружить до 20 лет. Гиперпаратиреоз может не вызывать проблем в течение многих лет, или он может вызывать усталость, слабость, боль в мышцах или костях, запор , расстройство желудка, камни в почках или истончение костей.
Врачи должны решить, является ли гиперпаратиреоз у мужчин1 достаточно серьезным, чтобы нуждаться в лечении, особенно у человека, у которого нет симптомов. Обычное лечение – это операция по удалению большинства или всех паращитовидных желез.Одним из вариантов является удаление трех самых больших желез и все, кроме небольшой части четвертого. Другой – удалить все четыре железы и одновременно пересадить небольшую часть одной железы в предплечье. Поддерживая часть одной железы, трансплантат паращитовидной железы продолжает выпускать ПТГ в кровоток, чтобы выполнять свою работу.
После операции на паращитовидной железе следует продолжить регулярное тестирование кальция в крови, потому что часто маленький кусочек оставшейся ткани околощитовидной железы увеличивается и вызывает рецидив гиперпаратиреоза.Если оставшаяся часть находится в предплечье и требуется дополнительная операция для удаления большего количества ткани околощитовидной железы, операцию на руке можно проводить под местной анестезией.
Иногда все четыре железы полностью удаляются, чтобы предотвратить рецидив, или могут быть случайно удалены во время операции на паращитовидной железе. Люди, у которых полностью удалены паращитовидные железы, должны ежедневно принимать добавки кальция и витамина D или другое связанное с этим лечение, чтобы предотвратить гипокальциемию или низкий уровень кальция в крови.
поджелудочной железы и двенадцатиперстной кишки
Расположенная за желудком, поджелудочная железа выполняет две основные функции: выпускать пищеварительные соки в кишечник и ключевые гормоны в кровоток. Двенадцатиперстная кишка является первой частью тонкой кишки рядом с поджелудочной железой. Гормоны поджелудочной железы обычно вырабатываются небольшими скоплениями специализированных клеток, называемых островками поджелудочной железы. Некоторые из основных гормонов, вырабатываемых островками поджелудочной железы,
- инсулин снижает уровень глюкозы в крови, также называемый сахар в крови
- глюкагон-повышает уровень глюкозы в крови
- -соматостатин-ингибирует секрецию некоторых других гормонов
- вазоактивный кишечный пептид (VIP) вызывает кишечные клетки, чтобы секретировать воду в кишечник
- гастрина – заставляет желудок вырабатывать кислоту для пищеварения
Гастриномы
У MEN1 гастрин может быть секретирован опухолями, называемыми гастриномами в поджелудочной железе, двенадцатиперстной кишке и лимфатических узлах.При воздействии слишком большого количества гастрина желудок выделяет избыток кислоты, что приводит к образованию тяжелых язв в желудке и тонкой кишке. Кроме того, слишком много гастрина обычно вызывает серьезную диарею.
Люди с MEN1 имеют вероятность развития гастрином от 20 до 60 процентов. 2 Заболевание, связанное с этими опухолями, называется синдромом Золлингера-Эллисона. Язвы, вызванные нелеченными гастриномами, намного более опасны, чем типичные язвы желудка или кишечника.Если их не лечить, они могут вызвать разрыв желудка или кишечника и даже смерть.
Гастриномы, связанные с MEN1, нелегко вылечить с помощью опухолевой хирургии, потому что трудно обнаружить множество мелких гастрином в поджелудочной железе, двенадцатиперстной кишке и лимфатических узлах. Основой лечения являются мощные лекарства, называемые ингибиторами кислотных насосов, которые блокируют выделение желудочной кислоты. Взятые внутрь, эти лекарства доказали свою эффективность в борьбе с осложнениями избытка гастрина в большинстве случаев синдрома Золлингера-Эллисона.
Редкие осложнения поджелудочной железы
Иногда у человека с MEN1 развивается островковая опухоль поджелудочной железы, которая выделяет высокий уровень гормонов. Например, инсулиномы вырабатывают слишком много инсулина, вызывая гипогликемию или низкий уровень глюкозы в крови. Около 10 процентов взрослых с MEN1 развивают инсулиномы. 3 Редкие опухоли поджелудочной железы могут выделять слишком много глюкагона, что может вызвать диабет, или слишком много VIP, что может вызвать водянистую диарею. Опухоли, которые секретируют адренокортикотропин (АКТГ), также могут возникать в поджелудочной железе.АКТГ обычно секретируется гипофизом и стимулирует надпочечники вырабатывать кортизол, гормон, который помогает организму реагировать на стресс. Опухоли в поджелудочной железе также могут редко секретировать гонадотропин-рилизинг-гормон (ГнРГ). ГнРГ обычно секретируется гипоталамусом и стимулирует гипофиз к выделению фолликулостимулирующего гормона (ФСГ), который регулирует фертильность у мужчин за счет выработки сперматозоидов и у женщин за счет овуляции. В целом, хирургия является основой лечения этих необычных типов опухолей.
Гипофиз
Гипофиз, маленькая железа, расположенная у основания мозга, производит много важных гормонов, которые регулируют основные функции организма. Нормальные основные гормоны гипофиза
- пролактин-контролирует образование грудного молока и влияет на фертильность и прочность костей
- гормон роста-регулирует рост тела, особенно в подростковом возрасте
- АКТГ-стимулирует надпочечники для производства кортизола
- тиреотропин-стимулирует щитовидную железу для производства гормонов щитовидной железы, которые регулируют обмен веществ
- лютеинизирующий гормон стимулирует яичники или яички для производства половых гормонов
- ФСГ-регулирует рождаемость
Пролактиномы
Гипофиз становится гиперактивным у каждого четвертого человека с МЕН1. 4 Эту сверхактивность обычно можно проследить до небольшой опухоли в железе, которая выделяет слишком много пролактина, называемой пролактиномой. Высокий уровень пролактина может вызвать чрезмерное производство грудного молока или повлиять на фертильность у женщин или на половое влечение и фертильность у мужчин.
Лечение может не потребоваться при пролактиномах. Если необходимо лечение, лекарство, известное как агонист дофамина, может эффективно уменьшить опухоль и снизить выработку пролактина. Иногда пролактиномы плохо реагируют на это лекарство.В таких случаях может потребоваться операция, облучение или и то, и другое.
Редкие осложнения гипофиза
Редко, MEN1 создает опухоли гипофиза, которые выделяют большое количество АКТГ, что, в свою очередь, стимулирует надпочечники вырабатывать избыток кортизола. Слишком много кортизола может привести к мышечной слабости, ослабленным костям и переломам, а также истончению кожи, среди других проблем. Опухоли гипофиза, которые вырабатывают гормон роста, вызывают чрезмерный рост или повреждение костей. В целом, хирургия является основой лечения этих необычных типов опухолей.
Рак опухоли, связанные с MEN1?
Опухоли, связанные с MEN1, обычно доброкачественные, то есть они не злокачественные. Тем не менее, они могут нарушать нормальную функцию, высвобождая гормоны или скучивая близлежащие ткани. Например, пролактинома может стать довольно большой у кого-то с MEN1. По мере роста опухоль может давить и повредить нормальную часть гипофиза или нервы для зрения. Иногда нарушение зрения является первым признаком опухоли гипофиза у человека с MEN1.
Другим типом доброкачественной опухоли, наблюдаемой примерно у трети людей с MEN1, является жировая опухоль сливового размера, называемая липомой, которая растет под кожей. Липомы не вызывают проблем со здоровьем и при желании могут быть удалены простой косметической хирургией.
Доброкачественные опухоли не распространяются и не проникают в другие части тела. Раковые клетки, напротив, отделяются от первичной опухоли и распространяются или метастазируют в другие части тела через кровоток или лимфатическую систему. Опухоли поджелудочной железы, связанные с MEN1, имеют тенденцию быть многочисленными и небольшими, но большинство из них доброкачественные и не выделяют в кровь активные гормоны.Со временем гастриномы могут стать злокачественными, но обычно они медленно растут.
В конце концов, примерно у половины людей с MEN1 разовьется раковая опухоль поджелудочной железы или карциноид. Карциноид – это медленно растущая эндокринная опухоль внутри груди или желудка человека с MEN1. Хотя карциноиды возникают из эндокринных клеток, которые присутствуют во многих частях тела, они редко выделяют гормон у человека с MEN1. Карциноиды желудка обычно не требуют лечения.
Лечение эндокринного рака поджелудочной железы у мужчин1
Поскольку тип эндокринного рака поджелудочной железы, связанный с MEN1, трудно распознать, трудно лечить и он медленно прогрессирует, у врачей разные взгляды на ценность хирургического вмешательства при лечении этих опухолей.
Один из подходов состоит в том, чтобы «наблюдать и ждать», используя медицинские или нехирургические методы лечения. Согласно этой точке зрения, хирургия поджелудочной железы имеет серьезные осложнения, поэтому ее не следует пытаться проводить, если она не излечит опухоль или не излечит состояние с избытком гормонов.
Другая школа выступает за раннюю хирургию, возможно, когда опухоль вырастет до определенного размера, для предотвращения или лечения эндокринного рака поджелудочной железы – даже если опухоль не выделяет слишком много гормона – до распространения рака. Однако нет четких доказательств того, что операция по предотвращению распространения рака поджелудочной железы на самом деле ведет к увеличению выживаемости пациентов с MEN1.
Врачи сходятся во мнении, что необходимо лечить чрезмерное выделение определенных гормонов, главным образом гастрина, из эндокринного рака поджелудочной железы у мужчин1, и лекарства часто эффективны для блокирования эффектов этих гормонов. Некоторые опухоли, такие как инсулиномы, обычно доброкачественные и единичные и излечимы хирургией поджелудочной железы. Такая операция должна быть тщательно продумана в каждом случае пациента.
Является ли MEN1 одинаковым во всех?
Хотя MEN1 имеет тенденцию следовать определенным моделям, это может повлиять на здоровье человека разными способами.Мало того, что опухоли MEN1 варьируются среди членов одной семьи, но некоторые семьи с MEN1, как правило, имеют более высокий уровень пролактин-секретирующих опухолей гипофиза и значительно более низкую частоту гастрин-секретирующих опухолей.
Возраст, в котором MEN1 может начать вызывать гиперактивность эндокринных желез, может сильно различаться у разных членов семьи. У одного человека может быть только умеренный гиперпаратиреоз, начинающийся в 50 лет, в то время как у родственника могут развиться осложнения от опухолей околощитовидной железы, поджелудочной железы и гипофиза к 18 годам.
Как определяется MEN1?
MEN1 определяется с помощью генного тестирования или, когда генное тестирование недоступно или дает отрицательный результат, с помощью лабораторных тестов, которые измеряют уровни гормонов. Реже, MEN1 диагностируется на основе медицинской и семейной истории человека.
Генетика носителей MEN1 и MEN1
У человека с MEN1 существует мутация или ошибка в гене MEN1 в каждой клетке тела человека. Было выявлено много различных мутаций гена MEN1.Каждая из этих мутаций может вызывать один и тот же спектр опухолей MEN1. Определенная мутация MEN1 в теле человека может быть молчаливой, то есть у человека нет симптомов, как у новорожденного. Или мутация MEN1 может быть выражена как синдром MEN1. Человек с мутацией MEN1, проявляющий симптомы или нет, называется носителем мутации MEN1 или носителем синдрома MEN1.
MEN1 является аутосомно-доминантным геном, что означает, что он наследуется ребенком от одного из родителей, у которого есть мутация MEN1.
Тестирование генов
Генетическое тестирование может определить, является ли человек носителем мутации MEN1. После идентификации носители проходят примерно ежегодное тестирование, процесс, называемый скринингом, на наличие биохимических признаков развивающейся опухоли. Родственники, у которых в семье обнаружено отсутствие мутации MEN1, могут быть освобождены от скрининга на MEN1. Ограниченное число лабораторий в Соединенных Штатах Америки предлагает тестирование генов MEN1 для выявления и выявления мутаций MEN1. Генные тесты дороги и могут занимать много времени.Как только у человека обнаруживается определенная мутация, генный тест для родственников становится проще и дешевле.
В 10-30 процентах семей с MEN1 мутации не обнаружено. 5 Тем не менее, неопознанная мутация MEN1 все еще может быть вероятной. Иногда человек с MEN1 не знает ни о каком другом случае MEN1 среди родственников. Наиболее распространенным объяснением является то, что знание истории здоровья семьи является неполным. Реже человек несет новую мутацию гена MEN1.
Генное тестирование может быть предложено людям, которые
- соответствуют клиническим критериям для MEN1 при наличии как минимум двух из следующих: увеличенные околощитовидные железы, эндокринная опухоль поджелудочной железы или двенадцатиперстной кишки или опухоль гипофиза
- не соответствуют клиническим критериям, но есть подозрение на наличие MEN1 – например, те, у кого множественные опухоли паращитовидной железы до 30 лет
- являются родственниками первой степени людей с MEN1 – детьми, братьями или сестрами, что дает им 50-процентный шанс унаследовать мутацию
Роль генетического консультирования
Генетическое консультирование может помочь членам семьи понять, как результаты теста могут повлиять на них индивидуально и в семье.Генетическое консультирование может включать обзор и обсуждение психосоциальных преимуществ и рисков генетического тестирования. Результаты генетического тестирования могут повлиять на самооценку, самооценку и личность и личность семьи. В генетическом консультировании могут быть рассмотрены вопросы, касающиеся того, как и с кем будут передаваться результаты генетических тестов, и их возможное влияние на важные вопросы, такие как страхование здоровья и страхование жизни. Эти обсуждения могут происходить, когда член семьи решает, следует ли продолжить генное тестирование, и снова позже, когда станут доступны результаты теста.Врач, медсестра или специалист по генетике предоставляет генетические консультации.
Лабораторные тесты
Лабораторные тесты могут проводиться периодически для выявления опухолей MEN1. Скрининг может выявить опухоли на ранних стадиях их развития, выявить опухоли, которые вернулись, и определить, насколько они велики и где они расположены. Раннее выявление развития опухоли позволяет врачам предпринять шаги, чтобы предотвратить возникновение серьезных осложнений у людей с MEN1. Типы тестов, используемых для скрининга опухолей, могут включать
- анализов крови – например, для измерения инсулина или ПТГ для выявления избыточной выработки гормонов опухолью MEN1.
- других биохимических тестов – например, для измерения кальция в моче, чтобы обнаружить результаты избыточного производства гормонов.
- иммунорадиометрических анализов, типа анализа крови, например, для измерения ПТГ для выявления опухолей околощитовидной железы. Тесты визуализации
- – например, ультразвук, компьютерная томография (КТ) и магнитно-резонансная томография (МРТ), позволяющие врачу обнаруживать опухоли, которые не секретируют гормоны. Поскольку визуальные тесты дороже, они, как правило, проводятся реже, чем анализы крови.
Типы выполняемых испытаний зависят от цели проверки. Периодический скрининг на опухоли MEN1 может иметь две разные цели:
- Распознать возможных носителей MEN1. Во-первых, может быть проведен скрининг для определения того, является ли человек носителем мутации MEN1. Этот скрининг включает в себя близких родственников человека, о котором известно, что он носит мужчин1. Хотя генное тестирование является одним из способов идентификации носителя MEN1, иногда эти другие методы используются из-за нехватки ресурсов или из-за того, что основная мутация не может быть идентифицирована.С этой целью скрининга тесты направлены на опухоли, которые являются наиболее частыми и развиваются наиболее рано. Примеры этих тестов включают тесты на ПТГ, кальций и пролактин.
- Для выявления ранних опухолей у известных носителей MEN1. Во-вторых, скрининг может проводиться на известных носителях MEN1 для выявления любой опухоли, которая может развиться в результате мутации. Это периодическое тестирование может распознать опухоль рано, чтобы оптимизировать ее лечение. Когда человек является известным носителем MEN1, проводится более детальное тестирование для выявления некоторых из менее вероятных, но все же вредных опухолей.
Лабораторные тесты на опухоли MEN1 можно повторять ежегодно, не дожидаясь появления симптомов. Это тестирование может начаться в возрасте 5 лет. У известных носителей тесты визуализации могут проводиться каждые 3 года для выявления опухолей, которые невозможно обнаружить при других лабораторных исследованиях.
Если индивидуальные тесты нормальные, периодическое тестирование опухоли должно продолжаться бесконечно. Однако, недоказанный носитель с нормальными тестами после 50 лет вряд ли унаследовал мутацию гена MEN1.
Можно ли вылечить MEN1?
MEN1 не может быть вылечена, но регулярное тестирование может обнаружить многие проблемы, вызванные опухолями MEN1 за много лет до развития серьезных осложнений. Раннее обнаружение этих опухолей позволяет врачам начать профилактическое лечение, уменьшая вероятность того, что MEN1 позже вызовет проблемы.
Даже после лечения остаточная ткань может отрастать или могут поражаться другие железы. Периодический и тщательный мониторинг позволяет врачам корректировать лечение индивидуума по мере необходимости и проверять наличие новых проблем, вызванных MEN1.У большинства людей с MEN1 долгая и продуктивная жизнь.
Должен ли человек, у которого есть MEN1, избегать детей?
Лицу, у которого есть MEN1 или у которого есть мутация гена MEN1, может быть трудно решить, иметь ли ребенка. Вот некоторые факты, которые следует учитывать:
- Мужчина или женщина с MEN1 подвержены риску 50-50 при каждой беременности иметь ребенка с MEN1.
- MEN1 имеет тенденцию соответствовать широкой схеме в пределах данной семьи, но тяжесть расстройства сильно варьируется от одного члена семьи к другому.В частности, опыт родителей с MEN1 не может быть использован для прогнозирования возможной степени тяжести MEN1 у ребенка.
- Опухоли, возникающие в результате MEN1, обычно не развиваются до зрелого возраста. Лечение может потребовать регулярного мониторинга и значительных затрат, но болезнь обычно не мешает активной, продуктивной взрослой жизни.
- Пролактин-высвобождающие опухоли у мужчины или женщины с MEN1 могут подавлять фертильность и затруднять зачатие.
- Гиперпаратиреоз во время беременности может повысить риск осложнений для матери и ребенка.
- Беременность обычно нормальная для матери или ребенка, который является носителем MEN1.
Генетические консультанты и другие профессионалы могут предоставить информацию, чтобы помочь с процессом принятия решения, но они не скажут отдельным лицам или парам, какое решение принять или как сделать это.
очков, которые нужно запомнить
- Множественная эндокринная неоплазия типа 1 (MEN1) является наследственным заболеванием, которое вызывает гормон-секретирующие опухоли двенадцатиперстной кишки и эндокринных желез, чаще всего околощитовидной железы, поджелудочной железы и гипофиза.
- Гиперактивные околощитовидные железы могут привести к усталости, слабости, мышечным или костным болям, запорам, несварению желудка, камням в почках или истончению костей.
- Эндокринные опухоли поджелудочной железы и двенадцатиперстной кишки, называемые гастриномами, могут вызывать опасные язвы желудка или кишечника.
- Опухоли гипофиза, называемые пролактиномами, могут вызвать чрезмерное производство грудного молока или повлиять на фертильность у женщин или на половое влечение и фертильность у мужчин.
- Хотя многие опухоли, связанные с MEN1, являются доброкачественными, примерно у половины людей с MEN1 в конечном итоге разовьется раковая опухоль.
- носителей MEN1 могут быть обнаружены с помощью генного тестирования или других лабораторных тестов.
- MEN1 невозможно вылечить, но регулярное тестирование может выявить проблемы, вызванные опухолями MEN1, за много лет до развития серьезных осложнений. Тщательный мониторинг позволяет врачам корректировать лечение индивидуума по мере необходимости.
Отзывы
[1] White ML, Doherty GM. Множественная эндокринная неоплазия. Клиника хирургической онкологии Северной Америки . 2008; 17: 439-459.
[2] Jensen RT. Ведение синдрома Золлингера-Эллисона у пациентов с множественной эндокринной неоплазией 1 типа. Journal of Internal Medicine. 1998; 243 (6): 477–488.
[3] Ларсен П.Р., Кроненберг Х.М., Мелмед С., Полонский К.С., ред. Уильямс Учебник по эндокринологии. 10-е изд. Филадельфия: Сондерс; 2003.
[4] Gardner DG, Shoback D, eds. Базовая и клиническая эндокринология Гринспена. 8-е изд. Нью-Йорк: Макгроу-Хилл; 2007.
[5] Ozawa A, Agarwal SK, Mateo CM, et al.Вариант MEN1 с паращитовидной железой / гипофизом обычно имеет причины, отличные от мутаций p27Kip1. Журнал клинической эндокринологии и обмена веществ. 2007; 92: 1948–1951.
Клинические испытания
Национальный институт диабета, болезней органов пищеварения и почек (NIDDK) и другие компоненты Национального института здоровья (NIH) проводят и поддерживают исследования многих заболеваний и состояний.
Что такое клинические испытания и подходят ли они вам?
Клинические испытания являются частью клинических исследований и лежат в основе всех достижений медицины.Клинические испытания смотрят на новые способы предотвращения, выявления или лечения заболеваний. Исследователи также используют клинические испытания для изучения других аспектов медицинской помощи, таких как улучшение качества жизни людей с хроническими заболеваниями. Узнайте, подходят ли вам клинические испытания.
Какие клинические испытания открыты?
Клинические испытания, которые в настоящее время открыты и проходят набор, можно посмотреть на www.ClinicalTrials.gov.
Эта информация может содержать информацию о медикаментах и, если их принимать по назначению, условия, которые они лечат.Когда подготовлено, этот контент включал самую последнюю доступную информацию. Для получения обновлений или для вопросов о любых лекарствах, свяжитесь с Управлением по контролю за продуктами и лекарствами США по бесплатному телефону 1-888-INFO-FDA (1-888-463-6332) или посетите www.fda.gov. Проконсультируйтесь с вашим врачом для получения дополнительной информации.
,Последнее обновление 15 мая 2020 г. в 17:04
Пилорический стеноз
Пилорический стеноз это состояние, которое в основном наблюдается в педиатрии. Это происходит во-вторых, гипертрофии и гиперплазии мышечных слоев пилоруса, наиболее дистальной части желудка. Это ухудшает опорожнение содержимого желудка в двенадцатиперстную кишку. В запущенных случаях может стать расширение желудка из-за обструкции.
Симптомы включают колики и метательную рвоту, которые в тяжелых случаях могут привести к эксиккозу.Рвота не содержит желчи, что может вызвать подозрение на стеноз привратника. Голод также возможен.
Небольшое примечание: по определению рвота – это сильная рвота из содержимого желудка из-за повышенного внутрибрюшного и внутрижелудочного давления. Если это происходит насильственно, может ли рвота быть классифицирована как «метательная» рвота. Младенцев обычно не рвут таким образом – они просто срыгивают немного молока без какого-либо значительного увеличения давления. Снарядная рвота у детей всегда должна вызывать подозрение, что что-то не так.
Причиной стеноза привратника у детей является многофакторная. Есть некоторые генетические факторы, связанные с аномальной иннервацией и другими вещами, и некоторые факторы окружающей среды, такие как воздействие макролидных антибиотиков, таких как эритромицин.
У взрослых это может произойти из-за опухолей, рубцовой пептической язвы, или из-за эффектов наркотиков или алкоголя. Наркотики и алкоголь могут вызывать преходящие пилорические спазмы.
Лечение детского стеноза привратника желудка – это операция в тяжелых случаях, однако многие случаи являются самоограничивающимися.
желудочная атония
Атония желудка, более известная как гастропарез, возникает, когда мышцы желудка парализованы. Это происходит чаще всего из-за вегетативной невропатии, часто из-за диабета или уремии, но это может также произойти после абдоминальной хирургии. Это соответствует очень проксимальному типу паралитического кишечника.
Атония нарушает смешанные и перистальтические движения, и из-за этого желудок не может опорожнять свое содержимое по направлению к кишечнику или назад через рвоту.Поэтому увеличивается пассивное растяжение стенки, что стимулирует выделение желудочного сока. Объем желудка быстро увеличивается, вызывая больше растяжения и секреции. Поскольку плазма является единственным источником секретируемого желудочного сока, развивается быстрый эксиккоз и / или гиповолемический шок.
Демпинг-синдром
Синдром демпинга – это состояние, при котором опорожнение желудка происходит слишком рано. Наиболее распространенной причиной является хирургический желудочно-кишечный анастомоз (желудочный шунт). Существует два типа: синдром раннего демпинга и синдром позднего демпинга, в зависимости от того, как долго после еды появляются симптомы.У некоторых людей есть обе формы.
У большинства людей с синдромом демпинга симптомы появляются через 30 – 60 минут после еды, что означает, что в начале синдром демпинга является наиболее распространенным типом. Через 30 – 60 минут после еды вся поступившая пища опорожняется в двенадцатиперстную кишку, что приводит к значительному растяжению двенадцатиперстной кишки. Это вызывает большие выделения в просвет. Осмотически активные частицы в пище не могут быть поглощены, это означает, что они остаются в просвете и вытягивают еще больше жидкости из кишечника.Чрезвычайная секреция приводит к гиповолемии и бреду. Большое количество жидкости и осмотически активных частиц часто приводит к водянистой диарее, но в некоторых случаях жидкость может всасываться в более дистальной части кишки, вызывая спонтанные симптомы исчезают.
Люди с синдромом демпинга в конце года не испытывают ранних симптомов, но имеют другой набор симптомов, которые появляются через 1-3 часа после еды. Чрезмерное опорожнение желудка вызывает быстрое всасывание сахара в кишечнике.Это стимулирует β-клетки, что вызывает пик уровня инсулина. Поглощение сахара длится недолго, поэтому высокие уровни инсулина приводят к гипогликемии с такими симптомами, как потливость, усталость и сердцебиение.
Предыдущая страница:
1. Нарушения функций жевания, глотания и пищевода – гастроэзофагеальная рефлюксная болезнь.
Следующая страница:
3. Рвота (острая, хроническая)

 Как распознать рак желудка
Как распознать рак желудка