Нормокинетики: Нарушение моторики при функциональных расстройствах ЖКТ. Возможности терапевтической коррекции на клиническом примере | Пахомова
Нарушение моторики при функциональных расстройствах ЖКТ. Возможности терапевтической коррекции на клиническом примере | Пахомова
1. Drossman D.A., HasLer W.L. Rome IV – Functional GI Disorders: Disorders of Gut-Brain Interaction. Gastroenterology. 2016;150(6):1257-1261. doi: 10.1053/j.gastro.2016.03.035.
2. Piessevaux H., De Winter B., Louis E., Muls V., De Looze D., Pelckmans P et al. Dyspeptic symptoms in the general population: a factor and cluster analysis of symptom groupings. Neurogastroenterol Motil. 2009;21(4):378-388. doi: 10.1111/j.1365-2982.2009.01262.x.
3. Shadi S.Y., Christie J. Functional dyspepsia in review: Patho-physiology and challenges in the diagnosis and management due to coexisting gastroesophageal reflux disease and irritable bowel syndrome. Gastroenterol Res Pract. 2013;2013:ID351086. doi: 10.1155/2013/351086.
Gastroenterol Res Pract. 2013;2013:ID351086. doi: 10.1155/2013/351086.
4. Hunt R., Quigley E., Abbas Z., Eliakim A., Emmanuel A., Goh K.-L. et al. WGO Global Guideline – Coping with common GI symptoms in the community. 2013. Available at: https//www.worldgastroenterology.org/guidelines/ global-guidelines/common-gi-symptoms/common-gi-symptoms-english.
5. Takaki M. Gut pacemaker cells: the interstitial cells of Cajal (ICC). J Smooth Muscle Res. 2003;39(5):137-161. doi: 10.1540/jsmr.39.137.
6. Newgreen D., Heather Y. Enteric Nervous System: Development and Developmental Disturbances. Part 2. Pediatric and Developmental Pathology. 2002;5(3):329-349. doi: 10.1007/s10024-001-0142-y.
7. Климов П.К., Устинов В.Н. Биоэлектрическая активность гладких мышц пищеварительного тракта и ее связь с сократительной деятельностью. Успехи физиологических наук. 1973;4(4):3-33.
Климов П.К., Устинов В.Н. Биоэлектрическая активность гладких мышц пищеварительного тракта и ее связь с сократительной деятельностью. Успехи физиологических наук. 1973;4(4):3-33.8. Zai H., Kusano M. Investigation of gastric emptying disorders in patients with functional dyspepsia reveals impaired inhibitory gastric emptying regulation in the early postcibal period. Digestion. 2009;79(1):13-18. doi: 10.1159/000167861.
9. Kindt S., Dubois D., Van Oudenhove L., Caenepeel P., Arts J., Bisschops R., Tack J. Relationship between symptom pattern, assessed by the PAGI-SYM questionnaire, and gastric sensorimotor dysfunction in functional dyspepsia. Neurogastroenterol Motil. 2009;21:1183-e1105. Available at: https://www.academia.edu/24803978/Relationship_between_symptom_pattern_assessed_by_the_PAGI-SYM_questionnaire_and_gastric_sensorimotor_dys-function_in_functional_dyspepsia.
10. Lee H.T., Kim BJ. Trimebutine as a modulator of gastrointestinal motility. Arch Pharm Res. 2011;34(6):861-864. doi: 10.1007/s12272-011-0600-7.
11. Yang YJ., Bang C.S., Baik G.H., Park T.Y., Shin S.P.. Suk K.T., Kim DJ. Prokinetics for the treatment of functional dyspepsia: Bayesian network meta-analysis. BMC Gastroenterology 2017;17(1):83. doi: 10.1186/s12876-017-0639-0.
12. Eamonn M.M. Quigley. Prokinetics in the Management of Functional Gastrointestinal Disorders. J Neurogastroenterol Motil. 2015;21(3):330-336. doi: 10.5056/jnm15094.
13. Roman FJ., Lanet S., Hamon J., Brunelle G., Maurin A., Champeroux P. et al. Pharmacological Properties of Trimebutine and N-Monodesmethyltrimebutine. J Pharmacol Exp Ther. 1999;289(3):1391-1397. Available at: http//jpet.aspetjournals.org/content/289/3/1391.short.
J Pharmacol Exp Ther. 1999;289(3):1391-1397. Available at: http//jpet.aspetjournals.org/content/289/3/1391.short.
14. Roman F., Pascaud X., Taylor J.E., Junien J.L. Interactions of trimebutine with guinea-pig opioid receptors. J Pharm Pharmacol. 1987;39(5):404-407. doi: 10.1111/j.2042-7158.1987.tb03409.x.
15. Бородулина Е.В., Мареев И.В., Колокольцова М.Ю., Самыкина И.А., Удут В.В. Сравнительная эффективность препаратов Необутин® Ретард, таблетки пролонгированного действия, покрытые пленочной оболочкой, 300 мг, и Тримедат®, таблетки 200 мг, у больных синдромом раздраженного кишечника. Фарматека. 2017;(S5-17):72-77. Режим доступа: https://pharmateca.ru/ru/archive/article/35740.
16. Минушкин О.Н. Сочетанные функциональные расстройства (заболевания) желудочно-кишечного таркта. Их диагностика и лечебные подходы. Медицинский совет. 2015;(13):20-25. doi: 10.21518/2079-701X-2015-13-20-25.
Их диагностика и лечебные подходы. Медицинский совет. 2015;(13):20-25. doi: 10.21518/2079-701X-2015-13-20-25.
17. Gwee K.A., Chua A.S.B. Functional dyspepsia and irritable bowel syndrome, are they different entities and does it matter. World J Gastroenterol. 2006;12(17):2708-2712. doi: 10.3748/wjg.v12.i17.2708.
18. Delvaux M., Wingate D. Trimebutine: mechanism of action, effects on gastrointestinal function and clinical results. J Int Med Res. 1997;25(5):225-246. doi: 10.1177/030006059702500501.
19. Aktas A., Caner B., Ozturk F., Bayhan H., Nazin Y., Mentes T. The effect of trimebutine maleate on gastric emptying in patients with non-ulcer dyspepsia. Ann Nucl Med. 1999;13(4):231-234. doi: 10.1007/bf03164897.
20. Буторова Л.И., Токмулина Г.М., Плавник Т.Э., Рассыпнова Л.И., Мамиева З.А. Римские критерии IV синдрома раздраженного кишечника: эволюция взглядов на патогенез, диагностику и лечение. Лечащий врач. 2017;(3):61-64. Режим доступа: https://www.lvrach.ru/2017/03/15436690/.
Буторова Л.И., Токмулина Г.М., Плавник Т.Э., Рассыпнова Л.И., Мамиева З.А. Римские критерии IV синдрома раздраженного кишечника: эволюция взглядов на патогенез, диагностику и лечение. Лечащий врач. 2017;(3):61-64. Режим доступа: https://www.lvrach.ru/2017/03/15436690/.
Роль прокинетиков в терапии нарушений моторики желудочно-кишечного тракта.
Оксана Михайловна Драпкина
– К нам присоединился хорошо известный профессор Симаненков Владимир Ильич.
Владимир Ильич Симаненков, профессор:
– Мне представляется, что деятельность интернет-сессий чрезвычайно важна и полезна в свете стратегической линии последипломного образования концепции непрерывного профессионального образования. Я всю жизнь проработал в Северо-Западном университете. Когда человек приезжает раз в пять лет, большая часть информации устарела, и на коротком цикле восстановить это все чрезвычайно сложно. И когда в режиме нон-стоп проводятся такие сессии, в любом уголке нашей огромной Родины врачи-интернисты могут получить самые свежие знания из первых уст. Потому что у вас выступают лидеры мнений – люди, которые имеют и огромный собственный опыт и, кроме того, находятся в гуще информационных потоков по всем основным разделам.
И когда в режиме нон-стоп проводятся такие сессии, в любом уголке нашей огромной Родины врачи-интернисты могут получить самые свежие знания из первых уст. Потому что у вас выступают лидеры мнений – люди, которые имеют и огромный собственный опыт и, кроме того, находятся в гуще информационных потоков по всем основным разделам.
Уважаемые коллеги, мое сегодняшнее сообщение посвящено роли прокинетиков в терапии нарушений моторики. Как писал профессор Шептулин, не бывает заболеваний пищеварительной системы, которые не сопровождались бы теми или иными моторными расстройствами. Другой вопрос, что условно выделяют первичные моторные расстройства, куда включают неэрозивные формы рефлюкской болезни, функциональную диспепсию, дисфункцию сфинктера Одди, дискинезию желчного пузыря, синдром раздраженной кишки, синдром функционального запора. И вторичные моторные расстройства с диспепсией, диареей или запором.
А как же нам помочь этим пациентам? Условно ваш покорный слуга разделил все препараты на две большие подгруппы. Это лекарственные средства прямо влияющие на моторику и лекарственные средства опосредованно влияющие на моторику. Дефицит времени не позволяет мне рассмотреть правую графу более детально. Но если мы с вами вспомним, например, ингибиторы протонной помпы. С одной стороны это самые мощные антисекреторные препараты. Но с другой стороны, меняя РН в антральном отделе, они меняют скорость антродуоденального перехода. И так можно было бы обсудить каждый из представленных классов.
Это лекарственные средства прямо влияющие на моторику и лекарственные средства опосредованно влияющие на моторику. Дефицит времени не позволяет мне рассмотреть правую графу более детально. Но если мы с вами вспомним, например, ингибиторы протонной помпы. С одной стороны это самые мощные антисекреторные препараты. Но с другой стороны, меняя РН в антральном отделе, они меняют скорость антродуоденального перехода. И так можно было бы обсудить каждый из представленных классов.
Давайте посмотрим на левую группу. Это лекарственные средства прямо влияющие на моторику. Можно выделать четыре основных группы. Это нормокинетики, спазмолитики, блокаторы моторики и прокинетики. Нормокинетики – это препараты, которые влияют на эндорфинные рецепторы в пищеварительной системе. И у нас зарегистрировано два препарата – это даларгин и тримебутин. Группа спазмолитиков представлена пятью подгруппами. Наибольшее распространение имеют миотропные спазмолитики, и из них можно выделить три основных группы: это блокаторы натрия, блокаторы кальция и ингибиторы фосфодиэстеразы четвертого типа.
Итак, прокинетики. У нас с вами, к сожалению, только четыре прокинетика. Это метоклопрамид, домперидон, итоприд и прукалоприд. Я желтеньким пометил цизаприд и мосаприд, поскольку их регистрация прекращена. Почему? Как оказалось, лекарственные средства, влияющие на дофаминергические рецепторы, потенциально могут ухудшать прогноз сердечнососудистых заболеваний или увеличивать вероятность их развития. И регистрация в ряде зарубежных стран этих двух прокинетиков была прекращена. Итак, в России зарегистрировано четыре прокинетика, из них прукалоприд, который появился на нашем рынке около двух лет тому назад, является энтерокинетиком, то есть он селективно работает на толстую кишку. Что касается верхних отделов желудочно-кишечного тракта, то у нас есть три препарата: метоклопрамид, домперидон и итоприд.![]()
Прежде чем поговорить о каждом из них, я хотел бы процитировать статью Владимира Трофимовича Ивашкина с соавторами 2012 года, где рассматривались перспективные прокинетики. Но я сейчас не буду останавливаться на детальном их рассмотрении. Ожидать, что в ближайшие два-три года они будут зарегистрированы в России, не приходится. Пока у нас их нет и будем ориентироваться на те, что зарегистрированы.
Есть такое понятие NNT – «Number needed to Treat». Этот параметр отражает количество пациентов, которое необходимо лечить данным образом, чтобы предотвратить один дополнительный эпизод заболевания или добиться положительного исхода для одного пациента по сравнению с контрольной группой, то есть с группой, в которой обычно применяется плацебо. Идеальный случай, когда NNT=1, тогда всем пациентам, которые получали это лекарство, стало лучше, а в контрольной группе ни у кого лучше не было. Но как мы понимаем, учитывая плацебо-эффекты, NNT=1 – это некий идеал. Чем больше NNT, тем менее эффективно лечение.
Чем больше NNT, тем менее эффективно лечение.
Зачем я вам напомнил этот показатель? Существуют данные об NNT для различных методов лечения такого моторного расстройства как функциональная диспепсия. Я обратил бы ваше внимание на первую строчку – это эрадикация Helicobacter pylori. Обратите внимание, что NNT для этого метода лечения – 17. И это значит следующее. В Маастрихтском соглашении сказано, что в странах с высокой инфицированностью Helicobacter pylori при функциональной диспепсии нужно проводить эрадикацию Helicobacter pylori. Вероятно, мы с вами не будем спорить с Маастрихтом-4, но мы с вами видим NNT, и мы можем сказать, что надеяться на кардинальные изменения клинических проявлений функциональной диспепсии после эрадикации очень трудно. А теперь два других строчки: это ингибиторы протонной помпы и прокинетики. Для ингибитора протонной помпы NNT – 10, а для прокинетиков – 4. К чему я клоню? Конечно, не к тому, что не нужно использовать ингибиторы протонной помпы при моторных расстройствах желудка. Нет, но к тому, что в ряде случаев клиническая эффективность прокинетиков, по меньше мере, не будет уступать ингибиторам, а в ряде случаев будет превышать. И все эти данные получены путем мета-анализа, то есть обладают высокой степенью доказательности.
Нет, но к тому, что в ряде случаев клиническая эффективность прокинетиков, по меньше мере, не будет уступать ингибиторам, а в ряде случаев будет превышать. И все эти данные получены путем мета-анализа, то есть обладают высокой степенью доказательности.
Теперь давайте вернемся к тем препаратам, о которых я говорил ранее. Что касается метоклопрамида, то это препарат, который на нашем рынке свыше 40 лет. Он является антагонистом рецепторов серотонинергических третьего типа, антагонистом дофаминергических рецепторов второго типа и агонистом рецепторов серотонина четвертого типа. И проблема в том, что этот препарат хорошо проходит через гематоэнцефалический барьер. Отсюда его влияние как на периферию, на нижнюю треть пищевода, желудок и дуоденум, так и на ЦНС. И вы видите, что побочные эффекты, они были зарегистрированы сразу после регистрации, экстрапирамидные нарушения, сонливость, астенизация. Но по мере многолетнего использования данного препарата было показано, что частота этих нарушений велика. И 26 июля 2013 года Европейское медицинское агентство (EMA) поручило Комитету по контролю за лекарственными средствами сформулировать изменения в использовании препаратов, содержащих метоклопрамид. Я не буду зачитывать все, скажу, что в сухом остатке. А в сухом остатке получается, что, во-первых, не нужно лечить метоклопрамидом больше пяти дней, во-вторых, не превышать дозу 30 миллиграмм и, в-третьих, нужно учитывать, что метоклопрамид не рекомендуется для лечения функциональных расстройств желудка, изжоги или при нарушениях антродуоденального перехода.
И 26 июля 2013 года Европейское медицинское агентство (EMA) поручило Комитету по контролю за лекарственными средствами сформулировать изменения в использовании препаратов, содержащих метоклопрамид. Я не буду зачитывать все, скажу, что в сухом остатке. А в сухом остатке получается, что, во-первых, не нужно лечить метоклопрамидом больше пяти дней, во-вторых, не превышать дозу 30 миллиграмм и, в-третьих, нужно учитывать, что метоклопрамид не рекомендуется для лечения функциональных расстройств желудка, изжоги или при нарушениях антродуоденального перехода.
И кому тогда вообще назначать метоклопрамид? Судя по литературным данным, остается одно, но существенное показание – это пациенты, страдающие онкологической патологией и получившие химиотерапию, с упорными рвотами, тошнотой и так далее. Этим пациентам можно назначать метоклопрамид.
Теперь поговорим о домперидоне. Домперидон также на нашем рынке достаточно давно. Мы знаем, что он является селективным D2 антагонистом, то есть блокирует рецепторы дофаминов второго типа. И исходно описанные побочные эффекты рассматривались как очень редкими. Что значит очень редкие? Это значит, что они появлялись реже, чем один раз по сравнению с тысячью случаев применения. Это связано с низкой проницаемостью гематоэнцефалического барьера по отношению к этому лекарственному средству. Но последние годы появились новые данные о возможности негативного влияния на сердечнососудистую систему домперидона. Первоначально забили тревогу у нас. Департамент государственного регулирования лекарственных средств направил производителям препаратов, содержащих домперидон, рекомендации об изменении инструкции по применению данных препаратов и о переводе их из безрецептурного в рецептурный статус. Но, наблюдая за продажами в аптеках за литературой, я как-то не заметил последствий этого письма. А в 2010 году в Европе были опубликованы результаты двух новых эпидемиологических исследований. И было показано, что у пожилых больных старше 60-ти лет, получавших высокие дозы домперидона, повышается риск развития жизнеугрожающих желудочковых аритмий и внезапной сердечной смерти.
И исходно описанные побочные эффекты рассматривались как очень редкими. Что значит очень редкие? Это значит, что они появлялись реже, чем один раз по сравнению с тысячью случаев применения. Это связано с низкой проницаемостью гематоэнцефалического барьера по отношению к этому лекарственному средству. Но последние годы появились новые данные о возможности негативного влияния на сердечнососудистую систему домперидона. Первоначально забили тревогу у нас. Департамент государственного регулирования лекарственных средств направил производителям препаратов, содержащих домперидон, рекомендации об изменении инструкции по применению данных препаратов и о переводе их из безрецептурного в рецептурный статус. Но, наблюдая за продажами в аптеках за литературой, я как-то не заметил последствий этого письма. А в 2010 году в Европе были опубликованы результаты двух новых эпидемиологических исследований. И было показано, что у пожилых больных старше 60-ти лет, получавших высокие дозы домперидона, повышается риск развития жизнеугрожающих желудочковых аритмий и внезапной сердечной смерти. И получение вот этих двух работ привели к тому, что в 2011 году регуляторные органы Великобритании приняли соответствующее решение, и в марте этого года Европейское медицинское агентство поручило Комитету по контролю лекарственных средств обобщить все данные, посвященные рискам, пользе и так далее побочным эффектам домперидона. К сожалению, судя по сайту, доклад этого комитета пока не опубликован. Но что же делать практическим врачам по отношению к этому препарату? Я думаю, что нужно сформулировать следующим образом: если у человека имеется хроническая сердечная недостаточность, если у него имеется удлинение интервала QT на электрокардиограмме, если он пожилой, то лучше на сегодняшний день от назначения домперидона воздержаться.
И получение вот этих двух работ привели к тому, что в 2011 году регуляторные органы Великобритании приняли соответствующее решение, и в марте этого года Европейское медицинское агентство поручило Комитету по контролю лекарственных средств обобщить все данные, посвященные рискам, пользе и так далее побочным эффектам домперидона. К сожалению, судя по сайту, доклад этого комитета пока не опубликован. Но что же делать практическим врачам по отношению к этому препарату? Я думаю, что нужно сформулировать следующим образом: если у человека имеется хроническая сердечная недостаточность, если у него имеется удлинение интервала QT на электрокардиограмме, если он пожилой, то лучше на сегодняшний день от назначения домперидона воздержаться.
И теперь давайте посмотрим на итоприд. Как и предшествующий препарат, он блокирует дофаминергические рецепторы второго типа. Но кроме того, он блокирует фермент холинэстеразу – фермент, который в норме расщепляет ацетилхолин. В результате он работает не только через аденилатциклазу, но и увеличивает период полураспада ацетилхолина, и в результате плотность и воздействие на D2 рецепторы как бы снижается. И в результате мы пока не имеем сообщений о негативном влиянии итоприда на интервал QT. Это плюсы фармакокинетики. Обратите внимание, что он метаболизируется без участия цитохрома Р450, значит мы можем не опасаться лекарственных взаимодействий нежеланных.
И в результате мы пока не имеем сообщений о негативном влиянии итоприда на интервал QT. Это плюсы фармакокинетики. Обратите внимание, что он метаболизируется без участия цитохрома Р450, значит мы можем не опасаться лекарственных взаимодействий нежеланных.
Теперь ключевой вопрос о брендах и дженериках. 21 ноября наш министр, профессор Скворцова выступала на президиуме правительства Российской Федерации. И в своем выступлении она подчеркнула, что Россия находится на третьем месте в мире по удельному весу дженериков. Хорошо это или плохо? Наверное, надо сначала спросить – а каково качество этих дженериков? И возвращаясь к этой теме, хочу подчеркнуть, что у нас зарегистрировано два итоприда. Это брендовый препарат Ganaton и дженериковый препарат Itomed. Когда мы сравниваем дженерик и бренд, нас интересует их эквивалентность. Существует три вида эквивалентности: фармацевтическая, терапевтическая и биоэквивалентность. И парадокс заключается в том, что ни FDA (Food and Drug Administration), ни Европейское медицинское агентство, ни российский законодатель не требует доказать терапевтическую эквивалентность дженериков. В нашем законе 2010 года сказано и/или терапевтическая эквивалентность. Но какая же дженериковая компания сама пойдет на проведение крайне дорогостоящих исследований терапевтической эквивалентности. Поэтому большинство компаний ограничивается проверкой биоэквивалентности на здоровых молодых ребятах.
В нашем законе 2010 года сказано и/или терапевтическая эквивалентность. Но какая же дженериковая компания сама пойдет на проведение крайне дорогостоящих исследований терапевтической эквивалентности. Поэтому большинство компаний ограничивается проверкой биоэквивалентности на здоровых молодых ребятах.
В классификаторе Римский Консенсус III выделяют два основных варианта функциональной диспепсии: постпрандиальный дистресс-синдром и эпигастральный болевой синдром. И Римские критерии III рекомендуют три основных подхода: ингибиторы протонной помпы, эрадикация Helicobacter pylori и прокинетики. И наша кафедра решила провести инициативное исследование – изучить клиническую эффективность препарата Itomed и посмотреть на его дизайн – открытое, контролируемое, рандомизированное, с параллельными группами, моноцентровое.
Вот дизайн этого исследования. Суть такая: путем рандомизации были выделены группы, которые получали Itomed, и группы, которые только по требованию редко получали не всасывающийся антацид. И что у нас получилось? Как правило, мы имеем дело с комбинированными нарушениями моторики. Римские критерии III выделили эпигастральный болевой синдром и постпрандиальный дистресс-синдром. А у наших реальных больных всегда ли эти два синдрома выделены в чистом виде? По нашим данным, чаще всего имеется сочетание и тяжести в эпигастрии, и чувство раннего насыщения, и боли в эпигастральной области. И посмотрите на динамику симптомов. Вы видите, что в рандомизированном исследовании Itomed показал свою клиническую эффективность. И обратите внимание, он влияет отчетливо на гастроэзофагеальный рефлюкс. А у пациентов с постпрандиальным синдромом он действует нетолько на тяжесть в эпигастральной области, не только на раннее насыщение, но и на боли в эпигастральной области. А вот не диспептические симптомы у пациентов с постпрандиальным дистресс-синдромом под влиянием Itomed особенно никак не изменились, точнее, они изменились, но так же, как при использовании плацебо.
И что у нас получилось? Как правило, мы имеем дело с комбинированными нарушениями моторики. Римские критерии III выделили эпигастральный болевой синдром и постпрандиальный дистресс-синдром. А у наших реальных больных всегда ли эти два синдрома выделены в чистом виде? По нашим данным, чаще всего имеется сочетание и тяжести в эпигастрии, и чувство раннего насыщения, и боли в эпигастральной области. И посмотрите на динамику симптомов. Вы видите, что в рандомизированном исследовании Itomed показал свою клиническую эффективность. И обратите внимание, он влияет отчетливо на гастроэзофагеальный рефлюкс. А у пациентов с постпрандиальным синдромом он действует нетолько на тяжесть в эпигастральной области, не только на раннее насыщение, но и на боли в эпигастральной области. А вот не диспептические симптомы у пациентов с постпрандиальным дистресс-синдромом под влиянием Itomed особенно никак не изменились, точнее, они изменились, но так же, как при использовании плацебо.
Вообще проблема плацебо в гастроэнтерологии крайне сложная, по некоторым авторам достигает 42% плацебо-эффект. Поэтому создается море возможностей для различных терапевтических спекуляций. Качество жизни улучшается. Конечно, когда перестает беспокоить боль и тяжесть, конечно, улучшается качество жизни и уменьшается тревожность. И кроме того, под влиянием данного лекарственного средства улучшается и физиологический, и психологический компонент здоровья. И на этой картинке видно, что у всех пациентов улучшение несомненное.
Поэтому создается море возможностей для различных терапевтических спекуляций. Качество жизни улучшается. Конечно, когда перестает беспокоить боль и тяжесть, конечно, улучшается качество жизни и уменьшается тревожность. И кроме того, под влиянием данного лекарственного средства улучшается и физиологический, и психологический компонент здоровья. И на этой картинке видно, что у всех пациентов улучшение несомненное.
Я благодарю вас за внимание. Но прежде, чем закончить, я хотел бы сказать следующее. Уважаемые коллеги, мне представляется, что мы с вами несколько деформировали структуру лекарственных назначений при моторных расстройствах. Порой мы используем препараты, влияющие на пищеварение, на кислотопродукцию, забывая о том, что в основе многих функциональных расстройств лежит моторная дисфункция и диссоциация секреторно-моторная. Мне думается, что арсенал интерниста, арсенал гастроэнтеролога не очень широкий пока, но у нас есть препараты, и мы должны знать и плюсы их, и минусы.
научное досье и клинические исследования uMEDp
Лечение функциональных заболеваний желудочно-кишечного тракта представляет нерешенную медицинскую проблему. К настоящему времени доказано, что в развитии этой патологии значительную роль играет висцеральная гиперчувствительность, которая во многих случаях формируется под влиянием хронического стресса и маркирует дисфункцию физиологических антистрессовых систем, в частности опиатергической системы. В этой связи перспективным представляется применениедля лечения функциональных заболеваний «балансирующего» регулятора моторики желудочно-кишечного тракта агониста опиатных рецепторов тримебутина. Экспериментальные и клинические исследования позволяют рассматривать тримебутин как таргетный препарат для коррекции висцеральной гиперчувствительности при синдроме раздраженного кишечника и функциональной диспепсии. В настоящем обзоре рассматриваются механизм лекарственного действия тримебутина и его эффективность как уникального прокинетика и спазмолитика
при функциональных заболеваниях желудочно-кишечного тракта.
Рис. 1. Ноцицептивные проводящие пути и место действия опиатов в терапии боли [4]
Рис. 2. Механизмы стрессорной индукции висцеральной гиперчувствительности [8]
Таблица 1. Нормализация параметров опорожнения желудка под влиянием тримебутина у пациентов с ФД [41]
Рис. 3. Сравнительная эффективность прокинетиков при лечении ФД
Таблица 2. Выраженность эффекта прокинетиков
Рис. 4. Сравнительная эффективность схем лечения с включением тримебутина или спазмолитиков у пациентов с функциональными расстройствами ЖКТ (СРК, ФД, сочетание СРК и ФД) и влияние этих препаратов на основные симптомы функциональных расстройств (модифицир
Таблица 3. Доля пациентов со снижением выраженности боли/дискомфорта более чем на 30% к 29-му дню от начала лечения
Доля пациентов со снижением выраженности боли/дискомфорта более чем на 30% к 29-му дню от начала лечения
Таблица 4. Снижение степени выраженности боли/дискомфорта к 29-му дню от начала лечения
Рис. 5. Динамика изменения суммарного балла по Шкале оценки желудочно-кишечных симптомов
Рис. 6. Динамика изменения симптомов функциональных заболеваний в баллах по Шкале оценки желудочно-кишечных симптомов за время лечения Тримедатом форте (А) и тримебутином 200 мг (Б)
Тримебутин был синтезирован Laboratoires Jouveinal (Франция) в 1969 г. На протяжении почти 50 лет в различных странах мира тримебутин как эффективный и безопасный спазмолитик успешно используется для лечения функциональных нарушений желудочно-кишечного тракта (ЖКТ) у детей и взрослых. За время клинического применения была накоплена обширная научная база данных, позволившая уточнить механизмы действия тримебутина. Установлено, что тримебутин обладает модулирующей прокинетической активностью, оказывает «балансирующее» воздействие на моторику ЖКТ, то есть является особым спазмолитиком для ЖКТ [1, 2].
Установлено, что тримебутин обладает модулирующей прокинетической активностью, оказывает «балансирующее» воздействие на моторику ЖКТ, то есть является особым спазмолитиком для ЖКТ [1, 2].
Доказано, что лекарственное действие тримебутина обусловлено взаимодействием с опиатными рецепторами (ОР) ЖКТ. Тримебутин и его активный метаболит (нортримебутин) являются неспецифическими агонистами периферических, премущественно κ- (энкефалинергических) и ноцицептивных, ОР на всем протяжении чувствительных нервных путей, проводящих сигналы от механических и болевых рецепторов ЖКТ в центральную нервную систему (ЦНС).
У пациентов с функциональными заболеваниями ЖКТ механизмы физиологической регуляции существенно изменены. В частности, при функциональной диспепсии (ФД) и синдроме раздраженного кишечника (СРК) с запором нарушена ритмическая активность ЖКТ в покое: снижены частота мигрирующего моторного комплекса (ММК) кишечника и формирование пропульсивной перистальтики. Одновременно у пациентов с функциональными заболеваниями ЖКТ резко снижена толерантность энтеральной нервной системы к растяжению и восприятию боли, ассоциированной с избыточным растяжением (феномен висцеральной гиперчувствительности). Доказано, что гиперчувствительность к растяжению и воздействиям окружающей среды является основной причиной абдоминальной боли при СРК [3].
Одновременно у пациентов с функциональными заболеваниями ЖКТ резко снижена толерантность энтеральной нервной системы к растяжению и восприятию боли, ассоциированной с избыточным растяжением (феномен висцеральной гиперчувствительности). Доказано, что гиперчувствительность к растяжению и воздействиям окружающей среды является основной причиной абдоминальной боли при СРК [3].
Формирование висцеральной гиперчувствительности при функциональных заболеваниях ЖКТ большинством исследователей расценивается как результат стрессорной нейромодуляции оси «мозг – ЖКТ» – сенсибилизации энтеральной и центральной нервной системы под влиянием хронического психологического и эмоционального стресса, который с детских лет испытывают эти пациенты. Известно, что при кратковременном стрессе и у пациентов без висцеральной гиперчувствительности стрессорной нейромодуляции оси «мозг – ЖКТ» противостоят так называемые стресс-лимитирующие системы. В ЖКТ стресс-лимитирующие системы включают ряд основных нейромедиаторов – антагонистов ацетилхолина: серотонин, норадреналин, дофамин и эндогенные опиатные пептиды. Эти амины могут действовать как центрально, так и на периферии, опосредуя эффекты симпатической системы.
Эти амины могут действовать как центрально, так и на периферии, опосредуя эффекты симпатической системы.
Подавляя активность холинергических нейронов, стресс-лимитирующие системы уменьшают секрецию, подвижность и расслабляют сфинктеры, увеличивают болевой порог в оси «мозг – ЖКТ» (рис. 1). Однако длительное воздействие хронического стресса приводит к стойкой активации гипоталамо-гипофизарной оси на фоне постепенно развивающегося относительного дефицита стресс-лимитирующих систем.
У пациентов с функциональными заболеваниями ЖКТ хронический стресс является причиной стереотипной нейромодуляции в оси «мозг – ЖКТ», направленной в сторону уменьшения толерантности к восприятию боли и формирования висцеральной гиперчувствительности (рис. 2) [5–8]. По данным клинических исследований, нарушенное восприятие нормальных стимулов от кишечника зафиксировано как минимум у 60% пациентов с СРК [7].
Таким образом, обезболивающее и спазмолитическое действие тримебутина при СРК базируется на торможении проведения импульсации от нервных окончаний энтеральной нервной системы в стенке кишки в чувствительные нейроны задних ганглиев спинного мозга. Тримебутин, как и другие опиатные пептиды, блокаторы кальциевых каналов и ГАМКергические препараты, ингибиторы обратного захвата норадреналина или серотонина, уменьшает восприятие боли, прерывая проведение болевого импульса на уровне первичных афферентов, нейронов второго порядка или вставочных нейронов спинного мозга (см. рис. 1) [9, 10]. Выраженность блокады болевой импульсации на фоне терапии тримебутином сравнима с таковой у местных анестетиков ряда лидокаина [10].
Тримебутин, как и другие опиатные пептиды, блокаторы кальциевых каналов и ГАМКергические препараты, ингибиторы обратного захвата норадреналина или серотонина, уменьшает восприятие боли, прерывая проведение болевого импульса на уровне первичных афферентов, нейронов второго порядка или вставочных нейронов спинного мозга (см. рис. 1) [9, 10]. Выраженность блокады болевой импульсации на фоне терапии тримебутином сравнима с таковой у местных анестетиков ряда лидокаина [10].
В отличие от «классических» агонистов периферических ОР в клинических исследованиях тримебутин оказался наиболее эффективен при лечении абдоминальной боли и запора у пациентов с функциональными заболеваниями ЖКТ [14, 15].
В одном из первых клинических исследований с применением тримебутина K. Lüttecke была показана сфокусированность эффектов препарата на стресс-индуцированных нарушениях моторики и абдоминальной боли у пациентов с СРК [16, 17]. Несколько позднее M. Galeone и соавт. (1986) установили, что у пациентов с СРК прием 600–800 мг тримебутина внутрь увеличивает пропульсивную перистальтику толстой кишки, нивелирует стихийные и вибрирующие сокращения – в целом нормализует моторику толстой кишки [18]. В другом исследовании того же периода S. Shannon и соавт. (1989) показали, что прием внутрь даже 200 мг тримебутина способен синхронизировать постпрандиальную двигательную активность сигмовидной кишки у пациентов с СРК с запорами, не влияя при этом на моторику ЖКТ у здоровых волонтеров [19]. J.C. Schang и соавт. (1993) также показали, что, уменьшая время кишечного транзита с 105 ± 9 до 60 ± 11 часов у пациентов с СРК, тримебутин не влияет на нормальную тощаковую и постпрандиальную моторику ЖКТ [20].
(1986) установили, что у пациентов с СРК прием 600–800 мг тримебутина внутрь увеличивает пропульсивную перистальтику толстой кишки, нивелирует стихийные и вибрирующие сокращения – в целом нормализует моторику толстой кишки [18]. В другом исследовании того же периода S. Shannon и соавт. (1989) показали, что прием внутрь даже 200 мг тримебутина способен синхронизировать постпрандиальную двигательную активность сигмовидной кишки у пациентов с СРК с запорами, не влияя при этом на моторику ЖКТ у здоровых волонтеров [19]. J.C. Schang и соавт. (1993) также показали, что, уменьшая время кишечного транзита с 105 ± 9 до 60 ± 11 часов у пациентов с СРК, тримебутин не влияет на нормальную тощаковую и постпрандиальную моторику ЖКТ [20].
Влияние тримебутина на симптомы СРК по данным рандомизированных клинических исследований (РКИ) было впервые оценено в метаанализе T. Poynard и соавт. [21]. В метаанализе 26 РКИ была впервые показана большая эффективность и безопасность тримебутина при коррекции симптомов СРК в сравнении с другими спазмолитиками и плацебо. Таргетность тримебутина в отношении симптомов СРК, обусловленных висцеральной гиперчувствительностью, была показана в систематическом обзоре M. Delvaux и D. Wingate [1]. На основании анализа экспериментальных данных и 12 РКИ авторы продемонстрировали, что тримебутин эффективно купирует характерный для СРК болевой синдром и увеличивает порог болевой чувствительности, уменьшая висцеральную гиперчувствительность и позитивно модифицируя субъективное восприятие висцеральной боли. Позднее в ряде исследований было также показано, что одновременно с коррекцией симптомов СРК тримебутин положительно влияет на психологический статус пациентов, уменьшая их тревожность и негативную вовлеченность в свое заболевание [22].
Таргетность тримебутина в отношении симптомов СРК, обусловленных висцеральной гиперчувствительностью, была показана в систематическом обзоре M. Delvaux и D. Wingate [1]. На основании анализа экспериментальных данных и 12 РКИ авторы продемонстрировали, что тримебутин эффективно купирует характерный для СРК болевой синдром и увеличивает порог болевой чувствительности, уменьшая висцеральную гиперчувствительность и позитивно модифицируя субъективное восприятие висцеральной боли. Позднее в ряде исследований было также показано, что одновременно с коррекцией симптомов СРК тримебутин положительно влияет на психологический статус пациентов, уменьшая их тревожность и негативную вовлеченность в свое заболевание [22].
В 2008 г. эффективность тримебутина при лечении функциональной абдоминальной боли и диспепсии была подтверждена в метаанализе 22 РКИ, посвященном применению спазмолитиков с различным механизмом действия, включившем 1778 пациентов с СРК [23]. У пациентов с СРК эффективность спазмолитиков как класса препаратов составила 53–61% и была выше, чем плацебо (31–41%). Показатель NNT (количество пациентов, которых необходимо пролечить, чтобы добиться положительного результата у одного больного) при применении спазмолитиков варьировал от 3,5 до 9.
Показатель NNT (количество пациентов, которых необходимо пролечить, чтобы добиться положительного результата у одного больного) при применении спазмолитиков варьировал от 3,5 до 9.
В 2009 г. эффективность тримебутина среди прочих спазмолитиков с разным механизмом действия (гиосцина, гиосциамина, отилония бромида, пинаверия бромида, альверина, мебеверина, пиренципина и некоторых других, не зарегистрированных в России) была проанализирована рабочей группой по изучению СРК [24]. В систематический обзор вошли 22 исследования, включившие 1778 пациентов. По данным экспертов, все спазмолитики, включая тримебутин, несмотря на некоторые неизбежные при изучении фукнциональных заболеваний методологические дефекты исследований, при лечении СРК оказались более эффективны, чем плацебо (отношение шансов (ОШ) 0,68, 95% доверительный интервал (ДИ) 0,57–0,81). В 2011 г. тримебутин был включен в Кохрейновский систематический обзор препаратов различной направленности действия, применяемых для лечения СРК. По данным L. Ruepert и соавт., тримебутин является эффективным спазмолитиком для купирования абдоминальной боли у пациентов с СРК [25].
По данным L. Ruepert и соавт., тримебутин является эффективным спазмолитиком для купирования абдоминальной боли у пациентов с СРК [25].
L. Rurpert и соавт. [25] анализировали влияние терапии на выраженность боли в животе при СРК (56 РКИ, 3725 пациентов). Они сравнивали эффективность плацебо, растительной клетчатки и псиллиума (12 исследований), четырех спазмолитиков (29 исследований) – дицикломина, мятного масла, пинавериума, тримебутина, двух антидепрессантов (15 исследований) – ингибиторов обратного захвата серотонина и амитриптилина. Исследователи пришли к выводу, что растительная клетчатка не влияет на выраженность абдоминальной боли при СРК. Спазмолитики эффективны у пациентов с болью в животе при СРК. Ингибиторы обратного захвата серотонина и трициклические антидепрессанты также эффективны, но эффект зависит от индивидуальных характеристик пациентов.
Соответственно в 2013 и 2015 гг. эффективность тримебутина продолжали исследовать в сравнении с наиболее широко применяемыми для лечения СРК спазмолитиками: пинавериумом (G. S. Karabulut и соавт., 2013) и мебеверином (M.Z. Rahman и соавт., 2015). По данным обоих РКИ, тримебутин не менее эффективно, чем пинаверия бромид и мебеверин, уменьшал абдоминальную боль и увеличивал частоту дефекаций у пациентов с СРК [26, 27]. В 2015 г. эти данные были подтверждены в обзоре Канадского агентства по лекарствам и технологиям в здравоохранении, где также было показано, что тримебутин более эффективно, чем оба указанных спазмолитика, улучшает качество жизни пациентов с СРК, особенно в детской популяции [28]. При этом терапия тримебутином была более безопасной – лишена неблагоприятных эффектов, характерных для спазмолитиков других классов: миорелаксантов, антихолинергических средств и пинаверия бромида. Склонность этих агентов самостоятельно вызывать запор, частое головокружение, сухость во рту, паралич аккомодации, задержку мочи и возможную спутанность сознания у пожилых пациентов ограничивает их полезность в клинической практике [29]. Таким образом, уровень доказательности исследований, в которых подтверждалась эффективность тримебутина, соответствовал I категории, уровень практических рекомендаций – категории А [30].
S. Karabulut и соавт., 2013) и мебеверином (M.Z. Rahman и соавт., 2015). По данным обоих РКИ, тримебутин не менее эффективно, чем пинаверия бромид и мебеверин, уменьшал абдоминальную боль и увеличивал частоту дефекаций у пациентов с СРК [26, 27]. В 2015 г. эти данные были подтверждены в обзоре Канадского агентства по лекарствам и технологиям в здравоохранении, где также было показано, что тримебутин более эффективно, чем оба указанных спазмолитика, улучшает качество жизни пациентов с СРК, особенно в детской популяции [28]. При этом терапия тримебутином была более безопасной – лишена неблагоприятных эффектов, характерных для спазмолитиков других классов: миорелаксантов, антихолинергических средств и пинаверия бромида. Склонность этих агентов самостоятельно вызывать запор, частое головокружение, сухость во рту, паралич аккомодации, задержку мочи и возможную спутанность сознания у пожилых пациентов ограничивает их полезность в клинической практике [29]. Таким образом, уровень доказательности исследований, в которых подтверждалась эффективность тримебутина, соответствовал I категории, уровень практических рекомендаций – категории А [30].
Во многих исследованиях были показаны влияние тримебутина на моторику верхних отделов ЖКТ и его эффективность как спазмолитика и прокинетика при лечении ФД. В уже упомянутом «раннем» систематическом обзоре M. Delvaux и D. Wingate (1997) показали, что у пациентов с ФД курсовой прием тримебутина эффективно уменьшает общее время нахождения пищи в желудке [1]. По данным A. Aktas (1999), это происходит потому, что при ФД тримебутин существенно сокращает лаг-период (VLAG) – время от начала поступления пищи в желудок до начала ее эвакуации и уменьшает объем удерживаемой в желудке пищи (R100 – процент от поступившего объема пищи, оставшегося в желудке через 100 минут) (табл. 1) [31].
Таким образом, тримебутин восстанавливает как нормальное время, через которое желудок должен начать эвакуацию пищи, так и нормальную продолжительность этого процесса посредством индукции III фазы ММК в тонкой кишке. Этот эффект не связан непосредственно с гиперацидностью в желудке и в полной мере сохраняется на фоне лечения ингибиторами протонной помпы [32]. По некоторым данным, тримебутин способен не менее эффективно стимулировать моторику выходного отдела желудка даже у коморбидных и тяжелобольных пожилых пациентов с гастропарезом на фоне цереброваскулярной патологии и сниженным уровнем сознания, а также способствовать разрешению послеоперационного пареза желудка и кишечника, гастропареза при инсулинзависимом сахарном диабете [33–35].
По некоторым данным, тримебутин способен не менее эффективно стимулировать моторику выходного отдела желудка даже у коморбидных и тяжелобольных пожилых пациентов с гастропарезом на фоне цереброваскулярной патологии и сниженным уровнем сознания, а также способствовать разрешению послеоперационного пареза желудка и кишечника, гастропареза при инсулинзависимом сахарном диабете [33–35].
Метаанализ T. Hiyama и соавт. (2007), посвященный оценке сравнительной эффективности прокинетиков как основного класса препаратов для лечения ФД, включил 27 плацебоконтролируемых РКИ с применением тримебутина и других прокинетиков (1844 пациента получали лечение, 1591 – плацебо). Метаанализ продемонстрировал эффективность даже краткосрочного (семь дней в дозе 600 мг) назначения тримебутина для коррекции симптомов ФД [36].
В последнем метаанализе Y.J. Yang и соавт. (2017) также сравнивали эффективность различных прокинетиков при лечении ФД (25 РКИ, 4473 пациента). Тримебутин при курсовом назначении оказался вторым после метоклопрамида по интегральной эффективности в отношении симптомов ФД [37]. Терапевтическая эффективность тримебутина почти не отличалась от эффективности метоклопрамида (OШ 1,32, 95% ДИ 0,27–6,06) и была выше эффективности мозаприда (OШ 1,99, 95% ДИ 0,87–4,72), домперидона (OШ 2,04, 95% ДИ 0,92–4,60) и итоприда (OШ 2,79, 95% ДИ 1,29–6,21) (рис. 3, табл. 2).
Терапевтическая эффективность тримебутина почти не отличалась от эффективности метоклопрамида (OШ 1,32, 95% ДИ 0,27–6,06) и была выше эффективности мозаприда (OШ 1,99, 95% ДИ 0,87–4,72), домперидона (OШ 2,04, 95% ДИ 0,92–4,60) и итоприда (OШ 2,79, 95% ДИ 1,29–6,21) (рис. 3, табл. 2).
Согласно выводам авторов, учитывая риск нежелательных явлений на фоне терапии метоклопрамидом или домперидоном, пациентам с ФД рекомендуется назначение коротких курсов этих препаратов или безопасная альтернатива – терапия тримебутином или мозапридом.
В большинстве РКИ с применением тримебутина подчеркивается наибольшая эффективность лечения у пациентов с изначально более выраженными симптомами и перекрестом симптомов функциональных заболеваний ЖКТ. Так, в популяции пациентов с сочетанием ФД и СРК, а также высокой частотой диарейного синдрома назначение тримебутина приводило к нормализации моторики толстой кишки, ускорению пропульсивной перистальтики и толстокишечного транзита (60 против 95 и 105 часов соответственно) за счет активизации электрофизиологической активности кишечника [38].
В России эффективность тримебутина у больных с ФД, СРК и пациентов с комбинацией ФД и СРК была подтверждена в наблюдательном исследовании (254 пациента, 30 – с СРК, 67 – с ФД, у 157 пациентов – сочетание СРК и ФД) [40]. Его целью было изучение практических алгоритмов фармакологического лечения и сравнительной эффективности регуляторов моторики и пробиотиков у пациентов с функциональными заболеваниями ЖКТ (тримебутин в схемах лечения применялся в стандартной дозе при курсовом приеме). Тримебутин достоверно более эффективно уменьшал выраженность каждого симптома функционального расстройства в сравнении со схемами, в которые были включены спазмолитики, за исключением запора и нарушения консистенции кала (твердый кал), в отношении этих симптомов эффективность тримебутина казалась сравнимой с таковой спазмолитиков (рис. 4).
В большинстве РКИ с применением тримебутина (за исключением исследований у пациентов отделений интенсивной терапии) проводилась оценка эффективности и безопасности курсового назначения препарата (две – четыре недели). Сравнивая эффекты курсового и краткосрочного (один – три дня) лечения тримебутина, авторы единодушно отмечают, что положительные свойства препарата в наибольшей мере проявляются не в первые дни, а после двух и более недель лечения [39]. С учетом активного пресистемного метаболизма тримебутина было высказано предположение, что при очень хорошей переносимости препарата увеличение разовой дозы тримебутина до 300 мг при сохранении суточной дозы 600 мг может привести к росту эффективности лечения при одновременном улучшении комплаентности больных, поскольку прием препарата будет сокращен до двух раз в день.
Сравнивая эффекты курсового и краткосрочного (один – три дня) лечения тримебутина, авторы единодушно отмечают, что положительные свойства препарата в наибольшей мере проявляются не в первые дни, а после двух и более недель лечения [39]. С учетом активного пресистемного метаболизма тримебутина было высказано предположение, что при очень хорошей переносимости препарата увеличение разовой дозы тримебутина до 300 мг при сохранении суточной дозы 600 мг может привести к росту эффективности лечения при одновременном улучшении комплаентности больных, поскольку прием препарата будет сокращен до двух раз в день.
Исследование эффективности и безопасности назначения тримебутина 300 мг по одной таблетке два раза в день, суммарно 600 мг в день (Тримедат® форте, таблетки пролонгированного действия, покрытые пленочной оболочкой, АО «Валента Фарм», Россия) при курсовом (28 дней) лечении боли, обусловленной функциональными заболеваниями ЖКТ и/или желчевыводящих путей, было выполнено в ходе открытого многоцентрового проспективного рандомизированного сравнительного исследования эффективности и безопасности III фазы [40]. Эффективность и безопасность препарата Тримедат® форте сравнивали с тримебутином 200 мг производства Франции по одной таблетке три раза в день, суммарно 600 мг в день. Исследование проводилось в 2015–2016 гг. на базах 16 крупных гастроэнтерологических клиник Москвы, Санкт-Петербурга, Ярославля, Рязани, Нижнего Новгорода, Уфы, Челябинска, Пятигорска и Реутова. В исследование вошли пациенты с хронической абдоминальной болью в сочетании хотя бы с одним из симптомов диспепсии – изжогой, отрыжкой, тошнотой, метеоризмом, запором, поносом и верифицированным диагнозом одного из функциональных заболеваний ЖКТ (неэрозивная гастроэзофагеальная рефлюксная болезнь, функциональная тошнота/рвота, ФД, СРК, дисфункция желчевыводящих путей). Среди пациентов было 56 мужчин (27%) и 151 женщина (73%) в возрасте 43,3 ± 13,6 года (от 18 до 69 лет). Эффективность лечения оценивали по частоте положительного ответа на лечение – определяли долю пациентов в группе с уменьшением жалоб более чем на 30% по Шкале оценки желудочно-кишечных симптомов к 29-му дню от начала лечения (первичная конечная точка), динамике изменения суммарного балла по Шкале оценки желудочно-кишечных симптомов к 7, 14, 21 и 29-му дню от начала лечения, динамике на фоне лечения баллов Шкалы оценки желудочно-кишечных симптомов по отдельным синдромам, динамике изменения качества жизни по опроснику SF-36 к 29-му дню от начала лечения (вторичные конечные точки) (табл.
Эффективность и безопасность препарата Тримедат® форте сравнивали с тримебутином 200 мг производства Франции по одной таблетке три раза в день, суммарно 600 мг в день. Исследование проводилось в 2015–2016 гг. на базах 16 крупных гастроэнтерологических клиник Москвы, Санкт-Петербурга, Ярославля, Рязани, Нижнего Новгорода, Уфы, Челябинска, Пятигорска и Реутова. В исследование вошли пациенты с хронической абдоминальной болью в сочетании хотя бы с одним из симптомов диспепсии – изжогой, отрыжкой, тошнотой, метеоризмом, запором, поносом и верифицированным диагнозом одного из функциональных заболеваний ЖКТ (неэрозивная гастроэзофагеальная рефлюксная болезнь, функциональная тошнота/рвота, ФД, СРК, дисфункция желчевыводящих путей). Среди пациентов было 56 мужчин (27%) и 151 женщина (73%) в возрасте 43,3 ± 13,6 года (от 18 до 69 лет). Эффективность лечения оценивали по частоте положительного ответа на лечение – определяли долю пациентов в группе с уменьшением жалоб более чем на 30% по Шкале оценки желудочно-кишечных симптомов к 29-му дню от начала лечения (первичная конечная точка), динамике изменения суммарного балла по Шкале оценки желудочно-кишечных симптомов к 7, 14, 21 и 29-му дню от начала лечения, динамике на фоне лечения баллов Шкалы оценки желудочно-кишечных симптомов по отдельным синдромам, динамике изменения качества жизни по опроснику SF-36 к 29-му дню от начала лечения (вторичные конечные точки) (табл. 3, 4, рис. 5, 6).
3, 4, рис. 5, 6).
Качество жизни, оцененное по физическому и психологическому компонентам опросника SF-36, к 29-му дню от начала лечения улучшилось в среднем в 1,2 раза по сравнению с исходным состоянием и также продемонстрировало не меньшую эффективность препарата Тримедат® форте и по сравнению с тримебутином 200 мг производства Франции по данному критерию.
Оценка влияния приема пищи на фармакокинетику препарата, проведенная у части пациентов в клиническом исследовании III фазы, показала, что прием препарата одновременно с высококалорийной пищей увеличивает биодоступность нортримебутина на 25,9% (отношение медиан AUC0-t) по сравнению с приемом натощак.
Данными проведенного клинического исследования была подтверждена высокая эффективность новой лекарственной формы препарата Тримедат® форте в купировании абдоминальной боли и проявлений диспепсического синдрома. Уменьшение кратности приема препарата привело к росту приверженности пациентов к назначенному лечению.
Таким образом, оказывая прокинетическое, спазмолитическое и обезболивающее действие, тримебутин занимает особое место в небогатом арсенале лекарственных препаратов для лечения функциональных заболеваний ЖКТ. Точка приложения тримебутина как периферического агониста ОР – разноуровневые афферентные нервные структуры ЖКТ. Взаимодействие тримебутина с ОР ЖКТ приводит:
- к ингибированию высвобождения ацетилхолина из нейронов энтеральных сплетений и нейромодуляции активности ацетилхолина в отношении гладких мышц ЖКТ;
- высвобождению эффектов эндогенных антихолинергических стресс-лимитирующих систем ЖКТ;
- блокировке передачи болевых и неболевых стимулов в NMDA-синапсах нейронов задних спинномозговых ганглиев на вставочные нейроны, что уменьшает передачу патологических стимулов в ЦНС с последующим уменьшением эффекторного ответа;
- увеличению толерантности к болевым и механическим стимулам – нивелированию висцеральной гиперчувствительности.

В медицинской практике соотношение центрального и периферического эффектов в лекарственном действии тримебутина часто понимают упрощенно. В механизме действия тримебутина значительную роль играет именно взаимодействие с чувствительными нервными структурами, обладающими существенно большей концентрацией ОР, чем стенка ЖКТ. По данным экспериментальных исследований, в стенке тонкой кишки содержание ноцицептивных ОР (δ-ОР) в 15–20 раз меньше, чем в задних ганглиях спинного мозга, и в 100 раз меньше, чем в головном мозге [41]. Именно широта воздействия тримебутина на разноуровневые ОР, расположенные «ниже» головного мозга (препарат не проникает через гематоэнцефалический барьер), позволяет оказывать устойчивое спазмолитическое и анальгетическое действие при функциональных заболеваниях ЖКТ, опосредованных патологией ЦНС и формированием висцеральной гиперчувствительности.
По данным многочисленных РКИ, тримебутин оказывает модулирующее влияние на ЖКТ, незаменимое при лечении заболеваний, основным звеном патогенеза которых служат висцеральная гиперчувствительность и высокий тонус гладкой мускулатуры у пациентов со стресс-индуцированной патологией: ФД, СРК с запором и смешанным вариантом СРК, хроническим идиопатическим запором. Модулирующeе влияние тримебутина на моторику и тонус мышц ЖКТ – коррекция нарушенной моторики кишечника путем индукции регуляции спонтанной активности без влияния на нормальную моторику – обусловлено различной степенью стрессорной нейромодуляции оси «мозг – ЖКТ», а следовательно, и сенситизации ОР у различных пациентов с функциональными заболеваниями. В целом ряде клинических исследований убедительно показано, что эффект тримебутина, по крайней мере характер влияния на моторику ЖКТ, зависит от вектора ее предшествовавшего нарушения. Так, влияние тримебутина на характерную для СРК абдоминальную боль вследствие растяжения кишки на фоне гиперчувствительности будет тем более выражено, чем выше чувствительность нервной системы к боли и чем ниже ее толерантность к любым периферическим проприоцептивным импульсам, которые в норме не должны осознаваться ЦНС. По мнению ряда авторов, тримебутин эффективен при СРК с запором потому, что у пациентов с висцеральной гиперчувствительностью имеют место адаптивная гиперреактивность периферических опиатергических структур, сенситизация и секреция новых ОР.
Модулирующeе влияние тримебутина на моторику и тонус мышц ЖКТ – коррекция нарушенной моторики кишечника путем индукции регуляции спонтанной активности без влияния на нормальную моторику – обусловлено различной степенью стрессорной нейромодуляции оси «мозг – ЖКТ», а следовательно, и сенситизации ОР у различных пациентов с функциональными заболеваниями. В целом ряде клинических исследований убедительно показано, что эффект тримебутина, по крайней мере характер влияния на моторику ЖКТ, зависит от вектора ее предшествовавшего нарушения. Так, влияние тримебутина на характерную для СРК абдоминальную боль вследствие растяжения кишки на фоне гиперчувствительности будет тем более выражено, чем выше чувствительность нервной системы к боли и чем ниже ее толерантность к любым периферическим проприоцептивным импульсам, которые в норме не должны осознаваться ЦНС. По мнению ряда авторов, тримебутин эффективен при СРК с запором потому, что у пациентов с висцеральной гиперчувствительностью имеют место адаптивная гиперреактивность периферических опиатергических структур, сенситизация и секреция новых ОР. Например, показано, что в кишечнике мышей экспериментальное воспаление и избыточный бактериальный рост стимулируют секрецию новых и увеличивают чувствительность μ-ОР [42]. Клинически это приводит к развитию нарушений функции ЖКТ, характерных для передозировки экзогенных опиатных анальгетиков: тошнота/рвота, анорексия, запор, чувство неполного опорожнения, вздутие живота, дискомфорт в животе, гастроэзофагеальный рефлюкс, псевдообструкция кишечника [9, 10, 43]. Причем считается, что все указанные эффекты реализуются посредством активации как центральных, так и периферических μ-ОР, поскольку их почти полностью устраняет неселективный антагонист ОР налоксон [44]. У таких пациентов тримебутин (неселективный агонист периферических ОР) демонстрирует эффекты не столько агониста, сколько конкурентного антагониста ОР, минимизируя указанные симптомы. Напротив, тримебутин ускоряет эвакуацию из желудка, индуцирует преждевременную фазу III ММК и модулирует сократительную способность толстой кишки. Вследствие гармонизации функций отдельных ОР тримебутин оказывает модулирующее (стимулирующее или расслабляющее) влияние на тонус гладкомышечных клеток и перистальтическую активность ЖКТ в зависимости от их исходного состояния.
Например, показано, что в кишечнике мышей экспериментальное воспаление и избыточный бактериальный рост стимулируют секрецию новых и увеличивают чувствительность μ-ОР [42]. Клинически это приводит к развитию нарушений функции ЖКТ, характерных для передозировки экзогенных опиатных анальгетиков: тошнота/рвота, анорексия, запор, чувство неполного опорожнения, вздутие живота, дискомфорт в животе, гастроэзофагеальный рефлюкс, псевдообструкция кишечника [9, 10, 43]. Причем считается, что все указанные эффекты реализуются посредством активации как центральных, так и периферических μ-ОР, поскольку их почти полностью устраняет неселективный антагонист ОР налоксон [44]. У таких пациентов тримебутин (неселективный агонист периферических ОР) демонстрирует эффекты не столько агониста, сколько конкурентного антагониста ОР, минимизируя указанные симптомы. Напротив, тримебутин ускоряет эвакуацию из желудка, индуцирует преждевременную фазу III ММК и модулирует сократительную способность толстой кишки. Вследствие гармонизации функций отдельных ОР тримебутин оказывает модулирующее (стимулирующее или расслабляющее) влияние на тонус гладкомышечных клеток и перистальтическую активность ЖКТ в зависимости от их исходного состояния. Тримебутин ослабляет рефлексы, вызванные расширением просвета кишки, и таким образом может модулировать висцеральную чувствительность и оказывать антиноцицептивное действие у больных с СРК [45]. Гипотеза о том, что периферические антагонисты ОР могут регулировать спазм и запор вследствие повышенной экспрессии ОР и/или увеличения активности опиоидергической системы ЖКТ как при хроническом стрессе, так и при длительном приеме опиатных анальгетиков, стимулирует поиск новых опиоидергических молекул [43, 46]. В исследованиях нового селективного периферического антагониста κ-ОР ЖКТ федотозина (fedotozine) были также продемонстрированы прокинетические свойства и эффективность при лечении пациентов с функциональными заболеваниями ЖКТ [47]. Однако в отличие от тримебутина большинство известных сегодня селективных агонистов ОР ЖКТ (лоперамид и новые препараты – ракекадотрил, элюксадолил, асимадолин) демонстрируют противоположное тримебутину влияние на моторику и применяются для лечения острой и хронической диареи.
Тримебутин ослабляет рефлексы, вызванные расширением просвета кишки, и таким образом может модулировать висцеральную чувствительность и оказывать антиноцицептивное действие у больных с СРК [45]. Гипотеза о том, что периферические антагонисты ОР могут регулировать спазм и запор вследствие повышенной экспрессии ОР и/или увеличения активности опиоидергической системы ЖКТ как при хроническом стрессе, так и при длительном приеме опиатных анальгетиков, стимулирует поиск новых опиоидергических молекул [43, 46]. В исследованиях нового селективного периферического антагониста κ-ОР ЖКТ федотозина (fedotozine) были также продемонстрированы прокинетические свойства и эффективность при лечении пациентов с функциональными заболеваниями ЖКТ [47]. Однако в отличие от тримебутина большинство известных сегодня селективных агонистов ОР ЖКТ (лоперамид и новые препараты – ракекадотрил, элюксадолил, асимадолин) демонстрируют противоположное тримебутину влияние на моторику и применяются для лечения острой и хронической диареи. При СРК с диареей селективные агонисты уменьшают моторику и секрецию ЖКТ, не блокируют висцеральную гиперчувствительность и практически не влияют на абдоминальную боль, ассоциированную с растяжением кишки [29, 44, 48]. В целом на фоне несколько разочаровывающих результатов клинических исследований с применением новых селективных периферических агонистов ОР и высокоселективных модуляторов разных классов серотониновых рецепторов прокинетическое, спазмолитическое и обезболивающее лечебное действие тримебутина (Тримедат) является уникальным по критерию «эффективность/безопасность» и может быть рекомендовано как терапия первого ряда при абдоминальной боли, диспепсии и запоре у пациентов с функциональными заболеваниями ЖКТ [49, 50].
При СРК с диареей селективные агонисты уменьшают моторику и секрецию ЖКТ, не блокируют висцеральную гиперчувствительность и практически не влияют на абдоминальную боль, ассоциированную с растяжением кишки [29, 44, 48]. В целом на фоне несколько разочаровывающих результатов клинических исследований с применением новых селективных периферических агонистов ОР и высокоселективных модуляторов разных классов серотониновых рецепторов прокинетическое, спазмолитическое и обезболивающее лечебное действие тримебутина (Тримедат) является уникальным по критерию «эффективность/безопасность» и может быть рекомендовано как терапия первого ряда при абдоминальной боли, диспепсии и запоре у пациентов с функциональными заболеваниями ЖКТ [49, 50].
ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ, РЕГУЛИРУЮЩИЕ МОТОРНУЮ ФУНКЦИЮ КИШЕЧНИКА.
В настоящее время частая причина обращения к врачам — это проблемы в работе ЖКТ. Практически для каждой из них характерно нарушение моторной функции. Однако они могут проявляться как симптомы какого-либо заболевания, не связанного с пищеварительной системой. В любом случае никак не обойтись без лекарств группы прокинетики.
В любом случае никак не обойтись без лекарств группы прокинетики.
Дорогие читатели! Наши статьи рассказывают о типовых способах решения проблем со здоровьем, но каждый случай носит уникальный характер.
Если вы хотите узнать, как решить именно Вашу проблему – начните с программы похудания. Это быстро, недорого и очень эффективно!
Узнать детали
Прокинетики: список препаратов нового поколения
Клиническая офтальмология. Медицинское обозрение. В статье рассмотрены механизмы действия препаратов — регуляторов моторики, а также эффективность их применения у детей при функциональных расстройствах органов пищеварения, проведен обзор разрешенных к применению у детей препаратов, нормализующих моторику ЖКТ и устраняющих функциональные расстройства органов пищеварения.
Мать и дитя. В нашей базе более статей присоединяйтесь! Подписаться Условия использования Личный кабинет. Расширенный поиск. Статьи на эту же тему. Дети Общие статьи 0. Педиатрия 0.
РМЖ – Русский медицинский журнал. Follow rusmedjournal. О статье Резюме Abstract eng. Рубрика: Педиатрия. Автор: О. Пирогова Минздрава России, Москва. Функциональные расстройства органов пищеварения ФРОП у детей являются распространенной патологией. Патогенез при ФРОП отличается многофакторностью. При этом ключевое звено патогенеза — нарушение нейрогуморальной регуляции моторной функции желудочно-кишечного тракта ЖКТ , которое может локализоваться на любом уровне регуляторной системы: местном, периферическом и центральном.
Дискоординация работы регуляторных звеньев различного уровня приводит к дискинезии органов ЖКТ и формированию разнообразной клинической картины, включая боль, диспепсические проявления, изменение характера стула.
Коррекцию нарушений моторики ЖКТ можно осуществлять на любом уровне регуляции. Наиболее предпочтительно использовать селективные препараты: спазмолитики, прокинетики, нормокинетики, а также блокаторы моторики. Особая роль принадлежит препаратам, воздействующим на энкефалические опиоидные рецепторы ЖКТ, которые находятся в окончаниях афферентных нейронов, мезентериальных сплетениях кишечника, энтеральной нервной системе и гладких мышцах ЖКТ.
Наиболее предпочтительно использовать селективные препараты: спазмолитики, прокинетики, нормокинетики, а также блокаторы моторики. Особая роль принадлежит препаратам, воздействующим на энкефалические опиоидные рецепторы ЖКТ, которые находятся в окончаниях афферентных нейронов, мезентериальных сплетениях кишечника, энтеральной нервной системе и гладких мышцах ЖКТ.
Однако большинство препаратов имеют ограничения для использования в детском возрасте или обладают выраженными побочными эффектами.
В статье рассмотрены механизмы действия препаратов — регуляторов моторики, а также эффективность их применения у детей при ФРОП, проведен обзор разрешенных к применению у детей препаратов, нормализующих моторику ЖКТ и устраняющих ФРОП. Для цитирования: О. Комарова Коррекция нарушений моторики при функциональных расстройствах органов пищеварения у детей.
Motor disorders correction in functional gastrointestinal disorders in children O. The FGIDs pathogenesis is multifactorial, with that, the pathogenesis key element is the neurohumoral regulation disorder of gastrointestinal motor function, which can be localized at any regulatory system level: local, peripheral and сentral.
Regulatory units discoordination of different levels leads to gastrointestinal dyskinesia and diverse clinical picture formation, including pain, dyspeptic manifestations, stool changing nature. Gastrointestinal motor disorders correction can be carried out at any regulation level. In this case, it is most preferable to use selective drugs: antispasmodics, prokinetics, normokinetics, as well as motor blockers.
A special role belongs to the drugs acting on the gastrointestinal enkephalin opioid receptors, localized in the afferent neuron endings, mesenteric intestinal plexuses, enteric nervous system, and gastrointestinal smooth muscles.
However, most drugs have limitations for use at the child age or have pronounced adverse events. The article describes the action mechanisms of drugs-motor regulators, as well as their effectiveness in children with FGIDs. A review of drugs approved for use in children, normalizing gastrointestinal motor and eliminating FGIDs, has been conducted.
For citation: Komarova O. Motor disorders correction in functional gastrointestinal disorders in children. Medical Review. Значительная часть ФРОП формируется в результате социальной дезадаптации ребенка, постоянного психологического напряжения, стресса, утомления, нарушения режима сна, учебы и отдыха [1, 2]. Таким образом, рассматривается многофакторный патогенез ФРОП.
При этом ключевым звеном патогенеза является нарушение нейрогуморальной регуляции моторной функции ЖКТ. Местная регуляция моторики ЖКТ осуществляется благодаря наличию клеток — водителей ритма — клеток Кахаля, которые расположены в гладкой мускулатуре и выполняют функцию передачи сигнала с энтеральных нейронов на гладкомышечные клетки [4, 5]. Помимо этого, регуляцию моторики осуществляют медиаторы — простагландины, кинины, оксид азота, гистамин и др.
Гладкие миоциты кишечника содержат множество рецепторов, например холинергические, дофаминовые, опиатные, 5-НТ4-рецепторы, посредством влияния на которые достигается согласованность в работе кишечника и осуществляется кишечный транзит.
Также большую роль в местной регуляции играют барорецепторы, активность которых регулируется давлением каловых масс, и желчные кислоты [5]. Психоэмоциональные реакции, а также органические поражения центральной нервной системы ЦНС оказывают эфферентное влияние на состояние вегетативной нервной системы симпатической и парасимпатической , которая через внекишечные и внутрикишечные ганглии, собственную нервную систему кишечника регулирует работу гладких миоцитов и желез.
Гуморальная регуляция осуществляется как на системном уровне, так и за счет продукции интестинальных гормонов, которые обеспечивают согласованную работу различных отделов и желез ЖКТ. Взаимосвязь нервной регуляции на местном и сегментарном уровне и местно-продуцируемых интестинальных пептидов приводит к вовлечению в процесс разных отделов или органов ЖКТ. Таким образом, нарушение нейрогуморальной регуляции моторной функции ЖКТ может локализоваться на любом уровне регуляторной системы: местном нервная система желудка и кишечника, рецепторный аппарат, энтероэндокринные клетки , периферическом проводящие пути и центральном головной мозг, включая кору больших полушарий.
Нарушение двигательной функции желудка и перстной кишки ДПК антро-пилорической моторики лежит в основе формирования ФД, нарушение моторики кишечника — СРК, функциональных запоров. При нарушении антро-пилорической моторики пациенты предъявляют жалобы на: чувство раннего насыщения, тяжести и переполнения в подложечной области, отрыжку, изжогу, горечь во рту, тошноту, плохой аппетит. Быстрое насыщение, чувство переполнения в желудке и боль после еды наблюдаются при нарушении аккомодации желудка к поступающей пище [9].
Чувство быстрого насыщения при приеме пищи может быть также обусловлено задержкой опорожнения антрального отдела желудка [10], хотя у части больных ФД оно может быть и ускорено [11].
Отрыжка появляется при повышении внутрижелудочного давления и легко возникает при недостаточности нижнего пищеводного сфинктера. При нарушении моторной функции ДПК может возникнуть рефлюкс желчи в желудок, спазм и атония ДПК, а также антиперистальтика. Такие симптомы, как тошнота и рвота, в первую очередь зависят от антиперистальтики и расстройства моторной функции ДПК. Тошнота возникает при значительном повышении интрадуоденального давления, особенно в случаях гипертонуса сфинктеров.
Тошнота возникает при значительном повышении интрадуоденального давления, особенно в случаях гипертонуса сфинктеров.
Также тошнота наблюдается при задержке опорожнения желудка, которое может способствовать рвоте и болям после еды [12, 13]. Боли, связанные с задержкой прохождения пищи по пищеводу и желудку, химуса — по кишечнику, как правило, носят тупой или неопределенный характер тянущие, давящие, распирающие и др.
В генезе болей в животе, имеющих острый характер приступообразные, схваткообразные, режущие или колющие , важная роль принадлежит гипертонусу того или иного отдела пищеварительного тракта. При дифференцировании боли важно исключить другие факторы, такие как воспаление, травма, нарушение кровообращения и др. Именно повышение порога чувствительности висцеральных рецепторов определяет восприятие боли и двигательную функцию ЖКТ, в регуляции которого особую роль играет внутренняя иннервация со стороны энтеральной нервной системы.
В последние годы большое значение придается чувствительности опиоидных рецепторов в центральных и периферических структурах. Коррекцию нарушенной моторики ЖКТ можно осуществлять на любом уровне регуляции. Двигательно-эвакуаторная функция пищеварительного тракта регулируется симпатической, парасимпатической и энкефалинергической системами.
Коррекцию нарушенной моторики ЖКТ можно осуществлять на любом уровне регуляции. Двигательно-эвакуаторная функция пищеварительного тракта регулируется симпатической, парасимпатической и энкефалинергической системами.
Большую роль играют желудочно-кишечные полипептиды, нейропептиды, биологически активные вещества. Все эти компоненты поддерживают равновесие между стимулирующими и ингибирующими воздействиями, что определяет тонус и сократительную активность гладких мышц ЖКТ. Активируется моторная функция холинергическими нервными волокнами.
На мембране гладкомышечных клеток ЖКТ находится большое количество разных рецепторов, в т. При воздействии нейромедиатора серотонина гладкая мускулатура сокращается. Под влиянием энкефалинов и эндорфинов перистальтика угнетается. Активаторы моторики ЖКТ усиливают моторную функцию посредством разных механизмов. Ацетилхолиновые препараты влияют на холинергические нервные волокна, другие — блокируют или активируют рецепторы, отвечающие за сокращение и расслабление гладкомышечных волокон.
В настоящее время для лечения нарушенной моторики предпочтительнее использовать селективные препараты: спазмолитики, прокинетики, нормокинетики, а также блокаторы моторики. К сожалению, большинство препаратов группы селективных миотропных спазмолитиков имеют ограничения для использования в детском возрасте мебеверин назначают детям старше 18 лет, алверина цитрат — с 14 лет, отилония бромид и пинаверия бромид — с 18 лет.
Показания к назначению гиосцина бутилбромида группа нейтротропных спазмолитиков — с летнего возраста на основании инструкций по применению препаратов. Блокаторы моторики типа лоперамида разрешены с 6-летнего возраста в форме таблеток , однако их не используют для курсового лечения, а обычно назначают симптоматически при диарейном синдроме. Усилению моторики способствуют многие препараты, используемые для лечения болезней ЖКТ, билиарного тракта, но не все из них рекомендуют в качестве прокинетиков.
Например, усиливают тонус гладкой мускулатуры ЖКТ слабительные, желчегонные препараты, простагландины, некоторые антибиотики в частности, эритромицин. Среди прокинетиков, разрешенных и применяемых в детской практике на территории РФ, — препараты метоклопрамид и домперидон.
Среди прокинетиков, разрешенных и применяемых в детской практике на территории РФ, — препараты метоклопрамид и домперидон.
Метоклопрамид является центральным антагонистом дофаминовых рецепторов D 1 и D 2. Среди важных побочных эффектов этого препарата — развитие экстрапирамидных нарушений, сонливость, астения; экстрапирамидные симптомы, включая дистонию или позднюю дискинезию, часто являются необратимыми [15]. При длительном применении возможно формирование гиперпролактинемии, ведущей к возникновению галактореи и аменореи, а также гинекомастии.
Препарат не рекомендуется для лечения заболеваний, в основе которых лежит нарушение антродуоденальной моторики. Метоклопрамид может использоваться только симптоматически для купирования тошноты и рвоты. Другой прокинетик — домперидон является периферическим антагонистом дофаминовых рецепторов D 2 и D 3. Фармакодинамическое действие домперидона связано с его блокирующим влиянием на периферические дофаминовые рецепторы, локализованные в стенке желудка и ДПК.
Домперидон повышает тонус нижнего пищеводного сфинктера, усиливает сократительную способность желудка, улучшает координированность сокращений антрального отдела желудка и ДПК, предупреждает возникновение ДГР.
Препарат давно применяется в педиатрии. Исходно побочные эффекты терапии домперидоном рассматривались как очень редкие реже 1 на 1 тыс. Это связано с низкой проницаемостью ГЭБ по отношению к этому лекарственному средству. Но в последние годы появились новые данные о возможном негативном влиянии домперидона на сердечно-сосудистую систему. При длительном применении домперидона существует риск желудочковых аритмий и внезапной сердечной смерти [16—19].
В настоящее время домперидон, так же как и метоклопрамид, назначается симптоматически при наличии тошноты и рвоты сроком не более чем на 7 дней [19]. При назначении домперидона очень важно следить за тем, чтобы пациенты не получали любые другие средства, способствующие удлинению интервала QT и ингибирующие CYP3A4 [20]. Нормокинетики — препараты, нормализующие моторику ЖКТ. Тримебутин не проникает через ГЭБ.
Нормокинетики — препараты, нормализующие моторику ЖКТ. Тримебутин не проникает через ГЭБ.
2.2.4. Средства, регулирующие функции желудочно-кишечного тракта
Клиническая офтальмология. Медицинское обозрение. В статье рассмотрены механизмы действия препаратов — регуляторов моторики, а также эффективность их применения у детей при функциональных расстройствах органов пищеварения, проведен обзор разрешенных к применению у детей препаратов, нормализующих моторику ЖКТ и устраняющих функциональные расстройства органов пищеварения. Мать и дитя. В нашей базе более статей присоединяйтесь!
Препараты для лечения нарушенной функции желудочно-кишечного тракта (АТХ код A03)
Консультант врача Электронная медицинская библиотека. Версия для слабовидящих. Часть функций, например, копирование текста к себе в конспект, озвучивание и т. Читать в приложении. Список сокращений и условные обозначения. Общие методические указания. Знакомство со структурой рецепта.
Список сокращений и условные обозначения. Общие методические указания. Знакомство со структурой рецепта.
Коррекция нарушений моторики при функциональных расстройствах органов пищеварения у детей
Моторику желудочно-кишечного тракта повышают М- холиномиметики и антихолинэстеразные средства, усиливающие тонус парасимпатической нервной системы, а также вещества, оказывающие местнораздражающее действие на слизистую оболочку желудка рвотные рефлекторного действия и кишечника слабительные средства. Настои ипекакуаны, термопсиса и др. Однако ей предшествует длительная “фаза тошноты”, что ограничивает применение этих препаратов в клинике как рвотных. При отравлениях для выведения яда из желудка назначают обычно рвотные средства центрального действия, например, апоморфин ,возбуждающий триггер-зону пусковую зону рвотного центра – рвота наступает через несколько минут после парентерального введения. Напротив, при длительной рвоте, не имеющей защитного характера, изнуряющей больного, приводящей к обезвоживанию организма и потере электролитов, необходимы противорвотные препараты. Рвота может быть результатом местного действия раздражающих веществ пища, лекарства или иметь центральный характер токсикоз беременных, лучевая терапия , побочное действие антибиотиков , антибластомных и других лекарств. Если рвота вызвана раздражением слизистой оболочки желудка, можно использовать вяжущие , обволакивающие и местноанестезирующие средства танин , настои ромашки, зверобоя , крахмальная слизь, анестезин и др. При рвоте центрального происхождения назначают нейролептические средства: перфеназин этаперазин , галоперидол и др. Они угнетают триггер-зону рвотного центра, но дают множество побочных нейролептических эффектов.
Напротив, при длительной рвоте, не имеющей защитного характера, изнуряющей больного, приводящей к обезвоживанию организма и потере электролитов, необходимы противорвотные препараты. Рвота может быть результатом местного действия раздражающих веществ пища, лекарства или иметь центральный характер токсикоз беременных, лучевая терапия , побочное действие антибиотиков , антибластомных и других лекарств. Если рвота вызвана раздражением слизистой оболочки желудка, можно использовать вяжущие , обволакивающие и местноанестезирующие средства танин , настои ромашки, зверобоя , крахмальная слизь, анестезин и др. При рвоте центрального происхождения назначают нейролептические средства: перфеназин этаперазин , галоперидол и др. Они угнетают триггер-зону рвотного центра, но дают множество побочных нейролептических эффектов.
В сети аптек 36,6 широко представлены средства, улучшающие моторику ЖКТ. Широкий ассортимент препаратов позволяет приобрести даже самые редкие лекарства, необходимые для лечения и профилактики заболеваний, связанных с желудочно-кишечным трактом, по выгодной цене.
Средства, улучшающие моторику ЖКТ
Но-шпа табл. Спазмалгон табл. Дротаверин табл. Реналган табл. Дротаверин-Дарница табл.
.
.
Событие
Областная научно-практическая конференция «Патология органов пищеварения в практике врача-терапевта в свете современных клинических рекомендаций» состоится 13 декабря 2019 года на базе ФБУН «Тюменский научно-исследовательский институт краевой инфекционной патологии» Роспотребнадзора.
Председатель: Кляшев Сергей Михайлович, д.м.н., заведующий кафедрой терапии ИНПР ФГБОУ ВО Тюменского ГМУ Минздрава России Специализация врачей: гастроэнтерологи, терапевты, врачи общей практики (семейные врачи), инфекционисты.
Место проведения: конференц-зал ФБУН «Тюменский научно-исследовательский институт краевой инфекционной патологии» Роспотребнадзора Адрес: г. Тюмень, ул. Республики д.147
Образовательная цель: Совершенствование знаний врачей в вопросах диагностики и дифференциальной диагностики хронических заболеваний органов пищеварения, возможностях консервативного лечения, ознакомление врачей терапевтических специальностей с современными методиками обследования, выявления факторов риска прогрессирования и осложнений хронических заболеваний желудочно-кишечного тракта, рационального выбора терапии, определения тактики ведения больных в стационаре и на амбулаторно-поликлиническом этапе в соответствии с клиническими рекомендациями Российской гастроэнтерологической ассоциации. Ожидаемые результаты: участники смогут лучше ориентироваться в современных методах диагностики и лечения возможностях предупреждения прогрессирования и профилактики осложнений хронических заболеваний органов пищеварения.
Программа
08.30 – 09.00 Регистрация участников
09.00 – 09.45 Лекция: «Абдоминальный ишемический синдром». Образовательные цели: совершенствование знаний врачей в вопросах дифференциальной диагностики болевого синдрома в брюшной полости, современных методах терапии и провилактики абдоминальной ишемии Лектор Кляшев Сергей Михайлович, д.м.н., профессор, заведующий кафедрой терапии ИНПР ФГБОУ ВО Тюменского ГМУ Минздрава России
09.45 – 10.30 Лекция: «Ожирение как причина хронических заболеваний» Обсуждение роли ожирения, как фактора формирования хронической патологии сердца, сосудов, возникновения сахарного диабета и современные возможности немедикаментозного и Тюменского кардиологического научного центра.
11.15 – 12.00 Лекция: «Радиационные (лучевые) поражения кишечника» Образовательные цели: совершенствование знаний терапевтов в вопросах диагностики и лечения лучевых поражений кишечника, определить тактику врача-терапевта в лечении данной патологии, определить показания и противопоказания к выбору терапии. Лектор Борисова Надежда Дмитриевна, ассистент кафедры терапии ИНПР ФГБОУ ВО Тюменского ГМУ МЗ РФ 12.00 – 12.45 Лекция: «Анемический синдром как маркер и фактор риска соматической патологии» Образовательные цели: совершенствование знаний терапевтов в вопросах диагностического поиска при анемическом синдроме, современных возможностях коррекции анемий. Лектор Криночкина Инна Рафаиловна, к.м.н., доцент кафедры терапии института НПР ФГБОУ ВО Тюменского ГМУ Минздрава России
Лектор Борисова Надежда Дмитриевна, ассистент кафедры терапии ИНПР ФГБОУ ВО Тюменского ГМУ МЗ РФ 12.00 – 12.45 Лекция: «Анемический синдром как маркер и фактор риска соматической патологии» Образовательные цели: совершенствование знаний терапевтов в вопросах диагностического поиска при анемическом синдроме, современных возможностях коррекции анемий. Лектор Криночкина Инна Рафаиловна, к.м.н., доцент кафедры терапии института НПР ФГБОУ ВО Тюменского ГМУ Минздрава России
12.45 – 13.15 Перерыв
13.15 – 13.45 Лекция: «Респираторные вирусные инфекции в практике терапевта: терапия с позиций клинических рекомендаций» Образовательные цели: Совершенствование знаний врачей в вопросах выбора противовирусных препаратов для лечения ОРВИ и гриппа, в зависимости от особенностей их механизма действия и клинических проявлений заболевания. Лектор Калинина Вера Леонидовна – к.м.н., доцент, кафедры терапии института НПР ФГБОУ ВО Тюменского ГМУ Минздрава России
13.45 – 14.15 Лекция: «Тяжелая бронхиальная астма у пациента с коморбидной патологией – современные возможности терапии» Лектор Криночкина Инна Рафаиловна, к. м.н., доцент кафедры терапии института НПР ФГБОУ ВО Тюменского ГМУ Минздрава России Лекции при поддержке компании «Эббот» (без начасления баллов НМО)
м.н., доцент кафедры терапии института НПР ФГБОУ ВО Тюменского ГМУ Минздрава России Лекции при поддержке компании «Эббот» (без начасления баллов НМО)
14.15 – 14.45 Лекция: «Метаболические заболевания печени. Для тех, кому нужно больше» Обсуждаются вопросы диагностики и дифференциальной диагностики метаболических заболеваний печени, возможности выявления осложнений и оценки риска прогрессирования, рационального выбора терапии, определения тактики ведения больных в стационаре и на амбулаторно-поликлиническом этапе. Лектор Степанова Ксения Борисовна, к.м.н., доцент кафедры инфекционных болезней ФГБОУ ВО Тюменского ГМУ Минздрава России
14.45 – 15.15 Лекция: «Нормокинетики – прокинетики: запускаем желудок» Образовательные цели: совершенствование знаний терапевтов о нарушении моторики желудка, современных методах диагностики, возможностях медикаментозного лечения моторных расстройств желудка. Лектор Хлынов Игорь Борисович, д.м.н., доцент кафедры госпитальной терапии Уральского государственного медицинского университета, Главный гастроэнтеролог Уральского федерального округа (г. Екатеринбург)
Екатеринбург)
15.15 – 15.45 Лекция: «Нормокинетики – спазмолитики. Восстанавливаем работу билиарного тракта и кишечника». Образовательные цели: осветить вопросы функциональной патологии органов пищеварения, актуализировать подходы к диагностике, определить тактику врача-терапевта в лечении данной патологии. Лектор Хлынов Игорь Борисович, д.м.н., доцент кафедры госпитальной терапии Уральского государственного медицинского университета, Главный гастроэнтеролог Уральского федерального округа (г. Екатеринбург)
15.45 – 16.00 Дискуссия, ответы на вопросы.
09.10.20 40-ОН Терапия | MicePartner
Программа конференции
09.00 – 10.00 Регистрация, подключение.
Председатель
Фатенков Олег Вениаминович – д.м.н., заведующий кафедрой и клиникой факультетской терапии ФГБОУ ВО Самарского государственного медицинского университета (далее – СамГМУ), главный внештатный специалист министерства здравоохранения Самарской области по терапии и общей врачебной практике.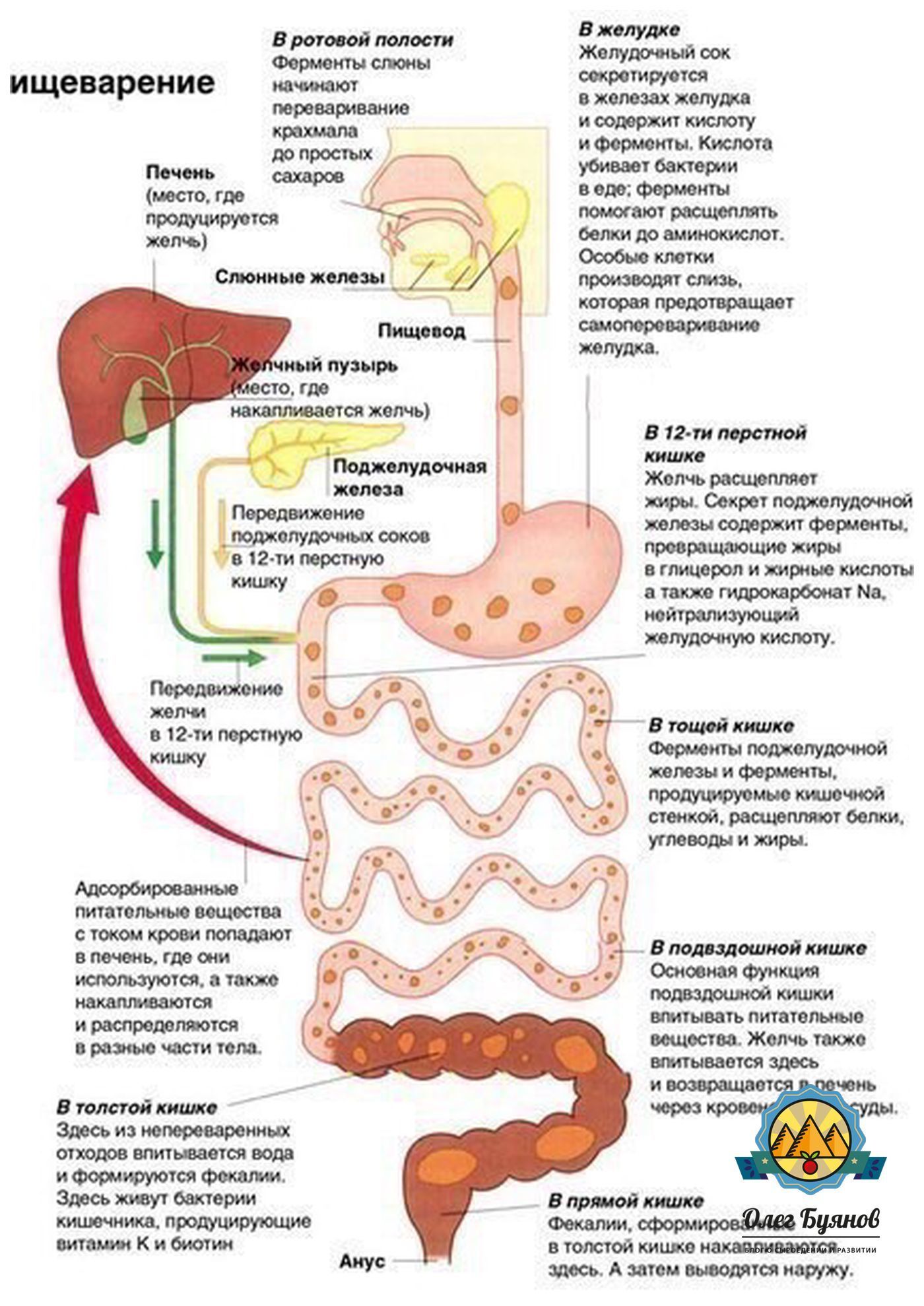
Купаев Виталий Иванович – д.м.н., профессор, заведующий кафедрой семейной медицины института профессионального образования СамГМУ, главный внештатный специалист Приволжского Федерального округа по общей врачебной практике.
10.00 – 10.10 Вступительное слово.
Фатенков Олег Вениаминович – д.м.н., заведующий кафедрой и клиникой факультетской терапии ФГБОУ ВО СамГМУ, главный внештатный специалист министерства здравоохранения Самарской области по терапии и общей врачебной практике.
Купаев Виталий Иванович – д.м.н., профессор, заведующий кафедрой семейной медицины института профессионального образования СамГМУ, главный внештатный специалист Приволжского Федерального округа по общей врачебной практике.
Симпозиум №1 «Современные подходы в терапии пациентов с ОРВИ»
Председатель
Фатенков Олег Вениаминович – д.м.н., заведующий кафедрой и клиникой факультетской терапии ФГБОУ ВО СамГМУ, главный внештатный специалист министерства здравоохранения Самарской области по терапии и общей врачебной практике.
10.10 – 10.20 «Лечение ОРВИ в период пандемии КОВИД-19»
Малышева Елена Борисовна – к.м.н., доцент кафедры госпитальной терапии и общей врачебной практики ПИМУ.
10.20 – 10.40 «Современные подходы к терапии кашля»
Жестков Александр Викторович – д.м.н., профессор, заведующий кафедрой микробиологии, иммунологии и аллергологии ФГБОУ ВО СамГМУ, заслуженный деятель науки РФ, главный внештатный специалист министерства здравоохранения Самарской области по аллергологии и иммунологии, главный пульмонолог Приволжского Федерального округа.
10.40 – 11.00 «Новые возможности терапии пациентов с БА и ХОБЛ»
Купаев Виталий Иванович – д.м.н., профессор, заведующий кафедрой семейной медицины института профессионального образования СамГМУ, главный внештатный специалист Приволжского Федерального округа по общей врачебной практике.
11.00 – 11.20 «Профилактика и лечение острых ринусинуситов в период подъема заболеваемости»
Крылова Ирина Александровна – к. м.н., доцент кафедры семейной медицины ИПО СамГМУ.
м.н., доцент кафедры семейной медицины ИПО СамГМУ.
11.20 – 11.40 Ответы на вопросы.
Симпозиум №2 «Продление жизни пациентов основной приоритет современного врача»
Председатель
Пирогова Юлия Юрьевна – к.м.н., доцент кафедры факультетской терапии, заведующая отделением гастроэнтерологии клиники факультетской терапии ФГБОУ ВО СамГМУ.
11.40 – 12.00 «Об этом должен знать каждый – концепция, продляющая жизнь»
Лебедев Петр Алексеевич – д.м.н., профессор, заведующий кафедрой терапии ФГБОУ ВО ИПО СамГМУ, председатель Самарского регионального отделения РНМОТ.
12.00 – 12.20 «Лечение артериальной гипертензии. Возможности хорошие, результаты оставляют желать лучшего» Доклад подготовлен при поддержке компании «Тева», баллы НМО не начисляются.
Шутов Александр Михайлович – д.м.н., профессор, заведующий кафедрой терапии и профессиональных болезней Ульяновского Государственного Университета
12. 20 – 12.40 «Рациональные подходы к диагностике и лечению ЖДА»
20 – 12.40 «Рациональные подходы к диагностике и лечению ЖДА»
Булгакова Светлана Викторовна – д.м.н., доцент, заведующая кафедрой гериатрии и возрастной эндокринологии ФГБОУ ВО СамГМУ, главный внештатный специалист Министерства здравоохранения Самарской области по геронтологии и гериатрии.
12.40 – 13.00 «Нормокинетики-Спазмолитики. Восстанавливаем работу билиарного тракта и кишечника»
Доклад подготовлен при поддержке компании «Эбботт», баллы НМО не начисляются.
Лебедева Екатерина Геннадьевна – к.м.н., доцент кафедры пропедевтики внутренних болезней и гастроэнтерологии МГМСУ.
13.00 – 13.20 «Терапия ГЭРБ: как лечить современно и своевременно?»
Колесова Татьяна Александровна – к.м.н., заведующая отделением гастроэнтерологии ГБУЗ СОКБ им. В.Д. Середавина, главный внештатный специалист министерства здравоохранения Самарской области по гастроэнтерологии.
13. 20 – 13.40 «ГЭРБ у коморбидного пациент»
20 – 13.40 «ГЭРБ у коморбидного пациент»
Юрченко Ирина Николаевна – к.м.н., доцент кафедры факультетской терапии ФГБОУ ВО СамГМУ, заведующая эндоскопическим отделением Клиник СамГМУ, врач-гастроэнтеролог, высшая квалификационная категория.
13.40 – 14.00 Дискуссия. Ответы на вопросы.
|
26 сентября 2019 года |
|
|
08.00- 08.30 Регистрация участников конференции. |
|
|
08.30-08.40 |
Приветствие участникам конференции, открытие: Департамент здравоохранения Тюменской области Главный гастроэнтеролог УрФО Новикова Татьяна Сергеевна Хлынов Игорь Борисович |
|
Симпозиум 1. |
|
|
Председатели: Начальник управления организации медицинской помощи и разработки ТПГГ Департамента здравоохранения Тюменской области Т.С. Новикова, профессор Ю.А. Кравчук, профессор Е.А. Лялюкова |
|
|
08.40-09.05
|
Лекция: «НАЖБП и метаболический синдром» Кравчук Юрий Алексеевич, д.м.н., профессор 2-ой кафедры терапии усовершенствования врачей Военно-медицинской академии им. С.М. Кирова (г. С-Петербург) |
|
09.05-09.30
|
Лекция: «НАЖБП. Скрытые угрозы и возможности терапии»
Лялюкова Елена Александровна, д.м.н., профессор кафедры внутренних болезней и семейной медицины ПДО ОмГМУ (г. |
|
09.30-09.55
|
Лекция: «Современные возможности лечения алкогольной болезни печени» Мирончев Олег Викторович, к.м.н., доцент кафедры клинической медицины ФГБОУ ВО Оренбургского государственного медицинского университета Минздрава России, председатель Оренбургского областного общества гастроэнтерологов. |
|
09.55-10.20
|
Лекция «Лекарственная болезнь печени. Современные аспекты терапии». Зиновьева Евгения Николаевна, главный врач Клиники «Эксперт», член общества гастроэнтерологов (г. Санкт Петербург). |
|
10.20-10.45
|
Лекция: «Для тех, кому нужно больше»
Хлынов Игорь Борисович, д. |
|
10.45-10.55 |
Дискуссии, ответы на вопросы |
|
Симпозиум 2. |
|
|
Председатели: главный гастроэнтеролог УрФО д.м.н. И.Б Хлынов, доцент А.О. Головенко |
|
|
10.55-11.20
|
Лекция «Пациент с ВЗК: шаг за шагом» Головенко Алексей Олегович, к.м.н., ассистент кафедры гастроэнтерологии ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России, г. Москва. |
|
11.
|
Лекция: «Клинические рекомендации по болезни Крона и язвенному колиту- 2019. Что нового?» Нанаева Бэлла Александровна, к.м.н., заведующий гастроэнтерологическим отделением ФГБУ «ГНЦК им. А.Н. Рыжих» Минздрава России (г. Москва) |
|
11.45-12.10
|
Лекция: «Альянс колопроктолога и гастроэнтеролога в ведении пациентов с ВЗК» Атрощенко Андрей Олегович, к.м.н., заведующий колопроктологическим отделением, Московский клинический научно-практический центр, ЦНИИ гастроэнтерологии Департамента здравоохранения г. Москва. |
|
12.10-12.20 |
Дискуссии, ответы на вопросы |
|
12. |
Кофе, обед |
|
Симпозиум 3. |
|
|
Председатели: главный гастроэнтеролог УрФО д.м.н. И.Б Хлынов, профессор В.Б. Гриневич |
|
|
13.00-13.25
|
Лекция «Общность патогенеза функциональных расстройств и органической патологии и подходов к лечению» Гриневич Владимир Борисович, д.м.н., профессор, главный внештатный гастроэнтеролог Министерства обороны РФ, заведующий 2-й кафедрой (терапии усовершенствования врачей) ФГБВОУ ВО «Военно-медицинская академия им. С.М. Кирова» МО РФ (г. С-Петербург) |
|
13.25-13.50
|
Лекция «Возможен ли контроль над хеликобактерной инфекцией»
Хлынов Игорь Борисович, д. |
|
13.50-14.15 |
Лекция: «Гастроэзофагеальная рефлюксная болезнь: тактика инициальной и поддерживающей терапии» Гриневич Владимир Борисович, д.м.н., профессор, главный внештатный гастроэнтеролог Министерства обороны РФ, заведующий 2-й кафедрой (терапии усовершенствования врачей) ФГБВОУ ВО «Военно-медицинская академия им. С.М. Кирова» МО РФ (г. С-Петербург) |
|
14.15-14.30 |
Дискуссии, ответы на вопросы |
|
Симпозиум 4 |
|
|
Председатели: главный гастроэнтеролог УрФО д. |
|
|
14.30-14.55
|
Лекция: «Место пробиотических продуктов в эрадикационной терапии Н.рylori» Лапина Татьяна Львовна, к.м.н., доцент кафедры пропедевтики внутренних болезней, лечебного факультета, Первого МГМУ им В.Х. Сеченова |
|
14.55-15.20
|
Лекция: «Синдром раздраженного кишечника: современные подходы к лечению» Хлынов Игорь Борисович, д.м.н., доцент кафедры госпитальной терапии Уральского государственного медицинского университета, Главный гастроэнтеролог Уральского федерального округа (г. Екатеринбург) |
|
15.15-15.25
|
Дискуссии, ответы на вопросы |
|
Симпозиум 5 |
|
|
Председатели: д. |
|
|
15.25-15.50
|
Лекция «Проблема запора в современном сообществе» Сарсенбаева Айман Силкановна, д.м.н., профессор кафедры терапии ИДПО ФГБОУ ВО Южно-Уральский государственный медицинский университет МЗ РФ, главный внештатный гастроэнтеролог Челябинской области (г.Челябинск). |
|
15.50-16.15
|
Лекция «Современные принципы терапии патологии желчевыводящих путей»
Хлынов Игорь Борисович, д.м.н., доцент кафедры госпитальной терапии Уральского государственного медицинского университета, Главный гастроэнтеролог Уральского федерального округа (г. |
|
16.15-16.40
|
Лекция: «Рациональный подход к ведению больного с перекрестом функциональных расстройств желудочно-кишечного тракта» Сарсенбаева Айман Силкановна, д.м.н., профессор кафедры терапии ИДПО ФГБОУ ВО Южно-Уральский государственный медицинский университет МЗ РФ, главный внештатный гастроэнтеролог Челябинской области (г.Челябинск). |
|
16.40-17.05
|
Лекция «Нормокинетики-прокинетики. Запускаем желудок» Хлынов Игорь Борисович, д.м.н., доцент кафедры госпитальной терапии Уральского государственного медицинского университета, Главный гастроэнтеролог Уральского федерального округа (г. Екатеринбург) |
|
17.05-17.15
|
Дискуссии, ответы на вопросы |
|
17.15-17.30 |
Закрытие конференции. Выдача сертификатов Шарапова Людмила Павловна к.м.н., главный внештатный гастроэнтеролог Департамента здравоохранения Тюменской области, заведующий консультативной поликлиникой № 1 ГБУЗ ТО «ОКБ № 1» (г. Тюмень). |
Нормокинетическая дискинезия желчевыводящих путей: новый диагноз
Задний план: Дискинезия желчевыводящих путей, диагностированная с помощью сканирования CCK-HIDA и фракция выброса менее 35%, была успешно вылечена лапароскопической холецистэктомией. Однако популяция пациентов с симптоматической болью в желчевыводящих путях и нормальным сканированием CCK-HIDA никогда не получает диагноз и, следовательно, не получает окончательного лечения. Некоторые из этих пациентов сообщают о воспроизводимой боли во время сканирования CCK-HIDA.Предполагается, что эти пациенты имеют новый диагноз – нормокинетическую дискинезию желчевыводящих путей и могут избавиться от боли при лечении холецистэктомией.
Методы: Был завершен ретроспективный обзор карт пациентов с болью в желчных путях в соответствии с критериями ROME III. Дополнительными критериями включения были (1) возраст старше 18 лет, (2) воспроизводимые желчные симптомы во время сканирования CCK-HIDA и (3) фракция выброса более 35%.Метод лечения – лапароскопическая холецистэктомия. Описательная статистика была предварительно сформирована, и данные были представлены как среднее ± стандартное отклонение и диапазон.
Результаты: Девятнадцать пациентов соответствовали критериям включения в это исследование с августа 2008 года по июль 2011 года. Было 15 женщин и 4 мужчин со средним возрастом 48,4 ± 13,0 лет. Средняя фракция выброса составила 75,1 ± 19,4%.Средняя продолжительность дооперационных симптомов составила 6,8 ± 5,9 месяцев, а послеоперационное наблюдение – 21,8 ± 10,6 месяцев. У семнадцати пациентов симптомы полностью исчезли, у одного – частичное, а у одного – без изменений. Уровень полного излечения составил 89,5%, а показатель улучшения – 94,7%.
Выводы: Мы предполагаем, что пациенты с болью в желчных путях, нормальным сканированием CCK-HIDA с фракцией выброса более 35% и с воспроизводимыми симптомами при инфузии CCK могли иметь новый диагноз: нормокинетическая дискинезия желчевыводящих путей.В настоящее время эти пациенты исключены из диагностики дискинезии желчевыводящих путей и, следовательно, из лечения. Мы выдвигаем гипотезу о возможном новом диагнозе, предлагаем холецистэктомию в качестве лечения и рекомендуем проспективный дизайн исследования для дальнейшей оценки.
Эффекты лапароскопической холецистэктомии при нормокинетической дискинезии желчевыводящих путей
. 2018 Янв; 215 (1): 116-119. DOI: 10.1016 / j.amjsurg.2017.04.012. Epub 2017 19 июня.Принадлежности Расширять
Принадлежности
- 1 McLaren Greater Lansing, Лансинг, штат Мичиган, США.Электронный адрес: [email protected].
- 2 McLaren Greater Lansing, Лансинг, штат Мичиган, США. Электронный адрес: [email protected].
- 3 McLaren Greater Lansing, Лансинг, штат Мичиган, США. Электронный адрес: [email protected].
- 4 McLaren Greater Lansing, Лансинг, штат Мичиган, США. Электронный адрес: [email protected].
- 5 McLaren Greater Lansing, Лансинг, штат Мичиган, США.Электронный адрес: [email protected].
Элемент в буфере обмена
Kerent D Pihl et al. Am J Surg. 2018 Янв.
Показать детали Показать вариантыПоказать варианты
Формат АннотацияPubMedPMID
.2018 Янв; 215 (1): 116-119. DOI: 10.1016 / j.amjsurg.2017.04.012. Epub 2017 19 июня.Принадлежности
- 1 McLaren Greater Lansing, Лансинг, штат Мичиган, США. Электронный адрес: kelf83 @ gmail.com.
- 2 McLaren Greater Lansing, Лансинг, штат Мичиган, США. Электронный адрес: [email protected].
- 3 McLaren Greater Lansing, Лансинг, штат Мичиган, США. Электронный адрес: [email protected].
- 4 McLaren Greater Lansing, Лансинг, штат Мичиган, США. Электронный адрес: [email protected].
- 5 McLaren Greater Lansing, Лансинг, штат Мичиган, США.Электронный адрес: [email protected].
Элемент в буфере обмена
Полнотекстовые ссылки Опции CiteDisplayПоказать варианты
Формат АннотацияPubMedPMID
Абстрактный
Это крупнейшее на сегодняшний день одноцентровое ретроспективное исследование, изучающее реакцию на лапароскопическую холецистэктомию у пациентов с бескаменной болезнью желчевыводящих путей.Был составлен обзор данных по 1116 пациентам с 2009 по 2014 год, у которых были признанные диагнозы, связанные с бескаменным холециститом и желчной коликой. Четыреста семьдесят четыре пациента были доступны для длительного наблюдения (6 месяцев и более). Было изучено множество факторов, связанных с сканированием холесцинтиграфии с введением холецистокинина (HIDA с CCK). Катагоризованы гиперкинетическая, нормокинетическая и гипокинетическая фракции выброса (ФВ), а также воспроизведение симптомов при введении ХЦК.Критерии ROME III (таблица 1) использовались для описания симптомов холецистита / желчной колики. (1). Было обнаружено, что скорость разрешения симптомов после лапароскопической холецистэктомии у нормокинетиков и гипокинетиков была одинаковой. Было также обнаружено, что воспроизведение симптомов после введения CCK было лучшим предиктором благоприятного ответа на операцию, чем рассчитанная фракция выброса.
Авторские права © 2017 Elsevier Inc.Все права защищены.
Похожие статьи
- Нормокинетическая дискинезия желчевыводящих путей: новый диагноз.
DuCoin C, Faber R, Ilagan M, Ruderman W, Wier D. DuCoin C и др. Surg Endosc. 2012 ноя; 26 (11): 3088-93. DOI: 10.1007 / s00464-012-2342-0. Epub 2012 31 мая. Surg Endosc. 2012 г. PMID: 22648109
- Ведение дискинезии желчного пузыря: результаты пациентов после положительной сцинтиграфии печени с иминодиуксусной кислотой (HIDA), меченной mtechnetium (Tc), с провокацией холецистокинином (CCK) и лапароскопической холецистэктомии.
Дэйв Р. В., Патак С., Кокбейн А. Дж., Лодж Дж. П., Смит А. М., Чоудхури Ф.Ю., Тугуд Дж. Дж. Дэйв Р.В. и др. Clin Radiol. 2015 Апрель; 70 (4): 400-7. DOI: 10.1016 / j.crad.2014.12.006. Epub 2015 12 января. Clin Radiol. 2015 г. PMID: 25588803
- Результаты лапароскопической холецистэктомии при дискинезии желчевыводящих путей у детей.
Лай С.В., Ротенберг С.С., Кей С.М., Шипман К.Е., Слейтер Б.Дж.Lai SW, et al. J Laparoendosc Adv Surg Tech A. 2017 августа; 27 (8): 845-850. DOI: 10.1089 / lap.2016.0338. Epub 2017 28 марта. J Laparoendosc Adv Surg Tech A. 2017. PMID: 28350202
- Дискинезия желчевыводящих путей: исследование более 200 пациентов и обзор литературы.
Canfield AJ, Hetz SP, Schriver JP, Servis HT, Hovenga TL, Cirangle PT, Burlingame BS. Кэнфилд А.Дж. и др.J Gastrointest Surg. 1998 сентябрь-октябрь; 2 (5): 443-8. DOI: 10,1016 / s1091-255x (98) 80035-8. J Gastrointest Surg. 1998 г. PMID: 9843604 Обзор.
- Оптимальное использование холецистокининовой холесцинтиграфии (CCK-HIDA) в клинической практике: обзор, основанный на доказательствах.
Ричмонд Б.К. Ричмонд Б.К. W V Med J. 2012 март-апрель; 108 (2): 8-11. W V Med J. 2012. PMID: 22655428 Обзор.
Процитировано
1 артикул- Дискинезия желчевыводящих путей у детей и подростков: мини-обзор.
Саймон Д.А., Friesen CA, Schurman JV, Colombo JM. Саймон Д.А. и др. Фронт Педиатр. 2020 24 марта; 8: 122. DOI: 10.3389 / fped.2020.00122. Электронная коллекция 2020.Фронт Педиатр. 2020. PMID: 32266192 Бесплатная статья PMC. Обзор.
Условия MeSH
- Бескаменный холецистит / диагностика
- Бескаменный холецистит / этиология
- Бескаменный холецистит / метаболизм
- Бескаменный холецистит / хирургия *
- Дискинезия желчевыводящих путей / осложнения
- Дискинезия желчевыводящих путей / диагностика
- Дискинезия желчевыводящих путей / метаболизм
- Дискинезия желчевыводящих путей / операция *
- Холецистэктомия, лапароскопическая *
LinkOut – дополнительные ресурсы
Источники полных текстов
Другие источники литературы
цитировать
КопироватьФормат: AMA APA ГНД NLM
Нормокинетическая дискинезия желчевыводящих путей: новый диагноз
Гриффен В.О., Бивинс Б.А., Роджерс Э.Л., Ширер Г.Р., Либшуц Д., Либер А. (1980) Холецистография холецистокинина в диагностике заболеваний желчного пузыря. Ann Surg 191: 636–640
PubMed Статья Google Scholar
Дроссман Д.А., Думитраску Д.Л. (2006) Рим III: новый стандарт функциональных желудочно-кишечных расстройств. J Gastrointest Liver Dis 15 (3): 237–241
Google Scholar
Sorenson M, Fancher S, Lang N, Eidt J, Broadwater J (1993) Аномальная фракция выброса ядра желчного пузыря предсказывает успех холецистэктомии у пациентов с дискинезией желчевыводящих путей. Am J Surg 166: 672–675
Статья Google Scholar
Йост Ф., Маргенталер Дж., Прести М., Бертон Ф., Мураяма К. (1999) Холецистэктомия – эффективное лечение дискинезии желчевыводящих путей. Am J Surg 178: 462–465
PubMed Статья CAS Google Scholar
Patel N, Lamb J, Hogle N, Fowler D (2004) Терапевтическая эффективность лапароскопической холецистэктомии при лечении дискинезии желчевыводящих путей. Am J Surg 187: 209–212
PubMed Статья Google Scholar
Гурусами К., Джуннаркар С., Фарук М., Дэвидсон Б. (2009) Холецистэктомия при подозрении на дискинезию желчного пузыря. Кокрановская база данных Syst Rev 1: CD007086. DOI: 10.1002 / 14651858.CD007086.pub2
Hansel S, DiBase J (2010) Функциональное расстройство желчного пузыря: дискинезия желчного пузыря. Gastroenterol Clin N Am 39: 369–379
Артикул Google Scholar
Карр Дж., Уоллс Дж., Брайан Л., Снайдер Д. (2009) Лечение дискинезии желчного пузыря на основе симптомов, результатов двухлетнего проспективного нерандомизированного параллельного когортного исследования. Surg Laparosc Endosc Percutan Tech 19: 222–226
PubMed Статья Google Scholar
Young S, Arregui M, Singh K (2006) Фракция выброса при сканировании HIDA не предсказывает сфинктер гипертензии Одди или клинический исход у пациентов с подозрением на хронический бескаменный холецистит. Хирургическая эндоскопия 20: 1872–1878
PubMed Статья CAS Google Scholar
Canfield A, Hetz S, Schriver J, Servis H, Hovenga T, Cirangle P, Burlingame B (1998) Дискинезия желчевыводящих путей: исследование более 200 пациентов и обзор литературы.J Gastrointest Surg 2: 443–448
PubMed Статья CAS Google Scholar
Финк-Беннетт Д., ДеРиддер П., Колози В., Гордон Р., Ярос Р. (1991) Холецистокининовая холесцинтиграфия: обнаружение аномальной двигательной функции желчного пузыря у пациентов с хронической бескаменной болезнью желчного пузыря. J Nucl Med 32: 1695–1699
PubMed CAS Google Scholar
Финк-Беннетт Д., ДеРиддер П., Колози В., Гордон Р., Рапп Дж. (1985) Холецистокинин-холесцинтиграфические данные при синдроме пузырного протока. J Nucl Med 26: 1123–1128
PubMed CAS Google Scholar
Финк-Беннетт Д., ДеРиддер П., Колози В., Гордон Р., Рапп Дж. (1984) Функциональная холецистокинина (ССК) холецистокинина (ССК) у пациентов с подозрением на заболевание бескаменных желчных путей. J Nucl Med 25: 10–12
Google Scholar
Финк-Беннетт Д., ДеРиддер П., Колози В., Гордон Р., Рапп Дж. (1986) Холецистокинин при бескаменной болезни желчевыводящих путей. J Nucl Med 27: 882–884
Google Scholar
Krishnamurthy GT, Bobba VR, Kingston E, Turner F (1998) Измерение опорожнения желчного пузыря последовательно с использованием однократной дозы 99m Tc-меченного гепатобилиарного агента. Гастроэнтерология 83: 773–776
Google Scholar
Krishnamurthy GT, Bobba VR, Kingston E (1981) Фракция выброса радионуклидов: метод количественного анализа двигательной функции желчного пузыря человека. Гастроэнтерология 80: 482–490
PubMed CAS Google Scholar
Ziessman HA, Muenz LR, Agarwal AK, ZaZa AA (2001) Нормальные значения для холесцинтиграфии синкалидом: сравнение двух методов. Радиология 221: 404–410
PubMed Статья CAS Google Scholar
Ziessman HA, Fahey FH, Hixson DJ (1992) Расчет фракции выброса желчного пузыря: преимущество непрерывной инфузии синкалида перед трехминутным методом инфузии. J Nucl Med 33: 537–547
PubMed CAS Google Scholar
Ziessman HA (1990) Холецистокининовая холесцинтиграфия: жертва собственного успеха? J Nucl Med 40: 2038–2042
Google Scholar
Lanzini A, Jazrawi RP, Northfield TC (1987) Одновременные количественные измерения абсолютного хранения и опорожнения желчного пузыря во время голодания и еды у людей. Гастроэнтерология 92: 852–861
PubMed CAS Google Scholar
Джазрави Р.П., Пацци П., Петрони М.Л. и др. (1995) Постпрандиальная моторная функция желчного пузыря: восполнение и оборот желчи при здоровье и холелитиазе. Гастроэнтерология 109: 582–591
PubMed Статья CAS Google Scholar
Pallotta N, Corazziari E, Scopinato F et al (1998) Неинвазивная оценка потока желчи через желчный пузырь у людей. Am J Gastroenterol 93: 1877–1885
PubMed Статья CAS Google Scholar
Раймонд Ф., Лепанто Л., Розенталь Л., Фрид Г.М. (1998) Tc99 Кинетика желчного пузыря mIDA и реакция на ХЦК при хроническом холецистите. Eur J Nucl Med 14: 378–381
Google Scholar
Hopman W, Jansen J, Rosebusch G (1986) Сокращение желчного пузыря, вызванное холецистокинином: болюсная инъекция или инфузия. Br Med J 292: 375–376
Статья CAS Google Scholar
Харви Р., Рид А. (1973) Влияние холецистокинина на моторику толстой кишки и симптомы у пациентов с синдромом раздраженного кишечника. Ланцет 1: 1–3
Статья Google Scholar
Morris-Stiff G, Falk G, Kraynk L, Rosenblatt S (2011) Тест HIDA на провокацию холецистокинина: воссоздание симптомов превосходит фракцию выброса в прогнозировании среднесрочных результатов. J Gastrointest Surg 15: 345–349
PubMed Статья Google Scholar
Westlake PJ et al (1990) Хроническая боль в правом верхнем квадранте без камней в желчном пузыре: прогнозирует ли сканирование HIDA исход после холесцинтиграфии? Am J Gastroenterol 85 (8): 986–990
PubMed CAS Google Scholar
Ziessman H, Tulchinsky M, Maurer A (2011) Консенсусный отчет по стандартизации холесцинтиграфии синкалидом. J Nucl Med 52:16
Артикул Google Scholar
Dibaise JK, Richmond BK, Ziessman HA et al (2011) Холецистинокинин-холесцинтиграфия у взрослых: согласованные рекомендации междисциплинарной группы. Clin Gastroenterol Hepatol 9: 376–384
PubMed Статья Google Scholar
Ziessman HA, Tulchinsky M, Lavely WC et al (2010) Холесцинтиграфия со стимуляцией цинкалидом: многоцентровое исследование для определения оптимальной методологии и нормальных значений фракции выброса желчного пузыря. J Nucl Med 51: 229–236
Статья Google Scholar
Riyad K, Chalmers C, Aldouri A, Fraser S, Menon K, Robinson P, Toogood G (2007) Роль 99m меченого технецием гепато-иминодиуксусной кислоты (HIDA) в сканировании лечение боли в желчных путях.HPB 9: 219–224
PubMed Статья CAS Google Scholar
Das A, Baijal SS, Sawaswat DM (1995) Влияние аспирина на моторику желчного пузыря у пациентов с желчнокаменной болезнью. Dig Dis Sci 40: 1782–1785
PubMed Статья CAS Google Scholar
Bingener J, Richards ML, Schwesinger WH et al (2004) Лапароскопическая холецистэктомия по поводу дискинезии желчевыводящих путей: корреляция результатов предоперационной холецистокининовой холесцинтиграфии с послеоперационным исходом.Surg Endosc 18: 802–806
PubMed Статья CAS Google Scholar
Carney DE, Kokoska ER, Grosfeld JL et al (2004) Предикторы успешного исхода холецистэктомии по поводу дискинезии желчевыводящих путей. J Pediatr Surg 39: 813–816
PubMed Статья Google Scholar
Chen PF, Nimeri A, Pham QH et al (2001) Клинический диагноз хронического бескаменного холецистита.Хирургия 130: 578–581
PubMed Статья CAS Google Scholar
DiBaise JK, Oleynikov D (2003) Предсказывает ли фракция выброса желчного пузыря исход холецистэктомии при подозрении на хроническую бескаменную дисфункцию желчного пузыря? Систематический обзор. Am J Gastroenterol 98 (12): 2605–2611
PubMed Статья Google Scholar
Patel NA, Lamb JJ, Hogle NJ et al (2004) Терапевтическая эффективность лапароскопической холецистэктомии при лечении дискинезии желчевыводящих путей.Am J Surg 187 (2): 209–212
PubMed Статья Google Scholar
Sunderland GT, Carter DC (1998) Клиническое применение холецистокининового провокационного теста. Br J Surg 75: 444–449
Артикул Google Scholar
Смайт А., Маджид А. В., Фиценри М. и др. (1998) Реквием по провокационному тесту на холецистокинин? Кишечник 43 (4): 571–574
PubMed Статья CAS Google Scholar
Adams D, Tarnasky P, Hawes R, Cunningham J, Brooker C, Brothers T, Cotton P (1998) Результат после лапароскопической холецистэктомии по поводу хронического бескаменного холецистита. Am Surg 64: 1–6
PubMed CAS Google Scholar
Bar-Meir S, Halpern Z, Bardan E, Gilat T (1984) Частота папиллярной дисфункции среди холецистэктомированных пациентов. Гепатология 4: 328–330
PubMed Статья CAS Google Scholar
Neoptolemos JP, Bailey IS, Carr-Locke DL (1988) Сфинктер дисфункции Одди: результаты лечения эндоскопической сфинктеротомией. Br J Surg 75: 454–459
PubMed Статья CAS Google Scholar
Murray WR (2011) Расслабление сфинктера Одди, вызванное ботулиническим токсином, может выбрать пациентов с бескаменной болью в желчных путях, которым будет полезна холецистэктомия. Surg Endosc 25: 813–816
PubMed Статья Google Scholar
Нормокинетическая дискинезия желчевыводящих путей: новый диагноз
Christopher G Ducoin, MD MPH , Daryl D Wier, MD FACS.Орландо Хелс, Центр пищеварительной и метаболической хирургии
Справочная информация:
Дискинезия желчевыводящих путей, диагностированная с помощью сканирования CCK-HIDA и фракции выброса менее 35%, успешно лечится лапароскопической холецистэктомией с разрешением симптомов от 77% до 97%. Тем не менее, есть группа пациентов с симптоматической болью в желчевыводящих путях, которые подвергаются негативному воздействию, включая «нормальное» сканирование CCK-HIDA с фракцией выброса более 35%, которые никогда не получают диагноз и, следовательно, не получают окончательного лечения.У некоторых из этих пациентов симптоматическая боль в желчных путях воспроизводится во время приема CCK-HIDA. Считается, что у этих пациентов установлен новый диагноз – нормокинетическая дискинезия желчевыводящих путей (НБД). NBD состоит из фракции выброса более 35%, полного отрицательного исследования и воспроизводимой боли в желчных путях с помощью сканирования CCK-HIDA. Предполагается, что после лечения холецистэктомией у этих пациентов исчезнет боль в желчных путях.
Методы:
С одобрения Институционального наблюдательного совета был завершен ретроспективный обзор карты пациентов с болью в желчных протоках в соответствии с критериями ROME III.В исследование вошли пациенты с отрицательным результатом обследования (минимум нормального УЗИ желчного пузыря и нормальной эндоскопией верхних отделов), зарегистрированными воспроизводимыми желчными симптомами при введении CCK во время сканирования HIDA и фракцией выброса более 35%. Метод лечения – лапароскопическая холецистэктомия. Точки данных включали: возраст, пол, продолжительность симптомов, фракцию выброса желчных протоков, продолжительность наблюдения, разрешение симптомов, тип операции и окончательную патологию.
Результаты:
За трехлетний период с августа 2008 г. по июль 2011 г. было обнаружено, что 19 пациентов соответствовали критериям включения в это исследование.У всех была задокументирована воспроизводимая боль в желчных путях при введении CCK во время сканирования HIDA и фракция выброса более 35% с полным отрицательным результатом. Было 15 женщин и 4 мужчин со средним возрастом 48,4 ± 13,0 лет, у всех фракция выброса превышала 35% со средним значением 75,1 ± 19,8%. Средняя продолжительность дооперационных симптомов составляла 7 ± 6 месяцев, а средний послеоперационный период наблюдения – 6 ± 3,5 месяцев. Пациенты наблюдались в клинике и связались с ними по окончании исследования.Всем пациентам была проведена лапароскопическая холецистэктомия. По окончательной патологии у 18 больных был хронический холецистит, у одного пациента – хронический холецистит с холестеролозом. Из пациентов, включенных в это исследование, у 16 было полное исчезновение симптомов, у двух – частичное исчезновение, а у одного – без изменений. Уровень полного излечения составил 84,2%, а показатель улучшения – 94,7%.
Заключение:
В литературе установлена эффективность лечения дискинезии желчевыводящих путей, диагностированной с помощью CCK-HIDA, и фракции выброса менее 35% с помощью лапароскопической холецистэктомии.Мы предполагаем, что тем пациентам, которые поступают с болью в желчевыводящих путях, полным отрицательным результатом обследования и воспроизводимыми симптомами при введении CCK во время сканирования HIDA, холецистэктомия будет полезна независимо от фракции выброса. Наибольшую пользу от этого получат те, у кого фракция выброса превышает 35%, которые в настоящее время исключены из диагностики дискинезии желчевыводящих путей и, следовательно, из лечения. Мы предполагаем новый диагноз – нормокинетическую дискинезию желчевыводящих путей и рекомендуем холецистэктомию в качестве лечения.
Номер сессии: SS03 – HPB (гепатобилиарная и поджелудочная железа)
Номер программы: S017
5,230
Связанные«Вернуться в архив рефератов SAGES 2012
Нормокинетическая дискинезия желчевыводящих путей: новый диагноз
Дискинезия желчевыводящих путей, диагностированная с помощью сканирования CCK-HIDA и фракции выброса менее 35%, успешно лечится лапароскопической холецистэктомией. Однако популяция пациентов с симптоматической болью в желчевыводящих путях и нормальным сканированием CCK-HIDA никогда не получает диагноз и, следовательно, не получает окончательного лечения.Некоторые из этих пациентов сообщают о воспроизводимой боли во время сканирования CCK-HIDA. Предполагается, что эти пациенты имеют новый диагноз – нормокинетическую дискинезию желчевыводящих путей и могут избавиться от боли при лечении холецистэктомией. Был завершен ретроспективный обзор карт пациентов с болью в желчных путях в соответствии с критериями ROME III. Дополнительными критериями включения были (1) возраст старше 18 лет, (2) воспроизводимые желчные симптомы во время сканирования CCK-HIDA и (3) фракция выброса более 35%.Метод лечения – лапароскопическая холецистэктомия. Описательная статистика была предварительно сформирована, и данные были представлены как среднее ± стандартное отклонение и диапазон. Девятнадцать пациентов соответствовали критериям включения в это исследование с августа 2008 года по июль 2011 года. Было 15 женщин и 4 мужчин со средним возрастом 48,4 ± 13,0 лет. Средняя фракция выброса составила 75,1 ± 19,4%. Средняя продолжительность дооперационных симптомов составила 6,8 ± 5,9 месяцев, а послеоперационное наблюдение – 21,8 ± 10,6 месяцев. У семнадцати пациентов симптомы полностью исчезли, у одного – частичное, а у одного – без изменений.Уровень полного излечения составил 89,5%, а показатель улучшения – 94,7%. Мы предполагаем, что пациенты с болью в желчных путях, нормальным сканированием CCK-HIDA с фракцией выброса более 35% и с воспроизводимыми симптомами при инфузии CCK могли иметь новый диагноз: нормокинетическая дискинезия желчевыводящих путей. В настоящее время эти пациенты исключены из диагностики дискинезии желчевыводящих путей и, следовательно, из лечения. Мы выдвигаем гипотезу о возможном новом диагнозе, предлагаем холецистэктомию в качестве лечения и рекомендуем проспективный дизайн исследования для дальнейшей оценки.
Нормокинетическое значение, произношение, происхождение и нумерология
нумерология нормокинетических имен – это 11 , и здесь вы можете узнать, как произносить нормокинетические, нормокинетические имена, нумерологию и похожие имена на нормокинетические.
Как произносится normokinetic?
Голосовое произношение:Щелкните и прослушайте аудио произношение несколько раз и узнайте, как произносится имя normokinetic.Если вы чувствуете, что произношение должно быть лучше, запишите произношение своим голосом и помогите другим.
Запишите произношение своим голосом
Запись произношения
Примечание: попробуйте записать произношение в течение 3 секунд.
Начать запись
00:00
Мы продолжаем добавлять значения и другую информацию ко всем именам. Так что продолжайте посещать снова, чтобы узнать значение этого имени и другую информацию.
«Поиск заканчивается при запуске совместного доступа»Если вы уже знаете значение слова normokinetic на английском или на любом другом языке, внесите свой вклад, который будет полезен для других пользователей, также вы можете редактировать любые данные, такие как пол, произношение и происхождение, для повышения точности.
нормокинетическое имя Нумерология
| Нумерология (число выражений) | 11 | ||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Число желаний сердца | 8 | ||||||||||||||||||||||||||
| Число личности | 3 9048 | 905 number 11
| N | Nourish | ||||||||
| O | Отличный | ||||||||
| R | Замечательный | ||||||||
| M | Главный | ||||||||
| I | Представьте себе | ||||||||
| N | Новый | ||||||||
| E | Entertainer | ||||||||
| T | Благодарный | ||||||||
| 🎵⚽🌱〽️⚽🎋🎐🎵🎗🌴🎐🌜 | |||
| ⓝⓞⓡⓜⓞⓚⓘⓝⓔⓣⓘⓒ | |||
| uoɹɯoʞᴉuǝʇᴉɔ | |||
| 𝕟𝕠𝕣𝕞𝕠𝕜𝕚𝕟𝕖𝕥𝕚𝕔 | |||
| 🅽🅾🆁🅼 🅾🅺🅸🅽🅴🆃🅸🅲 | |||
| N ♥ O ♥ R ♥ M ♥ O ♥ K ♥ I ♥ N ♥ E ♥ T ♥ I ♥ C ♥ | |||
| ҉N҉҉O҉҉R҉҉M҉҉O҉҉K҉҉I҉҉N҉҉E҉҉T҉҉I҉҉C҉ | ♥ 90几5 Ҝ 丨 几 乇 ㄒ 丨 匚 |
Как и выше, 30+ причудливых текстовых стилей доступны для имени « normokinetic » в нашем генераторе необычных текстов.Пойдите и проверьте все стили, чтобы получить больше удовольствия!
Популярные люди и знаменитости с нормокинетическим именем
На данный момент народов не найдено! Ваше имя нормокинетическое или Если вы знаете людей по нормокинетическому имени, добавьте его в список. Добавить Народы по нормокинетическому имени
Добавить людей по имени normokinetic
Комментарии пользователей о нормокинетике
- Комментариев пока нет. Прокомментируйте первым.
Вы можете заинтересовать
Имена, похожие на Normokinetic
Нужна помощь или отзывы? Сообщите нам
Влияние мио-инозитола in vitro на нормокинетические образцы спермы человека с нелинейной подвижностью
Eur Rev Med Pharmacol Sci 2019; 23 (23): 10557-10563DOI: 10.26355 / eurrev_201912_19697
Ф. Паллотти, Ф. Карнелутти, Г. Сенофонте, Т. Карлини, Ф. Фая, Д. Паоли, Ф. Ломбардо
Отделение экспериментальной медицины, лаборатория семинологии – Банк спермы «Лоредана Гандини», «Сапиенца» Римский университет, Рим, Италия. [email protected]
ЦЕЛЬ: Поскольку дефицит мио-инозитола (МИ) был связан с ухудшением качества спермы, мы стремились объективно оценить его влияние на кинетику сперматозоидов, используя систему компьютерного анализа спермы (CASA).
ПАЦИЕНТЫ И МЕТОДЫ: Мы оценили 59 нормокинетических образцов спермы с нелинейно-прогрессирующей подвижностью до и после инкубации с раствором ИМ. Образцы были собраны у здоровых людей в возрасте 20-40 лет, которые посещали нашу лабораторию семинологии для скрининга фертильности.
РЕЗУЛЬТАТЫ: Мы обнаружили значительное увеличение линейно-прогрессирующей подвижности (28,2% ± 10,8 против 30,9% ± 11,0, T0 против T1 соответственно; p <0,001) и значительное снижение нелинейно-прогрессивной подвижности (21.0% ± 9,9 против 18,1% ± 10,2, T0 против T1 соответственно; p <0,001) после инкубации с MI. Анализ CASA выявил значительное увеличение криволинейной скорости (VCL) (65,0 ± 19,0 против 67,9 ± 20,4 мкм / с, T0 против T1 соответственно; p = 0,049). В целом, было увеличение VCL в 42/59 выборках (около 70%), в основном у некурящих.
ВЫВОДЫ: Эти результаты предполагают, что ИМ оказывает положительное влияние на образцы спермы in vitro, но необходимо подтверждение посредством дальнейших исследований с учетом факторов, способных модулировать ответ ИМ, таких как курение и ожирение.



 Омск)
Омск)
 м.н., доцент кафедры госпитальной терапии Уральского государственного медицинского университета, Главный гастроэнтеролог Уральского федерального округа (г. Екатеринбург)
м.н., доцент кафедры госпитальной терапии Уральского государственного медицинского университета, Главный гастроэнтеролог Уральского федерального округа (г. Екатеринбург)
 20-11.45
20-11.45
 20 – 13.00
20 – 13.00
 м.н., доцент кафедры госпитальной терапии Уральского государственного медицинского университета, Главный гастроэнтеролог Уральского федерального округа (г. Екатеринбург)
м.н., доцент кафедры госпитальной терапии Уральского государственного медицинского университета, Главный гастроэнтеролог Уральского федерального округа (г. Екатеринбург)
 м.н. И.Б Хлынов, доцент Т.Л. Лапина
м.н. И.Б Хлынов, доцент Т.Л. Лапина
 м.н. И.Б. Хлынов, профессор А.С. Сарсенбаева
м.н. И.Б. Хлынов, профессор А.С. Сарсенбаева
 Екатеринбург)
Екатеринбург)