Панкреато билиарная система: Панкреато-билиарная зона в свете эндоскопических манипуляций
Панкреато-билиарная зона в свете эндоскопических манипуляций
Пестерев Л. Г., к. м. н.,
Смирнова О. Ю., к. м. н.
Двенадцатиперстная кишка, duodenum небольшая по длине, но очень важная по функции, является продолжением желудка, принимает выводные протоки печени и поджелудочной железы. В ней прекращается процесс желудочного пищеварения и начинается изменение пищевой кашицы под влиянием сока поджелудочной железы и желчи.
Расположена duodenum глубоко, фиксирована почти неподвижно. В ней различают 4 части: верхнюю (ампула, или луковица), нисходящую, нижнюю горизонтальную и восходящую.
Верхняя часть расположена спереди от позвоночника на уровне хряща между 12 грудным и 1 поясничным позвонками, покрыта брюшиной со всех сторон (интраперитонеально) и в области верхнего изгиба фиксирована при помощи печеночно-двенадцатиперстной связки.
Нисходящая часть расположена справа от позвоночника между 1 и 3 поясничными позвонками, при помощи нижнего изгиба переходит в нижнюю горизонтальную часть.
Слева от позвоночника нижняя горизонтальная часть переходит в восходящую часть, последняя слева от 2 поясничного позвонка — в тощую кишку. Переход осуществляется в виде изгиба, flexura duodenojejunalis, здесь же находится m.suspensorius duodeni (мышца Трейтца).
Стенка кишки построена по общему принципу: имеется слизистая, подслизистая, мышечная оболочки.
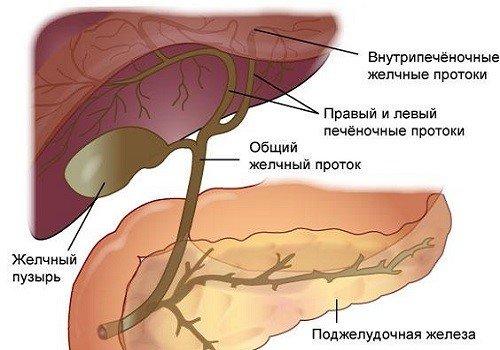
Из особенностей слизистой оболочки можно выделить отсутствие циркулярных складок в луковице кишки, наличие особых дуоденальных (Бруннеровых) желез (рис. 1). B нисходящей части кишки имеется продольная складка, заканчивающаяся сосочком с отверстием — papilla duodeni major (фатеров). Наличие продольной складки обусловлено прохождением через слои стенки двенадцатиперстной кишки общего желчного протока, который перед впадением в кишку, соединяется с протоком поджелудочной железы.
Рис. 1.
Общий желчный проток, ductus choledochus (billiaris), в свою очередь, является результатом слияния общего печеночного и пузырного протоков.
Рис. 2.
Эпителий располагается на собственной пластинке слизистой. В желчном пузыре мышечная пластинка отсутствует, поэтому слизистая лежит на слое гладко-мышечной ткани, сходной с мышечной оболочкой кишки.
За мышечной оболочкой лежит хорошо развитая перимускулярная (субсерозная) оболочка, состоящая из рыхлой соединительной ткани. Со стенки желчного пузыря она переходит в соединительную ткань печени.
Шейка желчного пузыря перекручена таким образом, что ее слизистая образует спиральную складку. Сходные полулунные складки имеются и в выстилке желчного пузыря.
Общий желчный проток прободает наружные оболочки двенадцатиперстной кишки вблизи места впадения протока поджелудочной железы. На полпути через стенку кишки оба протока сливаются друг с другом, а просвет протока, образовавшегося в результате слияния расширяется и называется а м п у л о й. Ампула идет косо через внутренние слои стенки двенадцатиперстной кишки, открываясь на верхушке сосочка, который выступает в просвет кишки (дуоденальный, или фатеров сосочек).
На полпути через стенку кишки оба протока сливаются друг с другом, а просвет протока, образовавшегося в результате слияния расширяется и называется а м п у л о й. Ампула идет косо через внутренние слои стенки двенадцатиперстной кишки, открываясь на верхушке сосочка, который выступает в просвет кишки (дуоденальный, или фатеров сосочек).
Считалось, что мышца, связанная с ампулой, и конечные отрезки двух протоков, входящих в ампулу, совместно образуют сфинктер Одди. Однако эта мышца развивается независимо от мышцы собственно стенки кишки и не является ее частью. Мышца вокруг преампулярной части желчного протока утолщается и служит в качестве сфинктера у выходной части желчного протока; ее иногда называют сфинктером Бойдена (рис. 3).
Рис. 3.
Мышца, которая развивается из самой ампулы и преампулярной части панкреатического протока, недостаточно развита, чтобы считать ее истинным сфинктером.
Сокращение мощного сфинктера Бойдена вокруг ампулярной части общего желчного протока закрывает путь в кишку секрету печени, в результате желчь (когда сфинктер закрыт) отводится по пузырному протоку в желчный пузырь, где она накапливается и концентрируется. Концентрация осуществляется путем всасывания воды и неорганических солей сквозь эпителий в сосуды собственной пластинки слизистой оболочки. Варианты строения пузырного и желчных протоков представлены на рис. 4.
Концентрация осуществляется путем всасывания воды и неорганических солей сквозь эпителий в сосуды собственной пластинки слизистой оболочки. Варианты строения пузырного и желчных протоков представлены на рис. 4.
Рис. 4.
Проток поджелудочной железы, ductus pancreaticus (Вирсунгов), расположен внутри этой железы, соединяется с общим желчным недалеко от впадения последнего в двенадцатиперстную кишку (рис. 5).
Рис. 5.
Поджелудочная железа, состоящая из головки, тела и хвоста, расположена в брюшной полости кпереди от тела 1 поясничного позвонка и покрыта брюшиной с одной стороны (экстраперитонеально). Главный проток окружен соединительной тканью. От него на определенных расстояниях под углом отходят ветви. Боковые ветви проходят между дольками и поэтому называютсямеждольковыми протоками (рис. 5). Они ветвятся и даютначало внутридольковым протокам, входящим в вещество долек. Просвет главного протока выстлан цилиндрическим эпителием.
Помимо главного (вирсунгова) протока, встречается еще один проток, ductus pancreaticus accessorius (Santorini)./biliary_tract-59cdd4e6845b340011ea825c.jpg) Открывается он в кишку проксимально от фатерова сосочка в виде papilla duodeni minor (рис. 3).Наличие его объясняется развитием железы.
Открывается он в кишку проксимально от фатерова сосочка в виде papilla duodeni minor (рис. 3).Наличие его объясняется развитием железы.
Рис. 6.
Поджелудочная железа закладывается в виде двух выростов эпителиальной (энтодермальной) выстилки развивающейся двенадцатиперстной кишки. Чаще оба выпячивания объединяются, но иногда каждый из этих выростов сохраняет связь с кишкой в виде протока. Варианты протоков представлены на рис. 6.
Хирургия гепато-панкреато-билиарной зоны | Fortis Memorial Research Institute
Отделение гепато-панкреато-билиарной хирургии в ИМИФ специализируется в диагностике и лечении целого набора доброкачественных и злокачественных хирургических заболеваний, связанных с печенью, поджелудочной железой, желчным пузырем и желчными путями. Наша профессиональная команда хирургов посвятила себя выполнению сложных операций на печени, поджелудочной железе, желчном протоке и пузыре.
Наша хирургическая команда обладает набором прекрасных навыков, необходимых как для проведения обычных, так и для выполнения современных лапароскопических операций, имеет прекрасный опыт резекций печени, операций по поводу рака желчного пузыря и желчных протоков, а также хирургического лечения заболеваний поджелудочной железы, включая панкреатит и рак поджелудочной железы.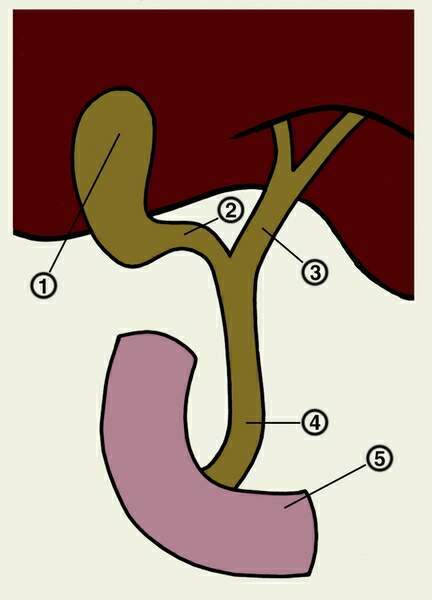
Мемориальный исследовательский институт Фортис является центром направления пациентов (учреждением) третьего уровня и в этой связи в нашем отделении постоянно и эффективно получают помощь пациенты с осложненными случаями таких заболеваний.
Со стороны технологий, в Отделении имеются интегрированные операционные блоки и ультрасовременные блоки интенсивной терапии, которые обеспечивают превосходный уровень оказания помощи пациентам в поддерживающем окружении. Сотрудники отделения все в большей степени вовлечены в выполнение пересадок печени и имеют опыт во всех связанных с этим аспектах трансплантологии, таких, как пересадка печени от умершего и живого донора.
Наша программа имеет давнюю традицию лечения терминальной стадии заболевания печени и портальной гипертензии, а также обеспечения полного цикла мероприятий по поддержанию жизни при трансплантации печени. Наша многопрофильная команда специалистов по пересадке печени состоит из хирургов-трансплантологов печени, гепатологов-трансплантологов, гастроэнтерологов, анестезиологов, патологов, радиологов, медсестер и прочих специалистов, которые имеют большой опыт в лечении печеночной недостаточности.
Предлагаемые услуг
- Печень
- Кисты печени;
- Цирроз печени;
- Эхинококковые кисты;
- Травма печени;
- Гепатоклеточный рак;
- Метастатической колоректальный рак
- Метастатические нейроэндокринные опухоли;
- Желчный пузырь
- Камни желчного пузыря
- Карцинома желчного пузыря;
- Ксантогранулематозный холецистит
- Желчные протоки
- Атрезия желчных путей;
- Постхолецистэктомические повреждения желчных путей;
- Стриктура желчных путей;
- Раки желчных путей;
- Камни желчных путей;
- Возвратный пиогенный холангит;
- Кисты холедоха;
- Портальная билиопатия
- Поджелудочная железа
- Острый панкреатит и его осложнения;
- Хронический панкреатит и его осложнения;
- Рак поджелудочной железы;
- Псевдокисты поджелудочной железы;
- Нейроэндокринные опухоли
- Травма поджелудочной железы;
- Панкреатические асцит и плевральный выпот.

- Разное
- Портальная гипертензия: наложение портосистемных шунтов при внепеченочной обструкции портальной вены и портальном фиброзе не цирротической этиологии;
- Аневризмы и псевдо аневризмы висцеральной артерии.
Ретракторная система Thompson при онкологических операциях на печени, желудке, поджелудочной железе и желчевыводящих путях
Универсальная онкологическая гепато-панкреато-билиарная ретракторная система Thompson предназначена для множественных видов хирургических операций при онкологических операциях на печени, желудке, поджелудочной железе и желчевыводящих путях. Ранорасширительная система легко настраивается над нужной областью органа, к которому нужен доступ. Используя двустороннюю планку ретрактора, система Thompson дает хирургам возможность получить стабильную, универсальную, бескомпромиссную экспозицию и ретракцию при трансплантации печени, резекции печени, онкологии и случаях ожирения.
Ключевые особенности ретракторной онкологической гепато-панкреато-билиарная ретракторной системы Thompson :
- Обеспечение устойчивости;
- Антискользящие лезвия Balfour (Белфур) анатомически разработаны мягко захватывают ткань, чтобы предотвратить соскальзывание во время отвода реберного края;
- Двусторонняя (билатеральная) устойчивость и жесткость.
 Стабильность при широкой экспозиции и асимметричной ретракции реберного края.
Стабильность при широкой экспозиции и асимметричной ретракции реберного края. - Микро регулируемый механизм обеспечивает контролируемую и сильную ретракцию ткани. Особенно полезно для отвода ребер.
- Позволяет использовать многомерную ретракцию и асимметрическую ретракцию реберного края, а также обеспечивает высокую стабильность для крупных пациентов;
- Позволяет хирургу возможность освободить руки;
- Легкость в установке;
- Простота в использовании.
Этот базовый набор ранорасширительной системы Thompson при онкологических операциях на печени, поджелудочной железе и желчевыводящих путях подойдет для каждой современной операционной. Набор можно пополнять дополнительными рукоятками и нужными лезвиями с разными размерами.
За более подробной информацией по ретракторним системам Thompson обращайтесь к нашим специалистам.
Ретракторная система Thompson с рентгенопрозрачными лезвиями при онкологических операциях на печени, желудке, поджелудочной железе и желчевыводящих путях
Универсальная онкологическая гепато-панкреато-билиарная ретракторная система Thompson с рентгенопрозрачными лезвиями предназначена для множественных видов хирургических операций при онкологических операциях на печени, желудке, поджелудочной железе и желчевыводящих путях с использованием цифровой рентгенографии. Ранорасширительная система легко настраивается над нужной областью органа, к которому нужен доступ. Используя двустороннюю планку ретрактора, система Thompson дает хирургам возможность получить стабильную, универсальную, бескомпромиссную экспозицию и ретракцию при трансплантации печени, резекции печени, онкологии и случаях ожирения. В сочетании с широким выбором рентгенопрозрачных лезвий онкологическая гепато-панкреато-билиарная ретракторная система с установкой билатеральной планки предлагает многоплановую ретракцию и неограниченную гибкость для самых сложных случаев брюшной полости и таза. Все лезвия (ложки, лопатки) сделаны из высокопрочной стали с рентгенопрозрачным покрытием и анодированным алюминием, предоставляя непревзойденную ретракцию, доступ и обзор. Также имеет первостепенное значение наличие ложек (лопаток) для пациентов с избыточным весом и ожирением. Ретракторная система Thompson для гепато-панкреато-билиарных вмешательств, где используется метод цифровой рентгенографии сокращает время проведения операции, уменьшает количество задействованных инструментов, уменьшает количество людей в операционной и уменьшает физическую нагрузку на хирургов.
Ранорасширительная система легко настраивается над нужной областью органа, к которому нужен доступ. Используя двустороннюю планку ретрактора, система Thompson дает хирургам возможность получить стабильную, универсальную, бескомпромиссную экспозицию и ретракцию при трансплантации печени, резекции печени, онкологии и случаях ожирения. В сочетании с широким выбором рентгенопрозрачных лезвий онкологическая гепато-панкреато-билиарная ретракторная система с установкой билатеральной планки предлагает многоплановую ретракцию и неограниченную гибкость для самых сложных случаев брюшной полости и таза. Все лезвия (ложки, лопатки) сделаны из высокопрочной стали с рентгенопрозрачным покрытием и анодированным алюминием, предоставляя непревзойденную ретракцию, доступ и обзор. Также имеет первостепенное значение наличие ложек (лопаток) для пациентов с избыточным весом и ожирением. Ретракторная система Thompson для гепато-панкреато-билиарных вмешательств, где используется метод цифровой рентгенографии сокращает время проведения операции, уменьшает количество задействованных инструментов, уменьшает количество людей в операционной и уменьшает физическую нагрузку на хирургов. Конструкция легко разбирается и транспортируется на стерилизацию.
Конструкция легко разбирается и транспортируется на стерилизацию.
Ключевые особенности ретракторной онкологической гепато-панкреато-билиарная ретракторной системы Thompson с рентгенопрозрачными лезвиями:
- Рентгенопрозрачный лезвия позволяют проводить холангиографию благодаря меньшим разрезам, это способствует сокращению операционного времени и более динамичной интеграции рентгеновских методов при хирургических вмешательствах;
- Позволяет проводить ретракцию на разной высоте, а также асимметричную ретракцию реберного края, обеспечивая при этом прочную стабильность для крупных пациентов;
- Превосходно подходит для операций, где используется метод цифровой рентгенографии;
- Лезвия Balfour (Белфур) анатомически разработаны мягко захватывают ткань, чтобы предотвратить соскальзывание во время отвода реберного края;
- Двусторонняя (билатеральная) устойчивость и жесткость. Стабильность при широкой экспозиции и асимметричной ретракции реберного края.

- Микро регулируемый механизм обеспечивает контролируемую и сильную ретракцию ткани. Особенно полезно для отвода ребер.
- Позволяет использовать многомерную ретракцию и асимметрическую ретракцию реберного края, а также обеспечивает высокую стабильность для крупных пациентов;
- Позволяет хирургу возможность освободить руки;
- Легкость в установке;
- Обеспечение устойчивости;
- Простота в использовании.
Этот базовый набор ранорасширительной системы Thompson при онкологических операциях на печени, поджелудочной железе и желчевыводящих путях с рентгенопрозрачными лезвиями подойдет для каждой современной операционной которая использует цифровую рентгенографию и холангиографию. Набор можно пополнять дополнительными рукоятками и нужными лезвиями с разными размерами.
За более подробной информацией по ретракторним системам Thompson обращайтесь к нашим специалистам.
Гепато-панкреато-биллиарная школа 2014
Гепато-панкреато-биллиарная школа 2014
«ДИАГНОСТИКА ЗАБОЛЕВАНИЙ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ – ВЗГЛЯД ТЕРАПЕВТА» ШКОЛА HPB ХИРУРГИИ.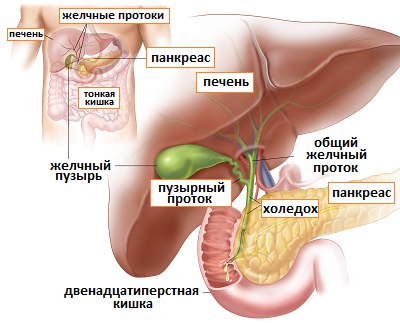 КБ № 122 – 2014 г.
КБ № 122 – 2014 г. «Школа HPB хирургии» Конференция в КБ № 122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014). Лекция проф. Л.К. Пальговой. Классификация заболеваний поджелудочной железы. Острый и хронический панкреатит. Диагностика заболеваний поджелудочной железы. Аутоиммунный панкреатит: критерии диагноза, вопросы дифференциальной диагностики, в том числе, с карциномой поджелудочной железы. Аномалии развития поджелудочной железы. Поражение поджелудочной железы при диффузных заболеваниях соединительной ткани.
«ЛУЧЕВАЯ ДИАГНОСТИКА ЗАБОЛЕВАНИЙ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ». ШКОЛА HPB ХИРУРГИИ КБ № 122
«Школа HPB хирургии» Конференция в КБ № 122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014). Лекция профессора В.А. Ратникова. Оценка возможностей МРТ, МСКТ, сцинтиграфии, ПЭТ-КТ, ЭУС, ЭРХПГ. Оценка очаговых поражений поджелудочной железы. В лекции рассмотрены преимущества и недостатки методов. Сформулированы принципы построения диагностических алгоритмов.
Лекция профессора В.А. Ратникова. Оценка возможностей МРТ, МСКТ, сцинтиграфии, ПЭТ-КТ, ЭУС, ЭРХПГ. Оценка очаговых поражений поджелудочной железы. В лекции рассмотрены преимущества и недостатки методов. Сформулированы принципы построения диагностических алгоритмов.
«ЭУС ПРИ ЗАБОЛЕВАНИЯ ПАНКРЕАТО-БИЛИАРНОЙ ЗОНЫ». ШКОЛА HPB ХИРУРГИИ. КБ № 122 – 2014 г.
Школа HPB хирургии» Конференция в КБ № 122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014). Лекция Alberto Larghi (Италия). Роль ЭУС при различных заболеваниях. Холедохолитиаз. Солидные образования поджелудочной железы. Кистозные неоплазии поджелудочной железы. Интервенционные вмешательства под ЭУС-контролем. Роль ЭУС при карциноме поджелудочной железы, нейроэндокринных опухолях. Что может выявить ЭУС в дополнение к КТ и МРТ.
МЕТОДЫ ПОЛУЧЕНИЯ МАТЕРИАЛА ПРИ ЭУС.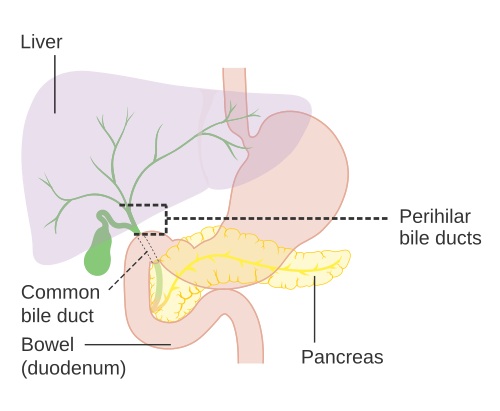 ШКОЛА HPB ХИРУРГИИ КБ № 122. ШКОЛА HPB ХИРУРГИИ. КБ № 122
ШКОЛА HPB ХИРУРГИИ КБ № 122. ШКОЛА HPB ХИРУРГИИ. КБ № 122
Школа HPB хирургии» Конференция в КБ № 122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014). Лекция М.С.Бурдюкова.
ДИАГНОСТИКА ЗАБОЛЕВАНИЙ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ – ВЗГЛЯД МОРФОЛОГА ШКОЛА HPB ХИРУРГИИ. КБ № 122.
Школа HPB хирургии» Конференция в КБ№122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014). Лекция С.Л.Воробьева.
МУЛЬТИДИСЦИПЛИНАРНЫЙ ПОДХОД В КЛИНИКЕ. ШКОЛА HPB ХИРУРГИИ. КБ № 122
«Школа HPB хирургии» Конференция в КБ № 122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014).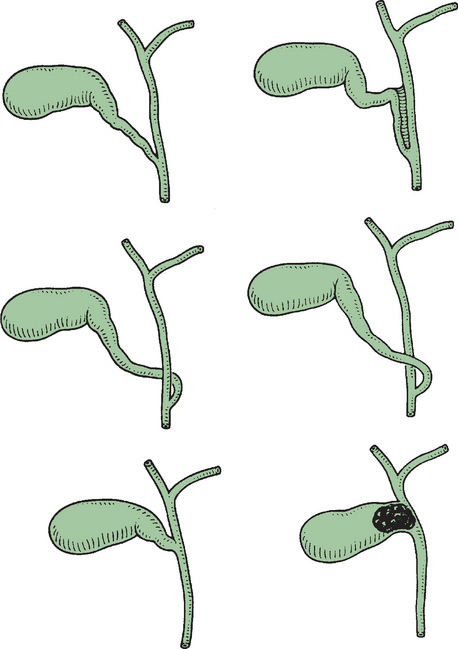 Лекция проф. В.А.Кащенко. Мультидисциплинарный подход к диагностике и лечению заболеваний гепато-панкреато-билиарной зоны. Проблемы взаимодействия хирургов, терапевтов и диагностов в клинике.
Лекция проф. В.А.Кащенко. Мультидисциплинарный подход к диагностике и лечению заболеваний гепато-панкреато-билиарной зоны. Проблемы взаимодействия хирургов, терапевтов и диагностов в клинике.
ХОЛЕСТАТИЧЕСКИЕ ЗАБОЛЕВАНИЯ ПЕЧЕНИ. ШКОЛА HPB ХИРУРГИИ. КБ № 122.
«Школа HPB хирургии» Конференция в КБ № 122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014). Лекция проф. К.Л.Райхельсон.
«КИСТОЗНЫЕ НЕОПЛАЗИИ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ» ШКОЛА HPB ХИРУРГИИ. КБ № 122 – 2014 г.
«Школа HPB хирургии» Конференция в КБ № 122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014). Лекция Васюковой Е.Л. – врач-хирург КБ№122. Рассмотрены вопросы диагностики, дифференциальной диагностики лечебной тактики при кистозных неоплазиях поджелудочной железы.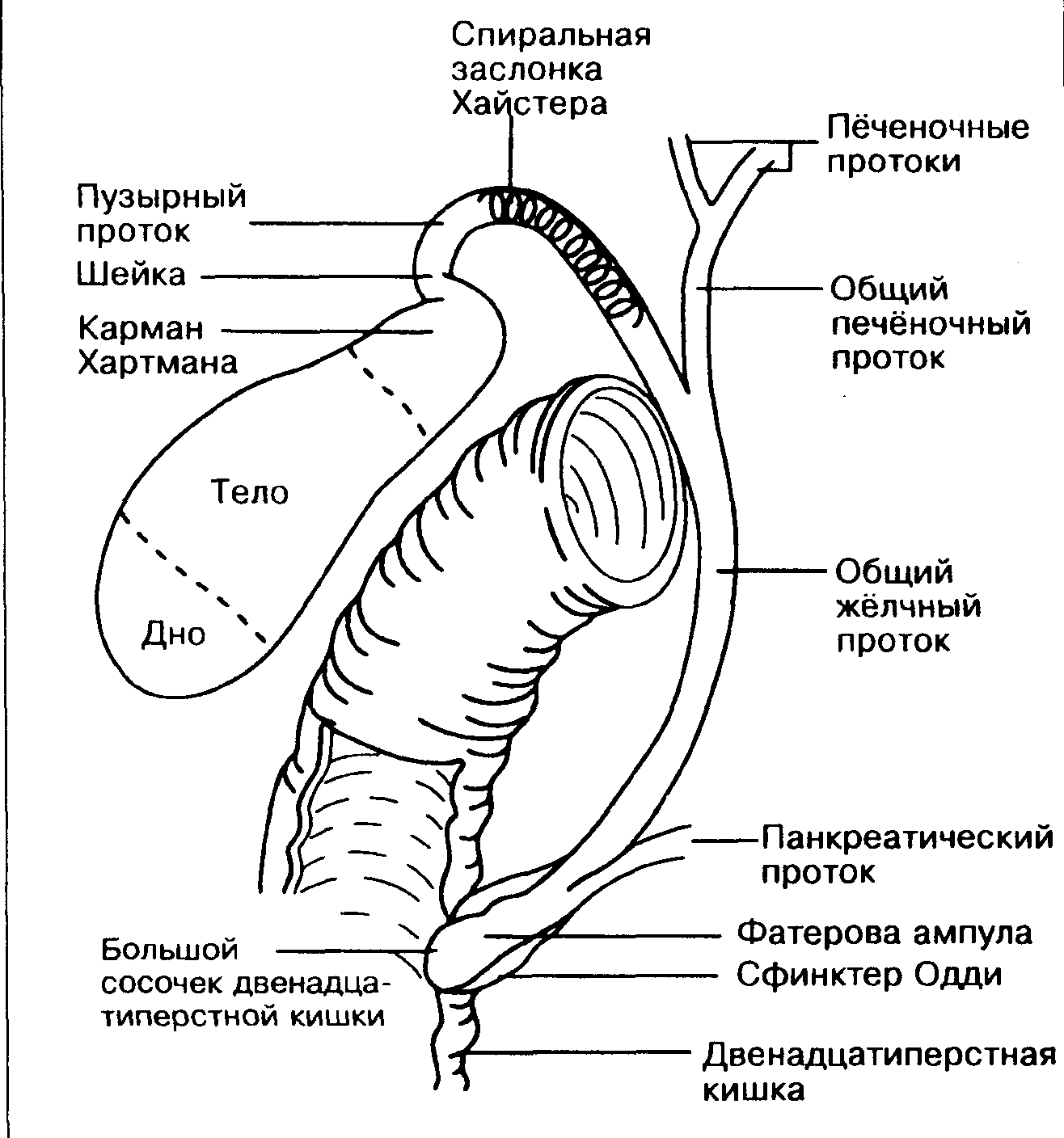 К кистозным неоплазиям относят следующие основные группы: серозная кистозная неоплазия (СКН/SCN), муцинозная кистозная неоплазия (МКН/MCN), внутрипротоковые папиллярные муцинозные неоплазии (ВПМН/IPMN), солидная псевдопапиллярная неоплазия, кистозная эндокринная опухоль и другие, гораздо более редкие формы.
К кистозным неоплазиям относят следующие основные группы: серозная кистозная неоплазия (СКН/SCN), муцинозная кистозная неоплазия (МКН/MCN), внутрипротоковые папиллярные муцинозные неоплазии (ВПМН/IPMN), солидная псевдопапиллярная неоплазия, кистозная эндокринная опухоль и другие, гораздо более редкие формы.
ЭРХПГ – ПОКАЗАНИЯ И КЛИНИЧЕСКИЕ ПРЕИМУЩЕСТВА. ШКОЛА HPB ХИРУРГИИ. КБ № 122.
«Школа HPB хирургии» Конференция в КБ № 122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014). Лекция A.Dechene (Германия).
ЭНДОСКОПИЯ В ДИАГНОСТИКЕ ЗАБОЛЕВАНИЙ БДС. ШКОЛА HPB ХИРУРГИИ. КБ № 122.
«Школа HPB хирургии» Конференция в КБ № 122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014).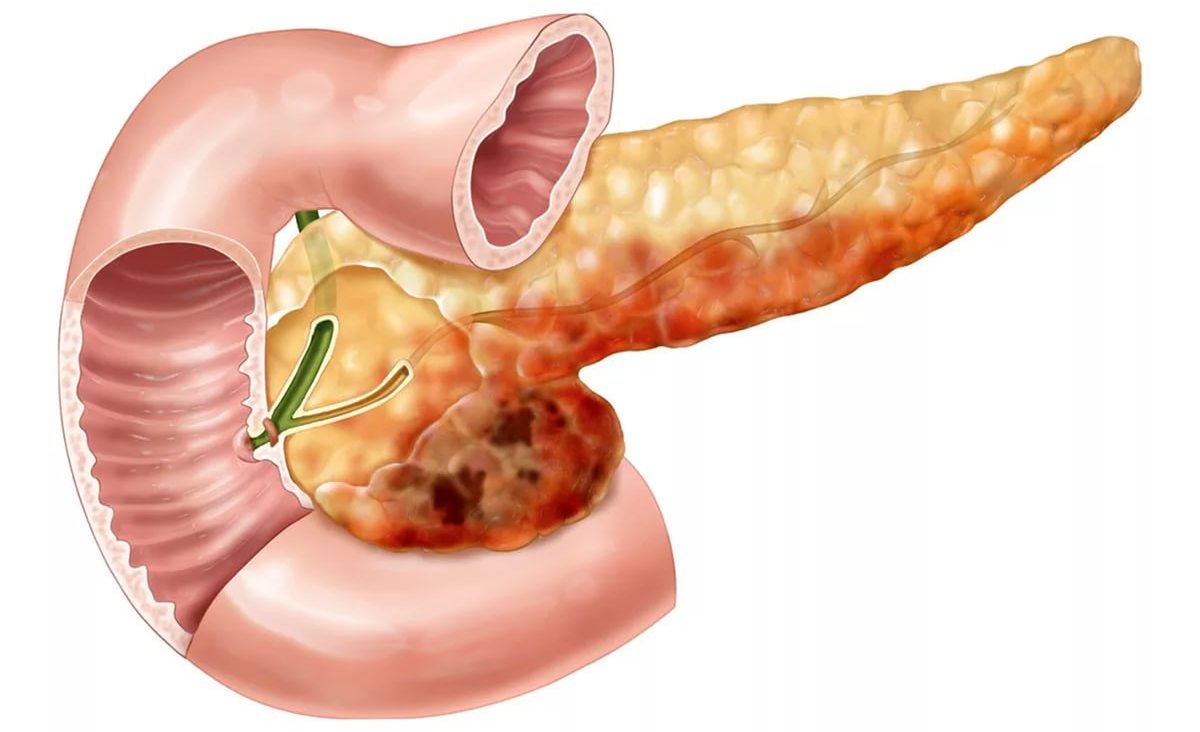 Лекция Е.Г.Солоницына – доцента кафедры факультетской хирургии СПбГУ (зав.кафедрой В.А.Кащенко), ведущего эндоскописта КБ№122.
Лекция Е.Г.Солоницына – доцента кафедры факультетской хирургии СПбГУ (зав.кафедрой В.А.Кащенко), ведущего эндоскописта КБ№122.
ДИАГНОСТИКА ЗАБОЛЕВАНИЙ ГЕПАТОБИЛИАРНОЙ ЗОНЫ. ШКОЛА HPB ХИРУРГИИ. КБ № 122 – 2014 г.
«Школа HPB хирургии» Конференция в КБ № 122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014). Лекция профессора Ратников В.А. Оценка возможностей МРТ, МСКТ, сцинтиграфия, ПЭТ-КТ, ЭУС, ЭРХПГ. Оценка состояния билиарного тракта, оценка очаговых поражений печени. В лекции рассмотрены преимущества и недостатки методов. Сформулированы принципы построения диагностических алгоритмов.
МОРФОЛОГИЧЕСКИЕ ИССЛЕДОВАНИЯ ПРИ ЗАБОЛЕВАНИЯХ ЖЕЛЧНЫХ ПРОТОКОВ. ШКОЛА HPB ХИРУРГИИ. КБ № 122.
Школа HPB хирургии» Конференция в КБ № 122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014). Лекция С.Л.Воробьева.
Лекция С.Л.Воробьева.
«ОПУХОЛИ ПАНКРЕАТО-БИЛИАРНОЙ СИСТЕМЫ» ШКОЛА HPB ХИРУРГИИ КБ № 122
«Школа HPB хирургии» Конференция в КБ № 122 «Избранные вопросы диагностики и лечения заболеваний панкреато-билиарной зоны» (2014). Лекция доцента Рыкова И.В – зав. Отделением онкологии КБ № 122. Рак поджелудочной железы – проблема поздней диагностики. Роль методов лучевой диагностики. Зачем нам нужна и почему важна биопсия опухоли поджелудочной железы? Значение оценки онкомаркеров. Хирургия+химиотерапия – как построить лечебную программу. Рак желчных протоков. Рак желчного пузыря.
Состояние панкреатобилиарной системы и интестинальной микрофлоры у детей с неалкогольной жировой болезнью печени Текст научной статьи по специальности «Клиническая медицина»
Орипнальш досл1дження Original Researches ■ < ■ | ГАСТРОЕНТЕРОЛОПЯ GASTROENTEROLOGY
Гастроентеролопчш захворювання у д1тей / Gastroenterological Diseases in Children
УДК 616.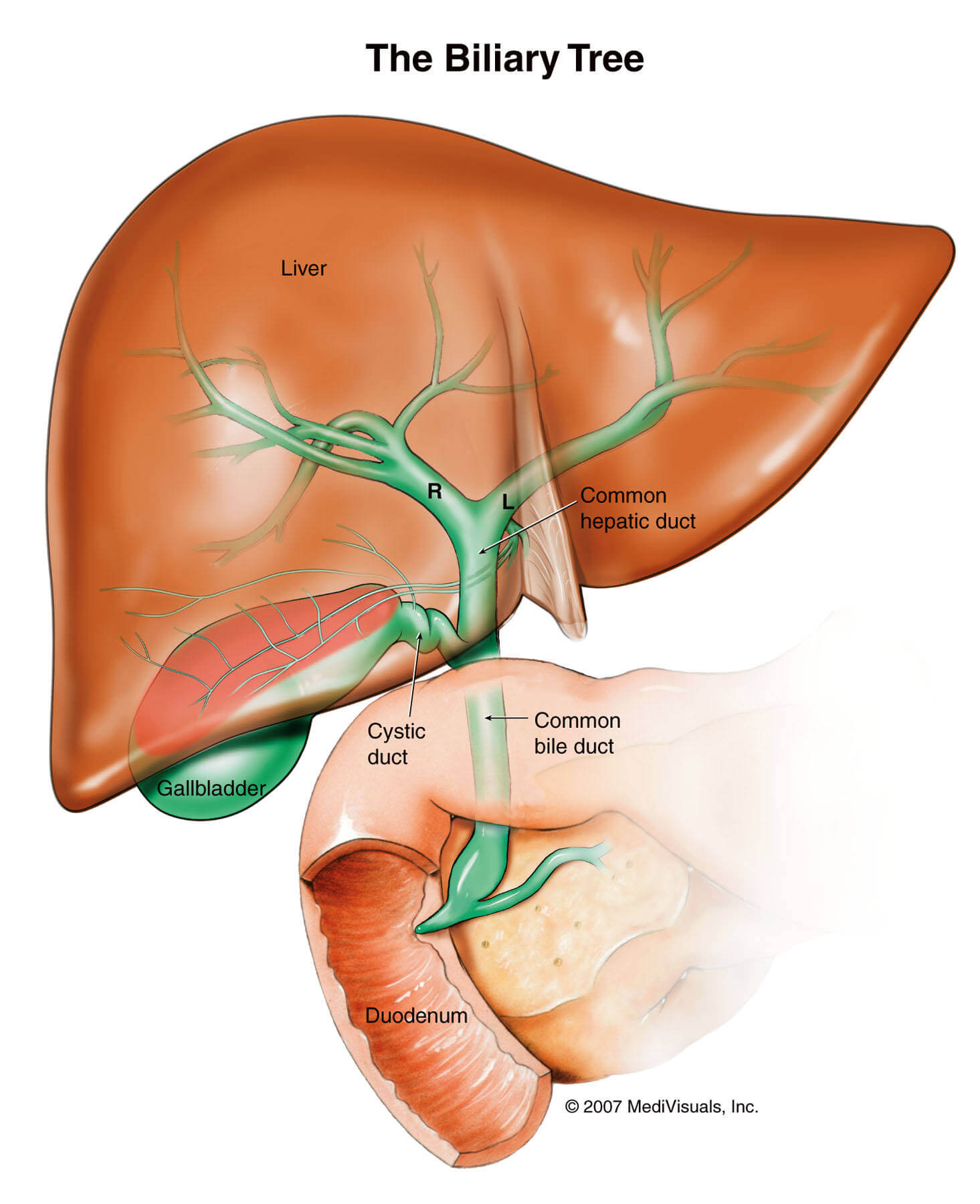 36-002.8+616-053.2/612.336.8
36-002.8+616-053.2/612.336.8
DOI: 10.22141/2308-2097.4.62.2016.81092
№
/ i
ЗАВГОРОДНЯ Н.Ю., ЛУК’ЯНЕНКО О.Ю., КОНЕНКО 1.С. ДУ «1нститутгастроентерологп НАМН Украни», м. Дн1про, Украна
СТАН ПАНКРЕАТОБШАРНОТ СИСТЕМИ ТА ЫТЕСТИНАЛЬНОТ МкРОФЛОРИ В д1ТЕЙ i3 НЕАЛКОГОЛЬНОЮ ЖИРОВОЮ
ХВОРОБОЮ ПЕЧiНКИ
Резюме. Неалкогольна жирова хвороба печнки (НАЖХП) об’еднуе таю патолопчн стани, як стеатоз печнки, неалкогольний стеатогепатит, фiброз та цироз печнки, i вважаеться печнковим проявом метаболiчного синдрому. Не лише печнка стае органом-мшенню в разi формування метаболiчного синдрому: доведена мож-ливсть розвитку стеатозу жовчного м^хура, пщшлунково! залози та б^арного тракту. арна система, синдром надмiрного бактерiального росту, дти.
арна система, синдром надмiрного бактерiального росту, дти.
Адреса для листування з авторами:
Завгородня Н.Ю.
Вщдш дитячо! гастроентерологЦ,
ДУ «1нститут гастроентерологЦ НАМН Украши»,
Слобожанський проспект, 96, м. Днтро, 49074, Украша
E-mail: [email protected]
© Завгородня Н.Ю., Лук’яненко О.Ю., Коненко 1.С., 2016 © «Гастроентерологш», 2016 © Заславський О.Ю., 2016
Вступ
Неалкогольна жирова хвороба печшки (НАЖХП) вважаеться печiнковою манiфестацieю метаболiчного синдрому й тюно пов’язана з ожирiнням, шсулшоре-зистентнiстю та дислiпiдемieю. Не лише печшка стае органом-мiшенню в разi формування метaболiчно-го синдрому: доведена можливють розвитку стеато-зу жовчного мiхура (ЖМ), пщшлунково! залози (ПЗ) та бшарного тракту [1].
Не лише печшка стае органом-мiшенню в разi формування метaболiчно-го синдрому: доведена можливють розвитку стеато-зу жовчного мiхура (ЖМ), пщшлунково! залози (ПЗ) та бшарного тракту [1].
Yen H. Pham й спiвавт. [2] продемонстрували, що жирова iнфiльтрацiя ПЗ значною мiрою асоцiйована з НАЖХП й виявляеться в 19 % дггей iз надмiрною вагою. Накопичення жиру в тканиш ПЗ е додатко-вим фактором впливу на метаболiзм глюкози, що пiдвищуe ризик розвитку метаболiчного синдрому та обумовлюе тяжкiсть перебiгу НАЖХП [3]. У той же час мшроциркуляторш порушення внаслiдок мета-болiчних змiн обтяжують функцiональний стан ПЗ, погiршуючи ii зовнiшньо- та внутрiшньосекреторну функцiю, формуючи так зване патологiчне коло [4]. Бшарно-панкреатичний рефлюкс, що розвиваеться на rai дисфункци сфiнктера Одщ (СО), також сприяе прогресуванню патологiчних змш тдшлунково! залози [5].
Збшшення вмiсту лiпiдiв у стiнцi ЖМ в пащентав iз НАЖХП призводить до порушення його скорот-ливо! функцп [6]. мфоцити) у печiнкову, жирову, м’язову тканини та розвитку низькорiвневоi системно! запально! вiдповiдi, наслiдком яко! е про-гресування НАЖХП [8].
мфоцити) у печiнкову, жирову, м’язову тканини та розвитку низькорiвневоi системно! запально! вiдповiдi, наслiдком яко! е про-гресування НАЖХП [8].
Наявнють тiсних анатомiчних та функцiональних зв’языв мiж печiнкою та iншими органами травлення обумовлюе потребу в комплексному пiдходi до дiагно-стики та лшування панкреатичних, бiлiарних та ште-стинальних розладiв у дiтей iз неалкогольною жировою хворобою печшки.
Мета: вивчити структурно-функцюнальний стан панкреатобшарно! системи та змiни тонкокишково! мшрофлори в дiтей iз неалкогольною жировою хворобою печшки.
Матерiали та методи
Шд нашим спостереженням перебувало 34 дитини з патологieю шлунково-кишкового тракту. Визначен-ня наявностi й ступеня стеатозу печшки здшснено за допомогою апарата FibroScan-touch-502 iз досль
дженням контрольованого параметра ультразвукового загасання (САР). Ультразвукове дослiдження оргашв черевно! порожнини проводили за загальноприй-нятою методикою на апаратi Toshiba Xario (Японiя). Оцiнку функцiонального стану бшарного тракту проводили за допомогою ультразвукового дослщжен-ня з пробним сшданком для визначення скоротливо! функци ЖМ й тонусу СО [9].
Ультразвукове дослiдження оргашв черевно! порожнини проводили за загальноприй-нятою методикою на апаратi Toshiba Xario (Японiя). Оцiнку функцiонального стану бшарного тракту проводили за допомогою ультразвукового дослщжен-ня з пробним сшданком для визначення скоротливо! функци ЖМ й тонусу СО [9].
Для характеристики стану тонкокишково! мшро-бюти (наявностi синдрому надмiрного бактерiального росту — СНБР) проводили водневий дихальний тест iз навантаженням глюкозою або лактозою з викори-станням газоаналiзатора Gastro + Gastrolyzer компани Bedfont Scientific Ltd (Великобританiя).
Ушм обстеженим проведенi антропометричнi до-слщження з визначенням iндексу маси тта (1МТ), що запропонований мiжнародною групою з ожирiння [10]. Обчислювали 1МТ за формулою:
1МТ= Маса шша (кг) .
3picm (м2)
Оцшку стану трофши проводили за рекоменда-цiями ВООЗ згiдно з центильними таблицями зна-чень 1МТ вщповщно до вiку й статi [11]. При значенш 1МТ у межах 85—95 центилiв дiагностували надмiрну вагу. При перевищенш 1МТ 95 центиля дiагностували ожирiння. Проводили вимiрювання окружноста талГ!, стегна та зiставлення отриманих значень iз даними центильних таблиць [12]. За наявносп показань до-слiджуваним хворим проводилася фiброезофагога-стродуоденоскотя (ФЕГДС). У сироватцi кровi визна-чали вмiст загального бiлка, загального бiлiрубiну, лужно! фосфатази, гаммаглутамiлтранспептидази (ГГТП), аланшамшотрансферази (АЛТ), аспартата-мiнотрансферази (АСТ) за допомогою бiохiмiчного аналiзатора Stat Fax 1904 Plus, Awareness Technology (США). Статистичний аналiз одержаних даних проведений за допомогою пакета прикладних програм Statistica 6.0. Вщмшноста визнавалися значущими при р < 0,05.
При значенш 1МТ у межах 85—95 центилiв дiагностували надмiрну вагу. При перевищенш 1МТ 95 центиля дiагностували ожирiння. Проводили вимiрювання окружноста талГ!, стегна та зiставлення отриманих значень iз даними центильних таблиць [12]. За наявносп показань до-слiджуваним хворим проводилася фiброезофагога-стродуоденоскотя (ФЕГДС). У сироватцi кровi визна-чали вмiст загального бiлка, загального бiлiрубiну, лужно! фосфатази, гаммаглутамiлтранспептидази (ГГТП), аланшамшотрансферази (АЛТ), аспартата-мiнотрансферази (АСТ) за допомогою бiохiмiчного аналiзатора Stat Fax 1904 Plus, Awareness Technology (США). Статистичний аналiз одержаних даних проведений за допомогою пакета прикладних програм Statistica 6.0. Вщмшноста визнавалися значущими при р < 0,05.
Розподiл дiтей на групи вщбувався згiдно з даними транзieнтноi еластрограф!! печiнки (FibroScan): контрольну групу (S0) становив 21 пашент без стеатозу печiнки (61,8 %), основну групу (S+) — 13 пашенпв !з стеатозом печшки (38,2 %). а-лось у третини хворих основно! групи. Спленомегал!я не була виявлена в жодного обстеженого хворого.
а-лось у третини хворих основно! групи. Спленомегал!я не була виявлена в жодного обстеженого хворого.
При анал1з1 показниыв бiохiмiчно! гепатограми були виявлеш вiдмiнностi рiвнiв АЛТ та АСТ, але зна-чущiсть вiдмiнностей не досягла достатнього рiвня (табл. 2).
Рисунок 2 — Структура скаргхворих досл’1джува-них груп
Рисунок 3 — Пор1вняльна характеристика поед-наноI патологи орган1в травлення в дослджених хворих
Рисунок 4 — Характеристика даних копролопчно-го досл дження дослджуваних хворих
%
80 70 60 50 40 30 20 10 0
ш
■ Контрольна група I Основна група
^ л* \ О
%
50 45 40 35 30 25 20 15 10 5 0
■ Основна група
■ Контрольна група
Амгпорея
Стеаторея 1 типу
Стеаторея 2 типу
Креаторея
Таблиця 1 — Характеристика даних об’ективного огляду хворих
Болснсть при пальпацГУ Групи
S0, n = 21 S+, n = 13 Усього, n = 34
n % n % n %
в правому пщребер’! 8 38,1 5 38,5 13 38,2
в eniracTpii 16 76,2 10 76,9 26 76,5
за ходом кишечника 7 33,3 9 69,2* 16 47,1
Гепатомегатя 2 9,5 5 38,5* 7 20,6
Примтка. * — Значущсть в’щм’шностей м1ж показниками пор1вняно з Б0-групою при р < 0,05 за U-кри-тер1ем Манна — У/THi.
* — Значущсть в’щм’шностей м1ж показниками пор1вняно з Б0-групою при р < 0,05 за U-кри-тер1ем Манна — У/THi.
Як вщомо, ГГТП е маркером холестазу, ризику розвит-ку ф1брозу печшки, шдвищення р1вня ГГТП асоцшеться з дислшщем1ею та шсулшорезистентнютю [14]. Р1вень гаммаглутамттранспептидази в нашому дослщженш був в1рогщно вищим у пащентав з1 стеатозом печ1нки, але в1н не перевищував загальноприйнятих нормативних показ-ниюв. Установлено, що р1вень ГГТП корелював 1з показ-ником САР (г = 0,533, p < 0,05), АЛТ (г = 0,631, p < 0,05), АСТ (г = 0,609, p < 0,05). Ивень АЛТ також виявив коре-ляц1ю з показником САР (г = 0,470, p < 0,05).
Ознаки порушення засвоення крохмалю та нейтрального жиру за даними копрограми в1рог1дно часть ше спостер1гались у групах хворих 1з стеатозом печш-ки, що може свщчити про розвиток у них супутньо! екзокринно! недостатност1 ПЗ (рис. 4). Однак, врахо-вуючи поширешсть супутньо! патологи кишечника, не можна виключити, що розлади в копролопчному досл1дженн1 пов’язан1 з прискоренням кишечного транзиту, тому оптимальним для оцшки екзокринно! функци п1дшлунково! залози слщ вважати визначення р1вня фекально! еластази в даних хворих.
Стеаторея 2 типу в1ропдно частше зустр1чалась у хворих з1 стеатозом печ1нки, що може свщчити про порушення жовчовидтьно! функц1!.
При пор1вняльному анал1з1 сонограф1чних даних виявлено в1рог1дне зб1льшення обсягу ЖМ у грут хво-
рих зi стеатозом порiвняно з групою хворих без нього (рис. 5).
Були виявлеш змiни ехогенностi та зернистост ПЗ у хворих зi стеатозом печiнки. Розмiри головки й тша пiдшлунковоi залози були вiрогiдно вищими в основ-нiй груш (рис. 5) Слд зауважити, що ознаки бшарного сладжу мали 7 пащентав (20,58 %) без вiрогiдних вщ-мiнностей у частотi виявлення мiж групами (р > 0,05).
При ощнщ скоротливоi функцii жовчного мiхура з’ясовано, що в 52,9 % пащентав (18 осiб) спостериа-лась гiпокiнезiя жовчного мiхура, у 47,1 % (16) — нор-мокшез1я.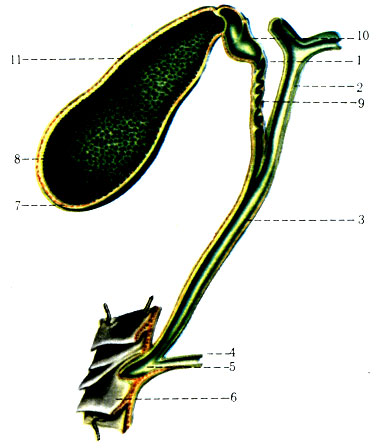 ча-лись ознаки катарально’1′ гастропатii з еритемою сли-зово’1′ антрального вщдлу без залежносп в!д наявностi стеатозу. Було виявлено, що в груш хворих зi стеатозом при оглядi дванадцятипало’1′ кишки спостериався симптом «манно’1′ крупи»: у найбтьш набряклих зонах
ча-лись ознаки катарально’1′ гастропатii з еритемою сли-зово’1′ антрального вщдлу без залежносп в!д наявностi стеатозу. Було виявлено, що в груш хворих зi стеатозом при оглядi дванадцятипало’1′ кишки спостериався симптом «манно’1′ крупи»: у найбтьш набряклих зонах
Таблиця 2 — Характеристика показниюв 6ioxiMi4-ноУ гепатограми в досл’1джуваних групах
Показник Групи
S0, n = 21 S+, n = 13
М ± m М ± m
Загальний 6Lnipy6iH, ммоль/л 10,58 ± 3,00 9,22 ± 3,10
Загальний бгпок, г/л 73,95 ± 3,83 74,77 ± 4,92
Лужна фосфатаза, Од/л 246,20 ± 81,71 214,48 ± 94,44
ГГТП, Од/л 15,09 ± 5,37 19,90 ± 6,75*
АЛТ, Од/л 17,07 ± 3,93 28,38 ± 9,82
АСТ, Од/л 14,99 ± 4,22 22,83 ± 11,72
Примтка.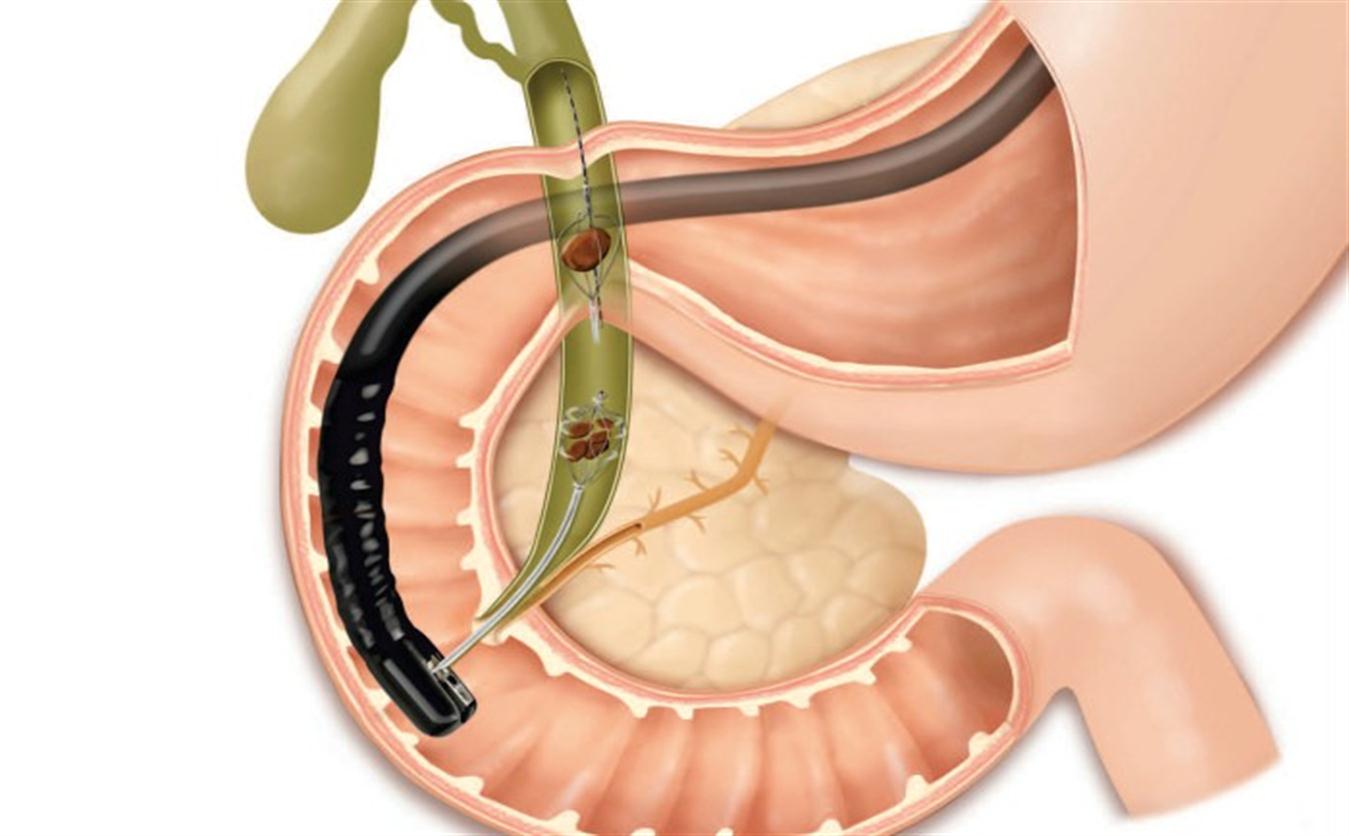 * — Значущсть вiдмiнностей м’жпоказниками при р < 0,05 за U-критерieм Манна — УУтн’1.
* — Значущсть вiдмiнностей м’жпоказниками при р < 0,05 за U-критерieм Манна — УУтн’1.
30 25 20 15 10 5 0
■ 3i стеатозом
■ Без стеатозу
Головка ПЗ, Тто ПЗ, Об’ем ЖМ, Товщина
см3
стшки ЖМ, мм
Рисунок 5 — Середн значення розм’р’в оргашв черевноУ порожнини в дослщжуваних хворих
%
60 50 40 30 20 10 0
Ппоюнез1я ЖМ
Нормокшез1я ЖМ
%
70 60 50 40 30 20 10 0
■ Основна група
■ Контрольна група
Нормотоыя СО Ппотоыя СО Ппертоыя СО
Рисунок 6 — Характеристика функцюнального станужовчного Mixypa та сф’шктера Одд! в дослджува-
ниххворих
виявлялися множинш бшяста зерна дiаметром до 1 мм, як! виступають над поверхнею (45,5 % хворих основно! групи проти 10,5 % — контрольно!, р < 0,05), що може бути ознакою ураження ПЗ. ератури
ератури
1. Ectopic Fat and Insulin Resistance: Pathophysiology and Effect of Diet and Lifestyle Intervention / M. Snel, J.T. Jonker, J. Schoones [et al.] // International Journal of Endocrinology. — 2012. — Vol. 2012. — P. 1-18. — doi:10.1155/2012/983814.
2. Prevalence of Pancreatic Steatosis at a Pediatric Tertiary Care Center / Pham Y.H., Bingham B.A., Bell C.S. [et al.] // South Med. J. — 2016. — № 109(3). — P. 196-198.
3. Pacifico L. Pancreatic fat and hepato-metabolic features in obese children with nonalcoholic fatty liver disease / L. Pacifico, C. Chiesa // Clin. Endocrinol. (Oxf). — 2015. — 1365-2265.
4. Самсонова Н.Г. Клинико-функциональное состояние поджелудочной железы при метаболическом синдроме / Н.Г. Самсонова, Л.А. Звенигородская // ЭиКГ.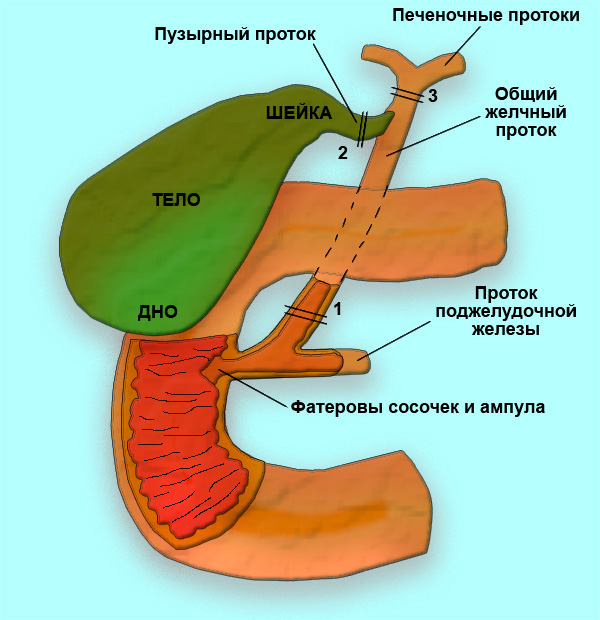 — 2012. — № 11. — С. 96-100.
— 2012. — № 11. — С. 96-100.
5. Стеатоз поджелудочной железы. Подходы к терапии / В.Б. Гриневич, Е.И. Сас, Ю.А. Кравчук, К.В. Матю-шенко //Гастроэнтерология. — 2012. — № 2—3. — С. 5.
6. The occurrence of gallbladder contractility disorders in children with some diseases presenting as abdominal pain / E. Czkwianianc, P. Raczynski, I. Kubinska[etal.]//Pol. Merkur. Lekarski. — 2009. — Vol. 26(155). — P. 420-424.
7. Small intestinal bacterial overgrowth and toll like receptor signaling in patients with nonalcoholic fatty liver disease / S. Kapil, A. Duseja, B.K. Sharma [et al.] // J. Gastroenterol. Hepatol. — 2015. — Vol. 31(1). — P. 213-221. — doi: 10.1111/jgh.13058.
8. Berg R.D. Bacterial translocation from the gastrointestinal tract / R.D. Berg // Trends Microbiol. — 1995. — № 3.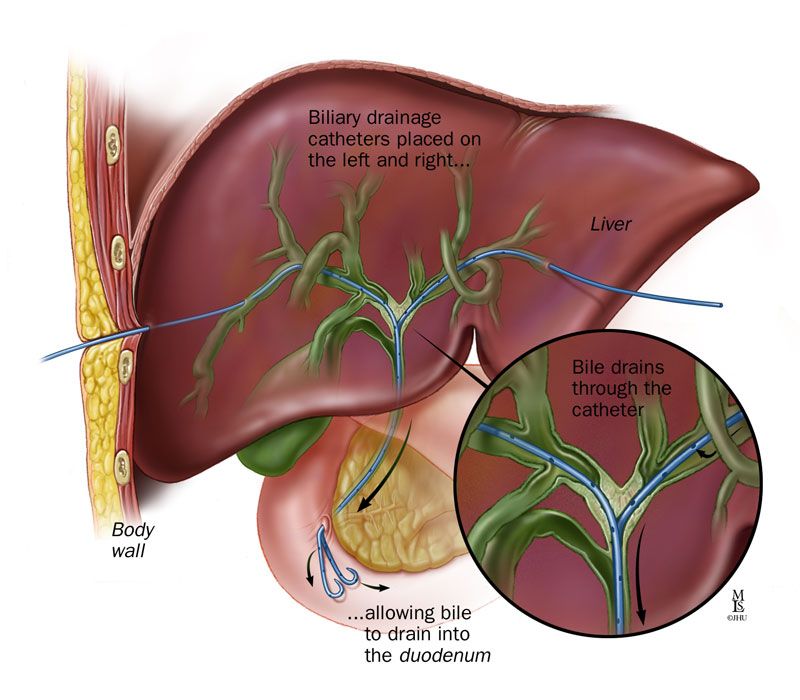 — P. 149-54.
— P. 149-54.
9. Increased intestinal permeability and tight junction alterations in nonalcoholic fatty liver disease / L. Miele, V. Valenza, G. La Torre [et al.]//Hepatology. — 2009. — Vol. 49, № 6. — P. 1877-1887.
10. Моторно-эвакуаторная функция желчного пузыря у детей с хроническими гепатитами и портальной ги-пертензией / Н.И. Гончаренко, Б.А. Тарасюк, Т.А. Гридина [и др.]//Перинатология и педиатрия. — 2011. — № 1(45). — С. 76-79.
11. Pediatric nonalcoholic fatty liver disease, metabolic syndrome and cardiovascular risk / L. Pacifico, V. Nobili, C. Anania [et al.] //World J. Gastroenterol. — 2011. — Vol. 17, № 26. — P. 3082-3091. — doi: 10.3748/wjg.v17.i26.3082.
12. Nonalcoholic fatty liver disease prevalence in urban school-aged children and adolescents from the Yangtze River delta region: a cross-sectional study / Xiaomin Zhang, Yanping
Wan, Shijun Zhang [et al. вання (II части-на)/ Степанов Ю.М., Абатуров O.G., Завгородня Н.Ю., Скирда 1.Ю. //Гастроентерологiя. — 2015. — № 3(57). — С. 122-131.
вання (II части-на)/ Степанов Ю.М., Абатуров O.G., Завгородня Н.Ю., Скирда 1.Ю. //Гастроентерологiя. — 2015. — № 3(57). — С. 122-131.
Отримано 19.09.16 ■
Завгородняя Н.Ю., Лукьяненко О.Ю., Коненко И.С.
ГУ «Институт гастроэнтерологии НАМН Украины», г. Днепр, Украина
СОСТОЯНИЕ ПАНКРЕАТОБИЛИАРНОЙ СИСТЕМЫ И ИНТЕСТИНАЛЬНОЙ МИКРОФЛОРЫ У ДЕТЕЙ С НЕАЛКОГОЛЬНОЙ ЖИРОВОЙ БОЛЕЗНЬЮ ПЕЧЕНИ
Резюме. Неалкогольная жировая болезнь печени (НАЖБП) объединяет такие патологические состояния, как стеатоз печени, неалкогольный стеатогепатит, фиброз и цирроз печени, и считается печеночным проявлением метаболического синдрома. Не только печень становится органом-мишенью в случае формирования метаболического синдрома: доказана возможность развития стеатоза желчного пузыря, поджелудочной железы и билиарного тракта. Жировая инфильтрация панкреатобилиарного тракта ассоциирована с нарушением процессов пищеварения, что сопровождается развитием дисбиотических изменений и интестинальных расстройств. Изменения кишечной микробиоты, в свою очередь, могут индуцировать системную воспалительную реакцию и способствовать развитию и прогрессированию НАЖБП. Цель: изучить структурно-функциональное состояние пан-креатобилиарной системы и изменения тонкокишечной микрофлоры у детей с неалкогольной жировой болезнью печени. Методы. У 34 детей с патологией желудочно-кишечного тракта определяли контролируемый параметр ультразвукового затухания с использованием аппарата FibroScаn. Оценку функционального состояния билиарного тракта осуществляли с помощью ультразвукового исследования органов брюшной полости с пробным завтраком для опре-
Жировая инфильтрация панкреатобилиарного тракта ассоциирована с нарушением процессов пищеварения, что сопровождается развитием дисбиотических изменений и интестинальных расстройств. Изменения кишечной микробиоты, в свою очередь, могут индуцировать системную воспалительную реакцию и способствовать развитию и прогрессированию НАЖБП. Цель: изучить структурно-функциональное состояние пан-креатобилиарной системы и изменения тонкокишечной микрофлоры у детей с неалкогольной жировой болезнью печени. Методы. У 34 детей с патологией желудочно-кишечного тракта определяли контролируемый параметр ультразвукового затухания с использованием аппарата FibroScаn. Оценку функционального состояния билиарного тракта осуществляли с помощью ультразвукового исследования органов брюшной полости с пробным завтраком для опре-
деления сократительной функции желчного пузыря и тонуса сфинктера Одди. Для характеристики состояния тонкокишечной микробиоты проводили водородный дыхательный тест с нагрузкой глюкозой или лактозой.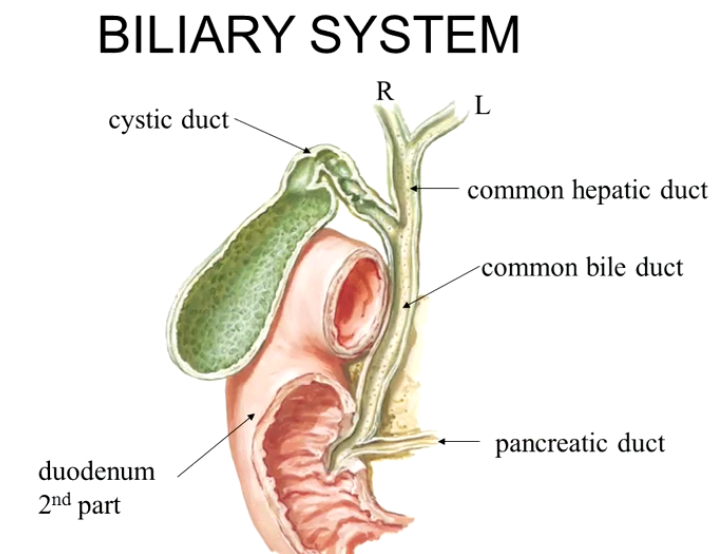 Распределение детей на группы происходило согласно данным транзиентной эластрографии печени (FibroScan): контрольную группу составил 21 пациент без стеатоза печени, основную группу — 13 пациентов со стеатозом печени. Результаты. Дети с неалкогольной жировой болезнью печени имеют признаки поражения не только печени, но и желчевыводящих путей и поджелудочной железы. Патология желчевыводящих путей у пациентов с НАЖБП чаще проявлялась в виде гипотонии сфинктера Одди и гипокинезии желчного пузыря. Нарушение функции поджелудочной железы у детей с НАЖБП может объясняться наличием функционального расстройства сфинктера Одди и проявлениями стеатоза поджелудочной железы. Изменения в состоянии микрофлоры тонкой кишки наблюдались у 27,6 % обследованных больных. Синдром избыточного бактериального роста достоверно чаще отмечался в группе больных со стеатозом печени.
Распределение детей на группы происходило согласно данным транзиентной эластрографии печени (FibroScan): контрольную группу составил 21 пациент без стеатоза печени, основную группу — 13 пациентов со стеатозом печени. Результаты. Дети с неалкогольной жировой болезнью печени имеют признаки поражения не только печени, но и желчевыводящих путей и поджелудочной железы. Патология желчевыводящих путей у пациентов с НАЖБП чаще проявлялась в виде гипотонии сфинктера Одди и гипокинезии желчного пузыря. Нарушение функции поджелудочной железы у детей с НАЖБП может объясняться наличием функционального расстройства сфинктера Одди и проявлениями стеатоза поджелудочной железы. Изменения в состоянии микрофлоры тонкой кишки наблюдались у 27,6 % обследованных больных. Синдром избыточного бактериального роста достоверно чаще отмечался в группе больных со стеатозом печени.
Ключевые слова: неалкогольная жировая болезнь печени, стеатоз печени, панкреатобилиарная система, синдром избыточного бактериального роста, дети.
Zavgorodnya N. Yu., Lukianenko O. Yu., Konenko I.S.
State Institution «Institute of Gastroenterology of the National Academy of Medical Sciences of Ukraine», Dnipro, Ukraine
THE STATE OF PANCREATOBILIARY SYSTEM AND INTESTINAL MICROFLORA IN CHILDREN WITH NONALCOHOLIC FATTY LIVER DISEASE
Summary. Nonalcoholic fatty liver disease (NAFLD) combines with a variety of liver pathologies, including hepatic steatosis, nonalcoholic steatohepatitis, fibrosis and cirrhosis, and acts as hepatic manifestation of metabolic syndrome. Not only the liver is a target organ in the formation of metabolic syndrome: also exist a possibility of gallbladder, pancreas and biliary tract steatosis. Fatty infiltration of the pancreatobiliary system associates with disturbance of digestive processes that promotes dysbiotic changes and intestinal disorders. Changes in intestinal microbiota, in turn, may induce systemic inflammatory response and promote NAFLD development and progression. Objective: to explore the structural and functional state of the pancreato-biliary system and changes of the enteric microflora in children with NAFLD. Methods. In 34 children with disorders of the gastrointestinal tract, we have determined controlled attenuation parameter by means of FibroScan. Assessment of functional status of biliary tract was performed using an ultrasound examination of the abdominal organs with test meal in order to determine gallbladder contractility and the sphincter of Oddi function. To characterize the state of the enteric microbiota, there was carried
Changes in intestinal microbiota, in turn, may induce systemic inflammatory response and promote NAFLD development and progression. Objective: to explore the structural and functional state of the pancreato-biliary system and changes of the enteric microflora in children with NAFLD. Methods. In 34 children with disorders of the gastrointestinal tract, we have determined controlled attenuation parameter by means of FibroScan. Assessment of functional status of biliary tract was performed using an ultrasound examination of the abdominal organs with test meal in order to determine gallbladder contractility and the sphincter of Oddi function. To characterize the state of the enteric microbiota, there was carried
out a hydrogen breath test with glucose or lactose loading. Children were divided into groups according to the the transient elas-tography of the liver (FibroScan): the control group was represented by 21 patients without liver steatosis, the main group — 13 patients with liver steatosis.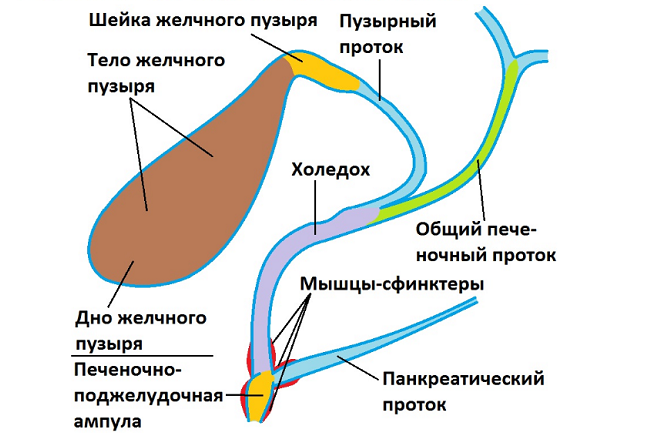 Results. Children with nonalcoholic fatty liver disease had signs of not only liver pathology, but also of the bile ducts and the pancreas. Biliary tract dysfunction in patients with NAFLD more often manifested as hypotension of the sphincter of Oddi and the gallbladder hypokinesia. Lesions of the pancreas function in children with NAFLD can be explained by the sphincter of Oddi disorders and manifestations of pancreatic steatosis. Intestinal pathology (irritable bowel syndrome and excessive bacterial growth) was significantly more common in the group of children with liver steatosis. Changes in the state of microflora of the small intestine were detected in 27.6 % of patients. The syndrome of excessive bacterial growth was observed significantly more in the group of patients with hepatic steatosis.
Results. Children with nonalcoholic fatty liver disease had signs of not only liver pathology, but also of the bile ducts and the pancreas. Biliary tract dysfunction in patients with NAFLD more often manifested as hypotension of the sphincter of Oddi and the gallbladder hypokinesia. Lesions of the pancreas function in children with NAFLD can be explained by the sphincter of Oddi disorders and manifestations of pancreatic steatosis. Intestinal pathology (irritable bowel syndrome and excessive bacterial growth) was significantly more common in the group of children with liver steatosis. Changes in the state of microflora of the small intestine were detected in 27.6 % of patients. The syndrome of excessive bacterial growth was observed significantly more in the group of patients with hepatic steatosis.
Key words: nonalcoholic fatty liver disease, hepatic steato-sis, pancreatobiliary system, syndrome of excessive bacterial growth, children.
Терапия при дисфункциях билиарного тракта :: ТРУДНЫЙ ПАЦИЕНТ
А.А.Ильченко
Центральный научно-исследовательский институт гастроэнтерологии, Москва.
В последнее десятилетие как в России, так и за рубежом, несмотря на определенные успехи терапии, связанные с появлением на фармацевтическом рынке новых эффективных лекарственных средств для коррекции функциональных расстройств органов пищеварения, не отмечается снижения числа функциональных заболеваний желчевыводящей системы. Распространенность функциональных нарушений билиарного тракта по разным оценкам колеблется от 12% до 58%. При этом среди женщин они встречаются в 2-3 раза чаще, чем среди мужчин.
Функциональные нарушения желчного пузыря и сфинктерного аппарата желчных путей характеризуются спонтанностью и разнообразием клинических проявлений, длительностью течения, сложностью диагностики, что в конечном итоге обуславливает высокую обращаемость больных за медицинской помощью. В то же время длительный и без результативный поиск соматического или неврологического заболевания, способствует формированию ипохондрии, депрессивных расстройств, усугубляют плохое самочувствие больного. Поздняя диагностика и не адекватная терапия могут значительно ухудшать качество жизни таких больных, формируют у пациентов устойчивое мнение о наличии тяжелой и неизлечимой болезни, вынуждают больных длительно соблюдать диету.
В то же время длительный и без результативный поиск соматического или неврологического заболевания, способствует формированию ипохондрии, депрессивных расстройств, усугубляют плохое самочувствие больного. Поздняя диагностика и не адекватная терапия могут значительно ухудшать качество жизни таких больных, формируют у пациентов устойчивое мнение о наличии тяжелой и неизлечимой болезни, вынуждают больных длительно соблюдать диету.
Длительно существующий болевой синдром, систематически приносящий страдания больному может стать причиной возникновения депрессивных расстройств. Присоединяющаяся к боли депрессия ухудшает переносимость боли, усиливает ее и является одним из факторов, способствующих ее хронизации. В настоящее время функциональные заболевания билиарного тракта принято рассматривать как проявление общего невроза. Однако это не исключает возможность их возникновения по типу висцеро-висцеральных рефлексов, обусловленных как патологией органов пищеварения, так и заболеваниями других органов и систем.
С клинической точки зрения функциональные нарушения билиарного тракта представляют особый интерес, так как способствуют формированию и прогрессированию целого ряда заболеваний органического характера. В первую очередь это касается патологии, связанной с присоединением воспалительного процесса в желчных путях и нарушением коллоидных свойств желчи, что в конечном итоге может потребовать применения оперативных методов лечения.
Дисфункции билиарного тракта являются одним из обязательных факторов, участвующих в формировании билиарного литогенеза, особенно на его начальных стадиях. В связи с этим ранняя диагностика и адекватная терапия функциональных нарушений желчного пузыря и сфинктерного аппарата желчных путей являются важной клинической задачей.
В настоящее время в соответствии с Римским консенсусом (Рим, 1999) функциональные заболевания пищеварительного тракта принято определять как комплексы постоянно или периодически возникающих клинических симптомов со стороны различных органов пищеварительной системы, необъяснимых структурными или биохимическими причинами.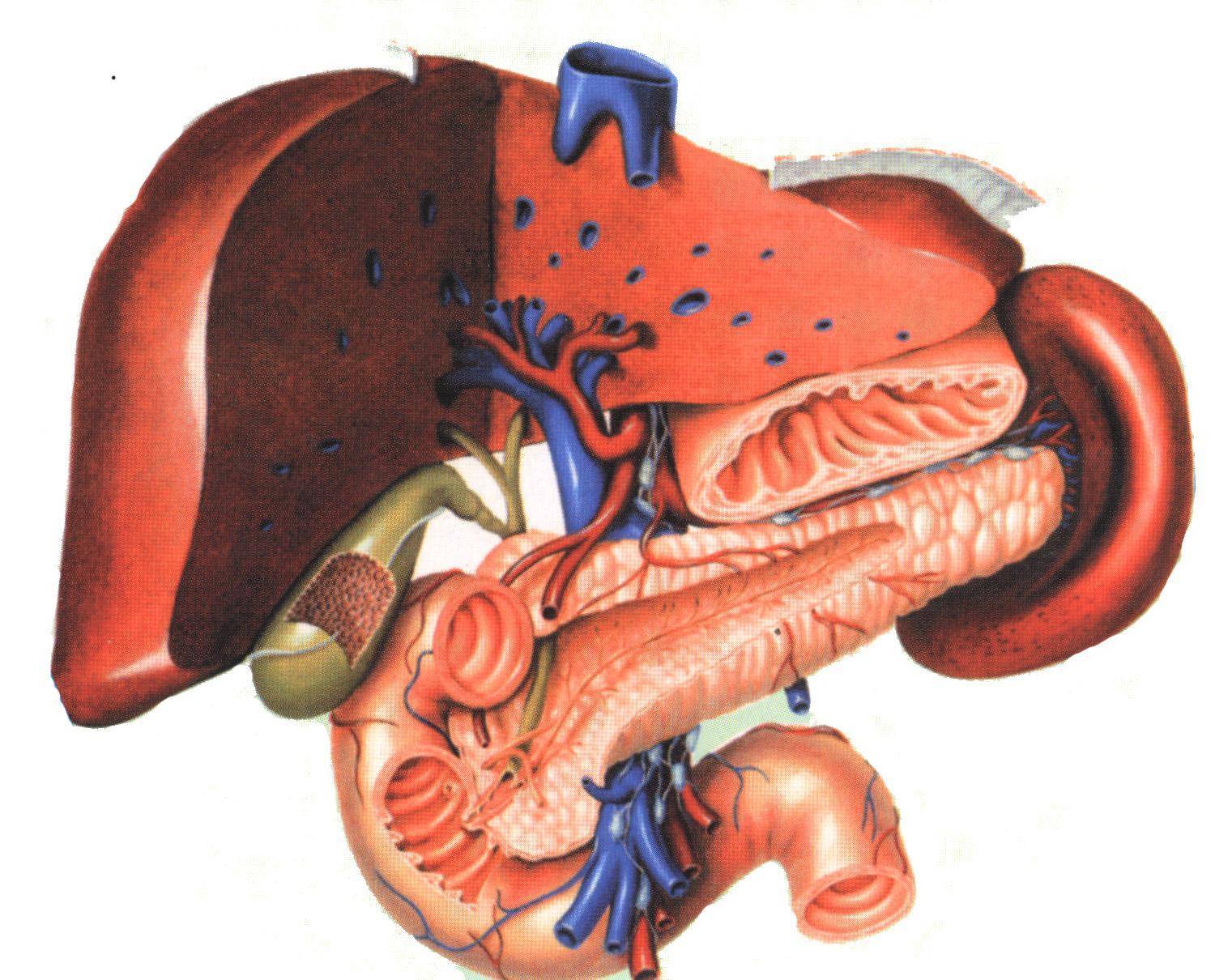
Применительно к билиарному тракту функциональные заболевания желчных путей можно обозначить как комплекс клинических симптомов, развившихся в результате моторно-тонических дисфункций желчного пузыря и сфинктерного аппарата желчных путей.
Независимо от этиологии дисфункций основной целью терапии при функциональных нарушениях билиарного тракта является восстановление нормальных потоков желчи во внепеченочных желчных путях и своевременного ее оттока в двенадцатиперстную кишку.
В большинстве случаев больные с дисфункцией билиарной системы могут лечиться амбулаторно. Однако при полиморфизме жалоб, конфликтных ситуациях в быту или на работе, трудностях проведения дифференциальной диагностики с другими заболеваниями билиарной системы, требующих применения сложных методов исследования, целесообразна госпитализация в терапевтический стационар сроком на 10-14 дней.
При наличии невротических расстройств показано применение седативных или тонизирующих средств, препаратов нормализующих сон.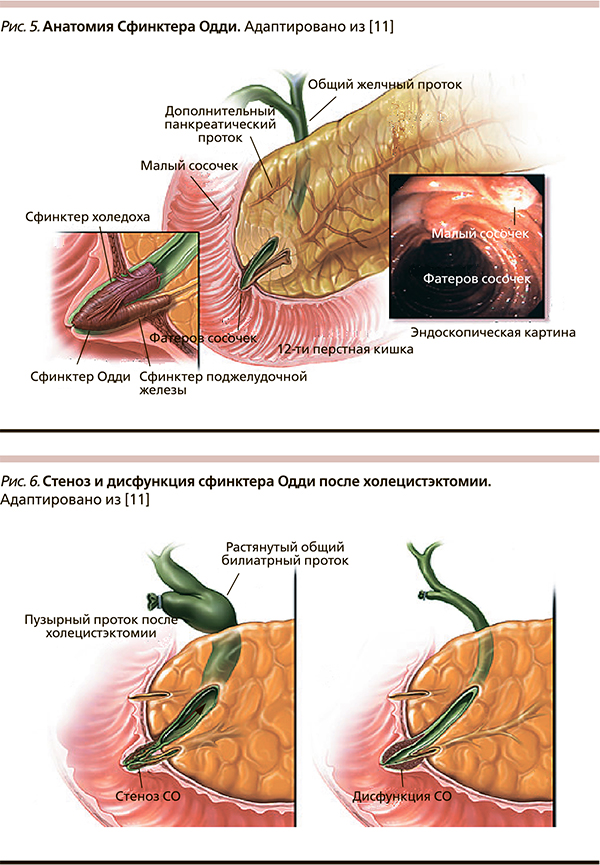 Важен контакт врача с пациентом с объяснением причин заболевания и возможных путей их устранения. При необходимости назначается консультация психотерапевта.
Важен контакт врача с пациентом с объяснением причин заболевания и возможных путей их устранения. При необходимости назначается консультация психотерапевта.
Диетотерапия занимает существенное место в лечении больных с функциональными заболеваниями билиарной системы, так как соблюдение правильного питания с учетом характера моторных нарушений способствует более быстрой реабилитации пациентов, улучшает качество жизни. Рекомендуется режим питания с частыми приемами небольших количеств пищи (5-6 разовое питание), что приводит к регулярному опорожнению желчного пузыря, нормализует давление в протоковой системе желчных путей и двенадцатиперстной кишке. Больным разрешается поздний прием пищи незадолго до сна.
Из рациона исключаются алкогольные напитки, газированная вода, копченые, жирные и жареные блюда, а также приправы, так как они могут вызывать спазм сфинктера Одди. В диетическом рационе необходимо учитывать влияние отдельных пищевых веществ на моторную функцию желчного пузыря и желчевыводящих путей.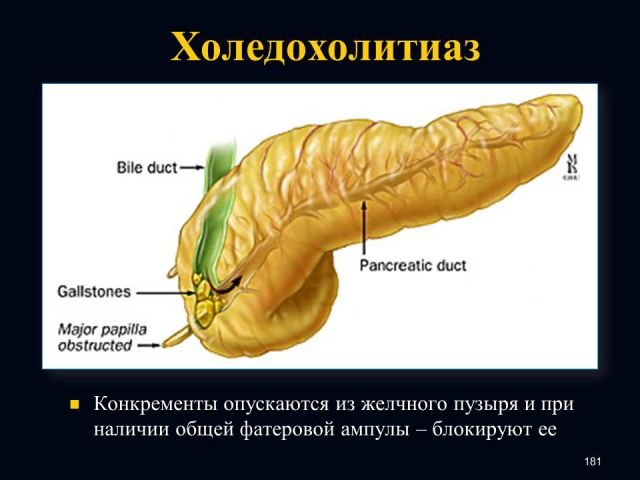 Так, при гиперкинетическом типе дисфункции должны быть резко ограничены продукты, стимулирующие сокращения желчного пузыря – животные жиры, растительные масла, наваристые мясные, рыбные, грибные бульоны. Показано применение продуктов, содержащих магний, который уменьшает тонус гладкой мускулатуры (гречневая крупа, пшено, пшеничные отруби, капуста). Исключается или ограничивается употребление яичных желтков, сдобы, кремов, орехов, крепкого кофе и чая.
Так, при гиперкинетическом типе дисфункции должны быть резко ограничены продукты, стимулирующие сокращения желчного пузыря – животные жиры, растительные масла, наваристые мясные, рыбные, грибные бульоны. Показано применение продуктов, содержащих магний, который уменьшает тонус гладкой мускулатуры (гречневая крупа, пшено, пшеничные отруби, капуста). Исключается или ограничивается употребление яичных желтков, сдобы, кремов, орехов, крепкого кофе и чая.
При гипокинетическом типе дисфункции желчного пузыря больные обычно хорошо переносят некрепкие мясные бульоны, уху, сливки, сметану, растительные масла, яйца всмятку. Растительное масло назначают по одной чайной ложке 2-3 раза в день за полчаса до еды в течение 2-3 недель. Для предотвращения запоров рекомендуют употребление продуктов, способствующих опорожнению кишечника (морковь, свекла, тыква, кабачки, зелень, арбузы, дыни, чернослив, курага, апельсины, груши, мед). Выраженный эффект на моторику желчных путей оказывают отруби.
Билиарная дисфункция может сопровождаться психоэмоциональными нарушениями, признаками эндогенной депрессии.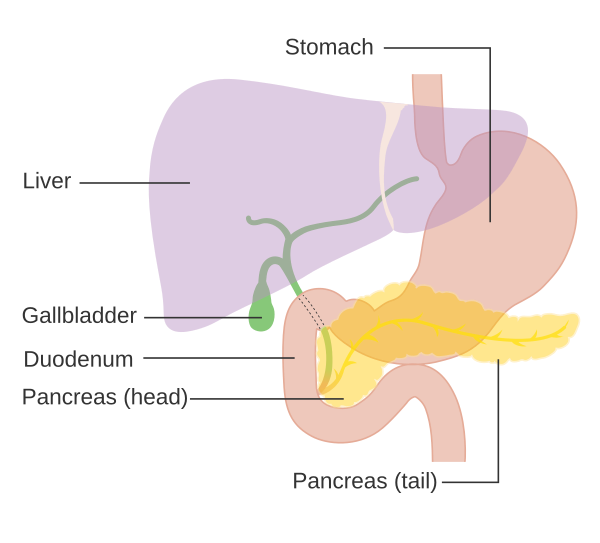 В зависимости от психоэмоциональных, нейровегетативных расстройств дифференцированно применяют средства, нормализующие психосоматический статус: адаптогены, седативные средства, транквилизаторы, антидепрессанты, нейролептики, ганглиблокаторы, физиотерапию, лечебную физкультуру и др. В последние годы антидепрессанты все чаще применяют для коррекции висцеральной гипералгезии при функциональных гастроинтестинальных расстройствах и нарушениях моторно-эвакуаторной функции желчного пузыря [6,7]. Среди нейролептиков заслуживает внимания сульпирид. Препарат, благодаря блокаде допаминовых D2-рецепторов, оказывает противорвотное и нормализующее влияние на моторику желудочно-кишечного тракта. С осторожностью назначают лицам пожилого возраста, так как эта категория пациентов часто имеет повышенную чувствительность к сульпириду.
В зависимости от психоэмоциональных, нейровегетативных расстройств дифференцированно применяют средства, нормализующие психосоматический статус: адаптогены, седативные средства, транквилизаторы, антидепрессанты, нейролептики, ганглиблокаторы, физиотерапию, лечебную физкультуру и др. В последние годы антидепрессанты все чаще применяют для коррекции висцеральной гипералгезии при функциональных гастроинтестинальных расстройствах и нарушениях моторно-эвакуаторной функции желчного пузыря [6,7]. Среди нейролептиков заслуживает внимания сульпирид. Препарат, благодаря блокаде допаминовых D2-рецепторов, оказывает противорвотное и нормализующее влияние на моторику желудочно-кишечного тракта. С осторожностью назначают лицам пожилого возраста, так как эта категория пациентов часто имеет повышенную чувствительность к сульпириду.
Клинические проявления при дисфункциях билиарного тракта обусловлены как нарушениями гуморальной, так и нервной регуляции в симпатических и парасимпатических отделах вегетативной нервной системы. Для коррекции вегетативной регуляции применяют различные вегетотропные препараты. В практическом плане на первое место вышло назначение -блокаторов (пропранолол и др.), оказывающих смешанное (периферическое и в меньшей степени центральное) действие, препаратов центрального и периферического -адреноблокирующего действия (пирроксан), а также комбинированных средств с холинолитическим и -адреноблокирующим действием (беллоид, беллатаминал, белласпон). Ганглиоблокаторы (ганглерон и др.) могут использоваться при вторичных билиарных дисфункциях у больных с хроническим холециститом с формирующимся правосторонним реактивным вегетативным синдромом за счет хронической ирритации симпатических структур вегетативной нервной системы, а также при появлении различных висцеро-висцеральных патологических рефлексов, в частности, при холецисто-кардиальном синдроме и рефлекторной стенокардии [3] .
Для коррекции вегетативной регуляции применяют различные вегетотропные препараты. В практическом плане на первое место вышло назначение -блокаторов (пропранолол и др.), оказывающих смешанное (периферическое и в меньшей степени центральное) действие, препаратов центрального и периферического -адреноблокирующего действия (пирроксан), а также комбинированных средств с холинолитическим и -адреноблокирующим действием (беллоид, беллатаминал, белласпон). Ганглиоблокаторы (ганглерон и др.) могут использоваться при вторичных билиарных дисфункциях у больных с хроническим холециститом с формирующимся правосторонним реактивным вегетативным синдромом за счет хронической ирритации симпатических структур вегетативной нервной системы, а также при появлении различных висцеро-висцеральных патологических рефлексов, в частности, при холецисто-кардиальном синдроме и рефлекторной стенокардии [3] .
При вегетативных расстройствах, сопровождающихся признаками повышенной нервно-мышечной возбудимости показано назначение минеральных корректоров (препаратов, содержащих кальций, магний, витамин D2).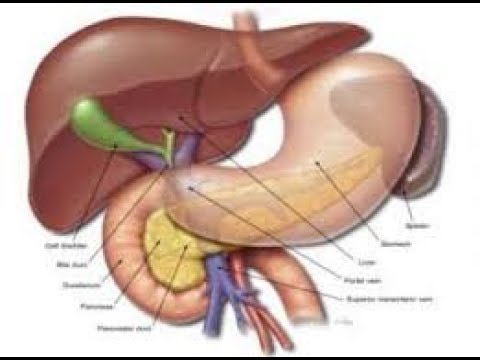 Эффективны иглорефлексотерапия, лазеротерапия, водолечение, сеансы гипноза, специальные комплексы лечебной физкультуры и дыхательной гимнастики.
Эффективны иглорефлексотерапия, лазеротерапия, водолечение, сеансы гипноза, специальные комплексы лечебной физкультуры и дыхательной гимнастики.
При дисфункции, обусловленной повышением тонуса сфинктеров билиарной системы, применяют спазмолитические средства. В качестве спазмолитиков используют как неселективные (метацин, платифиллин, баралгин и др), так и селективные М1-холиноблокаторы (гастроцепин). Однако следует учитывать, что при приеме данной группы препаратов могут наблюдаться целый ряд побочных эффектов: сухость во рту, задержка мочеиспускания, нарушение зрения, тахикардия, запоры, сонливость. Сочетание сравнительно низкой терапевтической эффективности препаратов этой группы с широким спектром побочных действий ограничивают их применение, особенно при терапии дисфункции сфинктера Одди. Из миотропных спазмолитиков применяют дротаверин, бенциклан, мебеверин, отилония цитрат, тримебутин или гимекромон, оказывающий селективное спазмолитическое действие на сфинктер Одди. Последний назначают за полчаса до еды по 200-400 мг (1-2 табл. ) 3 раза в день. Курс лечения 1-3 недели. В связи с холеретическим эффектом препарата при его продолжительном применении возможно развитие диареи.
) 3 раза в день. Курс лечения 1-3 недели. В связи с холеретическим эффектом препарата при его продолжительном применении возможно развитие диареи.
Препараты вышеуказанных групп оказывают в основном спазмолитический эффект и не влияют на характер патологических изменений в печени.
В связи с этим заслуживает внимания Гепабене – комбинированный препарат растительного происхождения, состоящий из экстракта дымянки аптечной и экстракта плодов расторопши пятнистой. Гепабене принимают после еды по 1 капсуле 3 раза в день. Доза может быть увеличена до 6 капсул в день (по 2 капсулы 3 раза в день). При ночных болях можно принимать также 1 капсулу перед сном.
Препарат показан как при первичной дисфункции сфинктерного аппарата и желчного пузыря, так и при функциональных расстройствах, сопровождающих патологию печени – жировой дистрофии печени, хронических гепатитах и циррозе печени. Препарат показан при дисфункции сфинктера Одди, развившейся после холецистэктомии и сопровождающейся билиарной недостаточностью I-II степени тяжести.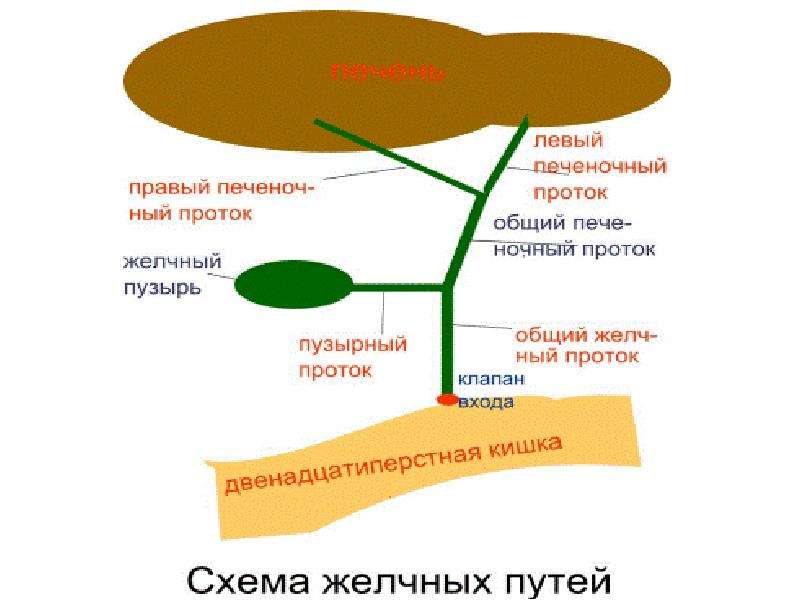
Последние исследования показали, что Гепабене можно с успехом применять у лиц с хроническим холециститом и различными формами билиарного сладжа, формированию которого способствуют функциональные нарушения желчного пузыря и сфинктерного аппарата желчных путей [1, 2, 5] .
При дисфункции желчного пузыря, обусловленной гипомоторной дискинезией для повышения сократительной функции, применяют прокинетики в течение 10-14 дней: домперидон 5-10 мг в день 3 раза в день за 30 минут до еды или метоклопрамид 5-10 мг в сутки. В качестве холецистокинетических средств применяют раствор сульфата магния 10-25% по 1-2 столовых ложки 3 раза в день или раствор сорбита 10% по 50-100 мл 2-3 раза в день за 30 минут до еды или через 1 час после еды.
Положительный эффект оказывают средства, уменьшающие дуоденальную гипертензию и нормализующие процессы пищеварения в тонкой кишке. При наличии микробной контаминации показано назначение доксициклина по 0,1 г 2 раза, тетрациклина по 0,25 г 4 раза, фурозолидона по 0,1 г 3 раза, нифуроксазида по 0,2 г 4 раза, интетрикса по 1 капс. 4 раза в течение 1-2 недель. После антибиотикотерапии необходим двухнедельный курс пробиотиков (бифиформ и др.) и пребиотиков – Хилак-форте по 40-60 капель 3 раза в сутки до или во время еды (после улучшения состояния суточную дозу можно уменьшить в 2 раза).
4 раза в течение 1-2 недель. После антибиотикотерапии необходим двухнедельный курс пробиотиков (бифиформ и др.) и пребиотиков – Хилак-форте по 40-60 капель 3 раза в сутки до или во время еды (после улучшения состояния суточную дозу можно уменьшить в 2 раза).
Эффективно дополняют медикаментозную терапию физиотерапевтические процедуры, которые назначают в период стихания обострения. Показаны тепловые процедуры (парафин, озокерит), а также УВЧ, ДМВ-терапия, ультразвук. Используются различные методы рефлексотерапии (игло- и лазеротерапия). При лечении вегетативных нарушений, лежащих в основе патологических нарушений в желчевыводящей системе, сопровождающихся повышенной эмоциональной возбудимостью и лабильностью, раздражительностью, появлением тревоги, страха, истощением нервной системы, эффективность применения акупунктуры и лазеропунктуры практически одинаковы. Для больных с повышенной раздражительностью и эмоциональной неустойчивостью лазеропунктура более приемлема, ввиду безболезненности процедур [4].
Основные критерии оценки эффективности лечебных мероприятий при функциональных нарушениях билиарного тракта:
Купирование клинических симптомов;
Восстановление моторной функции желчного пузыря;
Восстановление тонуса сфинктерного аппарата желчных путей;
Восстановление давления в двенадцатиперстной кишке.
Таким образом, применение современных методов диагностики дисфункции билиарного тракта с учетом клинических особенностей течения заболевания позволяет в настоящее время у большинства больных своевременно и точно диагностировать эту патологию.
Лекарственные препараты с различным, а иногда и с сочетанным механизмом действия, дают возможность подобрать более адекватную терапию, позволяющую значительно улучшить самочувствие и качество жизни пациентов с функциональными нарушениями билиарного тракта.Литература:
1. Ильченко А.А., Орлова Ю.Н. Применение гепабене у больных хроническим холециститом. Материалы 3-го Российского научного форума «Санкт-Петербург – Гастро-2001». Гастробюллетень № 2-3. 2001. С. 39.
Материалы 3-го Российского научного форума «Санкт-Петербург – Гастро-2001». Гастробюллетень № 2-3. 2001. С. 39.
2. Вихрова Т.В. Билиарный сладж и его клиническое значение. Дисс. канд. мед. наук. М.: 2003. 115 с.
3. Немцов Л.М. Дисмоторика желчного пузыря при билиарной патологии (клинико-патофизиологическая характеристика и коррекция). Витебск: ВГМУ, 2004. 183 с.
4. Маев И.В., Самсонов А.А., Салова Л.М. и др. Диагностика и лечение заболеваний желчевыводящих путей. Учебное пособие. М.: ГОУ ВУНМЦ МЗ РФ, 2003. 96 с.
5. Ильченко А.А. Желчнокаменная болезнь. М.: «Анахарсис», 2004. 200 с.
6. Mertz H., Fass R., Kodner A., et al. Effect of amitriptyllini on symptoms, sleep, and visceral perception in patients with functional dyspepsia. Am. J. Gastroenterol.. -1998. -Vol.93. -p.237-243.
7. Fioramonti J., Bueno L. Centrally acting agents and visceral sensitivity. Gut. – 2002. -Vol.51(Suppl 1). p. 91-95.
Биллярное дерево | MUSC Health
В желудке пища сначала расщепляется с целью переваривания, после чего она попадает в первую часть тонкой кишки, обычно называемую двенадцатиперстной кишкой. В двенадцатиперстную кишку добавляются пищеварительные соки (секреции), которые в дальнейшем превращают пищу в полезную для организма энергию. Эти выделения поступают через желчное дерево.
В двенадцатиперстную кишку добавляются пищеварительные соки (секреции), которые в дальнейшем превращают пищу в полезную для организма энергию. Эти выделения поступают через желчное дерево.
Желчное дерево – это система сосудов, которые направляют эти выделения из печени, желчного пузыря и поджелудочной железы через ряд каналов в двенадцатиперстную кишку.Выходное отверстие в двенадцатиперстной кишке называется сосочком Фатера. (Из-за структуры соединений с каждым органом желчное дерево или тракт имеет некоторое сходство с деревом и его ветвями, отсюда и название.)
Расщепление жиров – также известных как липиды, жиры – это очень концентрированные формы энергии, необходимые для правильного роста и поддержания организма – важная часть процесса пищеварения. Однако липиды, которые все еще присутствуют в пище, перешедшей из желудка в двенадцатиперстную кишку, довольно трудно растворить.
Печень
Печень, второй по величине орган в организме, вырабатывает желчь, которая помогает растворять липиды.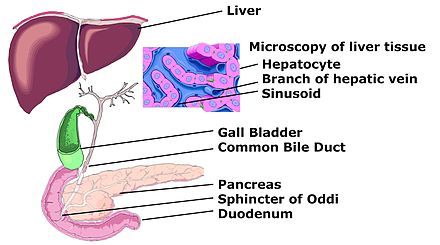 Желчь представляет собой желтую горькую жидкость – в основном вода, но также содержащую соли желчных кислот – которая растворяет жиры, так что ее энергия может быть поглощена организмом. Желчь также снижает кислотность содержимого желудка, когда оно попадает в двенадцатиперстную кишку.
Желчь представляет собой желтую горькую жидкость – в основном вода, но также содержащую соли желчных кислот – которая растворяет жиры, так что ее энергия может быть поглощена организмом. Желчь также снижает кислотность содержимого желудка, когда оно попадает в двенадцатиперстную кишку.
Желчный пузырь
Рентгеновское изображение желчного дерева во время ERCP.Желчный пузырь – это небольшой орган, прикрепленный к печени, который накапливает желчь для использования в случае необходимости.К сожалению, в желчи есть форма холестерина, которая может создавать аномальные камнеобразные образования, называемые желчными камнями. Затем желчные камни могут попасть в искривление пузырного протока, канала, который соединяет желчный пузырь с желчным деревом. Это препятствие может доставлять пациентам сильный дискомфорт.
Поджелудочная железа
Поджелудочная железа, орган, расположенный рядом с желудком и имеющий примерно такой же размер и форму, как небольшой банан, использует проток поджелудочной железы для подачи сока поджелудочной железы, который также способствует пищеварению. Эти соки или выделения называются экзокринными соками. Желчные протоки также могут быть заблокированы желчными камнями до такой степени, что поджелудочная железа не может поставлять экзокринные соки в двенадцатиперстную кишку. Это может привести к очень опасному состоянию под названием панкреатит.
Эти соки или выделения называются экзокринными соками. Желчные протоки также могут быть заблокированы желчными камнями до такой степени, что поджелудочная железа не может поставлять экзокринные соки в двенадцатиперстную кишку. Это может привести к очень опасному состоянию под названием панкреатит.
Визуализационная диагностика заболеваний поджелудочной железы: контрольное исследование
Abstract
ЦЕЛЬ: Оценить клиническую ценность различных имиджелогических методов в диагностике заболеваний поджелудочной железы и желчевыводящих путей и найти оптимальную процедуру.
МЕТОДЫ: Проанализировано 82 случая заболеваний поджелудочной железы и желчевыводящих путей, подтвержденных хирургическим путем и патологией. Было 38 случаев холелитиаза, 34 случая панкреатобилиарных опухолей и 10 других случаев. Имиджелогические методы включали B-US, CT, ERCP, PTC, поперечную МРТ и МР-холангиопанкреатографию (MRCP).
РЕЗУЛЬТАТЫ: Степень точности MRCP в определении местоположения панкреатобилиарной обструкции составила 100%. При дифференцировании злокачественной обструкции от доброкачественной чувствительность комбинации MRCP и поперечной МРТ составила 82.3%, специфичность – 93,8%, точность – 89,0%. Уровень точности определения характера обструкции составил 87,8%, что было выше, чем у B-US ( P = 0,0000) и CT ( P = 0,0330), но не было существенной разницы между прямой холангиопанкреатографией и комбинация MRCP и традиционной МРТ ( P = 0,6666).
При дифференцировании злокачественной обструкции от доброкачественной чувствительность комбинации MRCP и поперечной МРТ составила 82.3%, специфичность – 93,8%, точность – 89,0%. Уровень точности определения характера обструкции составил 87,8%, что было выше, чем у B-US ( P = 0,0000) и CT ( P = 0,0330), но не было существенной разницы между прямой холангиопанкреатографией и комбинация MRCP и традиционной МРТ ( P = 0,6666).
ВЫВОД: В большинстве случаев MRCP может заменить прямую холангиопанкреатографию для диагностики. Комбинация MRCP и поперечной МРТ должна рассматриваться как важное средство диагностики заболеваний поджелудочной железы и желчевыводящих путей, предоперационной оценки и послеоперационного наблюдения.
ВВЕДЕНИЕ
Панкреатобилиарные расстройства – распространенные заболевания, при которых часто поражается желчная система, вызывая симптомы механической желтухи. Это предварительное условие для исследования места обструкции и причин заболеваний поджелудочной железы и желчевыводящих путей. В данном исследовании проанализировано 82 случая заболеваний поджелудочной железы, подтвержденных хирургическим вмешательством и патологией. Цели проспективного исследования заключались в оценке клинической ценности различных имиджелогических методов в диагностике заболеваний поджелудочной железы и желчевыводящих путей и в поиске оптимальной процедуры обследования.
В данном исследовании проанализировано 82 случая заболеваний поджелудочной железы, подтвержденных хирургическим вмешательством и патологией. Цели проспективного исследования заключались в оценке клинической ценности различных имиджелогических методов в диагностике заболеваний поджелудочной железы и желчевыводящих путей и в поиске оптимальной процедуры обследования.
МАТЕРИАЛЫ И МЕТОДЫ
Пациенты
Объектами исследования были 82 пациента (54 мужчины и 28 женщин, средний возраст 60,0 года, диапазон 11-82 года), 67 (81,7%) пациентов имели симптом механической желтухи. Все пациенты прошли B-US, MR холангиопанкреатографию (MRCP) и поперечное МРТ. Пятьдесят семь пациентов прошли КТ с усилением или без него. Кроме того, 48 пациентам была проведена прямая холангиопанкреатография (41 ERCP и 7 PTC). Однако прямая холангиопанкреатография была безуспешной в 4 случаях из-за трудностей с канюляцией (2 ERCP), постгастроэнтеростомии (1 ERCP) и больного пациента (1 PTC).ЭРХПГ была неполной в других 4 случаях, потому что можно было увидеть только проток поджелудочной железы, а желчное дерево не было помутнено. Таким образом, во всех 82 случаях было выполнено 40 прямых холангиопанкреатографий (34 ERCP и 6 PTC), у 1 пациента было осложнение острого панкреатита после ERCP. Все пациенты с заболеваниями поджелудочной железы и желчевыводящих путей были подтверждены хирургическими данными и патологией, в том числе 12 – лапароскопической холецистэктомией (LC), 6 – эндоскопической тенотомией сфинктера (EST) и 1 – дренажом PTC (PTCD).Из 82 случаев у 38 был диагностирован холелитиаз, у 34 – панкреатобилиарные опухоли и у 10 – другие заболевания (таблица).
Таким образом, во всех 82 случаях было выполнено 40 прямых холангиопанкреатографий (34 ERCP и 6 PTC), у 1 пациента было осложнение острого панкреатита после ERCP. Все пациенты с заболеваниями поджелудочной железы и желчевыводящих путей были подтверждены хирургическими данными и патологией, в том числе 12 – лапароскопической холецистэктомией (LC), 6 – эндоскопической тенотомией сфинктера (EST) и 1 – дренажом PTC (PTCD).Из 82 случаев у 38 был диагностирован холелитиаз, у 34 – панкреатобилиарные опухоли и у 10 – другие заболевания (таблица).
Таблица 1
Заболевания поджелудочной железы ( n = 82)
| Заболевания поджелудочно-желчных путей | Число случаев |
| Холелитиаз a | 38 |
| Камень желчного пузыря | 14 |
| Камень внутрипеченочного желчного протока | 7 |
| Холедохолитиаз | 17 |
| Панкреатобилиарная опухоль b | 34 |
| Желчный рак | |
| Холангиокарцинома | 9 |
| Ампуллярная карцинома | 3 |
| Карцинома головки поджелудочной железы | 11 |
| Карцинома желчного сосочка | 5 |
| 2 | |
| Киста холедоха | 2 |
| Склерозирующий холангит | 2 |
| Хронический панкреатит | 4 |
Методы
МРТ-визуализация выполнялась с 1.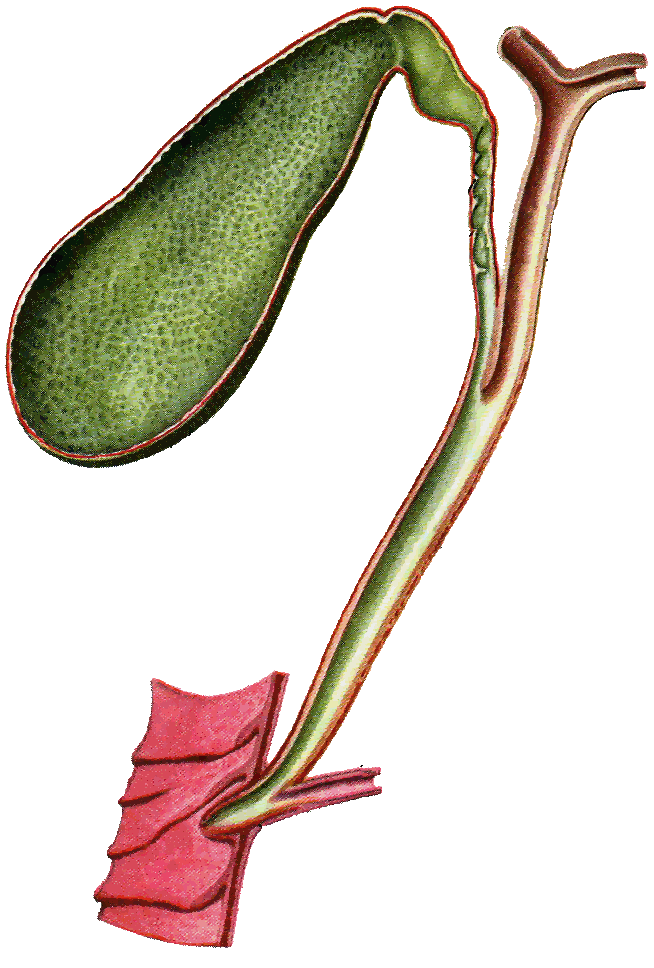 0T сверхпроводящий блок (Philips Gyroscan T10-NT, версия программного обеспечения 4.6.2), содержащий катушку для тела. Пациенты были обследованы в положении лежа на спине, спокойном дыхании и компрессии бандажом. Сначала были выполнены стандартные аксиальные исследования T1WI, T2WI и коронарного T2WI в верхней части живота с использованием последовательности Turbo Spin-Echo (TSE), а за ними последовали дополнительные аксиальные T2WI и / или T1WI последовательности с подавлением жира (восстановление с инверсией спектрального насыщения, SPIR). Стандартные аксиальные изображения служили ориентирами для определения местоположения МР-холангиопанкреатографии (MRCP).MRCP выполняли с коронарной, мультиспиральной, сильно взвешенной T2-последовательностью TSE (TR = 2000 мс, TE = 700 мс). Для уменьшения артефакта дыхательного движения использовалась техника без задержки дыхания. Исходные изображения MRCP были трехмерно (3D) реконструированы с использованием алгоритма проекции максимальной интенсивности (MIP).
0T сверхпроводящий блок (Philips Gyroscan T10-NT, версия программного обеспечения 4.6.2), содержащий катушку для тела. Пациенты были обследованы в положении лежа на спине, спокойном дыхании и компрессии бандажом. Сначала были выполнены стандартные аксиальные исследования T1WI, T2WI и коронарного T2WI в верхней части живота с использованием последовательности Turbo Spin-Echo (TSE), а за ними последовали дополнительные аксиальные T2WI и / или T1WI последовательности с подавлением жира (восстановление с инверсией спектрального насыщения, SPIR). Стандартные аксиальные изображения служили ориентирами для определения местоположения МР-холангиопанкреатографии (MRCP).MRCP выполняли с коронарной, мультиспиральной, сильно взвешенной T2-последовательностью TSE (TR = 2000 мс, TE = 700 мс). Для уменьшения артефакта дыхательного движения использовалась техника без задержки дыхания. Исходные изображения MRCP были трехмерно (3D) реконструированы с использованием алгоритма проекции максимальной интенсивности (MIP). Общее время визуализации составляло примерно 30 мин.
Общее время визуализации составляло примерно 30 мин.
Для компьютерной томографии (КТ) использовался компьютерный томограф всего тела (Picker PQ-2000). Все КТ-исследования проводились после того, как пациенты голодали в течение 4-8 часов и принимали пероральный контраст 500-1000 мл (0.5% -1% меглумина диатризоат) перед компьютерной томографией. При усиленном КТ-исследовании использовалось 80–100 мл неионных внутривенных контрастных веществ, вводимых через анекубитальную вену болюсно со скоростью 2–3 мл / с.
Прямая холангиопанкреатография (ERCP и PTC) выполнялась с помощью цифрового устройства визуализации (Philips Diagnost 93).
Анализ изображений
Все данные изображений 82 пациентов были тщательно изучены, чтобы выявить увеличение или стриктуру панкреатобилиарного тракта. Протокол исследования включал обнаружение обструктивных участков, различение злокачественных и доброкачественных причин и оценку клинической ценности различных методов визуализации (включая B-US, CT, MRCP, ERCP / PTC) при диагностике заболеваний поджелудочной железы и желчевыводящих путей. Программное обеспечение SAS использовалось для всех статистических анализов.
Программное обеспечение SAS использовалось для всех статистических анализов.
Диагностические принципы и критерии оценки для прямой холангиопанкреатографии и MRCP были идентичны, но в MRCP было более важно тщательно изучить как исходные изображения, так и изображения, реконструированные MIP. По результатам расширения или стриктуры панкреатобилиарного дерева и желчного пузыря обструктивные места панкреатобилиарного протока были разделены на три части: внутрипеченочный или внепеченочный желчный проток и главный панкреатический проток.Нормальный желчный пузырь 7-10 см в длину и 3-4 см в ширину. Расширение общего желчного протока определялось как более 8 мм в максимальном диаметре у пациентов без холецистэктомии в анамнезе и 10 мм у пациентов, перенесших холецистэктомию в анамнезе. Расширение внутрипеченочного желчного протока и главного протока поджелудочной железы было определено как более 3 мм в максимальном диаметре [1-4].
Причина панкреатобилиарной аномалии оценивалась с использованием пятибалльной шкалы для определения уровня достоверности: 1. определенно доброкачественная, 2. вероятно доброкачественная, 3. неопределенная, 4. вероятно злокачественная и 5. определенно злокачественная [5]. Если предполагалось, что причиной панкреатобилиарной аномалии является злокачественная, причины выбирались на основании следующих данных: визуализация опухоли, признак двойного протока, резкая обструкция желчного протока, неровность закупоренного края или асимметричная обструкция дистального края расширенный желчный проток. Анализ кривой рабочих характеристик приемника (ROC) был выполнен для сравнения результатов считывания изображений MRCP с результатами считывания комбинации изображений MRCP и стандартных изображений MR, а также с результатами считывания изображений ERCP.Бинормальные кривые ROC были подобраны с использованием программного обеспечения ROCKIT 0.9B . Диагностические возможности определялись путем расчета площади под кривой ROC (Az). Оценка 1 или 2 указала на доброкачественное поражение, оценки 4 или 5 указали на оценку злокачественного поражения.
определенно доброкачественная, 2. вероятно доброкачественная, 3. неопределенная, 4. вероятно злокачественная и 5. определенно злокачественная [5]. Если предполагалось, что причиной панкреатобилиарной аномалии является злокачественная, причины выбирались на основании следующих данных: визуализация опухоли, признак двойного протока, резкая обструкция желчного протока, неровность закупоренного края или асимметричная обструкция дистального края расширенный желчный проток. Анализ кривой рабочих характеристик приемника (ROC) был выполнен для сравнения результатов считывания изображений MRCP с результатами считывания комбинации изображений MRCP и стандартных изображений MR, а также с результатами считывания изображений ERCP.Бинормальные кривые ROC были подобраны с использованием программного обеспечения ROCKIT 0.9B . Диагностические возможности определялись путем расчета площади под кривой ROC (Az). Оценка 1 или 2 указала на доброкачественное поражение, оценки 4 или 5 указали на оценку злокачественного поражения. Считалось, что оценка 3 указывает на неопределенный диагноз. Были рассчитаны чувствительность, специфичность и точность ERCP, MRCP и комбинации MRCP и рутинной МРТ для дифференциации злокачественных и доброкачественных причин обструкции панкреатобилиарного тракта.
Считалось, что оценка 3 указывает на неопределенный диагноз. Были рассчитаны чувствительность, специфичность и точность ERCP, MRCP и комбинации MRCP и рутинной МРТ для дифференциации злокачественных и доброкачественных причин обструкции панкреатобилиарного тракта.
РЕЗУЛЬТАТЫ
Качество изображения MRCP
МР-холангиопанкреатография была успешно выполнена у всех 82 пациентов, и изображения MRCP были аналогичны изображениям прямой холангиопанкреатографии. MRCP-исследования диагностического качества были получены у 79 (96,3%) пациентов с тонким контрастом между панкреатобилиарной структурой и окружающим фоном. У остальных 3 пациентов с панкреатобилиарной опухолью наличие асцитической жидкости в верхней части живота и содержащих жидкость органов из-за непроходимости желудочно-кишечного тракта затрудняло визуализацию панкреатобилиарного дерева и ухудшало качество изображения MRCP.У 8 (16,7%) пациентов, у которых прямая холангиопанкреатография была неудачной или неполной, все исследования MRCP были успешными, а изображения MRCP были удовлетворительными.
Диагноз обструктивной локализации
Среди 82 пациентов с панкреатобилиарными заболеваниями 8, 60 и 21 случай имели панкреатобилиарные обструктивные участки во внутрипеченочном, внепеченочном желчном протоке и главном панкреатическом протоке, соответственно (всего 89 локализаций). ). MRCP может четко визуализировать расширение панкреатобилиарных протоков выше обструктивного уровня в их естественном состоянии, что делает его более подходящим для демонстрации обструкции внепеченочных желчных протоков.Общая точность MRCP в определении местоположения панкреато-билиарной обструкции составила 100%, что превосходит точность B-US ( P = 0,0002) и CT ( P = 0,0422), но не было никаких признаков. Это различие между MRCP и прямой холангиопанкреатографией ( P = 0,1487) (таблица).
Таблица 2
Точность уровня панкреато-билиарной обструкции (%) разными имиджелогическими методами
| Уровень | Внутрипеченочный | Внепеченочный | Основная поджелудочная железа | Всего |
| B-US | 100. 0 (8/8) 0 (8/8) | 81,7 (49/60) | 90,5 (19/21) | 85,4 (76/89) |
| CT | 100,0 (4/4) | 93,0 (40/43 ) | 100,0 (19/19) | 95,5 (63/66) |
| ERCP / PTC | 100,0 (5/5) | 96,7 (29/30) | 100,0 (8/8) | 97,7 (42/43) |
| MRCP | 100,0 (8/8) | 100,0 (60/60) | 100,0 (21/21) | 100,0 (89/89) |
злокачественный из доброкачественной обструкции
Чувствительность, специфичность и точность MRCP в различении злокачественных и доброкачественных причин панкреатобилиарной обструкции составила 64.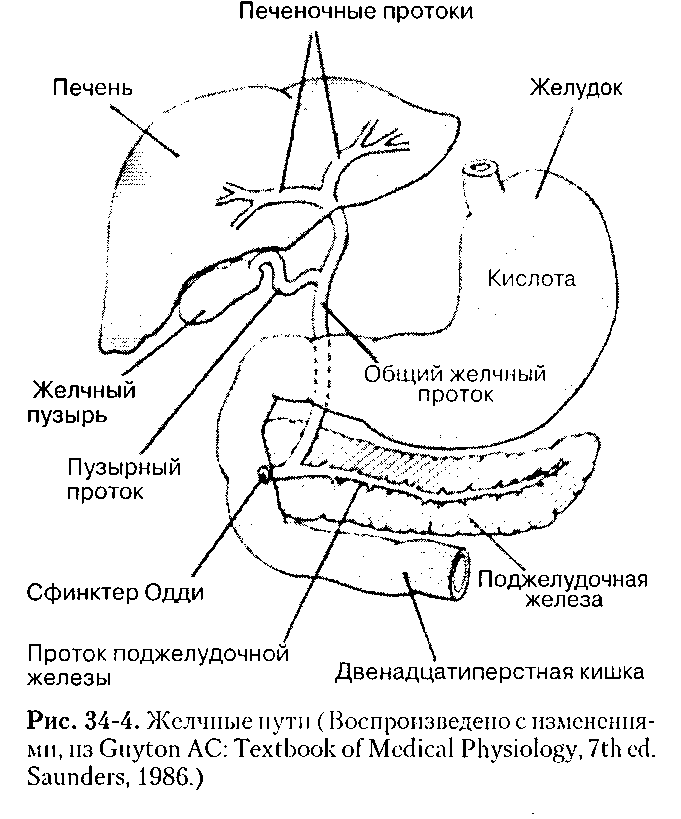 7%, 81,2% и 74,4% соответственно, в то время как показатели ERCP / PTC составили 77,8%, 86,4% и 82,5% соответственно. Разница не была значимой между MRCP и ERCP / PTC в области Az под кривой ROC ( P = 0,4590). Комбинация MRCP и рутинной МРТ, очевидно, может улучшить диагностические возможности по дифференциации причин панкреатобилиарной обструкции с чувствительностью 82,3%, специфичностью 93,8% и точностью 89,0%. Разница была значительной между MRCP и комбинацией MRCP и рутинной МРТ ( P = 0.0489) (таблица и рисунок).
7%, 81,2% и 74,4% соответственно, в то время как показатели ERCP / PTC составили 77,8%, 86,4% и 82,5% соответственно. Разница не была значимой между MRCP и ERCP / PTC в области Az под кривой ROC ( P = 0,4590). Комбинация MRCP и рутинной МРТ, очевидно, может улучшить диагностические возможности по дифференциации причин панкреатобилиарной обструкции с чувствительностью 82,3%, специфичностью 93,8% и точностью 89,0%. Разница была значительной между MRCP и комбинацией MRCP и рутинной МРТ ( P = 0.0489) (таблица и рисунок).
Анализ кривой ROC для дифференциации злокачественных и доброкачественных причин панкреатобилиарной обструкции.
Таблица 3
ROC-анализ панкреато-билиарной обструкции
| ERCP / PTC ( n = 40) | MRCP ( n = 82) | MRCP + MRI ( n = 82) | |
| Истинно-положительный | 14 | 22 | 28 |
| Истинно-отрицательный | 19 | 39 | 45 |
| Ложно-положительный | 3 | 9 | 3 |
| Ложноотрицательный | 4 | 12 | 6 |
| Чувствительность (%) | 77. 8 8 | 64,7 | 82,3 |
| Специфичность (%) | 86,4 | 81,2 | 93,8 |
| Точность (%) | 82,5 | 74,4 | 89,0 |
| A Z Значения ± SD | 0,9281 ± 0,0455 | 0,8833 ± 0,0400 | 0,9687 ± 0,0168 |
Диагностика обструктивных причин
Суммарная точность MRCP в диагностике причин панкреатобилиарной обструкции составила 75.6%, что было аналогично прямой холангиопанкреатографии (ERCP / PTC) ( P = 0,2345) и CT ( P = 0,7970), но лучше, чем у B-US ( P = 0,0131). Комбинация MRCP и рутинной МРТ значительно улучшила возможности клинической диагностики с точностью 87,8%, что превосходит таковую КТ ( P = 0,0330) и УЗИ ( P = 0,0000).
Комбинация MRCP и рутинной МРТ значительно улучшила возможности клинической диагностики с точностью 87,8%, что превосходит таковую КТ ( P = 0,0330) и УЗИ ( P = 0,0000).
Частота диагностики при комбинации MRCP и рутинной МРТ составила 92.1% и 94,1% для холелита и холедохолитиаза соответственно, что было лучше, чем у CT ( P = 0,0428) и US ( P = 0,0049). Но разница между ERCP / PTC и комбинированной MRCP и рутинной МРТ не была значительной ( P = 0,6445). Точность КТ, ERCP / PTC, MRCP и комбинированной MRCP и рутинной МРТ визуализации в различении различных панкреатобилиарных опухолей была значительно выше, чем у УЗИ ( P = 0,0002) (таблица).
Таблица 4
Точность диагностики причин обструкции (%)
| B-US | CT | ERCP / PTC | MRCP | MRCP + MRI | |||
| Холелитиаз | |||||||
| Камень желчного пузыря | 71,4 | 75,0 | 80,0 | 78,5 | 92,9 | ||
| Камень внутрипеченочного желчного протока | 85. 7 7 | 100,0 | 100,0 | 71,4 | 85,7 | ||
| Холедохолитиаз | 52,9 | 63,6 | 87,5 | 88,2 | 94,1 | ||
| Рак поджелудочной железы и желчного пузыря | |||||||
| Желчный рак | |||||||
| Желчный пузырь | 75,0 | 60,0 | 50,0 | 66,7 | |||
| Холангиокарцинома | 33,3 | 75,0 | 83. 3 3 | 77,8 | 88,9 | ||
| Ампуллярная карцинома | 33,3 | 50,0 | 100,0 | 66,7 | 66,7 | ||
| Рак головки поджелудочной железы | 63,6 | 81,8 | 100,062 | 63,6 | 81,8 | 100,062 | |
| Рак желчного сосочка | 40,0 | 66,7 | 100,0 | 60,0 | 80,0 | ||
| Другие заболевания | |||||||
| Повреждение желчного протока | 50. 0 0 | 100,0 | 100,0 | 100,0 | |||
| Киста холедоха | 100,0 | 100,0 | 100,0 | 100,0 | 100,0 | ||
| Склерозирующий холангит | 0 | 50,062 | 0 | 0 | 50,0 | ||
| Хронический панкреатит | 75,0 | 75,0 | 100,0 | 50,0 | 75,0 | ||
| Всего | 57.3 | 73,7 | 85,0 | 75,6 | 87,8 |
ОБСУЖДЕНИЕ
УЗИ или компьютерная томография (включая эндоскопическое УЗИ и спиральную компьютерную томографию) было первым методом диагностики заболеваний поджелудочной железы и желчных путей [6-9] . Прямая холангиопанкреатография, полученная с помощью ERCP или PTC, служит «золотым стандартом» в панкреатобилиарной имиджелогии.
Магнитно-резонансная холангиопанкреатография (MRCP), предложенная немецким исследователем Валлнером Б.К. и его группой в 1991 году [10], предложила новый метод визуализации для диагностики нарушений панкреатобилиарной системы [10-15].В настоящем исследовании MRCP была успешно выполнена у всех 82 пациентов, и изображения MRCP были аналогичны изображениям прямой холангиопанкреатографии. Исследования диагностического качества MRCP были получены в 79 случаях (96,3%), в том числе в 8 (16,7%) случаях прямая холангиопанкреатография была неудачной или неполной. Таким образом, MRCP может стать эффективной альтернативой прямой холангиопанкреатографии, когда диагностические ERCP и PTC оказались безуспешными или неадекватными [1,16].
В нашем исследовании точность MRCP в определении локализации панкреатобилиарной обструкции составила 100%, что превосходит точность B-US и CT, но существенно не различается между MRCP и прямой холангиопанкреатографией.По сравнению с обследованием ERCP / PTC, неинвазивный MRCP может показать всю систему панкреатобилиарного протока и продемонстрировать уровень, степень и диапазон обструкции, а также морфологические характеристики. Кроме того, MRCP может предоставить много ценной имиджологической информации и помочь определить лучший подход к паллиативному дренированию и другому интервенционному лечению пациентов с неоперабельными опухолями [17,18].
В имиджелогии панкреато-билиарной системы это очень важно для диагностики и дифференциации злокачественных и доброкачественных причин панкреато-билиарной обструкции.Комбинация MRCP и рутинной MR-визуализации может значительно улучшить возможности клинической диагностики за счет выявления патологических изменений окружающих структур [19–22]. Для панкреатобилиарных опухолей MRCP может определить местоположение и морфологические характеристики панкреатобилиарной обструкции, а также оценить диапазон поражения опухолей и хирургическую резектабельность. Кроме того, с преимуществами КТ и прямого холангиопанкреатографического исследования, комбинированная рутинная МРТ и MRCP могут выявить соответствующие окружающие структуры и повысить точность клинической диагностики [17,23,24].
Методы УЗИ и КТ наиболее часто используются при первичной оценке пациентов с желчнокаменной болезнью, и оба обладают высокой точностью диагностики камней в желчном пузыре и внутрипеченочных протоков. Чувствительность MRCP в диагностике камней желчного пузыря и внутрипеченочных протоков варьировалась в зависимости от размера, количества и расположения камней, а MRCP больше подходил для диагностики холедохолитиаза. Таким образом, MRCP может в основном обнаружить камни в общем желчном протоке и исключить другие панкреатобилиарные обструктивные заболевания [25–27].
С развитием лапароскопической техники лапароскопическая холецистэктомия (LC) и эндоскопическая тенотомия сфинктера (EST) стали широко использоваться в хирургии желчевыводящих путей [28]. MRCP может отобразить всю анатомическую структуру желчного дерева и помочь гарантировать успех лапароскопической холецистэктомии. Перед хирургическим вмешательством определение анатомических вариантов желчного дерева с помощью MRCP может привести к снижению риска повреждения желчного протока во время лапароскопической холецистэктомии [29]. Теперь ЭРХПГ больше не является рутинным обследованием пациентов с холедохолитиазом, и вместо этого в основном используется эндоскопическая тенотомия сфинктера для удаления камней в общем желчном протоке.
Что касается доброкачественных стриктур, вызванных холангитом, хирургической травмой или хроническим панкреатитом, MRCP может иметь некоторые трудности с отображением миниатюрных изменений панкреатобилиарного протока. Но использование динамического MRCP со стимуляцией секретином может быть полезным для диагностики папиллярного стеноза или дисфункции поджелудочной железы, а также для обнаружения пониженного экзокринного резерва поджелудочной железы [30–32]. Кроме того, в литературе указывается, что MRCP можно использовать на начальном этапе для оценки кисты холедоха [33].
В заключение, в недавних оптимальных имиджелогических процедурах диагностики заболеваний поджелудочной железы B-US по-прежнему является первым выбором для оценки.Комбинация MRCP и рутинной МРТ обеспечивает эффективный метод диагностики различных панкреатобилиарных обструкций, дифференциации злокачественных и доброкачественных причин и проведения послеоперационного наблюдения. МРТ и КТ поперечного сечения являются дополнительными методами для предоперационной диагностики и оценки опухолей поджелудочной железы. Прямая диагностическая холангиопанкреатография (ERCP / PTC) в основном используется в сложных случаях и сочетается с другим интервенционным лечением, включая EST или PTCD (рисунок).
Оптимальная методика имиджелогического исследования заболеваний поджелудочной железы.
Визуализирующая диагностика заболеваний поджелудочной железы: контрольное исследование
Резюме
ЦЕЛЬ: Оценить клиническую ценность различных имиджелогических методов диагностики заболеваний поджелудочной железы и желчевыводящих путей и найти оптимальную процедуру.
МЕТОДЫ: Проанализировано 82 случая заболеваний поджелудочной железы и желчевыводящих путей, подтвержденных хирургическим путем и патологией. Было 38 случаев холелитиаза, 34 случая панкреатобилиарных опухолей и 10 других случаев.Имиджелогические методы включали B-US, CT, ERCP, PTC, поперечную МРТ и МР-холангиопанкреатографию (MRCP).
РЕЗУЛЬТАТЫ: Степень точности MRCP в определении местоположения панкреатобилиарной обструкции составила 100%. При дифференцировании злокачественной обструкции от доброкачественной чувствительность комбинации MRCP и поперечной МРТ составила 82,3%, специфичность – 93,8%, а уровень точности – 89,0%. Степень точности определения характера обструкции составила 87,8%, что выше, чем у B-US ( P = 0.0000) и КТ ( P = 0,0330), но не было существенной разницы между прямой холангиопанкреатографией и комбинацией MRCP и традиционной МРТ ( P = 0,6666).
ВЫВОД: В большинстве случаев MRCP может заменить прямую холангиопанкреатографию для диагностики. Комбинация MRCP и поперечной МРТ должна рассматриваться как важное средство диагностики заболеваний поджелудочной железы и желчевыводящих путей, предоперационной оценки и послеоперационного наблюдения.
ВВЕДЕНИЕ
Панкреатобилиарные расстройства – распространенные заболевания, при которых часто поражается желчная система, вызывая симптомы механической желтухи.Это предварительное условие для исследования места обструкции и причин заболеваний поджелудочной железы и желчевыводящих путей. В данном исследовании проанализировано 82 случая заболеваний поджелудочной железы, подтвержденных хирургическим вмешательством и патологией. Цели проспективного исследования заключались в оценке клинической ценности различных имиджелогических методов в диагностике заболеваний поджелудочной железы и желчевыводящих путей и в поиске оптимальной процедуры обследования.
МАТЕРИАЛЫ И МЕТОДЫ
Пациенты
Объектами исследования были 82 пациента (54 мужчины и 28 женщин, средний возраст 60 лет.0 лет, от 11 до 82 лет), 67 (81,7%) случаев имели симптом механической желтухи. Все пациенты прошли B-US, MR холангиопанкреатографию (MRCP) и поперечное МРТ. Пятьдесят семь пациентов прошли КТ с усилением или без него. Кроме того, 48 пациентам была проведена прямая холангиопанкреатография (41 ERCP и 7 PTC). Однако прямая холангиопанкреатография была безуспешной в 4 случаях из-за трудностей с канюляцией (2 ERCP), постгастроэнтеростомии (1 ERCP) и больного пациента (1 PTC).ЭРХПГ была неполной в других 4 случаях, потому что можно было увидеть только проток поджелудочной железы, а желчное дерево не было помутнено. Таким образом, во всех 82 случаях было выполнено 40 прямых холангиопанкреатографий (34 ERCP и 6 PTC), у 1 пациента было осложнение острого панкреатита после ERCP. Все пациенты с заболеваниями поджелудочной железы и желчевыводящих путей были подтверждены хирургическими данными и патологией, в том числе 12 – лапароскопической холецистэктомией (LC), 6 – эндоскопической тенотомией сфинктера (EST) и 1 – дренажом PTC (PTCD).Из 82 случаев у 38 был диагностирован холелитиаз, у 34 – панкреатобилиарные опухоли и у 10 – другие заболевания (таблица).
Таблица 1
Заболевания поджелудочной железы ( n = 82)
| Заболевания поджелудочно-желчных путей | Число случаев |
| Холелитиаз a | 38 |
| Камень желчного пузыря | 14 |
| Камень внутрипеченочного желчного протока | 7 |
| Холедохолитиаз | 17 |
| Панкреатобилиарная опухоль b | 34 |
| Желчный рак | |
| Холангиокарцинома | 9 |
| Ампуллярная карцинома | 3 |
| Карцинома головки поджелудочной железы | 11 |
| Карцинома желчного сосочка | 5 |
| 2 | |
| Киста холедоха | 2 |
| Склерозирующий холангит | 2 |
| Хронический панкреатит | 4 |
Методы
МРТ-визуализация выполнялась с 1.0T сверхпроводящий блок (Philips Gyroscan T10-NT, версия программного обеспечения 4.6.2), содержащий катушку для тела. Пациенты были обследованы в положении лежа на спине, спокойном дыхании и компрессии бандажом. Сначала были выполнены стандартные аксиальные исследования T1WI, T2WI и коронарного T2WI в верхней части живота с использованием последовательности Turbo Spin-Echo (TSE), а за ними последовали дополнительные аксиальные T2WI и / или T1WI последовательности с подавлением жира (восстановление с инверсией спектрального насыщения, SPIR). Стандартные аксиальные изображения служили ориентирами для определения местоположения МР-холангиопанкреатографии (MRCP).MRCP выполняли с коронарной, мультиспиральной, сильно взвешенной T2-последовательностью TSE (TR = 2000 мс, TE = 700 мс). Для уменьшения артефакта дыхательного движения использовалась техника без задержки дыхания. Исходные изображения MRCP были трехмерно (3D) реконструированы с использованием алгоритма проекции максимальной интенсивности (MIP). Общее время визуализации составляло примерно 30 мин.
Для компьютерной томографии (КТ) использовался компьютерный томограф всего тела (Picker PQ-2000). Все КТ-исследования проводились после того, как пациенты голодали в течение 4-8 часов и принимали пероральный контраст 500-1000 мл (0.5% -1% меглумина диатризоат) перед компьютерной томографией. При усиленном КТ-исследовании использовалось 80–100 мл неионных внутривенных контрастных веществ, вводимых через анекубитальную вену болюсно со скоростью 2–3 мл / с.
Прямая холангиопанкреатография (ERCP и PTC) выполнялась с помощью цифрового устройства визуализации (Philips Diagnost 93).
Анализ изображений
Все данные изображений 82 пациентов были тщательно изучены, чтобы выявить увеличение или стриктуру панкреатобилиарного тракта. Протокол исследования включал обнаружение обструктивных участков, различение злокачественных и доброкачественных причин и оценку клинической ценности различных методов визуализации (включая B-US, CT, MRCP, ERCP / PTC) при диагностике заболеваний поджелудочной железы и желчевыводящих путей.Программное обеспечение SAS использовалось для всех статистических анализов.
Диагностические принципы и критерии оценки для прямой холангиопанкреатографии и MRCP были идентичны, но в MRCP было более важно тщательно изучить как исходные изображения, так и изображения, реконструированные MIP. По результатам расширения или стриктуры панкреатобилиарного дерева и желчного пузыря обструктивные места панкреатобилиарного протока были разделены на три части: внутрипеченочный или внепеченочный желчный проток и главный панкреатический проток.Нормальный желчный пузырь 7-10 см в длину и 3-4 см в ширину. Расширение общего желчного протока определялось как более 8 мм в максимальном диаметре у пациентов без холецистэктомии в анамнезе и 10 мм у пациентов, перенесших холецистэктомию в анамнезе. Расширение внутрипеченочного желчного протока и главного протока поджелудочной железы было определено как более 3 мм в максимальном диаметре [1-4].
Причина панкреатобилиарной аномалии оценивалась с использованием пятибалльной шкалы для определения уровня достоверности: 1.определенно доброкачественная, 2. вероятно доброкачественная, 3. неопределенная, 4. вероятно злокачественная и 5. определенно злокачественная [5]. Если предполагалось, что причиной панкреатобилиарной аномалии является злокачественная, причины выбирались на основании следующих данных: визуализация опухоли, признак двойного протока, резкая обструкция желчного протока, неровность закупоренного края или асимметричная обструкция дистального края расширенный желчный проток. Анализ кривой рабочих характеристик приемника (ROC) был выполнен для сравнения результатов считывания изображений MRCP с результатами считывания комбинации изображений MRCP и стандартных изображений MR, а также с результатами считывания изображений ERCP.Бинормальные кривые ROC были подобраны с использованием программного обеспечения ROCKIT 0.9B . Диагностические возможности определялись путем расчета площади под кривой ROC (Az). Оценка 1 или 2 указала на доброкачественное поражение, оценки 4 или 5 указали на оценку злокачественного поражения. Считалось, что оценка 3 указывает на неопределенный диагноз. Были рассчитаны чувствительность, специфичность и точность ERCP, MRCP и комбинации MRCP и рутинной МРТ для дифференциации злокачественных и доброкачественных причин обструкции панкреатобилиарного тракта.
РЕЗУЛЬТАТЫ
Качество изображения MRCP
МР-холангиопанкреатография была успешно выполнена у всех 82 пациентов, и изображения MRCP были аналогичны изображениям прямой холангиопанкреатографии. MRCP-исследования диагностического качества были получены у 79 (96,3%) пациентов с тонким контрастом между панкреатобилиарной структурой и окружающим фоном. У остальных 3 пациентов с панкреатобилиарной опухолью наличие асцитической жидкости в верхней части живота и содержащих жидкость органов из-за непроходимости желудочно-кишечного тракта затрудняло визуализацию панкреатобилиарного дерева и ухудшало качество изображения MRCP.У 8 (16,7%) пациентов, у которых прямая холангиопанкреатография была неудачной или неполной, все исследования MRCP были успешными, а изображения MRCP были удовлетворительными.
Диагноз обструктивной локализации
Среди 82 пациентов с панкреатобилиарными заболеваниями 8, 60 и 21 случай имели панкреатобилиарные обструктивные участки во внутрипеченочном, внепеченочном желчном протоке и главном панкреатическом протоке, соответственно (всего 89 локализаций). ). MRCP может четко визуализировать расширение панкреатобилиарных протоков выше обструктивного уровня в их естественном состоянии, что делает его более подходящим для демонстрации обструкции внепеченочных желчных протоков.Общая точность MRCP в определении местоположения панкреато-билиарной обструкции составила 100%, что превосходит точность B-US ( P = 0,0002) и CT ( P = 0,0422), но не было никаких признаков. Это различие между MRCP и прямой холангиопанкреатографией ( P = 0,1487) (таблица).
Таблица 2
Точность уровня панкреато-билиарной обструкции (%) разными имиджелогическими методами
| Уровень | Внутрипеченочный | Внепеченочный | Основная поджелудочная железа | Всего |
| B-US | 100.0 (8/8) | 81,7 (49/60) | 90,5 (19/21) | 85,4 (76/89) |
| CT | 100,0 (4/4) | 93,0 (40/43 ) | 100,0 (19/19) | 95,5 (63/66) |
| ERCP / PTC | 100,0 (5/5) | 96,7 (29/30) | 100,0 (8/8) | 97,7 (42/43) |
| MRCP | 100,0 (8/8) | 100,0 (60/60) | 100,0 (21/21) | 100,0 (89/89) |
злокачественный из доброкачественной обструкции
Чувствительность, специфичность и точность MRCP в различении злокачественных и доброкачественных причин панкреатобилиарной обструкции составила 64.7%, 81,2% и 74,4% соответственно, в то время как показатели ERCP / PTC составили 77,8%, 86,4% и 82,5% соответственно. Разница не была значимой между MRCP и ERCP / PTC в области Az под кривой ROC ( P = 0,4590). Комбинация MRCP и рутинной МРТ, очевидно, может улучшить диагностические возможности по дифференциации причин панкреатобилиарной обструкции с чувствительностью 82,3%, специфичностью 93,8% и точностью 89,0%. Разница была значительной между MRCP и комбинацией MRCP и рутинной МРТ ( P = 0.0489) (таблица и рисунок).
Анализ кривой ROC для дифференциации злокачественных и доброкачественных причин панкреатобилиарной обструкции.
Таблица 3
ROC-анализ панкреато-билиарной обструкции
| ERCP / PTC ( n = 40) | MRCP ( n = 82) | MRCP + MRI ( n = 82) | |
| Истинно-положительный | 14 | 22 | 28 |
| Истинно-отрицательный | 19 | 39 | 45 |
| Ложно-положительный | 3 | 9 | 3 |
| Ложноотрицательный | 4 | 12 | 6 |
| Чувствительность (%) | 77.8 | 64,7 | 82,3 |
| Специфичность (%) | 86,4 | 81,2 | 93,8 |
| Точность (%) | 82,5 | 74,4 | 89,0 |
| A Z Значения ± SD | 0,9281 ± 0,0455 | 0,8833 ± 0,0400 | 0,9687 ± 0,0168 |
Диагностика обструктивных причин
Суммарная точность MRCP в диагностике причин панкреатобилиарной обструкции составила 75.6%, что было аналогично прямой холангиопанкреатографии (ERCP / PTC) ( P = 0,2345) и CT ( P = 0,7970), но лучше, чем у B-US ( P = 0,0131). Комбинация MRCP и рутинной МРТ значительно улучшила возможности клинической диагностики с точностью 87,8%, что превосходит таковую КТ ( P = 0,0330) и УЗИ ( P = 0,0000).
Частота диагностики при комбинации MRCP и рутинной МРТ составила 92.1% и 94,1% для холелита и холедохолитиаза соответственно, что было лучше, чем у CT ( P = 0,0428) и US ( P = 0,0049). Но разница между ERCP / PTC и комбинированной MRCP и рутинной МРТ не была значительной ( P = 0,6445). Точность КТ, ERCP / PTC, MRCP и комбинированной MRCP и рутинной МРТ визуализации в различении различных панкреатобилиарных опухолей была значительно выше, чем у УЗИ ( P = 0,0002) (таблица).
Таблица 4
Точность диагностики причин обструкции (%)
| B-US | CT | ERCP / PTC | MRCP | MRCP + MRI | |||
| Холелитиаз | |||||||
| Камень желчного пузыря | 71,4 | 75,0 | 80,0 | 78,5 | 92,9 | ||
| Камень внутрипеченочного желчного протока | 85.7 | 100,0 | 100,0 | 71,4 | 85,7 | ||
| Холедохолитиаз | 52,9 | 63,6 | 87,5 | 88,2 | 94,1 | ||
| Рак поджелудочной железы и желчного пузыря | |||||||
| Желчный рак | |||||||
| Желчный пузырь | 75,0 | 60,0 | 50,0 | 66,7 | |||
| Холангиокарцинома | 33,3 | 75,0 | 83.3 | 77,8 | 88,9 | ||
| Ампуллярная карцинома | 33,3 | 50,0 | 100,0 | 66,7 | 66,7 | ||
| Рак головки поджелудочной железы | 63,6 | 81,8 | 100,062 | 63,6 | 81,8 | 100,062 | |
| Рак желчного сосочка | 40,0 | 66,7 | 100,0 | 60,0 | 80,0 | ||
| Другие заболевания | |||||||
| Повреждение желчного протока | 50.0 | 100,0 | 100,0 | 100,0 | |||
| Киста холедоха | 100,0 | 100,0 | 100,0 | 100,0 | 100,0 | ||
| Склерозирующий холангит | 0 | 50,062 | 0 | 0 | 50,0 | ||
| Хронический панкреатит | 75,0 | 75,0 | 100,0 | 50,0 | 75,0 | ||
| Всего | 57.3 | 73,7 | 85,0 | 75,6 | 87,8 |
ОБСУЖДЕНИЕ
УЗИ или компьютерная томография (включая эндоскопическое УЗИ и спиральную компьютерную томографию) было первым методом диагностики заболеваний поджелудочной железы и желчных путей [6-9] . Прямая холангиопанкреатография, полученная с помощью ERCP или PTC, служит «золотым стандартом» в панкреатобилиарной имиджелогии.
Магнитно-резонансная холангиопанкреатография (MRCP), предложенная немецким исследователем Валлнером Б.К. и его группой в 1991 году [10], предложила новый метод визуализации для диагностики нарушений панкреатобилиарной системы [10-15].В настоящем исследовании MRCP была успешно выполнена у всех 82 пациентов, и изображения MRCP были аналогичны изображениям прямой холангиопанкреатографии. Исследования диагностического качества MRCP были получены в 79 случаях (96,3%), в том числе в 8 (16,7%) случаях прямая холангиопанкреатография была неудачной или неполной. Таким образом, MRCP может стать эффективной альтернативой прямой холангиопанкреатографии, когда диагностические ERCP и PTC оказались безуспешными или неадекватными [1,16].
В нашем исследовании точность MRCP в определении локализации панкреатобилиарной обструкции составила 100%, что превосходит точность B-US и CT, но существенно не различается между MRCP и прямой холангиопанкреатографией.По сравнению с обследованием ERCP / PTC, неинвазивный MRCP может показать всю систему панкреатобилиарного протока и продемонстрировать уровень, степень и диапазон обструкции, а также морфологические характеристики. Кроме того, MRCP может предоставить много ценной имиджологической информации и помочь определить лучший подход к паллиативному дренированию и другому интервенционному лечению пациентов с неоперабельными опухолями [17,18].
В имиджелогии панкреато-билиарной системы это очень важно для диагностики и дифференциации злокачественных и доброкачественных причин панкреато-билиарной обструкции.Комбинация MRCP и рутинной MR-визуализации может значительно улучшить возможности клинической диагностики за счет выявления патологических изменений окружающих структур [19–22]. Для панкреатобилиарных опухолей MRCP может определить местоположение и морфологические характеристики панкреатобилиарной обструкции, а также оценить диапазон поражения опухолей и хирургическую резектабельность. Кроме того, с преимуществами КТ и прямого холангиопанкреатографического исследования, комбинированная рутинная МРТ и MRCP могут выявить соответствующие окружающие структуры и повысить точность клинической диагностики [17,23,24].
Методы УЗИ и КТ наиболее часто используются при первичной оценке пациентов с желчнокаменной болезнью, и оба обладают высокой точностью диагностики камней в желчном пузыре и внутрипеченочных протоков. Чувствительность MRCP в диагностике камней желчного пузыря и внутрипеченочных протоков варьировалась в зависимости от размера, количества и расположения камней, а MRCP больше подходил для диагностики холедохолитиаза. Таким образом, MRCP может в основном обнаружить камни в общем желчном протоке и исключить другие панкреатобилиарные обструктивные заболевания [25–27].
С развитием лапароскопической техники лапароскопическая холецистэктомия (LC) и эндоскопическая тенотомия сфинктера (EST) стали широко использоваться в хирургии желчевыводящих путей [28]. MRCP может отобразить всю анатомическую структуру желчного дерева и помочь гарантировать успех лапароскопической холецистэктомии. Перед хирургическим вмешательством определение анатомических вариантов желчного дерева с помощью MRCP может привести к снижению риска повреждения желчного протока во время лапароскопической холецистэктомии [29]. Теперь ЭРХПГ больше не является рутинным обследованием пациентов с холедохолитиазом, и вместо этого в основном используется эндоскопическая тенотомия сфинктера для удаления камней в общем желчном протоке.
Что касается доброкачественных стриктур, вызванных холангитом, хирургической травмой или хроническим панкреатитом, MRCP может иметь некоторые трудности с отображением миниатюрных изменений панкреатобилиарного протока. Но использование динамического MRCP со стимуляцией секретином может быть полезным для диагностики папиллярного стеноза или дисфункции поджелудочной железы, а также для обнаружения пониженного экзокринного резерва поджелудочной железы [30–32]. Кроме того, в литературе указывается, что MRCP можно использовать на начальном этапе для оценки кисты холедоха [33].
В заключение, в недавних оптимальных имиджелогических процедурах диагностики заболеваний поджелудочной железы B-US по-прежнему является первым выбором для оценки.Комбинация MRCP и рутинной МРТ обеспечивает эффективный метод диагностики различных панкреатобилиарных обструкций, дифференциации злокачественных и доброкачественных причин и проведения послеоперационного наблюдения. МРТ и КТ поперечного сечения являются дополнительными методами для предоперационной диагностики и оценки опухолей поджелудочной железы. Прямая диагностическая холангиопанкреатография (ERCP / PTC) в основном используется в сложных случаях и сочетается с другим интервенционным лечением, включая EST или PTCD (рисунок).
Оптимальная методика имиджелогического исследования заболеваний поджелудочной железы.
Визуализирующая диагностика заболеваний поджелудочной железы: контрольное исследование
Резюме
ЦЕЛЬ: Оценить клиническую ценность различных имиджелогических методов диагностики заболеваний поджелудочной железы и желчевыводящих путей и найти оптимальную процедуру.
МЕТОДЫ: Проанализировано 82 случая заболеваний поджелудочной железы и желчевыводящих путей, подтвержденных хирургическим путем и патологией. Было 38 случаев холелитиаза, 34 случая панкреатобилиарных опухолей и 10 других случаев.Имиджелогические методы включали B-US, CT, ERCP, PTC, поперечную МРТ и МР-холангиопанкреатографию (MRCP).
РЕЗУЛЬТАТЫ: Степень точности MRCP в определении местоположения панкреатобилиарной обструкции составила 100%. При дифференцировании злокачественной обструкции от доброкачественной чувствительность комбинации MRCP и поперечной МРТ составила 82,3%, специфичность – 93,8%, а уровень точности – 89,0%. Степень точности определения характера обструкции составила 87,8%, что выше, чем у B-US ( P = 0.0000) и КТ ( P = 0,0330), но не было существенной разницы между прямой холангиопанкреатографией и комбинацией MRCP и традиционной МРТ ( P = 0,6666).
ВЫВОД: В большинстве случаев MRCP может заменить прямую холангиопанкреатографию для диагностики. Комбинация MRCP и поперечной МРТ должна рассматриваться как важное средство диагностики заболеваний поджелудочной железы и желчевыводящих путей, предоперационной оценки и послеоперационного наблюдения.
ВВЕДЕНИЕ
Панкреатобилиарные расстройства – распространенные заболевания, при которых часто поражается желчная система, вызывая симптомы механической желтухи.Это предварительное условие для исследования места обструкции и причин заболеваний поджелудочной железы и желчевыводящих путей. В данном исследовании проанализировано 82 случая заболеваний поджелудочной железы, подтвержденных хирургическим вмешательством и патологией. Цели проспективного исследования заключались в оценке клинической ценности различных имиджелогических методов в диагностике заболеваний поджелудочной железы и желчевыводящих путей и в поиске оптимальной процедуры обследования.
МАТЕРИАЛЫ И МЕТОДЫ
Пациенты
Объектами исследования были 82 пациента (54 мужчины и 28 женщин, средний возраст 60 лет.0 лет, от 11 до 82 лет), 67 (81,7%) случаев имели симптом механической желтухи. Все пациенты прошли B-US, MR холангиопанкреатографию (MRCP) и поперечное МРТ. Пятьдесят семь пациентов прошли КТ с усилением или без него. Кроме того, 48 пациентам была проведена прямая холангиопанкреатография (41 ERCP и 7 PTC). Однако прямая холангиопанкреатография была безуспешной в 4 случаях из-за трудностей с канюляцией (2 ERCP), постгастроэнтеростомии (1 ERCP) и больного пациента (1 PTC).ЭРХПГ была неполной в других 4 случаях, потому что можно было увидеть только проток поджелудочной железы, а желчное дерево не было помутнено. Таким образом, во всех 82 случаях было выполнено 40 прямых холангиопанкреатографий (34 ERCP и 6 PTC), у 1 пациента было осложнение острого панкреатита после ERCP. Все пациенты с заболеваниями поджелудочной железы и желчевыводящих путей были подтверждены хирургическими данными и патологией, в том числе 12 – лапароскопической холецистэктомией (LC), 6 – эндоскопической тенотомией сфинктера (EST) и 1 – дренажом PTC (PTCD).Из 82 случаев у 38 был диагностирован холелитиаз, у 34 – панкреатобилиарные опухоли и у 10 – другие заболевания (таблица).
Таблица 1
Заболевания поджелудочной железы ( n = 82)
| Заболевания поджелудочно-желчных путей | Число случаев |
| Холелитиаз a | 38 |
| Камень желчного пузыря | 14 |
| Камень внутрипеченочного желчного протока | 7 |
| Холедохолитиаз | 17 |
| Панкреатобилиарная опухоль b | 34 |
| Желчный рак | |
| Холангиокарцинома | 9 |
| Ампуллярная карцинома | 3 |
| Карцинома головки поджелудочной железы | 11 |
| Карцинома желчного сосочка | 5 |
| 2 | |
| Киста холедоха | 2 |
| Склерозирующий холангит | 2 |
| Хронический панкреатит | 4 |
Методы
МРТ-визуализация выполнялась с 1.0T сверхпроводящий блок (Philips Gyroscan T10-NT, версия программного обеспечения 4.6.2), содержащий катушку для тела. Пациенты были обследованы в положении лежа на спине, спокойном дыхании и компрессии бандажом. Сначала были выполнены стандартные аксиальные исследования T1WI, T2WI и коронарного T2WI в верхней части живота с использованием последовательности Turbo Spin-Echo (TSE), а за ними последовали дополнительные аксиальные T2WI и / или T1WI последовательности с подавлением жира (восстановление с инверсией спектрального насыщения, SPIR). Стандартные аксиальные изображения служили ориентирами для определения местоположения МР-холангиопанкреатографии (MRCP).MRCP выполняли с коронарной, мультиспиральной, сильно взвешенной T2-последовательностью TSE (TR = 2000 мс, TE = 700 мс). Для уменьшения артефакта дыхательного движения использовалась техника без задержки дыхания. Исходные изображения MRCP были трехмерно (3D) реконструированы с использованием алгоритма проекции максимальной интенсивности (MIP). Общее время визуализации составляло примерно 30 мин.
Для компьютерной томографии (КТ) использовался компьютерный томограф всего тела (Picker PQ-2000). Все КТ-исследования проводились после того, как пациенты голодали в течение 4-8 часов и принимали пероральный контраст 500-1000 мл (0.5% -1% меглумина диатризоат) перед компьютерной томографией. При усиленном КТ-исследовании использовалось 80–100 мл неионных внутривенных контрастных веществ, вводимых через анекубитальную вену болюсно со скоростью 2–3 мл / с.
Прямая холангиопанкреатография (ERCP и PTC) выполнялась с помощью цифрового устройства визуализации (Philips Diagnost 93).
Анализ изображений
Все данные изображений 82 пациентов были тщательно изучены, чтобы выявить увеличение или стриктуру панкреатобилиарного тракта. Протокол исследования включал обнаружение обструктивных участков, различение злокачественных и доброкачественных причин и оценку клинической ценности различных методов визуализации (включая B-US, CT, MRCP, ERCP / PTC) при диагностике заболеваний поджелудочной железы и желчевыводящих путей.Программное обеспечение SAS использовалось для всех статистических анализов.
Диагностические принципы и критерии оценки для прямой холангиопанкреатографии и MRCP были идентичны, но в MRCP было более важно тщательно изучить как исходные изображения, так и изображения, реконструированные MIP. По результатам расширения или стриктуры панкреатобилиарного дерева и желчного пузыря обструктивные места панкреатобилиарного протока были разделены на три части: внутрипеченочный или внепеченочный желчный проток и главный панкреатический проток.Нормальный желчный пузырь 7-10 см в длину и 3-4 см в ширину. Расширение общего желчного протока определялось как более 8 мм в максимальном диаметре у пациентов без холецистэктомии в анамнезе и 10 мм у пациентов, перенесших холецистэктомию в анамнезе. Расширение внутрипеченочного желчного протока и главного протока поджелудочной железы было определено как более 3 мм в максимальном диаметре [1-4].
Причина панкреатобилиарной аномалии оценивалась с использованием пятибалльной шкалы для определения уровня достоверности: 1.определенно доброкачественная, 2. вероятно доброкачественная, 3. неопределенная, 4. вероятно злокачественная и 5. определенно злокачественная [5]. Если предполагалось, что причиной панкреатобилиарной аномалии является злокачественная, причины выбирались на основании следующих данных: визуализация опухоли, признак двойного протока, резкая обструкция желчного протока, неровность закупоренного края или асимметричная обструкция дистального края расширенный желчный проток. Анализ кривой рабочих характеристик приемника (ROC) был выполнен для сравнения результатов считывания изображений MRCP с результатами считывания комбинации изображений MRCP и стандартных изображений MR, а также с результатами считывания изображений ERCP.Бинормальные кривые ROC были подобраны с использованием программного обеспечения ROCKIT 0.9B . Диагностические возможности определялись путем расчета площади под кривой ROC (Az). Оценка 1 или 2 указала на доброкачественное поражение, оценки 4 или 5 указали на оценку злокачественного поражения. Считалось, что оценка 3 указывает на неопределенный диагноз. Были рассчитаны чувствительность, специфичность и точность ERCP, MRCP и комбинации MRCP и рутинной МРТ для дифференциации злокачественных и доброкачественных причин обструкции панкреатобилиарного тракта.
РЕЗУЛЬТАТЫ
Качество изображения MRCP
МР-холангиопанкреатография была успешно выполнена у всех 82 пациентов, и изображения MRCP были аналогичны изображениям прямой холангиопанкреатографии. MRCP-исследования диагностического качества были получены у 79 (96,3%) пациентов с тонким контрастом между панкреатобилиарной структурой и окружающим фоном. У остальных 3 пациентов с панкреатобилиарной опухолью наличие асцитической жидкости в верхней части живота и содержащих жидкость органов из-за непроходимости желудочно-кишечного тракта затрудняло визуализацию панкреатобилиарного дерева и ухудшало качество изображения MRCP.У 8 (16,7%) пациентов, у которых прямая холангиопанкреатография была неудачной или неполной, все исследования MRCP были успешными, а изображения MRCP были удовлетворительными.
Диагноз обструктивной локализации
Среди 82 пациентов с панкреатобилиарными заболеваниями 8, 60 и 21 случай имели панкреатобилиарные обструктивные участки во внутрипеченочном, внепеченочном желчном протоке и главном панкреатическом протоке, соответственно (всего 89 локализаций). ). MRCP может четко визуализировать расширение панкреатобилиарных протоков выше обструктивного уровня в их естественном состоянии, что делает его более подходящим для демонстрации обструкции внепеченочных желчных протоков.Общая точность MRCP в определении местоположения панкреато-билиарной обструкции составила 100%, что превосходит точность B-US ( P = 0,0002) и CT ( P = 0,0422), но не было никаких признаков. Это различие между MRCP и прямой холангиопанкреатографией ( P = 0,1487) (таблица).
Таблица 2
Точность уровня панкреато-билиарной обструкции (%) разными имиджелогическими методами
| Уровень | Внутрипеченочный | Внепеченочный | Основная поджелудочная железа | Всего |
| B-US | 100.0 (8/8) | 81,7 (49/60) | 90,5 (19/21) | 85,4 (76/89) |
| CT | 100,0 (4/4) | 93,0 (40/43 ) | 100,0 (19/19) | 95,5 (63/66) |
| ERCP / PTC | 100,0 (5/5) | 96,7 (29/30) | 100,0 (8/8) | 97,7 (42/43) |
| MRCP | 100,0 (8/8) | 100,0 (60/60) | 100,0 (21/21) | 100,0 (89/89) |
злокачественный из доброкачественной обструкции
Чувствительность, специфичность и точность MRCP в различении злокачественных и доброкачественных причин панкреатобилиарной обструкции составила 64.7%, 81,2% и 74,4% соответственно, в то время как показатели ERCP / PTC составили 77,8%, 86,4% и 82,5% соответственно. Разница не была значимой между MRCP и ERCP / PTC в области Az под кривой ROC ( P = 0,4590). Комбинация MRCP и рутинной МРТ, очевидно, может улучшить диагностические возможности по дифференциации причин панкреатобилиарной обструкции с чувствительностью 82,3%, специфичностью 93,8% и точностью 89,0%. Разница была значительной между MRCP и комбинацией MRCP и рутинной МРТ ( P = 0.0489) (таблица и рисунок).
Анализ кривой ROC для дифференциации злокачественных и доброкачественных причин панкреатобилиарной обструкции.
Таблица 3
ROC-анализ панкреато-билиарной обструкции
| ERCP / PTC ( n = 40) | MRCP ( n = 82) | MRCP + MRI ( n = 82) | |
| Истинно-положительный | 14 | 22 | 28 |
| Истинно-отрицательный | 19 | 39 | 45 |
| Ложно-положительный | 3 | 9 | 3 |
| Ложноотрицательный | 4 | 12 | 6 |
| Чувствительность (%) | 77.8 | 64,7 | 82,3 |
| Специфичность (%) | 86,4 | 81,2 | 93,8 |
| Точность (%) | 82,5 | 74,4 | 89,0 |
| A Z Значения ± SD | 0,9281 ± 0,0455 | 0,8833 ± 0,0400 | 0,9687 ± 0,0168 |
Диагностика обструктивных причин
Суммарная точность MRCP в диагностике причин панкреатобилиарной обструкции составила 75.6%, что было аналогично прямой холангиопанкреатографии (ERCP / PTC) ( P = 0,2345) и CT ( P = 0,7970), но лучше, чем у B-US ( P = 0,0131). Комбинация MRCP и рутинной МРТ значительно улучшила возможности клинической диагностики с точностью 87,8%, что превосходит таковую КТ ( P = 0,0330) и УЗИ ( P = 0,0000).
Частота диагностики при комбинации MRCP и рутинной МРТ составила 92.1% и 94,1% для холелита и холедохолитиаза соответственно, что было лучше, чем у CT ( P = 0,0428) и US ( P = 0,0049). Но разница между ERCP / PTC и комбинированной MRCP и рутинной МРТ не была значительной ( P = 0,6445). Точность КТ, ERCP / PTC, MRCP и комбинированной MRCP и рутинной МРТ визуализации в различении различных панкреатобилиарных опухолей была значительно выше, чем у УЗИ ( P = 0,0002) (таблица).
Таблица 4
Точность диагностики причин обструкции (%)
| B-US | CT | ERCP / PTC | MRCP | MRCP + MRI | |||
| Холелитиаз | |||||||
| Камень желчного пузыря | 71,4 | 75,0 | 80,0 | 78,5 | 92,9 | ||
| Камень внутрипеченочного желчного протока | 85.7 | 100,0 | 100,0 | 71,4 | 85,7 | ||
| Холедохолитиаз | 52,9 | 63,6 | 87,5 | 88,2 | 94,1 | ||
| Рак поджелудочной железы и желчного пузыря | |||||||
| Желчный рак | |||||||
| Желчный пузырь | 75,0 | 60,0 | 50,0 | 66,7 | |||
| Холангиокарцинома | 33,3 | 75,0 | 83.3 | 77,8 | 88,9 | ||
| Ампуллярная карцинома | 33,3 | 50,0 | 100,0 | 66,7 | 66,7 | ||
| Рак головки поджелудочной железы | 63,6 | 81,8 | 100,062 | 63,6 | 81,8 | 100,062 | |
| Рак желчного сосочка | 40,0 | 66,7 | 100,0 | 60,0 | 80,0 | ||
| Другие заболевания | |||||||
| Повреждение желчного протока | 50.0 | 100,0 | 100,0 | 100,0 | |||
| Киста холедоха | 100,0 | 100,0 | 100,0 | 100,0 | 100,0 | ||
| Склерозирующий холангит | 0 | 50,062 | 0 | 0 | 50,0 | ||
| Хронический панкреатит | 75,0 | 75,0 | 100,0 | 50,0 | 75,0 | ||
| Всего | 57.3 | 73,7 | 85,0 | 75,6 | 87,8 |
ОБСУЖДЕНИЕ
УЗИ или компьютерная томография (включая эндоскопическое УЗИ и спиральную компьютерную томографию) было первым методом диагностики заболеваний поджелудочной железы и желчных путей [6-9] . Прямая холангиопанкреатография, полученная с помощью ERCP или PTC, служит «золотым стандартом» в панкреатобилиарной имиджелогии.
Магнитно-резонансная холангиопанкреатография (MRCP), предложенная немецким исследователем Валлнером Б.К. и его группой в 1991 году [10], предложила новый метод визуализации для диагностики нарушений панкреатобилиарной системы [10-15].В настоящем исследовании MRCP была успешно выполнена у всех 82 пациентов, и изображения MRCP были аналогичны изображениям прямой холангиопанкреатографии. Исследования диагностического качества MRCP были получены в 79 случаях (96,3%), в том числе в 8 (16,7%) случаях прямая холангиопанкреатография была неудачной или неполной. Таким образом, MRCP может стать эффективной альтернативой прямой холангиопанкреатографии, когда диагностические ERCP и PTC оказались безуспешными или неадекватными [1,16].
В нашем исследовании точность MRCP в определении локализации панкреатобилиарной обструкции составила 100%, что превосходит точность B-US и CT, но существенно не различается между MRCP и прямой холангиопанкреатографией.По сравнению с обследованием ERCP / PTC, неинвазивный MRCP может показать всю систему панкреатобилиарного протока и продемонстрировать уровень, степень и диапазон обструкции, а также морфологические характеристики. Кроме того, MRCP может предоставить много ценной имиджологической информации и помочь определить лучший подход к паллиативному дренированию и другому интервенционному лечению пациентов с неоперабельными опухолями [17,18].
В имиджелогии панкреато-билиарной системы это очень важно для диагностики и дифференциации злокачественных и доброкачественных причин панкреато-билиарной обструкции.Комбинация MRCP и рутинной MR-визуализации может значительно улучшить возможности клинической диагностики за счет выявления патологических изменений окружающих структур [19–22]. Для панкреатобилиарных опухолей MRCP может определить местоположение и морфологические характеристики панкреатобилиарной обструкции, а также оценить диапазон поражения опухолей и хирургическую резектабельность. Кроме того, с преимуществами КТ и прямого холангиопанкреатографического исследования, комбинированная рутинная МРТ и MRCP могут выявить соответствующие окружающие структуры и повысить точность клинической диагностики [17,23,24].
Методы УЗИ и КТ наиболее часто используются при первичной оценке пациентов с желчнокаменной болезнью, и оба обладают высокой точностью диагностики камней в желчном пузыре и внутрипеченочных протоков. Чувствительность MRCP в диагностике камней желчного пузыря и внутрипеченочных протоков варьировалась в зависимости от размера, количества и расположения камней, а MRCP больше подходил для диагностики холедохолитиаза. Таким образом, MRCP может в основном обнаружить камни в общем желчном протоке и исключить другие панкреатобилиарные обструктивные заболевания [25–27].
С развитием лапароскопической техники лапароскопическая холецистэктомия (LC) и эндоскопическая тенотомия сфинктера (EST) стали широко использоваться в хирургии желчевыводящих путей [28]. MRCP может отобразить всю анатомическую структуру желчного дерева и помочь гарантировать успех лапароскопической холецистэктомии. Перед хирургическим вмешательством определение анатомических вариантов желчного дерева с помощью MRCP может привести к снижению риска повреждения желчного протока во время лапароскопической холецистэктомии [29]. Теперь ЭРХПГ больше не является рутинным обследованием пациентов с холедохолитиазом, и вместо этого в основном используется эндоскопическая тенотомия сфинктера для удаления камней в общем желчном протоке.
Что касается доброкачественных стриктур, вызванных холангитом, хирургической травмой или хроническим панкреатитом, MRCP может иметь некоторые трудности с отображением миниатюрных изменений панкреатобилиарного протока. Но использование динамического MRCP со стимуляцией секретином может быть полезным для диагностики папиллярного стеноза или дисфункции поджелудочной железы, а также для обнаружения пониженного экзокринного резерва поджелудочной железы [30–32]. Кроме того, в литературе указывается, что MRCP можно использовать на начальном этапе для оценки кисты холедоха [33].
В заключение, в недавних оптимальных имиджелогических процедурах диагностики заболеваний поджелудочной железы B-US по-прежнему является первым выбором для оценки.Комбинация MRCP и рутинной МРТ обеспечивает эффективный метод диагностики различных панкреатобилиарных обструкций, дифференциации злокачественных и доброкачественных причин и проведения послеоперационного наблюдения. МРТ и КТ поперечного сечения являются дополнительными методами для предоперационной диагностики и оценки опухолей поджелудочной железы. Прямая диагностическая холангиопанкреатография (ERCP / PTC) в основном используется в сложных случаях и сочетается с другим интервенционным лечением, включая EST или PTCD (рисунок).
Оптимальная методика имиджелогического исследования заболеваний поджелудочной железы.
Визуализирующая диагностика заболеваний поджелудочной железы: контрольное исследование
Резюме
ЦЕЛЬ: Оценить клиническую ценность различных имиджелогических методов диагностики заболеваний поджелудочной железы и желчевыводящих путей и найти оптимальную процедуру.
МЕТОДЫ: Проанализировано 82 случая заболеваний поджелудочной железы и желчевыводящих путей, подтвержденных хирургическим путем и патологией. Было 38 случаев холелитиаза, 34 случая панкреатобилиарных опухолей и 10 других случаев.Имиджелогические методы включали B-US, CT, ERCP, PTC, поперечную МРТ и МР-холангиопанкреатографию (MRCP).
РЕЗУЛЬТАТЫ: Степень точности MRCP в определении местоположения панкреатобилиарной обструкции составила 100%. При дифференцировании злокачественной обструкции от доброкачественной чувствительность комбинации MRCP и поперечной МРТ составила 82,3%, специфичность – 93,8%, а уровень точности – 89,0%. Степень точности определения характера обструкции составила 87,8%, что выше, чем у B-US ( P = 0.0000) и КТ ( P = 0,0330), но не было существенной разницы между прямой холангиопанкреатографией и комбинацией MRCP и традиционной МРТ ( P = 0,6666).
ВЫВОД: В большинстве случаев MRCP может заменить прямую холангиопанкреатографию для диагностики. Комбинация MRCP и поперечной МРТ должна рассматриваться как важное средство диагностики заболеваний поджелудочной железы и желчевыводящих путей, предоперационной оценки и послеоперационного наблюдения.
ВВЕДЕНИЕ
Панкреатобилиарные расстройства – распространенные заболевания, при которых часто поражается желчная система, вызывая симптомы механической желтухи.Это предварительное условие для исследования места обструкции и причин заболеваний поджелудочной железы и желчевыводящих путей. В данном исследовании проанализировано 82 случая заболеваний поджелудочной железы, подтвержденных хирургическим вмешательством и патологией. Цели проспективного исследования заключались в оценке клинической ценности различных имиджелогических методов в диагностике заболеваний поджелудочной железы и желчевыводящих путей и в поиске оптимальной процедуры обследования.
МАТЕРИАЛЫ И МЕТОДЫ
Пациенты
Объектами исследования были 82 пациента (54 мужчины и 28 женщин, средний возраст 60 лет.0 лет, от 11 до 82 лет), 67 (81,7%) случаев имели симптом механической желтухи. Все пациенты прошли B-US, MR холангиопанкреатографию (MRCP) и поперечное МРТ. Пятьдесят семь пациентов прошли КТ с усилением или без него. Кроме того, 48 пациентам была проведена прямая холангиопанкреатография (41 ERCP и 7 PTC). Однако прямая холангиопанкреатография была безуспешной в 4 случаях из-за трудностей с канюляцией (2 ERCP), постгастроэнтеростомии (1 ERCP) и больного пациента (1 PTC).ЭРХПГ была неполной в других 4 случаях, потому что можно было увидеть только проток поджелудочной железы, а желчное дерево не было помутнено. Таким образом, во всех 82 случаях было выполнено 40 прямых холангиопанкреатографий (34 ERCP и 6 PTC), у 1 пациента было осложнение острого панкреатита после ERCP. Все пациенты с заболеваниями поджелудочной железы и желчевыводящих путей были подтверждены хирургическими данными и патологией, в том числе 12 – лапароскопической холецистэктомией (LC), 6 – эндоскопической тенотомией сфинктера (EST) и 1 – дренажом PTC (PTCD).Из 82 случаев у 38 был диагностирован холелитиаз, у 34 – панкреатобилиарные опухоли и у 10 – другие заболевания (таблица).
Таблица 1
Заболевания поджелудочной железы ( n = 82)
| Заболевания поджелудочно-желчных путей | Число случаев |
| Холелитиаз a | 38 |
| Камень желчного пузыря | 14 |
| Камень внутрипеченочного желчного протока | 7 |
| Холедохолитиаз | 17 |
| Панкреатобилиарная опухоль b | 34 |
| Желчный рак | |
| Холангиокарцинома | 9 |
| Ампуллярная карцинома | 3 |
| Карцинома головки поджелудочной железы | 11 |
| Карцинома желчного сосочка | 5 |
| 2 | |
| Киста холедоха | 2 |
| Склерозирующий холангит | 2 |
| Хронический панкреатит | 4 |
Методы
МРТ-визуализация выполнялась с 1.0T сверхпроводящий блок (Philips Gyroscan T10-NT, версия программного обеспечения 4.6.2), содержащий катушку для тела. Пациенты были обследованы в положении лежа на спине, спокойном дыхании и компрессии бандажом. Сначала были выполнены стандартные аксиальные исследования T1WI, T2WI и коронарного T2WI в верхней части живота с использованием последовательности Turbo Spin-Echo (TSE), а за ними последовали дополнительные аксиальные T2WI и / или T1WI последовательности с подавлением жира (восстановление с инверсией спектрального насыщения, SPIR). Стандартные аксиальные изображения служили ориентирами для определения местоположения МР-холангиопанкреатографии (MRCP).MRCP выполняли с коронарной, мультиспиральной, сильно взвешенной T2-последовательностью TSE (TR = 2000 мс, TE = 700 мс). Для уменьшения артефакта дыхательного движения использовалась техника без задержки дыхания. Исходные изображения MRCP были трехмерно (3D) реконструированы с использованием алгоритма проекции максимальной интенсивности (MIP). Общее время визуализации составляло примерно 30 мин.
Для компьютерной томографии (КТ) использовался компьютерный томограф всего тела (Picker PQ-2000). Все КТ-исследования проводились после того, как пациенты голодали в течение 4-8 часов и принимали пероральный контраст 500-1000 мл (0.5% -1% меглумина диатризоат) перед компьютерной томографией. При усиленном КТ-исследовании использовалось 80–100 мл неионных внутривенных контрастных веществ, вводимых через анекубитальную вену болюсно со скоростью 2–3 мл / с.
Прямая холангиопанкреатография (ERCP и PTC) выполнялась с помощью цифрового устройства визуализации (Philips Diagnost 93).
Анализ изображений
Все данные изображений 82 пациентов были тщательно изучены, чтобы выявить увеличение или стриктуру панкреатобилиарного тракта. Протокол исследования включал обнаружение обструктивных участков, различение злокачественных и доброкачественных причин и оценку клинической ценности различных методов визуализации (включая B-US, CT, MRCP, ERCP / PTC) при диагностике заболеваний поджелудочной железы и желчевыводящих путей.Программное обеспечение SAS использовалось для всех статистических анализов.
Диагностические принципы и критерии оценки для прямой холангиопанкреатографии и MRCP были идентичны, но в MRCP было более важно тщательно изучить как исходные изображения, так и изображения, реконструированные MIP. По результатам расширения или стриктуры панкреатобилиарного дерева и желчного пузыря обструктивные места панкреатобилиарного протока были разделены на три части: внутрипеченочный или внепеченочный желчный проток и главный панкреатический проток.Нормальный желчный пузырь 7-10 см в длину и 3-4 см в ширину. Расширение общего желчного протока определялось как более 8 мм в максимальном диаметре у пациентов без холецистэктомии в анамнезе и 10 мм у пациентов, перенесших холецистэктомию в анамнезе. Расширение внутрипеченочного желчного протока и главного протока поджелудочной железы было определено как более 3 мм в максимальном диаметре [1-4].
Причина панкреатобилиарной аномалии оценивалась с использованием пятибалльной шкалы для определения уровня достоверности: 1.определенно доброкачественная, 2. вероятно доброкачественная, 3. неопределенная, 4. вероятно злокачественная и 5. определенно злокачественная [5]. Если предполагалось, что причиной панкреатобилиарной аномалии является злокачественная, причины выбирались на основании следующих данных: визуализация опухоли, признак двойного протока, резкая обструкция желчного протока, неровность закупоренного края или асимметричная обструкция дистального края расширенный желчный проток. Анализ кривой рабочих характеристик приемника (ROC) был выполнен для сравнения результатов считывания изображений MRCP с результатами считывания комбинации изображений MRCP и стандартных изображений MR, а также с результатами считывания изображений ERCP.Бинормальные кривые ROC были подобраны с использованием программного обеспечения ROCKIT 0.9B . Диагностические возможности определялись путем расчета площади под кривой ROC (Az). Оценка 1 или 2 указала на доброкачественное поражение, оценки 4 или 5 указали на оценку злокачественного поражения. Считалось, что оценка 3 указывает на неопределенный диагноз. Были рассчитаны чувствительность, специфичность и точность ERCP, MRCP и комбинации MRCP и рутинной МРТ для дифференциации злокачественных и доброкачественных причин обструкции панкреатобилиарного тракта.
РЕЗУЛЬТАТЫ
Качество изображения MRCP
МР-холангиопанкреатография была успешно выполнена у всех 82 пациентов, и изображения MRCP были аналогичны изображениям прямой холангиопанкреатографии. MRCP-исследования диагностического качества были получены у 79 (96,3%) пациентов с тонким контрастом между панкреатобилиарной структурой и окружающим фоном. У остальных 3 пациентов с панкреатобилиарной опухолью наличие асцитической жидкости в верхней части живота и содержащих жидкость органов из-за непроходимости желудочно-кишечного тракта затрудняло визуализацию панкреатобилиарного дерева и ухудшало качество изображения MRCP.У 8 (16,7%) пациентов, у которых прямая холангиопанкреатография была неудачной или неполной, все исследования MRCP были успешными, а изображения MRCP были удовлетворительными.
Диагноз обструктивной локализации
Среди 82 пациентов с панкреатобилиарными заболеваниями 8, 60 и 21 случай имели панкреатобилиарные обструктивные участки во внутрипеченочном, внепеченочном желчном протоке и главном панкреатическом протоке, соответственно (всего 89 локализаций). ). MRCP может четко визуализировать расширение панкреатобилиарных протоков выше обструктивного уровня в их естественном состоянии, что делает его более подходящим для демонстрации обструкции внепеченочных желчных протоков.Общая точность MRCP в определении местоположения панкреато-билиарной обструкции составила 100%, что превосходит точность B-US ( P = 0,0002) и CT ( P = 0,0422), но не было никаких признаков. Это различие между MRCP и прямой холангиопанкреатографией ( P = 0,1487) (таблица).
Таблица 2
Точность уровня панкреато-билиарной обструкции (%) разными имиджелогическими методами
| Уровень | Внутрипеченочный | Внепеченочный | Основная поджелудочная железа | Всего |
| B-US | 100.0 (8/8) | 81,7 (49/60) | 90,5 (19/21) | 85,4 (76/89) |
| CT | 100,0 (4/4) | 93,0 (40/43 ) | 100,0 (19/19) | 95,5 (63/66) |
| ERCP / PTC | 100,0 (5/5) | 96,7 (29/30) | 100,0 (8/8) | 97,7 (42/43) |
| MRCP | 100,0 (8/8) | 100,0 (60/60) | 100,0 (21/21) | 100,0 (89/89) |
злокачественный из доброкачественной обструкции
Чувствительность, специфичность и точность MRCP в различении злокачественных и доброкачественных причин панкреатобилиарной обструкции составила 64.7%, 81,2% и 74,4% соответственно, в то время как показатели ERCP / PTC составили 77,8%, 86,4% и 82,5% соответственно. Разница не была значимой между MRCP и ERCP / PTC в области Az под кривой ROC ( P = 0,4590). Комбинация MRCP и рутинной МРТ, очевидно, может улучшить диагностические возможности по дифференциации причин панкреатобилиарной обструкции с чувствительностью 82,3%, специфичностью 93,8% и точностью 89,0%. Разница была значительной между MRCP и комбинацией MRCP и рутинной МРТ ( P = 0.0489) (таблица и рисунок).
Анализ кривой ROC для дифференциации злокачественных и доброкачественных причин панкреатобилиарной обструкции.
Таблица 3
ROC-анализ панкреато-билиарной обструкции
| ERCP / PTC ( n = 40) | MRCP ( n = 82) | MRCP + MRI ( n = 82) | |
| Истинно-положительный | 14 | 22 | 28 |
| Истинно-отрицательный | 19 | 39 | 45 |
| Ложно-положительный | 3 | 9 | 3 |
| Ложноотрицательный | 4 | 12 | 6 |
| Чувствительность (%) | 77.8 | 64,7 | 82,3 |
| Специфичность (%) | 86,4 | 81,2 | 93,8 |
| Точность (%) | 82,5 | 74,4 | 89,0 |
| A Z Значения ± SD | 0,9281 ± 0,0455 | 0,8833 ± 0,0400 | 0,9687 ± 0,0168 |
Диагностика обструктивных причин
Суммарная точность MRCP в диагностике причин панкреатобилиарной обструкции составила 75.6%, что было аналогично прямой холангиопанкреатографии (ERCP / PTC) ( P = 0,2345) и CT ( P = 0,7970), но лучше, чем у B-US ( P = 0,0131). Комбинация MRCP и рутинной МРТ значительно улучшила возможности клинической диагностики с точностью 87,8%, что превосходит таковую КТ ( P = 0,0330) и УЗИ ( P = 0,0000).
Частота диагностики при комбинации MRCP и рутинной МРТ составила 92.1% и 94,1% для холелита и холедохолитиаза соответственно, что было лучше, чем у CT ( P = 0,0428) и US ( P = 0,0049). Но разница между ERCP / PTC и комбинированной MRCP и рутинной МРТ не была значительной ( P = 0,6445). Точность КТ, ERCP / PTC, MRCP и комбинированной MRCP и рутинной МРТ визуализации в различении различных панкреатобилиарных опухолей была значительно выше, чем у УЗИ ( P = 0,0002) (таблица).
Таблица 4
Точность диагностики причин обструкции (%)
| B-US | CT | ERCP / PTC | MRCP | MRCP + MRI | |||
| Холелитиаз | |||||||
| Камень желчного пузыря | 71,4 | 75,0 | 80,0 | 78,5 | 92,9 | ||
| Камень внутрипеченочного желчного протока | 85.7 | 100,0 | 100,0 | 71,4 | 85,7 | ||
| Холедохолитиаз | 52,9 | 63,6 | 87,5 | 88,2 | 94,1 | ||
| Рак поджелудочной железы и желчного пузыря | |||||||
| Желчный рак | |||||||
| Желчный пузырь | 75,0 | 60,0 | 50,0 | 66,7 | |||
| Холангиокарцинома | 33,3 | 75,0 | 83.3 | 77,8 | 88,9 | ||
| Ампуллярная карцинома | 33,3 | 50,0 | 100,0 | 66,7 | 66,7 | ||
| Рак головки поджелудочной железы | 63,6 | 81,8 | 100,062 | 63,6 | 81,8 | 100,062 | |
| Рак желчного сосочка | 40,0 | 66,7 | 100,0 | 60,0 | 80,0 | ||
| Другие заболевания | |||||||
| Повреждение желчного протока | 50.0 | 100,0 | 100,0 | 100,0 | |||
| Киста холедоха | 100,0 | 100,0 | 100,0 | 100,0 | 100,0 | ||
| Склерозирующий холангит | 0 | 50,062 | 0 | 0 | 50,0 | ||
| Хронический панкреатит | 75,0 | 75,0 | 100,0 | 50,0 | 75,0 | ||
| Всего | 57.3 | 73,7 | 85,0 | 75,6 | 87,8 |
ОБСУЖДЕНИЕ
УЗИ или компьютерная томография (включая эндоскопическое УЗИ и спиральную компьютерную томографию) было первым методом диагностики заболеваний поджелудочной железы и желчных путей [6-9] . Прямая холангиопанкреатография, полученная с помощью ERCP или PTC, служит «золотым стандартом» в панкреатобилиарной имиджелогии.
Магнитно-резонансная холангиопанкреатография (MRCP), предложенная немецким исследователем Валлнером Б.К. и его группой в 1991 году [10], предложила новый метод визуализации для диагностики нарушений панкреатобилиарной системы [10-15].В настоящем исследовании MRCP была успешно выполнена у всех 82 пациентов, и изображения MRCP были аналогичны изображениям прямой холангиопанкреатографии. Исследования диагностического качества MRCP были получены в 79 случаях (96,3%), в том числе в 8 (16,7%) случаях прямая холангиопанкреатография была неудачной или неполной. Таким образом, MRCP может стать эффективной альтернативой прямой холангиопанкреатографии, когда диагностические ERCP и PTC оказались безуспешными или неадекватными [1,16].
В нашем исследовании точность MRCP в определении локализации панкреатобилиарной обструкции составила 100%, что превосходит точность B-US и CT, но существенно не различается между MRCP и прямой холангиопанкреатографией.По сравнению с обследованием ERCP / PTC, неинвазивный MRCP может показать всю систему панкреатобилиарного протока и продемонстрировать уровень, степень и диапазон обструкции, а также морфологические характеристики. Кроме того, MRCP может предоставить много ценной имиджологической информации и помочь определить лучший подход к паллиативному дренированию и другому интервенционному лечению пациентов с неоперабельными опухолями [17,18].
В имиджелогии панкреато-билиарной системы это очень важно для диагностики и дифференциации злокачественных и доброкачественных причин панкреато-билиарной обструкции.Комбинация MRCP и рутинной MR-визуализации может значительно улучшить возможности клинической диагностики за счет выявления патологических изменений окружающих структур [19–22]. Для панкреатобилиарных опухолей MRCP может определить местоположение и морфологические характеристики панкреатобилиарной обструкции, а также оценить диапазон поражения опухолей и хирургическую резектабельность. Кроме того, с преимуществами КТ и прямого холангиопанкреатографического исследования, комбинированная рутинная МРТ и MRCP могут выявить соответствующие окружающие структуры и повысить точность клинической диагностики [17,23,24].
Методы УЗИ и КТ наиболее часто используются при первичной оценке пациентов с желчнокаменной болезнью, и оба обладают высокой точностью диагностики камней в желчном пузыре и внутрипеченочных протоков. Чувствительность MRCP в диагностике камней желчного пузыря и внутрипеченочных протоков варьировалась в зависимости от размера, количества и расположения камней, а MRCP больше подходил для диагностики холедохолитиаза. Таким образом, MRCP может в основном обнаружить камни в общем желчном протоке и исключить другие панкреатобилиарные обструктивные заболевания [25–27].
С развитием лапароскопической техники лапароскопическая холецистэктомия (LC) и эндоскопическая тенотомия сфинктера (EST) стали широко использоваться в хирургии желчевыводящих путей [28]. MRCP может отобразить всю анатомическую структуру желчного дерева и помочь гарантировать успех лапароскопической холецистэктомии. Перед хирургическим вмешательством определение анатомических вариантов желчного дерева с помощью MRCP может привести к снижению риска повреждения желчного протока во время лапароскопической холецистэктомии [29]. Теперь ЭРХПГ больше не является рутинным обследованием пациентов с холедохолитиазом, и вместо этого в основном используется эндоскопическая тенотомия сфинктера для удаления камней в общем желчном протоке.
Что касается доброкачественных стриктур, вызванных холангитом, хирургической травмой или хроническим панкреатитом, MRCP может иметь некоторые трудности с отображением миниатюрных изменений панкреатобилиарного протока. Но использование динамического MRCP со стимуляцией секретином может быть полезным для диагностики папиллярного стеноза или дисфункции поджелудочной железы, а также для обнаружения пониженного экзокринного резерва поджелудочной железы [30–32]. Кроме того, в литературе указывается, что MRCP можно использовать на начальном этапе для оценки кисты холедоха [33].
В заключение, в недавних оптимальных имиджелогических процедурах диагностики заболеваний поджелудочной железы B-US по-прежнему является первым выбором для оценки.Комбинация MRCP и рутинной МРТ обеспечивает эффективный метод диагностики различных панкреатобилиарных обструкций, дифференциации злокачественных и доброкачественных причин и проведения послеоперационного наблюдения. МРТ и КТ поперечного сечения являются дополнительными методами для предоперационной диагностики и оценки опухолей поджелудочной железы. Прямая диагностическая холангиопанкреатография (ERCP / PTC) в основном используется в сложных случаях и сочетается с другим интервенционным лечением, включая EST или PTCD (рисунок).
Оптимальная методика имиджелогического исследования заболеваний поджелудочной железы.
Хирургия печени, поджелудочной железы и желчевыводящей системы
Новые диагностические и хирургические возможности для состояний HPB означают, что доступны лучшие варианты лечения для терминальной стадии заболевания печени, злокачественных опухолей печени, доброкачественных опухолей и кист печени и поджелудочной железы, рака поджелудочной железы , и опухоли желчного пузыря. Другие состояния включают повреждения и стриктуры желчных протоков, доброкачественные опухоли и кисты, а также воспаление желчных протоков.
Групповой подходОперация HPB очень сложна, как и подготовка и координация, необходимые между хирургом и другими членами общей медицинской бригады. Гастроэнтеролог обычно является первым врачом, который обнаруживает рак поджелудочной железы или печени – будь то с помощью различных типов обследований или сложных процедур желудочно-кишечного тракта. Хирург HPB, врачи и онкологи-радиологи работают вместе, чтобы определить правильную комбинацию хирургического вмешательства и химиотерапии, необходимую человеку для наиболее эффективного лечения.Радиологи также играют жизненно важную роль, потому что они оценивают и / или ставят первоначальный диагноз на основе результатов обследований.
«Я посещаю несколько междисциплинарных онкологических конференций, где врачи собираются вместе, чтобы составить план лечения для каждого человека. Вместе мы работаем, чтобы определить последовательность лечения, которая будет наиболее эффективной », – говорит доктор Дауден. «Тип рака, физическое состояние человека и другие факторы являются частью дискуссии о том, проводим ли мы операцию до или после химиотерапии.Оценивается каждый человек и его индивидуальное состояние, потому что никогда не бывает универсального подхода ».
Когда доктор Дауден обдумывал, какую специальность ему выбрать, ему понравились вызовы и продуманное планирование, которые входят в каждую операцию HPB, которую он выполняет. Он также хотел чувствовать себя уверенно при проведении любых операций на брюшной полости, которые могут понадобиться его пациентам. Многим пациентам доктора Даудена был поставлен диагноз рака поджелудочной железы, и он подчеркивает, что этот диагноз не является автоматическим смертным приговором.
«Существует распространенное заблуждение, что рак поджелудочной железы является смертельным исходом для всех, но это не так. Этот рак трудно поддается лечению, но у нас есть много новых способов подойти к нему агрессивным и безопасным способом », – говорит доктор Дауден. «Не существует процедур HPB или рака поджелудочной железы, требующих поездки в Нэшвилл или Атланту. Для меня важно, чтобы люди знали, что самые современные операции и методы лечения рака доступны прямо здесь, в Чаттануге. Это то, чему меня научили, и я люблю давать людям возможность жить дольше и здоровее.
Чтобы увидеть профиль доктора Даудена, щелкните здесь. Чтобы назначить встречу с доктором Дауденом, позвоните по телефону (423) 267-0466.
Гепато-панкреат-билиарная хирургия (HPB) | TriHealth
Что такое гепато-панкреато-билиарная хирургия?
Хирургия HPB (гепато-панкреатико-билиарная) – это специальность хирургии, специфичная для доброкачественных и злокачественных заболеваний печени, поджелудочной железы и желчевыводящих путей. Хирургия HPB может быть сложной и требует специальной подготовки и / или опыта.TriHealth разработал свою программу хирургии HPB с целью предоставления современных и высококачественных услуг нашим пациентам и их семьям. Мы стремимся оказывать помощь многопрофильным образом. Это означает сотрудничество с нашими хирургами, практикующими медсестрами, специалистами в области гастроэнтерологии (GI), интервенционной радиологии (IR), медицинской онкологии, радиационной онкологии, генетики, питания и многого другого. Как пациент в программе хирургии HPB, вы имеете доступ ко всем этим услугам и специалистам.
Услуги хирургической программы HPB
- Индивидуальные планы ухода для каждого пациента
- Использование доказательных клинических методов для ускоренного выздоровления
- Многопрофильная помощь через:
- Многопрофильные клиники (MDC):
Иногда операция является лишь частью плана лечения; особенно, когда операция предназначена для лечения рака.Многопрофильные клиники предназначены для пациентов, которым может потребоваться дополнительное консервативное лечение до или после операции. Во время этих посещений в клинике пациенты могут посещать хирургических и нехирургических специалистов одновременно и в одном месте. Это позволяет нам составить комплексный и комплексный план лечения. - Конференции Совета по опухолям:
Принятие хирургических решений часто требует участия других специалистов.Совещания совета по опухолям – это возможность для всех специалистов, занимающихся лечением пациентов, собраться вместе, подробно рассмотреть случай пациента и разработать комплексный план лечения.
- Многопрофильные клиники (MDC):
- Диетологи
- Советники по генетике
- Исследования
- Велнес-программы до и после операции
- Планы лечения для выживших
Хирургические процедуры HPB
Комплексные операции на печени, поджелудочной железе и желчных путях, включая, но не ограничиваясь:
- Резекция печени (большая и малая)
- Удаление опухоли печени
- Резекция поджелудочной железы по поводу доброкачественных и злокачественных заболеваний (включая процедуру Уиппла)
- Резекция желчного протока
- Ремонт желчных протоков
- Комплексная резекция желчного пузыря
Все эти хирургические процедуры (включая обширные операции на поджелудочной железе и процедуру Уиппла) могут быть выполнены минимально инвазивным способом, когда это целесообразно, с использованием роботизированных или лапароскопических хирургических методов.
Самые современные возможности для вашего ухода
Программа хирургии HPB была разработана для оказания расширенной хирургической помощи пациентам со злокачественными или доброкачественными заболеваниями печени, поджелудочной железы и желчевыводящей системы. Программа HPB TriHealth использует междисциплинарный подход для предоставления индивидуализированных, современных планов лечения и высококачественного ухода.
Под руководством Хирургического института TriHealth Томаса Мейнарда, MD FACS, Erik Dunki-Jacobs, MD FACS и Дэвида Ли, MD , хирургическая бригада HPB специализируется на выполнении сложных хирургических процедур HPB минимально инвазивным способом.TriHealth – единственный региональный центр, предоставляющий услуги роботизированной хирургии HPB, и его хирурги считаются лидерами в этой области.
Посмотреть видео:
Познакомьтесь с нашей командой
Ведущие хирурги HPB TriHealth обладают более чем 45-летним опытом проведения сложных операций HPB и заявляют о том, что уровень серьезных осложнений является одним из самых низких в стране.
Помимо хирургов, в группу по уходу за HPB входят пациенты, практикующие медсестры, медсестры, фармацевты, фельдшеры, диетологи и другие медицинские работники.
Thomas C. Maynard MD FACS специализируется на хирургии поджелудочной железы и сложных желчных путях более 30 лет. В рамках программы хирургии HPB он преуспевает в традиционной открытой и малоинвазивной хирургии желчного пузыря, поджелудочной железы, верхних и нижних отделов желудочно-кишечного тракта.Его результаты в хирургии поджелудочной железы ставят его на первое место в стране. Он был первым в регионе, кто предложил минимально инвазивную хирургию поджелудочной железы, и получил награду «Выдающийся робот-хирург да Винчи» от журнала Intuitive в 2015 году. Доктор Мейнард неизменно входит в число лучших врачей в области панкреатической и общей хирургии, как сообщает Журнал Цинциннати. |
Эрик М.Dunki-Jacobs MD – онколог-хирург, прошедший стажировку, специализирующийся на поджелудочной железе, хирургии печени и хирургии верхних отделов желудочно-кишечного тракта. Он является лидером в области малоинвазивных и роботизированных хирургических техник. Он постоянно упоминается в журнале Cincinnati Magazine как один из «лучших документов» в этой области. |
Дэвид Ю.Ли MD – онколог-хирург, прошедший стажировку, с богатым опытом исследований в области лечения самых разных видов рака. Он использует одни из самых передовых доступных технологий с использованием минимально инвазивных процедур. Доктор Ли получил награды Общества хирургической онкологии за выдающиеся клинические и исследовательские достижения и был признан благотворительным фондом Гарольда Макалистера во время обучения в Институте рака Джона Уэйна. Он исследовал и опубликовал малоинвазивные методы хирургии печени, а также опубликовал материалы о влиянии предоперационной химиолучевой терапии и возраста на операцию на поджелудочной железе.Доктор Ли имеет сертификат в области комплексной общей хирургической онкологии и общей хирургии. |
Сара Патри NP – сертифицированная практикующая медсестра, специализирующаяся на ведении пациентов с HPB. Ее роль заключается в обеспечении как стационарной, так и амбулаторной клинической поддержки. |
Мария Холмс LPN работает с доктором Дунки-Джейкобс в амбулаторных условиях. Она отвечает за повседневное управление его офисом и тесно сотрудничает с его пациентами и их семьями, чтобы обеспечить удовлетворение их потребностей. |
Эйлин Скиано LPN работала непосредственно с доктором Мейнардом в качестве его фельдшера в амбулаторных условиях более 20 лет. Она отвечает за повседневное управление его кабинетом, планирование операций и тесно работает с пациентами и их семьями до и после операции. |
Кэти Витте LPN – навигатор по специальности, лицензированная практическая медсестра, которая работает в многопрофильных клиниках, объединяя пациентов HPB с другими специалистами, которые могут быть вовлечены в их лечение. |
Хирургические ординаторы. TriHealth гордится тем, что по программе общей хирургической ординатуры обучается следующее поколение хирургов. Доктора Мэйнард, Данки-Джейкобс и Ли работают преподавателями этой программы и участвуют в очном обучении. Скорее всего, хирургический ординатор будет участвовать в вашем послеоперационном уходе под непосредственным наблюдением доктора. Мейнард и Дунки-Джейкобс.
.

 Стабильность при широкой экспозиции и асимметричной ретракции реберного края.
Стабильность при широкой экспозиции и асимметричной ретракции реберного края.