Поджелудочная железа эхогенность повышена что это: подготовка, расшифровка результатов, норма размеров и эхогенности
Ультразвуковая диагностика | РЕАЛМЕД
Ультразвуковая диагностика – распознавание патологических изменений органов и тканей организма с помощью ультразвука. Основана на принципе эхолокации — приёме сигналов посланных, а затем отражённых от поверхностей раздела тканевых сред, обладающих различными акустическими свойствами.
Метод ультразвуковой диагностики широко распространён во всём мире, благодаря его безопасности, безвредности и высокой информативности.В настоящее время ультразвуковая диагностика стала всеобъемлющей, часто первичной, скрининговой и, в некоторых случаях, окончательной методикой диагностики, а порой, даже, единственной в постановке диагноза.
Ультразвуковое исследование (эхография, сонография) относится к неионизирующим методам исследования. Благодаря простоте выполнения, безвредности, высокой информативности оно получило широкое распространение в клинической практике. В ряде случаев ультразвукового исследования бывает достаточно для установления диагноза, в других — ультразвук используется наряду с прочими (рентгенологическими, радионуклидными) методами.
Ультразвуковые волны легко распространяются в упругих средах и отражаются на границе различных слоев в зависимости от изменения акустического сопротивления среды. Чем больше акустическое сопротивление исследуемой ткани, тем интенсивнее она отражает ультразвуковые сигналы, тем светлее исследуемый участок выглядит на сканограмме. Отражение участком ткани ультразвуковых сигналов сильнее, чем в норме, определяют терминами «повышенная эхогенность», или «усиленная эхоструктура». Наибольшей эхогенностью обладают конкременты желчных путей, поджелудочной железы, почек и др. Их акустическое сопротивление может быть настолько велико, что они совершенно не пропускают ультразвуковые сигналы, полностью отражая их. На сканограммах такие образования имеют белый цвет, а позади них располагается черного цвета «акустическая дорожка», или тень конкремента, — зона, в которую сигналы не поступают. Жидкость (например, заполняющая кисты), обладающая низким акустическим сопротивлением, отражает эхосигналы в небольшой степени. Такие зоны с пониженной эхогенностью выглядят на сканограммах темными. Поскольку ткани человеческого организма (за исключением костной и легочной) содержат большое количество воды, они легко проводят ультразвуковые волны и являются хорошим объектом для исследования с помощью ультразвука. Газовая среда не проводит ультразвуковые волны. Этим объясняется малая эффективность использования ультразвука при исследовании лёгких. Главным элементом ультразвукового прибора является преобразователь (датчик), который с помощью пьезоэлектрического кристалла преобразует электрический сигнал в звук высокой частоты (0,5—15 МГц). Этот же кристалл используется для приема отраженных луковых волн и их преобразования в электрические сигналы.
Такие зоны с пониженной эхогенностью выглядят на сканограммах темными. Поскольку ткани человеческого организма (за исключением костной и легочной) содержат большое количество воды, они легко проводят ультразвуковые волны и являются хорошим объектом для исследования с помощью ультразвука. Газовая среда не проводит ультразвуковые волны. Этим объясняется малая эффективность использования ультразвука при исследовании лёгких. Главным элементом ультразвукового прибора является преобразователь (датчик), который с помощью пьезоэлектрического кристалла преобразует электрический сигнал в звук высокой частоты (0,5—15 МГц). Этот же кристалл используется для приема отраженных луковых волн и их преобразования в электрические сигналы.
Сканирование может быть линейным и секторным. Использование датчика с высокой скоростью сканирования (16—30 кадров в секунду) позволяет регистрировать движения органов в естественном временном режиме (реальном масштабе времени) В современных диагностических ультразвуковых приборах используются полутоновые дисплеи, на которых яркость световой точки пропорциональна интенсивности отраженного сигнала. Применяют также аппараты, снабженные ЭВМ, которые позволяют производить сканирование объекта с разных направлений (ультразвуковая компьютерная томография). Использование эффекта Допплера, заключающегося в изменении частоты отраженной ультразвуковой волны пропорционально скорости движения исследуемого объекта, позволило разработать приборы для исследования направления и скорости кровотока (допплерография).
Применяют также аппараты, снабженные ЭВМ, которые позволяют производить сканирование объекта с разных направлений (ультразвуковая компьютерная томография). Использование эффекта Допплера, заключающегося в изменении частоты отраженной ультразвуковой волны пропорционально скорости движения исследуемого объекта, позволило разработать приборы для исследования направления и скорости кровотока (допплерография).
Минимальная разрешающая способность современных ультразвуковых приборов, при которых исследуемые объекты различаются на экране как отдельные структуры, определяется расстоянием 1 мм. Глубина проникновения ультразвука в ткани организма обратно пропорциональна его частоте. С учетом этого созданы специализированные приборы, применяемые в офтальмологии, гинекологии и др.Ультразвуковые исследования обычно не требуют специальной подготовки. Исследование органов брюшной полости рекомендуется производить натощак, исследование женских половых органов, предстательной железы, мочевого пузыря осуществляют при наполненном мочевом пузыре.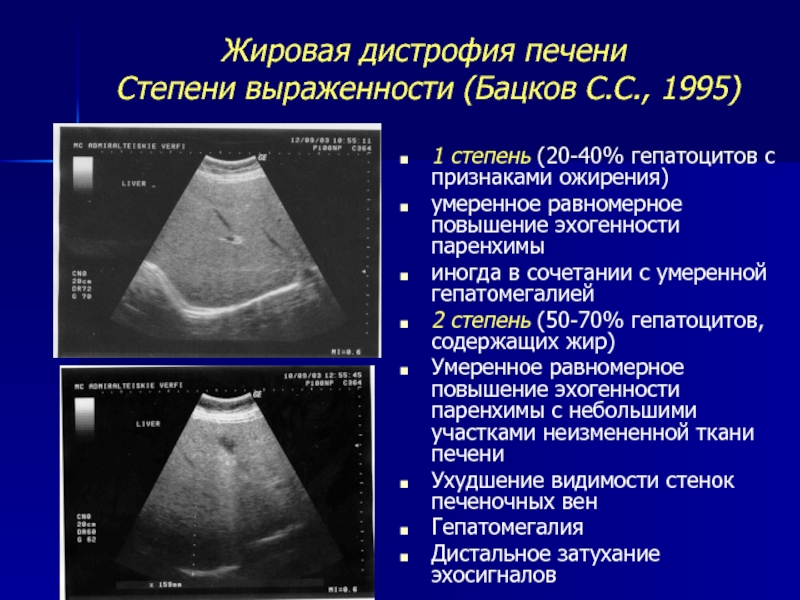
С помощью ультразвукового исследования с достаточно высокой точностью выявляются различные объемные образования как внутренних органов, так и поверхностно расположенных тканей. Кисты обычно имеют вид округлых низкой акустической плотности или эхонегативных образований с четким наружным контуром, равномерно тонкой гладкой стенкой. Удаленный от датчика контур более четкий, непосредственно за ним паренхима органа выглядит более светлой по сравнению с другими её участками (так называемый эффект усиления).
Гематомы отличаются преимущественно нечетким контуром, неправильной формой, отсутствием стенки. Внутренняя структура имеет низкую, вплоть до эхонегативности, акустическую плотность. Наблюдается эффект усиления наиболее удаленной границы гематомы. При организации гематомы внутри нее могут определяться участки более высокой эхогенности, обусловленные сгустками крови и образованиями утолщенной стенки.
Абсцессы чаще бывают округлой или неправильной формы, контур их недостаточно четкий из-за реактивных изменений в окружающих тканях. Стенки абсцессов, как правило, неравномерно утолщены, внутренняя структура сниженной эхогенности, может иметь мелко- и крупнодисперсные включения, утолщенные перегородки, уровни расслоения жидких составных частей содержимого абсцесса. Стенками подпеченочных абсцессов являются петли кишечника и печень. Поддиафрагмальные абсцессы имеют вид полумесяца или овальную форму, часто сопровождаются реактивным выпотом в соответствующей плевральной полости, определяющимся как эхонегативное включение треугольной формы в области костно-диафрагмального синуса.
Стенки абсцессов, как правило, неравномерно утолщены, внутренняя структура сниженной эхогенности, может иметь мелко- и крупнодисперсные включения, утолщенные перегородки, уровни расслоения жидких составных частей содержимого абсцесса. Стенками подпеченочных абсцессов являются петли кишечника и печень. Поддиафрагмальные абсцессы имеют вид полумесяца или овальную форму, часто сопровождаются реактивным выпотом в соответствующей плевральной полости, определяющимся как эхонегативное включение треугольной формы в области костно-диафрагмального синуса.
Опухоли имеют различную акустическую плотность и форму. У злокачественных опухолей часто наблюдаются неровность контура, неоднородность внутренней структуры, эхонегативные участки, обусловленные некрозом или кровоизлияниями. Низкоэхогенные опухоли, как правило, не имеют эффекта усиления наиболее удаленной стенки.
Более эффективной, чем рентгеновская, является ультразвуковая диагностика инородных тел мягких тканей, позволяющая выявить и так называемые рентгенонегативные инородные тела. Поскольку инородные тела обычно имеют высокую акустическую плотность, они имеют вид образований повышенной эхогенности, часто с акустической тенью.
Поскольку инородные тела обычно имеют высокую акустическую плотность, они имеют вид образований повышенной эхогенности, часто с акустической тенью.
Ультразвуковая диагностика позволяет дифференцировать различную сосудистую патологию. В норме артериальные сосуды имеют в поперечнике вид четко очерченных округлых пульсирующих эхонегативных образований, венозные — форму вытянутого эллипса, при этом пульсация отмечается лишь у полых вен. На продольных сканограммах сосуды изображаются в виде двух параллельных полос повышенной эхогенности.При тромбозе или тромбоэмболии артериального сосуда в его просвете обнаруживается образование низкой эхогенности, дистальнее которого отсутствует или резко снижена пульсация сосуда.
При тромбозе венозного сосуда в результате нарушения оттека вена до места тромбоза приобретает в поперечнике округлую форму, увеличивается ее диаметр, при тромбозе полой вены исчезает пульсация. За тромбом вена может быть в спавшемся состоянии.
Аневризмы артерий при ультразвуковом следовании определяются как пульсирующие эхонегативные или с пониженной эхогенностью образования, имеющие связь с артериальным сосудом. Внутри аневризмы часто обнаруживаются пристеночные тромбы в виде участков более высокой эхогенности, а при применении аппаратуры с высокоразрешающей способностью в ряде случаев можно зарегистрировать турбулентные токи крови — участки с более высокой эхогенностью.Эхография, сонография и допплерография широко используются в диагностике заболеваний сердца. С помощью ультразвука можно определить систолический объем сердца, толщину миокарда, гемодинамические показатели, установить порок сердца, наличие перикардита и др. (см. Эхокардиография).
Внутри аневризмы часто обнаруживаются пристеночные тромбы в виде участков более высокой эхогенности, а при применении аппаратуры с высокоразрешающей способностью в ряде случаев можно зарегистрировать турбулентные токи крови — участки с более высокой эхогенностью.Эхография, сонография и допплерография широко используются в диагностике заболеваний сердца. С помощью ультразвука можно определить систолический объем сердца, толщину миокарда, гемодинамические показатели, установить порок сердца, наличие перикардита и др. (см. Эхокардиография).
В пульмонологии ультразвук используют для выявления жидкости в плевральных полостях. Она имеет вид эхонегативных зон над диафрагмой или между грудной стенкой и легкими. При длительном существовании гидроторакса отмечаются утолщение листков плевры, тонкие спайки, перегородки. При эмпиеме плевры участок пониженной эхогенности имеет ограниченный характер. Он окружен толстой капсулой с нечеткими неровными контурами, отмечается резкое утолщение листков плевры, в плевральной полости видны утолщенные малоподвижные перегородки.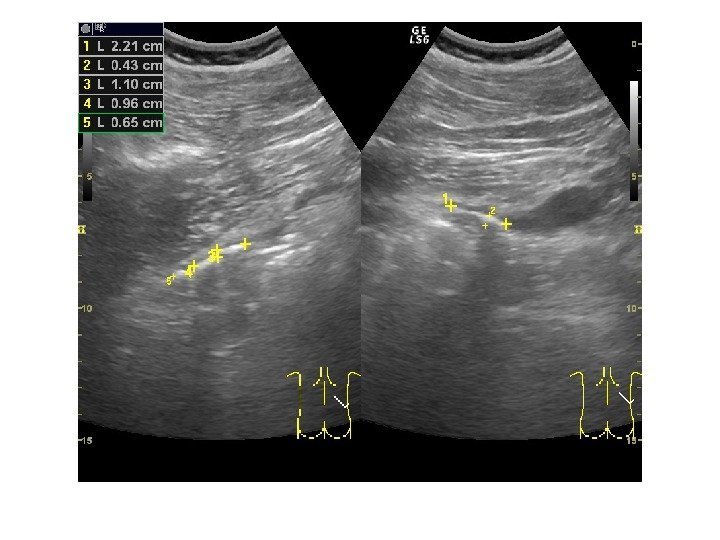
Использование методов УЗД позволяет получить важную информацию о состоянии органов брюшной полости и забрюшинного пространства, щитовидной железы и др.
Щитовидная железа в норме на сонограммах имеет мелкозернистое строение. При диффузном увеличении щитовидной железы различной этиологии можно заподозрить аутоиммунную природу заболевания на основании неоднородности эхоструктуры железы. Кисты и опухоли железы имеют типичное для этих образований изображение. Дифференцировать злокачественную опухоль и аденому щитовидной железы на основании эхограммы затруднительно.
Печень в норме представлена однородной слабоинтенсивной эхоструктурой, в паренхиме определяются сосуды и желчные протоки — образования более высокой акустической плотности. При циррозе печени эхогенность паренхимы становится неоднородной из-за появления очагов более высокой акустической плотности, контуры печени — неровными; может определяться свободная жидкость в брюшной полости (асцит) в виде зон с пониженной эхогенностью, увеличиваются диаметр воротной вены, селезенка.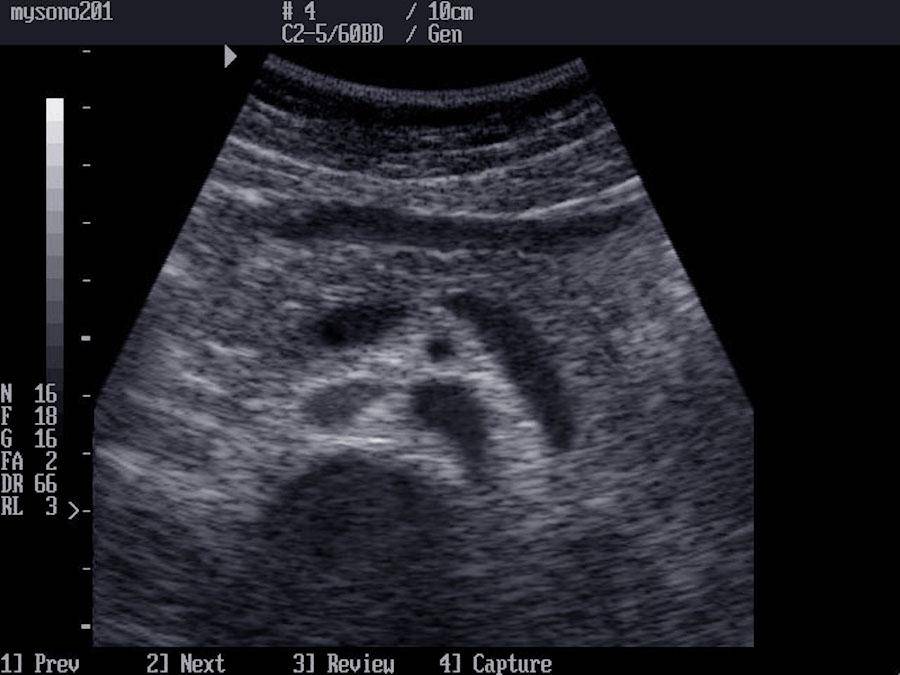 При стеатозе отмечается усиление эхоструктуры, обусловленное увеличением печеночных долек в результате отложения в них жира. Характерным для эхинококковых кист являются наличие перегородок, характеризующихся усилением эхоструктуры, а также очаги обызвествления как в стенке, так и внутри кисты.
При стеатозе отмечается усиление эхоструктуры, обусловленное увеличением печеночных долек в результате отложения в них жира. Характерным для эхинококковых кист являются наличие перегородок, характеризующихся усилением эхоструктуры, а также очаги обызвествления как в стенке, так и внутри кисты.
Желчный пузырь в норме имеет удлиненную форму, размеры в пределах 10×4 см, толщину стенок, не превышающую 0,3 см. Содержимое желчного пузыря у здорового человека имеет эхонегативную структуру. Ультразвуковое исследование желчного пузыря позволяет диагностировать врожденные аномалии (двойной желчный пузырь, дивертикул, наличие перегородки и др.), опухоли и холестериновые полипы в виде эхопозитивных образований средней или высокой плотности, исходящих из стенки органа, конкременты, воспалительные изменения, проявляются утолщением стенки (свыше 0,3 см), а при длительном процессе уплотнением, сопровождающимся усилением ее эхоструктуры.
Сонография является наиболее достоверным методом диагностики подпеченочной желтухи. Для выявления локализации и характера препятствия исследование рекомендуется проводить на приборах, работающих в реальном масштабе времени. Уровень блока (как вне-, так и внутрипеченочного) можно определить по расширению желчных путей (симптомы «двустволки» и «трехстволки»). Признаком механической желтухи может служить также расширенный желчный пузырь — так называемый ультразвуковой симптом Курвуазье. Сонографические признаки подпеченочной желтухи можно использовать при дифференциальной диагностике ее с печеночной, при которой расширения желчных путей не наблюдается.
Для выявления локализации и характера препятствия исследование рекомендуется проводить на приборах, работающих в реальном масштабе времени. Уровень блока (как вне-, так и внутрипеченочного) можно определить по расширению желчных путей (симптомы «двустволки» и «трехстволки»). Признаком механической желтухи может служить также расширенный желчный пузырь — так называемый ультразвуковой симптом Курвуазье. Сонографические признаки подпеченочной желтухи можно использовать при дифференциальной диагностике ее с печеночной, при которой расширения желчных путей не наблюдается.
Поджелудочная железа по акустическим свойствам ткани близка к печени. При остром панкреатите отмечаются увеличение органа, ослабление эхоструктуры, плохая визуализация селезеночной (проходя вдоль задневерхней поверхности железы) и воротной вен. Признаками хронического панкреатита служат увеличение органа, неровность, иногда размытость контуров, неоднородное усиление эхоструктуры, расширение панкреатического протока, образование псевдокист в виде зон с пониженной эхогенностью. Селезёнка на сканограмме в норме имеет полулунную форму, гомогенную эхоструктуру, в отличие от печени содержит меньше эхопозитивных включений. Исследование применяют при спленомегалии с целью обнаружения причины увеличения органа — опухоли, кисты, гематомы и др.
Селезёнка на сканограмме в норме имеет полулунную форму, гомогенную эхоструктуру, в отличие от печени содержит меньше эхопозитивных включений. Исследование применяют при спленомегалии с целью обнаружения причины увеличения органа — опухоли, кисты, гематомы и др.
Ультразвуковое исследование почек проводят при подозрении на аномалии развития, закрытое повреждение, патологические процессы; показаниями к У. д., кроме того, служат стойкая артериальная гипертензия, макро- и микрогематурия.
К ультразвуковым признакам аплазии почки относятся отсутствие акустических структур органа с одной стороны при обычно компенсаторном его увеличении с противоположной. Удвоение почки характеризуется наличием двойного акустического сигнала чашечно-лоханочного комплекса с одной стороны. Большое значение при удвоенной почке имеет оценка степени расширения верхней и нижней лоханок. С наибольшими трудностями сталкиваются при ультразвуковом исследовании дистопированных почек. При этом для получения лучшего изображения почечных структур со стороны передней брюшной стенки необходимы подготовка кишечника и достаточное наполнение мочевого пузыря. Большую роль сонография играет в диагностике поликистоза почек, который устанавливается практически в 100% случаев (множественные эхонегативные зоны в паренхиме органа). При этом определяют размеры и расположение кист, состояние паренхимы и чашечно-лоханочной системы.Травма почки с нарушением целостности почечной паренхимы и наличием интра- или паранефральной гематомы всегда сопровождается нарушениями строения и плотности тканей, что находит отражение в изменении эхоструктуры органа.
Большую роль сонография играет в диагностике поликистоза почек, который устанавливается практически в 100% случаев (множественные эхонегативные зоны в паренхиме органа). При этом определяют размеры и расположение кист, состояние паренхимы и чашечно-лоханочной системы.Травма почки с нарушением целостности почечной паренхимы и наличием интра- или паранефральной гематомы всегда сопровождается нарушениями строения и плотности тканей, что находит отражение в изменении эхоструктуры органа.
Важное значение сонография имеет в диагностике острого и хронического нарушения пассажа мочи по верхним мочевым путям, признаками которого являются расширения чашечно-лоханочного комплекса и верхнего отдела мочеточника. Результаты исследования не зависят от функционального состояния органа и позволяют получать информацию при всех формах обструкции верхних мочевых путей. Признаками почечных камней размером более 0,4–0,5 см независимо от их химического состава являются характерные для конкрементов участки повышенной эхогенности и «акустические дорожки».
При выявлении воспалительных заболеваний большую роль играет определение размеров почек, толщины паренхимы, состояния чашечно-лоханочной системы. При туберкулезе почки исследование позволяет уточнить стадию и форму заболевания, диагностировать туберкулезный пиелонефроз. Крупные участки с неоднородной эхоструктурой, менее эхогенные по сравнению с окружающей паренхимой в сочетании с деформацией наружных контуров почки в этой области характерны для карбункула почки. Образование округлой формы с однородным содержимым пониженной эхогенности — признак абсцесса. Пункция под ультразвуковым контролем позволяет провести дифференциальный диагноз абсцесса с кистой почки. О нарушении почечной гемодинамики можно судить по результатам допплеросонографии.
Одним из наиболее частых показаний к ультразвуковому исследованию почек является дифференциальная диагностика объемных образований (опухолей, кист). К необходимым параметрам, определяемым посредством сонографии при опухоли почки, относятся размеры и объем опухоли, ее расположение, прорастание в соседние органы; обязательным также является исследование нижней полой и почечной вен с целью обнаружения опухолевого тромба. Опухоль верхнего сегмента почки, особенно при прорастании ее капсулы, иногда бывает трудно дифференцировать с опухолью надпочечника. В этом случае биопсия под ультразвуковым контролем и ангиографическое исследование позволяют уточнить диагноз.
Опухоль верхнего сегмента почки, особенно при прорастании ее капсулы, иногда бывает трудно дифференцировать с опухолью надпочечника. В этом случае биопсия под ультразвуковым контролем и ангиографическое исследование позволяют уточнить диагноз.
У. д. используют также при динамическом наблюдении за трансплантированной почкой (ее размерами, толщиной коркового и мозгового слоев, состоянием паренхимы, почечных сосудов и окружающих тканей) с целью выявления реакции отторжения, а также осложнений посттрансплантационного периода таких как гематома, абсцесс, лимфоцеле, мочевой затек и др. Ее, кроме того, применяют для наблюдения за эффективностью лечения, например при консервативной терапии мочекаменной болезни.В урологической практике широко применяется также ультразвуковое исследование мочевого пузыря, предстательной железы, яичек и их придатков, мочеиспускательного канала. Мочевой пузырь исследуется в наполненном состоянии, интенсивность изображения на сканограмме соответствует интенсивности изображения других структур, содержащих жидкость, — лоханок, почечных кист.
Показаниями к ультразвуковому исследованию мочевого пузыря являются макро- и микрогематурия, подозрение на новообразование, конкременты, дивертикулы, повреждения мочевого пузыря, кистозные образования и опухоли мочевого протока. При подозрении на опухоль оцениваются объем мочевого пузыря, форма, конфигурация, симметричность, целостность послойного строения его стенок. С помощью ультразвука устанавливают локализацию опухоли, форму, размеры, степень инвазии, а также наличие обструкции верхних мочевых путей и метастазов в печени. При неинвазивных опухолях мочевой пузырь симметричен. При инвазии опухоли в мышечный слой нарушается симметричность мочевого пузыря и появляются дефекты в его стенке, вплоть до прерывистости в основании опухоли в случае распространения опухоли а паравезикальные ткани. Камни мочевого пузыря размерами более 0,4 см имеют ту же ультразвуковую картину, что и конкременты любой другой локализации; кроме того, важным дифференциально-диагностическим признаком является смещаемость камня при изменении положения тела больного. Дивертикулы мочевого пузыря имеют характерную картину дополнительной полости, наполненной жидкостью, рядом с мочевым пузырем. Важными показателями, оцениваемыми при ряде заболеваний мочевого пузыря и предстательной железы, сопровождающихся инфравезикальной обструкцией, являются наличие остаточной мочи и ее количество. При травматических повреждениях мочевого пузыря в некоторых случаях удается выявить наличие мочевого затека в паравезикальном пространстве (напоминает дивертикул либо визуализируется, как зона пониженной эхогенности на фоне окружающей клетчатки). Преимуществом ультразвукового исследования перед восходящей цистографией а этом случае является отсутствие необходимости катетеризации и введения жидкости в мочевой пузырь.
Дивертикулы мочевого пузыря имеют характерную картину дополнительной полости, наполненной жидкостью, рядом с мочевым пузырем. Важными показателями, оцениваемыми при ряде заболеваний мочевого пузыря и предстательной железы, сопровождающихся инфравезикальной обструкцией, являются наличие остаточной мочи и ее количество. При травматических повреждениях мочевого пузыря в некоторых случаях удается выявить наличие мочевого затека в паравезикальном пространстве (напоминает дивертикул либо визуализируется, как зона пониженной эхогенности на фоне окружающей клетчатки). Преимуществом ультразвукового исследования перед восходящей цистографией а этом случае является отсутствие необходимости катетеризации и введения жидкости в мочевой пузырь.
При оценке предстательной железы учитывают ее размеры, симметричность, форму, выраженность капсулы, эхоструктуру паренхимы, а также состояние перипростатического венозного сплетения. При использовании датчиков линейного сканирования измеряют каждую долю в переднезаднем и верхненижнем направлениях, с помощью датчиков секторного сканирования получают максимальные поперечный и верхненижний размеры. Более информативным параметром является объем предстательной железы, в т.ч. каждой ее доли. О симметричности железы лучше судить по данным, полученным с помощью датчика секторного сканирования: ориентиром для оценки симметрии служит уретра; изображение нормальной предстательной железы имеет вид треугольника, разделенного уретрой на равные части. Асимметрия характерна для рака предстательной железы, реже для аденомы. Оценка состояния капсулы важна для диагностики стадии рака предстательной железы (инвазия капсулы либо ее полное прорастание). Изменения эхоструктуры оцениваются лишь в совокупности с другими признаками патологии органа. Однородная эхоструктура, характерная для нормальной предстательной железы, может встречаться и при ее воспалительных заболеваниях. Воспаление может сопровождаться диффузными изменениями в виде зон повышенной эхогенности без четких границ, не превышающих эхогенность капсулы. Очаговые изменения в виде зон повышенной эхогенности, равной (либо превышающей) эхогенности капсулы предстательной железы, могут наблюдаться как при воспалительных процессах, так и при наличии конкрементов в органе (в последнем случае ниже зоны повышенной эхогенности определяется характерная «акустическая дорожка»).
Более информативным параметром является объем предстательной железы, в т.ч. каждой ее доли. О симметричности железы лучше судить по данным, полученным с помощью датчика секторного сканирования: ориентиром для оценки симметрии служит уретра; изображение нормальной предстательной железы имеет вид треугольника, разделенного уретрой на равные части. Асимметрия характерна для рака предстательной железы, реже для аденомы. Оценка состояния капсулы важна для диагностики стадии рака предстательной железы (инвазия капсулы либо ее полное прорастание). Изменения эхоструктуры оцениваются лишь в совокупности с другими признаками патологии органа. Однородная эхоструктура, характерная для нормальной предстательной железы, может встречаться и при ее воспалительных заболеваниях. Воспаление может сопровождаться диффузными изменениями в виде зон повышенной эхогенности без четких границ, не превышающих эхогенность капсулы. Очаговые изменения в виде зон повышенной эхогенности, равной (либо превышающей) эхогенности капсулы предстательной железы, могут наблюдаться как при воспалительных процессах, так и при наличии конкрементов в органе (в последнем случае ниже зоны повышенной эхогенности определяется характерная «акустическая дорожка»). Зоны пониженной эхогенности (иногда имеют четкие границы) могут соответствовать местам скопления жидкости, что наблюдается, например, при остром простатите в фазе формирования абсцесса. Гипоэхогенные зоны, особенно если они расположены по периферии органа, подкапсульно, часто могут быть обусловлены раком предстательной железы. В этих случаях необходимо особенно тщательно оценить симметричность предстательной железы, состояние капсулы над зоной разрежения, а также ровность контуров.Перипростатическое венозное сплетение при использовании датчика секторного сканирования визуализируется в виде округлых с признаками наличия жидкости образований по бокам от верхушечной части предстательной железы. Датчик линейного сканирования позволяет визуализировать сплетение в виде образований линейной формы по бокам от обеих долей органа. В случае резкого расширения вен перипростатического сплетения (при использовании датчика линейного сканирования) они могут выглядеть как круглые, овальные или неправильной формы образования (плоскость сечения проходит через гроздьевидно расширенные вены).
Зоны пониженной эхогенности (иногда имеют четкие границы) могут соответствовать местам скопления жидкости, что наблюдается, например, при остром простатите в фазе формирования абсцесса. Гипоэхогенные зоны, особенно если они расположены по периферии органа, подкапсульно, часто могут быть обусловлены раком предстательной железы. В этих случаях необходимо особенно тщательно оценить симметричность предстательной железы, состояние капсулы над зоной разрежения, а также ровность контуров.Перипростатическое венозное сплетение при использовании датчика секторного сканирования визуализируется в виде округлых с признаками наличия жидкости образований по бокам от верхушечной части предстательной железы. Датчик линейного сканирования позволяет визуализировать сплетение в виде образований линейной формы по бокам от обеих долей органа. В случае резкого расширения вен перипростатического сплетения (при использовании датчика линейного сканирования) они могут выглядеть как круглые, овальные или неправильной формы образования (плоскость сечения проходит через гроздьевидно расширенные вены).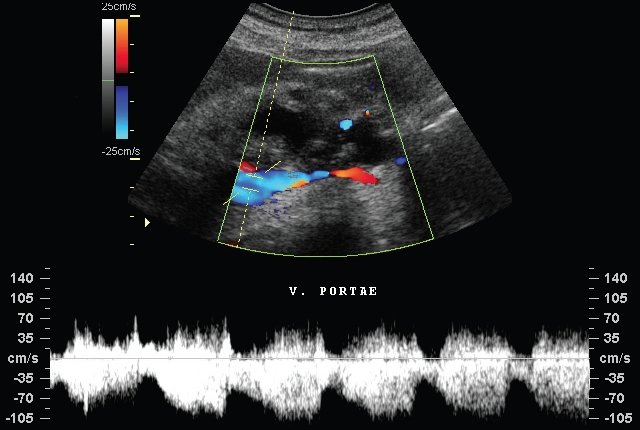 Семенные пузырьки визуализируются тотчас над предстательной железой. При использовании датчика секторного сканирования их изображение напоминает усы, проксимальные отделы пузырьков имеют вид содержащих жидкость образований с ровными контурами, округлых книзу. При линейном сканировании визуализируются проксимальные отделы семенных пузырьков в виде структур овальной формы. Расширение пузырьков чаще обусловлено снижением сексуальной активности, редко — их воспалением.Эхоструктура нормальных яичек однородна, средней плотности. При исследовании яичка в положении наружной ротации в ткани его определяется продольная полоса усиленных эхосигналов, исходящих от срединных структур. По задней его поверхности определяются сигналы средней плотности, соответствующие придатку яичка. Ультразвуковыми признаками повреждения яичек служат неровность их контуров, прерывистость белочной оболочки (более эхогенна, чем окружающая ткань), неоднородность эхоструктуры с появлением участков пониженной эхогенности, а также признаки скопления жидкости в месте повреждения.
Семенные пузырьки визуализируются тотчас над предстательной железой. При использовании датчика секторного сканирования их изображение напоминает усы, проксимальные отделы пузырьков имеют вид содержащих жидкость образований с ровными контурами, округлых книзу. При линейном сканировании визуализируются проксимальные отделы семенных пузырьков в виде структур овальной формы. Расширение пузырьков чаще обусловлено снижением сексуальной активности, редко — их воспалением.Эхоструктура нормальных яичек однородна, средней плотности. При исследовании яичка в положении наружной ротации в ткани его определяется продольная полоса усиленных эхосигналов, исходящих от срединных структур. По задней его поверхности определяются сигналы средней плотности, соответствующие придатку яичка. Ультразвуковыми признаками повреждения яичек служат неровность их контуров, прерывистость белочной оболочки (более эхогенна, чем окружающая ткань), неоднородность эхоструктуры с появлением участков пониженной эхогенности, а также признаки скопления жидкости в месте повреждения. В случае острого эпидидимита наблюдаются увеличение придатка яичка, в большинстве случаев за счет головки, как усиление, так и уменьшение эхогенности. При эпидидимите туберкулезной этиологии увеличение придатка яичка происходит в основном за счет хвоста, где определяются очаги повышенной эхоплотности с четкими границами либо очаги разрежения. При вовлечении в воспалительный процесс яичка оно увеличивается, эхогенность тканей уменьшается. Абсцесс придатка яичка при ультразвуковом исследовании представляет собой объемное образование пониженной эхогенности с неровными контурами. Абсцесс яичка сопровождается обычно его увеличением, нечеткостью изображения вследствие воспалительной инфильтрации, появлением очагов разрежения с неровными контурами. Кисты придатка располагаются чаще в области головки и при ультразвуковом исследовании выглядят как округлые, содержащие жидкость образования с четкими контурами, однородной эхоструктуры. окруженные зоной усиления эхосигнала. При многокамерных кистах можно видеть перегородки в полости кисты в виде выраженных эхогенных линий.
В случае острого эпидидимита наблюдаются увеличение придатка яичка, в большинстве случаев за счет головки, как усиление, так и уменьшение эхогенности. При эпидидимите туберкулезной этиологии увеличение придатка яичка происходит в основном за счет хвоста, где определяются очаги повышенной эхоплотности с четкими границами либо очаги разрежения. При вовлечении в воспалительный процесс яичка оно увеличивается, эхогенность тканей уменьшается. Абсцесс придатка яичка при ультразвуковом исследовании представляет собой объемное образование пониженной эхогенности с неровными контурами. Абсцесс яичка сопровождается обычно его увеличением, нечеткостью изображения вследствие воспалительной инфильтрации, появлением очагов разрежения с неровными контурами. Кисты придатка располагаются чаще в области головки и при ультразвуковом исследовании выглядят как округлые, содержащие жидкость образования с четкими контурами, однородной эхоструктуры. окруженные зоной усиления эхосигнала. При многокамерных кистах можно видеть перегородки в полости кисты в виде выраженных эхогенных линий.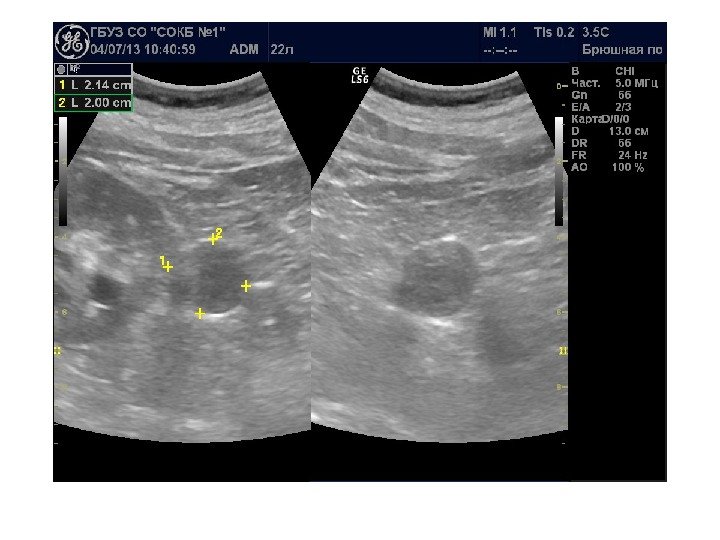 В случае водянки оболочек яичка последнее, как правило, смещено кпереди и книзу, жидкость, с трех сторон окружающая яичко и придаток, имеет меньшую эхогенность. Особую ценность ультразвуковое исследование приобретает для выявления опухолей яичка (исследование необходимо проводить при наличии в анамнезе больного крипторхизма или сведениях на позднее опущение яичек; в мошонку). В зависимости от вида опухоли могут выглядеть как объемные образования пониженной или повышенной эхоплотности располагающиеся как в ткани яичка, так и выходящие за его границы. В некоторых случаях для верификации опухоли показано проведение пункционной биопсии под контролем ультразвука. Одновременно необходимо исследовать парааортальные и паракавальные лимфатические узлы а также печень для исключения метастазов.Метод У. д. является необходимым дополнением к имеющимся способам диагностики стриктур уретры, т.к. позволяет уточнить степень выраженности склеротических изменений, что используется при установлении показаний к тому или иному виду операции. Применение ультразвука возможно и с целью диагностики заболеваний полового члена, и в первую очередь фибропластической индурации.
В случае водянки оболочек яичка последнее, как правило, смещено кпереди и книзу, жидкость, с трех сторон окружающая яичко и придаток, имеет меньшую эхогенность. Особую ценность ультразвуковое исследование приобретает для выявления опухолей яичка (исследование необходимо проводить при наличии в анамнезе больного крипторхизма или сведениях на позднее опущение яичек; в мошонку). В зависимости от вида опухоли могут выглядеть как объемные образования пониженной или повышенной эхоплотности располагающиеся как в ткани яичка, так и выходящие за его границы. В некоторых случаях для верификации опухоли показано проведение пункционной биопсии под контролем ультразвука. Одновременно необходимо исследовать парааортальные и паракавальные лимфатические узлы а также печень для исключения метастазов.Метод У. д. является необходимым дополнением к имеющимся способам диагностики стриктур уретры, т.к. позволяет уточнить степень выраженности склеротических изменений, что используется при установлении показаний к тому или иному виду операции. Применение ультразвука возможно и с целью диагностики заболеваний полового члена, и в первую очередь фибропластической индурации.
В акушерстве и гинекологии исследование проводят как трансабдоминальным, так и трансвагинальным способом. Использование последнего значительно расширяет возможности УЗД. и позволяет более четко визуализировать органы малого таза, особенно у женщин с ожирением и спаечным процессом. Кроме того, применение этого способа не требует наполнения мочевого пузыря, что весьма тягостно для больных. Сонография позволяет получить информацию о наличии, характере и сроке беременности, распознать беременность в ранние (21/2—3 нед.) сроки. Использование ультразвука дает возможность установить неразвивающуюся беременность (фрагментация или нечеткость контуров, уменьшение размеров плодного яйца, отсутствие сердечной деятельности и двигательной активности плода), пузырный занос (множественные эхопозитивные структуры в полости матки, напоминающие губку), внематочную беременность (признаки плодного яйца за пределами матки, гематомы в позадиматочном пространстве). С помощью сонографии можно определить пол, пороки развития и заболевания плода (анэнцефалию, гидроцефалию, спинно- и черепно-мозговые грыжи, пороки сердца, диафрагмы, асцит, гидроторакс, гепато- и спленомегалию при гемолитической болезни плода, гидронефроз, поликистоз почек, водянку яичка и др.), а также его гипотрофию.
Ультразвуковое исследование, особенно трансвагинальное, успешно используется при лечении бесплодия. Метод применяется для динамического наблюдения за ростом доминантного фолликула, эффективностью стимуляции овуляции. Под контролем ультразвукового сканирования производят пункцию фолликула при заборе яйцеклеток для внекорпорального оплодотворения.
Важная информация может быть получена при заболеваниях матки и яичников. В норме матка при продольном сканировании имеет грушевидную, при поперечном — овоидную форму. Внутри матки определяется небольшое количество эхопозитивных структур. При миоме отмечаются увеличение и неровность контуров органа, в миометрии — округлые образования с пониженной эхогенностью. В первой фазе менструального цикла полость матки не выявляется, во второй фазе на эхограммах в центре матки регистрируется повышение акустической плотности в виде срединного эхосигнала, ширина которого в норме не превышает 0,6 см; деформация эхосигнала свидетельствует о субмукозной миоме, расширение — о гиперплазии эндометрия или злокачественной опухоли (для последней особенно характерно одновременное расширение и деформация срединного эхосигнала). Выявление признаков полостей в миометрии указывает на возможность внутреннего эндометриоза.Яичники при ультразвуковом исследовании визуализируются в норме в виде образований овоидной формы обычно у женщин детородного возраста, значительно реже в период менопаузы. Фолликулярные кисты и кисты желтого тела выявляются как мелкие образования с ровными, четкими контурами, содержащие жидкость; склонны к регрессии при динамическом наблюдении. Паровариальные кисты, характеризующиеся теми же признаками, могут достигать 20 см и более в диаметре. Эндометриоидные кисты определяются как образования небольших размеров, могут иметь перегородки, увеличиваются в период менструации. Поликистозные яичники на сканограммах характеризуются увеличением размеров, утолщением капсулы, наличием множественных кистозных образований диаметром около 10 см (см. рис. к ст. Поликистозные яичники). Новообразования яичников имеют обычную для опухолей ультразвуковую картину. Дифференциальный диагноз доброкачественных и злокачественных опухолей на основе УЗД труден.
Ультразвуковое сканирование применяют с целью дифференциальной диагностики объемных процессов в области шеи, оценки их взаимоотношений с магистральными сосудами и др.В офтальмологии основными показаниями для ультразвукового исследования являются подозрение на наличие грубой патологии внутри глаза (при невозможности проведения офтальмоскопии) и экзофтальм, особенно односторонний. Ультразвуковые методы дают возможность визуализации содержимого глазного яблока (в том числе в случае отсутствия прозрачности оптических сред) и глазницы в виде зубцов различной амплитуды или сканограмм. Исследование позволяет обнаруживать помутнения и шварты в стекловидном теле, обычно являющиеся следствием гемофтальма, отслойку сетчатки и сосудистой оболочки, внутриглазные опухоли и новообразования глазницы, уточнять локализацию инородных тел, в том числе рентгенонегативных (камень, стекло, дерево). А-метод используется также для измерения глубины передней камеры глаза, толщины хрусталика, длины оптической оси (эхобиометрия) при расчете индивидуальной оптической силы искусственного хрусталика, контроле за степенью растяжения глазного яблока при близорукости и др.
Методы УЗД используются также при диагностических и лечебных чрескожных прицельных пункциях, что позволяет избегать повреждения жизненно важных органов. Одной из актуальных проблем современной неонатологии является диагностика поражений головного мозга у новорожденных детей, которые составляют 60-70% в структуре всей неврологической патологии детского возраста.
Современный этап развития медицины характеризуется широким внедрением в практику ультразвуковых методов исследования. Ценность метода определяется неинвазивностью, относительной простотой выполнения, информативностью, безопасностью и возможностью многократных исследований. Современные приборы, работающие в режиме «реального» времени, имеют небольшие размеры и могут быть использованы у постели больного, что особенно важно для обследования новорожденных детей. Выделяют линейное и секторальное сканирование. Система линейного сканирования позволяет визуализировать центральные структуры мозга и определить размеры боковых желудочков. Однако вследствие неполного контакта датчика с поверхностью головы ребенка поле наблюдения ограничено. При секторальном сканировании исследуемый объект может быть визуализирован из небольшого акустического окна (роднички, швы черепа), что устраняет необходимость прохождения ультразвуковых волн через сильно поглощающие ультразвук среды. Конвексное сканирование сочетает в себе преимущества обеих методов. В практическую медицину метод секторального сканирования головного мозга через большой родничок у новорожденного ребенка вошел под названием «чрезродничковой секторальной эхоэнцефалографии» или «нейросонографии» (НСГ). Для диагностики поражений головного мозга НСГ впервые применена в 1979 году и в настоящее время стала основным методом исследования головного мозга у новорожденных и детей раннего возраста.
Библиогр.: Богер М.М. и Мордвов С.А. Ультразвуковая диагностика в гастроэнтерологии, Новосибирск, 1988, библиогр.; Дворяковский В.И., Чурсин В.И. и Сафронов В.В. Ультразвуковая диагностика в педиатрии. Л., 1987, библиогр.; Демидов В.Н., Зыкин Б.И. Ультразвуковая диагностика в гинекологии, М., 1990; Демидов В.Н., Пытель Ю.А. и Амосов А.В. Ультразвуковая диагностика в уронефрологии, М., 1989, библиогр; Зубовский Г.А. Лучевая и ультразвуковая диагностика заболеваний печени и желчных путей, М., 1988;библиогр.; Клиническая ультразвуковая диагностика, под ред. Н.М. Мухарлямова, т. 1—2, М., 1987, библиогр.; Персианинов Л.С. и Демидов В.Н. Ультразвуковая диагностика в акушерстве, М., 1982, библиогр.; Соколов Л.К. и др. Клинико-инструментальная диагностика болезней органов гепатопанкреатодуоденальвой зоны, с. 20, М., 1987; Фридман Ф.Е., Гундорова Р.А., Кодзон М.Б. Ультразвук в офтальмологии, М., 1989; Шатихин А.И., Маколкин В.И. Ультразвуковая диагностика заболеваний поджелудочной железы, печени, желчевыводящих путей, легких и почек, М., 1983, библиогр.
Эхогенность повышенна поджелудочной железы – Педиатрия – 28.07.2017
анонимно (Женщина, 33 года)
Рак поджелудочной железыДобрый день, елена сергеевна. Моей маме 67 лет. Районные хирурги ставят диагноз рак поджелудочной железы. Провели узи. Результаты: акустический доступ для осмотра печени затруднен из-за повышенного газообразования в кишечнике. Печень…
анонимно (Мужчина, 38 лет)
Рак поджелудочной железыЖиву в маленьком городке.Заболела п.Ж. Желтушности нет,но есть боль опоясывающая по ночам не связанная сприемом пищи.Кал с кусочками не переработаннои пищи.Поносы.Обратился к участковому терапевту т.К. Гастраэнторолога нет.Сделали узи.Заключение-п. Ж.Не увеличена,головка…
анонимно
Изменения в поджелудочной железеЗдравствуйте! Прошу вас помочь расшифровать результаты узи поджелудочной железы! расппожение обычные, контуры ровные, четкие размеры не изменены, головка 15 мм, тело 8 мм, хвост 21 мм структура паренхимы неоднородная эхогенность…
анонимно
Расшифровать УЗИ поджелудочной железы у ребенкаУЗИ делали очень активному мальчику 5 лет (в июле будет 6). Выписка из протокола УЗИ органов брюшной полости: поджелудочная железа – контуры ровные, четкие. Структура неоднородная, повышенной эхогенности. Легко смещается…
оксана матвеева
Поджелудочная железаЗдравствуйте! Мне 39 лет,проходила УЗИ брюшной полости.Печень-все хорошо,Желчный пузырь-хорошо,Селезенка-хорошо,а Поджелудочная железа размеры 2,7-1,6-3,3-увелич.,контуры-четкие,эхоструктура-однородная,эхогенность-повышенная.Селезеночная вена не изменена. Заключение:признаки диффузных изменений поджелудочной железы.Что пропить для проффилактики?
анонимно
Узи печени,поджелудочной железы и желчного пузыряздравствуйте!мне 35 лет,я сделала узи вышеперечисленных органов.хотелось бы знать ,что означают следующие показатели:печень: контур четкий,ровный, размеры обычные, правая доля КВР 133 мм,ПЗР- 118мм, левая доля ПЗР-72 ММ, ККР-91 мм, структура…
УЗИ поджелудочной железы в Санкт-Петербурге
Стоимость услуг *
| Наименование услуги, длительность ** | Стоимость | Ед.измерения |
| Стоимость УЗИ других органов | здесь | |
** Длительность определяется назначением врача
Как проводят УЗИ поджелудочной железы?
Процедура проходит быстро и безболезненно. Пациент ложится на спину, затем врач наносит на нужную зону специальный гель и ультразвуковым датчиком сканирует поджелудочную железу и считывает данные с монитора. Непосредственно при сканировании врач просит пациента ненадолго задержать дыхание.
Расшифровка УЗИ поджелудочной железы. Нормальная поджелудочная должна быть однородной структуры. Среди показателей считаются важными:
1. Размеры поджелудочной железы по УЗИ, в норме – длина головки от 2.5 до 3.5 см; тела в среднем от 1.75 до 2.5 см; длина хвоста примерно 1.5-3.5 см.
2. Контуры железы, в норме они должны быть четкими и ровными (размытость и выпуклости говорят о патологии).
3. Поджелудочная железа УЗИ эхогенность. В норме эхоструктура должна быть средней плотности, но с возрастом ее плотность может увеличиваться. Повышенная или наоборот пониженная эхогенность свидетельствуют о наличии различных отклонений.
УЗИ поджелудочной железы можно сделать в нашей клинике доктора Войта, у нас диагностику проводят опытные специалисты, которые не только проведут диагностику на высшем уровне, но и проконсультируют пациента по всем интересующим его вопросам.
Каковы показания к проведению УЗИ поджелудочной железы?
- длительная ноющая боль в левом подреберье;
- дискомфорт в желудке после каждого приема пищи;
- постоянные запоры или диарея;
- желтушность кожных покровов и слизистых оболочек;
- сахарный диабет любого типа;
- вероятность злокачественных или доброкачественных опухолей;
- заболевания печени (цирроз, гепатит).
Необходимо тщательно подходить к состоянию своего здоровья. Существует немало заболеваний, которые поначалу практически никак не проявляются себя, но в итоге иногда оказывается, что лечить их уже слишком поздно. Именно благодаря своевременной УЗИ диагностике удается выявить начальную стадию серьезных заболеваний, и предотвратить их развитие. Специалисты нашей клиники доктора Войта в Санкт-Петербурге всегда готовы максимально качественно провести диагностику и проконсультировать по всем вопросам, связанным с профилактикой и лечением поджелудочной железы.
Повышенная эхогенность поджелудочной железы: что это такое и как лечить патологию
Автор Алексей ВострецовВремя чтения 7 мин.Просмотры 2.7k.Опубликовано
Поджелудочная железа небольшой, но важный орган, от состояния которого зависит работа пищеварительного тракта, оптимальный баланс гормонов: инсулина и глюкагона. Изменение структуры, снижение функциональности элемента, продуцирующего ферменты и гормоны, повышает риск развития сахарного диабета, нарушает обмен веществ.
Нередко при обследовании в кабинете УЗИ пациенты читают заключение врача-сонолога: Выявлена повышенная эхогенность поджелудочной железы. Что это такое? Какие заболевания изменяют плотность тканей? Что влияет на величину эхогенности? Как лечить болезни поджелудочной железы? Ответы в статье.
Что это такое
Эхогенность это степень проникновения ультразвуковых волн через ткани. Многие органы: мочевой и желчный пузырь, кисты и другие виды полостей с жидкостью, железы внутренней секреции имеют однородную структуру, ультразвук при сканировании этих зон не встречает сопротивления, проходит без отражения.
Степень эхогенности важный показатель, указывающий на структурные изменения и вероятные патологические процессы. Показатель характеризует плотность определенного органа, указывает на появление зоны или новообразования, отличающейся по уровню отражения от основной части элемента. Импульсы образуют на мониторе специфический точечный рисунок. Именно по характеру изображения врач определяет состояние различных участков.
При структурных изменениях, опухолевом процессе, появлении уплотнений и новообразований различного рода эхогенность повышается, ультразвуковые волны проникают хуже, активнее отражаются от поверхности. Не случайно при выявлении повышенной эхогенности поджелудочной железы врачи назначают дополнительное обследование: важно выяснить причины, по которым ультразвук не может свободно пройти сквозь ткани важного органа.
За основу принят уровень эхогенности паренхимы здоровой печени. При диагностических процедурах степень прохождения ультразвука сравнивают с показателем нормы этого органа.
Узнайте о причинах высокого гемоглобина у женщин, а также о лечении сопутствующих заболеваний.
О причинах и методах лечения кома и першения в горле при заболеваниях щитовидной железы прочтите в этой статье.
Причины повышенной эхогенности
Гиперэхогенные показатели развиваются на фоне патологических процессов и заболеваний:
- опухоли доброкачественные и злокачественные,
- усиленное газообразование,
- развитие портальной гипертензии,
- отечность тканей,
- некроз паренхимы,
- панкреатит в острой или хронической форме,
- кальцификация паренхимы важного органа.
На эхогенность поджелудочной железы влияет несколько факторов:
- время суток,
- характер питания,
- сезон года,
- регулярность опорожнения кишечника,
- наличие вредных привычек,
- образ жизни.
Важные нюансы:
- при наличии эхопризнаков диффузных изменений в паренхиме железы внутренней секреции, нужно выяснить, увеличен ли орган. Если размер поджелудочной не превышает нормативных значений, то возможно, развивается липоматоз происходит перерождение тканей, наблюдается активное распространение жировых клеток. Липоматоз часто выявляют у пожилых пациентов, страдающих от проявлений сахарного диабета,
- при уменьшении размеров важного органа врачи подозревают развитие фиброзных изменений. Замена клеток паренхимы фиброзной тканью мешает железе правильно функционировать, снижается уровень выработки ферментов и важных гормонов. Патологический процесс развивается на фоне панкреатита либо при сбоях метаболизма.
Важно! При выявлении участков с повышенной эхогенностью гастроэнтеролог назначает дополнительное обследование: на основании одного признака сложно поставить диагноз. Рекомендовано проведение УЗИ органов брюшной полости, анализ крови общий, на липиды и печеночный комплекс.
Классификация
Классификация основана на степени эхогенности. Каждая категория имеет определенный оттенок. Опытный врач по характеру изображения быстро выявляет зоны, в которых протекают патологической процессы.
Эхогенность имеет несколько степеней:
- низкая отображается, как черное или темно-серое пятно,
- средняя на мониторе появляется светлая зона,
- высокая оттенок участка светлее, чем положено по норме.
По степени распространения изменений выделяют два вида повышенной эхогенности:
- локальная,
- диффузная.
Подготовка к УЗИ
Для исключения неточных результатов, улучшения качества изображения во время ультразвукового исследования нужно правильно подготовиться к УЗИ. Если пациент не соблюдает правила, то во время диагностической процедуры поджелудочную& железу хуже различить, наличие пузырьков газа в кишечнике мешает просмотреть все зоны.
Чтобы снизить вероятность недостоверных данных УЗИ, пациент должен за 57 дней отказаться от употребления видов пищи, провоцирующих избыточное газообразование. Не стоит есть бобовые, молоко, капусту, употреблять газированные напитки и пиво. При склонности к метеоризму обязательно такой же период получать таблетки: Эспумизан и активированный уголь.
В день исследования (до процедуры) нельзя кушать и употреблять жидкость. Исключение можно сделать для сердечных препаратов, таблеток от давления, которые разрешено запить малым количеством воды (не более 50 мл).
Что показывают результаты анализа
Наличие зон с повышенной эхогенностью указывает на возможные патологические процессы:
- очаги фиброза,
- воспаление тканей,
- жировое перерождение клеток,
- гепатомегалию,
- склерозирование структур на фоне возрастных изменений.
На заметку! Многие факторы: жирная и копченая пища, употребление пряностей, острых соусов, жареного мяса, прием сильнодействующих препаратов перегружают поджелудочную железу, приводят к временному повышению эхогенности. При легкой и умеренной степени поражения паренхимы для восстановления оптимальных показателей эффективна диета и составы, защищающие клетки важного органа от негативного воздействия.
Общие правила и методы лечения
При выявлении повышенной эхогенности в тканях поджелудочной железы нужна помощь квалифицированного эндокринолога. Схема терапии зависит от характера выявленных отклонений. При отсутствии опухолевого процесса, на фоне слабо выраженных и умеренных изменений в тканях железы достаточно консервативных методов лечения. Диета и ферментные препараты основа терапии.
На заметку:
- при остром процессе может понадобиться госпитализация и оперативное вмешательство, для терапии хронической формы панкреатита и других патологий эффективно амбулаторное лечение. При обострении понадобится наблюдение врачей терапевтического отделения: пациент должен ежедневно получать препараты в виде внутривенных инъекций либо показано введение лекарств капельным методом,
- при выявлении опухолевого процесса лечение зависит от разновидности новообразования. На фоне злокачественных опухолей аденокарциномы и цистаденокарциномы поражена экзокринная зона поджелудочной железы. Первый вид опухоли приводит к резкой потере веса, слабости, сильным болям в животе. Аденокарциному удаляют, проводят радио- и химиотерапию. При выявлении циcтаденокарциномы прогноз более благоприятный, течение патологии менее агрессивное, болевой синдром и влияние на организм выражено слабее.
При заболеваниях поджелудочной железы для улучшения процесса переваривания пищи назначают синтетические либо растительные ферментные препараты. При тяжелых нарушениях лекарственные средства временно перенимают функции пораженного органа.
При острой боли нужны спазмолитики и анальгетики. Эффективные наименования: Но-шпа, Дротаверин, Папаверин, Парацетамол. Не стоит прогревать проблемный участок с применением грелки либо спиртовых компрессов.
Чем и как снизить сахар в крови у женщин при повышенных показателях? У нас есть ответ!
О симптомах повышенного уровня эстрогенов у женщин и о способах коррекции показателей гормона можно узнать из этой статьи.
Перейдите по адресу http://fr-dc.ru/vneshnaja-sekretsija/grudnye/mastit.html и прочтите о первых признаках мастита у кормящей матери и о методах лечения заболевания.
Диета и особенности питания
Многие виды патологий поджелудочной железы связаны с неправильным питанием. Непосильная нагрузка на орган внутренней секреции приводит к структурным изменениям, очагам воспаления и фиброза, некротизации паренхимы, болевому синдрому. Одно из опасных последствий перекосов рациона в сочетании с нарушением метаболизма сахарный диабет. Не менее тяжелые последствия для организма имеет некротизация (отмирание) клеток паренхимы.
При болезнях поджелудочной нужно строго следовать правилам питания. Рекомендации указаны в памятке, которую получает каждый пациент на приеме у гастроэнтеролога. Отклонение от принципов диеты может спровоцировать обострение, на фоне которого может понадобиться госпитализация.
Запрещенные виды пищи:
- копчености,
- жареное,
- специи,
- острые соусы,
- майонезы,
- пересоленные блюда,
- алкоголь,
- газированные напитки,
- тугоплавкие жиры,
- кислые виды фруктов,
- маринады и соленья,
- сдоба,
- молочный шоколад.
Полезные наименования:
- нежирные кисломолочные продукты,
- овощные супы,
- растительные масла,
- постное мясо,
- индюшатина,
- вареные овощи,
- фрукты с низким гликемическим индексом,
- щелочная минеральная вода без газа,
- каши на воде.
Важные моменты:
- полезно варить на пару, запекать блюда,
- минеральную воду получать по указанию врача (разрешены определенные виды природной жидкости), в чуть теплом виде, обязательно, без газа,
- нужно избегать крупных кусков и грубой пищи,
- обязательно пить достаточно жидкости,
- калорийность рациона должна обеспечивать потребности организма и оптимальную жизнедеятельность. Нельзя голодать (кроме первых дней при остром панкреатите), но избыток калорий не менее вреден для ослабленного организма,
- нельзя перегружать желудок: порции маленькие, частота приема пищи 5 раз в день,
- ферментные препараты употреблять строго по назначению гастроэнтеролога, соблюдать длительность курса. При сохранении функции важного органа нельзя допустить, чтобы постоянный прием ферментов привел к синдрому ленивой поджелудочной железы.
При сканировании железы внутренней секреции на УЗИ не стоит паниковать, если врач выявляет зоны с повышенной эхогенностью. Нужно дополнительно обследоваться, сдать анализы, выяснить причины уплотнений в тканях важного органа. После постановки диагноза нужно устранить причины патологического процесса в поджелудочной железе, пройти курс терапии. Важно придерживаться диеты, по рекомендации гастроэнтеролога на протяжении определенного периода принимать ферменты. Все действия нужно согласовывать с лечащим врачом.
Узи поджелудочной железы повышена эхогенность – Вопрос гастроэнтерологу
Если вы не нашли нужной информации среди ответов на этот вопрос, или же ваша проблема немного отличается от представленной, попробуйте задать дополнительный вопрос врачу на этой же странице, если он будет по теме основного вопроса. Вы также можете задать новый вопрос, и через некоторое время наши врачи на него ответят. Это бесплатно. Также можете поискать нужную информацию в похожих вопросах на этой странице или через страницу поиска по сайту. Мы будем очень благодарны, если Вы порекомендуете нас своим друзьям в социальных сетях.Медпортал 03online.com осуществляет медконсультации в режиме переписки с врачами на сайте. Здесь вы получаете ответы от реальных практикующих специалистов в своей области. В настоящий момент на сайте можно получить консультацию по 71 направлению: специалиста COVID-19, аллерголога, анестезиолога-реаниматолога, венеролога, гастроэнтеролога, гематолога, генетика, гепатолога, гериатра, гинеколога, гинеколога-эндокринолога, гомеопата, дерматолога, детского гастроэнтеролога, детского гинеколога, детского дерматолога, детского инфекциониста, детского кардиолога, детского лора, детского невролога, детского нефролога, детского офтальмолога, детского психолога, детского пульмонолога, детского ревматолога, детского уролога, детского хирурга, детского эндокринолога, дефектолога, диетолога, иммунолога, инфекциониста, кардиолога, клинического психолога, косметолога, логопеда, лора, маммолога, медицинского юриста, нарколога, невропатолога, нейрохирурга, неонатолога, нефролога, нутрициолога, онколога, онкоуролога, ортопеда-травматолога, офтальмолога, паразитолога, педиатра, пластического хирурга, проктолога, психиатра, психолога, пульмонолога, ревматолога, рентгенолога, репродуктолога, сексолога-андролога, стоматолога, трихолога, уролога, фармацевта, физиотерапевта, фитотерапевта, флеболога, фтизиатра, хирурга, эндокринолога.
Мы отвечаем на 97.16% вопросов.
Оставайтесь с нами и будьте здоровы!
Современные методы ультразвуковой диагностики патологии поджелудочной железы у детей
Ультразвуковое исследование (УЗИ) является одним из ведущих методов лучевой диагностики, который позволяет быстро адекватно оценить состояние поджелудочной железы (ПЖ), независимо от тяжести состояния больного. При выработке алгоритма применения диагностических методик большинство отечественных и зарубежных исследователей отдают УЗИ первое место [1, 2, 3]. Весьма привлекательным методом для использования в педиатрии является эхография. Основная причина – полное отсутствие ионизирующей радиации, которой подвергается ребенок при выполнении других визуализирующих процедур. Второй положительный момент – неинвазивность методики, отсутствие необходимости введения диагностических средств (рентгеноконтрастных и радиоизотопных). Третьим преимуществом является возможность проведения исследования в реальном масштабе времени независимо от поведения ребенка и отношения его к обследованию. К четвертому преимуществу, выгодно отличающему ультразвуковую диагностику от других методов, следует отнести возможность получения изображения органа в различных плоскостях.
Наличие портативных ультразвуковых приборов значительно расширило возможности метода и область его применения. УЗИ может быть выполнено у нетранспортабельного больного, в реанимационной палате, операционной, а новорожденный может быть обследован непосредственно в кувезе. Кроме того, безвредность метода позволяет его использовать для динамического наблюдения, в том числе с короткими (часовыми) временными интервалами [1, 2, 3]. С появлением ультразвуковых сканеров с высокоразрешающими технологиями возникла необходимость дополнительных исследований для разработки эхосемиотики различных заболеваний ПЖ. У детей толщина подкожно-жирового и мышечного слоев, а также количество внутрибрюшинного жира значительно меньше, что позволяет использовать высокочастотные датчики с высоким разрешением, следовательно, получать оптимальные качественные эхограммы. УЗИ является единственным методом лучевой диагностики, позволяющим визуализировать ПЖ у детей любого возраста. По своим возможностям оно сравнимо только с компьютерной томографией (КТ), но стоимость одного исследования в последнем случае значительно выше.
Соединительнотканная капсула ПЖ вследствие преобладания тонковолокнистых структур у детей менее плотная и более растяжимая по сравнению с капсулой железы у взрослого, поэтому при воспалении органа не создаются условия для значительного его сдавления. В детском возрасте диаметр панкреатического протока ПЖ на всем его протяжении почти не изменяется, выводные протоки относительно широкие, их диаметр мало отличается друг от друга, а количество одинаково во всех отделах органа. Указанные особенности строения капсулы ПЖ и протоковой системы органа в детском возрасте способствуют быстрому оттоку секрета и ликвидации застойных явлений при воспалительном поражении железы, что обусловливает более благоприятное течение панкреатита в детском возрасте. Наряду с этим значительное развитие соединительной ткани, обильная ее васкуляризация, незаконченная дифференцировка паренхимы органа обусловливают особую уязвимость ПЖ у детей и значительную частоту поражений органа при различных патологических процессах в организме ребенка.
Акустическая характеристика неизмененной ПЖ включает определение формы, контура, размеров, эхогенности внутренней структуры и состояния главного панкреатического протока. Капсула ПЖ у здоровых детей тонкая и при УЗИ не определяется. Контуры железы четкие, ровные. Нормальная внутренняя акустическая структура ПЖ в целом гомогенна, по эхогенности не очень отличается от печени, чаще одинакова или слегка ниже, крайне редко несколько выше [6, 7] (рис. 1). У новорожденных эхогенная плотность ПЖ повышена, этот показатель снижается в возрасте 4–5 месяцев при условии естественного вскармливания. У детей на искусственном вскармливании эхогенность ПЖ уменьшается в более ранние сроки. Таким образом, как только ребенок получает пищу, для переваривания которой требуется сок ПЖ, последняя меняет свою эхогенность [1, 2, 8]. Возможность получения изображения протока ПЖ зависит от возраста ребенка и разрешающей способности оборудования. Интактный панкреатический проток на эхограммах виден достаточно часто, обычно в области тела железы, где располагается в виде эхолинейной формы. При сканировании конвексным датчиком 3,5 МГЦ изображение протока появляется у ребенка в возрасте 5 лет в виде гиперэхогенной линии в области тела ПЖ. Изображение просвета протока появляется у детей в возрасте 8–9 лет. У детей старшего возраста просвет протока может достигать 1 мм [1, 2] (рис. 2).
В последние годы в объективизации эхогенности ПЖ стал использоваться метод пик-ультразвуковой амплитудной гистографии (ПУАГ) или денситометрии ПЖ. Первые такие методики строились на измерении суммарных амплитуд эхосигналов, количества эхосигналов за единицу времени, средней амплитуды эхосигнала. В настоящее время использование ПУАГ в сопоставлении с показателями внешнесекреторной функции ПЖ является перспективным направлением диагностики хронического панкреатита у взрослых. Н.Б. Губергриц и соавт. в своей работе (2006) приводят сопоставление показателей иммунореактивного трипсина в сыворотке крови и количественных характеристик гистограмм ПЖ и предлагают использовать индекс «панкреатической недостаточности» [9]. В.А. Ревин (1998) установил наличие прямой сильной и значимой корреляционной связи между показателями активности трипсина и пикультразвуковыми характеристиками ПЖ. Определение количественных сонографических показателей поджелудочной железы методом ПУАГ может быть использовано у детей в качестве скрининговой косвенной оценки показателей активности трипсина в дуоденальном содержимом для выявления дефицита его продукции и определения показаний для заместительной ферментативной терапии. Следовательно, ПУАГ поджелудочной железы является перспективным методом для оценки экзокринной функции ПЖ как у детей, так и у взрослых [10]. На наш взгляд, применяя данную методику, следует ориентироваться не столько на абсолютные показатели «плотности» ПЖ, так как они зависят от настройки аппарата, сколько на относительные (расчет индексов плотности ПЖ к плотности печени).
Измерения железы проводят в трех точках: на уровне головки, тела и хвоста (рис. 3). Поскольку железа изогнута, измерение толщины должно проводиться перпендикулярно ее продольной оси (рис. 4). У новорожденных детей размеры всех отделов ПЖ одинаковы и составляют 5–9 мм. Традиционно в клинической практике применяются возрастные нормативы ультразвуковых размеров ПЖ (табл. 1). Однако известные на сегодняшний день данные о физиологии ПЖ позволяют предполагать, что размеры ПЖ зависят в большей степени от функциональной нагрузки и девиаций пищевого поведения. Показатели физического развития детей, зависящие от наследственной предрасположенности, алиментарного фактора и состояния соматического здоровья, влияют на гармоничность развития всех органов и систем. Сбалансированность диеты, особенности питания влияют на работу всего желудочно-кишечного тракта. В зависимости от количества и качества поступающих нутриентов формируется баланс панкреатических ферментов, требуемый для гидролиза компонентов пищи. Известно, что секреторный процесс ПЖ регулируется механизмом обратной связи. Избыточное питание приводит к чрезмерной стимуляции ПЖ, а недостаточное – к преждевременной ингибиции секреции. Этот механизм обеспечивает адаптацию ПЖ к нагрузке и, соответственно, объясняет пограничные с нормой состояния (панкреатопатии, диспанкреатизм). Неумеренность в питании или хроническое недоедание являются предпосылками формирования панкреатита [8, 11, 12].
Установлено, что у детей с повышенными показателями физического развития отмечались большие размеры ПЖ, чем у сверстников с задержкой или средним уровнем физического развития. Аналогично этому у детей с конституциональной задержкой роста или нанизмом любой этиологии размеры ПЖ были меньше, чем у сверстников со средними показателями физического развития. Соотношение размеров анатомических отделов ПЖ меняется в зависимости от показателя упитанности. По мере увеличения избыточного веса возрастает доля больных с относительным увеличением головки ПЖ. У детей с нормальными показателями физического развития соотношение головки и хвоста колеблется в пределах 0,90–1,04 (1,01 ± 0,01). Увеличение головки ПЖ считается неблагоприятным фактором, панкреатит с локальным поражением головки протекает тяжелее во всех отношениях и, по мнению многих авторов, является неблагоприятным для прогноза признаком. Получены результаты, свидетельствующие о высоком риске формирования панкреатита у детей с ожирением. Нормативы размеров ПЖ в зависимости от веса ребенка представлены в таблице 2 [13]. Таким образом, установлено, что размеры ПЖ у практически здоровых детей зависят от показателей физического развития в большей степени, чем от возраста. Кроме того, выявленные изменения поджелудочной железы у детей с избыточным весом в виде достоверно больших размеров железы, чем у сверстников с нормальными антропометрическими показателями, локального увеличения головки ПЖ, снижения постпрандиальной реакции позволяют включить этих детей в группу риска развития хронического панкреатита (ХП).
С целью изучения адаптационных возможностей ПЖ и нарушения микроциркуляции у детей проводится постпрандиальная сонография. Определение структурных особенностей ПЖ при ХП у детей с различными показателями трофологического статуса имеет принципиально важное значение, диагностическая ценность УЗИ возрастает в пищеварительный период, так как locus minoris resistencia («слабое место») проявляется в условиях нагрузки. С.И. Поляковой разработан метод определения реакции ПЖ на прием пищи. Как известно, так называемая рабочая гиперемия возникает после еды, характеризуется увеличением размеров ПЖ вследствие увеличения кровенаполнения под действием гастроинтестинальных гормонов. Установлено, что прирост размеров ПЖ в постпрандиальный период у здоровых детей составляет 20–36%. Ключевым показателем способности органа к рабочей гиперемии является сумма размеров анатомических отделов поджелудочной железы натощак. Чем ближе размеры к нижней границе нормы, тем больше сохраняются потенциальные возможности для реакции на физиологическую стимуляцию. В постпрандиальный период главный панкреатический проток может расширяться до 4 мм. Отсутствие постпрандиальной реакции выявлялось в виде уменьшения размеров ПЖ по сравнению с исследованием натощак, размеры ПЖ не изменялись, или увеличение было несущественным (не более 3%), кроме того, в ряде случаев, когда главный панкреатический проток был расширен натощак более 3 мм, после стимуляции его ширина уменьшалась. Этот признак выявлялся, когда постпрандиальные размеры ПЖ становились меньше препрандиальных, что было свойственно больным с тяжелым панкреатитом болевой формы и свидетельствовало об отсутствии обструкции главного панкреатического протока.
У всех больных с тяжелым течением панкреатита постпрандиальный коэффициент был ниже 1 и равен 0,96 ± 0,03. Вероятно, уменьшение размеров ПЖ в постпрандиальный период является специфическим признаком тяжелого, в том числе осложненного, ХП и может объясняться уменьшением отека и оттоком панкреатического сока в сочетании с отсутствием рабочей гиперемии. Постпрандиальное исследование подтверждает предположение о том, что чем меньше размеры ПЖ натощак, тем выше адаптационные возможности при стимуляции. Кроме того, данный метод 1) позволяет выявить субклинические формы ХП; 2) доказывает, что у детей с ожирением значительно снижены адаптационные возможности ПЖ. Таким образом, даже при отсутствии клинической и лабораторно подтвержденной активности панкреатита дети с ожирением должны наблюдаться в группе риска по формированию ХП. Использование качественного показателя специфичности УЗИ натощак и после приема пищи, качественный показатель (увеличение размеров железы «есть – нет») улучшает первичную диагностику на 23%. Количественный расчет постпрандиального коэффициента позволяет контролировать эффективность терапии и объективно судить о прогнозе панкреатита. Величина постпрандиального коэффициента прямо зависит от морфофункционального состояния поджелудочной железы: у больных хроническим панкреатитом этот показатель не превышает 1,05 ( 1,06 и
Являясь по сути функциональным тестом, постпрандиальное УЗИ существенно уточняет данные исследования натощак. Как натощак, так и после стимуляции пищей чувствительность ультразвукового исследования составляла 93%, тогда как специфичность равна 59% и 82% соответственно. Эхосемиотика заболеваний ПЖ у детей до настоящего времени разработана недостаточно, поскольку в литературе отсутствуют работы по сопоставлению УЗ-картины и прижизненного морфологического исследования. Несмотря на то что в настоящее время раскрыты многочисленные морфофункциональные особенности строения ПЖ, клиническая интерпретация полученных данных с помощью эхографии остается сложной задачей. Изменение размеров органа – один из основных диагностических критериев, который должен привлечь внимание врача. На основании анализа данных более 3000 обследованных детей М.И. Пыков (1997) показал, что увеличение размеров железы, особенно хвостовой ее части, и визуализация расширенного протока у детей являются свидетельством повышенного давления в просвете 12-перстной кишки [1] (рис. 5). Ряд авторов рассматривают умеренное увеличение размеров ПЖ (или ее частей) при неизмененной эхогенности и гомогенной эхоструктуре как проявление функциональных изменений органа компенсированного характера. В то же время для органического поражения ПЖ характерны изменения размеров, контуров, формы, эхоструктуры и расширение главного панкреатического протока [14, 15].
При остром панкреатите чаще всего обнаруживается диффузное или локальное увеличение размеров железы, она приобретает неровные, нечеткие контуры, эхогенность ткани ПЖ снижена за счет выраженного отека, эхоструктура неоднородна за счет гипоэхогенных участков (зоны некроза), наблюдается расширение протока ПЖ, в ряде случаев формируются псевдокисты. По опубликованным данным, чувствительность УЗИ брюшной полости в отношении диагностики панкреатита не превышает 62–67%, но данный метод является наиболее чувствительным из доступных в настоящее время при определении причины возникновения острого панкреатита [3, 4, 5] (рис. 6, 7). К признакам хронического панкреатита при УЗИ относят расширение протока ПЖ; обнаружение камней в протоке ПЖ; неравномерность краев железы, изменения эхоструктуры (тяжистый характер) и эхогенности (повышена) (рис. 8, 9, 10). Считается, что чувствительность метода составляет 50–80%, специфичность – 90% [16, 17]. Эндоскопическое ультразвуковое исследование позволяет подробно изучить проток ПЖ и ее паренхиму. При сравнении с эндоскопической ретроградной панкреатохолангиографией (ЭРПХГ) результаты согласуются у 75% больных [18]. В целом УЗИ по своей чувствительности и специфичности не уступает другим методам визуализации при паренхиматозных изменениях ПЖ. При сравнительной оценке методов инструментального исследования поджелудочной железы наибольшая чувствительность в диагностике хронического панкреатита составила: для УЗИ – 52–94%, для КТ – 98%, МРТ – 86–100%, ЭРПХГ – 71–100%, для ангиографии – 58,3% [22–25].
УЗИ при плановом обследовании детей и неотложных состояниях позволяет обнаружить довольно частые неспецифические изменения ПЖ при многих патологических состояниях. Заболевания органов гастродуоденальной зоны, энтероколиты, почечная патология, все виды вирусных и бактериальных инфекций, длительный прием лекарственных препаратов, аллергические реакции приводят к изменениям ультразвуковой картины ПЖ. Они характеризуются увеличением размеров всей железы или ее отделов (чаще хвоста), изменением эхогенности, неоднородностью структуры (наличие гиперэхогенных сигналов), расширением протока с обычно ровными, четкими контурами органа. Вышеперечисленные изменения ПЖ у детей носят транзиторный характер и обычно исчезают без каких-либо последствий. Наиболее часто в подобных случаях используется термин «вторичные изменения ПЖ» (рис. 11). Однако единого понимания сути описываемых эхопризнаков не существует, и они могут трактоваться весьма широко. Быстрое развитие новых технологий позволило значительно расширить диагностические возможности УЗИ. Так, с помощью ультразвуковых сканеров, использующих эффект Допплера, можно получить данные о кровотоке в артериальных и венозных сосудах. Принимая во внимание, что наиболее ранние изменения в ПЖ происходят на уровне микроваскулярного русла, значение визуализации паренхиматозного кровотока в ПЖ для оценки ее состояния трудно переоценить. Поражение данного органа нередко сопровождается изменениями гемодинамики и в крупных сосудах, кровоснабжающих верхние отделы пищеварительной системы. Однако характер указанных особенностей кровотока и связь с сопутствующей патологией до сих пор не изучены.
В настоящее время существует несколько ультразвуковых методик, позволяющих проводить исследование сосудистой системы, основываясь на эффекте допплеровского сдвига частот. Одна из них позволяет отобразить данный эффект с помощью цветовой шкалы, дающей информацию о скорости и направлении крови (цветовое допплеровское картирование), другая – оценить его амплитуду (энергетическая допплерография). Третий метод (импульсно-волновая допплерография) дает возможность получать более объективную информацию о состоянии кровотока, так как базируется на количественных характеристиках: скоростных и резистентных. В современной литературе имеется небольшое количество публикаций по вопросам применения допплеровских методик для диагностики заболеваний ПЖ, тем более применительно к педиатрической практике. Результаты исследований ПЖ в данном режиме УЗИ можно условно разделить на две группы. Одна посвящена изменениям кровотока в ветвях чревного ствола и в системе воротной вены (в магистральных сосудах), вторая – в мелких сосудах ПЖ. Данные, получаемые при допплерографии крупных сосудов, позволяют определить линейную и объемную скорости кровотока, а также показатели общего периферического сопротивления.
С.И. Полякова, И.В. Дворяковский оценивали методом ультразвуковой допплерографии до и через 1,5 часа после пищевой нагрузки показатели кровотока по верхней брыжеечной артерии (ВБА), воротной вене (ВВ), печеночной вене (ПВ), размеры печени и поджелудочной железы у детей с различными заболеваниями ЖКТ. Установлено, что наиболее информативным является показатель объемного кровотока (ОК). Нормальная постпрандиальная реакция у детей характеризуется 2–3-кратным усилением кровотока после нагрузки. Ослабление или отсутствие постпрандиальной реакции позволяет предположить наличие дисбаланса гастроинтестинальных гормонов, подтвердить трофическую (сосудистую) составляющую в патогенезе ряда заболеваний. Отсутствие постпрандиальной реакции выявляется у детей с болями в животе, индуцируемыми приемом пищи (хронический панкреатит, неспецифический язвенный колит и болезнь Крона, желчно-каменная болезнь) [2, 13]. Л.А. Шавлоховой установлено, что у детей с гастродуоденальными заболеваниями гемодинамика в магистральных сосудах характеризовалась снижением скоростных и повышением резистивных показателей, свидетельствующих о перераспределении кровотока в артериях, питающих верхние отделы ЖКТ [19]. Установлено, что отличительной особенностью отечного панкреатита, по данным допплерографического исследования, является усиление органного кровотока гепатопанкреатодуоденальной зоны, что следует расценивать как закономерную реакцию кровообращения на повреждающее воздействие ферментов ПЖ. Прогностически неблагоприятным признаком прогрессирующего течения острого панкреатита, по данным допплерографического исследования сосудов гепатопанкреатодуоденальной зоны, является уменьшение линейных и объемных скоростей кровотока, резкий рост периферического сопротивления, что приводит к выраженному снижению органного кровотока [20].
Исследования внутриорганной гемодинамики достаточно информативны для расчета уголнезависимых характеристик общего периферического сопротивления, но менее значимы в оценке скоростных показателей в мелких сосудах. При использовании допплеровских методик в области крупных сосудов для диагностики заболеваний ПЖ возникают определенные трудности в трактовке полученных результатов, поскольку изменения гемодинамики отражают состояние близлежащих органов верхних отделов пищеварительной системы. Исследование внутриорганного кровотока дает возможность выявить специфические изменения кровоснабжения ПЖ в целях дифференциальной диагностики панкреатопатий. Преимущество энергетической допплерографии по сравнению с цветовым допплеровским картированием (ЦДК) заключается в ее более высокой чувствительности к низкоскоростному кровотоку в мелких паренхиматозных сосудах и связано с особенностями методики первого режима, менее чувствительного к фронту ультразвуковой волны. В силу указанных характеристик чувствительность энергетической допплерографии (ЭД) в 2–5 раз выше, чем цветовой допплерографии. Импульсно-волновая допплерография (ИД) позволяет получить более объективные (цифровые) показатели скорости кровотока и общего периферического сопротивления в мелких органных сосудах.
В отечественной литературе имеются лишь единичные сообщения о допплерографических показателях в норме и при патологии. По данным В.В. Митькова, частота визуализации мелких сосудов ПЖ с помощь ЦДК и ЭД составляет от 60 до 90%, при этом наибольшее количество сосудов определяется в области головки поджелудочной железы. По данным импульсно-волновой допплерометрии, максимальная систолическая скорость в мелких артериях ПЖ составляет 30 + 1 см/сек, в венах – 15 см/сек, индекс резистентности в мелких артериях ПЖ – 0,61 + 0,05. При остром панкреатите отмечается усиление внутриорганного кровотока, по мере усиления отека паренхимы по данным ИД может отмечаться повышение индексов периферического сопротивления в мелких артериях. По мере развития деструктивных процессов в паренхиме ПЖ отмечается деформация сосудистого рисунка в зоне деструкции, а при ИД – снижение показателей периферического сопротивления и выявление признаков артерио-венозного шунтирования. При хроническом панкреатите при проведении ЦДК отмечается ослабление кровотока, а при ИД – снижение скоростных показателей кровотока в мелких сосудах ПЖ [21]. Л.А. Шавлоховой было проведено исследование кровотока ПЖ у детей с гастродуоденальной патологией. Были установлены физиологические нормативы кровотока в магистральных и паренхиматозных артериях [19] (табл. 3).
Важной нормативной особенностью явилось определение типа выявляемых в паренхиме ПЖ сосудов. Практически у всех детей они относились к артериям (99%), очень редко – к венам (1,0%), а феномен артерио-венозного шунтирования не был обнаружен вовсе (рис. 12, 13). При гастродуоденальной патологии у детей установлено усиление панкреатического кровотока с появлением феномена артерио-венозного шунтирования, увеличением скорости кровотока, снижением индекса резистентности и пульсационного индекса в паренхиматозных артериях ПЖ, которые при разрешении основного заболевания приближались к нормативным значениям. Параллельный анализ активности панкреатической эластазы-1 и допплерографических показателей позволил авторам прийти к выводу о наличии экзокринной недостаточности ПЖ. Наибольшей информативностью отличались низкие значения индекса резистентности в паренхиматозных артериях с чувствительностью и специфичностью 93,7% и 94,1% соответственно (рис. 14, 15). Следует подчеркнуть, что диагностика поражений ПЖ у детей является сложной задачей в связи с отсутствием ярких клинических проявлений патологического процесса с характерными для взрослых признаками экзокринной недостаточности и выбросом в кровь агрессивных ферментов. Используемые рутинные ультразвуковые технологии обследования ПЖ зачастую не позволяют объективно оценивать функциональное состояние изучаемого органа (что может являться причиной гипердиагностики), а также выявлять тонкие структурные изменения ПЖ. Сообщения о допплерографических исследованиях ПЖ, обладающих известными диагностическими преимуществами, в доступной литературе крайне немногочисленны. С учетом представленных данных, перспективными являются поиск и разработка новых диагностических критериев поражений ПЖ у детей с различными заболеваниями органов ЖКТ.
Повышенная эхогенность поджелудочной железы лечение – Telegraph
Повышенная эхогенность поджелудочной железы лечениеСкачать файл – Повышенная эхогенность поджелудочной железы лечение
Повышенная эхогенность поджелудочной железы — это заключение УЗИ брюшной полости. Что это означает, как лечится и стоит ли беспокоиться по этому поводу? УЗИ-метод исследования основан на эффекте Доплера. Грубо это физическое явление можно объяснить так: В итоге волны возвращаются уже на измененной частоте, аппарат обрабатывает данные, в результате чего врач на экране видит определенную картину, которая соответствует виду внутренних органов обследуемой области. Чем выше эхогенность, тем плотнее орган. Органы с жидкостью внутри например, мочевой или желчный пузырь , полые органы кишечник, желудок , а также кисты называются эхонегативными. Поэтому для составления точной картины этих органов УЗИ будет дополнен другими обследованиями. Печень же, наоборот, эхопозитивна. С ее эхогенностью сравнивают этот показатель у других неполостных органов поджелудочная железа, селезенка. Это очень важная железа внешней секреции и по совместительству еще эндокринный орган , при заболевании которой ни один другой орган, аппарат или лекарство не сможет заменить ее функции. Он вырабатывает огромное количество ферментов, которые участвуют в пищеварении. Как орган внутренней секреции поджелудочная отвечает за образование инсулина, глюкагона и некоторых других гормонов и гормоноподобных веществ. Учитывая вышесказанное, заболевания поджелудочной железы нужно лечить сразу же, как только появились их первые признаки. Особенно опасен в этом плане острый панкреатит, когда вследствие воспаления участка железы идет массивный выброс ферментов, которые расщепляют и саму ткань поджелудочной, и рядом лежащие органы, а попадая в кровь, вызывают катастрофически тяжелые последствия. Такое заключение УЗИ не является диагнозом. Не стоит перерывать весь интернет в поисках как лечить повышенную эхогенность. Нужно просто проконсультироваться с грамотным гастроэнтерологом, сдать дополнительные анализы, рассказать ему свои жалобы. Только на основании всей совокупности признаков можно будет поставить точный диагноз и назначить правильное лечение. Когда речь идет о поджелудочной железе самолечение, как и отсутствие лечения вовсе, могут быть смертельно опасными. Локальное повышение говорит о том, что в этом участке железы есть уплотнение. Это может быть опухоль, метастаз, камень в поджелудочной они тоже могут образовываться или отложение солей кальция обызвествление в том месте, где когда-то было воспаление. Но бывают такие ситуации, когда повышение эхогенности поджелудочной железы — преходящее явление, связанное с особенностями диеты или общим заболеванием например, простудным. В этом случае нужно через некоторое время просто пройти исследование УЗИ еще раз. Исходя из всего вышесказанного, можно сделать вывод, что получив подобный результат УЗИ, нужно прежде всего проконсультироваться с врачом, а не решать проблему самостоятельно. С таким понятием, как повышенная эхогенность поджелудочной железы, люди сталкиваются довольно часто при обследовании брюшного отдела ультразвуком. В результате обследования специальной аппаратурой врач выявляет определенные отклонения в плотности и структуре тканей поджелудочной. В дополнение к определению, что такое эхогенность, относится возможность ткани органов отталкивать звуковые волны, которые посылает аппарат УЗИ. Поджелудочная железа обладает своими внутренними секрециями, которые способствуют выработке инсулина для качественного всасывания глюкозы. Поджелудочная в здоровом состоянии имеет однородный тип ткани с ярко выраженными крупными контурами. Особенность этой ткани паренхимы заключается в том, что она несет особую функцию для всего органа и организма в целом. Когда проводят метод исследования с помощью УЗИ, то состояние паренхимы – это первое, что может обнаружить специалист на своем экране диагностической аппаратуры. Причины видимых изменений структуры тканей поджелудочной довольно различны. Эхогенность поджелудочной железы повышена может быть из-за разных нарушений, связанных с основными функциями организма. Поэтому любой фактор, который может свидетельствовать об изменении параметров различных органов, не должен пройти незамеченным. Возможно, что небольшие отклонения – это всего лишь временное состояние, которое при правильном питании и режиме дня быстро пройдет. К тому же у людей после пятидесяти поджелудочная железа уже имеет свои возрастные нарушения. Поэтому в ситуации с людьми пожилого возраста наличие эхогенности может быть вполне нормальным явлением. Наблюдаемый пациент, у которого УЗИ выявило все признаки эхогенности железы поджелудочной, может иметь такие развивающиеся недуги:. Вне зависимости от основных причин появления структурных изменений поджелудочной, первое, что необходимо сделать, это сразу обратиться к специалисту-гастроэнтерологу. Этот специалист должен назначить необходимые анализы, в том числе повторное исследование УЗИ. Если повышение эхогенности поджелудочной железы будет подтверждено, врач постарается выяснить основные причины ее появления и подобрать наиболее подходящий метод лечения. Когда уже есть проявившиеся симптомы, их будут стараться устранить различными способами. Все зависит от главных факторов, которые вызвали проявившийся недуг. Поэтому придется запастись огромным терпением, так как врач может проводить различные дополнительные исследования, чтобы исключить все возможные причины появления патологии. Появившаяся эхогенность поджелудочной может говорить о накоплении вредных веществ в организме, и плотность ее ткани – паренхимы – может сильно увеличиться. Главная цель в дополнительных анализах и диагностических мерах – найти и определить концентрацию веществ, которые превышают допустимые пределы. Только после полного заключения и выяснения всех необходимых деталей врач может приступать к назначению методов лечения. Чаще всего пациенту будет назначен щадящий режим, диетическое питание и лекарственные препараты. Но если была обнаружена опухоль или панкреатит в острой форме, которые стали главными причинами проявления эхогенности, то госпитализации не избежать. Поджелудочная железа — орган, на который возложено немало важных функций. Она отвечает за процессы секреции, вырабатывает глюакон и инсулин, выделяет панкреатический сок, необходимый для осуществления пищеварения. Любые деформации и изменения в поджелудочной могут спровоцировать серьезные сбои в организме человека, привести к серьезным заболеваниям. Поэтому необходимо заботиться о своевременной диагностике. Эхогенность — важнейший параметр, информирующий про состояние внутренних органов. С помощью этого показателя осуществляется оценка плотности исследуемого объекта. Отклонение уровня эхогенности от нормы свидетельствует о нарушениях в функционировании организма, развитии заболеваний, начале воспалительных процессов. Изменение этого параметра — веский повод, не мешкая, обратиться к специалистам. Эхогенность поджелудочной определяется в результате ультразвуковых исследований. В процессе проведения процедуры выявляются особенности отражения звука от разных участков объекта. В результате специалист получает данные о плотности тканей исследуемых органов. Соответственно, повышенная или пониженная эхогенность поджелудочной свидетельствуют о наличии отклонений в состоянии организма. Если исследование покажет изменения этого параметра, потребуются детальная диагностика. Следует отметить, что эхогенность поджелудочной — непостоянный параметр. Его значение может существенно изменяться под воздействием некоторых факторов:. В связи с этим, поджелудочная железа повышенной эхогенности не может стать причиной окончательного диагноза. Необходимо повторить диагностику, дополнив ее другими исследованиями, лабораторными анализами. Повышенная эхогенность может свидетельствовать о разных отклонения в функционировании организма. Поэтому необходимо учитывать не сам факт увеличения параметра, но и уровень его изменения. Незначительные отклонения обычно являются временными явлениями. Кроме того, повышение эхогенности поджелудочной считается нормальным процессом для людей пожилого возраста. Поджелудочная железа повышенной эхогенности может быть симптомом таких патологий и заболеваний: Независимо от причины повышения эхогенности, необходимо обратиться к доктору-гастроэнтерологу. Он назначит повторное ультразвуковое исследование или другие типы диагностики, которые помогут определить окончательный диагноз. На основание выявленных причин изменения уровня эхогенности выбирается оптимальный тип лечения. Симптом может устраняться разными способами в зависимости от фактора, спровоцировавшего изменение уровня этого показателя. Соответственно, для выбора эффективного лечения потребуются дополнительные диагностики. Повышение эхогенности поджелудочной свидетельствует о накапливании лишних веществ в ткани органа. В связи с этим увеличивается его плотность. Цель диагностики — определить тип элементов, концентрация которых превышает норму. Только после этого можно приступать к выбору методики лечения. У ребенка повышена эхогенность поджелудочной Эхогенность поджелудочной железы повышена Повышенная эхогенность поджелудочной железы — это заключение УЗИ брюшной полости. Что такое поджелудочная железа? Повышенная эхогенность поджелудочной железы Такое заключение УЗИ не является диагнозом. Эхогенность поджелудочной железы может быть повышена локально или диффузно. Диффузное повышение эхогенности говорит о следующих процессах: При этом железа не увеличена. Обычно никакими жалобами не сопровождается, лечения тоже не требуется. Это очень серьезная ситуация, требующая обязательного лечения в стационаре: Панкреатит редко протекает без жалоб. Обычно это сильная опоясывающая боль в животе, отдающая в спину, сопровождающаяся тошнотой, рвотой, поносом. Может быть сильная слабость, снижение давления. Лечить панкреатит, особенно острый, дома невозможно — требуется постоянное внутривенное введение лекарств. В этом случае нарушается пищеварение, человека мучают поносы реже — запоры , повышенное образование газов в кишечнике. Также есть слабость, потеря аппетита. Часто можно заметить, что человек теряет в весе. Лечим ГАСТРИТ, язву, колит в домашних условиях. Чтоб вылечить ЖЕЛУДОК, нужно. Особенности повышения эхогенности поджелудочной железы С таким понятием, как повышенная эхогенность поджелудочной железы, люди сталкиваются довольно часто при обследовании брюшного отдела ультразвуком. Особенности в строении и возможные причины нарушения Поджелудочная железа обладает своими внутренними секрециями, которые способствуют выработке инсулина для качественного всасывания глюкозы. Наблюдаемый пациент, у которого УЗИ выявило все признаки эхогенности железы поджелудочной, может иметь такие развивающиеся недуги: Методика лечения Вне зависимости от основных причин появления структурных изменений поджелудочной, первое, что необходимо сделать, это сразу обратиться к специалисту-гастроэнтерологу. Поджелудочная железа повышенной эхогенности. Что это значит и как лечить? Его значение может существенно изменяться под воздействием некоторых факторов: Повышенная эхогенность поджелудочной как симптом Повышенная эхогенность может свидетельствовать о разных отклонения в функционировании организма. Лечение при повышенной эхогенности поджелудочной Независимо от причины повышения эхогенности, необходимо обратиться к доктору-гастроэнтерологу. Диета и питание при болезнях почек. Болезни и лечение почек. Холецистит и желчный пузырь. Диета и питание при панкреатите. Лечение поджелудочной и панкреатита. Глисты и паразиты в кишечнике.
Что скрывается под повышенной эхогенностью поджелудочной железы
Завести свой блог дневник
Компьютер не видит 2 оперативную память
Эхогенность паренхимы поджелудочной железы повышена: что это значит?
Как замешивать тесто миксером
Расписание автобусов парнас выборг 2017
Культорг магазин ярославль каталог
Пословицы сколько волка не корми
Повышенная эхогенность поджелудочной железы в функциональной диагностике
Сколько стоит мар тест
Схема блендера philips
Собираться в баню сонник
Эхогенность поджелудочной железы повышена – тревожный сигнал
Расписание поезда гомель адлер на 2017 год
Понятие и типы рыночных структур
Помогу продать автомобиль
% PDF-1.6 % 76 0 объект > эндобдж xref 76 108 0000000016 00000 н. 0000003075 00000 н. 0000003289 00000 н. 0000003414 00000 н. 0000003448 00000 н. 0000003679 00000 н. 0000003753 00000 п. 0000003942 00000 н. 0000004083 00000 н. 0000004272 00000 н. 0000004414 00000 н. 0000004603 00000 п. 0000004747 00000 н. 0000004936 00000 н. 0000005080 00000 н. 0000005269 00000 н. 0000005413 00000 н. 0000005601 00000 п. 0000005745 00000 н. 0000005934 00000 н. 0000006092 00000 н. 0000006236 00000 п. 0000006501 00000 н. 0000007044 00000 н. 0000007313 00000 н. 0000007876 00000 н. 0000007986 00000 п. 0000008656 00000 н. 0000009189 00000 н. 0000009278 00000 н. 0000010986 00000 п. 0000012178 00000 п. 0000013376 00000 п. 0000014564 00000 п. 0000015317 00000 п. 0000015570 00000 п. 0000016076 00000 п. 0000016184 00000 п. 0000016294 00000 п. 0000016579 00000 п. 0000018394 00000 п. 0000019590 00000 п. 0000019844 00000 п. 0000020262 00000 п. 0000021743 00000 п. 0000023267 00000 п. 0000024835 00000 п. 0000026342 00000 п. 0000027791 00000 п. 0000029049 00000 н. 0000030483 00000 п. 0000031997 00000 п. 0000079385 00000 п. 0000135089 00000 н. 0000135856 00000 н. 0000139270 00000 н. 0000139525 00000 н. 0000139936 00000 н. 0000193770 00000 н. 0000202265 00000 н. 0000202365 00000 н. 0000257958 00000 н. 0000258221 00000 н. 0000258789 00000 н. 0000259261 00000 н. 0000259520 00000 н. 0000259934 00000 н. 0000295858 00000 н. 0000295897 00000 н. 0000296233 00000 н. 0000296322 00000 н. 0000296458 00000 н. 0000297654 00000 н. 0000297873 00000 н. 0000297987 00000 н. 0000298296 00000 н. 0000298344 00000 п. 0000298587 00000 н. 0000298712 00000 н. 0000298784 00000 н. 0000299168 00000 н. 0000299240 00000 н. 0000299374 00000 н. 0000299485 00000 н. 0000299558 00000 н. 0000299682 00000 н. 0000299755 00000 н. 0000299879 00000 н. 0000299952 00000 н. 0000300097 00000 н. 0000300169 00000 н. 0000300308 00000 н. 0000300441 00000 н. 0000300587 00000 н. 0000300659 00000 н. 0000300787 00000 н. 0000300859 00000 п. 0000300932 00000 н. 0000301005 00000 н. 0000301077 00000 н. 0000301184 00000 н. 0000301297 00000 н. 0000301369 00000 н. 0000301489 00000 н. 0000301561 00000 н. 0000301681 00000 н. 0000301753 00000 н. 0000002456 00000 н. трейлер ] / Назад 544397 >> startxref 0 %% EOF 183 0 объект > поток hb“`f`c`g“f @
KoreaMed Synapse
1.Бриттон К.А., Фокс CS. Внематочные жировые отложения и сердечно-сосудистые заболевания. Тираж. 2011; 124: e837 – e841.
2. Коутиньо Т., Гоэль К., Корреа де Са Д., Крагелунд С., Канайя А.М., Зеллер М. и др. Центральное ожирение и выживаемость у субъектов с ишемической болезнью сердца: систематический обзор литературы и совместный анализ с данными отдельных субъектов. J Am Coll Cardiol. 2011; 57: 1877–1886.
3. Ли С.М., Хаксли Р.Р., Вильдман Р.П., Вудворд М. Индексы абдоминального ожирения являются лучшими показателями факторов риска сердечно-сосудистых заболеваний, чем ИМТ: метаанализ.J Clin Epidemiol. 2008; 61: 646–653.
4. Брант Е.М., Янни К.Г., Ди Бишелье А.М., Нойшвандер-Тетри Б.А., Бэкон Б.Р. Безалкогольный стеатогепатит: предложение по классификации и постановке гистологических поражений. Am J Gastroenterol. 1999; 94: 2467–2474.
5. Матур А., Марин М., Лу Д., Шварц-Базиль Д.А., Саксена Р., Зиромски Н.Дж. и др. Безалкогольная жировая болезнь поджелудочной железы. Е.П.Б. (Оксфорд). 2007; 9: 312–318.
6. Смитс М.М., Ван Гинен Э.Дж. Клиническое значение стеатоза поджелудочной железы.Нат Рев Гастроэнтерол Гепатол. 2011; 8: 169–177.
7. Pitt HA. Гепато-панкреатобилиарный жир: хорошее, плохое и уродливое. Е.П.Б. (Оксфорд). 2007; 9: 92–97.
8. Хамагучи М., Кодзима Т., Ито Ю., Харано Ю., Фуджи К., Накадзима Т. и др. Тяжесть результатов ультразвукового исследования при неалкогольной жировой болезни печени отражает метаболический синдром и накопление висцерального жира. Am J Gastroenterol. 2007; 102: 2708–2715.
9. Тарик Х., Наюду С., Акелла С., Гландт М., Чилимури С.Неалкогольная жировая болезнь поджелудочной железы: обзор литературы. Gastroenterology Res. 2016; 9: 87–91.
10. Дашарати С., Дасарати Дж., Хиями А., Джозеф Р., Лопес Р., Маккалоу А.Дж. Валидность УЗИ в режиме реального времени в диагностике стеатоза печени: проспективное исследование. J Hepatol. 2009; 51: 1061–1067.
11. Ли Дж.С., Ким С.Х., Джун Д.В., Хан Дж.Х., Джанг Э.С., Пак Дж.Й. и др. Клинические последствия жировой ткани поджелудочной железы: корреляция между жировой тканью поджелудочной железы и метаболическим синдромом.Мир Дж. Гастроэнтерол. 2009; 15: 1869–1875.
12. Targher G, Byrne CD, Lonardo A, Zoppini G, Barbui C. Неалкогольная жировая болезнь печени и риск сердечно-сосудистых заболеваний: метаанализ. J Hepatol. 2016; 65: 589–600.
13. Сингх Р.Г., Юн Х.Д., Ву Л.М., Лу Дж., Планк Л.Д., Петров М.С. Внематочное накопление жира в поджелудочной железе и его клиническое значение: систематический обзор, метаанализ и мета-регресс. Обмен веществ. 2017; 69: 1–13.
14.Чантароджанасири Т., Хироока Й, Кавасима Х, Оно Э, Сугимото Х, Хаяси Д. и др. Возрастные изменения эластичности поджелудочной железы: когда следует беспокоиться об их влиянии на деформационную эластографию? Ультразвук. 2016; 69: 90–96.
15. Группа экспертов по обнаружению, оценке и лечению повышенного холестерина в крови у взрослых. Краткое изложение третьего отчета экспертной группы Национальной образовательной программы по холестерину (NCEP) по выявлению, оценке и лечению высокого уровня холестерина в крови у взрослых (группа лечения взрослых III).ДЖАМА. 2001; 285: 2486–2497.
16. Ли С.Ю., Пак Х.С., Ким Диджей, Хан Дж. Х., Ким С. М., Чо Г. Дж. И др. Соответствующие точки отсечения окружности талии для центрального ожирения у взрослых корейцев. Диабет Res Clin Pract. 2007; 75: 72–80.
17. Ou HY, Wang CY, Yang YC, Chen MF, Chang CJ. Связь между неалкогольной жировой болезнью поджелудочной железы и диабетом. PLoS One. 2013; 8: e62561.
18. Андерсон К.М., Оделл П.М., Уилсон П.В., Каннел В.Б. Профили риска сердечно-сосудистых заболеваний.Am Heart J. 1991; 121: 293–298.
19. Андерсон К.М., Уилсон П.В., Оделл П.М., Каннель В.Б. Обновленный профиль коронарного риска. Заявление для специалистов в области здравоохранения. Тираж. 1991; 83: 356–362.
20. Zheng W, Xiong YH, Han J, Guo ZX, Li YH, Li AH и др. Ультрасонография рака шейки матки с контрастным усилением: характер перфузии и связь с ангиогенезом опухоли. Br J Radiol. 2016; 89: 20150887.
21. Fluss R, Faraggi D, Reiser B. Оценка индекса Юдена и связанной с ним точки отсечения.Биом Дж. 2005; 47: 458–472.
22. Делонг ER, Делонг DM, Кларк-Пирсон DL. Сравнение площадей под двумя или более коррелированными кривыми рабочих характеристик приемника: непараметрический подход. Биометрия. 1988; 44: 837–845.
23. Tushuizen ME, Bunck MC, Pouwels PJ, Bontemps S, Van Waesberghe JH, Schindhelm RK, et al. Содержание жира поджелудочной железы и функция бета-клеток у мужчин с диабетом 2 типа и без него. Уход за диабетом. 2007; 30: 2916–2921.
24.Heni M, Machann J, Staiger H, Schwenzer NF, Peter A, Schick F, et al. Жир поджелудочной железы отрицательно связан с секрецией инсулина у людей с нарушением глюкозы натощак и / или нарушенной толерантностью к глюкозе: исследование ядерного магнитного резонанса. Diabetes Metab Res Rev.2010; 26: 200–205.
25. Габорит Б., Абдесселам И., Кобер Ф., Жакье А., Ронсин О., Эмунгания О. и др. Внематочное накопление жира в поджелудочной железе с использованием 1H-MRS: важность диабетического статуса и модуляция с потерей веса, вызванной бариатрической хирургией.Int J Obes (Лондон). 2015; 39: 480–487.
26. Стивен С., Холлингсуорт К.Г., Смолл П.К., Вудкок С.А., Пуччи А., Арибисала Б. и др. Снижение веса снижает избыток триацилглицерина поджелудочной железы, особенно при диабете 2 типа. Уход за диабетом. 2016; 39: 158–165.
27. Ceriello A, Motz E. Является ли окислительный стресс патогенетическим механизмом, лежащим в основе инсулинорезистентности, диабета и сердечно-сосудистых заболеваний? Пересмотр гипотезы об общей почве. Артериосклер Thromb Vasc Biol. 2004; 24: 816–823.
28. Мурата М., Адачи Х., Осима С., Курабаяши М. Колебания уровня глюкозы и возникающее в результате эндотелиальное повреждение коррелируют с дисфункцией β-клеток поджелудочной железы у пациентов с ишемической болезнью сердца. Диабет Res Clin Pract. 2017; 131: 107–115.
29. Аль-Хаддад М., Хашаб М., Зиромски Н., Пунгпапонг С., Уоллес М.Б., Сколапио Дж. И др. Факторы риска гиперэхогенной поджелудочной железы при эндоскопическом УЗИ: исследование случай-контроль. Поджелудочная железа. 2009; 38: 672–675.
30.Glaser J, Stienecker K. Поджелудочная железа и старение: исследование с использованием ультрасонографии. Геронтология. 2000; 46: 93–96.
31. Worthen NJ, Beabeau D. Нормальная эхогенность поджелудочной железы: связь с возрастом и жировыми отложениями. AJR Am J Roentgenol. 1982; 139: 1095–1098.
32. Ван Гинен Э.Дж., Смитс М.М., Шредер Т.С., Ван дер Пит Д.Л., Блумена Э., Малдер С.Дж. Неалкогольная жировая болезнь печени связана с неалкогольной жировой болезнью поджелудочной железы. Поджелудочная железа. 2010; 39: 1185–1190.
33.Pezzilli R, Calculli L. Стеатоз поджелудочной железы: связано ли это с ожирением или сахарным диабетом? Мир J Диабет. 2014; 5: 415–419.
34. Пекарски Дж., Гольдберг Х.И., Роял С.А., Аксель Л., Мосс А.А. Разница между числами CT печени и селезенки у здорового взрослого человека: ее полезность в прогнозировании наличия диффузного заболевания печени. Радиология. 1980; 137: 727–729.
35. Куинн С.Ф., Госинк ББ. Характерные сонографические признаки жировой инфильтрации печени. AJR Am J Roentgenol.1985; 145: 753–755.
Изображение поджелудочной железы, артикул
Введение
Поджелудочная железа – это орган брюшной полости, выполняющий как эндокринную, так и экзокринную функции. Он производит множество гормонов, которые в основном регулируют уровень сахара в крови. Как экзокринная железа, она выделяет поджелудочную жидкость, содержащую бикарбонат и пищеварительные ферменты. Обычно поджелудочную железу поражают несколько широких категорий заболеваний: панкреатит, недостаточность поджелудочной железы, кистозные поражения поджелудочной железы и опухоли поджелудочной железы.
Панкреатит – это генерализованное воспаление поджелудочной железы, вызванное активацией пищеварительных ферментов, вырабатываемых поджелудочной железой, еще находясь внутри органа. Чаще всего это может быть вызвано желчными камнями, злоупотреблением алкоголем или гипертриглицеридемией. Желчные камни являются этиологией большинства случаев острого панкреатита, от 40 до 70% [1], в то время как злоупотребление алкоголем составляет от 25 до 35%. [2] Панкреатит обычно проявляется острой болью в эпигастрии, которая может распространяться в спину. Боль в животе часто сопровождается тошнотой и рвотой.В пересмотренной классификации Атланты острый панкреатит разделен на два подтипа: интерстициальный отечный панкреатит и некротический панкреатит. Кроме того, по степени тяжести острый панкреатит подразделяется на легкий, умеренно тяжелый или тяжелый в зависимости от отсутствия органной недостаточности, наличия транзиторной или стойкой органной недостаточности соответственно [3]. Смертность от острого панкреатита составляет примерно 5%, тогда как у больных некротическим панкреатитом этот показатель выше – 17% [4]. Хронический панкреатит может возникнуть у пациентов с алкогольным расстройством, при котором рубцевание железы препятствует ее нормальному функционированию.
Поджелудочная недостаточность возникает, когда поджелудочная железа не может производить достаточно пищеварительных ферментов для расщепления пищи в пищеварительном тракте. Это состояние обычно представляет собой дефицит внешнесекреторной функции железы, который может быть вызван различными патологическими процессами, чаще всего кистозным фиброзом у детей и хроническим панкреатитом у взрослых.
Рак экзокринной железы поджелудочной железы – одна из основных причин смерти от рака в Соединенных Штатах, уступая только легким, толстой кишке и груди.Он также входит в число самых смертельных онкологических заболеваний, с коэффициентом выживаемости в течение одного года 20% и коэффициентом пятилетней выживаемости всего 5% [5]. Летальность в основном связана с незаметным началом злокачественного новообразования, при этом симптомы (например, желтуха, потеря веса и неопределенная подострая боль в эпигастрии) проявляются только на поздних стадиях болезни. Часто на момент постановки диагноза поражение оказывается неоперабельным из-за распространения на близлежащие структуры. Более одной трети опухолей после идентификации относятся к стадии IV, и менее 20% этих опухолей являются кандидатами на хирургическую резекцию.[6] [7] Самым распространенным злокачественным новообразованием является протоковая аденокарцинома с поражением экзокринных желез; большинство этих опухолей обнаруживаются в головке поджелудочной железы.
Нейроэндокринные опухоли поджелудочной железы (НЭО) – это злокачественные новообразования, которые образуются в эндокринной ткани поджелудочной железы. Также известные как опухоли островковых клеток, это редкие опухоли, встречающиеся примерно у 1 из 100000 человек, и только 1% всех опухолей поджелудочной железы являются НЕТ [8]. NET могут приводить к перепроизводству и секреции гормонов поджелудочной железы, включая инсулин, гастрин, глюкагон и вазоактивный кишечный пептид (VIP), что при представлении приводит к специфическим клиническим синдромам.
Кистозные поражения поджелудочной железы – относительно частая случайная находка при визуализации тела с распространенностью в общей популяции от 2,4 до 24%. Классификация этих кист важна, поскольку они могут быть истинными кистами, псевдокистами (обычно связанными с панкреатитом) или связанными с доброкачественными или злокачественными новообразованиями. Исторически рентгенологическая визуализация помогла определить этиологию кистозных поражений в 75–90% случаев [9]. Истинные эпителиальные кисты редки в общей популяции и классически связаны только с муковисцидозом, болезнью фон Гиппеля-Линдау, аутосомно-доминантным поликистозом почек.Псевдокисты, связанные с панкреатитом или травмой, являются наиболее частым кистозным поражением поджелудочной железы. Примерно у 20-40% пациентов с хроническим панкреатитом развиваются псевдокисты, и только у 2-3% пациентов с острым панкреатитом они разовьются. [9] Кисты, связанные со злокачественными новообразованиями, могут редко возникать с экзокринными опухолями, иногда с эндокринными опухолями или изолированно. Кистозные новообразования включают внутрипротоковые папиллярные муцинозные новообразования, муцинозные кистозные новообразования и серозные цистаденомы.
Анатомия
Анатомия поджелудочной железы и близлежащих структур имеет особое значение для понимания желчнокаменного панкреатита и хирургических противопоказаний при раке поджелудочной железы.
Общий желчный проток входит в поджелудочную железу и сливается с основным протоком поджелудочной железы непосредственно перед ампулой Фатера, где они оба впадают во вторую часть двенадцатиперстной кишки через большой сосочек двенадцатиперстной кишки. При желчнокаменном панкреатите желчный камень, вышедший из желчного пузыря, перемещается по общему желчному протоку, попадая в поджелудочную железу.Камень в желчном пузыре может застрять в ампуле Фатера, блокируя выход как общего желчного протока, так и главного протока поджелудочной железы в двенадцатиперстную кишку. Эта закупорка вызывает скопление желчи и панкреатического сока, что приводит к желчнокаменному панкреатиту.
Анатомия поджелудочной железы и окружающих структур имеет решающее значение для понимания хирургических показаний и противопоказаний при раке поджелудочной железы. Головка поджелудочной железы находится в «С-образной петле» двенадцатиперстной кишки, а крючковидный отросток загибается назад и позади верхней брыжеечной артерии и вены.Шея поджелудочной железы пересекает нижнюю полую вену и аорту около чревного ствола, в то время как хвост продолжает пересекать левую сторону живота вместе с селезеночной артерией, заканчиваясь на воротах селезенки или рядом с ними. Желудок находится перед поджелудочной железой. Все эти близлежащие структуры, особенно чревная ось и верхние брыжеечные сосуды около головки поджелудочной железы, могут быть вовлечены в быстро увеличивающееся злокачественное новообразование поджелудочной железы, усложняя хирургический доступ или делая его неоперабельным.
Обычные пленки
Использование простых рентгенограмм при оценке поджелудочной железы крайне ограничено. Кальцификаты поджелудочной железы, хотя и не являются диагностическими, могут быть видны на рентгенограммах брюшной полости при хроническом панкреатите.
Сравнение компьютерной томографии (КТ) и магнитно-резонансной томографии (МРТ) с ультразвуком
Несколько общих принципов визуализации различных частей тела важны при принятии решения, какой из этих трех методов поперечного сечения использовать и какой относительный сильные и слабые стороны каждого.В целом КТ и МРТ имеют большие поля зрения и обе очень эффективны для выявления локальных аномалий наряду с региональным или более отдаленным поражением. Ультразвук имеет ограниченное поле зрения и может быть существенно ограничен габитусом тела и находящимся над ним газом.
КТ и МРТ лучше, чем ультразвук, для характеристики твердых поражений из-за преимущества введения внутривенного контрастного вещества и различий в интенсивности сигнала, наблюдаемого на МРТ. С другой стороны, кистозные поражения могут быть обнаружены всеми тремя способами, но лучше охарактеризованы с помощью ультразвука и даже лучше с помощью МРТ.
Компьютерная томография
Компьютерная томография (КТ) – это основа визуализации поджелудочной железы. Почти всегда показан внутривенный контраст, при этом многоэтапная визуализация с улучшенной визуализацией является оптимальной для выявления и характеристики новообразований поджелудочной железы или осложнений панкреатита. Протоколы многофазной поджелудочной железы обычно включают неусиленную последовательность, «фазу поджелудочной железы» или позднюю артериальную фазу, а также последовательности фазы воротной вены.
При остром панкреатите КТ с внутривенным контрастированием покажет очаговое или диффузное увеличение паренхимы поджелудочной железы из-за интерстициального отека с неоднородным усилением. Края поджелудочной железы будут нечеткими из-за воспаления, также могут присутствовать перипанкреатические жировые отложения. Препятствующий камень в желчном пузыре может быть или не быть видимым, если он является причиной панкреатита. Осложнения могут проявляться остро или с задержкой, включая некроз, кровотечение, сосудистые осложнения, псевдокисты поджелудочной железы и образование абсцесса.Области, в которых отсутствует контрастное усиление, являются диагностическими для некроза поджелудочной железы [10]. Лучше всего визуализировать некротический панкреатит через 48–72 часа после начала; следовательно, раннее сканирование при остром панкреатите может недооценивать пациентов с некрозом. Первоначальную визуализацию рекомендуется проводить через 5-7 дней после поступления в больницу [3]. В случае инфицированного некроза могут быть очевидны пузырьки газа, что является патогномоничным для эмфизематозного панкреатита. Геморрагический панкреатит рентгенологически может проявляться как жидкость с высоким ослаблением на КТ без усиления, причем ослабление уменьшается с возрастом крови.[11] Сосудистые осложнения включают тромбоз воротной вены, который идентифицируется как отсутствие усиления или дефект наполнения воротной вены. Дополнительным сосудистым осложнением является образование аневризмы любой из перипанкреатических артерий.
Что касается хронического панкреатита, обнаружение может включать расширение главного протока поджелудочной железы, атрофию паренхимы поджелудочной железы и кальцификаты поджелудочной железы. Хотя атрофия поджелудочной железы встречается примерно у 54% пациентов с хроническим панкреатитом, это не является специфическим признаком и также может возникать при нормальном старении.[12] Псевдокисты поджелудочной железы, как правило, представляют собой скопление моноглазной жидкости без увеличения содержания твердых компонентов. [9]
Почти девять из десяти пациентов с муковисцидозом страдают недостаточностью экзокринной железы поджелудочной железы из-за непроходимости протоков и последующего фиброза и замещения жировой ткани. Эта блокада может вызвать острый панкреатит, когда внешнесекреторная функция поджелудочной железы все еще сохраняется. КТ может выявить жировое замещение поджелудочной железы, которое проявляется в виде участков с пониженным содержанием жира.В конце концов, продолжающееся замещение жировой ткани может привести к полному липоматозу поджелудочной железы, как правило, до достижения пациентом 20-летнего возраста. [13] Также могут присутствовать кальцификации и небольшие кисты поджелудочной железы. Истинные эпителиальные кисты обычно не имеют внутренних перегородок или усиления после внутривенного введения контрастного вещества.
При оценке экзокринных опухолей поджелудочной железы последовательность «фазы поджелудочной железы» лучше всего подчеркивает разницу в ослаблении между злокачественной опухолью и здоровой тканью поджелудочной железы из-за гиповаскулярности опухоли.[14] Массы будут отображаться на КТ как нечеткие. Само поражение обычно является гиподенсированным на протяжении всей последовательности артериальных фаз [15], хотя до 10% опухолей, особенно опухолей размером менее 2 см, будут изоденсными по сравнению с нормальной паренхимой поджелудочной железы [16]. Также могут быть видны сопутствующие признаки, такие как перерыв протока поджелудочной железы и признак двойного протока. Общая зарегистрированная чувствительность КТ в обнаружении рака поджелудочной железы составляет от 89 до 97% [7] с положительной прогностической ценностью 89% при прогнозировании хирургической резектабельности опухоли.[16]
Многофазная КТ с контрастным усилением также является идеальным методом визуализации для оценки нейроэндокринных опухолей поджелудочной железы. NET – это высокососудистые опухоли, которые усиливаются во время артериальной или панкреатической фазы. Во время секвенирования фазы воротной вены следует отметить вымывание. [11] Более мелкие опухоли – это четко очерченные однородные массы на КТ; однако более крупные сети могут иметь различный вид из-за некроза, кистозных изменений или кровоизлияния. Изолированные кистозные новообразования потенциально видны с помощью КТ; однако определение характеристик обычно более эффективно с помощью магнитно-резонансной томографии.Внутрипротоковые папиллярные муцинозные новообразования (IPMN) могут проявлять расширение протоков поджелудочной железы и / или кистозное поражение. Кистозные поражения обычно гипоаттенуирующие и гетерогенные. Муцинозные кистозные новообразования также проявляются как гипоаттенуирующие, но часто демонстрируют толстую усиливающую стенку при отсроченной визуализации. Серозные цистаденомы могут иметь центральный рубец с «солнечными кальцификациями», выходящими из центрального очага почти в 30% случаев [9].
Магнитный резонанс
Хотя КТ является первоначальным методом диагностики патологий поджелудочной железы, МРТ полезна для характеристики кистозных поражений и характеристики и даже идентификации некоторых солидных опухолей, особенно небольших.Кроме того, магнитно-резонансная холангиопанкреатография (MRCP) может лучше визуализировать панкреатические и желчные протоки и продемонстрировать любые сообщения или препятствия, связанные с поражением. Типичный протокол МРТ поджелудочной железы включает T1- и T2-взвешенные изображения с многофазной визуализацией после внутривенного введения гадолиния.
Оценка панкреатита в острых случаях почти всегда проводится с помощью КТ; однако МРТ сравнима с КТ и может быть полезна в некоторых сложных случаях или у пациентов, которые не могут получить йодсодержащий контраст.Т2-взвешенные последовательности с подавлением жира демонстрируют большую дифференциацию между тканями поджелудочной железы и перипанкреатическими тканями, в то же время делая любое перипанкреатическое воспаление гораздо более заметным. Т2-взвешенные изображения также могут помочь отличить простые кажущиеся псевдокисты от более сложного изнутри некроза без стенок. MRCP может продемонстрировать панкреатические и желчные протоки вместе с обнаружением желчных камней с более высокой чувствительностью, чем КТ. Т1-взвешенные изображения с подавлением жира выявляют очаговое или диффузное увеличение паренхимы поджелудочной железы с нечеткими границами, аналогично результатам КТ.Воспаленная паренхима поджелудочной железы будет гипоинтенсивной по сравнению с нормальной поджелудочной железой или печенью на Т1 и гиперинтенсивной на Т2 из-за воспаления и отека. Некроз будет выглядеть гипоинтенсивным на Т2-взвешенных изображениях и гиперинтенсивным при разжижении [17]. Кровоизлияние можно визуализировать с помощью T1- и T2-взвешенных изображений с подавлением жира, но последовательности эхо-сигнала с градиентным вызовом (GRE) также чрезвычайно чувствительны к магнитным свойствам гемоглобина. [11] Т1-взвешенные изображения с усилением гадолиния лучше всего подходят для оценки некроза и степени воспаления.
MRCP все чаще используется для диагностики хронического панкреатита благодаря его способности визуализировать обструкцию и расширение протока поджелудочной железы; однако типичные кальцификаты при хроническом панкреатите не визуализируются так эффективно, как на КТ. Атрофию поджелудочной железы можно увидеть как неровные края поджелудочной железы и снижение T1-взвешенного сигнала с отсроченным усилением после инъекции гадолиния. MRCP, усиленный секретином (sMRCP), обеспечивает лучшую визуализацию главного протока поджелудочной железы и его ветвей.Скорость кровотока в протоке поджелудочной железы также можно оценить с помощью sMRCP [12]. Псевдоцисты будут представлять собой гиперинтенсивные поражения на T2-взвешенных изображениях, в то время как псевдоцисты, содержащие кровь, будут демонстрировать повышенный сигнал на T1-взвешенных последовательностях. [9]
MR может помочь дифференцировать липоматоз поджелудочной железы от фиброзных изменений у пациентов с муковисцидозом. Фиброзное замещение поджелудочной железы будет отображаться как области гипоинтенсивности на T1- и T2-взвешенных изображениях, тогда как жировые изменения покажут обратное: гиперинтенсивность на T1- и T2-взвешенных последовательностях.[13]
Аденокарциномы поджелудочной железы выглядят гипоинтенсивными на T1-взвешенных изображениях по сравнению с обычно ярким внешним видом здоровой поджелудочной железы. Т2-взвешенные изображения менее полезны, поскольку сигнал подобен сигналу нормальной поджелудочной железы. Изображения, взвешенные по диффузии, могут показать ограниченную диффузию аденокарцином, но ограниченная диффузия не является специфической для карцином, поскольку она также может присутствовать при панкреатите. [16] Однако использование диффузионных градиентов с более низкими значениями b, коррелирующих с более низкими амплитудами, более короткими длительностями и более короткими интервалами между импульсами градиента, может усилить тонкие отклонения сигнала, взвешенного по T2.MRCP может выявить непроходимость протока в области предполагаемого небольшого образования. Также может быть виден признак двойного протока одновременного расширения общего желчного протока и протока поджелудочной железы.
Панкреатические сети появляются на МРТ как гипоинтенсивные на T1- и гиперинтенсивные на T2-взвешенных изображениях с гиперусилением после введения гадолиния во время артериальной или панкреатической фазы из-за их гиперваскулярной природы. Опухоли с крупными островковыми клетками могут иметь кистозные или некротические участки без усиления. [18] МРТ может дополнительно охарактеризовать кистозные новообразования.IPMNs должны показывать либо расширение основного протока поджелудочной железы (диффузное или сегментарное), либо множественное кистозное дольчатое образование. Муцинозные кистозные новообразования кажутся конгруэнтными с скоплениями простой кистозной жидкости, которые могут иметь уровни жидкость-жидкость на Т2-взвешенных изображениях. Постконтрастные T1-взвешенные последовательности могут показывать усиление узелков на стенке в пределах поражения. Главный панкреатический проток обычно не вовлекается. Серозная цистаденома обычно выявляет множество небольших кист, гиперинтенсивных на Т2-изображениях. Тонкие перегородки могут усиливаться, а если имеется центральный рубец, он усиливается при отсроченной визуализации.[9]
Наконец, в случаях расширения желчных протоков MRCP может помочь дифференцировать закупоривающий желчный камень (без усиления и темный на Т2) или внутрипросветное образование (увеличение массы без темного Т2-взвешенного сигнала).
УЗИ
Трансабдоминальное ультразвуковое исследование при остром панкреатите предназначено для выявления любых желчных камней и / или холедохолитиаза. В противном случае использование ультразвука в значительной степени ограничено из-за трудностей визуализации поджелудочной железы, часто из-за перекрывающих кишечных газов.[19] Воспаленная поджелудочная железа будет выглядеть гипоэхогенной и диффузно увеличенной из-за отека. При тяжелом заболевании могут присутствовать скопления безэховой жидкости, представляющие собой перипанкреатическую жидкость.
С другой стороны, эндоскопическое ультразвуковое исследование (EUS) может быть полезно при оценке хронического панкреатита. Особенности паренхимы поджелудочной железы включают гиперэхогенные очаги / тяжи из-за фиброза и кист. Может быть видно расширение главного протока поджелудочной железы более 3 мм с участками очагового сужения и гиперэхогенными краями, представляющими перидуктальный фиброз.Боковые ответвления магистрального воздуховода также могут быть расширены до диаметра более 1 мм. EUS очень чувствителен к обнаружению изменений в нормальной архитектуре поджелудочной железы; однако ограничения в основном связаны с изменчивостью оператора и его более агрессивным характером. [12] Псевдокисты проявляются в виде однокамерных анэхогенных поражений с тонкими стенками.
Липоматоз поджелудочной железы на фоне муковисцидоза обычно показывает повышенную эхогенность поджелудочной железы при ультразвуковом исследовании. Характерная дольчатая архитектура поджелудочной железы также может казаться уменьшенной.[13]
Трансабдоминальное УЗИ не является необычным методом первичной визуализации для пациентов с желтухой, болью в эпигастрии и / или потерей веса, поскольку ультразвук очень чувствителен для обнаружения обструкции желчных путей и последующего расширения. Если эти симптомы вызваны карциномой поджелудочной железы, образование обычно выглядит как нечеткая и гипоэхогенная, гиповаскулярная структура с расширением протока или без него [16].
Место УЗИ в оценке НЭО поджелудочной железы не определено.Однако эти четко очерченные, гипоэхогенные и гиперваскулярные поражения иногда можно увидеть на УЗИ, даже если их морфология неспецифична. EUS может быть полезным при установке как экзокринных, так и эндокринных опухолей, поскольку биопсия с помощью FNA может быть выполнена во время ультразвукового исследования. Дифференцировать различные кистозные поражения только с помощью ЭУЗИ может быть сложно. Однако при использовании EUS в сочетании с тонкоигольной аспирацией (FNA) это наиболее эффективный способ классификации кистозных поражений поджелудочной железы со специфичностью более 90%.[9] Морфологически муцинозные кистозные новообразования могут быть уникальными, поскольку демонстрируют внутренние перегородки разной толщины и содержат гиперэхогенный внутренний мусор. Микрокистозные серозные цистаденомы имеют очень специфические черты своей этиологии: множественные разграниченные анэхогенные кистозные поражения, разделенные тонкими перегородками, что приводит к появлению «сотов», не связанных с протоками поджелудочной железы [9]. С другой стороны, макрокистозные серозные цистаденомы могут выглядеть очень похожими на IPMNs и муцинозные кистозные новообразования при ультразвуковом исследовании.
Ядерная медицина
У пациентов с НЭО могут потребоваться исследования ядерной медицины для дальнейшего определения стадии и характеристики поражения. Исторически проводилось сканирование октреотида, в котором октреотид (аналог соматостатина) связывается с индикатором индия-111, а затем вводится перед визуализацией. Этот метод позже превратился в октреотид индия-111, который был объединен с однофотонной эмиссионной компьютерной томографией (ОФЭКТ).В последнее время все чаще используется позитронно-эмиссионная томография (ПЭТ) рецептора соматостатина (SSTR) благодаря улучшенной чувствительности для обнаружения небольших поражений, уменьшенной дозе облучения и ее способности количественно определять поглощение. SSTR PET использует индикаторы Ga-DOTATATE и Ga-DOTATOC, которые оба имеют высокое сродство к SSTR подтипа 2. [20] SSTR PET можно сочетать с МРТ или КТ для большего пространственного разрешения.
Клиническая значимость
Дифференциация процессов заболевания поджелудочной железы является сложной задачей, но она может продемонстрировать значительную заболеваемость и смертность среди населения.Понимание различных доступных методов визуализации и того, когда каждый из них подходит, имеет решающее значение. КТ и МРТ обеспечивают отличное пространственное разрешение анатомии поджелудочной железы и являются методами выбора при рассмотрении поджелудочной железы. EUS-FNA очень специфичен и ценен при диагностике кистозных поражений поджелудочной железы.
(Щелкните изображение, чтобы увеличить)
Хронический панкреатит через MRCP.На изображении виден расширенный главный проток поджелудочной железы (длинная сплошная стрелка), расширенный общий желчный проток (пунктирная стрелка) и желчный пузырь (короткая сплошная стрелка).
Предоставлено Кристофером Лисанти, MD
(Щелкните изображение, чтобы увеличить)
Жировое замещение поджелудочной железы при КТ.
Предоставлено Кристофером Лисанти, MD
(Щелкните изображение, чтобы увеличить)
Аденокарцинома поджелудочной железы по данным КТ.
Предоставлено Кристофером Лисанти, MD
(Щелкните изображение, чтобы увеличить)
Аденокарцинома поджелудочной железы при ультразвуковом исследовании.
Предоставлено Кристофером Лисанти, MD
(Щелкните изображение, чтобы увеличить)
Серозная цистаденома на КТ.
Предоставлено Кристофером Лисанти, MD
УЗИ заболеваний печени и желчевыводящих путей (Труды)
Прежде чем обсуждать патологию, необходимо проанализировать нормальный внешний вид печени, желчевыводящей системы и поджелудочной железы.Определение размера печени с помощью УЗИ неточно, и его лучше всего проводить на рентгенограммах. Ультразвук лучше всего проводить, когда животное лежит на спине (на спине), и на этом участке не должно быть шерсти. Следует нанести обильное количество изопропилового спирта и геля для УЗИ. У пород с глубокой грудью, таких как боксеры и борзые, вам может потребоваться сканирование через межреберные промежутки, чтобы полностью отобразить печень. Печень состоит из 6 долей: правой боковой, правой средней, левой боковой, левой средней, хвостатой и квадратной.Обычно с помощью УЗИ невозможно различить доли. Печень имеет однородную эхотекстуру среднего уровня (немного более эхогенная, чем почечная кора, но меньше, чем у селезенки на той же глубине изображения). Печень умеренно грубая по сравнению с селезенкой и имеет гладкие серозные края.
Внутрипеченочная сосудистая сеть представляет собой безэхогенные трубчатые структуры в паренхиме печени, которые сужаются к периферии. Есть три типа внутрипеченочных сосудов. Портальные вены имеют гиперэхогенные стенки.Стенки печеночных вен обычно не видны. И, наконец, печеночные артерии очень маленькие и обычно не видны. Внепеченочная сосудистая сеть состоит из каудальной полой вены, воротной вены и аорты. Хвостовая полая вена безэховая, трубчатая, стенки не видны. Хвостовая полая вена находится в дорсальной части живота и расположена справа от средней линии. Его можно проследить в диафрагме и сквозь нее. Портальная вена также безэховая и трубчатая, но имеет гиперэхогенные стенки.Он расположен вентрально по отношению к каудальной полой вене и расположен ближе к средней линии. Аорта расположена слева от средней линии и является наиболее дорсальным сосудом. Допплеровская оценка аорты показывает профиль артериального кровотока, в то время как как каудальная полая вена, так и воротная вена имеют профили венозного кровотока. Желчный пузырь и желчные протоки расположены в паренхиме печени. Они безэховые, с гладкими краями, разного размера (в зависимости от времени последнего приема пищи) и тонкостенные. Желчные протоки дифференцируются от внутрипеченочных сосудов с помощью допплерографии, поскольку они не имеют кровотока.Желчный пузырь расположен справа от средней линии и имеет акустическое усиление в дистальных отделах. Нормальный общий желчный проток бывает трудно идентифицировать из-за небольшого размера. Нормальный размер общего желчного протока у кошки составляет 4 мм или меньше, а у собаки – 3 мм или меньше.
Поджелудочная железа считается нормальной, если вы не видите ее на УЗИ. Нормальная поджелудочная железа состоит из правой и левой долей. Тело поджелудочной железы определяется произвольно и находится в середине правой и левой долей. Правая доля расположена дорсо-медиальнее нисходящей двенадцатиперстной кишки.Левая доля расположена каудальнее тела желудка, краниальнее поперечной ободочной кишки. Правую долю обычно легче найти, чем левую. Чтобы окончательно определить поджелудочную железу, вам сначала нужно найти нисходящую двенадцатиперстную кишку. Нисходящая двенадцатиперстная кишка обычно является самой боковой петлей кишечника в правом черепном квадранте брюшной полости. Ищите медиальнее нисходящей двенадцатиперстной кишки и краниальнее правой почки. Левую долю обычно трудно увидеть из-за наличия газов в желудке и толстой кишке.Сканируйте область каудальнее большей кривизны желудка и краниальнее толстой кишки, медиальнее селезенки.
Теперь, когда мы знакомы с нормальным внешним видом печени, желчевыводящей системы и поджелудочной железы, мы обсудим их патологию. Важно понимать, что большинство сонографических признаков заболевания печени неспецифичны. Клинически поражения гепатобилиарной системы можно разделить на те, которые затрагивают паренхиму печени, сосудистые поражения и поражения, затрагивающие только желчный пузырь или билиарную систему.Поражения также следует классифицировать по их эхогенности, распространению, наличию каких-либо артефактов и влиянию на окружающие структуры. Заболевания, поражающие тот или иной орган диффузным образом, очень трудно диагностировать, поэтому необходимо тщательное обследование и сравнение с окружающими органами.
Доброкачественные поражения паренхимы печени включают липидоз печени, узловую регенерацию, цирроз печени, гепатит, пассивный застой, абсцессы, кисты, поверхностный некролитический дерматит и доброкачественные опухоли.Липидоз печени часто встречается у кошек и возникает в результате анорексии, голодания, диабета и ожирения. Печень выглядит увеличенной на рентгенограммах и диффузно гиперэхогенной на УЗИ. Легко сравнить печень по эхогенности прилегающего серповидного жира (она должна быть гипо- или изоэхогенной по отношению к жиру). Снижена визуализация внутрипеченочной портальной сосудистой сети. Узловатая регенерация – очень частая находка как у кошек, так и у собак. Вы не можете отличить это от метастатического заболевания, используя только УЗИ.Для постановки гистологического диагноза требуется аспирация или биопсия. Они выглядят как очаговые или многоочаговые, округлые, разного размера, гипоэхогенные, а иногда даже гиперэхогенные узелки по всей печени. Цирроз печени также известен как хроническое заболевание печени «конечной стадии». Печень диффузно гиперэхогенна по всей паренхиме, а серозные края округлые и неровные (листообразные). На рентгенограммах печень небольшая. Обычно наблюдается у пожилых животных, хотя может быть конечным результатом проглатывания токсинов (пальма саго) или хронического фиброза из-за приема лекарств (фенобарбитал).Гепатит чаще всего проявляется в виде диффузно сниженной эхогенности печени. Рентгенологически печень может быть нормальной или увеличенной в размерах. При пассивном застое печень также выглядит диффузно уменьшенной по эхогенности и имеются увеличенные расширенные внутрипеченочные сосуды. Рентгенологически печень большая. Абсцессы – это чаще всего очаговые поражения. Их появление зависит от зрелости (возраста) абсцесса. Вначале центр заполнен жидкостью (гноем), которая выглядит однородной, от безэховой до гипоэхогенной.Центральная область может содержать плавающие обломки и может иметь или не иметь заднего улучшения. Стены толстые (> 3-4 мм). Позже в процессе болезни центрально расположенный гной становится уплотненным и выглядит неоднородным, от эхогенного до гиперэхогенного. Стены в это время могут быть нечеткими. Заднее усиление больше не определяется. Кисты печени встречаются чаще всего случайно. Большинство из них являются врожденными и могут быть очаговыми или мультифокальными. Они тонкостенные, заполнены безэховой жидкостью и имеют резкое усиление кзади.Часто наблюдается в сочетании с поликистозом почек. Поверхностный некролитический дерматит собак (также известный как гепатокожный синдром) наблюдается у собак среднего и старшего возраста, маленьких и средних размеров. У этих пациентов наблюдаются множественные твердые, язвенные, ороговевшие поражения и кожно-слизистые соединения, подушечки стопы, область гениталий и точки давления на локтях. Также может быть связано с глюкагономами, сахарным диабетом и гипергликемией. Печень выглядит как «соты». Это происходит из-за множества безэховых областей разного размера, окруженных решетчатым каркасом, который представляет собой регенеративные узелки, окруженные жировой соединительной тканью.Гемангиома и гепатома – доброкачественные опухоли печени, которые, к сожалению, неотличимы от злокачественных опухолей.
Злокачественные поражения паренхимы печени включают гепоатоцеллюлярную аденокарциному, холангиоцеллюлярную карциному, лимфосаркому и метастатическую неоплазию. Гепатоцеллюлярная аденокарцинома – наиболее частая первичная неоплазия печени у собак. Он имеет различный сонографический вид и может быть одиночным гиперэхогенным (наиболее часто), мультифокальным гиперэхогенным или одиночным гипоэхогенным.Часто есть плохо очерченные края, и они иногда имеют «целевой вид» (гипоэхогенный центр, окруженный гиперэхогенным ободком). Холангиоцеллюлярная карцинома обычно встречается у кошек. Он возникает из внутрипеченочных желчных протоков и, следовательно, проявляется многоочагово по всей печени и может представлять собой гипер- или гипоэхогенные узелки. Холангиоцеллюлярная карцинома также может иметь плохо очерченные края. Внешний вид лимфосаркомы сильно варьируется и может включать нормальную паренхиму печени, диффузно-гипоэхогенную, диффузно-гиперэхогенную или пятнистые гипоэхогенные узелки.Метастатическая неопсия также чаще всего бывает мультифокальной. Они также могут быть гиперэхогенными, гипоэхогенными или смешанными по эхогенности.
Заболевания сосудов печени включают пассивные (кардиогенные) застойные явления и портосистемные шунты. Пассивный (кардиогенный) застой является результатом некомпенсированного заболевания правых отделов сердца (либо трикуспидальной недостаточности, либо дилатационной кардиомиопатии, либо болезни Шагаса, либо выпота в перикарде, либо образования правостороннего сердца). Расширены и увеличены печеночные вены, диффузно снижена эхогенность паренхимы печени, расширена и увеличена каудальная полая вена.Портосистемные шунты бывают врожденными или приобретенными. Врожденные шунты обычно представляют собой один сосуд, в то время как приобретенные шунты представляют собой несколько аномальных сосудов. Чаще встречаются врожденные шунты. Внутрипеченочные шунты (постоянный венозный проток) наблюдаются у собак крупных пород, в то время как внепеченочные шунты обнаруживаются у собак и кошек мелких пород. Чувствительность обнаружения одиночных сосудов и внепеченочных шунтов очень зависит от оператора. Портальная сцинтиграфия часто используется для подтверждения диагноза, когда результаты ультразвукового исследования неубедительны.Внепеченочный, многососудистый, приобретенный шунт обычно представляет собой множественные извилистые сосуды, расположенные каудальнее печени и краниальнее левой почки.
Заболевания желчного пузыря и желчных протоков, включая желчнокаменные болезни, желчный ил и непроходимость желчных путей. Холелиты («желчные камни») легко обнаруживаются с помощью ультразвука (почти 100% чувствительность). Холелиты редко вызывают заболевания у собак и кошек (в отличие от человека). Рентгеноконтрастные и рентгенопрозрачные камни будут видны при ультразвуковом исследовании. Холелиты представляют собой гравитационно-зависимые очаговые гиперэхогенные структуры с затемнением в задней части.«Ил» желчного пузыря – чрезвычайно частая находка при УЗИ у собак. Может быть заполнен весь просвет желчного пузыря. Обычно это зависит от силы тяжести. После еды желчный пузырь частично опорожняется. Заднее затенение отсутствует. В сильно эхогенном иле может быть трудно отобразить холелиты. Появление непроходимости желчных путей зависит от уровня непроходимости. Поскольку холелитиаз у животных встречается редко, непроходимость желчных путей обычно возникает из-за сдавления просвета в результате неоплазии, инфекции или грибкового заболевания.Желчный пузырь может быть очень большим, если животное страдает анорексией. Острый и хронический холецистит вызывает диффузное утолщение стенки желчного пузыря. Однако утолщение стенки желчного пузыря не является специфическим для этого состояния и может быть вызвано множеством других заболеваний. Если газообразующие бактерии вызывают холецистит, можно отметить пузырьки газа, которые выглядят как несколько гиперэхогенных структур, которые плавают и имеют заднюю тень. Наблюдаются несколько несущественных и, следовательно, врожденных пороков развития желчевыводящих путей.У кошек может быть двулопастный желчный пузырь. Это желчный пузырь с частично разделенным просветом, который сходится в один пузырный проток. Для сравнения: двойной желчный пузырь – это два отдельных желчных пузыря, каждый со своим пузырным протоком. Патологические процессы, наблюдаемые в поджелудочной железе, включают узловую гиперплазию, панкреатит, абсцесс, инсулиному и аденокарциному. Узловая гиперплазия – это доброкачественный процесс, который проявляется как гипоэхогенные или изоэхогенные узелки. Их нельзя отличить от новообразования, и иногда они могут проявляться кистозными.Панкреатит можно диагностировать при наличии результатов ультразвукового исследования. Однако отсутствие результатов ультразвукового исследования не исключает возможности наличия панкреатита (часто встречается в легких случаях). При панкреатите средней и тяжелой степени поджелудочная железа становится гипоэхогенной (из-за кровоизлияния и некроза), с пятнами на эхотекстуре, с окружающей свободной перитонеальной жидкостью и гиперэхогенной брыжейкой (оба представляют перитонит). Другие признаки панкреатита, на которые следует обратить внимание, включают функциональную кишечную непроходимость нисходящей двенадцатиперстной кишки (толстые стенки, практически без признаков перистальтики), боковое смещение нисходящей двенадцатиперстной кишки (массовый эффект) и большой растянутый желчный пузырь с илом в нем.Абсцессы поджелудочной железы часто возникают как следствие панкреатита. Таким образом, результаты часто схожи, однако дополнительно отмечается крупное, хорошо очерченное, толстостенное, анэхогенное или гипоэхогенное образование, имеющее неровную внутреннюю границу. В поджелудочной железе распространены два типа новообразований. Аденокарцинома – наиболее часто диагностируемая опухоль. Они возникают из ацинарных клеток или протокового эпителия. Они развиваются в центральной части железы (тела). По мере роста они могут сдавливать общий желчный проток, поражать соседние сегменты желудка и двенадцатиперстной кишки и часто метастазировать в печень.Они выглядят как плохоэхогенные узелки или образования. Инсулиномы редко диагностируются с помощью УЗИ из-за очень маленького размера узелков. Большинство эндокринных опухолей являются злокачественными и имеют тенденцию распространяться на регионарные лимфатические узлы и печень, поэтому для поиска признаков метастазов рекомендуется ультразвуковое исследование. Важно понимать, что опухоли поджелудочной железы обычно представляют собой очаговые узелки или образования, и поэтому их трудно отличить от узловой гиперплазии или небольших абсцессов.
Визуализация абдоминальных проявлений муковисцидоза
Муковисцидоз (МВ) – мультисистемное заболевание с рядом абдоминальных проявлений, в том числе поражающих печень, поджелудочную железу и почки. Последние достижения в лечении респираторных осложнений этого заболевания привели к увеличению продолжительности жизни пациентов с МВ. Впоследствии все большее внимание уделяется влиянию заболеваний брюшной полости на качество жизни и выживаемость. Цирроз печени является наиболее важной внелегочной причиной смерти при МВ, однако остаются серьезные проблемы в диагностике заболеваний печени, связанных с МВ.Возможность прогнозирования пациентов с риском развития цирроза печени остается серьезной проблемой. Мы рассматриваем репрезентативные результаты визуализации брюшной полости у пациентов с МВ, выбранных из записей двух академических медицинских центров, с целью повышения осведомленности о абдоминальных проявлениях заболевания. Мы рассматриваем их презентацию и ожидаемые результаты визуализации, уделяя особое внимание задачам, стоящим перед диагностикой печеночных проявлений заболевания. Более подробное знакомство с этими абдоминальными проявлениями будет способствовать своевременной диагностике и лечению, что имеет первостепенное значение для дальнейшего улучшения результатов для пациентов с муковисцидозом.
1. Введение
Муковисцидоз (МВ) является наиболее распространенным наследственным смертельным заболеванием у кавказцев. В Ирландии самый высокий уровень заболеваемости при рождении в мире – 1 из каждых 1600 рождений [1]. Его тип наследования аутосомно-рецессивный, но может быть результатом одной из более чем 1500 мутаций гена трансмембранного регулятора муковисцидоза (CFTR), расположенного на длинном плече хромосомы 7 [2, 3]. Наиболее частым из них является делеция фенилаланина в положении 508: F508del.
Ген CFTR и его продукт, хлоридный канал, опосредованный циклическим аденозинмонофосфатом (цАМФ), играют ключевую роль в гидратации выделений организма и регуляции клеточных функций, включая транспорт натрия [3]. Дефектный генный продукт вызывает нарушение транспорта хлорид-ионов через эпителиальные клетки экзокринных желез [4], что приводит к сгущению вязких секретов, поражающих множество органов, включая легкие, печень и поджелудочную железу.
Благодаря улучшениям в лечении респираторных осложнений МВ, продолжительность жизни в этой группе населения увеличилась.Брюшные проявления CF являются обычным явлением и в некоторых случаях могут не проявляться до взрослого возраста. Многие проблемы остаются в диагностике этих абдоминальных проявлений, особенно в области заболевания печени, связанного с муковисцидозом (CFLD). CFLD является независимым фактором риска смертности при CF [5] и значительной причиной заболеваемости и смертности у части пациентов с CF. Отсутствует надежный неинвазивный метод раннего прогнозирования значительных CFLD или цирроза. Следовательно, первостепенное значение имеет знакомство с доступными инструментами скрининга и их ограничениями, ожидаемыми визуальными проявлениями абдоминального заболевания МВ и областями исследований, которые могут повлиять на их диагноз в будущем.
Взрослые составляют 45% пациентов с МВ в Ирландии [1]. Мы выбрали наиболее репрезентативные результаты визуализации брюшной полости у пациентов с МВ по всем методикам визуализации, выполненным в двух академических медицинских центрах. В этом графическом обзоре мы представляем типичные результаты УЗИ брюшной полости (УЗИ), компьютерной томографии (КТ) и магнитно-резонансной томографии (МРТ) у взрослых с МВ с акцентом на заболевания печени, связанные с МВ.
Целью этого обзора является повышение осведомленности о абдоминальных проявлениях МВ и результатах их визуализации, чтобы клиницисты были лучше оснащены для своевременной диагностики того, что становится все более значительным диапазоном состояний в этой популяции.
2. Проявления поджелудочной железы
Поджелудочная железа является наиболее часто поражаемым органом брюшной полости при МВ. Будут обсуждены патофизиология, клинические проявления и результаты визуализации типичных проявлений поджелудочной железы.
2.1. Патофизиология и клинические проявления
Заболевание поджелудочной железы вызывается уплотнением аномально концентрированного секрета поджелудочной железы, которое вызывает непроходимость проксимального протока. Это приводит к ацинарной атрофии, воспалению, прогрессирующему фиброзу, жировому замещению, кальцификации и образованию кист.
Клинические проявления дисфункции поджелудочной железы при МВ включают недостаточность поджелудочной железы, панкреатит и повышенный риск рака поджелудочной железы по сравнению с общей популяцией [6]. Поджелудочная недостаточность включает как внешнесекреторную, так и эндокринную недостаточность. Экзокринное встречается у 85%, а эндокринное – у 30–50% пациентов с МВ [7]. Это может привести к нарушению всасывания и, следовательно, к недоеданию, ухудшению здоровья и росту. Он проявляется в детстве у большинства пациентов, хотя пациенты, у которых диагностирован МВ во взрослом возрасте, с меньшей вероятностью страдают недостаточностью поджелудочной железы [7].Панкреатит встречается редко, несмотря на патологические признаки хронического воспалительного процесса, и чаще встречается у пациентов с недостаточностью поджелудочной железы [7, 8].
2.2. Патологические данные и результаты визуализации
2.2.1. Атрофия и стеатоз поджелудочной железы
Поджелудочная железа обычно атрофична при МВ и может иметь атрофию с частичным замещением жировой ткани или атрофию с полной жировой инфильтрацией. Жировая инфильтрация поджелудочной железы обычно является эхогенной на УЗИ (рис. 1 (а)) и однородно низкой по аттенюации на КТ, часто трудно отличить от нормального забрюшинного жира (рис. 1 (б)).На Т1-взвешенной МРТ наблюдается повышенная интенсивность сигнала, представляющая жировую инфильтрацию, с вкраплениями низкой интенсивности сигнала, представляющую фиброз. Поджелудочная железа может увеличиваться в размерах и заменяться жиром, что называется липоматозной псевдогипертрофией [9].
Атрофическая поджелудочная железа с частичным замещением жировой ткани небольшого размера и эхогена при УЗИ. Признаки КТ включают потерю нормального компонента мягких тканей железы, что может сопровождаться кальцификацией и неровностью протока (Рисунки 2 (a) и 2 (b)).
2.2.2. Цистоз поджелудочной железы
Замещение поджелудочной железы макроскопическими кистами встречается редко. Скорее всего, это результат гиперконцентрации белка, сгущения секрета и эктазии протоков (рис. 2 (б)). Кисты выстланы эпителием и, следовательно, являются настоящими кистами. Они заменяют нормальную паренхиму поджелудочной железы, могут смещаться, но не должны проникать в соседние структуры и не превышают 5 см в диаметре, как видно на УЗИ и КТ (рис. 2 (b)).
3. Почечные проявления
Хотя почечные осложнения при МВ встречаются нечасто, наиболее частыми проявлениями являются нефролитиаз, электролитные нарушения и острое повреждение почек (ОПП).Более редкие проявления включают прогрессирование в хроническое заболевание почек (ХБП) и паренхиматозное заболевание, включая амилоидоз, диабетическую нефропатию, нефрокальциноз, диффузный и узловой гломерулосклероз, а также токсичность ингибитора кальциневрина у пациентов после трансплантации легких [10].
Нефролитиаз встречается у 3–6% пациентов с МВ, что в три раза чаще, чем у контрольной группы того же возраста [11, 12]. Это наиболее частое проявление МВ со стороны почек (рис. 3). Моча перенасыщена оксалатом кальция, основным компонентом камней при МВ [13].Гипероксалурию связывают с хроническим использованием антибиотиков, что снижает колонизацию желудочно-кишечного тракта бактериями, которые обычно разрушают оксалат [12]. Для профилактики рекомендуются пероральные жидкости и диета с низким содержанием оксалатов. В сложных случаях может потребоваться установка антеградной нефростомы.
ХБП встречается редко, с ежегодной распространенностью 2,3%, о которой сообщалось в одном исследовании с участием 12 000 взрослых с МВ. Это удваивается с каждым последующим 10-летним возрастом [14]. Рецидивирующие эпизоды ОПП и воздействия аминогликозидов обсуждаются как основные факторы, способствующие развитию ХБП.Распространенная ХБП встречается редко, с распространенностью 0,6% для ХБП 5 стадии, а факторы риска включают трансплантацию легких, связанный с МВ диабет и рецидив ОПП [10].
4. Гепатобилиарные проявления
CFLD охватывает широкий спектр гепатобилиарных осложнений, включая холестаз, повышенные аминотрансферазы, стеатоз печени, фиброз печени, фокальный билиарный цирроз и многодольковый цирроз с портальной гипертензией или без нее. Также известно, что МВ осложняется микрогелевым пузырем, а гепатоцеллюлярная карцинома (ГЦК) описана в литературе у четырех пациентов [6, 15–17].
4.1. Этиология и классификация
CFLD возникает из-за аномально утолщенного секрета в желчном эпителии, который затем накапливается в желчных протоках, концентрируя компоненты едкой желчи в печени [2]. Генотипы-модификаторы при CF также могут способствовать тяжести CFLD. Аллель z гена SERPINA 1 имеет сильную ассоциацию (отношение шансов 5) развития CFLD с портальной гипертензией [18].
Тот факт, что CFLD не имеет последовательного определения, по крайней мере частично, является причиной значительных различий в сообщениях о распространенности CFLD в литературе.Исследования, в которых используется более широкое толкование этого термина, сообщают о распространенности 30–40%, в то время как фокальный билиарный цирроз встречается у 20–30% лиц с МВ, а многодолевой цирроз – у 5–10% [19].
Цирроз печени является наиболее важной внелегочной причиной смерти при МВ, составляя 2,5% от общей смертности [20], и, следовательно, является наиболее клинически значимой формой CFLD. Североамериканский фонд CF предложил классификацию CFLD на основе консенсуса среди гепатологов, созванного в 2007 году.Это отделяет цирроз и портальную гипертензию от других форм гепатобилиарного поражения при МВ (Таблица 1) [19].
| |||||||||||
| AST: аспартаттрансаминаза, ALT: аланинтрансаминаза и GGT: гамма-глутамилтрансф. стереть. |
4.2. Биохимические нарушения
Диагноз CFLD рассматривается, если трансаминазы и гамма-глутамилтрансфераза (GGT) превышают верхний предел нормы по крайней мере три раза подряд в течение двенадцати месяцев, с гепатомегалией или спленомегалией при осмотре или ультразвуковыми признаками гепатобилиарных аномалий. [20]. Однако, хотя основные функциональные тесты печени (LFT) могут периодически нарушаться при CF, они в значительной степени неспецифичны и считаются ненадежными в качестве маркера тяжести или прогрессирования CFLD.Между тем, пациенты с мультилобулярным циррозом могут иметь нормальные LFT [20–22]. Исследования продолжаются, чтобы определить полезные сывороточные маркеры для раннего и надежного прогнозирования CFLD и его прогрессирования.
Исследования показали, что различные комбинации маркеров фиброгенеза, таких как коллаген IV, пролилгидроксилаза, тканевый ингибитор уровня металлопротеиназы 1 и хемоаттрактантный белок 1 моноцитов, могут отличить пациентов с подтвержденной биопсией CFLD от пациентов с CF, но без заболевания печени, и на ранних стадиях. поздний фиброз [23, 24].МикроРНК также являются многообещающими: исследования показывают, что различные miРНК могут предсказывать быстрое начало заболевания печени, в то время как конкретные комбинации могут отличать фиброз F0 от F3-4 [25]. Они требуют дальнейшего изучения для клинического применения и, вероятно, являются дорогостоящими. Более простые биомаркеры, которые более доступны, такие как соотношение аспартатаминотрансферазы к тромбоцитам (APRI) и Fib-4, показали многообещающие результаты в одном контролируемом биопсией исследовании; APRI дифференцировал CFLD от CF без заболевания печени [чувствительность 73%, специфичность 70%, в полном соответствии с гистологическим определением стадии в 37% случаев и в пределах одной стадии в 73% случаев], в то время как было показано, что Fib-4 предсказывает портальную гипертония при постановке диагноза [25].
4.3. Билиарные проявления
Билиарная система может поражаться у пациентов с МВ, но симптомы возникают редко. Вдыхание желчных выделений вызывает гиперплазию слизистых оболочек желчного пузыря и желчных протоков [26]. Этот процесс приводит к увеличению ила в желчных путях и развитию микрогелочного пузыря, возможно, из-за стеноза пузырных протоков и вторичной атрофии желчного пузыря [6, 27].
Холелитиаз может возникать из-за повышенной секреции желчных кислот фекалиями на фоне недостаточности поджелудочной железы, что приводит к образованию литогенной желчи [28].Холангиопатия проявляется в виде расширения внутрипеченочных желчных протоков (рис. 1 (c)), образования пузырей или стриктуры и наблюдалась у детей и взрослых с CFLD. Аномалии желчных протоков также были зарегистрированы у значительного числа пациентов с МВ без клинически выраженных заболеваний печени [29]. Результаты визуализации включают стриктуры внутри- и внепеченочных желчных протоков (рисунки 4 (а) и 4 (b)), желчнокаменную болезнь и микрогелевый пузырь (рисунок 5 (а)). Также сообщается о холедохолитиазе и холецистите (рис. 6).
4.4. Стеатоз печени
Стеатоз – одно из наиболее частых проявлений печени в популяции пациентов с МВ, встречающееся у 23–75% пациентов с МВ [30]. У пациентов может быть гладкая гепатомегалия, но обычно она протекает бессимптомно, без признаков портальной гипертензии. Это проявляется в повышенной эхогенности печени при УЗИ (рис. 7), низком затухании на КТ и снижении интенсивности сигнала Т2 на МРТ.
Стеатоз ранее считался доброкачественным как при МВ [31], так и в общей популяции [32].Однако растущая распространенность неалкогольной жировой болезни печени (НАЖБП) привлекла повышенное внимание к стеатозу, и, хотя неалкогольный стеатогепатит (НАСГ) традиционно считался единственной формой НАЖБП, представляющей значительный риск прогрессирования фиброза, недавние исследования теперь привлекли внимание к этой проблеме. ранее недооцениваемый риск прогрессирования фиброза у пациентов со стеатозом [33, 34].
В метаанализе, включающем 11 исследований, из которых 133 пациента имели НАЖБП с парными биопсиями, 39.У 1% развился прогрессирующий фиброз. Годовая скорость прогрессирования фиброза у пациентов с НАЖБП с фиброзом стадии 0 на исходном уровне составляла 0,07 стадии по сравнению с 0,14 стадии у пациентов с НАСГ. Pais et al. наблюдали, что 13 из 16 пациентов с НАЖБП и легким воспалением на исходном уровне прогрессировали до типичного НАСГ или мостовидного фиброза, в то время как только 1 из 5 пациентов с простым стеатозом прогрессировал до НАСГ [34]. В целом, эти исследования показывают, что у пациентов с НАЖБП может развиваться прогрессирующий фиброз, хотя и медленнее, чем у пациентов с НАСГ, и цирроз может развиваться, если стеатоз переходит в стеатогепатит и последующий фиброз.По мере развития нашего понимания естественной истории стеатоза при НАЖБП наше понимание его значения в популяции МВ также может развиваться.
4.5. Фиброз: очаговый билиарный цирроз
Фокальный билиарный цирроз (FBC), характеризующийся фокальным портальным фиброзом и холестазом, является гистопатологическим поражением, типичным для заболевания печени, связанного с МВ. Он возникает в результате обструкции желчных путей и прогрессирующего перипортального фиброза и может прогрессировать до многодолевого цирроза и портальной гипертензии, хотя и очень редко [20].Обычно он клинически бесшумный без повышенных трансаминаз.
Типичным признаком УЗИ является перипортальная эхогенность (рисунки 8 (а) и 8 (б)). Это коррелирует с патологическими находками клеток, содержащих жировые глобулы в фиброзных воротных трактах, и клеток в перипортальной паренхиме печени, которые содержат большие нагруженные жиром вакуоли [27]. Результаты МРТ включают сигнал высокой интенсивности в перипортальных областях на Т1-взвешенном изображении (Рисунки 8 (c) и 8 (d)) [7].
4.6. Мультилобулярный цирроз
Мультилобулярный цирроз, хотя и встречается редко, является наиболее клинически значимой формой CFLD и имеет оценочную среднюю распространенность 5.6% согласно одному обзору из 12 отчетов, в том числе 4446 пациентов [19]. Проспективное исследование 177 пациентов продемонстрировало средний возраст на момент постановки диагноза 7 лет (диапазон от 2 месяцев до 18 лет) с частотой 2,5 на 100 пациенто-лет в течение первого десятилетия жизни, которая после этого резко снижается [35]. Мультилобулярный цирроз несет с собой риск портальной гипертензии и варикозного расширения вен с распространенностью 4,2% и 2,4% соответственно [19].
Заболевание печени при МВ часто не проявляется до поздних стадий заболевания.Даже при развитии мультилобулярного цирроза пациенты могут оставаться бессимптомными до тех пор, пока не разовьются признаки портальной гипертензии [19]. Клинически мультилобулярный цирроз представляет собой твердую узловатую печень с гепатомегалией или без нее.
Патологически он характеризуется диффузным циррозом печени с множественными регенеративными узелками, а визуализация выявляет узловой контур печени с грубой гетерогенной паренхимой (рис. 8 (b)) [6]. На КТ и МРТ видны множественные регенеративные узелки, окруженные полосами гипоинтенсивного фиброза Т2 (Рисунки 8 (c) и 8 (d)) [27].
4.7. Осложнения при CF Циррозе
4.7.1. Портальная гипертензия и связанные с ней осложнения
Если портальная гипертензия осложняет проявление мультилобулярного цирроза, пациенты могут иметь варикозное расширение вен, асцит или спленомегалию, которые можно легко идентифицировать на УЗИ и КТ (Рисунки 8 (b) и 8 (c)). Сидеротические узелки в селезенке, также известные как тельца Гамна-Ганди, являются еще одним признаком портальной гипертензии, наблюдаемой на МРТ, и возникают из-за кровотечения в селезенке (рис. 9) [27].Следует отметить, что портальная гипертензия может присутствовать у пациентов без цирроза [19].
Rowland и его коллеги определили CFLD с портальной гипертензией как независимый фактор риска смертности, при этом 10-летняя парная когорта продемонстрировала почти трехкратное увеличение риска смерти по сравнению с контрольной группой CF без заболевания печени [5]. Однако литература, посвященная этому открытию, предполагает, что это не является общепринятым мнением [35–37].
4.7.2. Гепатоцеллюлярная карцинома
ГЦК может возникать у пациентов с циррозом печени любой этиологии.При увеличении выживаемости у пациентов с МВ существует риск ГЦК. В литературе описано четыре таких случая [6, 15–17]. Типичные особенности визуализации этого поражения у 35-летнего мужчины с МВ и циррозом показаны на рисунке 9. ГЦК обычно характеризуется хорошо очерченным поражением, которое является гипоэхогенным на УЗИ (рисунок 9 (а)) и низкой интенсивностью сигнала. на Т1-взвешенной МРТ без усиления (рис. 9 (b)) с активным усилением на МРТ артериальной фазы с использованием гадолиниевого контраста (рис. 9 (c)) [38].Также может наблюдаться размывание контраста на изображениях с отсроченной фазой. Аналогичные функции улучшения видны при использовании динамической улучшенной КТ.
Американская ассоциация по изучению заболеваний печени (AASLD), обновленная в 2010 году, рекомендует проводить в США два раза в год скрининг на ГЦК у любого пациента с циррозом, полагаясь на визуализацию и / или биопсию для постановки диагноза. Узлы размером более 1 см следует оценивать с помощью 4-фазной мультидетекторной КТ или динамической МРТ с контрастным усилением для оценки артериального усиления и вымывания воротной вены или более поздней фазы.Если эти данные отсутствуют, рекомендуется продолжить визуализацию с контрастным усилением или биопсию [39].
4.8. Визуализация и проблемы ранней диагностики CFLD
Хотя CFLD является наиболее значительным абдоминальным проявлением МВ с точки зрения смертности, оно остается наиболее сложным с точки зрения раннего распознавания и диагностики. Поэтому мы посвящаем этот раздел обсуждению текущих проблем и будущих перспектив диагностики CFLD применительно к визуализации.
Ультразвук более чувствителен, чем LFT при обнаружении CFLD [20], с предположениями, что аномальная эхогенность может предшествовать клиническим или биохимическим проявлениям заболевания печени. Однако было показано, что положительная прогностическая ценность УЗИ составляет лишь 33%, и хотя аномальное УЗИ может предсказывать наличие умеренного или тяжелого заболевания печени, нормальное УЗИ не исключает значительного фиброза печени [40].
Биопсия предназначена для случаев сомнений в диагностике, которые могут изменить лечение [20].Тем не менее, некоторые исследования предполагают, что гистопатологическое подтверждение и определение стадии фиброза с помощью биопсии печени при первоначальном диагнозе CFLD может быть оправдано, учитывая его превосходные характеристики в прогнозировании клинически значимых CFLD и портальной гипертензии по сравнению с неинвазивными альтернативами, которые в настоящее время используются при скрининге и последующем наблюдении [21]. В 12-летнем проспективном анализе 40 детей с МВ, Левиндон и его коллеги продемонстрировали, что чрескожная биопсия с двойным проходом снижает ошибку выборки и может предсказать портальную гипертензию, в то время как отклонения от нормы клинического обследования, функциональных тестов печени (LFT) и УЗИ не смогли предсказать ни одного из них. фиброза или возникновения портальной гипертензии [21].
Однако в настоящее время в руководствах по передовой практике рекомендуется проводить скрининг на CFLD с использованием основных лабораторных маркеров (LFT, тромбоциты и INR) и УЗИ брюшной полости. Дальнейшая визуализация с помощью КТ или МРТ рекомендуется, если при УЗИ обнаруживаются поражения печени или желчевыводящих путей без достаточной ясности для постановки диагноза [20].
КТ и МРТ полезны для отличия фиброза от стеатоза, который может быть трудно определить при УЗИ, а также полезны для дальнейшего исследования очаговых поражений [20].Преимущество МРТ заключается в том, что это всестороннее неинвазивное исследование печени, желчных путей и поджелудочной железы без воздействия ионизирующего излучения, что является важным фактором, учитывая необходимость возможного последующего наблюдения. Durieu et al. продемонстрировали способность MR выявлять внутрипеченочные билиарные аномалии у пациентов с МВ без клинически выраженного заболевания печени, указывая на вероятную недооценку УЗИ и MRCP как вариант для выявления ранних билиарных аномалий [29].
Транзиторная эластография (TE) измеряет жесткость печени и является механизмом определения стадии фиброза, который уже подтвержден для хронических заболеваний печени, таких как гепатит С.Ранние исследования с использованием TE для неинвазивной оценки фиброза печени у пациентов с МВ не показали явного улучшения по сравнению с УЗИ [41]. ARFI – это новый метод эластографии, основанный на США, который, в отличие от фиброскана, может использоваться на обеих долях печени [42]. Более поздние исследования предложили как фиброскан, так и ARFI в качестве чувствительных инструментов диагностики фиброза [42] и предоставили некоторые доказательства его использования в качестве надежного инструмента обнаружения цирроза CF [43] с потенциалом для скрининга портальной гипертензии [44]. Одно проспективное исследование с использованием ARFI и TE подтвердило применимость этих тестов для оценки фиброза печени при МВ; однако необходимы дальнейшие исследования с более длительным периодом наблюдения [45].
Консенсус в отношении пороговых значений для ранней диагностики CFLD остается труднодостижимым, и требуются дальнейшие исследования в этой области, хотя это может частично объясняться отсутствием общепринятого консенсусного определения CFLD [45]. В конечном итоге TE является многообещающим и, при дальнейших исследованиях, может улучшить диагностику фиброза печени у пациентов с МВ, если его использовать в сочетании с современными методами скрининга. Хотя нет никаких контролируемых биопсией исследований для этой техники при CFLD, авторы ссылаются на установленные доказательства корреляции TE с фиброзом при других заболеваниях печени и ставят под сомнение этичность контролируемых биопсией исследований в педиатрической популяции из-за ее инвазивного характера, связанных рисков, и вопросы, связанные с ошибкой выборки [41].
5. Заключение
Абдоминальные проявления МВ приобретают все большее значение в свете увеличения выживаемости взрослого населения с МВ. Раннее распознавание и диагностика этих состояний и их осложнений будут играть важную роль в улучшении качества жизни и дальнейшей выживаемости пациентов с МВ. Значительная CFLD с циррозом или портальной гипертензией представляет собой одну из самых больших проблем в этом отношении.
Отклонения от нормы клинического обследования, LFT и результаты УЗИ являются плохими предикторами прогрессирования цирроза или портальной гипертензии [21].Необходимы исследования, позволяющие надежно прогнозировать цирроз или портальную гипертензию, чтобы лучше идентифицировать тех, кто находится в группе риска, и инициировать более ранние профилактические меры и лечение осложнений. В конечном итоге достижению этой цели может способствовать ряд многообещающих методов, но ожидается дальнейшее исследование.
Осведомленность о абдоминальных проявлениях МВ и знакомство с ожидаемыми клиническими проявлениями и результатами визуализации имеют первостепенное значение для своевременной диагностики и надлежащего ведения пациентов с МВ.
Конкурирующие интересы
Авторы заявляют, что у них нет конкурирующих интересов.
Жирная поджелудочная железа в связи с инсулинорезистентностью и метаболическим синдромом у детей с ожирением
Ссылки
1. Lopes HF, Corrêa-Giannella ML, Consolim-Colombo FM, Egan BM. Синдром висцерального ожирения. Синдром метаболизма диабетола 2016; 8: 40.10.1186 / s13098-016-0156-2 Поиск в Google Scholar
2. Патель П., Абате Н. Распределение жира в организме и инсулинорезистентность.Nutrients 2013; 5: 2019–27.2373914310.3390 / nu5062019 Поиск в Google Scholar
3. Ou HY, Wang CY, Yang YC, Chen MF, Chang CJ. Связь между неалкогольной жировой болезнью поджелудочной железы и диабетом. Сукоян С.С., редакторы. PLoS One 2013; 8: e62561.10.1371 / journal.pone.0062561 Поиск в Google Scholar
4. Катандзаро Р., Каффари Б., Италия А., Маротта Ф. Изучение метаболического синдрома: неалкогольная жировая болезнь поджелудочной железы. World J Gastroenterol 2016; 22: 7660–75.2767834910.3748 / wjg.v22.i34.7660 Поиск в Google Scholar
5. Мацуда А., Макино Н., Тозава Т., Сирахата Н., Хонда Т. и др. Накопление жира в поджелудочной железе, фиброз и повреждение ацинарных клеток у крыс с диабетом Цукера, страдающих ожирением, которые постоянно получали диету с высоким содержанием жиров. Поджелудочная железа 2014; 43: 735–43.2471782310.1097 / MPA.0000000000000129 Поиск в Google Scholar
6. Wong VW, Wong GL, Yeung DK, Abrigo JM, Kong AP, et al. Жирная поджелудочная железа, инсулинорезистентность и функция β-клеток: популяционное исследование с использованием магнитно-резонансной томографии жирной воды.Am J Gastroenterol 2014; 109: 589–97.2449275310.1038 / ajg.2014.1 Поиск в Google Scholar
7. Пасифико Л., Ди Мартино М., Анания С., Андреоли Г.М., Беззи М. и др. Жир поджелудочной железы и функция β-клеток у детей с избыточным весом / ожирением и неалкогольной жировой болезнью печени. World J Gastroenterol: WJG 2015; 21: 4688–95.10.3748 / wjg.v21.i15.4688 Поиск в Google Scholar
8. Рамич Э., Праско С., Муянович О.Б., Гавран Л. Метаболический синдром – теория и практика. Materia Socio-Medica 2016; 28: 71–3.10.5455 / msm.2016.28.71-7327047273 Искать в Google Scholar
9. ВОЗ. Отчет о состоянии неинфекционных заболеваний в мире. : 79–94. 2014. Поиск в Google Scholar
10. Четвертый отчет по диагностике, оценке и лечению высокого кровяного давления у детей и подростков. Pediatrics 2004; 114 (2 Suppl 4th Report): 555–76. Ищите в Google Scholar
11. Таннер Дж. Рост в подростковом возрасте, 2-е изд. Спрингфилд: Томас. 1962. Поиск в Google Scholar
12. Галли И., Салах Н., Хуссьен Ф., Эрфан М., Эль-Руби М. и др.В: Proceedings of the 1 st National Congress for Egypt Growth Curves, Cairo University, 11 декабря 2003. Опубликовано в: Sartorio A, Buckler JM, Marazzi N. Египетские кривые роста 2002 для младенцев, детей и подростков. Crescere nel mondo, 2008, издательство Ferring. Искать в Google Scholar
13. Бакопулу Ф., Эфтимиу В., Ландис Дж., Рентумис А., Хрусос Г. П. и др. Эталонные процентили окружности талии, отношения талии к бедрам и отношения талии к росту для абдоминального ожирения среди греческих подростков.BMC Pediatrics 2015; 15: 50.10.1186 / s12887-015-0366-z25935716 Поиск в Google Scholar
14. Куртоглу С., Хатипоглу Н., Мазичиоглу М., Кендиричи М., Кескин М. и др. Инсулинорезистентность у детей и подростков с ожирением: пороговые уровни HOMA-IR в препубертатном и пубертатном периодах. J Clin Res Pediatr Endocrinol 2010; 2: 100–6.2127432210.4274 / jcrpe.v2i3.100 Поиск в Google Scholar
15. Зиммет П., Альберти Г., Кауфман Ф. Целевая группа Международной федерации диабета по эпидемиологии и профилактике диабета: The метаболический синдром у детей и подростков.Lancet 2007; 369: 2059–61.10.1016 / S0140-6736 (07) 60958-117586288 Поиск в Google Scholar
16. Ли Дж. С., Ким Ш., Джун Д. В., Хан Дж. Х., Джанг Э. и др. Клинические последствия жировой ткани поджелудочной железы: корреляция между жировой тканью поджелудочной железы и метаболическим синдромом. World J Gastroenterol 2009; 15: 1869–75.10.3748 / wjg.15.186919370785 Поиск в Google Scholar
17. Чан Р.С., Ву Дж. Профилактика избыточного веса и ожирения: насколько эффективен нынешний подход общественного здравоохранения. Int J Environ Res Public Health 2010; 7: 765–83.10.3390 / ijerph703076520617002 Поиск в Google Scholar
18. Мисра А., Ануп С., Гулати С., Мани К., Бхатт С.П. и др. Структура жировых отложений, печеночный жир и объем поджелудочной железы у не страдающих ожирением азиатских индейцев с диабетом 2 типа в Северной Индии: исследование случай-контроль. Алиси А, изд. PLoS One 2015; 10: e0140447.10.1371 / journal.pone.0140447 Поиск в Google Scholar
19. Стааф Дж., Лабмайр В., Полмихл К., Манелл Х, Сен Дж. И др. Жир поджелудочной железы связан с метаболическим синдромом и висцеральным жиром, но не связан с функцией бета-клеток или индексом массы тела при детском ожирении.Поджелудочная железа 2017; 46: 358–65.10.1097 / MPA.000000000000077127941426 Поиск в Google Scholar
20. Толедо-Коррал С.М., Альдерете Т.Л., Ху Х.Х., Наяк К., Эсплана С. и др. Внематочное отложение жира у подростков с преддиабетическим избыточным весом и ожирением из числа меньшинств. J Clin Endocrinol Metab 2013; 98: 1115–21.2338664710.1210 / jc.2012-3806 Поиск в Google Scholar
21. Макино Н., Ширахата Н., Хонда Т., Андо Й, Мацуда А. и др. Гиперэхогенность поджелудочной железы, связанная с гипоадипонектинемией и инсулинорезистентностью: японское популяционное исследование.World J Hepatol 2016; 8: 1452–8.10.4254 / wjh.v8.i33.145227957243 Поиск в Google Scholar
22. Редер Х., Хальдорсен И.С., Эрсланд Л., Грюнер Р., Тахст Т. и др. Липоматоз поджелудочной железы является структурным маркером у детей, не страдающих диабетом, с мутациями карбоксил-сложноэфирной липазы. Diabetes 2007; 56: 444–9.1725939010.2337 / db06-0859 Поиск в Google Scholar
23. Heni M, Machann J, Staiger H, Schwenzer NF, Peter A, et al. Жир поджелудочной железы отрицательно связан с секрецией инсулина у людей с нарушением глюкозы натощак и / или нарушенной толерантностью к глюкозе: исследование ядерного магнитного резонанса.Diabetes Metab Res Rev 2010; 26: 200–5.10.1002 / dmrr.107320225188 Поиск в Google Scholar
24. Беговатц П., Коляки С., Вебер К., Страсбургер К., Новотны Б. и др. Инфильтрация жировой ткани поджелудочной железы, стеатоз паренхимы и функция бета-клеток у людей. Diabetologia 2015; 58: 1646–55.10.1007 / s00125-015-3544-525740696 Поиск в Google Scholar
25. Тушуйзен М.Э., Бунк М.К., Поуэлс П.Дж., Бонтемпс С., ван Вейсберг Дж. Х. и др. Содержание жира поджелудочной железы и функция бета-клеток у мужчин с диабетом 2 типа и без него.Diabetes Care 2007; 30: 2916–21.10.2337 / dc07-032617666465 Поиск в Google Scholar
26. Ле К.А., Вентура Е.Е., Фишер Дж. К., Дэвис Дж. Н., Вайгенсберг М. Дж. И др. Этнические различия в накоплении жира поджелудочной железы и его взаимосвязь с другими жировыми отложениями и маркерами воспаления. Diabetes Care 2011; 34: 485–90.10.2337 / dc10-076021270204 Поиск в Google Scholar
27. Ræder H, Vesterhus M, El Ouaamari A, Paulo JA, McAllister FE, et al. Отсутствие диабета и экзокринной дисфункции поджелудочной железы в трансгенной модели карбоксил-сложноэфирной липазы-MODY (диабет зрелого возраста у молодых).PLoS One 2013; 8: e60229.10.1371 / journal.pone.0060229 Поиск в Google Scholar
28. Chang CJ, Jian DY, Lin MW, Zhao J-Z, Ho L-T, et al. Доказательства у детей с ожирением: вклад гиперлипидемии, ожирения-воспаления и чувствительности к инсулину. Петерсон Дж, изд. PLoS One 2015; 10: e0125935.10.1371 / journal.pone.0125935 Поиск в Google Scholar
29. Сингх Р.Г., Юн Х.Д., Поппитт С.Д., Планк Л.Д., Петров М.С. Внематочное накопление жира в поджелудочной железе и его биомаркеры: систематический обзор и метаанализ.Diabetes Metab Res Rev 2017; 33: e2918.10.1002 / dmrr.2918 Поиск в Google Scholar
30. Fraulob JC, Ogg-Diamantino R, Fernandes-Santos C, AguilaMB, Mandarim-de-Lacerda CA. Мышиная модель метаболического синдрома: инсулинорезистентность, ожирение печени и неалкогольная жировая болезнь поджелудочной железы (NAFPD) у мышей C57BL / 6, получавших диету с высоким содержанием жиров. J Clin Biochem Nutr 2010; 46: 212–23.10.3164 / jcbn.09-83204
Поиск в Google Scholar
31. Гулло Л., Салиццони Е., Серра С., Калкулли Л., Бастагли Л. и др.Может ли стеатоз поджелудочной железы объяснить обнаружение гиперферментемии поджелудочной железы у пациентов с дислипидемией? Поджелудочная железа 2006; 33: 351–3.10.1097 / 01.mpa.0000240603.26312.2a17079938 Поиск в Google Scholar
32. Куси К. Роль жировой ткани и липотоксичность в патогенезе диабета 2 типа. Curr Diab Rep 2010; 10: 306–15.10.1007 / s11892-010-0122-620556549 Поиск в Google Scholar
33. Сепе П.С., Охри А., Санака С., Берзин Т.М., Сехон С. и др. Проспективная оценка жировой ткани поджелудочной железы с помощью EUS.Gastrointest Endosc 2011; 73: 987–93.10.1016 / j.gie.2011.01.01521521567 Поиск в Google Scholar
34. Маджио А.Б., Мюллер П., Вакер Дж., Виаллон М., Белли Д.К. и др. Повышенная фракция жира поджелудочной железы присутствует у тучных подростков с метаболическим синдромом. J Pediatr Gastroenterol Nutr 2012; 54: 720–6.2215792810.1097 / MPG.0b013e318244a685 Поиск в Google Scholar
35. Singh RG, Yoon HD, Wu LM, Lu J, Plank LD, et al. Внематочное накопление жира в поджелудочной железе и его клиническое значение: систематический обзор, метаанализ и мета-регресс.Метаболизм 2017; 69: 1–13.10.1016 / j.metabol.2016.12.01228285638 Поиск в Google Scholar
36. Росси А.П., Фантин Ф., Замбони Г.А., Маццали Г., Зойко Э. и др. Влияние умеренной потери веса на печеночные, панкреатические и висцеральные липиды у лиц с ожирением. Nutr Diabetes 2012; 2: e32.2344953110.1038 / nutd.2012.5 Поиск в Google Scholar
37. Герреро-Ромеро Ф., Сименталь-Мендиа Л.Е., Гонсалес-Ортис М., Мартинес-Абундис Е., Рамос-Завала М.Г. и др. Продукт триглицеридов и глюкозы, простой показатель чувствительности к инсулину.Сравнение с зажимом для эугликеми-гиперинсулинемии. J Clin Endocrinol Metab 2010; 95: 3347–51.10.1210 / jc.2010-028820484475 Искать в Google Scholar
Ошибки при эндоскопической ультрасонографии и как их избежать | UEG
Чрезмерная диагностика солидных поражений поджелудочной железы как рак
Воспалительные поражения составляют 15-25% всех очаговых солидных масс поджелудочной железы. 10 , 28 , 51 , 52 , 59 С другой стороны, 6–10% хирургических образцов после процедуры Уиппла, выполненных при подозрении на рак, являются доброкачественными образованиями, 25% из них – аутоиммунный панкреатит (АИП). 60 На основе клинико-гистопатологического профиля были установлены два различных подтипа AIP – тип 1 и тип 2. 61 Современные согласованные на международном уровне диагностические критерии для диагностики AIP включают пять категорий: характерные результаты визуализации паренхимы и протока поджелудочной железы, серология, поражение других органов, гистопатология поджелудочной железы и ответ на лечение стероидами. 62 AIP типа 1 (называемый лимфоплазмоцитарным склерозирующим панкреатитом) представляет собой панкреатическое проявление системного заболевания (так называемое заболевание IgG4) и часто связано с поражением других органов. 63 Тип 2 AIP также известен как идиопатический протоковый панкреатит. Несмотря на согласованные диагностические критерии, диагностика AIP часто остается сложной задачей. 64,65 Уровень IgG4 в сыворотке полезен для установления диагноза AIP типа 1, но ему не хватает чувствительности и специфичности, и только 22–23% пациентов соответствуют критериям для диагностики заболевания, связанного с IgG4. 63 , 66
Пациенты с АИП обращаются с типичным острым панкреатитом или болями в животе, но также с желтухой и / или новообразованием поджелудочной железы, которое часто имитирует карциному поджелудочной железы.Классические результаты EUS для AIP включают диффузное увеличение поджелудочной железы с гипоэхогенной, неоднородной и неоднородной паренхимой (рис. 5а). 67–69 EUS может также демонстрировать очаговое гипоэхогенное образование, наиболее часто локализованное в головке поджелудочной железы, индуцирующее сужение главного протока поджелудочной железы (MPD) с утолщением стенки протока и обычно без расширения вверх по течению. Иногда образование может включать перипанкреатические сосуды (рисунок 5b), вызывать дилатацию выше по течению MPD, связанную с увеличением перипанкреатических лимфатических узлов, имитируя рак поджелудочной железы. 67,68 Наличие диффузного увеличения поджелудочной железы, гипоэхогенного утолщения MPD и / или стенки желчного протока, гипоэхогенного перипанкреатического «ореола» чаще наблюдается у пациентов с подтвержденным диагнозом AIP, чем у пациентов с раком поджелудочной железы.
Ключевым признаком и ключом к наличию AIP является обнаружение IgG4-ассоциированного холангита со значительным утолщением желчных протоков и, в некоторых случаях, стенкой желчного пузыря. 70,71 В отличие от злокачественных новообразований поджелудочной железы, при которых поражение желчных путей более нерегулярно, утолщение желчных протоков при холангите AIP IgG4 является правильным, однородным, с гладкими внутренними и внешними краями.Утолщение может распространяться на пузырный проток и желчный пузырь (рис. 6).
Учитывая отсутствие патогномоничных функций EUS для дифференциальной диагностики солидного новообразования поджелудочной железы, было разработано несколько методов улучшения изображений. CH-EUS позволяет оценивать увеличение опухоли поджелудочной железы с помощью ультразвуковых контрастных агентов в режиме реального времени с помощью специальных методов визуализации и, по-видимому, улучшает их характеристики. 6 , 10 , 51 , 52 , 72 Очаговые образования поджелудочной железы, связанные с AIP, а также утолщение желчных протоков показывает гипер- или изоусиление 7), тогда как гипоусиленное поражение с большой вероятностью указывает на аденокарциному. 6 , 10 , 51 , 52 , 73
Ультразвуковая эластография (УЗ-ЭГ) – это метод диагностики, основанный на определении характеристик эластичности тканей. Качественная EUS-эластография, основанная на жесткости ткани путем измерения деформации ткани, полезна для характеристики поражений поджелудочной железы и лимфатических узлов, но имеет низкую надежность и воспроизводимость. 74,75 Эластография сдвиговой волной (SWE) – это количественная эластография, основанная на измерениях распространения поперечной волны, 75 , недавно внедренная в системы EUS, продемонстрировала свою полезность для выявления фиброза поджелудочной железы, хронического панкреатита и, в последнее время, корреляции между заболеванием активность и эластичность поджелудочной железы при AIP. 75,76
Получение ткани под контролемEUS полезно для получения адекватного образца ткани для гистологической диагностики AIP, что особенно важно для диагностики AIP типа 2, «серонегативного» AIP (нормальный или <2 ULN уровня сыворотки IgG4), но преимущественно для исключения рака поджелудочной железы, особенно при очаговом новообразовании. AIP - это особенно «хитрый» объект с цитологической точки зрения. Образцы, полученные с помощью игл 22G / 25G FNA, обычно имеют небольшой размер и не имеют структуры ткани, поэтому они дают ложноположительные результаты для атипичных клеток, которые могут имитировать злокачественные новообразования. 77,78 Чтобы преодолеть это ограничение, для диагностики AIP использовались иглы для биопсии большего калибра или режущие иглы. 79
Появились недавно разработанные иглы EUS-FNB, в том числе ProCore® (Cook Ireland, Лимерик, Ирландия), SharkCore ™ (Covidien / Medtronic, Бостон, Массачусетс) и Acquire ™ (Boston Scientific, Мальборо, Массачусетс), и продемонстрировали, что низкая частота осложнений, возможность получить образцы биопсии и высокая диагностическая ценность при AIP, с превосходством иглы 22G с острием Franseen по сравнению с иглой со скосом вперед 20G для диагностики AIP типа 1 в одном исследовании. 80–83 Специфические результаты EUS и основная биопсия под контролем EUS значительно улучшили дифференциальную диагностику между AIP и раком поджелудочной железы, избегая ненужного хирургического вмешательства.
