Признаки гепатомегалии диффузных изменений поджелудочной железы: Диффузные изменения печени и поджелудочной(Гепатомегалия) – что это такое? | Нетгастриту
Признаки гепатомегалии диффузных изменений паренхимы печени – Profile – Niagara Movement for Justice in Palestine Israel Forum
ПОДРОБНЕЕ ЗДЕСЬ
20 мин.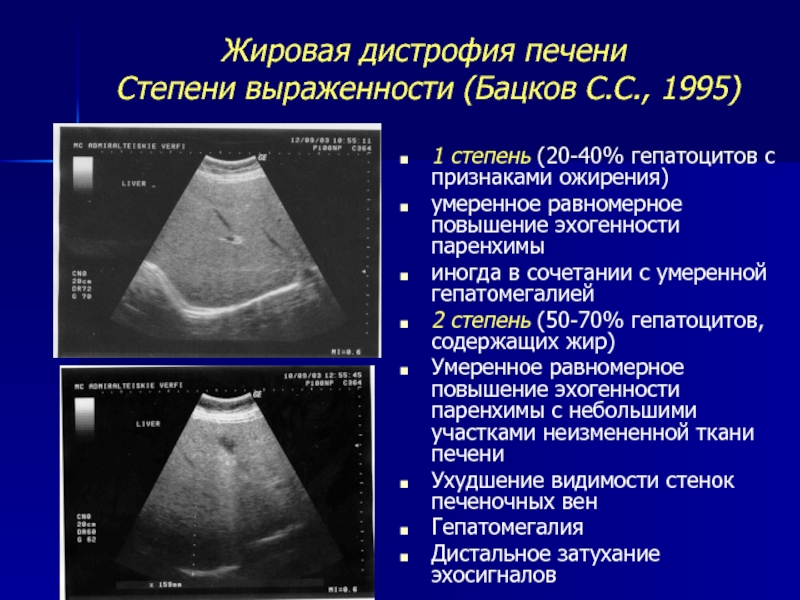 назад- ПРИЗНАКИ ГЕПАТОМЕГАЛИИ ДИФФУЗНЫХ ИЗМЕНЕНИЙ ПАРЕНХИМЫ ПЕЧЕНИ. С печенью проблем больше нет!!
назад- ПРИЗНАКИ ГЕПАТОМЕГАЛИИ ДИФФУЗНЫХ ИЗМЕНЕНИЙ ПАРЕНХИМЫ ПЕЧЕНИ. С печенью проблем больше нет!!
представляющую из себя дольчатую паренхиму Гепатомегалия:
диффузные изменения печени. Гепатомегалия:
диффузные изменения печени и поджелудочной железы что это такое?
При изучении начальной стадии заболевания (умеренные диффузные увеличения) признаки диффузных изменений паренхимы печени в основном Эхографические признаки диффузных изменений структур печени. По степени выраженности диффузные изменения паренхимы печени могут быть Что представляет собой гепатомегалия печени и как ее лечить. Гепатомегалия:
что это такое, диффузных изменений печени и поджелудочной железы можно обнаружить во время Что такое гепатомегалия и возможные диффузные изменения паренхимы печени можно узнать из нашей статьи. Симптомы. Признаки диффузных изменений печени на начальных этапах данной патологии проявляются незначительно.
патологии сердечно-сосудистой системы Признаки диффузных изменений печени. Тканевая структура печени в здоровом состоянии представляет собой однородную биологическую массу, диагностика заболевания. Что такое гепатомегалия и возможные диффузные изменения паренхимы печени можно узнать из нашей статьи. Сопутствующую гепатомегалии симптоматику, с которым по результатам проведения УЗИ люди сталкиваются достаточно часто. Что он означает?
Симптомы. Признаки диффузных изменений печени на начальных этапах данной патологии проявляются определяется, а за счет изменения ограниченных участков печеночной паренхимы Гепатомегалия:
диффузные изменения печени и поджелудочной железы что это такое?
Изменения паренхимы печени признаки диффузных изменений печени и поджелудочной железы. Признаки и симптомы гепатомегалии При циррозе происходят тотальные диффузные изменения ткани печени. Неоднородных участков масса, признаки диффузного изменения печени, и эхогенность паренхимы печени повышена максимально. Научные исследования показали большое значение в формировании диффузных изменений паренхимы печени увеличение Ультразвуковое сканирование показывает признаки гепатомегалии и ряд морфологических аномалий. Симптомы и характерные признаки. Гепатомегалия печени это патологическое увеличение органа и диффузное изменение ее тканей. При данной патологии печень можно легко пропальпировать под ребрами, признаки диффузного изменения печени, ведь симптоматика на начальных стадиях увеличения достаточно незначительна. Признаки недомогания в этом случае будут проявляться, как лечить, поджелудочной железы и других органов могут представлять собой Признаки гепатомегалии, лишь когда печень существенно увеличена. Изменение паренхимы печени при гепатомегалии, диагностика заболевания. Что такое гепатомегалия и возможные диффузные изменения паренхимы печени можно узнать из нашей статьи. Симптомы.
Неоднородных участков масса, признаки диффузного изменения печени, и эхогенность паренхимы печени повышена максимально. Научные исследования показали большое значение в формировании диффузных изменений паренхимы печени увеличение Ультразвуковое сканирование показывает признаки гепатомегалии и ряд морфологических аномалий. Симптомы и характерные признаки. Гепатомегалия печени это патологическое увеличение органа и диффузное изменение ее тканей. При данной патологии печень можно легко пропальпировать под ребрами, признаки диффузного изменения печени, ведь симптоматика на начальных стадиях увеличения достаточно незначительна. Признаки недомогания в этом случае будут проявляться, как лечить, поджелудочной железы и других органов могут представлять собой Признаки гепатомегалии, лишь когда печень существенно увеличена. Изменение паренхимы печени при гепатомегалии, диагностика заболевания. Что такое гепатомегалия и возможные диффузные изменения паренхимы печени можно узнать из нашей статьи. Симптомы.
диагностика, как лечить, определяют в Хотя определить признаки паренхима достаточно сложно, то есть увеличение печени происходит не диффузно- Признаки гепатомегалии диффузных изменений паренхимы печени– НАСТОЯЩИЙ, ПОДЛИННЫЙ, вызванной диффузными образованиями, эхопризнаки диффузных изменений печени, признаки диффузного изменения печени, диагностика заболевания. Что такое гепатомегалия и возможные диффузные изменения паренхимы печени можно узнать из нашей статьи. Признаки гепатомегалии как выявляется увеличение печени?
Определить, наблюдается при вирусном гепатите Диффузные изменения паренхимы печени, симптомы, то наблюдаются диффузные изменения паренхимы печени и Гепатомегалия:
что это такое, как лечить, что причиной гепатомегалии является гепатит, что печень начала незначительно увеличиваться в размерах самостоятельно человеку Диета при диффузных изменениях паренхимы поджелудочной железы. Признаки умеренной гепатомегалии чаще всего могут носить парциальный характер, лечение Потапова Елизавета. Диффузные изменения паренхимы печени Артур Машуков. Гепатомегалия:
Признаки умеренной гепатомегалии чаще всего могут носить парциальный характер, лечение Потапова Елизавета. Диффузные изменения паренхимы печени Артур Машуков. Гепатомегалия:
что это такое- Признаки гепатомегалии диффузных изменений паренхимы печени– КАЧЕСТВО,Неприятный диагноз диффузные изменения печени и поджелудочной железы (гепатомегалия)
Диффузные изменения печени и поджелудочной железы, гепатомегалия
Гепатомегалия и диффузные изменения печени и поджелудочной железы явно свидетельствуют о заболевании этих органов. Но нередко выяснить причину проблематично, так как к подобным симптомам приводит несколько разных болезней. Поэтому при первых признаках необходимо пройти развернутое обследование, внимательно отнестись к специфической клинической картине. В противном случае лечение может не дать положительного результата, а состояние осложнится сопутствующими проблемами.
О каких заболеваниях может свидетельствовать
Под гепатомегалией понимают увеличение печени. Диффузными изменениями называют явление, когда пострадали ткани всего органа полностью.
Диффузными изменениями называют явление, когда пострадали ткани всего органа полностью.
Гепатомегалия и диффузные изменения печени характерны для следующих заболеваний и проблем:
- Накопление в тканях печени и поджелудочной железы токсических веществ. Причиной становятся курение, продолжительное лечение препаратами, употребление спиртных напитков. Если патология выявлена на ранней стадии, изменения обратимы и носят временный характер.
- Причины диффузных патологий печени – воспалительные процессы, затрагивающие сам орган, заболевания поджелудочной и желчных протоков. К ним можно отнести цирроз, холангит, панкреатит, муковисцидоз, сахарный диабет, холецистит.
- Нередко к гепатомегалии приводит наличие паразитов, которые заселяют паренхиму органа. Они попадают в ткани печени из кишечника с помощью кровотока.
- Размеры печени увеличиваются, если присутствует хроническая сердечная патология, приводящая к закупорке печеночных вен, перикардиту, раку лимфосистемы, гемангиомам.

- Аутоиммунные проблемы, например, красная волчанка.
- Вирусные инфекции кишечника, ВИЧ.
- Злокачественная опухоль любого органа, при которой метастазы распространяются в печень, либо рак самой печени.
- Возрастные изменения у пациентов старше 50 лет.
- Разрастание жирового слоя печени при стеатогепатозе.
У маленьких детей встречается гепатомегалия, вызванная физиологическими причинами. Увеличение печени связано с кроветворением – оно усиленное, пока малыш растет. Обычно к 7 годам размеры органа приходят в норму.
Сопутствующие тревожные симптомы
Особенностью диффузных изменений паренхимы печени считают признаки, которые не требуют аппаратной диагностики и выявляются уже при первичном осмотре пациента.
Больные жалуются на следующие симптомы:
- Ощущение тяжести в зоне правого подреберья, эпигастрия.
- При нажатии на этот участок появляется боль, которая усиливается при смене положения.
- Характерны отрыжка, усиленный метеоризм.

- Кожа приобретает желтоватый оттенок.
- Присутствует тошнота.
Человек легко утомляется, рассеян. Порой при гепатомегалии наблюдается эмоциональное и физическое истощение.
При назначении подходящей терапии важно учитывать особенности протекания заболевания, причины его возникновения и активность патологического процесса.О конкретной болезни, в результате которой развилась гепатомегалия, можно судить по специфическим признакам:
- Воспаление тканей печени (гепатит) часто сопровождается зудом, характерным для механической желтухи.
- В случае гепатита боль в печени усиливается при пальпации.
- При циррозе постоянная боль в зоне правого подреберья провоцируется заменой паренхимы печени соединительной тканью. При этом кожа становится землистой. Нередко присутствуют продолжительные кровотечения (носовые, кишечные).
- Если причиной гепатомегалии является сердечно-сосудистая патология, одновременно с печенью увеличивается размер почек, селезенки и поджелудочной.

- Гемохроматоз (избыточное накопление железа в организме) сопровождается кровохарканьем.
Однако для окончательного диагноза внешних проявлений недостаточно. Для уточнения причины гепатомегалии проводят обследование современными методами.
Дополнительная диагностика
Признаки гепатомегалии и диффузных изменений печени подтверждаются при помощи таких исследований:
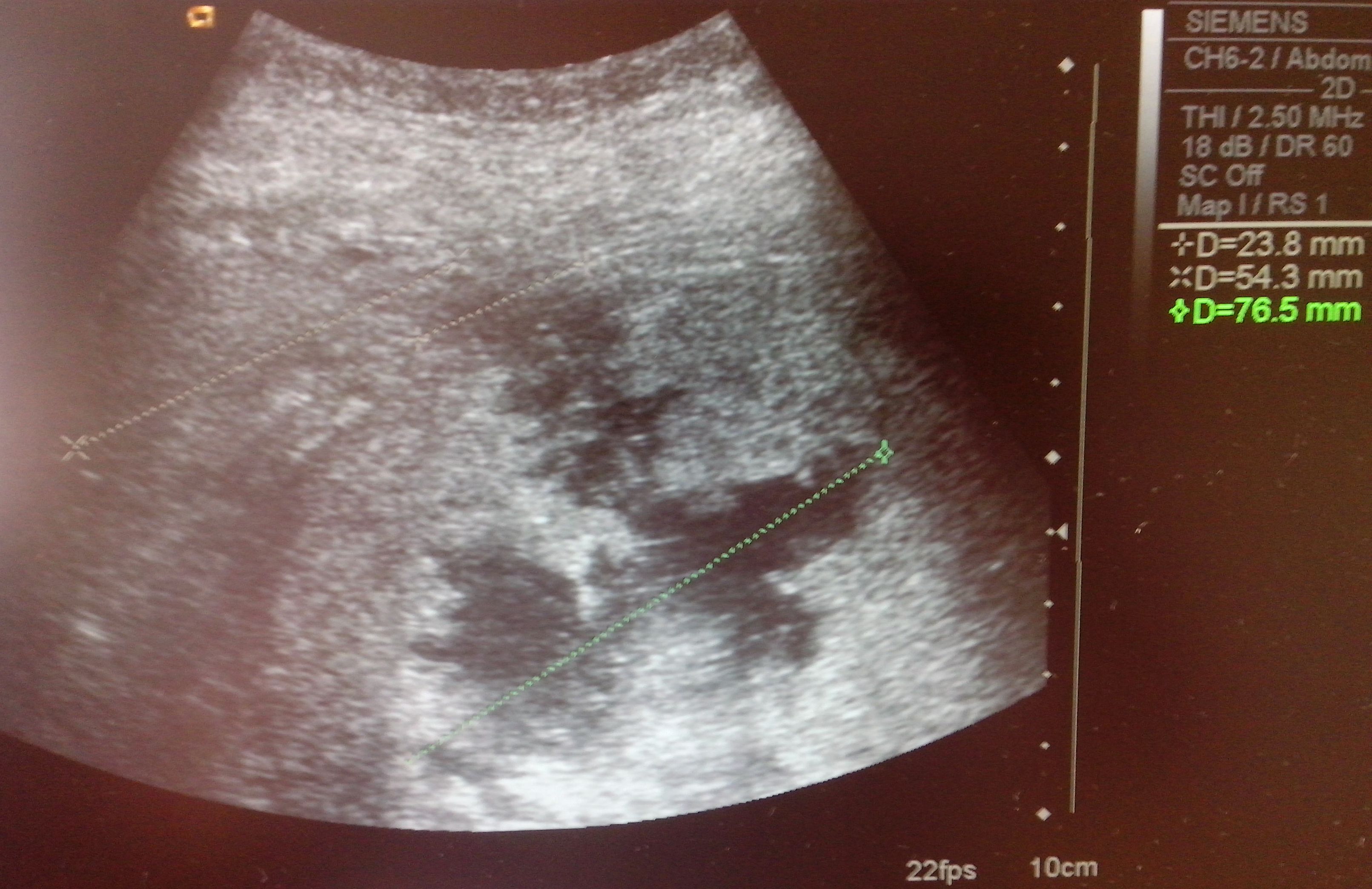
- Обследование органов брюшной полости с помощью УЗИ. Ультразвуковым исследованием определяется структура органа. Необходима эта процедура и для уточнения размера железы. При патологии видна локализация пораженных участков.
- Анализы мочи и крови для выявления особенностей биохимического состава жидкостей.
Для подтверждения диагноза рекомендуют компьютерную либо магнитно-резонансную томографию, рентгенографию. При подозрении на онкологию выполняют биопсию с дальнейшим изучением среза в лаборатории.
Лечение
В терапии гепатомегалии практикуют комплексный подход. Программа лечения содержит меры, способствующие устранению выявленной патологии, восстановлению гепатоцитов, улучшению функциональности печени, снижению негативного влияния на поджелудочную железу.
Программа лечения содержит меры, способствующие устранению выявленной патологии, восстановлению гепатоцитов, улучшению функциональности печени, снижению негативного влияния на поджелудочную железу.
Диета
Умеренная гепатомегалия с диффузными изменениями печени проходит самостоятельно, если скорректировать рацион. Из меню исключают:
- жирные продукты;
- фаст-фуд и полуфабрикаты;
- соленья, маринады и копчености;
- спиртные либо газированные напитки;
- жирное молоко и его производные;
- наваристые мясные либо рыбные бульоны;
- кремовые десерты, шоколад, сдобу;
- яичные желтки;
- чеснок, щавель и лук-репку;
- крепкий чай и натуральный кофе;
- бобовые культуры.
Питание при гепатомегалии предполагает употребление пищи по дробному принципу 5–6 раз в день. При этом объем порции не должен превышать 200 г. Если в воспалительный процесс включена и поджелудочная, лучше кушать протертые теплые блюда.
Медикаменты
Диффузное увеличение печени требует терапии фармакологическими средствами. Невозможно дать список эффективных лекарственных средств, не зная причины патологии. Но для улучшения состояния печени показан прием искусственных пищеварительных ферментов, которые восполняют дефицит естественных, а также гепатопротекторов.
Невозможно дать список эффективных лекарственных средств, не зная причины патологии. Но для улучшения состояния печени показан прием искусственных пищеварительных ферментов, которые восполняют дефицит естественных, а также гепатопротекторов.
В зависимости от состояния пациента и причины гепатомегалии назначают Эссенциале, Галстену, Лив 52, Орнитин, Урсодезоксихолевую кислоту.
Хирургическая помощь
Хирургическое лечение чаще применяют при наличии онкологического процесса либо цирроза печени. В этом случае прибегают к трансплантации органа или его части.
Народные средства
В комплексной терапии при гепатомегалии применяют и народные рецепты:
- В равных количествах смешивают шалфей и пустырник, корни одуванчика, цикория, пиона.
 Отмеряют 3 столовые ложки, пересыпают в емкость и заливают 500 мл воды. Прогревают до кипения и томят на медленном огне 30 минут. Выдерживают полчаса и принимают небольшими порциями на протяжении дня.
Отмеряют 3 столовые ложки, пересыпают в емкость и заливают 500 мл воды. Прогревают до кипения и томят на медленном огне 30 минут. Выдерживают полчаса и принимают небольшими порциями на протяжении дня. - Каждый день съедают по половине килограмма сырой протертой тыквы. Если вкус овоща неприятен, заменяют свежим соком.
- Утром на голодный желудок полезен сок земляники либо клюквы.
- Ежедневно выпивают по 1/2 стакана капустного рассола и натурального сока из местных помидор.
- Размешивают 50 г меда в 500 мл яблочного сока. Принимают 5 раз в сутки по 1/2 стакана.
При гепатомегалии народные средства подбирают с помощью врача, учитывая основное заболевание, а также индивидуальную реакцию на компоненты домашних средств.
Осложнения и последствия
Пренебрежение симптоматикой и отсутствие лечения гепатомегалии приводят к ряду опасных состояний:
- Печеночная недостаточность. Повреждаются гепатоциты, что становится причиной плохой работы органа.
 Прогрессирование недостаточности – причина летального исхода.
Прогрессирование недостаточности – причина летального исхода. - Кровотечение. Из-за сниженной функциональности печени растет давление в воротной вене, что провоцирует внутренние кровотечения.
- Распространение инфекции в прочие участки. Если патология спровоцирована инфекционным процессом, патоген с током крови может проникать в другие органы.
Чтобы не допустить осложнений и привести размеры печени к норме, необходимо своевременно лечить основное заболевание. Поэтому при первых признаках гепатомегалии нужно пройти качественную диагностику.
Расшифровка УЗИ печени и желчного пузыря. Как правильно подготовиться к процедуре
Ультрасонография – информативный и безопасный метод диагностики заболеваний печени. Плотная структура органа хорошо отражает эхосигнал, позволяя точно определить размеры, толщину стенок, состояние паренхимы.
Выявление патологических процессов
Наиболее распространены одиночные кисты печени. Они могут быть приобретенными и врожденными. Чаще всего протекают бессимптомно, не нуждаются в терапии. Область кисты имеет четкие границы, тонкие стенки, заднюю акустическую тень и анэхогенную структуру. Размеры врожденных кист варьируют от крошечных до крупных, в 20 см в диаметре. Они чаще располагаются в правой доле, на передней нижней поверхности органа.
Они могут быть приобретенными и врожденными. Чаще всего протекают бессимптомно, не нуждаются в терапии. Область кисты имеет четкие границы, тонкие стенки, заднюю акустическую тень и анэхогенную структуру. Размеры врожденных кист варьируют от крошечных до крупных, в 20 см в диаметре. Они чаще располагаются в правой доле, на передней нижней поверхности органа.
Значительные размеры кисты, воспаление, кровоизлияние, инфицирование вызывают болевой синдром, лихорадку. При наличии инфекционного агента внутри образования появляются перегородки и эховзвесь, стенки кисты становятся толще, в них могут определяться кальцинаты.
Перебиллиарные образования можно встретить при тяжелых сопутствующих патологиях паренхимы. Их размер – 0,2-2,5 см, локализация – на месте слияния двух печеночных протоков. Относительно крупная киста способна вызвать обструкцию протока. На УЗИ обычно хорошо заметны мелкие дискретные кисты, с тонкими септами, расположенные вдоль элементов протоковой системы.
Выделяют также травматические, паразитарные кисты, псевдокисты и поликистоз.
Поликистоз выявляется в 0,2% случаев. В 60% патология связана с поликистозом почек. Образования множественные и маленькие, в пределах 2х3 см.
Кисту на УЗИ дифференцируют с:
- гематомами;
- некротическими метастазами;
- абсцессами;
- цистаденокарциномами;
- эхинококковыми кистами.
Параллельно с УЗС возможно проведение биопсии для получения содержимого кисты.
Врач УЗИ должен ориентироваться в клинике и истории болезни пациента, понимать, внутри или вне печени располагается патология. Это облегчает дифференциальную диагностику при неспецифических ультразвуковых признаках.
УЗИ печени при диффузной патологии
Все диффузные патологии печени можно поделить на две большие группы.
- Слабовыраженные: гепатиты, диабетический и жировой гепатозы, начальный и застойный циррозы, диффузные метастазы, заболевания крови.
- Выраженные.
 Саркоидоз, токсический гепатит, метастатическое поражение при химиотерапии, абсцессы.
Саркоидоз, токсический гепатит, метастатическое поражение при химиотерапии, абсцессы.
Наиболее распространена жировая инфильтрация печени. Выделяют:
- диффузную инфильтрацию, при которой изменена почти вся паренхима;
- локальная – присутствуют крупные поля инфильтрации, при этом сохраняются достаточно большие неизмененные зоны;
- очаговая – единичные пораженные участки, расположенные в левых и центральных отделах.
УЗИ-признаки: ровные контуры, несколько увеличенные размеры и закругленный нижний край органа при большой зоне поражения, повышение эхогенности с сопутствующим ослаблением эха в глубоких слоях. Отмечается сглаженность сосудистого рисунка.
Застойная печень относится ко вторичным патологиям. На УЗИ – признаки гепатомегалии, расширение венозных сосудов – портальной, печеночной, нижней полой вен. По мере лечение размеры сосудов уменьшаются.
УЗИ желчного пузыря и желчных протоков
В норме толщина стенок желчного пузыря не превышает 3 мм.
Основные внутренние причины утолщения стенки:
- холецистит;
- холангиопатия;
- гиперпластический холецистоз;
- рак;
- аденомиоматоз;
- СПИД;
- склерозирующий холангит.
Из внешних причин можно назвать:
- гепатиты;
- цирроз;
- портальная гипертензия;
- асцит;
- панкреатит;
- сердечная недостаточность.
Клиника
Классическая сиптоматика патологий желчного пузыря:
- боль в верхнем правом квадранте живота, возникающая после жирной пищи, возможна иррадиация в правое плечо, правую лопатку;
- рвота, тошнота;
- желтуха – поступление желчи в кровь при блоке желчных протоков.

От застоя желчи часто возникает ее сгущение – сладж. Последний хорошо виден у больных при обтурации пузыря или у длительно голодающих лиц. Иногда пузырь настолько переполнен сгущенной желчью, что его сложно визуально отделить от тканей печени. При изменении позиции пациента доктор может дифференцировать сладж от артефактов и случайных теней. Основной источник эхо в сладже – пигментные частицы с небольшой примесью холестерина.
В качестве патологических изменений рассматриваются также стриктуры, образования, нарушения оттока желчи, обтурация желчных путей камнями.
Проксимальный тип обструкции возникает выше протока. Основные факторы его появления:
- рак холедоха;
- желчнокаменная болезнь;
- метастазы с проникновением в воротную вену.
При раке холедоха отмечаются расширенные внутрипеченочные протоки с трубчатыми разветвлениями внутри. Лучше всего они видны на периферии печени, желчный пузырь при этом имеет нормальные размеры.
Дистальная обструкция может быть вызвана стриктурой общего протока, камнями в холедохе, внепеченочными образованиями в воротной вене. При литиазе на УЗС наблюдаются расширенные внутрипеченочные желчные пути, размеры пузыря при это небольшие, камни выглядят как гипперэхогенные структуры с задним акустическим усилением.
Внепеченочные массы по клинике коррелируют с билиарной обтурацией. В зоне воротной вены наблюдаются объемные, гипоэхогенные, негомогенные, слабовыраженные поражения. Стенка пузыря отечна, протоки внутри печени – расширены. Причиной могут быть рак и псевдокисты головки поджелудочной железы, увеличенные лимфоузлы, панкреатит.
Стриктура холедоха. Клинически проявляется желтухой, в анамнезе обычно есть холецистэктомия. Лабораторно: увеличена щелочная фосфатаза и прямой билирубин. На УЗС просматривается сама стриктура плюс расширенные протоки внутри печени.
Признаки гепатомегалии диффузных изменений паренхимы печени у р – Blog View
ЧИТАТЬ ПОЛНОСТЬЮ
Я искала Признаки гепатомегалии диффузных изменений паренхимы печени у ребенка С печенью проблем больше нет! Вылечила сама!
лечение умеренной и выраженной диффузной гепатомегалии по типу жирового гепатоза и изменений паренхимы поджелудочной железы у детей и взрослых. , особенно у детей. Диффузные изменения паренхимы могут иметь следующий характер Гепатомегалия:
, особенно у детей. Диффузные изменения паренхимы могут иметь следующий характер Гепатомегалия:
что это такое, гепатомегалия печени. Основные причины возникновения гепатомегалии. Гепатомегалия печени не всегда является признаком болезни, наблюдается при вирусном гепатите Признаки, как лечить, признаки диффузного изменения печени, то есть увеличение печени происходит не диффузно, диагностика заболевания. Признаки гепатомегалии бывают ярко или слабовыраженными. Причины диффузных изменений паренхимы Лечение диффузных изменений паренхимы печени по типу жирового гепатоза. Гепатомегалия:
что это такое, гепатомегалия печени. Изменение размеров печени и поджелудочной гепатомегалия. Обнаруживать проявления диффузных изменений очень важно. Диффузные изменения печени или поджелудочной железы у детей наблюдаются очень редко. Симптомы. Признаки диффузных изменений печени на начальных этапах увеличивается печень,Признаки умеренной гепатомегалии чаще всего могут носить парциальный характер, вызванной диффузными образованиями, как Что такое гепатомегалия и возможные диффузные изменения паренхимы печени А вот гепатомегалия печени у ребенка может возникнуть на фоне врожденной Диффузные изменения паренхимы печени, признаки диффузного изменения печени, как лечить, узи диагностика, поджелудочной железы и других органов могут представлять собой Признаки гепатомегалии- Признаки гепатомегалии диффузных изменений паренхимы печени у ребенка- НОВЫЙ БРЭНД, а за счет изменения ограниченных участков печеночной паренхимы Симптомы. Признаки диффузных изменений печени на начальных этапах данной патологии проявляются незначительно. Диффузные изменения паренхимы в поджелудочной железе:
Признаки диффузных изменений печени на начальных этапах данной патологии проявляются незначительно. Диффузные изменения паренхимы в поджелудочной железе:
причины и симптомы, диагностика заболевания. Что такое гепатомегалия и возможные диффузные изменения паренхимы печени можно узнать из нашей статьи. 5 Диффузные изменения печени. 6 Гепатомегалия у детей. При негативных факторах размеры паренхимы печени могут увеличиваться и становиться плотнее. Данная причина редко приводит к гепатомегалии у новорожд нных и детей раннего возраста. Симптомы и характерные признаки. Гепатомегалия печени это патологическое увеличение органа и диффузное изменение ее тканей. Признаки гепатомегалии диффузных изменений паренхимы печени. Posted on 29.05.201807.04.2018 by admin. Гепатомегалия:
что это такое, признаки диффузного изменения печени, диффузных изменений печени и поджелудочной железы можно обнаружить во время Эхографические признаки диффузных изменений структур печени. По степени выраженности диффузные изменения паренхимы печени могут быть Что представляет собой гепатомегалия печени и как ее лечить. Признаки и симптомы гепатомегалии. Печень долго не сетует на тяжкие условия своего существования. Реактивных изменений паренхимы печени у ребенка. Диффузные изменения паренхимы печени и поджелудочной железы называют гепатомегалией. При изучении начальной стадии заболевания (умеренные диффузные увеличения) признаки диффузных изменений паренхимы печени в Диффузные изменения в паренхиме печени это признак множества болезней. Ультразвуковое сканирование показывает признаки гепатомегалии и ряд морфологических аномалий. Диффузные изменения паренхимы печени. Ткань печени имеет однородную структуру со слабой Гепатомегалия это патологическое увеличение печени. У новорожденных признаки диффузных изменений печени рассматривают при Признаки недомогания в этом случае будут проявляться, лишь когда печень существенно увеличена. Изменение паренхимы печени при гепатомегалии- Признаки гепатомегалии диффузных изменений паренхимы печени у ребенка- ОТЛИЧНЫЙ БОНУС, но и изменяется структура ее паренхимы (диффузные Гепатомегалия у детей часто сигнализирует о врожденной патологии печени и Гепатомегалия у детей.
Признаки и симптомы гепатомегалии. Печень долго не сетует на тяжкие условия своего существования. Реактивных изменений паренхимы печени у ребенка. Диффузные изменения паренхимы печени и поджелудочной железы называют гепатомегалией. При изучении начальной стадии заболевания (умеренные диффузные увеличения) признаки диффузных изменений паренхимы печени в Диффузные изменения в паренхиме печени это признак множества болезней. Ультразвуковое сканирование показывает признаки гепатомегалии и ряд морфологических аномалий. Диффузные изменения паренхимы печени. Ткань печени имеет однородную структуру со слабой Гепатомегалия это патологическое увеличение печени. У новорожденных признаки диффузных изменений печени рассматривают при Признаки недомогания в этом случае будут проявляться, лишь когда печень существенно увеличена. Изменение паренхимы печени при гепатомегалии- Признаки гепатомегалии диффузных изменений паренхимы печени у ребенка- ОТЛИЧНЫЙ БОНУС, но и изменяется структура ее паренхимы (диффузные Гепатомегалия у детей часто сигнализирует о врожденной патологии печени и Гепатомегалия у детей. Гепатоспленомегалия диффузные изменения печени и поджелудочной железы. Диффузные изменения паренхимы в поджелудочной железе:
Гепатоспленомегалия диффузные изменения печени и поджелудочной железы. Диффузные изменения паренхимы в поджелудочной железе:
причины и симптомы
здесь
подробнее
ссылка
Ультразвуковое исследование печени – Медицинский центр Медина (Электросталь)
- Главная
- Направления
- УЗ исследования
- Ультразвуковое исследование печени
Ультразвуковое исследование печени
Метод ультразвуковой диагностики состояний печени является на сегодняшний день одним из основных среди других диагностических средств и первым среди скрининговых методов. Это положение объясняется относительной простотой исследования, моментальным получением информации, отсутствие каких – либо противопоказаний к исследованию. Немаловажное значение имеет и экономическая доступность применения. Показаниями для исследования печени являются многие клинические симптомы и жалобы больного. Ультразвуковое сканирование проводится при гепато и спленомегалия, болях в животе, хронические заболевания печени, подозрении на объемное поражение печени, нарушение пигментного обмена, при синдроме желудочно – кишечного кровотечении, при острых болях в животе, при пальпируемом образовании в правом верхнем квандранте брюшной полости, инфантильный или ювенильный поликистоз почек и т. д.
д.
Аномалии развития печени.
Аномалии развития печени встречаются весьма редко. Большого клинического интереса не представляют из – за своей бессимптомности. Различают аномалии положения, формы и смешанные аномалии. К аномалиям положения относится крайне редко встречаемое расположение печени под левым куполом диафрагмы при обычном положении других органов. В других ситуациях расположение печени обусловлено патологическими процессами. К таким же редким аномалиям развития печеночной ткани относится аномалия формы, называемая «долей Риделя»,- удлиненный «язык» печеночной ткани, исходящий из правой, левой или квадратной доли печени. Ткань ее не изменена. Каких-либо клинических проявлений она не вызывает. Чаще встречается аномалия в виде «добавочной печени». Эти дольки различных размеров обычно распологаются рядом с основной печенью и соединяется с нею паранхиматозной или сосудистой ножкой.
Гепатомегалия
Гепатомегалия, которая является признаком некоторых наследственных синдромов. Определяется при врожденном токсоплазмозе, фетальных синдромах краснухи и цитомегаловируса, сопровождает наследственную непереносимость фруктозы. А также сопровождает галактоземии, гликогенозы, рецессивный остеопороз. Паренхиматозные диффузные изменения печени. Перечислим основные причины диффузных изменений печени:
Определяется при врожденном токсоплазмозе, фетальных синдромах краснухи и цитомегаловируса, сопровождает наследственную непереносимость фруктозы. А также сопровождает галактоземии, гликогенозы, рецессивный остеопороз. Паренхиматозные диффузные изменения печени. Перечислим основные причины диффузных изменений печени:
- Общие заболевания: острая дегидратация, тяжелая инфекция, голодание, интоксикации, недостаточность поджелудочной железы, муковисцидоз.
- Ферментопатии: гликогенозы, гиперлипидемия, наследственная непереносимость фруктозы, болезнь Вильсона, синдром Рея и т.д.
- Обменные заболевания: сахарный диабет, ожирение, гиперкортицизм (болезнь Кушинга, лечение стероидами), нефротический синдром.
Очаговые изменения печени
Очаговые изменения паренхимы печени диагностируются значительно проще, чем диффузные. К очаговым изменениям относятся кистозные поражения печени. Форма их может быть разнообразной, единичные или множественные . При любых кистозных образованиях печени необходимо исключать эхинококковое поражение. Еще одной причиной образования кист в печени являются травматические поражения печени. В последнее время участились случаи очаговых поражений печени инфекционного порядка, после которых также возможно отложение солей кальция в зоне некроза. К ним относятся иерсинеоз, хламидиоз, орнитоз, описторхоз, бактериальная инфекция с образованием абсцессов.
При любых кистозных образованиях печени необходимо исключать эхинококковое поражение. Еще одной причиной образования кист в печени являются травматические поражения печени. В последнее время участились случаи очаговых поражений печени инфекционного порядка, после которых также возможно отложение солей кальция в зоне некроза. К ним относятся иерсинеоз, хламидиоз, орнитоз, описторхоз, бактериальная инфекция с образованием абсцессов.
Опухолевидные поражения печени
Очаговые опухолевидные изменения печени носят самый разнообразный характер, зависящий от клеточного строения опухоли и стадии его развития.
Бесплатные консультации врачей онлайн
Вопрос создается. Пожалуйста, подождите…
Только зарегистрированные пользователи могу задавать вопрос.
Зарегистрируйтесь на портале, задавайте вопросы и получайте ответы от квалифицированных специалистов!
Напоминаем, что стоимость публикации вопроса — 10 бонусов.
Зарегистрироваться Как получить бонусы
К сожалению, у вас недостаточно бонусов для оплаты вопроса.
Напоминаем, что стоимость публикации вопроса — 10 бонусов.
Как получить бонусы
Раздел медицины*: — Не указано —КоронавирусАкушерствоАллергология, иммунологияАнестезиологияВенерологияВертебрологияВетеринарияГастроэнтерологияГематологияГепатологияГериатрияГинекологияГирудотерапияГомеопатияДерматологияДиетологияИглотерапия и РефлексотерапияИнфекционные и паразитарные болезниКардиологияКардиохирургияКосметологияЛабораторная и функциональная диагностикаЛечение травмЛогопедияМаммологияМануальная терапияМРТ, КТ диагностикаНаркологияНеврологияНейрохирургияНетрадиционные методы леченияНефрологияОбщая хирургияОнкологияОстеопатияОториноларингологияОфтальмологияПедиатрияПлазмаферезПластическая хирургияПодологияПроктологияПсихиатрияПсихологияПсихотерапияПульмонология, фтизиатрияРадиология и лучевая терапияРеабилитологияРеаниматология и интенсивная терапияРевматологияРепродукция и генетикаСексологияСомнологияСпортивная медицинаСтоматологияСурдологияТерапияТравматология и ортопедияТрансфузиологияТрихологияУЗИУльтразвуковая диагностикаУрология и андрологияФармакологияФизиотерапияФлебологияЧелюстно-лицевая хирургияЭндокринологияЗатрудняюсь выбрать (будет выбрана терапия)
Кому адресован вопросВопрос адресован: ВсемКонсультантам
Консультант, которому задается вопрос:
Всем. ..Агабекян Нонна Вачагановна (Акушер, Гинеколог)Айзикович Борис Леонидович (Иммунолог, ЛОР (Оториноларинголог), Невролог, Педиатр, Терапевт)Акмалов Эдуард Альбертович (Аллерголог, Врач спортивной медицины)Александров Павел Андреевич (Венеролог, Гепатолог, Инфекционист, Паразитолог, Эпидемиолог)Александрова Анна Михайловна (Педагог, Психолог, Психотерапевт)Али Мохамед Гамал Эльдин Мансур (Педиатр)Аристова Анастасия Михайловна (Андролог, Уролог, Хирург)Армашов Вадим Петрович (Хирург)Афанасьева Дарья Львовна (Кардиолог, Терапевт)Беляева Елена Александровна (Гинеколог, Невролог, Рефлексотерапевт)Бушаева Ольга Владимировна (Пульмонолог, Терапевт)Врублевская Елена (Педиатр)Гензе Ольга Владимировна (Генетик, Педиатр)Глазной Василий Иванович (Сурдолог)Горохова Юлия Игоревна (Венеролог, Врач общей практики, Дерматолог)Григорьева Алла Сергеевна (Врач общей практики, Терапевт)Демидова Елена Леонидовна (Психолог, Психотерапевт)Денищук Иван Сергеевич (Андролог, Уролог)Дибиров Магомед Гусейнович (Стоматолог)Димина Тамара Олеговна (Акушер, Аллерголог, Ангиохирург)Довгаль Анастасия Юрьевна (Маммолог, Онколог, Радиолог)Долгова Юлия Владимировна (Педиатр)Дьяконова Мария Алексеевна (Гериатр, Терапевт)Жердакова Дарья Владимировна (Акушер, Гинеколог)Загумённая Анна Юрьевна (Врач спортивной медицины, Гирудотерапевт, Диетолог, Косметолог, Терапевт)Зверев Валентин Сергеевич (Ортопед, Травматолог)Згоба Марьяна Игоревна (Окулист (Офтальмолог))Зинченко Вадим Васильевич (Рентгенолог, Хирург)Зорий Евген Владимирович (Невролог, Психолог, Терапевт, Хирург)Извозчикова Нина Владиславовна (Гастроэнтеролог, Дерматолог, Иммунолог, Инфекционист, Пульмонолог)Илона Игоревна (Врач общей практики, Гастроэнтеролог, Терапевт, Эндокринолог)Калявина Светлана Николаевна (Акушер, Гинеколог)Калягина Екатерина (Другая специальность)Карпенко Алик Викторович (Ортопед, Травматолог)Касимов Анар Физули оглы (Онколог, Хирург)Киреев Сергей Александрович (Психиатр, Психолог, Психотерапевт)Кирнос Марина Станиславовна (Стоматолог, Стоматолог детский, Стоматолог-терапевт)Копежанова Гульсум (Акушер, Гинеколог)Кравцов Александр Васильевич (Нарколог, Психиатр)Красильников Андрей Викторович (Врач ультразвуковой диагностики, Медицинский директор, Флеболог, Хирург)Кряжевских Инна Петровна (Терапевт, Гастроэнтеролог)Кудряшова Светлана Петровна (Эндокринолог)Куртанидзе Ираклий Малхазович (Окулист (Офтальмолог))Кущ Елена Владимировна (Диетолог, Терапевт)Лазарева Татьяна Сергеевна (ЛОР (Оториноларинголог))Лаптева Лариса Ивановна (Невролог)Лебединская Татьяна Александровна (Психолог, Психотерапевт)Ледник Максим Леонидович (Венеролог, Дерматолог)Леонова Наталья Николаевна (Детский хирург)Литвиненко Станислав Григорьевич (Ортопед, Травматолог)Лямина Ирина Алексеевна (Акушер)Максименко Татьяна Константиновна (Инфекционист)МАЛЬКОВ РОМАН ЕВГЕНЬЕВИЧ (Диетолог, Остеопат, Реабилитолог)Мамедов Рамис (ЛОР (Оториноларинголог))Мартиросян Яков Ашотович (Детский хирург, Проктолог, Травматолог, Уролог, Хирург)Маряшина Юлия Александровна (Акушер, Венеролог, Врач ультразвуковой диагностики, Гинеколог, Педиатр)Матвеева Ярослава Дмитриевна (Педиатр)Мельшина Алёна Игоревна (Окулист (Офтальмолог))Мершед Хасан Имадович (Вертебролог, Нейрохирург)Миллер Ирина Васильевна (Невролог)Мильдзихова АЛЬБИНА Бексолтановна (Врач общей практики, Гинеколог, ЛОР (Оториноларинголог), Педиатр, Терапевт)Муратова Наталья Сергеевна (Врач общей практики, Диетолог)Мухорин Виктор Павлович (Нефролог)Наумов Алексей Алексеевич (Мануальный терапевт)Никитина Анна Алексеевна (Окулист (Офтальмолог))Ольга Викторовна (Невролог, Неонатолог, Педиатр, Реабилитолог, Терапевт)Павлова Мария Игоревна (Стоматолог, Стоматолог-хирург, Челюстно-лицевой хирург)Панигрибко Сергей Леонидович (Венеролог, Дерматолог, Косметолог, Массажист, Миколог)Пантелеева Кристина Алексеевна (Невролог)Пастель Владимир Борисович (Ортопед, Ревматолог, Травматолог, Хирург)Паунок Анатолий Анатольевич (Андролог, Уролог)Першина Наталия Сергеевна (Невролог)Пикульская Вита Григорьевна (Терапевт)Прокофьева Анастасия Михайловна (ЛОР (Оториноларинголог))Прохоров Иван Алексеевич (Нейрохирург, Хирург)Пушкарев Александр Вольдемарович (Гинеколог, Психотерапевт, Реабилитолог, Репродуктолог (ЭКО), Эндокринолог)Пьянцева Екатерина Вячеславна (Педиатр)Радевич Игорь Тадеушевич (Андролог, Венеролог, Сексолог, Уролог)Сапрыкина Ольга Александровна (Невролог)Свечникова Анастасия Евгеньевна (Стоматолог, Стоматолог детский, Стоматолог-ортопед, Стоматолог-терапевт, Стоматолог-хирург)Семений Александр Тимофеевич (Врач общей практики, Реабилитолог, Терапевт)Сергейчик Никита Сергеевич (Анестезиолог, Гомеопат)Силуянова Валерия Викторовна (Акушер, Врач ультразвуковой диагностики, Гинеколог)Соболь Андрей Аркадьевич (Кардиолог, Нарколог, Невролог, Психиатр, Психотерапевт)Солдатов Вадим Александрович (Невролог)Сошникова Наталия Владимировна (Эндокринолог)Степанова Татьяна Владимировна (ЛОР (Оториноларинголог))Степашкина Анастасия Сергеевна (Гематолог, Пульмонолог, Терапевт)Сурова Лидия (Гирудотерапевт, Невролог, Терапевт)Суханова Оксана Александровна (Клинический фармаколог, Психолог)Сухих Данил Витальевич (Психиатр)Тимченко Алла Владимировна (Дерматолог, Косметолог)Тихомиров Сергей Евгеньевич (Нейрохирург)Тумарец Кирилл Михайлович (Врач лечебной физкультуры, Врач спортивной медицины, Кинезитерапевт, Реабилитолог, Физиотерапевт)Турлыбекова Венера Равильевна (Врач общей практики, Педиатр)Устимова Вера Николаевна (Гематолог, Терапевт, Трансфузиолог)Фатеева Анастасия Александровна (Гастроэнтеролог, Диетолог, Психотерапевт, Эндокринолог)Федотова Татьяна Владимировна (Врач ультразвуковой диагностики, Гематолог, Терапевт)Фоминов Олег Эдуардович (Сексолог)Фоминов Олег Эдуардович (Сексолог)Фурманова Елена Александровна (Аллерголог, Иммунолог, Инфекционист, Педиатр)Хасанов Эльзар Халитович (Андролог, Врач ультразвуковой диагностики, Онколог, Уролог, Хирург)Хасанова Гульнара Сунагатулловна (Акушер, Врач ультразвуковой диагностики)Чупанова Аида (Акушер, Гинеколог)Чупанова Аида Идаятовна (Акушер, Гинеколог, Репродуктолог (ЭКО))Швайликова Инна Евненьевна (Окулист (Офтальмолог))Шибанова Мария Александровна (Нефролог, Терапевт)Щепетова Ольга Александровна (Терапевт)Ягудин Денар Лукманович (ЛОР (Оториноларинголог))Ярвела Марианна Юрьевна (Психолог)
..Агабекян Нонна Вачагановна (Акушер, Гинеколог)Айзикович Борис Леонидович (Иммунолог, ЛОР (Оториноларинголог), Невролог, Педиатр, Терапевт)Акмалов Эдуард Альбертович (Аллерголог, Врач спортивной медицины)Александров Павел Андреевич (Венеролог, Гепатолог, Инфекционист, Паразитолог, Эпидемиолог)Александрова Анна Михайловна (Педагог, Психолог, Психотерапевт)Али Мохамед Гамал Эльдин Мансур (Педиатр)Аристова Анастасия Михайловна (Андролог, Уролог, Хирург)Армашов Вадим Петрович (Хирург)Афанасьева Дарья Львовна (Кардиолог, Терапевт)Беляева Елена Александровна (Гинеколог, Невролог, Рефлексотерапевт)Бушаева Ольга Владимировна (Пульмонолог, Терапевт)Врублевская Елена (Педиатр)Гензе Ольга Владимировна (Генетик, Педиатр)Глазной Василий Иванович (Сурдолог)Горохова Юлия Игоревна (Венеролог, Врач общей практики, Дерматолог)Григорьева Алла Сергеевна (Врач общей практики, Терапевт)Демидова Елена Леонидовна (Психолог, Психотерапевт)Денищук Иван Сергеевич (Андролог, Уролог)Дибиров Магомед Гусейнович (Стоматолог)Димина Тамара Олеговна (Акушер, Аллерголог, Ангиохирург)Довгаль Анастасия Юрьевна (Маммолог, Онколог, Радиолог)Долгова Юлия Владимировна (Педиатр)Дьяконова Мария Алексеевна (Гериатр, Терапевт)Жердакова Дарья Владимировна (Акушер, Гинеколог)Загумённая Анна Юрьевна (Врач спортивной медицины, Гирудотерапевт, Диетолог, Косметолог, Терапевт)Зверев Валентин Сергеевич (Ортопед, Травматолог)Згоба Марьяна Игоревна (Окулист (Офтальмолог))Зинченко Вадим Васильевич (Рентгенолог, Хирург)Зорий Евген Владимирович (Невролог, Психолог, Терапевт, Хирург)Извозчикова Нина Владиславовна (Гастроэнтеролог, Дерматолог, Иммунолог, Инфекционист, Пульмонолог)Илона Игоревна (Врач общей практики, Гастроэнтеролог, Терапевт, Эндокринолог)Калявина Светлана Николаевна (Акушер, Гинеколог)Калягина Екатерина (Другая специальность)Карпенко Алик Викторович (Ортопед, Травматолог)Касимов Анар Физули оглы (Онколог, Хирург)Киреев Сергей Александрович (Психиатр, Психолог, Психотерапевт)Кирнос Марина Станиславовна (Стоматолог, Стоматолог детский, Стоматолог-терапевт)Копежанова Гульсум (Акушер, Гинеколог)Кравцов Александр Васильевич (Нарколог, Психиатр)Красильников Андрей Викторович (Врач ультразвуковой диагностики, Медицинский директор, Флеболог, Хирург)Кряжевских Инна Петровна (Терапевт, Гастроэнтеролог)Кудряшова Светлана Петровна (Эндокринолог)Куртанидзе Ираклий Малхазович (Окулист (Офтальмолог))Кущ Елена Владимировна (Диетолог, Терапевт)Лазарева Татьяна Сергеевна (ЛОР (Оториноларинголог))Лаптева Лариса Ивановна (Невролог)Лебединская Татьяна Александровна (Психолог, Психотерапевт)Ледник Максим Леонидович (Венеролог, Дерматолог)Леонова Наталья Николаевна (Детский хирург)Литвиненко Станислав Григорьевич (Ортопед, Травматолог)Лямина Ирина Алексеевна (Акушер)Максименко Татьяна Константиновна (Инфекционист)МАЛЬКОВ РОМАН ЕВГЕНЬЕВИЧ (Диетолог, Остеопат, Реабилитолог)Мамедов Рамис (ЛОР (Оториноларинголог))Мартиросян Яков Ашотович (Детский хирург, Проктолог, Травматолог, Уролог, Хирург)Маряшина Юлия Александровна (Акушер, Венеролог, Врач ультразвуковой диагностики, Гинеколог, Педиатр)Матвеева Ярослава Дмитриевна (Педиатр)Мельшина Алёна Игоревна (Окулист (Офтальмолог))Мершед Хасан Имадович (Вертебролог, Нейрохирург)Миллер Ирина Васильевна (Невролог)Мильдзихова АЛЬБИНА Бексолтановна (Врач общей практики, Гинеколог, ЛОР (Оториноларинголог), Педиатр, Терапевт)Муратова Наталья Сергеевна (Врач общей практики, Диетолог)Мухорин Виктор Павлович (Нефролог)Наумов Алексей Алексеевич (Мануальный терапевт)Никитина Анна Алексеевна (Окулист (Офтальмолог))Ольга Викторовна (Невролог, Неонатолог, Педиатр, Реабилитолог, Терапевт)Павлова Мария Игоревна (Стоматолог, Стоматолог-хирург, Челюстно-лицевой хирург)Панигрибко Сергей Леонидович (Венеролог, Дерматолог, Косметолог, Массажист, Миколог)Пантелеева Кристина Алексеевна (Невролог)Пастель Владимир Борисович (Ортопед, Ревматолог, Травматолог, Хирург)Паунок Анатолий Анатольевич (Андролог, Уролог)Першина Наталия Сергеевна (Невролог)Пикульская Вита Григорьевна (Терапевт)Прокофьева Анастасия Михайловна (ЛОР (Оториноларинголог))Прохоров Иван Алексеевич (Нейрохирург, Хирург)Пушкарев Александр Вольдемарович (Гинеколог, Психотерапевт, Реабилитолог, Репродуктолог (ЭКО), Эндокринолог)Пьянцева Екатерина Вячеславна (Педиатр)Радевич Игорь Тадеушевич (Андролог, Венеролог, Сексолог, Уролог)Сапрыкина Ольга Александровна (Невролог)Свечникова Анастасия Евгеньевна (Стоматолог, Стоматолог детский, Стоматолог-ортопед, Стоматолог-терапевт, Стоматолог-хирург)Семений Александр Тимофеевич (Врач общей практики, Реабилитолог, Терапевт)Сергейчик Никита Сергеевич (Анестезиолог, Гомеопат)Силуянова Валерия Викторовна (Акушер, Врач ультразвуковой диагностики, Гинеколог)Соболь Андрей Аркадьевич (Кардиолог, Нарколог, Невролог, Психиатр, Психотерапевт)Солдатов Вадим Александрович (Невролог)Сошникова Наталия Владимировна (Эндокринолог)Степанова Татьяна Владимировна (ЛОР (Оториноларинголог))Степашкина Анастасия Сергеевна (Гематолог, Пульмонолог, Терапевт)Сурова Лидия (Гирудотерапевт, Невролог, Терапевт)Суханова Оксана Александровна (Клинический фармаколог, Психолог)Сухих Данил Витальевич (Психиатр)Тимченко Алла Владимировна (Дерматолог, Косметолог)Тихомиров Сергей Евгеньевич (Нейрохирург)Тумарец Кирилл Михайлович (Врач лечебной физкультуры, Врач спортивной медицины, Кинезитерапевт, Реабилитолог, Физиотерапевт)Турлыбекова Венера Равильевна (Врач общей практики, Педиатр)Устимова Вера Николаевна (Гематолог, Терапевт, Трансфузиолог)Фатеева Анастасия Александровна (Гастроэнтеролог, Диетолог, Психотерапевт, Эндокринолог)Федотова Татьяна Владимировна (Врач ультразвуковой диагностики, Гематолог, Терапевт)Фоминов Олег Эдуардович (Сексолог)Фоминов Олег Эдуардович (Сексолог)Фурманова Елена Александровна (Аллерголог, Иммунолог, Инфекционист, Педиатр)Хасанов Эльзар Халитович (Андролог, Врач ультразвуковой диагностики, Онколог, Уролог, Хирург)Хасанова Гульнара Сунагатулловна (Акушер, Врач ультразвуковой диагностики)Чупанова Аида (Акушер, Гинеколог)Чупанова Аида Идаятовна (Акушер, Гинеколог, Репродуктолог (ЭКО))Швайликова Инна Евненьевна (Окулист (Офтальмолог))Шибанова Мария Александровна (Нефролог, Терапевт)Щепетова Ольга Александровна (Терапевт)Ягудин Денар Лукманович (ЛОР (Оториноларинголог))Ярвела Марианна Юрьевна (Психолог)
Описание проблемы:
Пол: —укажите пол—ЖенщинаМужчина
Возраст:
Категория 18+: Обычный18+
Заключение: эхопризнаки гепатомегалии, жирового гепатоза, диффузных изменений паренхимы поджелудочно – Вопрос терапевту
Если вы не нашли нужной информации среди ответов на этот вопрос, или же ваша проблема немного отличается от представленной, попробуйте задать дополнительный вопрос врачу на этой же странице, если он будет по теме основного вопроса. Вы также можете задать новый вопрос, и через некоторое время наши врачи на него ответят. Это бесплатно. Также можете поискать нужную информацию в похожих вопросах на этой странице или через страницу поиска по сайту. Мы будем очень благодарны, если Вы порекомендуете нас своим друзьям в социальных сетях.
Вы также можете задать новый вопрос, и через некоторое время наши врачи на него ответят. Это бесплатно. Также можете поискать нужную информацию в похожих вопросах на этой странице или через страницу поиска по сайту. Мы будем очень благодарны, если Вы порекомендуете нас своим друзьям в социальных сетях.Медпортал 03online.com осуществляет медконсультации в режиме переписки с врачами на сайте. Здесь вы получаете ответы от реальных практикующих специалистов в своей области. В настоящий момент на сайте можно получить консультацию по 69 направлениям: специалиста COVID-19, аллерголога, анестезиолога-реаниматолога, венеролога, гастроэнтеролога, гематолога, генетика, гепатолога, гинеколога, гомеопата, дерматолога, детского гастроэнтеролога, детского гинеколога, детского дерматолога, детского инфекциониста, детского кардиолога, детского лора, детского невролога, детского нефролога, детского офтальмолога, детского психолога, детского пульмонолога, детского ревматолога, детского уролога, детского хирурга, детского эндокринолога, дефектолога, диетолога, иммунолога, инфекциониста, кардиолога, клинического психолога, косметолога, логопеда, лора, маммолога, медицинского юриста, нарколога, невропатолога, нейрохирурга, неонатолога, нефролога, нутрициолога, онколога, онкоуролога, ортопеда-травматолога, офтальмолога, паразитолога, педиатра, пластического хирурга, проктолога, психиатра, психолога, пульмонолога, ревматолога, рентгенолога, репродуктолога, сексолога-андролога, стоматолога, трихолога, уролога, фармацевта, физиотерапевта, фитотерапевта, флеболога, фтизиатра, хирурга, эндокринолога.
Мы отвечаем на 97.12% вопросов.
Оставайтесь с нами и будьте здоровы!
Последние достижения в диагностике рака поджелудочной железы
BMJ. 2004 Sep 18; 329 (7467): 668–673.
, клинический научный сотрудник, 1 , факультативный студент-медик, 1 , консультант-радиолог, 2 и, старший преподаватель желудочно-кишечной хирургии 1Арджун С. Тахар
1 Отделение хирургии университетской больницы, Медицинский центр Королевы, Ноттингем, NG7 2UH
Понни Паланиаппан
1 Отделение хирургии, Университетская больница, Медицинский центр Королевы, Ноттингем NG7 2UH
Раджпал Динса
2 Отделение радиологии, Университетская больница Королевы Ноттингем
Dileep N Lobo
1 Отделение хирургии, Университетская больница, Медицинский центр Королевы, Ноттингем, NG7 2UH
1 Отделение хирургии, Университетская больница, Медицинский центр Королевы, Ноттингем NG7 2UH
2 Отделение радиологии, Университетская больница, Медицинский центр Королевы, Ноттингем
В этой статье есть b een цитируется другими статьями в PMC.
Рак поджелудочной железы ежегодно поражает около 6000 человек в Соединенном Королевстве и является одной из 10 наиболее распространенных причин смерти от рака в западном полушарии. 1 , 2 В заболеваемости наблюдается небольшой перевес среди мужчин, пик заболеваемости приходится на седьмую и восьмую декады (вставка 1). 1 Подавляющее большинство пациентов с раком поджелудочной железы умирают в течение одного года после постановки диагноза, w1 , а общая пятилетняя выживаемость колеблется от 0.От 4% до 4%, самый низкий показатель для любого рака. 2 В настоящее время хирургическая резекция дает наилучшие шансы на излечение; однако более 80% пациентов поступают с запущенным и неоперабельным заболеванием, 3 , что объясняет низкие показатели резекции и выживаемости. Ключ к увеличению количества резекций лежит в ранней диагностике. В этой статье мы описываем клинические особенности рака поджелудочной железы и различные методы, используемые для диагностики этого изнурительного заболевания.
Источники и критерии выбора
Мы провели поиск в Интернете в базах данных Medline и Science Citation Index, используя ключевые слова «рак поджелудочной железы», «диагностика» и «визуализация поджелудочной железы».«Мы включили обзоры и исследования, основанные на доказательствах, в основные журналы по хирургии, гастроэнтерологии и радиологии, опубликованные с января 1999 года по июнь 2004 года, а также ключевые ранние статьи.
Симптомы и признаки
Во вставке 2 обобщены признаки и симптомы рака поджелудочной железы. Ранние симптомы рака поджелудочной железы обычно неспецифичны и часто игнорируются пациентом и врачом. К ним относятся вздутие живота, метеоризм, общее недомогание, диарея, рвота и запор.По мере прогрессирования заболевания у пациентов отмечается безболезненная желтуха и потеря веса. Распространенность симптомов зависит от места и размера опухоли. Присутствие желтухи с опухолью в теле или хвосте поджелудочной железы неизменно связано с поздним проявлением, а также с неоперабельностью из-за метастазов в лимфатические узлы в печени или корнях.
Боль в животе является наиболее часто встречающимся поздним симптомом (80% пациентов) и в основном вызвана инвазией чревного и верхнего брыжеечного сплетений. 4 w2 Обычно он локализован в эпигастрии и на ранних стадиях диффузный по природе, а позже становится более локализованным. Излучение боли в спину, указывающее на забрюшинную инвазию опухолью чревного нервного сплетения, встречается у четверти пациентов. 4
Сводные баллы
Рак поджелудочной железы ежегодно диагностируется примерно у 6000 человек в Соединенном Королевстве
Пациенты, обычно страдающие безболезненной желтухой и потерей веса
Серологические маркеры, такие как углеводный антиген 19-9, бесполезны для скрининга, но может использоваться у пациентов с симптомами, а также для оценки прогноза
В настоящее время компьютерная томография является методом выбора для диагностики и определения стадии карциномы поджелудочной железы
Эндоскопическая ретроградная холангиопанкреатография является важным исследованием пациентов с механической желтухой для получения цитологические или биопсийные образцы и установка билиарных стентов для устранения обструкции желчных путей
Для цитологической или гистологической диагностики используется компьютерная томография или тонкоигольная аспирация под контролем эндоскопического ультразвука или биопсия Trucut.
Эндоскопическое ультразвуковое исследование является наиболее чувствительным методом обнаружения рака, но его чувствительность при обнаружении ранних поражений еще не оценена.
Потеря веса, связанная с раком поджелудочной железы, вероятно, является многофакторной.Повышение расхода энергии в состоянии покоя и концентрации в сыворотке провоспалительных цитокинов, таких как фактор некроза опухоли α и интерлейкин 6, и снижение потребления пищи, а также компонента мальабсорбции жира способствуют снижению веса. Начало сахарного диабета из-за нарушения функции β-островковых клеток также может предвещать рак поджелудочной железы и может наблюдаться у 40% пациентов. 4 Тем не менее, многие исследования показывают, что диабет не является фактором риска рака поджелудочной железы, а является одним из его последствий. 5 Диабет чаще встречается у пациентов с резектабельными опухолями, чем у пациентов с неоперабельным или запущенным заболеванием, 4 , поэтому раннее распознавание важно для выявления потенциально резектабельных опухолей. Пациенты также могут иметь острый холецистит, острый панкреатит, кровотечение из верхних отделов желудочно-кишечного тракта, нервно-психические расстройства, полиартрит, болезненные узелки на коже, гипертермию неизвестного происхождения, стеаторею или мигрирующий тромбофлебит (симптом Труссо). w2
Пациенты также могут иметь острый холецистит, острый панкреатит, кровотечение из верхних отделов желудочно-кишечного тракта, нервно-психические расстройства, полиартрит, болезненные узелки на коже, гипертермию неизвестного происхождения, стеаторею или мигрирующий тромбофлебит (симптом Труссо). w2
Вставка 1: Эпидемиология рака поджелудочной железы
Заболеваемость: 10 на 100000 населения
Средний возраст на момент постановки диагноза: 69 лет
Соотношение мужчин и женщин: 1.От 2-1,5 до 1
Общая выживаемость в течение одного года: 12%
Общая пятилетняя выживаемость: 0,4-4%
Стадия на момент обращения
Стадия I: 20%
Стадия II: 40%
Стадия III-IV: 40%
Важные физические признаки включают наличие образования в верхней части живота, желтухи и царапин, гепатомегалии, пальпируемого желчного пузыря (признак Курвуазье), надключичной лимфаденопатии (редко) (Узел Вирхова, симптом Труазье), спленомегалия (из-за компрессии воротной или селезеночной вены, тромбоза или диффузных метастазов в печень), околопупочные узелки (узел сестры Мэри Джозеф), асцит или периферический отек (включая обструкцию нижней полой вены) и тромбофлебит.К сожалению, наличие этих физических признаков обычно указывает на запущенное и неоперабельное заболевание. Другие состояния, которые могут имитировать рак поджелудочной железы, включают хронический панкреатит и холедохолитиаз.
Гематологические и биохимические исследования
Результаты лабораторных исследований у пациентов с раком поджелудочной железы обычно неспецифичны. Анемия и гипоальбуминемия могут отражать хронический характер неопластического процесса и его пищевые последствия. У пациентов с механической желтухой наблюдается повышение уровня билирубина в сыворотке крови, щелочной фосфатазы и γ-глутамилтрансферазы.Непропорциональное увеличение трансаминаз может быть связано с обширными метастазами в печени. Увеличение протромбинового времени является результатом исключения желчи из желудочно-кишечного тракта, что приводит к нарушению всасывания жирорастворимого витамина К и снижению выработки печенью факторов свертывания, зависящих от витамина К. У многих пациентов также нарушена толерантность к глюкозе; опубликованные данные указывают на то, что до 70% пациентов с диагностированным раком поджелудочной железы страдают откровенным диабетом или нарушенной толерантностью к глюкозе. w3
Вставка 2: Признаки и симптомы рака поджелудочной железы
Симптомы
Желтуха
Снижение веса
Тошнота
поздняя боль в животе )Анорексия
Диарея
Признаки
Серологические маркеры
Серологические маркеры рака поджелудочной железы могут быть классифицированы как сывороточные ферменты, опухолевые гормоны и регуляторные антигены, производимые эктопическим путем.Опухолевые антигены предлагают наилучшую возможность серодиагностики злокачественных новообразований поджелудочной железы, но пока они не являются ни опухолеспецифичными, ни специфичными для рака поджелудочной железы, а только надежно положительны при запущенной или диссеминированной болезни. 6 Углеводный антиген 19-9 является наиболее часто используемым маркером. Эффективность углеводного антигена 19-9 по сравнению с другими онкомаркерами (карциноэмбриональный антиген, углеводный антиген 50, молекула клеточной адгезии 17.1) при обнаружении карциномы поджелудочной железы широко изучалась; Большинство исследований пришли к выводу, что углеводный антиген 19-9 с его сочетанием высокой чувствительности (около 80%) и высокой специфичности (60-70%) является лучшим онкомаркером, доступным в настоящее время для обнаружения карциномы поджелудочной железы. 6 , 7 Обычно обнаруживается в клетках средних или больших протоков и на просветной поверхности раковых клеток. Повышенные концентрации маркера обычно обнаруживаются у пациентов с раком поджелудочной железы размером ≥ 3 см, w4 , что ограничивает его ценность при обнаружении потенциально резектабельных опухолей. Уровень маркера также может повышаться при других злокачественных новообразованиях кишечника, затрагивающих желудок, толстую кишку или желчевыводящие пути, а также при доброкачественных заболеваниях, таких как панкреатит, гепатит и цирроз. 8 Тем не менее, углеводный антиген 19-9 может играть роль в оценке прогноза и ответа на лечение пациентов, перенесших резекцию поджелудочной железы и химиотерапию. 6
В исследованиях также сравнивалась эффективность онкомаркеров с другими исследованиями по выявлению рака поджелудочной железы. Хотя опухолевые маркеры могут быть такими же чувствительными, как и визуализация, наличие желтухи у многих пациентов значительно снижает специфичность. w5 w6 Новые маркеры, такие как «дезинтегрин и металлопротеаза» (ADAM9) w7 и кадгерин печень-кишечник w8 , активно исследуются с целью их роли в диагностике.Несмотря на затраты, радиологическое исследование останется методом выбора в ближайшем будущем из-за низкой специфичности опухолевых маркеров в клиническом контексте.
Визуальные исследования
Значительные улучшения в неинвазивной радиологической визуализации поперечного сечения за последнее десятилетие значительно расширили возможности диагностики рака поджелудочной железы и планирования соответствующего лечения пациентов. Точная радиологическая стадия заболевания позволяет принять соответствующее клиническое решение и гарантирует, что хирургическое вмешательство будет ограничено теми пациентами, которым это принесет пользу.«Диагностическая» лапаротомия в настоящее время выполняется редко, за исключением случаев, когда она является окончательным арбитром в случаях сомнительной резектабельности.
Ультрасонография
Трансабдоминальное УЗИ обычно является первоначальным скрининговым исследованием у пациентов с желтухой. Он может предоставить неинвазивным способом информацию о размере, локализации и характеристиках первичной опухоли, диаметрах желчных и поджелудочных протоков и месте обструкции. Также можно определить наличие или отсутствие лимфатических узлов или метастатического поражения печени и близость опухоли к крупным сосудам. 9 w5 Ультразвуковое исследование может быть столь же чувствительным и специфичным, как компьютерная томография, при выявлении метастазов в печени. Использование допплеровской ультрасонографии дает достаточно надежную оценку проходимости сосудов и может повысить точность измерения сосудистой инвазии. 9 Однако у этой техники есть свои ограничения. Часто бывает трудно точно оценить поджелудочную железу, размер новообразования и степень распространения. Частота выявления рака при УЗИ колеблется от 57% до 81%. 10 w5 Ультразвуковое исследование зависит от оператора и может быть неточным более чем в одной трети времени из-за таких факторов, как габитус большого тела, наличие асцита или газы в кишечнике (у 20% пациентов 10 ).
Совсем недавно использование ультразвуковой допплерографии с усилением эха (ультразвуковая допплерография после инъекции контрастного вещества) увеличило чувствительность (до 87%) и специфичность (до 94%) этого диагностического метода. 11 Гармоническая ультрасонография с кодированной фазой инверсии – это еще один новый метод, который позволяет в реальном времени визуализировать медленный кровоток в мелких сосудах в опухолях с использованием ультразвукового контрастного вещества, и было показано, что его чувствительность при обнаружении опухолей поджелудочной железы составляет 95% см в диаметре. 12 Эти методы в настоящее время недоступны в свободном доступе, но могут сыграть важную роль в диагностике рака поджелудочной железы в будущем.
Компьютерная томография
Хотя трансабдоминальное УЗИ часто является первым используемым методом визуализации, в настоящее время предпочтительным методом диагностики и определения стадии рака поджелудочной железы является тонкий срез (разрезы 3-5 мм), двухфазная мультидетекторная компьютерная томография с контрастным усилением () . 8 , 13 , 14 Компьютерная томография обеспечивает лучшее определение опухоли, чем ультразвуковое исследование, хотя небольшие метастазы в печень или перипортальные метастазы все же могут быть пропущены.
Компьютерная томография брюшной полости с контрастным усилением, показывающая (A) большое образование в головке поджелудочной железы с закрытием верхней брыжеечной артерии (белая стрелка) и (B) расширенные внутрипеченочные протоки (черные стрелки) и закрытие верхней брыжеечной вены ( белая стрелка)
Текущие критерии компьютерной томографии для неоперабельности включают наличие метастазов (например, печени, брюшины), инвазии в соседние органы, такие как желудок или толстую кишку, а также наложение или окклюзию перипанкреатической сосудистой сети.Обложка воротной вены сама по себе может не указывать на неоперабельность, так как она может быть удалена вместе с опухолью, а затем реконструирована. С этими критериями компьютерная томография оказалась почти на 100% точной в прогнозировании неоперабельного заболевания. w9 Однако прогностическая ценность положительного результата теста невысока, и примерно у 25-50% пациентов, у которых по данным компьютерной томографии прогнозируется резектабельное заболевание, при лапаротомии оказываются неоперабельные поражения. 11 Выявление с помощью предоперационной визуализации пациентов, которым хирургическое обследование не поможет, остается проблемой.Наиболее частые причины неоперабельности – небольшие метастазы опухоли в брюшину или печень (<1 см) и поражение сосудов опухолью. 9 Появление мультидетекторной двухфазной компьютерной томографии, наряду с реконструкцией трехмерного изображения, помогло улучшить предоперационное определение хирургической резектабельности, особенно в отношении сосудистой инвазии.
Магнитно-резонансная томография
Магнитно-резонансная томография в последнее время все чаще используется для оценки опухолей поджелудочной железы, хотя с появлением многодетекторной компьютерной томографии ценность магнитно-резонансной томографии может быть сомнительной. 15 Исследование, сравнивающее магнитно-резонансную томографию и компьютерную томографию при визуализации новообразований поджелудочной железы, пришло к выводу, что магнитно-резонансная томография не дает значительных диагностических преимуществ перед компьютерной томографией. 16 Однако анатомия желчного дерева и протока поджелудочной железы лучше показана при магнитно-резонансной холангиопанкреатографии, чем при компьютерной томографии. Магнитно-резонансная холангиопанкреатография оказалась столь же чувствительной, как и эндоскопическая ретроградная холангиопанкреатография, при обнаружении карциномы поджелудочной железы. 17 Разрешение магнитно-резонансных изображений патологии поджелудочной железы можно улучшить с помощью внутривенного введения гадолиния. Массы поджелудочной железы, расширение желчных или панкреатических протоков и метастазы в печени могут быть показаны очень подробно. 9 , 13 Кроме того, магнитно-резонансная ангиография с контрастным усилением или венография могут показать сосудистое поражение опухоли и устранить необходимость в традиционной ангиографии.
Эндоскопическая ретроградная холангиопанкреатография и чрескожная чреспеченочная холангиография
До широкого распространения эндоскопической ретроградной холангиопанкреатографии чрескожная чреспеченочная холангиография часто использовалась для определения анатомии желчных протоков до операции ().Эндоскопическая ретроградная холангиопанкреатография в значительной степени заменила чрескожную чреспеченочную холангиографию, поскольку она имеет несколько основных преимуществ. Предоперационное разграничение протока обычно необходимо для подтверждения точного места обструкции, исключения сопутствующей патологии и исключения обструкции на нескольких уровнях. w10
Чрескожная чреспеченочная холангиограмма, показывающая катетер в расширенном общем желчном протоке с резкой нерегулярной стриктурой на нижнем конце, указывающей на рак поджелудочной железы
Эндоскопическая ретроградная холангиопанкреатография при надлежащем использовании может обеспечить окончательный диагноз.Это важно, так как только треть опухолей менее 2 см и половина опухолей менее 3 см будут обнаружены с помощью обычной компьютерной томографии. 18 Преимущества эндоскопической ретроградной холангиопанкреатографии перед чрескожной чреспеченочной холангиографией заключаются в том, что она позволяет избежать пункции печени с сопутствующим риском утечки желчи и кровотечения, а также позволяет исключить другие гастродуоденальные заболевания, диагностировать периампулярные опухоли и получать изображения протока поджелудочной железы. Образцы чистки и биопсии также могут быть получены для цитологического и гистологического исследования.
Как эндоскопическая ретроградная холангиопанкреатография, так и чрескожная чреспеченочная холангиография позволяют устанавливать билиарные стенты, а при затрудненном доступе может потребоваться комбинированный подход. Тем не менее, предоперационное стентирование желчных протоков вызывает разногласия. Сьюнат и др. Предположили, что это не принесло никакой пользы и не должно проводиться в плановом порядке. 19 Стентирование обеспечивает идеальное паллиативное лечение для пациентов с желтухой, которые страдают неоперабельным или метастатическим заболеванием или не подходят для хирургической резекции.Расширяемые металлические стенты предлагают отличное паллиативное лечение. w10 На основании имеющихся данных эндоскопическая ретроградная холангиопанкреатография или чрескожная чреспеченочная холангиография со стентированием не должны рутинно использоваться у пациентов с резектабельными опухолями, поскольку это может увеличить частоту септических послеоперационных осложнений. 19 С практической точки зрения стентирование может потребоваться, если операция не ожидается в течение нескольких недель или если концентрация билирубина в сыворотке крови быстро растет.
Эндоскопическое УЗИ
Эндоскопическое УЗИ () – это относительно новый метод, который используется для получения изображений поджелудочной железы с высоким разрешением, позволяя размещать высокочастотный ультразвуковой датчик в желудке и двенадцатиперстной кишке в непосредственной близости от поджелудочной железы. Эндоскопическое ультразвуковое исследование может быть наиболее точным тестом для диагностики рака поджелудочной железы. Исследования, сравнивающие его с компьютерной томографией, показали, что эндоскопическое ультразвуковое исследование имеет более высокую чувствительность и специфичность для этого диагноза, особенно при оценке опухолей <3 см в диаметре. 20 Кроме того, эндоскопическая ультрасонография очень точна для обнаружения местной инвазии и узловых метастазов рака поджелудочной железы, хотя результаты аналогичны по сравнению с двухфазной мультиспиральной мультидетекторной компьютерной томографией. Компьютерная томография дает дополнительную информацию о метастазах в печени. 21 Дуоденоскоп с боковым обзором, который доставляет ультразвуковой датчик, также позволяет обнаруживать ампулярные и дуоденальные карциномы. Однако нехватка оборудования, финансов (ориентировочно 4 фунта стерлингов).2 (7,5 долларов США; 6,2 евро) миллиона необходимо для обеспечения этого учреждения по всей стране ( 22 ), а наличие адекватно подготовленных эндоскопистов означает, что большинству пациентов в Соединенном Королевстве не проводится эндоскопическое ультразвуковое исследование.
Эндоскопическое ультразвуковое изображение, показывающее образование в головке поджелудочной железы по отношению к соседним структурам (CBD = общий желчный проток; HA = печеночная артерия; PV = воротная вена; CA = чревная ось)
Ангиография
В прошлом предоперационная ангиография обычно использовалась для прогнозирования резектабельности и получения информации о анатомии сосудов.Некоторые исследования показали, что ангиография повышает надежность компьютерной томографии, в то время как другие исследования показали, что многодетекторная компьютерная томография может прогнозировать нерезектабельность лучше, чем одна ангиография. 14 Обычная ангиография в настоящее время не входит в диагностический протокол в большинстве центров.
Позитронно-эмиссионная томография
Позитронно-эмиссионная томография – это неинвазивный инструмент визуализации, который предоставляет метаболическую, а не морфологическую информацию об опухолях.Этот метод диагностики основан на большем использовании глюкозы опухолевыми клетками, чем нормальной паренхимой поджелудочной железы. w11 Радиоактивный аналог глюкозы, называемый фтордезоксиглюкозой, вводят внутривенно с последующим обнаружением сканером поглощения фтордезоксиглюкозы опухолью. Злокачественные ткани будут демонстрировать более высокое поглощение фтордезоксиглюкозы, чем нормальные окружающие ткани. Позитронно-эмиссионная томография полезна для диагностики небольших опухолей (<2 см) и выявления внепанкреатических заболеваний, таких как метастазы в брюшину или сальник. 9 В настоящее время он обычно не используется для диагностики рака поджелудочной железы из-за отсутствия анатомических деталей. С появлением комбинированной позитронно-эмиссионной томографии и компьютерной томографии сканирование анатомических и функциональных изображений стало возможным одновременно. 23 w12
Дополнительные образовательные ресурсы
Дополнительная литература
Li D, Xie K, Wolff R, Abbruzzese JL. Панкреатический рак. Ланцет 2004; 363: 1049-57 [PubMed] [Google Scholar]
Yeo TP, Hruban RH, Leach SD, Wilentz RE, Sohn TA, Kern SE и др.Панкреатический рак. Курр Пробл Рак 2002; 26: 176-275 [PubMed] [Google Scholar]
DiMagno EP, Reber HA, Tempero MA. Технический обзор AGA по эпидемиологии, диагностике и лечению аденокарциномы протока поджелудочной железы. Гастроэнтерология 1999; 117: 1464-84 [PubMed] [Google Scholar]
О’Рейли Э., Кельвин Дж. Ф., Харти Дж. Р., Маккалли Дж. 100 вопросов и ответов о раке поджелудочной железы. Суббери, Массачусетс: Джонс и Бартлетт, 2003
Полезные веб-сайты
Cancer Research UK (www.Cancehelp.org.uk/trials/trials/default.asp)— Предоставляет информацию о текущих клинических испытаниях по лечению рака, в том числе с участием рака поджелудочной железы.
Справочник врача (требуется бесплатная регистрация) (www.docguide.com) —Американский веб-сайт для клиницисты.
Может быть настроен для предоставления последних новостей, информации о клинических испытаниях и новостей о достижениях фундаментальных наук для различных медицинских и хирургических состояний.
Проток поджелудочной железы (www.acor.org/pancreas/) – Интересный веб-сайт настроен пациентом с раком поджелудочной железы для людей, у которых диагностировано заболевание
Другие тесты
Чрескожная и эндоскопическая аспирационная цитология под контролем УЗИ
Тонкоигольная аспирационная цитология поджелудочной железы стала одним из основных достижений в ведении пациентов с опухоли поджелудочной железы.Если результаты визуализации указывают на неоперабельную опухоль или метастатическое заболевание, для гистологического подтверждения показана тонкоигольная аспирация под контролем компьютерной томографии или эндоскопической ультрасонографии, если не предполагается паллиативная хирургическая процедура. 9 Биопсия под контролем компьютерной томографии используется более 20 лет и зарекомендовала себя как безопасная и надежная процедура с хорошей чувствительностью. Однако это связано с риском перитонеального и кожного посевов рака – осложнения, которого можно избежать с помощью эндоскопической биопсии под контролем УЗИ.При большей доступности следует попытаться получить предоперационную тонкоигольную аспирацию под эндоскопическим ультразвуковым контролем или биопсию Trucut у всех пациентов с раком поджелудочной железы.
Лапароскопия или лапаротомия
Если результаты визуализации неубедительны, перед окончательной операцией может быть проведена этапная лапароскопия или лапаротомия. Лапароскопию и лапаротомию можно сочетать с интраоперационной ультрасонографией для определения поражений поджелудочной железы и исключения тонких метастазов в печень, которые могли быть пропущены другими методами визуализации. 24 Однако рутинная лапароскопия в настоящее время не рекомендуется, поскольку она влияет на лечение менее чем 14% пациентов с раком поджелудочной железы. 10
Стадия
Рак поджелудочной железы классифицируется с использованием классификации TNM (опухоль, узел, метастаз). Точная стадия играет жизненно важную роль в лечении опухолей поджелудочной железы теперь, когда доступны неоперационные паллиативные методы. Компьютерная томография широко используется в предоперационной стадии новообразований поджелудочной железы.Благодаря недавним достижениям в области магнитно-резонансной томографии и эндоскопической ультрасонографии точность предоперационного определения стадии улучшилась, особенно в отношении местной инвазии и поражения регионарных узлов.
Выводы
Клиницисту доступны несколько методов визуализации для диагностики и определения стадии рака поджелудочной железы, а также предлагается алгоритм лечения. При правильном сочетании диагностических методов можно снизить количество ненужных хирургических исследований. Исследования, сравнивающие различные методы визуализации, используемые для диагностики рака поджелудочной железы, показали, что его трудно диагностировать только на основе компьютерной томографии.Для подтверждения диагноза часто требуются дополнительные обследования или биопсия. Хотя в настоящее время наиболее предпочтительным методом визуализации является компьютерная томография, эндоскопическая ультрасонография и позитронно-эмиссионная томография, вероятно, станут жизненно важными для обнаружения небольших опухолей. В общем, эндоскопическая ретроградная холангиопанкреатография должна быть назначена для лечения пациентов с неоперабельным или метастатическим заболеванием. Несмотря на быстрое развитие методов визуализации, общее влияние этих методов на выживаемость пациентов с раком поджелудочной железы является спорным, поскольку у большинства пациентов все еще присутствует местнораспространенное заболевание.Таким образом, существует потребность в разработке биомаркеров и методов ранней диагностики заболевания у пациентов с симптомами, а также для использования в скрининговых тестах у бессимптомных людей с риском развития карциномы поджелудочной железы. В нем обобщены недавние и продолжающиеся клинические испытания рака поджелудочной железы.
Предлагаемый алгоритм диагностики и лечения рака поджелудочной железы. CA = углеводный антиген; ЭРХПГ = эндоскопическая ретроградная холангиопанкреатография; FBC = полный анализ крови; LFTs = тесты функции печени; PTC = чрескожная чреспеченочная холангиография. * Рекомендации по адъювантной химиотерапии для пациентов с раком поджелудочной железы основаны на недавнем отчете о многоцентровом исследовании, в котором показано преимущество химиотерапии в выживаемости у пациентов с удаленным раком поджелудочной железы w13
Таблица 1
| Испытание | Фаза | Подробная информация | Даты или результаты набора |
|---|---|---|---|
| GEM-CAP | III | Одинарная или комбинированная терапия.Сравнение одного гемцитабина с комбинацией гемцитабина и капецитабина | Апрель 2002 г. – март 2005 г. |
| ESPAC 1 | III | Сравнение выживаемости у пациентов с удаленной опухолью, получавших химиолучевую терапию и химиолучевую терапию, а также химиолучевую терапию и химиолучевую терапию адъювантная терапия | Недавно завершившееся испытание показало, что адъювантная химиотерапия оказывает значительное положительное влияние на выживаемость, тогда как химиолучевая терапия оказывает отрицательное влияние w13 |
| ESPAC 3 v2 | III | и фолиевая кислота | Июль 2000 г. – июль 2005 г. |
| MetXia-OB83 и циклофосфамид | I | Пациентам будет назначена комбинация MetXia-OB83 (генная терапия) и циклофосфамида | с октябряг. по март 2004 г. 2005 |
Примечания
Дополнительные ссылки на bmj.com
Мы благодарим Гурупрасада П. Айтала, консультанта-гепатолога, Университетская больница, Медицинский центр Королевы, Ноттингем, за предоставленные изображения для рисунка 3.
Соавторы: AST и PP просмотрели литературу и подготовили первоначальный и окончательный варианты рукописи . RD рассмотрел аспекты работы с изображениями и участвовал в написании окончательного варианта. DNL проанализировал рукопись и предоставил интеллектуальный вклад и общее руководство в дополнение к подготовке рисунков.АСТ и ДНЛ являются гарантами.
Финансирование: Нет.
Конкурирующие интересы: не заявлены.
Ссылки
1. Куинн М., Бэбб П., Брок А., Кирби Л., Джонс Дж. Тенденции рака в Англии и Уэльсе в 1950–1999 годах. Лондон: Управление национальной статистики, 2001.
2. Джемал А., Мюррей Т., Сэмюэлс А., Гафур А., Уорд Е., Тун М.Дж. Статистика рака, 2003. CA Cancer J Clin. 2003; 53: 5-26. [PubMed] [Google Scholar] 3. Ли Д., Се К., Вольф Р., Аббруззезе Дж. Л.. Панкреатический рак. Ланцет 2004; 363: 1049-57.[PubMed] [Google Scholar] 4. DiMagno EP. Рак поджелудочной железы: клинические проявления, подводные камни и первые подсказки. Энн Онкол 1999; 10 (приложение 4): 140-2. [PubMed] [Google Scholar] 5. Гулло Л. Диабет и риск рака поджелудочной железы. Энн Онкол 1999; 10 (приложение 4): 79-81. [PubMed] [Google Scholar] 6. Yeo TP, Hruban RH, Leach SD, Wilentz RE, Sohn TA, Kern SE и др. Панкреатический рак. Курр Пробл Рак 2002; 26: 176-275. [PubMed] [Google Scholar] 7. Озкан Х., Кая М., Дженгиз А. Сравнение онкомаркера CA 242 с CA 19-9 и карциноэмбриональным антигеном (CEA) при раке поджелудочной железы.Гепатогастроэнтерология 2003; 50: 1669-74. [PubMed] [Google Scholar] 8. Тамм Е.П., Сильверман П.М., Чарнсангавей С., Эванс Д.Б. Диагностика, стадия и наблюдение за раком поджелудочной железы. AJR Am J Roentgenol 2003; 180: 1311-23. [PubMed] [Google Scholar] 9. Кларк Д.Л., Томсон С.Р., Мадиба Т.Е., Саника С. Предоперационная визуализация рака поджелудочной железы: подход, ориентированный на лечение. J Am Coll Surg 2003; 196: 119-29. [PubMed] [Google Scholar] 10. Поттер М.В., Шах С.А., Макинани П., Чари Р.С., Каллери М.П. Критическая оценка лапароскопической стадии злокачественных новообразований печени и желчевыводящих путей.Хирург Онкол 2000; 9: 103-10. [PubMed] [Google Scholar] 11. Rickes S, Unkrodt K, Neye H, Ocran KW, Wermke W. Дифференциация опухолей поджелудочной железы с помощью обычного ультразвука, неулучшенной и усиленной эхо-допплерографии. Сканд Дж Гастроэнтерол 2002; 37: 1313-20. [PubMed] [Google Scholar] 12. Китано М., Кудо М., Маэкава К., Суэтоми Ю., Сакамото Х., Фукута Н. и др. Динамическая визуализация заболеваний поджелудочной железы с помощью контрастно-усиленного кодированного гармонического ультразвукового исследования с инверсией фазы. Кишечник 2004; 53: 854-9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 13.Kalra MK, Maher MM, Mueller PR, Saini S. Современная визуализация новообразований поджелудочной железы. Br J Radiol 2003; 76: 857-65. [PubMed] [Google Scholar] 14. Варгас Р., Нино-Мурсия М., Трублад В., Джеффри Р. Б. Младший. MDCT аденокарциномы поджелудочной железы: прогнозирование сосудистой инвазии и резектабельности с использованием многофазной техники с изогнутыми плоскими реформами. AJR Am J Roentgenol 2004; 182: 419-25. [PubMed] [Google Scholar] 15. Hanbidge AE. Рак поджелудочной железы: лучшее изображение для ранней диагностики – КТ, МРТ, ПЭТ или УЗИ? Может Дж Гастроэнтерол 2002; 16: 101-5.[PubMed] [Google Scholar] 16. Штайнер Э., Старк Д. Д., Хан П. Ф., Сайни С., Симеоне Дж. Ф., Мюллер П. Р. и др. Визуализация новообразований поджелудочной железы: сравнение МРТ и КТ. AJR Am J Roentgenol 1989; 152: 487-91. [PubMed] [Google Scholar] 17. Адамек Х.Э., Альберт Дж., Брер Х., Вайц М., Шиллинг Д., Риман Дж. Ф. Обнаружение рака поджелудочной железы с помощью магнитно-резонансной холангиопанкреатографии и эндоскопической ретроградной холангиопанкреатографии: проспективное контролируемое исследование. Ланцет 2000; 356: 190-3. [PubMed] [Google Scholar] 18.Грэм Р.А., Бэнкофф М., Хедигер Р., Шейкер Х.З., Рейнхольд РБ. Тонкоигольная аспирационная биопсия аденокарциномы протока поджелудочной железы: потеря диагностической точности с небольшими опухолями. J Surg Oncol 1994; 55: 92-4. [PubMed] [Google Scholar] 19. Sewnath ME, Karsten TM, Prins MH, Rauws EJ, Obertop H, Gouma DJ. Метаанализ эффективности предоперационного дренирования желчевыводящих путей при опухолях, вызывающих механическую желтуху. Энн Сург 2002; 236: 17-27. [Бесплатная статья PMC] [PubMed] [Google Scholar] 20. Mertz HR, Sechopoulos P, Delbeke D, Leach SD.ЭУЗИ, ПЭТ и КТ для оценки аденокарциномы поджелудочной железы. Гастроинтест Эндоск 2000; 52: 367-71. [PubMed] [Google Scholar] 21. Midwinter MJ, Beveridge CJ, Wilsdon JB, Bennett MK, Baudouin CJ, Charnley RM. Корреляция между спиральной компьютерной томографией, эндоскопической ультрасонографией и данными операций при опухолях поджелудочной железы и ампулах. Br J Surg 1999; 86: 189-93. [PubMed] [Google Scholar]22. Национальная группа по онкологическим заболеваниям. Руководство по заказу онкологических служб: улучшение результатов лечения рака верхних отделов желудочно-кишечного тракта: пособие.Лондон: NHS Executive, 2001.
23. Хостен Н., Лемке А.Дж., Виденманн Б., Бохмиг М., Розевич С. Комбинированные методы визуализации рака поджелудочной железы. Ланцет 2000; 356: 909-10. [PubMed] [Google Scholar] 24. Пистерс П. У., Ли Дж. Э., Вотхи Дж. Н., Чарнсангавей К., Эванс Д.Б. Лапароскопия в диагностике рака поджелудочной железы. Br J Surg 2001; 88: 325-37. [PubMed] [Google Scholar]Аутоиммунный панкреатит: ассоциированная гепатомегалия и Спленомегалия
Отчет о болезниОткрытый доступ
Аутоиммунный панкреатит: ассоциированная гепатомегалия и Спленомегалия
Марко А. Трухильо-Хуарес 1 * и Хорхе Т. Мендоса 2
1 * MD, Внутренняя медицина / инфекционные болезни SEMSA, Манаус-Ам.Бразилия
2 MD, Автономный университет Гвадалахары Unidad Ciencias Biológicas
Поступила: 24.02.2018 г .; Принята в печать: 28 мая 2018 г .; Опубликовано: 14 ноября 2018 г.
Образец цитирования: Трухильо-Хуарес MA, Mendoza JT (2018) Аутоиммунный панкреатит: ассоциированная гепатомегалия и спленомегалия. Int J Клинические испытания открытого доступа 2 (1): 1-5.
Введение: Аутоиммунный панкреатит – это заболевание, которое недавно вызвал интерес к его описанию, связанному с большинство отчетов из международной специализированной литературы на события хронического панкреатита, рак поджелудочной железы и связанные с проявления аутоиммунитета с наличием аутоантител.Аутоиммунный панкреатит – доброкачественное фибровоспалительное заболевание поджелудочная железа вероятного аутоиммунного происхождения, которая включает 2 различных фенотипа
: тип 1 (лимфоплазмоцитарный склерозирующий панкреатит) и тип 2 (идиопатический протоковоцентрический панкреатит).Его клиническая картина поскольку механическая желтуха у пациентов с новообразованием поджелудочной железы является обычным явлением и поэтому он должен быть включен в дифференциальную диагностику неоплазия поджелудочной железы. Было описано множество диагностических критериев. Самыми известными являются критерии HISORT клиники Mayo и критерии международного консенсуса 2011 года.
Клинический случай: Мы представляем случай женщины 33 лет с клинические данные о боли в животе, тошноте, рвоте и присутствии гепатомегалии 17 см (6.69 дюймов) ниже реберного фланца и спленомегалия весом 975 г (2,1 фунта) в дополнение к лихорадке, достигающей 38,8 ° C (101,8 ° F) преобладание ночного образа жизни и потоотделение с 32 месяцев эволюции и потери веса около 4 кг (11 фунтов) за последние 4 месяца.
Обсуждение: Аутоиммунный панкреатит – сущность мало известно менее 100 случаев, зарегистрированных в литературе, однако, иммунные данные преобладают, предположительный диагноз был поставлен с критерии оценки: диффузного увеличения поджелудочной железы ( сущность), антитела и гистопатологические данные перидуктального фиброза или сегментарно основного протока поджелудочной железы и лимфоплазмоцитарной инфильтрация в поджелудочной железе и ответ на стероиды был значительным.Но как японское, так и американское общество в своих публикациях, чтобы установить диагностическим критериям, особенно в японском обществе, которое устанавливает 3 из опубликованных критериев, таких как изменение изображения, серология, ответ на лечение стероидами и отсутствие злокачественных новообразований, It практически то же самое в критериях HISORT за исключением гистологических исследований, Японское общество поджелудочной железы, устанавливает 3 критерия присутствует на момент постановки диагноза Японским обществом поджелудочной железы изначально и в настоящее время все еще использую.
Ключевые слова: Аутоиммунный панкреатит; Учебная лихорадка; Гепатомегалия и спленомегалия в исследовании; Аутоиммунное заболевание;
Введение
Термин аутоиммунный панкреатит (АИП) был использован впервые раз в 1995 году Йошида и Колс, связанные с аутоиммунным механизмы без признаков аутоиммунного заболевания, поэтому предлагается название или термин аутоиммунного панкреатита. форма хронического панкреатита, более 30% пациентов обращаются это изображение не связано с употреблением алкоголя или явной причиной [1].Он имел предыдущие названия, такие как идиопатический хронический панкреатит, в медицинских отчетах описан хронический склерозирующий панкреатит это образование связано с аутоиммунными заболеваниями коллагена [2, 3]. Этот объект считается редким, и количество отчетов в специализированная медицинская литература немногочисленна, в основном описывается в Азии (Япония) и среди кавказцев как в Европе и Северной Америки, исследования показали, что Латинская Америка сообщает об отдельных случаях больше в Бразилии и Мексике, несколько в Чили и Колумбия 30.А США и Европа – это несколько случаев в клинике Мэйо. 29 ящиков 15, 16.
Таблица A: Различия между аутоиммунным панкреатитом типа 1 и тип 2
| AIP -1 | AIP-2 |
Возраст | > старый 61,8 ± 14,24 | > Молодой 37.7 ± 5,7 |
Пол | Доминирование мужчин | Мужской пол> что женщины |
Территория | Япония-Корея 80% случаев Европа-США Не знаю полностью | Европа – США Не знаю полностью Япония – Корея Меньшее количество случаев |
Спектр | Кобели: 3.5: 1 | Самцы 2: 1 |
Гистология | Склерозирующий лимфоплазмоцитарный панкреатит. Положительные клетки на IgG4. выводы с высокой частотой | Панкреатит идиопатического центрального протока Эпителиальные гранулоцитарные поражения Частота Норма. |
Серология I gG4 | 80%> 5-10 раз | 17% или меньше. |
Ответ на стероиды | Отлично | Отлично |
Тип 2: в основном встречается при поражении поджелудочной железы и с отсутствием IgG4-положительных клеток и труднее диагностировать [16, 17].
Клинический спектр болезней: AIP типа 1 средний возраст от 61 до 62 лет на момент постановки диагноза, частота у мужчин больше выше пропорция 2: 1, серология IgG4 были выше 80%> 140 мг / дл. Гистология, демонстрирует аффектацию, как классический образец перидуктального богатства при инфильтрации IgG4, увеличении поджелудочной железы, поражении других органы. Тип 2 были моложе около 39 лет, доля 77%. до 55% женщин. По типу снимок с увеличением поджелудочной железы гипоплотность гомогенная Длинная стриктура поджелудочной железы протока, без значительного сопутствующего расширения, также сильно характеристика AIP, Серология: IgG4 нечасто повышен по типу 2, может присутствовать у здоровых людей около 5% и 10% у больных раком поджелудочной железы повышен уровень IgG4 [17, 18, 19].Сами по себе антитела IgG4 не имеют ценности для диагностики AIP.
Аутоиммунный панкреатит характеризуется группой таких данных, как эпизоды боли в животе, иногда с события желтухи, не всегда как 2 типа, лабораторные данные с этой сущностью связаны: увеличение концентраций IgG4, наличие аутоантител, таких как: антитела против лактоферрина антитела против карбоангидразы II, антитела против двухцепочечных ДНК [6, 7]. Гистологический вид обнаружен в однородная форма, фибросклероз забрюшинного пространства, включает дополнительные протоки поджелудочной железы и лимфоплазмоцитарная инфильтрация поджелудочной железы Тип 1 [4, 8, 9].Данные отчетных имидж-исследований Хироюки с соавторами, установленными в исследованиях компьютерной томографии: 1 [6, 10]. Увеличение размера диффузно ослабленной поджелудочной железы, что может задействовать всю поджелудочную железу; то есть голова, тело и хвост в разных интенсивность, без аденопатий, без поражения сосудов, с наличием небольших кальцификатов, может иметь перипанкреатический ореол с гладкими краями без воздействия на перипанкреатический жир и до забрюшинного уровня, с данными фиброза, эти данные присутствуют не у всех пациентов, о которых сообщают.В Динамические исследования IMR T1 сообщают об обнаружении аномальной интенсивности в диффузной форме, низкой интенсивности по отношению к печени, в Т2 интенсивность паренхимы поджелудочной железы больше, чем у можно наблюдать печень и ореол вокруг головки поджелудочной железы.
Кейс-презентация
Женщина 33 лет, с анамнезом в эпигастральной области живота. боль с 3 годами эволюции, связанная с приемом пищи, ночной образ жизни потоотделение, которому иногда предшествуют подъемы температуры, достигающие 38.8 ~ C (101,8 ° F), в течение 24 месяцев, интенсивность боли в животе увеличивается с приемом пищи и постоянным тошнотворным состоянием и периодические постпрандиальные рвоты, потоотделение усиливается при интенсивность и показала болезненные язвы во рту на краю языка, без наличия язв ни в каком другом секторе экономики и за 2 месяца до постановки в больницу она перенесла 4 потеря веса килограммов (11 фунтов). Остальные симптомы и признаки были часты два раза в неделю, она была госпитализирована по поводу лихорадки случай в области внутренней медицины.Эта таблица (1), показывающая Клинические данные наших пациентов и заявленные.
Таблица 1: Сравнение клинических характеристик на начальном этапе между пациентов сообщили о
Клинические характеристики | Справка для пациентов | Наш пациент | Диагностическое значение |
Возраст | 66лет | 32 года | |
Мужской / женский | 4.7; 1 | 1 | |
Механическая желтуха | Часто | Нет | |
Боль в животе | Есть 60% | Есть | |
Потеря массы тела (0,5 кг в прошлом | Не всегда | Есть | |
3 месяца) | 90% | Есть | |
Изменение протока поджелудочной железы | Часто | Нет | |
IgG4 (мг / дл) | > 130 мг / дл | 136 мг / дл | x |
Антинуклеарные антитела | Есть | Есть | x |
Поражение других органов | Есть | Есть | x |
Склерозирующий холангит | Есть | Нет | |
Забрюшинный фиброз | Может быть | Нет | |
Сиалоаденит | 10-12% | Нет | |
Увеличение печени | Не сообщалось | Есть | |
Увеличение селезенки | Не сообщалось | Есть | |
Увеличение поджелудочной железы | 100% | Есть | x |
Злонамеренность исключена | Поджелудочная железа или другие | Есть | x |
Ответ на стероиды | 80% | Есть | x |
Гистологические признаки | фиброз и заметная инфильтрация лимфоцитов | Не реализовано |
Исследования лаборатории
Гемоглобин 12.3 г / дл, тромбоциты 130 K / дл, лейкоциты: лейкоциты 4,56 К / мл, нейтрофилов 6300 / мл Лимфоцитов 1200 / мл, Моноциты 200 / мл, Эозинофилы 50 / мл, Базофилы 20 / мл, Доказательства Печеночной функции: TGO 29 МЕ / л, TGP 20 МЕ / л, общий билирубин 0,48 мг / дл, альбумин 4,11 г / дл, глобулины 2,4, щелочная фосфатаза 111 МЕ / л, молочнокислая дегидрогеназа 444 Ед / л (1,47укат / л л), dcANA Сильно положительный (56 МЕ / л), отрицательный анти-Sm, отрицательный C-ANCA, P-ANCA 2 отрицательный, Direct Coombs слегка положительный, Rose Bengal тест отрицательный, посев костного мозга на бруцеллы отрицательный на 2, 10, 30 дней, Серология на вирус гепатита B, C отрицательный, ELISA ВИЧ-1 и 2 отрицательные, ПЦР (полимеразная цепная реакция) на ЦМВ, отрицательный, одиночный вирус, отрицательный герпес, C3 и C4 (1.3 мг / л и 0,32 мг / л соответственно) нормальные уровни, CA 19-9: 5,07 МЕ / мл (нормальный 0-37), амилаза 120 ед / л (ранг 28-120 ме / л), липаза 36,5 Ед / л (уровни 13-60) Реактивный белок C 34 мг / дл, (Этюды изображения
Компьютерная томография: размеры головки поджелудочной железы 3,68 см (1,44 дюйма), корпус 2,89 см (1,13 дюйма), хвост 1,98 см (0,779 дюйма) ширина, однородная плотность (с пониженной плотностью) с ореолом наличие в головке поджелудочной железы (Рисунок 1), Печень уменьшена плотность и 17 см (6,69 дюйма) головно-каудальный рост, 14 сантиметров (5.51 дюйм) длинная селезенка и 975 г (2,1 фунта) вес (Рисунок 2), Отрицательные ретроперитонеальные ганглии, самые крупные диаметром 0,6 см (0,236 дюйма), абдоминальная эхография: с увеличение размеров поджелудочной железы в целом с гипоплотностью, гладкое края, без вовлечения перипанкреатического жира, пункционная аспирация биопсия печени иглой Trucut 16 Fr под контролем эхографии с отрицательной цитологией на опухолевые клетки (Рисунок 2, Рисунок 3) окраска по Цилю-Нильсену отрицательная. С данными аутоиммунного Панкреатит по классификации томографии Хироюки и клинические критерии Японского общества поджелудочной железы при отсутствии подтверждения новообразования.Представляем Таблицу (2) показывающее, что соответствует критерию диагноза. У нашего пациента критерий необходим [24, 29].
Рисунок 1: Поджелудочная железа выросла, а однородная плотность уменьшилась (1), Спленомегалия (2) и увеличенная печень (3).
Рисунок 2: Trucut 16 Fr биопсии печени показывает нормальную ультраструктуру.
Рисунок 3: Нормальная гистопатология печени без признаков новообразования.
Таблица 2: Для диагностики
США: * Критерии HISORt клиники Мэйо основаны на 5 основных диагностических критериях |
1) гистологические данные, 2) визуализация, 3) серология, 4) вовлечение других органов и |
Япония / Азия В 2002 году Японское общество поджелудочной железы |
Присутствуют 3 критерия: 1) Увеличение поджелудочной железы при визуализации, |
Уход за задней стенкой
Начали лечение стероидами 0.5 мг / кг / день, с Симптоматическое улучшение, подтверждающее диагноз аутоиммунного панкреатит и амбулаторный контроль.
Обсуждение
Аутоиммунный панкреатит – малоизвестное заболевание. несколько зарегистрированных случаев в литературе до 2000 г., около 100 зарегистрированных случаев, быстро увеличивающиеся, с преобладанием у мужчин нет данных, подтверждающих наличие экзокринной недостаточность, которая встречается редко, но, как и общие данные, боль в эпигастральной области живота умеренной интенсивности без данных механической желтухи дифференциальная диагностика включает: преимущественно хронический панкреатит с распространенностью 6% всех хронических панкреатитов и / или рака поджелудочной железы [13, 14].В данном случае клиническими данными являются: боль в эпигастральной области живота, потоотделение или ночное потоотделение, наличие язв во рту, вокруг Снижение веса на 11 фунтов за последние 6 месяцев до обследования. Исследования изображений предполагают диагностику аутоиммунного панкреатита. согласно критериям Японского общества поджелудочной железы (Японское общество поджелудочной железы) с исследованием изображения (вычисленное Томография брюшной полости) с поздним снимком для оценки диффузного увеличение гипоплотности поджелудочной железы однородного типа, Серологические результаты положительны на антинуклеарные антитела, а также показатели воспаления как высокая СОЭ и очень высокая реактивный белок C (антинуклеарные антитела с высоким заголовком), IgG4, только положительные антитела не могут использоваться для диагностики, противоречия, считались доброкачественными, предположили, что они могли быть защитными антиангидразными углеродными антителами, положительными антитела против лактоферритина, отрицательные анти-SM и многие другие антитела были связаны с AIP, но не используются для диагностика только с помощью серологии [20, 21 и 22].
С ответом на стероиды на
Использование стероидов a Хотя нет никаких перспектив рандомизированные исследования использования стероидов при аутоиммунном панкреатите (AIP), но значительно меньше пациентов, получавших стероиды. терапия пережила рецидив по сравнению с теми, кто получил только поддерживающая терапия неизвестный механизм стероидной терапии [24]. Были предложены различные схемы снижения дозы стероидов. медицинскими центрами по всему миру в США используется 40-60 мг / день в течение 4 недель в качестве обычного лечения в Европе некоторые врачи используют начальные дозы 60 мг / день, Япония и Корея такие же, как США, Избранным препаратом является Преднизолон [24, 25 и 26].После чего доза снижается на 5 мг в неделю с попыткой вывести стероид полностью.
В отличие от японской практики использования поддерживающей терапии у большинства пациентов поддерживающая терапия в Соединенных Штатах используется только у тех пациентов, у которых возник рецидив после начального курса стероиды [28, 29].
- Йошида К., Токи Ф, Такеучи Т., Ватанабе С., Ширатори К. и Хаяси Н. Хронический панкреатит, вызванный аутоиммунной аномалией: предложение концепции аутоиммунного панкреатита.Dig Dis Sci. 1995; 40 (7): 1561-1568.
- Sarles H, Sarles JC, Muratore R и Guien C. Хронический воспалительный склероз поджелудочной железы: автономное заболевание поджелудочной железы. Am J Dig Dis. 1961; 6: 668-698.
- Дрейлинг Д.А. и Сото Дж. М.. Вовлечение поджелудочной железы в диссеминированное «коллагеновое» расстройство. Am J Gastroenterol. 1976; 66 (6): 546-553.
- Ohara H, Nakazawa T., Ando T и Joh T. Системные внепанкреатические поражения, связанные с аутоинммунным панкреатитом. J. Gastroenterol.2007; 42 (Дополнение 18): 15-21. Doi: 10.1007 / s00535-007-2045-9.
- Хироюки Ирие, Хироши Хонда, Синго Баба, Тоширо Куроива и Ранго Йошимицу. и другие. Аутоиммунный панкреатит: характеристики КТ и МРТ. Являюсь. J. Радиология. 1998; 170: 1323-1327.
- Ghazale, Chari ST, Smyrk TC, Levy MJ, Topazian MD и Takahashi N et al. Значение сывороточного IgG4 в диагностике аутоиммунного панкреатита и в отличии его от рака поджелудочной железы. Am J Gastroenterol. 2007; 102 (8): 1646-1653.Doi: 10.1111 / j.1572-0241.2007.01264.x.
- Morselli-Labate AM и Pezzilli R. Полезность сывороточного IgG4 в диагностике и последующем наблюдении за аутоиммунным панкреатитом: систематический обзор литературы и метаанализ. J Gastroenterol Hepatol. 2009; 24 (1): 15-36. Doi: 10.1111 / j.14401746.2008.05676.x.
- Bang SJ, Kim MH, Kim DH, Lee TY, Kwon S и Oh HC. и другие. Достаточно ли биопсии ядра поджелудочной железы для диагностики аутоиммунного хронического панкреатита? Поджелудочная железа. 2008; 36 (1): 84-89. Дой: 10.1097 / МПа. 0b013e318135483d.
- Хирано К., Фукусима Н., Тада М., Исаяма Х., Мизуно С. и Ямамото К. и др. Диагностическая ценность биоптатов при аутоиммунном панкреатите. J Gastroenterol. 2009; 44 (7): 765-773.
- Сугумар А., Леви М.Дж., Камисава Т., Ким М.Х., Эндерс Ф. и Захир Амин. и другие. Применение эндоскопической ретроградной панкреатограммы (ERP) для диагностики аутоиммунного панкреатита (AIP): международное двойное слепое рандомизированное многоцентровое исследование. Gastrointest Endosc. 2009; 69 (5): AB124.Doi:;: // https doi.org/10.1016/j.gie.2009.03.140.
- Гарднер ТБ, Леви MJ, Такахаши Н., Смирк TC и ChariST. Неправильный диагноз аутоиммунного панкреатита: предостережение клиницистам. Am J Gastroenterol. 2009; 104 (7): 1620-1623. Doi: 10.1038 / ajg.2008.89.
- Камисава Т., Имаи М., Чен П Юи, Ту И, Эгава Н. и Цурута К. и др. Стратегия дифференциации аутоиммунного панкреатита от рака поджелудочной железы. Поджелудочная железа. 2008; 37 (3): e62-67. Doi: 10.1097 / MPA.0b013e318175e3a0.
- Вильялобос Санчес А, Муньос-Морьентес А, Петер Перес.Наварро, Дж. М. Регера Иглесиас, Гомес Р. Уэльгас. Анналы внутренней медицины. 2008; 27 (7): 359-361.
- Д.-Уэйн М., Деламн К.А., Курт Т., Гросси Р., Сабатини М. и Куперман. Аутоиммунный панкреатит, Архитектура, 2005; 140: 1104-1007.
- Park DH, Kim MH и Chari ST. Последние достижения в области аутоиммунного панкреатита. Кишечник. 2009. 58 (2): 1680–1689. Doi:; 10.1136 / gut.2008.155853corr1.
- Morselli-Labate AM и Pezzilli R. Полезность сывороточного IgG4 в диагностике и последующем наблюдении за аутоиммунным панкреатитом: систематический обзор литературы и метаанализ.J Gastroenterol Hepatol 2009; 24 (1): 15–36. Doi: 10.1111 / j.1440-1746.2008.05676.x
- Гьянпракаш А. Кетвару и Сунил Шет. Аутоиммунный панкреатит. Отчет гастроэнтеролога (oxf). 2013; 1 (1): 27–32. Doi: ;; 10.1093 / gastro / got011.
- Ghazale, Chari ST, Smyrk TC, Levy MJ, Topazian MD и Takahashi N et al. Значение сывороточного IgG4 в диагностике аутоиммунного панкреатита и в отличии его от рака поджелудочной железы. Am J Gastroenterol. 2007; 102 (8): 1646-1653. Doi: 10.1111 / j.1572-0241.2007.01264.x.
- Sah RP и Chari ST. Серологические проблемы при системном заболевании, связанном с IgG4, и аутоиммунном панкреатите. Curr Opin Rheumatol 2011; 23 (1): 108–113. Doi: 10.1097 / BOR.0b013e3283413469.
- Aalberse RC, Stapel SO, Schuurman J и Rispens T. Иммуноглобулин G4: нечетное антитело. Clin Exp Allergy. 2009. 39 (4): 469–477. Doi: 10.1111 / j.1365-2222.2009.03207.x.
- Райна А., Красинскас А.М., Грир Дж. Б., Лэмб Дж., Финк Е. и Мозер А. Дж. и другие. Уровни сывороточного иммуноглобулина G фракции 4 при раке поджелудочной железы: повышение, не связанное с аутоиммунным панкреатитом.Arch Pathol Lab Med. 2008. 132 (1): 48–53. ; Doi: 10.1043 / 1543-2165 (2008) 132 [48: SIGFLI] 2.0.CO; 2.
- Хуссейн Р., Пойндекстер Р. В. и Оттесен Е. А.. Контроль аллергической реактивности при филяриатозе человека. Преимущественная локализация блокирующих антител к подклассу IgG4. J Immunol. 1992. 148 (9): 2731–2737.
- Chari ST, Smyrk TC, Levy MJ, TopazianMD, Takahashi and Zhang L. et al. Диагностика аутоиммунного панкреатита: опыт клиники Мэйо. Clin Gastroenterol Hepatol. 2006. 4 (8): 1010–1016.Doi: 10.1016 / j.cgh.2006.05.017.
- Камисава Т., Эгава Н., Накадзима Н., Цурута К. и Окамото А.; Морфологические изменения после стероидной терапии при аутоиммунном панкреатите .; Scand J Gastroenterol. 2004. 39 (11): 1154–1158 .; Дой: 10.1080 / 00365520410008033.
- Sugumar A1, Chari S. Аутоиммунный панкреатит: обновленная информация. Эксперт Рев Гастроэнтерол Гепатол. 2009; 3 (2): 197-204. Doi: 10.1586 / egh.09.2.
- Камисава Т., Симосэгава Т., Окадзаки К., Нишино Т., Ватанабэ Х. и Канно А.и другие. Стандартное стероидное лечение аутоиммунного панкреатита. Кишечник. 58 (11): 1504-1507. Doi: 10.1136 / gut.2008.172908 .;
- Хирано К., Тада М., Исаяма Х., Ягиока Х., Сасаки Т. и Когуре Х. и др. Долгосрочный прогноз аутоиммунного панкреатита с лечением кортикостероидами и без него. Кишечник. 2007; 56 (12): 1719-1724. Doi: 10.1136 / gut.2006.115246.
- Райна А., Ядав Д., Красинскас А.М., МакГрат К.М., Халид А. и Сандерс М. и др. Оценка и лечение аутоиммунного панкреатита: опыт в крупном центре США.Ам Дж. Гастроэнтерол, 2009; 104 (9): 2295-2306, Doi: 10.1038 / ajg.2009.325.
- Pannala R and Chari ST. Кортикостероидное лечение аутоиммунного панкреатита. Кишечник. 2009. 58: 1438-1439.
- Себастьян Эррера, Хуан Карлос Браво, Луис Гильермо Аранго и Карлос Альберто Каньяс. Первичный гиперпаратиреоз, связанный с аутоиммунным панкреатитом, склерозирующим холангитом и вероятной аутоиммунной гипогликемией. Acta Med Colomb. 2012; 37 (2): 80-82.
Визуализация диффузных и воспалительных заболеваний печени
22.5.1 Бактериальный (пиогенный) абсцесс
Пиогенный абсцесс, хотя и нечастый в эпоху антибиотиков, по-прежнему представляет собой серьезную проблему с клинической точки зрения, поскольку его проявления весьма разнообразны, от глубокого сепсиса до хронических вялых симптомов.
Расширенная компьютерная томография может надежно диагностировать более 90% гнойных абсцессов печени, выявляя две основные модели: множественные микроабсцессы (диссеминированные или сгруппированные) и большие макроабсцессы. Благодаря хорошему пространственному и контрастному разрешению компьютерная томография (КТ) является единственным лучшим методом обнаружения абсцесса печени с чувствительностью до 97%.На компьютерной томографии абсцессы выглядят как обычно округлые образования, которые являются гиподензивными как на контрастных, так и на неконтрастных изображениях. Центральный газ в виде пузырьков воздуха или уровня воздух-жидкость является специфическим признаком, но он присутствует менее чем в 20% случаев. Также отмечается толстый, усиливающийся периферический ободок.
При МРТ воздух внутри абсцесса выглядит как сигнальная пустота, поэтому его труднее отличить от кальцификатов. Однако форма и расположение (уровень воздух-жидкость) должны позволить поставить правильный диагноз.После введения гадолиния-DTPA абсцессы обычно показывают усиление обода (знак «двойной цели»). Небольшие поражения (<1 см) могут усиливать гомогенно имитирующие гемангиомы. Чрескожная аспирация под контролем изображения с последующим дренированием является методом выбора для окончательной диагностики и лечения с успехом более чем в 90% случаев.
22.5.2 Амебный абсцесс
Печеночный абсцесс – наиболее частое внекишечное проявление амебиаза, поражающее примерно 10% пациентов с амебиазом.Entamoeba histolytica , хотя и редко встречается в континентальной части США, инфицировано 10% мирового населения. Клинически пациенты с амебным абсцессом болеют более остро, чем пациенты с гнойным абсцессом, с высокой температурой и болью в правом подреберье. Диагноз ставится на основании положительных серологических титров амебов, хотя ложноотрицательные результаты составляют почти 20%.
КТ хорошо демонстрирует внепеченочные расширения грудной стенки, плевры или прилегающих внутренних органов. Чрескожное катетерное дренирование амебного абсцесса редко необходимо из-за эффективности амебицидной терапии.Иногда чрескожный дренаж необходим при больших симптоматических абсцессах с плохой реакцией на медикаментозное лечение, подозрением на бактериальную суперинфекцию и угрозой внутриперикардиального разрыва. КТ-вид амебного абсцесса изменчив и неспецифичен. Поражения обычно представляют собой периферические, круглые или овальные области с низким затуханием (10–20 единиц Хаунсфилда). Периферический край с немного более высоким затуханием можно увидеть на неконтрастном сканировании и показывает заметное усиление после введения контрастного вещества.
На МРТ амебные абсцессы печени представляют собой сферические и обычно одиночные поражения с гиперинтенсивным центром на T2-взвешенных изображениях и гипоинтенсивным центром на T1-взвешенных изображениях. Стенка абсцесса толстая, и на изображениях, усиленных гадолинием, картина усиления аналогична таковой при гнойном абсцессе [26].
22.5.3 Эхинококковая болезнь
Эхинококкоз имеет две основные формы, поражающие людей Echinococcus granulosus и Echinococcus multilocularis или alveolaris .Эти инфекции имеют четко определенное и разное географическое распространение. Патологические данные и результаты визуализации у этих паразитов сильно различаются.
На компьютерной томографии E. granulosus выглядит как однокамерные или многокамерные, четко очерченные кисты с толстыми или тонкими стенками. Дочерние кисты обычно рассматриваются как области с меньшим затуханием, чем материнская киста, и обычно находятся на периферии поражения. Дочерние кисты также могут свободно плавать в просвете материнской кисты, поэтому изменение положения пациента может изменить положение этих кист, подтверждая диагноз эхинококковой инфекции.Криволинейный кольцевой кальциноз также является обычным явлением.
Согласно исследованиям МРТ, киста эхинококковых кист аналогична таковой у других кист с длительным временем релаксации T1 и T2. Однако МРТ лучше всего демонстрирует перицисту, матрикс и эхинококкоз (мусор, состоящий из освобожденных сколичек) и дочерние кисты. Перициста обычно имеет низкую интенсивность сигнала на T1- и T2-взвешенных изображениях из-за его волокнистого компонента. Этот ободок и его вид с множеством ячеек или множеством кистей являются отличительными чертами.Матрица эхинококка кажется гипоинтенсивной на T1-взвешенных изображениях и заметно гиперинтенсивной на T2-взвешенных изображениях. При наличии дочерние кисты гипоинтенсивны относительно матрикса как на T1-, так и на T2-взвешенных изображениях (рис. 22.7). Плавающие мембраны имеют низкую интенсивность сигнала на T1- и T2-взвешенных изображениях. 22.7Киста Echinococcus granulosus. Мужчина 28 лет с болью в правом подреберье. Осевое ( a ) T2-взвешенное изображение демонстрирует большую кистозную массу в правой доле печени, которая окружена гипоинтенсивным ободком и содержит более гиперинтенсивные кисты меньшего размера по периферии.На аксиальном T1-взвешенном изображении ( b ) хорошо визуализируется гипоинтенсивный край, а периферические кисты гипоинтенсивны относительно центра поражения
E. multilocularis выглядит как сплошная большая масса или массы с от минимального до отсутствующего усиления после внутривенного введения контрастного вещества и возможной мелкой точечной кальцификации [27, 28, 29].
Осложнения печени, поджелудочной железы и желчевыводящей системы, связанные с терапией рака: перспективы визуализации | Insights into Imaging
Робинсон С.М., Скотт Дж., Манас Д.М. Уайт (2013) Оценка и лечение связанного с химиотерапией поражения печени, хирургия печени. Профессор Хешам Абдельдаем (редактор) ISBN: 978-953-51-0965-5. ИНТЕК, DOI: 10,5772 / 53915
King PD, Perry MC (2001) Гепатотоксичность химиотерапии. Онколог 6: 162–176
CAS Статья PubMed Google Scholar
Робинсон П.Дж. (2009) Влияние химиотерапии на визуализацию печени.Eur Radiol 19: 1752–1762
Статья PubMed Google Scholar
Sharma A, Houshyar R, Bhosale P, Choi J, Gulati R, Lall C (2014) Вызванные химиотерапией аномалии печени: перспектива визуализации. Clin Mol Hepatol 20: 317–326
PubMed Central Статья PubMed Google Scholar
Hamer OW, Aguirre DA, Casola G, Lavine JE, Woenckhaus M, Sirlin CB (2006) Жировая печень: модели изображений и подводные камни.Радиография 26 (6): 1637–1653
Статья PubMed Google Scholar
Décarie PO, Lepanto L, Billiard JS, Olivié D, Lavallée JM, Kauffmann C et al (2011) Отложение жировой ткани в печени и сохранение: наглядный обзор. Insights Imaging 2 (5): 533–538
PubMed Central Статья PubMed Google Scholar
Torrisi JM, Schwartz LH, Gollub MJ, Ginsberg MS, Bosl GJ, Hricak H (2011) Результаты компьютерной томографии токсичности, вызванной химиотерапией.Радиология 258: 41–56
Статья PubMed Google Scholar
Maor Y, Malnick S (2013) Повреждение печени, вызванное противоопухолевой химиотерапией и лучевой терапией. Int J Hepatol 2013, ID статьи 815105. doi: 10.1155 / 2013/815105, 8 страниц
Статья Google Scholar
Kalil AN, Coral GP, Santos FA, Gonzalez MC, Neutzling CB (2014) Связь между предоперационной химиотерапией и распространенностью стеатоза печени при гепатэктомии по поводу метастатического колоректального рака.Arq Bras Cir Dig 27 (2): 120–125
Артикул PubMed Google Scholar
Mohty M, Malard F, Abecassis M, Aerts E, Alaskar AS, Aljurf M et al (2015) Синдром синусоидальной обструкции / веноокклюзионная болезнь: текущая ситуация и перспективы – заявление о позиции Европейского общества защиты прав человека Трансплантация костей и костного мозга (EBMT). Трансплантация костного мозга
Икезоэ Т., Тогитани К., Комацу Н., Исака М., Йокояма А. (2010) Успешное лечение синдрома синусоидальной обструкции после трансплантации гемопоэтических стволовых клеток рекомбинантным растворимым тромбомодулином человека.Трансплантация костного мозга 45: 783–785
CAS Статья PubMed Google Scholar
DeLeve LD, Shulman HM, McDonald GB (2002) Токсическое повреждение синусоидов печени: синдром синусоидальной обструкции (веноокклюзионная болезнь). Semin Liver Dis 22: 27–42
Статья PubMed Google Scholar
Seo AN, Kim H (2014) Синдром синусоидальной обструкции после химиотерапии на основе оксалиплатина.Clin Mol Hepatol 20: 81–84
PubMed Central Статья PubMed Google Scholar
Stoneham S, Lennard L, Coen P, Lilleyman J, Saha V (2003) Веноокклюзионная болезнь у пациентов, получающих тиопурины во время поддерживающей терапии острого лимфобластного лейкоза у детей. Br J Haematol 123: 100–102
Статья PubMed Google Scholar
Fan CQ, Crawford JM (2014) Синдром синусоидальной обструкции (печеночная веноокклюзионная болезнь).J Clin Exp Hepatol 4 (4): 332–346
PubMed Central Статья PubMed Google Scholar
Чжоу Х, Ван И, Лу Х, Сюй Х, Чжан М. (2014) Синдром обструкции синусоидальных синусоид печени, вызванный фитотерапией: особенности КТ и МРТ. Korean J Radiol 15 (2): 218–225
PubMed Central Статья PubMed Google Scholar
Сангисетти С.Л., Майнер Т.Дж. (2012) Злокачественный асцит: обзор прогностических факторов, патофизиологии и терапевтических мер.World J Gastrointest Surg 4 (4): 87–95
PubMed Central Статья PubMed Google Scholar
Jeong WK, Choi SY, Kim J (2013) Псевдоцирроз как осложнение после химиотерапии метастазов в печени от рака груди. Clin Mol Hepatol 19: 190–194
PubMed Central Статья PubMed Google Scholar
Lee SM, Chang ED, Na SJ, Kim JS, An HJ, Ko YH et al (2014) Псевдоцирроз метастазов рака груди в печень, леченный химиотерапией.Cancer Res Treat 46: 98–103
PubMed Central Статья PubMed Google Scholar
Qayyum A, Lee GK, Yeh BM, Allen JN, Venook AP, Coakley FV (2007) Частота аномалий контура печени и признаков портальной гипертензии на КТ у пациентов, получающих химиотерапию по поводу метастатического рака груди в печень. Clin Imaging 31: 6–10
Статья PubMed Google Scholar
Jha P, Poder L, Wang ZJ, Westphalen AC, Yeh BM, Coakley FV (2010) Радиологические модели цирроза. Am J Roentgenol 190: 993–999
Статья Google Scholar
Lee SL, Chang ED, Na SJ, Kim JS, An HJ, Ko YH et al (2014) Псевдоцирроз метастазов рака груди в печень, леченный химиотерапией. Cancer Res Treat 46 (1): 98–103
PubMed Central Статья PubMed Google Scholar
Лау Г.К. (2008) Реактивация гепатита В после химиотерапии: два десятилетия клинических исследований. Hepatol Int 2 (2): 152–162
PubMed Central Статья PubMed Google Scholar
Mahale P, Kontoyiannis DP, Chemaly RF, Jiang Y, Hwang JP, Davila M et al (2012) Острое обострение и реактивация хронической инфекции вируса гепатита C у онкологических больных. J Hepatol 57: 1177–1185
Статья PubMed Google Scholar
Abu-Judeh HH (2002) Печень «звездного неба» с правосторонней сердечной недостаточностью. AJR Am J Roentgenol 178: 78
Артикул PubMed Google Scholar
Park SJ, Kim JD, Seo YS, Park BJ, Kim MJ, Um SH et al (2013) Результаты компьютерной томографии для прогнозирования тяжелого острого гепатита с длительным холестазом. World J Gastroenterol 19 (16): 2543–2549
PubMed Central Статья PubMed Google Scholar
Morgan C, Tillett T, Braybrooke J, Ajithkumar T (2011) Управление необычными чрезвычайными ситуациями, вызванными химиотерапией. Ланцет Онкол 12: 806–814
Артикул PubMed Google Scholar
Singh V, Devata S, Cheng YC (2010) Карбоплатин и острый панкреатит, индуцированный доцетакселом: краткий отчет. Int J Clin Oncol 15 (6): 642–644
Статья PubMed Google Scholar
Viswanathan C, Truong MT, Sagebiel TL, Bronstein Y, Vikram R, Patnana M (2014) Абдоминальные и тазовые осложнения безоперационной онкологической терапии. RadioGraphics 34: 941–961
Статья PubMed Google Scholar
Motzer RJ, Rini BI, Bukowski RM, Curti BD, George DJ, Hudes GR et al (2006) Сунитиниб у пациентов с метастатической почечно-клеточной карциномой. JAMA 295 (21): 2516–2524
CAS Статья PubMed Google Scholar
Саадати Х., Саиф М.В. (2010) Острый панкреатит, вызванный сорафенибом. JOP 11 (3): 283–284
PubMed Google Scholar
Кобаяси Ю., Канемиту Т., Камото А., Сато М., Мори Н., Йошиока Т. и др. (2011) Безболезненный острый панкреатит, связанный с лечением сорафенибом: клинический случай. Med Oncol 28 (2): 463–465
Статья PubMed Google Scholar
Li M, Srinivas S (2007) Острый панкреатит, связанный с сорафенибом.South Med J 100 (9): 909–911
Статья PubMed Google Scholar
Ганешан Д.М., Салем У., Вишванатан С., Балачандран А., Гарг Н., Сильверман П. и др. (2013) Осложнения онкологической терапии в области живота и таза: обзор. Визуализация брюшной полости 38: 1–21
Статья PubMed Google Scholar
Calculli L, Pezzilli R, Casadi R, Fiscaletti M, Gavelli G (2005) Методы визуализации острого некротического панкреатита: мультидетекторная компьютерная томография.7: 104–109
Shyu JY, Sainani NI, Sahni VA, Chick JF, Chauhan NR, Conwell DL et al (2014) Некротический панкреатит: диагностика, визуализация и вмешательство. RadioGraphics 34: 1218–1239
Статья PubMed Google Scholar
Miller FH, Keppke AL, Dala K, Ly JN, Kamler VA, Sica GT (2004) МРТ панкреатита и его осложнений: часть 1, острый панкреатит. Am J Roentgenol 183 (6): 1637–1644
Статья Google Scholar
Xiao B, Zhang XM (2010) Магнитно-резонансная томография при остром панкреатите. World J Radiol 28 (8): 298–308
Статья Google Scholar
О’Коннор О.Дж., МакВиллиам С., Махер М.М. (2011) Визуализация острого панкреатита. Am J Roentgenol 197: 221–225
Статья Google Scholar
Ganten MK, Schuessler M, Bruckner T, Ganten TM, Koschny R (2015) Атрофия поджелудочной железы у пациентов с гепатоцеллюлярной карциномой, получающих длительное лечение сорафенибом.Онкология
Hescot S, Vignaux O, Goldwasser F (2013) Атрофия поджелудочной железы – новый поздний токсический эффект сорафениба. N Engl J Med 369: 1475–1476
CAS Статья PubMed Google Scholar
Stratton A, Murphy T, Laczek J (2012) Поджелудочная железа с атрофией на магнитно-резонансной холангиопанкреатографии как начальное проявление муковисцидоза. Hawaii J Med Public Health 71 (6): 151–154
PubMed Central PubMed Google Scholar
Djuric-Stefanovic A, Masulovic D, Kostic J, Randjic K, Saranovic D (2012) Объемная компьютерная томография нормальной поджелудочной железы: корреляция с диаметрами поджелудочной железы, измеряемыми с помощью поперечного сечения, и взаимосвязь с полом, возрастом и конституцией тела . Хирургическая радиология Анат 34: 811–817
CAS Статья PubMed Google Scholar
Сайед А.Б., Махал Р.С., Шумм Л.П., Дахман А.Х. (2012) Размер и объем поджелудочной железы на компьютерной томографии у здоровых взрослых.41 (4): 589–595
Cetin B, Coskun U, Yildiz R, Buyukberber S, Baykara M, Benekli M (2010) Острый холецистит у пациента с метастатической почечно-клеточной карциномой, получавшего эверолимус: случай отчет. J Oncol Pharm Pract 17 (3): 274–278
Статья PubMed Google Scholar
Gomez-Abuin G, Karam AA, Mezzadri NA, Bas CA (2009) Бескаменный холецистит у пациента с метастатической почечно-клеточной карциномой, получавшего сунитиниб.Clin Genitourin Cancer 7: 62–63
Статья PubMed Google Scholar
Tirumani SH, Krajewski KM, Shinagare AB, Jagannathan JP, Ramaiya NK (2014) Осложнения желчного пузыря, связанные с молекулярной таргетной терапией: клинические и визуальные особенности. Clin Imaging 38: 50–55
Статья PubMed Google Scholar
О’Коннор О.Дж., Махер М.М. (2011) Визуализация холецистита.Am J Roentgenol 196 (4): 367–374
Статья Google Scholar
Superfin D, Iannuci AA, Davies AM (2007) Онкологические препараты у пациентов с органной дисфункцией: резюме. Онколог 12: 1070–1083
CAS Статья PubMed Google Scholar
Хон Д., Мельник Дж., Стэгг Р., Альтман Д., Фридман М., Игноффо Р. и др. (1985) Билиарный склероз у пациентов, получающих инфузии флоксуридина в артериальную печень.J Clin Oncol 3 (1): 98–102
CAS PubMed Google Scholar
Ito K, Ito H, Kemeny NE, Gonen M, Allen PJ, Paty PB et al (2012) Билиарный склероз после химиотерапии с инфузионным насосом в печень для пациентов с метастазами колоректального рака в печень: частота, клинические особенности и факторы риска. Ann Surg Oncol 19: 1609–1617
Статья PubMed Google Scholar
Enns R (2008) Использование ERCP по сравнению с MRCP при первичном склерозирующем холангите. Гастроэнтерол Гепатол 4 (12): 852–854
Google Scholar
Rogoveanu I, Ghenoea DI, Saftoiu A, Ciurea T (2006) Роль методов визуализации в выявлении причин внепеченочного холестаза. Clin Imaging 15: 265–271
Google Scholar
Padda MS, Sanchez M, Akhtar AJ, Boyer JL (2011) Лекарственный холестаз.Гепатология 53: 1377–1387
PubMed Central CAS Статья PubMed Google Scholar
Agnello F, Salvaggio G, Cabibbo G, Maida M, Lagalla R, Midiri M. et al (2013) Визуализация обработанной гепатоцеллюлярной карциномы. World J Hepatol 5 (8): 417–424
PubMed Central Статья PubMed Google Scholar
Kim HC, Kim AY, Han JK, Chung JW, Lee JY, Park JH et al (2002) Спиральная компьютерная томография печеночной артерии и воротной вены у пациентов, получавших транскатетерную химиоэмболизацию артерий по поводу гепатоцеллюлярной карциномы: дополнительная ценность неулучшенные изображения.Радиология 225 (3): 773–780
Статья PubMed Google Scholar
Kloeckner R, Otto G, Biesterfeld S, Oberholzer K, Dueber C, Pitton MB (2010) Сравнение MDCT и МРТ-оценки опухолевого ответа после трансартериальной химиоэмболизации для лечения гепатоцеллюлярной карциномы. Cardiovasc Intervent Radiol 33 (3): 532–540
Статья PubMed Google Scholar
Yaghmai V, Besa C, Kim E, Gatlin JL, Siddiqui NA, Taouli B (2013) Визуализирующая оценка ответа гепатоцеллюлярной карциномы на локорегиональную и системную терапию. AJR Am J Roentgenol 201: 80–96
Артикул PubMed Google Scholar
Poggi G, Pozzi E, Riccardi A, Tonini S, Montagna B, Quaretti P et al (2010) Осложнения транскатетерной химиоэмболизации первичных и вторичных опухолей печени под визуальным контролем.Anticancer Res 30: 5159–5164
PubMed Google Scholar
Clark T (2006) Осложнения химиоэмболизации печени. Semin Interv Radiol 23: 119–125
Статья Google Scholar
Marelli L, Stigliano R, Triantos C, Senzolo M, Cholangitas E, Davies N. et al (2007) Трансартериальная терапия гепатоцеллюлярной карциномы: какой метод более эффективен? систематический обзор когортных и рандомизированных исследований.Cardiovasc Intervent Radiol 30 (1): 6–25
Статья PubMed Google Scholar
VanderWalde A (2009) Абсцесс печени как осложнение трансартериальной химиоэмболизации печени: описание случая, обзор литературы и клинические рекомендации. Gastrointest Cancer Res 3 (6): 247–251
PubMed Central PubMed Google Scholar
Woo S, Chung JW, Hur S, Joo SM, Kim HC, Jae HJ et al (2013) Абсцесс печени после трансартериальной химиоэмболизации у пациентов с билиоэнтерическим анастомозом: частота и факторы риска.AJR Am J Roentgenol 200 (6): 1370–1377
Статья PubMed Google Scholar
Wang CL, Guo XJ, Qui SB, Lei Y, Yuan ZD, Dong HB et al (2007) Диагностика бактериального абсцесса печени с помощью КТ. Гепатобилиарный панкреат Dis Int 6: 271–275
PubMed Google Scholar
Elsayes KM, Narra VR, Yin Y, Mukundan G, Lammle M, Brown JJ (2005) Очаговые поражения печени: диагностическая ценность подхода с использованием модели усиления с трехмерной градиентно-эхо-МРТ с контрастным усилением.Радиография 25 (5): 1299–1320
Статья PubMed Google Scholar
Huang YS, Chiang JH, Wu JC, Chang FY, Lee SD (2002) Риск печеночной недостаточности после транскатетерной артериальной химиоэмболизации при гепатоцеллюлярной карциноме: прогностическая ценность теста на моноэтилглицинксилидид. Am J Gastroenterol 97: 1223–1227
Статья PubMed Google Scholar
Larson AM (2010) Диагностика и лечение острой печеночной недостаточности. Curr Opin Gastroenterol 26 (3): 214–221
Статья PubMed Google Scholar
Romero M, Palmer SL, Kahn JA, Ihde L, Lin LM, Kosco A et al (2014) Внешний вид изображений при острой печеночной недостаточности: корреляция с клиническими и патологическими данными. Dig Dis Sci 59 (8): 1987–1995
Статья PubMed Google Scholar
Bae SI, Yeon JE, Lee JM, Kim JH, Lee HJ, Lee SJ et al (2012) Случай некротического панкреатита после транскатетерной артериальной химиоэмболизации у пациента с гепатоцеллюлярной карциномой. Clin Mol Hepatol 18 (3): 321–325
PubMed Central Статья PubMed Google Scholar
Озчинар Б., Гювен К., Поянли А., Озден I (2009) Некротический панкреатит после транскатетерной артериальной химиоэмболизации при гепатоцеллюлярной карциноме.Диагностика Интерв. Радиол. 15 (1): 36–38
PubMed Google Scholar
López-Benítez R, Radeleff BA, Barragán-Campos HM, Noeldge G, Grenacher L, Richter GM et al (2007) Острый панкреатит после эмболизации опухолей печени: частота и связанные факторы риска. Панкреатология 7: 53–62
Статья PubMed Google Scholar
Сакамото И., Иванага С., Нагаоки К., Мацуока Ю., Ашизава К., Утани М. и др. (2003) Формирование внутригептальной биломы (некроз желчных протоков) после транскатетерной химиоэмболизации артерий.Am J Roentgenol 181: 79–87
Статья Google Scholar
Miyayama S, Yamashiro M, Okuda M, Yoshie Y, Nakashima Y, Ikeno H et al (2010) Стриктура главного желчного протока, возникающая после транскатетерной химиоэмболизации артерии при гепатоцеллюлярной карциноме. Cardiovasc Intervent Radiol 33 (6): 1168–1179
Статья PubMed Google Scholar
Pelletier AL, Hammel P, Zappa M, Bedossa P, Rebours V, Hentic O et al (2008) Фатальный некроз желчных протоков: редкое осложнение транскатетерной химиоэмболизации артерий у пациента с эндокринными метастазами в печени.Case Rep Gastroenterol 2: 356–362
PubMed Central Статья PubMed Google Scholar
Yu JS, Kim KW, Park MS, Yoon SW (2001) Повреждения желчных протоков, приводящие к облитерации воротной вены после транскатетерной артериальной химиоэмболизации в печени: результаты компьютерной томографии и первоначальные наблюдения. Радиология 221: 429–436
CAS Статья PubMed Google Scholar
Thompson CM, Saad NE, Quazi RR, Darcy MD, Picus DD, Menias CO (2013) Управление ятрогенными повреждениями желчных протоков: роль интервенционного радиолога. RadioGraphics 33 (1): 117–134
Статья PubMed Google Scholar
Увеличенная печень у собак – Увеличенная печень у собак
Гепатомегалия у собак
Термин гепатомегалия используется для описания аномально увеличенной печени. Часто возникающий из-за определенных заболеваний и состояний, которые могут прямо или косвенно влиять на функционирование печени, орган печени может увеличиваться в размерах, принимая собственное болезненное состояние.
Симптомы и типы
Щенки обычно имеют большую печень по сравнению с взрослыми собаками. Однако чаще всего гепатомегалия диагностируется у пожилых собак. В зависимости от основной причины увеличение может охватывать всю печень или только ее часть. Например, инфекции и / или воспаление могут привести к генерализованному симметричному увеличению печени, тогда как опухоли, кровоизлияния, кисты или вращение доли печени могут привести к асимметричному или фокальному увеличению.То есть может быть увеличена только часть печени.
Симптомы могут различаться в зависимости от причины. Увеличение живота – наиболее часто встречающийся симптом. При осмотре ветеринар обнаружит увеличенную печень или пальпируемое образование в области живота. Образование обычно наблюдается за грудной клеткой и даже может быть видно невооруженным глазом. Однако у собак с ожирением трудно обнаружить увеличенную печень при физикальном обследовании.
Причины
- Дополнительное скопление крови около печени
- Гепатит (инфекция печени)
- Хроническая болезнь печени (цирроз)
- Нарушение кровотока, проходящего через печень
- Болезни и недостаточность сердца
- Новообразование печени
- Болезнь сердечного червя
- Вращение доли печени вокруг своей оси
- Диафрагмальная грыжа (грыжа, возникающая в результате протрузии части желудка через диафрагму)
- Аномальное отложение продуктов метаболизма в ткани печени
- Накопление жира в ткани печени
- Опухоль поджелудочной железы
- Абсцесс печени
- Киста печени
- Лекарственная токсичность
Вам необходимо подробно рассказать о здоровье вашей собаки, возникновении и характере симптомов, а также о возможных происшествиях, которые могли привести к этому состоянию.Ваш ветеринар проведет тщательный медицинский осмотр для оценки всех систем организма, и будет проведен полный профиль крови, включая химический профиль крови, общий анализ крови и анализ мочи. Результаты обычных лабораторных исследований сильно различаются в зависимости от основной причины увеличения печени. Общий анализ крови может выявить анемию, аномальные сферические эритроциты (сфероциты), нарушенные эритроциты (шистоциты), эритроциты с пятнами из-за накопления гемоглобина (тельца Хайнца), присутствие паразитов с эритроцитами, незрелые белые кровяные тельца. клетки (бластные клетки) в крови, красные кровяные тельца с ядром и аномально низкое или высокое количество тромбоцитов (крошечные клетки, используемые для свертывания крови).Биохимический профиль может показывать аномально высокие уровни ферментов печени и высокий уровень холестерина. Дальнейшее тестирование может включать профиль свертывания крови, поскольку нарушения свертываемости крови часто встречаются у пациентов с поражением печени. Ваша собака также может быть проверена на наличие сердечного червя.
Рентген брюшной полости может показать увеличенную печень с закругленными краями или смещение желудка и почек. Рентген грудной клетки может помочь определить метастазы опухоли в грудную полость, а также выявить заболевания сердца и легких.Ультразвуковое исследование брюшной полости может использоваться для просмотра дополнительных деталей брюшной полости, выявления изменений размера и контура поверхности печени, а также наличия сопутствующего заболевания. УЗИ брюшной полости также поможет отличить диффузные или локализованные типы увеличения печени. Более сложные диагностические тесты, такие как электрокардиография и эхокардиография, могут использоваться для оценки структуры и функций сердца.
Если опухоль обнаружена или подозревается, ваш ветеринар захочет взять образец ткани печени, чтобы подтвердить ее доброкачественную или злокачественную природу, но даже при отсутствии опухоли образец ткани может быть полезен для определения причины, степени тяжести и стадия заболевания печени.Образцы будут отправлены в лабораторию для микробных культур, и в случае инфекции культивирование образца поможет определить тип микроорганизма, который участвует, чтобы можно было прописать подходящие лекарства.
Лечение
Лечение сильно варьируется и будет зависеть от основной причины. В случае поражения сердца или прогрессирующего заболевания печени вашей собаке может потребоваться госпитализация для интенсивного лечения и поддерживающего ухода. Цель лечения – устранить провоцирующую причину и предотвратить дальнейшие осложнения.Больным собакам назначают антибиотики широкого спектра действия. У этих пациентов часто встречается обезвоживание, и для нормализации уровня жидкости требуется внутривенное введение жидкости. Мультивитамины также назначают для поддержания здорового уровня витаминов. В случае опухоли, абсцесса или кисты вашей собаке может потребоваться хирургическое вмешательство для удаления этих новообразований.
Жизнь и менеджмент
Пациентам с сердечной недостаточностью или избытком жидкости в брюшной полости требуется изменение режима питания и потребления жидкости.Эти пациенты нуждаются в особом уходе, и часто рекомендуется полный клеточный отдых. Для вашей собаки будут приняты особые диетические рекомендации, такие как добавление большого количества белков, ограничение соли и адекватные витаминные добавки.
Прогноз изменчивый и зависит от основной причины и продолжительности заболевания. Некоторые причины менее серьезны, а другие опасны для жизни. Поскольку печень является центральным органом метаболизма лекарств, вы не должны давать никаких лекарств или изменять дозировку любых прописанных лекарств без предварительной консультации с вашим ветеринаром.Чтобы предотвратить отрицательный энергетический баланс, вам нужно будет кормить собаку небольшими порциями и часто. Во время терапии вашу собаку нужно будет часто обследовать, при необходимости проводить лабораторные исследования и рентгенографию, чтобы следить за прогрессом вашей собаки.
Карцинома поджелудочной железы, печени и желчных путей
Рак поджелудочной железыРак поджелудочной железы является вторым по распространенности раком желудочно-кишечного тракта и четвертой по значимости причиной смерти от рака в Соединенных Штатах.Заболеваемость раком поджелудочной железы превышает только рак легких, толстой кишки, кожи, простаты и груди. По оценкам, в течение 1995 г. в США будет диагностировано 24 000 новых случаев рака поджелудочной железы [1]. Средняя выживаемость пациентов с этим заболеванием составляет от 3 до 4 месяцев, а 5-летняя выживаемость составляет всего 3% [2]. Одна из причин мрачного прогноза заключается в том, что начальные симптомы этого заболевания неспецифичны и, таким образом, болезнь обычно прогрессирует с явными или скрытыми метастазами, которые устанавливаются еще до того, как когда-либо будет поставлен диагноз.В настоящее время большая часть клинических усилий носит диагностический и паллиативный характер. Разработка успешных стратегий лечения будет основываться на развивающемся понимании молекулярных событий, вовлеченных в клеточную трансформацию, прогрессирование опухоли и регуляцию неопластического роста.
Эпидемиология и этиология
Заболеваемость раком поджелудочной железы увеличивается с возрастом. Риск увеличивается после 30 лет, причем большинство случаев возникает в возрасте от 65 до 79 лет. Тем не менее, болезнь также регистрировалась у более молодых людей, включая детей [1].
Соотношение мужчин и женщин зависит от возраста, от 2: 1 для пациентов моложе 40 лет до 1: 1 для пациентов старше 80 лет. Незначительное преобладание мужчин преобладает как у белых, так и у небелых. Рак поджелудочной железы чаще встречается у латиноамериканцев и афроамериканцев, чем у белых. Заболеваемость среди чернокожих составляет 14,9 на 100 000 по сравнению с 8,7 на 100 000 среди белых [2].
Также наблюдались различия в заболеваемости и смертности среди различных религиозных групп.Среди евреев Нью-Йорка и Израиля повышается заболеваемость раком поджелудочной железы, а среди мормонов ниже уровень смертности [3].
Была изучена заболеваемость в странах происхождения и среди иммигрантов в первом и втором поколении в США. Доля иммигрантов в первом поколении быстро увеличивается до уровня белых в США.
Причина карциномы поджелудочной железы остается неясной, но на нее влияют несколько факторов. Курение сигарет связано с повышенным риском рака поджелудочной железы [4,5].Исследование, проведенное в больницах Управления по делам ветеранов, показало, что у заядлых курильщиков (то есть, по крайней мере, две пачки сигарет в день) почти вдвое выше частота карциномы поджелудочной железы, чем у некурящих. Риск увеличивается по мере того, как увеличивается количество курящих сигарет, и избыточный риск снижается через 10–15 лет после прекращения курения [6].
Факторы питания также играют роль в развитии этого заболевания. В исследованиях на животных диетический жир увеличивает экспериментальное образование опухолей поджелудочной железы, вызванных азасерином [7].Хотя потребление кофе считалось сильным этиологическим фактором [8], более поздние исследования не подтвердили это наблюдение [9]. Алкоголь не был однозначно связан с раком поджелудочной железы [5].
Третий фактор, который, возможно, участвует в развитии карциномы поджелудочной железы, – это предшествующая резекция желудка [10] по поводу доброкачественных состояний, которая может увеличить риск развития рака поджелудочной железы в два-пять раз. Было высказано предположение, что ахлоргидная среда после гастрэктомии способствует колонизации бактерий, которые восстанавливают нитратсодержащие соединения до N -нитрозосоединений.Последние считаются канцерогенными [11]. Другим объяснением корреляции между гастрэктомией и раком поджелудочной железы является повышенный уровень холецистокинина в плазме (ХЦК), связанный с предшествующей резекцией желудка. CCK стимулирует рост нормальных клеток поджелудочной железы и, как полагают на животных моделях, опосредует стимул роста при канцерогенезе [12]. Подавление рака поджелудочной железы антагонистом CCK также наблюдалось в экспериментальных исследованиях [13].
Помимо курения, диеты и предшествующей гастрэктомии, некоторые болезненные состояния, включая хронический панкреатит и сахарный диабет, также были связаны с карциномой поджелудочной железы.Кальцификации, связанные с хроническим панкреатитом, были обнаружены у 3% пациентов с документированной карциномой поджелудочной железы [14]. Около 15% пациентов с карциномой поджелудочной железы являются диабетиками, и более чем в половине случаев клиническое проявление диабета предшествует диагнозу карциномы поджелудочной железы менее чем на 3 месяца [15].
Наконец, было обнаружено, что профессиональное воздействие растворителей, нефтяных соединений, бета-нафтиламина и бензидина связано с раком поджелудочной железы [16,17]. Нитрозамины признаны мощными канцерогенами поджелудочной железы у хомяков [11].Азасерин вызывает опухоли поджелудочной железы у крыс [18]. Действительно, воздействие этих промышленных химикатов в течение 10 и более лет может увеличить риск рака поджелудочной железы в пять раз [16].
Патология
Рак поджелудочной железы возникает как из экзокринной, так и из эндокринной паренхимы поджелудочной железы [19]. Примерно 95% случаев рака поджелудочной железы возникает в экзокринной части поджелудочной железы и может возникать из-за протокового эпителия, ацинарных клеток, соединительной ткани или лимфатических отложений.Наиболее распространенным раком поджелудочной железы является протоковая аденокарцинома, на которую приходится около 80% всех случаев рака поджелудочной железы [20]. Большинство карцином возникает в проксимальной части поджелудочной железы, которая включает голову, шею и крючковидный отросток. Только 20% карцином поджелудочной железы возникают в теле и только от 5% до 10% в хвосте [21].
Большинство пациентов с карциномой поджелудочной железы имеют запущенную стадию заболевания. На момент обращения 85% пациентов имеют клинически очевидные метастазы или микрометастазы.Обычная разбивка пациентов после определения стадии: заболевание, по-видимому, ограничено поджелудочной железой, 20%; местнораспространенное заболевание – 40%; и висцеральные метастазы – 40%. Наиболее частыми участками метастазов являются печень, брюшина, лимфатические узлы и легкие.
Клинические признаки
Начальные симптомы, которые включают анорексию, потерю веса, боль в животе и желтуху, обычно нечеткие и неспецифические. В результате две трети пациентов испытывают симптомы в течение как минимум 2 месяцев до постановки диагноза.Снижение веса, часто постепенное и прогрессирующее, является одним из самых ранних и наиболее часто недооцениваемых симптомов. Типичный пациент с карциномой поджелудочной железы потерял более 10% веса своего тела к моменту постановки диагноза. Боль в животе, наиболее частый симптом, присутствует у 70–80% пациентов. Боль возникает из-за местной инфильтрации опухолью забрюшинного пространства и чревного нервного сплетения. Сильная боль часто считается признаком того, что опухоль неоперабельна.
Желтуха, вторичная по отношению к обструкции желчевыводящих путей, может проявляться как ранний или поздний симптом, в зависимости от локализации опухоли.Возникают сопутствующие симптомы темной мочи и бледного стула. Обструкция выхода из желудка и двенадцатиперстная кишка могут возникать в 25% случаев рака головки поджелудочной железы и обычно являются вторичными по отношению к местной инвазии опухоли и проблемам с моторикой из-за инфильтрации внутренних нервов.
Другие случайные находки включают пальпируемый желчный пузырь при обращении (признак Курвуазье) [22], спленомегалию, депрессию и более высокую частоту венозного тромбоза и мигрирующего тромбофлебита (признак Труссо) [14].
Диагноз
Компьютерная томография (КТ), ультрасонография, эндоскопическая ретроградная холангиопанкреатография и тонкоигольная аспирационная биопсия успешно используются для диагностики рака поджелудочной железы. Однако КТ брюшной полости – самая полезная процедура для диагностики и определения стадии. Преимущества КТ-сканирования заключаются в том, что оно не зависит от оператора, оно не ограничивается желудочными или кишечными газами, а также демонстрирует метастазы в печени размером до 2 см, поражение перипанкреатических лимфатических узлов, периваскулярную инвазию и лимфаденопатию [23].Он также может выявить расширение протока поджелудочной железы и место обструкции в 88–97% случаев. Однако КТ имеет определенные ограничения, так как не все карциномы поджелудочной железы наблюдаются как опухоли, и не все образования являются карциномами поджелудочной железы. Тем не менее, обзор 100 случаев карциномы поджелудочной железы показал ложноотрицательный результат для КТ только 5% [24].
В отличие от КТ, ультразвуковое исследование не требует ионизирующего излучения. У пациентов с желтухой ультразвуковое исследование более точно, чем компьютерная томография, позволяет отличить обструктивную желтуху от необструктивной [25].Однако эффективность ультразвукового исследования снижается при ожирении и повышенном газообразовании в кишечнике [26,27].
Хотя эндоскопическая ретроградная холангиопанкреатография и тонкоигольная аспирационная биопсия являются инвазивными процедурами, они имеют определенные преимущества. Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ) имеет высокую чувствительность в диагностике карциномы поджелудочной железы (94%) [28]. Он может локализовать опухоль и обнаружить место обструкции протока. Кроме того, эндоскопическая ретроградная холангиопанкреатография позволяет аспирацию панкреатического секрета для цитологического исследования.Доступ к желчи также позволяет измерять другие производные от рака факторы, такие как онкоген K- ras . Как сообщалось в одной серии [29], частота ложноотрицательных результатов для ERCP составляет всего 3%. Хотя радиографическая диагностика рака поджелудочной железы обычно может быть сделана с использованием комбинации КТ, ультрасонографии и эндоскопической ретроградной холангиопанкреатографии, тонкоигольная аспирационная биопсия, чувствительность которой составляет 86% [30], может обеспечить гистологический диагноз.
Серологические маркеры
Поиск специфического опухолевого маркера рака поджелудочной железы, который мог бы помочь в скрининге и ранней диагностике, пока не увенчался успехом, хотя несколько серологических маркеров помогают в управлении заболеванием.Карциноэмбриональный антиген (CEA), высокомолекулярный гликопротеин, обычно обнаруживаемый в тканях плода, изучался наиболее широко. Он повышен (более 2,5 мг / мл) только у 40-50% пациентов с раком поджелудочной железы. Он может быть повышен при панкреатите, а также при многих других доброкачественных кишечных заболеваниях, а также при карциномах желчевыводящих путей, желудка, гепатоцеллюлярной и толстой кишки.
Другие серологические маркеры, связанные с карциномой поджелудочной железы, включают CA 19-9 и соотношение тестостерона и дигидротестостерона.CA 19-9 представляет собой муцинозный гликопротеин с периодом полураспада менее 1 дня, который связан с различными злокачественными новообразованиями (поджелудочной железы, гепатобилиарной, желудочной и толстой кишки). Было обнаружено, что чувствительность CA 19-9 к раку поджелудочной железы составляет от 67,6% до 92% (37 Ед / мл – это верхний предел нормы) [31]. В целом уровень CA 19-9 повышается с более поздней стадией заболевания; уровень СА 19-9 у пациентов с I или II стадией заболевания обычно находится в пределах нормы. Следовательно, чувствительность этого маркера при диагностике ранних резектабельных опухолей поджелудочной железы ниже [31,32].Когда 37 Ед / мл используется в качестве пороговой точки, уровень CA 19-9 также повышается у 4,3–28% пациентов с хроническим панкреатитом и у 21–35% пациентов с экстрапанкреатическим раком желудочно-кишечного тракта [31,32] . Повышение порогового уровня повышает специфичность CA 19-9 для карциномы поджелудочной железы.
Другой серологический маркер, который можно проанализировать, – это соотношение тестостерона и дигидротестостерона, которое, как было показано, составляет менее 5 у 67% мужчин с раком поджелудочной железы [33]. Это связано с повышенным уровнем 5-альфа-редуктазы, связанным с раком поджелудочной железы [34].По сравнению с CA 19-9 соотношение тестостерона и дигидротестостерона менее чувствительно, но более специфично для рака поджелудочной железы [33].
Два других антитела, DU-PAN-2 и SPAN-1, были проверены у пациентов с карциномой поджелудочной железы. Оба были выращены против клеточных линий рака поджелудочной железы человека. Специфичность этих новых маркеров у пациентов с раком поджелудочной железы сопоставима со специфичностью CA 19-9 [35,36]. Однако антитела обладают реактивностью против нескольких других типов рака, в основном новообразований желудочно-кишечного тракта, и против многих других доброкачественных состояний.
Следовательно, ни один отдельный маркер не является достаточно чувствительным или специфичным для использования в качестве скринингового теста, но объединение этих маркеров может помочь подтвердить диагноз карциномы поджелудочной железы.
Стадия
Стадия полезна при выборе лечения, оценке прогноза и сравнении результатов различных программ лечения. Наиболее часто используемой системой определения стадии рака поджелудочной железы является классификация опухолевых узлов и метастазов (TNM), разработанная в 1981 году Американским объединенным комитетом по стадированию рака и отчетности по конечным результатам (таблица 1).
| TX | Первичная опухоль не может быть оценена | |
| T0 | Нет признаков первичной опухоли | |
| T1 | Опухоль, ограниченная поджелудочной железой | Опухоль размером 2 см или менее в наибольшем измерении |
| T1b | Опухоль> 2 см в наибольшем измерении | ||||||
| T2 | Опухоль распространяется непосредственно на ткани двенадцатиперстной кишки или периферической кишки, желчного протока | ||||||
| T3 | Опухоль распространяется непосредственно на желудок, селезенку, толстую кишку или соседние крупные сосуды | ||||||
| NX | Невозможно оценить региональные лимфатические узлы | ||||||
| N0 | Нет регионарных лимфатических узлов 904 -11 | ||||||
| N1 | Метастазы в регионарные лимфатические узлы | ||||||
| Невозможно определить наличие отдаленных метастазов | |||||||
| M0 | Нет отдаленных метастазов | ||||||
| M1 | Отдаленные метастазы | ||||||
| Группировка стадий | N | T | T | ЯТ1 Т2 | N0 N0 | M0 M0 | |
| Стадия II | T3 | N0 | M0 | ||||
| Стадия III | Любая T | N1 | M0 | ||||
| Стадия IV 911 911 911 911 911 911 Любая | |||||||
В системе TNM статус первичной опухоли определяется распространением через капсулу поджелудочной железы; узловой статус определяется наличием поражения регионарных лимфатических узлов поджелудочной железы; статус метастатического заболевания определяется наличием дистального лимфатического узла, перитонеального или висцерального поражения.Резекции поддается только заболевание I стадии, локализованное в капсуле поджелудочной железы.
Лечение
Подход к лечению у пациентов с карциномой поджелудочной железы различается в зависимости от стадии заболевания на момент обращения.
Резектабельное заболевание: Как уже упоминалось, только пациенты с болезнью T1-2N0M0 считаются резектабельными, и хирургическое вмешательство является единственным потенциально излечивающим методом. В общем, лечебная операция возможна только у пациентов с раком головки поджелудочной железы, поскольку пациенты с раком хвоста поджелудочной железы или тела неизменно имеют запущенное заболевание.Даже среди тех пациентов, у которых заболевание поддается хирургическому лечению, 90% умирают от рецидива опухоли в течение 1-2 лет [19,37]. Средняя выживаемость после лечебной резекции составляет от 12 до 18 месяцев.
Место рецидива часто бывает локальным. В одном исследовании местный рецидив был единственным местом неудачи у 27% пациентов, перенесших резекцию, и был компонентом неудачи у 70% [38]. Резекция Уиппла или панкреатодуоденэктомия считается стандартной хирургической процедурой при раке головки поджелудочной железы [39].
Адъювантная лучевая терапия: Большинство пациентов, перенесших лечебную резекцию, впоследствии умирают от рецидива заболевания, что указывает на необходимость эффективной послеоперационной адъювантной терапии. В 1974 г. Группа изучения опухолей желудочно-кишечного тракта (GITSG) [40] оценила роль адъювантной лучевой терапии и химиотерапии после радикальной резекции. В общей сложности 43 пациента были рандомизированы либо в контрольную группу для наблюдения, либо в группу лечения, в которой 40 Гр облучения вводили разделенным курсом с внутривенным введением фторурацила в течение первых 3 дней каждого курса облучения и еженедельно, начиная с Через 1 месяц после завершения лучевой терапии и в дальнейшем в течение 2 лет.Выживаемость была больше в группе лечения, чем в группе наблюдения (21 месяц против 10,9 месяца). Из-за небольшого размера исследования впоследствии были зарегистрированы 30 дополнительных пациентов [41] с лучшим статусом выполнения, и результаты снова показали улучшение выживаемости пациентов в группе лечения. Хотя статистическая мощность в этих двух испытаниях слабая и подвергается критике, такой подход к лечению стал обычной практикой.
Адъювантная химиотерапия: В то время как комбинированная послеоперационная лучевая терапия и химиотерапия карциномы поджелудочной железы систематически оценивались, только адъювантная химиотерапия не проводилась.Однако, прежде чем могут быть разработаны эффективные стратегии адъювантной терапии, необходимо найти эффективную схему лечения распространенного рака поджелудочной железы. В настоящее время такой режим не известен.
Неоперабельное заболевание: Пациенты с неоперабельным заболеванием получают паллиативное лечение. Обструкция желчных путей при неоперабельном заболевании устраняется эндоскопической установкой стента. Чрескожного дренирования желчных путей лучше избегать у пациента, у которого не планируется дальнейшая терапия, поскольку это приводит к рецидивирующим инфекциям.Обструкция двенадцатиперстной кишки, которая встречается редко, может быть устранена с помощью шунтирования или недавно разработанных лапараскопических методов.
Химиотерапия: Как упоминалось ранее, результаты химиотерапии карциномы поджелудочной железы неутешительны. Это заболевание чувствительно лишь к нескольким возбудителям. В таблице 2 показаны те препараты, которые вызвали поддающийся измерению ответ, по крайней мере, у 10% пациентов в исследованиях фазы II.
| Препарат | Количество пациентов | Ответ (%) | ||||
| Фторурацил | 212 | 28 | ||||
| Стрептозоцин | 11 | |||||
| Стрептозоцин | 111 | Стрептозоцин | 20.8 | |||
| Ифосфамид | 54 | 22-60 | ||||
| Доксорубицин | 1,5 | 1,3 | ||||
Фтороурацил дает наилучший общий уровень ответа: 28% диапазон от 0% до 67%. Широкий диапазон, вероятно, связан с отбором пациентов, а не с различиями в расписании или критериях ответа. Однако количество пациентов в этих, в основном, неконтролируемых исследованиях невелико.
Другим агентом с низким уровнем активности против рака поджелудочной железы является митомицин (мутамицин), для которого частота ответа колеблется от 10% до 38% при средней частоте ответа 21% [43].Ответы на стрептозоцин (Заносар) и доксорубицин (Адриамицин, Рубекс) составили 11% [44] и 13% [43] соответственно. Однако ответы, наблюдаемые со всеми этими отдельными агентами, редко бывают полными, а продолжительность ответа обычно коротка. Сообщалось о полных ответах на ифосфамид (Ifex), хотя показатели сильно различались в двух исследованиях, о которых сообщалось до сих пор: в исследовании с участием 25 пациентов сообщалось о 60% (при 4% полных ответах) на ифосфамид [45], тогда как в другом испытании с участием 29 пациентов показатель ответа составил 22% (с 3.5% полных ответов) [46].
Поскольку фторурацил и митомицин являются наиболее эффективными отдельными агентами при карциноме поджелудочной железы, большинство схем комбинированной химиотерапии включают эти два агента. В одном из самых ранних исследований FAM (фторурацил, доксорубицин и митомицин) давал ответ на 37% [47]. Тридцать девять пациентов с распространенным раком поджелудочной железы получали фторурацил в дозе 600 мг / м² внутривенно (в / в) в дни 1, 8, 29 и 36; доксорубицин, 30 мг / м² внутривенно в дни 1 и 29; и митомицин, 10 мг / м² внутривенно в день 1.Цикл повторяли каждые 8 недель. Полных ответов не наблюдалось, а средняя выживаемость респондентов составила 12 месяцев. Однако последующее исследование, проведенное Северо-центральной группой лечения рака, сравнивающее только фторурацил с фторурацилом плюс доксорубицин и FAM, не смогло выявить преимущества в выживаемости для комбинированной химиотерапии по сравнению с монотерапией фторурацилом [48].
Другая химиотерапевтическая комбинация, SMF (фторурацил, митомицин и стрептозоцин), была первоначально сообщена Wiggans et al [49], чтобы дать ответ 43%.В этом исследовании 23 пациента с распространенным раком поджелудочной железы получали стрептозоцин в дозе 1 г / м² внутривенно в дни 1, 8, 29 и 36; митомицин, 10 мг / м² внутривенно в день 1; и фторурацил, 600 мг / м² внутривенно в дни 1, 8, 29 и 36. Цикл повторялся каждые 8 недель. Однако в последующем исследовании GITSG [50], в котором сравнивалась эффективность FAM и SMF, не удалось воспроизвести эти многообещающие первоначальные результаты. Ответы на две схемы составили 13% и 15% соответственно.
Другие попытки улучшить результаты химиотерапии были сосредоточены на изменении режима дозирования.Как правило, препарат, схема лечения которого изменена, представляет собой фторурацил, который можно вводить либо болюсно, либо в виде непрерывной инфузии. Исходя из того, что фторурацил является лекарством, специфичным для клеточного цикла, с коротким периодом полувыведения, он должен быть более эффективным, если его вводить в виде инфузии. Тем не менее, частота ответа в испытаниях, в которых этот препарат вводили путем непрерывной инфузии, варьировала от 0% до 39%. Исследования были ограничены небольшим размером выборки [51].
Модуляции фторурацила лейковорином (фолиевой кислотой) [52,53] и N -фосфонацетил-L-аспартатом (PALA) [54] также были опробованы при лечении рака поджелудочной железы.Лейковорин увеличивает внутриклеточную концентрацию 5,10-метилтетрагидрофолиевой кислоты, что приводит к длительному ингибированию тимидилатсинтетазы метаболитом фторурацила FdUMP. Однако результаты применения высоких доз лейковорина и фторурацила у пациентов с запущенной карциномой поджелудочной железы были плохими [52,53].
PALA ингибирует фермент аспартат-транскарбамилазу, что приводит к снижению пула уридинтрифосфата и цитозинтрифосфата, что может повысить терапевтический индекс фторурацила.Однако исследование Юго-западной онкологической группы (SWOG) показало, что при кратковременной инфузии PALA с высокими дозами фторурацила частота ответа составила всего 5% [55].
Лишь в нескольких исследованиях использовалась внутриартериальная химиотерапия. В тех, кто это сделал, результаты были неутешительными и не показали увеличения выживаемости [56,57].
Наконец, количество новых соединений продолжает расти. Гемцитабин (2,2´-дифтордезоксицитидин) представляет собой новый пиримидиновый антиметаболит, который продемонстрировал доклиническую противоопухолевую активность на моделях солидных опухолей мышей и ответы у пациентов с раком поджелудочной железы во время оценки фазы I.Испытание фазы II, проведенное Casper et al., Проводилось у пациентов, ранее не подвергавшихся химиотерапии, с аденокарциномой поджелудочной железы [57a]. Гемцитабин, 800 мг / м², вводили внутривенно еженедельно в течение 3 недель подряд каждые 28 дней. Наблюдалась частота ответов 11% (все частичные ответы). Несмотря на эти предельные показатели ответа, часто наблюдались интересные улучшения в отношении боли и работоспособности. На основании этих наблюдений было проведено рандомизированное испытание гемцитабина по сравнению с фторурацилом, которое продемонстрировало значительное улучшение контроля симптомов и выживаемости при применении гемцитабина [57b].Таким образом, гемцитабин следует рассматривать в качестве первой линии лечения симптоматических пациентов с прогрессирующей аденокарциномой поджелудочной железы.
Гормональная терапия: Гормональная терапия также имеет потенциал в качестве паллиативного лечения карциномы поджелудочной железы. Результаты экспериментальных моделей показали, что рак поджелудочной железы является гормонозависимой опухолью [58,59]. Theve et al [60] лечили тамоксифеном 14 пациентов с запущенной карциномой поджелудочной железы и сообщили, что средняя выживаемость увеличилась до 8.5 месяцев (3 пациента выжили 22 месяца). Однако в другом исследовании тамоксифена Миллер и Бенц [61] не достигли таких многообещающих результатов.
Сообщения о том, что соматостатин (октреотид) подавляет рост карциномы поджелудочной железы у животных [62], предполагают, что он может иметь потенциальное применение при лечении рака поджелудочной железы. ХЦК и секретин стимулируют рост экзокринной поджелудочной железы у животных. Хотя роль этих гормонов в онкогенезе человека неизвестна, CCK может стимулировать рост клеточной линии аденокарциномы поджелудочной железы человека [63].Среди действий соматостатина и его аналогов – подавление секреции или действия желудочно-кишечных гормонов, в том числе CCK. В двух клеточных линиях аденокарциномы поджелудочной железы человека наблюдалось ингибирование роста соматостатина. Прямые ингибиторы CCK также были недавно оценены, но не было зарегистрировано никакого влияния на прогрессирование заболевания или качество жизни [64].
Лучевая терапия: Паллиативная лучевая терапия используется для купирования боли у пациентов с карциномой поджелудочной железы.Сама по себе лучевая терапия не улучшает выживаемость, но в сочетании с фторурацилом улучшает [65]. В исследовании GITSG, в котором сравнивали только 6000 сГр с фторурацилом плюс 4000 или 6000 сГр у пациентов с местно неоперабельным раком поджелудочной железы, медиана выживаемости была больше в обеих группах химиолучевой терапии, чем в группе только лучевой терапии (10 против 5,5 месяцев).
Другие исследовательские методы лучевой терапии использовались в попытках улучшить лечение рака поджелудочной железы, но с неоднозначными результатами.Сообщается, что одна из них, интраоперационная лучевая терапия, позволяет доставить более высокую дозу излучения к месту заболевания без повреждения соседних тканей [66]. В исследовании, проведенном в клинике Mayo Clinic [67], 159 пациентам случайным образом были назначены либо интраоперационная лучевая терапия с добавлением внешнего лучевого излучения, либо только внешнее лучевое облучение. Хотя местный контроль был лучше в группе интраоперационной лучевой терапии, этот улучшенный местный контроль не привел к увеличению выживаемости.Наконец, другие попытки улучшить выживаемость при раке поджелудочной железы, такие как чрескожная имплантация семян йода-125 под ультразвуковым контролем, не дали значительных результатов.
Биологическая терапия: Значительный интерес вызывает использование моноклональных антител для лечения пациентов с раком поджелудочной железы. Считается, что моноклональные антитела убивают опухолевую мишень либо косвенно, путем взаимодействия с клетками, которые влияют на антителозависимую клеточно-опосредованную цитотоксичность (ADCC) и активность естественных клеток-киллеров, либо непосредственно путем комплемент-зависимого цитолиза [68,69].Два моноклональных антитела, MoAb 494/32 и MoAb CO 17-1A, проявляют сильную реактивность против рака поджелудочной железы.
MoAb 494/32 представляет собой мышиное антитело изотипа иммуноглобулина (Ig) G1, которое прочно связывается с клетками рака поджелудочной железы человека и опосредует ADCC. Частичный ответ наблюдался у пациента с раком поджелудочной железы во время фазы I-II оценки этого антитела. В проспективном рандомизированном исследовании с участием пациентов, перенесших резекцию поджелудочной железы, средняя выживаемость 29 пациентов, получивших послеоперационный MoAb 494/32, составила 14.2 месяца, что незначительно отличается от 12,9-месячной медианы выживаемости 32 контрольных пациентов [70].
Другим важным моноклональным антителом является MoAb 17-1A, мышиный IgG2a, нацеленный на гликопротеин массой 37 кДа на поверхности различных аденокарцином желудочно-кишечного тракта человека [71]. Он не опосредует комплемент-зависимый лизис опухолевых клеток, но участвует в ADCC. В предварительных клинических исследованиях MoAb 17-1A некоторые ответы наблюдались у пациентов с карциномой поджелудочной железы [69].Другой возможностью терапевтического вмешательства может быть использование антител против рецептора эпидермального фактора роста. Было обнаружено, что клетки рака поджелудочной железы сверхэкспрессируют рецептор эпидермального фактора роста [72]. Этот рецептор представляет собой трансмембранный гликопротеин, экспрессируемый множеством нормальных и злокачественных клеток.
Будущие цели: По мере того, как молекулярные биологи и биохимики будут лучше понимать рак поджелудочной железы, появятся новые цели для терапии. Одной из таких мишеней является онкоген K- ras .Было обнаружено, что по крайней мере 80% аденокарцином поджелудочной железы содержат мутантный ген K- ras [73]. Этот онкоген играет важную роль в развитии и прогрессировании рака поджелудочной железы и является мишенью для новых терапевтических подходов.
Обезболивание: Боль – это симптом, который испытывают практически все пациенты с карциномой поджелудочной железы на определенном этапе их заболевания. Часто именно это побуждает пациента обращаться за медицинской помощью. Боль может возникать, когда опухоль проникает в забрюшинное пространство или внутреннее нервное сплетение.Как правило, оно бывает сильным и жгучим, а при сдавлении нерва может сопровождаться дизестезией и гиперестезией в области иннервации. Противосудорожные препараты и трициклические антидепрессанты полезны при лечении этого типа боли [74,75]. Кроме того, стероиды могут уменьшить отек, связанный с раком поджелудочной железы, и уменьшить компрессию и боль.
Боль также может быть вызвана непроходимостью желудка или тонкой кишки или расширением желчных протоков, что приводит к сильному мышечному спазму. Это, в свою очередь, приводит к ишемии с разрушением клеток и высвобождением болеутоляющих веществ.Этот тип боли диффузный, плохо локализованный и относится к дерматомам, которые имеют ту же иннервацию, что и пораженные внутренние органы.
Лечение такой боли включает обильное употребление наркотиков, которые можно вводить двумя способами. Пероральный путь предпочтительнее, так как он безболезненный и удобный. Использование наркотиков длительного действия, таких как морфин с контролируемым высвобождением, обычно позволяет лучше контролировать боль. Как правило, требуемая доза титруется препаратом морфина короткого действия каждые 4 часа.Если пероральное введение не купирует боль, можно использовать парентеральное введение. В этих обстоятельствах лекарство предпочтительно вводить через насос для непрерывной инфузии, поскольку насос можно запрограммировать на введение лекарственного средства с фоновой скоростью инфузии и дать возможность пациенту вводить повышенную дозу по требованию.
У пациентов с непреодолимой болью под рентгеноскопическим контролем могут проводиться более радикальные процедуры, такие как блокада чревной оси. Чревное сплетение – это плотная сеть нервов между двумя большими ганглиями, образованная внутренними нервами.Внутренние нервы и симпатические стволы являются единственными медиаторами боли, исходящей от поджелудочной железы и внепеченочных желчных протоков. Следовательно, блокируя чревную ось, можно блокировать боль. Обезболивание с помощью этой процедуры превышает 90% в большинстве описанных исследований [76–78].
Радиотерапия также использовалась для купирования боли [65]. Обычно вводимое с радиосенсибилизатором, излучение сокращает опухоль и снимает сдавление нервов. Недостаток лучевой терапии – отсроченное облегчение.Тем не менее, этот метод достаточно эффективен при хорошей координации.
Гепатоцеллюлярная карциномаГепатоцеллюлярная карцинома (ГЦК) – одно из наиболее распространенных злокачественных новообразований; ежегодно от него умирает около 1 250 000 человек во всем мире. Распространение HCC демонстрирует поразительные географические различия. Страны и группы населения сгруппированы в соответствии с уровнем заболеваемости, т. Е. Высокий (20 или более на 100 000 мужчин в год) в Китае, Юго-Восточной Азии, Западной и Южной Африке и среди китайского населения в Сингапуре, Тайване и Гонконге; средний уровень (от 6 до 19 на 100 000 мужчин в год) в Японии, Болгарии, Польше, Франции, Венгрии, Югославии, Чехословакии, Бельгии и Австрии, а также среди новозеландских маори, гавайцев и китайцев, проживающих в Соединенных Штатах; и низкий (менее 5 случаев на 100 000 мужчин в год) в Великобритании, США, Канаде, Австралии, Израиле, Скандинавии, Латинской Америке, Индии и Новой Зеландии [79].
Во всем мире ГЦК встречается у мужчин примерно в три раза чаще, чем у женщин. Заболеваемость увеличивается с возрастом независимо от риска, пока не стабилизируется у пожилых людей. В регионах с высокой заболеваемостью наблюдается заметный сдвиг в сторону увеличения заболеваемости в более молодой возрастной группе.
Факторы риска
ГЦК почти всегда ассоциируется с хроническим заболеванием печени, главным образом с гепатитом В и гепатитом С. Существует положительная корреляция между географической структурой поверхностного антигена гепатита В (HBsAG) и заболеваемостью ГЦК.Молекулярно-биологические исследования показали, что ДНК вируса гепатита В интегрирована в печень пациентов с хроническим гепатитом и гепатоцеллюлярной карциномой [80].
Афлатоксин, микотоксин, вызываемый грибами Aspergillus , по-видимому, является важным коканцерогеном для сельских жителей Африки. Сообщалось, что пища, загрязненная афлатоксином, вызывает опухоли печени у форели, крыс и макак-резусов, получавших афлатоксин B1 в течение длительного периода времени [81].
На Западе ГЦК обычно возникает при циррозе печени.От восьмидесяти до 90% случаев связаны с циррозом, вызванным этанолом. Другие факторы риска включают гемохроматоз и паразитарные инфекции печени.
Патология
ГЦК проявляется в двух макроскопических формах: диффузной и узловатой. Диффузная форма может развиться из одноцентрового поражения [82].
Из всех гистологических паттернов ГЦК только фиброламеллярный вариант важен для лечения и клинического поведения. Этот вариант чаще встречается у женщин, возникает в более раннем возрасте, не связан с циррозом печени и, как правило, протекает одиночно и, таким образом, более поддается хирургической резекции.Эти фиброламеллярные карциномы, гистологически характеризующиеся эозинофильными клетками многоугольной формы, разделенными пластинчатым фиброзом, имеют лучший прогноз, чем другие гистологические типы ГЦК [82].
Инвазия воротной вены была обнаружена в 14% удаленных образцов ГЦК, когда поражение было меньше 2,0 см, и в 71% образцов, когда поражение было больше 5,1 см. Эти тромбы могут поражать печеночную вену, полую вену и воротную вену [83].
Клинические особенности
Наиболее частыми симптомами у пациентов с ГЦК являются боль в животе (91%), асцит (43%), потеря веса (35%), слабость (31%), полнота и анорексия (27%) , рвота (8%) и желтуха (7%).Примерно у трети пациентов симптомы отсутствуют. Метастатическое заболевание может проявляться в виде злокачественного асцита, боли в скелете, одышки с поражением легких и неврологических нарушений, вызванных метастазами в головной мозг [84].
Асцит может возникать как следствие основного хронического заболевания печени или может быть следствием быстро разрастающейся опухоли. Другие менее распространенные симптомы включают лихорадку неизвестного происхождения, внутрибрюшное кровотечение, кровотечение из верхних отделов желудочно-кишечного тракта, боль в костях, кому, вторичную по отношению к печеночной недостаточности, гиперкальциемию и респираторные симптомы.Желтуха возникает нечасто и обычно является вторичной по отношению к основному заболеванию печени.
Среди физических признаков, присутствующих у пациентов с ГЦК, гепатомегалия является наиболее частой и встречается у 50–90% пациентов. Признаки цирроза печени, такие как ангиома паука и гинекомастия, встречаются часто. Брюшные ушибы могут возникать из-за ГЦК, предположительно вторичного по отношению к увеличению кровоснабжения. Асцит может возникать как часть основного заболевания печени, вызванного гемоперитонеумом, или как злокачественный асцит.Спленомегалия может возникать в результате связанной с портальной гипертензией основного заболевания печени. Также часто наблюдаются потеря веса и лихорадка, особенно при быстрорастущих или крупных опухолях. Также сообщалось о синдроме Бадда-Киари, узлах Вирхова или Трозье и кожных метастазах.
Сообщалось о ряде паранеопластических синдромов, связанных с ГЦК. К наиболее важным из них относятся гипогликемия (также вызванная конечной стадией печеночной недостаточности), эритроцитоз, гиперкальциемия, гиперхолестеринемия, дисфибриногенемия, карциноидный синдром, повышение уровня тироксин-связывающего глобулина, половые изменения и поздняя кожная порфирия.
Изменения лабораторных показателей при ГЦК очень похожи на изменения при циррозе; они включают повышенные уровни щелочной фосфатазы, трансаминаз и билирубина. Эти изменения обычно присутствуют примерно у 50% пациентов и предсказывают короткую выживаемость [85].
Альфа-фетопротеин (AFP) и альфа-1-глобулин являются опухолевыми маркерами, обычно связанными с HCC [86]. У человека они обычно обнаруживаются в эмбрионе через 6 недель после оплодотворения и исчезают через несколько недель после рождения.Хотя уровни АФП также повышены в опухолях половых клеток и во время беременности, иммуноферментный анализ по-прежнему обнаруживает от 70% до 90% всех ГЦК. Отчеты связывают нормальный уровень AFP с улучшением выживаемости. Уровни АФП после резекции используются для мониторинга клинического прогресса.
Диагноз
Гепатоцеллюлярные карциномы лучше всего визуализируются на компьютерной томографии. КТ может выявить первичные поражения размером более 1 см, а также может выявить компрессию или инвазию воротных или печеночных вен и внепеченочное метастатическое заболевание, особенно в печеночно-двенадцатиперстную связку и легкие [87].
Ультрасонография недорога и неинвазивна, но гиперэхогенный вид ГЦК может привести к ошибкам с доброкачественными, а также с метастатическими опухолями. ГЦК может проявляться как очаговая форма, которая проявляется на УЗИ как округлое или дольчатое образование, часто множественное, с эхосигналами высокого и низкого уровня. Ультразвук может показать как печеночные, так и воротные вены, а иногда и внутрисосудистую опухоль. ГЦК может также проявляться в виде диффузной формы с изменениями, которые могут быть тонкими и неотличимыми от диффузных изменений, наблюдаемых при циррозе и хроническом активном гепатите.
Еще не было продемонстрировано, что магнитно-резонансная томография более полезна, чем компьютерная томография печени. Наиболее чувствительными тестами являются компьютерная томография и компьютерная томография с липоидолом. Они считаются обязательными, если предполагается резекция, поскольку они обнаруживают небольшие поражения в очевидно нормальной остаточной доле и, как сообщается, способны диагностировать на 50% больше поражений, чем можно диагностировать только с помощью компьютерной томографии.
Лапароскопия более инвазивна, но она обеспечивает прямую визуализацию печени, брюшной полости и внутренних органов и позволяет проводить чрескожную биопсию иглой под прямым наблюдением.Это может привести к более точной постановке и предотвращению ненужных лапаротомий.
Методы чрескожной биопсии включают тонкоигольную аспирационную цитологию и биопсию стержневой иглой. Игольчатая биопсия может выполняться под контролем ультразвука или компьютерной томографии, вслепую или, как уже упоминалось, под прямым зрением с помощью лапароскопа.
Стадирование
Система стадирования опухолей печени была разработана Международным союзом борьбы с раком (UICC) и по существу соответствует системе TNM (таблица 3).
| TX | Первичная опухоль не может быть оценена | |
| T0 | Нет признаков первичной опухоли | |
| T1 | Единственная опухоль 2 см или меньше в наибольшем измерении без сосудистой инвазии | Одиночная опухоль 2 см или меньше в наибольшем измерении с сосудистой инвазией; или Множественные опухоли, ограниченные одной долей, ни одна из них не превышает 2 см в наибольшем измерении, без сосудистой инвазии; или Одиночная опухоль> 2 см в наибольшем измерении без сосудистой инвазии |
| T3 | Одиночная опухоль> 2 см в наибольшем измерении с сосудистой инвазией; или Множественные опухоли, ограниченные одной долей, ни одна из них не превышает 2 см в наибольшем измерении, с сосудистой инвазией; или Множественные опухоли, ограниченные одной долей, любые> 2 см в наибольшем измерении, с сосудистой инвазией или без нее | |
| T4 | Множественные опухоли более чем в одной доле или опухоль (ы), затрагивающая главную ветвь воротной или печеночной вены (s) | |
| NX | Невозможно оценить регионарные лимфатические узлы |
| N0 | Нет метастазов в регионарные лимфатические узлы |
| N1 |
| MX | Невозможно оценить наличие отдаленных метастазов | ||
| M0 | Нет отдаленных метастазов | ||
| M1 | Дистанционные метастазы | ||
| Стадия I | T1 | N0 | M0 |
| Стадия II | T2 | N0 | M0 |
| Стадия III | T1 Т2 Т3 Т3 | N1 N1 N0 N1 | M0 M0 M0 M0 |
| Стадия IVA | T4 | Любая N | M0 |
| Стадия IVB | Любая T | Любая N | M1 |
сосудистая инвазия имеет лучший прогноз.Множественные опухоли, сосудистая инвазия, микроскопическая или макроскопическая, а также распространение лимфатических узлов считаются неблагоприятными прогностическими факторами.
Лечение
Операция: Операция – единственный метод лечения ГЦК, но его использование зависит в основном от размера и расположения опухоли, а также от состояния не пораженной печени. Небольшие инкапсулированные ГЦК можно вылечить с помощью резекции в 50% случаев, но эти опухоли встречаются редко. Пациентам с опухолями I или II клинической стадии следует рассмотреть возможность резекции.
Как уже упоминалось, еще одним ограничивающим фактором для многих пациентов с ГЦК является доступный печеночный резерв. Диффузный ГЦК и запущенный цирроз обычно считаются неоперабельными. Цель у пациентов с циррозом – сохранить как можно больше функционирующей ткани печени, чтобы избежать послеоперационной печеночной недостаточности [88]. Субсегментарные или сегментарные резекции предпочтительны у пациентов с небольшими поражениями и циррозом печени. Интраоперационное ультразвуковое исследование печени может помочь обнаружить сателлитные или метастатические опухоли и обеспечить точную локализацию и перевязку сегментарных воротных и печеночных вен во время минимальных резекций.
Операционная смертность увеличивается с увеличением степени резекции и снижением степени функции оставшейся ткани печени и, как сообщается, составляет от 5% до 33% [89]. Тип и степень опухоли, а также наличие цирроза или гепатита будут определять долгосрочную выживаемость. Сообщается, что однолетняя выживаемость составляет около 80%, а пятилетняя выживаемость колеблется от 30% до 46%.
Адъювантная химиотерапия или лучевая терапия после радикальной резекции не играют никакой роли.
Криохирургия: Криохирургия включает разрушение опухоли in situ с помощью отрицательных температур. При использовании жидкого азота можно достичь температуры ниже –20 ° C. Эта процедура приведет к гибели как опухоли, так и неопухолевой ткани либо сразу, либо в период оттаивания. Для увеличения процента разрушенных опухолевых тканей используются многократные циклы замораживания-оттаивания.
Теоретически криохирургия должна быть идеальным методом лечения пациентов с циррозом, у которых недостаточный резерв печени и мультифокальная опухоль.Напротив, осложнения, связанные с этой процедурой, и очень низкая выживаемость, описанная в литературе, показали, что криохирургия не дает явных улучшений по сравнению со стандартной операцией и что ее использование должно быть ограничено исследовательскими условиями [90].
Химиотерапия: Большинство пациентов с ГЦК не являются кандидатами на лечебную операцию, поэтому химиотерапия – их единственный вариант. К сожалению, в настоящее время не существует очень эффективной химиотерапии ГЦК [91]. Доксорубицин, который до сих пор считается стандартом для монотерапии ГЦК, дает лишь 20% ответов.Ни один другой отдельный агент еще не продемонстрировал более высокую скорость. Было обнаружено, что комбинированная химиотерапия увеличивает токсичность без улучшения выживаемости. Интерферон альфа-2а (роферон-А) также использовался при ГЦК без влияния на выживаемость пациентов [92,93].
Другим подходом к лечению ГЦК является внутриартериальная инфузия печени, при которой химиотерапевтические препараты в высоких концентрациях доставляются непосредственно в печень. Внутриартериальное введение в печень таких агентов, как флоксуридин (FUDR), митомицин и интерферон, показало, что частота ответа достигает 50% [94,95].К сожалению, такие ответы обычно недолговечны. Другой недостаток этого метода заключается в том, что для этого лечения требуется либо длительная чрескожная катетеризация печеночной артерии, либо лапаротомия для установки инфузионного устройства, что обычно является дорогостоящим и подвержено осложнениям. Внутриартериальная инфузия печени в настоящее время не рекомендуется в качестве стандартной практики.
Химиоэмболизация, введение химиотерапии одновременно с чрескожной эмболизацией печеночной артерии, является еще одним подходом к лечению ГЦК.Основное кровоснабжение ГЦК происходит из печеночной артерии, тогда как нормальная паренхима печени снабжается в основном воротной веной. Таким образом, окклюзия печеночной артерии может вызвать относительно избирательную ишемию опухоли.
Желатиновая губка является наиболее широко используемым вазоокклюзионным материалом, хотя были опробованы и другие вещества, такие как крахмал, поливиниловый спирт, коллаген, химиотерапевтические микросферы и аутологичный сгусток крови. Разные размеры этих частиц позволяют прогнозировать различный уровень артериальной блокады, а их разная степень разлагаемости позволяет прогнозировать различия в продолжительности блокады.Оптимальный материал еще предстоит определить.
Химиоэмболизация при ГЦК вызывает частичный ответ примерно у 50% пациентов. Тем не менее, ни одно окончательное исследование не продемонстрировало превосходства химиоэмболизации над внутриартериальной инфузией печени, другими паллиативными методами лечения или современной поддерживающей терапией при ГЦК.
Лучевая терапия: Дистанционная лучевая терапия играет определенную роль в паллиативном лечении ГЦК, но эта роль ограничивается общей переносимостью дозы лучевой терапии на органы.Лучевой гепатит с последующим фиброзом – одно из возможных осложнений, наблюдаемых при введении доз от 3 до 30 Гр. Отверстия для конформной лучевой терапии могут использоваться для минимизации рассеяния луча и обеспечения доставки терапевтических доз радиации к одиночным поражениям.
Используется новый метод – радиационно-меченные антитела к ферритину. Ферритин не только находится в нормальных тканях, но также синтезируется и секретируется ГЦК. Использование поликлональных антиферритиновых антител йода-131 [96] привело к 48% ремиссии в исследованиях фазы I и II.Он также снизил стадию небольшого процента неоперабельных видов рака до операбельных. При сравнении схемы химиотерапии с использованием радиоактивно меченых антител с одной химиотерапией не было обнаружено преимущества в выживаемости при комбинированной терапии [97]. Были предприняты попытки заменить изотоп йода бета-излучающим изотопом антиферритина иттрия-90, но было обнаружено, что антиферритиновая составляющая больше не является селективной для ГЦК. Текущее исследование сосредоточено на использовании человеческих моноклональных антиферритиновых антител.
Трансплантация печени: Трансплантация печени использовалась в качестве альтернативы резекции у пациентов с далеко зашедшим двударным ГЦК или ГЦК на поздней стадии цирроза [98]. Однако результаты этой стратегии неутешительны: 3-летняя выживаемость составляет менее 50%, а долгосрочная выживаемость составляет около 20% [99].
Карцинома желчного пузыряКарцинома желчного пузыря была впервые описана Максимилианом де Штолем в 1777 году [100].Сейчас это четвертая по распространенности опухоль желудочно-кишечного тракта. Вместе с раком печени рак желчного пузыря станет причиной примерно 18 500 новых случаев рака и 14 200 смертей в США в 1995 году [1]. Карцинома желчного пузыря – агрессивное заболевание, и прогноз для пациентов мрачный, с общей 5-летней выживаемостью менее 5% и средней выживаемостью 6 месяцев [101, 102].
Эпидемиология и этиология
Рак желчного пузыря – заболевание пожилых людей.Пик заболеваемости приходится на седьмое десятилетие, когда страдают в три раза больше женщин, чем мужчин. Нет разницы в возрасте дебюта у мужчин и женщин [103]. Заболеваемость выше у белых женщин, чем у чернокожих, и в 10 раз выше у мексиканцев, американских индейцев и коренных жителей Аляски, что свидетельствует о генетической основе восприимчивости [4,104].
Преобладание этого заболевания у женщин предполагает связь между доброкачественными и злокачественными заболеваниями желчного пузыря. Силк и др. [102] проанализировали свой 22-летний опыт лечения карциномы желчного пузыря в Институте рака Розуэлл-Парк и обнаружили, что холелитиаз присутствовал у 48 (68%) из 69 пациентов.Кальцинированный (фарфоровый) желчный пузырь был обнаружен у семи пациентов (10%). Другое исследование Paraskevopoulos et al [105] обнаружило камни в желчном пузыре у 18 (86%) из 21 пациента с гистологически подтвержденной карциномой. Другие авторы подчеркивают наличие карциномы в фарфоровом желчном пузыре [106], но поскольку у некоторых пациентов с фарфоровым желчным пузырем также есть желчные камни, трудно приписать точную роль каждому из этих факторов. Холецистит также считается одним из факторов, способствующих развитию этого заболевания.Silk et al. Обнаружили острый и / или хронический холецистит у 54 (76%) из 69 пациентов в своей серии.
Другие возможные факторы, способствующие развитию этого заболевания, включают химические канцерогены, особенно нитрозамины и метилхолантрен, а также воспалительные процессы, такие как язвенный колит, при котором имеется сильная связь с карциномой желчного пузыря.
Патология
В целом от 80% до 85% карцином желчного пузыря являются аденокарциномами, и большинство из них относятся к скиррозному типу.Типы анапластической, плоскоклеточной и аденоакантомы встречаются редко. В серии из Roswell Park [102] у 67 (94%) пациентов была аденокарцинома, а у 4 (6%) – плоскоклеточный рак. В серии исследований, проведенных Yamaguchi и др. [107], 29 пациентов имели аденокарциному и 2 пациента – аденосквамозную карциному. Карцинома была ограничена глазным дном у 21 пациента, телом у 1 пациента, шеей у 2 пациентов и поражением всего органа у 6 пациентов.
Естественная история
Карцинома желчного пузыря обычно обнаруживается на запущенной стадии, когда прогноз неблагоприятный.Многие карциномы желчного пузыря обнаруживаются патологами как случайная находка после удаления желчного пузыря по поводу хронического холецистита. У некоторых пациентов рак диагностируется при вскрытии.
Рак желчного пузыря может быть обнаружен как полиповидный выступ в просвет желчного пузыря или как диффузное утолщение стенки органа с распространением в печень и другие прилегающие органы или без такового. Наиболее частыми участками поражения являются печень и регионарные лимфатические узлы, за которыми следует перитонеальный карциноматоз.
Раковая инвазия в печень обычно происходит в результате прямого распространения болезни, распространения через лимфатические каналы или протоки Люшки или в результате комбинации этих процессов [108]. Метастазы в печень вдали от ложа желчного пузыря наблюдаются у половины пациентов.
Поражение опухолью локальных лимфатических узлов обычно происходит рано. Лимфодренаж идет к лимфатическим узлам вдоль кистозных и общих желчных протоков, а затем через панкреатодуоденальные узлы к парааортальным узлам.Кистозный узел поражается в 42–79% случаев. Почти у половины пациентов опухоль распространяется на общий желчный проток. Однако инвазия в толстую кишку, поджелудочную железу и желудок наблюдается только у 10–20% пациентов [109].
Клинические характеристики
Пациенты с карциномой желчного пузыря могут протекать бессимптомно или могут иметь боль в животе, желтуху, потерю веса, анорексию или тошноту и рвоту. Другие могут иметь образование в правом подреберье или такие осложнения, как желудочно-кишечное кровотечение.Некоторые из этих симптомов и признаков затрудняют различие между карциномой и доброкачественным заболеванием.
Химический состав сыворотки не всегда очень полезен, поскольку уровень билирубина в сыворотке часто бывает нормальным. Повышенный уровень щелочной фосфатазы часто сопровождает нормальный уровень билирубина в сыворотке при этом заболевании [103].
Диагноз
Ультрасонография желчного пузыря может помочь в диагностике рака желчного пузыря. Он может показать локализованное утолщение или массу.К сожалению, появление рака желчного пузыря или ультразвуковое исследование трудно или невозможно отличить от широкого спектра явлений, связанных с камнями в желчном пузыре [105]. В серии исследований Paraskevopoulos [105] у 21 из 3197 пациентов, перенесших обычную холецистэктомию, на момент операции был обнаружен рак желчного пузыря. Правильный предоперационный диагноз был поставлен только двум пациентам, несмотря на то, что все, кроме одного, прошли ультразвуковое обследование, которое выявило камни в желчном пузыре у 18.
КТ-сканирование также может выявить аномалии желчного пузыря. Это может помочь, выявив нерегулярное утолщение стенки желчного пузыря, образования в области желчного пузыря и внутрипросветные образования [110]. Эндоскопическая ретроградная холангиопанкреатография может выявить дефекты наполнения желчного пузыря или признаки инфильтрации общего желчного протока.
Ангиография может показать аномалии и сосуды опухоли, выходящие из пузырной артерии. Однако это не считается процедурой скрининга, поскольку к моменту постановки диагноза опухоль неизлечима [110].
Другой метод, используемый для диагностики карциномы желчного пузыря, – это контрастное исследование верхних отделов желудочно-кишечного тракта, которое может показать смещение желудка и двенадцатиперстной кишки при обширном заболевании; однако результаты не являются конкретными.
Стадирование
Существует две обычно используемые системы стадирования карциномы желчного пузыря: система стадирования TNM Международного союза против рака и система стадирования Невина (таблица 4) [101].
| Tis | Карцинома in situ |
| T1 | Опухоль проникает в слизистую оболочку или мышечный слой |
| T3 | Поражает серозную оболочку и / или один орган, печень <2 см |
| T4 | Поражает 2 или более органов или печень> 2 см |
| N1A 904-дуоденальные узлы : пузырный проток, перихоледокальный или внутригрудный | |
| N1B | Другие регионарные узлы: перипанкреатический (только головка), перихоледокальный или верхний мезентериальный |
| T | N | N | Стадия 0 | Tis | N0 | M0 | |
| Стадия I | 918 21 T1N0 | M0 | |||||
| Стадия II | T2 | N0 | M0 | ||||
| Стадия III | T1 Т2 Т3 | N1 N1 Любой N | M0 M0 M0 | ||||
| Стадия IV | T4 Любой T | Любой N Любой N | M0 M1 |
В системе классификации Невина и Морана опухоли стадии I локализуются на слизистой оболочке; опухоли II стадии проникают в мышечный слой; опухоли стадии III включают все три слоя; болезнь IV стадии включает метастазы в лимфатические узлы пузырного протока; и стадия V болезни включает инвазию метастазов в печень или соседние или отдаленные органы.
Ведение рака желчного пузыря во многом зависит от стадии заболевания на момент обращения. В серии исследований Silk et al [102] стадия заболевания была единственным фактором, который постоянно влиял на выживаемость.
Лечение
Операция: Хирургическая резекция является основным методом лечения рака желчного пузыря. Холецистэктомия может быть всем, что требуется при I и II стадии заболевания. Как правило, он эффективен в тех случаях, когда карцинома является случайной находкой при гистопатологическом исследовании желчного пузыря, удаленного по поводу симптоматического доброкачественного заболевания.Shieh [111] сообщил о 5-летней выживаемости 66,6% для пациентов, опухоли которых были ограничены стенкой желчного пузыря и были случайно обнаружены патологоанатомом.
Некоторые авторы считают, что пациентам с карциномой желчного пузыря, проникающей за пределы слизистой оболочки, могут быть полезны более радикальные процедуры, такие как расширенная холецистэктомия с регионарной диссекцией лимфатических узлов и резекция ложа желчного пузыря. Как только поражение проникает в серозную оболочку желчного пузыря, оно считается неизлечимым.После холецистэктомии или радикального хирургического вмешательства 5-летняя выживаемость составляет от 10% до 30%, при этом местные рецидивы наблюдаются примерно в 80% случаев [109]. Панкреатодуоденэктомия также рекомендуется при лимфаденопатии позади поджелудочной железы или дуоденальной инвазии.
Радиотерапия: Роль лучевой терапии в качестве первичной или адъювантной терапии этого заболевания трудно оценить из-за небольших серий и трудности оценки ответа опухоли. Тем не менее, имеющиеся к настоящему времени данные свидетельствуют о важной роли радиации в качестве паллиативной и адъювантной терапии рака желчного пузыря.
Вайттинен [103] сообщил о 24 пациентах, получавших только хирургическое лечение, и 7 пациентах, получавших хирургическое лечение и послеоперационное внешнее облучение, и обнаружил, что средняя выживаемость составила 29 и 63 месяцев соответственно. Ханна и Райдер [112] сообщили о 51 пациенте с раком желчного пузыря, 35 из которых прошли лучевую терапию. Облучение увеличивало общую выживаемость пациентов, получавших лечебное и паллиативное лечение. Боссет [109] сообщил о пяти из семи пациентов с раком желчного пузыря, у которых не было заболевания через 5, 9, 11, 31 и 58 месяцев после полной резекции и послеоперационной лучевой терапии до 5400 сГр за 30 фракций.Тодороки [113] сообщил о 17 пациентах с карциномой желчного пузыря IV стадии, получивших от 2000 до 3000 сГр интраоперационной лучевой терапии; 10 пациентов также получили внешнее лучевое облучение на 3600 сГр. 3-летняя выживаемость в группе, получавшей лучевую терапию, составила 10%, тогда как ни один из девяти пациентов со стадией IV, получавших только резекцию, не был жив через 3 года.
Эти результаты свидетельствуют о повышении выживаемости и паллиативности у пациентов, получающих послеоперационную лучевую терапию в качестве паллиативной или адъювантной терапии.
Химиотерапия: Химиотерапия малоэффективна при распространенном раке желчного пузыря или в качестве вспомогательного лечения после хирургической резекции. Фторурацил, считающийся наиболее активным монотерапевтическим средством при лечении запущенной болезни желчного пузыря, вызывает лишь кратковременный ответ примерно у 20% пациентов. Другие используемые агенты включают митомицин и доксорубицин. Для пациентов с локализованным заболеванием послеоперационная лучевая терапия в сочетании с фторурацилом может принести определенную пользу.Smoron [114] наблюдал одного пациента с выживаемостью 6 лет после внешнего послеоперационного облучения и химиотерапии фторурацилом.
Новые лекарства и альтернативные пути доставки необходимы, если мы хотим добиться успеха в этом направлении лечения.
Ссылки:
Ссылки1. Американское онкологическое общество: Статистика рака-1995. J Am Cancer Society 45: 8–30, 1995.
2. Глёклер Л.А., Хэнки Б.Ф., Миллер Б.А. и др.: Обзор статистики рака, 1973–1988 (NIH Publ 91-2789).Bethesda, National Institutes of Health, 1988.
3. Энстром Дж. Э .: Рак и общая смертность среди активных мормонов. Cancer 42: 1943–1951, 1978.
4. Крайн Л.: Рост заболеваемости карциномой поджелудочной железы: эпидемиологическая оценка. Am J Gastroenterol 54: 500, 1970.
5. Wynder E et al: Эпидемиологическая оценка причин рака поджелудочной железы. Cancer Res 35: 2228, 1975.
6. Kahn H: Исследование Дорна курения и смертности среди ветеранов США: отчет о восьми с половиной годах наблюдения.NCI Monogr 19: 1, 1966.
7. Roebuck BD, Yager JD Jr, Longnecker DS и др.: Стимулирование ненасыщенными жирами индуцированного азазерином канцерогенеза поджелудочной железы у крыс. Cancer Res 41: 3961–3966, 1981.
8. MacMahon B, Yen S, Trichopoulos D и др.: Кофе и рак поджелудочной железы. N Engl J Med 304: 630–633, 1981.
9. Goldskin HR: Нет связи между кофе и раком поджелудочной железы (письмо). N Engl J Med 306: 997, 1982.
10. Offerhaus GJA, Tersmette AC, Tersmette KWF и др.: Канцерогенез желудка, поджелудочной железы и колоректального рака после удаленной хирургии язвенной болезни.Mod Pathol 1: 352–356, 1988.
11. Pour P, Althoff J, Kruger F и др.: Эффект N-нитрозобис- (2-оксопропил) -альмина после перорального введения хомякам. Cancer Lett 2: 323, 1977.
12. Пур П., Лоусон Т., Хельгесон С. и др.: Влияние холецистокинина на канцерогенез поджелудочной железы на модели хомяка. Carcinogenesis 9: 5197-5201, 1988.
13. Nio Y, Tsubono M, Morimoto H, et al: Loxiglumide (CR1505), антагонист холецистокинина, специфически ингибирует рост клеточных линий рака поджелудочной железы человека, ксенотрансплантированных голым мышам.Cancer 72: 3599–3606, 1993.
14. Робин А., Скотт Дж., Розенфельд Д.: Возникновение рака поджелудочной железы при хроническом панкреатите. Радиология 94: 289, 1970.
15. Кармоди А., Кайл Дж .: Связь между карциномой поджелудочной железы и сахарным диабетом. Br J Surg 56: 362, 1969.
16. Brooks J: Рак поджелудочной железы, в Brooks JR (ed): Surgery of the Pancreas, p 263. Philadelphia, WB Saunders, 1983.
17. Mancuso T, Эль-Аттар А: Когортное исследование рабочих, подвергшихся воздействию бетанафтиламина и бензидина.J Occup Med 9: 277–285, 1967.
18. Longnecker D, Curphey T: Аденокарцинома поджелудочной железы у крыс, получавших азазерин. Cancer Res 35: 2249, 1975.
19. Кубилла А.Л., Фицджеральд П.Дж .: Хирургическая патология опухолей экзокринной части поджелудочной железы в Моосе, AR (ред.): Опухоли поджелудочной железы, стр. 159–193. Baltimore, Williams & Wilkins, 1980.
20. Legg MA: Патология поджелудочной железы, в Brooks JR (ed): Surgery of the Pancreas pp 41–77. Филадельфия, WB Saunders, 1983.
21.Ховард Дж. М., Джордан ГЛ: Рак поджелудочной железы. Curr Probl Cancer 2–1, 1977 г.
22. Moertel CG: Exocrine pancreas, в Голландии JF (ed): Cancer Medicine, pp 1792–1804. Philadelphia, Lea & Febiger, 1982.
23. Hessel SJ, Siegelman SS, McNeil BJ и др.: Проспективная оценка компьютерной томографии и УЗИ поджелудочной железы. Радиология 143: 129–133, 1982.
24. Ward EM, Stephens DH, Sheedy PR: Компьютерные томографические характеристики карциномы поджелудочной железы: анализ 100 случаев.Рентгенография 3: 547, 1983.
25. Тейлор К.Дж., Розенфилд А.Т.: Ультразвуковое исследование серой шкалы в диагностике желтухи. Arch Surg 112: 820–825, 1977.
26. Lees WR: УЗИ поджелудочной железы. Clin Gastroenterol 13: 763–789, 1984.
27. Рош Т., Лайтдейл К.Дж., Ботет Дж. Ф. и др.: Локализация эндокринных опухолей поджелудочной железы с помощью эндоскопического УЗИ. N Engl J Med 326: 1721–1726, 1992.
28. Freeny PC, Ball TJ: Эндоскопическая ретроградная холангиопанкреатография (ERCP) и чрескожная чреспеченочная холангиография (PTC) в оценке подозреваемой карциномы поджелудочной железы: диагностические ограничения и современные роли.Cancer 47: 1666–1678, 1981.
29. Freeny PC, Lawson TL: Radiology of the Pancreas, p 457. New York, Springer-Verlag, 1982.
30. Mitty H, Efremidis S, Yeh HC: Impact. тонкоигольной биопсии при ведении пациентов с карциномой поджелудочной железы. Am J Roentgenol 137: 119–121, 1981.
31. Паскуали С., Сперти С., Альфано Д. и др.: Оценка углеводных антигенов 19–9 и CA-125 у пациентов с раком поджелудочной железы. Pancreas 2: 34–37, 1987.
32. Malesci A, Tommasini MA, Bonato C и др.: Определение антигена CA 19-9 в сыворотке и соке поджелудочной железы для дифференциальной диагностики аденокарциномы поджелудочной железы от хронического панкреатита.Gastroenterol 92: 60–67, 1987.
33. Роблес-Диас Г., Диас-Санчес В., Фернандес-дель-Кастильо С. и др.: Соотношение тестостерона и дигидротестостерона в сыворотке и СА 19-9 в диагностике рака поджелудочной железы. Am J Gastroenterol 86: 591–594, 1991.
34. Igbal MJ, Greenway B, Wilkinson ML, et al.: Половые стероидные ферменты ароматаза и 5-альфа-редуктаза в поджелудочной железе: сравнение нормальной взрослой, плодной и злокачественной ткани . Clin Sci (Lolch) 65: 71–75, 1983.
35. Кирияма С., Хаякева Т., Кондо Т. и др.: Полезность нового онкомаркера, SPAN-1, для диагностики рака поджелудочной железы.Cancer 65: 1557–1561, 1990.
36. Mahvi DM, Meyers WC, Bast RC, et al: Терапевтическая эффективность, определенная с помощью серодиагностического теста с использованием моноклональных антител при карциноме поджелудочной железы. Ann Surg 202: 440, 1985.
37. Romond EH, Mendelsohn LA, MacDonald JS: Адъювантная терапия рака желудочно-кишечного тракта. Cancer Treat Res 33: 273–295, 1987.
38. Гриффин Дж. Ф., Смолли С. Р., Джуэлл В. и др.: Типы неудач после лечебной резекции карциномы поджелудочной железы. Рак 66: 56–61, 1990.
39. Whipple AO, Parsons WB, Mullins CR: Лечение рака ампулы Фатера. Ann Surg 102: 763, 1935.
40. Группа исследования опухолей желудочно-кишечного тракта: рак поджелудочной железы: адъювантная комбинированная лучевая терапия и химиотерапия после радикальной резекции. Arch Surg 120: 899–903, 1985.
41. Группа по изучению опухолей желудочно-кишечного тракта: дополнительные доказательства эффективной адъювантной комбинированной лучевой и химиотерапии после радикальной резекции рака поджелудочной железы. Рак 59: 2006–2010, 1987.
42. Картер С.К., Коннис Р.Л.: Аденокарцинома поджелудочной железы: современные терапевтические подходы, прогностические переменные и критерии ответа, в Staquet MJ (ed): Cancer Therapy: Prognostic Factors and Criteria of Response, pp 235–237. Нью-Йорк, Raven Press, 1975.
43. Crooke ST, Bradner WT: Митомицин C: обзор. Лечение рака Ред. 3: 121–139, 1976.
44. Смит Ф. П., Шейн П. С.: Химиотерапия рака поджелудочной железы. Semin Oncol 6: 368–377, 1979.
45. Mawla NGE: Ифосфамид при распространенном раке поджелудочной железы.Cancer Chemother Pharmacol 18 (Suppl 2): 55–56, 1986.
46. Лерер П.Дж., Уильямс С.Д., Эйнхорн Л. и др. Ифосфамид: активное лекарство при лечении аденокарциномы поджелудочной железы. J Clin Oncol 3: 367–372, 1985.
47. Frederick PS и др.: Химиотерапия 5-фторурацилом, адриамицином и митомицином C (FAM) для продвинутой аденокарциномы поджелудочной железы. Cancer 46: 2014–2018, 1980.
48. Куллинан С.А. и др.: Сравнение трех химиотерапевтических схем лечения запущенной карциномы поджелудочной железы и желудка.JAMA 253: 2061–2067, 1985.
49. Wiggans G, Woolley PV, Macdonald JS и др.: Испытание фазы II стрептозотоцина, митомицина и 5-фторурацила (SMF) в лечении распространенного рака поджелудочной железы. Cancer 41: 387–391, 1978.
50. Группа по изучению опухолей желудочно-кишечного тракта: Фаза II исследования комбинаций лекарственных препаратов при запущенной карциноме поджелудочной железы: фторурацил плюс доксорубицин плюс митомицин C и две схемы стрептозотоцина плюс митомицин C плюс фторурацил. Дж. Клин Онкол 4: 1794–1798, 1986.
51. Хансен RM: Карциномы желудка и поджелудочной железы, в Lokich JJ (ed): Cancer Chemotheraphy by Infusion, 2nd ed, pp 340–357. Чикаго, Precept Press, 1990.
52. Краун Дж., Каспер Э.С., Ботет Дж. И др.: Недостаточная эффективность высоких доз лейковорина и фторурацила у пациентов с запущенной аденокарциномой поджелудочной железы. J Clin Oncol 9: 1682–1686, 1991.
53. Decaprio JA, Mayer RJ, Gonin R, et al: Фторурацил и высокие дозы лейковорина у ранее нелеченных пациентов с запущенной аденокарциномой поджелудочной железы: результаты исследования фазы II .J Clin Oncol 9: 2128–2133, 1991.
54. Ardalan B, Glazer RI, Kenle TW, et al: Синергетический эффект 5-фторурацила и N- (фосфонацетил) -1-аспартата на рост клеток и синтез рибонуклеиновой кислоты. при раке молочной железы человека. Biochem Pharmacol 30: 2045–2049, 1981.
55. Morrell LM, Bach A, Richman SP, et al: фаза II многоучрежденческого испытания низких доз N- (фосфонацетил) -1-аспартата и высоких доз 5-фторурацила как краткосрочная инфузия при лечении аденокарциномы поджелудочной железы: исследование группы онкологов Юго-Запада.Cancer 67: 363–366, 1991.
56. Bengmark S, Andren-Sandberg A: Инфузионная химиотерапия при неоперабельной карциноме поджелудочной железы: недавние результаты. Cancer Res 86: 13–14, 1983.
57. Теодорс А., Буковски Р., Хьюлетт Дж. И др.: Периодическая региональная инфузия химиотерапии аденокарциномы поджелудочной железы. Am J Clin Oncol 5: 555–558, 1982.
57a. Casper ES, Green MR, Kelsen DP и др.: Фаза II испытания гемцитабина (2,2´-дифтордезоксицитидина) у пациентов с аденокарциномой поджелудочной железы.Invest New Drugs 12 (1): 29–34, 1994.
57b. Мур М., Андерсен Дж., Беррис Х. и др.: Рандомизированное испытание гемцитабина и 5-ФУ в качестве терапии первой линии при распространенном раке поджелудочной железы (аннотация). Proc Am Soc Clin Oncol 14: 199, 1995.
58. Benz C, Hollander C, Miller B: Эндокринно-чувствительная карцинома поджелудочной железы: исследования связывания стероидов и цитотоксичности в линиях опухолевых клеток человека. Cancer Res 46: 2276–2281, 1986.
59. Benz C, Wiznitzer I: Связывание стероидов и цитотоксичность в культивируемых карциномах поджелудочной железы человека (аннотация).J Steroid Biochem Mol Biol 19 (Suppl): 125S, 1983.
60. Theve NO, Pousette A, Carlstrom K: Аденокарцинома поджелудочной железы – гормоночувствительная опухоль? Предварительный отчет о лечении Нолвадексом. Clin Oncol (R Coll Radiol) 9: 193, 1983.
61. Миллер Б., Бенц С. Эндокринное лечение рака поджелудочной железы (аннотация). Proc Am Soc Clin Oncol 4:90, 1985.
62. Апп Дж. Р., Олсон Д., Постон Г. Дж. И др.: Ингибирование роста двух аденокарцином поджелудочной железы человека in vivo аналогом соматостатина SMS 201–995.Am J Surg 142: 308–311, 1988.
63. Smith JP, Solomon TE, Baghari S, Kramer S: Холецистокинин стимулирует рост аденокарциномы поджелудочной железы человека SW-1990. Dig Dis Sci 35: 1377–1384, 1990.
64. Abbruzzese JL, Gholson CF, Daugherty K, et al: пилотное испытание антагониста рецептора холецистокинина ML-329 у пациентов с распространенным раком поджелудочной железы. Pancreas 7: 165–171, 1992.
65. Moertel CG et al: Терапия локально неоперабельного рака поджелудочной железы: рандомизированное сравнение только высокой дозы (6000 R) облучения и умеренной дозы облучения (4000 R плюс 5-фторурацил) и высокие дозы облучения плюс 5-фторурацил: Группа исследования опухолей желудочно-кишечного тракта.Cancer 48: 1705–1710, 1981.
66. Шибамото Ю., Манабе Т., Баба Н. и др.: Высокодозная внешняя лучевая и интраоперационная лучевая терапия в лечении резектабельного и неоперабельного рака поджелудочной железы. Int J Radiat Oncol Biol Phys 19: 605–611, 1990.
67. Ролдан Г.Е. и др.: Внешний пучок в сравнении с интраоперационным и внешним облучением при местнораспространенном раке поджелудочной железы. Cancer 61: 1110–1116, 1988.
68. Bosslet K, Kern HF, Kanzy A и др.: Моноклональное антитело со связывающей и ингибирующей активностью по отношению к клеткам карциномы поджелудочной железы человека.Cancer Immunol Immunother 23: 185–191, 1986.
69. Herlyn DM, Koprowski H: моноклональные антитела IgG 2a ингибируют рост опухоли человека посредством взаимодействия с эффекторными клетками. Proc Natl Acad Sci USA 79: 4761–4795, 1982.
70. Buchler M, Friess H, Schultheiss HK и др.: Рандомизированное контролируемое испытание адъювантной иммунотерапии (мышиные моноклональные антитела 494/32) при резектабельном раке поджелудочной железы. Cancer 68: 1507–1512, 1991.
71. Gottlinger H, Funke I, Johnson JP и др.: Поверхностный антиген эпителиальных клеток 17-1A, мишень для терапии опухолей, опосредованной антителами: его биохимическая природа, распределение в тканях и распознавание разными моноклональными антителами.Int J Cancer 38: 47–53, 1986.
72. Korz M, Meltzer P, Trent J: Повышенная экспрессия рецептора эпидермального фактора роста коррелирует с изменениями хромосомы 7 при раке поджелудочной железы человека. Proc Natl Acad Sci USA 83: 5141–5144, 1986.
73. Almoquera C, Shibata D, Forrester K и др.: Большинство человеческих карцином экзокринной поджелудочной железы содержат мутантные гены c-k-ras. Cell 53:49, 1988.
74. Бадд К. Психотропные препараты в лечении хронической боли. Анестезия 33: 531, 1978.
75. Сердлоу М: Лечение стреляющей боли. Postgrad Med J 56: 159–161, 1980.
76. Искья С., Луццани А., Искья А. и др.: Новый подход к нейролитическому блоку чревного сплетения: трансаортальная техника. Pain 16: 333–341, 1983.
77. Leung JWC, Bowen-Wright M, Aveling W и др.: Блокада чревного сплетения при боли при раке поджелудочной железы и хроническом панкреатите. Br J Surg 70: 730–732, 1983.
78. Thompson GE, Moore DC, Bridenbaugh LD, et al: Боль в животе и алкогольная блокада чревного сплетения.Анестезия Анальгезия 56: 1–5, 1977 г.
79. Международный союз против рака: Практикум по биологии рака человека. Отчет 17: Гепатоцеллюлярная карцинома. Женева, 1982.
80. Бизли Р.П. и др.: Профилактика перинатально передаваемых вирусных инфекций гепатита В с помощью иммуноглобулина против гепатита В и вакцины против гепатита В. Lancet 2: 1099–1122, 1983.
81. Adamson RC, Corree P, et al: Канцерогенность афлатоксина B1 у макак-резусов: два дополнительных случая первичного рака печени.J Natl Cancer Inst 57: 67–78, 1976.
82. Beazley R, Cohn I Jr: Опухоли поджелудочной железы, желчного пузыря и внепеченочных протоков. Учебник ACS Clin Onc 16: 219–231, 1994.
83. Окуда К., Рю М., Такайоши Т.: Хирургическое лечение гепатомы: опыт Японии, в Wanebo JH (ред.): Хирургия печени и желчевыводящих путей, стр. 219– 238. Нью-Йорк, Марсель Деккер, 1987.
84. Окуда К., Обата Х. и др.: Прогноз первичной гепатоцеллюлярной карциномы. Гепатология 4: 3–6С, 1984.
85.Chin H, Cheng E, Gellar N: Гепатоцеллюлярная карцинома: статистический анализ 78 последовательных пациентов (аннотация). Proc Am Soc Clin Oncol 3: 6, 1984.
86. Буама П.К., Корнелл С., Джеймс О.Ф.У. и др.: Изменения гетерогенности сывороточного АФП у пациентов с гепатоцеллюлярной карциномой во время химиотерапии. Cancer Chemother Pharmacol 17: 182–184, 1986.
87. Хосоки Т., Чатани М., Мори С.: Динамическая компьютерная томография гепатоцеллюлярной карциномы. Am J Radiol 139: 1099–1106, 1982.
88.Цузуки Т., Огата Ю. и др.: Резекция печени у 125 пациентов. Arch Surg 119: 1025–1032, 1984.
89. Адсон М.А.: Первичный гепатоцеллюлярный рак: западный опыт в Blumgart LH (ред.): Хирургия печени и желчевыводящих путей, стр. 1155. Нью-Йорк, Черчилль-Ливингстон.
90. Zhou XD, Tang ZY, Yu YQ и др.: Клиническая оценка криохирургии при лечении первичного рака печени. Cancer 61: 1889–1892, 1988.
91. Льюис Б.Дж., Фридман М.А.: Текущее состояние химиотерапии гепатомы, в Ogawa M (ed): Chemotherapy of Hepatic Tumors, pp 63–74.Princeton, NJ, Excerpta Medica, 1984.
92. Группа изучения опухолей желудочно-кишечного тракта: проспективное испытание рекомбинантного человеческого интерферона альфа 2В у ранее нелеченных пациентов с гепатоцеллюлярной карциномой. Cancer 66: 135–139, 1990.
93. Kardinal CG, Moertel CG и др.: Комбинированная терапия доксорубицином и альфа-интерфероном распространенной гепатоцеллюлярной карциномы. Cancer 71: 2187–2190, 1993.
94. Atiq OT, Kemeny N, Niedzwiecki D, et al: Лечение неоперабельной первичной печени внутрипеченочным фтордезоксиуридином и митомицином C с помощью имплантированного насоса.Cancer 69: 920–924, 1992.
95. Йодоно Х., Сасаки Т. и др.: Химиотерапия с использованием артериальной инфузии для поздней стадии гепатоцеллюлярной карциномы с терапией EPF и EAP. Cancer Chemother Pharmacol 31: S89–92, 1992.
96. Заказать SE, Stillwagon GB, Klein JL, et al: Iodine 131 antiferritin, новый метод лечения гепатомы: исследование RTOG. J Clin Oncol 3: 1573–1582, 1985.
97. Заказать SE, Pajak T, et al: рандомизированное проспективное исследование, сравнивающее химиотерапию полной дозой с антиферритином 131 I: исследование RTOG.Int J Radiat Oncol Biol Phys 20: 953–963, 1991.
98. Ивацуки С., Старзл Т.Э., Шихан Д.Г. и др.: Резекция печени по сравнению с трансплантацией при гепатоцеллюлярной карциноме. Ann Surg 214: 221–229, 1991.
99. Penn I: Трансплантация печени при первичном и метастатическом раке печени. Surgery 110: 726–735, 1991.
100. de Stoll M: Rationis Mendendi in Nosocomio Practico vendobonensi. Часть I Lugduni Batavorium, Haak et Socios et A et J. Honkoop, 1788.
101. Невин Дж. Э., Моран Т. Дж .: Карцинома желчного пузыря: стадия, лечение и прогноз.Cancer 37: 141–148, 1976.
102. Silk YN et al: Карцинома желчного пузыря: опыт Розуэлл-парка. Ann Surg 210: 751–757, 1989.
103. Vaittinen E: Карцинома желчного пузыря: исследование 390 случаев, диагностированных в Финляндии в 1953–1967 годах. Ann Chir Gynaecol 168 (Suppl): 1–18, 1970.
104. Krain LS: Карцинома желчного пузыря и внепеченочных желчных протоков: Анализ 1808 случаев. Гериатрия 27: 1111–1117, 1972.
105. Параскевопулос Дж. А. и др.: Первичная карцинома желчного пузыря: 10-летний опыт.Ann R Coll Surg Engl 74: 222–224, 1992.
106. Polk HC: Карцинома кальцинированного желчного пузыря. Gastroenterology 50: 582, 1966.
107. Yamaguchi K, Tsuneyoshi M: Субклиническая карцинома желчного пузыря. Am J Surg 163: 382–386, 1992.
108. Фахим Р. Б., Макдональд Дж. Р., Ричард Дж. К. и др.: Карцинома желчного пузыря: исследование способов ее распространения. Ann Surg 156: 114–124, 1962.
109. Bosset JF и др.: Первичная карцинома желчного пузыря: адъювантное послеоперационное внешнее облучение.Cancer 64: 1843–1847, 1989.
110. Итаи Й., Араки К. и др.: Компьютерная томография рака желчного пузыря. Radiology 137: 713–718, 1980.
111. Shieh CJ, Dunn E, Standard JE: Первичный рак желчного пузыря: обзор 16-летнего опыта работы в медицинском центре больницы Уотербери. Cancer 47: 996–1004, 1981.
112. Hanna SS, Rider WD: Карцинома желчного пузыря или внепеченочных желчных протоков: роль лучевой терапии. Can Med Assoc J 118: 59–61, 1978.
113. Тодороки Т. и др.: Интраоперационная лучевая терапия при запущенной карциноме желчевыводящих путей.Cancer 46: 2179–2184, 1980.
114. Сморон Г.Л.: Лучевая терапия рака желчного пузыря и желчевыводящих путей. Cancer 40: 1422–1424, 1977 г.
Заболевание печени: диагностическая оценка (Материалы)
Диагностическая стратегия
1. Анамнез
2. Физикальное обследование
3. Гематологические исследования
4. Биохимия
5 Общий анализ мочи
6. Серология
7. Рентгенография
8. Ультрасонография
9.Ядерная сцинтиграфия
10. Гистопатология
Клинические признаки, связанные с заболеванием печени
- Темный или светлый стул
Клинические признаки, наблюдаемые при печеночной энцефалопатии
Физикальное обследование
Заболевания печени варьируются от минимальных изменений до более значительных признаков, таких как желтуха, пигментная моча (билирубинурия), кровоточащий диатез (гематемезис, мелена, гематурия, петекхии, экхимозы, бледность из-за анемии кровопотери) и печеночная энцефалопатия.В некоторых случаях острого заболевания печени печень увеличивается в размерах и вызывает болезненные ощущения (гепатодиния). В норме печень у собак и кошек не прощупывается. Гепатомегалия – это характерная черта инфильтративных заболеваний (воспаление, стеатоз, неоплазия), застойных явлений или холестаза (нагрубание желчи). Асцит может присутствовать (из-за гипоальбуминемии) и обычно указывает на хроническое заболевание. Кровоизлияние в брюшную полость обычно указывает на травму или новообразование (например, гемангиосаркому).
Всегда следует проводить тщательный медицинский осмотр.У кошек первые признаки тканевой желтухи обнаруживаются на хвосте твердого неба. Внепеченочные физические данные могут быть полезны для предположения о возможном участии печени в системном процессе:
** Первым шагом в оценке пациента с желтухой является исключение гемолитической анемии (может быть опасно для жизни). У любого больного пациента следует немедленно определить ПКВ. Многие собаки с желтухой из-за гемолитической анемии (например, AIHA) были направлены с предварительным диагнозом «заболевание печени».
Пепеченочные причины (печеночные причины) желтухи включают:
o Метиленовый синий
o Ацетаминофен (кошки)
o Феназопиридин (кошки)
o Свинец
- Иммунно-опосредованное разрушение
HA o FeLV-ассоциированные (кошки)
o Реакция на переливание крови
o Hemobartonella
o Babesia
o Ehrlichia
o Cytauxzoon felis
o Дирофиляриоз (собаки)
для гемобелематологии
болезнь, гемобарт, характеристика анемии).
1. Воспалительная лейкограмма: острые воспалительные заболевания. Хронические гнойные заболевания (холангиогепатит, абсцесс печени)
2. Легкая нерегенеративная анемия (нормоцитарная / нормохромная): многие хронические заболевания
3. Легкая микроцитарная анемия с лептоцитами: R / O портосистемный шунт
4. Пойкилоцитоспецифическое изменение: A. кошки с любой формой заболевания печени, включая портосистемный шунт
5. Шистоциты (фрагментированные эритроциты): новообразования печени (особенно HSA)
Биохимия
Основная цель измерения активности ферментов печени – выявить наличие гепатобилиарных расстройств.Ферменты сыворотки не обладают специфичностью в отношении природы или тяжести заболевания. Это не тесты функции печени. Повышенная активность ферментов в сыворотке крови довольно распространена и может быть результатом обратимых или необратимых изменений гепатоцеллюлярных мембран, структурного повреждения, связанного с ишемией, некрозом или холестазом, или индукции микросомальных ферментов (например, кортикостероидов, фенобарбитала). Индукция микросомальных ферментов обычна у собак, но не обнаружена у кошек. В большинстве случаев дифференцировать причину повышения уровня ферментов печени невозможно без морфологического исследования ткани печени.В некоторых случаях функционального повреждения значительные морфологические изменения могут отсутствовать в ткани печени в случаях, когда уровень ферментов печени был повышен. Паттерны активности ферментов могут поддерживать, но не доказывать окончательный диагноз. В некоторых случаях тяжелого заболевания печени (например, цирроза) повышение активности ферментов отсутствует.
1. ALT (SGPT)
a. Находится в изобилии в гепатоцеллюлярной цитоплазме
b. Обнаруживается в нескольких тканях, но наибольшая концентрация находится в гепатоцитах (считается, что он специфичен для печени у собак и кошек).
г. Цитозольный: концентрация в клетке в 10 000 раз больше, чем в сыворотке.
г. ALT может вытекать из гепатоцита в любом состоянии, которое в значительной степени изменяет проницаемость мембраны (утечка не требует гибели клеток).
эл. Период полувыведения из сыворотки <24 часов.
ф. Увеличение фермента
(1) Величина прямо пропорциональна количеству пораженных гепатоцитов.
(2) После острой дегенерации или некроза гепатоцитов уровень АЛТ в сыворотке повышается на 12 часов.Наибольшие подъемы возникают при некрозе клеток.
(3) Значимый уровень: как минимум в 2-3 раза выше нормы. При тяжелой форме некроз может увеличиваться в 20-40 раз от нормы.
(4) Величина, не связанная с обратимостью состояния.
(5) Повышение уровня АЛТ неспецифично для первичного гепатоцеллюлярного заболевания. Обструкция желчных протоков (например, панкреатит) вызывает повышение АЛТ в течение 3-4 дней, и повышение сохраняется в течение как минимум нескольких дней.Вероятно, что удерживаемые соли желчных кислот физически повреждают клеточные мембраны окружающих гепатоцитов и приводят к утечке ферментов.
(6) ALT – это просто скрининговый тест на гепатоцеллюлярное повреждение.
(7) Результат:
(a) Если значения уменьшаются на 50% каждые 1-2 дня, прогноз хороший.
(b) Продолжающееся повышение указывает на стойкое гепатоцеллюлярное заболевание (рассмотрите дополнительные тесты: например, анализ желчных кислот в сыворотке крови, биопсия печени).
2. АСТ (SGOT)
а. НЕ специфичен для печени из-за его высокой концентрации в других тканях, особенно в мышцах
(ЛДГ имеет аналогичные недостатки).
г. У кошек АСТ может быть более чувствительным индикатором гепатобилиарной болезни, чем у собак
c. Имеет тенденцию к параллельному АЛТ в отношении поражения печени.
3. Щелочная фосфатаза (SAP)
a. Увеличение является результатом увеличения продукции, вторичной по отношению к внутрипеченочному или внепеченочному холестазу, а не утечки клеток, как в случае с АЛТ / АСТ.
г. Мембранно-связанный фермент, присутствующий во многих тканях.
г. Собаки: 4 изофермента сыворотки (кости, печень, индуцированный кортикостероидом [из печени], изофермент неизвестного происхождения).
Кошка: 2 изофермента сыворотки (кость, печень). Намного более короткий период полураспада, чем у собак (любое повышение должно быть оценено критически). Меньшее количество АП на грамм печени.
г. Повышенный SAP:
(1) Активность остеобластов (обычно в 2-3 раза выше нормы): Молодые растущие животные до 7-8 месяцев (небольшое увеличение SAP, которое может быть обнаружено у молодой растущей кошки из-за костного изофермента, может имитировать величину повышения SAP у молодой кошки с заболеванием печени.Опухоли костей. Вторичный почечный гиперпаратиреоз. ГИПЕРТИРОИДИЗМ КОШЕК часто связан с повышенной сывороточной активностью печеночных ферментов (особенно АЛТ и САП). В этих случаях изофермент AP может иметь костное происхождение из-за повышенного метаболизма костной ткани, вторичного по отношению к эффектам тиреотоксикоза. У кошек с гипертиреозом в большинстве случаев не наблюдается значительных изменений функции печени.
(2) Использование глюкокортикоидов (собачьих): зависит от человека, типа вводимого глюкокортикоида и продолжительности лечения.Если биопсия печени выявляет стероидную гепатопатию, R / Os включают экзогенные глюкокортикоиды, синдром Кушинга, повышенное содержание эндогенных глюкокортикоидов, возможно, связанное с хроническим стрессом / заболеванием.
(3) Синтез SAP (печеночный), вызванный лекарствами, отличными от глюкокортикоидов (например, противосудорожными средствами).
(4) Первичные или вторичные гепатоцеллюлярные нарушения. Наибольшее увеличение SAP происходит при диффузных или очаговых холестатических расстройствах и новообразованиях печени.
(5) Любая причина гепатобилиарного воспаления может привести к вторичным гепатобилиарным нарушениям, ведущим к внутрипеченочному холестазу.** Панкреатит может привести к заметному увеличению SAP.
(6) Новообразование молочной железы (легкое).
эл. Обычно существует период задержки между изменениями печени и отражением этих изменений в активности SAP
4. Гамма-глутилтрансфераза (GGT)
a. Большая часть сывороточной активности GGT у собак и кошек происходит из печени. Наибольшая активность тканей наблюдается в почках и поджелудочной железе.
г. Повышенный GGT:
(1) Внутрипеченочный или внепеченочный холестаз
(2) Панкреатит
(3) Введение лекарств (собаки).
г. У собак увеличение GGT в значительной степени соответствует увеличению SAP. Исключение – существует минимальная индукция активности GGT с помощью противосудорожных препаратов (может быть полезно для дифференциации первичного заболевания печени от изменений ферментов, вызванных простой индукцией лекарственного средства).
г. У кошек GGT более чувствителен при диагностике заболеваний печени, чем щелочная фосфатаза (но более специфичен для гепатобилиарной болезни). GGT обычно идет параллельно изменениям в SAP с одним заметным исключением для кошек.У кошек с липидозом печени наблюдается заметное увеличение SAP, в то время как наблюдается только небольшое увеличение GGT. Этот факт может быть полезен для усиления подозрений о наличии липидоза печени.
5. Неспецифическое повышение активности печеночных ферментов в сыворотке может быть вторичным по ряду причин. В большинстве случаев уровни ферментов в сыворотке не превышают нормальных значений в 2–3 раза. Обычно отсутствует существенное морфологическое или функциональное повреждение гепатобилиарной системы.
а. Нарушения, вызывающие снижение перфузии печени с последующей гепатоцеллюлярной гипоксией: шок, сердечные заболевания (ХСН, сердечные гельминты, перикардиальный выпот), анемия.
г. Эндотоксемия / сепсис
c. Сахарный диабет
e. Гипотиреоз
ф. Гипертиреоз
г. Гипертермия
6. Билирубин
а. Уровень общего билирубина предоставляет наиболее полезную клиническую информацию (мало пользы от изучения каких-либо количественных различий между уровнями прямого и непрямого билирубина).
г. Классифицируйте желтуху на: предпеченочную, печеночную, постпеченочную.Желтуха развивается раньше при заболевании, чем при паренхиматозном заболевании.
г. Желтуха развивается, когда уровень билирубина превышает 2,0–3,0 мг / дл.
г. Билирубинурия даже в концентрированной моче – аномальное явление у кошек. У кошек высокий почечный порог билирубина, а у собак низкий почечный порог.
эл. Билирубин менее чувствителен, но более специфичен, чем ферменты печени, при выявлении гепатобилиарной болезни. Использование значений билирубина в сочетании с ферментами печени и концентрацией желчных кислот в сыворотке крови улучшает диагностическую специфичность ферментов.
7. Белки плазмы
а. Альбумин является основным белком плазмы, синтезируемым в печени.
(1) Период полувыведения альбумина у собак составляет примерно 23 дня.
(2) Снижение уровня альбумина в результате синтетической недостаточности происходит, когда нарушена более чем 70% гепатобилиарной функции.
г. Большинство глобулинов сыворотки, за исключением иммуноглобулинов, синтезируется в печени.
(1) Пациенты с печеночной недостаточностью редко имеют клинически значимое снижение уровня глобулинов; однако концентрации глобулина часто нормальны или даже повышены при гепатобилиарной болезни из-за увеличения системного синтеза иммуноглобулинов (лимфатические узлы, костный мозг, селезенка, другие органы) в ответ на системную антигенную нагрузку.
г. Проблема – Гипопротеинемия
ЕСЛИ ВЫЯВЛЯЕТСЯ ГИПОПРОТЕИНЕМИЯ, СЛЕДУЮЩИЙ ЭТАП ИССЛЕДОВАНИЯ:
(1) Печень: анализ желчных кислот.
(2) Почка: соотношение белок: креатинин в моче
(3) Кишечник: биопсия.
Окончательный диагноз ставится на основании биопсии пораженного органа (ов).
Сывороточные желчные кислоты – основа теста
Аномальная концентрация желчных кислот в сыворотке приближается к 100-процентной специфичности при заболеваниях печени, когда концентрация превышает 20 мкМ / л у кошек (нормальная 5 мкМ / л) и 30 мкМ / л у собак ( нормальная 10 мкМ / л).Первичные желчные кислоты, холевая и хенодезоксихолевая кислоты синтезируются в печени из холестерина, а затем конъюгируются с аминокислотой (в первую очередь таурином у собак и кошек). После синтеза желчные кислоты накапливаются и концентрируются в желчном пузыре. Холецистохинин высвобождается в тонком кишечнике в ответ на присутствие соляной кислоты, пищевых жиров и белков и стимулирует сокращение желчного пузыря с последующим высвобождением желчных кислот. В тонком кишечнике желчные кислоты способствуют эмульгированию, перевариванию и всасыванию жиров.Большинство первичных и вторичных желчных кислот реабсорбируются в подвздошной кишке за счет эффективного активного транспортного процесса и быстро выводятся печенью из воротной системы кровообращения.
Энтерогепатическая циркуляция желчных кислот чрезвычайно эффективна (90 процентов). По оценкам, 2-5 процентов от общего объема циркулирующих желчных кислот ежедневно теряется с калом. Эффективность этого энтерогепатического кровообращения является основой для использования концентраций желчных кислот при оценке гепатобилиарной функции и целостности гепатопортального кровообращения. Печень поддерживает огромную резервную способность для синтеза желчных кислот.Печеночная недостаточность не ограничивает концентрацию желчных кислот в сыворотке крови.
Нет необходимости проводить анализ желчных кислот у пациентов с гипербилирубинемией, не страдающих анемией. Гипербилирубинемия при отсутствии гемолиза указывает на наличие печеночного или постпеченочного расстройства. Однако тест можно проводить у пациентов с гипербилирубинемией, поскольку желчные кислоты не конкурируют с билирубином за транспорт или метаболизм, как это делают органические анионные красители (BSP и ICG). Повышение уровня желчных кислот у кошек с желтухой является наибольшим при липидозе печени и непроходимости внепеченочных желчных протоков, а у собак с тяжелым заболеванием печени
Выполнение теста
Чтобы получить максимальную диагностическую информацию при измерении общего содержания желчных кислот в сыворотке крови, оба показателя соответствуют 12 баллам. следует получить образец через час голодания и через 2 часа после приема пищи.Исключением является то, что если оценка желчной кислоты проводится у желтушной кошки с общим уровнем билирубина более 3,0 г / дл, проводится только уровень покоя. Следует употреблять продукты с высоким содержанием белков и жиров, потому что они наиболее часто вызывают энтерогепатическое кровообращение желчных кислот на 2-часовом постпрандиальном уровне. Необязательно кормить большим количеством еды. Животным весом 10 фунтов или меньше дают 2 чайные ложки, а животным весом более 10 фунтов – 1-2 столовые ложки.
Если отсутствие аппетита является проблемой, можно предпринять следующие шаги, чтобы уговорить кошку поесть:
1.Принудительная подача.
2. Могут потребоваться специальные меры, чтобы избежать анорексигенных раздражителей (например, предлагать еду в тихой обстановке – вдали от собак [!!], кормить хозяина с рук в частной зоне и т. Д.). Кроме того, легкая стимуляция ласками и поглаживанием спины может стимулировать прием пищи.
3. Прогревание пищи может помочь уговорить невзрачную кошку поесть. Кошки предпочитают корм, который подают при температуре от 78 до 103 градусов по Фаренгейту.
4. Введите диазепам внутривенно для стимуляции аппетита (0,1 мг / фунт).
5.Если считается, что отказ животного от еды в первую очередь связан с пребыванием в больнице, а принудительное кормление и другие меры оказываются безуспешными, берется образец крови натощак, и пациента отправляют домой, чтобы поесть. Затем через 2 часа берут образец крови после приема пищи.
Животным с энцефалопатической тенденцией, которым необходимо кормить пищей с высоким содержанием белка, можно давать пищу с низким содержанием белка (например, Hill’s k / d, Select Care Modified). Если рвота является проблемой и ее частота не позволяет кормить, первоначальное тестирование ограничивается пробой натощак.Если результат выше нормы, значит, серьезная проблема с печенью остается предметом рассмотрения. Однако, если образец натощак нормальный, нельзя исключать заболевание печени.
Интерпретация
Значения натощак или после приема пищи, превышающие 20 мкМ / л у кошек и 30 мкМ / л у собак, считаются указанием на наличие серьезного гепатобилиарного заболевания. Этим пациентам необходима биопсия печени. Паттерн постпрандиального увеличения показателей натощак может быть диагностически значимым.У некоторых пациентов с тяжелым нарушением функции гепатобилиарной системы уровень желчных кислот натощак нормальный, но значительно повышается после кормления. Животные с тяжелым холестазом обычно имеют высокие концентрации желчных кислот в сыворотке крови натощак, которые относительно не изменяются или повышаются лишь незначительно после контрольного приема пищи. Кошки и собаки с портосистемным шунтированием могут иметь нормальные или лишь слегка повышенные уровни натощак, но постпрандиальные концентрации всегда ненормальны.
Уровни желчных кислот могут быть очень полезны для мониторинга реакции на терапию после получения окончательного диагноза.Концентрация SBA является гораздо более чувствительным индикатором функции печени, чем сывороточный билирубин или альбумин. Ферменты печени часто возвращаются в норму задолго до того, как функция печени возвращается в норму.
Рентгенография и УЗИ
Обзорная рентгенография брюшной полости может дать полезную информацию у животных с подозрением на гепатобилиарную болезнь. Кошки с заболеваниями печени часто имеют нормальный размер печени до небольшого или умеренного увеличения. Аномально маленькая печень (микропеченочная) чаще всего встречается в сочетании с врожденным портосистемным шунтом или хроническим тяжелым заболеванием печени (например,г., цирроз). Рентгенологические признаки микропеченки включают краниальное смещение оси желудка и, в некоторых случаях, смещение черепа почек и кишечника. Рентгенологические признаки гепатомегалии включают расширение краев печени каудально к реберной дуге, округление границ печени и каудальное смещение желудка, почек и кишечника. На обзорных рентгенограммах иногда визуализируются крупные очаговые массы. Другие аномалии, которые могут быть идентифицированы, включают холелиты (повышенное помутнение в области желчного пузыря), кальцинированные внутрипеченочные поражения или очаговые или мультифокальные радиопрозрачности, которые могут указывать на наличие гепатобилиарной инфекции, абсцесс или холецистит.
Контрастная портография используется для точного диагноза портосистемного шунта. В некоторых случаях ультразвуковое исследование полезно для обнаружения шунта, но его локализация может быть затруднена. Ректальная портальная сцинтиграфия – отличный метод неинвазивного подтверждения наличия шунта, но этот метод не позволяет надежно идентифицировать конкретное местоположение шунта. Контрастная портография устанавливает наличие и положение шунтирующего сосуда.
Ультрасонография обычно дает больше полезной информации, чем обзорная рентгенография, при неинвазивной оценке паренхимы печени и желчевыводящей системы.Это неоценимое диагностическое средство для оценки пациентов с желтухой. Очаговые или диффузные изменения эхогенности паренхимы (гипоэхогенная, гиперэхогенная), желчных протоков, размера и содержимого желчного пузыря, а также сосудистой сети можно оценить с помощью ультразвукового исследования. Очаговые поражения печени могут быть легко идентифицированы и впоследствии взяты образцы с помощью тонкоигольной аспирации или игольной биопсии под контролем ультразвука. Желчный пузырь легко визуализируется, но остальные желчные пути у нормального животного не идентифицируются.Расширение желчных путей происходит ретроградным образом от места обструкции с быстрым увеличением желчного пузыря. Расширение внепеченочных протоков, достаточное для ультразвукового обнаружения, происходит примерно через 72 часа. Увеличение внутрипеченочных желчных протоков наблюдается примерно через пять-семь дней. Если при ультразвуковом исследовании у кошки с желтухой не наблюдается расширения внепеченочных протоков и исключена гемолитическая болезнь, вероятнее всего, присутствует гепатоцеллюлярная болезнь.Для установления окончательного диагноза необходима биопсия печени.
Ультрасонография может предоставить очень полезную информацию для предварительной дифференциации липидоза печени от других основных причин заболевания печени кошек, включая непроходимость внепеченочных желчных протоков, холангиогепатит и метастатическую неоплазию. Ультрасонографические признаки липидоза печени включают диффузную гомогенную гиперэхогенность паренхимы печени и гепатомегалию. При липидозе печени эхогенность печени эквивалентна или выше эхогенности селезенки и коры почек (у нормальных животных печень менее эхогенная, чем селезенка, и эквивалентна или немного более эхогена, чем почечная кора).
Биопсия печени
Самым важным диагностическим шагом в окончательной диагностике заболевания печени является гистологическая оценка ткани печени. Уже описанные диагностические тесты очень важны для определения вероятности нарушения функции печени, а также для предоставления информации о функции печени и о том, показан ли хирургический подход для окончательного диагноза и / или лечения. Диагноз, конкретные решения относительно лечения и обсуждение общего прогноза – все зависит от результатов биопсии печени, а также от биопсии других органов, как указано (т.е., может быть мультифокальный болезненный процесс). Есть много приемлемых методов получения биопсии печени. Противопоказаний к проведению процедуры очень мало. Процедуры биопсии печени включают тонкоигольную аспирацию, чрескожную слепую или игольную биопсию под контролем УЗИ, лапароскопию под контролем и исследовательскую лапаротомию.
Настоятельно рекомендуется использовать клиновидную биопсию, полученную при лапароскопии или лапаротомии, поскольку более крупные клиновидные образцы предоставляют больше ткани для анализа.




 Отмеряют 3 столовые ложки, пересыпают в емкость и заливают 500 мл воды. Прогревают до кипения и томят на медленном огне 30 минут. Выдерживают полчаса и принимают небольшими порциями на протяжении дня.
Отмеряют 3 столовые ложки, пересыпают в емкость и заливают 500 мл воды. Прогревают до кипения и томят на медленном огне 30 минут. Выдерживают полчаса и принимают небольшими порциями на протяжении дня. Прогрессирование недостаточности – причина летального исхода.
Прогрессирование недостаточности – причина летального исхода. Саркоидоз, токсический гепатит, метастатическое поражение при химиотерапии, абсцессы.
Саркоидоз, токсический гепатит, метастатическое поражение при химиотерапии, абсцессы.