Профилактика рака желудка: Профилактика рака желудка
Профилактика рака желудка
Причины появления онкологических патологий не выяснены до сих пор. Относительно любого вида рака выявлены факторы повышенного риска появления. Люди, попадающие под действие негативных факторов, включены в зону риска. С учётом повышенного уровня опасности такие люди должны быть предельно внимательны в отношении собственного здоровья. Примеры негативного исхода лечения запущенных стадий раковых болезней становятся памяткой для группы потенциального риска. Для избегания основной патологической проблемы (рак желудка) медиками разработан комплекс процедур, направленных на предупреждение появления онкологии у людей с повышенным риском возникновения патологии. Профилактика рака желудка – это комплекс действий и требований, которые имеют своей целью предупреждение возникновения патологического процесса возникновения опухолей в этом органе пищеварения человека.
Рак – агрессивный по отношению к человеку вид новообразования.
При любом виде рака, включая онкологию желудка, происходит снижение качества человеческой жизни. Развиваются
сопутствующие патологии.
Первичная и вторичная группа профилактических мероприятий
Для предупреждения развития патологии онкологии желудка применяют два основных направления профилактических мер.
Первичная профилактика включает мероприятия, имеющие отношение к неопределённому кругу лиц, то есть затрагивающие
интересы не только включённых в группу повышенного риска. Основные положения первичной профилактики: правильное
питание; отказ от вредных привычек; проведение осмотров у врача с целью раннего диагностирования и лечения
онкологического процесса.
Подробнее о первичной профилактике рака желудка.
Правильное питание – основа здоровья человека и его активности на протяжении долгих лет жизни. Лишний вес, спровоцированный неправильной системой употребления пищи, приводит к нарушениям в работе: сосудов и сердца; лёгких; позвоночника; суставов. При превышении допустимых показателей по ожирению наступает летальный исход для больного.
Если человек ставит целью правильно питаться, потребуется соблюдать ряд правил, которые помогут продуктам быстрее и
качественнее усваиваться. Для здорового человека правильное питание подразумевает употребление в пищу: овощей;
фруктов; ягод; орехов; круп; молочных продуктов; нежирных сортов мяса и рыбы. Греча, рис, полба богаты клетчаткой и
питательными веществами. Рацион должен состоять из лёгкой пищи, а потребление желательно осуществлять в соответствии
с режимом, придётся соблюдать порядок ежедневно в течение жизни. Рацион включает разные супы, которые благотворно
сказываются на пищеварительном процессе. Желательно употребление достаточного количества чистой питьевой воды,
позволяя правильно функционировать почкам и всей выделительной системе.
Греча, рис, полба богаты клетчаткой и
питательными веществами. Рацион должен состоять из лёгкой пищи, а потребление желательно осуществлять в соответствии
с режимом, придётся соблюдать порядок ежедневно в течение жизни. Рацион включает разные супы, которые благотворно
сказываются на пищеварительном процессе. Желательно употребление достаточного количества чистой питьевой воды,
позволяя правильно функционировать почкам и всей выделительной системе.
Рекомендуется отказаться от острой пищи либо сократить количественный показатель её потребления. Острая пища
способствует раздражению слизистой оболочки пищевода и желудка, провоцирует хронические патологии. С аналогичной
целью ограничивают потребление солёных и копчёных блюд. Приготовленная на пару и варёная пища легче усваивается
организмом. В жареной пище содержится небольшое количество канцерогенов, которые постепенно накапливаются в теле и
запускают отравление организма. При соблюдении правил правильного питания человек будет испытывать лёгкость, высокую
трудоспособность и станет значительно реже болеть. Важно дополнять правильное питание физической активностью.
Важно дополнять правильное питание физической активностью.
Отказ от вредных привычек
К вредным привычкам относятся такие виды зависимости, как никотиновая и алкогольная, до перерастания последней в стадию алкоголизма. Алкоголизм – самостоятельная патология, имеющая собственный патогенез образования и развития. Отдельной болезнью признаётся наркотическая зависимость. Лечением алкоголизма и наркомании занимается врач-нарколог. Вредные привычки способны вызывать массу патологических явлений в человеческом организме. Оказывают отравляющее воздействие на все органы и ткани с течением времени. Никотин может спровоцировать онкологические процессы в органах. Поражаются: лёгкие; желудок; горло. Употребление табака на пустой желудок спровоцирует появление гастрита.
При переходе указанной патологии в хроническую форму человек включается в группу риска развития рака желудка. При
длительном воздействии этанола на организм происходит отравление системы пищеварения.
Проведение осмотров у врача для раннего диагностирования и лечения онкологического процесса Ключевой фактор,
влияющий на шансы выздоровления при онкологии – время. Опасность явления: при первоначальном появлении онкологии
патология бессимптомна. Болезнь выявляется, находясь в третьей и четвёртой стадии развития. Часто диагностика на
ранних этапах происходит при осуществлении обследования на предмет выявления иных патологических процессов. Наличие
онкологии выдает присутствие в анализах крови онкомаркеров. Применение первичной профилактики позволит избежать
многочисленных проблем со здоровьем, снизит риск появления злокачественного новообразования.
Подробнее о вторичной профилактике рака желудка
Вторичная профилактика включает медицинские процедуры, помогающие устранению имеющихся патологий с целью избежать перерастания их в онкологию. Для достижения максимального эффекта профилактических мер требуется в точности соблюдать клинические рекомендации лечащего врача. С целью профилактики желательно посещать гастроэнтеролога с периодичностью раз в 12 месяцев. Лечение гастрита и язвы желудка Хронические патологические явления занимают первое место среди выделяемых причин появления онкологического процесса. Для применения наиболее эффективных методов воздействия будут проведены соответствующие медицинские диагностические процедуры.
По итогу диагностики назначается лечение. Чаще всего, оно включает приём фармакологических средств, разработанных
для лечения соответствующего вида патологии. Терапевтическое воздействие дополняется специально разработанными
диетами, которые позволяют организму восстановиться от последствий гастрита и язвы.
Для лечения болезни потребуется провести соответствующую диагностику. При незначительных размерах врач удалит полип
ещё при проведении процедуры эндоскопии. При значительных размерах образования потребуется провести резекцию
желудка. Оперативное вмешательство дополняется диетой и фармакологической терапией. Третичная профилактика онкологии
желудка Третичная профилактика – это специальный вид предупредительных мероприятий, который связан с лечением других
видов онкологий желудочно-кишечного тракта. При развитии рака кишечника метастазирование распространяется и на
желудок. Для предотвращения онкологии желудка требуется вовремя выявить, диагностировать и лечить иные виды
онкологии на ранних стадиях развития.
Профилактика рака желудка | Профилактика онкологических заболеваний ЖКТ
ПРОФИЛАКТИЧЕСКАЯ ГАСТРОСКОПИЯ И КОЛОНОСКОПИЯ
Тем, у кого никогда не было заболеваний органов ЖКТ, рекомендуется пройти первую профилактическую эндоскопию в возрасте 50 лет. Но если в вашей семье среди родственников первой линии (мать, отец, бабушки, дедушки) были случаи онкологических заболеваний (рака желудка), то в таком случае для профилактики гастро- и колоноскопию необходимо проходить раз в 10 лет, начиная с 30-ти летнего возраста.
Если у вас присутствует страх перед эндоскопическими исследованиями, рекомендуется обратиться в Региональный центр эндоскопии. Наши специалисты работают на оборудовании экспертного уровня, поэтому вся процедура пройдет максимально комфортно.
Во время гастроскопии эндоскоп вводится через рот пациента и проводится последовательный тщательный осмотр ротоглотки, пищевода, желудка и двенадцатиперстной кишки. Обследование направлено на профилактику и обнаружение на ранних стадиях рака органов верхних отделов ЖКТ. При колоноскопии эндоскоп вводится в анальное отверстие и последовательно осматриваются все отделы толстой кишки и часть тонкой кишки. Своевременная профилактическая колоноскопия поможет выявить злокачественные новообразования в кишечнике. Специалисты нашей клиники проходили обучение в ведущих зарубежных клиниках по эндоскопии в Японии, Австрии и Германии. Полученный опыт позволяет докторам Регионального центра эндоскопии обнаружить рак пищевода, желудка и толстой кишки на ранней стадии, дать рекомендации по профилактике. Также наши врачи успешно делятся своими знаниями и занимаются преподаванием учебных курсов по эндоскопии как российским врачам, так и специалистам из стран Европы.
При колоноскопии эндоскоп вводится в анальное отверстие и последовательно осматриваются все отделы толстой кишки и часть тонкой кишки. Своевременная профилактическая колоноскопия поможет выявить злокачественные новообразования в кишечнике. Специалисты нашей клиники проходили обучение в ведущих зарубежных клиниках по эндоскопии в Японии, Австрии и Германии. Полученный опыт позволяет докторам Регионального центра эндоскопии обнаружить рак пищевода, желудка и толстой кишки на ранней стадии, дать рекомендации по профилактике. Также наши врачи успешно делятся своими знаниями и занимаются преподаванием учебных курсов по эндоскопии как российским врачам, так и специалистам из стран Европы.
Большую часть выявленных новообразований можно удалить прямо во время проведения диагностического исследования. Врачи полностью удалят неоплазия и направят биоматериал в патоморфологическую лабораторию. Опытный эндоскопист с помощью глубоких знаний и современной аппаратуры может определить природу того или иного новообразования в процессе визуального осмотра.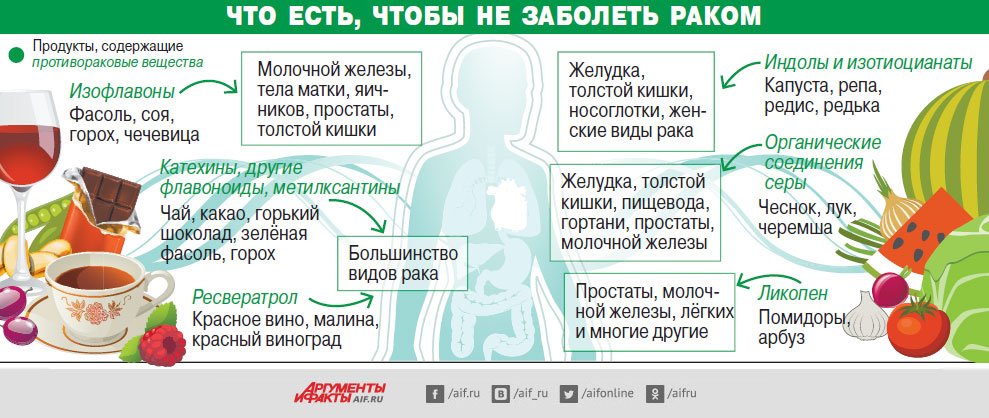 Но для окончательной постановки диагноза «онкология ЖКТ» необходимо провести биопсию и гистологическое исследование биоматериала.
Но для окончательной постановки диагноза «онкология ЖКТ» необходимо провести биопсию и гистологическое исследование биоматериала.
Подробнее…
Памятка – рак желудка
Категория: Онкология.
Во время процедуры специальный зонд, имеющий световод, вводится в желудок, врач осматривает все его отделы, а также двенадцатиперстную кишку.
Доктор может взять на анализ желудочный сок или кусочки ткани слизистой. Больным, имеющим повышенный онкологический риск по раку желудка, рекомендуется проходить ФГС один – два раза в год.
В целях профилактики появления рака желудка нужно соблюдать общие правила гигиены, исключить по возможности стрессовые ситуации, которые могут привести к язве ЖКТ. Необходимо уменьшить влияние вредных факторов окружающей среды (промышленные отходы, автомобильные выхлопные газы). Следует обязательно укреплять иммунитет, с этой целью будут полезны занятия физкультурой, ежедневные прогулки, закаливающие процедуры.
Онкопрофилактическая диета
В целях профилактики рака желудка нужно соблюдать специальную диету. В рацион требуется включать фрукты, овощи, зелень и коренья. В свежих фруктах и овощах присутствуют противораковые элементы, которые не только могут защищать желудок от развития опухолей, но и действовать на болезнь как химические лекарственные препараты (при отсутствии токсичности).
Риск заболеть раком уменьшится, если ежедневно употреблять 200 – 250 мл молока. Хорошим средством профилактики злокачественных новообразований в желудке являются томаты. Рекомендуется ежедневно съедать по два – три спелых красных помидора. Они содержат антиоксиданты, способные стимулировать иммунитет.
Мощным антиоксидантом, препятствующим появлению онкологических болезней, является витамин Е. Много его содержится в растительном масле, орехах. В целях профилактики рака желудка нужно ежедневно есть 150 орехов или употреблять не менее 2-3 столовых ложек любого растительного масла. В онкопрофилактическую диету должны входить корень сельдерея, хрен, редька, редис. В их составе присутствуют индол и изотиоцианат – мощные антиканцерогенные вещества. Ежедневно рекомендуется съедать по 50 граммов этих корнеплодов.
В онкопрофилактическую диету должны входить корень сельдерея, хрен, редька, редис. В их составе присутствуют индол и изотиоцианат – мощные антиканцерогенные вещества. Ежедневно рекомендуется съедать по 50 граммов этих корнеплодов.
В качестве профилактики рака желудка нужно употреблять одну луковицу в день. В луке содержится кверцетин, он препятствует образованию раковых клеток. Следует включать в рацион жирные сорта рыбы (лосось, тунец, сардина, сельдь, скумбрия, макрель), в них содержится большое количество омега -3 – жирных кислот, которые повышают противоопухолевый иммунитет. Замечательным средством профилактики рака желудка считается зеленый чай. Этот напиток нужно пить ежедневно.
Профилактика появления рака желудка предусматривает действия, направленные на предупреждение появления хронических заболеваний желудочно – кишечного тракта. На протяжении жизни необходимо соблюдать общие правила санитарно – гигиенического режима, правильно питаться, по возможности исключить появление стрессовых ситуаций, которые могут привести к появлению язвы желудка.
Предотвращение появления таких предраковых заболеваний, как пернициозная анемия, хроническая язва желудка и двенадцатиперстной кишки имеют исключительное значение в профилактических мероприятиях, направленных на недопущение развития злокачественных новообразований этих органов.
Уменьшение влияния вредных факторов окружающей среды, таких как автомобильные выхлопные газы, промышленные отходы.
Нитраты, нитриты, в большом количестве содержащиеся в тепличных растениях (помидоры, огурцы), копченостях, также необходимо ограничить в питании, так как данные продукты являются опасным и с точки зрения канцерогенного влияния на организм.
Соблюдать умеренность в применении различных медикаментозных средств.
Свежие фрукты и овощи, богатые витаминами, макро и микроэлементами, сбалансируют рацион питания. также свежие овощи и фрукты служат хорошим источником антиоксидантов, которые эффективны в борьбе против появления раковых клеток.
Каждодневные вечерние прогулки, занятия физической культурой и закаливающие процедуры, все это укрепит иммунитет, придаст бодрости и дополнительных жизненных сил.
Рак желудка – один из самых опасных видов злокачественных опухолей. Зачастую он выявляется лишь на поздних стадиях и приводит к высокой смертности. После радикальной операции пятилетняя выживаемость больных раком желудка около 40%. Но большинству пациентов адекватное лечение провести не удается. Из-за этого не более 12 % всех заболевших переживут пяти летний рубеж. Поэтому профилактика рака желудка сего дня очень актуальна.
На протяжении последних десятилетий заболеваемость раком желудка неуклонно падает. Связывают это с улучшением питания и широким использованием холодильников для хранения продуктов. Но в нашей стране рак желудка – массовое явление. Заболеваемость у мужчин выше, чем у женщин.
Факторы риска развития рака желудка
- низкий уровень жизни;
- плохое питание;
- злоупотребление нитратами, солью, консервированными продуктами, крепкими спиртными напитками;
- недостаточное потребление белков, овощ ей, фруктов, витаминов;
- полипы, язва желудка, низкая кислотность желудочного сока;
- хеликобактериоз;
-
очень редко – врожденные генетические нарушения (семейный рак желудка).

Предопухолевые процессы
Предраковым заболеванием считается хронический атрофический гастрит. Он вызывает уменьшение желез слизистой, угнетение функций желудка, ослабление выработки пищеварительных ферментов и соляной кислоты. Сначала клетки слизистой желудка теряют обычный вид и становятся похожими на клетки кишечника. Это так называемая кишечная метаплазия. В дальнейшем возникает дисплазия (неправильное развитие). Вот характерная последовательность изменения клеток слизистой желудка: атрофия – кишечная метаплазия – дисплазия – рак.
Хронический атрофический гастрит не имеет яркой клинической картины. Человека беспокоят неприятные ощущения после еды – ноющие тупые боли в подложечной области, тяжесть в желудке, тошнота, отрыжка, иногда с тухлым запахом. Могут быть нарушения стула (поносы или запоры), повышенное газообразование.
Хеликобактериоз
Многие исследования показали, что заражение хеликобактером (Helicobacter pylori) повышает риск рака желудка в 2-4 раза. Инфицированность населения составляет около 40 %. Заразиться можно через грязные руки, загрязненные продукты, во время поцелуев. Профилактика заражения проста: мыть перед едой руки с мылом, обдавать кипятком фрукты, овощи, а также не целоваться с больными людьми.
Инфицированность населения составляет около 40 %. Заразиться можно через грязные руки, загрязненные продукты, во время поцелуев. Профилактика заражения проста: мыть перед едой руки с мылом, обдавать кипятком фрукты, овощи, а также не целоваться с больными людьми.
Как же бактерия противостоит воздействию соляной кислоты желудочного сока и не погибает? Выжить помогает особый фермент, уреаза – она расщепляет мочевину из содержимого желудка. В результате вокруг бактерии образуется облачко аммиака, который нейтрализует кислоту и дает возможность продержаться несколько часов. За это время бактерия ввинчивается в выстилку желудка при помощи спиральных жгутиков, удаляется от поверхности. Там бактерия может жить десятилетиями. Она медленно размножается, постепенно разрушает слизистую оболочку желудка и способствует развитию гастрита, язвы и рака желудка. Излечение хеликобактериоза улучшает состояние слизистой.
Кроме того, Helicobacter pylori является главной причиной злокачественной опухоли, развивающейся из скоплений лимфоидной ткани в слизистой – В-клеточной лимфомы желудка. Удивительно, что излечение хеликобактериоза приводит к полной регрессии лимфомы желудка и выздоровлению.
Удивительно, что излечение хеликобактериоза приводит к полной регрессии лимфомы желудка и выздоровлению.
Разработаны надежные методы диагностики хеликобактериоза и схемы его эффективного лечения при помощи антибиотиков. Если obacter pylori обнаружена у одного члена семьи, то, как правило, заражены все остальные. Поэтому необходимо лечение всей семьи. К сожалению, инфекция часто рецидивирует. Поэтому необходимо периодически обследоваться и после лечения. Наилучшей первичной профилактикой рака желудка является правильное питание и соблюдение онкопрофилактической диеты. Очень важно своевременное выявление и лечение хронического атрофического гастрита, язвы, полипов, хеликобактериоза.
В настоящее время, существует возможность следить за состоянием желудка с помощью фиброгастроскопии (ФГС). Специальный зонд со световодом вводится в желудок. Во время процедуры врач может осмотреть все отделы желудка и двенадцатиперстную кишку, взять для анализов желудочный сок и кусочки ткани слизистой и даже удалить полипы желудка, не прибегая к полостной операции. ФГС безопасна и безвредна. Больным с повышенным онкологическим риском по раку желудка рекомендуется проходить фиброгастроскопию 1-2 раза в год. Регулярная ФГС позволяет своевременно выявить злокачественную опухоль и провести лечение.
ФГС безопасна и безвредна. Больным с повышенным онкологическим риском по раку желудка рекомендуется проходить фиброгастроскопию 1-2 раза в год. Регулярная ФГС позволяет своевременно выявить злокачественную опухоль и провести лечение.
Следует внимательно относиться к своему состоянию. В зависимости от расположения и вида опухоли, проявления болезни могут быть самые разные:
- кровотечение, черный стул;
- боли в подложечной области;
- чувство тяжести, распирания в подложечной области после еды, отрыжка, тошнота и рвота;
- нарушение глотания, чувство помех и при прохождении твердой пищи;
- потеря аппетита, отвращение к ранее любимой пище, например к мясу, общая слабость, потеря веса.
Если у вас появились какие – либо из перечисленных симптомов, необходимо срочно обратиться к онкологу и пройти обследование.
Профилактика заболеваний
Профилактика Онкологических заболеваний.

Рак желудка – профилактика
Профилактика опухолей желудка
Профилактика рака желудка состоит в максимальном исключении влияния нижеперечисленных причин.
Очень важно всем пациентам с атрофическим гастритом, язвой желудка, полипами желудка, а также пациентам, имеющим родственников, страдающих раком желудка, ежегодно проходить гастроскопию.
Меры по профилактике:
– Снижение употребления в пищу соленых, копченых, вяленых продуктов, нитратов и введение в питание овощей, фруктов, продуктов с повышенным содержанием клетчатки. Полноценное питание с достаточным включением животных и растительных белков;
– Категорический отказ от курения и употребления алкогольных напитков;
– Регулярное наблюдение и своевременное лечение предраковых состояний – полипоза желудка, хронического гастрита и хронической язвы желудка;
– Регулярное обследование лиц, относящихся к группе риска по раку желудка – с отягощенной наследственностью, врожденным полипозом кишечника, лица, прибывшие из районов с повышенным уровнем заболеваемости раком желудка;
– После 45-50 лет любому человеку полезно 1 раз в год профилактически обследовать желудок даже при отсутствии жалоб, так заболеваемость раком желудка значительно возрастает, начиная с этого возраста.
Врач-гастроэнтеролог или онколог более точно определит необходимость обследования в каждом конкретном случае и даст рекомендации по профилактике рака желудка.
Причин, вызывающих рак желудка, очень много. Некоторые из них изучены очень хорошо, роль других активно исследуется. К ним относятся и особенности питания, и хронические заболевания желудка и пищевода, и вредные привычки, и наследственная предрасположенность, и перенесенные в прошлом операции на желудке. Рак желудка редко возникает «из ничего», то есть на не измененной стенке желудка. Чаще его возникновению предшествуют хронические изменения стенки желудка.
Профилактика рака пищевода
1. Здоровый образ жизни
o Отказ от курения
o Ограничение приема крепких спиртных напитков
o Избегать потребления чрезмерно горячей пищи и напитков
o Снижение избыточного веса
2. Своевременное выявление предраковых заболеваний, их лечение и регулярное профилактическое обследование
o Гастроэзофагеальная рефлюксная болезнь (заброс желудочного содержимого в пищевод)
o Пищевод Барретта
o Ахалазия пищевода
o Рубцовая стриктура
Рак пищевода – крайне серьезное, но не фатальное заболевание, его можно и нужно лечить! Успех лечения напрямую зависит от своевременного обращения пациента и раннего выявления заболевания. Чем, раньше будет установлен диагноз, тем, эффективнее окажется лечение и лучше прогноз заболевания!
Чем, раньше будет установлен диагноз, тем, эффективнее окажется лечение и лучше прогноз заболевания!
Что такое рак пищевода?
Рак пищевода – это злокачественная опухоль, развивающаяся из клеток, покрывающих слизистую оболочку пищевода.
Выделяют два наиболее частых типа злокачественных опухолей пищевода в зависимости от типа клеток, из которых они развиваются:
· плоскоклеточный рак пищевода: опухоль, развивающаяся из клеток плоского эпителия, покрывающего пищевод. Это самая частая форма рака пищевода. Плоскоклеточный рак чаще встречается в верхнем и среднем отделах пищевода.
· аденокарцинома пищевода: опухоль, развивающаяся из железистых (секреторных) клеток, источником которых могут быть железы пищевода или измененная в результате заброса желудочного сока слизистая нижней части пищевода (пищевод Барретта). Аденокарциномы обычно развиваются в нижней части пищевода на границе с желудком.
Мужчины заболевают раком пищевода в 3,5 раза чаще женщин (в России). Пик заболеваемости приходится на возраст 50-59 лет. В нашей стране ежегодно выявляют более 7 тыс. новых случаев рака пищевода.
Пик заболеваемости приходится на возраст 50-59 лет. В нашей стране ежегодно выявляют более 7 тыс. новых случаев рака пищевода.
Рак пищевода, как и другие злокачественные опухоли, обладает способностью прорастать в прилежащие органы и давать метастазы – отсевы опухоли в результате распространения опухолевых клеток с током лимфы и крови. В отсутствие лечения опухоль может достигать больших размеров и прорастать в соседние органы: трахею, бронхи, перикард (сердечную сумку), аорту. Метастазирование рака пищевода по лимфатическим путям приводит к появлению метастазов в лимфатических узлах на шее, в надключичной области, в грудной полости и верхних отделах живота. Распространение опухолевых клеток с током крови (гематогенное метастазирование) проявляется отдаленными метастазами в различных органах-мишенях – легких, печени, надпочечниках, костях.
Причины возникновения рака пищевода
В развитии рака пищевода ведущую роль играет хроническое воспаление слизистой оболочки в результате механического, термического или химического раздра¬жения.
К основным факторам риска рака пищевода относят:
· курение табака
· злоупотребление крепкими спиртными напитками
· химический ожог пищевода (уксусная кислота, щелочи)
· хронический заброс желудочного содержимого в пищевод (гастроэзофагеальная рефлюксная болезнь)
· Предраковые заболевания:
o пищевод Барретта – состояние, при котором клетки плоского эпителия слизистой оболочки пищевода замещаются клетками кишечного типа. Обычно это происходит в результате длительного заброса желудочного сока и желчи в пищевод (врожденный короткий пищевод, грыжа пищеводного отверстия диафрагмы, недостаточность мышечного клапана между пищеводом и желудком – нижнего пищеводного сфинктера).
o Ахалазия пищевода – нервно-мышечное заболевание, при котором нарушается моторика стенок пищевода и способность нижнего пищеводного сфинктера расслабляться при глотании. В результате пища подолгу задерживается в расширенном пищеводе, не проходя в желудок.
o Рубцовая стриктура – рубцовое сужение пищевода после перенесенного химического ожога или в результате хронического воспаления
· частое употребление очень горячей пищи и напитков (термический ожог)
· ожирение
· пожилой возраст
· мужской пол
Клинические проявления рака пищевода
Основным проявлением рака пищевода является постепенно нарастающая дисфагия (затрудненное прохождение пищи по пищеводу). Вначале пациенты отмечают задержку при приеме грубой и сухой пищи и вынуждены запивать ее жидкостью, в дальнейшем нарушается прохождение кашицеобразной пищи и, наконец, приходит момент, когда больной не в состоянии проглотить даже воду.
Другие симптомы, на которые следует обратить внимание
· боли при глотании
· боли за грудиной или между лопатками
· похудание
· осиплость голоса
· поперхивание и кашель при приеме пищи
· изжога
· появление увеличенных лимфатических узлов в надключичной области или на шее
Вышеописанные симптомы могут быть не связаны с раком пищевода, однако, при возникновении любого из них необходимо незамедлительно обратиться к врачу!
ПРОФИЛАКТИКА РАКА РОТОВОЙ ПОЛОСТИ
Все наслышаны о серьезности раковых заболеваний, но не все знают, что даже соблюдение простых профилактических мероприятий позволит предостеречь развитие этих серьезных заболеваний.
Что же для этого нужно? Надо устранить все раздражающие, вредные воздействия на слизистую рта, строго соблюдать гигиену ротовой полости, включая надлежащее лечение уже возникших предраковых заболеваний. Если на слизистой оболочке щек, деснах, языке появляются изъязвления, особенно расположенные около острых краев или близ разрушенных зубов, следует сгладить острые края или удалить разрушенные зубы. Коронки или протезы, травмирующие слизистую оболочку, должны быть немедленно сняты. Если где-либо и после этого язвы не заживают, необходима срочная консультация в онкологическом диспансере.
Отказ от курения — профилактика различных нарушений: ороговения красной каймы губ и слизистой оболочки полости рта, в частности лейкоплакий и лейкокератозов. Надо остерегаться вредного воздействия солнечных лучей, холодного или горячего воздуха на красную кайму губ. В целях защиты губ от этих нежелательных воздействий рекомендуется смазывать их ланолином или каким-либо нейтральным маслом. Надо избегать различных раздражающих пищевых веществ.
Надо избегать различных раздражающих пищевых веществ.
При каких-либо изменениях в слизистой оболочке ротовой полости и языке нужно тщательно обследовать пищеварительный тракт; при выявлении заболевания желудка и кишечника надо устранить причины, их вызывающие, и провести надлежащее лечение. Показана пища, богатая разными витаминами, особенно витаминами комплекса В.
Успех в лечении предраковых заболеваний может быть достигнут при своевременном — в самые ранние стадии болезни — обращении за специальной медицинской помощью. Медицина располагает большими возможностями распознавания предраковых состояний, их правильной ранней диагностики и лечения. Здоровые зубы украшают лицо человека. Отсутствие зубов — не только косметический недостаток, оно отрицательно влияет на общее состояние организма человека. Усвоение пищи зависит от хорошего ее пережевывания. Плохое пережевывание обусловливает заболевания желудка и кишечника. При отсутствии даже отдельных зубов увеличивается нагрузка на сохранившиеся, и они начинают быстрее разрушаться. При малейшем повреждении, нарушении целостности эмали, появлении темных точек на поверхности зубов, намечающихся или уже сформировавшихся полостях на жевательной, боковых, пришеечных частях зуба надо немедленно обратиться к врачу.
При малейшем повреждении, нарушении целостности эмали, появлении темных точек на поверхности зубов, намечающихся или уже сформировавшихся полостях на жевательной, боковых, пришеечных частях зуба надо немедленно обратиться к врачу.
Состояние зубов в значительной степени зависит от общего состояния организма, вот почему закаливание, занятия физической культурой, соблюдение режима питания, труда и отдыха способствуют сохранению зубов здоровыми.
Рак полости рта в значительной степени может быть предотвращен. Меры профилактики следующие: раз в несколько месяцев осматривайте свой рот и губы на предмет наличия болячек, чешуек, уплотнений или изменений цвета. Запрокиньте голову, чтобы осмотреть твердое и мягкое нёбо. Возьмите язык марлей или тканью и осмотрите всю его поверхность. Посмотрите, нет ли белых, красных и темных пятен на внутренней поверхности щек и губ. Легким надавливанием проверьте, не болит ли что, нет ли маленьких опухолей. Обратите внимание на области вокруг ушей и на лимфатические железы на шее, бросьте табак. Существует непосредственная связь между раком ротовой полости и курением. Смертность от рака ротовой полости выше у курильщиков по сравнению с некурящими в четыре раза. Рак ротовой полости также непосредственно связан с курением трубки или сигар — здесь болезнетворным фактором может оказаться тепло, выделяемое при горении табака; жевание табака или нюхание табака также опасны. Это приводит к непосредственному контакту смол с тканями полости рта; регулярно посещайте стоматолога. Он может заметить развитие рака. Хронические раздражения, такие, например, как вызываемые зазубринами, выступающими пломбами или плохо, сидящими зубными протезами, должны быть немедленно исправлены. Такого рода раздражения могут привести к образованию злокачественной опухоли; У фермеров, и других людей, работающих на открытом воздухе, воздействие солнечного света на протяжении многих лет иногда приводит к развитию рака губы, так же как и развитию рака кожи. Воздействие ветра и мороза также может стать способствующим фактором; сократите потребление алкоголя.
Существует непосредственная связь между раком ротовой полости и курением. Смертность от рака ротовой полости выше у курильщиков по сравнению с некурящими в четыре раза. Рак ротовой полости также непосредственно связан с курением трубки или сигар — здесь болезнетворным фактором может оказаться тепло, выделяемое при горении табака; жевание табака или нюхание табака также опасны. Это приводит к непосредственному контакту смол с тканями полости рта; регулярно посещайте стоматолога. Он может заметить развитие рака. Хронические раздражения, такие, например, как вызываемые зазубринами, выступающими пломбами или плохо, сидящими зубными протезами, должны быть немедленно исправлены. Такого рода раздражения могут привести к образованию злокачественной опухоли; У фермеров, и других людей, работающих на открытом воздухе, воздействие солнечного света на протяжении многих лет иногда приводит к развитию рака губы, так же как и развитию рака кожи. Воздействие ветра и мороза также может стать способствующим фактором; сократите потребление алкоголя. Злоупотребление алкоголем в сочетании с табаком или без оного — существенный фактор в развитии рака ротовой полости; тщательно соблюдайте правила гигиены полости рта.
Злоупотребление алкоголем в сочетании с табаком или без оного — существенный фактор в развитии рака ротовой полости; тщательно соблюдайте правила гигиены полости рта.
Лейкоплакия полости рта — нераковое состояние, имеющее тенденцию перерастать в злокачественное; оно часто возникает из-за неправильного ухода за зубами. Лейкоплакия – это состояние, при котором на границе губ, языка или ротовой полости образуется безболезненное утолщенное пятно из клеток (напоминающее кусочек сырой бумаги). Если возникает лейкоплакия, следует регулярно проводить биопсию и. медицинские осмотры.
Хорошо питайтесь.
Информационные листовки по профилактике онкологических заболеваний.
Профилактика онкологических заболеваний
|
Совместная борьба с онкологией Рак на протяжении многих лет является второй по значимости причиной смертности в России. |
Природа рака сложная, по этой причине мировая медицинская наука до сих пор не определила все причины, которые приводят человека к онкологическим заболеваниям. Но накопленный огромный опыт позволяет специалистам эффективно лечить многие виды рака.
Во всем мире с онкологией борются исходя из принципа «болезнь легче предупредить, чем лечить». Как показывают научные исследования, наряду с наследственной предрасположенностью, появление рака провоцируют образ жизни человека, стрессы и экология.
К сожалению, пока большинство людей снисходительно относятся к рекомендациям врачей вести здоровый образ жизни. Между тем, это очень важно! Вы должны понять сами и донести до близких, что здоровый образ жизни помогает организму поставить барьер для многих видов онкологических заболеваний. Наверное, для некоторых, в силу имеющихся привычек, будет трудно отказаться от курения, злоупотребления алкоголем, но это надо сделать ради здоровья. Кроме того, нельзя переедать. Надо принимать здоровую, богатую белками, углеводами, жирами и микроэлементами пищу. Следует регулярно, лучше ежедневно, включать в рацион фрукты и овощи. Необходимо больше времени проводить на свежем воздухе, занимаясь физкультурой, например, рано утром или вечером ходить в среднем темпе не менее 45 минут. Надо научиться защищать себя от отрицательных эмоций. Кому-то в этом может помочь чтение книг, просмотр фильмов, посещение концертов и спектаклей, общение с близкими людьми. Надеюсь, что эти рекомендации вы не отложите на послезавтра, а начнете применять уже сегодня.
Наверное, для некоторых, в силу имеющихся привычек, будет трудно отказаться от курения, злоупотребления алкоголем, но это надо сделать ради здоровья. Кроме того, нельзя переедать. Надо принимать здоровую, богатую белками, углеводами, жирами и микроэлементами пищу. Следует регулярно, лучше ежедневно, включать в рацион фрукты и овощи. Необходимо больше времени проводить на свежем воздухе, занимаясь физкультурой, например, рано утром или вечером ходить в среднем темпе не менее 45 минут. Надо научиться защищать себя от отрицательных эмоций. Кому-то в этом может помочь чтение книг, просмотр фильмов, посещение концертов и спектаклей, общение с близкими людьми. Надеюсь, что эти рекомендации вы не отложите на послезавтра, а начнете применять уже сегодня.
Чтобы вам было понятно, что рак это ни нечто далекое и вас не касающиеся, приведу несколько цифр медицинской статистики. В Димитровграде проживает порядка 120 тысяч человек. Так вот ежегодно в нашей стране от онкологических заболеваний умирает почти 300 тысяч человек. Представили масштаб проблемы?
Представили масштаб проблемы?
В прошлом году в Димитровграде от разных форм рака умерли 200 горожан. Сейчас на учете в первичном онкологическом отделении находится 3104 человека.
Что же, помимо здорового образа жизни, можно противопоставить раку? К счастью, в настоящее время современные методы лечения позволяют значительно продлить жизнь пациенту, а в некоторых случаях и победить болезнь. Эффект лечения напрямую зависит от времени выявления онкологии. Чем раньше обнаружат рак, тем выше шансы на успех лечения!
В связи с этим большую роль играют регулярные медицинские осмотры и диагностические исследования. И на этом этапе мы снова вынуждены говорить об ответственности человека к своему здоровью, к его готовности систематически, в профилактических целях, посещать врача. Кстати, в 2015 году у 54 горожан онкологические заболевания выявили во время профессиональных медицинских осмотров.
Так, женщинам рекомендую ежемесячно проводить самообследование молочных желез. Они должны регулярно посещать гинеколога, терапевта, дерматовенеролога, раз в год проходить ультразвуковое обследование молочных желез. Также после 40 лет женщины должны раз в два года делать маммографию. При показаниях чаще – раз в год.
Они должны регулярно посещать гинеколога, терапевта, дерматовенеролога, раз в год проходить ультразвуковое обследование молочных желез. Также после 40 лет женщины должны раз в два года делать маммографию. При показаниях чаще – раз в год.
Регулярные медицинские обследования необходимы и мужчинам, которые, к сожалению, к своему здоровью, за редким исключением, относятся достаточно легкомысленно.
Вы должны быть внимательные к себе. Например, вас должно насторожить изменение при мочеиспускании и дефекации, длительно незаживающая рана, необычные кровотечения или выделения, утолщение или уплотнение в молочной железе и не только, расстройства желудка и затруднение глотания, явные изменения родинки или бородавки, надсадный кашель или охрипший голос. В таких случаях надо обращаться к специалистам – участковым терапевтам, гинекологам. После необходимых минимальных обследований, которые они вам назначат, исходя из результатов анализов, человека направят к узкому специалисту.
Еще несколько слов о визите к доктору. Вы должны знать, что все врачи первичного амбулаторно-поликлинического звена (участковые врачи-терапевты) и узкие специалисты обязаны при выявлении у пациента подозрения на онкологическое заболевание, направлять его на дополнительные виды исследований и консультаций, в том числе в первичное онкологическое отделение клинической больницы. Записаться на прием к врачу-онкологу можно в окне регистратуры и по телефону. Также существует электронная запись по направлению врачей-специалистов.
Вы должны знать, что все врачи первичного амбулаторно-поликлинического звена (участковые врачи-терапевты) и узкие специалисты обязаны при выявлении у пациента подозрения на онкологическое заболевание, направлять его на дополнительные виды исследований и консультаций, в том числе в первичное онкологическое отделение клинической больницы. Записаться на прием к врачу-онкологу можно в окне регистратуры и по телефону. Также существует электронная запись по направлению врачей-специалистов.
Сейчас в первичном онкологическом отделении четыре ставки врача-онколога, что позволяет организовать работу поликлиники в две смены. Поэтому срок ожидания консультации у врача-специалиста не более трех дней. К слову, в 2014-2015 годах на работу приняли двух врачей-онкологов. Кроме того, в настоящее время в первичном онкологическом отделении проходят практику два клинических ординатора по специальности «онкология» с последующим трудоустройством в Клинической больнице №172 ФМБА России.
Первичное онкологическое отделение оснащено необходимым медицинским оборудованием. В клинико-диагностической лаборатории проводятся исследования крови на онкомаркеры.
В клинико-диагностической лаборатории проводятся исследования крови на онкомаркеры.
Для повышения ранней диагностики онкологических заболеваний в клинической больнице стали чаще проводить разные виды скринингов – онкоцитологию (обследование, направленное на ранее выявление рака шейки матки), ПСА (выявление рака предстательной железы), маммографию (выявление рака молочной железы).
В 2014 году в многопрофильном стационаре №1 открыли кабинет колоноскопии, что расширило перечень эндоскопических обследований пациентов, в данном случае самого достоверного метода диагностики рака толстой кишки.
Также в МПС №1, только в 2015 году открыли кабинет бронхоскопии для ранней диагностики бронхолегочной патологии.
В поликлинике для взрослых №2 с 2014 года функционирует смотровой кабинет для мужчин города Димитровграда. В нем проводят профилактические осмотры мужчин от 30 лет и старше. Цель его работы – ранее выявление злокачественных опухолей и предопухолевых заболеваний визуальной локализаций (кожные покровы, губы, органы полости рта, щитовидная железа, периферические лимфатические узлы, наружные половые органы, прямая кишка). В этом кабинете в 2015 году у трех пациентов выявили злокачественные новообразования.
В этом кабинете в 2015 году у трех пациентов выявили злокачественные новообразования.
Кроме того, в 2014 году в первичном онкологическом отделении, в рамках политики по внедрению новых скрининговых методов исследования для ранней диагностики рака, открыли кабинет тонкоигольной пункционной биопсии под контролем УЗИ.
В первичном онкологическом отделении и поликлинике для взрослых №3 функционируют маммографические кабинеты. В подразделениях клинической больницы работают рентгеновские кабинеты и флюорографические аппараты.
Новые возможности для ранней диагностики заболеваний, в том числе онкологических, появились у специалистов клинической больницы с вводом в эксплуатацию 64-срезового мультиспиральногокомпьютерного томографа. Современная японская техника позволяет получить четкое послойное изображение (срез) любой области человека толщиной менее миллиметра и больше, помогает специалистам оценить состояние исследуемых органов и тканей, локализацию и распространенность патологического процесса, в частности злокачественных новообразований легких и других органов.
Работа по улучшению диагностических возможностей клинической больницы будет продолжена. Так, например, в 2016 году планируется (после приобретения инструментария) проводить биопсию предстательной железы под контролем УЗИ.
Настороженность населения к здоровью, расширение диагностических возможностей клинической больницы, позволили медицинским работникам увеличить процент раннего выявления рака. Наблюдается снижение онкологических заболеваний (402 против 466 в 2014 году) и смертности (200 против 222 годом ранее).
В 2015 году были поставлены на учет 402 пациента. Среди впервые выявленных больных с онкологическими диагнозами на первом месте рак кожи (74 случая), на втором месте – рак молочной железы (61), на третьем – легких (36).
Учитывая тяжесть заболевания, клиническая больница старается, чтобы онкологические пациенты могли получать необходимую медицинскую помощь в Димитровграде. Сейчас в хирургическом отделении МПС №1 развернуты койки для хирургического и химиотерапевтического лечения онкологических больных. В 2015 году в этом подразделении появились койки паллиативной помощи, финансируемые из федерального бюджета. Но, к сожалению, часть больных, в силу медицинских показаний, приходится направлять в Ульяновск – на консилиум специалистов: врача-онколога, врача-радиолога и химиотерапевта, чтобы они определили тактику лечения пациента, как в условиях стационара в региональном центре, так и по месту жительства.
В 2015 году в этом подразделении появились койки паллиативной помощи, финансируемые из федерального бюджета. Но, к сожалению, часть больных, в силу медицинских показаний, приходится направлять в Ульяновск – на консилиум специалистов: врача-онколога, врача-радиолога и химиотерапевта, чтобы они определили тактику лечения пациента, как в условиях стационара в региональном центре, так и по месту жительства.
Помимо этого, клиническая больница по медицинским показаниям направляет больных горожан в специализированные онкологические диспансеры и специализированные федеральные клиники и больницы, в первую очередь в медицинские организации ФМБА России. Так, в 2015 году высокотехнологичную медицинскую помощь в Москве получили 92 жителя Димитровграда.
Надеюсь, что представленная информация поможет читателям в профилактике рака.
Будьте здоровы!
Профилактика рака: Особенности питания
Питание играет важную роль в этиологии злокачественных опухолей. Известно, что заболеваемость и смертность от злокачественных опухолей значительно варьирует в различных географических регионах. Например, заболеваемость раком желудка очень высока в Японии, Корее, Китае и низка в Северной Америке. В то же время заболеваемость злокачественными опухолями толстой кишки, молочной железы, простаты низка в странах Юго-Восточной Азии и высока в Северной Америке и Западной Европе.
Известно, что заболеваемость и смертность от злокачественных опухолей значительно варьирует в различных географических регионах. Например, заболеваемость раком желудка очень высока в Японии, Корее, Китае и низка в Северной Америке. В то же время заболеваемость злокачественными опухолями толстой кишки, молочной железы, простаты низка в странах Юго-Восточной Азии и высока в Северной Америке и Западной Европе.
Исследования мигрантов из стран Юго-Восточной Азии в США показали, что у японцев и китайцев, проживающих в США, уже в первом поколении снизилась заболеваемость раком желудка и выросла заболеваемость раком толстой кишки.
Исследования мигрантов позволили предположить, что географическая вариабельность в заболеваемости злокачественными опухолями обусловлена некими факторами окружающей среды и образа жизни, а не популяционными генетическими особенностями. Поэтому была сформулирована гипотеза о роли питания в. этиологии злокачественных опухолей. Наблюдения за некоторыми религиозными группами, в частности, адвентистами Седьмого Дня, которые придерживаются особой диеты, не включающей в себя мясных продуктов, показало, что у них заболеваемость раком толстой кишки, молочной железы, тела матки и простаты значительно ниже, чем у остального населения, проживающего рядом с ними.
Наблюдения за некоторыми религиозными группами, в частности, адвентистами Седьмого Дня, которые придерживаются особой диеты, не включающей в себя мясных продуктов, показало, что у них заболеваемость раком толстой кишки, молочной железы, тела матки и простаты значительно ниже, чем у остального населения, проживающего рядом с ними.
Связь между особенностями питания и заболеваемостью злокачественными опухолями была впервые показана в корреляционных исследованиях. Было выявлено, что потребление жиров (особенно животных), мяса и молока на душу населения и количество потребляемых калорий положительно коррелирует с заболеваемостью раком толстой кишки, молочной железы, матки и простаты.
Экспериментальные исследования показали, что ограничение потребления калорий, а также насыщенных жиров животного происхождения ингибирует процесс канцерогенеза, индуцированный химическими канцерогенными веществами. В некоторых экспериментальных исследованиях снижение потребления жиров без соответствующего снижения потребляемых калорий также приводило к снижению количества индуцированных опухолей и удлинению латентного периода их развития, т. е. ингибированию процесса канцерогенеза. Ингибирование процесса канцерогенеза, индуцированного химическими канцерогенными веществами, в результате ограничения потребления энергии и животных жиров было отмечено для злокачественных опухолей молочной железы и толстой кишки, а также легкого, кожи и некоторых неэпителиальных опухолей. Необходимо отметить, что как в эксперименте, так и в эпидемиологических исследованиях очень трудно полностью разграничить влияние потребления калорий от потребления жиров, т.к. животный жир является наиболее энергоемким компонентом питания и основным источником калорий.
е. ингибированию процесса канцерогенеза. Ингибирование процесса канцерогенеза, индуцированного химическими канцерогенными веществами, в результате ограничения потребления энергии и животных жиров было отмечено для злокачественных опухолей молочной железы и толстой кишки, а также легкого, кожи и некоторых неэпителиальных опухолей. Необходимо отметить, что как в эксперименте, так и в эпидемиологических исследованиях очень трудно полностью разграничить влияние потребления калорий от потребления жиров, т.к. животный жир является наиболее энергоемким компонентом питания и основным источником калорий.
Механизм ингибирования опухолевого роста, связанный с ограничением потребляемых калорий, можно объяснить снижением пролиферации клеток и стимулированием апоптоза, усилением репарации ДНК, снижением образования свободных радикалов и соответственно повреждения ими клеток, изменением гормонального профиля, в частности, снижением уровня, как общего, так и свободного эстрадиола и тестостерона.
Маркерами потребляемой энергии в детстве и во взрослом возрасте являются рост (темп роста), масса тела, а также уровень физической активности. У женщин очень важным маркером потребляемых калорий в детском возрасте является и возраст начала менструации. Эпидемиологические исследования показали, что все перечисленные характеристики влияют на риск развития рака.
Механизм канцерогенного эффекта жиров связывают с их влиянием на процессы синтеза и метаболизма стероидных половых гормонов, таких как эстрадиол и тестостерон. Жирные кислоты, особенно насыщенные, ингибируют связывание эстрадиола с белками плазмы крови, что является причиной высокой концентрации циркулирующего в крови свободного эстрадиола. Было показано, что снижение потребления жиров приводит к снижению уровней эстрона и эстрадиола у женщин детородного возраста. У женщин в менопаузе снижение потребления жиров с 40 до 20% привело к выраженному (на 17 %) снижению концентрации в плазме крови общего эстрадиола. Потребление жиров влияет также на концентрацию мужского полового гормона тестостерона. Показано, что концентрация в крови тестостерона достоверно коррелирует с потреблением жиров. Например, концентрация в крови тестостерона значительно выше у афро-американцев, чем африканцев, проживающих в Африке. У последних значительно ниже и потребление жиров. В то же время заболеваемость раком простаты значительно выше у афро-американцев. Исследование гормонального профиля больных раком простаты и контрольной группы в странах с низкой и высокой заболеваемостью раком простаты в Японии и Нидерландах показало, что как потребление жиров, так и концентрация тестостерона в крови значительно выше у голландцев.
Потребление жиров влияет также на концентрацию мужского полового гормона тестостерона. Показано, что концентрация в крови тестостерона достоверно коррелирует с потреблением жиров. Например, концентрация в крови тестостерона значительно выше у афро-американцев, чем африканцев, проживающих в Африке. У последних значительно ниже и потребление жиров. В то же время заболеваемость раком простаты значительно выше у афро-американцев. Исследование гормонального профиля больных раком простаты и контрольной группы в странах с низкой и высокой заболеваемостью раком простаты в Японии и Нидерландах показало, что как потребление жиров, так и концентрация тестостерона в крови значительно выше у голландцев.
Механизм действия жиров на процесс канцерогенеза в толстой кишке связан с их влиянием на метаболизм кишечной флоры и концентрацию вторичных жирных кислот, которые способствуют канцерогенезу у лабораторных животных. Кроме того, жиры стимулируют образование в толстой кишке фекапентанов, веществ, обладающих мутагенным действием, и, скорее всего, играют важную роль в процессе канцерогенеза в этом органе. В результате переработки жиров в кишечнике образуются фекальные стеролы, некоторые из которых играют ключевую роль в пролиферации толстокишечного эпителия. Показано, что у людей с высоким потреблением жиров в кале отмечается высокая концентрация вторичных жирных кислот, фекапентанов, более выражен метаболизм кишечной флоры, а также и процесс превращения липидов в мутагенные фекальные стеролы.
В результате переработки жиров в кишечнике образуются фекальные стеролы, некоторые из которых играют ключевую роль в пролиферации толстокишечного эпителия. Показано, что у людей с высоким потреблением жиров в кале отмечается высокая концентрация вторичных жирных кислот, фекапентанов, более выражен метаболизм кишечной флоры, а также и процесс превращения липидов в мутагенные фекальные стеролы.
Связь между потреблением животных жиров и риском рака толстой кишки, молочной железы, простаты была показана во многих аналитических эпидемиологических исследованиях. В большинстве работ, публикованных до середины 80-х гг. XX в., было выявлено, что риск рака толстой кишки, молочной железы, простаты повышен у людей с высоким потреблением животных жиров и мяса. Однако аналитические эпидемиологические исследования последующих лет, в которых использовались более точные методы оценки потребления жиров и других нутриентов и усовершенствованные методы статистического анализа, поставили под сомнение это утверждение.
Когортное исследование американских медсестер, которое включало в себя 90 тыс. участниц, не выявило повышения риска рака молочной железы в группе женщин с высоким потреблением жира вообще и в частности, насыщенных жирных кислот и холестерина. Однако метаанализ 12 исследований методом “случай-контроль” показал небольшое, но статистически достоверное повышение риска рака молочной железы, связанное с высокими указателями потребления жира вообще и насыщенных жиров в частности. Таким образом, роль потребления жиров в этиологии рака молочной железы остается неясной.
Высказывается предположение, что в исследованиях, в которых такая связь выявлена, скорее всего, не удалось отделить эффекта потребления энергии от эффекта потребления жиров. Как уже говорилось выше, жир является наиболее энергоемким нутриентом и большая часть потребляемых человеком калорий (более 40%), особенно в развитых странах, представлена жирами.
Что же касается эпидемиологических исследований рака толстой кишки, то в большинстве из них показана связь между потреблением жиров, особенно насыщенных, а также мяса с риском развития рака этого органа. Например, в уже упомянутом когортном исследовании американских медсестер было выявлено статистически достоверное повышение риска рака ободочной кишки у женщин с высоким потреблением животных жиров, говядины, свинины, баранины и колбасных изделий. В этом и другом американском когортном исследовании медработников было показано, что риск рака и аденоматозных полипов ободочной кишки зависит от соотношения потребления мяса к употреблению птицы и рыбы, т.е. чем выше потребление мяса по сравнению с потреблением птицы и рыбы, тем выше риск рака этого органа.
Например, в уже упомянутом когортном исследовании американских медсестер было выявлено статистически достоверное повышение риска рака ободочной кишки у женщин с высоким потреблением животных жиров, говядины, свинины, баранины и колбасных изделий. В этом и другом американском когортном исследовании медработников было показано, что риск рака и аденоматозных полипов ободочной кишки зависит от соотношения потребления мяса к употреблению птицы и рыбы, т.е. чем выше потребление мяса по сравнению с потреблением птицы и рыбы, тем выше риск рака этого органа.
Углеводы наряду с жирами являются важным источником калорий. В развивающихся странах углеводы составляют 70% и более потребляемой энергии. В развитых странах доля углеводов в рационе питания снижается за счет роста потребления жиров. В продуктах питания углеводы представлены в виде крахмала, сахаров и других полисахаридов, большая часть которых составляет так называемую клетчатку. Основным источником крахмала являются злаки (хлеб), крупы, картофель, горох, бобы. Клетчатка является неотъемлемым компонентом растительной пищи, овощей, фруктов и нерафинированных (неочищенных) круп.
Клетчатка является неотъемлемым компонентом растительной пищи, овощей, фруктов и нерафинированных (неочищенных) круп.
Гипотеза о защитной роли клетчатки была сформулирована английским врачом Беркиттом на основании наблюдений в Африке, где заболеваемость раком толстой кишки низка, а потребление продуктов питания с высоким содержанием клетчатки высоко. Предполагается, что у людей, потребляющих много клетчатки, увеличен объем каловых масс, что ведет к снижению в толстой кишке концентрации канцерогенных веществ.
Клинические метаболические исследования показали, что добавление к ежедневному рациону 10–13 г целлюлозы или клетчатки зерновых (wheat bran) значительно снижает концентрацию в кале вторичных желчных кислот, их метаболическую и мутагенную активность.
Большинство аналитических эпидемиологических исследований подтвердили гипотезу о протективном эффекте клетчатки. Метаанализ 16 исследований методом “случай-контроль” подтвердил обратную связь между потреблением клетчатки и пищи, богатой клетчаткой, и риском рака ободочной кишки. Проспективное исследование американских медработников, в котором под наблюдением находились около 10 тыс. мужчин, выявило, что потребление клетчатки, источником которой являются фрукты и овощи, а также зерновые и крупы, снижает риск аденоматозных полипов и рака ободочной кишки. Однако в когортном исследовании американских медсестер, как и в ряде других эпидемиологических исследований, было показано, что протективным эффектом против рака толстой кишки обладает лишь клетчатка овощей и фруктов. А этот защитный эффект может также быть результатом действия витаминов, индолов, протеаз и других компонентов фруктов и овощей.
Проспективное исследование американских медработников, в котором под наблюдением находились около 10 тыс. мужчин, выявило, что потребление клетчатки, источником которой являются фрукты и овощи, а также зерновые и крупы, снижает риск аденоматозных полипов и рака ободочной кишки. Однако в когортном исследовании американских медсестер, как и в ряде других эпидемиологических исследований, было показано, что протективным эффектом против рака толстой кишки обладает лишь клетчатка овощей и фруктов. А этот защитный эффект может также быть результатом действия витаминов, индолов, протеаз и других компонентов фруктов и овощей.
Защитный эффект потребления овощей и фруктов в развитии злокачественных опухолей у человека доказан для рака полости рта и глотки, пищевода, желудка, ободочной и прямой кишки, легкого. Объем эпидемиологических научных доказательств слабее для злокачественных опухолей гортани, поджелудочной железы, молочной железы и мочевого пузыря. Однако потребление овощей и фруктов, скорее всего, снижает риск развития этих опухолей. В некоторых эпидемиологических исследованиях снижение ОР в связи с потреблением овощей и фруктов было отмечено и для опухолей шейки матки, эндометрия, почки и простаты. Кроме того, показано, что потребление овощей и фруктов снижает риск всех форм злокачественных опухолей в целом. В одном когортном исследовании было показано, что у мужчин, которые ели много зеленых и желтых овощей, риск смерти от всех форм рака был равен 0,3. Выраженным защитным эффектом обладают лук и чеснок. В исследовании, проведенном нами в Москве, было показано, что потребление чеснока значительно снижает риск рака желудка. Антиканцерогенный эффект чеснока можно объяснить его бактерицидными свойствами, в частности, против Helicobacter pylori, инфицированность которым является известным фактором риска развития рака желудка.
В некоторых эпидемиологических исследованиях снижение ОР в связи с потреблением овощей и фруктов было отмечено и для опухолей шейки матки, эндометрия, почки и простаты. Кроме того, показано, что потребление овощей и фруктов снижает риск всех форм злокачественных опухолей в целом. В одном когортном исследовании было показано, что у мужчин, которые ели много зеленых и желтых овощей, риск смерти от всех форм рака был равен 0,3. Выраженным защитным эффектом обладают лук и чеснок. В исследовании, проведенном нами в Москве, было показано, что потребление чеснока значительно снижает риск рака желудка. Антиканцерогенный эффект чеснока можно объяснить его бактерицидными свойствами, в частности, против Helicobacter pylori, инфицированность которым является известным фактором риска развития рака желудка.
Овощи и фрукты содержат активные вещества, которые в эксперименте на лабораторных животных ингибируют развитие опухолей. К ним, в первую очередь, относятся витамины С, Е, бета-каротин, селен, обладающие антиоксидантными свойствами, витамин А, фолиевая кислота, а также фитоэстрогены (изофлавинолы), флавоноиды, такие как кверцитин, индолы и т. д.
д.
Витамин А играет центральную роль в дифференцировке клеток, что послужило основанием для гипотезы о том, что витамин А может быть ингибитором канцерогенеза. Эта гипотеза была подтверждена в экспериментальных исследованиях. Предшественниками витамина А являются каротиноиды, которые в эксперименте оказались ингибиторами канцерогенеза, особенно на модели рака кожи. Аналитические эпидемиологические исследования подтвердили протективный эффект каротиноидов и в меньшей степени витамина А. Необходимо подчеркнуть, что источником витамина А являются продукты животного происхождения, в то время как каротиноиды поступают в организм человека исключительно с продуктами растительного происхождения.
В исследованиях методом “случай-контроль” и когортных исследованиях, в которых оценивалось потребление витамина А и каротиноидов с помощью анкеты, а также проводился анализ крови на содержание этих витаминов, выявлено, что высокий уровень потребления каротиноидов с пищей и высокая их концентрация в крови снижает риск рака легкого. Потребление каротиноидов снижает риск рака гортани, пищевода, желудка, молочной железы, мочевого пузыря, шейки матки.
Потребление каротиноидов снижает риск рака гортани, пищевода, желудка, молочной железы, мочевого пузыря, шейки матки.
Витамин С является антиоксидантом и, кроме того, ингибирует эндогенное образование в желудке нитрозоаминов из поступающих с пищей аминов и нитритов. В ряде исследований методом “случай-контроль” отмечен протективный эффект потребления витамина С. Показано, что у людей, потребляющих с пищей много витамина С, снижен риск развития рака полости рта, гортани, пищевода, желудка и шейки матки. Как и в отношении других витаминов, остается не до конца ясно, обладает ли протективным эффектом витамин С или другие компоненты фруктов и овощей, в состав которых входит витамин С. Витамин Е также является мощным антиоксидантом. В экспериментальных исследованиях показано, что витамин Е ингибирует процесс канцерогенеза. Результаты эпидемиологических исследований, в которых изучалось влияние потребления витамина Е с пищей и его концентрации в крови, противоречивы. Однако следует отметить, что в исследованиях, где изучалась связь между концентрацией в крови витамина Е, была показана обратная зависимость между уровнем витамина Е и риском возникновения злокачественных опухолей и особенно тех, которые причинно не связаны с курением.
Ингибирующий канцерогенез эффект селена был показан множеством экспериментальных исследований. Кроме того, эпидемиологическими исследованиями отмечена обратная корреляция между уровнем потребления селена и заболеваемостью злокачественными опухолями. Корреляция особенно выражена для рака толстой кишки и молочной железы. Результаты аналитических эпидемиологических исследований менее убедительны. В некоторых проспективных исследованиях, в которых изучалась концентрация селена в крови, выявлено снижение риска злокачественных опухолей молочной железы и легкого с увеличением концентрации селена в крови. Что же касается других форм рака, то эпидемиологические исследования не могут ни подтвердить, ни опровергнуть возможности защитного влияния селена на их развитие.
В соленых, копченых и консервированных продуктах могут содержаться различные канцерогенные вещества. Есть основания предполагать, что нитрозоамины, а также их предшественники (нитраты, нитриты) в пище связаны с повышенным риском рака пищевода и желудка. Повышенный риск рака желудка наблюдается среди людей, потребляющих много соли.
Повышенный риск рака желудка наблюдается среди людей, потребляющих много соли.
Несмотря на то, что в настоящее время наших знаний не достаточно для того, чтобы точно указать на все компоненты питания, способствующие развитию рака или снижающие риск его развития, не вызывает сомнения, что увеличение потребления овощей, зелени и фруктов и снижение потребления жира (особенно животного) приведет к снижению заболеваемости злокачественными опухолями.
Профилактика рака желудка | Тамбовская областная клиническая больница имени В.Д. Бабенко
Рак желудка – достаточно распространенное онкологическое заболевание и одно из самых опасных, поскольку обнаруживается оно уже на далеко зашедших стадиях, а соответствующее лечение больные получают крайне редко. После радикальной операции пятилетняя выживаемость больных раком желудка около 40 %. Но большинству пациентов адекватное лечение провести не удается. Из-за этого не более 12 % всех заболевших переживут пятилетний рубеж. Поэтому профилактика рака желудка сегодня очень актуальна. Известно, что рак желудка возникает преимущественно после сорока лет и может развиться у людей обоих полов.
Поэтому профилактика рака желудка сегодня очень актуальна. Известно, что рак желудка возникает преимущественно после сорока лет и может развиться у людей обоих полов.
Врачи особое внимание уделяют пациентам с желудочно – кишечными заболеваниями. Ответственность самого больного, перенесшего заболевания язвы желудка и двенадцатиперстной кишки, полипов, хеликобактериоза, пернициозной анемии, хронического атрофического гастрита – должно взрасти мотивацию на профилактику рака, необходимостью следить за собственным здоровьем, и при обнаружении желудочных заболеваний, принять соответствующие меры к их излечению.
Эпидемиология
Рак желудка занимает в мире четвёртое место среди злокачественных образований. Это заболевание имеет высокий показатель смертности (более 700 000 в год), что делает его вторым в структуре онкологической смертности после рака лёгкого.
В России рак желудка стабильно занимает второе место 15,8% у мужчин и 12,4% у женщин. заболевание широко распространено в Корее, Великобритании, Южной Америке и Исландии. В Корее рак желудка занимает первое место в структуре онкологической заболеваемости (20,8%) и второе место по смертности.
заболевание широко распространено в Корее, Великобритании, Южной Америке и Исландии. В Корее рак желудка занимает первое место в структуре онкологической заболеваемости (20,8%) и второе место по смертности.
Метастазы у 80—90% больных раком желудка, шестимесячная выживаемость составляет 65% в случае ранней диагностики заболевания и менее 15% на поздних стадиях процесса. В среднем самая высокая выживаемость при раке желудка отмечается в Японии— 53%, в других странах она не превышает 15—20%.
В одном случае из 50 у пациентов, обращающихся с жалобами на, диспепсию выявляется рак желудка.
Этиология
Среди факторов, способствующих развитию рака желудка, называются особенности диеты и факторы окружающей среды, курение, инфекционный и генетический факторы.
Доказана зависимость частоты возникновения рака желудка от недостатка употребления аскорбиновой кислоты, избыточного употребления соли, маринованных, пережаренных, копчёных продуктов, острой пищи, животного масла. Среди причин рака желудка называется злоупотребление алкоголем, особенно водкой. Отмечается прямая корреляционная связь частоты возникновения рака желудка с содержанием в почве меди, молибдена, кобальта и обратная — цинка и марганца.
Среди причин рака желудка называется злоупотребление алкоголем, особенно водкой. Отмечается прямая корреляционная связь частоты возникновения рака желудка с содержанием в почве меди, молибдена, кобальта и обратная — цинка и марганца.
Важным фактором развития рака желудка является дуоденогатральный рефлюкс, приводящий к хроническому рефлюкс-гастриту. Так, риск рака желудка увеличивается через 5—10 лет после операций на желудке, особенно после резекции.
Клиника
Следует внимательно относиться к своему состоянию. В зависимости от расположения и вида опухоли, проявления болезни могут быть самые разные:
- кровотечение, черный стул,
- боли в подложечной области,
- чувство тяжести, распирания в подложечной области после еды, отрыжка, тошнота и рвота,
- нарушение глотания, чувство помехи при прохождении твердой пищи,
- потеря аппетита, отвращение к ранее любимой пище, например к мясу, общая слабость, потеря веса.

Хеликобактериоз
Заражение хеликобактером (Helicobacter pylori) повышает риск рака желудка в 2-4 раза. Инфицированность населения составляет около 40 %. Заразиться можно через грязные руки, загрязненные продукты, во время поцелуев. Профилактика заражения проста: мыть перед едой руки с мылом, обдавать кипятком фрукты, овощи.
Как же бактерия противостоит воздействию соляной кислоты желудочного сока и не погибает? Выжить помогает особый фермент, уреаза — она расщепляет мочевину из содержимого желудка. В результате вокруг бактерии образуется облачко аммиака, который нейтрализует кислоту и дает возможность продержаться несколько часов. За это время бактерия ввинчивается в выстилку желудка при помощи спиральных жгутиков, и удаляется от поверхности. Там бактерия может жить десятилетиями. Она медленно размножается, постепенно разрушает слизистую оболочку желудка и способствует развитию гастрита, язвы и рака желудка. Излечение хеликобактериоза улучшает состояние слизистой.
Кроме того, Helicobacter pylori является главной причиной злокачественной опухоли, развивающейся из скоплений лимфоидной ткани в слизистой — В-клеточной лимфомы желудка. Удивительно, что излечение хеликобактериоза приводит к полной регрессии лимфомы желудка и выздоровлению.
Разработаны надежные методы диагностики хеликобактериоза и схемы его эффективного лечения при помощи антибиотиков. Если Helicobacter pylori обнаружена у одного члена семьи, то, как правило, заражены все остальные. Поэтому необходимо лечение всей семьи. К сожалению, инфекция часто рицидивирует. Поэтому необходимо периодически обследоваться и после лечения.
Предраковым заболеванием считается хронический атрофический гастрит. Он вызывает уменьшение желез слизистой, угнетение функций желудка, ослабление выработки пищеварительных ферментов и соляной кислоты. Сначала клетки слизистой желудка теряют обычный вид и становятся похожими на клетки кишечника. Это так называемая кишечная метаплазия. В дальнейшем возникает дисплазия (неправильное развитие). Вот характерная последовательность изменения клеток слизистой желудка: атрофия — кишечная метаплазия — дисплазия — рак.
Хронический атрофический гастрит не имеет яркой клинической картины. Человека беспокоят неприятные ощущения после еды — ноющие тупые боли в подложечной области, тяжесть в желудке, тошнота, отрыжка, иногда с тухлым запахом. Могут быть нарушения стула (поносы или запоры), повышенное газообразование.
Профилактика рака желудка
Профилактика рака желудка заключается, прежде всего, в ведении правильного образа жизни. Чтобы избежать онкологии желудка, следует:
- Избегать жирных, жареных, острых и соленых продуктов;
- Правильно питаться, вводить в рацион большое количество овощей и фруктов;
- Избегать употребления спиртных напитков;
- Стараться вести активный образ жизни, заниматься физкультурой, больше времени проводить на свежем воздухе;
- Избегать находиться в загрязненной промышленными отходами или выхлопными газами среде;
- Избегать употребления с едой нитратов и нитритов.
Профилактика рака желудка – обследование
Профилактическое обследование на рак желудка в областной поликлинике ГБУЗ «ТОКБ им. В.Д. Бабенко»проводится амбулаторно, занимая не более пяти рабочих дней. В него могут войти:
- Фиброгастродуоденоскопия. В настоящее время, существует возможность следить за состоянием желудка с помощью фиброгастроскопии (ФГС). Специальный зонд со световодом вводится в желудок. Во время процедуры врач может осмотреть все отделы желудка и двенадцатиперстную кишку, взять для анализов желудочный сок и кусочки ткани слизистой и даже удалить полипы желудка, не прибегая к полостной операции. ФГС безопасна и безвредна. Больным с повышенным онкологическим риском по раку желудка рекомендуется проходить фиброгастроскопию 1-2 раза в год. Регулярная ФГС позволяет своевременно выявить злокачественную опухоль и провести лечение.
- Узи.
- При наличии образования в желудке – его биопсия и гистологическое исследование.
Завершает данное обследование обязательная консультация врача (онколога), специализирующегося на раке желудка, который расшифрует результаты обследования и сделает соответствующие выводы. По необходимости, может быть немедленно предложено подходящее лечение.
Профилактика рака желудка особенно важна для людей, ведущих пассивный образ жизни и не следующих вышеуказанным нормам питания, а также страдающих вышеупомянутыми желудочными заболеваниями.
Одно из правил школы здоровья гласит: «Если ты хочешь здоровье вернуть и не ведать болезней, тягость забот отгони и считай недостойным сердиться. Скромно обедай, о винах забудь, не сочти бесполезным бодрствовать после еды, полуденного сна избегая. Пусть спутниками в твоей жизни будут трое: весёлый характер, душевный покой и умеренность в пище».
Кроме того, в группе риска относительно развития желудочной онкологии находятся люди, близкие родственники которых (отцы, матери, братья, сестры, братья и сестры родителей) страдали данным заболеванием. В этом случае, профилактика рака желудка просто необходима. Очень важна она и для людей, которым уже исполнилось сорок-сорок пять лет. Для всех упомянутых групп рекомендуется проведение профилактического обследования на регулярной основе, раз в два-три года.
Последние исследования доказывают, что при должной профилактике рака желудка риск его развития снижается более чем на 40%. Кроме того, периодически именно профилактические обследования помогают обнаружить данное заболевание на зачаточной стадии, когда его лечение нередко завершается вполне успешно.
Если у вас появились какие-либо из перечисленных симптомов, необходимо срочно обратиться к врачу и пройти обследование в нашей больнице.
Каковы факторы риска рака желудка?
Фактор риска – это все, что увеличивает ваши шансы заболеть таким заболеванием, как рак. Различные виды рака имеют разные факторы риска. Некоторые факторы риска, например, курение, можно изменить. Другие, такие как возраст человека или семейная история, изменить нельзя.
Но наличие фактора риска или даже нескольких факторов риска не означает, что вы заболеете. Многие люди с одним или несколькими факторами риска никогда не заболевают раком, в то время как другие, заболевшие раком, могут иметь мало известных факторов риска или вообще не иметь их.
Ученые обнаружили несколько факторов риска, повышающих вероятность заболевания раком желудка. Некоторыми из них можно управлять, а другими – нет.
Пол
Рак желудка чаще встречается у мужчин, чем у женщин.
Возраст
Рак желудка может возникать у молодых людей, но риск возрастает с возрастом. Большинство людей, у которых диагностирован рак желудка, находятся в возрасте 60, 70 или 80 лет.
Этническая принадлежность
В Соединенных Штатах рак желудка чаще встречается у испаноязычных американцев, афроамериканцев, коренных американцев и жителей островов Азиатско-Тихоокеанского региона, чем у неиспаноязычных белых.
География
Во всем мире рак желудка чаще встречается в Восточной Азии, Восточной Европе, Южной и Центральной Америке. Это заболевание реже встречается в Африке и Северной Америке.
Инфекция Helicobacter pyloriИнфекция бактериями Helicobacter pylori ( H pylori ), по-видимому, является основной причиной рака желудка, особенно рака нижней (дистальной) части желудка. Длительное инфицирование желудка этим микробом может привести к атрофическому гастриту и другим предраковым изменениям внутренней оболочки желудка.
Люди с раком желудка имеют более высокий уровень инфицирования H. pylori , чем люди без этого рака. Инфекция H pylori также связана с некоторыми типами лимфомы желудка. Даже в этом случае у большинства людей, переносящих этот микроб в желудке, никогда не развивается рак.
Избыточный вес или ожирение
Избыточный вес или ожирение связаны с повышенным риском рака кардии (верхней части желудка рядом с пищеводом).
Диета
Риск рака желудка повышен у людей, в рацион которых входит большое количество продуктов, консервированных солением, таких как соленая рыба, мясо и маринованные овощи.
Регулярное употребление в пищу обработанного, жареного или угольного мяса, по-видимому, увеличивает риск рака желудка без кардии.
Употребление в пищу небольшого количества фруктов или совсем без них, вероятно, увеличивает риск рака желудка. С другой стороны, употребление большого количества свежих фруктов (особенно цитрусовых) и сырых овощей, по-видимому, снижает риск рака желудка.
Употребление алкоголя
Употребление алкоголя, вероятно, увеличивает риск рака желудка. Доказательства этой связи наиболее убедительны для людей, которые пьют 3 или более напитков в день.
Употребление табака
Курение увеличивает риск рака желудка, особенно рака верхней части желудка около пищевода. У курящих людей заболеваемость раком желудка увеличивается примерно вдвое.
Предыдущая операция на желудке
Рак желудка чаще развивается у людей, которым удалили часть желудка для лечения незлокачественных заболеваний, таких как язвы.Это может быть связано с тем, что желудок вырабатывает меньше кислоты, что позволяет присутствовать большему количеству вредных бактерий. Рефлюкс (резерв) желчи из тонкой кишки в желудок после операции также может увеличить риск. Эти виды рака обычно развиваются через много лет после операции.
Некоторые виды полипов желудка
Полипы – это незлокачественные новообразования на слизистой оболочке желудка. Большинство типов полипов (таких как гиперпластические полипы или воспалительные полипы), похоже, не сильно увеличивают риск рака желудка, если вообще увеличивают.Но аденоматозные полипы, также называемые аденомами , иногда могут перерасти в рак.
Злокачественная анемия
Определенные клетки слизистой оболочки желудка обычно вырабатывают вещество, называемое внутренним фактором (IF) , которое необходимо организму для поглощения витамина B12 из пищи. Люди без достаточного количества IF могут столкнуться с дефицитом витамина B12, который влияет на способность организма вырабатывать новые эритроциты, а также может вызывать другие проблемы.Это состояние, называемое злокачественной анемией , может быть вызвано определенными аутоиммунными заболеваниями, а также некоторыми видами хирургического вмешательства на желудке. Наряду с анемией (слишком мало красных кровяных телец) люди с этим заболеванием имеют повышенный риск рака желудка.
Болезнь Менетрие (гипертрофическая гастропатия)
В этом состоянии чрезмерный рост внутренней оболочки желудка вызывает большие складки на слизистой оболочке и приводит к низкому уровню кислоты в желудке. Поскольку это заболевание встречается очень редко, точно неизвестно, насколько это увеличивает риск рака желудка.
Унаследованные синдромы рака
Некоторые люди наследуют генные мутации (изменения) от своих родителей, которые приводят к состояниям, которые могут повысить риск рака желудка. Эти наследственные синдромы составляют лишь небольшой процент случаев рака желудка во всем мире.
Наследственный диффузный рак желудка (HDGC)
Этот наследственный синдром значительно увеличивает риск развития рака желудка. Это состояние встречается редко, но риск рака желудка на протяжении всей жизни среди пораженных людей составляет до 70%.Женщины с этим синдромом также имеют повышенный риск инвазивного лобулярного рака груди. Этот синдром чаще всего вызывается мутациями в гене CDh2 .
Синдром Линча (наследственный неполипозный колоректальный рак, или HNPCC)
Синдром Линча (ранее известный как HNPCC) – это наследственное генетическое заболевание, повышающее риск колоректального рака, рака желудка и некоторых других видов рака. Этот синдром вызван мутациями в одном из генов восстановления несоответствия (MMR), например MLh2 или MSh3 . Эти гены обычно помогают восстанавливать поврежденную ДНК.
Семейный аденоматозный полипоз (ФАП)
У людей с ФАП появляется много полипов в толстой кишке, а иногда и в желудке и кишечнике, начиная с раннего возраста. Люди с этим синдромом имеют очень высокий риск заболеть колоректальным раком и немного повышенный риск заболеть раком желудка. FAP вызывается мутациями в гене APC .
Аденома желудка и проксимальный полипоз желудка (GAPPS)
Это редкое заболевание вызвано мутацией в определенной части гена APC .У людей с GAPPS развивается множество полипов в желудке, и у них повышается риск рака желудка.
Синдром Ли-Фраумени
Люди с этим синдромом имеют повышенный риск развития нескольких типов рака, включая рак желудка в относительно молодом возрасте. Синдром Ли-Фраумени вызван мутацией в гене TP53 .
Синдром Пейтца-Егерса (PJS)
У людей с этим заболеванием развиваются полипы в желудке и кишечнике, а также в других областях, включая нос, дыхательные пути легких и мочевой пузырь.Полипы в желудке и кишечнике называются гамартомами . Они могут вызвать такие проблемы, как кровотечение или непроходимость кишечника. PJS также может вызывать появление темных пятен в виде веснушек на губах, внутренней стороне щек и других областях. Люди с PJS имеют повышенный риск нескольких типов рака, включая рак толстой кишки, поджелудочной железы, желудка и груди. Этот синдром вызван мутациями в гене STK11 .
Семейный анамнез рака желудка
Люди, у которых есть родственники первой степени родства (родители, братья, сестры или дети), у которых был рак желудка, с большей вероятностью разовьются это заболевание, даже без одного из унаследованных синдромов рака, описанных выше.Тем не менее, большинство людей, заболевших раком желудка, не имеют семейного анамнеза.
Общий вариабельный иммунный дефицит (ОВИН)
У людей с ОВИН иммунная система не может вырабатывать достаточно антител для защиты от микробов. Это может привести к частым инфекциям, а также к другим проблемам, включая атрофический гастрит и злокачественную анемию. Люди с ОВИН чаще заболевают лимфомой желудка и раком желудка.
Инфекция, вызванная вирусом Эпштейна-Барра (EBV)
Вирус Эпштейна-Барра вызывает инфекционный мононуклеоз (также называемый моно).Большинство людей заражаются этим вирусом в какой-то момент своей жизни, обычно в детстве или подростковом возрасте.
EBV был связан с раком носоглотки и некоторыми формами лимфомы. Он также обнаружен в раковых клетках от 5% до 10% людей с раком желудка, хотя пока неясно, действительно ли вирус вызывает рак желудка. Рак желудка, связанный с ВЭБ, обычно растет медленнее и имеет меньшую тенденцию к распространению.
Отдельные профессии
Рабочие угольной, металлургической и резиновой промышленности, похоже, имеют более высокий риск заболеть раком желудка.
Имеющие кровь группы А
Группы групп крови относятся к определенным веществам, которые обычно присутствуют на поверхности эритроцитов и некоторых других типов клеток. Эти группы важны для подбора крови для переливания. По неизвестным причинам люди с кровью типа А имеют более высокий риск заболеть раком желудка.
Профилактика рака желудка | Стэнфордское здравоохранение
Факторы риска рака желудка
Знание факторов риска рака желудка – шаг в правильном направлении.Некоторые факторы риска, такие как семейный анамнез, вам не подвластны. Но вы можете контролировать другие факторы риска, такие как диета и курение табачных изделий.
Рак желудка и диета
Врачи считают, что неуклонное снижение заболеваемости раком желудка за последние несколько десятилетий во многом связано с изменениями в том, что мы едим:
- Консервация продуктов : Теперь мы сохраняем продукты в холодильнике, а не солением, копчением или маринованием.
- Здоровое питание : Употребление в пищу продуктов с большим содержанием клетчатки, витамина А и витамина С также может снизить риск рака желудка.
- Бросить курить : Бросить курить, вероятно, является лучшим решением, которое вы можете сделать для своего здоровья. Это снижает риск возникновения многих проблем со здоровьем. Он снижает риск многих видов рака, включая рак желудка, головы и шеи, гортани, пищевода, легких, мочевого пузыря, почек и поджелудочной железы.
Профилактика рака желудка
Вы можете снизить риск рака желудка, выполнив следующие действия:
- Ограничьте количество употребляемого алкоголя и не употребляйте табачные изделия.
- Избегайте копченостей и солений, а также соленого мяса и рыбы.
- Ешьте свежие фрукты и овощи и много цельнозерновых продуктов, таких как цельнозерновой хлеб, крупы, макароны и рис.
- Поддерживайте здоровый вес.
Рак желудка и лекарства
Аспирин и другие нестероидные противовоспалительные препараты (НПВП), такие как ибупрофен, могут снизить риск развития некоторых видов рака желудка. Однако они могут вызвать желудочно-кишечное кровотечение.Многие врачи рассматривают аспирин или НПВП как дополнительное преимущество в предотвращении рака, если вы принимаете их при других заболеваниях, таких как артрит. Но они не рекомендуют принимать их только для снижения риска рака.
6 советов по профилактике рака желудка
Хотя рак желудка является четвертым по распространенности онкологическим заболеванием в мире, количество случаев заболевания за последние несколько десятилетий снизилось. Нет никакой гарантии, что вы сможете предотвратить это, но вы можете многое сделать, чтобы снизить свои шансы на его появление.Вот как дать себе все возможные преимущества.
Проверка на язвы. Helicobacter pylori ( H. pylori ) – обычные бактерии. Это не всегда вызывает у людей тошноту, но может инфицировать слизистую оболочку желудка и вызвать язвы. Это также канцероген, а это значит, что он может вызывать рак. Если у вас язва желудка, вашему врачу может потребоваться проверить, есть ли у вас инфекция H. pylori , и вылечить ее.
Куча продукции. Убедитесь, что каждый прием пищи включает много свежих фруктов и овощей.Это может снизить вероятность заболевания раком желудка. Апельсины, лимоны и грейпфрут – отличный выбор. Что касается грейпфрута, вы можете спросить своего врача, повлияет ли он на какие-либо лекарства, которые вы принимаете (включая статины, которые многие люди принимают для снижения уровня ЛПНП или «плохого» холестерина). Американское онкологическое общество рекомендует выбирать рыбу, птицу или бобы вместо обработанного мяса или красного мяса и цельнозерновой хлеб, макаронные изделия и крупы вместо очищенных зерен (например, цельнозерновую муку вместо белой муки).
Сократите употребление копченостей. Раньше, когда еще не было холодильников, люди курили, мариновали и солили пищу, чтобы сохранить ее. Большое количество соли и консервантов может повредить слизистую оболочку желудка и повысить вероятность рака желудка. Так что ограничьте употребление копченых и маринованных продуктов, в том числе соленого мяса и рыбы.
Избавьтесь от привычки. Курение подвергает вас риску многих видов рака, включая рак желудка. Если вам нужна помощь в отказе от курения, поговорите со своим врачом.И избегайте также “пассивного курения” других людей.
Сделайте ход. Физические упражнения – это повседневная привычка, которая окупается с головы до ног. Хорошая физическая форма и активность могут снизить риск различных видов рака и других проблем со здоровьем.
Проверьте свой вес. У людей с избыточным весом больше шансов заболеть раком желудка. Если вы не уверены, находится ли ваш вес в пределах нормы, спросите своего врача.
Используйте аспирин с умом. Вы можете принимать аспирин, ибупрофен и другие лекарства, отпускаемые без рецепта, например, для облегчения боли, лихорадки или отека.Это также может снизить ваши шансы на рак желудка и толстой кишки. Но вы не должны принимать эти лекарства для предотвращения рака желудка, так как они также могут вызвать внутреннее кровотечение. Ваш врач может объяснить, что лучше для вас.
Рассмотрите возможность генетического тестирования. Есть ли в вашей семье рак желудка? Генетический тест может сказать вам, несете ли вы определенные гены, которые делают вас более чувствительными к раку желудка, включая ген CDh2 и синдром Линча.
Профилактика рака желудка (PDQ®) – версия для пациента
О PDQ
Запрос данных врача (PDQ) – это обширная база данных по раку Национального института рака (NCI).База данных PDQ содержит резюме последней опубликованной информации о профилактике, обнаружении, генетике, лечении, поддерживающей терапии, а также дополнительной и альтернативной медицине. Большинство резюме представлено в двух версиях. Версии для медицинских работников содержат подробную информацию на техническом языке. Версии для пациентов написаны на понятном нетехническом языке. Обе версии содержат точную и актуальную информацию о раке, и большинство версий также доступно на испанском языке.
PDQ – это услуга NCI. NCI является частью Национальных институтов здравоохранения (NIH). NIH – это центр биомедицинских исследований при федеральном правительстве. Обзоры PDQ основаны на независимом обзоре медицинской литературы. Это не политические заявления NCI или NIH.
Цель этого обзора
В этом обзоре информации о раке PDQ содержится текущая информация о профилактике рака желудка (желудка). Он предназначен для информирования и помощи пациентам, семьям и лицам, осуществляющим уход.Он не дает официальных руководящих принципов или рекомендаций для принятия решений в отношении здравоохранения.
Рецензенты и обновления
Редакционные коллегии составляют сводки информации о раке PDQ и поддерживают их в актуальном состоянии. Эти советы состоят из экспертов в области лечения рака и других специальностей, связанных с раком. Резюме регулярно пересматриваются, и в них вносятся изменения при появлении новой информации. Дата в каждой сводке («Обновлено») – это дата самого последнего изменения.
Информация в этом обзоре пациентов была взята из версии для медицинских работников, которая регулярно проверяется и обновляется по мере необходимости редакционной коллегией PDQ по скринингу и профилактике.
Информация о клиническом испытании
Клиническое испытание – это исследование, призванное ответить на научный вопрос, например, лучше ли одно лечение, чем другое. Испытания основаны на прошлых исследованиях и на том, что было изучено в лаборатории. Каждое испытание отвечает на определенные научные вопросы, чтобы найти новые и более эффективные способы помощи больным раком. Во время клинических испытаний лечения собирается информация об эффектах нового лечения и о том, насколько хорошо оно работает. Если клиническое испытание покажет, что новое лечение лучше, чем то, что используется в настоящее время, новое лечение может стать «стандартным».«Пациенты могут захотеть принять участие в клиническом испытании. Некоторые клинические испытания открыты только для пациентов, которые еще не начали лечение.
Клинические испытания можно найти в Интернете на сайте NCI. Для получения дополнительной информации позвоните в Информационную службу рака (CIS), контактный центр NCI, по телефону 1-800-4-CANCER (1-800-422-6237).
Разрешение на использование данного обзора
PDQ является зарегистрированным товарным знаком. Содержимое документов PDQ можно свободно использовать как текст. Его нельзя идентифицировать как сводную информацию о раке NCI PDQ, если не отображается вся сводка и не обновляется регулярно.Тем не менее, пользователю будет разрешено написать предложение, например: «В сводке информации о раке PDQ NCI о профилактике рака груди указываются риски следующим образом: [включить выдержку из резюме]».
Лучше всего процитировать это резюме PDQ:
Редакционная коллегия PDQ® Screening and Prevention. PDQ Профилактика рака желудка. Бетесда, Мэриленд: Национальный институт рака. Обновлено <ММ / ДД / ГГГГ>. Доступно по адресу: https://www.cancer.gov/types/stomach/patient/stomach-prevention-pdq.Дата обращения <ММ / ДД / ГГГГ>. [PMID: 26389468]
Изображения в этом обзоре используются с разрешения автора (ов), художника и / или издателя только для использования в обзорах PDQ. Если вы хотите использовать изображение из сводки PDQ и не используете все сводки, вы должны получить разрешение от владельца. Он не может быть предоставлен Национальным институтом рака. Информацию об использовании изображений в этом обзоре, а также многих других изображений, связанных с раком, можно найти в Visuals Online. Visuals Online – это коллекция из более чем 3000 научных изображений.
Заявление об отказе от ответственности
Информация, содержащаяся в этом резюме, не должна использоваться для принятия решений о страховом возмещении. Более подробную информацию о страховом покрытии можно найти на сайте Cancer.gov на странице «Управление онкологическими услугами».
Свяжитесь с нами
Более подробную информацию о том, как связаться с нами или получить помощь на веб-сайте Cancer.gov, можно найти на нашей странице «Свяжитесь с нами для получения помощи». Вопросы также можно отправить на Cancer.gov через электронную почту веб-сайта.
профилактика, факторы риска и лечение
Gastroenterol Hepatol Bed Bench.2011 Осень; 4 (4): 175–185.
, 1 , 2 и 3Хакиме Зали
1 Факультет парамедицинских наук, Университет медицинских наук Шахида Бехешти, Тегеран, Иран
Mostafa Rezaei-Tavirani
Исследовательский центр, Университет медицинских наук Шахида Бехешти, Тегеран, Иран
Мона Азоди
3 Кафедра биологии, Факультет фундаментальных наук, отделение науки и исследований, Исламский университет Азад, Тегеран, Иран
1 Факультет Парамедицинские науки, Университет медицинских наук Шахида Бехешти, Тегеран, Иран
2 Исследовательский центр протеомики, Университет медицинских наук Шахида Бехешти, Тегеран, Иран
3 Отделение биологии, Факультет фундаментальных наук, научно-исследовательский филиал , Исламский университет Азад, Тегеран, Иран
Автор, ответственный за переписку. Перепечатка или переписка: Мостафа Резаи-Тавирани, доктор философии, Исследовательский центр протеомики, Университет медицинских наук Шахида Бехешти, Тегеран, Иран. Эл. Почта: [email protected]Поступила 25 апреля 2011 г .; Принято 8 июля 2011 г.
Авторские права © 2011 Исследовательский институт гастроэнтерологии и заболеваний печениЭта работа находится под лицензией Creative Commons Attribution-NonCommercial 3.0 Unported License, которая позволяет пользователям читать, копировать, распространять и создавать производные работы в некоммерческих целях с материал при условии правильного цитирования автора оригинальной работы.
Эта статья цитируется в других статьях в PMC.Abstract
Рак начинается с изменения одной единственной клетки. Это изменение может быть инициировано внешними факторами и генетическими факторами. Рак является ведущей причиной смерти во всем мире, и в 2008 году на его долю приходилось 7,6 миллиона смертей (около 13% всех смертей). Рак легких, желудка, печени, толстой кишки и груди является причиной большинства смертей от рака каждый год. В этом обзоре представлены различные аспекты рака желудка; включая клиническую, патологическую характеристику рака желудка, этиологию, заболеваемость, факторы риска, профилактику и лечение.
Ключевые слова: Аденокарцинома, Карцинома желудка, Рак желудка
Введение
Рак является ведущей причиной смерти во всем мире: в 2008 году на его долю приходилось 7,9 миллиона смертей (около 13% всех смертей). Рост ожидаемой продолжительности жизни означает, что также увеличивается риск развития рака. Прогнозируется, что количество смертей от рака во всем мире будет продолжать расти, и к 2030 году, по оценкам, погибнет 12 миллионов человек. Поскольку большинство раковых заболеваний возникает у взрослых в пожилом возрасте, бремя рака гораздо важнее, чем других болезней, в группах населения с большой продолжительностью жизни (1 –3).Восемь ведущих мировых убийц рака также входят в восьмерку самых распространенных с точки зрения заболеваемости. Вместе они составляют около 60% всех случаев рака и смертей. Это рак легких, желудка, груди, прямой и толстой кишки, рта, печени, шейки матки и пищевода.
Рак желудка является вторым по распространенности во всем мире раком, и почти две трети всех случаев заболевания приходится на развивающиеся страны. Это четвертый по частоте рак у мужчин, а у женщин – пятое по статистике на 2008 год.Хотя заболеваемость раком желудка снижается, он по-прежнему остается серьезной проблемой для здоровья и частой причиной смертности от рака во всем мире (4, 5). Канцерогенез рака желудка относится к накоплению генетических изменений множества генов, таких как онкогены, гены-супрессоры опухолей и гены репарации несовпадений (6).
Динамический баланс между пролиферацией клеток и апоптозом очень важен для поддержания гомеостаза в организме человека, и канцерогенез желудка связан с этим дисбалансом (7).Считается, что развитие рака желудка является медленным процессом, при этом основными этиологическими детерминантами рака желудка является воздействие химических канцерогенов и / или инфекция, вызываемая Helicobacter pylori . (8, 9). Сообщалось, что рак желудка также экспрессирует белок, связанный с множественной лекарственной устойчивостью (MRP), и проявляет более низкую чувствительность к противораковым препаратам (10). Рак желудка чаще встречается у пожилых людей, обычно он возникает в седьмом и восьмом десятилетии жизни. Средний возраст постановки диагноза составил 67 лет в одной большой серии.Хотя это подозревается, в настоящее время остается неясным, связан ли рак желудка у молодых пациентов с худшим клиническим исходом (11, 12).
Клинические / патологические характеристики рака желудка
Желудок является наиболее часто поражаемым участком (60–75%) желудочно-кишечного тракта, за которым следуют тонкая кишка, илеоцекальная область и прямая кишка (13). В желудке может возникнуть несколько различных типов рака. Самый распространенный тип – аденокарцинома. Примерно 90% случаев рака желудка – это аденокарцинома.Считается, что аденокарцинома возникает из одной клетки. Аденокарцинома желудка – распространенный рак пищеварительного тракта во всем мире, хотя в Соединенных Штатах он встречается редко. Чаще всего это происходит у мужчин старше 40 лет. Заболеваемость большинством типов аденокарциномы желудка в Соединенных Штатах с годами снизилась. Исследователи считают, что это снижение может быть связано с тем, что люди едят меньше соленой, консервированной и копченой пищи. Существует два типа аденокарциномы желудка в зависимости от анатомического расположения: кардия, или проксимальная, и дистальная, некардиальная аденокарцинома.Их следует рассматривать как отдельные объекты из-за различных эпидемиологических отношений, связанных факторов риска и прогноза. Исторически наиболее частым типом была карцинома дистального отдела желудка. Однако, поскольку частота опухолей кардии продолжает расти, а заболеваемость раком дистальных отделов желудка снижается (14, 15), частота проксимальной аденокарциномы в последние годы превысила заболеваемость раком дистальных отделов. Это прискорбное изменение в эпидемиологии заболевания, поскольку рак кардии желудка обычно имеет худший прогноз, чем рак дистального отдела желудка (15).Борман выделил четыре основных паттерна роста карциномы желудка и разделил их на следующие категории (некоторые опухоли демонстрируют комбинацию этих паттернов): полиповидные (тип I), грибковые (тип II), изъязвленные (тип III) и диффузно инфильтративные (тип IV). ). Было признано, что язва желудка может быть доброкачественной или злокачественной. Грубые признаки, которые были связаны со злокачественными новообразованиями при язве желудка, включают неровные, скрученные края и расположение на большей кривизне рядом с привратником.
На практике для уверенного отличия доброкачественных язв от злокачественных во многих случаях требуется микроскопическое исследование биоптатов (16).При микроскопическом исследовании рак желудка делится на два основных типа: хорошо дифференцированный, кишечного типа и недифференцированный, диффузный тип (17) ().
Морфологические и клеточные иллюстрации, связанные с раком желудка. Подозрительная язва желудка, диагностированная как рак при биопсии и резекция (а). Опухолевые клетки заполняют собственную пластинку, оставляя доброкачественные железы практически нетронутыми (b). Опухолевые клетки проникают в собственную мышечную мышцу (c). При карциноме диффузного типа железистые структуры абортивны (d).
Этот гистологический тип встречается во всем мире, тогда как кишечный тип встречается в регионах с высокой заболеваемостью раком желудка и следует предсказуемому постепенному прогрессированию развития рака от метаплазии. Карциномы желудка кишечного типа обычно характеризуются наличием железообразующих митотически активных столбчатых клеток с увеличенными, темными (гематоксилин) ядрами, с накоплением муцина в просвете этих злокачественных желез и без значительного внутриклеточного накопления муцина ( 18).
По сравнению с клетками карцином кишечного типа, клетки диффузной карциномы были меньше, более однородны по общей форме и размеру ядра и обладали меньшей митотической активностью (19). Лимфома желудка составляет 3–5% всех злокачественных опухолей желудка (20). Хотя заболеваемость карциномой желудка снизилась, заболеваемость первичной лимфомой желудка увеличивается (21). H. pylori играет роль в развитии большинства лимфом MALT ().
Иллюстрация диффузной крупноклеточной В-клеточной лимфомы желудка.
Однако его точный механизм до конца не изучен, хотя хроническое воспаление может увеличивать вероятность злокачественной трансформации через пролиферацию В-клеток в ответ на H. pylori, опосредованную инфильтрирующими опухоль Т-клетками (20). H. pylori может играть аналогичную роль в развитии DLBCL (диффузной В-крупноклеточной лимфомы), и несколько исследований показали полную ремиссию только после эрадикационной терапии (21).
Причины и частота возникновения рака желудка
Развитие рака желудка – это многофакторный процесс, и на вероятность возникновения влияют многие состояния, в том числе семейный анамнез рака желудка, инфекция Helicobacter pylori (распространенная бактерия, которая также может вызывать язвы желудка), история аденоматозного полипа желудка размером более 2 сантиметров, история хронического атрофического гастрита, история злокачественной анемии, ожирение, алкоголь, курение, красное мясо и низкий социально-экономический статус – все это считается важным.
Важными факторами риска причин рака желудка являются H. pylori , ожирение, курение, красное мясо, алкоголь и низкий социально-экономический статус (22).
В 1994 году Международное агентство по изучению рака и Всемирная организация здравоохранения классифицировали Helicobacter pylori как канцероген типа I. Точный механизм, приводящий к раку желудка, не совсем ясен. Воздействие инфекции H. pylori на рак желудка оказывается многофакторным, с участием факторов хозяина и окружающей среды, а также различных бактериальных штаммов. H. pylori наиболее тесно связан с раком кишечника желудка, который развивается поэтапно, но ведет к злокачественному новообразованию, аналогичному раку толстой кишки. В модели канцерогенеза желудка Correa воспаление желудка приводит к атрофии слизистой оболочки, метаплазии, дисплазии и, в конечном итоге, к карциноме (23). Исследования показали, что инфекция H. pylori является независимым фактором риска дистального рака желудка с повышенным в 3–6 раз риском по сравнению с пациентами без инфекции (24–26).У пациентов с H. pylori наличие определенных полиморфизмов генов увеличивает риск развития рака желудка. Гены, кодирующие фактор некроза опухоли альфа (TNF-α), и интерлейкины IL-1, IL-8 и IL-10, каждый, были связаны с более высокой частотой рака в условиях H. pylori (27, 28). В то время как рак кишечника желудка тесно связан с хроническим H. pylori , эта сильная связь не наблюдается при диффузном раке желудка. Однако диффузный или кардиальный рак желудка связан с другими факторами риска, такими как более высокий социально-экономический класс (29), ожирение (30, 31) и кровь типа А (32).
Этнические и географические факторы
Заболеваемость раком желудка выше среди неевропейского населения. В Соединенных Штатах самый высокий уровень заболеваемости обнаружен у коренных американцев (21,6 на 100 000) и азиатского населения (20 на 100 000). И раса, и пол влияют на риск развития болезни и последующую смертность. Самый высокий уровень смертности на основе сочетания этнической принадлежности и пола – у мужчин афроамериканского происхождения (12,4 на 100 000) (33). Тем не менее, общие показатели 5-летней выживаемости среди разных рас примерно одинаковы.Заболеваемость раком желудка также сильно различается в зависимости от географического положения. В отличие от населения Америки, социальное бремя рака желудка намного выше в Японии, где он является наиболее распространенным типом опухоли, составляя примерно 19% новых диагнозов опухолей, основанных на данных реестра рака 2001 года (34). У японских мужчин заболеваемость составляет 116/100 000 (34).
Genetics
Существует множество генов, повышающих риск рака желудка, которые подробно описаны в. Конкретные гены, такие как гены-супрессоры опухолей MCC, APC и p53, были идентифицированы в большом проценте случаев рака желудка (35).Несколько исследований идентифицировали E-cadherin, кальций-зависимую молекулу адгезии, которая отвечает за связывание клеток с соседними клетками, как важный компонент в каскаде желудочного канцерогенеза (36–38). Генетическая предрасположенность включает наследственную передачу единственного мутировавшего аллеля CDh2. Если имеется приобретенная мутация второго аллеля в гене E-кадгерина, то потеря внутриклеточной адгезии приводит к увеличению внутриклеточной проницаемости (39). Широкий спектр мутаций в этом домене был идентифицирован в семьях рака желудка (40).Множественные синдромы связаны с карциномой желудка; большинство из них связаны с образованием полипов желудочно-кишечного тракта и также имеют повышенный риск рака других локализаций. К ним относятся семейный аденоматозный полипоз (FAP) и болезнь Коудена. Генетический дефект FAP расположен в гене APC, который участвует в сигнальном пути опухоли Wnt. Этот ген расположен на хромосоме 5q и вызывает развитие различных типов опухолей, в том числе рака толстой кишки и желудка (41).
Экологические и поведенческие факторы
Существует множество экологических и поведенческих факторов, которые влияют на развитие рака желудка.Курение в настоящее время считается важным фактором. Метаанализ 1997 г. выявил повышение риска рака желудка на 44% для нынешних и бывших курильщиков (42). Во втором более всестороннем метаанализе, проведенном в 2007 году, это увеличение риска составило 60% для мужчин и 20% для женщин (43). В популяционном исследовании случай-контроль воздействие курения в любое время в течение жизни пациента имело популяционный риск 18% и 45% развития карциномы желудка как некардии, так и кардии, соответственно (44).
В отличие от воздействия табака, потребление алкоголя не всегда было связано с раком желудка (45–49). Однако алкоголь считается фактором риска прогрессирования заболевания (50), а совместное действие алкоголя и курения увеличивает риск рака желудка без кардии в 5 раз (47). Было показано, что диета с большим количеством свежих овощей и фруктов имеет защитную связь с раком желудка (51, 54). В некоторых исследованиях было показано, что потребление большого количества соли и обработанного мяса положительно связано с раком желудка (51–53, 56, 57). Было показано, что соленые продукты усиливают канцерогенное действие нитратов у крыс (58).Пациенты с ожирением имеют повышенный риск рака желудка кардиального типа (31, 59). Большое проспективное когортное исследование показало, что индекс массы тела (ИМТ) зависит от повышенного риска рака желудка у пациентов с избыточной массой тела (коэффициент заболеваемости 1,32) и ожирением (2,73) (59). В одном исследовании использование аспирина или нестероидных противовоспалительных препаратов было связано примерно с 50% снижением риска некардиальных аденокарцином желудка (60). Пациенты, перенесшие операцию на желудке по поводу доброкачественного заболевания, также в 2–4 раза имеют повышенный риск рака желудка.Эта ассоциация может быть результатом снижения продукции кислоты в остатке желудка и хронического воспаления из-за рефлюкса желчи в остаток желудка (61).
Воздействие высоких доз радиации – необычный фактор риска рака желудка, обнаруживаемый в основном у выживших после облучения от атомной бомбы во время Второй мировой войны (62). Защитный эффект витамина С или бета-каротина ранее был связан со снижением заболеваемости раком желудка.
Рандомизированное контролируемое исследование с профилактикой химиотерапии показало, что анти- H.pylori , добавление аскорбиновой кислоты и добавление бета-каротина были связаны со значительным регрессом предраковых поражений на фоне атрофического гастрита (63). В недавнем метаанализе было обнаружено, что антиоксиданты обладают защитной ролью против рака пищевода, а бета-каротин защищает от рака желудка кардии (отношение шансов (OR): 0,57) (64).
Симптомы рака желудка
Симптомы у большинства пациентов с карциномой желудка проявляются только после того, как у них появятся обширные поражения с местными или отдаленными метастазами.Общие симптомы включают боль в эпигастрии, вздутие живота или пальпируемое образование в эпигастрии. У других пациентов могут быть тошнота и рвота из-за непроходимости выходного отверстия желудка, раннее насыщение из-за пластического линита, дисфагия из-за поражения кардии или признаки и симптомы кровотечения из верхних отделов желудочно-кишечного тракта из-за изъязвления опухоли. У других пациентов с распространенным раком желудка могут быть клинические признаки метастатического заболевания, такие как анорексия, потеря веса, желтуха, асцит и увеличение печени (65).
Диагностика рака желудка
Раннее выявление важно для улучшения результатов у пациентов с раком желудка. При более раннем выявлении вероятность излечения при безоперационной эндоскопической терапии увеличивается. Диагностика часто откладывается, потому что симптомы могут не проявиться на ранних стадиях заболевания. Кроме того, пациенты могут самостоятельно лечить симптомы, общие для рака желудка с другими, менее серьезными желудочно-кишечными расстройствами (вздутие живота, газы, изжога и чувство сытости).Следующие тесты могут помочь диагностировать рак желудка: общий анализ крови (CBC) для проверки на анемию, эзофагогастродуоденоскопия (EGD) с биопсией, анализ стула для проверки наличия крови в стуле, серия исследований верхних отделов желудочно-кишечного тракта. Незначительные изменения морфологии и цвета слизистой оболочки являются важными факторами для постановки диагноза. Морфологические характеристики EGC включают легкое возвышение и неглубокое вдавление слизистой оболочки, а также разрыв с окружающей слизистой оболочкой и участки с неровной поверхностью. Бледное покраснение или обесцвечивание слизистой оболочки свидетельствует о серьезном заболевании (66).Гибкое улучшение цвета при помощи спектральных изображений (FICE) – это эндоскопический метод, разработанный для улучшения рисунка капилляров и ямок на слизистой оболочке желудка. Технология FICE основана на выборе спектрального коэффициента пропускания с определенной длиной волны.67 Хромоэндоскопия выполняется путем распыления красителей, таких как индигокармин, на слизистую оболочку после тщательной промывки слизи. Этот метод полезен для определения латерального распространения опухоли (68–71).
Лечение рака желудка
Операция по удалению желудка (гастрэктомия) – единственное лечение, которое может вылечить это состояние.Может помочь лучевая терапия и химиотерапия. Для многих пациентов химиотерапия и лучевая терапия после операции могут улучшить шансы на выздоровление.
Используемые в настоящее время химиотерапевтические агенты для лечения рака желудка не очень эффективны, поскольку обнаружение и лечение этого рака выполняются на поздних стадиях заболевания (72). Химиотерапия или облучение могут улучшить симптомы и продлить жизнь, но не являются лечебными. У некоторых пациентов процедура обходного хирургического вмешательства может облегчить симптомы (72–74).
Наиболее часто используемые компоненты химиотерапии: митомицин, фторурацил, цисплатин, инъекции паклитаксела, инъекции доцетаксела. Сейчас ведется множество исследований по выявлению новых хемотропных агентов; кальпротектин, по-видимому, является гораздо более мощным цитотоксическим агентом для опухолевых клеток AGS по сравнению с этопозидом (кальпротектин влияет примерно в 20 раз больше, чем этопозид на раковые клетки) (75, 76).
Ожидания (прогноз) рака желудка
Прогноз рака желудка варьируется.Опухоли в нижних отделах желудка лечат чаще, чем в верхних – кардии желудка или пищеводно-желудочного перехода. Насколько далеко опухоль проникает в стенку желудка и вовлечены ли лимфатические узлы при постановке диагноза, влияет на шансы на излечение. Когда опухоль распространилась за пределы желудка, излечение невозможно, и лечение направлено на улучшение симптомов (2).
Профилактика рака желудка
Программы массового скрининга оказались успешными в выявлении заболеваний на ранних стадиях в Японии, где риск рака желудка намного выше, чем в Соединенных Штатах.Значение скрининга в США и других странах с более низкими показателями рака желудка неясно. По крайней мере, треть всех случаев рака можно предотвратить. Профилактика предлагает наиболее экономичную долгосрочную стратегию борьбы с раком.
Употребление табака – единственный наиболее предотвратимый фактор риска смертности от рака во всем мире, вызывающий, по оценкам, 22% смертей от рака в год. В 2004 году 1,6 миллиона из 7,4 миллиона смертей от рака были вызваны употреблением табака. Ввиду серьезности обращения вспять табачной эпидемии ВОЗ реализовала инициативы по мониторингу масштабов проблемы и помощи странам в принятии эффективных мер по борьбе с табачной эпидемией.Эти инструменты являются важными компонентами национальных программ профилактики рака и будут играть ключевую роль в снижении заболеваемости раком.
Модификация диеты – еще один важный подход к борьбе с раком. Между отсутствием физической активности и ожирением существует связь со многими типами рака. Диеты с низким потреблением красного мяса и высоким содержанием фруктов и овощей могут иметь защитный эффект от многих видов рака. (Они также связаны с более низким уровнем сердечно-сосудистых заболеваний.) Всемирная ассамблея здравоохранения приняла в мае 2004 г. Глобальную стратегию ВОЗ по питанию, физической активности и здоровью с целью сокращения смертности и заболеваний.
Бактерия Helicobacter pylori увеличивает риск рака желудка. Развитие атрофии и метаплазии слизистой оболочки желудка тесно связано с инфекцией H. pylori. Окислительный и нитрозативный стресс в сочетании с воспалением играет важную роль в канцерогенезе желудка. Профилактические меры включают вакцинацию и предотвращение заражения. Было показано, что H. pylori неоднородна на геномном уровне с высокой вариабельностью некоторых генов. Возможность профилактической вакцинации была доказана на животных моделях (мыши, собаки) с использованием цельноклеточных вакцин, а также субъединичных вакцин, содержащих выбранные антигены, такие как VacA, CagA, NAP, hsp, уреаза или каталаза.Одна из трудностей, с которыми встретились исследования вакцин, – это отсутствие коррелятов защиты; другой – разработать вакцину, которая будет эффективна на уровне слизистых оболочек. На людях было проведено несколько исследований фазы I с использованием: рекомбинантных аттенуированных сальмонелл, экспрессирующих уреазу H. pylori, которые показали посредственную иммуногенность при пероральном введении; оральная цельноклеточная вакцина с адъювантом LT дикого типа. Это исследование было прекращено из-за чрезмерных побочных эффектов; очищенная уреаза, вводимая совместно с LT, также приостановлена; рекомбинантная вакцина VacA, CagA и NAP в квасцах, которая оказалась безопасной и сильно иммуногенной.Были задействованы компании Antex, Acambis и Chiron в США и Commonwealth Serum Labs в Австралии. Профилактическая вакцина будет рентабельной для предотвращения рака желудка и язвы двенадцатиперстной кишки (9).
Перспективы на будущее
Согласно прогнозам, число смертей от рака в мире увеличится на 45% с 2008 по 2030 год (с 7,9 миллиона до 11,5 миллиона смертей), отчасти под влиянием роста и старения населения мира. Предполагаемый рост учитывает ожидаемое небольшое снижение смертности от некоторых видов рака в странах с высокими ресурсами.Согласно статистике ВОЗ, количество новых случаев рака за тот же период увеличится с 11,3 миллиона в 2008 году до 15,5 миллиона в 2030 году.
За последние два десятилетия произошел огромный скачок в диагностике, определении стадий и лечении рака желудочно-кишечного тракта. Идентификация антигенов клеточной поверхности привела к введению моноклональных антител, которые могут позволить более целенаправленный подход к лечению. Еще один важный аспект, который следует учитывать, – это возрастающая чувствительность и специфичность методов визуализации, таких как EUS и ПЭТ-КТ, в диагностике и определении стадии рака желудка.Одной из важных областей является использование молекулярной визуализации с множеством новых радиофармацевтических агентов, которые нацелены на повышенные регулируемые специфические рецепторы в раковых клетках.
Примечания
( Цитируйте как: Zali K, Rezaei-Tavirani M, Azodi M. Рак желудка: профилактика, факторы риска и лечение. Gastroenterol Hepatol Bed Bench 2011; 4 (4): 175-185). )
Список литературы
1. Рустги А.К. Новообразования желудка. В: Гольдман Л., Аузиелло Д., редакторы. Сесил лекарство.23-е изд. Филадельфия, Пенсильвания: Сондерс Эльзевьер; 2007. [Google Scholar] 2. Гундерсон Л.Л., Донохью Дж. Х., Альбертс С.Р. Рак желудка. В: Abeloff MD, et al., Редакторы. Клиническая онкология Абелова. 4-е изд. Филадельфия, Пенсильвания: Сондерс Эльзевьер; 2008. [Google Scholar] 4. Дерахшан М.Х., Язданбод А., Саджади А.Р., Шокухи Б., Макколл К.Э., Малекзаде Р. Высокая частота аденокарциномы, возникающей из правой стороны кардии желудка в Северо-Западном Иране. Кишечник. 2004. 53: 1262–66. [Бесплатная статья PMC] [PubMed] [Google Scholar] 5.Fan XM, Wong BCY, Wang WP, Zhow XM, Cho CH, Yuen ST и др. Ингибирование функции протеосом индуцировало апоптоз при раке желудка. Int J Cancer. 2001; 93: 481–88. [PubMed] [Google Scholar] 6. Холиан О, Вахид С., Аттен М.Дж., Аттар Б.М. Ингибирование пролиферации клеток рака желудка ресвератролом: роль оксида азота. Am J Physiol Gastrointest Liver Physiol. 2002; 282: 809–16. [PubMed] [Google Scholar] 7. Чжоу XM, Вонг BC, Fan XM, Zhang HB, Lin MC, Kung HF и др. Нестероидные противовоспалительные препараты вызывают апоптоз в раковых клетках желудка за счет активации bax и bak.Канцерогенез. 2001; 22: 1393–97. [PubMed] [Google Scholar] 8. Сасадзуки С., Иноуэ М., Ивасаки М., Отани Т., Ямамото С., Икеда С. и др. Влияние инфекции Helicobacter pylori в сочетании со статусом cagA и пепсиногена на развитие рака желудка среди японских мужчин и женщин: вложенное исследование случай-контроль. Cancer Epidemiol. Биомаркеры Пред. 2006; 15: 1341–47. [PubMed] [Google Scholar] 9. Отака М., Кониси Н., Одашима М., Джин М., Вада И., Мацухаши Т. и др. Действительно ли монгольская песчанка является подходящим животным-хозяином для изучения гастрита и рака, вызванных инфекцией Helicobacter pylori? Biochem Biophys Res Commun.2006; 347: 297–300. [PubMed] [Google Scholar] 10. Томонага М., Ока М., Нарасаки Ф., Фукуда М., Накано Р., Такатани Х. и др. Ген белка, ассоциированного с множественной лекарственной устойчивостью, придает лекарственную устойчивость при раке желудка и толстой кишки у человека. Jpn J Cancer Res. 1996; 87: 1263–70. [Бесплатная статья PMC] [PubMed] [Google Scholar] 11. Hundahl SA, Phillips JL, Menck HR. Отчет Национальной базы данных по раку о плохой выживаемости пациентов с карциномой желудка в США, получавших гастрэктомию: Пятое издание Американского объединенного комитета по стадированию рака, проксимальному заболеванию и гипотезе «другого заболевания».Рак. 2000; 88: 921–32. [PubMed] [Google Scholar] 12. Лай Дж. Ф., Ким С., Ли С. Клинико-патологические характеристики и прогноз для молодых пациентов с аденокарциномой желудка после радикальной резекции. Энн Сург Онкол. 2008; 15: 1464–69. [PubMed] [Google Scholar] 13. Papaxoinis G, Papageorgiou S, Rontogianni D, Kaloutsi V, Fountzilas G, Pavlidis N, et al. Первичная неходжкинская лимфома желудочно-кишечного тракта: клинико-патологическое исследование 128 случаев в Греции. Исследование Hellenic Cooperative Oncology Group (HeCOG) Leuk Lymphoma.2006; 47: 2140–46. [PubMed] [Google Scholar] 14. He YT, Hou J, Chen ZF. Тенденции заболеваемости раком кардии пищевода и желудка в регионах высокого риска в Китае. Eur J Cancer Пред. 2008; 17: 71–76. [PubMed] [Google Scholar] 15. Маэда Х., Окабаяси Т., Нисимори И. Клинико-патологические особенности аденокарциномы кардии желудка: чем она отличается от рака дистального отдела желудка. J Am Coll Surg. 2008; 206: 306–10. [PubMed] [Google Scholar] 16. Адачи Ю., Мори М., Цунэёси М. Доброкачественная язва желудка, сильно напоминающая злокачественное новообразование: клинико-патологическое исследование 20 резецированных случаев.J Clin Gastroenterol. 1993. 16: 103–108. [PubMed] [Google Scholar] 17. Лорен П. Два основных гистологических типа карциномы желудка: диффузная и так называемая карцинома кишечного типа. Попытка гистоклинической классификации. Acta Pathol Microbiol Scand. 1965; 64: 31–49. [PubMed] [Google Scholar] 18. Ming SC. Карцинома желудка: патобиологическая классификация. Рак. 1977; 39: 2475–85. [PubMed] [Google Scholar] 19. Vauhkonen M, Vauhkonen H, Sipponen P. Патология и молекулярная биология рака желудка.Лучшие Практики Рес Клин Гастроэнтерол. 2006; 20: 651–74. [PubMed] [Google Scholar] 20. Ферруччи П.Ф., Зукка Э. Патогенез и лечение первичной лимфомы желудка: что изменилось за последние 10 лет? Br J Haematol. 2007; 136: 521–38. [PubMed] [Google Scholar] 21. Cogliatti SB, Schmid U, Schumacher U, Eckert F, Hansmann ML, Hedderich J, et al. Первичная B-клеточная лимфома желудка: клинико-патологическое исследование 145 пациентов. Гастроэнтерология. 1991; 101: 1159–70. [PubMed] [Google Scholar] 22. Hundahl SA, Phillips JL, Menck HR.Отчет Национальной базы данных по раку о плохой выживаемости пациентов с карциномой желудка в США, получавших гастрэктомию: Пятое издание Американского объединенного комитета по стадированию рака, проксимальному заболеванию и гипотезе «другого заболевания». Рак. 2000; 88: 921–32. [PubMed] [Google Scholar] 23. Корреа П. Канцерогенез желудка человека: многоэтапный и многофакторный процесс – лекция Первой премии Американского онкологического общества по эпидемиологии и профилактике рака. Cancer Res. 1992; 52: 6735–40. [PubMed] [Google Scholar] 24.Совместная группа по хеликобактерам и раку. Рак желудка и Helicobacter pylori : комбинированный анализ 12 исследований случай-контроль, проведенных в рамках проспективных когорт. Кишечник. 2001; 49: 347–53. [Бесплатная статья PMC] [PubMed] [Google Scholar] 25. Форман Д., Ньюэлл Д. Г., Фуллертон Ф. Связь между инфекцией Helicobacter pylori и риском рака желудка: данные проспективного исследования. Br Med J. 1991; 302: 1302–305. [Бесплатная статья PMC] [PubMed] [Google Scholar] 26. Парсоннет Дж., Фридман Г.Д., Вандерстин Д.П.Инфекция Helicobacter pylori и риск рака желудка. N Engl J Med. 1991; 325: 1127–31. [PubMed] [Google Scholar] 27. Эль-Омар Э.М., Кэррингтон М., Чоу WH. Полиморфизм интерлейкина-1 связан с повышенным риском рака желудка. Природа. 2000; 404: 398–402. [PubMed] [Google Scholar] 28. Rad R, Dossumbekova A, Neu B. Полиморфизм генов цитокинов влияет на экспрессию цитокинов слизистой оболочки, воспаление желудка и специфическую колонизацию хозяина во время инфекции Helicobacter pylori. Кишечник. 2004. 53: 1082–89.[Бесплатная статья PMC] [PubMed] [Google Scholar] 29. Пауэлл Дж., МакКонки СС. Увеличение заболеваемости аденокарциномой кардии желудка и прилегающих участков. Br J Рак. 1990; 62: 440–43. [Бесплатная статья PMC] [PubMed] [Google Scholar] 30. Веселый А.Х., Схоутен Л.Дж., Голдбом Р.А., ван ден Брандт П.А. Индекс массы тела, рост и риск аденокарциномы пищевода и кардии желудка: проспективное когортное исследование. Кишечник. 2007; 56: 1503–11. [Бесплатная статья PMC] [PubMed] [Google Scholar] 31. Линдблад М., Родригес Л.А., Лагергрен Дж.Масса тела, табак и алкоголь, а также риск развития кардии пищевода, кардии желудка и некардиальной аденокарциномы желудка среди мужчин и женщин во вложенном исследовании случай-контроль. Контроль причин рака. 2005; 16: 285–94. [PubMed] [Google Scholar] 32. Haenszel W, Correa P, Cuello C. Рак желудка в Колумбии. II. Эпидемиологическое исследование предшественников поражений методом случай-контроль. J Natl Cancer Inst. 1976; 57: 1021–26. [PubMed] [Google Scholar] 33. Джемал А., Сигель Р., Уорд Э. Статистика рака, 2008. CA Cancer J Clin. 2009; 59: 71–96. [PubMed] [Google Scholar] 34.Маругаме Т., Мацуда Т., Камо К., Катанода К., Аджики В., Собуэ Т. Заболеваемость и заболеваемость раком в Японии в 2001 году на основе данных из 10 популяционных онкологических регистров. Jpn J Clin Oncol. 2007; 37: 884–91. [PubMed] [Google Scholar] 35. Рю М.Г., Пак В.С., Юнг Й.Дж., Чой С.В., Мельцер С.Дж. Аллельные делеции MCC / APC и p53 – частые поздние события в канцерогенезе желудка у человека. Гастроэнтерология. 1994; 106: 1584–88. [PubMed] [Google Scholar] 36. Ильяс М, Томлинсон И.П. Взаимодействие APC, E-кадгерина и бета-катенина в развитии и прогрессировании опухоли.J Pathol. 1997. 182: 128–37. [PubMed] [Google Scholar] 37. Брукс-Уилсон А.Р., Каура П., Суриано Г. Мутации Е-кадгерина зародышевой линии при наследственном диффузном раке желудка: оценка 42 новых семей и обзор критериев генетического скрининга. J Med Genet. 2004; 41: 508–17. [Бесплатная статья PMC] [PubMed] [Google Scholar] 38. Гилфорд П., Хопкинс Дж., Харрауэй Дж. Мутации зародышевой линии E-кадгерина при семейном раке желудка. Природа. 1998; 392: 402–405. [PubMed] [Google Scholar] 39. Робертсон Э.В., Янковский Я. Генетика рака желудочно-пищеводного тракта: парадигмы, парадоксы и прогностическая ценность.Am J Gastroenterol. 2008. 103: 443–49. [PubMed] [Google Scholar] 40. Oliveira C, Seruca R, Carneiro F. Генетика, патология и клиники семейного рака желудка. Int J Surg Pathol. 2006; 14: 21–33. [PubMed] [Google Scholar] 41. Маккай А.Б., Филипе М.И., Лемуан Н.Р. Аномалии, влияющие на локусы гена-супрессора опухоли APC и MCC на хромосоме 5q, часто возникают при раке желудка, но не при раке поджелудочной железы. Int J Cancer. 1993; 55: 598–603. [PubMed] [Google Scholar] 42. Треданиэль Дж., Боффетта П., Буйатти Е., Сараччи Р., Хирш А.Табакокурение и рак желудка: обзор и метаанализ. Int J Cancer. 1997. 72: 565–73. [PubMed] [Google Scholar] 43. Ладейрас-Лопес Р., Перейра А. К., Ногейра А. Курение и рак желудка: систематический обзор и метаанализ когортных исследований. Контроль причин рака. 2008; 19: 689–701. [PubMed] [Google Scholar] 44. Энгель LS, Чоу WH, Воган TL. Риски рака пищевода и желудка, приписываемые населению. J Natl Cancer Inst. 2003; 95: 1404–13. [PubMed] [Google Scholar] 45. Йе В., Экстром А.М., Ханссон Л.Е., Бергстрем Р., Нирен О.Табак, алкоголь и риск рака желудка с разбивкой по участкам и гистологическому типу. Int J Cancer. 1999; 83: 223–29. [PubMed] [Google Scholar] 46. Lagergren J, Bergstrom R, Lindgren A, Nyren O. Роль употребления табака, нюхательного табака и алкоголя в этиологии рака пищевода и кардии желудка. Int J Cancer. 2000; 85: 340–46. [PubMed] [Google Scholar] 47. Sjödahl K, Lu Y, Nilsen TI. Курение и употребление алкоголя в связи с риском рака желудка: популяционное проспективное когортное исследование. Int J Cancer.2007. 120: 128–32. [PubMed] [Google Scholar] 48. Всемирный фонд исследований рака и Американский институт исследований рака. Вашингтон, округ Колумбия: Американский институт исследования рака; 1997. Продовольствие, питание и профилактика рака: глобальная перспектива. [Google Scholar] 49. Gammon MD, Schoenberg JB, Ahsan H. Табак, алкоголь, социально-экономический статус и аденокарциномы пищевода и кардии желудка. J Natl Cancer Inst. 1997. 89: 1277–84. [PubMed] [Google Scholar] 50. Люнг В.К., Линь С.Р., Чинг Дж.Й. Факторы, предсказывающие прогрессирование кишечной метаплазии желудка: результаты рандомизированного исследования эрадикации Helicobacter pylori .Кишечник. 2004. 53: 1244–49. [Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Грэм С., Хоги Б., Маршалл Дж. Диета в эпидемиологии рака желудка. Nutr Cancer. 1990; 13: 19–34. [PubMed] [Google Scholar] 52. Риш HA, Jain M, Choi NW. Факторы питания и заболеваемость раком желудка. Am J Epidemiol. 1985; 122: 947–59. [PubMed] [Google Scholar] 53. Buiatti E, Palli D, Decarli A. Исследование рака желудка и диеты методом случай-контроль в Италии. Int J Cancer. 1989; 44: 611–16. [PubMed] [Google Scholar] 54.Lunet N, Valbuena C, Carneiro F, Lopes C, Barros H. Антиоксидантные витамины и риск рака желудка: исследование случай-контроль в Португалии. Nutr Cancer. 2006; 55: 71–77. [PubMed] [Google Scholar] 56. ван ден Брандт PA, Botterweck AA, Goldbohm RA. Потребление соли, потребление вяленого мяса, использование холодильника и заболеваемость раком желудка: проспективное когортное исследование (Нидерланды). Контроль причин рака. 2003. 14: 427–38. [PubMed] [Google Scholar] 57. Buiatti E, Palli D, Decarli A. Исследование рака желудка и диеты по типу случай-контроль в Италии: II.Связь с питательными веществами. Int J Cancer. 1990; 45: 896–901. [PubMed] [Google Scholar] 58. Цугане С., Сасадзуки С. Диета и риск рака желудка: обзор эпидемиологических данных. Рак желудка. 2007. 10: 75–83. [PubMed] [Google Scholar] 59. Веселый А.Х., Схоутен Л.Дж., Голдбом Р.А., ван ден Брандт П.А. Индекс массы тела, рост и риск аденокарциномы пищевода и кардии желудка: проспективное когортное исследование. Кишечник. 2007; 56: 1503–11. [Бесплатная статья PMC] [PubMed] [Google Scholar] 60. Фэрроу, округ Колумбия, Воган, Т.Л., Ханстен, полиция.Использование аспирина и других нестероидных противовоспалительных препаратов и риск рака пищевода и желудка. Биомаркеры эпидемиологии рака Пред. 1998. 7: 97–102. [PubMed] [Google Scholar] 61. Стальникович Р., Бенбассат Дж. Риск рака желудка после операции на желудке по поводу доброкачественных заболеваний. Arch Intern Med. 1990; 150: 2022–2026. [PubMed] [Google Scholar] 62. Sauvaget C, Lagarde F, Nagano J, Soda M, Koyama K, Kodama K. Факторы образа жизни, радиация и рак желудка у выживших после атомной бомбы (Япония) Контроль причин рака.2005; 16: 773–80. [PubMed] [Google Scholar] 63. Correa P, Fontham ET, Bravo JC. Химиопрофилактика дисплазии желудка: рандомизированное испытание антиоксидантных добавок и терапии против Helicobacter pylori. J Natl Cancer Inst. 2000; 92: 1881–88. [PubMed] [Google Scholar] 64. Кубо А., Корли Д.А. Мета-анализ потребления антиоксидантов и риска аденокарциномы кардии пищевода и желудка. Am J Gastroenterol. 2007; 102: 2323–30. [PubMed] [Google Scholar] 65. Олеарчик А.С. Карцинома желудка. Критический обзор 243 случаев.Am J Gastroenterol. 1978; 70: 25–45. [PubMed] [Google Scholar] 66. Томас Р.Л., Райс Р.П. Кальцифицирующая муцинозная аденокарцинома желудка. Радиология. 1967; 878: 1002–1003. [PubMed] [Google Scholar] 67. Low VH, Levine MS, Rubesin SE, Laufer I, Herlinger H. Диагностика рака желудка: чувствительность исследований с двойным контрастированием с барием. AJR Am J Roentgenol. 1994; 162: 329–34. [PubMed] [Google Scholar] 68. Рубесин С.Е., Левин М.С., Лауфер И. Рентгенография верхних отделов желудочно-кишечного тракта с двойным контрастированием: стандартный подход к заболеваниям желудка.Радиология. 2008; 246: 33–48. [PubMed] [Google Scholar] 69. Томпсон Г., Сомерс С., Стивенсон Г. В.. Доброкачественная язва желудка: надежный рентгенологический диагноз. AJR Am J Roentgenol. 1983; 141: 331–3. [PubMed] [Google Scholar] 70. Levine MS, Creteur V, Kressel HY, Laufer I, Herlinger H. Доброкачественные язвы желудка: диагностика и последующее наблюдение с рентгенографией с двойным контрастированием. Радиология. 1987. 164: 9–13. [PubMed] [Google Scholar] 71. Карман РД. Новый рентгенологический признак язвенного рака желудка. J Am Med Assoc. 1921; 77: 990–92.[Google Scholar] 72. Ван Де Вельде CJH. Современная роль хирургии и мультимодального лечения при локализованном раке желудка. Энн Онкол. 2008; 19: 93–98. [PubMed] [Google Scholar] 73. Бреннер Х., Ротенбахер Д., Арндт В. Эпидемиология рака желудка. Методы Мол биол. 2009; 472: 467–77. [PubMed] [Google Scholar] 74. Грин Флорида, Пейдж Д.Л., Балч С.М., Флеминг И.Д., Морроу М., редакторы. Руководство по стадированию рака AJCC. 6-е изд. Нью-Йорк, Нью-Йорк: Спрингер; 2002. Желудок; С. 99–106. [Google Scholar] 75. Зали Х., Резаи-Тавирани М., Кариминия А., Юсефи Р., Шокргозар М.А.Оценка ингибирующей рост и индуцирующей апоптоз активности человеческого кальпротектина на линии желудочных клеток человека (AGS) Иранский биомедицинский журнал. 2008; 12: 7–14. [PubMed] [Google Scholar] 76. Резаи Тавирани М., Зали Х., Насири С., Шокргозар М.А. Человеческий кальпротектин, мощное противораковое средство с минимальным побочным эффектом. IJCP. 2009; 2: 76–84. [Google Scholar]причин, факторов риска и профилактики рака желудка
Нет четкого указания на то, что вызывает рак желудка (желудка).Рак желудка возникает, когда в клетках желудка возникают ошибки, известные как мутации, в их ДНК. Эти мутации заставляют клетки расти и бесконтрольно делиться. Эти аномальные клетки накапливаются, образуя опухоль в желудке, которая может метастазировать (распространяться) в другие части тела, такие как печень, брюшина, легкие и кости.
Факторы риска рака желудка
Хотя причина рака желудка неизвестна, существуют различные факторы, которые могут увеличить риск развития этого заболевания.Эти факторы риска могут включать:
- Употребление табака
- Диета с высоким содержанием соленых и копченых продуктов
- Недостаточное употребление фруктов и овощей
- Семейный анамнез рака желудка
- Полипы желудка
- Пагубная анемия (состояние, при котором организм не может вырабатывать достаточно здоровых эритроцитов из-за недостатка витамина B12)
- Инфекция Helicobacter (H) pylori
- Длительное воспаление желудка
Снижение риска рака желудка
Чтобы снизить риск развития рака желудка:
- Бросить курить
- Увеличьте количество фруктов и овощей в своем рационе
- Избегайте диеты с высоким содержанием копченых и маринованных продуктов, соленого мяса и рыбы
- Поддержание здорового веса
Известно, что небольшой процент случаев рака желудка вызывается синдромом наследственного диффузного рака желудка.Если у вас есть личная история инвазивного лобулярного рака груди до 50 лет или у ваших близких членов семьи был рак желудка, вы можете поговорить со специалистом-генетиком о прохождении теста на мутацию гена CDh2. Другой синдром наследственного рака с повышенным риском рака желудка – это синдром Линча.
Риск и профилактика – Нет желудка для рака
Некоторые из факторов, которые могут увеличить риск развития рака желудка, включают возраст, пол, этническую принадлежность, курение, семейный анамнез, диету и H.Пилори.
H. pylori – распространенная излечимая инфекция, которая может привести к воспалению желудка и повысить риск развития рака желудка.
В Соединенных Штатах рак желудка чаще встречается у американских индейцев, коренных жителей Аляски, азиатов, испаноязычных американцев и афроамериканцев, чем у неиспаноязычных белых.
Американское общество клинической онкологии Факторы риска рака желудка
Некоторые риски невозможно контролировать, но другие можно УМЕНЬШИТЬ, сосредоточив внимание на своем здоровье и выборе.Просмотрите эти списки и посмотрите, каковы могут быть ваши риски.
Риски, связанные с поведением / образом жизни
- Употребление алкоголя и табака
- Ожирение
- Диеты, богатые копчеными, солеными и маринованными продуктами
- Диеты с низким содержанием свежих фруктов и овощей
- Воздействие пыли и дыма на окружающую среду
Демография / семейная история
Прочие факторы риска
- Возраст 50 и старше
- Мужской пол
- Имеющие группу крови А
- Длительное воспаление желудка (гастрит)
- Helicobacter pylori (H.pylori) бактериальная инфекция
- Мегалобластная (злокачественная) анемия
- Полипы желудка или лимфома желудка в анамнезе
- Раса (чаще встречается у азиатов, жителей островов Тихого океана, латиноамериканцев и афроамериканцев, чем у неиспаноязычных кавказских американцев)
- Болезнь Менетрие
- Аутоиммунный атрофический гастрит
Генетические риски рака желудка
- Раннее обнаружение – ключ к выживанию при раке желудка.
- Изменения образа жизни, такие как отказ от курения и диета, богатая фруктами и овощами, потенциально могут снизить риск рака желудка.
- Лечение инфекции H. pylori (распространенной бактериальной инфекции желудка) может снизить риск развития рака желудка.
- Знание вашего семейного анамнеза и обсуждение его с вашим лечащим врачом может помочь определить, подвержены ли вы риску наследственных онкологических синдромов. Если у вас есть семейная история рака желудка или лобулярного рака груди, вы можете пройти генетическое консультирование и генетическое тестирование, не выходя из дома, нажав здесь https: // www.genomemedical.com/programs/nostomachforcancer/
Скрининг – это тестирование на раннюю стадию рака кажущихся здоровыми людей, у которых нет никаких симптомов. Для возможности выявления любого рака требуется точный и надежный тест, который позволит выявить имеющиеся опухоли. Он не должен давать положительный результат у людей, не страдающих раком.
В таких странах, как Япония, где широко распространен рак желудка, массовое обследование населения помогло выявить рак на ранней, излечимой стадии.Обследование включает рентгеновские снимки с проглатыванием бария и эндоскопический скрининг. Возможно, это уменьшило количество людей, умирающих от этой болезни, но это не доказано. До сих пор неясно, снижает ли скрининг количество людей, у которых в конечном итоге развивается рак желудка на поздней стадии.
В настоящее время в США не существует эффективных методов скрининга рака желудка или программ, направленных на его профилактику или раннее выявление. То же самое касается Канады и Соединенного Королевства.
Исследования, проведенные в США, не показали, что рутинный скрининг полезен для людей со средним риском рака желудка, потому что это заболевание встречается не так часто.Тем не менее, люди с определенными факторами риска рака желудка могут получить пользу от скрининга.
Пациентам и семьям с клиническими признаками, указывающими на наследственный диффузный рак желудка (HDGC), но без мутации CDh2 зародышевой линии, рекомендуется интенсивное эндоскопическое наблюдение в экспертном центре за родственниками первой степени родства пациентов, отвечающих критериям HDGC.


 Поэтому противодействие онкологическим заболеваниям является одной из приоритетных для медицинского сообщества. Как решается данная задача в Димитровграде? Этот вопрос мы адресовали Искандеру ГакифовичуШарафутдинову, заведующему первичным онкологическим отделением производственной поликлиники ФГБУЗ КБ №172 ФМБА России.
Поэтому противодействие онкологическим заболеваниям является одной из приоритетных для медицинского сообщества. Как решается данная задача в Димитровграде? Этот вопрос мы адресовали Искандеру ГакифовичуШарафутдинову, заведующему первичным онкологическим отделением производственной поликлиники ФГБУЗ КБ №172 ФМБА России.