Пенетрирующая язва это: Перфорация и пенетрация язвы – Tartu Ülikooli Kliinikum
Пенетрирующая язва желудка и двенадцатиперстной кишки. Прободная язва реферат по медицине
Пенетрирующая язва желудка и двенадцатиперстной кишки. Прободная язва Пенетрирующая язва желудка и двенадцатиперстной кишки – проникновение язвы в рядом расположенные органы и ткани. Выделяют 3 стадии пенетрации: стадия проникновения язвы через все слои стенки органа, стадия фиброзного сращения с подлежащими тканями и стадия завершенной пенетрации. Клиническая картина зависит от локализации язвы и органа, в который она пенетрирует. Язвы желудка чаще пенетрируют в малый сальник, при этом отмечаются выраженный болевой синдром, плохо поддающийся консервативной терапии, почти постоянная боль, связь с приемом пищи выражена нечетко. Язвы двенадцатиперстной кишки чаще пенетрируют в поджелудочную железу; иррадиация боли в поясничную область, гиперамилаземия. Пенетрация язвы в печеночно- двенадцатиперстную связку может привести к развитию механической желтухи. Язвы желудка могут пенетрировать в брюшную стенку (редко), язвы кардиального и субкардиального отдела желудка с пенетра-цией в малый сальник иногда обусловливают возникновение боли стенокардического характера. В диагностике основное значение имеют: рентгенологическое исследование (выход ниши за контур желудка при профильном исследовании) и фиброгастроскопия (глубокий язвенный дефект). Осложнения: перфорация язвы в свободную брюшную полость с развитием разлитого перитонита, профузное кровотечение из крупных сосудов малого сальника или под- желудочно-двенадцатиперстной артерии. Лечение оперативное. Целесообразность его диктуется тяжестью и частотой возникающих осложнений, неэффективностью консервативной терапии. Операцию следует проводить только после курса противоязвенного лечения. При язве желудка выполняют резекцию его, при дуоденальной язве – селективную проксимальную ваготомию или стволовую ваго-томию в сочетании с антрум-резекцией. Прогноз благоприятный. Профилактика: своевременное адекватное (в том числе оперативное) лечение язвенной болезни. ПРОБОДНАЯ ЯЗВА – быстро возникающее сообщение просвета желудка или двенадцатиперстной кишки со свободной брюшной полостью. Около 10% язв осложняется перфорацией.
В диагностике основное значение имеют: рентгенологическое исследование (выход ниши за контур желудка при профильном исследовании) и фиброгастроскопия (глубокий язвенный дефект). Осложнения: перфорация язвы в свободную брюшную полость с развитием разлитого перитонита, профузное кровотечение из крупных сосудов малого сальника или под- желудочно-двенадцатиперстной артерии. Лечение оперативное. Целесообразность его диктуется тяжестью и частотой возникающих осложнений, неэффективностью консервативной терапии. Операцию следует проводить только после курса противоязвенного лечения. При язве желудка выполняют резекцию его, при дуоденальной язве – селективную проксимальную ваготомию или стволовую ваго-томию в сочетании с антрум-резекцией. Прогноз благоприятный. Профилактика: своевременное адекватное (в том числе оперативное) лечение язвенной болезни. ПРОБОДНАЯ ЯЗВА – быстро возникающее сообщение просвета желудка или двенадцатиперстной кишки со свободной брюшной полостью. Около 10% язв осложняется перфорацией. Симптомы, течение. За 3-4 дня до перфорации у больных отмечается резкое обострение язвенной болезни, при осмотре-некоторое напряжение мышц и локальная пер-куторная болезненность в области язвы. Затем внезапно (чаще при физическом напряжении) появляется резкая «кинжальная» боль в эпигастрии, которая быстро распространяется по всему животу. Боль резко усиливается при движениях. В начальной стадии заболевания может быть однократная рвота рефлекторного характера. Положение больного чаще вынужденное- с приведенными к животу коленями. Выражение лица страдальческое, испуганное. Язык суховат, обложен. Живот резко напряжен («доскообразный»), болезнен во всех отделах, резко положительны симптомы раздражения брюшины. Печеночная тупость отсутствует или сглажена. Тахикардия. При рентгенологическом исследовании-серп воздуха под диафрагмой (в зависимости от времени, прошедшего с момента перфорации, в 60-80%). Выделяют 3 стадии заболевания: рефлекторную (до 6 ч), мнимого благополучия (6-12ч) и прогрессирования перитонита (свыше 12ч).
Симптомы, течение. За 3-4 дня до перфорации у больных отмечается резкое обострение язвенной болезни, при осмотре-некоторое напряжение мышц и локальная пер-куторная болезненность в области язвы. Затем внезапно (чаще при физическом напряжении) появляется резкая «кинжальная» боль в эпигастрии, которая быстро распространяется по всему животу. Боль резко усиливается при движениях. В начальной стадии заболевания может быть однократная рвота рефлекторного характера. Положение больного чаще вынужденное- с приведенными к животу коленями. Выражение лица страдальческое, испуганное. Язык суховат, обложен. Живот резко напряжен («доскообразный»), болезнен во всех отделах, резко положительны симптомы раздражения брюшины. Печеночная тупость отсутствует или сглажена. Тахикардия. При рентгенологическом исследовании-серп воздуха под диафрагмой (в зависимости от времени, прошедшего с момента перфорации, в 60-80%). Выделяют 3 стадии заболевания: рефлекторную (до 6 ч), мнимого благополучия (6-12ч) и прогрессирования перитонита (свыше 12ч). В стадии мнимого благополучия интенсивность болевого синдрома несколько уменьшается, улучшается состояние больного, живот становится мягче и менее болезненным, однако перитонит прогрессирует, состояние больных постепенно ухудшается.
В стадии мнимого благополучия интенсивность болевого синдрома несколько уменьшается, улучшается состояние больного, живот становится мягче и менее болезненным, однако перитонит прогрессирует, состояние больных постепенно ухудшается.
Лечение пенетрирующей язвы желудка и двенадцатиперстной кишки в Израиле. Профилактика и диагностика пенетрирующей язвы желудка и двенадцатиперстной кишки Израиль
Пенетрирующая язва желудка и двенадцатиперстной кишки — форма язвенной болезни, при которой происходит проникновение язвы в органы и ткани, расположенные рядом. Происходит постепенное углубление язвы, которая достигает наружной оболочки желудка и проникает в ткань, прилегающую к стенке желудка или двенадцатиперстной кишки.
Симптоматика и разновидности
Язвы желудка пенетрируют в тело поджелудочной железы или малый сальник. Язвы задней стенки луковицы двенадцатиперстной кишки проникают в печень или желчные пути, в головку поджелудочной железы. Развитие пенетрации язвы происходит постепенно и ее достаточно сложно выявить.
Пациенты жалуются на постоянные боли в верхней половине живота. Связь с приемом пищи или временем суток отсутствует. Прием антацидных препаратов боль не уменьшает. Как правило, боль отдает в тот орган, в который язва пенетрирует. Если язва пентрирует в поджелудочную железу, боли возникают в пояснице или спине, носят опоясывающий характер. При пенетрации в малый сальник, пациент жалуется на боль под правой реберной дугой, отдающую в правое плечо, шею, ключицу.
Выделяют 3 стадии пенетрации:
- стадия проникновения язвы через все слои стенки органа;
- стадия фиброзного сращения с подлежащими тканями;
- стадия завершенной пенетрации.
Обследование и диагностика
Диагноз пенетрирующей язвы желудка и двенадцатиперстной кишки в Израиле устанавливают при помощи фиброгастродуоденоскопии. О наличии заболевания говорит характерный вид пенетрирующей язвы. Края обычно округлые, возвышаются вокруг язвы в виде валиков. При рентгеноскопическом исследовании обнаруживают увеличенную глубину язвы и уменьшение подвижности того органа, в который пенетрирует язва. Ультразвуковое исследование брюшной полости показывает изменения в органах, в которые проникла язва. Уточнить диагноз можно при лапароскопии.
Ультразвуковое исследование брюшной полости показывает изменения в органах, в которые проникла язва. Уточнить диагноз можно при лапароскопии.
Лечение и профилактика заболевания
Лечение пенетрирующей язвы желудка и двенадцатиперстной кишки в Израиле оперативное. Его целесообразность диктуется отсутствием эффекта от консервативного лечения, частотой и тяжестью осложнений. Оперативное вмешательство проводится только после курса противоязвенной терапии. При язве желудка выполняют его резекцию, при язве двенадцатиперстной кишки – стволовую или проксимальную ваготомию.
Профилактика заключается в своевременном адекватном лечении язвенной болезни.
Прогноз и качество жизни
Осложнения заболевания: перфорация язвы в брюшную полость с развитием разлитого перитонита, кровотечение из поджелудочно-двенадцатиперстной артерии или крупных сосудов малого сальника. Прогноз благоприятный.
Пенетрирующая язва желудка и двенадцатиперстной кишки. Прободная язва
Пенетрирующая
язва желудка и двенадцатиперстной кишки – проникновение язвы в рядом
расположенные органы и ткани.
В
диагностике основное значение имеют: рентгенологическое исследование (выход
ниши за контур желудка при профильном исследовании) и фиброгастроскопия
(глубокий язвенный дефект).
Осложнения: перфорация язвы в свободную брюшную полость с развитием разлитого перитонита, профузное кровотечение из крупных сосудов малого сальника или под-желудочно-двенадцатиперстной артерии.
Лечение оперативное. Целесообразность его диктуется тяжестью и частотой возникающих осложнений, неэффективностью консервативной терапии. Операцию следует проводить только после курса противоязвенного лечения. При язве желудка выполняют резекцию его, при дуоденальной язве – селективную проксимальную ваготомию или стволовую ваго-томию в сочетании с антрум-резекцией.
Прогноз благоприятный.
Профилактика: своевременное адекватное (в том числе оперативное) лечение язвенной болезни.
ПРОБОДНАЯ ЯЗВА – быстро возникающее сообщение просвета желудка или двенадцатиперстной кишки со свободной брюшной полостью. Около 10% язв осложняется перфорацией.
Симптомы,
течение. За 3-4 дня до перфорации у больных отмечается резкое обострение
язвенной болезни, при осмотре-некоторое напряжение мышц и локальная
пер-куторная болезненность в области язвы. Затем внезапно (чаще при физическом
напряжении) появляется резкая «кинжальная» боль в эпигастрии, которая быстро
распространяется по всему животу. Боль резко усиливается при движениях. В
начальной стадии заболевания может быть однократная рвота рефлекторного
характера. Положение больного чаще вынужденное- с приведенными к животу
коленями. Выражение лица страдальческое, испуганное. Язык суховат, обложен.
Живот резко напряжен («доскообразный»), болезнен во всех отделах, резко
положительны симптомы раздражения брюшины. Печеночная тупость отсутствует или
сглажена. Тахикардия. При рентгенологическом исследовании-серп воздуха под
диафрагмой (в зависимости от времени, прошедшего с момента перфорации, в 60-80%).
Затем внезапно (чаще при физическом
напряжении) появляется резкая «кинжальная» боль в эпигастрии, которая быстро
распространяется по всему животу. Боль резко усиливается при движениях. В
начальной стадии заболевания может быть однократная рвота рефлекторного
характера. Положение больного чаще вынужденное- с приведенными к животу
коленями. Выражение лица страдальческое, испуганное. Язык суховат, обложен.
Живот резко напряжен («доскообразный»), болезнен во всех отделах, резко
положительны симптомы раздражения брюшины. Печеночная тупость отсутствует или
сглажена. Тахикардия. При рентгенологическом исследовании-серп воздуха под
диафрагмой (в зависимости от времени, прошедшего с момента перфорации, в 60-80%).
Выделяют
3 стадии заболевания: рефлекторную (до 6 ч), мнимого благополучия (6-12ч) и
прогрессирования перитонита (свыше 12ч). В стадии мнимого благополучия
интенсивность болевого синдрома несколько уменьшается, улучшается состояние
больного, живот становится мягче и менее болезненным, однако перитонит
прогрессирует, состояние больных постепенно ухудшается.
В диагностике помогают: язвенный анамнез (80-90%), «кинжальная» боль, «доскообразный» живот, тахикардия при нормальной температуре.
Лечение оперативное. Перед операцией – премедикация антибиотиками. При разлитом гнойном перитоните у соматически отягощенных больных при перфорации острой язвы показано ушивание перфоративного отверстия. При желудочной локализации язвы до ушивания целесообразно взять кусочек из края язвы для гистологического исследования (перфорация раковой опухоли?). В остальных случаях при перфорации дуоденальной язвы применяют ваготомию (различные варианты) с дренирующими операциями (лучше иссечение язвы и ушивание дефекта в поперечном направлении-типа пилоропластики по Гейнеке – Микуличу). При перфорации язвы желудка производят резекцию его.
Профилактика:
своевременное лечение (в том числе хирургическое) язвенной болезни. При отказе
больного от операции или невозможности ее выполнения при небольших сроках с
момента перфорации возможно применение метода Тейлора-постоянная аспирация
желудочного содержимого с помощью тонкого желудочного зонда, парентеральное
введение жидкости, массивная антибиотикотерапия.
Прикрытая перфорация – микроперфорация язвы со спонтанным закрытием дефекта сальником или соседним органом, кусочком пищи. Характерно типичное начало заболевания, затем резкое изменение клинической картины: уменьшение болей, напряжение мышц нерезкое, чаще определяется в правой подвздошной области (затекание содержимого по правому боковому каналу), здесь же положительные симптомы раздражения брюшины. При рентгенологическом исследовании органов брюшной полости-серп газа под диафрагмой.
Осложнения: поддиафрагмальный, подпеченочный абсцессы, абсцесс сальниковой сумки,
Лечение в первые 2 сут – как при типичной перфорации; через 2 сут при хорошем общем состоянии больного и отсутствии перитонеальных явлений лечение такое же, как при пенетрирующей язве.
Прогноз благоприятный.
Список литературы
Для подготовки данной работы были использованы материалы с сайта http://max.1gb.ru/
Дата добавления: 08.06.2006
Опасность прободной язвы и способы её лечения.

Дата публикации: .
Заболеваемость прободной язвой в РБ почти в два раза выше, чем в Европе.
Чем это обусловлено? В основном слабой мотивированностью самих больных к лечению. Около 60% пациентов с диагнозами «язвенная болезнь» и «прободная язва» не выполняют рекомендации врачей по лечению как на «терапевтическом этапе», так и после эпизода прободения.
На операционный стол нередко попадают пациенты, которые узнают о том, что страдают язвенной болезнью, только в момент перфорации язвы. Прободная язва чаще развивается у людей молодого и среднего возраста, при этом среди больных преобладают мужчины. Последнее время прободная язва всё чаще стала развиваться у женщин (пик заболеваемости приходится на возрастную группу 50-60 лет).
Почему именно данные категории людей оказались столь уязвимыми? Молодые мужчины в принципе реже обращаются к врачу. Следовательно, они не получают адекватной лекарственной терапии язвенной болезни, которая помогла бы избежать осложнений в виде кровотечения, пенетрации, прободения язвы.
После подтверждения прободения язвы желудка требуется срочное хирургическое лечение, в противном случае прогноз неблагоприятный.
Причины прободной язвы: несоблюдение предписанной диеты, постоянное нахождение в стрессе, умственные и нервные перенапряжения, несоизмеримые с возможностями физические нагрузки, сбои в работе иммунной системы.
При прободной язве практически моментально возникает сильная слабость и интенсивный болевой синдром в области живота, озноб, тошнота, часто возникает рвота и появляется сухость во рту.
Важно помнить, что если подтверждено прободение язвы желудка, медлить нельзя, следует сразу соглашаться на проведение операции.
Если хирургическое вмешательство не будет проведено, то далее развивается гнойный перитонит. Нестерпимая боль возвращается, возникает постоянная тошнотаи сильная рвота, наблюдается вздутие живота и повышение температуры. В этом случае вероятность положительного прогноза в значительной степени снижается.
Нестерпимая боль возвращается, возникает постоянная тошнотаи сильная рвота, наблюдается вздутие живота и повышение температуры. В этом случае вероятность положительного прогноза в значительной степени снижается.
Поскольку признаки прободения язвы всегда явные, то при их появлении следует в срочном порядке вызывать скорую помощь. Неотложная помощь при прободной язве в домашних условиях заключается в обеспечении полного покоя. Желательно уговорить человека лечь в постель и до приезда специалистов скорой помощи лучше ничего не предпринимать. Для минимизации болевого синдрома можно постараться принять самое удобное положение. Как правило, болевые ощущения немного снижаются, если лечь на бок и прижать ноги к животу. Желательно постараться убедить человека, чтобы он слишком часто не менял позу. Категорически запрещено употреблять какую-либо пищу и воду. Это связано с тем, что продукты и жидкость сразу попадает в брюшную полость. До приезда скорой помощи следует регулярно отслеживать пульс и давление, а также наблюдать за внешним видом человека. Падение давления, учащение сердцебиения, побледнение кожных покровов — это симптомы приближающегося болевого шока.
До приезда скорой помощи следует регулярно отслеживать пульс и давление, а также наблюдать за внешним видом человека. Падение давления, учащение сердцебиения, побледнение кожных покровов — это симптомы приближающегося болевого шока.
Диагностика. В срочном порядке проводится общий анализ крови, рентгенография органов брюшной полости, УЗИ ОБП, эндоскопическое исследование, позволяющее установить точное место локализация дефекта и оценить степень повреждения.
Лечение. Вылечить прободную язву желудка никакими консервативными способами нельзя. Хирургическое лечение — это единственный способ устранения прободной язвы желудка. Выделяют три основных подхода: ушивание язвенного дефекта, иссечение язвы, резекция желудка. У большей части пациентов осуществляется закрытие перфорации путем ушивания дефекта. Иссечение прободной язвы желудка производится только у каждого десятого больного. Показания к резекции желудка возникают при осложненном течении язвенной болезни (каллёзная и пенетрирующая язва, множественные язвы, стеноз выходного отдела желудка), подозрении на злокачественный процесс, повторной перфорации язвы желудка, огромных размерах перфоративного отверстия. Примерно у 10% пациентов применяются малоинвазивные – лапароскопические методики хирургического вмешательства. Использование лапароскопических операций позволяет достоверно снизить частоту послеоперационных осложнений.
Примерно у 10% пациентов применяются малоинвазивные – лапароскопические методики хирургического вмешательства. Использование лапароскопических операций позволяет достоверно снизить частоту послеоперационных осложнений.
Операция – это только начальный этап лечения прободной язвы. Положительный прогноз после оперативного лечения всецело зависит от грамотно проведенной реабилитации.
Диета. Ее цель — снижение нагрузки на орган пищеварения и восстановление его моторики. Только соблюдая строгую диету в течение не менее полугода можно предотвратить развитие рецидива. На 2-3 сутки после операции разрешается в небольшом количестве выпить минеральной воды, слабого чай или сладкого фруктового киселя. На 4-5 сутки в рацион вводится перетертые разваренные крупяные супы, а также отвар шиповника. В малых количествах разрешается кушать рыбное суфле и паровые котлеты из диетических сортов мяса. На 10 день в рацион включается малое количество картофельного пюре.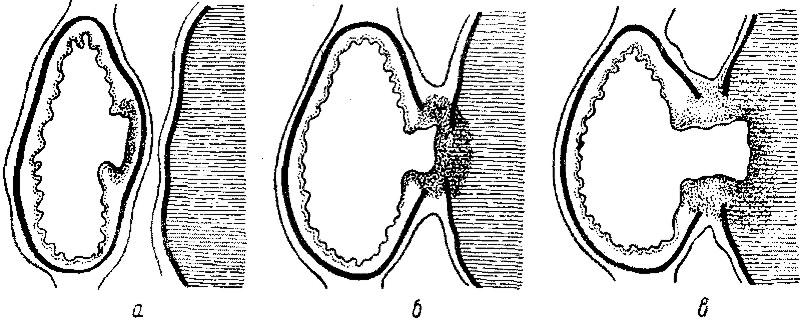 С этого времени постепенно следует вводить в меню вареную тыкву и морковь в мягком виде. От соли следует отказаться.
С этого времени постепенно следует вводить в меню вареную тыкву и морковь в мягком виде. От соли следует отказаться.
Молочные продукты можно начинать вводить в рацион через 2 недели, но при этом необходимо наблюдать за реакцией организма. При удовлетворительном самочувствии можно регулярно принимать нежирный творог и натуральный йогурт. Хлеб впервые должен появиться в рационе не раньше, чем через месяц.
В послеоперационный период рекомендуется кушать до 6-7 раз в день, но очень маленькими порциями. Блюда в рационе должны быть пюреобразными или полужидкими. Пища должна готовиться на пару или отвариваться.
Прогноз зависит от разных факторов. Основными являются возраст, наличие сопутствующих патологий, состояние больного, длительность заболевания.
Безусловно, прободная язва — это очень тяжелое осложнение, которое довольно часто застает врасплох. Но отчаиваться ни в коем случае не стоит, ведь современные методы лечения позволяют полностью восстановиться после сложной операции. Для этого нужно проявить силу воли, соблюдать все рекомендации врача и строгую диету на протяжении длительного периода реабилитации.
Для этого нужно проявить силу воли, соблюдать все рекомендации врача и строгую диету на протяжении длительного периода реабилитации.
Врач-хирург 1 х/о
Николаева О.С.
Хирургическое лечение пенетрирующих язв двенадцатиперстной кишки Текст научной статьи по специальности «Клиническая медицина»
При сочетанных стриктурах пищевода и желудка адекватным объемом оперативного вмешательства является резекция. Операцию необходимо выполнять не ранее чем через 2 — 3 месяца после ожога: к данному сроку обычно заканчивается формирование стриктуры.
Резекция желудка была выполнена 32 больным. Мы отдаем предпочтение резекции желудка по Бильрот-П — Бальфуру. Резекция желудка в объеме 2/3 также необходима при ожогах нижней трети пищевода, так как по сле восстановления проходимости пищевода замыкательная функция кардии страдает, что приводит к рефлюкс-эзофагиту, эрозивному эзофагиту.
30 больных с непосредственными хо рошими и удовлетворительными результатами выписаны на амбулаторное лечение. Осложнения наблюдались у 1 пациента — несостоятельность гастроэнтероанастомоза. Летальные исходы отмечены у 2 больных: у одного — в связи с аспирационной пневмонией на фоне ожога надгортанника, у второго — с несостоятельностью культи двенадцатиперстной кишки (после резекции желудка по Бильрот-П — Витебскому).
Осложнения наблюдались у 1 пациента — несостоятельность гастроэнтероанастомоза. Летальные исходы отмечены у 2 больных: у одного — в связи с аспирационной пневмонией на фоне ожога надгортанника, у второго — с несостоятельностью культи двенадцатиперстной кишки (после резекции желудка по Бильрот-П — Витебскому).
Поддерживающее бужирование — крайне важный этап лечения, требующий настойчивости врача и желания пациента. При его несоблюдении очень часто возникает рецидив стриктуры пищевода. В течение 1 месяца после выписки больной бужируется 2 — 3 раза в неделю, в тече ние 2-го месяца — 1 раз в неделю, в течение 3-го месяца — 1 раз в 2 недели, на 4-м и 5-м месяце — 1 раз в 3 недели, далее — по появлению дисфагии. При резком ухудшении больные госпитализировались для форсированного блокирования под наркозом с последующим амбулаторным бужированием по описанной выше схеме.
Наблюдение за больными, разработанная тактика обследования и лечения больных с сочетанными рубцовыми стриктурами пищевода и желудка позволила у 90 % больных добиться хороших и удовлетворительных результатов.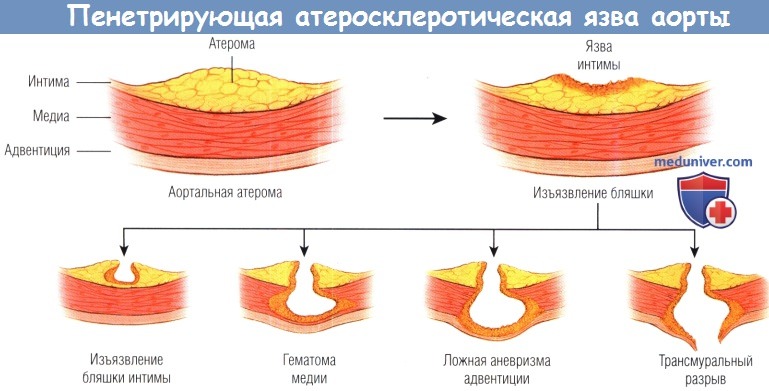
ВЫВОДЫ
1. Рубцовый стеноз желудка формируется спустя 1 месяц после ожога, «ожоговая болезнь» в желудке длится до 7 месяцев после ожога. Операцией выбора при ожоговом стенозе желудка является его резекция по способу Бильрот-П — Бальфура.
2. Методом выбора в лечении рубцово-измененного пищевода является бужирование с эндоскопическим пособием. Поддерживающее бужирование пищевода необходимо проводить на протяжении 1,5 — 2 лет после ожога.
Г.Ф. Жигаев, Е.В. Кривигина
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ПЕНЕТРИРУЮЩИХ ЯЗВ ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ
Бурятский государственный университет (Улан-Удэ) Республиканская клиническая больница им. Н.А. Семашко (Улан-Удэ)
Одним из самых тяжелых и опасных осложнений язвенной болезни двенадцатиперстной кишки является пенетрация язвы в головку поджелудочной железы, частота которой составляет 30 — 90 % (Долгушин А. Н., 1993; Кузин М.И., 2001; Жанталинова Н.А., 2005; Синенченко Г.И. с соавт., 2005; Демин Д.И. с соавт., 2006).
Н., 1993; Кузин М.И., 2001; Жанталинова Н.А., 2005; Синенченко Г.И. с соавт., 2005; Демин Д.И. с соавт., 2006).
Работа основана на анализе результатов хирургического лечения 93 больных с пенетрирующими дуоденальными язвами. Мужчин было 73 (78,5 %), женщин — 20 (21,5 %).
Клиническая картина была атипичной с симптомами поражения органа, в который язва пенетриро-валала: в головку поджелудочной железы — у 80,5 % больных, в гепатодуоденальную связку — у 9,3 %, в печень — у 8,3 %, в корень брыжейки поперечной ободочной кишки — у 1,9 % больных.
При пенетрации язвы в головку поджелудочной железы в клинической картине доминировали симптомы острого панкреатита, боли носили опоя сывающий характер, были постоянными, локализо вались в проекции поджелудочной железы и левом подреберье. У 9 больных вследствие перехода периульцерозной инфильтрации на большой дуоденальный сосочек (БДС) отмечалась иктеричность склер, у 4 — желтуш-ность кожных покровов. В разные периоды заболевания 41 больному проводилось лечение по поводу острого холецистита или механической желтухи и хронического панкреатита. Все это позволяет считать, что язвенная болезнь двенадцатиперстой кишки, осложненная пенетрацией, является необратимым процессом, сопровождается глубокими метаболическими и морфологическими изменениями в зоне язвы.
В разные периоды заболевания 41 больному проводилось лечение по поводу острого холецистита или механической желтухи и хронического панкреатита. Все это позволяет считать, что язвенная болезнь двенадцатиперстой кишки, осложненная пенетрацией, является необратимым процессом, сопровождается глубокими метаболическими и морфологическими изменениями в зоне язвы.
Для диагностики пенетрирующих язв использовали рентгенологические и эндоскопические методы исследования.
Показаниями к операции были безуспешность консервативной терапии в течение 5 — 6 недель, а также сочетанные осложнения язвенной болезни.
Резекционные методики применены у 46 больных. В послеоперационном периоде у 2 из них раз вилась несостоятельность культи двенадцатиперстной кишки с летальным исходом, причиной несостоятельности явился послеоперационный панкреатит с панкреонекрозом.
При локализации язвы на задней стенке двенадцатиперстной кишки с развитием стеноза и пенетра-ции в головку поджелудочной железы мы прибегали к резекции «на выключение» язвы с наложением гастроэнтероанастомоза на длинной петле с межкишечным соустьем по Брауну (Бильрот-П — Бальфур). Важным преимуществом этого метода является профилактика рефлюкса в панкреатические протоки, повреждения паренхимы железы и развития послеоперацион ного панкреатита. По этой методике оперировано 9 больных, непосредственные и отдаленные результаты хорошие.
Отдаленные результаты после резекции желудка проанализированы у 12 (12,9 %) больных. У 64 (68,8 %) больных они оказались отличными и хорошими, у 21 (22,6 %) — удовлетворительными, у 8 (8,6 %) — неудовлетворительными.
Изучение кислотности желудоч ного сока, функционального состояния поджелудочной железы, данных рентгенологического, эндоскопического исследований показало высокую эффективность резекции желудка по Бильрот-П — Бальфуру, в том числе и резекции «на выключение» язвы.
Таким образом, резекция «на выключение» язвы с гастроэнтероанастомозом по Бильрот-11 — Бальфуру может решить сложную хирургическую проблему пенетрирующих дуоденальных язв, сопровождающихся хроническим рецидивирующим панкреатитом без нарушения проходимости выводных протоков поджелудочной железы. Это дает основание рекомендовать такие вмешательства в качестве операции выбора при лечении пенетрирующих язв, осложненных хроническим рецидивирующим панкреатитом.
Е.В. Кривигина, Г.Ф. Жигаев
ОЦЕНКА СЕКРЕТОРНОЙ ФУНКЦИИ ОПЕРИРОВАННОГО ЖЕЛУДКА ПО ПОВОДУ ЯЗВЕННОЙ БОЛЕЗНИ
Бурятский государственный университет (Улан-Удэ) Республиканская клиническая больница им. Н.А. Семашко (Улан-Удэ)
ВВЕДЕНИЕ
Несмотря на то, что резекция желудка по поводу осложнений язвенной болезни до настоящего времени остается широко распространенным методом оперативного вмешательства (Полинкевич Б. С. с соавт., 2006; Хаджибаев А.М. с соавт., 2006), механизмы развития патологических процессов оперированного желудка остаются не вполне выясненными. Некоторые авторы (Ширинов З.Т. с соавт., 2005; Зубарев П.Н. с соавт., 2006; Lechago J. et al., 1993) считают, что функциональное состояние культи желудка зависит от изменений нейрогормональной регуляции.
С. с соавт., 2006; Хаджибаев А.М. с соавт., 2006), механизмы развития патологических процессов оперированного желудка остаются не вполне выясненными. Некоторые авторы (Ширинов З.Т. с соавт., 2005; Зубарев П.Н. с соавт., 2006; Lechago J. et al., 1993) считают, что функциональное состояние культи желудка зависит от изменений нейрогормональной регуляции.
Цель исследования: изучить функциональное состояние оперированного желудка, выяснить степень участия некоторых нейрогормональных регуляторных факторов в нарушении его секреторной функции.
МАТЕРИАЛЫ И МЕТОДЫ
Обследовано 85 больных (77 мужчин и 8 женщин) с клиническими и эндоскопическими признаками патологических процессов в культе резецированного желудка: демпинг-синдром — у 33,3 % больных, рефлюкс-гастрит — у 72,5 %, анастомозит — у 65,2 %, дуоденальный (энтеральный) рефлюкс — у 31,9 %, пептическая язва гастроэнтероанастомоза — у 11,6 %, синдром приводящей петли — у 4,3 % больных. Средний возраст составлял 27,1 ± 1,4 года. До операции у больных язвенной болезнью факторами риска были: нерегулярное питание — в 65,0 % случаев, курение — в 65,0 %, наследственная отягощенность — в 42,4 %, Hp — в 94,7 %.
Средний возраст составлял 27,1 ± 1,4 года. До операции у больных язвенной болезнью факторами риска были: нерегулярное питание — в 65,0 % случаев, курение — в 65,0 %, наследственная отягощенность — в 42,4 %, Hp — в 94,7 %.
Средний размер язвы двенадцатиперстной кишки составлял 0,81 ± 0,04 см, желудка — 0,92 ± 0,11 см, двойная локализация, «зеркальные» язвы луковицы двенадцатиперстной кишки выявлены в 9,88 % случаев.
Методом случайной выборки все больные были разделены на 2 группы, репрезентативные по основным клинико-функциональным показателям. Первую группу (28 человек) составили пациенты, перенесшие резекцию желудка по Бильрот-I с прямым гастродуоденальным анастомозом, вторую — 57 пациентов, оперированных по Бильрот-II — Витебскому. Контрольную группу составили 12 практически здоровых добровольцев.
Исследовали содержание в периферической крови гормонов: гастрина, соматотропного гомона (СТГ), кортизола, трийодтиронина (Т3), тироксина (Т4), нейропептидов (лей-энкефалинов, бета-эндорфинов). Ферментообразующую функцию культи желудка оценивали по содержанию пепсиногена в крови.
Ферментообразующую функцию культи желудка оценивали по содержанию пепсиногена в крови.
3.4. Хирургическое лечение / КонсультантПлюс
– При хирургическом лечении пациентов с ПЯ врачу-хирургу рекомендуется выбрать один из трех видов хирургических вмешательств: ушивание прободного отверстия, иссечение прободной язвы или резекцию желудка. При этом необходимо стремиться к вмешательству минимального объема [10, 15, 17, 42 – 50].Уровень убедительности рекомендации C (уровень достоверности доказательств – 5)- У пациентов с ПЯ размером менее 2 см рекомендуется ушивание язвенного дефекта узловыми или П-образными швами. Аппликация пряди большого сальника при этом не является обязательной процедурой [15, 47, 48, 50].Уровень убедительности рекомендации C (уровень достоверности доказательств – 5)Комментарий. При ушивании ПЯ необходимость аппликации сальника к язвенному дефекту остается на усмотрение хирурга. Опубликованные ретроспективные исследования не могут доказать преимущество аппликации сальника при ушивании язвы. Указанный прием не имел преимущества в частоте осложнений, продолжительности операции и времени стационарного лечения [15, 47, 48, 50].- В лечении пациентов с ПЯ диаметром более 2 см рекомендуется индивидуальный подход, основанный на локализации язвы. В случае больших язв желудка, с подозрением на малигнизацию рекомендуется резекция со срочным патологоанатомическим исследованием операционного материала (при возможности). В случае больших язв двенадцатиперстной кишки рекомендуется выполнить резекцию или ушивание с/без пилоропластики и наружным дренированием желчных протоков. Гастростомия и дуоденостомия рекомендуются только в исключительных случаях, когда врач-хирург не может устранить перфорацию одним из указанных выше способов [15, 49 – 56].Уровень убедительности рекомендации C (уровень достоверности доказательств – 5)
Указанный прием не имел преимущества в частоте осложнений, продолжительности операции и времени стационарного лечения [15, 47, 48, 50].- В лечении пациентов с ПЯ диаметром более 2 см рекомендуется индивидуальный подход, основанный на локализации язвы. В случае больших язв желудка, с подозрением на малигнизацию рекомендуется резекция со срочным патологоанатомическим исследованием операционного материала (при возможности). В случае больших язв двенадцатиперстной кишки рекомендуется выполнить резекцию или ушивание с/без пилоропластики и наружным дренированием желчных протоков. Гастростомия и дуоденостомия рекомендуются только в исключительных случаях, когда врач-хирург не может устранить перфорацию одним из указанных выше способов [15, 49 – 56].Уровень убедительности рекомендации C (уровень достоверности доказательств – 5)Комментарий. Ушивание прободного отверстия можно выполнить в большинстве случаев. Исключение составляют следующие ситуации:
– Прорезывание швов ушиваемых тканей, сомнения в герметичности ушитого прободного отверстия из-за инфильтрации тканей вокруг язвенного дефекта;
– Стеноз пилородуоденальной зоны;
– Прободение гигантской или пенетрирующей язвы;
– Подозрение на малигнизацию язвы.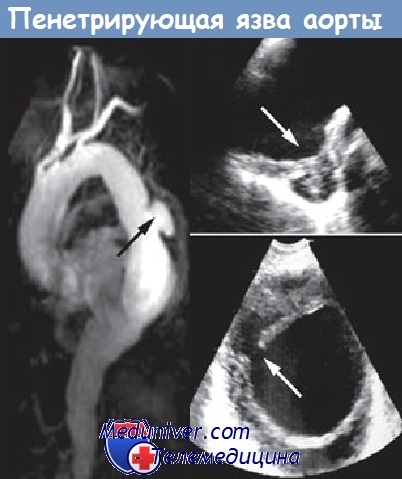
Методы ушивания прободного отверстия:
– Ушивание узловыми или П-образными швами;
– Ушивание узловыми однорядными швами с подшиванием пряди сальника в виде плаща к линии шва;
– Ушивание узловыми однорядными швами с тампонированием перфорационного отверстия прядью сальника на ножке (операция Оппеля-Поликарпова).
Ушивание прободной язвы двенадцатиперстной кишки может быть дополнено ваготомией на усмотрение врача-хирурга [54 – 59]. Следует учесть, что применение эрадикации Helicobacter pylori в комбинации с инъекционной формой ингибиторов протонового насоса в 1-е сутки после операции приносит эффект сопоставимый с применением ваготомии и может заменить ее [60 – 67].В выборе оптимальной тактики необходимо ориентироваться на локализацию, размеры язвенного дефекта, инфильтрата, наличие стеноза ДПК, владение врачом-хирургом навыков выполнения вмешательства.
При прободной каллезной язве желудка диаметром более 2 см рекомендуется иссекать прободную язву желудка с зоной инфильтрации, а дефект в его стенке ушивать узловыми швами без сужения просвета желудка [53, 57].
При прободных каллезных язвах передней и задней стенок двенадцатиперстной кишки рекомендуется рассмотреть возможность выполнения резекции желудка. При невозможности выполнить резекцию желудка язва экономно иссекается, рана задней стенки ушивается без натяжения, а на передней стенке выполняется пилоропластика в любой модификации.
Иссечение язвы желудка на малой кривизне или на большой кривизне, чаще всего, требует мобилизации желудка, как и при его резекции. Язву двенадцатиперстной кишки следует иссекать вместе с зоной инфильтрации.
При невозможности устранения гигантских прободных язв (более 2 см), осложненных обширным плотным инфильтратом, в рамках одного вмешательства, рекомендуется разделить операцию на 2 этапа:
1-й этап – экстренный – производится ушивание прободного отверстия независимо от локализации;
2-й этап – плановый, выполняется резекция желудка или гастрэктомия, с возможной резекцией вовлеченных в воспалительный процесс органов [12, 15, 68, 69, 70].С точки зрения подавления желудочной кислотопродукции к радикальным операциям относятся дистальная резекция в объеме не менее 2/3 желудка, и антрумэктомия с различными вариантами ваготомии. При анализе отдаленных результатов операций по шкале Visick установлено, что лучшие результаты лечения были получены после первичной резекции 2/3 желудка по Бильрот-I (95,2% больных) и антрумэктомии с передней селективной и задней стволовой ваготомией (95%), после резекции желудка по Бильрот-II положительные результаты получены у 78,1% больных [70]. Условия для резекции желудка: компенсированное состояние пациента и владение врачом-хирургом методикой резекции желудка [15, 70].При наличии ПЯ двенадцатиперстной кишки, осложненной стенозом, рекомендуется прибегнуть к одному из перечисленных приемов: ушить прободное отверстие с наложением обходного гастроэнтероанастомоза на длинной петле с межкишечным анастомозом; иссечь язву с выполнением пилоропластики по Финнею или выполнить резекцию желудка [13, 15, 68, 69, 70]. Изолированное ушивание язвы двенадцатиперстной кишки на фоне ее стеноза приводит к развитию гастростаза и несостоятельности ушитого перфоративного отверстия.При сочетании двух осложнений язвенной болезни – кровотечения и прободения язвы передней стенки двенадцатиперстной кишки, рекомендуется ее ушивание, при невозможности ушивания – иссечение, пилоропластика [15, 45, 56 – 59].
При анализе отдаленных результатов операций по шкале Visick установлено, что лучшие результаты лечения были получены после первичной резекции 2/3 желудка по Бильрот-I (95,2% больных) и антрумэктомии с передней селективной и задней стволовой ваготомией (95%), после резекции желудка по Бильрот-II положительные результаты получены у 78,1% больных [70]. Условия для резекции желудка: компенсированное состояние пациента и владение врачом-хирургом методикой резекции желудка [15, 70].При наличии ПЯ двенадцатиперстной кишки, осложненной стенозом, рекомендуется прибегнуть к одному из перечисленных приемов: ушить прободное отверстие с наложением обходного гастроэнтероанастомоза на длинной петле с межкишечным анастомозом; иссечь язву с выполнением пилоропластики по Финнею или выполнить резекцию желудка [13, 15, 68, 69, 70]. Изолированное ушивание язвы двенадцатиперстной кишки на фоне ее стеноза приводит к развитию гастростаза и несостоятельности ушитого перфоративного отверстия.При сочетании двух осложнений язвенной болезни – кровотечения и прободения язвы передней стенки двенадцатиперстной кишки, рекомендуется ее ушивание, при невозможности ушивания – иссечение, пилоропластика [15, 45, 56 – 59]. При перфорации язвы передней стенки двенадцатиперстной кишки и кровотечении из язвы задней ее стенки в первую очередь рекомендуется стремиться к малоинвазивным методам лечения (эндоскопический гемостаз, прошивание язвы задней стенки желудка с интраоперационным эндоскопическим контролем), ушивание или иссечение язвы передней стенки. При неэффективности или невозможности малоинвазивных методов лечения рекомендована резекция желудка [13, 15, 55 – 59]. Кровоточащий сосуд в дне язвы задней стенки верифицируется, прошивается и перевязывается. Края язвы задней стенки иссекаются по периметру язвы на протяжении 1 – 2 мм на глубину слизистого и подслизистого слоев. После этого, обычно, восстанавливается их подвижность и дифференцировка. Это позволяет ушить дефект стенки над дном язвы и прошитыми сосудами без натяжения и риска повреждения подлежащих тканей поджелудочной железы, большого сосочка двенадцатиперстной кишки, холедоха и других структур гепатодуоденальной связки.При невозможности ушить или иссечь прободную язву, а также выполнить резекцию желудка, рекомендуется ввести в прободное отверстие дренажную трубку или катетер самоудерживающийся крупноголовчатый латексный типа Пеццера (18 – 20 номер по шкале Шарьера), герметизировать дренажный канал сальником, наружный конец трубки вывести через контрапертуру на переднюю брюшную стенку, эвакуировать экссудат и зашить рану передней брюшной стенки или сформировать лапаростому [15, 68, 70].
При перфорации язвы передней стенки двенадцатиперстной кишки и кровотечении из язвы задней ее стенки в первую очередь рекомендуется стремиться к малоинвазивным методам лечения (эндоскопический гемостаз, прошивание язвы задней стенки желудка с интраоперационным эндоскопическим контролем), ушивание или иссечение язвы передней стенки. При неэффективности или невозможности малоинвазивных методов лечения рекомендована резекция желудка [13, 15, 55 – 59]. Кровоточащий сосуд в дне язвы задней стенки верифицируется, прошивается и перевязывается. Края язвы задней стенки иссекаются по периметру язвы на протяжении 1 – 2 мм на глубину слизистого и подслизистого слоев. После этого, обычно, восстанавливается их подвижность и дифференцировка. Это позволяет ушить дефект стенки над дном язвы и прошитыми сосудами без натяжения и риска повреждения подлежащих тканей поджелудочной железы, большого сосочка двенадцатиперстной кишки, холедоха и других структур гепатодуоденальной связки.При невозможности ушить или иссечь прободную язву, а также выполнить резекцию желудка, рекомендуется ввести в прободное отверстие дренажную трубку или катетер самоудерживающийся крупноголовчатый латексный типа Пеццера (18 – 20 номер по шкале Шарьера), герметизировать дренажный канал сальником, наружный конец трубки вывести через контрапертуру на переднюю брюшную стенку, эвакуировать экссудат и зашить рану передней брюшной стенки или сформировать лапаростому [15, 68, 70]. В ближайшем послеоперационном периоде проконсультировать пациента в региональном хирургическом центре.
В ближайшем послеоперационном периоде проконсультировать пациента в региональном хирургическом центре. Открыть полный текст документа
Диагностика перфорации пенетрирующей язвы задней стенки двенадцатиперстной кишки
Vladimirova Elizaveta Semenovna MD, PhD, professor, Scientific Consultant to the Department of Thoracoabdominal Surgery, «N. V. Sklifosovsky Research Institute for Emergency Medicine» of the Moscow Health Department, 3 Bolshaya Sukharevskaya Square, Moscow, 129090, Russian Federation, [email protected], 0000-0002-7088-8645
Tveritneva Lyubov Fedorovna MD, PhD, Leading Researcher of the Department for Emergency Surgery, Endoscopy, and Intensive Care, «N. V. Sklifosovsky Research Institute for Emergency Medicine» of the Moscow Health Department, 3 Bolshaya Sukharevskaya Square, Moscow, 129090, Russian Federation, sklif@zdrav. mos.ru, 0000-0002-6999-3755
mos.ru, 0000-0002-6999-3755
Beresneva Era Arsenievna MD, PhD, professor, Scientific Consultant to the Radiology Department, «N. V. Sklifosovsky Research Institute for Emergency Medicine» of the Moscow Health Department, 3 Bolshaya Sukharevskaya Square, Moscow, 129090, Russian Federation, [email protected]
Alekseyechkina Olga Anatolievna MD, PhD, Senior Researcher to the Laboratory of Ultrasonic Research Methods, «N. V. Sklifosovsky Research Institute for Emergency Medicine» of the Moscow Health Department, 3 Bolshaya Sukharevskaya Square, Moscow, 129090, Russian Federation, [email protected], 0000-0002-1265-8032
Popova Irina Evgenievana MD, PhD, Senior Researcher of the Radiology Department, «N. V. Sklifosovsky Research Institute for Emergency Medicine» of the Moscow Health Department, 3 Bolshaya Sukharevskaya Square, Moscow, 129090, Russian Federation, sklif@zdrav. mos.ru, 0000-0002-5798-1407
mos.ru, 0000-0002-5798-1407
Titova Galina Pavlovna MD, PhD, professor, Head of the Research Laboratory of Electron Microscopy, MD, Head of the Laboratory of Electron Microscopy, «N. V. Sklifosovsky Research Institute for Emergency Medicine» of the Moscow Health Department, 3 Bolshaya Sukharevskaya Square, Moscow, 129090, Russian Federation, [email protected]
Selina Irina Evgenievna MD, PhD, Leading Researcher of the Radiology Department, «N. V. Sklifosovsky Research Institute for Emergency Medicine» of the Moscow Health Department, 3 Bolshaya Sukharevskaya Square, Moscow, 129090, Russian Federation, [email protected], 0000-0001-5768-5328
Keywords: penetrating ulcer in the posterior wall of the duodenum, X-ray examination, complications, retroperitoneal phlegmon
Отчет о клиническом случае и обзор литературы
Реферат
Проникающие атеросклеротические язвы (ПАУ) аорты определяются как атеросклеротические поражения с изъязвлением интимы и средней части аорты, которые могут привести к полному разрыву адвентициальной стенки. Целью данной статьи было описать необычный случай хирургически пролеченного пациента с ПАУ брюшной аорты с иллюстрацией основных характеристик, а также проанализировать и проанализировать существующие литературные данные. ПАУ обычно развиваются у пожилых людей и пациентов с гипертонией, а также у пациентов с запущенным атеросклерозом.Хотя изначально он был описан для нисходящей грудной аорты, аналогичное клинико-патологическое образование также встречается в брюшной аорте. Пациентов с симптомами ПАУ следует немедленно лечить, если они подходят для операции. Исключительное наблюдение с помощью методов визуализации необходимо у пациентов с бессимптомной небольшой (<2 см) PAU, с фокальной диссекцией или без нее.
Целью данной статьи было описать необычный случай хирургически пролеченного пациента с ПАУ брюшной аорты с иллюстрацией основных характеристик, а также проанализировать и проанализировать существующие литературные данные. ПАУ обычно развиваются у пожилых людей и пациентов с гипертонией, а также у пациентов с запущенным атеросклерозом.Хотя изначально он был описан для нисходящей грудной аорты, аналогичное клинико-патологическое образование также встречается в брюшной аорте. Пациентов с симптомами ПАУ следует немедленно лечить, если они подходят для операции. Исключительное наблюдение с помощью методов визуализации необходимо у пациентов с бессимптомной небольшой (<2 см) PAU, с фокальной диссекцией или без нее.
Ключевые слова: Проникающая атеросклеротическая язва, брюшная аорта, острый аортальный синдром
ВВЕДЕНИЕ
Проникающая атеросклеротическая язва (PAU) – это атеросклеротическое поражение, часто наблюдаемое в нисходящей грудной аорте (AA) тяжелой степени (DTA). атеросклеротические пациенты.О ПАУ впервые сообщил Шеннан в 1934 году [1], и в настоящее время они включены в категорию острого аортального синдрома (ААС), включая явное расслоение аорты (АД), ПАУ и интрамуральную гематому (ИМГ) с распространенностью от 2% до 7%. ААС [2–4].
Хотя точный патогенез в значительной степени неизвестен, считается, что PAU образуется вторично по отношению к разрыву бляшки аорты, который может вызвать разрыв интимы аорты или разрыв аорты. Несколько факторов могут быть вовлечены в формирование входной слезы при ААС, включая движение корня аорты, геометрию аорты, напряжение стенки, внутренние аномалии ткани аорты и разрыв аортальной бляшки [5-8].
PAU бессимптомны и ограничиваются интимным слоем, а прогрессирующее проникновение в эластичную пластинку и среду может привести к большому спектру клинических состояний с разнообразным поведением. ПАУ может самоограничиваться интимой аорты из-за фиброзного компонента атероматозной бляшки с развитием небольшой ограниченной области изъязвления, в то время как в других случаях поражение может распространяться до внешней стенки аорты, вызывая очаговые поражения. ОБЪЯВЛЕНИЕ. Более того, одним из осложнений ПАУ является образование ИМГ, которое может привести к псевдоаневризме или мешковидной аневризме (СА) с риском разрыва аорты [4,9].
Естественная история ПАУ остается неуловимой, а оптимальный терапевтический режим остается спорным. В то время как бессимптомные случаи ПАУ можно лечить консервативно с тщательным наблюдением, эндоваскулярное восстановление на самом деле является золотым стандартом для сложных ПАУ при ДТА. На уровне AA часто выполняется открытый ремонт. Мы представляем случай хирургического лечения ПАУ на уровне инфраренальной аорты. Обширный обзор литературы (с 1974 по 2015 год) проводится для обсуждения управления PAU в AA.
CASE
Пациент 69 лет был направлен в сосудистое отделение с жалобами на резкую боль, особенно локализованную в правой поясничной области, в течение последнего месяца. При физикальном обследовании у пациента был сохранен симметричный пульс в верхних и нижних конечностях и никаких признаков пальпируемого новообразования в брюшной полости. Его личный анамнез выявил артериальную гипертензию и гиперлипидемию. Пациент курил в течение 45 лет. Лабораторный тест выявил небольшое увеличение лейкоцитов (лейкоциты, 11500 / мкл; нормальный диапазон, 5000 / мкл-10000 / мкл) и С-реактивного белка (CRP, 3 мг / дл; нормальный диапазон, <0.5 мг / дл) и небольшое снижение гемоглобина (Hb, 13 г / дл; нормальный диапазон, 13,8-17,2 г / дл).
Изображения сканирования компьютерной томографии (КТ) с контрастным усилением в брюшной и грудной областях выявили наличие SA в анатомической области AA, имитирующей ветроуказатель (), а также большое IMH и утолщение и кальцификацию стенки аорты, результаты совместимы с PAU (,). Учитывая относительно хорошее состояние здоровья пациента, мы решили провести открытую операцию. Реконструкция аорты заключалась в замене пораженного сегмента аорты трубчатым дакроновым трансплантатом ().Послеоперационное течение без осложнений, пациентка выписана из стационара на 5-е сутки после операции. Согласно гистопатологическому отчету, имелось диффузное изъязвление интимы и тромба под атеросклеротической интимой и средними слоями ().
Размеры проникающей атеросклеротической язвы, имитирующей ветроуказатель, по данным компьютерной томографии.
(A – D) Изображения компьютерной томографии с контрастным усилением брюшной и грудной области выявили наличие мешковидной аневризмы (стрелки) и большой интрамуральной гематомы, результаты сопоставимы с проникающей атеросклеротической язвой.
(A – C) Осевые изображения, полученные с помощью компьютерной томографии брюшной полости, выявили наличие мешковидной аневризмы в анатомической области брюшной аорты, имитирующей ветроуказатель.
(A, B) Интраоперационные изображения проникающей атеросклеротической язвы.
Гистопатологическое изображение выявило артериальную стенку с атеросклеротическими поражениями с диффузными изъязвлениями интимы и тромбом под атеросклеротической интимой и средними слоями (H&E, × 20).
ОБСУЖДЕНИЕ
AAS был определен как клиническая сущность Vilacosta et al.[10] и Vilacosta и San Román [11], которые описали три различных патофизиологических механизма, проявляющихся сходным клиническим образом. Это заболевание встречается в основном у пожилых людей в возрасте от шестого до восьмого десятилетия жизни. ПАУ возникают в основном при ДТА и обычно связаны с гипертонией (примерно 94% случаев) и привычкой к курению. У большинства этих пациентов есть другие проявления атеросклеротического заболевания, и у половины этих пациентов в анамнезе есть аневризма грудной аорты или аневризма брюшной аорты.Клиническая картина имитирует симптоматику классической БА с болью в передней части грудной клетки при язвах восходящей аорты и межлопаточной болью или болью в спине при поражениях, расположенных в области ДТА. В отличие от классической диссекции, ишемия или эмболизация конечностей или других органов встречаются реже [12,13].
Однако PAU демонстрирует больший риск разрыва [12–14]. На КТ и магнитно-резонансной томографии ПАУ характеризуются контрастным кратером, который сообщается с просветом аорты [15].Обычное описание компьютерной томографической ангиографии (КТА) включает измерение максимального диаметра аорты в месте язвы, глубины язвы и длины (ширины) дефекта интимы в месте язвы, в то время как скорость роста в брюшной полости PAU составляет около 3 мм / год [15,16]. Сосуществующая внеаортальная гематома, которая имеет размер> 20 мм в ширину или> 10 мм в глубину, или которая прогрессирует до полного диаметра брюшной аорты, все они считаются сложными PAU [9,15,16]. Некоторые авторы распространяют определение ПАУ на язвенные поражения, не выходящие за пределы стенки аорты [17,18].
Тем не менее, согласно классификации клиник Мэйо, тремя радиологическими диагностическими критериями для ПАУ на КТ с контрастированием являются трансмуральный разрыв с внеаортальной гематомой, четко выраженный кратер язвы в стенке аорты и субадвентициальная расширенная СА. за стенкой аорты [2]. Vorp et al. [19] сообщили о важности формы и симметрии, помимо размера, при оценке риска разрыва.
Несмотря на эти усилия, все еще существует нехватка предикторов естественного течения и поведения PAU, и стандартное лечение не разработано [13].
ПАУ может прогрессировать в СА, очаговую АД или разрыв аорты. На уровне АА образование СА наблюдается чаще, чем очаговое расслоение. Hollier et al. [20] рекомендовали хирургическое вмешательство при асимметричных СА независимо от их размера, учитывая риск разрыва. Рекомендуется проводить лечение как можно раньше у относительно молодых и здоровых пациентов.
Изолированное расслоение АА наблюдается редко (от 0,4% до 2% всех АП) [19]. Наличие ПАУ может способствовать развитию очаговой абдоминальной АД.Начало этого расслоения часто бывает острым, с болями в животе и пояснице, хотя некоторые случаи остаются бессимптомными и выявляются случайно.
Анализ взаимодействия жидкости и структуры пришел к выводу, что низкое напряжение сдвига стенки (ниже 1,5 Н / м 2 ) и высокие колебания напряжения сдвига (индекс колебательного сдвига = 0,13) в течение сердечного цикла в области PAU могут считаться ключевыми гемодинамическими факторами. что приводит к разрыву ПАУ [20].
Дифференциальные диагнозы включают воспалительную аневризму брюшной аорты (IAAA) и воспалительный аортит, например, артериит Такаясу, гигантоклеточный артериит, болезнь Бехчета, болезнь Кавасаки, ревматоидный артрит, саркоидоз, синдром Когана, анкилозирующий лугуперматоз, эритроцитарный эритроцит, системный луговой эритроцит. .
IAAA определяется необычно утолщенной стенкой аневризмы, блестящим белым перианевризматическим и забрюшинным фиброзом и плотными спайками прилегающих внутрибрюшных структур. Дифференциальный диагноз устанавливается на основании отрицательных посевов бактериальной крови, отрицательных кожных проб, отрицательных серологических тестов, локализации АК и типичных анатомических особенностей на КТА, в то время как биопсия может быть оправдана для исключения злокачественных новообразований. Пациентам с воспалительным аортитом должна быть назначена иммуносупрессивная терапия, основанная на риске разрыва, связанном с размером аневризмы и наличием вторичной сосудистой недостаточности органа, связанной с фиброзным стенозом, до и после хирургического вмешательства.
Инвазивное лечение (открытое хирургическое вмешательство или эндоваскулярная трансплантация стента) показано в острых или симптоматических случаях, в то время как курсовое наблюдение с периодической оценкой методами визуализации рекомендуется для бессимптомных или хронических случаев небольших (<2 см) ПАЕ [20]. Открытое хирургическое вмешательство с установкой трансплантата связано с более высокой операционной заболеваемостью и смертностью из-за плохого общего состояния пациента и сопутствующих заболеваний. Напротив, эндоваскулярная трансплантация стента является менее инвазивной процедурой и более подходит для таких слабых пациентов.Поскольку ПАУ является очаговым поражением, адекватная зона приземления практически присутствует. Следовательно, риск миграции или эндопротечки низок, хотя наличие IMH, по-видимому, снижает эффективность эндоваскулярной терапии. Кроме того, открытая операция может быть предпочтительнее для более молодых и здоровых пациентов, у которых разница в операционном риске между двумя стратегиями гораздо меньше, а также для пациентов, для которых важна долгосрочная устойчивость. Здесь мы сообщаем об особом случае открытого хирургического лечения пациента с AA PAU, учитывая параметры, которые поддерживают открытое хирургическое вмешательство.
1) Обзор литературы
Для выявления клинических исследований, описывающих случаи и / или серии пациентов с ПАУ, с 1974 года (первая публикация проникающей язвы аорты) по 2015 год с использованием ключевые слова «проникающие атеросклеротические язвы», «брюшная аорта» и их комбинации, а результаты поиска были обобщены по возрасту, полу, факторам риска, клиническим проявлениям и лечению. Из-за крайней неоднородности исследований взвешенные оценки, сравнения и корреляции не проводились.
Обзор литературы выявил в основном сообщения о случаях PAU на уровне AA и редкую серию более 10 случаев. Мы собрали 298 опубликованных случаев PAU AA () [12,13,17,18,21–61].
Таблица 1
Случаи и / или серии ПАУ, стратифицированные по году публикации, количеству пациентов, возрасту, полу, факторам риска и характеристикам лечения
| Исследование (справочное) | Количество пациентов | Средний возраст (лет) | Пол (мужской / женский) | Риск | Лечение |
|---|---|---|---|---|---|
| Лагай [21] | 3 | 58 | 3/0 | HTN-CAD | ABI ( 2) -трубка (1) |
| Cornud et al.[22] | 1 | 53 | 1/0 | CAD | Трубка |
| Barbier et al. [23] | 1 | 73 | 0/1 | NA | ABI |
| Aschraft et al. [24] | 1 | 60 | 0/1 | HTN-PAD | Трубка |
| Нора и Холлиер [25] | 1 | 56 | 1/0 | HTN | Хирургическое вмешательство трансплантат |
| Barba et al.[26] | 1 | 37 | 1/0 | NA | Промежуточный трансплантат хирургический |
| Ротвелл и Лейн [27] | 1 | 72 | 1/0 | HTN | Трубка |
| Harris et al. [13] | 10 | 74 | 10/0 | HTN-CKD-CAD | Медицинский (3), хирургический промежуточный трансплантат (7) |
| Origuchi et al. [28] | 4 | 59 | 3/1 | HTN (1) | ABI (3) -трубка (1) |
| Goldstein et al.[29] | 1 | 67 | 1/0 | HTN-CAD | Дакроновый аорто-подвздошный трансплантат |
| Moriyama et al. [30] | 1 | 74 | 1/0 | HTN | Плетеный аорто-подвздошный трансплантат из дакрона |
| Тейлор и Калман [31] | 4 | 73 | 4/0 | HTN- CAD-PAD | Дакроновая трубка (2) -Дакроновая накладка (2) |
| Hayashi et al. [32] | 1 | 73 | 1/0 | NA | Медицинский |
| Quint et al.[33] | 1 | NA | Медицинский | ||
| Toda et al. [34] | 2 | 70 | 2/0 | HTN-CAD-PAD | Хирургический промежуточный трансплантат |
| Farooq et al. [35] | 2 | 68 | 2/0 | HTN (2) -PAD | ABI (1) -трубка (1) |
| Ganaha et al. [12] | 31 | 71 | 15/16 | HTN | Промежуточный стент-графт |
| Tsuji et al.[17] | 4 | 79,5 | 4/0 | HTN (4) -CAD (2) | EVAR (4) |
| Vasquez et al. [36] | 1 | 81 | 1/0 | HTN (1) | Стент-графт |
| Saiki et al. [37] | 1 | 81 | 0/1 | HTN (1) | Резекционный трансплантат (AFB) |
| Feld et al. [38] | 1 | 68 | 1/0 | CKD | EVAR (1) |
| Minor et al.[39] | 2 | 55 | 2/0 | HTN-CAD-PAD | ABI (2) |
| Ventura et al. [40] | 1 | 68 | 0/1 | HTN (1) | ABI |
| Takagi et al. [41] | 1 | 64 | 1/0 | NA | Хирургический промежуточный трансплантат |
| Batt et al. [18] | 8 | 70 | 7/1 | HTN (4) -CAD (3) -PAD (6) | Хирургический промежуточный трансплантат (5) (трубка 3-дакроновый аорто-подвздошный трансплантат 2) – EVAR (3) |
| Черненков и др.[42] | 1 | 80 | 1/0 | HTN | Трубка |
| Tanigushi et al. [43] | 1 | 82 | 0/1 | CAD | Трубка Хемашилда, левый аорторенальный обходной анастомоз |
| Sensi et al. [44] | 11 | 76,7 | 10/1 | HTN (9) -CKD (1) -CAD (6) | ABI (4) -трубка (1) – EVAR (6) |
| Eggebrecht et al. [45] | 22 | 69.1 | 16/6 | HTN (2) -CKD (9) -CAD (12) | EVAR (22) |
| Thalheimer et al. [46] | 1 | 57 | 1/0 | HTN-CAD-PAD | Трубка (1) |
| Dalainas et al. [47] | 2 | 68,6 | 2/0 | HTN (2) -CKD (2) -CAD (5) | EVAR (2) |
| Piffaretti et al. [48] | 13 | 73 | 12/1 | HTN (13) -CKD (2) -CAD (2) -PAD (6) | EVAR (13) |
| Fyntanidou et al.[49] | 4 | 67 | 4/0 | HTN (4) -CKD (1) -CAD (1) | EVAR (4) |
| Lindblad et al. [50] | 19 | 72 | 16/3 | NA | EVAR (19) |
| Afifi et al. [51] | 1 | 76 | 0/1 | HTN-CAD-PAD | EVAR (1) |
| Hyhlik-Dürr et al. [52] | 20 | 72 | 20/0 | HTN (19) -CKD (4) -CAD (8) | EVAR (20) |
| Kutsukata et al.[53] | 1 | 64 | 0/1 | HTN | Дакроновый аорто-подвздошный трансплантат (1) |
| Ferro et al. [54] | 1 | 64 | 0/1 | HTN-CAD | EVAR (1) |
| Kainuma et al. [55] | 1 | 67 | 1/0 | HTN | EVAR (1) |
| Nathan et al. [56] | 20 | NA | EVAR (10) – открытый ремонт (10) | ||
| Sadeghi-Azandaryani et al.[57] | 1 | 76 | 1/0 | HTN-CAD | EVAR (1) |
| Казань и др. [58] | 3 | 71 | 2/1 | HTN (1) -CAD | EVAR (3) |
| Palombo et al. [59] | 3 | 67 | 3/0 | HTN (3) -CKD (2) -CAD (4) -PAD (2) | EVAR (3) |
| Papazoglou et al. [60] | 1 | 69 | 1/0 | HTN | EVAR |
| Georgiadis et al.[61] | 19 | 70 | 18/1 | HTN (18) -CKD (8) -CAD (11) -PAD (9) | EVAR (19) |
| Всего | 230 | 49/164 (29,9%) a | 115/164 (70,1%) b |
Средний возраст пациентов составлял 72 года, и среди PAU почти преобладали мужчины ( 90,3%). Гипертония (80%) и сопутствующая окклюзионная болезнь коронарных или периферических артерий (30.7%) очень распространены. Бессимптомные ПАУ случайно выявляются в 40,3% зарегистрированных случаев. Большинство пациентов с ПАУ АА жалуются на боль (43,8%). У небольшой части (11,9%) пациентов наблюдается гиповолемический шок, вторичный по отношению к разрыву осложненной ПАУ. Большинство авторов указали на эндоваскулярную пластику стент-графта как на лечение выбора (62%), в то время как консервативное лечение было выбрано только для 2,6% пациентов. Открытое хирургическое вмешательство выполнено 35,4% пациентов.
В заключение, PAU обычно развиваются в грудном отделе аорты, но могут также возникать и в AA и могут прогрессировать в очаговую AD, SA или разрыв аорты.Симптоматическая ПАУ; большие, глубокие (> 2 см) ПАУ; и осложненная ПАУ AA (переходящая в SA или очаговую AD) требует хирургического лечения, если пациент подходит для операции. В данном случае мы провели открытую операцию в связи с более молодым возрастом и хорошим общим состоянием пациента; Тип трансплантата или раздвоенной трубки зависит от расположения ПАУ и состояния артериальной стенки. Эндоваскулярный доступ – менее инвазивная альтернатива открытой хирургии, с превосходными краткосрочными результатами, согласно недавней литературе.Однако в настоящее время недостаточно долгосрочных исследований ПАУ.
Проникающая язва аорты и интрамуральная гематома
Интрамуральная гематома аорты (ВМГ) – это острое заболевание аорты, которое определяется наличием кровоизлияния в стенке аорты и отсутствием признаков разрыва интимы. Проникающая язва аорты (ПАУ) – это хроническое заболевание аорты, определяемое язвенным разрывом созревания интимы в просвете аорты.IMH обычно проявляется гладкой интимой и некоторой степенью атеросклероза, тогда как PAU ассоциируется с системным атеросклерозом и, часто, утолщенной интимой с кратерами (рис. 1). Стэнсон и др. Точно описали ПАУ как изъязвление атероматозной бляшки, которое разрушает внутреннюю эластичную пластинку и способствует образованию гематомы в средах стенки аорты. 1
PAU может быть причиной IMH, который может развиться как расслоение аорты (AD). IMH отличается от AD отсутствием лоскута интимы. 2 Стэнфордская классификация определяет IMH аналогично AD: IMH типа A включает восходящую аорту и дугу, тогда как IMH типа B (IMHB) локализуется только в нисходящей грудной аорте. 3 Частота возникновения IMH и PAU до сих пор не выяснена. В литературе сообщалось о ИМГ с частотой от 2% до 45% (примерно 12% среди всех острых расслоений) на основании Международного реестра острых расслоений аорты (IRAD). 4,5 Имеется мало данных о заболеваемости ПАУ, хотя их количество составляет 2.Было описано от 3% до 7,6% у пациентов с симптомами. 6 У пациентов, поступивших с острым БА, язва была выявлена у 7,6%, что может указывать на то, что ПАУ вызывает расслоение чаще, чем считалось ранее. 6
ЭТИОЛОГИЯ
Этиология IMH и PAU остается предметом дискуссий. Оба объекта демонстрируют сходные механизмы воспаления и экспрессии матриксных металлопротеиназ и медиальных пролиферативных изменений с трансформацией гладкомышечных клеток от сократительного фенотипа к мутантному.Более того, у обоих обычно наблюдается апоптоз и медиальная дегенерация. 7 Предлагаемая концепция образования IMH заключается в том, что он возникает из-за разрыва vasa vasorum в медиальном слое стенки аорты, вызывая вторичный разрыв в направлении просвета аорты. 2 Гипертония и инфаркт стенки аорты связаны с этой патофизиологией. Другая гипотеза состоит в том, что IMH возникает из-за небольших входных разрывов в интиме с последующим тромбозом этих слез, что затрудняет обнаружение этих слез при визуализирующих исследованиях. 2,8 Хотя окончательного вердикта нет, несколько потенциальных факторов риска были идентифицированы для ИМГ, такие как пожилой возраст, большой диаметр аорты и увеличенная толщина стенки аорты. 4,5,9
PAU может развиваться в результате прогрессирующей эрозии атероматозных бляшек на стенах, проникая через эластичную пластинку. Было показано, что артериальная гипертензия, гиперлипопротеинемия и склероз аорты являются предрасполагающими признаками ПАУ. Поскольку все эти факторы чаще присутствуют у пожилых пациентов, ПАУ чаще встречается у пожилых людей. 10 Тем не менее, PAU может также возникать у молодых пациентов в результате разрывов интимы, которые остаются стабильными без прогрессирования AD или IMH. Осложненная ПАУ определяется развитием аневризм, псевдоаневризм, расслоений или разрывов аорты. Тщательная оценка ПАУ путем измерения диаметра и глубины язвы является обязательной для предотвращения аортальных осложнений. 11
ДИАГНОСТИКА
Клинический
На основании клинической оценки ИМГ нельзя надежно отличить от классической БА. 8 Tolenaar et al сравнили клиническую картину между IMHB и острым AD типа B (ABAD), показав, что IMHB проявляется преимущественно у мужчин (62% против 33%; P <0,001) в более старшем возрасте (69 ± 12 против 63 ± 14; P <0,001), чаще с болью в груди (80% против 69%; P = 0,020) и периаортальной гематомой (22% против 13%; P = 0,020). 5 Кроме того, у пациентов с IMHB реже наблюдались дефицит пульса и ишемия брыжейки / конечностей, 5 аналогично предыдущим наблюдениям. 9 Распространенность общего ИМГ среди пациентов с нетравматическим острым синдромом аорты колеблется от 6% до 50%. 9,12-17 Такое несоответствие может быть объяснено различиями в определении изображений и выборе пациентов: потенциально в справочных центрах могут чаще наблюдаться пациенты с ИМГ, у которых уже развился классический БА.
Клиническая картина ПАУ очень разнообразна. По сути, ПАУ – это бессимптомные поражения аорты, выявленные во время визуализации, показанной по другим причинам. 10 При сравнении PAU отдельно с PAU плюс IMH, две группы показали сходство по возрасту, распространенности сопутствующих заболеваний, частоте появления разрыва или степени восстановления. 18 ПАУ с ИМГ было связано с более высоким риском неэффективности лечения эндоваскулярной репарации аневризмы грудной клетки (TEVAR), определяемой как необходимость открытого или эндоваскулярного повторного вмешательства, разрыва аорты или смерти, связанной с аортой ( P = 0,03). В этой когорте у пациентов с ПАУ, ассоциированной с ИМГ, было больше неотложных вмешательств без разницы в выживаемости по всем причинам через 24 месяца. 18
Imaging
Когда-то считалось, что IMH встречается относительно редко по сравнению с AD. Однако, благодаря современной визуализации, в нескольких исследованиях наблюдалась распространенность IMH от 10% до 30% у пациентов с подозрением на AD. 11-14,16 Методы КТ и МРТ дополнительно подтвердили гипотезу о том, что IMH, PAU и AD могут быть вариантами одного и того же процесса. AD с тромбированным ложным просветом может напоминать IMH при визуализации, потому что входные слезы больше не видны.Для того, чтобы различать эти состояния, визуализация поперечного сечения считается золотым стандартом. При IMHB периаортальная гематома наблюдается чаще, чем у пациентов с ABAD. Наличие плеврального выпота может затруднить различие между неповрежденной и нарушенной адвентицией. Однако тесная связь между IMH и адвентицией может спровоцировать развитие периаортальной гематомы и разрыв. 5 Всесторонний анализ изображений может выявить специфические анатомические ключи, а также повреждения интимы внутренней кривизны дуги аорты, которые часто можно обнаружить у пациентов с ИМГ.Эти знаки могут быть полезны при указании и планировании TEVAR. 19
Для IMH аксиальная визуализация выявляет утолщение стенки аорты более чем на 0,5 см в виде эксцентрического или концентрического рисунка с линейным тангенциальным дефектом внутрипросветного наполнения в качестве отличительной особенности (рис. 2). Напротив, острая БА с тромбированным ложным просветом показывает криволинейные интрамуральные сгустки, часто не имеющие четко выраженной внешней стенки из-за гематомы средостения и плевральных выпотов. 11 В целом ИМГ чаще поражает нисходящую аорту с частотой от 50% до 85%. 4,5 Оценка измерений диаметра аорты у пациентов с IMHB и ABAD показала, что корень аорты и синотубулярное соединение были значительно больше у пациентов с ABAD (3,6 см против 3,4 см; P = 0,047 и 3,4 см против 3 см; P = 0,002, соответственно), тогда как максимальный диаметр нисходящей аорты был равен (оба 4 см). 5
Для PAU критерием визуализации является локализованное скопление контраста, выходящего из просвета (рис. 3). Некоторые исследователи показали, что ПАУ в основном располагается в нисходящей аорте (61.2%), затем абдоминальная (29,7%) и дугообразная (6,8%) (рисунки 4 и 5) локализации. 7,20 PAU может иметь множественные язвы и несколько диапазонов диаметра и глубины; тем не менее, показание к лечению было предложено, когда он распространяется более чем на 20 мм в глубину. 3,21 У этих пациентов настенный тромб имеет неровную поверхность просвета, которая может локально сужать просвет. Иными словами, тромб IMH имеет гладкую поверхность, представленную пластинкой аорты, и может распространяться в продольном направлении.
ПРОГНОЗ
IMH и PAU могут прогрессировать со смертельным исходом, особенно при наличии обоих заболеваний (рис. 6). IMH, сопутствующий PAU, связан с повышенным риском расширения и разрыва. 11,22 Для одного только IMH, даже если у 34% пациентов будет регресс, от 16% до 47% пациентов будут прогрессировать до развития AD, 2,9,22,23 и от 20% до 45% будут разовьется разрыв аорты. 2 Лучшим предиктором регресса IMH без осложнений является нормальный диаметр аорты в острой фазе. 17 Evangelista et al. Сообщили, что среди 68 пациентов с IMH у 22% развилась веретенообразная аневризма, у 8% – мешковидная аневризма и у 24% – псевдоаневризма (в среднем за 45 месяцев). 23 База данных IRAD недавно показала аналогичную годовую смертность IMH по сравнению с классической AD (5,3% против 8,7% и 10,3% против 8,2% для типов A и B, соответственно), без существенной разницы в общей внутрибольничной смертности. частота заболеваний нисходящей аорты (4,4% против 11,1%; P = 0,062) и восходящей аорты (26.6% против 26,5%; P = 0,998). 4 Подобно AD типа A, IMH с вовлечением восходящей аорты является летальным состоянием и является показанием для срочной операции из-за риска тампонады сердца, разрыва или сжатия устья коронарных артерий. 2,4,9 Сообщалось, что у пациентов с расслоением нисходящей аорты расширение живота значительно чаще встречается при ABAD по сравнению с IMH (64,9% против 40,2%; P <0,001). Иногда IMH может вызывать обструкцию боковой ветви аорты, что приводит к ишемии органа-мишени и требует интервенционной терапии. 5
Доказательства прогрессирования бессимптомной ПАУ ограничены. Формирование псевдоаневризмы может происходить от 15% до 50%. Связь диаметра ПАУ и риска разрыва остается неясной, хотя пациенты с диаметром язвы> 20 мм и / или глубиной язвы> 20 мм связаны с высоким риском прогрессирования заболевания и должны рассматриваться как возможные кандидаты на раннее эндоваскулярное или хирургическое восстановление. . 11,20
УПРАВЛЕНИЕ
Медицинский
Первичное ведение пациентов с неосложненной ИМГБ состоит из медикаментозной терапии и интенсивного наблюдения. 4,5,16 Медицинское лечение включает неотложную нормализацию артериального давления и снижение фракции выброса левого желудочка, поскольку они являются основными детерминантами расширения и разрыва расслоения. Было показано, что бета-блокаторы снижают смертность с 67% до 95% 22 , и их следует назначать в наиболее переносимых дозах. Блокаторы кальциевых каналов считаются альтернативным препаратом выбора. Для нормализации артериального давления, вызванного стимуляцией адренорецепторов, следует начать адекватную анальгетическую терапию, предпочтительно с сульфатом морфина. 8,11,16,20,22
В исследовании Tolenaar et al., Два пациента с IMHB и периаортальной гематомой умерли в результате разрыва аорты, несмотря на адекватное лечение, 5 подчеркивая важность периаортальной гематомы как фактора риска развития нежелательных явлений в неотложных случаях IMH. . Однако различие между периаортальной гематомой и плевральным выпотом имеет важное значение, поскольку плевральный выпот является не признаком надвигающегося разрыва аорты, а скорее реактивным скоплением жидкости в грудном отделе. 5 Для пациентов с IMHB рефрактерная боль в груди, признаки увеличения размера гематомы, разрыва аорты и прогрессирующего плеврального выпота являются показаниями для эндоваскулярного или хирургического лечения. 22 Всякий раз, когда IMH затрагивает восходящую аорту, значительно увеличивается уровень смертности, и необходимы срочные вторичные вмешательства. IMH, локализованный в дуге аорты или нисходящей аорте, с меньшей вероятностью будет связан с неблагоприятными исходами, и может быть проведена консервативная медикаментозная терапия. 9
В современной литературе нет убедительных рекомендаций по лечению бессимптомной ПАУ, выходящей за рамки контроля артериального давления. Однако симптоматическая ПАУ имеет разрушительное естественное течение с прогрессированием и разрывом; поэтому рекомендуется срочный ремонт. 11,20
Интервенционное лечение
Эндоваскулярное восстановление показано пациентам с симптоматическим / осложненным ИМГБ из-за риска разрыва 11,20,24 (Рисунок 7) и связано с более низкой периоперационной заболеваемостью и смертностью, чем открытое восстановление. 19,25-27 Очаговый характер поражения аорты делает пациентов с IMHB подходящими кандидатами для эндоваскулярного лечения. 5,7 Хотя в литературе нет убедительных рекомендаций по лечению IMH, кажется разумным, что это аналогично лечению AD в соответствующих сегментах аорты. 3,28 В настоящее время TEVAR показан пациентам с прогрессированием IMH в сторону явного расслоения или разрыва. 19,28
Дефекты интимы без IMH подходят для лечения TEVAR, если они локализованы в нисходящей аорте.Если поражена восходящая аорта, показано хирургическое вмешательство. 29 У пациентов с дефектами интимы и ИМГ наличие прилегающей атероматозной стенки должно способствовать более обширному лечению аорты с использованием более длинных эндотрансплантатов, поскольку неглубокие язвы часто недооцениваются при визуализации. Лечение более длинными эндотрансплантатами обеспечивает запас прочности при недостаточном лечении дефекта интимы. 21 Важным риском TEVAR при расширенном IMH является то, что эндотрансплантат может прорваться через интимальную поверхность в нижележащий тромбированный ложный просвет.Таким образом, эндотрансплантат должен быть закреплен в не вовлеченной стенке выше и ниже дефекта интимы. 3 Нет данных в поддержку профилактического применения TEVAR для пациентов с неосложненным ИМГ без дефекта интимы, хотя в некоторых случаях такое лечение проводилось. Открытая операция должна быть зарезервирована для пациентов, которым нельзя вылечить установку стент-графта, например, в случаях IMH с поражением восходящей дуги / дуги (рис. 8).
Для пациентов с PAU TEVAR оказался безопасным вариантом. 18 TEVAR особенно показан пациентам с симптомами ПАУ, осложненным формированием или разрывом псевдоаневризмы. 19 Пациенты с ПАУ часто старше и ослаблены, поэтому эндоваскулярная техника должна рассматриваться как оптимальная терапия. Однако у пациентов с ПАУ, осложненной ИМГ, остается дискуссия, следует ли проводить операцию в острой фазе или дождаться разрешения ВМГ, поскольку это может быть важным вопросом для повышения эффективности TEVAR на позднем этапе. Patel et al. Показали, что лечение TEVAR с распространением на дугу аорты было связано с лучшими долгосрочными результатами ( P =.011) и что TEVAR после PAU показал положительные результаты по сравнению с открытым хирургическим вмешательством. 30 Эндоваскулярное восстановление было связано с более короткой продолжительностью пребывания в больнице и аналогичными отдаленными результатами в популяции пациентов с ПАУ высокого риска по сравнению с открытым хирургическим вмешательством. 30 Пятилетний период отсутствия сердечно-сосудистых событий составил 67,8%. Учитывая потенциальную потребность в повторных вмешательствах, TEVAR становится препаратом первого выбора для пациентов с ПАУ. Однако из-за обширных атеросклеротических поражений дуги TEVAR приводил к более высокому уровню периоперационного инсульта (8.4% против 16,2%).
Последующее наблюдение
Рекомендуется 5-летнее наблюдение как для IMH типа A, так и для типа B. 31 Исследователи IRAD считают, что всем пациентам показана пожизненная медикаментозная терапия для строгого регулирования артериального давления. 5 Кроме того, сообщалось, что расширение аорты при IMHB во время последующего наблюдения было значительно реже по сравнению с пациентами ABAD (39% против 61%; P = 0,034). 5
ЗАКЛЮЧЕНИЕ
IMH и PAU – это различные заболевания аорты с разной эпидемиологией и патофизиологией, но строго связанные друг с другом.Хотя ИМГ возникает в острой форме, ПАУ является хроническим заболеванием, которое может быстро развиваться, причем оба протекают с непредсказуемым естественным течением. Лечение IMH аналогично классическому AD, с открытой операцией для лечения поражения восходящей аорты и TEVAR и / или медикаментозной терапией для пациентов только с нисходящей локализацией, на основе подхода, специфичного для осложнения. PAU имеет различные формы проявления и неизвестную частоту, которую можно недооценить, поскольку она часто сопровождается высокой частотой бессимптомных поражений.Поскольку ПАУ поражает преимущественно пожилых пациентов, при наличии показаний ТЭВАР является методом выбора.
Фоке Наута, доктор медицины, из Центра исследования торакальной аорты, Policlinico San Donato IRCCS, Миланский университет в Италии. Он заявил, что не имеет финансовых интересов, связанных с этой статьей.
Арнуд Камман, доктор медицины, из Центра исследования грудной аорты, Policlinico San Donato IRCCS, Миланский университет в Италии. Он заявил, что не имеет финансовых интересов, связанных с этой статьей.
Санти Тримарчи, доктор медицины, из Центра исследования торакальной аорты, Policlinico San Donato IRCCS, Миланский университет в Италии. Он заявил, что не имеет финансовых интересов, связанных с этой статьей. С доктором Тримарчи можно связаться по телефону +39 02 5277 4344; [email protected].
- Stanson AW, Kazmier FJ, Hollier LH, et al. Проникающие атеросклеротические язвы грудного отдела аорты: естественное течение и клинико-патологические корреляции. Ann Vasc Surg. 1986; 1: 15-23.
- Nienaber CA, Eagle KA.Расслоение аорты: новые рубежи в диагностике и лечении: Часть I: От этиологии к диагностическим стратегиям. Тираж. 2003; 108: 628-635.
- Хирацка Л.Ф., Бакрис Г.Л., Бекман Дж. А. и др. Руководство ACCF / AHA / AATS / ACR / ASA / SCA / SCAI / SIR / STS / SVM, 2010 г., по диагностике и ведению пациентов с заболеванием грудной аорты: отчет Фонда Американского колледжа кардиологов / Целевой группы по практике Американской кардиологической ассоциации Рекомендации, Американская ассоциация торакальной хирургии, Американский колледж радиологии, Американская ассоциация инсультов, Общество сердечно-сосудистых анестезиологов, Общество сердечно-сосудистой ангиографии и вмешательств, Общество интервенционной радиологии, Общество торакальных хирургов и Общество сосудистой медицины.Тираж. 2010; 121: e266-369.
- Харрис К.М., Браверман А.С., Игл К.А. и др. Острая интрамуральная гематома аорты: анализ Международного реестра острых расслоений аорты. Тираж. 2012; 126 (приложение 1): S91-96.
- Tolenaar JL, Harris KM, Upchurch GR Jr, ди Eusanio Met al; Следователи IRAD. Различия и сходство между интрамуральной гематомой нисходящей аорты и острым расслоением типа B. J Vasc Surg. 2013; 58: 1498-1504.
- D’Souza S, Duncan A, Aguila F, et al.TEVAR при неаневризматической патологии грудной аорты. Катетер Cardiovasc Interv. 2009; 74: 783-786.
- Sundt TM. Интрамуральная гематома и проникающая атеросклеротическая язва аорты. Ann Thorac Surg. 2007; 83: S835-841; обсуждение S846-850.
- Nienaber CA, Sievers HH. Интрамуральная гематома при остром аортальном синдроме; более одного варианта вскрытия? Тираж. 2002; 106: 284-285.
- Evangelista A, Mukherjee D, Mehta RH и др .; Следователи IRAD. Острая интрамуральная гематома аорты: загадка эволюции.Тираж. 2005; 111: 1063–1070.
- Чо К.Р., Стэнсон А.В., Поттер Д.Д. и др. Проникающая атеросклеротическая язва нисходящей грудной аорты и дуги. J Thorac Cardiovasc Surg. 2004; 127: 1393-1401.
- Ганаха Ф., Миллер Д.К., Сугимото К. и др. Прогноз интрамуральной гематомы аорты с проникающей атеросклеротической язвой и без нее: клинический и рентгенологический анализ. Тираж. 2002; 106: 342-348.
- O’Gara PT, DeSanctis RW. Острое расслоение аорты и его варианты.Тираж. 1995; 92: 1376-1378.
- Nienaber CA, von Kodolitsch Y, Petersen B, et al. Интрамуральное кровоизлияние в грудную аорту: диагностические и терапевтические значения. Тираж. 1995; 92: 1465-1472.
- Симидзу Х., Йохино Х., Удагава Х. и др. Прогноз интрамурального кровотечения по сравнению с классическим расслоением аорты. Am J Cardiol. 2000; 85: 792-795.
- Сонг Дж. К., Ким Х. С., Сон Дж. М. и др. Результаты лечения пациентов с интрамуральной гематомой аорты. Am J Med.2002; 113: 181-187.
- von Kodolitsch Y, Csösz S, Koschyk DH, et al. Интрамуральная гематома аорты: предикторы прогрессирования расслоения и разрыва. Тираж. 2003; 107: 1158-1163.
- Евангелиста А., Домингес Р., Себастия С. и др. Прогностическое значение клинических и морфологических данных в краткосрочной эволюции интрамуральной гематомы аорты: терапевтическое значение. Eur Heart J. 2004; 25: 81-87.
- Patel HJ, Williams DM, Upchurch GR Jr и др. Проблема ассоциированной интрамуральной гематомы с эндоваскулярным восстановлением проникающих язв нисходящей грудной аорты.J Vasc Surg. 2010; 51: 829-835.
- Eggebrecht H, Plicht B, Kahlert P, et al. Интрамуральная гематома и проникающие язвы: показания к эндоваскулярному лечению. Eur J Vasc Endovasc Surg. 2009; 38: 659-665.
- Натан Д.П., Бунн В., Лай Е. и др. Проявление, осложнения и естественное течение проникающей атеросклеротической язвенной болезни. J Vasc Surg. 2012; 55: 10-15.
- Svensson LG, Kouchoukos NT, Miller DC, et al. Согласованный экспертный документ по лечению заболеваний нисходящей грудной аорты с использованием эндоваскулярных стент-графтов.Ann Thorac Surg. 2008; 85 (1 доп.): С1-41.
- Ince H, Nienaber CA. Диагностика и ведение пациентов с расслоением аорты. Сердце. 2007; 93: 266-270.
- Евангелиста А., Домингес Р., Себастия С. и др. Долгосрочное наблюдение за интрамуральной гематомой аорты: предикторы исхода. Тираж. 2003; 108: 583-589.
- Nienaber CA, Fattori R, Lund G, et al. Нехирургическая реконструкция расслоения грудной аорты с установкой стент-графта. N Engl J Med. 1999; 340: 1539-1545.
- Leurs L, Bell R, Degrieck Y, et al; EUROSTAR, сотрудники Регистра торакальных эндотрансплантатов Великобритании.Эндоваскулярное лечение заболеваний грудной аорты: совокупный опыт регистров торакальных эндотрансплантатов EUROSTAR и Соединенного Королевства. J Vasc Surg. 2004; 40: 670-679.
- Geisbüsch P, Kotelis D, Weber TF, et al. Ранние и среднесрочные результаты после эндоваскулярной пластики проникающих язв аорты стент-графтом. J Vasc Surg. 2008; 48: 1361-1368.
- Clough RE, Mani K, Lyons OT, et al. Эндоваскулярное лечение острого аортального синдрома. J Vasc Surg. 2011; 54: 1580-1587.
- Erbel R, Aboyans V, Boileau C, et al; Авторы / члены рабочей группы.Руководство ESC 2014 г. по диагностике и лечению заболеваний аорты: документ, охватывающий острые и хронические заболевания аорты грудной и брюшной аорты у взрослых. Целевая группа по диагностике и лечению заболеваний аорты Европейского общества кардиологов (ESC). Eur Heart J. 29 августа 2014 г. pii: ehu281. [Epub перед печатью]
- Уильямс Д.М., Кронин П., Дасика Н. и др. Псевдоаневризмы артерии ветви аорты, сопровождающие расслоение аорты. Часть I: Анатомия псевдоаневризмы.J Vasc Interv Radiol. 2006; 17: 765-771.
- Patel HJ, Sood V, Williams DM, et al. Поздние результаты лечения проникающих язв грудной аорты: преимущества эндоваскулярного доступа. Ann Thorac Surg. 2012; 94: 516-522; обсуждение: 522-523.
- Moizumi Y, Komatsu T, Motoyoshi N и др. Клинические особенности и отдаленные исходы интрамуральной гематомы аорты типа А и типа В. J Thorac Cardiovasc Surg. 2004; 127: 421-427.
Проникающая атеросклеротическая язва восходящей аорты с гемоперикардом: история болезни | Journal of Cardiothoracic Surgery
PAU обычно возникает у пожилых мужчин с гипертонией, употреблением табака и ишемической болезнью сердца [5].Это поражение может вызвать интрамуральное кровоизлияние, аневризму аорты, псевдоаневризму или даже расслоение аорты. ПАУ обычно затрагивает нисходящую аорту и, хотя редко в восходящей аорте, обычно приводит к летальному исходу [6] при разрыве. Coady et al. [6] показали, что частота разрыва аорты заметно выше для интрамуральной гематомы (35%) и PAU (42%), чем для расслоения аорты (тип A 7,5%, тип B 4,1%). ПАУ часто протекает бессимптомно и почти всегда диагностируется случайно. Первоначальный клинический вид ПАУ аналогичен таковому при классическом расслоении аорты.Важно дифференцировать ПАУ от других ААС, а также от острой тромбоэмболии легочной артерии и острого инфаркта миокарда. Мы можем дифференцировать все эти заболевания в отделении неотложной помощи на основе истории болезни пациента, физикального обследования, электрокардиографии, сердечных биомаркеров, D-димеров, трансторакальной эхокардиографии, чреспищеводной эхокардиографии, рентгенографии грудной клетки, компьютерной томографии и магнитно-резонансной томографии. Поскольку компьютерная томография обеспечивает быструю и высококачественную реконструкцию двух- и трехмерного изображения, это лучший метод диагностики ПАУ, которая проявляется в виде очагового контрастного выхода с неровными краями, которые выходят за пределы ожидаемых границ стенки аорты, как правило. связано с тяжелым атероматозным заболеванием [5].Хотя ПАУ имеет высокий риск разрыва аорты, некоторые авторы считают, что немедленное хирургическое лечение не всегда требуется, поскольку болезнь может иметь доброкачественное течение. В исследовании Harris et al. [7], у нескольких пациентов во время наблюдения развилось расслоение аорты или разрыв аорты. Кроме того, эти авторы подчеркнули, что по сравнению с риском острого разрыва аорты, большинство пациентов с ПАУ подвергались более высокому риску хирургического вмешательства из-за их преклонного возраста и плохого общего состояния здоровья. Более того, хирургическое лечение нисходящей грудной аорты часто связано с такими осложнениями, как респираторное заболевание, почечная недостаточность или ишемия позвоночника.По этим причинам пациенты с ПАУ с вовлечением нисходящей аорты могут первоначально лечиться консервативно с агрессивной медикаментозной терапией и тщательным наблюдением, как при расслоении нисходящей аорты [8]. Хирургическое вмешательство становится необходимым при появлении признаков расширения интрамуральной гематомы (ВМГ), разрыва перикардиальной или плевральной полости, непреодолимой боли в груди и нестабильности гемодинамики. Кроме того, пациенты с ПАУ должны находиться под наблюдением, особенно в течение первого месяца после появления ААС [2].Однако пациентам с ПАУ в восходящей аорте, даже бессимптомным пациентам, хирургическое вмешательство рекомендуется как можно скорее, поскольку они имеют высокий риск развития классического расслоения аорты типа А, ВМГ типа А или острого разрыва восходящей аорты с тампонада сердца. Благодаря усовершенствованию эндоваскулярных методик и развитию устройств, эндоваскулярное восстановление грудной аорты (TEVAR) стало подходом первой линии при заболеваниях аорты из-за высокого технического успеха (96.4–98,3%) и низкие показатели заболеваемости и смертности [9, 10]. Было доказано, что TEVAR дает отличные краткосрочные и среднесрочные результаты при ПАУ нисходящей аорты и является первой линией лечения, когда показано вмешательство. Однако TEVAR PAU в восходящей аорте встречается редко, поскольку PAU обычно обнаруживается случайно у бессимптомных пациентов и осложняется расслоением аорты, IMH или острым разрывом аорты у пациентов с AAS. Обычный открытый ремонт по-прежнему является первоочередной задачей в большинстве этих случаев.Эндоваскулярная терапия восходящей аорты часто используется как «средство спасения» за пределами предполагаемого показания. Однако несколько исследований подтвердили безопасность и возможность эндоваскулярного восстановления восходящей аорты у пациентов из группы высокого риска, не подходящих для открытого восстановления [11, 12]. Совсем недавно Хойнежад и др. [13] разработали одобренное FDA исследование по освобождению исследуемых устройств под эгидой FDA для изучения результатов эндоваскулярного восстановления восходящей аорты. Они продемонстрировали положительное ремоделирование исключенных сегментов аорты, как и в исследованиях наблюдения с участием нисходящей аорты.Хотя в исследование были включены только шесть пациентов и только один из них был показан из-за восходящей ПАУ, мы ожидаем, что эндоваскулярное восстановление может быть осуществимо у пациентов с ПАУ в восходящей аорте в будущем.
Проникающая атеросклеротическая язва аорты – wikidoc
Главный редактор: C. Майкл Гибсон, M.S., M.D. [1]; Заместитель главного редактора: Сахар Мемар Монтазерин, доктор медицины [2] Джафер Зоркун, доктор медицинских наук, [3]
Синонимы и ключевые слова: : Проникающая язва аорты
Обзор
Проникающая атеросклеротическая язва аорты – это изъязвление атероматозной бляшки, которое разрушило внутренний эластичный слой стенки аорты, достигло медиального слоя и привело к образованию гематомы в средней части.
Историческая перспектива
- В 1934 году доктор Шеннан первым описал термин «проникающая атеросклеротическая язва аорты». [2]
- В 1986 году доктор Стэнсон дал дальнейшее определение этому заболеванию. [3]
Классификация
- Проникающая атеросклеротическая язва аорты классифицируется аналогично расслоению аорты.
- Узнайте больше о классификации расслоения аорты, щелкнув здесь.
Патофизиология
Причины
Отличие проникающей атеросклеротической язвы аорты от других заболеваний
- Проникающую атеросклеротическую язву аорты необходимо дифференцировать от других заболеваний, вызывающих внезапную острую боль в груди, одышку и боль в спине. Такие состояния могут включать расслоение аорты, острый коронарный синдром и интрамуральную гематому аорты.
- Другие дифференциальные диагнозы проникающей атеросклеротической язвы аорты включают воспалительную аневризму аорты и состояния, вызывающие воспалительный аортит, такие как артериит Такаясу, гигантоклеточный артериит, болезнь Бехчета, болезнь Кавасаки, ревматоидный артрит, саркоидоз, синдром Когана, синдром анкилозирующего эхондроза и т. гранулематоз. [4]
- Для получения дополнительной информации о дифференциальной диагностике проникающей атеросклеротической язвы аорты щелкните здесь.
Эпидемиология и демография
- Точная распространенность проникающей атеросклеротической язвы аорты неизвестна.
- Частота проникающей атеросклеротической язвы аорты составляет 1,62 на 100 000 человек во всем мире. [5]
- В отличие от типичного расслоения аорты, проникающие атеросклеротические язвы аорты чаще всего возникают у пожилых пациентов с тяжелым атеросклерозом. [4]
- Это обычно поражает людей на седьмом десятилетии жизни или в более старшем возрасте. [3]
- Проникающая атеросклеротическая язва аорты чаще поражает мужчин, чем женщин.
Факторы риска
Скрининг
- Недостаточно доказательств, чтобы рекомендовать рутинный скрининг на проникающую атеросклеротическую язву аорты.
Естественное течение, осложнения и прогноз
Диагностика
Диагностическое исследование выбора
- В таблице ниже представлено сравнение исследований с диагностической визуализацией для диагностики проникающей атеросклеротической язвы аорты: [10]
Анамнез и симптомы
Медицинский осмотр
Результаты лабораторных исследований
- Нет диагностических лабораторных данных, связанных с проникающей атеросклеротической язвой аорты.
Электрокардиограмма
- Нет данных ЭКГ, связанных с проникающей атеросклеротической язвой аорты.
| Проникающая атеросклеротическая язва аорты [12] |
Рентгеновский снимок
Эхокардиграфия
КТ
- КТ с внутривенным контрастированием – это предпочтительное диагностическое исследование для диагностики проникающей атеросклеротической язвы аорты. [7]
- Находки, указывающие на проникающую атеросклеротическую язву аорты, включают локализованную язву, переходящую из интимы в стенку аорты, или утечку контраста через кальцинированную бляшку.
- Обычно поражает среднюю и дистальную треть нисходящей аорты.
- Язва обычно определяется очаговым утолщением или увеличением стенки аорты.
МРТ
- МРТ превосходит обычную компьютерную томографию в диагностике проникающей атеросклеротической язвы аорты. [17]
- Обнаружение, указывающее на диагноз, включает четко выраженную язву с феноменом пустотного потока на изображениях T1.
Другие результаты визуализации
- Результаты КТ-ангиографии, связанные с проникающей атеросклеротической язвой аорты, могут включать наличие ложной аневризмы.
Другие диагностические исследования
- Нет других диагностических исследований, связанных с проникающей атеросклеротической язвой аорты.
Лечение
| Проникающая атеросклеротическая язва аорты с ложной аневризмой [18] |
Лечебная терапия
- Лечение направлено на предотвращение развития проникающей атеросклеротической язвы аорты в расслоение аорты.Показания к лечебным вмешательствам включают рецидивирующую и рефрактерную боль, признаки локализованного разрыва, быстро растущую язву аорты и наличие периаортальной гематомы или плеврального выпота. [19] [20]
- Раннее вмешательство показано при язве диаметром более 20 мм.
Хирургический
- Хирургические вмешательства могут быть показаны при проникающей атеросклеротической язве аорты в зависимости от анатомического расположения язвы, клинической картины и сопутствующих заболеваний.Однако, поскольку большинство пациентов не подходят для хирургического вмешательства из-за преклонного возраста и сопутствующих заболеваний, эндоваскулярная реконструкция аорты (TEVAR) используется чаще. [20] [21]
Первичная профилактика
- Нет установленных мер по первичной профилактике проникающей атеросклеротической язвы аорты.
Вторичная профилактика
- Нет установленных мер для вторичной профилактики проникающей атеросклеротической язвы аорты.
Указания
Руководство ESC по диагностике и лечению заболеваний аорты, 2014 г. (НЕ РЕДАКТИРОВАТЬ)
[10]| Рекомендации | Класс | Уровень |
|---|---|---|
| я | С | |
| IIa | С |
| я | С |
| я | С | |
| IIa | С |
| IIb | С |
Сокращения: CT : компьютерная томография; MRI : магнитно-резонансная томография; PAU : проникающая язва аорты; TEVAR : эндоваскулярное восстановление грудной аорты.
См. Также
Внешние ссылки
Список литературы
- ↑ Дело любезно предоставлено доктором Винсентом Татко, Radiopaedia.org, rID: 48455
- ↑ Пири, Томас М. (1936). «Расслаивающие аневризмы аорты». Американский журнал сердца . 12 (6): 650–665. DOI: 10.1016 / S0002-8703 (36) -3. ISSN 0002-8703.
- ↑ 3,0 3,1 3,2 3,3 3,4 Стэнсон, Энтони У.; Kazmier, Francis J .; Холлиер, Ларри Х .; Эдвардс, Уильям Д .; Пайролеро, Питер С .; Шиди, Патрик Ф .; Джойс, Джон В .; Джонсон, Микаэль С. (1986). «Проникающие атеросклеротические язвы грудного отдела аорты: естественное течение и клинико-патологические корреляции». Анналы сосудистой хирургии . 1 (1): 15–23. DOI: 10.1016 / S0890-5096 (06) 60697-3. ISSN 0890-5096.
- ↑ 4,0 4,1 4,2 Котсис, Томас; Спиропулос, Базилей Георгиу; Асалумидис, Николаос; Христофору, Панагица; Кацени, Константина; Папаконстантину, Иоаннис (2019).«Проникающие атеросклеротические язвы брюшной аорты: отчет о болезни и обзор литературы». Международный специалист по сосудистым заболеваниям . 35 (3): 152–159. DOI: 10.5758 / vsi.2019.35.3.152. ISSN 2288-7970.
- ↑ 5,0 5,1 DeMartino, Randall R .; Сен, Индрани; Хуанг, Инь; Бауэр, Томас С.; Одерич, Густаво С .; Почеттино, Альберто; Гризон, Кевин; Калра, Манджу; Джонстон, Джилл; Шуджа, Фахад; Хармсен, В. Скотт; Маседо, Танила; Мандрекар, Джей; Чемберлен, Аланна М.; Вайс, Саломея; Гудни, Филип П.; Роджер, Вероник (2018). «Оценка населения заболеваемости расслоением аорты, интрамуральной гематомой и проникающей язвой и связанной с ней смертностью с 1995 по 2015 год». Кровообращение: качество сердечно-сосудистой системы и результаты . 11 (8). DOI: 10.1161 / CIRCOUTCOMES.118.004689. ISSN 1941-7713.
- ↑ Coady, Michael A .; Риццо, Джон А .; Элефтериадес, Джон А. (1999). «ПАТОЛОГИЧЕСКИЕ ВАРИАНТЫ РАССЕКЦИИ ГОЛОВНОЙ АОРТЫ». Кардиологическая клиника . 17 (4): 637–657. DOI: 10.1016 / S0733-8651 (05) 70106-5. ISSN 0733-8651.
- ↑ 7,0 7,1 7,2 Хаяси, Хидеюки; Мацуока, Йоджиро; Сакамото, Ичиро; Суэёси, Эйдзун; Окимото, Томоаки; Хаяси, Куниаки; Мацунага, Наофуми (2000). «Проникающая атеросклеротическая язва аорты: особенности визуализации и концепция заболевания». РадиоГрафика . 20 (4): 995–1005. DOI: 10.1148 / радиография.20.4.g00jl01995. ISSN 0271-5333.
- ↑ Уэда, Такуя; Чин, Энн; Петрович, Иван; Флейшманн, Доминик (2012). «Наглядный обзор острого аортального синдрома: отличительные и перекрывающиеся особенности, выявленные с помощью мультидетекторной КТ-ангиографии с ЭКГ-синхронизацией». Анализ изображений . 3 (6): 561–571. DOI: 10.1007 / s13244-012-0195-7. ISSN 1869-4101.
- ↑ Натан, Дерек П .; Бунн, Уильям; Лай, Эрик; Ван, Грейс Дж .; Десаи, Нимеш; Ву, Эдвард Ю.; Fairman, Ronald M .; Джексон, Бенджамин М. (2012). «Представление, осложнения и естественное течение проникающей атеросклеротической язвенной болезни». Журнал сосудистой хирургии . 55 (1): 10–15. DOI: 10.1016 / j.jvs.2011.08.005. ISSN 0741-5214.
- ↑ 10,0 10,1 Эрбель Р., Абояс В., Буало С., Боссоне Э, Бартоломео Р. Д., Эггебрехт Х., Евангелиста А., Фальк В., Франк Н., Гэмперли О., Грабенвёгер М., Хаверих А., Иунг Б., Манолис А. Дж. , Meijboom F, Nienaber CA, Roffi M, Rousseau H, Sechtem U, Sirnes PA, Allmen RS, Vrints CJ (ноябрь 2014 г.).”Рекомендации ESC по диагностике и лечению заболеваний аорты: документ, охватывающий острые и хронические заболевания аорты грудной и брюшной аорты у взрослых. Целевая группа по диагностике и лечению заболеваний аорты Европейского общества кардиологов (ESC) “. Eur. Сердце J . 35 (41): 2873–926. DOI: 10,1093 / eurheartj / ehu281. PMID 25173340.
- ↑ 11,0 11,1 Боссоне, Эдуардо; ЛаБаунти, Трой М; Орел, Ким А. (2018).«Острые синдромы аорты: диагностика и лечение, актуальная информация». Европейский журнал сердца . 39 (9): 739–749d. DOI: 10.1093 / eurheartj / ehx319. ISSN 0195-668X.
- ↑ Дело любезно предоставлено профессором Франком Гайяром, Radiopaedia.org, rID: 10163
- ↑ Эггебрехт, Хольгер; Баумгарт, Дитрих; Шмермунд, Аксель; Герольд, Ульф; Хунольд, Питер; Якоб, Хайнц; Эрбель, Раймунд (2003). «Проникающая атеросклеротическая язва аорты: лечение эндоваскулярной установкой стент-графта». Текущее мнение в области кардиологии . 18 (6): 431–435. DOI: 10.1097 / 00001573-200311000-00002. ISSN 0268-4705.
- ↑ Чжо, Хтоо; Садик, Сана; Чоудхури, Арнаб; Голамрезаи, Рашин; Йо, Линус (2016). «Нечастая причина боли в груди – проникающая атеросклеротическая язва аорты». Журнал перспектив внутренней медицины общественной больницы . 6 (3): 31506. DOI: 10.3402 / jchimp.v6.31506. ISSN 2000-9666.
- ↑ Зоммер Т., Фешке В., Хольцкнехт Н., Смекал А.В., Келлер Э., Люттербей Дж., Крефт Б., Куль С., Гизеке Дж., Абу-Рамадан Д., Шильд Х (май 1996 г.).«Расслоение аорты: сравнительное исследование диагностики с помощью спиральной КТ, мультипланарной чреспищеводной эхокардиографии и МРТ». Радиология . 199 (2): 347–52. DOI: 10.1148 / радиология.199.2.8668776. PMID 8668776.
- ↑ Дело любезно предоставлено профессором Франком Гайяром, Radiopaedia.org, rID: 10163
- ↑ Harris, James A .; Бис, Костаки Г .; Гловер, Джон Л .; Бендик, Филип Дж .; Шетти, Анил; Браун, О. Уильям (1994). «Проникающие атеросклеротические язвы аорты». Журнал сосудистой хирургии . 19 (1): 90–99. DOI: 10.1016 / S0741-5214 (94) 70124-5. ISSN 0741-5214.
- ↑ Дело любезно предоставлено профессором Франком Гайяром, Radiopaedia.org, rID: 10163
- ↑ Ганаха, Фумикио; Миллер, Д. Крейг; Сугимото, Кодзи; До, Ён Су; Минамигучи, Хироки; Сайто, Харуо; Митчелл, Р. Скотт; Дэйк, Майкл Д. (2002). «Прогноз интрамуральной гематомы аорты с проникающей атеросклеротической язвой и без нее». Тираж . 106 (3): 342–348. DOI: 10.1161 / 01.CIR.0000022164.26075.5A. ISSN 0009-7322.
- ↑ 20,0 20,1 Эггебрехт, Хольгер; Герольд, Ульф; Шмермунд, Аксель; Линд, Александр Ю .; Кунт, Оливер; Мартини, Стефан; Кюль, Хильмар; Кинбаум, Питер; Петерс, Юрген; Якоб, Хайнц; Эрбель, Раймунд; Баумгарт, Дитрих (2006). «Эндоваскулярное лечение стент-графтом проникающей язвы аорты». Американский журнал сердца . 151 (2): 530–536. DOI: 10.1016 / j.ahj.2005.05.020. ISSN 0002-8703.
- ↑ Демерс, Филипп; Миллер, Д. Крейг; Митчелл, Р. Скотт; Ки, Стивен Т; Чагонджян, Линн; Дэйк, Майкл Д. (2004). «Восстановление проникающих атеросклеротических язв в нисходящей грудной аорте стент-графтом: среднесрочные результаты». Летопись торакальной хирургии . 77 (1): 81–86. DOI: 10.1016 / S0003-4975 (03) 00816-6. ISSN 0003-4975.
Шаблон: WikiDoc Sources
Язва другого типа: проникающая язва аорты
Введение
Язвы.Все о них слышали. Вы знаете, проблема с пищеварением, которая возникает из-за слишком большого количества желудочного сока и облегчается антацидами. Вид, вызывающий боли в животе. Скорее всего, вы слышали термин «кислый желудок».
Ну угадайте, что? «Язва» – это более общий медицинский термин, описывающий дискретную локализованную эрозию биологической поверхности. В случае язвы желудка (желудка) происходит эрозия защитной оболочки желудка, которая вызывает боль из-за того, что более глубокие ткани стенки желудка подвергаются воздействию желудочной кислоты, и это связано с употреблением острой пищи.
Определение проникающих язв аорты
Аорта, как и желудок, также склонна к развитию язв. Официальный медицинский термин – «проникающие язвы аорты», сокращенно PAU. Другой термин для этого состояния – «проникающая атеросклеротическая язва». Как вы помните, аорта – это кровеносный сосуд (самый большой в организме!). Стенка аорты состоит из трех слоев: интимы, среднего и адвентициального.
Внутренний слой аорты – это тонкий непрерывный слой клеток, называемый эндотелием, который выстилает внутреннюю часть аорты.Эти клетки находятся в прямом контакте с кровью. Подумайте о своем газоне. Дерн, сидящий поверх грязи, похож на эндотелиальный слой аорты.
Проникающие язвы аорты – это заболевание, состоящее из очаговой эрозии эндотелия аорты. Это означает, что небольшой участок листа клеток, выстилающий клетки аорты, исчезает.
PAU являются частью спектра заболеваний аорты, называемых острым аортальным синдромом (тема будущего сообщения).
Вернувшись во двор, представьте себе небольшой участок мертвой травы на лужайке, где внизу обнажена грязь, а вся трава исчезла.
Патофизиология проникающих язв аорты
В нормальном здоровом состоянии внутренняя оболочка аорты состоит из сияющего блеска здоровых клеток. Однако блестящий блеск может стать тусклым и неравномерным в результате атеросклеротического заболевания.
Атеросклероз – это дегенеративный процесс, обычно связанный со старением, когда организм откладывает холестерин и кальций в слизистой оболочке кровеносного сосуда (в данном случае аорты).
Эти атеросклеротические отложения могут быть большими или маленькими.Когда в атеросклеротическом отложениях (одном конкретном участке стенки аорты) содержится чрезмерное количество кальция, это называется «бляшкой». Бляшки могут образовываться в любом месте сосудистой сети тела, а когда они возникают в аорте, могут возникнуть проблемы.
Аорта представляет собой гибкую и эластичную структуру, которая расширяется и сжимается вместе с импульсом. Пульс представляет собой динамическое изменение кровеносного сосуда, связанное с выбросом крови из сердца. Биение сердца вызывает прилив крови из сердца, который заставляет аорту физически расширяться и сокращаться.
С увеличением жесткости стенки аорты, связанной с атеросклерозом, по мере старения, напряжения и деформации стенки аорты изменяются в зависимости от кровотока. Когда есть бляшка из холестерина и кальция в сочетании с жесткой аортой, эти бляшки могут внезапно разорваться.
Когда бляшка разрывается, кровь просачивается под поверхность эндотелиальных клеток и вызывает разрушение внутренней оболочки стенки аорты.
Альт! Это разрушение стенки аорты в результате разрыва бляшки представляет собой проникающую язву аорты.Помимо язвы возникает интрамуральная гематома (кровотечение в стенку аорты).
Как часто возникают проникающие язвы аорты?
Проникающие язвы аорты (ПАУ) встречаются примерно у 7-8% всех пациентов с заболеванием аорты.
Каковы симптомы проникающей язвы аорты?
Самый частый симптом – боль в спине. Большинство пациентов описывают это как новую боль в середине спины между лопатками. Боль может быть острой и колющей или тупой и иррадирующей.Острая колющая боль обычно локализуется в одной точке спины. Тупая, излучающая боль обычно распространяется по всей верхней части спины.
Другие симптомы включают боль в груди, которая по характеристикам схожа с болью, связанной с сердечным приступом. Если проникающая язва аорты расположена в брюшной аорте, боль будет в пояснице. В 20% случаев у пациентов с проникающими язвами аорты симптомы отсутствуют.
Как узнать, есть ли у вас проникающая язва аорты?
В большинстве случаев вы не можете определить, есть ли у вас проникающая язва аорты.Эти проникающие язвы аорты развиваются внезапно (буквально при ударе сердца). Если боль настолько сильна, что вам нужно обратиться в отделение неотложной помощи, врачи проведут серию анализов.
Если компьютерная томография выполняется во время посещения отделения неотложной помощи (а так и должно быть), то проникающую язву аорты обычно можно диагностировать по эрозии и гематоме стенки аорты.
Однако многие пациенты ходят без каких-либо признаков или симптомов и не подозревают, что у них проникающая язва аорты.
Каков риск для здоровья проникающей язвы аорты?
Как упоминалось выше, проникающие язвы аорты являются частью спектра острого аортального синдрома. Риск проникающей язвы аорты заключается в том, что аорта может разорваться. Язвы на стенке аорты – это буквально дефект, который снижает целостность стенки аорты. В случае разрыва аорты массивное внутреннее кровотечение может привести к смерти.
Проникающие язвы аорты также могут привести к расслоению аорты.Мы обсуждали расслоение аорты в предыдущем посте ЗДЕСЬ. Расслоение аорты – это совершенно другое неотложное состояние аорты, которое также несет в себе риск смерти.
Каковы факторы риска развития проникающей болезни аорты?
Как и большинство заболеваний аорты, включая аневризмы аорты и расслоение аорты, высокое кровяное давление (гипертония), повышенный уровень холестерина в крови (гиперхолестеринемия) и атеросклероз в анамнезе увеличивают риск развития проникающих язв аорты.
Для получения дополнительной информации о факторах риска развития заболевания аорты загрузите свою копию моей книги здесь.
Что делать, если вы подозреваете, что у вас проникающая язва аорты?
В большинстве случаев проникающие язвы аорты выявляются с помощью ряда тестов, включая компьютерную томографию, которые выполняются при появлении новой, сильной боли в груди или спине в отделении неотложной помощи.
Если у вас есть какие-либо факторы риска развития заболевания аорты, упомянутые выше, то вы должны считаться обследованным специалистом по аорте.
Каковы методы лечения проникающих язв аорты?
Многие проникающие язвы аорты можно лечить с помощью лекарств. Эти лекарства предназначены для значительного контроля артериального давления и холестерина в крови. Если язвы разрастутся, они могут превратиться в псевдоаневризму аорты, которая потенциально потребует хирургического вмешательства или лечения аортальным стентом.
Аналогичным образом, если проникающая язва аорты прогрессирует до расслоения аорты, то расслоение аорты, в зависимости от тяжести и степени, может нуждаться в лечении хирургическим вмешательством на аорте или эндоваскулярной пластикой с использованием аортального стент-графта.
Сводка
Проникающие язвы аорты – необычное, но потенциально опасное для жизни заболевание, возникающее в результате разрушения внутренней оболочки аорты. Этот процесс также называют проникающим атеросклеротическим заболеванием, поскольку он связан с накоплением холестерина и кальция в кровеносных сосудах тела (атеросклероз).
Вопрос
До этого вы когда-нибудь задумывались о том, что аорта может быть предрасположена к развитию язв, как и желудок?
Делитесь своими комментариями и присоединяйтесь к обсуждению.
Важное соображение при демонстрации боли в груди
Проникающая язва аорты у пожилых женщин: важный аспект при проявлениях боли в груди
Информация о статье
Николас Снельс *
Университет Гриффита, Австралия
* Автор для переписки: Dr.Николас Снелс, Университет Гриффита, Австралия
Поступила: 24.07.2019; Дата принятия: 14 августа 2019 г .; Опубликовано: 15 ноября 2019 г.
Образец цитирования: Snels N. Проникающая язва аорты у пожилых женщин: важное соображение при проявлениях боли в груди. Архив клинических и медицинских историй болезни 3 (2019): 463-465.
Посмотреть / Скачать Pdf Поделиться в FacebookАбстрактные
Введение: Боль в груди – одна из наиболее частых жалоб в отделения неотложной помощи.Последние достижения в области визуализации позволили лучше определить острые синдромы аорты, совокупность заболеваний, включая расслоение аорты, в дополнение к более редким язвам аорты и интрамуральным тромбам. Здесь я представляю случай женщины с болью в груди, вызванной проникающей язвой аорты.
История болезни: 74-летняя женщина обратилась с жалобой на боль в груди продолжительностью четыре дня на фоне, значимом для гипертонии, курения и васкулопатии в семейном анамнезе. Физикальное обследование с последующим радиологическим обследованием выявило проникающую язву аорты в восходящей аорте.Пациентка была направлена в сосудистую бригаду, которая лечила ее консервативно с помощью гипотензивных средств.
Заключение: Существует множество причин возникновения острой боли в груди. Язвы дуги аорты – редкая причина, однако ее следует учитывать при работе с этими пациентами, учитывая возможность разрыва аорты.
Ключевые слова
Боль в груди, язва аорты, расслоение аорты, дуга аорты
Статьи о боли в груди, Статьи о язве аорты, Статьи о расслоении аорты, Статьи о дуге аорты
Подробнее о статье
1.Введение
Боль в груди составляет значительную часть обращений в отделения неотложной помощи [1]. Надлежащее распознавание и устранение причины этой боли очень важно из-за высокой смертности, связанной с несколькими причинами боли в груди. Хотя расслоение аорты хорошо изучено, современные методы визуализации позволили лучше распознать и изучить другие острые синдромы аорты, а именно язвы дуги аорты и интрамуральные гематомы [2]. Распознавание и надлежащее лечение этих образований важно, поскольку при отсутствии лечения они могут вызвать разрыв аорты.Несмотря на это, нет единого мнения относительно визуализации и лечения этих состояний.
2. История болезни
Госпожа X, женщина 74 лет, обратилась в отделение неотложной помощи с перемежающейся болью в груди в течение четырех дней, острой по своей природе и иррадиирующей в правое плечо и спину. Ее медицинский опыт имел важное значение для лечения дислипидемии и гипертонии, без личного кардиологического анамнеза. Ее подходящими лекарствами были фуросемид 20 мг гривы и розувастатин 20 мг.В семейном анамнезе у нее был инфаркт миокарда по отцовской линии, в дополнение к брату, умершему от разрыва аневризмы аорты. Она была на пенсии и ранее курила с 40-летним стажем.
При осмотре она чувствовала себя комфортно, без боли, нормальное давление, частота пульса 74 удара в минуту. В остальном ее осмотр был в основном ничем не примечательным. Электрокардиограмма (ЭКГ) показала нормальный синусовый ритм. Серийные тропонины были отрицательными. Рентген грудной клетки без особенностей, боль не реагировала на тринитрат глицерина (GTN).Продолжающаяся боль, несмотря на эти исследования, побудила компьютерную томографию (КТ) аортограммы исключить расслоение аорты. Это продемонстрировало небольшие проникающие атеросклеротические язвы размером до 4 мм в дуге аорты, дистальнее левого подключичного начала, без расслоения и интрамуральной гематомы.
Она была направлена в сосудистую бригаду, получала регулярную анальгезию и проводила консервативное лечение проникающей атеросклеротической язвы амлодипином и рамиприлом с целью снижения артериального давления ниже 120/80.При последующем осмотре через 4 месяца состояние ее симптомов улучшилось, а повторное обследование показало стабильные изъязвления в аорте.
3. Обсуждение
С момента первого описания в 1930-х годах патофизиология проникающих язв аорты (ПАЯ) до конца не изучена [2]. Предполагается, что причиной этого состояния является эрозия и изъязвление атеросклеротических бляшек через внутреннюю эластичную пластинку аорты. Его можно классифицировать как тип острого аортального синдрома, термин, который охватывает интрамуральные гематомы и наиболее хорошо изученные расслоения аорты.Без лечения бляшка может вызвать локальное расслоение средней оболочки и предрасполагать к разрыву аорты, что приводит к значительной смертности.
Пациенты с ПАУ, как правило, пожилого возраста, на фоне артериальной гипертензии и основного атеросклероза [3]. Это контрастирует с расслоением аорты, где атеросклероз может быть различным, а группа пациентов моложе. Несмотря на то, что проникающие язвы трудно отличить клинически, в них отсутствуют такие признаки, как неравномерность пульса и неврологический дефицит, которые могут быть очевидны при расслоении аорты.Некоторые пациенты могут вообще не испытывать боли, при этом язва является случайной находкой во время других исследований. Различить подтипы острого аортального синдрома сложно, но это важно, учитывая вариабельность прогноза и вариантов лечения [4]. Для исследования пауков и наблюдения за прогрессированием заболевания использовались различные методы визуализации. КТ была наиболее распространенным методом, однако также использовались МРТ и ангиография аорты [5]. Эхокардиография также была исследована и может помочь дифференцировать острый аортальный синдром, однако крупномасштабные данные отсутствуют.
В настоящее время лечение проникающих язв аорты недостаточно развито. Ведение в основном ориентируется на расположение язвы. Нисходящие язвы эффективно лечились с помощью агрессивного контроля артериального давления, что в конечном итоге привело к заживлению язвы [6]. Восходящие язвы склонны к разрыву; следовательно, традиционно использовался хирургический подход. Хирургическое вмешательство осложняется сопутствующими заболеваниями, приводящими к образованию язвы, и эндоваскулярный доступ для таких пациентов становится все более актуальным.
4. Заключение
Хотя проникающие язвы аорты – редкая причина боли в груди, они остаются важным отличием, поскольку предрасполагают аорту к возможному разрыву. Клинически их по-прежнему трудно отличить от расслоения аорты, а достижения в области визуализации позволили дифференцировать паузу от других острых синдромов аорты. Лечение по-прежнему в значительной степени зависит от местоположения, однако в этом случае после консервативного лечения наблюдается симптоматическое улучшение.
Информированное согласие
У пациента было получено информированное согласие на написание этого описания случая. См. Прилагаемую подписанную форму согласия.
Конфликт интересов
У автора нет сведений о конфликте интересов.
Список литературы
- Bhuiya F, Pitts S, McCaig L. Визиты в отделение неотложной помощи по поводу боли в груди и боли в животе: США, 1999–2008 годы. Краткий обзор данных NCHS 43 (2010): 1-8.
- Baikoussis N, Apostolakis E.Проникающая атеросклеротическая язва грудного отдела аорты: диагностика и лечение. Hellenic J Cardiology 51 (2010): 153-157.
- Коади М., Риццо Дж., Хаммонд Дж. И др. Проникающая язва грудного отдела аорты: что это такое? Как мы это узнаем? Как мы с этим справляемся ?. Журнал сосудистой хирургии 27 (61998): 1006-1016.
- Ганаха Ф., Миллер Д., Сугимото К. и др. Прогноз интрамуральной гематомы аорты с проникающей атеросклеротической язвой и без нее: клинический и рентгенологический анализ.Тираж 106 (2002): 342-348.
- Vilacosta I, San Román J, Aragoncillo P, et al. Проникающая атеросклеротическая язва аорты: документирование чреспищеводной эхокардиографии. Журнал Американского колледжа кардиологии 32 (1998): 83-89.
- Казеруни Э., Бри Р., Уильямс Д. Проникающие атеросклеротические язвы нисходящей грудной аорты: оценка с помощью КТ и отличие от расслоения аорты. Радиология 183 (1992): 759-765.
Проникающая язва аорты и интрамуральная гематома
Акин И., Кише С., Инс Х., Ниенабер С. Проникающая язва аорты, интрамуральная гематома, острый синдром аорты: когда что делать. J Cardiovasc Surg (Турин). 2012; 53 (1 Приложение 1): 83–90.
CAS Google Scholar
Vilacosta I, San Roman JA. Острый аортальный синдром. Сердце (Br Card Soc). 2001. 85 (4): 365–8.
Артикул CAS Google Scholar
Коади М.А., Риццо Дж. А., Хаммонд Г. Л., Пирс Дж. Г., Копф Г. С., Элефтериадес Дж. А.Проникающая язва грудного отдела аорты: что это такое? Как мы это узнаем? Как мы с этим справляемся? J Vasc Surg. 1998; 27 (6): 1006–15 (обсуждение 15–6) .
Артикул CAS PubMed PubMed Central Google Scholar
Харрис Дж. А., Бис К. Г., Гловер Дж. Л., Бендик П. Дж., Шетти А., Браун О. В.. Проникающие атеросклеротические язвы аорты. J Vasc Surg. 1994; 19 (1): 90–8 (обсуждение 8–9) .
Артикул CAS PubMed Google Scholar
Stanson AW, Kazmier FJ, Hollier LH, Edwards WD, Pairolero PC, Sheedy PF и др. Проникающие атеросклеротические язвы грудного отдела аорты: естественное течение и клинико-патологические корреляции. Ann Vasc Surg. 1986; 1 (1): 15–23.
Артикул CAS Google Scholar
Sundt TM. Интрамуральная гематома и проникающая атеросклеротическая язва аорты. Ann Thorac Surg. 2007; 83 (2): S835–41 (обсуждение S46-50) .
Артикул PubMed Google Scholar
Шеннан Т. Расслаивающие аневризмы. Серия отчетов Специального совета по медицинским исследованиям. 1934; N8 (193).
Patel PJ, Grande W, Hieb RA. Эндоваскулярное лечение острых синдромов аорты. Semin Intervent Radiol. 2011; 28 (1): 10–23.
Артикул PubMed PubMed Central Google Scholar
Svensson LG, Labib SB, Eisenhauer AC, Butterly JR. Разрыв интимы без гематомы: важный вариант расслоения аорты, который может ускользнуть от современных методов визуализации.Тираж. 1999. 99 (10): 1331–6.
Артикул CAS PubMed PubMed Central Google Scholar
Чо К.Р., Стэнсон А.В., Поттер Д.Д., Черри К.Дж., Шафф Х.В., Сундт Т.М. 3-й. Проникающая атеросклеротическая язва нисходящей грудной аорты и дуги. J Thorac Cardiovasc Surg. 2004; 127 (5): 1393–9 (обсуждение 9-401) .
Артикул PubMed Google Scholar
Мадду К.К., Шуайб В., Теллерия Дж., Джонсон Дж.О., Хоса Ф. Нетравматические острые неотложные состояния аорты: Часть 1, Острый аортальный синдром. AJR Am J Roentgenol. 2014. 202 (3): 656–65.
Артикул PubMed Google Scholar
Натан Д.П., Бунн В., Лай Е., Ван Г.Дж., Десаи Н., Ву Е.Ю. и др. Проявление, осложнения и естественное течение проникающей атеросклеротической язвенной болезни. J Vasc Surg. 2012; 55 (1): 10–5.
Артикул PubMed PubMed Central Google Scholar
Quint LE, Williams DM, Francis IR, Monaghan HM, Sonnad SS, Patel S и др. Язвенные поражения аорты: особенности визуализации и естественное течение. Радиология. 2001. 218 (3): 719–23.
Артикул CAS PubMed Google Scholar
Трокслер М., Мавор А.И., Гомер-Ванниасинкам С. Проникающие атеросклеротические язвы аорты. Br J Surg. 2001. 88 (9): 1169–77.
Артикул CAS PubMed Google Scholar
Сингхал П., Лин З. Проникающая атероматозная язва восходящей аорты: описание случая и обзор литературы. Heart Lung Circ. 2008. 17 (5): 380–2.
Артикул CAS PubMed Google Scholar
Титл С.Л., Линч Р.Дж., Коул П.Е., Сингх Х.С., Риццо Дж. А., Копф Г.С. и др. Промежуточное наблюдение при проникающей язве и интрамуральной гематоме аорты. J Thorac Cardiovasc Surg. 2002. 123 (6): 1051–9.
Артикул PubMed Google Scholar
Георгиадис Г.С., Антониу Г.А., Георгакаракос Е.И., Николопулос Е.С., Папанас Н., Треллопулос Г. и др. Хирургическая или эндоваскулярная терапия проникающих язв брюшной аорты и их естественное течение: систематический обзор. J Vasc Interv Radiol. 2013. 24 (10): 1437–49.
Артикул PubMed Google Scholar
Тода Р., Морияма Ю., Игуро Ю., Мацумото Н., Масуда Н., Уэно Т. Проникающая атеросклеротическая язва. Хирург сегодня. 2001. 31 (1): 32–5.
Артикул CAS PubMed Google Scholar
Вули К.Ф., Спаркс Э.Х., Будулас Х. Боль в аорте. Prog Cardiovasc Dis. 1998. 40 (6): 563–89.
Артикул CAS PubMed Google Scholar
Фарук М.М., Клинг К., Ямини Д., Гелаберт Х.А., Бейкер Д.Д., Фрайшлаг Я.А. Проникающее изъязвление инфраренального отдела аорты: сообщения о случаях эмболического и бессимптомного поражения.Ann Vasc Surg. 2001; 15 (2): 255–9.
Артикул CAS PubMed Google Scholar
Диджей Голдштейн, Флорес Р.М., Тодд Дж. Разрыв неаневризматической атеросклеротической инфраренальной аорты. J Vasc Surg. 1997. 26 (4): 700–3.
Артикул CAS PubMed Google Scholar
Ганаха Ф., Миллер Д.К., Сугимото К., До Ю.С., Минамигучи Х., Сайто Х. и др. Прогноз интрамуральной гематомы аорты с проникающей атеросклеротической язвой и без нее: клинический и рентгенологический анализ.Тираж. 2002. 106 (3): 342–348.
Артикул Google Scholar
Крукенберг Э. К вопросу о расслаивающейся аневризме. Бейтр Патол Анат Аллг Патол. 1920; 67: 329–51.
Google Scholar
Пак К. Х., Лим К., Чой Дж. Х., Сунг К., Ким К., Ли Ю. Т. и др. Распространенность дефекта интимы аорты в острой интрамуральной гематоме типа А, леченной хирургическим путем. Ann Thorac Surg.2008. 86 (5): 1494–500.
Артикул PubMed Google Scholar
Чао С.П., Уокер Т.Г., Калва СП. Естественный анамнез и компьютерная томография интрамуральной гематомы аорты. Рентгенография. 2009. 29 (3): 791–804.
Артикул PubMed PubMed Central Google Scholar
Евангелиста А., Мукерджи Д., Мехта Р. Х., О’Гара П. Т., Фаттори Р., Купер Дж. В. и др. Острая интрамуральная гематома аорты: загадка эволюции.Тираж. 2005. 111 (8): 1063–70.
Артикул PubMed PubMed Central Google Scholar
Sundt TM. Внутримуральная гематома и проникающая язва аорты. Curr Opin Cardiol. 2007. 22 (6): 504–9.
Артикул PubMed Google Scholar
Song JK, Kim HS, Kang DH, Lim TH, Song MG, Park SW и др. Различные клинические особенности интрамуральной гематомы аорты по сравнению с расслоением восходящей аорты.J Am Coll Cardiol. 2001. 37 (6): 1604–10.
Артикул CAS PubMed Google Scholar
Tolenaar JL, Harris KM, Upchurch GR Jr, Evangelista A, Moll FL, di Eusanio M, et al. Различия и сходство между интрамуральной гематомой нисходящей аорты и острым расслоением типа B. J Vasc Surg. 2013. 58 (6): 1498–504.
Артикул PubMed PubMed Central Google Scholar
Nienaber CA. Комментарий: стадирование интрамуральной гематомы аорты: враг за гладкой поверхностью? J Endovasc Ther. 2010. 17 (5): 622–3.
Артикул PubMed Google Scholar
Song JK, Yim JH, Ahn JM, Kim DH, Kang JW, Lee TY и др. Исходы пациентов с острой интрамуральной гематомой аорты типа А. Тираж. 2009. 120 (21): 2046–52.
Артикул PubMed PubMed Central Google Scholar
Riambau V, Böckler D, Brunkwall J, Cao P, Chiesa R, Coppi G и др. Выбор редакции – лечение заболеваний нисходящей грудной аорты: руководящие принципы клинической практики Европейского общества сосудистой хирургии (ESVS). Eur J Vasc Endovasc Surg. 2017; 53 (1): 4–52.
Артикул CAS PubMed Google Scholar
von Kodolitsch Y, Csosz SK, Koschyk DH, Schalwat I, Loose R, Karck M, et al. Интрамуральная гематома аорты: предикторы прогрессирования расслоения и разрыва.Тираж. 2003. 107 (8): 1158–63.
Артикул Google Scholar
Харрис К.М., Браверман А.С., Игл К.А., Возницки Е.М., Пайериц Р.Э., Мирмель Т. и др. Острая интрамуральная гематома аорты: анализ Международного реестра острых расслоений аорты. Тираж. 2012; 126 (11 Suppl 1): S91–6.
Артикул PubMed PubMed Central Google Scholar
Евангелиста А., Домингес Р., Себастия С., Салас А., Перманьер-Миральда Г., Авельяно Г. и др. Прогностическое значение клинико-морфологических данных в краткосрочной эволюции интрамуральной гематомы аорты. Терапевтическое значение. Eur Heart J. 2004; 25 (1): 81–7.
Артикул PubMed Google Scholar
Эрбель Р., Альфонсо Ф., Буало С., Дирш О., Эбер Б., Хаверих А. и др. Диагностика и лечение расслоения аорты. Eur Heart J.2001. 22 (18): 1642–81.
Артикул CAS PubMed Google Scholar
Choi SH, Choi SJ, Kim JH, Bae SJ, Lee JS, Song KS, et al. Полезные результаты КТ для прогнозирования прогрессирования интрамуральной гематомы аорты до явного расслоения аорты. J Comput Assist Tomogr. 2001. 25 (2): 295–9.
Артикул CAS PubMed Google Scholar
Tsai TT, Nienaber CA, Eagle KA.Острые синдромы аорты. Тираж. 2005. 112 (24): 3802–13.
Артикул PubMed PubMed Central Google Scholar
Hagan PG, Nienaber CA, Isselbacher EM, Bruckman D, Karavite DJ, Russman PL, et al. Международный регистр острой расслоения аорты (IRAD): новый взгляд на старую болезнь. ДЖАМА. 2000. 283 (7): 897–903.
Артикул CAS Google Scholar
Eggebrecht H, Naber CK, Bruch C, Kroger K, von Birgelen C, Schmermund A, et al. Значение D-димеров фибрина плазмы для выявления острого расслоения аорты. J Am Coll Cardiol. 2004. 44 (4): 804–9.
Артикул CAS PubMed Google Scholar
Шинохара Т., Сузуки К., Окада М., Шиигай М., Симидзу М., Маэхара Т. и др. Количество растворимых фрагментов эластина в сыворотке повышается при остром расслоении аорты. Артериосклер Thromb Vasc Biol.2003. 23 (10): 1839–44.
Артикул CAS PubMed PubMed Central Google Scholar
Suzuki T, Distante A, Zizza A, Trimarchi S, Villani M, Salerno Uriarte JA, et al. Диагностика острого расслоения аорты с помощью D-димера: опыт Международного реестра острых расслоений аорты по биомаркерам (IRAD-Bio). Тираж. 2009. 119 (20): 2702–7.
Артикул PubMed PubMed Central Google Scholar
Яноши Р.А., Горла Р., Цагакис К., Калерт П., Горачек М., Брукшен Ф. и др. Эндоваскулярное лечение осложненной проникающей язвы аорты: 11-летний опыт работы в одном центре. J Endovasc Ther. 2016; 23 (1): 150–9.
Артикул PubMed Google Scholar
Чикконе М.М., Дентамаро И., Маси Ф., Карбонара С., Риччи Г. Достижения в диагностике острых синдромов аорты: роль методов визуализации. Vasc Med. 2016; 21 (3): 239–50.
Артикул CAS PubMed PubMed Central Google Scholar
Salvolini L, Renda P, Fiore D, Scaglione M, Piccoli G, Giovagnoni A. Острые синдромы аорты: роль многодетекторной КТ ряда. Eur J Radiol. 2008. 65 (3): 350–8.
Артикул PubMed Google Scholar
Бишофф М.С., Гейсбуш П., Петерс А.С., Хихлик-Дурр А., Боклер Д. Проникающая язва аорты: определение рисков и терапевтические стратегии.Герц. 2011. 36 (6): 498–504.
Артикул CAS PubMed PubMed Central Google Scholar
Evangelista A, Carro A, Moral S, Teixido-Tura G, Rodriguez-Palomares JF, Cuellar H, et al. Методы визуализации для ранней диагностики острого аортального синдрома. Nat Rev Cardiol. 2013. 10 (8): 477–86.
Артикул PubMed PubMed Central Google Scholar
Nienaber CA. Роль визуализации при острых синдромах аорты. Eur Heart J Cardiovasc Imaging. 2013. 14 (1): 15–23.
Артикул PubMed Google Scholar
Qahtani SA, Kandeel AY, Breault S, Jouannic AM, Qanadli SD. Распространенность острого коронарного синдрома у пациентов с подозрением на тромбоэмболию легочной артерии или острый синдром аорты: обоснование концепции тройного исключения. J Clin Med Res. 2015; 7 (8): 627–31.
Артикул PubMed PubMed Central Google Scholar
Evangelista A, Garcia-del-Castillo H, Gonzalez-Alujas T, Dominguez-Oronoz R, Salas A, Permanyer-Miralda G и др. Диагностика расслоения восходящей аорты с помощью чреспищеводной эхокардиографии: полезность M-режима для распознавания артефактов. J Am Coll Cardiol. 1996. 27 (1): 102–7.
Артикул CAS PubMed Google Scholar
Roselli EE, Idrees J, Greenberg RK, Johnston DR, Lytle BW. Эндоваскулярная трансплантация стента для восстановления восходящей аорты у пациентов из группы высокого риска.J Thorac Cardiovasc Surg. 2015; 149 (1): 144–51.
Артикул PubMed PubMed Central Google Scholar
Карпентер С.В., Кодолич Ю.В., Дебус Е.С., Виппер С., Цилимпарис Н., Ларена-Авельянеда А. и др. Острые синдромы аорты: определение, прогноз и варианты лечения. J Cardiovasc Surg. 2014; 55 (2 Приложение 1): 133–44.
CAS Google Scholar
Hata M, Hata H, Sezai A, Yoshitake I, Wakui S, Shiono M.Оптимальная стратегия лечения острого расслоения аорты типа А с интрамуральной гематомой. J Thorac Cardiovasc Surg. 2014. 147 (1): 307–11.
Артикул PubMed PubMed Central Google Scholar
Кадзи С., Акасака Т., Хорибата Ю., Нишигами К., Шоно Х., Катаяма М. и др. Долгосрочный прогноз пациентов с интрамуральной гематомой аорты типа А. Тираж. 2002; 106 (12 Suppl 1): I248–52.
PubMed Google Scholar
Ватанабэ С., Ханью М., Араи Ю., Нагасава А. Начальное лечение острой интрамуральной гематомы типа А и расслоения аорты. Ann Thorac Surg. 2013. 96 (6): 2142–6.
Артикул PubMed PubMed Central Google Scholar
Bosiers MJ, Donas KP, Mangialardi N, Torsello G, Riambau V, Criado FJ, et al. Европейский многоцентровый регистр для применения техники Chimney / Snorkel при лечении патологических состояний дуги аорты.Ann Thorac Surg. 2016; 101 (6): 2224–30.
Артикул PubMed Google Scholar
Куримото Ю., Маруяма Р., Удихира К., Нисиока Н., Хасегава К., Иба Ю. и др. Эндоваскулярное восстановление грудной аорты при сложных заболеваниях дуги аорты с использованием фенестрированных стент-графтов из зоны 0. Ann Thorac Surg. 2015; 100 (1): 24–32 (обсуждение-3) .
Артикул PubMed Google Scholar
Li Z, Lu Q, Feng R, Zhou J, Zhao Z, Bao J, et al. Результаты эндоваскулярной пластики расслоения восходящей аорты у пациентов, непригодных для прямого хирургического вмешательства. J Am Coll Cardiol. 2016; 68 (18): 1944–54.
Артикул PubMed PubMed Central Google Scholar
Копье Р., Хаулон С., Оки Т., Цилимпарис Н., Канаока И., Милн С.П. и др. Последующие результаты пластики аневризмы дуги внутренними разветвленными эндотрансплантатами. Eur J Vasc Endovasc Surg.2016; 51 (3): 380–5.
Артикул CAS PubMed Google Scholar
Eggebrecht H, Plicht B, Kahlert P, Erbel R. Внутримуральная гематома и проникающие язвы: показания к эндоваскулярному лечению. Eur J Vasc Endovasc Surg. 2009. 38 (6): 659–65.
Артикул CAS Google Scholar
Geisbusch P, Kotelis D, Weber TF, Hyhlik-Durr A, Kauczor HU, Bockler D.Ранние и среднесрочные результаты после эндоваскулярной пластики проникающих язв аорты стент-графтом. J Vasc Surg. 2008. 48 (6): 1361–8.
Артикул PubMed Google Scholar
Ботта Л., Бутацци К., Руссо В., Парлапиано М., Гостоли В., Ди Бартоломео Р. и др. Эндоваскулярная пластика проникающих атеросклеротических язв нисходящей грудной аорты: ранние и среднесрочные результаты. Ann Thorac Surg. 2008. 85 (3): 987–92.
Артикул PubMed Google Scholar
Grimm M, Loewe C, Gottardi R, Funovics M, Zimpfer D, Rodler S и др. Новое понимание механизмов и лечения интрамуральной гематомы, поражающей всю грудную аорту. Ann Thorac Surg. 2008. 86 (2): 453–6.
Артикул PubMed Google Scholar
Евангелиста А., Домингес Р., Себастия С., Салас А., Перманьер-Миральда Г., Авельяно Г. и др. Долгосрочное наблюдение за интрамуральной гематомой аорты: предикторы исхода.Тираж. 2003. 108 (5): 583–9.
Артикул PubMed Google Scholar
Schoder M, Grabenwoger M, Holzenbein T, Domanovits H, Fleischmann D, Wolf F, et al. Эндоваскулярная пластика стент-графта при осложненных проникающих атеросклеротических язвах нисходящей грудной аорты. J Vasc Surg. 2002. 36 (4): 720–6.
Артикул PubMed Google Scholar
Kos X, Bouchard L, Otal P, Chabbert V, Chemla P, Soula P и др. Стент-графтное лечение проникающих язв грудного отдела аорты. J Endovasc Ther. 2002; 9 (Дополнение 2): II25–31.
Артикул PubMed Google Scholar
Цудзи Ю., Танака Ю., Китагава А., Хино Ю., Танигучи Т., Сугимото К. и др. Эндоваскулярная пластика стент-графта при проникающей атеросклеротической язве в инфраренальной части брюшной аорты. J Vasc Surg. 2003. 38 (2): 383–8.
Артикул PubMed Google Scholar
Eggebrecht H, Baumgart D, Schmermund A, von Birgelen C, Herold U, Wiesemes R, et al. Эндоваскулярная пластика стент-графтом при проникающей атеросклеротической язве нисходящей аорты. Am J Cardiol. 2003. 91 (9): 1150–3.
Артикул PubMed Google Scholar
Демерс П., Миллер, округ Колумбия, Митчелл Р.С., Ки С.Т., Чагонджиан Л., Дейк М.Д.Пластика проникающих атеросклеротических язв в нисходящей грудной аорте стент-графтом: среднесрочные результаты. Ann Thorac Surg. 2004. 77 (1): 81–6.
Артикул PubMed Google Scholar
Бринстер Д. Р., Уитли Г. Х. 3-й, Уильямс Дж., Рамая В. Г., Дитрих Э. Б., Родригес-Лопес Дж. А.. Лучше ли лечить проникающие язвы аорты эндоваскулярным методом? Ann Thorac Surg. 2006. 82 (5): 1688–91.
Артикул PubMed Google Scholar
Eggebrecht H, Herold U, Schmermund A, Lind AY, Kuhnt O, Martini S и др. Эндоваскулярное лечение проникающей язвы аорты с помощью стент-графта: результаты за средний период наблюдения 27 месяцев. Am Heart J. 2006; 151 (2): 530–6.
Артикул PubMed Google Scholar
Piffaretti G, Tozzi M, Lomazzi C, Rivolta N, Caronno R, Castelli P. Эндоваскулярное восстановление брюшной инфраренальной проникающей язвы аорты: проспективное обсервационное исследование.Int J Surg. 2007. 5 (3): 172–5.
Артикул PubMed Google Scholar
Dalainas I, Nano G, Medda M, Bianchi P, Casana R, Ramponi F, et al. Эндоваскулярное лечение проникающих язв аорты: среднесрочные результаты. Eur J Vasc Endovasc Surg. 2007. 34 (1): 74–8.
Артикул CAS PubMed Google Scholar
D’Souza S, Duncan A, Aguila F, Oderich G, Ricotta J, Kalra M, et al.TEVAR при неаневризматической патологии грудной аорты. Катетер Cardiovasc Interv. 2009. 74 (5): 783–6.
Артикул PubMed Google Scholar
Clough RE, Mani K, Lyons OT, Bell RE, Zayed HA, Waltham M, et al. Эндоваскулярное лечение острого аортального синдрома. J Vasc Surg. 2011; 54 (6): 1580–7.
Артикул PubMed Google Scholar
Паломбо Д., Люцертини Дж., Робальдо А, Пане В, Спинелла Г.Лечение проникающей язвы аорты эндопротезированием: опыт единого центра. Int Angiol. 2011.
Черни М., Фуновикс М., Содек Дж., Дамфарт Дж., Шодер М., Джурашек А. и др. Результаты после эндоваскулярного восстановления грудной аорты при проникающих атеросклеротических язвах. Ann Thorac Surg. 2011; 92 (2): 562–6 обсуждение 6–7 .
Артикул PubMed Google Scholar
Местрес Г., Родригес Р., Гарсия-Мадрид С., Монтана Х, Баррел М., Круз Л.Ф. и др.Эндоваскулярное лечение проникающих язв аорты: среднесрочное наблюдение. Преподобный Эсп Кардиол (англ. Ред.). 2012; 65 (1): 54–9.
Артикул Google Scholar
Георгиадис Г.С., Треллопулос Г., Антониу Г.А., Георгакаракос Е.И., Николопулос Е.С., Пелекас Д. и др. Эндоваскулярная терапия проникающих язв инфраренального отдела аорты. ANZ J Surg. 2013. 83 (10): 758–63.
PubMed Google Scholar
Моннин-Барес В., Тони Ф., Родьер М., Бах В., Хачини Р., Блин Д. и др. Эндоваскулярное лечение интрамуральных гематом аорты с использованием стент-графта. J Vasc Interv Radiol. 2009. 20 (6): 713–21.
Артикул PubMed Google Scholar
Мэннинг Б.Дж., Диас Н., Манно М., Орландер Т., Малина М., Сонессон Б. и др. Эндоваскулярное лечение острого осложненного расслоения типа B: морфологические изменения в промежуточном периоде наблюдения. J Endovasc Ther.2009. 16 (4): 466–74.
Артикул PubMed Google Scholar
Li DL, Zhang HK, Cai YY, Jin W, Chen XD, Tian L, et al. Острая интрамуральная гематома аорты типа B: стратегия лечения и роль эндоваскулярного восстановления. J Endovasc Ther. 2010. 17 (5): 617–21.
Артикул PubMed Google Scholar
Lavingia KS, Ahanchi SS, Redlinger RE, Udgiri NR, Panneton JM.Ремоделирование аорты после торакального эндоваскулярного восстановления аорты при интрамуральной гематоме. J Vasc Surg. 2014; 60 (4): 929–35 (обсуждение 35-6) .
Артикул PubMed Google Scholar
Bischoff MS, Meisenbacher K, Wehrmeister M, Bockler D, Kotelis D. Показания к лечению и исход эндоваскулярного восстановления интрамуральной гематомы аорты типа B. J Vasc Surg. 2016; 64 (6): 1569–79.
Артикул PubMed PubMed Central Google Scholar
Куллиас Г.Дж., Уитли Г.Х. 3-й. Современные гибридные процедуры для дуги аорты: метаанализ. Ann Thorac Surg. 2010. 90 (2): 689–97.
Артикул Google Scholar
Хуанг Q, Чен XM, Ян Х, Линь QN, Цинь X. Эффект реваскуляризации левой подключичной артерии в грудном эндоваскулярном восстановлении аорты: систематический обзор и метаанализ. Eur J Vasc Endovasc Surg. 2018; 56 (5): 644–51.
Артикул PubMed Google Scholar
Redlinger RE Jr, Ahanchi SS, Panneton JM. Лазерная фенестрация in situ во время экстренной грудной эндоваскулярной пластики аорты является эффективным методом реваскуляризации левой подключичной артерии. J Vasc Surg. 2013. 58 (5): 1171–7.
Артикул PubMed Google Scholar
Patel HJ, Dake MD, Bavaria JE, Singh MJ, Filinger M, Fischbein MP, Williams DM, Matsumura JS, Oderich G. Разветвленная эндоваскулярная терапия дистального отдела дуги аорты: предварительные результаты многоцентрового исследования осуществимости эндопротез грудной ветви.Ann Thorac Surg. 2016; 102 (4): 1190–8.
Артикул PubMed PubMed Central Google Scholar
Feezor RJ, Martin TD, Hess PJ Jr, Daniels MJ, Beaver TM, Klodell CT, et al.
